Трансформант дрожжей ogataea haglerorum, продуцирующий бета-маннаназу, содержащий в составе хромосомы синтетический ген mans - RU2764793C1
Код документа: RU2764793C1
Чертежи

Описание
Изобретение относится к области биотехнологии и касается получения рекомбинантного штамма дрожжей Ogataea haglerorum N107 - продуцента β-маннаназы.
β-маннаназа (эндо-β-1,4-маннаназа β-1,4-D-маннаназа, 1,4-β-D-маннан манногидролаза, Е.С. 3.2.1.78) относится к гемицеллюлазам, к классу ферментов О-гликозид-гидролаз и катализирует расщепление внутренних β-1,4-гликозидных связей в основной полимерной цепи молекулы маннана.
Маннан - важный компонент гемицеллюлозной фракции клеточной стенки многих растений, полисахарид, который в зависимости от строения подразделяют на четыре субсемейства: линейный маннан, галактоманнан, глюкоманнан или галактоглюкоманнан [Carbohydr Polym. 2001, 44, 107-112; Process Biochem. 2010, 45, 1203-1213]. В каждом из этих полисахаридов основная цепь состоит из остатков D-маннозы или комбинации остатков D-маннозы и D-глюкозы, связанных β-1,4-гликозидными связями.
Полная деградация маннана требует комплекса маннолитических ферментов, включающих β-маннаназу, β-1,4-маннозидазу (ЕС 3.2.1.25) и β-глюкозидазу (ЕС 3.2.1.21).
Основную роль в разрушении маннана играет β-маннаназа, которая катализирует случайный гидролиз маннана до низкомолекулярных манноолигосахаридов, преимущественно до маннобиозы и маннотриозы [Crit Rev Biotechnol. 2007, 27(4), 197-216]. Низкомолекулярные манноолигосахариды и манноза могут усваиваться живыми организмами.
β-маннаназу применяют в целлюлозно-бумажной промышленности для отбеливания пульпы, в пищевой промышленности (растворимый кофе, экстракция растительных масел из семян, диетические пищевые продукты), производстве синтетических моющих средств, получении биотоплива из лигноцеллюлозы [Appl Microbiol Biotechnol. 2008, 79, 165-178. DOI 10.1007/s00253-008-1423-4]. Важной областью применения β-маннаназы является кормовая промышленность. Наличие маннанов в кормах приводит к повышению вязкости содержимого желудочно-кишечного тракта птицы и животных с однокамерным желудком из-за способности маннанов связывать свободную воду. Введение в корма животных β-маннаназы увеличивает их питательную ценность и энергетический уровень, уменьшает вязкость перевариваемого субстрата, способствует улучшению физиологического состояния животных, приросту их массы и продуктивности [Crit Rev Biotechnol. 2007, 27(4), 197-216]. Манноза - продукт расщепления маннанов, легко усваивается организмом. Неусвояемые формы манноолигосахаридов - маннотриоза и маннобиоза, являются хорошим субстратом для роста бифидобактерий и способствуют улучшению показателей здоровья птицы. Введение маннаназы и других ферментов, разрушающих растительные субстраты, в рацион животных с однокамерным желудком и птиц позволяет использовать такие дешевые корма, как ячмень, овес и отходы сельскохозяйственного производства (отруби, жом), содержащие трудноусвояемые компоненты.
Природными источниками β-маннаназ являются преимущественно бактерии и грибы. Среди грамположительных бактерий преобладают виды рода Bacillus и Clostridium [Carbohydr Polym. 2006, 66, 88-96; J Food Biochem. 2011, 35, 1451-1460; J. Bacteriol. 2004, 186 (19), 6544-6552]. β-Маннаназы синтезируются некоторыми штаммами грамотрицательных бактерий, таких как Pseudomonas [Biochem J. 1995, 305, 1005-1010], Vibrio [Biosci Biotechnol Biochem. 2009, 73, 109-116]. Обширная группа маннолитиков среди грибов представлена родами Aspergillus и Trichoderma [J. Biotechnol. 1998, 63, 199-210; PLOS One. 2011, 6(12), e29302. doi:10.1371/journal. Pone.0029302].
Большое количество генов β-маннаназ экспрессировано в гетерологичных хозяевах. Гены β-маннаназ из бактериальных источников экспрессированы в Escherichia coli, Bacillus megaterium, Brevibacillus brevis, Pichia pastoris, Kluyveromyces cicerisporous, гены β-маннаназ из грибов экспрессированы в Pichia pastoris, Saccharomyces cerevisiae, Yarrowia lipolytica, Aspergillus sp., Trichoderma reesei [Biotechnology Advances. 2016. doi:10.1016/j.biotechadv.2016.11.00; Process Biochemistry 2010, 45, 1203-1213. doi:10.1016/j.procbio.2010.05.011].
Штаммы грибов, как правило, продуцируют комплекс ферментов, относящихся к карбогидразам и разрушающих растительные субстраты, а именно, β-маннаназу, ксиланазу, целлюлазу, глюканазу и пектиназу. В этом ферментном коктейле на долю β-маннаназ приходится не более 3% [Carbohydr Polym. 2004, 57, 23-29].
Для производства моноферментных препаратов используют рекомбинантные дрожжевые штаммы.
Наиболее продуктивные рекомбинантные штаммы - продуценты β-маннаназы получены на основе дрожжей Pichia pastoris.
Метилотрофные дрожжи Pichia pastoris являются модельным организмом для экспрессии гетерологичных генов под контролем сильного регулируемого метанолом промотора гена АОХ1. При использовании несбраживаемых источников углерода (глицерина, метанола и т.п.) дрожжи Pichia pastoris способны к росту с образованием биомассы высокой плотности, что позволяет получать значительные количества гетерологичного белка [Appl. Microbiol. Biotechnol., 2000, 54(6), 741-750]. Процесс культивирования метилотрофных дрожжей достаточно прост, поскольку их рост не блокируется продуктами метаболизма [FEMS Microbiol. Rev., 2000, 24:45-66, doi: 10.111 l/j.l574-6976.2000.tb00532.x].
На базе дрожжей Pichia pastoris получены рекомбинантные штаммы, содержащие гены маннаназ из грибов.
В дрожжах Pichia pastoris Х-33 экспрессирован ген manM Aspergillus sulphureus с кодонами, адаптированными для этого вида дрожжей. Штамм продуцирует 3 мг/мл белка, активность фермента составляет 1100 ед./мл КЖ через 96 ч культивирования в 10 л ферментере. Рекомбинантная β-маннаназа имеет максимальную активность при рН 2,4 и температуре 50°С, удельная активность фермента 344,8 ед./мг [Biologia 2009, 64/2, 235-238. doi: 10.2478/sl 1756-009-0043-5].
β-Маннаназы грибного происхождения, в основном, проявляют максимальную активность при кислых значениях рН (2.0-4.5) и характеризуются невысокой удельной активностью по сравнению с бактериальными β-маннаназами.
Известны примеры создания высокопродуктивных рекомбинантных штаммов-продуцентов на основе дрожжей Pichia pastoris, содержащих гены бактериальных β-маннаназ, преимущественно из бактерий рода Bacillus. Бактериальные β-маннаназы проявляют максимальную активность при нейтральных и щелочных значениях рН и характеризуются в массе своей относительно высокой удельной активностью по сравнению с грибными β-маннаназами, например, удельная активность очищенной β-маннаназы из Bacillus subtilis SA-22 составляет 34780 ед./мг, из Bacillus circulans М-21 -19373 ед./мг, из Bacillus subtilis WY34 - 8302 ед./мг, из Bacillus sp.MSJ-5 - 5383 ед./мг [Int J Pharm Bio Sci. 2014, 5(1): (B), 176-192] и, в целом, более термостабильны, чем грибные β-маннаназы, что важно для промышленного использования фермента [Appl. Microbiol. Biotechnol. 2012, 93, 1817-1830. DOI 10.1007/s00253-012-3887-5].
Получен продуцент на основе штамма P. pastoris GS115, в котором экспрессирован ген β-маннаназы из Bacillus megaterium FBI01. Активность маннаназы составляет 22000 ед./мл через 120 ч ферментации и не меняется при увеличении времени культивирования до 190 ч. Удельная активность фермента в КЖ составляет 3427 ед./мг, очищенного фермента - 16718 ед./мг. Фермент проявляет максимальную активность при рН 6.5 и температуре 55°С [WO 2012079222].
Ген β-маннаназы mannS из Bacillus subtilis MAFIC-S11, имеющий адаптированные для дрожжей P. pastoris ко доны, экспрессирован в дрожжах P. pastoris. Для секреции использована модифицированная сигнальная последовательность [Biotechnology and Bioengineering 2009, 103, 1192-1201]. Штамм секретирует 6,6 мг/мл белка, активность маннаназы составляет 24600 ед./мл через 144 ч ферментации в 10 л ферментере. Фермент имеет максимальную активность при рН 6,0 и температуре 50°С [Appl Biochem Biotechnol. 2013,169, 2326-2340. DOI 10.1007/sl2010-013-0156-8].
Рекомбинантный штамм Pichia pastoris, содержащий искусственно созданный ген маннаназы ManGold, секретирует 3,25 мг/мл фермента, активность маннаназы составляет 35000 ед./мл через 96 ч ферментации [CN 110093331].
Еще одной известной метилотрофной системой для гетерологичной экспрессии являются термотолерантные дрожжи Ogataea (Hansenuld). Дрожжи рода Ogataea, как и дрожжи Pichia pastoris, обладают уникальной организацией и регуляцией метаболизма в присутствии метанола благодаря наличию сильных промоторов, индуцируемых метанолом. Подобно Pichia pastoris, дрожжи рода Ogataea сочетают преимущества простоты выращивания на недорогой ростовой среде с высокой секретирующей способностью, а также при культивировании в биореакторе позволяют получать биомассу с высокой плотностью клеток, что способствует высокому выходу целевого продукта [FEMS Yeast Res. 2005, 5, 1079-1096; Microb. Cell Fact. 2006, 5, 39; Curr Microbiol. 2014, 69, 143-148; FEMS Microbiology Letters, 2019, 366, fnz052].
В отличие от Pichia pastoris дрожжи рода Ogataea являются термотолерантными, что позволяет проводить ферментацию при температуре не ниже 37°С. Повышение температуры процесса ферментации снижает контаминацию и затраты на охлаждение биореактора [Appl. Microbiol. Biotechnol. 2010, 85, 861-867. doi: 10.1007/s00253-009-2248-5] и в результате сокращает длительность ферментации.
Вид Ogataea haglerorum выделен из дрожжей рода Ogataea в 2017 г. в результате проведения анализа последовательностей D1/D1 гена LSU rRNA, ITS1-5.8S-ITS2, фактора элонгации трансляции EF-1α и комплексного генетического анализа Наумовым Г.И. с соавторами [Int. J. Syst. Evol. Microbiol. 2017, 67, 2465-2469. DOI 10.1099/ijsem.0.002012].
Для дрожжей Ogataea haglerorum разработаны генетические технологии конструирования штаммов-продуцентов, включая экспрессионный вектор и метод введения ДНК в клетки реципиента [Биотехнология, 2019, 35 (6), 51-56]. Описано использование штамма Ogataea haglerorum ВКПМ Y-2584 для экспрессии различных генов фитазы. Других сведений об использовании дрожжей Ogataea haglerorum для экспрессии гетерологичных генов не выявлено.
Задачей заявляемого изобретения является расширение арсенала рекомбинантных микроорганизмов, продуцирующих β-маннаназу.
Задача решена путем получения трансформанта дрожжей Ogataea haglerorum, продуцирующего β-маннаназу из Bacillus subtilis, содержащего в составе хромосомы оптимизированный синтетический ген MANS, кодирующий указанную β-маннаназу, нуклеотидная последовательность которого приведена в перечне последовательностей под номером SEQ ID NO:l.
В заявляемом изобретении термотолерантные метилотрофные дрожжи рода Ogataea впервые использованы для гетерологичной экспрессии β-маннаназы.
Получение заявляемого трансформанта включает:
- трансформацию в клетки дрожжей Ogataea haglerorum экспрессионной кассеты, содержащей синтетический ген MANS β-маннаназы из Bacillus subtilis; нуклеотидная последовательность которого приведена в перечне последовательностей под номером SEQ ID N0:1, промотор, работающий в дрожжах Ogataea (Hansenuld), сигнальный пептид для осуществления секреции фермента в культуральную жидкость, терминатор, маркерный ген и, предпочтительно, сайт для гомологичной интеграции в хромосому. Интеграцию осуществляют путем как гомологичной, так и негомологичной рекомбинации. Трансформацию экспрессионной кассеты в клетки дрожжей Ogataea (Hansenuld) осуществляют любым подходящим методом, например, методом электоропорации [http://tools.thermofisher.coni/content/sfs/manuals/pich_man.pdf] или методом с использованием полиэтиленгликоля или протопластов [http://vvfww.thermofisher.com/order/catalog/product/K173001];
- отбор репликативного трансформанта, способного продуцировать β-маннаназу;
- отбор трансформанта, способного к синтезу β-маннаназы, с множественной интеграцией экспрессионной кассеты в состав хромосомы.
Конструирование экспрессионной кассеты осуществляют стандартными методами генетической инженерии [Sambrook J., Maniatis Т., Fritsch Е. Molecular cloning: a laboratory manual. - N.Y.: Cold Spring Harbor Laboratory, 1989] с использованием генетических элементов, подходящих для работы с дрожжами рода Ogataea (Hansenuld). В качестве промоторов могут быть использованы МОХ, FMD, DAS, TPS1, FLD1, PHO1, YNT1, YNI1, YNR1, GAP, ACT, РМА1, АОХ, MAL, АМО, TEF1, РЕХ14, РЕХ11 [FEMS Yeast Research, 2005, 5, 1079-1096; Curr Microbiol., 2014, 69, 143-148; FEMS Microbiol Lett., 2018, 365, 1-6; FEMS Yeast Res., 2012, 12, 271-278].
В качестве сигнальных пептидов используют лидерную последовательность PHO1, пре-про-лидерную последовательность MFa из Saccharomyces cerevisiae или Ogataea thermomethanolica, GAM1 из Schwanniomyces occidentalis [FEMS Yeast Research, 2005, 5, 1079-1096; Curr Microbiol., 2014, 69, 143-148; Appl Biochem Biotechnol., 2016, 178, 710-724].
В качестве терминаторов транскрипции используют МОХ, AMO1, PHO5, АОХ1 [Appl. Microbiol. Biotechnol., 2000, 54, 741-750; FEMS Yeast Res., 2012, 12, 271-278; FEMS Yeast Research, 2003, 4, 185-193; FEMS Yeast Research, 2003, 4, 175-184].
В качестве селективных маркеров используют любые подходящие маркеры, например, гены резистентности к антибиотикам зеоцину, генетицину (G418), гигромицину В, норзеотрицину или бластицидину а также гены комплементирующие ауксотрофные мутации в геноме дрожжей рода Ogataea, например, LEU2, HIS3, TRP3, ADE2, URA3, МЕТб, ADE11 [FEMS Yeast Res., 2012, 12, 271-278; Yeast, 1995, 11, 343-353].
В качестве последовательностей, обеспечивающих эффективную трансформацию и автономную репликацию, используют HARS1, HARS2, HARS3, HARS 36 [Mol. Gen Genet. 1986, 202, 302-308; Yeast, 1995, 11, 343-353; Journal of Bacteriology, 1996, 178 (15), 4420-4428].
В качестве плечей для гомологичной интеграции используют, в частности, последовательности генов МОХ, TRP, URA3, LEU2, GAP, кластер генов для рибосомальной ДНК, HARS, АМО, TEF1 [FEMS Yeast Research, 2005, 5, 1079-1096; FEMS Yeast Research, 2003, 4, 185-193; FEMS Yeast Res., 2012, 12, 271-278] или другие последовательности, гомологичные участкам хромосомы дрожжей рода Ogataea.
Синтетический ген MANS размером 1032 п.н. с проведенной нами оптимизацией ко донов для метил отрофных дрожжей синтезирован в компании ООО «Иннова плюс» (Санкт-Петербург) по заказу НИЦ «Курчатовский институт»-ГосНИИгенетика. Нуклеотидная последовательность синтетического гена MANS приведена в перечне последовательностей под номером SEQ ID NO:1.
Ген MANS кодирует белок ManS, который по последовательности аминокислот наиболее близок к β-маннаназам из бактерий рода Bacillus subtilis. На основании анализа, проведенного с использованием программы BLAST, установлено, что β-маннаназа ManS идентична β-маннаназам из Bacillus subtilis MAFIC-SI 1 [GenBank accession number: JX426102], Bacillus subtilis WL-7 [GenBank accession number: AAT27435], Bacillus subtilis 168 [GenBank accession number: CAB 12407] на 97.4-97.7%.
β-Маннаназа из Bacillus subtilis MAFIC-SI 1 экспрессирована в дрожжах Pichia pastoris. Ген β-маннаназы mannS (1029 п. н.) из Bacillus subtilis MAFIC-SI 1 с адаптированными кодонами для дрожжей Pichia pastoris кодирует полипептид размером 342 аминокислоты (расчетный мол. вес 38.7 кДа). Рекомбинантный белок имеет молекулярный вес около 40 кДа. Фермент показал максимальную активность при рН 6.0 и температуре 50°С, удельная активность 3706 ед./мг. Кинетические параметры Km и Vmax определены как 8 мг/мл и 20000 ед./мг, соответственно [Appl Biochem Biotechnol. 2013,169, 2326-2340. DOI 10.1007/sl2010-013-0156-8].
β-Маннаназа из Bacillus subtilis WL-7, продуцируемая клетками Escherichia coli, -фермент с молекулярным весом 38 кДа - проявляет максимальную активность при рН 6.0 и температуре 55°С, удельная активность 10080 ед./мг [J. Microbiol. Biotechnol. 2004, 14(6), 1295-1302].
β-Маннаназа из Bacillus subtilis 168 (1011 п.н., 336 аминокислот, молекулярный вес 38 кДа) проявляет оптимальную активность при рН 6.0-6.5 и температуре 40-45°С [WO 1999/64573].
Изобретение проиллюстрировано следующими фигурами.
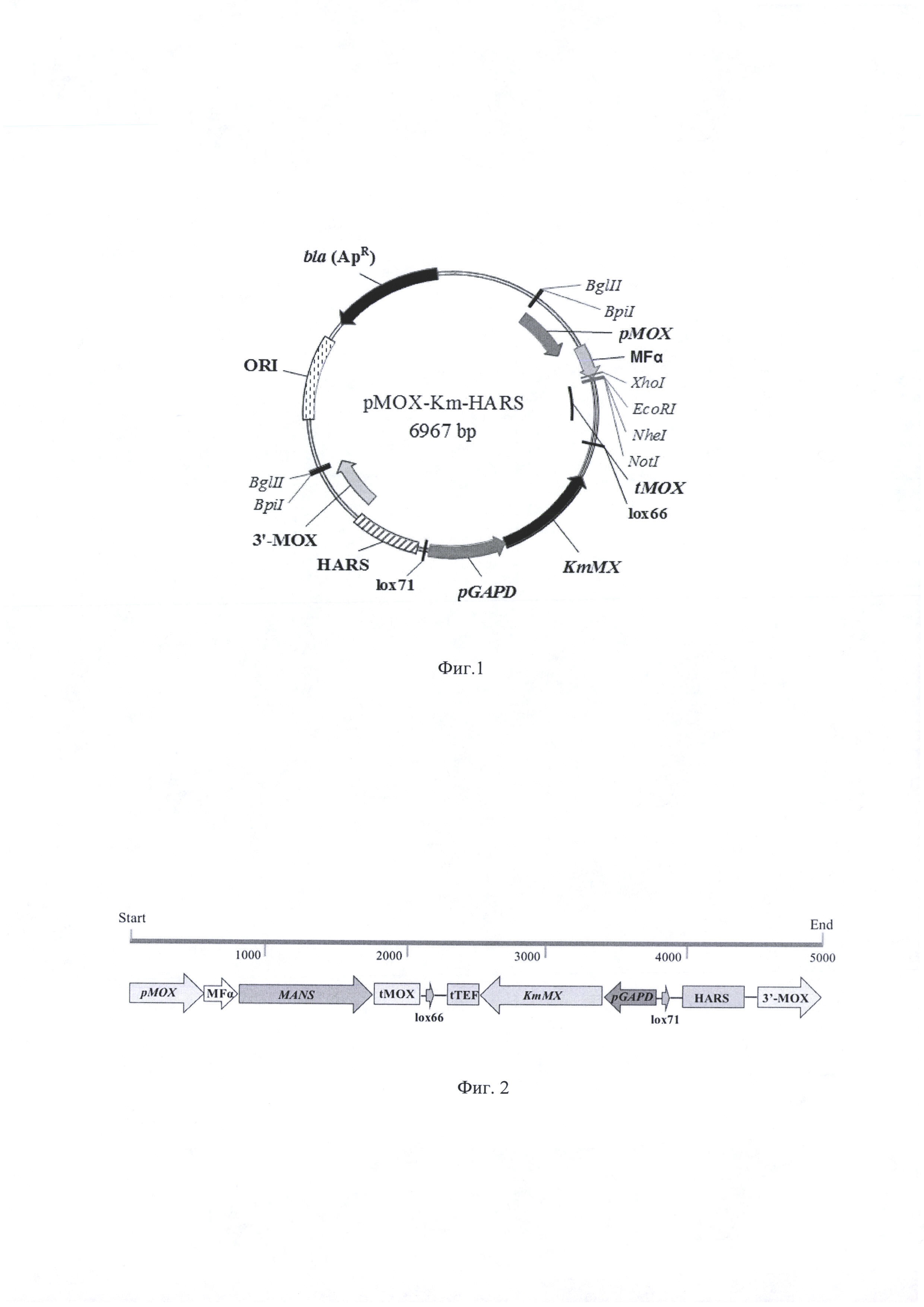
Фиг. 1. Экспрессионный вектор pMOX-Km-HARS
Фиг. 2. Экспрессионная кассета.
Фиг. 3 Зависимость активности β-маннаназы от рН и стабильность фермента при разных значениях рН.
Фиг. 4 Зависимость активности β-маннаназы от температуры и стабильность фермента при разной температуре.
Пример 1. Конструирование трансформантов дрожжей Ogataea haglerorum, содержащих оптимизированный ген, кодирующий β-маннаназу из Bacillus subtilis
Ген MANS амплифицируют с матрицы методом ПЦР с использованием олигонуклеотидов manS-F и manS-R:
manS-F: 5'-ctgaattcagatctagatctgaagctcac-3',
manS-R: 5'-cagcggccgcttactactcaacgattggagtc-3'.
Амплификацию проводят в присутствии Кара-полимеразы (KapaBiosystems, США) при следующих условиях:
1 цикл: 98°С - 2 мин.
35 циклов: 98°С - 20 с, 53°С - 15 с, 72°С - 60 с
1 цикл: 72°С - 3 мин.
Полученную последовательность ДНК по сайтам EcoRI и NotI встраивают в состав экспрессионного вектора pMOX-Km-HARS (рис 1), созданного на основе коммерческого вектора pBluescript II KS+(Х52327, Stratagene) [Биотехнология, 2019, 35 (6), 51-56].
Получают плазмиду, содержащую экспрессионную кассету (фиг. 2), в состав которой входят следующие генетические элементы.
1. Синтетический ген MANS, встроенный в рамку считывания с нуклеотидной последовательностью сигнального пептида MFα из дрожжей Saccharomyces cerevisiae, транскрипция которого находится под контролем промотора рМОХ, наработанного с хромосомной ДНК из штамма Ogataea polymorpha ВКПМ Y-1546 (линия CBS4732);
2. Терминатор транскрипции tMOX, наработанный с хромосомной ДНК из штамма Ogataea polymorpha ВКПМ Y-1546;
3. Дрожжевой селективный маркер KmMX, фланкированный сайтами 1ох66 и 1ох71, транскрипция которого находится под контролем промотора pGAPD гена глицеральдегид-3-фосфат дегидрогеназы, наработанного с хромосомной ДНК из штамма Ogataea polymorpha ВКПМ Y-1546, и терминатора транскрипции tTEF. Маркер КтМХ обеспечивает устойчивость дрожжей Ogataea haglerorum к антибиотику генетицину (G418);
4. Последовательность HARS, наработанная с хромосомной ДНК из штамма Ogataea polymorpha ВКПМ Y-916 (линия DL1), обеспечивающая сохранение трансформируемой ДНК в клетках реципиентного штамма и являющаяся возможным местом интеграции;
5. Область интеграции - нуклеотидная последовательность 3'- области региона МОХ.
Экспрессионную кассету трансформируют в штамм Ogataea haglerorum ВКПМ Y-2584, который предварительно выращивают в жидкой питательной среде YP (мас. %: дрожжевой экстракт - 1, пептон - 2, вода - остальное) с добавлением глюкозы (2 мас. %) при 37°С в течение 6 ч до достижения культурой оптической плотности (OD600) 1,5. Клетки собирают центрифугированием (здесь и далее 6000 об/мин.) в течение 10 мин. при комнатной температуре, ресуспендируют в буфере TED состава: 100 мМ Tris-HCl, 50 мМ EDTA, рН 8.0, 25 мМ дитиотрейтола в 1 л воды SQ, инкубируют при 37°С в течение 15 мин. и собирают центрифугированием в течение 10 мин. при комнатной температуре. Далее клетки промывают дважды холодным буфером STM состава: 270 мМ сахароза, 10 мМ Tris-HCl, рН 8.0, 1 мМ MgCh в 1 л воде SQ, собирают центрифугированием в течение 10 мин при температуре 5°С. Обработанные таким образом клетки ресуспендируют в холодном растворе STM в концентрации 1-5×109 клеток на 1 мл. Аликвоту объемом 60 мкл клеточной суспензии переносят в охлажденный эппендорф, добавляют 500 нг ДНК экспрессионной кассеты и инкубируют во льду 5 минут.Смесь клеток и ДНК переносят в предварительно охлажденную кювету для электропорации. Электропорацию проводят при 1500 В, 200 Ом, 25uF. После электропорации к клеткам добавляют 1 мл жидкой среды YP с глюкозой (2 мас. %), переносят клеточную суспензию в стерильные пробирки на 1,5 мл и инкубируют при 37°С в течение 60 мин. при качании.
Селекцию трансформантов проводят на агаризованной среде YP с глюкозой (2 мас. %) и генетицином (G418) в количестве 200 мкг/мл при температуре 37°С в течение 4-х суток.
Для последующего отбора трансформантов с наибольшей активностью β-маннаназы осуществляют их культивирование в пробирках в жидкой среде YP с глюкозой (2 мас. %) и генетицином (0,02 мас. %) при 37°С в течение 24 ч на качалке (250 об/мин). Затем проводят индукцию метанолом, который добавляют дважды в количестве 3 об. % через 24 и 48 ч культивирования при 37°С на качалке (250 об/мин). Общее время культивирования 6 дней. В качестве контроля используют штамм Ogataea haglerorum ВКПМ Y-2584, содержащий экспрессионный вектор pMOX-Km-HARS.
Активность β-маннаназы в культуральной жидкости (КЖ) определяют методом ДНС с использованием динитросалициловой кислоты [Anal. Chem., 1959, 31 (3), 426-428], используя маннозу как стандарт. В качестве субстрата используют галактоманнан Locust bean gum (LBG, Sigma, США). Стандартная реакционная смесь состоит из 0,1 мл 1% раствора субстрата в 0,1М ацетатном буфере, рН 5,0 и 0,1 мл рабочего раствора анализируемого образца. Рабочий раствор анализируемого образца готовят из КЖ путем разведения ее дистиллированной водой таким образом, чтобы значение оптической плотности при длине волны 540 нм (OD540) находилось в пределах рабочей зоны градуировочного графика. Реакционную смесь инкубируют при 45°С в течение 10 мин, затем добавляют 0,3 мл раствора ДНС и инкубируют при 98°С в течение 5 мин. Оптическую плотность OD540 измеряют в плашке на 96 лунок на спектрофотометре Multiskan spectrum (Thermo scientific).
За единицу ферментативной активности маннаназы (1 ед.) принимают количество фермента, действующего на субстрат с высвобождением 1 μМ восстанавливающих Сахаров (маннозы) за одну минуту.
12 независимо отобранных трансформантов культивируют в пробирках и определяют активность β-маннаназы в бесклеточной культуральной жидкости (КЖ). Результаты определения приведены в табл.1. В КЖ контрольного образца - штамма ВКПМ Y-2584, содержащего экспрессионный вектор pMOX-Km-HARS, активность β-маннаназы не тестируется.

По результатам ферментации отбирают трансформант Т1 с наибольшей активностью β-маннаназы в КЖ.
Трансформант Т1 растят в неселективных условиях, в жидкой среде YP с глюкозой (2 мас. %), в пробирках на качалке при 37°С в течение 24 ч, затем производят пять последовательных пересевов культуры из неселективных условий в пробирки со свежей средой YP, содержащей глюкозу (2 мас. %), культивируя каждый раз при тех же условиях, после чего рассевают культуру до отдельных колоний на чашки Петри с агаризованной неселективной средой YP, содержащей глюкозу (2 мас. %). С помощью репликатора отбирают 100 независимых колоний и анализируют их на способность расти на среде YP с глюкозой (2 мас. %) и генетицином (200 мкг/мл) и контрольной среде - YP с глюкозой (2 мас. %). Появление отдельных колоний, не растущих на селективной среде с антибиотиком, указывает на то, что экспрессионная кассета содержится в клетках трансформанта Т1 в виде автономно-реплицирующейся ДНК.
Далее проводят селекцию на стабилизацию (многокопийную интеграцию) экспрессионной кассеты. Трансформант Т1 инкубируют в жидкой среде YP с глюкозой (2 мас. %) при 37°С в течение 24 ч на качалке (250 об/мин.). Переносят 1/10 объема культуры в свежую жидкую среду YP с глюкозой (2 мас. %) и инкубируют при 37°С в течение 24 ч на качалке (250 об/мин.). Затем 1/50 объема культуры переносят в колбу с 50 мл селективной среды YP с глюкозой (2 мас. %) и генетицином (200 мкг/мл) и инкубируют при 37°С в течение 24 ч на качалке (250 об/мин.). Затем рассевают культуру до отдельных колоний на чашки с селективной средой YP с глюкозой (2 мас. %) и разной концентрацией генетицина (200, 400 и 600 мкг/мл). Через 3-е суток инкубации при 37°С наблюдают появление гетерогенных по размеру колоний. Отбирают колонии крупного размера, клетки которых стабильно наследуют способность сохранять устойчивость к генетицину после продолжительного роста культуры в неселективных условиях. Отобранные колонии культивируют в пробирках в неселективных условиях с индукцией метанолом и определяют активность β-маннаназы и количество секретируемого белка (табл. 2).


Как следует из результатов, представленных в табл.2, полученные трансформанты стабильно сохраняют устойчивость к генетицину после продолжительного роста культуры в неселективных условиях, и при этом обладают сравнимой или большей активностью β-маннаназы по сравнению с трансформантом Т1.
Наилучшими показателями по активности β-маннаназы и количеству секретируемого в КЖ белка, обладает трансформант Ogataea haglerorum N107.
Пример 2. Получение β-маннаназы при культивировании трансформанта Ogataea haglerorum N107 в колбах
Посевную культуру готовят в пробирках в 5 мл среды YP с глюкозой (2 мас. %). Пробирки инкубируют при 37°С в течение 24 ч на качалке (250 об/мин). В колбу на 0,75 л с 50 мл жидкой среды YP с глюкозой (2 мас. %) переносят 5 мл посевной культуры и колбу инкубируют при 37°С на качалке (250 об/мин.) в течение 6 дней. Метанол (3 об. %) добавляют к культуре через 24 и 48 часов культивирования. Биомассу отделяют центрифугированием в течение 15 мин.
Культуральную жидкость без биомассы (КЖ) используют для определения активности β-маннаназы по методу ДНС и определения количества секретируемого белка по методу Бредфорд с использованием кита Quick Start Bradford Protein Assay (Bio-Rad, США).
Рекомбинантный трансформант продуцирует белок в количестве 1.0±0.2 мг/мл, активность неочищенного фермента β-маннаназы составляет 12000±500 ед./мл КЖ.
Пример 3. Характеристика рекомбинантной β-маннаназы
Для определения оптимального значения рН для функционирования фермента активность β-маннаназы по отношению к субстрату LBG (галактоманнан Locust bean gum, Sigma, США) измеряют в диапазоне значений рН 1.0-10.0 с использованием 0.1М растворов цитратного (рН 1.0-3.0), ацетатного (рН 4.0-5.0), фосфатного (рН 6.0-8.0) и боратного (рН 9.0-10.0) буферов. Реакцию проводят при температуре 45°С в течение 10 мин. Относительную активность рассчитывают как процент от средней максимальной активности фермента, измеренной в трех независимых реакциях в диапазоне значений рН 1.0-10.0. Для функционирования β-маннаназы, синтезированной дрожжами Ogataea haglerorum, содержащими ген MANS, оптимальными являются значения рН 5.0-6.0 (фиг.3).
Стабильность полученной β-маннаназы при разных рН определяют путем измерения остаточной активности (в %) после инкубации фермента в течение 24 ч при температуре 35°С в 0,1М буферных растворах с рН 1.0-10.0. Реакцию с субстратом LBG проводят при рН 5.0 и температуре 45°С в течение 10 мин. Остаточную активность (стабильность фермента) рассчитывают, как процент от активности образца фермента (хранится при +5°С в холодильнике), измеренной в 0,1 М ацетатном буфере (рН 5.0) и температуре 45°С (фиг. 3).
Установлено, что фермент стабилен при значениях рН от 5.0 до 10.0 (сохраняет более 90% активности). В кислой области рН от 1.0 до 3.0 фермент сохраняет около 30% активности, при рН 4.0 - 75% активности.
Для определения температурного профиля активности фермента β-маннаназы проводят реакции образцов с субстратом LBG в 0.1 М ацетатном буфере (рН 5.0) в диапазоне температур от 25 до 80°С с шагом 5°С. Относительную активность рассчитывают, как процент от средней максимальной активности фермента, измеренной в трех реакциях в диапазоне значений температур от 25 до 80°С. Результаты приведены на фиг. 4.
Установлено, что фермент проявляет максимальную активность при температуре 55°С. В интервале температур 35-45°С (температура тела животного) фермент сохраняет 45-65% активности. При температурах выше 65°С активность фермента значительно падает.
Перед определением термостабильности β-маннаназы образцы выдерживают в 0.1 М ацетатном буфере (рН 5.0) при температурах от 25°С до 60°С с шагом 5°С в течение 24 ч. Реакцию с субстратом проводят при температуре 45°С в течение 10 мин. Остаточную активность (стабильность фермента) рассчитывают, как процент от наибольшей активности фермента.
Фермент проявляет высокую стабильность (сохраняет более 90% активности) в диапазоне температур 25-40°С (фиг. 4), близкой к температуре желудочно-кишечного тракта животных.
Для определения молекулярного веса полученной β-маннаназы проводят электрофоретическое разделение белков из образца КЖ в 12% полиакриламидном геле в денатурирующих условиях (SDS-PAGE) в камере для вертикального электрофореза Mini-PROTEAN Tetra Bio-Rad (Bio-Rad США). Для визуализации белков используют Кумасси бриллиантовый синий R250.
Установлено, что β-маннаназа, синтезированная трансформантом Ogataea haglerorum N107, имеет молекулярный вес 40 кДа (фиг. 5).
Таким образом, заявляемый трансформант дрожжей Ogataea haglerorum, содержащий в составе хромосомы оптимизированную последовательность гена MANS, проявляет стабильность и продуцирует рекомбинантную β-маннаназу, обладающую высокой удельной активностью, проявляющую максимальную активность при рН 5.0-6.0 и температуре 55°С, стабильную при значениях рН от 5.0 до 10.0 и в диапазоне температур ниже 40°С.
Пример 4. Получение β-маннаназы при культивировании трансформанта Osataea haslerorum N107 в ферментере
Из суточной биомассы трансформанта Ogataea haglerorum N107 с чашки Петри со средой YP с глюкозой (2 мас. %) готовят суспензию клеток в стерильной дистиллированной воде, определяют оптическую плотность клеточной суспензии (OD600). В качалочные колбы объемом 750 мл с рабочим объемом 110 мл жидкой посевной среды YP с глюкозой (2 мас. %) вносят суспензию клеток до получения OD600 равной 0.1. Колбы инкубируют при температуре 37°С на качалке при 220 об/мин. до достижения культурой оптической плотности равной 12.
Основную ферментацию проводят в ферментере КФ-103 (ООО-фирма «Проинтех») объемом 3 л на среде, состав которой указан в табл. 3.


Состав раствора микроэлементов РТМ1 указан в табл. 4.

Исходный объем жидкости в ферментере составляет 1 л. Культивирование проводят при следующих параметрах: температура 37°С; начальное перемешивание 500 об/мин., аэрация 1.0 л/мин., рН 4.6 поддерживается титрованием 25% водным раствором аммиака. Значение рО2 поддерживают на уровне 20.0% (от насыщения среды воздухом) с использованием каскадной регулировки скорости вращения мешалки.
В рабочий ферментер вносят культуру, выращенную на качалке в колбах, до стартового значения оптической плотности равной 1.8. Наращивание биомассы осуществляют в два этапа. На первом этапе проводят рост биомассы на глюкозе, введенной в ферментер с начальной средой (16 часов). На втором этапе производят наращивание биомассы до значения сырого веса 18±1 (мас. %) путем подачи в ферментер глюкозной подпитки состава (мас. %): глюкоза - 28.6, раствор микроэлементов РТМ1 -1.1 (об./об.), биотин - 0.0004, вода - остальное.
Далее в ферментер со скоростью 1,2 г/ч на л подают раствор метанольной подпитки состава (мас. %): метанол - 95.9, раствор микроэлементов РТМ1 - 1.4 об./об., биотин - 0.00054, вода - остальное. Индукцию метанолом продолжают в течение 134 ч.
Во время культивирования отбирают образцы КЖ для определения активности маннаназы при рН 5.0 и температуре 55°С по методу ДНС [Anal. Chem., 1959, 31 (3), 426-428]. Концентрацию белка в отобранных образцах КЖ определяют по методу Бредфорд с использованием кита Quick Start Bradford Protein Assay (Bio-Rad, США). Результаты приведены в табл. 5

Таким образом, при культивировании в 3-х литровом ферментере трансформант Ogataea haglerorum N107 продуцирует 4.25 мг/мл белка, при этом активность β-маннаназы через 160 ч культивирования при 37°С составляет 51066 ед./мл КЖ.
Отобранный трансформант Ogataea haglerorum N107 депонирован в Биоресурсном центре Всероссийская Коллекция Промышленных Микроорганизмов (БРЦ ВКПМ) НИЦ «Курчатовский институт» - ГосНИИгенетика (117545 Москва, 1-ый Дорожный проезд, д. 1) как Ogataea haglerorum N107 ВКПМ Y-4639.
Штамм характеризуется следующими признаками:
Культурально-морфологические характеристики заявляемого штамма:
При культивировании при температуре 37°С в течение 48 ч на агаризованной среде YP (мас. %: дрожжевой экстракт - 1, пептон - 2, агар - 2, вода - остальное) с добавлением глюкозы - 2 (мас. %) клетки имеют овальную форму, 3-4 мкм в диаметре. Клетки почкуются, при этом почкование истинное, многостороннее. Истинного мицелия не образуют.
Споруляция происходит при инкубации культуры на агаризованной среде следующего состава (мас. %): хлорид калия - 0.5, ацетат натрия - 1.0, агар - 2.0, вода - остальное при 25°С в течение 3-4 дней. Аски имеют тетраэдрическую форму, включают 4 аскоспоры.
На агаризованной среде YP с добавлением глюкозы (2, мас. %) колонии светло-бежевого цвета с ровным краем, матовой поверхностью, линзовидным профилем и пастообразной консистенцией.
При росте в жидкой среде YP (мас. %: дрожжевой экстракт - 1, пептон - 2, вода -остальное) с добавлением глюкозы - 2 (мас. %), при 37°С в течение 24 ч культивирования - жидкость мутная, осадок белый, коагуляции не наблюдается, пристеночных пленок не образует.
Физиолого-биохимические признаки заявляемого штамма:
Штамм способен к росту как в аэробных, так и в анаэробных условиях.
В качестве единственного источника углерода штамм способен использовать глюкозу, глицерин, метанол, этанол, L-рамнозу, сахарозу, мальтозу; не способен ассимилировать D-глюконат, L-арабинозу, сукцинат, лактозу, крахмал.
Штамм способен синтезировать β-маннаназу при культивировании в жидкой среде YP в присутствии глюкозы, биосинтез фермента усиливается при культивировании в присутствии метанола.
--->
Перечень последовательностей
<110> Федеральное государственное бюджетное учреждение "Государственный
научно-исследовательский институт генетики и селекции промышленных
микроорганизмов Национального исследовательского центра "Курчатовский
институт" (НИЦ «Курчатовский институт» - ГосНИИгенетика).
State Research Institute for Genetics and Selection of Industrial
Microorganisms of National Research Center «Kurchatov Institute»
(NRC «Kurchatov Institute» – GOSNIIGENETIKA).
<120> Трансформант дрожжей Ogataea haglerorum, продуцирующий
бета-маннаназу, содержащий в составе хромосомы синтетический ген MANS
<130> 20-02
<160> 1
<210> 1
<211> 1032
<212> DNA
<213> Artificial Sequence
<220>
<223> синтетический ген MANS, кодирующий бета-маннаназуManS из Bacillus
subtilis
<400> 1
agatctagat ctgaagctca cactgtttcc ccagtgaacc caaacgctca acaaactact 60
aagactgtta tgaactggtt ggctcacttg ccaaacagaa ctgaaaacag agttttgtcc 120
ggtgctttcg gtggttactc tcacgacact ttctccatgg ctgaggctga cagaatcaga 180
tctgctactg gtcaatcccc agctatctac ggttgtgact acgctagagg ttggttggag 240
actgctaaca tcgaggacac tatcgacgtt tcttgtaacg gagacttgat gtcctactgg 300
aaaaacggtg gtatcccaca aatctctttg cacttggcta acccagcttt ccaatccggt 360
cacttcaaga ctccaatcac taacgaccaa tacaagaaaa tcttggactc ttccactgct 420
gagggtaaga gattgaacgc tatgttgtcc aagatcgctg acggtttgca agagttggag 480
aaccaaggtg ttccagtttt gttcagacca ttgcacgaga tgaacggtga gtggttctgg 540
tggggtttga cttcttacaa ccaaaaggac aacgagagaa tctccttgta caagcaattg 600
tacaagaaaa tctaccatta catgactgac actagaggtt tggaccactt gatctgggtt 660
tactctccag acgctaacag agacttcaag actgacttct acccaggtgc ttcctacgtt 720
gacatcgttg gtttggacgc ttacttccaa gacgcttact ccatcaacgg ttacgaccaa 780
ttgactgctt tgaacaaacc attcgctttc acagaggttg gtccacaaac tgctaacggt 840
tctttcgact actccttgtt catcaacgct atcaagcaaa gatacccaaa gactatctac 900
ttcttggctt ggaacgacga gtggtctcca gctgttaaca agggtgcttc tgctttgtac 960
cacgactcct ggactttgaa caagggtgag atttggaacg gtgactcctt gactccaatc 1020
gttgagtagt aa 1032
<---
Реферат
Изобретение относится к биотехнологии. Предложен трансформант дрожжей Ogataea haglerorum, продуцирующий β-маннаназу ЕС 3.2.1.78 из Bacillus subtilis, содержащий в составе хромосомы оптимизированный синтетический ген, кодирующий указанную β-маннаназу, нуклеотидная последовательность которого приведена в перечне последовательностей под номером SEQ ID NO: 1. Изобретение обеспечивает расширение арсенала рекомбинантных микроорганизмов, продуцирующих β-маннаназу. 4 ил., 5 табл., 4 пр.

Комментарии