Гетеротелехелатный блок-сополимер и способ его получения - RU2169742C2
Код документа: RU2169742C2
Чертежи









Описание
Настоящее изобретение относится к гетеротелехелатному блок-сополимеру, который имеет различные функциональные группы на обоих концах молекулы, к способу его получения и к его применению для получения высокомолекулярной мицеллы. Более конкретно, в этом изобретении описан полимер, который имеет различные функциональные группы на обоих концах молекулы и в то же время содержит в основной цепи полиэтиленоксид в качестве гидрофильного сегмента и полиэфир в качестве гидрофобного сегмента.
В этом изобретении термин "полимер" включает в себя олигомер.
Уровень техники
В настоящее
время высокомолекулярные мицеллы или наносферы, состоящие из блок-сополимера гидрофильно/гидрофобного типа, в котором гидрофильный полимер типа полиэтиленоксида сочетается с гидрофобным полимером на
молекулярном уровне, привлекают внимание в качестве носителя при подаче лекарства или т. п. Такие высокомолекулярные мицеллы и наносферы были приготовлены из блок-сополимера гидрофильно/гидрофобного
типа, в котором гидрофильный полимер типа полиэтиленоксида сочетается с гидрофобным полимером на молекулярном уровне.
Однако в традиционных способах получения блок-сополимера гидрофильно/гидрофобного типа существует ограничение на виды введенных концевых функциональных групп, причем были предложены только блок-сополимеры, в которых функциональные группы были ограничены метоксильной и гидроксильной группами. Если бы удалось осуществить введение необязательных функциональных групп на поверхность мицеллы в выбранном соотношении, то стало бы возможной разработка функциональной высокомолекулярной мицеллы, которая могла быть полезной при подаче лекарства в определенные органы.
Ближайшим аналогом настоящего изобретения является WO 95/03357, где описаны частицы, которые не выводятся быстро из кровяного потока макрофагами ретикулоендотелиальной системы и могут быть модифицированы для достижения различных скоростей высвобождения или для поступления к нужным определенным клеткам или органам. Частицы имеют биоразлагаемый твердый сердечник, содержащий биологически активный материал и поли(алкиленгликолевые) группы на поверхности.
В WO 95/03357 отмечается, что белок, например антитело, связан за счет концевой гидроксигруппы поли(алкиленгликоля), что образует поверхность частиц. В WO 95/03357, однако, не указано, не предполагается, такой блок-полимер, как в настоящем изобретении, который имеет альдегидную группу на конце поли(этиленгликоля) (отметим: ацетали легко превращаются в альдегиды в разбавленных водных кислотах).
Как хорошо понятно специалисту в данной области, альдегидная группа (-CHO) легко превращается в иминное соединение через основание Шиффа, как показано в следующем
уравнении:

Таким образом, т. к. полимер по настоящему изобретению легко может образовывать полимер-протеиновые конъюгаты посредством аминогруппы, которая существует, например, в белке, указанный полимер по настоящему изобретению может использоваться намного более удобно, например, при модификации белка, чем полимер, указанный в WO 95/03357.
Таким образом, полимер по настоящему изобретению четко отличается от предшествующего уровня техники.
Целью настоящего изобретения является разработка блок-сополимера, который имеет различные функциональные группы на обоих концах молекулы, в качестве многофункционального полимера, способного образовывать высокомолекулярную мицеллу.
Описание изобретения
Авторы настоящего изобретения установили, что можно легко получить блок-сополимер, имеющий защищенную или незащищенную
альдегидную группу на одном конце молекулы и различные функциональные группы на другом конце, когда алкиленовая производная, имеющая определенного вида альдегидную группу и гидроксильную группу,
применяется как инициатор полимеризации в живой цепи и когда в качестве мономеров полимеризуются оксид этилена и лактид или лактон.
Они также подтвердили, что полученный таким образом блок-сополимер образует высокомолекулярную мицеллу, которая вполне стабильна в водном растворителе.
Это изобретение предлагает гетеротелехелатный блок-сополимер, который имеет
различные функциональные группы на обоих концах молекулы и который представлен следующей формулой:

в которой R1 и R2 независимо означают C1-10-алкокси, арилокси или арил-C1-3-алкилокси или R1 и R2 в сочетании друг с другом означают этилендиоксигруппу (-O-CH(R')-CH2-O-, в которой R' означает атом водорода или C1-6-алкил), которая может быть замещена C1-6-алкилом, или в сочетании друг с другом означают оксогруппу (=O), L означает группу
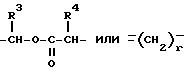
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-C1-3-алкил и r означает целое число от 2 до 5, m означает целое число от 2 до 10000, n означает целое число от 2 до 10000, p означает целое число от 1 до 5, q означает целое число от 0 до 20,
Z означает, когда q равно нулю, атом водорода, щелочной металл, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, 2-меркаптопропионил или 2-аминопропионил, или аллил, или винилбензил, означая, когда q является целым числом от 1 до 20, C1-6-алкоксикарбонил, карбоксил, меркапто- или аминогруппу.
В другом аспекте это изобретение представляет способ получения блок-сополимера указанной выше формулы (I), причем этот способ включает следующие стадии:
Стадия 1)
Инициатор полимеризации, представленный следующей формулой (II)

в которой R1-1 и R2-1 независимо означают C1-10-алкоксигруппу или в сочетании друг с другом означают этилендиоксигруппу, которая может быть замещена C1-6 -алкилом, p означает целое число от 1 до 5 и M означает шелочной металл,
заставляют взаимодействовать с этиленоксидом таким образом, чтобы можно было получить соединение, представленное следующей формулой (III):

в которой R1-1, R2-1, p и M - такие, как определено в формуле (II), и m означает целое число от 2 до 10000.
Стадия 2)
Соединению формулы (II) дают прореагировать с лактидом или лактоном, который представлен следующей
формулой (III-a) или (III-b):
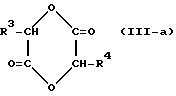
или
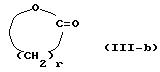
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-C1-3-алкил и r означает целое число от 2 до 5,
таким образом, чтобы можно было получить соединение, представленное следующей формулой (IV):

в которой L означает группу
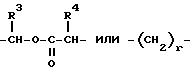
и R1-1, R2-1, p, m и M - такие, как определено выше.
Указанная выше стадия обеспечивает получение живой цепи полимера этого изобретения (который включен в полимер формулы (I)), которая применяется в качестве промежуточного соединения для дальнейшего наращивания некоторого количества полимерного сегмента и т.п.
Стадия 3)
i) Алкоксид щелочного металла формулы
(IV) селективно гидролизуют, получая блок-сополимер следующей формулы (V):
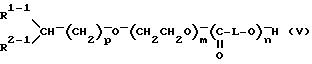
в которой R1-1, R2-1, p, m, L и n - такие, как определено выше; или
ii) блок-сополимер формулы (IV) полностью гидролизуют, получая блок-сополимер следующей формулы (VI):
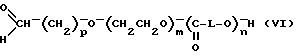
в которой p, m, L и n - такие, как определено выше.
Указанная выше стадия обеспечивает получение блок-сополимера этого изобретения, который имеет защищенную альдегидную группу или собственно альдегидную группу в начале полимерной цепи (α-терминальная группа) и гидроксильную группу в конце цепи (ω-терминальная группа).
Стадия 4)
Блок-сополимеру формулы (V), который имеет защищенную альдегидную группу в начале полимерной цепи, дают
прореагировать с
i) уксусной кислотой, акриловой кислотой, метакриловой кислотой, коричной кислотой или паратолуолсульфоновой кислотой, или их реакционноспособными производными, или
ii) аллилгалогенидом, или винилбензилгалогенидом, или
iii) галогенидом, представленным следующей формулой (VII):

в которой X представляет собой атом хлора, брома или иода, q' является целым числом от 1 до 20 и Z' является C1-6-алкоксикарбонилом или защищенной аминогруппой;
с образованием блок-сополимеров этого изобретения, каждый из которых имеет соответствующие функциональные группы, отличающиеся от гидроксильной группы, в ω-конце цепи макромолекулы.
Стадия 5)
Полученный на стадии 4)-i) эфир паратолуолсульфоновой кислоты может быть подвергнут дальнейшему превращению, посредством трансэтерификации, в
блок-сополимер, имеющий другие функциональные группы (например, меркапто- или амино-) в конце полимерной цепи (ω). Блок-сополимер, который имеет альдегидзащищающую группу или
карбоксилзащищающую группу и который был получен по указанным выше стадиям, может быть превращен посредством гидролиза в блок-сополимер этого изобретения, в котором одна из защищающих групп или все
защищающие группы удалены.
В соответствии с другим замыслом это изобретение обеспечивает высокомолекулярную мицеллу на основе использования блок-сополимера формулы (I).
Часть полученного таким образом гетеротелехелатного полимера настоящего изобретения может применяться в качестве исходного вещества для получения другого полимера. Как будет видно из составляющих их компонентов, можно ожидать, что эти полимеры будут обладать биологическим сродством и высокой биологической пригодностью. Поэтому они могут использоваться для производства материалов, непосредственно вводимых в живые организмы, таких как носитель для подачи лекарств. Сверх того, в соответствии с третьим замыслом изобретения оно представляет высокомолекулярную мицеллу, которая вполне стабильна в водном растворителе. Поэтому полимер этого изобретения также является эффективным для подачи лекарств в определенные органы.
Краткое описание чертежей
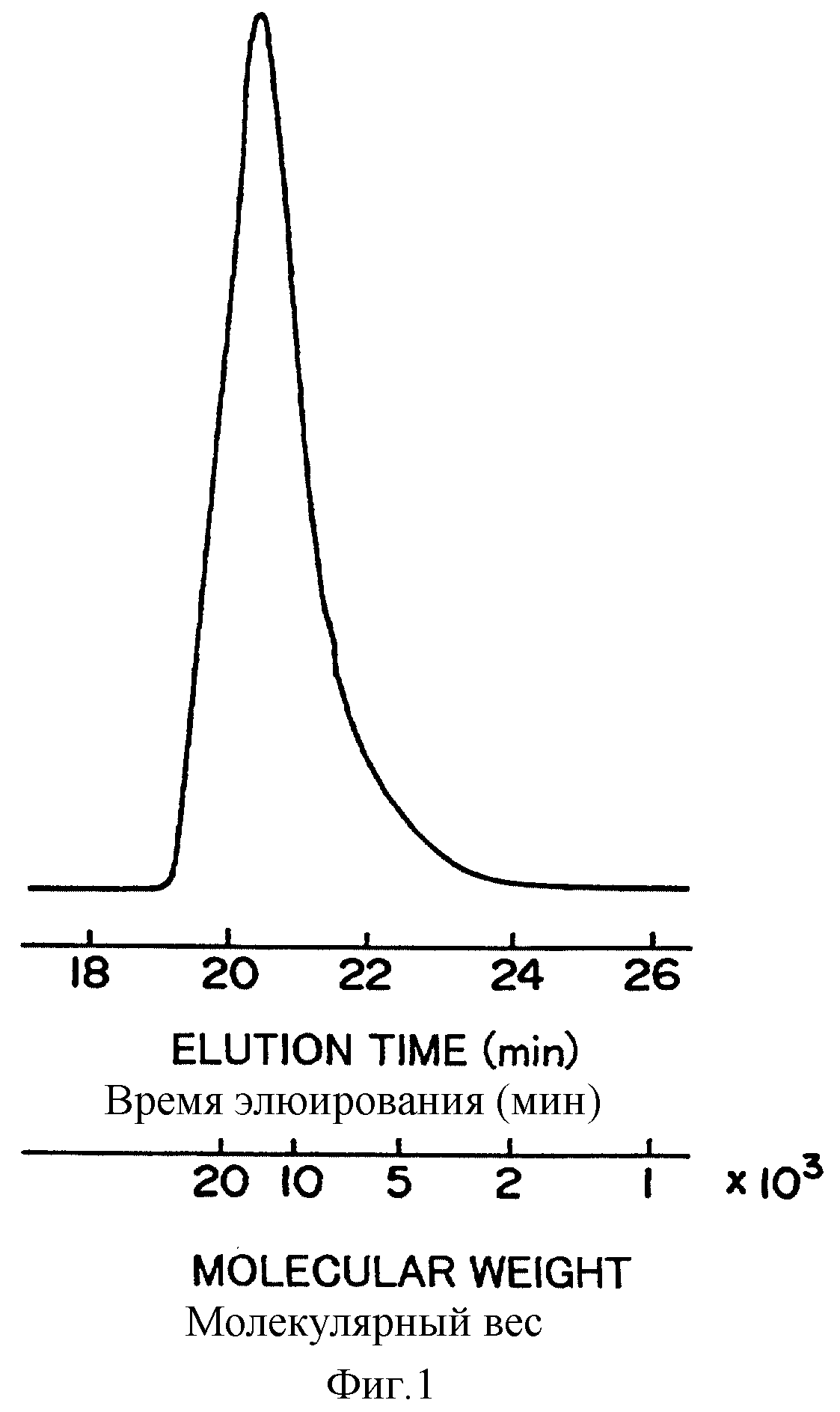
На фиг. 1 приведена
гель-проникающая хроматограмма для полиэфироксид/полилактидного блок-сополимера с ацетальной

Рабочие условия: Ти - Эс - Кей - Гель (G4000HXL, G3000HXL, G2500HXL)
Элюент: тетрагидрофуран,
содержащий 2% триэтиламина
Скорость потока: 1 мл/мин
На фиг. 2 представлен спектр ядерного протонного магнитного резонанса (ПМР) полиэтиленоксид/полилактидного блок-сополимера с
ацетальной α-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 1).
На фиг. 3 представлен спектр протонного магнитного резонанса полиэтиленоксид/поли(δ-валеролактонового) блок-сополимера с ацетальной α-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 3).
На фиг. 4 представлен спектр протонного магнитного резонанса полиэтиленоксид/полилактидного блок-сополимера с альдегидной α-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 4).
На фиг. 5 представлен спектр протонного магнитного резонанса полиэтиленоксид/полилактидного блок-сополимера с ацетальной α-терминальной группой и метакрилоильной ω-терминальной группой (образец Примера 5).
На фиг. 6 представлен спектр протонного магнитного резонанса полиэтиленоксид/полилактидного блок-сополимера с ацетальной α -терминальной группой и аллильной ω-терминальной группой (образец Примера 6).
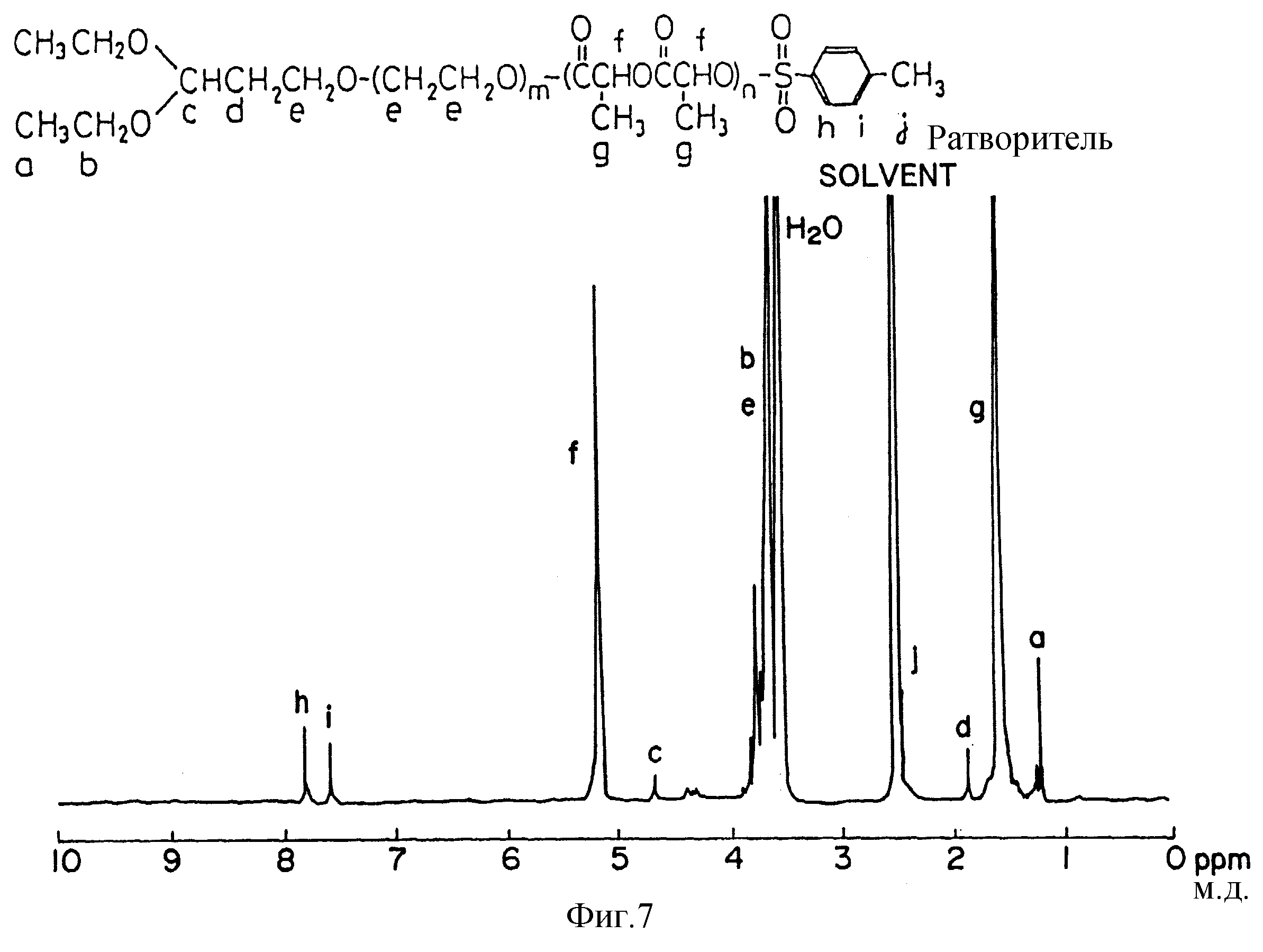
На фиг. 7 представлен спектр протонного магнитного резонанса полиэтиленоксид/полилактидного блок-сополимера с ацетальной α-терминальной группой и паратолуолсульфонильной ω-терминальной группой (образец Примера 7).
На фиг. 8 приведено распределение по размерам частиц высокомолекулярной мицеллы, найденное с использованием динамического лазерного рассеяния в водном растворе полиэтиленоксид/полилактидного блок-сополимера с альдегидной α\-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 4).
Подробное описание изобретения
В этом изобретении алкильная часть алкоксигруппы и алкил означают
алкильную группу с линейной или разветвленной цепочкой. Следовательно, алкильная часть C1-10-алкоксигруппы или C1-10-алкил в формулах (II) и (III-a) включают метил, этил, пропил,
изопропил, бутил, втор-бутил, трет-бутил, пентил, изо-пентил, гексил, 2-метилпентил, 3-метилпентил, октил, 2-этилгексил, децил и 4-пропилпентил. Из них алкильная часть в алкоксигруппе R1 и
R2 предпочтительно является алкилом C1-6, в частности алкилом C1-3.
Следовательно, особенно предпочтительные примеры алкоксигруппы R1 и R2 включают метокси-, этокси-, пропокси- и изопропокси-. Примеры R1 и R2 включают арил, особенно фенил, и арил C1-3-алкил, особенно бензил или фенетил. Эти группы могут быть одинаковыми или различными, но предпочтительно они являются одинаковыми. Хотя R1 и R2 в сочетании друг с другом может означать этилендиоксигруппу (-O-CH(R')-CH2-O-, в которой R' означает атом водорода или C1-6-алкил), которая может быть замещена C1-6-алкилом, предпочтительно они представляют собой этилендиокси-, пропилендиокси- или 1,2-бутилендиоксигруппы.
При гидролизе заместители R1 и R2 удобно объединяются с образованием оксогруппы (= O), или иными словами, с образованием блок-сополимера этого изобретения, который имеет альдегидную группу в α-терминальной части молекулы.
Знак "p" в формуле (I) означает целое число от 1 до 5. В связи
с тем, что сегмент

произведен из инициатора полимеризации (смотрите формулу (II)), в процессе этого изобретения R1, R2 и p предпочтительно выбирают таким образом, чтобы этот сегмент составлял блок ацетальной группы, такой как диметоксиметокси-, 2,2-диметоксиэтокси-, 3, 3-диметоксипропокси-, 4,4-диметоксибутокси-, диэтоксиметокси-, 2,2-диэтоксиэтокси-, 3,3-диэтоксипропокси-, 4,4-диэтоксибутокси-, дипропоксиметокси-, 2,2-дипропоксиэтокси-, 3,3-дипропоксипропокси- или 4,4-дипропоксибутокси-.
Радикалы R3 и R4 могут означать или атом водорода, или C1-10-алкил, или арил, или арил-C1-3-алкил, поскольку они пригодны для цели этого изобретения. Однако с точки зрения биологической пригодности предпочтительным является атом водорода (произведен из глутаровой кислоты) и метил (произведен из молочной кислоты).
В соответствии со способом получения с использованием полимеризации живых цепей этого изобретения знак "m" в формуле (I) теоретически может принимать любое значение, если устанавливается количественное соотношение между мономерным этиленоксидом и инициатором полимеризации. Однако для достижения цели этого изобретения, предпочтительно, m является целым числом от 2 до 10000. Для того, чтобы этот сегмент мог придать гидрофильность блок-сополимеру этого изобретения, предпочтительно, m является целым числом, равным по меньшей мере 10. С целью легкого достижения узкого молекулярно-весового распределения этого сегмента и обеспечения превосходной биологической пригодности блок-сополимера m является целым числом, равным по меньшей мере 500, предпочтительно по меньшей мере 200.
Что касается знака "n", который означает молекулярный вес полиэфирного сегмента формулы (I), его оптимальное значение изменяется в зависимости от свойств групп R3 и R4 как можно понять из того факта, что этот сегмент в основном придает гидрофобность блок-сополимеру этого изобретения. Следуя способу полимеризации этого изобретения, n может принимать любые значения, таким же образом, как в случае полиэтиленоксидного сегмента. Поэтому значение n не ограничено. Однако обычно оно составляет от 2 до 10000.
Более того, для поддержания хорошего баланса гидрофильности и гидрофобности относительно полиэтиленоксидного сегмента целое число m предпочтительно принимает значения от 10 до 200, в частности от 10 до 100.
Сегмент

Указанный выше живой полимер может легко обеспечить полимер, в котором Z означает атом водорода (или полимер, который имеет гидроксильную группу в ω-положении), так как алкоголятная часть живого полимера легко гидролизуется. Указанная гидроксильная группа может быть далее превращена в другие функциональные группы с использованием различных реакций, таких как этерификация кислотой или спиртом. Таким образом, когда q равно нулю, Z может быть ацетилом (-COCH3), акрилоилом (-COCH=CH2), метакрилоилом (-COC(CH3)=CH2), циннамоилом (-CHCH= CH-фенил) и паратолуолсульфонилом (-SO2-фенилен-CH3) и, кроме того, может быть аллилом (-CH2-CH=CH2) и винилбензилом (-CH2-фенилен-CH=CH2). Когда эти функциональные группы имеют этиленово ненасыщенную связь, с использованием указанной связи могут быть получены полимеры со свисающими цепями. Когда Z означает паратолуолсульфонильную группу, она может быть превращена в другую функциональную группу известным методом с использованием трансэтерификации. Поэтому Z может быть 2-меркаптопропионилом или 2-аминопропионилом.
Когда q является целым числом от 1 до 20, предпочтительно от 1 до 4, особенно предпочтительно 2, сегмент
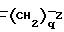
В приведенной в конце описания таблице указаны примеры блок-сополимеров этого изобретения, которые включают указанные выше заместители (или сегменты) в различных взаимных сочетаниях.
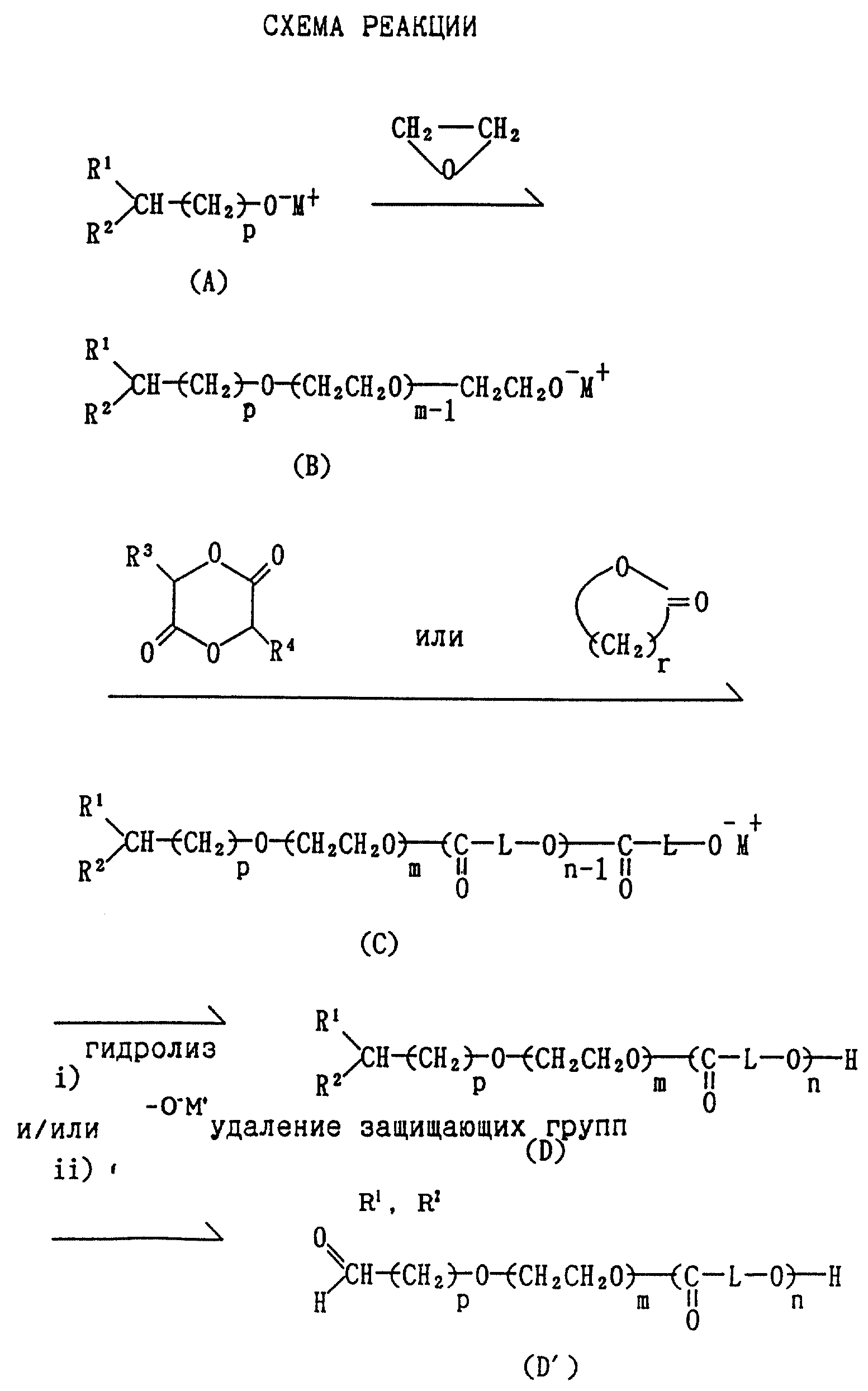
Упомянутые выше гетеротелехелатные блок-сополимеры, которые могут быть представлены этим изобретением, эффективно получаются по способу этого изобретения, который иллюстрирован схемами реакции (см. в конце описания).
Получение (B) из (A)
Ацеталь - защищенный алкоксид щелочного металла (A) заставляют взаимодействовать с этиленоксидом с образованием соединения (B), к которому
добавляется полиэтиленоксидный сегмент. Соединение (A) может быть приготовлено путем обработки ацеталь - защищенного спирта металлизирующим реагентом, таким как щелочной металл, подобный натрию или
калию; металлоорганическим соединением, подобным нафталиннатрию, нафталинкалию, кумилкалию и кумил-цезию; или гидридом металла, таким как гидрид натрия или гидрид калия.
Указанное выше превращение (A) в (B) должно протекать без растворителя или предпочтительно в безводном апротонном растворителе и в широком интервале температур, например от -50 до 300oC, предпочтительно 10-60oC, удобно при комнатной температуре (20-30oC). Эта реакция может быть проведена либо при повышенном, либо при пониженном давлении. Не ограничивающие примеры применяемых растворителей включают бензол, толуол, ксилол, тетрагидрофуран, диоксан и ацетонитрил. Не ограничивающие примеры реакторов включают круглодонную колбу, автоклав и запаянную под давлением трубку. Предпочтительно реактор запаивают герметично от воздуха и более предпочтительно его заполняют инертным газом. Концентрация реагирующей жидкости составляет от 0,1 до 95 вес.%, предпочтительно от 1 до 80 вес.%, наиболее предпочтительно от 3 до 10 вес.%.
Получение (C) из (B)
Реакционной смеси, содержащей (B), дают прореагировать с лактидом или лактоном с образованием живой
цепи блок-сополимера (C), в котором полиэфирный сегмент добавляется по ω-терминальной гидроксильной группе полиэтиленоксида. Условия этой реакции могут быть практически такими же, как для
предыдущего превращения (A) в (B). Применяемый лактид или лактон способен образовывать такую цепь, которая была определена в связи с радикалами R3 и R4 в группе L формулы (I). Не
ограничивающие примеры лактидов включают лактид молочной кислоты и лактид гликолевой кислоты. С другой стороны, примеры подходящих лактонов включают бета-пропиолактон, гамма-бутиролактон,
дельта-валеролактон и эпсилон-капролактон. Среди них предпочтительными, с точки зрения хорошей реакционной способности, являются гамма-бутиролактон и дельта-валеролактон.
В приведенных выше стадиях молярное соотношение инициатора полимеризации к этиленоксиду, лактиду или лактону составляет от 1:1 до 1:10000, более предпочтительно от 1:5 до 1:10000, наиболее предпочтительно от 1:10-200 до 1:50-200.
Способ этого изобретения не только дает возможность регулировать молекулярный вес каждого сегмента в соответствии с соотношением инициатора полимеризации к использованному маномеру, но также обеспечивает монодисперсный или мономодальный блок-сополимер, в котором каждый из полученных сегментов имеет весьма узкое молекулярно-весовое распределение.
Полученный указанным выше способом живой полимер (C) входит в объем защиты полимера этого изобретения. Однако алкоголят (C) может быть превращен i) в полимер D посредством частичного гидролиза в мягких условиях (например, просто при добавлении воды) или ii) в полимер D', который имеет альдегидную группу в α-терминальном положении и гидроксильную группу в ω -терминальном положении, посредством обработки C в условиях, в которых ацетальная группа может одновременно гидролизоваться. Эта реакция гидролиза может быть осуществлена с использованием или кислот, таких как трифторуксусная кислота, хлористоводородная кислота, серная кислота, азотная кислота, муравьиная кислота и фтористоводородная кислота, или щелочей, таких как гидроксид натрия и гидроксид калия, и в случае необходимости при нагревании.
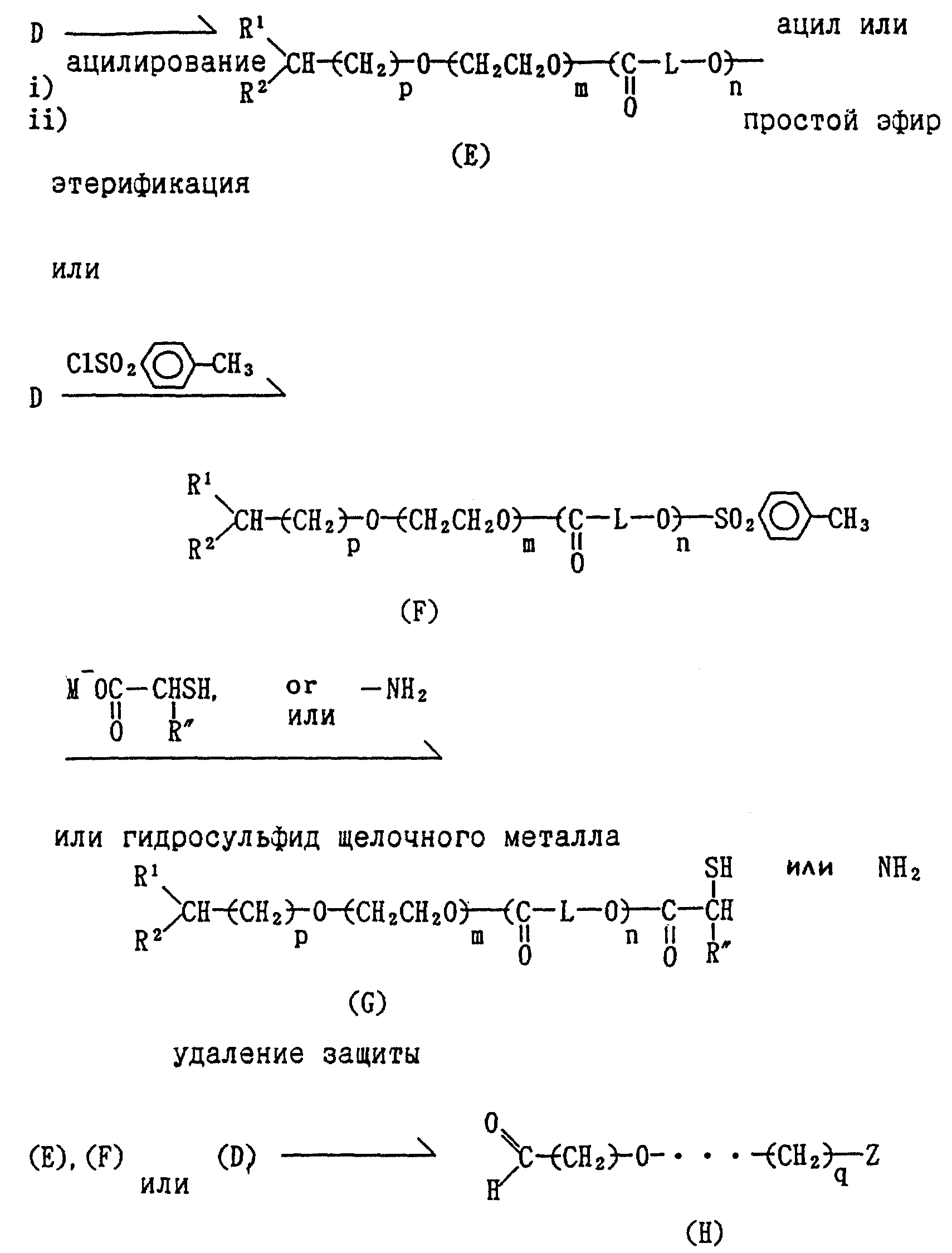
Получение (E)-(G) из (D)
Инициируют взаимодействие D с
i) уксусной кислотой, акриловой кислотой, метакриловой кислотой
или паратолуолсульфоновой кислотой с образованием ω-терминального ацильного соединения с концевой группой в ω-положении, или
ii) галогенидом, представленным формулой (V)
галоид-E,
где галоид- и E в формуле (V) соответствуют группам, отличающимся от ацильной группы в блоке
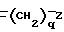
Указанные выше реакции могут быть осуществлены с использованием известных процессов этерификации кислотой или спиртом. Что касается органической кислоты в указанной выше стадии i), удобно использовать реакционноспособную производную органической кислоты, такую как ангидрид кислоты и галогенид кислоты.
Когда необходимо ввести меркаптогруппу в ω-концевую часть, то эффективным является инициирование взаимодействия паратулолсульфированного соединения F с электрофильным реагентом, таким как тиоацетат натрия, тиоацетат калия или гидросульфид калия, таким образом, чтобы тиоэфирную группу можно было ввести в ω -концевую группу, и затем эту тиоэфирную группу обрабатывают кислотой или щелочью и после этого можно получить полимер, представленный формулой G.
Когда необходимо ввести аминогруппу в ω-концевую часть, то эффективным является инициирование гидролиза соединения D с использованием электрофильного реагента, такого как N-(2-бромэтил)фтальимид, N-(3-бромпропил)фтальимид, 1-бром-2-(аминобензол)этан или N-(2-бромэтил)бензилкарбамат, и после этого проводят обработку кислотой или щелочью, для того чтобы удалить группы R1 и R2 и одновременно гидролизовать ω-концевую имидную связь, и таким образом может быть получен полимер, который содержит ω-концевую аминогруппу.
Удаление групп R1 и R2 из полимеров D, E, F и G, с целью получения альдегида с концевой группой в α-положении, может быть осуществлено в результате упомянутого выше превращения C в D'. Что касается выделения полимера из жидкой реакционной смеси, оно может быть осуществлено посредством осаждения собственно полимера растворителем, гель-фильтрующей хроматографией, диализом, ультрафильтрацией или т.п.
Таким же способом были получены гетеротелехелатные блок-сополимеры различного типа, представленные формулой (I) этого изобретения. Полученные полимеры (за исключением живых полимеров) способны образовывать высокомолекулярные мицеллы, которые весьма стабильны в водном растворителе.
Эта высокомолекулярная мицелла может быть получена, например, в результате воздействия на раствор или суспензию полимера органического растворителя, термической и ультразвуковой обработки, отдельно или в сочетании. Термическую обработку осуществляют посредством диспергирования или растворения смеси одного или нескольких типов блок-сополимеров этого изобретения в воде при температуре, находящейся в интервале от 30 до 100oC, более предпочтительно от 30 до 50oC. Обработку ультразвуком осуществляют посредством диспергирования или растворения смеси одного или нескольких типов блок-сополимеров этого изобретения в воде при мощности, находящейся в интервале от 1 до 20 Вт в течение от 1 секунды до 24 ч, предпочтительно в интервале от 1 до 3 Вт в течение 3 ч.
Обработку органическим растворителем осуществляют посредством растворения смеси одного или нескольких типов блок-сополимеров в органическом растворителе, диспергирования полученного раствора в воде с последующим выпариванием органического растворителя. Примеры органических растворителей включают хлороформ, бензол, толуол, хлористый метилен и др.
Кроме того, возможно получение высокомолекулярной мицеллы этого изобретения посредством растворения упомянутой смеси в метаноле, этаноле, тетрагидрофуране, диоксане, диметилсульфоксиде, диметилформамиде или т. п. растворителе, и затем полученный раствор подвергают диализу относительно водного растворителя. Фракционный молекулярный вес мембраны, применяемой для диализа, не ограничен, поскольку его оптимальное значение изменяется в соответствии с молекулярным весом блок-сополимера, подлежащего обработке. Однако обычно фракционный молекулярный вес мембраны составляет не более 1000000, предпочтительно 5000 - 20000.
В качестве водного растворителя можно использовать воду и буферный раствор. Соотношение используемого водного раствора к указанному выше органическому растворителю при диализе обычно составляет от 1 до 1000 раз, предпочтительно от 10 до 100 раз. Температура конкретно не ограничивается. Обычно обработку проводят при 5 - 25oC.
Полученные таким образом высокомолекулярные мицеллы этого изобретения имеют критическую концентрацию мицелл не выше 4 - 12 мг/л, причем они гораздо более стабильны в водном растворе, чем низкомолекулярные мицеллы, такие как липосома, которая была детально рассмотрена в качестве носителя для подачи лекарств. Это означает, что при введении в кровь высокомолекулярной мицеллы этого изобретения можно ожидать, что она будет иметь значительно большее характерное время жизни в крови, и, таким образом, можно сказать, что полимер этого изобретения имеет превосходные свойства в качестве носителя для подачи лекарств.
Ниже это изобретение подробно поясняется рабочими примерами, однако эти рабочие примеры никоим образом не ограничивают объем защиты этого изобретения.
Пример 1
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного
раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В этот раствор добавляют 8,8 г этиленоксида и перемешивают при комнатной температуре и атмосферном давлении. После взаимодействия в течение 2 суток добавляют в этот реакционный раствор лактид в количестве 7,2 г и затем перемешивают 1 час. Этот раствор выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок выделяют методом центрифугирования и очищают посредством лиофильной сушки из бензола. Выход продукта 15 г (94%). Полимер, выделенный методом гель-проникающей хроматографии, является мономодальным, его молекулярный вес равен 16000 (фиг. 1).
В соответствии со спектром протонного ядерного магнитного резонанса (ПМР) полученного полимера в дейтерохлороформе было установлено, что он является гетеротелехелатным олигомером, имеющим как полиэтиленоксидные, так и полилактидные блоки, и количественно содержит ацетальную группу в α-концевой части и гидроксильную группу в ω-концевой части (фиг. 2). Среднечисловой молекулярный вес каждого сегмента блок-полимера, найденный по интегральному отношению в спектре, равен 8800 для полиэтиленоксида и 7000 для полилактида.
Пример 2
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,
3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В этот раствор добавляют 5,7 г этиленоксида и перемешивают при комнатной температуре и атмосферном давлении. После взаимодействия в течение 2 суток добавляют в этот реакционный раствор 7,2 г лактида и затем перемешивают 1 час. Этот раствор выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок выделяют методом центрифугирования и очищают посредством лиофильной сушки из бензола. Выход продукта 12,4 г (95%). Полимер, выделенный методом гель-проникающей хроматографии, является мономодальным, его молекулярный вес равен 12000.
В соответствии со спектром протонного ядерного магнитного резонанса полученного полимера в дейтерохлороформе было установлено, что он является гетеротелехелатным олигомером, имеющим как полиэтиленоксидные, так и полилактидные блоки, и количественно содержит ацетальную группу в α-концевой части и гидроксильную группу в ω-концевой части. Среднечисловой молекулярный вес каждого сегмента блок-полимера, найденный по интегральному отношению в спектре, равен 5400 для полиэтиленоксида (ПЭО) и 6600 для полилактида (ПЛ).
Пример 3
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,
3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В этот раствор добавляют 8,8 г этиленоксида и перемешивают при комнатной температуре и атмосферном давлении. После взаимодействия в течение 2 суток добавляют в этот реакционный раствор 5,0 г дельта-валеролактона и перемешивают 1 час. Этот раствор выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок выделяют методом центрифугирования и очищают посредством лиофильной сушки из бензола. Выход продукта 13,5 г (97%). Полимер, выделенный методом гель-проникающей хроматографии, является мономодальным, его молекулярный вес равен 14000.
В соответствии со спектром протонного ядерного магнитного резонанса полученного полимера в дейтерохлороформе было установлено, что он является гетеротелехелатным олигомером, имеющим как полиэтиленоксидные, так и поли(дельта-валеролактонные) блоки, и количественно содержит ацетальную группу в α-концевой части и гидроксильную группу в ω-концевой части (фиг. 3). Среднечисловой молекулярный вес каждого сегмента блок-полимера, найденный по интегральному отношению в спектре, равен 8800 для полиэтиленоксида и 5200 для поли (дельта-валеролактона).
Пример 4
Добавляют 50
мл 2-молярного раствора соляной кислоты к 50 мл метанола, в котором растворен образец блок-сополимера, полученного в Примере 2, смесь перемешивают 1 час при комнатной температуре. После этого раствор
нейтрализуют водным раствором гидроксида натрия и в течение 4 ч подвергают его диализу (фракционный молекулярный вес 1000) относительно 20-кратного количества воды и очищают посредством лиофильной
сушки. Выход продукта 0,85 г (85%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
В соответствии со спектром протонного ядерного магнитного резонанса полученного полимера в дейтерохлороформе в нем отсутствует ацетальная группа в α-концевой части и вместо нее появляется пик, обусловленный альдегидом. Установлено, что продукт является гетеротелехелатным ПЭО/ПЛ олигомером, содержащим альдегидную группу в α-концевой части и гидроксильную группу в ω-концевой части (фиг. 4).
Пример 5
Добавляют 20 мл пиридина и 1 г ангидрида метакриловой кислоты к 20 мл хлороформа, в котором растворен 1 г образца блок-сополимера,
полученного в Примере 2, и смесь перемешивают 24 часа при комнатной температуре. После этого раствор нейтрализуют и промывают водным раствором соляной кислоты. Хлороформовую фазу выливают в
охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,8 г (80%). Установлено, что
молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
В соответствии со спектром ядерного (углеродного) магнитного резонанса полученного полимера в дейтерохлороформе в нем полностью отсутствует гидроксильная группа в ω-терминальной части и вместо нее появляется пик, обусловленный метакрилоильной группой. Установлено, что продукт является гетеротелехелатным ПЭО/ПЛ олигомером, содержащим ацетальную группу в α-терминальной части и метакрилоильную группу в ω -терминальной части (фиг. 5).
Пример 6
Добавляют 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и 5 мл бромистого аллила к 20 мл тетрагидрофурана, в котором
растворен 1 г блок-сополимера, полученного в Примере 2, и смесь перемешивают 4 часа при комнатной температуре. Полученный продукт выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот
осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,98 г (98%). Установлено, что молекулярный вес полимера, выделенного методом
гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
В соответствии со спектром ядерного (углеродного) магнитного резонанса полученного полимера в дейтерохлороформе в нем полностью отсутствует гидроксильная группа в ω-концевой части и вместо нее появляется пик, обусловленный аллильной группой. Установлено, что продукт является гетеротелехелатным ПЭО/ПЛ олигомером, содержащим ацетальную группу в

Пример 7
Добавляют 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и 5 г паратолуолсульфонилхлорида к 20 мл тетрагидрофурана, в котором
растворен 1 г блок-сополимера, полученного в Примере 4, и смесь перемешивают 4 часа при комнатной температуре. Полученный продукт выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот
осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,95 г (95%). Установлено, что молекулярный вес полимера, выделенного методом
гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
В соответствии со спектром ядерного (углеродного) магнитного резонанса полученного полимера в дейтерохлороформе в нем полностью отсутствует гидроксильная группа в ω-концевой части и вместо нее появляется пик, обусловленный паратолуолсульфонильной группой. Установлено, что продукт является гетеротелехелатным ПЭО/ПЛ олигомером, содержащим ацетальную группу в α-концевой части и паратолуолсульфонильную группу в ω-концевой части (фиг. 7).
Пример 8
Растворяют 50 мг блок-сополимера, полученного в Примере 2, в воде или подходящем буферном растворе до достижения концентрации 0,01 - 0,1 вес. /объем.%. Когда образование мицеллы в этом растворе
подтверждается распределением частиц по размерам, измеренным методом динамического светорассеяния, было установлено образование единственной полимерной мицеллы со средним диаметром зерна 30 нм (фиг.
8). Критическая концентрация мицелл для этой полимерной мицеллы составляет 10 мг/л.
Пример 9
В реактор загружают 30 мл тетрагидрофурана, 0,13 г 3,3-диэтоксипропанола и 2 мл 0,
5-молярного раствора нафталинкалия в тетрагидрофуране и полученную смесь перемешивают 3 минуты в атмосфере аргона; таким образом получают 3,3-диэтоксипропаноксид калия.
В этот раствор добавляют 7,0 г этиленоксида, который затем перемешивают при комнатной температуре и атмосферном давлении. После взаимодействия в течение 2 суток добавляют в этот реакционный раствор 7,2 г лактида молочной кислоты и затем перемешивают эту смесь еще 1 час. Полученный таким образом раствор выливают в охлажденный пропанол, осаждая образовавшийся полимер. Осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 11,5 г (79%). Полимер, выделенный методом гель-проникающей хроматографии, является мономодальным, его среднечисловой молекулярный вес равен 11000.
Спектр протонного ядерного магнитного резонанса полученного полимера в дейтерохлороформе свидетельствует, что он является гетеротелехелатным олигомером, имеющим как полиэтиленоксидные, так и полилактидные блоки, и количественно содержит ацетальную группу в α-концевой части и гидроксильную группу в ω-концевой части. Что касается среднечислового молекулярного веса каждого сегмента блок-полимера, найденного по интегральному отношению в спектре, то он равен 5800 для полиэтиленоксида и 5100 для полилактида.
Растворяют 200 мг полученного блок-сополимера в 40 мл диметилацетамида и образовавшийся раствор подвергают диализу относительно воды с использованием мембраны для диализа, имеющей фракционный молекулярный вес 12000 - 14000, в течение 24 часов (воду меняли спустя 2,5 и 8 ч, каждый раз по 2 л). Измерения методом динамического светорассеяния показали, что в полученном растворе образовались высокомолекулярные мицеллы со средним размером частиц 40 нм. Критическая концентрация мицелл для этой полимерной мицеллы составляет 5 мг/л.
Пример 10
Добавляют по каплям 0,
1-нормальную соляную кислоту к 10 мл мицеллярного раствора, полученного в Примере 9, так чтобы значение pH установилось равным 2, и затем раствор перемешивают в течение 2 ч при комнатной температуре.
После этого раствор нейтрализуют 0,1-нормальным водным раствором гидроксида натрия и затем образовавшийся раствор подвергают диализу относительно воды с использованием мембраны для диализа, имеющей
фракционный молекулярный вес 12000 - 14000, в течение 24 часов (воду меняли спустя 2,5 и 8 ч, каждый раз по 2 л). Измерения методом динамического светорассеяния показали, что в полученном растворе
образовались высокомолекулярные мицеллы со средним размером частиц 40 нм. Критическая концентрация мицелл для этой полимерной мицеллы составляет 5 мг/л.
Этот мицеллярный раствор подвергли лиофильной сушке и затем остаток растворили в дейтеро-диметилсульфоксиде и исследовали методом ЯМР. Было установлено, что сигнал, обусловленный наличием ацетальной группы при 1,2 и 4,6 м. д., полностью исчез и что наблюдается сигнал, обусловленный наличием водорода метиленкарбонильной группы и водорода альдегидной группы при 2,7 (триплет) и 9,8 м.д. (синглет) соответственно. Из соотношения площадей этих сигналов было найдено, что 95% ацеталя гидролизовались в альдегид.
Пример 11
Растворяют 200 мг блок-сополимера ПЭО/ПЛ (среднечисловой молекулярный
вес каждого сегмента равен 4500 для полиэтиленоксида и 13000 для полилактида), полученного таким же образом, как в Примере 1, в 40 мл диметилацетамида. Образовавшийся раствор подвергают диализу
относительно воды с использованием мембраны для диализа, имеющей фракционный молекулярный вес 12000 - 14000, в течение 24 часов (воду меняли спустя 2,5 и 8 ч, каждый раз по 2 л). Измерения методом
динамического светорассеяния показали, что в полученном растворе образовались высокомолекулярные мицеллы со средним размером частиц 30 нм. Критическая концентрация мицелл для этой полимерной мицеллы
составляет 4 мг/л.
Промышленная применимость
Это изобретение обеспечивает гетеротелехелатный олигомер или полимер, который имеет различные функциональные группы на обоих
концах молекулы и в то же время содержит в основной цепи гидрофильный сегмент и гидрофобный сегмент. Из составляющих компонентов можно ожидать, что этот олигомер или полимер будет обладать
превосходной биологической пригодностью. Сверх того, этот олигомер или полимер способен образовывать высокомолекулярную мицеллу, которая вполне стабильна в водном растворителе. Поэтому весьма вероятно,
что олигомер или полимер может использоваться для живых организмов или может применяться в такой области, где получается и/или используется носитель для подачи лекарств.
Реферат
Описывается новый гетеротелехелатный блок-сополимер, который представлен формулой I, в которой R1 и R2, соединенные вместе, означают этилендиоксигруппу (-O-CH(R')-СН2-О, в которой R' означает атом водорода или C1-6-алкил), которая может быть замещена C1-6-алкилом, или в сочетании друг с другом означают оксогруппу (=O), L означает группу (а), в которой R3 и R4 независимо означают атом водорода, С1-10-алкил, арил или арил-С1-3-алкил и r означает целое число от 2 до 5, m означает целое число от 2 до 10000, n означает целое число от 2 до 10000, p означает целое число от 1 до 5, q означает целое число от 0 до 20, Z означает, когда q равно нулю, атом водорода, щелочной металл, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, 2-меркаптопропионил или 2-аминопропионил, или аллил, или винилбензил, в то время как, когда q является целым числом от 1 до 20, Z означает С1-6-алкоксикарбонил, карбокси-, меркапто- или аминогруппу. Описанные выше олигомер или полимер образуют высокомолекулярную мицеллу, которая стабильна в водном растворителе. Указанные олигомер или полимер могут быть полезными в качестве носителя при подаче лекарства. Описан также способ получения указанного олигомера или полимера методом полимеризации живых цепей. 3 с. и 9 з. п. ф-лы, 1 табл., 8 ил.

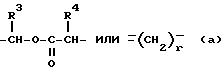
Формула

в которой R1 и R2 независимо означают C1-10-алкокси или арил-С1-3-алкилокси, или R1 и R2, соединенные вместе, означают этилендиоксигруппу (-O-CH(R')-СН2-O, в которой R1 означает атом водорода или С1-6-алкил), которая может быть замещена С1-6 -алкилом, или в сочетании друг с другом, означают оксогруппу (=0);
L означает группу

или
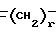
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-С1-3-алкил, и r означает целое число от 2 до 5;
m означает целое число от 2 до 10000;
n означает целое число от 2 до 10000;
p означает целое число от 1 до 5;
q означает целое число от 0 до 20,
Z означает, когда q равно нулю, атом водорода, щелочной металл, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, 2-меркаптопропионил, или 2-аминопропионил, или аллил, или винилбензил, в то время как, когда q является целым числом от 1 до 20, Z означает С1-6-алкоксикарбонил, карбокси-, меркапто- или аминогруппу.
Стадия 1)
взаимодействие инициатора полимеризации, представленного следующей формулой II:
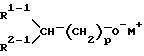
в которой R1-1 и R2-1 независимо означают C1-10-алкокси- или, соединенные вместе, означают этилендиоксигруппу, которая может быть замещена С1-6-алкилом, p означает целое число от 1 до 5 и М означает щелочной металл,
c этиленоксидом таким образом, чтобы можно было получить соединение, представленное следующей формулой III:

в которой R1-1 и R2-1, p и M такие, как определено в формуле II;
m означает целое число от 2 до 10 000;
Стадия 2)
взаимодействие соединения формулы III с лактидом или лактоном, который представлен следующей формулой III-a или III-b:

или

в которой R3 и R4 независимо означают атом водорода, С1-10-алкил, арил или арил-С1-3-алкил и r означает целое число от 2 до 5,
таким образом, чтобы можно было получить блок-сополимер, представленный следующей формулой IV:
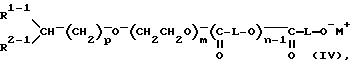
в которой L означает группу
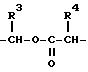
или

R1-1, R2-1, p, m, n, М такие, как определено выше;
и, кроме того, в некоторых случаях
Стадия 3)
i) селективный гидролиз алкоксида щелочного металла формулы IV c получением блок-сополимера следующей формулы V:
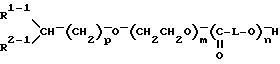
в которой R1-1 , R2-1, p, m, L и n такие, как определено выше; или
ii) полный гидролиз блок-сополимера формулы IV с получением блок-сополимера следующей формулы VI:
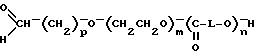
в которой p, m, L и n такие, как определено выше;
Стадия 4)
взаимодействие блок-сополимера формулы V с i) уксусной кислотой, акриловой кислотой, метакриловой кислотой, коричной кислотой или паратолуолсульфоновой кислотой, или их реакционноспособными производными, или с ii) аллилгалогенидом, или винилбензилгалогенидом, или с iii) галогенидом, представленным следующей формулой VII:

в которой X представляет собой атом хлора, брома или йода, q' является целым числом от 1 до 20, и Z' является С1-6,- алкоксикарбонилом или защищенной аминогруппой; и в некоторых случаях
Стадия 5)
трансэтерификацию полученной на стадии 4) -i) производной эфира паратолуолсульфоновой кислоты или гидролиз полученных на стадиях 4) - i), ii) или iii) производных.

Комментарии