Композиции, содержащие липазы, и способы обработки поверхности - RU2612215C2
Код документа: RU2612215C2
Чертежи


Описание
Ссылка на перечень последовательностей
Данная заявка содержит Перечень последовательностей в компьютерно-читаемой форме, включенный путем ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к композициям, содержащим липазные ферменты и отбеливающие агенты, а также способам получения и использования таких композиций, которые предпочтительно представляют собой продукты для ухода за тканями и бытового ухода.
Уровень техники
Производители моющих средств продолжают пытаться обеспечить композиции для очистки, в частности композиции для очистки тканей и посуды, которые обеспечивают наиболее надежные чистящие системы. В случае очистки липазными ферментами, они могут быть особенно подвержены окислению, особенно если такие ферменты вступают в контакт с отбеливателем при хранении или во время стадии мытья или обработки, либо оба включены в стадию мытья или обработки, или один или другой компонент перенесены со стадии предварительной обработки, в частности, например со стадии предварительной отбеливающей обработки. Это приводит к потере активности или эффективности композиции в целом, и, в частности, к потере ферментативной активности. Определенные отбеливающие компоненты особенно проблематичны, например, предварительно полученные перкислоты и отбеливающие катализаторы или ускорители. WO 2007/001262 относится к композициям для очистки, содержащим органические катализаторы с улучшенной совместимостью ферментов, особенно улучшенной совместимостью фермента амилазы. Остается потребность в композиции, которая облегчает эту проблему.
Сущность изобретения
В соответствии с настоящим изобретением представлен способ очистки и/или обработки ткани, твердой поверхности и/или другой поверхности для ухода за тканями и/или бытового ухода, включающий стадии, на которых:
а) вводят в контакт ткань, твердую поверхность и/или другую поверхность для ухода за тканями и/или бытового ухода с водным раствором, содержащим липазу; и (ii) отбеливающий компонент и (iii) необязательное моющее вспомогательное вещество;
b) промывают и высушивают ткань или твердую поверхность;
характеризующийся тем, что липаза имеет улучшенную стабильность к окислительному распаду по сравнению со зрелым полипептидом SEQ ID NO: 1 и липазную активность, предпочтительно вариант липазы содержит вариант липазы, содержащий замену в одном или более положениях, выбранных из группы положений, соответствующих Т37, N39 и G91, зрелого полипептида SEQ ID ΝΟ: 1. Настоящее изобретение также представляет способ получения композиции моющего средства, содержащей вариант липазы, проявляющий улучшенную стабильность к окислительному распаду по сравнению с вариантом липазы SEQ ID NO: 1, и липазную активность, при этом способ включает стадию, на которой смешивают вариант липазы с моющим вспомогательным веществом. Предпочтительно вариант липазы представляет собой вариант SEQ ID NO: 1, содержащий замену в одном или более положениях, выбранных из группы положений, соответствующих Т37, N39 и G91, зрелого полипептида SEQ ID ΝΟ: 1. В соответствии с дополнительным аспектом настоящего изобретения представлена композиция, содержащая вариант липазы, имеющий липазную активность и проявляющий улучшенную стабильность к окислительному распаду, и моющее вспомогательное вещество. Настоящее изобретение также представляет композицию для очистки и/или обработки, содержащую вариант липазы, имеющий липазную активность и содержащий замену в одном или более положениях, выбранных из группы положений, соответствующих Т37, N39 и G91, зрелого полипептида SEQ ID ΝΟ: 1, и моющее вспомогательное вещество. Может быть предпочтительным, чтобы композиции также содержали отбеливающий компонент.
В соответствии с дополнительным аспектом настоящего изобретения представлен способ получения композиции моющего средства, содержащей липазу и проявляющей улучшенную стабильность к окислительному распаду, включающий стадию, на которой смешивают вариант липазы, содержащий замену в одном или более положениях, выбранных из группы положений, соответствующих Т37, N39 и G91, зрелого полипептида SEQ ID NO: 1, при этом вариант имеет липазную активность, с моющим вспомогательным веществом.
Вариант липазы, проявляющий улучшенную стабильность к окислительному распаду, может быть определен при помощи следующего теста в Примере 1. Варианты липазы, проявляющие улучшенную стабильность к окислительному распаду, имеют RРмытья, по меньшей мере, 1,01, или, по меньшей мере, 1,2 или даже, по меньшей мере, 1,5. Традиционная липаза для сравнения представляет собой липазу с SEQ ID ΝΟ: 1.
Подробное описание изобретения
Определения
Если не указано иное, все уровни компонентов или композиций относятся к активной части такого компонента или композиции и не включают примеси, например, остаточные растворители или побочные продукты, которые могут присутствовать в коммерчески доступных источниках таких компонентов или композиций.
Все процентные содержания и соотношения (1) рассчитаны по массе, если не указано иное, и (2) рассчитаны, исходя из общей массы композиции, если не указано иное.
Как используют в данной заявке, формы единственного числа при использовании в формуле изобретения подразумевают один или более заявленных или описанных объектов.
Как используют в данной заявке, термины «включают», «включает» и «включая» подразумевают как неограничивающие.
Как используют в данной заявке, термин «твердый» включает гранулированную, порошкообразную, стержневидную и таблетированную формы продукта.
Как используют в данной заявке, термин «жидкость» включает жидкие, гелеобразные, пастообразные и газообразные формы продуктов.
Как используют в данной заявке, термин «липаза» или «липолитический фермент» или «липидная эстераза» представляет собой фермент в классе ЕС 3.1.1 как определено Enzyme Nomenclature. Он может иметь липазную активность (триацилглицерол липаза, ЕС 3.1.1.3), кутиназную активность (ЕС 3.1.1.74), стеролэстеразную активность (ЕС 3.1.1.13) и/или воск-сложноэфирную гидролазную активность (ЕС 3.1.1.50). Для целей в соответствии с настоящим изобретением, липазную активность определяют в соответствии с процедурой, описанной в Примерах. В одном аспекте, варианты в соответствии с настоящим изобретением имеют, по меньшей мере, 20%, например, по меньшей мере, 25%, по меньшей мере, 30%, по меньшей мере, 35%, по меньшей мере, 40%, по меньшей мере, 45%, по меньшей мере, 50%», по меньшей мере, 55%, по меньшей мере, 60%, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%», или, по меньшей мере, 100%) липазной активности зрелого полипептида SEQ ID ΝΟ: 1.
Как используют в данной заявке, термин «аллельный вариант» означает любую из двух или более альтернативных форм гена, занимающих один и тот же хромосомный локус. Аллельная вариация возникает в природе за счет мутации, и может в результате приводить к полиморфизму в популяциях. Генные мутации могут быть молчащими (без изменений в кодируемом полипептиде) или могут кодировать полипептиды, имеющие измененные аминокислотные последовательности. Аллельный вариант полипептида является полипептидом, кодируемым аллельным вариантом гена.
Как используют в данной заявке, термин «кДНК» означает молекулу ДНК, которая может быть получена путем обратной транскрипции из зрелой сплайсированной молекулы мРНК, полученной из эукариотической или прокариотической клетки. кДНК не содержит интронные последовательности, которые могут присутствовать в соответствующей геномной ДНК. Исходный, первичный РНК транскрипт является предшественником мРНК, который обрабатывается с помощью серий стадий, включая сплайсинг, перед появлением в виде зрелой сплайсированной мРНК.
Как используют в данной заявке, термин «кодирующая последовательность» означает полинуклеотид, который непосредственно определяет аминокислотную последовательность варианта. Границы кодирующей последовательности, как правило, определяют при помощи открытой рамки считывания, которая начинается с инициирующего кодона, такого как ATG, GTG или TTG и заканчивается терминирующим кодоном, таким как ТАА, TAG или TGA. Кодирующая последовательность может быть геномной ДНК, кДНК, синтетической ДНК или их комбинацией.
Как используют в данной заявке, термин «контрольные последовательности» означает последовательности нуклеиновых кислот, необходимые для экспрессии полинуклеотида, кодирующего вариант в соответствии с настоящим изобретением. Каждая контрольная последовательность может быть нативной (то есть, из того же гена) или чужеродной (то есть, из другого гена) к полинуклеотиду, кодирующему вариант, или нативной или чужеродной друг к другу. Такие контрольные последовательности включают, но не ограничиваясь приведенным, лидерную, полиаденилированную последовательность, пропептидную последовательность, промотор, сигнальную пептидную последовательность и транскрипционный терминатор. Как минимум, контрольные последовательности включают промотор и транскрипционные и трансляционные стоп сигналы. Контрольные последовательности могут быть обеспечены линкерами с целью введения специфических сайтов рестрикции, облегчающих лигирование контрольных последовательностей с кодирующей областью полинуклеотида, кодирующего вариант.
Как используют в данной заявке, термин «экспрессия» включает любую стадию, вовлеченную в продуцирование варианта, включая, но не ограничиваясь приведенным, транскрипцию, посттранскрипционную модификацию, трансляцию, посттрансляционную модификацию и секрецию.
Как используют в данной заявке, термин «вектор экспрессии» означает молекулу линейной или циклической ДНК, которая содержит полинуклеотид, кодирующий вариант, и функционально связана с контрольными последовательностями, которые обеспечивают ее экспрессию.
Как используют в данной заявке, термин «фрагмент» означает полипептид, имеющий одну или более (например, несколько) аминокислот, удаленных с аминного и/или карбоксильного конца зрелого полипептида; при этом фрагмент имеет липазную активность. В одном аспекте, фрагмент содержит, по меньшей мере, 50%, по меньшей мере, 55%, по меньшей мере, 60%, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, и, по меньшей мере, 95% количества аминокислот зрелого полипептида.
Как используют в данной заявке, термин «условия высокой строгости» означает для зондов, по меньшей мере, 100 нуклеотидов в длину, предварительную гибридизацию и гибридизацию при 42°С в 5Х SSPE, 0,3% SDS, 200 микрограмм/мл резаной и денатурированной ДНК из молок лососевых, и 50%» формамида, в соответствии со стандартными процедурами саузерн-блоттинга в течение от 12 до 24 часов. Материал-носитель окончательно промывают три раза, каждый в течение 15 минут с использованием 2Х SSC, 0,2% SDS при 65°С.
Как используют в данной заявке, термин «клетка-хозяин» означает любой тип клетки, который является восприимчивым к трансформации, трансфекции, трансдукции, или подобным с конструктом нуклеиновой кислоты или вектором экспрессии, содержащим полинуклеотид в соответствии с настоящим изобретением. Термин «клетка-хозяин» охватывает любое потомство родительской клетки, которое не является идентичным родительской клетке из-за мутаций, которые происходят во время репликации.
Как используют в данной заявке, термин «улучшенное свойство» означает характеристику, связанную с вариантом, который является улучшенным по сравнению с родительским. Такие улучшенные свойства включают улучшенную производительность в присутствии органического катализатора. В некоторых предпочтительных воплощениях настоящее изобретение относится к композиции или способу, в котором вариант имеет улучшенную стабильность к органическому катализатору, выбранному из группы, состоящей из органических катализаторов, имеющих следующие формулы:

их смесей, где каждый R1 независимо представляет собой разветвленную алкильную группу, содержащую от 3 до 24 атомов углерода, или линейную алкильную группу, содержащую от 1 до 24 атомов углерода, в частности, где R представляет собой 2-бутилоктил, и предпочтительно улучшенная стабильность существует в присутствии Формулы 2, в которой R представляет собой 2-бутилоктил.
Как используют в данной заявке, термин «выделенный» означает вещество в форме или среде, которые не встречаются в природе. Неограничивающие примеры выделенных веществ включают (1) любое не встречающееся в природе вещество, (2) любое вещество, включая, но не ограничиваясь приведенным, любой фермент, вариант, нуклеиновую кислоту, белок, пептид или кофактор, которое, по меньшей мере, частично удалено из одного или более или всех составляющих, встречающихся в природе, с которым оно связано в природе; (3) любое вещество, модифицированное рукою человека относительно этого вещества, найденного в природе; или (4) любое вещество, модифицированное путем увеличения количества вещества по отношению к другим компонентам, с которыми оно природно связано (например, множество копий гена, кодирующего вещество; использование более сильного промотора, чем промотор, природно связанный с геном, кодирующим вещество). Выделенное вещество может присутствовать в пробе ферментационного бульона.
Как используют в данной заявке, термин «условия низкой строгости» означает для зондов, по меньшей мере, 100 нуклеотидов в длину, предварительную гибридизацию и гибридизацию при 42°С в 5Х SSPE, 0,3% SDS, 200 микрограмм/мл резаной и денатурированной ДНК из молок лососевых, и 25% формамида, в соответствии со стандартными процедурами саузерн-блоттинга в течение от 12 до 24 часов. Материал-носитель окончательно промывают три раза, каждый в течение 15 минут с использованием 2Х SSC, 0,2% SDS при 50°С.
Как используют в данной заявке, термин «зрелый полипептид» означает полипептид в его конечной форме после трансляции и любых посттрансляционных модификаций, таких как N-терминальный процессинг, С-терминальное усечение, гликозирование, фосфорилирования и т.д. В одном аспекте, зрелый полипептид представляет собой аминокислоты от 1 до 269 SEQ ID NO: 1.
Как используют в данной заявке, термин «условия средней строгости» означает для зондов, по меньшей мере, 100 нуклеотидов в длину, предварительную гибридизацию и гибридизацию при 42°С в 5Х SSPE, 0,3% SDS, 200 микрограмм/мл разаной и денатурированной ДНК из молок лососевых, и 35% формамида, в соответствии со стандартными процедурами саузерн-блоттинга в течение от 12 до 24 часов. Материал-носитель окончательно промывают три раза, каждый в течение 15 минут с использованием 2Х SSC, 0,2% SDS при 55°С.
Как используют в данной заявке, термин «условия средней-высокой строгости» означает для зондов, по меньшей мере, 100 нуклеотидов в длину, предварительную гибридизацию и гибридизацию при 42°С в 5Х SSPE, 0,3% SDS, 200 микрограмм/мл резаной и денатурированной ДНК из молок лососевых, и либо 35% формамида, в соответствии со стандартными процедурами саузерн-блоттинга в течение от 12 до 24 часов. Материал-носитель окончательно промывают три раза, каждый в течение 15 минут с использованием 2Х SSC, 0,2% SDS при 60°С.
Как используют в данной заявке, термин «мутант» означает полинуклеотид, кодирующий вариант.
Как используют в данной заявке, термин «конструкт нуклеиновой кислоты» означает молекулу нуклеиновой кислоты, или одно- или двухцепочечную, которая выделена из гена, встречающегося в природе, или модифицирована, чтобы содержать сегменты нуклеиновых кислот таким образом, чтобы иначе они не могли бы существовать в природе, или которая является синтетической, содержащей один или более контрольных последовательностей.
Как используют в данной заявке, термин «функционально связанный» означает конфигурацию, в которой контрольная последовательность расположена в соответствующем положении по отношению к кодирующей последовательности полинуклеотида, таким образом, что контрольная последовательность направляет экспрессию кодирующей последовательности.
Как используют в данной заявке, термин «родитель» или «родительская липаза» означает липазу, в которой изменение производится для получения вариантов фермента в соответствии с настоящим изобретением. Родитель может быть полипептидом (дикого типа), встречающимся в природе, или его вариантом или фрагментом.
Идентичность последовательностей: Сходство между двумя аминокислотными последовательностями или между двумя нуклеотидными последовательностями описывается параметром «идентичность последовательностей». Для целей настоящего изобретения, идентичность последовательностей между двумя аминокислотными последовательностями определяют, используя алгоритм Нидлмана-Вунша (Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443-453) как выполнено в Needle программе EMBOSS пакета (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, Trends Genet. 16: 276-277), предпочтительно версии 5.0.0 или более поздней. Использованными параметрами являются штраф на внесение делеции в выравнивание 10, штраф на продолжение делеции 0,5 и EBLOSUM62 (EMBOSS версии BLOSUM62) постановочная матрица. Результаты выполнения Needle, обозначенные «самая длинная идентичность» (полученная, используя - опцию без замечаний), используют как процентную идентичность и рассчитывают следующим образом:
(Идентичные остатки × 100)/(Длина выравнивания - Общее количество делеций в выравнивании)
Для целей настоящего изобретения, идентичность последовательностей между двумя дезоксирибонуклеотидными последовательностями определяют, используя алгоритм Нидлмана-Вунша (Needleman and Wunsch, 1970, ранее) как выполнено в Needle программе EMBOSS пакета (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, ранее), предпочтительно версии 5.0.0 или более поздней. Использованными параметрами являются штраф на внесение делеции в выравнивание 10, штраф на продолжение делеции 0,5 и EDNAFULL (EMBOSS версии NCBI NUC4.4) постановочная матрица. Результаты выполнения Needle, обозначенные «самая длинная идентичность» (полученная, используя - опцию без замечаний), используют как процентную идентичность и рассчитывают следующим образом:
(Идентичные дезоксирибонуклеотиды × 100)/(Длина выравнивания - Общее количество делеций в выравнивании)
Как используют в данной заявке, термин «подпоследовательность» означает полинуклеотид, имеющий один или более (например, несколько) нуклеотидов, удаленных с 5' и/или 3' конца последовательности, кодирующей зрелый полипептид; при этом подпоследовательность кодирует фрагмент, имеющий липазную активность. В одном аспекте, подпоследовательность содержит, по меньшей мере, 50%, по меньшей мере, 55%, по меньшей мере, 60%, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, и, по меньшей мере, 95% количества нуклеотидов последовательности, кодирующей зрелый полипептид.
Как используют в данной заявке, термин «вариант» означает полипептид, имеющий липазную активность, содержащий замену в одном или более (например, нескольких) положениях. Замена означает замену аминокислоты, занимающей положение, на отличающуюся аминокислоту. Варианты в соответствии с настоящим изобретением имеют, по меньшей мере, 20%, например, по меньшей мере, 25%, по меньшей мере, 30%, по меньшей мере, 35%, по меньшей мере, 40%, по меньшей мере, 45%, по меньшей мере, 50%, по меньшей мере, 55%, по меньшей мере, 60%, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 95%, или, по меньшей мере, 100% липазной активности зрелого полипептида SEQ ID NO: 1.
Как используют в данной заявке, термин «условия очень высокой строгости» означает для зондов, по меньшей мере, 100 нуклеотидов в длину, предварительную гибридизацию и гибридизацию при 42°С в 5Х SSPE, 0,3% SDS, 200 микрограмм/мл резаной и денатурированной ДНК из молок лососевых, и 50% формамида, в соответствии со стандартными процедурами саузерн-блоттинга в течение от 12 до 24 часов. Материал-носитель окончательно промывают три раза, каждый в течение 15 минут с использованием 2Х SSC, 0,2% SDS при 70°С.
Как используют в данной заявке, термин «условия очень низкой строгости» означает для зондов, по меньшей мере, 100 нуклеотидов в длину, предварительную гибридизацию и гибридизацию при 42°С в 5Х SSPE, 0,3% SDS, 200 микрограмм/мл резаной и денатурированной ДНК из молок лососевых, и 25% формамида, в соответствии со стандартными процедурами саузерн-блоттинга в течение от 12 до 24 часов. Материал-носитель окончательно промывают три раза, каждый в течение 15 минут с использованием 2Х SSC, 0,2% SDS при 45°С.
Как используют в данной заявке, термин липаза «дикого типа» означает липазу, экспрессируемую микроорганизмом, встречающимся в природе, таким, как бактерия, дрожжи или мицелиальный гриб, встречающийся в природе.
Правила для обозначения вариантов
Для целей настоящего изобретения, зрелый полипептид, раскрытый в SEQ ID NO: 1, используют для определения соответствующего аминокислотного остатка в другой липазе. Аминокислотную последовательность другой липазы выравнивают со зрелым полипептидом, раскрытым в SEQ ID ΝΟ:1, и, исходя из выравнивания, номер положения аминокислоты, соответствующий любому аминокислотному остатку в зрелом полипептиде, раскрытом в SEQ ID NO: 1определяют, используя алгоритм Нидлмана-Вунша (Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443-453), который выполняется в Needle программе EMBOSS пакета (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, Trends Genet. 16: 276-277), предпочтительно версия 5.0.0 или более поздняя. Использованными параметрами являются штраф на внесение делеции в выравнивание 10, штраф на продолжение делеции 0,5 и EBLOSUM62 (EMBOSS версия BLOSUM62) постановочная матрица.
Идентификация соответствующего аминокислотного остатка в другой липазе может быть определена путем выравнивания множественных полипептидных последовательностей, используя несколько компьютерных программ, включая, но не ограничиваясь приведенным, MUSCLE (сравнение множественных последовательностей путем log-ожидания; версия 3.5 или более поздняя; Edgar, 2004, Nucleic Acids Research 32: 1792-1797), MAFFT (версия 6.857 или более поздняя; Katoh and Kuma, 2002, Nucleic Acids Research 30: 3059-3066; Katoh et al., 2005, Nucleic Acids Research 33: 511-518; Katoh and Toh, 2007, Bioinformatics 23: 372-374; Katoh et al., 2009, Methods in Molecular Biology 537: 39-64; Katoh and Toh, 2010, Bioinformatics 26: 1899-1900). и EMBOSS EMMA с использованием ClustalW (1.83 или более поздняя; Thompson et al., 1994, Nucleic Acids Research 22: 4673-4680), используя их соответствующие параметры умолчания.
Если другой фермент отличался от зрелого полипептида SEQ ID ΝΟ: 1 таким образом, что сравнение основывалось на традиционной последовательности дает сбой при обнаружении их взаимосвязи (Lindahl and Elofsson, 2000, J. Mol Biol. 295: 613-615), то могут быть использованы другие алгоритмы сравнения последовательностей попарно. Большая чувствительность поиска на основе последовательностей может быть достигнута используя программы поиска, которые используют вероятностные представления семейств полипептидов (профилей) для поиска по базам данных. Например, PSI-BLAST программа генерирует профили за счет итеративного процесса поиска по базе данных и является способной к обнаружениию отдаленных гомологов (Atschul et al., 1997, Nucleic Acids Res. 25: 3389-3402). Еще большая чувствительность может быть достигнута, если семейство или суперсемейство для полипептида имеет один или более представителей в базах данных структуры белка. Программы, такие как GenTHREADER (Jones, 1999, J. Mol Biol. 287: 797-815; McGuffin and Jones, 2003, Bioinformatics 19: 874-881) используют информацию из множества источников (PSI-BLAST, прогнозирование вторичной структуры, профили структурного выравнивания и возможности сольватации), как входящие данные в нейронной сети, что предсказывает структурную складку для запрашиваемой последовательности. Аналогично, способ Gough et al., 2000, J. Mol. Biol. 313: 903-919, может быть использован для выравнивания последовательности неизвестной структуры с моделями суперсемейства, представленными в базе данных SCOP. Эти выравнивания могут быть в свою очередь использованы, чтобы сгенерировать гомологичные модели для полипептида и такие модели могут быть оценены на правильность использования множества инструментов, разработанных для такой цели.
Для белков известной структуры, некоторые инструменты и ресурсы являются доступными для восстановления и генерирования структурных выравниваний. Например, SCOP суперсемейства белков были структурно выравнены и такие выравнивания являются доступными и загружаемыми. Две или более белковые структуры могут быть выравнены, используя множество алгоритмов, таких как матрица выравнивания расстояния (Holm and Sander, 1998, Proteins 33: 88-96) или комбинаторное удлинение (Shindyalov and Bourne, 1998, Protein Engineering 11: 739-747), и внедрение этих алгоритмов может дополнительно быть использовано в базах данных запрашиваемой структуры со структурой, представляющей интерес, для обнаружения возможных структурных гомологов (например, Holm and Park, 2000, Bioinformatics 16: 566-567).
В описании вариантов в соответствии с настоящим изобретением, описанная ниже номенклатура адаптирована для легкости ссылки. Применяют приемлемые однобуквенные или трехбуквенные аббревиатуры аминокислот IUPAC.
Замены. Для аминокислотной замены используют следующую номенклатуру: исходная аминокислота, положение, замещенная аминокислота. Соответственно, замена треонина в положении 226 на аланин обозначают как «Thr226Ala» или «Т226А». Множественные мутации разделены путем добавления отметок («+»), например, «Gly205Arg+Ser41 lPhe» или «G205R+S411F», представляющие замены в положениях 205 и 411 глицина (G) на аргинин (R) и серина (S) на фенилаланин (F), соответственно.
Множественные замены. Варианты, содержащие множественные замены, разделены путем добавления отметок («+»), например, «Argl70Tyr+Glyl95Glu» или «R170Y+G195E», представляющие замену аргинина и глицина в положениях 170 и 195 на тирозин и глутаминовую кислоту, соответственно.
Различные замены. Когда различные изменения могут быть введены в положение, различные изменения разделяют запятой, например, «Arg170Tyr,Glu» или «R170Y,E» представляет замену аргинина в положении 170 на тирозин или глутаминовую кислоту. Таким образом, «Tyr167Gly,Ala+Arg170Gly,Ala» обозначает следующие варианты: «Tyr167Gly+Arg170Gly», «Tyr167Gly+Arg170Ala», «Tyr167Ala+Arg170Gly» и «Tyr167Ala+Arg170Ala».
Варианты липазы
Для достижения стабильности к окислительному распаду варианта липазы, определяют значение относительной производительности (RРмытья), т.е. производительность мытья (Р) варианта липазы для тестирования, и делят на производительность мытья липазы SEQ ID NO: 1. Таким образом, RРмытья = Р(вариант липазы в соответствии с настоящим изобретением) / P(SEQ ID NO: 1 липазы). Варианты липазы, имеющие улучшенную стабильность к окислительному распаду, будут иметь значение RРмытья, по меньшей мере, 1,01, предпочтительно, по меньшей мере, 1,1, или даже, по меньшей мере, 1,5.
Вариант липазы, приемлемый для использования в настоящем изобретении, содержит замену в одном или более положениях, выбранных из группы положений, соответствующих Т37, N39 и G91. Предпочтительно вариант липазы представляет собой выделенный вариант липазы. Приемлемые варианты липазы для использования в настоящем изобретении предпочтительно содержат замену в одном или более (например, нескольких) положениях, соответствующих положениям T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q или даже G91A зрелого полипептида SEQ ID ΝΟ: 1, где вариант имеет липазную активность. Наиболее предпочтительно такое одно или более замен объединяют с одним, предпочтительно обоими из T231R и N233R.
Предпочтительно вариант имеет идентичность последовательности, по меньшей мере, 60%, например, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 91%, по меньшей мере, 92%, по меньшей мере, 93%, по меньшей мере, 94%, по меньшей мере, 95%, по меньшей мере, 96%, по меньшей мере, 97%, по меньшей мере, 98%, или, по меньшей мере, 99%, но менее, чем 100%, с аминокислотной последовательностью родительской липазы.
В другом воплощении, вариант имеет, по меньшей мере, 60%, например, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 91%, по меньшей мере, 92%, по меньшей мере, 93%, по меньшей мере, 94%, по меньшей мере, 95%, например, по меньшей мере, 96%, по меньшей мере, 97%, по меньшей мере, 98%, или, по меньшей мере, 99%, но менее, чем 100%, идентичности последовательности со зрелым полипептидом SEQ ID NO: 1.
В одном аспекте, количество замен в вариантах в соответствии с настоящим изобретением составляет 1-20, например, 1-10 и 1-5, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 замен.
В другом аспекте, вариант содержит замену в одном или более (например, нескольких) положениях, соответствующих положениям T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q зрелого полипептида SEQ ID ΝΟ:1. В другом аспекте, вариант содержит изменение в двух положениях, соответствующих любому из положений T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q зрелого полипептида SEQ ID ΝΟ:1. В другом аспекте, вариант содержит изменение в трех положениях, соответствующих любому из положений T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q зрелого полипептида SEQ ID NO: 1.
В другом аспекте, вариант содержит или состоит из замены ия в положении, соответствующем положению Т37 зрелого полипептида SEQ ID ΝΟ: 1, которое замещено на Ala, Arg, Asn, Asp, Cys, Gln, Glu, Gly, His, Ile, Leu, Lys, Met, Phe, Pro, Ser, Thr, Trp, Tyr или Val., предпочтительно на Ala, Arg, Asn, Asp, Gln, Glu, Gly, His, Ile, Leu, Phe, Pro, Ser, Trp, Tyr или Val. В другом аспекте, вариант содержит или состоит из замены Т37А, T37D, Т37Е, T37F, T37G, Т37Н, T37I, T37L, T37N, Т37Р, T37Q, T37R, T37S, T37V, T37W или T37Y зрелого полипептида SEQ ID NO: 1.
В другом аспекте, вариант содержит или состоит из замены в положении, соответствующем положению N39 зрелого полипептида SEQ ID NO: 1, которое замещено на Ala, Arg, Asn, Asp, Cys, Gln, Glu, Gly, His, Ile, Leu, Lys, Met, Phe, Pro, Ser, Thr, Trp, Tyr или Val., предпочтительно на Ala, Arg, Asp, Cys, Gln, Glu, Gly, Ile, Leu, Lys, Met, Phe, Pro, Thr, Trp, Tyr или Val. В другом аспекте, вариант содержит или состоит из замены N39A, N39C, N39D, N39E, N39F, N39G, N391, N39K, N39L, N39M, N39P, N39Q, N39R, N39T, N39V, N39W, N39Y зрелого полипептида SEQ ID NO: 1.
В другом аспекте, вариант содержит или состоит из замены в положении, соответствующем положению G91, зрелого полипептида SEQ ID ΝΟ: 1, которое замещено на Ala, Arg, Asn, Asp, Cys, Gln, Glu, Gly, His, Ile, Leu, Lys, Met, Phe, Pro, Ser, Thr, Trp, Tyr или Val., предпочтительно на Asp, Gln, His, Ile или Pro. В другом аспекте, вариант содержит или состоит из замены G91D, G91H, G91I, G91P, G91Q зрелого полипептида SEQ ID ΝΟ: 1. В предпочтительном аспекте вариант содержит или состоит из замены в положении, соответствующем G91, которое представляет собой G91A.
В другом аспекте, вариант содержит или состоит из замен в положениях, соответствующих положениям Т37 и N39, например таким, как описано выше.
В другом аспекте, вариант содержит или состоит из замен в положениях, соответствующих положениям Т37 и G91, например таким, как описано выше.
В другом аспекте, вариант содержит или состоит из замен в положениях, соответствующих положениям N39 и G91, например таким, как описано выше.
В другом аспекте, вариант содержит или состоит из замен в положениях, соответствующих положениям Т37, N39 и G91, например таким, как описано выше.
Варианты могут дополнительно включать одно или более дополнительных замен в одном или более (например, нескольких) других положениях.
Замены аминокислот могут иметь незначительный характер, что является консервативными заменами аминокислот или инсерциями, которые существенно не влияют на складывание и/или активность белка; небольшие делении, обычно 1-30 аминокислот; небольшие удлинения амино- или карбоксильного конца, такого как амино-концевой остаток метионина; небольшие остатки линкерного пептида до 20-25; или небольшое удлинение, которое облегчает очистку путем изменения суммарного заряда или другой функции, такой как полигистидиновый тракт, антигенный эпитоп или связывающий домен.
Примеры консервативных замен находятся в пределах групп основных аминокислот (аргинин, лизин и гистидин), кислых аминокислот (глутаминовая кислота и аспарагиновая кислота), полярных аминокислот (глутамин и аспарагин), гидрофобных аминокислот (лейцин, изолейцин и валин), ароматических аминокислот (фенилаланин, триптофан и тирозин) и небольших аминокислот (глицин, аланин, серии, треонин и метионин).
Альтернативно, замены аминокислот имеют такую природу, что физико-химические свойства полипептидов изменены. Например, аминокислотные изменения могут улучшить термическую стабильность полипептида, изменить субстратную специфичность, изменить рН оптимум и т.п.
Например, варианты могут содержать замену в положении, соответствующем положениям D96, Т143, А150, Е210, G225, Т231, N233 и Р250 зрелого полипептида SEQ ID NO: 1. В некоторых воплощениях замену выбирают из D96G, Т143А, A150G, E210Q, G225R, T231R, N233R и P250R.
В предпочтительном воплощении вариант липазы для использования в настоящем изобретении относится к вариантам, выбранным из:


Незаменимые аминокислоты в полипептиде могут быть определены в соответствии с процедурами, известными в данной области техники, такими как сайт-направленный мутагенез или аланин-сканирующий мутагенез (Cunningham and Wells, 1989, Science 244: 1081-1085). В последнем способе, одиночные аланиновые мутации вводят в каждый остаток в молекуле, и полученные в результате мутантные молекулы тестируют на липазную активность для идентификации аминокислотных остатков, которые являются критическими для активности молекулы. См. также, Hilton et al., 1996, J. Biol. Chem. 271: 4699-4708. Активный сайт фермента или другое биологическое взаимодействие может быть также определено с помощью физического анализа структуры, как определено с помощью таких методов, как ядерный магнитный резонанс, кристаллография, дифракция электронов или фотоаффинное мечение, в сочетании с мутацией предполагаемого контактного сайта аминокислот.См., например, de Vos et al., 1992, Science 255: 306-312; Smith et al., 1992, J. Mol. Biol. 224: 899-904; Wlodaver et al., 1992, FEBS Lett. 309: 59-64, Идентичность незаменимых аминокислот, также может быть выведена из выравнивания с родственным полипептидом.
Варианты могут состоять из, по меньшей мере, 50%, по меньшей мере, 55%, по меньшей мере, 60%, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, и, по меньшей мере, 95% количества аминокислот зрелого полипептида.
В воплощении, вариант имеет улучшенную производительность, в частности в присутствии отбеливающего компонента. Предпочтительные варианты имеют улучшенную производительность в присутствии органического катализатора, выбранного из группы, состоящей из органических катализаторов, имеющих следующие формулы:

их смесей, где каждый R1 независимо представляет собой разветвленную алкильную группу, содержащую от 3 до 24 атомов углерода, или линейную алкильную группу, содержащую от 1 до 24 атомов углерода; и восстанавливают вариант.
В некоторых воплощениях R1 независимо представляет собой разветвленную алкильную группу, содержащую от 8 до 18 атомов углерода, или линейную алкильную группу, содержащую от 8 до 18 атомов углерода.
В некоторых воплощениях R1 независимо выбирают из группы, состоящей из 2-пропилгептила, 2-бутилоктила, 2-пентилнонила, 2-гексилдецила, н-додецила, н-тетрадецила, н-гексадецила, н-октадецила, изо-нонила, изо-децила, изо-тридецила и изо-пентадецила. Предпочтительно R1 выбирают из группы, состоящей из 2-бутилоктила, 2-пентилнонила, 2-гексилдецила, изо-тридецила и изо-пентадецила. Предпочтительные варианты имеют улучшенную производительность в присутствии катализатора формулы Ь), в которой R представляет собой 2-бутилоктил.
Родительские липазы
Родительская липаза может быть полипептидом с, по меньшей мере, 60% идентичностью последовательности со зрелым полипептидом SEQ ID NO: 1.
В аспекте, родитель имеет идентичность последовательностей со зрелым полипептидом SEQ ID NO: 1, по меньшей мере, 60%, например, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, по меньшей мере, 91%, по меньшей мере, 92%, по меньшей мере, 93%, по меньшей мере, 94%, по меньшей мере, 95%, по меньшей мере, 96%, по меньшей мере, 97%, по меньшей мере, 98%, по меньшей мере, 99%, или 100%, который имеет липазную активность. В одном аспекте, аминокислотная последовательность родителя отличается на не более, чем 20 аминокислот, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, И, 12, 13, 14, 15, 16, 17, 18, 19 или 20 от зрелого полипептида SEQ ID NO: 1.
В другом аспекте, родитель содержит или состоит из аминокислотной последовательности SEQ ID NO: 1. В другом аспекте, родитель содержит или состоит из зрелого полипептида SEQ ID NO: 1. В другом аспекте, родитель содержит или состоит из аминокислот от 1 до 269 SEQ ID NO: 1.
В другом аспекте, родитель представляет собой фрагмент зрелого полипептида SEQ ID ΝΟ:1, содержащий, по меньшей мере, 50%, по меньшей мере, 55%, по меньшей мере, 60%, по меньшей мере, 65%, по меньшей мере, 70%, по меньшей мере, 75%, по меньшей мере, 80%, по меньшей мере, 85%, по меньшей мере, 90%, и, по меньшей мере, 95% количества аминокислот зрелого полипептида.
В другом воплощении, родитель представляет собой аллельный вариант зрелого полипептида SEQ ID NO: 1.
Полипептид SEQ ID NO: 1 или его фрагмент могут быть использованы для создания зондов нуклеиновых кислот для идентификации и клонирования ДНК, кодирующей родителя из штаммов различных родов или видов в соответствии со способами, хорошо известными в данной области техники. В частности, такие зонды можно использовать для гибридизации с геномной ДНК или кДНК в рассматриваемой клетке, в соответствии со стандартными процедурами саузерн-блоттинга, для того, чтобы идентифицировать и выделить соответствующий ген в этом процессе. Такие зонды могут быть значительно короче, чем целая последовательность, но должны составлять, по меньшей мере, 15, например, по меньшей мере, 25, по меньшей мере, 35, или, по меньшей мере, 70 нуклеотидов в длину. Предпочтительно, зонд нуклеиновой кислоты составляет, по меньшей мере, 100 нуклеотидов в длину, например, по меньшей мере, 200 нуклеотидов, по меньшей мере, 300 нуклеотидов, по меньшей мере, 400 нуклеотидов, по меньшей мере, 500 нуклеотидов, по меньшей мере, 600 нуклеотидов, по меньшей мере, 700 нуклеотидов, по меньшей мере, 800 нуклеотидов, или, по меньшей мере, 900 нуклеотидов в длину. Могут быть использованы как ДНК, так и РНК зонды. Зонды типично маркируют для обнаружения соответствующего гена (например,32Р,3H,35S, биотин или авидин). Настоящее изобретение охватывает такие зонды.
Геномная ДНК или кДНК библиотека, полученная из таких других штаммов, может быть подвергнута скринингу на ДНК, которая гибридизуется с зондами, описанными выше, и кодирует родителя. Геномную или другую ДНК из таких других штаммов могут быть отделять, используя агарозный или полиакриламидный гель-электрофорез в, или другие методы разделения. ДНК из библиотек или отделенная ДНК могут быть перенесены и иммобилизованы на нитроцеллюлозу или другой приемлемый материал-носитель. Для того чтобы идентифицировать клон или ДНК, которая гибридизуется с SEQ ID ΝΟ: 1 или их подпоследовательность, материал-носитель используют в саузерн-блоттинге.
Полипептид может быть гибридным полипептидом, в котором часть одного полипептида слита по N-концу или С-концу с частью другого полипептида.
Родитель может быть слитым полипептидом или расщепляемым слитым полипептидом, в котором другой полипептид слит по N-концу или С-концу полипептида в соответствии с настоящим изобретением. Слитый полипептид получают путем сливания полинуклеотида, кодирующего другой полипептид, с полинуклеотидом в соответствии с настоящим изобретением. Способы получения слитых полипептидов известны в данной области техники, например, лигирование кодирующих последовательностей, которые кодируют полипептиды таким образом, что они находятся в рамке и, что экспрессия слитого полипептида находится под контролем того же промотора(ов) и терминатора. Слитые полипептиды могут быть также сконструированы с использованием интеиновой технологии, в которой слитые полипептиды создают пост-трансляционно (Cooper et al., 1993, EMBO J. 12: 2575-2583; Dawson et al., 1994, Science 266: 776-779).
Слитый полипептид может дополнительно содержать сайт расщепления между двумя полипептидами. После секреции слитого белка сайт расщепляется, высвобождая два полипептида. Примеры сайтов расщепления включают, но не ограничиваясь приведенным, сайты, раскрытые в Martin et al., 2003, J. Ind. Microbiol. Biotechnol. 3: 568-576; Svetina et al., 2000, J. Biotechnol. 76: 245-251; Rasmussen-Wilson et al., 1997, Appl. Environ. Microbiol. 63: 3488-3493; Ward et al., 1995, Biotechnology 13: 498-503; и Contreras et al., 1991, Biotechnology 9: 378-381; Eaton et al., 1986, Biochemistry 25: 505-512; Collins-Racie et al., 1995, Biotechnology 13: 982-987; Carter et al., 1989, Proteins: Structure, Function, and Genetics 6: 240-248; и Stevens, 2003, Drug Discovery World 4: 35-48.
Родитель может быть получен из микроорганизмов любого рода. Для целей настоящего изобретением, термин «полученный из», как используют в данной заявке в связи с данным источником, должен означать, что родитель, кодируемый полинуклеотидом, производится от источника или штамма, в котором полинуклеотид от источника был вставлен. В одном аспекте, родитель секретируется внеклеточно.
Родитель может быть бактериальной липазой. Например, родитель может быть грамм-позитивным бактериальным полипептидом, таким, как Bacillus, Clostridium, Enterococcus, Geobacillus, Lactobacillus, Lactococcus, Oceanobacillus, Staphylococcus, Streptococcus, Streptomyces, Thermobifida fusca alias Thermomonospora fusca липаза или грамм-негативным бактериальным полипептидом, таким как Campylobacter, Ε. coli, Flavobacterium, Fusobacterium, Helicobacter, Ilyobacter, Neisseria, Pseudomonas, Salmonella или Ureaplasma липаза.
В одном аспекте, родитель представляет собой Bacillus alkalophilus, Bacillus amyloliquefaciens, Bacillus brevis, Bacillus circulans, Bacillus clausii, Bacillus coagulans, Bacillus firmus, Bacillus lautus, Bacillus lentus, Bacillus licheniformis, Bacillus megaterium, Bacillus pumilus, Bacillus stearothermophilus, Bacillus subtilis или Bacillus thuringiensis липазу.
В другом аспекте, родитель представляет собой Streptococcus equisimilis, Streptococcus pyogenes, Streptococcus uberis или Streptococcus equi subsp. Zooepidemicus липазу.
В другом аспекте, родитель представляет собой Streptomyces achromogenes, Streptomyces avermitilis, Streptomyces coelicolor, Streptomyces griseus или Streptomyces lividans липазу.
Родитель может быть грибковой липазой. Например, родитель может быть дрожжевой липазой, такой как Candida, Kluyveromyces, Pichia, Saccharomyces, Schizosaccharomyces или Yarrowia липаза; или мицелиальной грибковой липазой, такой как Acremonium, Agaricus, Alternaría, Aspergillus, Aureobasidium, Botryospaeria, Ceriporiopsis, Chaetomidium, Chrysosporium, Claviceps, Cochliobolus, Coprinopsis, Coptotermes, Corynascus, Cryphonectria, Cryptococcus, Diplodia, Exidia, Filibasidium, Fusarium, Gibberella, Holomastigotoides, Humicola, Irpex, Lentinula, Leptospaeria, Magnaporthe, Melanocarpus, Meripilus, Mucor, Myceliophthora, Neocallimastix, Neurospora, Paecilomyces, Pénicillium, Phanerochaete, Piromyces, Poitrasia, Pseudoplectania, Pseudotrichonympha, Rhizomucor, Schizophyllum, Scytalidium, Talaromyces, Thermoascus, Thielavia, Tolypocladium, Trichoderma, Trichophaea, Verticillium, Volvariella или Xylaria липаза.
В другом аспекте, родитель представляет собой Saccharomyces carlsbergensis, Saccharomyces cerevisiae, Saccharomyces diastaticus, Saccharomyces douglasii, Saccharomyces kluyveri, Saccharomyces norbensis или Saccharomyces oviformis липазу.
В другом аспекте, родитель представляет собой Acremonium cellulolyticus, Aspergillus aculeatus, Aspergillus awamori, Aspergillus foetidus, Aspergillus fumigatus, Aspergillus japonicus, Aspergillus nidulans, Aspergillus niger, Aspergillus oryzae, Chrysosporium inops, Chrysosporium keratinophilum, Chrysosporium lucknowense, Chrysosporium merdarium, Chrysosporium pannicola, Chrysosporium queenslandicum, Chrysosporium tropicum, Chrysosporium zonatum, Fusarium bactridioides, Fusarium cerealis, Fusarium crookwellense, Fusarium culmorum, Fusarium graminearum, Fusarium graminum, Fusarium heterosporum, Fusarium negundi, Fusarium oxysporum, Fusarium reticulatum, Fusarium roseum, Fusarium sambucinum, Fusarium sarcochroum, Fusarium sporotrichioides, Fusarium sulphureum, Fusarium torulosum, Fusarium trichothecioides, Fusarium venenatum, Humicola grísea, Humicola insolens, Humicola lanuginosa, Irpex lacteus, Mucor miehei, Myceliophthora thermophila, Neurospora crassa, Pénicillium funiculosum, Pénicillium purpurogenum, Phanerochaete chrysosporium, Thielavia achromatica, Thielavia albomyces, Thielavia albopilosa, Thielavia australeinsis, Thielavia fimeti, Thielavia microspora, Thielavia ovispora, Thielavia peruviana, Thielavia setosa, Thielavia spededonium, Thielavia subthermophila, Thielavia terresmpus, Trichoderma harzianum, Trichoderma koningii, Trichoderma longibrachiatum, Trichoderma reesei или Trichoderma viride липазу.
В другом аспекте, родитель представляет собой Humicola lanuginosa липазу, например, липазу SEQ ID NO: 1 или ее зрелый полипептид.
Следует иметь в виду, что для вышеупомянутых видов, настоящее изобретение охватывает как совершенные и несовершенные состояния, так и другие таксономические эквиваленты, например, анаморфы, независимо от названия вида, с помощью которых они известны. Специалисты в данной области техники легко распознают идентичность соответствующих эквивалентов.
Штаммы этих видов легко доступны для общественности в ряде коллекций культур, таких как American Type Culture Collection (АТСС), Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH (DSMZ), Centraalbureau Voor Schimmelcultures (CBS) и Agricultural Research Service Patent Culture Collection, Northern Regional Research Center (NRRL).
Родитель может быть идентифицирован и получен из других источников, включая микроорганизмы, выделенные из природных (например, почвы, компоста, воды и т.д.) или ДНК образцов, полученных непосредственно из природных материалов (например, почвы, компоста, воды и т.д.), используя указаные выше зонды. Методы выделения микроорганизмов и ДНК непосредственно из природных сред обитания, хорошо известны в данной области техники. Полинуклеотид, кодирующий родителя, может затем быть получен путем аналогичного скрининга геномной ДНК или кДНК библиотеки другого микроорганизма или смешанной ДНК пробы. Как только полинуклеотид, кодирующий родителя, был обнаружен с помощью зонда(ов), полинуклеотид может быть выделен или клонирован с использованием методов, которые известны специалистам в данной области техники (см., например, Sambrook et al., 1989, выше).
Получение вариантов
Настоящее изобретение также относится к способу получения варианта липазы, включающему стадии, на которых вводят в родительскую липазу замену в одном или более положениях, соответствующих положениям Т37, N39 или G91, зрелого полипептида SEQ ID NO: 1, при этом вариант имеет липазную активность и по сравнению с родительской липазой имеет улучшенную производительность в присутствии органического катализатора, выбранного из группы, состоящей из органических катализаторов, имеющих следующие формулы:

(с) их смеси, где каждый R1 независимо представляет собой разветвленную алкильную группу, содержащую от 3 до 24 атомов углерода, или линейную алкильную группу, содержащую от 1 до 24 атомов углерода; и восстанавливают вариант.
В некоторых воплощениях настоящее изобретение относится к способу, в котором R1 независимо представляет собой разветвленную алкильную группу, содержащую от 8 до 18 атомов углерода, или линейную алкильную группу, содержащую от 8 до 18 атомов углерода.
В некоторых воплощениях настоящее изобретение относится к способу, в котором R1 независимо выбирают из группы, состоящей из 2-пропилгептила, 2-бутилоктила, 2-пентилнонила, 2-гексилдецила, н-додецила, н-тетрадецила, н-гексадецила, н-октадецила, изо-нонила, изо-децила, изо-тридецила и изо-пентадецила. Предпочтительно R1 выбирают из группы, состоящей из 2-бутилоктила, 2-пентилнонила, 2-гексилдецила, изо-тридецила и изо-пентадецила.
Органический катализатор типично используют в количестве, обеспечивающем 0,001-0,02 г активного вещества на литр моющего раствора или в количестве, обеспечивающем от 0,01 до 4,5, от 0,5 до 4,0, от 1,0 до 3,5, от 1,5 до 3,0, или от 2,0 до 2,5 м.д. активного вещества на литр моющего раствора.
В некоторых воплощениях настоящее изобретение относится к способу, в котором источник органических пероксикислот присутствует в качестве отбеливающего агента. Источником органических пероксикислот может быть предварительно полученная перкислота или диацилпероксид, или он может содержать источник перекиси водорода и активатор отбеливания.
Приемлемые отбеливающие агенты включают диацилпероксиды, активаторы отбеливания, перекись водорода, источники перекиси водорода, предварительно полученные перкислоты и их смеси.
В общем, при использовании отбеливающего агента, композиции в соответствии с настоящим изобретением могут содержать от приблизительно 0,1% до приблизительно 50% или даже от приблизительно 0,1% до приблизительно 25% отбеливающего агента по массе рассматриваемой композиции для очистки. Отбеливающий агент, как правило, является источником органических пероксикислот или активированным источником перекиси.
Когда присутствует, перкислота и/или активатор отбеливания, как правило, присутствует в композиции в количестве от приблизительно 0,1 до приблизительно 60 мас. %, от приблизительно 0,5 до приблизительно 40 мас. % или даже от приблизительно 0,6 до приблизительно 10 мас. %, исходя из композиции. Одна или более гидрофобных перкислот или их предшественников могут быть использованы в сочетании с одной или более гидрофильной перкислотой или ее предшественником.
Количества источника перекиси водорода и перкислоты или активатора отбеливания могут быть выбраны таким образом, чтобы молярное соотношение доступного кислорода (из источника пероксида) и перкислоты составляло от 1:1 до 35:1, или даже от 2:1 до 10:1.
В некоторых воплощениях настоящее изобретение относится к способу, в котором родительская липаза содержит аминокислотную последовательность с, по меньшей мере, 60% идентичностью со зрелым полипептидом SEQ ID NO: 1; состоит из аминокислотной последовательности зрелого полипептида SEQ ID NO: 1или ее фрагмента, имеющего липазную активность.
В некоторых воплощениях настоящее изобретение относится к способу, в котором вариант представляет собой: (а) полипептид, содержащий аминокислотную последовательность с, по меньшей мере, 60% идентичностью со зрелым полипептидом SEQ ID NO: 1; (b) полипептид, кодируемый полинуклеотидом, который гибридизуется в, по меньшей мере, условиях низкой строгости с: (i) последовательностью, кодирующей зрелый полипептид SEQ ID ΝΟ:1; или (ii) полноразмерной комплементарной нитью (i), или (с) полипептид, кодируемый полинуклеотидом, содержащим нуклеотидную последовательность с, по меньшей мере, 60% идентичностью с последовательностью, кодирующей зрелый полипептид SEQ ID ΝΟ: 1.
В некоторых воплощениях настоящее изобретение относится к способу, в котором замену выбирают из T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q.
В некоторых воплощениях настоящее изобретение относится к способу, в котором вариант дополнительно содержит замену в одном или более положениях, соответствующих положениям D96, Т143, А150, Е210, G225, Т231, N233 и Р250 зрелого полипептида SEQ ID NO: 1.
В некоторых воплощениях настоящее изобретение относится к способу, в котором замену выбирают из D96G, Т143А, A150G, E210Q, G225R, T231R, N233R и P250R.
Варианты могут быть получены с использованием любого способа мутагенеза, известного в данной области техники, такого как сайт-направленный мутагенез, синтетическое конструирование гена, полусинтетическое конструирование гена, произвольный мутагенез, перестановка и т.д.
Сайт-направленный мутагенез представляет собой метод, в котором одну или более (например, несколько) мутаций вводят в одном или более определенных сайтов в полинуклеотиде, кодирующем родитель.
Сайт-направленный мутагенез может быть выполнен in vitro с помощью ПЦР, включая использование олигонуклеотидных праймеров, содержащих желаемую мутацию. Сайт-направленный мутагенез также может быть выполнен in vitro с помощью кассетного мутагенеза, включая расщепление рестриктазой в сайте в плазмиде, содержащем полинуклеотид, кодирующий родитель и последующего лигирования олигонуклеотида, содержащего мутацию в полинуклеотиде. Обычно рестриктаза, которая дигестирует плазмид и олигонуклеотид, является одинаковой, позволяя липким концам плазмиды и вставки лигировать друг с другом. См., например, Scherer and Davis, 1979, Proc. Natl. Acad. Sci. USA 76: 4949-4955; и Barton et al., 1990, Nucleic Acids Res. 18: 7349-4966.
Сайт-направленный мутагенез может быть также выполнен in vivo способами, известными в данной области техники. См., например, Публикацию патентной заявки США №2004/0171154; Storici et al., 2001, Nature Biotechnol 19: 773-776; Kren et al., 1998, Nat. Med. 4: 285-290; и Calissano and Macino, 1996, Fungal Genet. Newslett. 43: 15-16.
Любой способ сайт-направленного мутагенеза может быть использован в настоящем изобретении. Есть много доступных коммерческих наборов, которые могут быть использованы для получения вариантов.
Синтетическое конструирование гена вызывает in vitro синтез молекулы, сконструированного полинуклеотида для кодирования рассматриваемого полипептида. Синтез гена может быть выполнен с использованием ряда способов, таких как мультиплексная технология на основе микросхем, описанная Tian et al. (2004, Nature 432: 1050-1054 и аналогичные технологии, в которых олигонуклеотиды синтезируют и собирают на фотопрограммируемых микрофлюидальных микросхемах.
Одиночные или множественные аминокислотные замены, делеции и/или инсерции могут быть сделаны и испытаны с использованием известных способов мутагенеза, рекомбинации и/или перестановки, с последующей соответствующей процедурой скрининга, такой как те, которые раскрыты Reidhaar-Olson and Sauer, 1988, Science 241: 53-57; Bowie and Sauer, 1989, Proc. Natl Acad. Sci. USA 86: 2152-2156; WO 95/17413; или WO 95/22625. Другие способы, которые могут быть использованы, включают подверженный погрешностям ПЦР, фаговый дисплей (например, Lowman et al., 1991, Biochemistry 30: 10832-10837; патент США №5,223,409; WO 92/06204) и область-направленный мутагенез (Derbyshire et al., 1986, Gene 46: 145; Ner et al., 1988, DNA 7: 127).
Способы мутагенеза/перестановки могут быть объединены с высокопроизводительными автоматизированными способами скрининга для обнаружения активности клонированных, мутагенезированных полипептидов, экспрессированных клетками-хозяевами (Ness et al., 1999, Nature Biotechnology 17: 893-896). Молекулы мутагенезированных ДНК, которые кодируют активные полипептиды, могут быть выделены из клеток-хозяев и быстро задана последовательность, используя стандартные способы в данной области техники. Эти способы позволяют быстро определить важность отдельных аминокислотных остатков в полипептиде.
Полусинтетическое конструирование гена осуществляется путем объединения аспектов синтетического конструирования гена и/или сайт-направленного мутагенеза, и/или произвольного мутагенеза, и/или перестановки. Полусинтетическое конструирование характерно для способа, который использует фрагменты полинуклеотида, который синтезируют, в сочетании с ПЦР способами. Определенные области генов могут быть синтезированы таким образом, de novo, в то время как другие области могут быть амплифицированы с помощью сайт-специфических мутагенных праймеров, в то время как другие области могут быть подвергнуты амплификации, ПЦР, подверженному погрешностям, или ПЦР не подверженному погрешностям. Полинуклеотидные подпоследовательности могут затем перестанавливать.
Полинуклеотиды
Также в данной заявке раскрыты выделенные полинуклеотиды, кодирующие вариант в соответствии с настоящим изобретением.
Конструкты нуклеиновой кислоты
Также в данной заявке описаны конструкты нуклеиновой кислоты, содержащие полинуклеотид, кодирующий вариант в соответствии с настоящим изобретением, функционально связанные с одной или более контрольными последовательностями, которые направляют экспрессию кодирующей последовательности в приемлемой клетке-хозяине, в условиях, совместимых с контрольными последовательностями.
Полинуклеотидом можно манипулировать различными маршрутами для обеспечения экспрессии варианта. Манипуляция с полинуклеотидом до его вставки в вектор может быть желаемой или необходимой, в зависимости от вектора экспрессии. Методы модификации полинуклеотидов, использующие методы рекомбинантных ДНК, хорошо известны в данной области техники.
Контрольная последовательность может быть промотором, полинуклеотидом, который распознается клеткой-хозяином для экспрессии полинуклеотида. Промотор содержит транскрипционные контрольные последовательности, которые обеспечивают экспрессию варианта. Промотор может быть любым полинуклеотидом, который демонстрирует транскрипционную активность в клетке-хозяине, включая мутантные, усеченные и гибридные промоторы, и может быть получен из генов, кодирующих внеклеточные или внутриклеточные полипептиды либо гомологичные, либо гетерологичные к клетке-хозяину.
Примеры приемлемых промоторов для направления транскрипции конструктов нуклеиновой кислоты в соответствии с настоящим изобретением в бактериальной клетке-хозяине являются промоторами, полученными из Bacillus amyloliquefaciens альфа-амилазного гена (amyQ), Bacillus licheniformis альфа-амилазного гена (amyL), Bacillus licheniformis пенициллиназного гена (penP), Bacillus stearothermophilus мальтогенного амилазного гена (amyM), Bacillus subtilis левансукразного гена (sacB), Bacillus subtilis xylA и xylB генов, Bacillus thuringiensis cryIIIA гена (Agaisse and Lereclus, 1994, Molecular Microbiology 13: 97-107), E.coli lac оперона, Ε. coli trc промотора (Egon et al., 1988, Gene 69: 301-315), Streptomyces coelicolor агаразного гена (dagA) и прокариотного бета-лактамазного гена (Villa-Kamaroff et al., 1978, Proc. Natl. Acad. Sci. USA 75: 3727-3731), а также tac промотора (DeBoer et al., 1983, Proc. Natl. Acad. Sci. USA 80: 21-25). Дополнительные промоторы описаны в «Useful proteins from recombinant bacteria» in Gilbert et al., 1980, Scientific American 242: 74-94; и в Sambrook et al., 1989, выше. Примеры тандемных промоторов описаны в WO 99/43835.
Примеры приемлемых промоторов для направления транскрипции конструктов нуклеиновой кислоты в соответствии с настоящим изобретением в мицелиальной грибковой клетке-хозяине представляют собой промоторы, полученные из генов для Aspergillus nidulans ацетамидазы, Aspergillus niger нейтральной альфа-амилазы, Aspergillus niger кислотно-стабильной альфа-амилазы, Aspergillus niger или Aspergillus awamori глюкоамилазы (glaA), Aspergillus oryzae TAKA амилазы, Aspergillus oryzae щелочной протеазы, Aspergillus oryzae триозфосфатной изомеразы, Fusarium oxysporum трипсинподобной проетазы (WO 96/00787), Fusarium venenatum амилоглюкозидазы (WO 00/56900), Fusarium venenatum Dana (WO 00/56900), Fusarium venenatum Quinn (WO 00/56900), Rhizomucor miehei липазы, Rhizomucor miehei аспартопротеазы, Trichoderma reesei бета-глюкозидазы, Trichoderma reesei целлобиогидролазы I, Trichoderma reesei целлобиогидролазы II, Trichoderma reesei эндоглюканазы I, Trichoderma reesei эндоглюканазы II, Trichoderma reesei эндоглюканазы III, Trichoderma reesei эндоглюканазы IV, Tpuchoderma reesei эндоглюканазы V, Trichoderma reesei ксиланазы I, Trichoderma reesei ксиланазы II, Trichoderma reesei бета-ксилозидазы, а также NA2-tpi промотора (модифицированного промотора из Aspergillus нейтрального альфа-амилазного гена, в котором нетранслированный лидер был заменен на нетранслированный лидер из Aspergillus триозафосфатизомеразного гена; неограничивающие примеры включают модифицированные промоторы из Aspergillus niger нейтрального альфа-амилазного гена, в котором нетранслированный лидер был заменен на нетранслированный лидер из Aspergillus nidulans или Aspergillus oryzae триозафосфатизомеразного гена); и их мутантных, усеченных и гибридных промоторов.
В дрожжевом хозяине, полезные промоторы получают из генов для Saccharomyces cerevisiae енолазы (ENO-1), Saccharomyces cerevisiae галактокиназы (GAL1), Saccharomyces cerevisiae спирт дегидрогеназы/глицеральдегид-3-фосфатдегидрогеназы (ADH1, ADH2/GAP), Saccharomyces cerevisiae триозафосфатизомеразы (TPI), Saccharomyces cerevisiae металлотионеина (CUP1) и Saccharomyces cerevisiae 3-фосфоглицерат киназы. Другие полезные промоторы для дрожжевых клеток-хозяев описаны Romanos et al., 1992, Yeast 8: 423-488.
Контрольная последовательность может быть также терминатором транскрипции, который распознается клеткой-хозяином для прекращения транскрипции. Терминаторная последовательность функционально связана с 3'-концом полинуклеотида, кодирующего вариант. Может быть использован любой терминатор, функционирующий в клетке-хозяине.
Предпочтительные терминаторы для бактериальных клеток-хозяев получают из генов для Bacillus clausii щелочной протеазы (aprH), Bacillus licheniformis альфа-амилазы (amyL) и Escherichia coli рибосомной РНК (rrnB).
Предпочтительные терминаторы для мицелиальных грибковых клеток-хозяев получают из генов для Aspergillus nidulans антранилат синтазы, Aspergillus niger глюкоамилазы, Aspergillus niger альфа-глюкозидазы, Aspergillus oryzae TAKA амилазы и Fusarium oxysporum трипсин-подобной протеазы.
Предпочтительные терминаторы для дрожжевых клеток-хозяев получают из генов для Saccharomyces cerevisiae енолазы, Saccharomyces cerevisiae цитохрома С (CYC1) и Saccharomyces cerevisiae глицеральдегид-3-фосфатдегидрогеназы. Другие полезные терминаторы для дрожжевых клеток-хозяев описаны Romanos et al., 1992, ранее.
Контрольная последовательность может быть также мРНК стабилизаторной областью ниже промотора и выше кодирующей последовательности гена, что увеличивает экспрессию гена.
Примеры приемлемых мРНК стабилизаторных областей получают из Bacillus thuringiensis сгуША гена (WO 94/25612) и Bacillus subtilis SP82 гена (Hue et al., 1995, Journal of Bacteriology 177: 3465-3471).
Контрольная последовательность может также быть лидерной, нетранслируемой областью мРНК, что важно для трансляции клеткой-хозяином. Лидерная последовательность функционально связана с 5'-концом полинуклеотида, кодирующего вариант.Может быть использован любой лидер, функционирующий в клетке-хозяине.
Предпочтительные лидеры для мицелиальных грибковых клеток-хозяев получают из генов для Aspergillus oryzae TAKA амилазы и Aspergillus nidulans триозофосфатизомеразы.
Приемлемые лидеры для дрожжевых клеток-хозяев получают из генов для Saccharomyces cerevisiae енолазы (ENO-1), Saccharomyces cerevisiae 3-фосфоглицераткиназы, Saccharomyces cerevisiae альфа-фактора и Saccharomyces cerevisiae спирт дегидрогеназы/глицеральдегид-3-фосфатдегидрогеназы (ADH2/GAP).
Контрольная последовательность может быть также полиаденилированной последовательностью, последовательность функционально связана с 3'-концом последовательности, кодирующей вариант, и при транскрипции, распознается клеткой-хозяином как сигнал для добавления остатков полиаденозина в транскрибированную мРНК. Может быть использована любая полиаденилированная последовательность, функционирующая в клетке-хозяине.
Предпочтительные полиаденилированные последовательности для мицелиальных грибковых клеток-хозяев получают из генов для Aspergillus nidulans антранилат синтазы, Aspergillus niger глюкоамилазы, Aspergillus niger альфа-глюкозидазы, Aspergillus oryzae TAKA амилазы и Fusarium oxysporum трипсин-подобной протеазы.
Полезные полиаденилированные последовательности для дрожжевых клеток-хозяев описываются Guo and Sherman, 1995, Mol. Cellular Biol. 15: 5983-5990.
Контрольная последовательность может быть также областью, кодирующей сигнальный пептид, которая кодирует сигнальный пептид, связанный с N-концом варианта, и направляет вариант в секреторный путь клетки. 5'-конец кодирующей последовательности полинуклеотида может по своей природе содержать последовательность, кодирующую сигнальный пептид, природно связанную в трансляционной рамке считывания с сегментом кодирующей последовательности, которая кодирует вариант. Альтернативно, 5'-конец кодирующей последовательности может содержать последовательность, кодирующую сигнальный пептид, чуждую кодирующей последовательности. Чуждая последовательность, кодирующая сигнальный пептид, может потребоваться, если кодирующая последовательность природно не содержит последовательность, кодирующую сигнальный пептид. Альтернативно, чуждая последовательность, кодирующая сигнальный пептид, может просто заменить природную последовательность, кодирующую сигнальный пептид, в целях повышения секреции варианта. Тем не менее, может быть использована любая последовательность, кодирующая сигнальный пептид, которая направляет экспрессированный вариант в секреторный путь клетки-хозяина.
Эффективные последовательности, кодирующие сигнальный пептид, для бактериальных клеток-хозяев являются последовательностями, кодирующими сигнальный пептид, полученными из генов для Bacillus NCIB 11837 мальтогенной амилазы, Bacillus licheniformis субтилизина, Bacillus licheniformis бета-лактамазы, Bacillus stearothermophilus альфа-амилазы, Bacillus stearothermophilus нейтральных протеаз (nprT, nprS, nprМ) и Bacillus subtilis prsA. Дополнительные сигнальные пептиды описаны Simonen and Palva, 1993, Microbiological Reviews 57: 109-137.
Эффективные последовательности, кодирующие сигнальный пептид, для мицелиальных грибковых клеток-хозяев являются последовательностями, кодирующими сигнальный пептид, полученными из генов для Aspergillus niger нейтральной амилазы, Aspergillus niger глюкоамилазы, Aspergillus oryzae ТАКА амилазы, Humicola insolens целлюлазы, Humicola insolens эндоглюканазы V, Humicola lanuginosa липазы и Rhizomucor miehei аспарагиновой протеиназы.
Полезные сигнальные пептиды для дрожжевых клеток-хозяев получают из генов для Saccharomyces cerevisiae альфа-фактора и Saccharomyces cerevisiae инвертазы. Другие полезные последовательности, кодирующие сигнальный пептид, описываются Romanos et al., 1992, ранее.
Контрольная последовательность может быть также последовательностью, кодирующей пропептид, которая кодирует пропептид, расположенный на N-конце варианта. Полученный в результате полипептид известен как профермент или прополипептид (или зимоген в некоторых случаях). Прополипептид, как правило, неактивен и может быть преобразован в активный полипептид путем каталитического или аутокаталитического расщепления пропептида из прополипептида. Последовательность, кодирующая пропептид, может быть получена из генов для Bacillus subtilis щелочной протеазы (aprE), Bacillus subtilis нейтральной протеазы (nprT), Myceliophthora thermophila лакказы (WO 95/33836), Rhizomucor miehei аспарагиновой протеиназы и Saccharomyces cerevisiae альфа-фактора.
Если присутствуют как последовательности сигнального пептида, так и пропептида, то последовательность пропептида располагается рядом с N-концом варианта, а последовательность сигнального пептида располагается рядом с N-концом последовательности пропептида.
Также может быть желательным добавление регуляторных последовательностей, которые регулируют экспрессию варианта по отношению к росту клетки-хозяина. Примерами регуляторных систем являются те, которые вызывают экспрессию гена, чтобы быть включенными или выключенными в ответ на химический или физический стимул, включая наличие регуляторного соединения. Регуляторные системы в прокариотических системах включают lac, tac и trp операторные системы. В дрожжах, могут быть использованы система ADH2 или система GAL1. В мицелиальных грибах могут быть использованы Aspergillus niger глюкоамилазный промотор, Aspergillus oryzae ТАКА альфа-амилазный промотор и Aspergillus oryzae глюкоамилазный промотор. Другие примеры регуляторных последовательностей являются теми, которые позволяют амплификацию генов. В эукариотических системах, эти регуляторные последовательности включают ген дигидрофолатредуктазы, который амплифицируется в присутствии метотрексата, и гены металлотионеина, которые амплифицируются тяжелыми металлами. В этих случаях, полинуклеотид, кодирующий вариант, функционально связан с регуляторной последовательностью.
Векторы экспрессии
Настоящее изобретение также относится к рекомбинантным векторам экспрессии, содержащим полинуклеотид, кодирующий вариант в соответствии с настоящим изобретением, промотор и транскрипционные и трансляционные стоп сигналы. Различные нуклеотидные и контрольные последовательности могут быть соединены вместе для получения рекомбинантного вектора экспрессии, который может включать один или более удобных сайтов рестрикции, чтобы позволить вставку или замену полинуклеотида, кодирующего вариант на таких сайтах. Альтернативно, полинуклеотид может быть экспрессирован путем вставки полинуклеотида или конструкта нуклеиновой кислоты, содержащей полинуклеотид, в соответствующий вектор для экспрессии. При создании вектора экспрессии, кодирующая последовательность расположена в векторе таким образом, что кодирующая последовательность функционально связана с соответствующими контрольными последовательностями для экспрессии.
Рекомбинантный вектор экспрессии может быть любым вектором (например, плазмидом или вирусом), который может быть легко подвергнут процедурам рекомбинантных ДНК и может привести к экспрессии полинуклеотида. Выбор вектора, как правило, будет зависеть от совместимости вектора с клеткой-хозяином, в которую вектор должен быть введен. Вектор может быть линейным или замкнутым циклическим плазмидом.
Вектор может быть автономно репликационным вектором, т.е. вектором, который существует как внехромосомный объект, репликация которого не зависит от хромосомной репликации, например, плазмидом, внехромосомным элементом, минихромосомой или искусственной хромосомой. Вектор может содержать любые средства для обеспечения саморепликации. Альтернативно, вектор может быть таким, что, когда введен в клетку-хозяин, интегрируется в геном и реплицируется вместе с хромосомой(ами), в которую он был интегрирован. Дополнительно, могут быть использованы один вектор или плазмид или два или более векторов или плазмидов, которые вместе содержат общую ДНК, чтобы быть введеными в геном клетки-хозяина, или транспозон.
Вектор предпочтительно содержит один или более селективных маркеров, которые позволяют легко отбирать трансформированные, трансфицированные, трансдуцированные или тому подобные клетки. Селективный маркер представляет собой ген продукта, обеспечивающего биоцидную или вирусную стойкость, стойкость к тяжелым металлам, прототрофию к ауксотрофам, и тому подобное.
Примерами бактериальных селективных маркеров являются Bacillus licheniformis или Bacillus subtilis dal гены или маркеры, которые придают устойчивость к антибиотикам, такую как устойчивость к ампициллину, хлорамфениколу, канамицину, неомицину, спектиномицину или тетрациклину. Приемлемые маркеры для дрожжевых клеток-хозяев включают, но не ограничиваясь приведенным, ADE2, HIS3, LEU2, LYS2, МЕТЗ, TRP1 и URA3. Селективные маркеры для использования в мицелиальных грибковых клетках-хозяевах включают, но не ограничиваясь приведенным, amdS (ацетамидазу), argB (орнитин карбамоилтрансферазу), bar (фосфинотрицин ацетилтрансферазу), hph (гигромицинфосфотрансферазу), niaD (нитрат редуктазу), pyrG (оротидин-5'-фосфат декарбоксилазу), sC (сульфат аденилтрансферазу) и trpC (антранилатсинтазу), а также их эквиваленты. Предпочтительными для использования в клетке Aspergillus являются Aspergillus nidulans или Aspergillus oryzae amdS и pyrG гены и Streptomyces hygroscopicus bar ген.
Вектор предпочтительно содержит элемент(ы), который позволяет интеграцию вектора в геном клетки-хозяина или автономную репликацию вектора в клетке независимо от генома.
Для интеграции в геном клетки-хозяина, вектор может быть основан на полинуклеотидной последовательности, кодирующей вариант или любой другой элемент вектора для интеграции в геном путем гомологичной или негомологичной рекомбинации. Альтернативно, вектор может содержать дополнительные полинуклеотиды для направления интеграции путем гомологичной рекомбинации в геном клетки-хозяина в точном месте(ах) в хромосоме(ах). Чтобы увеличить вероятность интеграции в точном месте, интеграционные элементы должны содержать достаточное количество нуклеиновых кислот, например от 100 до 10000 пар оснований, от 400 до 10000 пар оснований, и от 800 до 10000 пар оснований, которые имеют высокую степень идентичности последовательностей с соответствующей последовательностью-мишенью, чтобы повысить вероятность гомологичной рекомбинации. Интеграционные элементы могут быть любой последовательностью, которая является гомологичной с последовательностью-мишенью в геноме клетки-хозяина. Дополнительно, интеграционные элементы могут быть некодирующими или кодирующими полинуклеотидами. С другой стороны, вектор может быть интегрирован в геном клетки-хозяина путем негомологичной рекомбинации.
Для автономной репликации вектор может дополнительно содержать источник репликации, дающий возможность вектору автономно реплицироваться в рассматриваемой клетке-хозяине. Источником репликации может быть любой плазмидный репликатор, опосредующий автономную репликацию, которая функционирует в клетке. Термин «источник репликации» или «плазмидный репликатор» означает полинуклеотид, который позволяет репликацию плазмида или вектора in vivo.
Примерами бактериальных источников репликации являются источники репликации плазмидов pBR322, pUC19, pACYC177 и pACYC184, позволяющие репликацию в Ε. coli, и pUB110, pE194, рТА1060 и pΑΜβ1, позволяющие репликацию в Bacillus.
Примерами источников репликации для использования в дрожжевой клетке-хозяине являются 2 микрон источник репликации, ARS1, ARS4, комбинация ARS1 и CEN3, и комбинация ARS4 и CEN6.
Примерами источников репликации, полезных в мицелиальных грибковых клетках, являются АМА1 и ANSI (Gems et al., 1991, Gene 98: 61-67; Cullen et al., 1987, Nucleic Acids Res. 15: 9163-9175; WO 00/24883). Выделение гена АМА1 и конструирование плазмидов или векторов, содержащих ген, может быть достигнуто в соответствии со способами, описанными в WO 00/24883.
Более, чем одна копия полинуклеотида в соответствии с настоящим изобретением может быть вставлена в клетку-хозяин для увеличения продуцирования варианта. Увеличение числа копий полинуклеотида может быть получено интегрированием, по меньшей мере, одной дополнительной копии последовательности в геном клетки-хозяина или включением амплифицируемого селектируемого маркерного гена в полинуклеотид, где клетки, содержащие амплифицированные копии селектируемого маркерного гена, и, таким образом, дополнительные копии полинуклеотида, могут быть выбраны путем культивирования клеток в присутствии соответствующего селектируемого агента.
Процедуры, используемые для лигирования элементов, описанных выше, чтобы сконструировать рекомбинантные векторы экспрессии в соответствии с настоящим изобретением, хорошо известны специалистам в данной области техники (см., например, Sambrook et al., 1989, ранее).
Клетки-хозяева
Настоящее изобретение также относится к рекомбинантным клетка-хозяевам, содержащим полинуклеотид, кодирующий вариант в соответствии с настоящим изобретением, функционально связанный с одной или более контрольными последовательностями, которые направляют получение варианта в соответствии с настоящим изобретением. Конструкт или вектор, содержащий полинуклеотид, вводят в клетку-хозяин, так что конструкт или вектор поддерживаются в виде хромосомного интегранта или в виде самореплицирующегося экстра-хромосомного вектора, как описано ранее. Термин «клетка-хозяин» охватывает любое потомство родительской клетки, которое не идентично родительской клетке, в связи с мутациями, которые происходят во время репликации. Выбор клетки-хозяина будет в значительной степени зависеть от гена, кодирующего вариант, и его источника.
Клетка-хозяин может быть любой клеткой, полезной в рекомбинантном получении варианта, например, прокариотом или эукариотом.
Прокариотная клетка-хозяин может быть любой грамм-позитивной или грамм-негативной бактерией. Грамм-позитивные бактерии включают, но не ограничиваясь приведенным, Bacillus, Clostridium, Enterococcus, Geobacillus, Lactobacillus, Lactococcus, Oceanobacillus, Staphylococcus, Streptococcus и Streptomyces. Грамм-негативные бактерии включают, но не ограничиваясь приведенным, Campylobacter, Ε. coli, Flavobacterium, Fusobacterium, Helicobacter, Ilyobacter, Neisseria, Pseudomonas, Salmonella и Ureaplasma.
Бактериальная клетка-хозяин может быть любой Bacillus клеткой, включая, но не ограничиваясь приведенным, Bacillus alkalophilus, Bacillus amyloliquefaciens, Bacillus brevis, Bacillus circulons, Bacillus clausii, Bacillus coagulans, Bacillus firmus, Bacillus lautus, Bacillus lentus, Bacillus licheniformis, Bacillus megaterium, Bacillus pumilus, Bacillus stearothermophilus, Bacillus subtilis и Bacillus thuringiensis клетки.
Бактериальная клетка-хозяин может быть также любой Streptococcus клеткой, включая, но не ограничиваясь приведенным, Streptococcus equisimilis, Streptococcus pyogenes, Streptococcus uberis и Streptococcus equi subsp.Zooepidemicus клетки.
Бактериальная клетка-хозяин может быть также любой Streptomyces клеткой, включая, но не ограничиваясь приведенным, Streptomyces achromogenes, Streptomyces avermitilis, Streptomyces coelicolor, Streptomyces griseus и Streptomyces lividans клетки.
Введение ДНК в Bacillus клетку может быть направлено протопластной трансформацией (см., например, Chang and Cohen, 1979, Mol. Gen. Genet. 168: 111-115), компетентной клеточной трансфорацией (см., например, Young and Spizizen, 1961, J. Bacterio!. 81: 823-829, или Dubnau and Davidoff-Abelson, 1971, J. Mol. Biol. 56: 209-221), электропорацией (см., например, Shigekawa and Dower, 1988, Biotechniques 6: 742-751), или конъюгацией (см., например, Koehler and Thome, 1987, J. Bacterio!. 169: 5271-5278). Введение ДНК в Ε. coli клетку может быть направлено протопластной трансформацией (см., например, Hanahan, 1983, J. Mol. Biol. 166: 557-580) или электропорацией (см., например, Dower et al., 1988, Nucleic Acids Res. 16: 6127-6145). Введение ДНК в Streptomyces клетку может быть направлено протопластной трансформацией, электропорацией (см., например, Gong et al., 2004, Folia Microbiol. (Praha) 49: 399-405), конъюгацией (см., например, Mazodier et al., 1989, J. Bacteriol. 171: 3583-3585) или трансдукцией (см., например, Burke et al., 2001, Proc. Natl. Acad. Sci. USA 98: 6289-6294). Введение ДНК в Pseudomonas клетку может быть направлено электропорацией (см., например, Choi et al., 2006, J. Microbiol. Methods 64: 391-397), или конъюгацией (см., например, Pinedo and Smets, 2005, Appl. Environ. Microbiol. 71: 51-57). Введение ДНК в Streptococcus клетку может быть направлено природной конкуренцией (см., например, Perry and Kuramitsu, 1981, Infect. Immun. 32: 1295-1297), протопластной трансфорацией (см., например, Catt and Jollick, 1991, Microbios 68: 189-207), электропорацией (см., например, Buckley et al., 1999, Appl. Environ. Microbiol. 65: 3800-3804) или конъюгацией (см., например, Clewell, 1981, Microbiol. Rev. 45: 409-436). Однако, любой способ, известный в данной области техники для введения ДНК в клетку-хозяин может быть использован.
Клетка-хозяин может также быть эукариотом, таким как клетка млекопитающих, насекомых, растений или грибковая клетка.
Клетка-хозяин может быть грибковой клеткой. «Грибы» как используют в данной заявке включают тип Ascomycota, Basidiomycota, Chytridiomycota и Zygomycota, а также Oomycota и все митоспорные грибы (как определено Hawksworth et al., In, Ainsworth and Bisby's Dictionary of The Fungi, 8th edition, 1995, CAB International., University Press, Cambridge, UK).
Грибковая клетка-хозяин может быть дрожжевой клеткой. «Дрожжи» как используют в данной заявке включают ascosporogenous дрожжи (Endomycetales), basidiosporogenous дрожжи и дрожжи семейства Fungi Imperfecti (Blastomycetes). Поскольку классификация дрожжей может изменяться в будущем, для целей настоящего изобретения, дрожжи должны быть определены как описано в Biology and Activities of Yeast (Skinner, Passmore, and Davenport, editors, Soc. App.Bacterio I. Symposium Series No. 9, 1980).
Дрожжевой клеткой-хозяином может быть Candida, Hansenula, Kluyveromyces, Pichia, Saccharomyces, Schizosaccharomyces или Yarrowia клетка, например Kluyveromyces lactis, Saccharomyces carlsbergensis, Saccharomyces cerevisiae, Saccharomyces diastaticus, Saccharomyces douglasii, Saccharomyces kluyveri, Saccharomyces norbensis, Saccharomyces oviformis или Yarrowia lipolytica клетка.
Грибковой клеткой-хозяином может быть мицелиальная грибковая клетка. «Мицелиальные грибы» включают все мицелиальные формы подгруппы Eumycota и Oomycota (как определено Hawksworth et al., 1995, ранее). Мицелиальные грибы в общем характеризуются мицелиальной стенкой, состоящей из хитина, целлюлозы, глюкана, хитозана, маннана и других сложных полисахаридов. Вегетативный рост вызван удлинением гифов и углеродный катаболизм является обязательно аэробным. Напротив вегетативный рост, вызванный дрожжами, такими как Saccharomyces cerevisiae вызван почкованием одноклеточного таллома и углеродный катаболизм может быть ферментативным.
Мицелиальная грибковая клетка-хозяин может быть Acremonium, Aspergillus, Aureobasidium, Bjerkandera, Ceriporiopsis, Chrysosporium, Coprinus, Coriolus, Cryptococcus, Filibasidium, Fusarium, Humicola, Magnaporthe, Mucor, Myceliophthora, Neocallimastix, Neurospora, Paecilomyces, Pénicillium, Phanerochaete, Phlebia, Piromyces, Pleurotus, Schizophyllum, Talaromyces, Thermoascus, Thielavia, Tolypocladium, Trametes или Trichoderma клеткой.
Например, мицелиальная грибковая клетка-хозяин может быть Aspergillus awamori, Aspergillus foetidus, Aspergillus fumigatus, Aspergillus japonicus, Aspergillus nidulans, Aspergillus niger, Aspergillus oryzae, Bjerkandera adusta, Ceriporiopsis aneirina, Ceriporiopsis caregiea, Ceriporiopsis gilvescens, Ceriporiopsis pannocinta, Ceriporiopsis rivulosa, Ceriporiopsis subrufa, Ceriporiopsis subvermispora, Chrysosporium inops, Chrysosporium keratinophilum, Chrysosporium lucknowense, Chrysosporium merdarium, Chrysosporium pannicola, Chrysosporium queenslandicum, Chrysosporium tropicum, Chrysosporium zonatum, Coprinus cinereus, Coriolus hirsutus, Fusarium bactridioides, Fusarium cerealis, Fusarium crookwellense, Fusarium culmorum, Fusarium graminearum, Fusarium graminum, Fusarium heterosporum, Fusarium negundi, Fusarium oxysporum, Fusarium reticulatum, Fusarium roseum, Fusarium sambucinum, Fusarium sarcochroum, Fusarium sporotrichioides, Fusarium sulphureum, Fusarium torulosum, Fusarium trichothecioides, Fusarium venenatum, Humicola insolens, Humicola lanuginosa, Mucor miehei, Myceliophthora thermophila, Neurospora crassa, Pénicillium purpurogenum, Phanerochaete chrysosporium, Phlebia radiata, Pleurotus eryngii, Thielavia terrestris, Trametes villosa, Trametes versicolor, Trichoderma harzianum, Trichoderma koningii, Trichoderma longibrachiatum, Trichoderma reesei или Trichoderma viride клеткой.
Грибковые клетки могут быть трансформированы процессом, включающим образование протопластов, трансформацию протопластов и регенерацию клеточной стенки способом, известным в чистом виде. Приемлемые процедуры трансформации Aspergillus и Trichoderma клеток-хозяев описаны в ЕР 238023, Yelton et al., 1984, Proc. Natl. Acad. Sci. USA 81: 1470-1474, и Christensen et al., 1988, Bio/Technology 6: 1419-1422. Приемлемые способы трансформации Fusarium видов описаны Malardier et al., 1989, Gene 78: 147-156, и WO 96/00787. Дрожжи могут быть трансформированы при помощи процедур, описанных Becker and Guarente, In Abelson, J.N. and Simon, M.I., editors, Guide to Yeast Genetics and Molecular Biology, Methods in Enzymology, Volume 194, pp 182-187, Academic Press, Inc., New York; Ito et al., 1983, J. Bacteriol. 153: 163; и Hinnen et al., 1978, Proc. Natl Acad. Sci. USA 75: 1920.
Способы получения
Также в данной заявке раскрыты способы получения варианта, включающие стадии, на которых: (а) культивируют клетку-хозяина в соответствии с настоящим изобретением в условиях, приемлемых для экспрессии варианта; и (b) восстанавливают вариант.
Клетки-хозяева культивируют в питательной среде, приемлемой для получения варианта с использованием способов, известных в данной области техники. Например, клетку можно культивировать путем культивирования встряхиванием в колбе, или мелкомасштабной или крупномасштабной ферментации (в том числе непрерывной, периодической, подпиткой или твердотельной ферментации) в лабораторных или промышленных ферментерах, выполняемого в приемлемой среде и в условиях, позволяющих экспрессию и/или выделение варианта. Культивирование проводят в приемлемой питательной среде, содержащей источники углерода и азота и неорганические соли, с использованием методов, известных в данной области техники. Приемлемые среды доступны от коммерческих поставщиков или могут быть получены в соответствии с опубликованными композициями (например, в каталогах коллекции American Type Culture). Если вариант секретируется в питательную среду, вариант может быть восстановлен непосредственно из среды. Если вариант не секретируется, он может быть восстановлен из клеточных лизатов.
Вариант может быть обнаружен с использованием способов, известных в данной области техники, которые являются специфическими для вариантов. Эти способы обнаружения включают, но не ограничиваясь приведенным, использование специфических антител, образование ферментного продукта или исчезновение ферментного субстрата. Например, для определения активности варианта может быть использован ферментный анализ.
Вариант может быть восстановлен с использованием способов, известных в данной области техники. Например, вариант может быть восстановлен из питательной среды с помощью обычных процедур включая, но не ограничиваясь приведенным, сбор, центрифугирование, фильтрацию, экстракцию, сушку распылением, испарение или осаждение.
Вариант может быть очищен с помощью различных процедур, известных в данной области техники, включая, но не ограничиваясь приведенным, хроматографию (например, ионообменную, аффинную, гидрофобную, хроматофокусирование и эксклюзионную хроматографию), электрофоретические процедуры (например, препаративное изоэлектрическое фокусирование), дифференциальную растворимость (например, осаждение сульфатом аммония), SDS-PAGE или экстракцию (см., например, Protein Purification, Janson и Ryden, editors, VCH Publishers, New York, 1989), чтобы получить по существу чистые варианты.
В альтернативном аспекте, вариант не восстанавливается, скорее клетка-хозяин в соответствии с настоящим изобретением, экспрессирующая вариант, используется как источник варианта.
Композиции
Также в данной заявке раскрыты композиции в виде частиц, как описано в ЕР11170520, содержащие вариант липазы, содержащий замену в одном или более положениях, соответствующих положениям T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q зрелого полипептида SEQ ID NO: 1, при этом вариант имеет липазную активность.
В некоторых воплощениях композиция в виде частиц содержит: (а) частицы, содержащие источник органических пероксикислот; и (b) частицы, содержащие катализатор отбеливания; и (с) частицы, содержащие (i) ядро, содержащее фермент, окруженный (ii) покрытием с замедленным высвобождением, при этом фермент представляет собой вариант липазы, содержащий замену в одном или более положениях, соответствующих положениям T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q зрелого полипептида SEQ ID ΝΟ: 1, при этом вариант имеет липазную активность.
В некоторых воплощениях композиция в виде частиц содержит: (а) частицы, содержащие источник органических пероксикислот; и (b) частицы, содержащие катализатор отбеливания; и (с) частицы, содержащие (i) ядро, содержащее фермент, который представляет собой липолитический фермент первого цикла стирки, окруженный (и) покрытием с замедленным высвобождением, при этом вариант липазы содержит замену в одном или более положениях, соответствующих положениям T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q зрелого полипептида SEQ ID NO: 1, при этом вариант имеет липазную активность.
Применения
Также в данной заявке раскрыто применение варианта липазы, содержащего замену в одном или более положениях, соответствующих положениям T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q зрелого полипептида SEQ ID ΝΟ: 1, при этом вариант имеет липазную активность, для получения частиц липазы как описано в EP 11170520.
В некоторых воплощениях способ получения частиц липазы включает стадии, на которых: (а) тестируют на восприимчивость к катализатору отбеливания, по меньшей мере, один фермент, путем определения моющей производительности для объединения фермента с катализатором отбеливания и источником органических пероксикислот, и сравнивают с производительностью без катализатора отбеливания, для идентификации восприимчивого к катализатору отбеливания фермента; (b) обеспечивают ядро, содержащее восприимчивый фермент, и окружают ядро покрытием с замедленным высвобождением, при этом, по меньшей мере, один фермент представляет собой вариант липазы, содержащий замену в одном или более положениях, соответствующих положениям T37A,D,E,F,G,H,I,L,N,P,Q,R,S,V,W,Y, N39A,C,D,E,F,G,I,K,L,M,P,Q,R,T,V,W,Y и G91D,H,I,P,Q зрелого полипептида SEQ ID NO: 1.
Предпочтительно липаза присутствует в композиции в количествах от 0,00001% до 2%, более предпочтительно от 0,0001% до 0,02%, наиболее предпочтительно от 0,001% до 0,01% мас. %. Типично композиция для очистки и/или обработки присутствует в воде в количестве от 0,001 до 5%, так что предпочтительные уровни варианта липазы на стадии водной обработки составляют от 0,000001 до 1000 м.д.
Отбеливающий компонент
Отбеливающий компонент, приемлемый для включения в способы и композиции в соответствии с настоящим изобретением, содержит один или смесь более одного отбеливающих компонентов. Приемлемые отбеливающие компоненты включают катализаторы отбеливания, фотоотбеливатели, активаторы отбеливания, перекись водорода, источники перекиси водорода, предварительно полученные перкислоты и их смеси. В общем, когда используют отбеливающий компонент, композиции в соответствии с настоящим изобретением могут содержать от приблизительно 0,00001 до 90 мас. %, предпочтительно от 0,0001% до приблизительно 50% или даже от приблизительно 0,001% до приблизительно 25% отбеливающего компонента по массе рассматриваемой композиции для очистки. Примеры приемлемых отбеливающих компонентов включают:
(1) Предварительно полученные перкислоты: Приемлемые предварительно полученные перкислоты включают, но не ограничиваясь приведенным, соединения, выбранные из группы, состоящей из предварительно полученных пероксикислот или их солей, типично пероксикарбоновой кислоты или ее соли, или пероксисульфоновой кислоты или ее соли.
Предварительно полученная пероксикислота или ее соль предпочтительно представляет собой пероксикарбоновую кислоту или ее соль, типично имеющие химическую структуру, соответствующую следующей химической формуле:

где: R14 выбирают из алкильных, аралкильных, циклоалкильных, арильных или гетероциклических групп; группа R14 может быть линейной или разветвленной, замещенной или незамещенной; и Y представляет собой любой приемлемый противоион, достигающий нейтральности электронного заряда, предпочтительно Y выбирают из водорода, натрия или калия. Предпочтительно, R14 является линейным или разветвленным, замещенным или незамещенным С6-9 алкилом. Предпочтительно, пероксикислоту или ее соль выбирают из пероксигексаноевой кислоты, пероксигептаноевой кислоты, пероксиоктаноевой кислоты, пероксинонаноевой кислоты, пероксидеканоевой кислоты, их любой соли, или их любой комбинации. Особо предпочтительными пероксикислотами являются фталимидо-перокси-алканоевые кислоты, в частности ε-фталимидо перокси гексаноевая кислота (РАР). Предпочтительно, пероксикислота или ее соль имеет температуру плавления в диапазоне от 30°С до 60°С.
Предварительно полученная пероксикислота или ее соль могут также быть пероксисульфоновой кислотой или ее солью, типично имеющими химическую структуру, соответствующую следующей химической формуле:

где: R15 выбирают из алкильных, аралкильных, циклоалкильных, арильных или гетероциклических групп; группа R15 может быть линейной или разветвленной, замещенной или незамещенной; и Z представляет собой любой приемлемый противоион, достигающий нейтральности электронного заряда, предпочтительно Z выбирают из водорода, натрия или калия. Предпочтительно R15 является линейным или разветвленным, замещенным или незамещенным С6-9 алкилом.
Предпочтительно такие отбеливающие компоненты могут присутствовать в композициях в соответствии с настоящим изобретением в количестве от 0,01 до 50%, наиболее предпочтительно от 0,1% до 20%.
(2) Источники перекиси водорода включают, например, неорганические пергидратные соли, в том числе соли щелочных металлов, такие как натриевые соли пербората (обычно моно- или тетра-гидрат), перкарбоната, персульфата, перфосфата, персиликатные соли и их смеси. В одном аспекте настоящего изобретения неорганические пергидратные соли являются такими как те, которые выбраны из группы, состоящей из натриевых солей пербората, перкарбоната и их смесей. В случае использования, неорганические пергидратные соли обычно присутствуют в количествах от 0,05 до 40 мас. %, или от 1 до 30 мас. % всей композиции, и, как правило, включены в такие композиции в виде кристаллического твердого вещества, которое может быть покрыто. Приемлемые покрытия включают неорганические соли, такие как силикат щелочного металла, карбонатные или боратные соли или их смеси, или органические материалы, такие как водорастворимые или диспергируемые полимеры, воски, масла или жирные мыла.
Предпочтительно такие отбеливающие компоненты могут присутствовать в композициях в соответствии с настоящим изобретением в количестве от 0,01 до 50%, наиболее предпочтительно от 0,1% до 20%.
(3) Приемлемые активаторы отбеливания являются теми, которые имеют R-(C=O)-L, где R представляет собой алкильную группу, необязательно разветвленную, содержащую, когда активатор отбеливания является гидрофобным, от 6 до 14 атомов углерода, или от 8 до 12 атомов углерода, и, когда активатор отбеливания является гидрофильным, менее, чем 6 атомов углерода или даже менее, чем 4 атома углерода; и L является отходящей группой. Примерами приемлемых отходящих групп являются бензойная кислота и ее производные - особенно бензолсульфонат. Приемлемые активаторы отбеливания включают додеканоилоксибензолсульфонат, деканоилоксибензолсульфонат, деканоилоксибензойную кислоту или ее соли, 3,5,5-триметилгексаноилоксибензолсульфонат сульфонат, тетраацетилэтилендиамин (TAED) и нонаноилоксибензолсульфонат (NOBS). Приемлемые активаторы отбеливания также раскрыты в WO 98/17767. В то время как любой приемлемый активатор отбеливания может быть использован, в одном аспекте в соответствии с настоящим изобретением рассматриваемая композиция для очистки может содержать NOBS, TAED или их смеси. Когда присутствует, перкислота и/или активатор отбеливания, как правило, присутствует в потребительском продукте в количестве от приблизительно 0,1 до приблизительно 60 мас. %, от приблизительно 0,5 до приблизительно 40 мас. % или даже от приблизительно 0,6 до приблизительно 10 мас. %, исходя из продукта для ухода за тканями и бытового ухода. Одна или более гидрофобных перкислот или их предшественников могут быть использованы в сочетании с одной или более гидрофильной перкислотой или ее предшественником.
Предпочтительно, такие отбеливающие компоненты могут присутствовать в композициях в соответствии с настоящим изобретением в количестве от 0,01 до 50%, наиболее предпочтительно от 0,1% до 20%.
Количества источника перекиси водорода и перкислоты или активатора отбеливания могут быть выбраны таким образом, что молярное соотношение доступного кислорода (из источника пероксида) и перкислоты составляет от 1:1 до 35:1, или даже от 2:1 до 10:1.
(4) Диацилпероксиды - предпочтительные отбеливатели на основе диацилпероксидов включают выбранные из диацил пероксидов общей формулы:
R1-C(Ο)-ΟΟ-(Ο)C-R2,
где R1 представляет собой C6-C18 алкил, предпочтительно C6-C12 алкильную группу, содержащую линейную цепь из, по меньшей мере, 5 атомов углерода и необязательно содержащую один или более заместителей (например, -N+ (СН3)3, -СООН или -CN) и/или один или более прерывающих фрагментов (например, -CONH-или -СН=СН-), интерполированных между соседними атомами углерода алкильного радикала и R2 представляет собой алифатическую группу, совместимую с пероксидным фрагментом, так что R1 и R2 вместе содержат в общем от 8 до 30 атомов углерода. В одном предпочтительном аспекте R1 и R2 представляют собой линейные незамещенные С6-С12 алкильные цепи. Наиболее предпочтительно R1 и R2идентичны. Диацил пероксиды, в которых как R1 так и R2 представляют собой С6-С12алкильные группы, являются особенно предпочтительными. Предпочтительно, по меньшей мере, одна из, наиболее предпочтительно только одна из групп R (R1 или R2) не содержит разветвленных или подвешенных циклов в альфа-положении, или предпочтительно ни в альфа-, ни в бета-положениях, или наиболее предпочтительно ни в альфа-, ни в бета-, ни в гамма-положениях. В одном дополнительном предпочтительном воплощении DAP может быть асимметричным, так что предпочтительно гидролиз ацильной группы R1 является быстрым для образования перкислоты, но гидролиз ацильной группы R2 является медленным.
Отбеливатели на основе тетраацил пероксида предпочтительно выбирают из тетраацилпероксидов общей формулы:
R3-C(O)-OO-C(O)-(CH2)n-C(O)-OO-C(O)-R3,
где R3 представляет собой С1-С9 алкил, предпочтительно С3-С7 группу и n является целым числом от 2 до 12, предпочтительно от 4 до 10 включительно.
Предпочтительно, отбеливатели на основе диацил и/или тетраацилпероксида присутствуют в количестве, достаточном для обеспечения, по меньшей мере, 0,5 м.д., более предпочтительно, по меньшей мере, 10 м.д., и даже более предпочтительно, по меньшей мере, 50 м.д. по массе моющего раствора. В предпочтительном воплощении, отбеливатели присутствуют в количестве, достаточном для обеспечения от приблизительно 0,5 до приблизительно 300 м.д., более предпочтительно от приблизительно 30 до приблизительно 150 м.д. по массе моющего раствора.
Предпочтительно отбеливающий компонент содержит катализатор отбеливания (5 и 6).
(5) Предпочтительными являются органические (неметаллические) катализаторы отбеливания, включающие катализатор отбеливания, способный акцептировать атом кислорода от пероксикислоты и/или ее соли, и переносить атом кислорода на окисляемый субстрат. Приемлемые катализаторы отбеливания включают, но не ограничиваясь приведенным: иминий катионы и полиионы; иминий цвиттерионы; модифицированные амины; модифицированные аминоксиды; N-сульфонилимины; N-фосфонилимины; N-ацилимины; тиадиазолдиоксиды; перфторимины; циклические сахарные кетоны и их смеси.
Приемлемые иминий катионы и полиионы включают, но не ограничиваясь приведенным, N-метил-3,4-дигидроизохинолиний тетрафторборат, полученный, как описано в Tetrahedron (1992), 49(2), 423-38 (см., например, соединение 4, р. 433); N-метил-3,4-дигидроизохинолиний п-толуолсульфонат, полученный как описано в патенте США 5,360,569 (см., например, колонка 11, Пример 1); и N-OKmrc-3,4-дигидроизохинолиний п-толуолсульфонат, полученный как описано в патенте США 5,360,568 (см., например, колонка 10, Пример 3).
Приемлемые иминий цвиттерионы включают, но не ограничиваясь приведенным, N-(3-сульфопропил)-3,4-дигидроизохинолиний, внутренняя соль, полученную, как описано в патенте США 5,576,282 (см., например, колонка 31, Пример II); N-[2-(сульфоокси)додецил]-3,4-дигидроизохинолиний, внутренняя соль, полученную, как описано в патенте США 5,817,614 (см., например, колонка 32, Пример V); 2-[3-[(2-этилгексил)окси]-2-(сульфоокси)пропил]-3,4-дигидроизохинолиний, внутренняя соль, полученную, как описано в WO 05/047264 (см., например, страницу 18, Пример 8) и 2-[3-[(2-бутилоктил)окси]-2-(сульфоокси)пропил]-3,4-дигидроизохинолиний, внутренняя соль.
Приемлемые модифицированные аминные катализаторы переноса кислорода включают, но не ограничиваясь приведенным, 1,2,3,4-тетрагидро-2-метил-1-изохинолинол, который может быть получен в соответствии с процедурами, описанными в Tetrahedron Letters (1987), 28(48), 6061-6064. Приемлемые модифицированные аминные катализаторы переноса кислорода включают, но не ограничиваясь приведенным, натрий 1-гидрокси-N-окси-N-[2-(сульфоокси)децил]-1,2,3,4-тетрагидроизохинолин.
Приемлемые N-сульфонилиминные катализаторы переноса кислорода включают, но не ограничиваясь приведенным, 3-метил-1,2-бензизотиазол 1,1-диоксид, полученный в соответствии с процедурой, описанной в the Journal of Organic Chemistry (1990), 55(4), 1254-61.
Приемлемые N-фосфонилиминные катализаторы переноса кислорода включают, но не ограничиваясь приведенным, [R-(Е)]-N-[(2-хлоро-5-нитрофенил)метилен]-Р-фенил-Р-(2,4,6-триметилфенил)-фосфиновый амид, который может быть получен в соответствии с процедурами, описанными в the Journal of the Chemical Society, Chemical Communications (1994), (22), 2569-70.
Приемлемые N-ацилиминные катализаторы переноса кислорода включают, но не ограничиваясь приведенным, [N(Е)]-N-(фенилметилен)ацетамид, который может быть получен в соответствии с процедурами, описанными в Polish Journal of Chemistry (2003), 77(5), 577-590.
Приемлемые тиадиазолдиоксидные катализаторы переноса кислорода включают, но не ограничиваясь приведенным, 3-метил-4-фенил-1,2,5-тиадиазол 1,1-диоксид, который может быть получен в соответствии с процедурами, описанными в патенте США 5,753,599 (колонка 9, Пример 2).
Приемлемые перфториминные катализаторы переноса кислорода включают, но не ограничиваясь приведенным, (Z)-2,2,3,3,4,4,4-гептафтор-N-(нонафторбутил)бутанимидоилфторид, который может быть получен в соответствии с процедурами, описанными в Tetrahedron Letters (1994), 35(34), 6329-30.
Приемлемые катализаторы переноса кислорода на основе циклических сахарных кетонов включают, но не ограничиваясь приведенным, 1,2:4,5-ди-O-изопропилиден-D-эритро-2,3-гексодиуро-2,6-пиранозу, как получено в патенте США 6,649,085 (колонка 12, Пример 1).
Предпочтительно, катализатор отбеливания содержит иминиевую и/или карбонильную функциональную группу и, как правило, способен образовывать оксазиридиниевую и/или диоксирановую функциональную группу после принятия атома кислорода, особенно после принятия атома кислорода от пероксикислоты и/или ее соли. Предпочтительно, катализатор отбеливания включает оксазиридиниевую функциональную группу и/или способен образовывать оксазиридиниевую функциональную группу после принятия атома кислорода, особенно после принятия атома кислорода от пероксикислоты и/или ее соли. Предпочтительно, катализатор отбеливания содержит циклическую иминиевую функциональную группу, предпочтительно, где циклический фрагмент имеет размер цикла от пяти до восьми атомов (включая атом азота), предпочтительно шесть атомов. Предпочтительно, катализатор отбеливания содержит арилиминиевую функциональную группу, предпочтительно би-циклическую арилиминиевую функциональную группу, предпочтительно 3,4-дигидроизохинолиний функциональную группу. Как правило, иминная функциональная группа представляет собой четвертичную иминную функциональную группу, и, как правило, способна образовывать четвертичную оксазиридиниевую функциональную группу, после принятия атома кислорода, особенно после принятия атома кислорода от пероксикислоты и/или ее соли. В другом аспекте, композиция моющего средства содержит отбеливающий компонент, имеющий logPo/w не более, чем 0, не более, чем -0,5, не более, чем -1,0, не более, чем -1,5, не более, чем -2,0, не более, чем -2,5, не более, чем -3,0, или даже не более, чем -3,5. Способ определения logPo/w описан более подробно ниже.
Как правило, отбеливающий ингредиент способен образовывать отбеливатели, имеющие XSO от 0,01 до приблизительно 0,30, от 0,05 до приблизительно 0,25, или даже от приблизительно 0,10 до 0,20. Способ определения XSO описан более подробно ниже. Например, отбеливающие ингредиенты, имеющие структуру изохинолиния, способны образовывать отбеливатели, которые имеет структуру оксазиридиния. В этом примере, Xso относится к оксазиридиниевым отбеливателям.
Предпочтительно, катализатор отбеливания имеет химическую структуру, соответствующую следующей химической формуле

где: n и m независимо означают от 0 до 4; каждый R1 независимо выбран из замещенного или незамещенного радикала, выбранного из группы, состоящей из водорода, алкила, циклоалкила, арила, конденсированного арила, гетероциклического кольца, конденсированного гетероциклического кольца, нитро, гало, циано, сульфонато, алкокси, кето, карбоксильного и карбоалкокси радикалов, и любые два вицинальные заместителя R1 могут быть объединены с образованием конденсированного арильного, конденсированного карбоциклического или конденсированного гетероциклического кольца; каждый R2 независимо выбран из замещенного или незамещенного радикала, независимо выбранного из группы, состоящей из водорода, гидрокси, алкила, циклоалкила, алкарила, арила, аралкила, алкиленов, гетероциклического кольца, алкокси, арилкарбонильных групп, карбоксиалкильных групп и амидных групп; любой R2 может быть соединен вместе с любым другим из R2 с образованием части общего цикла; любой геминальный R2 может объединяться с образованием карбонила; и при этом любые два R2 могут объединяться с образованием замещенного или незамещенного конденсированного ненасыщенного фрагмента; R3 представляет собой С1-С20 замещенный или незамещенный алкил; R4 представляет собой водород или фрагмент Qt-A, где: Q представляет собой разветвленный или неразветвленный алкилен, t=0 или 1, и А представляет собой анионную группу, выбранную из группы, состоящей из OSO3-, SO3-, СО2-, ОСО2-, ОРО32-, ОРО3Н- и ОРО2-; R5 представляет собой водород или фрагмент -CR11R12-Y-Gb-Yc-[(CR9R10)y-O]k-R8, где: каждый Y независимо выбран из группы, состоящей из О, S, N-H или N-R8; и каждый R8 независимо выбран из группы, состоящей из алкила, арила и гетероарила, при этом указанные фрагменты являются замещенными или незамещенными, и независимо от того, являются ли они замещенными или незамещенными, указанные фрагменты имеют менее, чем 21 атом углерода; каждый G независимо выбран из группы, состоящей из СО, SO2, SO, PO и РО2; R9 и R10 независимо выбраны из группы, состоящей из водорода и С1-С4 алкила; R11 и R12 независимо выбраны из группы, состоящей из водорода и алкила, или, взятые вместе, могут объединяться с образованием карбонила; b=0 или 1; с может равняться 0 или 1, но с должно равняться 0, если b=0; у означает целое число от 1 до 6; k означает целое число от 0 до 20; R6 представляет собой Н, или алкильный, арильный или гетероарильный фрагмент; причем указанные фрагменты являются замещенными или незамещенными; и X, если присутствует, представляет собой приемлемый уравновешивающий заряд противоион, предпочтительно X присутствует если R4 представляет собой водород, приемлемый X, включает, но не ограничиваясь приведенным: хлорид, бромид, сульфат, метосульфат, сульфонат, п-толуолсульфонат, бортетрафторид и фосфат.
В одном воплощении в соответствии с настоящим изобретением, катализатор отбеливания имеет структуру, соответствующую общей формуле, приведенной ниже:

где R13 представляет собой разветвленную алкильную группу, содержащую от трех до 24 атомов углерода (включая разветвленные атомы углерода) или линейную алкильную группу, содержащую от одного до 24 атомов углерода; предпочтительно R13 представляет собой разветвленную алкильную группу, содержащую от восьми до 18 атомов углерода, или линейную алкильную группу, содержащую от восьми до восемнадцати атомов углерода; предпочтительно R13 выбирают из группы, состоящей из 2-пропилгептила, 2-бутилоктила, 2-пентилнонила, 2-гексилдецила, н-додецила, н-тетрадецила, н-гексадецила, н-октадецила, изо-нонила, изо-децила, изо-тридецила и изо-пентадецила; предпочтительно R13 выбирают из группы, состоящей из 2-бутилоктила, 2-пентилнонила, 2-гексилдецила, изо-тридецила и изо-пентадецила.
Предпочтительно, отбеливающий компонент содержит источник перкислоты в дополнение к катализатору отбеливания, в особенности органическому катализатору отбеливания. Источник перкислоты может быть выбран из (а) предварительно полученной перкислоты; (b) перкарбонатной, перборатной или персульфатной соли (источник перекиси водорода) предпочтительно в сочетании с активатором отбеливания; и (с) пергидролазного фермента и сложного эфира для образования перкислоты in situ в присутствии воды на стадии обработки ткани или твердой поверхности.
Если присутствует, перкислота и/или активатор отбеливания в общем присутсвует в композиции в количестве от приблизительно 0,1 до приблизительно 60 мас. %, от приблизительно 0,5 до приблизительно 40 мас. % или даже от приблизительно 0,6 до приблизительно 10 мас. % исходя из композиции. Одна или более гидрофобных перкислот или их предшественников могут быть использованы в сочетании с одной или более гидрофильными перкислотами или их предшественниками.
Количества источника перекиси водорода и перксилоты или активатора отбеливания могут быть выбраны таким образом, что молярное соотношение доступного кислорода (из источника пероксида) и перксилоты составляет от 1:1 до 35:1, или даже от 2:1 до 10:1.
(6) Металлсодержащие катализаторы отбеливания - Отбеливающий компонент может быть обеспечен при помощи каталитического комплекса металла. Один тип металлсодержащего катализатора отбеливания представляет собой каталитическую систему, содержащую катион переходного металла с определенной каталитической активностью отбеливания, например катионы меди, железа, титана, рутения, вольфрама, молибдена или марганца, вспомогательный катион металла, имеющий небольшую или вообще не имеющий каталитической активности отбеливания, например катионы цинка или алюминия, и секвестрант, имеющий определенные константы стабильности каталитических и вспомогательных катионов металлов, в частности, этилендиаминтетрауксусную кислоту, этилендиаминтетра(метиленфосфониевую кислоту) и их водорастворимые соли. Такие катализаторы раскрыты в U.S. 4,430,243. Предпочтительные катализаторы описаны в WO 09/839406, US 6218351 и WO 00/012667. Особенно предпочтительными являются катализаторы на основе переходного металла или их лиганды, которые являются поперечномостиковыми полидентатными N-донорными лигандами.
При желании композиции в данной заявке можно катализировать с помощью соединения марганца. Такие соединения и уровни использования хорошо известны в данной области техники и включают, например, катализаторы на основе марганца, раскрытые в U.S. 5,576,282.
Кобальтовые катализаторы отбеливания, полезные в данной заявке, известны и описаны, например, в U.S. 5,597,936; U.S. 5,595,967, Такие кобальтовые катализаторы легко получают известными способами, такими как описаны, например в U.S. 5,597,936 и U.S. 5,595,967.
Композиции в данной заявке могут также приемлемым образом содержать комплекс переходного металла с лигандами, такими как биспидоны (US 7,501,389) и/или жесткие макрополициклические лиганды - сокращенно «MRL». С практической точки зрения, а не в качестве ограничения, композиции и способы в данной заявке можно регулировать, чтобы обеспечить порядок, по меньшей мере, одной части на сто миллионов молекул активного MRL в водной моющей среде, и типично обеспечивают от приблизительно 0,005 м.д. до приблизительно 25 м.д., от приблизительно 0,05 м.д. до приблизительно 10 м.д., или даже от приблизительно 0,1 м.д. до приблизительно 5 м.д. MRL в моющем растворе.
Подходящие переходные металлы в данном катализаторе отбеливания на основе переходного металла включают, например, марганец, железо и хром. Приемлемые MRLs включают 5,12-диэтил-1,5,8,12-тетраазабицикло[6.6.2]гексадекан.
Приемлемые MRLs на основе переходных металлов легко получают известными способами, такими, как описаны, например, в U.S. 6,225,464 и WO 00/32601.
(7) Фотоотбеливатели - приемлемые фотоотбеливатели включают, например, сульфированный фталоцианин цинка, сульфированные фталоцианины алюминия, ксантеновые красители и их смеси. Предпочтительные отбеливающие компоненты для использования в композициях в соответствии с настоящим изобретением, включают источник перекиси водорода, активатор отбеливания и/или органическую пероксикислоту, которые необязательно образовываются in situ путем реакции источника перекиси водорода и активатора отбеливания, в сочетании с катализатором отбеливания. Предпочтительные отбеливающие компоненты включают катализаторы отбеливания, предпочтительно органические катализаторы отбеливания, как описано выше.
Особенно предпочтительными отбеливающими компонентами являются катализаторы отбеливания, в частности органические катализаторы отбеливания.
Композиции в соответствии с настоящим изобретением являются, в частности твердыми или жидкими композициями для очистки и/или обработки. В предпочтительном аспекте в соответствии с настоящим изобретением, композиция имеет форму единичной дозы с одним или с несколькими отделениями.
Вспомогательные вещества
В то время как это не является существенным для целей настоящего изобретения, неограничивающий перечень вспомогательных веществ, который проиллюстрирован в данной заявке, приемлемый для использования в композициях и способах в данной заявке, может быть желательно вводить в определенных воплощениях в соответствии с настоящим изобретением, например, чтобы способствовать или улучшать производительность очистки, для обработки субстрата, который подлежит очистке или чтобы изменить эстетику потребительского продукта, как и в случае отдушек, окрашивающих веществ, красителей и тому подобное. Уровни любых таких вспомогательных веществ, включенных в любой продукт для ухода за тканями и бытового ухода, предназначены для дополнения любых веществ, перечисленных в данной заявке для включения. Точный характер этих дополнительных компонентов и уровни их включения будут зависеть от физической формы потребительского продукта и от характера операции очистки, для которой он должен быть использован. Приемлемые вспомогательные вещества включают, но не ограничиваясь приведенным, поверхностно-активные вещества, модифицирующие добавки, хелатирующие агенты, агенты, ингибирующие перенос красителя, диспергаторы, ферменты и стабилизаторы ферментов, каталитические материалы, активаторы отбеливания, перекись водорода, источники перекиси водорода, предварительно полученные перкислоты, полимерные диспергирующие агенты, агенты для удаления/против повторного отложения глинистых загрязнений, блескообразователи, подавители пенообразования, красители, оттеночные красители, отдушки, системы доставки отдушек, агенты структурной эластичности, смягчители для ткани, носители, гидротропы, технологические добавки, растворители и/или пигменты. В дополнение к приведенному ниже описанию, приемлемые примеры таких других вспомогательных веществ и уровни использования можно найти в патентах США №№5,576,282, 6,306,812 В1 и 6,326,348 В1, которые включены в данную заявку путем ссылки.
Как указывалось, вспомогательные ингредиенты не являются существенными для потребительских продуктов Заявителей. Таким образом, определенные воплощения потребительских продуктов Заявителей не содержат одно или более из следующих вспомогательных веществ: поверхностно-активные вещества, модифицирующие добавки, хелатирующие агенты, агенты, ингибирующие перенос красителя, диспергаторы, дополнительные ферменты и стабилизаторы ферментов, каталитические материалы, активаторы отбеливания, перекись водорода, источники перекиси водорода, предварительно полученные перкислоты, полимерные диспергирующие агенты, агенты для удаления/против повторного отложения глинистых загрязнений, блескообразователи, подавители пенообразования, красители, отдушки, системы доставки отдушек, агенты структурной эластичности, смягчители для ткани, носители, гидротропы, технологические добавки, растворители и/или пигменты. Однако если одно или более вспомогательных веществ присутствуют, такие одно или более вспомогательных веществ могут присутствовать, как описано в данной заявке ниже.
Приемлемые оттеночные агенты для тканей
Композиция может содержать оттеночный агент для тканей. Приемлемые оттеночные агенты для тканей включают красители, конъюгаты краситель-глина и пигменты. Приемлемые красители включают низкомолекулярные красители и полимерные красители. Приемлемые низкомолекулярные красители включают низкомолекулярные красители, выбранные из группы, состоящей из красителей, подпадающих под классификации Индекса цвета (СЛ.) прямой синий, прямой красный, прямой фиолетовый, кислотный синий, кислотный красный, кислотный фиолетовый, основной синий, основной фиолетовый и основной красный или их смесей.
В другом аспекте, приемлемые низкомолекулярные красители включают низкомолекулярные красители, выбранные из группы, состоящей из номеров Индекса цвета (Society of Dyers and Colourists, Bradford, UK) прямой фиолетовый 9, прямой фиолетовый 35, прямой фиолетовый 48, прямой фиолетовый 51, прямой фиолетовый 66, прямой фиолетовый 99, прямой синий 1, прямой синий 71, прямой синий 80, прямой синий 279, кислотный красный 17, кислотный красный 73, кислотный красный 88, кислотный красный 150, кислотный фиолетовый 15, кислотный фиолетовый 17, кислотный фиолетовый 24, кислотный фиолетовый 43, кислотный красный 52, кислотный фиолетовый 49, кислотный фиолетовый 50, кислотный синий 15, кислотный синий 17, кислотный синий 25, кислотный синий 29, кислотный синий 40, кислотный синий 45, кислотный синий 75, кислотный синий 80, кислотный синий 83, кислотный синий 90 и кислотный синий 113, кислотный черный 1, основной фиолетовый 1, основной фиолетовый 3, основной фиолетовый 4, основной фиолетовый 10, основной фиолетовый 35, основной синий 3, основной синий 16, основной синий 22, основной синий 47, основной синий 66, основной синий 75, основной синий 159 и их смесей. В другом аспекте, приемлемые низкомолекулярные красители включают низкомолекулярные красители, выбранные из группы, состоящей из номеров Индекса цвета (Society of Dyers and Colourists, Bradford, UK) кислотный фиолетовый 17, кислотный фиолетовый 43, кислотный красный 52, кислотный красный 73, кислотный красный 88, кислотный красный 150, кислотный синий 25, кислотный синий 29, кислотный синий 45, кислотный синий 113, кислотный черный 1, прямой синий 1, прямой синий 71, прямой фиолетовый 51 и их смесей. В другом аспекте, приемлемые низкомолекулярные красители включают низкомолекулярные красители, выбранные из группы, состоящей из номеров Индекса цвета (Society of Dyers and Colourists, Bradford, UK) кислотный фиолетовый 17, прямой синий 71, прямой фиолетовый 51, прямой синий 1, кислотный красный 88, кислотный красный 150, кислотный синий 29, кислотный синий 113 или их смесей.
Приемлемые полимерные красители включают полимерные красители, выбранные из группы, состоящей из полимеров, содержащих конъюгированные хромогены (конъюгаты краситель-полимер) и полимеры с хромогенами, сополимеризованными в каркас полимера и их смесей.
В другом аспекте, приемлемые полимерные красители включают полимерные красители, выбранные из группы, состоящей из ткань-субстантивных красителей, продаваемых под названием Liquitint® (Milliken, Spartanburg, South Carolina, USA), конъюгатов краситель-полимер, образованных из, по меньшей мере, одного реакционноспособного красителя и полимера, выбранного из группы, состоящей из полимеров, содержащих фрагмент, выбранный из группы, состоящей из гидроксильного фрагмента, фрагмента первичного амина, фрагмента вторичного амина, тиольного фрагмента и их смесей. В еще одном аспекте, приемлемые полимерные красители включают полимерные красители, выбранные из группы, состоящей из Liquitint® (Milliken, Spartanburg, South Carolina, USA) Violet CT, карбоксиметилцеллюлозы (CMC), конъюгированной с реакционноспособным синим, реакционноспособным фиолетовым или реакционноспособным красным красителем, например CMC, конъюгированной с СЛ. реакционноспособным синим 19, продаваемый Megazyme, Wicklow, Ireland под названием продукта AZO-CM-CELLULOSE, код продукта S-ACMC, алкоксилированных трифенил-метан полимерных красителей, алкоксилированных тиофен полимерных красителей и их смесей.
Предпочтительные оттеночные красители включают отбеливающие агенты, описанные в WO 08/87497 А1. Эти отбеливающие агенты могут быть охарактеризованы с помощью следующей структуры (I):

где R1 и R2 могут быть независимо выбраны из:
a) [(CH2CR'HO)x(CH2CR''HO)yH]
где R' выбирают из группы, состоящей из Н, СН3, CH2O(СН2СН2О)zH и их смесей; где R'' выбирают из группы, состоящей из Н, CH2O(CH2CH2O)zH и их смесей; где х+у≤5; где у≥1; и где z=0-5;
b) R1 представляет собой алкил, арил или арил алкил и R2 представляет собой [(CH2CR'HO)x(CH2CR''HO)yH]
где R' выбирают из группы, состоящей из Н, СН3, CH2O(CH2CH2O)zH и их смесей; где R'' выбирают из группы, состоящей из Н, CH2O(CH2CH2O)zH и их смесей; где х+у≤10; где у≥1; и где z=0-5;
c) R1 представляет собой [СН2СН2(OR3)CH2OR4] и R2 представляет собой [CH2CH2(OR3)CH2OR4]
где R3 выбирают из группы, состоящей из Н, (CH2CH2O)zH и их смесей; и где z=0-10;
где R4 выбирают из группы, состоящей из (С1-С16)алкильных, арильных групп и их смесей; и
d) где R1 и R2 могут быть независимо выбраны из амино аддитивного продукта стиролоксида, глицидилметилового эфира, изобутил глицидилового эфира, изопропилглицидилового эфира, трет-бутилглицидилового эфира, 2-этилгексил глицидилового эфира и глицидилгексадецилового эфира, с последующим добавлением от 1 до 10 алкиленоксидных звеньев.
Предпочтительный отбеливающий агент в соответствии с настоящим изобретением может быть охарактеризован следующей структурой (II):

где R' выбирают из группы, состоящей из Н, СН3, CH2O(СН2СН2О)zH и их смесей; где R'' выбирают из группы, состоящей из Н, CH2O(СН2СН2О)zH и их смесей; где х+у≤5; где у≥1; и где z=0-5.
Дополнительный предпочтительный отбеливающий агент в соответствии с настоящим изобретением может быть охарактеризован следующей структурой (III):

типично содержащей смесь, имеющую в общем 5 групп ЕО. Приемлемые предпочтительные молекулы имеют Структуру I, имеющую следующие подвешенные группы в «части а» выше:


Дополнительные отбеливающие агенты для использования включают описанные в USPN 2008 34511 A1 (Unilever). Предпочтительный агент представляет собой «Фиолетовый 13».
Приемлемые конъюгаты краситель-глина включают конъюгаты краситель-глина, выбранные из группы, содержащей, по меньшей мере, один катионный/основной краситель и смектитовую глину, и их смеси. В другом аспекте, приемлемые конъюгаты краситель-глина включают конъюгаты краситель-глина, выбранные из группы, состоящей из одного катионного/основного красителя, выбранного из группы, состоящей из С.I. основного желтого с 1 по 108, С.I. основного оранжевого с 1 по 69, С.I. основного красного с 1 по 118, С.I. основного фиолетового от 1 по 51, С.I. основного синего с 1 по 164, С.I. основного зеленого с 1 по 14, С.I. основного коричневого с 1 по 23, С.I. основного черного с 1 по 11, и глины, выбранной из группы, состоящей из монтморрилонитовой глины, гекторитовой глины, сапонитовой глины и их смесей. В еще одном аспекте, приемлемые конъюгаты краситель-глина включают конъюгаты краситель-глина, выбранные из группы, состоящей из: конъюгата монтморрилонит-основной синий В7 С.I. 42595, конъюгата монтморрилонит-основной синий В9 С.I. 52015, конъюгата монтморрилонит-основной фиолетовый V3 С.I. 42555, конъюгата монтморрилонит-основной зеленый G1 С.I. 42040, конъюгата монтморрилонит-основной красный R1 С.I. 45160, конъюгата монтморрилонит- С.I. основной черный 2, конъюгата гекторит-основной синий В7 С.I. 42595, конъюгата гекторит-основной синий В9 С.I. 52015, конъюгата гекторит-основной фиолетовый V3 С.I. 42555, конъюгата гекторит-основной зеленый G1 С.I. 42040, конъюгата гекторит-основной красный R1 С.I. 45160, конъюгата гекторит-C.I. основной черный 2, конъюгата сапонит-основной синий В7 С.I. 42595, конъюгата сапонит-основной синий В9 С.I. 52015, конъюгата сапонит-основной фиолетовый V3 С.I. 42555, конъюгата сапонит-основной зеленый G1 С.I. 42040, конъюгата сапонит-основной красный R1 С.I. 45160, конъюгата сапонит-C.I. основной черный 2 и их смесей.
Приемлемые пигменты включают пигменты, выбранные из группы, состоящей из флавантрона, индантрона, хлорированного индантрона, содержащего от 1 до 4 атомов хлора, пирантрона, дихлорпирантрона, монобромдихлорпирантрона, дибромдихлорпирантрона, тетрабромпирантрона, перилен-3,4,9,10-тетракарбоновой кислоты диимида, где имидные группы могут быть не замещены или замещены С1-С3-алкилом или фенилом или гетероциклическим радикалом, и где фенил и гетероциклические радикалы могут дополнительно иметь заместители, которые не придают растворимость в воде, амиды антрапиримидинкарбоновых кислот, виолантрон, изовиолантрон, диоксазиновые пигменты, фталоцианин меди, который может содержать до 2 атомов хлора на молекулу, полихлоро-фталоцианин меди или полибромхлоро-фталоцианин меди, содержащий до 14 атомов брома на молекулу и их смеси.
В другом аспекте, приемлемые пигменты включают пигменты, выбранные из группы, состоящей из Ультрамаринового синего (С.I. Пигмент синий 29), Ультрамаринового фиолетового (С.I. Пигмент фиолетовый 15) и их смесей.
Указанные оттеночные агенты для тканей могут быть использованы в сочетании (может быть использована любая смесь оттеночных агентов для тканей). Приемлемые оттеночные агенты описаны более подробно в US 7,208,459 В2. Предпочтительные уровни красителя в композициях в соответствии с настоящим изобретением составляют от 0,00001 до 0,5 мас. %, или от 0,0001 до 0,25 мас. %.
Концентрация предпочтительных красителей в воде для стадии обработки и/или очистки составляет от 1 части на миллиард до 5 м.д., предпочтительно от 10 частей на миллиард или 20 частей на миллиард до 5 м.д.. В предпочтительных композициях, концентрация поверхностно-активного вещества составляет от 0,2 до 3 г/л.
Инкапсуляты
Композиция может содержать инкапсулят. В одном аспекте, инкапсулят содержит сердцевину, оболочку, имеющую внутреннюю и внешнюю поверхность, указанная оболочка инкапсулирует указанную сердцевину.
В одном аспекте указанного инкапсулята, указанная сердцевина может содержать вещество, выбранное из группы, состоящей из отдушек; блескообразователей; красителей; репеллентов от насекомых; силиконов; восков; ароматизаторов; витаминов; агентов для смягчения тканей; средств по уходу за кожей в одном аспекте, парафинов; ферментов; антибактериальных средств; отбеливателей; ощущаемых веществ; и их смесей; и указанная оболочка может содержать вещество, выбранное из группы, состоящей из полиэтиленов; полиамидов; поливиниловых спиртов, необязательно содержащих другие сомономеры; полистиролов; полиизопренов; поликарбонатов; сложных полиэфиров; полиакрилатов; аминопластов, в одном аспекте указанный аминопласт может содержать полимочевины, полиуретан и/или полимочевинауретан, в одном аспекте указанная полимочевина может содержать полиоксиметиленмочевину и/или меламинформальдегид; полиолефинов; полисахаридов, в одном аспекте указанный полисахарид может содержать альгинат и/или хитозан; желатина; шеллака; эпоксидных смол; виниловых полимеров; нерастворимых в воде неорганических веществ; силикона и их смесей.
В одном аспекте указанного инкапсулята, указанная сердцевина может содержать отдушку.
В одном аспекте указанного инкапсулята, указанная оболочка может содержать меламин формальдегид и/или перекрестно сшитый меламинформальдегид.
В одном аспекте раскрыты приемлемые инкапсуляты, которые могут содержать вещество сердцевины и оболочку, при этом указанная оболочка, по меньшей мере, частично окружает указанное вещество сердцевины. По меньшей мере, 75%, 85% или даже 90% указанных инкапсулятов могут иметь прочность на разрушение от приблизительно 0,2 МПа до приблизительно 10 МПа, от приблизительно 0,4 МПа до приблизительно 5 МПа, от приблизительно 0,6 МПа до приблизительно 3,5 МПа, или даже от приблизительно 0,7 МПа до приблизительно 3 МПа; и просачивание полезного агента от 0% до приблизительно 30%, от 0% до приблизительно 20%, или даже от 0% до приблизительно 5%.
В одном аспекте, по меньшей мере, 75%, 85% или даже 90% указанных инкапсулятов могут иметь размер частиц от приблизительно 1 микрона до приблизительно 80 микрон, от приблизительно 5 микрон до 60 микрон, от приблизительно 10 микрон до приблизительно 50 микрон, или даже от приблизительно 15 микрон до приблизительно 40 микрон.
В одном аспекте, по меньшей мере, 75%, 85% или даже 90% указанных инкапсулятов могут иметь толщину стенки частиц от приблизительно 30 нм до приблизительно 250 нм, от приблизительно 80 нм до приблизительно 180 нм, или даже от приблизительно 100 нм до приблизительно 160 нм.
В одном аспекте, указанное вещество сердцевины инкапсулятов может содержать вещество, выбранное из группы, состоящей из сырья отдушки и/или необязательного вещества, выбранного из группы, состоящей из растительного масла, в том числе неразбавленных и/или смешанных растительных масел, включая касторовое масло, кокосовое масло, хлопковое масло, виноградное масло, рапсовое масло, соевое масло, кукурузное масло, пальмовое масло, льняное масло, сафлоровое масло, оливковое масло, арахисовое масло, кокосовое масло, пальмоядровое масло, касторовое масло, лимонное масло и их смеси; сложных эфиров растительных масел, сложных эфиров, включая дибутиладипат, дибутилфталат, бутилбензил адипат, бензил октил адипат, трикрезилфосфат, триоктилфосфат и их смеси; углеводородов с неразветвленной или разветвленной цепью, в том числе углеводородов с неразветвленной или разветвленной цепью, имеющих температуру кипения более, чем приблизительно 80°С; частично гидрогенизированных терфенилов, диалкилфталатов, алкилбифенилов, в том числе моноизопропилбифенила, алкилированного нафталина, в том числе дипропилнафталина, уайт-спирита, в том числе керосина, минерального масла и их смесей; ароматических растворителей, в том числе бензола, толуола и их смесей; силиконовых масел; и их смесей.
В одном аспекте, указанное вещество стенки инкапсулятов может содержать приемлемую смолу, включая продукт реакции альдегида и амина, приемлемые альдегиды включают формальдегид. Приемлемые амины включают меламин, мочевину, бензогуанамин, гликолурил и их смеси. Приемлемые меламины включают метилол меламин, метилированный метилолмеламин, иминомеламин и их смеси. Приемлемые мочевины включают диметилолмочевину, метилированную диметилолмочевину, мочевину-резорцинол и их смеси.
В одном аспекте, приемлемые уловители формальдегида могут применяться с инкапсулятами, например, в капсульной суспензии и/или добавляться в потребительский продукт перед, во время или после того, как инкапсуляты добавляют в такой потребительский продукт.
Приемлемые капсулы могут быть получены, следуя методикам USPA 2008/0305982 A1; и/или USPA 2009/0247449 A1. Альтернативно, приемлемые капсулы можно приобрести от Appleton Papers Inc. of Appleton, Wisconsin USA.
В предпочтительном аспекте композиция может также содержать средство, способствующее осаждению, предпочтительно, состоящее из группы, содержащей катионные или неионные полимеры. Приемлемые полимеры включают катионные крахмалы, катионную гидроксиэтилцеллюлозу, поливинилформальдегид, камедь рожкового дерева, маннаны, ксилоглюканы, тамариндовую камедь, полиэтилентерефталат и полимеры, содержащие диметиламиноэтилметакрилат, необязательно с одним или мономерами, выбранными из группы, содержащей акриловую кислоту и акриламид.
Отдушки - В одном аспекте композиция содержит отдушку, содержащую одно или более вещество сырья отдушки, выбранное из группы, состоящей из 1,1'-оксибис-2-пропанола; 1,4-циклогександикарбоновой кислоты, диэтилового сложного эфира; (этоксиметокси)циклодо декана; 1,3-нонандиола, моноацетата; (3-метилбутокси)уксусной кислоты, 2-пропенилового сложного эфира; бета-метил циклододеканэтанола; 2-метил-3-[(1,7,7-триметилбицикло[2.2.1]гепт-2-ил)окси]-1-пропанола; оксациклогексадекан-2-она; альфа-метил-бензолметанол ацетата; транс-3-этокси-1,1,5-триметилциклогексана; 4-(1,1-диметилэтил)циклогексанол ацетата; додекагидро-3а,6,6,9а-тетраметилнафто[2,1-b]фурана; бета-метил бензол пропаналя; бета-метил-3-(1-метилэтил)бензолпропаналя; 4-фенил-2-бутанона; 2-метилбутаноевой кислоты, этилового сложного эфира; бензальдегида; 2-метилбутаноевой кислоты, 1-метилэтилового сложного эфира; дигидро-5-пентил-2(3Н)фуранона; (2Е)-1-(2,6,6-триметил-2-циклогексен-1-ил)-2-бутен-1-она; додеканаля; ундеканаля; 2-этил-альфа, альфа-диметилбензолпропаналя; деканаля; альфа, альфа-диметилбензолэтанол ацетата; 2-(фенилметилен)октаналя; 2-[[3-[4-(1,1-диметилэтил)фенил]-2-метилпропилиден]амино]бензойной кислоты, метилового сложного эфира; 1-(2,6,6-триметил-3-циклогексен-1-ил)-2-бутен-1-она; 2-пентилциклопентанона; 3-оксо-2-пентил циклопентануксусной кислоты, метилового сложного эфира; 4-гидрокси-3-метоксибензальдегида; 3-этокси-4-гидроксибензальдегида; 2-гептилциклопентанона; 1-(4-метилфенил)этанона; (3Е)-4-(2,6,6-триметил-1-циклогексен-1-ил)-3-бутен-2-она; (3Е)-4-(2,6,6-триметил-2-циклогексен-1-ил)-3-бутен-2-она; бензолэтанола; 2Н-1-бензопиран-2-она; 4-метоксибензальдегида; 10-ундеценаля; пропаноевой кислоты, фенилметилового сложного эфира; бета-метилбензолпентанола; 1,1-диэтокси-3,7-диметил-2,6-октадиена; альфа, альфа-диметилбензолэтанола; (2Е)-1-(2,6,6-триметил-1-циклогексен-1-ил)-2-бутен-1-она; уксусной кислоты, фенилметилового сложного эфира; циклогексанпропаноевой кислоты, 2-пропенилового сложного эфира; гексаноевой кислоты, 2-пропенилового сложного эфира; 1,2-диметокси-4-(2-пропенил)бензола; 1,5-диметил-бицикло[3.2.1]октан-8-он оксима; 4-(4-гидрокси-4-метилпентил)-3-циклогексен-1-карбоксальдегида; 3-бутен-2-ола; 2-[[[2,4(или 3,5)-диметил-3-циклогексен-1-ил]метилен] амино]бензойной кислоты, метилового сложного эфира; 8-циклогексадецен-1-она; метил ионона; 2,6-диметил-7-октен-2-ола; 2-метокси-4-(2-пропенил)фенола; (2Е)-3,7-диметил-2,6-октадиен-1-ола; 2-гидрокси-бензойной кислоты, (3Z)-3-гексенилового сложного эфира; 2-тридеценнитрила; 4-(2,2-диметил-6-метиленциклогексил)-3-метил-3-бутен-2-она; тетрагидро-4-метил-2-(2-метил-1-пропенил)-2Н-пирана; уксусной кислоты, (2-метилбутокси)-, 2-пропенилового сложного эфира; бензойной кислоты, 2-гидрокси-, 3-метилбутилового сложного эфира; 2-бутен-1-она, 1-(2,6,6-триметил-1-циклогексен-1-ила)-, (Z)-; циклопентанкарбоновой кислоты, 2-гексил-3-оксо-, метилового сложного эфира; бензолпропаналя, 4-этил-альфа.,альфа.-диметил-; 3-циклогексен-1-карбоксальдегида, 3-(4-гидрокси-4-метилпентил)-; этанона, 1-(2,3,4,7,8,8а-гексагидро-3,6,8,8-тетраметил-1Н-3а,7-метаноазулен-5-ил)-, [3R-(3.альфа.,3а.бета.,7.бета.,8а.альфа.)]-; ундеканаля, 2-метил-2Н-пиран-2-она, 6-бутилтетрагидро-; бензолпропаналя, 4-(1,1-диметилэтил)-.альфа.-метил-; 2(3Н)-фуранона, 5-гептилдигидро-; бензойной кислоты, 2-[(7-гидрокси-3,7-диметилоктилиден)амино]-, метила; бензойной кислоты, 2-гидрокси-, фенилметилового сложного эфира; нафталина, 2-метокси-; 2-циклопентен-1-она, 2-гексил-; 2(3Н)-фуранона, 5-гексилдигидро-; оксиранкарбоновой кислоты, 3-метил-3-фенил-, этилового сложного эфира; 2-оксабицикло[2.2.2]октана, 1,3,3-триметил-; бензолпентанола,.гамма.-метил-; 3-октанола, 3,7-диметил-; 3,7-диметил-2,6-октадиеннитрила; 3,7-диметил-6-октен-1-ола; терпинеол ацетата; 2-метил-6-метилен-7-октен-2-ола, дигидро производного; 3а,4,5,6,7,7а-гексагидро-4,7-метано-1Н-инден-6-ол пропаноата; 3-метил-2-бутен-1-ол ацетата; (7)-3-гексен-1-ол ацетата; 2-этил-4-(2,2,3-триметил-3-циклопентен-1-ил)-2-бутен-1-ола; 4-(октагидро-4,7-метано-5Н-инден-5-илиден)-бутаналя; 3-2,4-диметил-циклогексен-1-карбоксальдегида; 1-(1,2,3,4,5,6,7,8-октагидро-2,3,8,8-тетраметил-2-нафталенил)-этанона; 2-гидрокси-бензойной кислоты, метилового сложного эфира; 2-гидрокси-бензойной кислоты, гексилового сложного эфира; 2-фенокси-этанола; 2-гидрокси-бензойной кислоты, пентилового сложного эфира; 2,3-гептандиона; 2-гексен-1-ола; 6-октен-2-ола, 2,6-диметил-; дамаскона (альфа, бета, гамма или дельта или их смесей), 4,7-метано-1Н-инден-6-ола, 3а,4,5,6,7,7а-гексагидро-, ацетата; 9-ундеканаля; 8-ундеканаля; изоциклоцитраля; этанона, 1-(1,2,3,5,6,7,8,8а-октагидро-2,3,8,8-тетраметил-2-нафталенил)-; 3-циклогексен-1-карбоксальдегида, 3,5-диметил-; 3-циклогексен-1-карбоксальдегида, 2,4-диметил-; 1,6-октадиен-3-ола, 3,7-диметил-; 1,6-октадиен-3-ола, 3,7-диметил-, ацетата; лилиаля (п-трет-буциналя) и циклопентанона, 2-[2-(4-метил-3-циклогексен-1-ил)пропил]- и 1-метил-4-(1-метилэтенил)циклогексена и их смесей.
В одном аспекте композиция может содержать частицы инкапсулированной отдушки, содержащие либо водорастворимое гидроксильное соединение, либо меламин-формальдегид или модифицированный поливиниловый спирт. В одном аспекте инкапсулят содержит (а), по меньшей мере, частично водорастворимый твердый матрикс, содержащий одно или более водорастворимых гидроксильных соединений, предпочтительно крахмал; и (b) масло отдушки, инкапсулированное твердым матриксом.
В дополнительном аспекте отдушка может быть предварительно сформирована в комплекс с полиамином, предпочтительно полиэтиленимином, например с образованием основания Шиффа.
Полимеры
Потребительский продукт может содержать один или более полимеров. Примеры представляют собой карбоксиметилцеллюлозу, поли(винил-пирролидон), поли(этиленгликоль), поли(виниловый спирт), поли(винилпиридин-N-оксид), поли(винилимидазол), поликарбоксилаты, такие как полиакрилаты, сополимеры малеиновой/акриловой кислоты и сополимеры лаурилметакрилата/акриловой кислоты.
Потребительский продукт может содержать один или более амфифильных чистящих полимеров, таких как соединение, имеющее следующую общую структуру: бис((C2H5O)(C2H4O)n)(CH3)-N+-CxH2x-N+-(CH3)-бис((C2H5O)(C2H4O)n), где n = от 20 до 30, и x = от 3 до 8, или их сульфатированные или сульфонированные варианты.
Потребительский продукт может содержать амфифильные алкоксилированные очищающие жир полимеры, которые имеют сбалансированные гидрофильные и гидрофобные свойства, такие, что они удаляют частицы жира из тканей и поверхностей. Конкретные воплощения амфифильных алкоксилированных очищающих жир полимеров в соответствии с настоящим изобретением включают структуру основы и множество алкоксилатных групп, присоединенных к этой структуре основы. Они могут включать алкоксилированные полиалкиленимины, предпочтительно имеющие внутренний блок полиэтиленоксида и внешний блок полипропиленоксида.
Алкоксилированные поликарбоксилаты, такие как полученные из полиакрилатов, являются полезными в данной заявке, чтобы обеспечить дополнительную производительность удаления жира. Такие вещества описаны в WO 91/08281 и РСТ 90/01815. Химически, эти вещества включают полиакрилаты, имеющие одну этокси боковую цепь на каждые 7-8 акрилатных звеньев. Боковые цепи имеют формулу -(CH2CH2O)m(СН2)nCH3 где m составляет 2-3 и n составляет 6-12. Боковые цепи связаны сложным эфиром с полиакрилатным «каркасом», чтобы обеспечить «гребень» структуры полимерного типа. Молекулярная масса может варьироваться, но обычно находится в диапазоне от приблизительно 2000 до приблизительно 50000. Такие алкоксилированные поликарбоксилаты могут содержать от приблизительно 0,05% до приблизительно 10%, по массе композиций в данной заявке.
Поверхностно-активные вещества, полученные из изопреноидов в соответствии с настоящим изобретением и их смеси с другими со-поверхностно-активными веществами и другими вспомогательными ингредиентами, особенно приемлемы для использования с амфифильным привитым сополимером, предпочтительно амфифильный привитой сополимер содержит (i) полиэтиленгликольный каркас; и (ii) и, по меньшей мере, один подвешенный фрагмент, выбранный из поливинилацетата, поливинилового спирта и их смесей. Предпочтительным амфифильным привитым сополимером является Sokalan НР22, поставляемый BASF. Приемлемые полимеры включают случайные привитые сополимеры, предпочтительно поливинилацетат привитой сополимер полиэтиленоксида, имеющий полиэтиленоксидный каркас и множество поливинилацетатных боковых цепей. Молекулярная масса полиэтиленоксидного каркаса предпочтительно составляет приблизительно 6000 и массовое соотношение полиэтиленоксида и поливинилацетата составляет приблизительно от 40 до 60 и не более чем 1 точка прививки на 50 звеньев этиленоксида.
Карбоксилатный полимер - Потребительские продукты в соответствии с настоящим изобретением могут также содержать один или более карбоксилатных полимеров, таких как малеатный/акрилатный произвольный сополимер или полиакрилатный гомополимер. В одном аспекте, карбоксилатный полимер представляет собой полиакрилатный гомополимер, имеющий молекулярную массу от 4000 Да до 9000 Да, или от 6000 Да до 9000 Да.
Высвобождающий загрязнения полимер - Потребительские продукты в соответствии с настоящим изобретением могут также содержать один или более высвобождающих загрязнения полимеров, имеющих структуру, как определено в одной из следующих структур (I), (II) или (III):

где:
a, b и с означают от 1 до 200;
d, е и f означают от 1 до 50;
Ar представляет собой 1,4-замещенный фенилен;
sAr представляет собой 1,3-замещенный фенилен, замещенный в положении 5 SO3Me;
Me представляет собой Li, К, Mg/2, Са/2, Al/3, аммоний, моно-, ди-, три- или тетраалкиламмоний, где алкильные группы представляют собой C1-C18 алкил или С2-С10 гидроксиалкил, или их смеси;
R1, R2, R3, R4, R5 и R6 независимо выбирают из Н или C1-C18 н- или изо-алкила; и
R7 является линейным или разветвленным C1-C18 алкилом, или линейным или разветвленным С2-С30 алкенилом, или циклоалкильной группой с от 5 до 9 атомами углерода, или С8-С30 арильной группой, или С6-С30 арилалкильной группой.
Приемлемые высвобождающие загрязнения полимеры представляют собой сложно полиэфирные высвобождающие загрязнения полимеры, такие как Repel-o-tex полимеры, включая Repel-o-tex, SF-2 и SRP6, которые поставляются Rhodia. Другие приемлемые высвобождающие загрязнения полимеры включают Техсаге полимеры, включая Техсаге SRA100, SRA300, SRN100, SRN170, SRN240, SRN300 и SRN325, поставляемые от Clariant. Другие приемлемые высвобождающие загрязнения полимеры представляют собой Marloquest полимеры, например Marloquest SL, поставляемый от Sasol.
Целлюлозный полимер - Потребительские продукты в соответствии с настоящим изобретением могут также включать один или более целлюлозных полимеров, в том числе тех, которые выбраны из алкил целлюлозы, алкил алкоксиалкил целлюлозы, карбоксиалкилцеллюлозы, алкил карбоксиалкилцеллюлозы. В одном аспекте, целлюлозные полимеры выбраны из группы, содержащей карбоксиметилцеллюлозу, метилцеллюлозу, метил гидроксиэтилцеллюлозу, метил карбоксиметилцеллюлозу и их смеси. В одном аспекте, карбоксиметилцеллюлоза имеет степень карбоксиметильного замещения от 0,5 до 0,9 и молекулярную массу от 100000 Да до 300000 Да.
Ферменты
Потребительские продукты могут содержать один или более ферментов, которые обеспечивают производительность очистки и/или полезные эффекты ухода за тканями. Примеры приемлемых ферментов включают, но не ограничиваясь приведенным, гемицеллюлазы, пероксидазы, протеазы, целлюлазы, ксиланазы, липазы, фосфолипазы, эстеразы, кутиназы, пектиназы, маннаназы, пектат лиазы, кератиназы, редуктазы, оксидазы, фенолоксидазы, липоксигеназы, лигниназы, пуллуланазы, танназы, пентозаназы, маланазы, β-глюканазы, арабинозидазы, гиалуронидазу, хондроитиназу, лакказу и амилазы, или их смеси. Типичное сочетание представляет собой ферментный коктейль, который может содержать, например, протеазу и липазу в сочетании с амилазой. В случае присутствия в потребительском продукте, вышеупомянутые дополнительные ферменты могут присутствовать на уровнях от приблизительно 0,00001% до приблизительно 2%, от приблизительно 0,0001%) до приблизительно 1% или даже от приблизительно 0,001% до приблизительно 0,5% фермента белка по массе потребительского продукта.
В одном аспекте предпочтительные ферменты будут включать протеазу. Приемлемые протеазы включают металлопротеазы и серинпротеазы, включая нейтральные или щелочные микробные серинпротеазы, такие как субтилизины (ЕС 3.4.21.62). Приемлемые протеазы включают протеазы животного, растительного или микробного происхождения. В одном аспекте, такая приемлемая протеаза может быть микробного происхождения. Приемлемые протеазы включают химически или генетически модифицированные мутанты указанных выше приемлемых протеаз. В одном аспекте, приемлемая протеаза может быть серинпротеазой, такой как щелочная микробная протеаза и/или протеазой трипсинового типа. Примеры приемлемых нейтральных или щелочных протеаз включают:
(a) субтилизины (ЕС 3.4.21.62), включая те, которые получены из Bacillus, таких как Bacillus lentus, В. alkalophilus, В. subtilis, В. amyloliquefaciens, Bacillus pumilus и Bacillus gibsonii, описанные в US 6,312,936 Bl, US 5,679,630, US 4,760,025, US 7,262,042 и WO 09/021867.
(b) протеазы трипсинового типа или химотрипсинового типа, такие как трипсин (например, свиного или коровьего происхождения), включая Fusarium протеазу, описанную в WO 89/06270, и химотрипсиновые протеазы, полученные из Cellumonas, описанные в WO 05/052161 и WO 05/052146.
(c) металлопротеазы, включая те, которые получены из Bacillus amyloliquefaciens, описанные в WO 07/044993А2.
Предпочтительные протеазы включают те, которые получены из Bacillus gibsonii или Bacillus Lentus.
Приемлемые коммерчески доступные протеазные ферменты включают те, которые продаются под торговыми названиями Alcalase®, Savinase®, Primase®, Durazym®, Polarzyme®, Kannase®, Liquanase®, Liquanase Ultra®, Savinase Ultra®, Ovozyme®, Neutrase®, Everlase® и Esperase® от Novozymes A/S (Denmark), которые продаются под торговыми названиями Maxatase®, Maxacal®, Maxapem®, Properase®, Purafect®, Purafect Prime®, Purafect Ox®, FN3®, FN4®, Excellase® и Purafect ОХР® от Genencor International., которые продаются под торговыми названиями Opticlean® и Optimase® от Solvay Enzymes, которые доступны от Henkel/ Kemira, а именно BLAP (последовательность показана на фигуре 29 US 5,352,604 со следующими мутациями S99D + S101R + S103A + V104I + G159S, в данной заявке имеет название В LAP), BLAP R (BLAP с S3T + V4I + V199M + V205I + L217D), BLAP X (BLAP с S3T + V4I + V205I) и BLAP F49 (BLAP с S3T + V4I + A194P + V199M + V205I + L217D) - все от Henkel/Kemira; и КАР (Bacillus alkalophilus subtilisin с мутациями A230V + S256G + S259N) от Kao.
Приемлемые альфа-амилазы включают альфа-амилазы бактериального или грибкового происхождения. Химически или генетически модифицированные мутанты (варианты) включены. Предпочтительная щелочная альфа-амилаза получена из штамма Bacillus, например Bacillus licheniformis, Bacillus amyloliquefaciens, Bacillus stearothermophilus, Bacillus subtilis или других видов Bacillus, таких как Bacillus sp.NCIB 12289, NCIB 12512, NCIB 12513, DSM 9375 (USP 7,153,818) DSM 12368, DSMZ no. 12649, KSM AP1378 (WO 97/00324), KSM K36 или KSM K38 (EP 1,022,334). Предпочтительные амилазы включают:
(a) варианты, описанные в WO 94/02597, WO 94/18314, WO 96/23874 и WO 97/43424, в особенности варианты с заменами в одном или более из следующих положений относительно фермента, перечисленные как SEQ ID No. 2 в WO 96/23874: 15, 23, 105, 106, 124, 128, 133, 154, 156, 181, 188, 190, 197, 202, 208, 209, 243, 264, 304, 305, 391, 408 и 444;
(b) варианты, описанные в USP 5,856,164 и WO 99/23211, WO 96/23873, WO 00/60060 и WO 06/002643, в особенности варианты с одним или более заменами в следующих положениях относительно АА560 фермента, перечисленные как SEQ ID No. 12 в WO 06/002643: 26, 30, 33, 82, 37, 106, 118, 128, 133, 149, 150, 160, 178, 182, 186, 193, 203, 214, 231, 256, 257, 258, 269, 270, 272, 283, 295, 296, 298, 299, 303, 304, 305, 311, 314, 315, 318, 319, 339, 345, 361, 378, 383, 419, 421, 437, 441, 444, 445, 446, 447, 450, 461, 471, 482, 484, предпочтительно содержащие также делеции D183* и G184*.
(c) варианты, проявляющие, по меньшей мере, 90% идентичность с SEQ ID No. 4 в WO 06/002643, фермент дикого типа из Bacillus SP722, в особенности варианты с делециями в 183 и 184 положениях и варианты, описанные в WO 00/60060, которая включена в данную заявку путем ссылки.
(d) варианты, проявляющие, по меньшей мере, 95% идентичность с ферментом дикого типа из Bacillus sp.707 (SEQ ID NO: 7 в US 6,093,562), в особенности содержащие одну или более из следующих мутаций М202, М208, S255, R172 и/или М261. Предпочтительно указанная амилаза содержит одну или более из M202L, M202V, M202S, М202Т, M202I, M202Q, M202W, S255N и/или R172Q. Особо предпочтительными являются содержащие M202L или М202Т мутации.
(e) варианты, описанные в WO 09/149130, предпочтительно проявляющие, по меньшей мере, 90% идентичность с SEQ ID NO: 1или SEQ ID NO:2 в WO 09/149130, фермент дикого типа из Geobacillus Stearophermophilus или его усеченную версию.
Приемлемые коммерчески доступные альфа-амилазы включают DURAMYL®, LIQUEZYME®, TERMAMYL®, TERMAMYL ULTRA®, NATALASE®, SUPRAMYL®, STAINZYME®, STAINZYME PLUS®, FUNGAMYL® и BAN® (Novozymes A/S, Bagsvaerd, Denmark), KEMZYM® AT 9000 Biozym Biotech Trading GmbH Wehlistrasse 27b A-1200 Wien Austria, RAPID ASE®, PURASTAR®, ENZYSIZE®, OPTISIZE HT PLUS®, POWERASE® и PURASTAR OXAM® (Genencor International Inc., Palo Alto, California) и KAM® (Kao, 14-10 Nihonbashi Kayabacho, 1-chôme, Chuo-ku Tokyo 103-8210, Japan). В одном аспекте, приемлемые амилазы включают NATALASE®, STAINZYME® и STAINZYME PLUS® и их смеси.
В одном аспекте, такие ферменты могут быть выбранными из группы, состоящей из: липаз, включая «липазы первого цикла», например, описанные в патенте США 6,939,702 В1 и US РА 2009/0217464. В одном аспекте, липаза является липазой первого цикла стирки, предпочтительно вариантом липазы дикого типа из Thermomyces lanuginosus, содержащей одну или более из T231R и N233R мутаций. Последовательность дикого типа содержит 269 аминокислот (аминокислоты 23 - 291) Swissprot номер доступа Swiss-Prot 059952 (получена из Thermomyces lanuginosus (Humicola lanuginosa)). Предпочтительные липазы будут включать те, которые продаются под торговыми названиями Lipex® и Lipolex®.
В одном аспекте, другие предпочтительные ферменты включают эндоглюканазы, полученные из микробов, проявляющие эндо-бета-1,4-глюканазную активность (Е.С.3.2.1.4), включая бактериальный полипептид, эндогенный к члену рода Bacillus, имеющий последовательность, по меньшей мере, 90%, 94%, 97% и даже 99% идентичности с аминокислотной последовательностью SEQ ID NO:2 в 7,141,403 В2) и их смеси. Приемлемые эндоглюканазы продаются под торговыми названиями Celluclean® и Whitezyme® (Novozymes A/S, Bagsvaerd, Denmark).
Другие предпочтительные ферменты включают пектатлиазы, которые продаются под торговыми названиями Pectawash®, Pectaway®, Xpect® и маннаназы, которые продаются под торговыми названиями Mannaway® (все от Novozymes A/S, Bagsvaerd, Denmark) и Purabrite® (Genencor International Inc., Palo Alto, California).
Поверхностно-активные вещества - Композиции в соответствии с настоящим изобретением могут содержать поверхностно-активное вещество или систему поверхностно-активных веществ, где поверхностно-активное вещество может быть выбрано из неионных поверхностно-активных веществ, анионных поверхностно-активных веществ, катионных поверхностно-активных веществ, амфолитных поверхностно-активных веществ, цвиттерионных поверхностно-активных веществ, полуполярных неионных поверхностно-активных веществ и их смесей. Если присутствует, поверхностно-активное вещество типично присутствует на уровне от приблизительно 0,1% до приблизительно 60%, от приблизительно 1% до приблизительно 50% или даже от приблизительно 5% до приблизительно 40% по массе рассматриваемого потребительского продукта.
Приемлемые анионные моющие поверхностно-активные вещества включают сульфатные и сульфонатные моющие поверхностно-активные вещества.
Приемлемые сульфонатные моющие поверхностно-активные вещества включают алкилбензолсульфонат, в одном аспекте, С10-13алкилбензолсульфонат. Приемлемый алкилбензолсульфонат (LAS) можут быть получен путем сульфонирования коммерчески доступного линейного алкилбензола (LAB); приемлемый LAB включает низкие 2-фенил LAB, такие, которые поставляются Sasol под торговым названием Isochem®, или которые поставляются Petresa под торговым названием Petrelab®, другие приемлемые LAB включают высокие 2-фенил LAB, такие, которые поставляются Sasol под торговым названием Hyblene®. Приемлемое анионное моющее поверхностно-активное вещество представляет собой алкил бензол сульфонат, который получают путем DETAL катализируемого процесса, хотя другие маршруты синтеза, такие как HF, могут также быть приемлемыми. В одном аспекте используют соль магния LAS.
Приемлемые сульфатные моющие поверхностно-активные вещества включают алкилсульфат, в одном аспекте, C8-18 алкилсульфат, или главным образом С12 алкилсульфат.
Другим приемлемым сульфатным моющим поверхностно-активным веществом является алкилалкоксилированный сульфат, в одном аспекте, алкилэтоксилированный сульфат, в одном аспекте, C8-18 алкилалкоксилированный сульфат, в другом аспекте, C8-18 алкилэтоксилированный сульфат, типично алкилалкоксилированный сульфат имеет среднюю степень алкоксилирования от 0,5 до 20, или от 0,5 до 10, типично алкилалкоксилированный сульфат представляет собой C8-18 алкилэтоксилированный сульфат, имеющий среднюю степень этоксилирования от 0,5 до 10, от 0,5 до 7, от 0,5 до 5 или даже от 0,5 до 3.
Алкилсульфат, алкилалкоксилированный сульфат и алкилбензолсульфонаты могут быть линейными или разветвленными, замещенными или незамещенными.
Моющее поверхностно-активное вещество может быть разветвленным в середине цепи моющим поверхностно-активным веществом, в одном аспекте, разветвленным в середине цепи анионным моющим поверхностно-активным веществом, в одном аспекте, разветвленным в середине цепи алкилсульфатом и/или разветвленным в середине цепи алкилбензолсульфонатом, например, разветвленным в середине цепи алкилсульфатом. В одном аспекте, разветвлениями в середине цепи являются С1-4 алкильные группы, типично метальные и/или этильные группы.
Приемлемые неионные моющие поверхностно-активные вещества выбраны из группы, состоящей из: C8-C18 алкилэтоксилатов, например NEODOL® неионных поверхностно-активных веществ от Shell; С6-С12 алкилфенолалкоксилатов, где алкоксилатные звенья могут быть этиленоксизвеньями, пропиленоксизвеньями или их смесью; С12-С18 спирта и С6-С12 алкилфенол конденсатов с этиленоксид/пропиленоксид блок полимерами, например Pluronic® от BASF; С14-С22 разветвленных в середине цепи спиртов; С14-С22 разветвленных в середине цепи алкилалкоксилатов, типично имеющих среднюю степень алкоксилирования от 1 до 30; алкилполисахаридов, в одном аспекте, алкилполигликозидов; полигидрокси амидов жирных кислот; эфира с поли(оксиалкилированными) спиртовыми поверхностно-активными веществами на конце; и их смесей.
Приемлемые неионные моющие поверхностно-активные вещества включают алкил полиглюкозид и/или алкил алкоксилированный спирт.
В одном аспекте, неионные моющие поверхностно-активные вещества включают алкилалкоксилированные спирты, в одном аспекте C8-18 алкилалкоксилированный спирт, например C8-18 алкилэтоксилированный спирт, алкилалкоксилированный спирт может иметь среднюю степень алкоксилирования от 1 до 50, от 1 до 30, от 1 до 20, или от 1 до 10. В одном аспекте, алкил алкоксилированный спирт может быть C8-18 алкилэтоксилированным спиртом, имеющим среднюю степень этоксилирования от 1 до 10, от 1 до 7, от более 1 до 5 или от 3 до 7. Алкилалкоксилированный спирт может быть линейным или разветвленным, и замещенным или незамещенным.
Приемлемые неионные поверхностно-активные вещества включают те, которые продаются под торговым названием Lutensol® от BASF.
Приемлемые катионные моющие поверхностно-активные вещества включают соединения алкилпиридиния, соединения алкил четвертичного аммония, соединения алкил четвертичного фосфония, соединения алкил третичного сульфония и их смеси.
Приемлемые катионные моющие поверхностно-активные вещества представляют собой соединения четвертичного аммония, имеющие общую формулу:
(R)(R1)(R2)(R3)N+X-,
где R является линейным или разветвленным, замещенным или незамещенным С6-18 алкильным или алкенильным фрагментом, R1 и R2 независимо выбирают из метальных или этильных фрагментов, R3 представляет собой гидроксильный, гидроксиметильный или гидроксиэтильный фрагмент, X представляет собой анион, обеспечивающий нейтральность заряда, приемлемые анионы включают: галогениды, например хлорид; сульфат и сульфонат. Приемлемые катионные моющие поверхностно-активные вещества представляют собой хлориды моно-С6-18 алкил моно-гидроксиэтил ди-метил четвертичного аммония. Высоко приемлемые катионные моющие поверхностно-активные вещества представляют собой хлорид моно-С8-10алкил моно-гидроксиэтил ди-метил четвертичного аммония, хлорид моно-С10-12 алкил моно-гидроксиэтил ди-метил четвертичного аммония и хлорид моно-С10 алкил моно-гидроксиэтил ди-метил четвертичного аммония.
Приемлемые амфотерные/цвиттерионные поверхностно-активные вещества включают аминоксиды и бетаины. Амин-нейтрализованные анионные поверхностно-активные вещества - Анионные поверхностно-активные вещества в соответствии с настоящим изобретением и вспомогательные анионные со-поверхностно-активные вещества, могут существовать в кислотной форме и указанная кислотная форма может быть нейтрализована с образованием соли поверхностно-активного вещества, которая желательна для использования в композициях моющих средств в соответствии с настоящим изобретением. Типичные агенты для нейтрализации включают основания металлического противоиона, такие как гидроксиды, например, NaOH или КОН. Дополнительные предпочтительные агенты для нейтрализации анионных поверхностно-активных веществ в соответствии с настоящим изобретением и вспомогательных анионных поверхностно-активные веществ или со-поверхностно-активных веществ в их кислотных формах включают аммоний, амины и алканоламины. Алканоламины являются предпочтительными. Приемлемые не ограничивающие примеры включают моноэтаноламин, диэтаноламин, триэтаноламин, и другие линейные или разветвленные алканоламины, известные в данной области техники; например, высоко предпочтительные алканоламины включают 2-амино-1-пропанол, 1-аминопропанол, моноизопропаноламин или 1-амино-3-пропанол. Аминная нейтрализация может быть выполнена полностью или частично, например часть смеси анионных поверхностно-активных веществ может быть нейтрализована натрием или калием и часть смеси анионных поверхностно-активных веществ может быть нейтрализована аминами или алканоламинами.
Системы поверхностно-активных веществ, содержащие смеси одного или более анионных и в дополнение одного или более неионных поверхностно-активных веществ необязательно с дополнительным поверхностно-активным веществом, таким как катионное поверхностно-активное вещество, могут быть предпочтительными. Предпочтительные массовые соотношения анионного и неионного поверхностно-активного вещества составляют, по меньшей мере, 2:1, или даже, по меньшей мере, от 1:1 до 1:10.
Модифицирующие добавки - Композиции в соответствии с настоящим изобретением могут содержать одну или более моющих модифицирующих добавок или систем модифицирующих добавок. Если использована модифицирующая добавка, то рассматриваемый потребительский продукт будет типично содержать, по меньшей мере, приблизительно 1%, от приблизительно 2% до приблизительно 60% или даже от приблизительно 5% до приблизительно 10% модифицирующей добавки по массе рассматриваемого потребительского продукта. Композиция может даже, по существу, быть свободной от модифицирующей добавки; по существу свободной означает «не добавленный специально» цеолит и/или фосфат. Типичные цеолитные модифицирующие добавки включают цеолит А, цеолит Ρ и цеолит MAP. Типичная фосфатная модифицирующая добавка представляет собой натрий три-полифосфат.
Хелатирующие агенты и ингибиторы роста кристаллов - Композиции в данной заявке могут содержать хелатирующий агент и/или ингибитор роста кристаллов. Приемлемые молекулы включают медные, железные и/или марганцевые хелатирующие агенты и их смеси. Приемлемые молекулы включают DTPA (диэтилентриаминпентауксусную кислоту), HEDP (гидроксиэтанифосфониевую кислоту), DTP MP (диэтилентриаминпента(метиленфосфониевую кислоту)), 1,2-дигидроксибензол-3,5-дисульфониевой кислоты динатриевой соли гидрат, этилендиамин, диэтилентриамин, этилендиаминдиянтарную кислоту (EDDS), N-гидроксиэтилэтилендиаминтри-уксусную кислоту (HEDTA), триэтилентетраамингексауксусную кислоту (ТТНА), N-гидроксиэтилиминодиуксусную кислоту (HEIDA), дигидроксиэтилглицин (DHEG), этилендиаминтетрапропионовую кислоту (EDTP), карбоксиметилинулин и 2-фосфонобутан 1,2,4-трикарбоновую кислоту (Bayhibit® AM) и их производные. Типично потребительский продукт может содержать от приблизительно 0,005% до приблизительно 15% или даже от приблизительно 3,0% до приблизительно 10% хелатирующего агента или ингибитора роста кристаллов по массе рассматриваемого потребительскогой продукта.
Агенты, ингибирующие перенос красителя - Композиции в соответствии с настоящим изобретением могут также содержать один или более агентов, ингибирующих перенос красителя. Приемлемые полимерные агенты, ингибирующие перенос красителя, включают, но не ограничиваясь приведенным, поливинилпирролидоновые полимеры, полиамин N-оксидные полимеры, сополимеры N-винилпирролидона и N-винилимидазола, поливинилоксазолидоны и поливинилимидазолы или их смеси. Если присутствуют в рассматриваемом потребительском продукте, агенты, ингибирующие перенос красителя, могут присутствовать на уровнях от приблизительно 0,0001% до приблизительно 10%, от приблизительно 0,01% до приблизительно 5% или даже от приблизительно 0,1% до приблизительно 3% по массе потребительского продукта.
Блескообразователи - Композиции в соответствии с настоящим изобретением могут также содержать дополнительные компоненты, которые могут придавать оттенок изделиям подлежащим очистке, такие как флуоресцентные блескообразователи.
Композиция может содержать С.I. флуоресцентный блескообразователь 260 в альфа-кристаллической форме, имеющий следующую структуру:

В одном аспекте, блескообразователь представляет собой растворимый в холодной воде блескообразователь, например С.I. флуоресцентный блескообразователь 260 в альфа-кристаллической форме.
В одном аспекте блескообразователь главным образом находится в альфа-кристаллической форме, что означает, что типично, по меньшей мере, 50 мас. %, по меньшей мере, 75 мас. %, по меньшей мере, 90 мас. %, по меньшей мере, 99 мас. %, или даже по существу весь, С.I. флуоресцентный блескообразователь 260 находится в альфа-кристаллической форме.
Блескообразователь типично находится в форме микронизированных частиц, имеющих средневесовой размер первичных частиц от 3 до 30 микрометров, от 3 микрометров до 20 микрометров, или от 3 до 10 микрометров.
Композиция может содержать С.I. флуоресцентный блескообразователь 260 в бета-кристаллической форме, и массовое соотношение: (i) С.I. флуоресцентного блескообразователя 260 в альфа-кристаллической форме, и (ii) С.I. флуоресцентного блескообразователя 260 в бета-кристаллической форме может составлять, по меньшей мере, 0,1, или, по меньшей мере, 0,6.
ВЕ680847 относится к способу получения C.I флуоресцентного блескообразователя 260 в альфа-кристаллической форме.
Коммерческие оптические блескообразователи, которые могут быть полезны в настоящем изобретении, можно разделить на подгруппы, которые включают, но не ограничиваясь приведенным, производные стильбена, пиразолин, кумарин, карбоновую кислоту, метинцианины, дибензотиофен-5,5-диоксид, азолы, 5- и 6-членные гетероциклы и другие различные агенты. Примеры таких блескообразователей описаны в «The Production and Application of Fluorescent Brightening Agents», M. Zahradnik, Published by John Wiley & Sons, New York (1982). Конкретные неорганичивающие примеры оптических блескообразователей, которые полезны в композициях в соответствии с настоящим изобретением, являются идентифицированными в патенте США №4,790,856 и патенте США №3,646,015.
Дополнительный приемлемый блескообразователь имеет структуру, приведенную ниже:

Приемлемые уровни флуоресцентного блескообразователя включают нижние уровни от приблизительно 0,01, от приблизительно 0,05, от приблизительно 0,1 или даже от приблизительно 0,2 мас. % до верхних уровней 0,5 или даже 0,75 мас. %.
В одном аспекте блескообразователь может быть загружен на глину с образованием частицы. Силикатные соли - Композиции в соответствии с настоящим изобретением могут также содержать силикатные соли, такие как натрий или калий силикат.Композиция может содержать от 0 мас. % до менее, чем 10 мас. % силикатной соли, до 9 мас. %, или до 8 мас. %, или до 7 мас. %, или до 6 мас. %, или до 5 мас. %, или до 4 мас. %, или до 3 мас. %, или даже до 2 мас. %, и предпочтительно от выше 0 мас. %, или от 0,5 мас. %, или даже от 1 мас. % силикатной соли. Приемлемой силикатной солью является силикат натрия.
Диспергаторы - Композиции в соответствии с настоящим изобретением могут также содержать диспергаторы. Приемлемые водорастворимые органические материалы включают гомо- или со-полимерные кислоты или их соли, в которых поликарбоновая кислота содержит, по меньшей мере, два карбоксильных радикала, отделенных друг от друга не более, чем двумя атомами углерода.
Стабилизаторы ферментов - Ферменты для использования в композициях могут быть стабилизированы различными методами. Задействованные ферменты в данной заявке могут быть стабилизированы путем присутствия водорастворимых источников ионов кальция и/или магния в готовых продуктах для ухода за тканями и бытового ухода, которые доставляют такие ионы к ферментам. В случае водных композиций, содержащих протеазу, обратимый ингибитор протеазы, такой как соединение бора, включая борат, 4-формилфенилборную кислоту, фенилборную кислоту и их производные, или соединения, такие как формиат кальция, формиат натрия и 1,2-пропандиол, могут быть добавлены для дальнейшего улучшения стабильности.
Растворители - Приемлемые растворители включают воду и другие растворители, такие как липофильные жидкости. Примеры приемлемых липофильных жидкостей включают силоксаны, другие силиконы, углеводороды, эфиры гликолей, производные глицерина, такие как эфиры глицерина, перфторированные амины, перфторированные и гидрофторэфирные растворители, низколетучие нефторированные органические растворители, диольные растворители, другие экологически чистые растворители и их смеси.
Структурообразователь/Загустители
Структурированные жидкости могут быть либо внутренне структурированы, в результате чего структура образована первичными ингредиентами (например, материалом поверхностно-активного вещества) и/или внешне структурированы путем обеспечения трехмерной матричной структуры с использованием вторичных ингредиентов (например, полимеров, глины и/или силикатного материала). Композиция может содержать структурообразователь, предпочтительно от 0,01 мас. % до 5 мас. %, от 0,1 мас. % до 2,0 мас. % структурообразователя. Структурообразователь типично выбирают из группы, состоящей из диглицеридов и триглицеридов, этиленгликоль дистеарата, микрокристаллической целлюлозы, материалов на основе целлюлозы, микроволоконной целлюлозы, гидрофобно модифицированных набухаемых в щелочи эмульсий, таких как Polygel W30 (3VSigma), биополимеров, ксантановой камеди, геллановой камеди и их смесей. Приемлемый структурообразователь включает гидрогенизированное касторовое масло и его неэтоксилированные производные. Приемлемый структурообразователь раскрыт в патенте США №6,855,680. Такие структурообразователи имеют нитевидную структурирующую систему, имеющую диапазон аспектовых соотношений. Другие приемлемые структурообразователи, и способы их получения описаны в WO 2010/034736.
Кондиционирующие агенты
Композиция в соответствии с настоящим изобретением может содержать жирное соединение с высокой температурой плавления. Жирное соединение с высокой температурой плавления, полезное в данной заявке, имеет температуру плавления 25°С или выше, и его выбирают из группы, состоящей из жирных спиртов, жирных кислот, производных жирных спиртов, производных жирных кислот и их смесей. Такие соединения с низкой температурой плавления не должны быть включены в этот раздел. Неограничивающие примеры соединений с высокой температурой плавления описаны в International Cosmetic Ingredient Dictionary, Fifth Edition, 1993, и CTFA Cosmetic Ingredient Handbook, Second Edition, 1992.
Жирное соединение с высокой температурой плавления включено в композицию на уровне от приблизительно 0,1% до приблизительно 40%, предпочтительно от приблизительно 1% до приблизительно 30%, более предпочтительно от приблизительно 1,5% до приблизительно 16% по массе композиции, от приблизительно 1,5% до приблизительно 8% с точки зрения обеспечения улучшенных полезных эффектов кондиционирования, таких как ощущение скользкости во время нанесения на влажные волосы, ощущения мягкости и увлажнения на сухих волосах.
Композиции в соответствии с настоящим изобретением могут содержать катионный полимер. Концентрации катионного полимера в композиции типично находятся в диапазоне от приблизительно 0,05% до приблизительно 3%, в другом воплощении от приблизительно 0,075% до приблизительно 2,0%, и в еще одном воплощении от приблизительно 0,1% до приблизительно 1,0%. Приемлемые катионные полимеры будут иметь плотности катионного заряда, по меньшей мере, приблизительно 0,5 мэкв/гм, в другом воплощении, по меньшей мере, приблизительно 0,9 мэкв/гм, в другом воплощении, по меньшей мере, приблизительно 1,2 мэкв/гм, в еще одном воплощении, по меньшей мере, приблизительно 1,5 мэкв/гм, но в одном воплощении также менее, чем приблизительно 7 мэкв/гм, и в другом воплощении менее, чем приблизительно 5 мэкв/гм, при рН целевого использования композиции, где рН будет, в общем, находится в диапазоне от приблизительно рН 3 до приблизительно рН 9, в одном воплощении от приблизительно рН 4 до приблизительно рН 8. В данной заявке, «плотность катионного заряда» полимера относится к соотношению количества положительных зарядов на полимере к молекулярной массе полимера. Средняя молекулярная масса таких приемлемых катионных полимеров будет в общем составлять от приблизительно 10000 до 10 миллионов, в одном воплощении от приблизительно 50000 до приблизительно 5 миллионов, и в другом воплощении от приблизительно 100000 до приблизительно 3 миллионов.
Приемлемые катионные полимеры для использования в композициях в соответствии с настоящим изобретением содержат катионные азот-содержащие фрагменты, такие как четвертичные аммониевые или катионные протонированные амино фрагменты. Любые анионные противоионы могут быть использованы в сочетании с катионными полимерами, пока полимеры растворимы в воде, в композиции, или в коацерватной фазе композиции, и пока противоионы физически и химически совместимы с основными компонентами композиции или иным ненадлежащим образом не придают производительность продукта, стабильность или эстетику. Неограничивающие примеры таких противоионов включают галогениды (например, хлорид, фторид, бромид, иодид), сульфат и метилсульфат.
Неограничивающие примеры таких полимеров описаны в CTFA Cosmetic Ingredient Dictionary, 3rd edition, edited by Estrin, Crosley, and Haynes, (The Cosmetic, Toiletry, and Fragrance Association, Inc., Washington, D.C. (1982)).
Другие приемлемые катионные полимеры для использования в композиции включают полисахаридные полимеры, катионные производные гуаровых камедей, содержащие четвертичный азот эфиры целлюлозы, синтетические полимеры, сополимеры этерифицированной целлюлозы, гуара и крахмала. При использовании, катионные полимеры в данной заявке растворимы в композиции или растворимы в сложной коацерватной фазе в композиции, образованной катионным полимером и компонентом анионного, амфотерного и/или цвиттерионного поверхностно-активного вещества, как описано в данной заявке ранее. Сложные коацерваты катионного полимера также могут быть образованы другими заряженными материалами в композиции.
Приемлемые катионные полимеры описаны в патентах США №№3,962,418; 3,958,581; и патентной публикации США №2007/0207109А1, все из которых включены в данную заявку путем ссылки.
Композиция в соответствии с настоящим изобретением может содержать неионный полимер в качестве кондиционирующего агента. Полиалкиленгликоли, имеющие молекулярную массу более, чем приблизительно 1000, полезны в данной заявке. Полезными являются те, которые имеют следующую общую формулу:

где R95 выбирают из группы, состоящей из Н, метила и их смесей. Кондиционирующие агенты, и в частности силиконы, могут быть включены в композицию. Кондиционирующие агенты, полезные в композициях в соответствии с настоящим изобретением, типично содержат нерастворимую в воде, диспергируемую в воде, нелетучую жидкость, образующую эмульгированные жидкие частицы. Приемлемые кондиционирующие агенты для использования в композиции представляют собой кондиционирующие агенты, характеризуемые в общем как силиконы (например, силиконовые масла, катионные силиконы, силиконовые камеди, силиконы с высоким коэффициентом преломления и силиконовые смолы), органические кондиционирующие масла (например, углеводородные масла, полифолефины и жирные сложные эфиры) или их комбинации, или такие кондиционирующие агенты, которые иным образом образуют жидкие диспергированные частицы в матриксе водного поверхностно-активного вещества в данной заявке. Такие кондиционирующие агенты должны быть физически и химически совместимы с основными компонентами композиции, и не должны ненадлежащим иным образом ухудшать стабильность, эстетику или производительность продукта.
Концентрация кондиционирующего агента в композиции должна быть достаточной, чтобы обеспечить желаемые полезные эффекты кондиционирования. Такая концентрация может варьироваться в зависимости от кондиционирующего агента, требуемого для производительности кондиционирования, среднего размера частиц кондиционирующего агента, типа и концентрации других компонентов, и других подобных факторов.
Концентрация силиконового кондиционирующего агента типично находится в диапазоне от приблизительно 0,01% до приблизительно 10%. Неограничивающие примеры приемлемых силиконовых кондиционирующих агентов, и необязательных суспендирующих агентов для силикона, описаны в переизданном патенте США №34,584, патентах США №№5,104,646; 5,106,609; 4,152,416; 2,826,551; 3,964,500; 4,364,837; 6,607,717; 6,482,969; 5,807,956; 5,981,681; 6,207,782; 7,465,439; 7,041,767; 7,217,777; патентных заявках США №№2007/0286837А1; 2005/0048549 А1; 2007/0041929Al; Британском патенте №849,433; Немецком патенте № DE 10036533, все из которых включены в данную заявку путем ссылки; Chemistry and Technology of Silicones, New York: Academic Press (1968); General Electric Silicone Rubber Product Data Sheets SE 30, SE 33, SE 54 и SE 76; Silicon Compounds, Petrarch Systems, Inc. (1984); и в Encyclopedia of Polymer Science and Engineering, vol. 15, 2d ed., pp 204-308, John Wiley & Sons, Inc. (1989).
Композиции в соответствии с настоящим изобретением могут также содержать от приблизительно 0,05% до приблизительно 3%, по меньшей мере, одного органического кондиционирующего масла в качестве кондиционирующего агента, отдельно или в сочетании с другими кондиционирующими агентами, такими как силиконы (описаны в данной заявке). Приемлемые кондиционирующие масла включают углеводородные масла, полиолефины и жирные сложные эфиры. Также приемлемыми для использования в композициях в данной заявке являются кондиционирующие агенты, описанные Procter & Gamble Company в патентах США №№5,674,478 и 5,750,122. Также приемлемыми для использования в данной заявке являются кондиционирующие агенты, описанные в патентах США №№4,529,586, 4,507,280,4,663,158, 4,197,865, 4,217,914, 4,381,919 и 4,422,853.
Гигиена и неприятный запах - Композиции в соответствии с настоящим изобретением могут также содержать один или более из цинка рицинолеата, тимола, солей четвертичного аммония, таких как Bardac®, полиэтилениминов (таких, как Lupasol® от BASF) и их комлексов с цинком, серебра и соединений серебра, в особенности разработанных для медленного высвобождения Ag+ или нано-серебряных дисперсий.
Пробиотики - Композиции могут содержать пробиотики, такие, как описанные в WO 2009/043709.
Усилители пенообразования - Если желательно высокое пенообразование, усилители пенообразования, такие как С10-С16 алканоламиды или С10-С14 алкил сульфаты, могут быть включены в композиции, типично на 1%-10% уровнях. С10-С14 моноэтанол и диэтаноламиды иллюстрируют типичный класс таких усилителей пенообразования. Применение таких усилителей пенообразования с высокопенообразующими вспомогательными поверхностно-активными веществами, такими, как аминоксиды, бетаины и султаины, указанными выше, является также полезным. При желании, водорастворимые соли магния и/или кальция, такие, как MgCl2, MgSO4, CaCl2, CaSO4 и т.п., могут быть добавлены на уровнях, типично, 0,1%-2%, с обеспечением дополнительной пены и для улучшения производительности удаления жира.
Подавители пенообразования. Соединения для уменьшения или подавления образования пены могут быть включены в композиции в соответствии с настоящим изобретением. Пеноподавление может быть особенно важным в так называемом «высококонцетрированном процессе очистки» как описано в патенте США №4,489,455 и 4,489,574, и в стиральных машинах с фронтальной загрузкой.
Широкое разнообразие материалов может быть использовано в качестве подавителей пенообразования, и подавители пенообразования хорошо известны специалистам в данной области техники. См., например, Kirk Othmer Encyclopedia of Chemical Technology, Third Edition, Volume 7, pages 430-447 (John Wiley & Sons, Inc., 1979). Примеры подавителей пенообразования включают монокарбоновые жирные кислоты и их растворимые соли, высокомолекулярные углеводороды, такие как парафин, сложные эфиры жирных кислот (например, триглицериды жирных кислот), сложные эфиры жирных кислот одноатомных спиртов, алифатические С18-С40 кетоны (например, стеарон), N-алкилированные амино триазины, восковые углеводороды, предпочтительно имеющие температуру плавления ниже приблизительно 100°С, силиконовые подавители пенообразования и вторичные спирты. Подавители пенообразования описаны в патентах США №№2,954,347; 4,265,779; 4,265,779; 3,455,839; 3,933,672; 4,652,392; 4,978,471; 4,983,316; 5,288,431; 4,639,489; 4,749,740; и 4,798,679; 4,075,118; Европейской патентной заявке №89307851.9; ЕР 150,872; и DOS 2,124,526.
Для любых композиций моющих средств, которые будут использованы в автоматических стиральных машинах, пена не должна образовываться в той степени, что она переполняет стиральную машину. Подавители пенообразования, когда используются, предпочтительно присутствуют в «количестве пеноподавления». Под «количеством пеноподавления» подразумевают, что составитель композиции может выбрать количество этого агента, контролирующего пенообразование, которое будет в достаточной степени контролировать пену, чтобы привести к получению моющего средства для стирки с низким пенообразования для использования в автоматических стиральных машинах.
Композиции в данной заявке будут, в общем, содержать от 0% до приблизительно 10% подавителя пенообразования. При использовании в качестве подавителей пенообразования, монокарбоновые жирные кислоты и их соли, будут присутствовать типично в количествах до приблизительно 5%, по массе, композиции моющего средства. Предпочтительно, используют от приблизительно 0,5% до приблизительно 3% жирных монокарбоксилатных подавителей пенообразования. Силиконовые подавители пенообразования типично используют в количествах до приблизительно 2,0%, по массе, композиции моющего средства, хотя могут быть использованы большие количества. Моностеарил фосфатные подавители пенообразования, в общем, используют в количествах в диапазоне от приблизительно 0,1% до приблизительно 2%, по массе композиции. Углеводородные подавители пенообразования типично используют в количествах в диапазоне от приблизительно 0,01% до приблизительно 5,0%, хотя могут быть использованы большие количества. Спиртовые подавители пенообразования типично используют при 0,2%-3% по массе готовых композиций.
Водорастворимая пленка - Композиции в соответствии с настоящим изобретением могут также быть инкапсулированы в водорастворимую пленку. Предпочтительные материалы пленок предпочтительно представляют собой полимерные материалы. Материал пленки может, например, быть получен литьем, выдувным формованием, экструзией или экструзией с раздувом полимерного материала, как известно в данной области техники.
Предпочтительные полимеры, сополимеры или их производные, приемлемые для использования в качестве материала мешочка, выбирают из поливиниловых спиртов, поливинилпирролидона, полиалкиленоксидов, акриламида, акриловой кислоты, целлюлозы, эфиров целлюлозы, сложных эфиров целлюлозы, амидов целлюлозы, поливинил ацетатов, поликарбоновых кислот и солей, полиаминокислот или пептидов, полиамидов, полиакриламида, сополимеров малеиновой/акриловой кислот, полисахаридов, включая крахмал и желатин, природных камедей, таких как ксантан и каррагенан. Более предпочтительные полимеры выбирают из полиакрилатов и водорастворимых акрилатных сополимеров, метилцеллюлозы, натрий карбоксиметилцеллюлозы, декстрина, этилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, мальтодекстрина, полиметакрилатов, и наиболее предпочтительно выбирают из поливиниловых спиртов, сополимеров поливинилового спирта и гидроксипропилметилцеллюлозы (НРМС) и их комбинаций. Предпочтительно, уровень полимера в материале мешочка, например PVA полимера, составляет, по меньшей мере, 60%. Полимер может иметь любую средневесовую молекулярную массу, предпочтительно от приблизительно 1000 до 1000000, более предпочтительно от приблизительно 10000 до 300000, еще более предпочтительно от приблизительно 20000 до 150000. Смеси полимеров также могут быть использованы в качестве материала мешочка.
Обычно, различные материалы пленок и/или пленки различной толщины могут быть использованы при изготовлении отделений в соответствии с настоящим изобретением. Полезный эффект при выборе различных пленок состоит в том, что полученные в результате отделения могут проявлять различную растворимость или характристики высвобождения.
Наиболее предпочтительные материалы пленок педставляют собой PVA пленки, известные под MonoSol торговым наименованием М8630, М8900, Н8779 (как описано в одновременно поданных Заявителями заявках №№44528 и 11599) и описанные в US 6166117 и US 6787512, и PVA пленки соответствующих характеристик растворимости и деформируемости.
Материал пленки в данной заявке может также содержать один или более дополнительных ингредиентов. Например, может быть полезно добавить пластификаторы, например глицерин, этиленгликоль, диэтиленгликоль, пропилен гликоль, сорбит и их смеси. Другие добавки включают функциональные моющие добавки, которые будут доставлены в промывную воду, например органические полимерные диспергаторы и т.д.
Способы получения композиций
Композиции в соответствии с настоящим изобретением могут быть составлены в любой приемлемой форме и получены любым способом, выбранным составителем, неограничивающие примеры которых описаны в примерах Заявителей и в U.S. 4,990,280; U.S. 20030087791 A1; U.S. 20030087790 A1; U.S. 20050003983 A1; U.S. 20040048764 A1; U.S. 4,762,636; U.S. 6,291,412; U.S. 20050227891 A1; EP 1070115 A2; U.S. 5,879,584; U.S. 5,691,297; U.S. 5,574,005; U.S. 5,569,645; U.S. 5,565,422; U.S. 5,516,448; U.S. 5,489,392; U.S. 5,486,303, все из которых включены в данную заявку путем ссылки. Композиции в соответствии с настоящим изобретением или полученные в соответствии с настоящим изобретением включают композиции для очистки и/или обработки включая, но не ограничиваясь приведенным, продукты для обработки ткани, твердых поверхностей и любых других поверхностей в области ухода за тканями и бытового ухода, в том числе: для обработки воздуха, включая освежители воздуха и системы доставки ароматов, автокосметику, средства для мытья посуды, для кондиционирования ткани (в том числе смягчения и/или освежения), моющие средства для стирки, добавки и/или средства для ухода при стрике и полоскании, для очистки и/или обработки твердых поверхностей, включая очистители для пола и унитаза, гранулированные или порошкообразные универсальные или «высокопроизводительные» моющие агенты, особенно чистящие моющие средства; жидкие, гелеобразные или пастообразные универсальные моющие агенты, особенно так называемые высокопроизводительные жидкие типы; жидкие моющие средства для тонких тканей; средства для мытья посуды вручную или облегченные средства для мытья посуды, особенно сильнопенящегося типа; средства для посудомоечных машин, в том числе различные таблетки, гранулированные, жидкие типы и ополаскиватели для бытового и институционального использования: шампуни для автомобилей или ковров, очистители ванных комнат, включая очистители для унитазов; а также вспомогательные вещества для очистки, такие как отбеливающие добавки и «стики для выведения пятен» или типы для предварительной обработки, продукты с пропитанным субстратом, такие как салфетки, добавляемые в сушильную машину. Предпочтительными являются композиции и способы очистки и/или обработки ткани и/или твердых поверхностей, наиболее предпочтительно ткани. Композиции предпочтительно представляют собой композиции, используемые на стадии предварительной обработки или стадии основного мытья процесса мытья, наиболее предпочтительно для использования на стадии стирки ткани.
Как используют в данной заявке, термин «композиция для очистки и/или обработки ткани и/или твердой поверхности» представляет собой подмножество композиций для очистки и обработки, которое включает, если не указано иное, гранулированные или порошкообразные формы универсальных или «высокопроизводительных» моющих средств, особенно чистящих моющих средств; жидкие, гелеобразные или пастообразные универсальные моющие агенты, особенно так называемые высокопроизводительные жидкие типы; жидкие моющие средства для тонкой ткани; средства для мытья посуды вручную или облегченные средства для мытья посуды, особенно сильнопенящегося типа; средства для посудомоечных машин, в том числе различные таблетки, гранулированные, жидкие типы и ополаскиватели для бытового и институционального использования; чистящие жидкости и дезинфицирующие средства, шампуни для автомобилей или ковров, очистители для ванных комнат, включая очистители для унитазов; продукты для кондиционирования ткани, включая смягчение и/или освежение, которые могут быть в жидкой, твердой форме и/или форме салфеток, добавляемых в сушильную машину; а также вспомогательные вещества для очистки, такие как отбеливающие добавки и «стики для выведения пятен» или типы для предварительной обработки, продукты с пропитанным субстратом, такие как листы с добавлением высушивателя. Все такие продукты, которые применимы, могут быть в стандартной, концентрированной или даже высококонцентрированной форме, даже в том случае, когда такие продукты могут в определенном аспекте быть неводными.
Способ применения
Настоящее изобретение включает способ очистки и/или обработки ткани или твердой поверхности или другой поверхности при уходе за тканями или бытовом уходе. В предпочтительном аспекте настоящего изобретения, способ включает стадию, на которой вводят в контакт поверхность, подлежащую обработке, на стадии предварительной обработки или стадии мытья основного процесса мытья, наиболее предпочтительно для использования на стадии стирки ткани. В одном воплощении вариант липазы и отбеливающие компоненты добавляют последовательно в способе очистки и/или обработки поверхности. Например, в предпочтительном способе может быть стадия предварительной обработкой с отбеливанием, на которой отбеливающий компонент могут вводить в контакт с поверхностью на стадии предварительной обработки, и предварительно обработанную поверхность в присутствии отбеливающего компонента вводят в контакт на второй стадии с вариантом липазы. Альтернативно вариант липазы может контактировать с поверхностью до последующего добавления отбеливающего компонента.
Как используют в данной заявке, мытье включает, но не ограничиваясь приведенным, оттирание и механическое перемешивание. Высушивание таких поверхностей или тканей может быть осуществлено с помощью любого из обычных способов, используемых в бытовых или в промышленных установках. Композиции для очистки в соответствии с настоящим изобретением идеально подходят для использования в применениях для стирки. Соответственно, настоящее изобретение включает способ стирки ткани. Способ включает стадии, на которых ткань, подлежащую стирке, вводят в контакт с указанным чистящим раствором для стирки, содержащим, по меньшей мере, одно воплощение композиции для очистки Заявителей, чистящую добавку или их смесь. Ткань может содержать практически любую ткань, пригодную для стирки в нормальных потребительских условиях использования или в условиях использования в учереждениях. Предпочтительно раствор имеет рН от приблизительно 8 до приблизительно 10,5. Композиции могут быть использованы в концентрациях от приблизительно 500 м.д. до приблизительно 15000 м.д. в растворе. Температура воды обычно находится в диапазоне от приблизительно 5°С до приблизительно 90°С. Соотношение воды и ткани, как правило, составляет от приблизительно 1:1 до приблизительно 30:1.
Настоящее изобретение далее описано с помощью следующих примеров, которые не следует рассматривать как ограничивающие объем настоящего изобретения.
Примеры
Пример 1: Анализ автоматической механической нагрузки для стирки
Для оценки стабильности к окислительному распаду варианта липазы, значение для относительной производительности (КРмытья) определено: производительность мытья (Р) варианта липазы в соответствии с настоящим изобретением по сравнению с липазой SEQ ID ΝΟ: 1 или RP=Ρ (вариант липазы в соответствии с настоящим изобретением) / P(SEQ ID NO: 1 липазы). Производительность мытья определяют путем проведения стирки, моющих экспериментов с использованием анализа автоматической механической нагрузки (AMSA). При помощи AMSA, может быть исследована производительность мытья большого количества липазно-моющих растворов небольшого объема. AMSA пластина имеет количество щелей для тестовых растворов и крышку, плотно сжимающую запятнанную ткань напротив всех открытых щелей. Во время мытья, пластину, тестовые растворы, ткань и крышку энергично встряхивают, чтобы привести тестовый раствор в контакт с тканью и применить механическую нагрузку обычным, периодическим колебательным образом. Для дальнейшего описания см. WO 02/42740 в особенности параграф «Специальные воплощения способа» на странице 23-24.
Эксперименты со стиркой проводят в экспериментальных условиях, указанных ниже:

химической формуле:

Жесткость воды доводили до 18°dH путем добавления CaCl2, MgCl2 и NaHCO3 (Ca2+:Mg2+=4:1:7,5) в тестовую систему. После стирки ткани промывали под струей водопроводной воды и высушивали в течение 5 минут при 85°С в термошкафу.
Производительность мытья определяют как яркость цвета постиранной ткани. Яркость также может быть выражена как интенсивность света, отраженного от пробы при освещении белым светом. Когда проба зарязнена, интенсивность отраженного света ниже, чем у чистой пробы. Поэтому интенсивность отраженного света может быть использована для оценки производительности мытья.
Измерения цвета выполняют при помощи профессионального планшетного сканера (Kodak iQsmart, Kodak, Midtager 29, DK-2605 Brandby, Denmark), который используют для получения изображения постиранной ткани.
Чтобы извлечь значение для интенсивности света из отсканированных изображений, 24-битовые пиксельные значения из изображений преобразуются в значения для красного, зеленого и синего (RGB). Значение интенсивности (Int) рассчитывают путем сложения значений RGB вместе в качестве векторов, а затем берут длину результирующего вектора:

Производительность мытья (Р) варианта липазы рассчитывают в соответствии со следующей формулой: Р=ΔInt=Int(v)-Int(r), где Int(v) является значением интенсивности света поверхности ткани, постиранной вариантом липазы, и Int(r) является значением интенсивности света поверхности ткани, постиранной без варианта липазы.
Расчет балла относительной производительности (RРмытья): балл относительной производительности представляют как результат полной шкалы, которую мыли в соответствии с определением:
Баллы относительной производительности (RPмытья) дают производительность (Р) варианта липазы в соответствии с настоящим изобретением по сравнению с обычной липазой: RP=Р (вариант липазы в соответствии с настоящим изобретением) / Р(обычная липаза). Композицию липазы рассматривают как проявляющую улучшенную производительность мытья, если она более эффективна, чем обычная липаза.
Пример 2: G91 варианты с улучшенной производительностью в присутствии катализаторов отбеливания
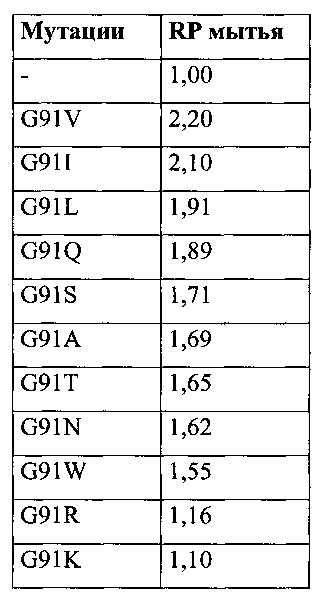
Пример 3: Т37 варианты с улучшенной производительностью в присутствии катализаторов отбеливания

Пример 4: N39 варианты с улучшенной производительностью в присутствии катализаторов отбеливания

Пример 5: Варианты с двумя или более мутациями и с улучшенной производительностью в присутствии катализаторов отбеливания


Примеры композиций 1-6
Гранулированные композиции моющих средств для стирки, предназначенные для стирки вручную или в стиральных машинах с вертикальной загрузкой.


Примеры композиций 7-12
Гранулированные композиции моющих средств для стирки, предназначенные для автоматических стиральных машин с фронтальной загрузкой
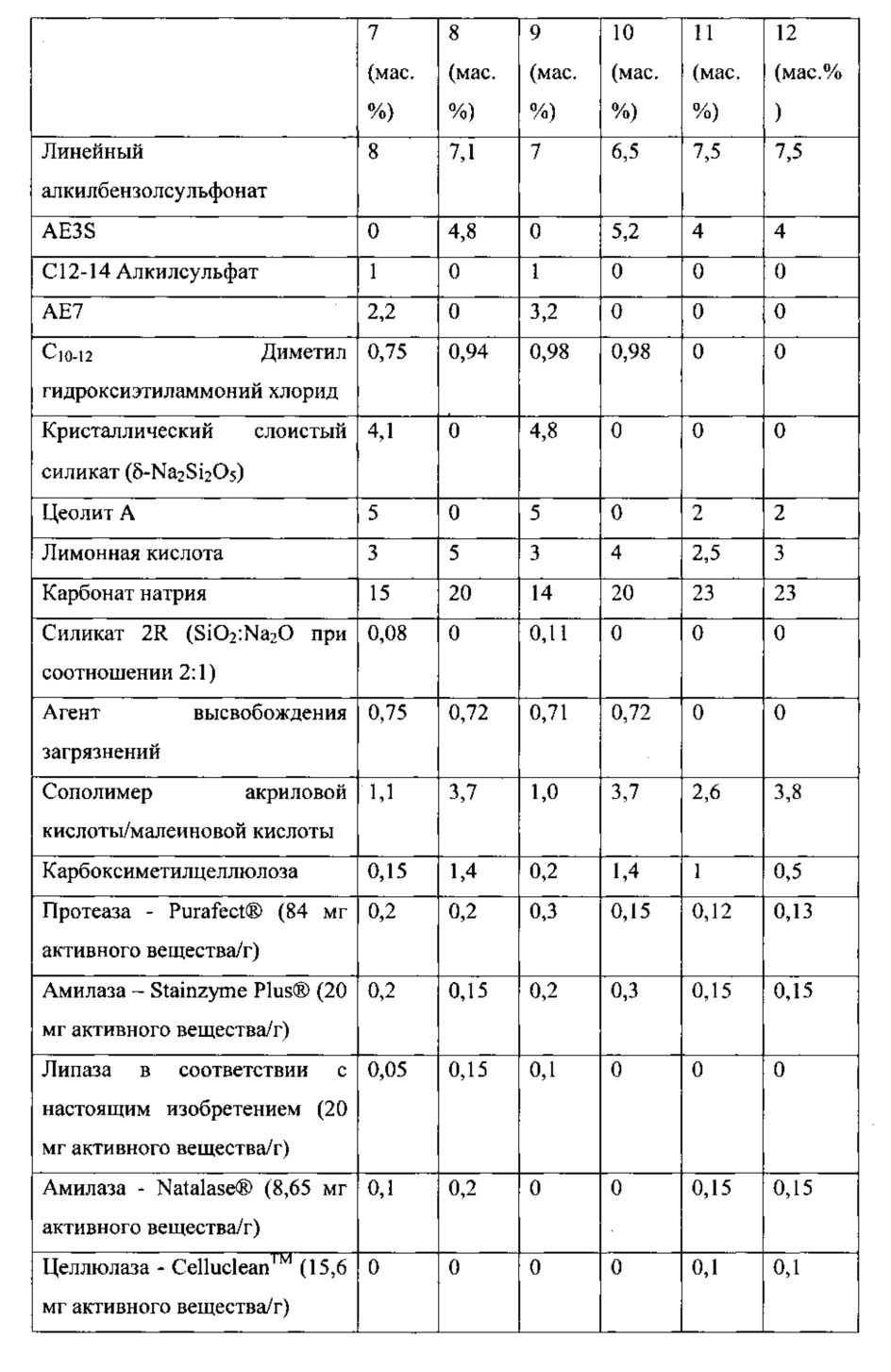

Любую из указанных выше композиций используют для стирки тканей в концентрации от 7000 до 10000 м.д. в воде, 20-90°С, и 5:1 соотношении ткань:вода. Типичное значение рН составляет приблизительно 10. Ткани затем сушат. В одном аспекте, ткани активно сушат с использованием сушилки. В одном аспекте, ткани активно сушат утюгом. В другом аспекте, ткани просто оставляют высушиваться на линии, где они подвергаются воздействию воздуха и необязательно солнечному свету.
Примеры композиций 13-18
Высокопроизводительные жидкие композиции моющих средств для стирки


Примеры композиций 19-31 - Композиции стандартной дозы
Ниже приведены композиции для моющих средств для стирки стандартной дозы. Такие композиции стандартной дозы могут содержать одно или несколько отделений.


Сырье и примечания для Примеров композиций 1-23
Линейный алкилбензолсульфонат, имеющий среднюю длину алифатической углеродной цепи С11-С12 поставляется от Stepan, Northfield, Illinois, USA
C12-14 диметилгидроксиэтил аммоний хлорид, поставляется от Clariant GmbH, Sulzbach, Germany
AE3S представляет собой Стзалкил этокси (3) сульфат поставляется от Stepan, Northfield, Illinois, USA
AE7 представляет собой С12-15 спирт этоксилат, со средней степенью этоксилирования 7, поставляется от Huntsman, Salt Lake City, Utah, USA
AE9 представляет собой С12-13 спирт этоксилат, со средней степенью этоксилирования 9, поставляется от Huntsman, Salt Lake City, Utah, USA
HSAS представляет собой разветвленный в середине цепи первичный алкил сульфат с длиной углеродной цепи приблизительно 16-17
Натрий триполифосфат поставляется от Rhodia, Paris, France
Цеолит А поставляется от Industrial Zeolite (UK) Ltd, Grays, Essex, UK
1,6R Силикат поставляется от Koma, Nestemica, Czech Republic
Карбонат натрия поставляется от Solvay, Houston, Texas, USA
Полиакрилат MW 4500 поставляется от BASF, Ludwigshafen, Germany
Карбоксиметилцеллюлоза представляет собой Finnfix® V, поставляется от CP Kelco, Arnhem, Netherlands
Приемлемые хелатирующие агенты представляют собой, например, диэтилентетраамин пентауксусную кислоту (DTPA), поставляется от Dow Chemical., Midland, Michigan, USA или гидроксиэтан дифосфонат (HEDP), поставляется от Solutia, St Louis, Missouri, USA
Savinase®, Natalase®, Stainzyme®, Lipex®, Celluclean™, Mannaway® и Whitezyme® все представляют собой продукты от Novozymes, Bagsvaerd, Denmark.
Протеазы могут поставляться от Genencor International., Palo Alto, California, USA (например, Purafect Prime®) или от Novozymes, Bagsvaerd, Denmark (например, Liquanase®, Coronase®).
Флуоресцентный блескообразователь 1 представляет собой Tinopal® AMS, Флуоресцентный блескообразователь 2 представляет собой Tinopal® CBS-X, сульфонированный цинк фталоцианин и прямой фиолетовый 9 представляет собой Pergasol® Violet BH-Z, все поставляются от Ciba Specialty Chemicals, Basel, Switzerland
Перкарбонат натрия поставляется от Solvay, Houston, Texas, USA
Перборат натрия поставляется от Degussa, Hanau, Germany
NOBS представляет собой натрий нонаноилоксибензолсульфонат, поставляется от Future Fuels, Batesville, Arkansas, USA
TAED представляет собой тетраацетилэтилендиамин, поставляется под Peractive® наименованием бренда от Clariant GmbH, Sulzbach, Germany
Органический катализатор отбеливания имеет следующую структуру, где R13 представляет собой 2-бутилоктил, и производится в соответствии с патентной заявкой США 2006/0089284 А1,

S-ACMC представляет собой карбоксиметилцеллюлозу, конъюгированную с С.I. реакционноспособным синим 19, продается Megazyme, Wicklow, Ireland под названием продукта AZO-CM-CELLULOSE, код продукта S-ACMC.
Агент высвобождения загрязнений представляет собой Texcare® SRA300, поставляется от Clariant, Frankfurt, Germany
Сополимер акриловой кислоты/малеиновой кислоты имеет молекулярную массу 70000 и акрилат:малеат соотношение 70:30, поставляется от BASF, Ludwigshafen, Germany
Na соль этилендиамин-N,N'-диянтарной кислоты, (S,S) изомер (EDDS) поставляется от Octel, Ellesmere Port, UK
Гидроксиэтандифосфонат (HEDP) поставляется от Dow Chemical., Midland, Michigan, USA
Подавитель пенообразования аггломерат поставляется от Dow Corning, Midland, Michigan, USA
HSAS представляет собой разветвленный в середине цепи алкил сульфат, как описано в US 6,020,303 и US 6,060,443
С12-14 диметил аминоксид поставляется от Procter & Gamble Chemicals, Cincinnati, Ohio, USA
Liquitint® Violet CT и этоксилированные тиофеновые красители поставляются от Milliken, Spartanburg, South Carolina, USA
Размеры и значения, раскрытые в данной заявке, не должны быть истолкованы как строго ограниченные точными приведенными численными значениями. Вместо этого, если не указано иное, каждый такой размер должен обозначать как приведенное значение, так и функционально эквивалентный диапазон, окружающий это значение. Например, размер, обозначенный как «40 мм», означает «приблизительно 40 мм».
Реферат
Изобретение относится к композициям, содержащим липазные ферменты и отбеливающие агенты, а также к способам получения и использованию таких композиций. Описан способ очистки ткани, или твердой поверхности, или другой поверхности при уходе за тканями и бытовом уходе, включающий стадии, на которых: (a) вводят в контакт поверхность с водным раствором, содержащим (i) липазу; и (ii) отбеливающий компонент и (iii) необязательное моющее вспомогательное вещество; (b) промывают и высушивают ткань или твердую поверхность; при этом липаза включает вариант родительской липазы, причем родительская липаза содержит аминокислотную последовательность с, по меньшей мере, 60% идентичностью со зрелым полипептидом SEQ ID NO: 1 и причем вариант липазы имеет аминокислотную последовательность с, по меньшей мере, 60% идентичностью со зрелым полипептидом SEQ ID NO: 1, или его фрагмент, имеющий липазную активность, причем указанный вариант содержит следующие замены: (a) G91A+D96G+T231R+N233R; (b) T37R+N39R+G91A+D96G+T231R+N233R; (c) G91A+D96G+G225R+T231R+N233R; или (d) G91A+D96G+A150G+T231R+N233R, соответствующие указанным положениям в зрелом полипептиде SEQ ID NO: 1, причем вариант имеет липазную активность. Технический результат - улучшенная стабильность к окислительному распаду. 3 н. и 20 з.п. ф-лы, 5 пр.
Формула







Комментарии