Фторсилоксановые матриксные системы доставки лекарств с регулируемой диффузией и способ ее получения - RU2307667C2
Код документа: RU2307667C2
Описание
Область, к которой относится изобретение
Данное изобретение относится к сополимерам, используемым при изготовлении матриксных систем доставки лекарств с регулируемой диффузией.
Более конкретно, данное изобретение относится к матриксным системам доставки лекарства с регулируемой диффузией, полученным с применением одного или нескольких силоксановых полимеров с фторированными боковыми цепями.
Предпосылки создания изобретения
Обычные системы доставки, включающие частое периодическое дозирование, не являются идеальными или практическими во многих случаях. Например, в случае более токсичных лекарств обычное периодическое дозирование может привести к высоким начальным количествам лекарства во время дозирования с последующими низкими уровнями лекарства между дозами, часто в несколько раз меньше величин, имеющих терапевтическое значение. Точно так же обычное периодическое дозирование может не быть практическим или терапевтически эффективным в некоторых случаях, как например, в случае лечения глаза или мозга вследствие наличия гематоэнцефалического барьера.
В течение двух последних десятилетий были достигнуты значительные успехи в создании систем доставки лекарств с регулируемым высвобождением. Эти успехи были достигнуты при попытке преодолеть некоторые недостатки систем доставки лекарств, отмеченные выше. В общем, системы доставки лекарств с регулируемым высвобождением включают как системы доставки лекарств пролонгированного действия, предназначенные для доставки лекарств в течение заданного промежутка времени, так и системы прицельной доставки лекарств, предназначенные для доставки лекарства в конкретное место или конкретный орган организма. Системы доставки лекарств с пролонгированным регулируемым высвобождением и прицельного действия могут значительно отличаться способом высвобождения и делятся на три основные категории. Эти основные категории регулируемого высвобождения включают диффузионное регулируемое высвобождение, химическое эрозионное регулируемое высвобождение и активируемое растворителем регулируемое высвобождение. В системе доставки с диффузионным регулируемым высвобождением лекарство окружено инертным барьером и диффундирует из внутреннего резервуара или лекарство диспергировано в полимере и диффундирует из полимерной матрицы. В системе доставки с химическим эрозионным регулируемым высвобождением лекарство равномерно распределено в биоразлагающемся полимере. Биоразлагающийся полимер предназначен для разложения в результате гидролиза с целью равномерного высвобождения лекарства. В системах доставки с регулируемым активируемым растворителем высвобождением лекарство иммобилизовано на полимерах в системе доставки. При активации растворителем полимер, чувствительный к растворителю, разлагается или набухает с высвобождением лекарства.
К сожалению, до сих пор существующие системы доставки с регулируемым высвобождением лекарства не обеспечивают средства, которыми можно манипулировать и регулировать скорость высвобождения конкретных лекарств при наличии их большого набора из систем доставки с регулируемым высвобождением.
Ввиду наличия недостатков имеющихся систем доставки с регулируемым высвобождением существует необходимость создания таких систем доставки с регулируемым высвобождением лекарства, которые позволяют регулировать скорость высвобождения лекарства в зависимости от вида лекарства, которое нужно ввести, места доставки, цели доставки и/или терапевтических требований индивидуального пациента.
Сущность изобретения
Новые матриксные системы доставки лекарства с регулируемой диффузией согласно данному изобретению, полученные в результате полимеризации одного или нескольких силоксановых мономеров с фторированными боковыми цепями, позволяют манипулировать и регулировать скорость высвобождения лекарства в зависимости от вида лекарства, которое нужно ввести, места доставки, цели доставки и/или терапевтических требований индивидуального пациента. Новые мономеры, пригодные для получения матриксных систем доставки лекарства с регулируемой диффузией, представляют собой полидиметилсилоксаны с метакрилатными группами на концах, содержащие, по меньшей мере, одну перфторированную боковую цепь. Перфторированная боковая цепь содержит концевую -CF2-H группу. Функциональная группа -CF2-Н в боковой цепи чрезвычайно неустойчива в матриксных системах доставки лекарства с регулируемой диффузией. Молекулярный вес и степень замещения фтором могут меняться, и фторсилоксановые мономеры могут быть сополимеризованы с большим количеством мономеров. Такая вариабельность позволяет получить материалы, обладающие разнообразными желательными физическими характеристиками или свойствами. В то же время конечная группа -CF2-H обеспечивает улучшенную растворимость. Улучшенная растворимость обеспечивает повышенную совместимость фторсилоксанового мономера с разнообразными гидрофильными мономерами и лекарствами, содержащими группы, связывающие водород.
Соответственно, цель данного изобретения состоит в создании биосовместимых матриксных систем доставки лекарств с регулируемой диффузией.
Другая цель данного изобретения заключается в создании матриксных систем доставки лекарств с регулируемой диффузией, которые позволяют регулировать скорость высвобождения лекарств.
Еще одна цель настоящего изобретения состоит в создании матриксных систем доставки лекарств с регулируемой диффузией, которые позволяют регулировать скорость высвобождения в зависимости от вида лекарства, которое нужно ввести.
Еще одна цель данного изобретения состоит в создании матриксных систем доставки лекарств с регулируемой диффузией, которые позволяют регулировать скорости высвобождения лекарств в зависимости от расположения места доставки в организме.
Другая цель данного изобретения состоит в создании матриксных систем доставки лекарств с регулируемой диффузией, которые позволяют регулировать скорости высвобождения лекарств в зависимости от цели введения лекарства.
Еще одна цель данного изобретения состоит в создании матриксных систем доставки лекарств с регулируемой диффузией, которые позволяют регулировать скорости высвобождения лекарств в зависимости от терапевтических требований индивидуального пациента.
Эти и другие цели и преимущества данного изобретения, некоторые из которых конкретно указаны, а другие не описаны, станут очевидными из нижеследующего описания и формулы изобретения.
Подробное описание изобретения
Данное изобретение относится к новым фторсилоксановым мономерам, пригодным для изготовления новых матриксных систем доставки лекарств с регулируемой диффузией. Такие матриксные системы доставки лекарств с регулируемой диффузией позволяют осуществлять и регулирование скоростей доставки лекарств, которые могут быть основаны на виде вводимого лекарства, месте доставки, цели доставки и/или терапевтических требованиях индивидуального пациента. Новые фторсилоксановые мономеры согласно данному изобретению представляют собой полидиметилсилоксаны с концевыми метакрилатными группами, содержащие, по меньшей мере, одну перфторированную боковую цепь. Перфторированная боковая цепь содержит концевую группу -CF2-H, которая является чрезвычайно неустойчивой. Фторсилоксановые мономеры согласно данному изобретению обычно имеют формулу 1

где R1 могут быть одинаковыми или разными, выбранными из группы, состоящей из C1-7алкилов, таких как, например, но не ограничиваясь этим, метил, пропил или бутил, предпочтительно метил для улучшения биосовместимости, и С6-10арилов, таких как, например, но не ограничиваясь этим, фенил; R2 представляет собой C1-7алкилен, такой, например, как, но не ограничиваясь этим, метилен, этилен или гептилен, но предпочтительно, пропилен; х - целое число, равное или большее 1 и менее 26; p и q могут быть одинаковыми или различными целыми числами, равными или более 1 и менее 100, и z обозначает целое число, равное или более 1 и менее 11.
Силоксановые мономеры с фторированными боковыми цепями согласно данному изобретению могут быть синтезированы, как показано на Схеме 1
Схема 1.
Синтез фторсилоксанов с концевыми метакрилатными группами.

Один или несколько силоксановых мономеров с фторированными боковыми цепями по изобретению, полученные, как описано выше, могут сочетаться с одним или более фармацевтически активными агентами и полимеризоваться и/или сополимеризоваться с другими мономерами. За счет регулирования концентрации гидрофобной основной силоксановой цепи, полярного конца -CF2-H и любого сомономера (сомономеров), если он используется, достигается конкретный гидрофобно/гидрофильный баланс характеристик или свойств.
Этим гидрофобно/гидрофильным балансом характеристик можно манипулировать для достижения желательной скорости высвобождения лекарства. Желательную скорость высвобождения лекарства можно определить, исходя из вида лекарства, которое нужно ввести, места доставки и/или терапевтических требований индивидуального пациента. Гидрофобно/гидрофильный баланс характеристик диктует растворимость лекарства и является основным фактором, регулирующим скорость высвобождения лекарства. В некоторых случаях полярный конец -CF2-H может использоваться для образования водородной связи с лекарствами, содержащими полярные группы, для снижения скорости высвобождения лекарства.
Фармацевтически активные агенты или лекарства, применяемые в матриксных системах доставки лекарств с регулируемой диффузией согласно изобретению, включают, например, не ограничиваясь этим, агенты для лечения глаукомы, такие, например, но не ограничиваясь этим, как бета-блокаторы тимололмалеат, батаксолол и метипранолол, митотики, такие, например, но не ограничиваясь этим, как пилокарпин, ацетилхолина хлорид, изофлуорофат, демакария бромид, эхотиофатйодид, фосфолинйодид, карбахол и физостигимин, эпинефрин и соли, такие, например, но не ограничиваясь этим, как допивефрина хлорид, дихлорфенамида ацетазоламид и метазоламид, агенты для лечения катаракты и диабетической ретинопатии, такие, например, но не ограничиваясь этим, как ингибиторы альдозоредуктазы толрестат, лизиноприл, эналаприл и статил, тиольные сшивающие агенты, противораковые агенты, такие, например, но не ограничиваясь этим, как ретиновая кислота, метотрексат, адриамицин, блеомицин, триамцинолин, митомицин, цисплатина, винкристин, винбластин, актиномицин-D, ара-с, бисантрен, активированный цитоксан, мелфалан, митрамицин, прокарбазин и тамоксифен, иммуномодуляторы, агенты, препятствующие свертыванию крови, такие, например, но не ограничиваясь этим, как активатор тканевого пазминогена, урокиназа и стрептокиназа, агенты, препятствующие повреждению тканей, такие, например, но не ограничиваясь этим, как дисмутаза надокиси, белки и нуклеиновые кислоты, такие, например, но не ограничиваясь этим, как моно- и поликлональные антитела, ферменты, белковые гормоны и гены, фрагменты генов и плазмиды, стероиды, в частности противовоспалительные или противофиброзные агенты, такие, например, но не ограничиваясь этим, как лотепреднол, этабонат, кортизон, гидрокортизон, преднизолон, преднизон, дексалитазон, прогестероноподобные соединения, медризон (HMS) и флуорметолон, нестероидные противовоспалительные агенты, такие, например, но не ограничиваясь этим, как трометамин кетролака, натриевая соль диклофенака, супрофен, антибиотики, такие, например, но не ограничиваясь этим, как лоридин (дефалоридин), хлорамфеникол, клиндамицин, амикацин, тобрамицин, метициллин, линкомицин, оксициллин, амфотерицин В, полимиксин В, семейство цефалоспоринов, ампициллин, бакитрацин, карбенициллин, цефалотин, колистин, эритромицин, стрептомицин, неомицин, сульфацетамид, ванкомицин, нитрат серебра, сульфизоксазола диоламин и тетрациклин, другие антипатогенные вещества, включая противовирусные агенты, такие, например, но не ограничиваясь этим, как гидроксуридин, трифлуороуридин, видарабин (арабинозид аденина), ацикловир (ациклогуанизин), пириметамин, трисульфапиримидин-2, клиндамицин, нистатин, флуцитозин, натамицин и миконазол, производные пиперазина, такие, например, но не ограничиваясь этим, как диэтилкарбамазин, агенты против паралича аккомодации и мидриатические средства, такие, например, но не ограничиваясь этим, как атропин, циклогель, скополамин, гоматропин и мидриацил.
Другие фармацевтические агенты или лекарства включают антихолинергетики, антикоагулянты, антифибринолитики, антигистаминные средства, противомалярийные средства, антитоксины, хелатирующие агенты, гормоны, иммуноподавляющие средства, тромболитики, витамины, соли, десенсибилизаторы, простагландины, аминокислоты, метаболиты и противоаллергенные средства.
Фармацевтические агенты или лекарства, представляющие особый интерес, включают гидрокортизон (5-20 мкг/л плазмы), гентамицин (6-10 мкг/мл сыворотки), 5-флуороурацил (˜30 мг/кг веса в сыворотке), сорбинил, интерлейкин-2, факан-а (а - компонент глютатиона), тиол-тиопронин, бендазак, ацетилсалициловую кислоту, трифтортимидин, интерферон (α, β, γ), иммуномодуляторы, такие, например, но не ограничиваясь этим, как лимфокилен и монокины и факторы роста.
Мономеры, пригодные для сополимеризации с силоксановыми мономерами, содержащими фторированную боковую цепь, и один или более фармацевтически активных агентов включают, не ограничиваясь этим, например, метилметакрилат, N,N-диметилакриламид, акриламид, N-метилакриламид, 2-гидроксиэтилметакрилат, гидроксиэтоксиэтилметакрилат, гидроксидиэтоксиэтилметакрилат, метоксиэтилметакрилат, метоксиэтоксиэтилметакрилат, метоксидиэтоксиэтилметакрилат, поли(этиленгликоль)метакрилат, метоксиполи(этиленгликоль)-метакрилат, метакриловую кислоту, метакрилат натрия, глицерилметакрилат, гидроксипропилметакрилат, N-винилпирролидон и гидроксибутилметакрилат. Предлагаемые матриксные системы доставки лекарств с регулируемой диффузией по изобретению, полученные с применением одного или более силоксановых мономеров с фторированными боковыми цепями, описаны более подробно в примерах, следующих ниже.
Пример 1: Синтез поли(25 мол.% метилсилоксана)-со-(75 мол.% диметилсилоксана) с концевыми метакрилатными группами (M2D75D25H).
В круглодонную колбу объемом 100 мл в атмосфере сухого азота добавляли D4 (371,9 г, 1,25М), D4H (100,4 г, 0,42М) и М2 (27,7 г, 0,7М). В качестве инициатора добавляли трифторметансульфокислоту. Реакционную смесь выдерживали 24 часа при энергичном перемешивании и при комнатной температуре. Затем добавляли бикарбонат натрия (10 г, 0,119М) и снова перемешивали реакционную смесь в течение 24 часов. Полученный раствор фильтровали через 0,3 мкм фильтр из Teflon™ (E.I. Du Font De Nemours and Co., Wilmington, Delaware). Отфильтрованный раствор выдерживали под вакуумом и помещали под вакуум (<0,1 мм Hg) при 50°С для удаления не прореагировавших циклических силиконов. Полученный силоксановый полимер с группами гидрида кремния представлял собой вязкую прозрачную жидкость. Выход 70%.
SEC: Mn=7500 Mw/Mn=2,2;1H-ЯМР (CDCl3, TMC, ч/млн.): 0,1 (s, 525H, Si-СН3), 0,5 (t, 4H, Si-CH2), 1,5-1,8 (m, 8Н, Si-CH2-


Пример 2: Синтез поли(25 мол.% (3-(2,2,3,3,4,4,5, 5-октафторпентокси)-пропилметилсилоксана)-со-(75 мол.% диметилсилоксана) с концевыми метакрилатными группами.
В круглодонную колбу объемом 500 мл, снабженную магнитной мешалкой и конденсатором для воды, добавляли M2D75D25H (15 г, 0,002М), аллилоксиоктафторпентин (27,2 г, 0,1М), комплекс тетраметилдисилоксан - платина (2,5 мл 10%-ного раствора в смеси ксилолов), 75 мл диоксана и 150 мл безводного тетрагидрофурана в атмосфере азота. Реакционную смесь нагревали до 75°С и осуществляли мониторинг реакции при помощи ИК и1H-ЯМР спектроскопии по потере гидрида кремния. Реакцию завершали через 4-5 часов отгонки с обратным холодильником. Полученный раствор помещали в роторный выпариватель для удаления тетрагидрофурана и диоксана. Полученный технический продукт разбавляли 300 мл 20%-ного раствора метиленхлорида в пентане и пропускали через 15 г колонку с силикагелем, используя в качестве элюента 50%-ный раствор метиленхлорида в пентане. Собранный раствор снова помещали в роторный выпариватель для удаления растворителя и полученное прозрачное масло помещали под вакуумом (<0,1 мм Hg) при 50°С на 4 часа. Полученный силоксан с боковыми октафторированными группами представлял собой вязкую прозрачную жидкость. Выход 65%.
SEC: Mn=18 000, Mw/Mn=2,3;1Н-ЯМР (CDCl3, TMC, ч/млн.): 0,1 (s, 525H, Si-СН3), 0,5 (t, 54H, Si-СН2-), 1,5-1,8 (m, 58Н, Si-CH2-


Пример 3: Отливка пленки.
Отливали пленку, используя 70 частей DP 100 полидиметилсилоксана с концевыми метакрилатными группами, содержащего 25 мол.% октафторпропил-окси цепей, 30 частей диметилакриламида, 0,5% Darocur™ 1173 (Ciba-Geigy, Basel, Switzerland) и 5 вес.% лекарственного вещества Флуохинолона ацетонид (FA). Отверждение проводили УФ-излучением в течение 2 часов. Пленку экстрагировали изопропанолом в течение 24 часов, сушили воздухом затем гидратировали в боратном буферном растворе. Полученная пленка характеризовалась модулем, равным 170 г/мм2, прочностью на разрыв 3 г/мм и содержанием воды, равным 30,0 вес.%.
Пример 4: Отливка пленки.
Отливали пленку, используя 30 частей DP 100 полидиметилсилоксана с концевыми метакрилатными группами, содержащего 25 мол.% боковых октафторпропилокси групп, 70 частей диметилакриламида, 0,5% Darocur™ 1173 и 5 вес.% лекарства FA. Отверждение осуществляли УФ-излучением в течение 2 часов. Пленку экстрагировали в изопропаноле в течение 24 часов, сушили в вакууме для удаления изопропанола.
Пример 5: Изготовление системы доставки лекарств с регулируемой диффузией.
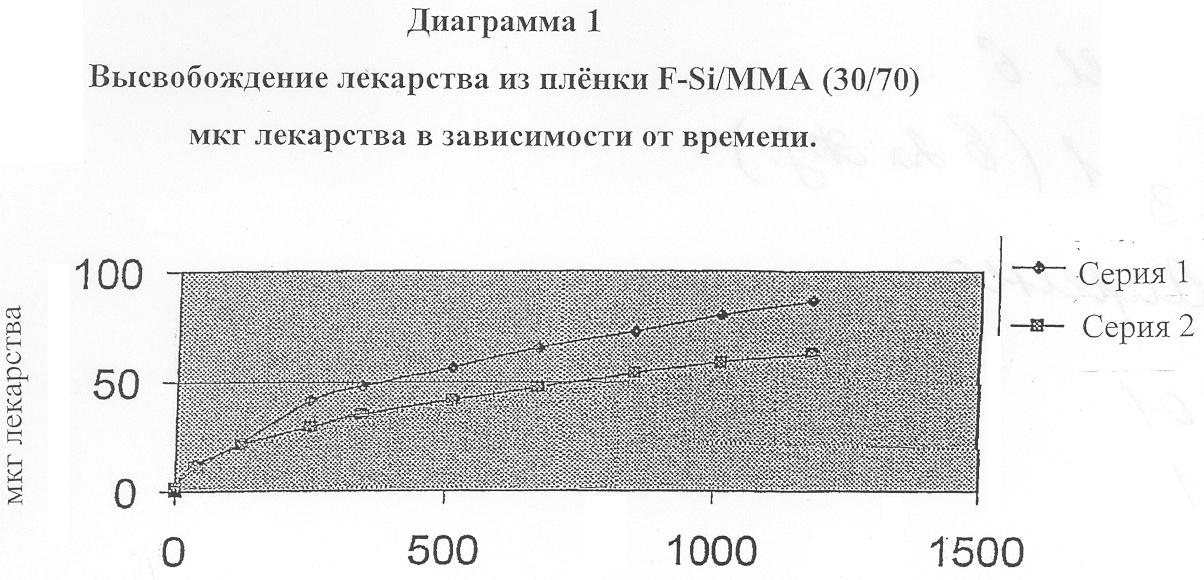
Готовили диск размером 10 мм из пленок, полученных в Примере 3 и 4, и устанавливали его в диффузионной ячейке Kontes в растворе ацетатного буфера с рН 4. Пленку, полученную в Примере 3, далее называли образцом 1, а пленку, полученную в Примере 4, - образцом 2. Скорость высвобождения лекарства осуществляли мониторингом с применением УФ-облучения при температуре 34°С. Лучшие результаты были получены для образца 2, состоящего из 30 частей фторсилоксана с концевыми метакрилатными группами (DP 100, 25 мол.% фторсодержащих боковых цепей), 70 частей метилметакрилата и 5% FA. В Таблице 1 и на чертеже приведены характеристики высвобождения для пленок серии 1 и серии 2, которые являются дубликатами образца 2, мониторинг был проведен в течение 1200 часов. Для каждой серии была установлена линейная зависимость нулевого порядка вскоре после начала высвобождения лекарства. При допущении, что эта линейная зависимость сохранена, должно установиться постоянное высвобождение лекарства через 800 часов (серия 1) и через 1000 часов (серия 2).
Матриксные системы доставки лекарства с регулируемой диффузией по изобретению могут быть любой формы и любого размера, подходящих для использования в той области, для которой они предназначены. Например, в случае применения в качестве внутренней стенки глазного имплантата матриксная система доставки лекарства с регулируемой диффузией имеет площадь, предпочтительно, не более 3 мм2. Способы изготовления предлагаемых матриксных систем доставки лекарства с регулируемой диффузией включают отливку формованием, экструзией и другими методами, известными специалистам. Полученные матриксные системы доставки лекарств с регулируемой диффузией упаковывают и стерилизуют методами, известными специалистам.
Матриксные системы доставки лекарств с регулируемой диффузией согласно изобретению могут быть использованы в самых различных терапевтических целях. В области офтальмологии предлагаемая матриксная система доставки лекарства с регулируемым высвобождением применяется, например, для имплантации во внутреннюю часть глаза. Однако матриксная система доставки лекарства с регулируемым высвобождением по изобретению может быть также использована и в других хирургических операциях, известных специалистам в области офтальмологии. Хотя в данном описании описаны определенные мономеры, сополимеры, матриксные системы доставки лекарства с регулируемой диффузией и способы их изготовления и применения, специалистам в данной области ясно, что, не выходя за рамки данного изобретения, можно осуществить его различные модификации. Данное изобретение не ограничивается конкретными мономерами, сополимерами и системами, описанными в данном описании, в той степени, в которой его объем определен формулой изобретения.
Реферат
Изобретение относится к сополимерам, используемым при изготовлении матриксных систем доставки лекарств с регулируемой диффузией. Описывается матриксная система доставки лекарства с регулируемой диффузией, содержащая силоксановый сополимер, содержащий фторированную боковую цепь, полученный сополимеризацией фторсилоксанового мономера, имеющего формулу

где переменные определены в формуле изобретения, и одного или более сополимеризуемых мономеров, и терапевтически эффективным количеством, по меньшей мере, одного фармацевтически активного агента, и способ ее получения. Благоприятные параметры растворимости фторированных боковых цепей сополимерной матриксной системы доставки лекарств с регулируемой диффузией позволяют манипулировать скоростями высвобождения лекарств в зависимости от конкретного терапевтического применения и конкретных потребностей пациента. 3 н. и 8 з.п. ф-лы, 1 ил., 1 табл.
Формула


Документы, цитированные в отчёте о поиске
Изделия для пролонгированного выделения одного или нескольких фармацевтически активных веществ

Комментарии