Бензойная кислота, производные бензойной кислоты и конъюгаты гетероарилкарбоновой кислоты с гидроморфоном, пролекарства, способы получения и их применение - RU2573388C2
Код документа: RU2573388C2
Чертежи




















Описание
РОДСТВЕННЫЕ ЗАЯВКИ
В данной заявке заявлен приоритет по предварительной заявке на патент США № 61/551,600, поданной 26 октября 2011, озаглавленной "Бензойная кислота, производные бензойной кислоты и конъюгаты гетероарилкарбоновой кислоты с гидроморфоном, их пролекарства, способы получения и применение", идентифицированной патентным реестром № 24553US01 в юридическом бюро McAndrews, Held and Malloy, Ltd., и по предварительной заявке на патент США № 61/657,201, поданной 8 июля 2012, озаглавленной "Бензойная кислота, производные бензойной кислоты и конъюгаты гетероарилкарбоновой кислоты с гидроморфоном, их пролекарства, способы получения и применение", идентифицированной патентным реестром № 24553US03 в юридическом бюро McAndrews, Held and Malloy, Ltd., описание которых включено сюда в качестве ссылки полностью.
ФИНАНСИРУЕМЫЕ ИЗ ФЕДЕРАЛЬНОГО БЮДЖЕТА ИССЛЕДОВАНИЯ И РАЗРАБОТКИ
[не применяется]
МИКРОФИША/АВТОРСКОЕ ПРАВО
[не применяется]
УРОВЕНЬ ТЕХНИКИ
Опиоиды являются высоко эффективными аналгетиками и их часто прописывают для лечения острой и хронической боли. Их также часто применяют в качестве противокашлевых средств. Опиоиды, однако, также вызывают эйфорию и/или "эффект склонности к лекарственному препарату" и могут вызвать сильную зависимость. В результате они часто вызывают зависимость с далеко идущими социальными и связанными со здоровьем последствиями.
Из-за присущей им тенденции к вызыванию зависимости, желательно, чтобы любые фармацевтические композиции, содержащие опиоидный агонист, были настолько резистентными к зависимости или сдерживающими зависимость, насколько это возможно на практике. Преступники часто делают попытки вдыхать, вводить инъекцией или другим образом незаконно использовать продукт для достижения более сильного или немедленного эффекта от опиоидного агониста.
Несмотря на то, что они могут вызывать привыкание и, потенциально, наркотическую зависимость, морфиноподобные лекарственные средства, особенно, кодеин, гидрокодон, гидроморфон и оксикодон обычно прописывают для лечения тяжелой, острой и хронической боли в течение десятилетий. В частности из-за того, что в настоящее время нет лучшей альтернативы для облегчения сильной боли, которая не поддается другим, менее сильным обезболивающим средствам, таким как нестероидные противовоспалительные лекарственные средства (НСПВЛС). В связи с этим существует необходимость в снижении потенциальной зависимости к опиоидным обезболивающим средствам. На сегодняшний день предпринималось несколько попыток, которые, к сожалению, не решили проблему.
Гидроморфон (4,5-α-эпокси-3-гидрокси-17-метилморфинан-6-он) является гидрированным кетоном морфина, который применяют в качестве опиоидного аналгетика центрального действия и противокашлевого средства. Гидроморфон является полусинтетическим наркотическим аналгетиком, получаемым из морфина, который обладает множеством действий, качественно похожих на действие морфина, и его применяют в медицине в качестве альтернативы морфину. Его в основном применяют для облегчения боли и в качестве наркотического противокашлевого средства в случаях сухого, вызывающего боль кашля. Гидроморфон взаимодействует преимущественно с опиоидными рецепторами в центральной нервной системе (ЦНС). Его обезболивающие свойства преимущественно основаны на агонистическом действии на μ-опиоидный рецептор. Гидроморфон также является частичным агонистом δ-опиоидного рецептора и агонистом κ-опиоидного рецептора. Дополнительно, гидроморфон обладает противокашлевыми свойствами, подавляющими кашлевой рефлекс в медуллярном кашлевом центре мозга.
Пациенты, принимающие опиоидные обезболивающие средства, такие как гидроморфон, для облегчения боли и/или кашля, могут непреднамеренно стать зависимыми от них. При развитии толерантности к опиоидам, более высокие количества лекарственного средства становятся необходимыми для облегчения симптомов и создания чувства состояния, изначально достигавшегося с предписанной дозой. Это ведет к увеличению дозы, которое, при отсутствии контроля, может быстро привести к возникновению зависимости. В некоторых случаях пациенты приобретают зависимость менее чем за тридцать дней.
Вызванная опиоидом констипация (ВОК) является частым побочным эффектом лечения боли опиоидами. Он возникает у приблизительно 40-90% пациентов, которые постоянно получают опиоидные лекарственные средства. Кроме того, пациенты, страдающие ВОК, могут стать резистентными к слабительным средствам. Хотя механизм еще до конца не понят, полагают, что связывание агонистов с периферийными μ-опиоидными рецепторами в желудочно-кишечном тракте (ЖКТ) является первопричиной ВОК. Активация этого опиоидного рецептора ухудшает координацию функции ЖКТ энтерической частью вегетативной нервной системы (ЭЧВНС), что снижает перистальтику кишечника через задержку времени прохождения фекалий при взаимодействии с нормальным тонусом и сокращаемостью толстого кишечника. В то время как сокращения кругового слоя мышечной оболочки усиливаются, вызывая не пропульсивное разминание и продвижение (застой) и повышенную абсорбцию жидкости, тонус продольных гладких мышц снижается, вызывая пониженную продвигающую вперед перистальтику и дополнительное время для обезвоживания фекалий. Более того, тонус анального сфинктера повышается, что еще больше затрудняет дефекацию. Клиническое проявление этих эффектов обычно выражается в виде симптомов тяжелого/сухого стула, натуживания, неполного опорожнения, вздутия и увеличения размеров живота.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В представленной методике применяется конъюгация опиоида гидроморфона с определенными арилкарбоновыми кислотами для снижения потенциальной передозировки или зависимости, которая достигается необходимостью выделения активного гидроморфона через ферментное или метаболическое расщепление конъюгата in vivo. Данная методика также представляет способы доставки гидроморфона в виде конъюгатов, которые высвобождают гидроморфон после перорального введения, одновременно являясь резистентными к привыканию при введении обходными путями, такими как внутривенная инъекция ("вкалывание") и интраназальное введение ("нюхание").
Преимущества определенных вариантов гидроморфоновых пролекарств в соответствии с данной методикой включают, но не ограничены ими, снижение потенциального привыкания, снижение или исключение вызванной опиоидом констипации (ВОК), снижение риска химического или физического манипулирования, дающего полную дозу выделяемого гидроморфона, снижение изменения концентрации в плазме у различных пациентов по сравнению с обычным гидроморфоном, улучшенные лекарственные формы вследствие модификации физических и химических свойств и улучшенный профиль побочных эффектов через пониженное превращение гидроморфонового пролекарства до нежелательного гидроморфон-3-глюкуронида.
В некоторых аспектах в данной методике представлены композиции для немедленного выделения конъюгированного гидроморфона, что позволяет доставку гидроморфона в кровеносную систему человека или животного терапевтически биоэквивалентным методом при пероральном введении. В по крайней мере одном аспекте, композиции/составы данной методики могут уменьшить обычные побочные эффекты, характерные для неконъюгированного гидроморфона и подобных соединений. Описанная методика в по крайней мере одном аспекте обеспечивает медленное/замедленное/контролируемое выделение композиции конъюгированного гидроморфона, которое обеспечивает медленную/замедленную/контролируемую доставку гидроморфона в кровеносную систему человека или животного с безопасным терапевтическим окном при, например, пероральном введении. По крайней мере некоторые композиции/составы данной методики могут снизить потенциал к привыканию/зависимости, характерный для неконъюгированного гидроморфона и подобных соединений.
В дополнительных аспектах в данной методике применяют конъюгацию природных не токсичных лигандов с гидроморфоном для создания нового класса пролекарств. Пролекарства в соответствии с данной методикой могут легко распознаваться метаболическими системами и гидролизуются с выделением активного опиоида контролируемым образом при пероральном введении. Другие пути введения являются для соединений в соответствии с данным изобретением не эффективными или менее эффективными, что позволяет предотвратить или снизить привыкание к лекарственному средству. Дополнительные способы привыкания к лекарственному средству также устраняются из-за резистентности к физическим изменениям и предотвращения или снижения эйфории при проглатывании высоких доз пролекарств в соответствии с данным изобретением. В зависимости от выбора лиганда, профили фармакокинетики (ФК) гидроморфона, высвобождаемого из пролекарств в соответствии с данным изобретением, могут быть изменены для оптимизации уровней в крови с течением времени для конкретных показаний и для улучшения профиля безопасности. Кроме того, при выборе подходящих лигандов пролекарства в соответствии с данным изобретением могут доставлять гидроморфон в системный кровоток без взаимодействия с опиоидными рецепторами в энтерической части вегетативной нервной системы, тем самым снижая или предотвращая вызванную опиоидом констипацию (ВОК).
В другом аспекте, в данной методике представлены арилкарбоновые кислоты, химически присоединенные к гидроморфону для получения пролекарств, которые могут выделять активный опиоид. Пролекарства в соответствии с данным изобретением не обладают значительным обезболивающим действием и при выборе подходящих лигандов значительно снижают количества гидроморфона, выделенные в системный кровоток при введении интраназально или внутривенно. Более того, наркотик не может быть "экстрагирован" из пролекарств в соответствии с данным изобретением простым физическим повреждением из-за природы ковалентной связи енольного эфира и/или фенольного эфира между гидроморфоном и арилкарбоновой кислотой. Такой класс соединений в соответствии с данным изобретением может быть менее привлекательным для потенциально наркозависимых людей, чем традиционные лекарственные формы, и могут иметь улучшенный профиль безопасности и пониженное количество побочных эффектов.
Кроме того, при выборе подходящих лигандов все или большинство неактивных пролекарств в соответствии с данным изобретением могут переносить проход через желудочно-кишечный тракт (ЖКТ) до тех пор, пока они не абсорбируются, тем самым предотвращая взаимодействие гидроморфона с опиоидными рецепторами в энтерической части вегетативной нервной системы. Такое отсутствие связывания с периферийными опиоидными рецепторами может значительно понизить или даже предотвратить вызванную опиоидом констипацию.
В по крайней мере одном аспекте, в данном изобретении представлена по крайней мере одна композиция пролекарства, содержащая по крайней мере один конъюгат, где конъюгат содержит по крайней мере один гидроморфон, и по крайней мере одну арилкарбоновую кислоту.
В другом аспекте, в данном изобретении представлена по крайней мере одна композиция пролекарства гидроморфона, содержащая арилкарбоновую кислоту, химически связанную с гидроморфоном взаимодействием группы карбоновой кислоты арилкарбоновой кислоты с C-6 енольным таутомером гидроморфона.
В другом аспекте, в данном изобретении представлено по крайней мере одно пролекарство, содержащее по крайней мере один гидроморфон, химически связанный с по крайней мере одной арилкарбоновой кислотой через взаимодействие группы карбоновой кислоты арилкарбоновой кислоты с C-3 гидроксилом гидроморфона.
В другом аспекте, в данном изобретении представлено пролекарство, содержащее по крайней мере один гидроморфон, химически связанный с по крайней мере одной арилкарбоновой кислотой через взаимодействие группы карбоновой кислоты арилкарбоновой кислоты с C-6 енольным таутомером гидроморфона и взаимодействие по крайней мере одной арилкарбоновой кислоты с C-3 гидроксилом гидроморфона.
В других аспектах, в данном изобретении представлено по крайней мере одно пролекарство с по крайней мере одной арилкарбоновой кислотой, содержащее карбоксильную группу, присоединенную непосредственно к по крайней мере одной арильной группе.
В другом аспекте, в данном изобретении представлено по крайней мере одно пролекарство с по крайней мере одним гидроморфоном, химически присоединенным к по крайней мере одному бензоату общей формулы I:

где R1, R2 и R3 независимо выбирают из группы, включающей водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат.
В по крайней мере одном аспекте данного изобретения представлено пролекарство гидроморфона с по крайней мере одной арилкарбоновой кислотой, содержащее карбоксильную группу, которая соединена одним карбоновым мостиком с арильной группой.
В другом аспекте, в данном изобретении представлено по крайней мере одно пролекарство гидроморфона, химически присоединенное к по крайней мере одному фенилацетату следующей общей формулы II:

где R1, R2, R3 и R4 независимо выбирают из группы, включающей водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат.
В других аспектах, в данном изобретении представлены пролекарства гидроморфона, содержащие по крайней мере одну арилкарбоновую кислоту, содержащую карбоксильную группу, которая соединена двумя углеродными мостиками с арильной группой.
В дополнительных аспектах в данном изобретении представлены композиции пролекарств гидроморфона, содержащие бензилацетаты и циннаматы, имеющие следующую общую формулу III или IV или их сочетание:

где R1, R2, R3 и R4 независимо выбирают из группы, включающей водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат.
В других аспектах, пролекарства гидроморфона в соответствии с данным изобретением включают по крайней мере одну арилкарбоновую кислоту, содержащую карбоксильную группу, присоединенную к арильной группе алкильной цепью.
В других аспектах, пролекарства гидроморфона в соответствии с данным изобретением включают по крайней мере одну арилкарбоновую кислоту, содержащую карбоксильную группу, присоединенную к арильной группе алкенильной цепью.
В дополнительных аспектах, пролекарства гидроморфона в соответствии с данным изобретением содержат по крайней мере одну арилкарбоновую кислоту, которая содержит углеродную цепь между арильным кольцом и карбоксильную группу с одной или более боковыми цепями.
В дополнительных аспектах, пролекарства гидроморфона в соответствии с данным изобретением содержат по крайней мере одну арилкарбоновую кислоту, которая содержит одну или более функциональных групп в дополнение к по крайней мере одной карбоксильной группе.
В других аспектах, пролекарства гидроморфона в соответствии с данным изобретением содержат по крайней мере одну арилкарбоновую кислоту, которая содержит по крайней мере одну гетероарилкарбоновую кислоту.
В дополнительных аспектах, в данном изобретении представлены композиции пролекарств гидроморфона, содержащие гетероарилкарбоновую кислоту следующей общей формулы V, VI, VII, VIII, IX, X, XI, XII или XIII или их сочетание:

где R1, R2 и R3 независимо выбирают из группы, включающей водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат.
В других аспектах, в данном изобретении представлено по крайней мере одно пролекарство гидроморфона, которое содержит арилкарбоновую кислоту, содержащую шестичленное кольцо.
В других аспектах, в данном изобретении представлено по крайней мере одно пролекарство гидроморфона, которое содержит арилкарбоновую кислоту, содержащую только одну свободную группу карбоновой кислоты.
В дополнительных аспектах, в данном изобретении представлено по крайней мере одно пролекарство гидроморфона, которое содержит арилкарбоновую кислоту, содержащую от 1 до 4 фенильных заместителей.
В определенных аспектах, в данном изобретении представлен по крайней мере один конъюгат пролекарства гидроморфона, которое является нейтральным пролекарством.
В определенных аспектах, в данном изобретении представлен по крайней мере один конъюгат пролекарства гидроморфона, который является свободной кислотой.
В определенных аспектах, в данном изобретении представлен по крайней мере один конъюгат пролекарства гидроморфона, который является свободным основанием.
В дополнительных аспектах, в данном изобретении представлен по крайней мере один конъюгат пролекарства гидроморфона, который является фармацевтически приемлемой анионной или катионной солевой формой или смесью солей.
В определенных аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением разрушаются in vivo, выделяя активный гидроморфон и арилкарбоновую кислоту или ее производные или метаболиты.
В определенных аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением вводят перорально и они гидролизуются in vivo, выделяя гидроморфон из пролекарства.
В других аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением демонстрируют отсутствие или незначительное фармакологическое действие при введении.
В других аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением таким образом выделяют гидроморфон, который аналогичен свободному или немодифицированному гидроморфону при введении в эквимолярных дозах.
В дополнительных аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением контролируют и ограничивают выделение гидроморфона в системный кровоток, если пролекарство вводят путями, отличными от перорального.
В определенных аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением выделяют гидроморфон контролируемым или замедленным образом при введении.
В других аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением демонстрируют отсутствие или пониженные побочные эффекты по сравнению с немодифицированным гидроморфоном при введении в эквимолярных дозах.
В дополнительных аспектах, введение композиций пролекарства гидроморфона в соответствии с данным изобретением дает концентрации гидроморфона в плазме или крови, которые значительно понижены по сравнению с немодифицированным гидроморфоном при введении в эквимолярных дозах при внутривенном или интраназальном введении.
В других аспектах, введение композиций пролекарства гидроморфона в соответствии с данным изобретением не вызывает или вызывает пониженную эйфорию или наркотическое действие по сравнению с немодифицированным гидроморфоном при интраназальном или внутривенном введении в эквимолярных дозах.
В некоторых аспектах введение композиций пролекарства гидроморфона в соответствии с данным изобретением не вызывает быстрый пик концентрации гидроморфона (Cmax) в крови или плазме при пероральном введении.
В других аспектах, введение композиций пролекарства гидроморфона в соответствии с данным изобретением дает замедленный Tmax по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах.
В дополнительных аспектах, введение композиций пролекарства гидроморфона в соответствии с данным изобретением дает более низкое значение Cmax по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах.
В других аспектах, физические манипуляции с композициями пролекарства гидроморфона в соответствии с данным изобретением не вызывают высвобождения свободного гидроморфона.
В других аспектах, композиций пролекарства гидроморфона в соответствии с данным изобретением демонстрируют резистентность к определенным химическим манипуляциям, предназначенным для высвобождения свободного гидроморфона.
В других аспектах, введение композиций пролекарства гидроморфона в соответствии с данным изобретением не вызывает или не дает незначительную активность на μ-опиоидных рецепторах.
В других аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением не подвержены или ограниченно подвержены ферментному гидролизу до абсорбции в кишечнике.
В других аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением демонстрируют пониженное превращение в гидроморфон-3-глюкуронид (H3G) по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах.
В других аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением предотвращают или снижают вызванную опиоидом констипацию (ВОК) по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах.
В других аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением содержат дополнительные активные фармацевтические ингредиенты (АФИ), включая, например, ибупрофен, ацетаминофен или аспирин.
В определенных аспектах, композициями пролекарств гидроморфона в соответствии с данным изобретением могут быть 3-аспирин-гидроморфон, 3,6-ди-аспирин-гидроморфон, 6-o-салицилат-гидроморфон, 3-циннамат-гидроморфон, 6-напроксен-гидроморфон, 3-изониацин-гидроморфон, 3-п-салициловый-гидроморфон, 3-фенамат-гидроморфон, 3-бензоат-гидроморфон и 3,6-ди-бензоат-гидроморфон.
В других аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением имеют пероральную лекарственную форму. В некоторых аспектах, пероральные лекарственные формы в соответствии с данным изобретением являются твердыми лекарственными формами. В дополнительных аспектах, наполнителями в соответствии с данным изобретением являются антиадгезивы, связующие агенты, покрытия, разрыхлители, наполнители, вкусовые добавки, красители, глиданты, смазывающие агенты, консерванты, сорбенты и подсластители.
В дополнительных аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением представлены в виде таблеток, капсул, мягких желатиновых капсул, капсул с модифицированным высвобождением, таблеток с замедленным высвобождением, капсул с контролируемым высвобождением, суппозиториев, порошков для инъекций, пероральных жидкостей, сиропов от кашля, чрескожной пленки, пероральной тонкой пленки, суспензии или инъекций.
В определенных аспектах, композиции пролекарств гидроморфона в соответствии с данным изобретением представлены с эффективностью пероральной лекарственной формы, которая эквимолярна от около 0,1 мг до около 200 мг немодифицированного гидроморфона.
В других аспектах, в данном изобретении представлен способ лечения пациента, которому необходимо обезболивающее действие, введением количества по крайней мере одной композиции пролекарства гидроморфона в соответствии с данным изобретением, которое терапевтически эквивалентно эффективному количеству неконъюгированного гидроморфона.
В других аспектах, в данном изобретении представлен способ синтеза композиций пролекарства гидроморфона в соответствии с данным изобретением.
В других аспектах, в данном изобретении представлен способ лечения пациента, нуждающегося в обезболивающем действии, путем введения количества 3-аспирин-гидроморфона, 3,6-ди-аспирин-гидроморфона, 6-салицилат-гидроморфона, 3-циннамат-гидроморфона или 3-бензоат-гидроморфона, которое терапевтически эквивалентно эффективному количеству неконъюгированного гидроморфона.
В дополнительных аспектах, в данном изобретении представлен фармацевтический набор, содержащий определенное количество отдельных доз, содержащих количество по крайней мере одного конъюгата, которое терапевтически эквивалентно эффективному количеству неконъюгированного гидроморфона, где по крайней мере один конъюгат содержит по крайней мере один гидроморфон и по крайней мере одну арилкарбоновую кислоту.
КРАТКОЕ ОПИСАНИЕ НЕСКОЛЬКИХ ВИДОВ ЧЕРТЕЖЕЙ
Фигура 1. Пример химических структур некоторых гидроксибензоатов для применения в получении композиций пролекарства гидроморфона в соответствии с данным изобретением.
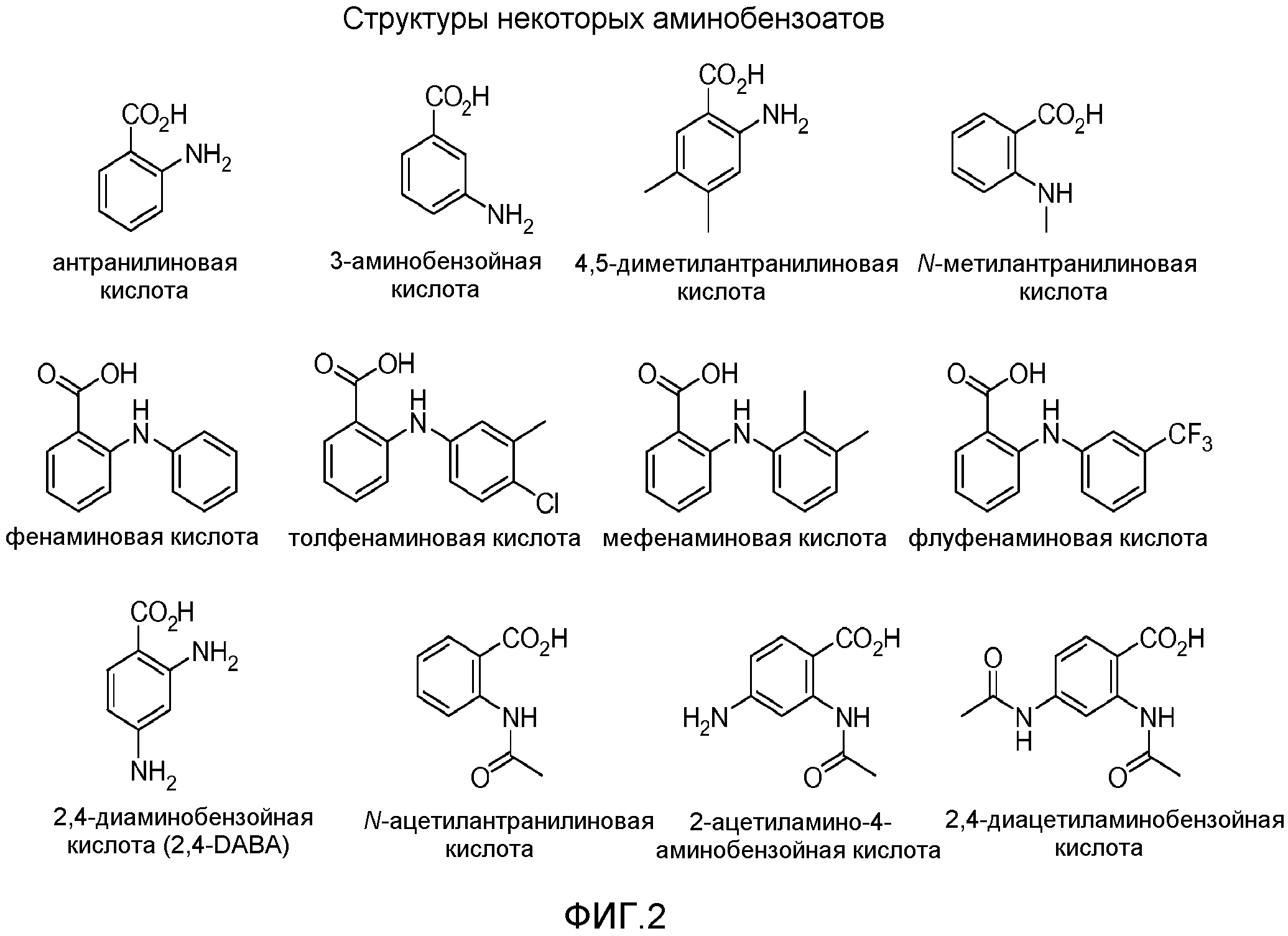
Фигура 2. Пример химических структур некоторых аминобензоатов для применения в получении композиций пролекарства гидроморфона в соответствии с данным изобретением.
Фигура 3. Пример химических структур некоторых аминогидроксибензоатов для применения в получении композиций пролекарства гидроморфона в соответствии с данным изобретением.
Фигура 4. Пример химических структур некоторых гетероарилкарбоновых кислот для применения в получении композиций пролекарства гидроморфона в соответствии с данным изобретением.
Фигура 5. Пример химических структур некоторых фенилацетатов для применения в получении композиций пролекарства гидроморфона в соответствии с данным изобретением.
Фигура 6. Пример химических структур некоторых бензилацетатов для применения в получении композиций пролекарства гидроморфона в соответствии с данным изобретением.
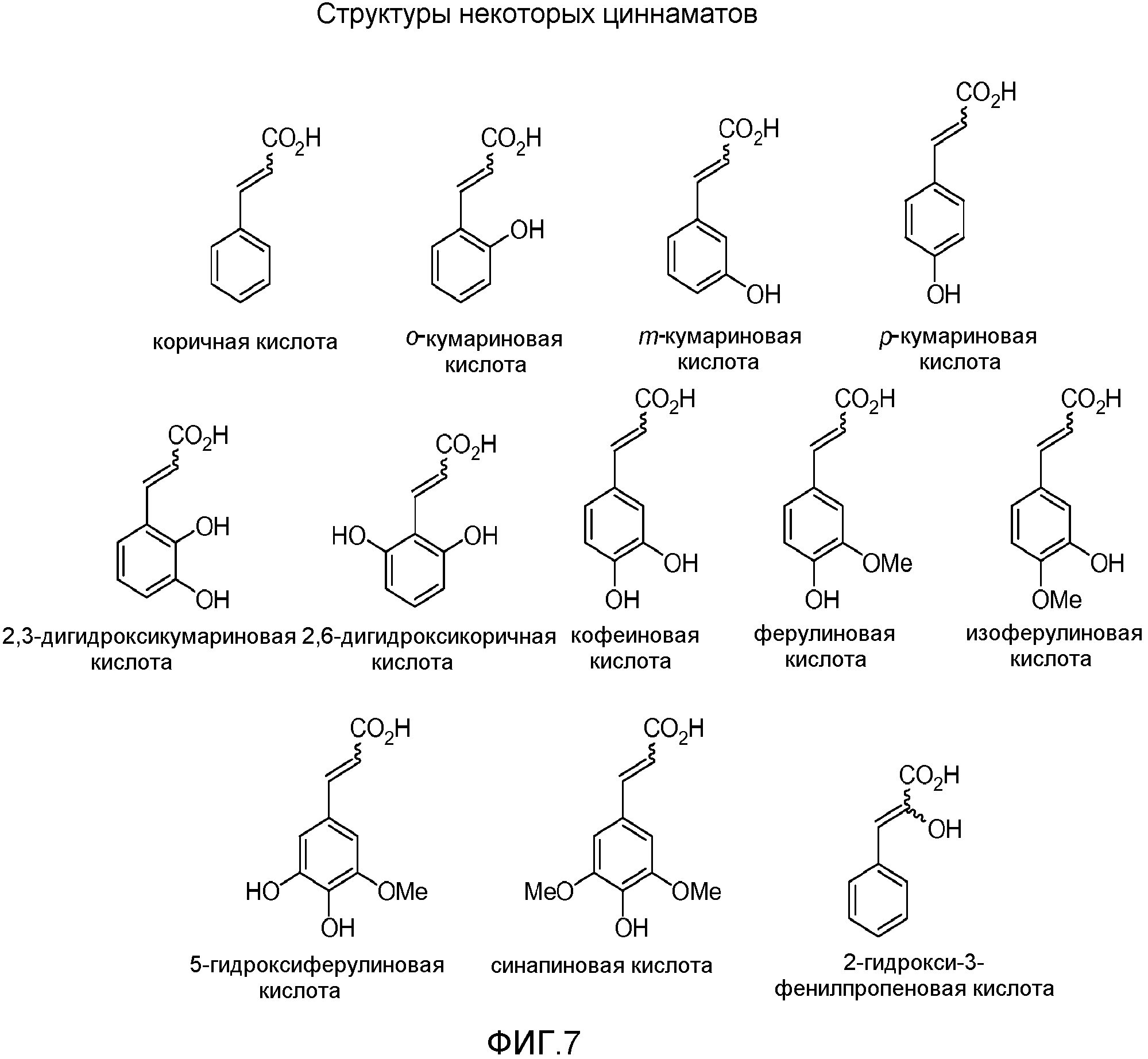
Фигура 7. Пример химических структур некоторых циннаматов для применения в получении композиций пролекарства гидроморфона в соответствии с данным изобретением.
Фигура 8. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 3-аспирин-ГМ, 3,6-ди-аспирин-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 9. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 6-o-салицилат-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 10. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 3-циннамат-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 11. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 6-напроксен-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 12. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 3-изониацин-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 13. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 3-п-салицилат-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 14. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 3-фенамат-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 15. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 3-бензоат-ГМ, 3,6-ди-бензоат-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 16. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 3,6-ди-аспирин-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
Фигура 17. Фармакокинетический профиль выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально дозы 3,6-ди-аспирин-ГМ и ГМ, эквимолярные 2,0 мг/кг гидроморфона.
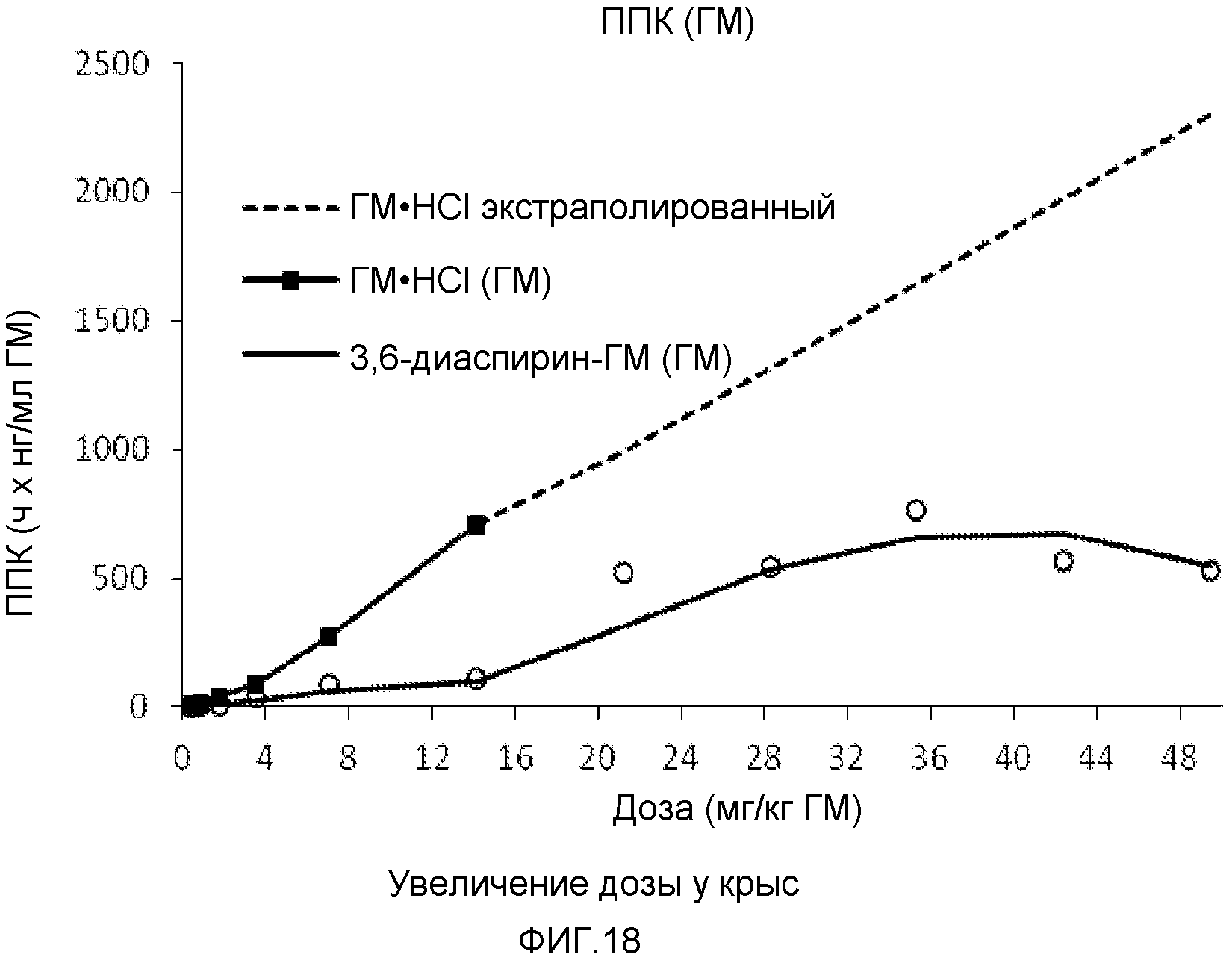
Фигура 18. Площадь под кривой (ППК) выделенного гидроморфона (ГМ) в плазме крыс, которым дают перорально повышенные эквимолярные дозы ГМ и 3,6-ди-аспирин-ГМ.
Фигура 19. Площадь под кривой (ППК) и пиковые концентрации в плазме (Cmax) в плазме крыс, которым дают перорально эквимолярные дозы ГМ, неизмененный 3,6-ди-аспирин-ГМ и продукты гидролитического распада 3,6-ди-аспирин-ГМ.
Фигура 20. Расстояние прохождения в желудочно-кишечном тракте (ЖКТ), полученное в подтвержденном исследовании сократительной способности у крыс, которым дают перорально эквимолярные дозы ГМ и 3,6-ди-аспирин-ГМ.
Фигура 21. Примеры схем синтеза для синтеза некоторых пролекарств гидроморфона в соответствии с данным изобретением.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Композиция
В данном изобретении представлены композиции, содержащие арилкарбоновые кислоты, которые химически конъюгированы с гидроморфоном (4,5-α-эпокси-3-гидрокси-17-метилморфинан-6-оном) с получением новых пролекарств и композиций гидроморфона. В некоторых вариантах химическая связь между этими двумя группами может быть установлена взаимодействием функциональной группы карбоновой кислоты арилкарбоновой кислоты с одной из следующих функциональных групп гидроморфона:
(a) C-6 енольным таутомером гидроморфона
(b) C-3 гидроксилом гидроморфона,
(c) или обоих C-3 гидроксила и C-6 енольного таутомера гидроморфона.
Применение "опиоида" включает любое лекарственное средство, которое активирует опиоидные рецепторы, найденные в мозге, спинном мозге и кишечнике. Существует четыре широких класса опиоидов: природные алкалоиды опия, такие как морфин (прототипный опиоид) кодеин и тебаин; эндогенные опиоидные пептиды, такие как эндорфины; полусинтетические, такие как героин, оксикодон и гидрокодон, которые получают модификацией природных алкалоидов опия (опиатов) и которые имеют похожие структуры; и чистые синтетические, такие как фентанил и метадон, которые не получают из опия, и которые могут иметь сильно отличающиеся от алкалоидов опия химические структуры. Дополнительные примеры опиоидов включают гидроморфон, оксиморфон, метадон, леворфанол, дигидрокодеин, меперидин, дифеноксилат, суфентанил, алфентанил, пропоксифен, пентазоцин, налбуфин, буторфанол, бупренорфин, мептазинол, дезоцин и их фармацевтически приемлемые соли.
Применение "терапевтического эквивалента" означает лекарственные продукты, которые являются фармацевтическими эквивалентами и имеют такое же клиническое действие при введении пациентам в условиях, указанных на этикетке.
Применение "биоэквивалента" означает фармацевтический эквивалент или фармацевтические альтернативные продукты, которые демонстрируют сравнимую биодоступность (т.е. системные концентрации гидроморфона в плазме) при изучении в похожих экспериментальных условиях.
Применение "гидроморфона" включает полусинтетическое наркотическое обезболивающее средство, которое обладает множественным действием, качественно подобным действию морфина и применяется в медицине как альтернатива морфину. Его в основном применяют для облегчения боли и в качестве наркотического противокашлевого средства в случаях сухого болезненного кашля. Торговые наименования включают Dilaudid®, Exalgo®, Hydrostat® и Palladone® (замедленное высвобождение). Другие фармацевтически приемлемые соли гидроморфона также включены в определенные варианты данного изобретения. Химической структурой гидроморфона является:

Арилкарбоновые кислоты в соответствии с данным изобретением могут быть сгруппированы в различные категории и субкатегории. В определенных вариантах карбоксильная группа может быть присоединена непосредственно к ароматическому кольцу или отделена алкильной или алкенильной цепью. В других вариантах данного изобретения, длина цепи алкильной или алкенильной группы не должна превышать два неразветвленных углерода, но не ограничена по количеству атомов потенциальных боковых цепей или дополнительных функциональных групп.
В других вариантах, данное изобретение включает только углеродные арильные группы и арильные группы с гетероатомами (гетероарил). Арильная или гетероарильная группа определенных вариантов в соответствии с данным изобретением, которая связана непосредственно или через алкильную или алкенильную группу с карбоксильной функциональной группой, может быть 6-членным кольцом и содержать ноль, один или более одного гетероатома. Дополнительные замещенные или незамещенные ароматические или алифатические кольца могут быть конденсированы с этим 6-членным арилом или гетероарилом в определенных вариантах данного изобретения.
В некоторых вариантах данного изобретения, арилкарбоновые кислоты могут иметь одну или более групп свободной карбоновой кислоты, и общее количество фенильных заместителей на 6-членном кольце может быть четыре или менее.
В зависимости от отдельных арилкарбоновых кислот, которые связаны с гидроморфоном, пролекарства в соответствии с данным изобретением могут быть нейтральными, свободной кислотой, свободным основанием или различными фармацевтически приемлемыми анионными или катионными солями или смесями солей в любом соотношении положительных и отрицательных компонентов.
В определенных вариантах, соли пролекарств в соответствии с данным изобретением включают, но не ограничены ими: ацетат, l-аспартат, безилат, бикарбонат, карбонат, d-камзилат, l-камзилат, цитрат, эдизилат, формиат, фумарат, глюконат, гидробромид/бромид, гидрохлорид/хлорид, d-лактат, l-лактат, d,l-лактат, d,l-малат, l-малат, d-малат, мезилат, памоат, фосфат, сукцинат, сульфат, бисульфат, d-тартрат, l-тартрат, d,l-тартрат, мезо-тартрат, бензоат, глуцептат, d-глюкуронат, гибензат, изетионат, малонат, метилсульфат, 2-напсилат, никотинат, нитрат, оротат, стеарат, тозилат, тиоцианат, ацефиллинат, ацетурат, аминосалицилат, аскорбат, борат, бутират, камфорат, камфокарбонат, деканоат, гексаноат, холат, ципионат, дихлорацетат, эдентат, этилсульфат, фурат, фузидат, галактарат (мукат), галактуронат, галлат, гентизат, глутамат, глутарат, глицерофосфат, гептаноат (энантат), гидроксибензоат, гиппурат, фенилпропионат, йодид, ксинафоат, лактобионат, лаурат, малеат, миндалят, метансульфонат, миристат, нападизилат, олеат, оксалат, пальмитат, пикрат, пивалат, пропионат, пирофосфат, салицилат, салицилсульфат, сульфосалицилат, таннат, терефталат, тиосалицилат, триброфенат, валерат, вальпроат, адипат, 4-ацетамидобензоат, камзилат, октаноат, эстолат, эзилат, гликолят, тиоцианат, ундециленат, натрий, калий, кальций, магний, цинк, алюминий, литий, холинат, лизиний, аммоний и трометамин.
Пролекарства определенных вариантов данного изобретения созданы так, чтобы разлагаться in vivo либо ферментами, либо другим способом с выделением активного гидроморфона и соответствующей арилкарбоновой кислоты(кислот) или их метаболитов. Арилкарбоновые кислоты в соответствии с данным изобретением должны быть не токсичными при данных уровнях дозирования и, предпочтительно, известными лекарственными средствами, натуральными продуктами, метаболитами или ОПКБ (общепризнанными как безопасные) соединениями (например, консервантами, красителями, вкусовыми добавками и т.д.) или их не токсичными миметиками.
В некоторых вариантах, арилкарбоновые кислоты в соответствии с данным изобретением содержат карбоксильную группу, которая присоединена непосредственно к арильной группе. Эти арилкарбоновые кислоты могут быть разделены на две субкатегории: бензоаты и гетероарилкарбоновые кислоты.
Бензоаты
Бензоаты определенных вариантов данного изобретения включают аминобензоаты (например, аналоги антранилиновой кислоты, такие как фенаматы) и гидроксибензоаты (например, аналоги салициловой кислоты). Общая химическая структура бензоатов в соответствии с данным изобретением представлена следующей общей формулой I:

где R1, R2 и R3 независимо выбирают из группы, включающей водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат.
Бензоаты широко распространены в природе в виде натуральных продуктов и метаболитов. Множественные аналоги бензойной кислоты также применяют в пищевой и фармацевтической промышленности. Некоторые из наиболее многочисленных бензоатов являются производными с гидроксильными или аминогруппами или их сочетанием. Гидроксильные и амино функциональные группы могут присутствовать в свободной форме или с другими химическими группами на концах. В определенных вариантах данного изобретения другими химическими группами предпочтительно являются, но не ограничены ими, метильная или ацетильная группы. В некоторых вариантах данного изобретения фенильное кольцо может иметь дополнительные заместители.
Некоторые примеры гидроксибензоатов в соответствии с данным изобретением включают, но не ограничены ими, бензойную кислоту, салициловую кислоту, ацетилсалициловую кислоту (аспирин), 3-гидроксибензойную кислоту, 4-гидроксибензойную кислоту, 6-метилсалициловую кислоту, o,m,p-крезотиновую кислоту, анакардиновую кислоту, 4,5-диметилсалициловую кислоту, o,m,p-тимотиновую кислоту, дифлузинал, o,m,p-анизиновую кислоту, 2,3-дигидроксибензойную кислоту (2,3-ДГБ), α,β,γ-резорциловую кислоту, протокатеховую кислоту, гентизиновую кислоту, пиперониловую кислоту, 3-метоксисалициловую кислоту, 4-метоксисалициловую кислоту, 5-метоксисалициловую кислоту, 6-метоксисалициловую кислоту, 3-гидрокси-2-метоксибензойную кислоту, 4-гидрокси-2-метоксибензойную кислоту, 5-гидрокси-2-метоксибензойную кислоту, ванилиновую кислоту, изованилиновую кислоту, 5-гидрокси-3-метоксибензойную кислоту, 2,3-диметоксибензойную кислоту, 2,4-диметоксибензойную кислоту, 2,5-диметоксибензойную кислоту, 2,6-диметоксибензойную кислоту, вератровую кислоту (3,4-диметоксибензойную кислоту), 3,5-диметоксибензойную кислоту, галлиевую кислоту, 2,3,4-тригидроксибензойную кислоту, 2,3,6-тригидроксибензойную кислоту, 2,4,5-тригидроксибензойную кислоту, 3-O-метилгаллиевую кислоту (3-OMGA), 4-O-метилгаллиевую кислоту (4-OMGA), 3,4-O-диметилгаллиевую кислоту, сиреневую кислоту и 3,4,5-триметоксибензойную кислоту.
Некоторые примеры аминобензоатов в соответствии с данным изобретением включают, но не ограничены ими, антранилиновую кислоту, 3-аминобензойную кислоту, 4,5-диметилантранилиновую кислоту, N-метилантранилиновую кислоту, N-ацетилантранилиновую кислоту, фенаминовые кислоты (например, толфенаминовую кислоту, мефенаминовую кислоту, флуфенаминовую кислоту), 2,4-диаминобензойную кислоту (2,4-DABA), 2-ацетиламино-4-аминобензойную кислоту, 4-ацетиламино-2-аминобензойную кислоту и 2,4-диацетиламинобензойную кислоту.
Некоторые примеры аминогидроксибензоатов в соответствии с данным изобретением включают, но не ограничены ими, 4-аминосалициловую кислоту, 3-гидроксиантранилиновую кислоту и 3-метоксиантранилиновую кислоту.
Гетероарилкарбоновые кислоты
Общие структуры некоторых гетероарилкарбоновых кислот в соответствии с данным изобретением представлены следующими общими формулами V, VI, VII, VIII, IX, X, XI, XII или XIII:


где R1, R2 и R3 такие, как определены выше.
Подходящие примеры гетероарилкарбоновых кислот в соответствии с данным изобретением включают производные пиридина, некоторые из которых вовлечены в метаболизм никотината и триптофана. В этих соединениях по крайней мере один атом углерода фенильного кольца замещен атомом азота. Кроме карбоксильной группы, данный ряд соединений в соответствии с данным изобретением может иметь дополнительные заместители, предпочтительно, но не ограничиваясь ими, гидроксильные группы.
Некоторые примеры гетероарилкарбоновых кислот в соответствии с данным изобретением включают, но не ограничены ими, никотиновую кислоту (ниацин), изоникотиновую кислоту, пиколиновую кислоту, 3-гидроксипиколиновую кислоту, 6-гидроксиникотиновую кислоту, цитразиновую кислоту, 2,6-дигидроксиникотиновую кислоту, кинуреновую кислоту, ксантуреновую кислоту, 6-гидроксикинуреновую кислоту, 8-метоксикинуреновую кислоту, 7,8-дигидроксикинуреновую кислоту и 7,8-дигидро-7,8-дигидроксикинуреновую кислоту.
Фенилацетаты
В некоторых вариантах данного изобретения арилкарбоновые кислоты в соответствии с данным изобретением включают карбоксильную группу, которая отделена одним атомом углерода от арильной части. Эти арилкарбоновые кислоты включают разветвленные фенилпропионовые кислоты (т.е., 2-метил-2-фенилацетаты) или другие производные фенилацетата (Фигура 4). Общая структура по крайней мере одного фенилацетата в соответствии с данным изобретением представлена следующей общей формулой II:
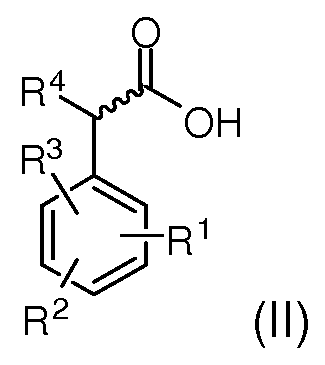
где R1, R2, R3 и R4 такие, как определены выше.
Фенилуксусные кислоты охватывают различные подвиды природных продуктов, метаболитов и фармацевтических препаратов. Одним из таких фармацевтически важных подвидов являются "профены", тип НСПВП и производных определенных фенилпропионовых кислот (например, аналоги 2-метил-2-фенилуксусной кислоты). Некоторые другие фенилацетаты имеют центральные функции в метаболизме фенилаланина и тирозина.
Некоторые примеры фенилацетатов в соответствии с данным изобретением включают, но не ограничены ими, фенилуксусную кислоту (гидратроповую кислоту), 2-гидроксифенилуксусную кислоту, 3-гидроксифенилуксусную кислоту, 4-гидроксифенилуксусную кислоту, гомопротокатехиновую кислоту, гомогентизиновую кислоту, 2,6-дигидроксифенилуксусную кислоту, гомованилиновую кислоту, гомоизованилиновую кислоту, гомовератриновую кислоту, атроповую кислоту, d,l-троповую кислоту, диклофенак, d,l-миндальную кислоту, 3,4-дигидрокси-d,l-миндальную кислоту, ванилил-d,l-миндальную кислоту, изованилил-d,l-миндальную кислоту, ибупрофен, фенопрофен, карпрофен, флурбипрофен, кетопрофен и напроксен.
Бензилацетаты
В дополнительных вариантах, арилкарбоновые кислоты в соответствии с данным изобретением содержат карбоксильную группу, которая отделена двумя атомами углерода от арильной части. Эти арилкарбоновые кислоты включают бензилацетаты и их замещенные производные, и аналоги циннаминовой кислоты (Фигура 5). Оба класса соединений широко распространены в природе в форме натуральных продуктов или метаболитов (например, метаболизм фенилаланина). Общие структуры некоторых бензилацетатов и циннаматов в соответствии с данным изобретением представлены следующими общими формулами (III) и (IV):


где R1, R2, R3 и R4 такие, как определены выше.
Бензилуксусные кислоты определены этиленовой группой между карбоксильной функциональной группой и фенильным кольцом. И алкильная цепь и арильная часть могут иметь заместители, предпочтительно, гидроксильные группы. Некоторые соединения этого класса могут быть найдены при метаболизме фенилаланина.
Некоторые примеры бензилацетатов в соответствии с данным изобретением включают, но не ограничены ими, бензилуксусную кислоту, мелилотовую кислоту, 3-гидроксифенилпропановую кислоту, 4-гидроксифенилпропановую кислоту, 2,3-дигидроксифенилпропановую кислоту, d,l-фенилмолочную кислоту, o,m,p-гидрокси-d,l-фенилмолочную кислоту, фенилпировиноградную кислоту.
Циннаматы
Коричные кислоты (3-фенилакриловые кислоты) включают ненасыщенные аналоги бензилуксусных кислот. Циннаматы существуют в двух изомерных формах: цис (Z) и транс (E). Изомеры циннамата определенных вариантов в соответствии с данным изобретением предпочтительно имеют, но не ограничены ей, транс конфигурацию. Так же как и бензилацетаты, производные коричной кислоты могут быть замещены на алкенильную или арильную часть молекулы. Предпочтительные заместители некоторых вариантов в соответствии с данным изобретением включают гидроксильную и метоксигруппы. Считается, что определенные циннаматы играют ключевую роль в метаболизме фенилаланина.
Некоторые примеры циннаматов в соответствии с данным изобретением включают, но не ограничены ими, коричную кислоту, o,m,p-кумариновую кислоту, 2,3-дигидроксикоричную кислоту, 2,6-дигидроксикоричную кислоту, кофеиновую кислоту, ферулиновую кислоту, изоферулиновую кислоту, 5-гидроксиферулиновую кислоту, синаповую кислоту, 2-гидрокси-3-фенилпропеновую кислоту.
Физиологические преимущества
В определенных вариантах, пролекарства гидроморфона и композиции в соответствии с данным изобретением могут вводиться перорально и, при введении, выделять активный гидроморфон после гидролиза в теле. Так как арилкарбоновые кислоты в соответствии с данным изобретением являются природными метаболитами или их миметиками или фармацевтически активными соединениями, эти пролекарства могут легко распознаваться физиологическими системами, что вызывает гидролиз и выделение гидроморфона. Пролекарства в соответствии с данным изобретением, в определенных вариантах, являются либо не активными, либо имеют ограниченную фармакологическую активность и, следовательно, могут проходить метаболический путь, который отличается от исходного лекарственного средства. При выборе подходящих арилкарбоновых кислот ("лигандов") в соответствии с данным изобретением выделение гидроморфона в системный кровоток может контролироваться, даже если пролекарство вводят путями, отличными от перорального.
В по крайней мере одном варианте пролекарства гидроморфона в соответствии с данным изобретением выделяют гидроморфон так же, как свободный или немодифицированный гидроморфон. В другом варианте, пролекарства гидроморфона в соответствии с данным изобретением выделяют гидроморфон в контролируемой или замедленной форме. Такое контролируемое выделение может потенциально облегчать определенные побочные эффекты и улучшать профиль безопасности исходного лекарственного средства. Побочные эффекты, которые облегчаются в соответствии с данным изобретением, могут включать головокружение, дурноту, сонливость, тошноту, рвоту, застой желудка, боль в желудке, высыпания, затрудненное мочеиспускание, затрудненное дыхание и потерю сознания.
Кроме того, гидроморфон и другие опиоиды также сильно вызывают привыкание и предрасположены к возникновению зависимости. Злоупотребление рекреационными опиоидами является общей проблемой и обычно начинается с пероральных доз, принимаемых с целью достижения эйфории ("кайф", "балдеж"). В течение времени наркозависимый часто повышает пероральные дозы для достижения более сильного "балдежа" или для компенсации повышенной устойчивости к опиоиду. Быстрый метаболизм и короткая длительность действия гидроморфона обесславливает его предрасположенность к возникновению зависимости. Такое поведение может усиливаться и вызывает переход к другим способам введения, таким как интраназальное ("нюхание") и внутривенное ("вкалывание").
В некоторых вариантах данного изобретения, гидроморфон, который конъюгирован с подходящим лигандом арилкарбоновой кислоты, не демонстрирует быстрых пиков в уровне крови при пероральном введении, которые необходимы потенциальному наркозависимому. В определенных вариантах, пролекарства в соответствии с данным изобретением демонстрируют замедленный Tmax и низкие значения Cmax по сравнению с эквимолярной дозой исходного лекарственного средства. Поэтому чувство "кайфа" теряется при пероральном приеме пролекарств в соответствии с данным изобретением даже в более высоких дозах, при одновременности облегчения боли.
В других вариантах, конъюгаты гидроморфона в соответствии с данным изобретением не гидролизуются эффективно при введении не пероральным путем. В результате пролекарства в соответствии с данным изобретением не создают высокие концентрации в крови или плазме выделенного гидроморфона при инъекции или вдыхании по сравнению со свободным гидроморфоном, вводимым этими путями. Более того, так как лиганды в определенных вариантах данного изобретения связаны ковалентно с гидроморфоном, опиоид не высвобождается любыми физическими манипуляциями. Это является преимуществом пролекарств в соответствии с данным изобретением по сравнению с другими составами гидроморфона, которые выделяют свободный гидроморфон с помощью физических манипуляций (например, размалывание, раскрашивание и т.д.).
В по крайней мере одном варианте пролекарства в соответствии с данным изобретением не оказывают или оказывают незначительное действие на μ-опиоидные рецепторы. В другом варианте пролекарства в соответствии с данным изобретением не подвергаются ферментному гидролизу до тех пор, пока они не адсорбируются в кишечнике. Не привязываясь к определенной теории полагают, что активное пролекарство гидроморфона в соответствии с данным изобретением эффективно "маскируется" присоединенной арилкарбоновой кислотой и может обходить периферийные μ-опиоидные рецепторы, не влияя на ЖКНС, тем самым снижая или предотвращая ВОК.
Гидроморфон в значительной степени метаболизируется в печени до гидроморфон-3-глюкуронида (H3G). Хотя H3G не обладает обезболивающим действием, он может вызывать нейровозбуждение, возбуждение, спутанность сознания и галлюцинации. Если H3G может преодолевать гематоэнцефалический барьер (ГЭБ), он может аккумулироваться в центральной нервной системе (ЦНС) и вызывать миоклонию, аллодинию и пароксизм, которые наблюдают у пациентов, которым хронически вводят высокие дозы гидроморфона. Этот эффект может быть усилен у пациентов с почечной дисфункцией.
В по крайней мере одном другом варианте, пролекарства в соответствии с данным изобретением вызывают пониженное превращение гидроморфона в H3G после перорального введения по сравнению с неконъюгированным гидроморфоном. Не привязываясь к определенной теории, полагают, что они могут иметь улучшенный профиль побочных эффектов, особенно улучшать нейровозбужденное поведение по сравнению со свободным гидроморфоном.
Композиции
Композиции и пролекарства в соответствии с данным изобретением могут быть в виде пероральных лекарственных форм. Такие лекарственные формы включают, но не ограничены ими, таблетки, капсулы, мягкие желатиновые капсулы, каплеты, лепешки, пастилки, порошок, суспензию, сироп, раствор или пероральные тонкие пленки (ПТП). Предпочтительными формами для перорального введения являются капсулы, таблетки, растворы и ПТП.
Композиции и пролекарства в соответствии с данным изобретением также могут иметь твердые лекарственные формы, которые включают наполнители. Наполнители в соответствии с данным изобретением включают, но не ограничены ими, антиадгезивы, связующие агенты, покрытия, разрыхлители, наполнители, вкусовые добавки и красители, глиданты, смазывающие агенты, консерванты, сорбенты и подсластители.
Пероральные композиции в соответствии с данным изобретением также могут быть включены в раствор или суспензию в водной жидкости или не водной жидкости. Композицией может быть эмульсия, такая как масло в воде жидкая эмульсия и вода в масле жидкая эмульсия. Масла могут вводиться добавлением очищенных и стерилизованных жидкостей в готовую энтеральную формулу, которую затем помещают в зонд для искусственного кормления пациента, который не способен глотать.
Мягкие таблетки или мягкие желатиновые капсулы могут быть получены, например, диспергированием композиции в подходящем сосуде (обычно применяют растительные масла) для получения высоковязкой смеси. Эту смесь затем инкапсулируют в пленку на основе желатина с применением методики и оборудования, известного в области производства мягкого желатина. Полученные таким образом лекарственные формы затем сушат до постоянного веса.
Жевательные таблетки, например, могут быть получены смешиванием композиций с наполнителями, составленными так, чтобы получить относительно мягкие, ароматизированные, таблетированные лекарственные формы, которые предназначены для разжевывания, а не для проглатывания. Можно применять обычное оборудование и методики для получения таблеток, например, непосредственное прессование и гранулирование, т.е. брикетирование, перед прессованием. Специалисты, занимающиеся производством твердых лекарственных форм, осведомлены в применяемых методиках и оборудовании, и жевательные лекарственные формы являются широко применяемыми лекарственными формами в фармацевтической промышленности.
Таблетки в пленочной оболочке, например, могут быть получены нанесением покрытия на таблетки с применением методик, таких как методы нанесения покрытий с применением вращающейся чаши или методов воздушной суспензии для нанесения слоя контактирующей пленки на таблетку.
Прессованные таблетки, например, могут быть получены смешиванием композиции с наполнителями, которые придают связующие свойства или разрыхляющие свойства. Смесь либо непосредственно прессуют с применением методов и оборудования, известных специалистам в данной области техники. Полученные прессованные таблетированные лекарственные формы затем упаковывают в соответствии с потребностями рынка, например, в отдельные упаковки, рулоны, объемные бутылки, блистеры и т.д.
Данная методика также включает применение биологически приемлемых носителей, которые могут быть получены из множества материалов. Не ограничиваясь ими, такие материалы включают разбавители, связующие агенты и адгезивы, смазывающие агенты, пластификаторы, разрыхлители, красители, объемообразующие препараты, вкусовые добавки, подсластители и различные материалы, такие как буферы и адсорбенты для получения конкретной лекарственной композиции.
Связующие агенты в соответствии с данным изобретением могут быть выбраны из широкого спектра материалов, таких как гидроксипропилметилцеллюлоза, этилцеллюлоза или другие подходящие производные целлюлозы, повидон, сополимеры акриловой и метакриловой кислоты, фармацевтическая глазурь, камеди, производные молока, такие как сыворотка, крахмалы и производные, а также другие обычные связующие агенты, известные специалистам в данной области техники. Типовые не ограничивающие растворители включают воду, этанол, изопропиловый спирт, метиленхлорид или их смеси и сочетания. Примеры не ограничивающих объемообразующих веществ включают сахар, лактозу, желатин, крахмал и двуокись кремния.
Должно быть понятно, что при добавлении к указанным выше ингредиентами композиции в соответствии с данным изобретением могут включать другие подходящие агенты, такие как вкусовые добавки, консерванты и антиоксиданты. Такие антиоксиданты могут быть приемлемы в качестве продуктов питания и могут включать витамин E, каротин, БГТ и другие антиоксиданты.
Другие соединения, которые могут быть добавлены примешиванием, включают, например, медицински инертные ингредиенты, например, твердые и жидкие разбавители, такие как лактоза, декстроза, сахароза, целлюлоза, крахмал или фосфат кальция для таблеток или капсул, оливковое масло или этилолеат для мягких капсул и воды или растительное масло для суспензий или эмульсий; смазывающие агенты, такие как двуокись кремния, тальк, стеариновая кислота, стеарат магния или кальция и/или полиэтиленгликоли; желатинирующие агенты, такие как коллоидные глины; загущающие агенты, такие как трагакант или альгинат натрия, связующие агенты, такие как крахмалы, аравийские камеди, желатин, метилцеллюлоза, карбоксиметилцеллюлоза или поливиниопирролидон; разрыхляющие агенты, такие как крахмал, альгиновая кислота, альгинаты и гликолят крахмала натрия; шипучие смеси; красители; подсластители; смачивающие агенты, такие как лецитин, полисорбаты или лаурилсульфаты; и другие терапевтически приемлемые дополнительные ингредиенты, такие как увлажнители, консерванты, буферы и антиоксиданты, которые являются известными добавками для таких композиций.
Для перорального введения тонкоизмельченные порошки или гранулы, содержащие разбавляющие, диспергирующие и/или поверхностно-активные агенты, могут быть представлены в сухой форме, в воде или в сиропе, в капсулах или саше в сухом состоянии, в неводной суспензии, в которую могут быть включены суспендирующие агенты, или в суспензии в воде или сиропе. Если желательно, могут быть добавлены вкусовые добавки, консерванты, суспендирующие агенты, загустители или эмульгирующие агенты.
Жидкие дисперсии для перорального введения могут включать сиропы, эмульсии или суспензии. Сиропы могут содержать, в качестве носителя, например, сахарозу или сахарозу с глицерином и/или маннитом, и/или сорбитом. В частности, сироп для пациентов с диабетом может содержать в качестве носителей только те продукты, например сорбит, которые не метаболизируются до глюкозы или которые метаболизируются только в очень небольших количествах до глюкозы. Суспензии и эмульсии могут содержать носитель, например, натуральную камедь, агар, альгинат натрия, пектин, метилцеллюлозу, карбоксиметилцеллюлозу или поливиниловый спирт.
Одобренные в настоящее время композиции гидроморфона включают таблетки, капсулы, капсулы с модифицированным высвобождением, таблетки с замедленным высвобождением, капсулы с контролируемым высвобождением, суппозитории, порошки для инъекций, пероральные жидкости, сироп от кашля и формы для инъекций. Конъюгированный гидроморфон в соответствии с данным изобретением в определенных вариантах может быть составлен в любые из указанных, одобренных в настоящее время, композиций неконъюгированного гидроморфона.
Другие, одобренные в настоящее время, композиции гидроморфона включают сочетание терапии гидроморфоном и одним или более другими не наркотическими активными ингредиентами в зависимости от предназначенного применения. Примеры таких активных лекарственных препаратов включают, но не ограничены ими, ацетаминофен, ибупрофен и аспирин. Конъюгированный гидроморфон в соответствии с данным изобретением может быть составлен с одним или более сочетаниями этих и других активных веществ или в виде отдельного активного ингредиента без любых других активных веществ.
Способы применения
Композиции конъюгата или пролекарств в соответствии с данным изобретением могут применяться в способах лечения пациента, страдающего заболеванием, расстройством или состоянием, требующим или опосредованным связыванием или ингибирующим связыванием опиоида с опиоидными рецепторами пациента. Лечение включает пероральное введение пациенту по крайней мере одного конъюгата гидроморфона, как описано в соответствии с данным изобретением, в количестве, терапевтически эквивалентном эффективному количеству неконъюгированного гидроморфона. Конъюгат может демонстрировать пониженные пиковые концентрации в плазме (Cmax) и низкую площадь под кривой (ППК) выделенного гидроморфона при введении через не пероральные пути, такие как интраназальный и внутривенный, по сравнению с эквивалентным молярным количеством неконъюгированного гидроморфона. В некоторых аспектах пероральное введение по крайней мере одного конъюгата может обеспечить замедленную скорость выделения гидроморфона в течение времени и терапевтически биоэквивалентную ППК с незначительным или отсутствием пика в Cmax или эквивалентного значения Cmax по сравнению с другими формами с контролируемым высвобождением гидроморфона (например, Exalgo®). В других вариантах по крайней мере один конъюгат может демонстрировать меньшую вариабельность в концентрациях гидроморфона в плазме после перорального введения по сравнению с неконъюгированным гидроморфоном.
В других вариантах по крайней мере представлен один конъюгат в количестве, достаточном для получения терапевтически биоэквивалентной ППК (площади под кривой) гидроморфона по сравнению с молярным эквивалентным количеством неконъюгированного гидроморфона. В других вариантах представлен конъюгат в количестве, достаточном для получения терапевтически биоэквивалентной ППК гидроморфона по сравнению с молярным эквивалентным количеством неконъюгированного гидроморфона, но имеющий более низкое значение Cmax (пиковую концентрацию) гидроморфона в плазме или не обеспечивает эквивалентное значение Cmax в плазме. В некоторых аспектах представлен конъюгат в количестве, достаточном для получения терапевтически эквивалентного значения Cmax гидроморфона по сравнению с молярным эквивалентным количеством неконъюгированного гидроморфона. В других вариантах по крайней мере представлен один конъюгат в количестве, достаточном для получения повышенной ППК или повышенного значения Cmax гидроморфона, или обоих, по сравнению с молярным эквивалентным количеством неконъюгированного гидроморфона.
В других аспектах представлен по крайней мере один конъюгат в количестве, терапевтически эквивалентном эффективному количеству неконъюгированного гидроморфона, но снижает или предотвращает вызванную опиоидом констипацию (ВОК). В некоторых вариантах по крайней мере представлен один конъюгат в количестве, терапевтически эквивалентом эффективному количеству неконъюгированного гидроморфона, но снижающий или предотвращающий нейровозбудительную токсичность, вызванную гидроморфон-3-глюкуронидом.
Подходящие заболевания, расстройства или состояния, которые можно лечить пролекарствами или композициями в соответствии с данным изобретением, включают наркотическую или лекарственную зависимость, острую или хроническую боль и тяжелый кашель.
Дозы конъюгатов в соответствии с данным изобретением зависят от их молекулярной массы и соответствующего массового процента гидроморфона как части целого конъюгата, и поэтому могут быть выше, чем дозы свободного гидроморфона.
Пероральная доза для взрослого человека, в пересчете на гидрохлорид гидроморфона, составляет от 2 мг до 16 мг на дозу для композиций с немедленным высвобождением, и от 8 мг до 64 мг на дозу для композиций с замедленным высвобождением. Педиатрическая пероральная доза составляет от 0,03 мг/кг/дозу до 0,08 мг/кг/дозу для детей и подростков с массой тела менее 50 кг и от 1 мг до 2 мг на дозу для детей и подростков с массой тела более 50 кг. Педиатрические пероральные дозы для подавления кашля варьируются от 0,5 мг до 1 мг на дозу. Дозы должны быть оттитрованы до подходящего обезболивающего действия при минимизации побочных эффектов. Дозы для пролекарств в соответствии с данным изобретением могут быть выше, в зависимости от их молекулярной массы и соответствующей массовой доли гидроморфона в конъюгате. Пересчет дозы с гидрохлорида гидроморфона в пролекарство гидроморфона может быть осуществлен с применением следующей формулы:
ГМ = гидроморфон
HCl = гидрохлорид
ММ = молекулярная масса
fBA = поправочный коэффициент, рассчитанный для разностей в биодоступности между немодифицированным гидроморфоном и пролекарствами в соответствии с данным изобретением. Этот поправочный коэффициент определен для каждого пролекарства в соответствии с данным изобретением.
Подходящие дозы конъюгированного гидроморфона в соответствии с данным изобретением включают, но не ограничены ими, композиции, содержащие от около 0,1 мг или выше, альтернативно, от около 0,5 мг или выше, альтернативно, от около 2,5 мг или выше, альтернативно, от около 5,0 мг или выше, альтернативно, от около 7,5 мг или выше, альтернативно, от около 10 мг или выше, альтернативно, от около 20 мг или выше, альтернативно, от около 30 мг или выше, альтернативно, от около 40 мг или выше, альтернативно, от около 50 мг или выше, альтернативно, от около 60 мг или выше, альтернативно, от около 70 мг или выше, альтернативно, от около 80 мг или выше, альтернативно, от около 90 мг или выше, альтернативно, от около 100 мг или выше, альтернативно, от около 150 мг или выше, альтернативно, от около 200 мг или выше, и включают любые дополнительные приращения, например, 0,1, 0,2, 0,25, 0,3, 0,4, 0,5, 0,6, 0,7, 0,75, 0,8, 0,9 или 1,0 мг и их различные множители (например, ×1, ×2, ×2,5, ×5, ×10, ×100, и т.д.).
В другом аспекте, количество на лекарственную форму основано на содержании свободного или неконъюгированного гидроморфона в конъюгате гидроморфона.
Данная технология также включает лекарственные композиции, включающие одобренные в настоящее время композиции гидроморфона, где доза может быть рассчитана с применением указанной выше формулы, определенной через количество гидроморфона. В данном изобретении представлены лекарственные формы, составленные в виде монотерапии или комбинированной терапии с другими активными фармацевтическими ингредиентами (АФИ).
Пролекарства в соответствии с данным изобретением могут вводиться для облегчения боли или подавления кашля или для лечения любого состояния, которое может потребовать блокирования опиоидных рецепторов.
Конъюгаты в соответствии с данным изобретением могут снижать побочные эффекты опиоидных обезболивающих средств, включая пониженные или ингибированные констипационные эффекты.
Общие методы синтеза
В данном изобретении также представлен способ синтеза для получения конъюгированного гидроморфона в соответствии с данным изобретением. В определенных вариантах, синтез пролекарств в соответствии с данным изобретением включает стадии:
Конъюгаты с фенольным сложным эфиром (3-лиганд-ГМ):
1. Защита лиганда, при необходимости.
2. Активация группы карбоновой кислоты лиганда, при необходимости.
3. Добавление активированного лиганда к гидроморфону или наоборот в присутствии основания.
4. Удаление защитной группы(групп) лиганда, если применимо.
Конъюгаты с енольным сложным эфиром (6-лиганд-ГМ):
1. Защита лиганда, при необходимости.
2. Активация группы карбоновой кислоты лиганда, при необходимости.
3. Защита фенольной (3-OH) гидроксильной группы гидроморфона, при необходимости.
4. Добавление активированного лиганда к гидроморфону или наоборот в присутствии основания.
5. Удаление защитной группы(групп) лиганда и/или гидроморфона, если применяется.
Диконъюгаты фенольного сложного эфира/енольного сложного эфира (3,6-ди-лиганд-ГМ):
1. Защита лиганда, при необходимости.
2. Активация группы карбоновой кислоты лиганда, при необходимости.
3. Добавление активированного лиганда к гидроморфону или наоборот в присутствии основания.
4. Удаление защитной группы(групп) лиганда, если применимо.
Если арилкарбоновая кислота содержит любые дополнительные реакционноспособные функциональные группы, которые могут вмешиваться в сочетание с гидроморфоном, может быть необходимым сначала присоединять одну или более защитных групп. Могут применяться любые подходящие защитные группы, в зависимости от типа функциональной группы и условий реакции. Некоторые примеры защитных групп включают: ацетил (Ac), β-метоксиэтоксиметиловый эфир (МЭМ), метоксиметиловый эфир (МОМ), п-метоксибензиловый эфир (ПМБ), триметилсилил (ТМС), трет-бутилдиметилсилил (ТБДМС), триизопропилсилил (ТИПС), карбобензилокси (Cbz), п-метоксибензилкарбонил (Moz), трет-бутилоксикарбонил (Boc), 9-флуоренилметилоксикарбонил (Fmoc), бензил (Bn), п-метоксибензил (MPM), тозил (Ts). Также может применяться временное образование ацеталей или кеталей из функциональных групп карбонила.
Может быть необходимым активировать группу карбоновой кислоты лигандов для того, чтобы взаимодействовать с гидроморфоном и образовывать приемлемые количества конъюгатов. Такая активация может проводиться множеством методов с применением различных сочетающих агентов, известных специалисту в данной области техники. Примеры таких сочетающих агентов включают: N,N-дициклогксилкарбодиимид (ДЦК), N-(3-диметиламинопропил)-N'-этилкарбодиимид (EDCI), N,N'-диизопропилкарбодиимид (ДИК), 1,1'-карбонилдиимидазол (КДИ) или другие карбодиимиды; гексафторфосфат (бензотриазол-1-илокси)трис(диметиламино)фосфония (BOP), гексафторфосфат бромтрипирролидинофосфония (PyBroP), гексафторфосфат (бензотриазол-1-илокси)трипирролидинофосфония (PyBOP) или другие реагенты на основе фосфония; гексафторфосфат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HBTU), тетрафторборат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (TBTU), гексафторфосфат фтор-N,N,N',N'-тетраметилформамидиния (TFFH), тетрафторборат N,N,N',N'-тетраметил-O-(N-сукцинимидил)урония (TSTU) или другие реагенты на основе аминия. Арилкарбоновая кислота также может быть превращена в подходящий ацилгалогенид, ацилазид или смешанный ангидрид.
Основание может потребоваться на любой стадии в схеме синтеза конъюгата арилкарбоновой кислоты с гидроморфоном. Подходящие основания включают, но не ограничены ими: 4-метилморфолин (NMM), 4-(диметиламино)пиридин (DMAP), N,N-диизоопропилэтиламин, бис(триметилсилил)амид лития, диизопропиламид лития (LDA), трет-бутоксид любого щелочного металла (например, трет-бутоксид калия), любой гидрид щелочного металла (например, гидрид натрия), алкоксид любого щелочного металла (например, метоксид натрия), триэтиламин или любой другой третичный амин.
Подходящие растворители, которые могут применяться для любой реакции в схеме синтеза конъюгата арилкарбоновой кислоты с гидроморфоном, включают, но не ограничены ими: ацетон, ацетонитрил, бутанол, хлороформ, дихлометан, диметилформамид (ДМФ), диметилсульфоксид (ДМСО), диоксан, этанол, этилацетат, диэтиловый эфир, гептан, гексан, метанол, метил-трет-бутиловый эфир (МТБЭ), изопропанол, изопропилацетат, диизопропиловый эфир, тетрагидрофуран, толуол, ксилол или воду.
Фармацевтические наборы
В данном изобретении также представлены фармацевтические наборы для лечения или профилактики симптомов отмены лекарственного средства или боли у пациента. Пациентом может быть человек или животное. Подходящие пациенты включают детей, пожилых людей и обычных пациентов. Набор содержит определенное количество отдельных доз в упаковке, содержащей фармацевтически эффективное количество по крайней мере одного конъюгата гидроморфона в соответствии с данным изобретением. Набор также может включать инструкции по применению набора. Определенное количество отдельных доз может содержать от около 1 до около 100 отдельных доз, альтернативно, от около 1 до около 60 отдельных доз, альтернативно, от около 10 до около 30 отдельных доз, включая около 1, около 2, около 5, около 10, около 15, около 20, около 25, около 30, около 35, около 40, около 45, около 50, около 55, около 60, около 70, около 80, около 100, и включают любые их дополнительные приращения, например, 1, 2, 5, 10 и их множители (например, ×1, ×2, ×2,5, ×5, ×10, ×100, и т.д.).
Описанное изобретение и его преимущества будут лучше понятны из представленных ниже примеров. Эти примеры представлены для описания конкретных вариантов данного изобретения. Данные конкретные примеры не предназначены для ограничения объема и сути данного изобретения. Специалист в данной области техники поймет, что полный объем данного изобретения охватывает объект, определенный формулой изобретения, прилагаемой к данному описанию, и любые изменения, модификации или эквиваленты этой формулы.
ПРИМЕРЫ
Пример 1: Анализ пероральной фармакокинетики
Определенные конъюгаты пролекарств в соответствии с данным изобретением дозируют в виде пероральных растворов крысам и сравнивают с эквимолярным раствором гидрохлорида гидроморфона. Пероральные исследования проводят в дозах, эквимолярных 2,0 мг/кг гидроморфона. Выделение гидроморфона из пролекарств варьируется в зависимости от лиганда, присоединенного к гидроморфону. Воздействие гидроморфона, выделенного из пролекарств в представленных примерах варьируется от 45% ППК до 113% ППК, %-Cmax от 37% до 185% и %-Tmax от 13% до 200% по сравнению с неконъюгированным гидрохлоридом гидроморфона. Кривые ФК профиля представлены на фигурах 8-15 и параметры ФК суммированы в таблице 1 ниже.
Концентрации гидроморфона в плазме, вызванные 3-циннамат-ГМ, 3-п-салицилат-ГМ, 3-бензоат-ГМ и 3,6-дибензоат-ГМ, были ниже во все интервалы времени по сравнению с неконъюгированным гидроморфоном. Значение Cmax гидроморфона, выделенного из 6-напроксен-ГМ, было таким же, как пиковая концентрация в плазме неконъюгированного гидроморфона, но общее воздействие после перорального введения этого конъюгата было значительно ниже по сравнению с исходным лекарством. Концентрации гидроморфона в плазме, вызванные 6-о-салицилат-ГМ и 3-изониацин-ГМ, были такими же, как для неконъюгированного гидроморфона, за исключением значительного снижения в первый момент времени (0,25 часа), что дало более низкое значение Cmax для этих двух конъюгатов. Концентрации в плазме гидроморфона, выделенного из 3-фенамат-ГМ, были повышены в течение первого часа после перорального введения и затем снизились быстро по сравнению с неконъюгированным гидроморфоном. Концентрации гидроморфона в плазме были сравнимы после перорального введения 3-аспирин-ГМ, 3,6-диаспирин-ГМ и неконъюгированного гидроморфона.
Пример 2: Анализ интраназальной фармакокинетики
Определенные конъюгаты пролекарств в соответствии с данным изобретением дозируют в интраназальных растворах крысам и сравнивают с эквимолярным раствором гидрохлорида гидроморфона. Интраназальное исследование проводят в дозах, эквимолярных 2,0 мг/кг гидроморфона. Выделение гидроморфона из пролекарств варьируется в зависимости от лиганда, присоединенного к гидроморфону.
Концентрации гидроморфона в плазме после интраназального введения 3,6-диаспирин-ГМ были значительно снижены по сравнению с исходным лекарственным средством (Фигура 16). Значения ППК и Cmax 3,6-диаспирин-ГМ составляют 17% и 20% от соответствующих параметров ФК неконъюгированного гидроморфона.
Пример 3: Анализ внутривенной фармакокинетики
Определенные конъюгаты пролекарств в соответствии с данным изобретением дозируют во внутривенных растворах крысам и сравнивают с эквимолярным раствором гидрохлорида гидроморфон. Выделение гидроморфона из пролекарств варьируется в зависимости от лиганда, присоединенного к гидроморфону.
Гидроморфон и 3,6-диаспирин-ГМ дозируют внутривенно крысам в дозе 0,20 мг/кг. Концентрации гидроморфона в плазме после внутривенного введения 3,6-диаспирин-ГМ значительно ниже по сравнению с неконъюгированным гидроморфоном (Фигура 17). Значения ППК и Cmax 3,6-диаспирин-ГМ составляют 6% и 3% от соответствующих параметров ФК неконъюгированного гидроморфона.
Пример 4: Анализ увеличения дозы
Определенные конъюгаты пролекарств в соответствии с данным изобретением дозируют в повышенных дозах в виде пероральных растворов крысам. Когда 3,6-диаспирин-ГМ дозируют выше терапевтического уровня, действие (ППК) гидроморфона достигает плато. Однако после перорального введения гидрохлорида гидроморфона, действие (ППК) гидроморфона остается приблизительно пропорционально дозе даже для доз свыше терапевтического уровня и вызывает смерть тестируемых животных при дозах выше 14 мг/кг (см. Фигуру 18). Эти данные подтверждают, что 3,6-диаспирин-ГМ имеет пониженный потенциал к передозировке по сравнению с гидрохлоридом гидроморфона.
Не привязываясь к определенной теории, полагают, что плато воздействия (ППК) наблюдается, когда 3,6-диаспирин-ГМ дозируют в количестве выше терапевтического уровня, благодаря насыщению гидролитических ферментов.
Пример 5: Анализ защищенности от несанкционированного доступа
Определенные конъюгаты пролекарств в соответствии с данным изобретением подвергают различным известным широко применяемым "методам экстракции" для тестирования гидролиза и/или разложения пролекарства. Экстрагирование раствора 3,6-диаспирин-ГМ из композиции дает только неактивное пролекарство с неотъемлемой защитой от фармакологически неправильного употребления. Это показывает, что гидроморфон не может быть выделен из 3,6-диаспирин-ГМ с помощью физических манипуляций или экстракции раствора. Кроме того, 3,6-диаспирин-ГМ является химически стабильным при применении обычных "методов экстракции" и гидролизуется и/или разлагается только в крайне тяжелых условиях, давая комплексную смесь продуктов разложения в виде высоко кислых или щелочных растворов. Кроме того, продукты разложения имеют пониженную пероральную, ИН и ВВ биодоступность, что делает экстрагирование неэффективным и бессмысленным. Результаты анализа экстрагирования суммированы в таблице 2 ниже.
Кроме того, 3,6-диаспирин-ГМ подвергают 16 жестким гидролитическим условиям и полученные продукты распада отслеживают и подсчитывают ВЭЖХ. Кроме гидроморфона наблюдают три промежуточных продукта распада и затем синтезируют и дозируют перорально крысам. Для каждого гидролитического состояния рассчитывают виртуальные значения ППК и Cmax на основе композиции полученной смеси и индивидуальных параметров ФК для каждого из ее компонентов (см. Фигуру 19). Эти данные показывают, что разрушение 3,6-диаспирин-ГМ дает смесь соединений, которые при пероральном введении демонстрируют воздействие (ППК) гидроморфона, которое ниже, чем воздействие (ППК) гидрохлорида гидроморфон или не разрушенного 3,6-диаспирин-ГМ, и максимальное воздействие (Cmax) гидроморфона, которое ниже максимального воздействия (Cmax) гидрохлорида гидроморфона.
Пример 6: Анализ вызванной опиоидом констипации
Анализы связывания рецепторов и анализы подтвержденной двигательной активности желудочно-кишечного тракта (ЖКТ) у крыс проводят для определенных конъюгатов пролекарств в соответствии с данным изобретением. Анализы связывания рецепторов показали, что 3,6-диаспирин-ГМ имеет незначительное сродство к тонкокишечным μ-опиоидным рецепторам, которые расположены в кишечнике.
Анализ подтвержденной двигательной активности ЖКТ у крыс демонстрирует, что в эквимолярных дозах 3,6-диаспирин-ГМ снижает транзит ЖКТ в меньшей степени, чем гидрохлорид гидроморфона. Действие 3,6-диаспирин-ГМ на двигательную активность ЖКТ такое же, как у гидрохлорида гидроморфона только когда 3,6-диаспирин-ГМ дают в дозе в два раза больше эквимолярной дозы исходного лекарственного средства (Фигура 20). Эти данные позволяют предположить, что 3,6-диаспирин-ГМ обладает потенциалом к снижению или исключению вызванной опиоидом констипации (ВОК), связанной с введением неконъюгированного гидроморфона.
Не привязываясь к определенной теории полагают, что 3,6-диаспирин-ГМ остается практически нетронутым до абсорбции в слизистую кишечника, где он превращается в гидроморфон после того, как обойдет периферийные опиоидные рецепторы. Снова, не привязываясь к определенной теории, также полагают, что выделенный гидроморфон затем проходит через базолатеральную мембрану в системный кровоток. Этот теоретический механизм согласуется с потенциалом к снижению или предотвращению вызванной опиоидом констипации, связанной с введением 3,6-диаспирин-ГМ по сравнению с неконъюгированным гидроморфоном.
Пример 7: Определенные схемы синтеза
Синтез 3-аспирин-ГМ·HCl (Фигура 21A):
Триэтиламин (0,42 мл, 3 ммоль) добавляют к гидрохлориду гидроморфона (0,322 г, 1 ммоль) в дихлорметане (10 мл), затем хлорид O-ацетилсалицилоила (0,248 г, 1,25 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 4 часов. Смесь выливают в этилацетат (100 мл) и промывают водным насыщенным NaHCO3 (30 мл × 3) и насыщенным раствором соли (30 мл). Органический слой сушат над безводным Na2SO4 и концентрируют. Остаток очищают хроматографией на колонке (8% метанол в дихлорметане) с получением 0,385 г аморфного твердого вещества, которое растворяют в метаноле (6 мл) и затем обрабатывают 1N HCl/MeOH (1,3 мл). Растворитель выпаривают, и TBME (6 мл) добавляют к остатку. Полученное белое твердое вещество собирают и ополаскивают TBME (1 мл × 2). Выход составляет 0,395 г (81,6%).
Синтез 3-циннамат-ГМ·HCl (Фигура 21B):
Соединение синтезируют с применением методики, применяемой для 3-аспирин-ГМ, за исключением того, что хлорид O-ацетилсалицилоила заменяют на хлорид циннамоила. Выход составляет 65,2%.
Синтез 3-бензоат-ГМ·HCl (Фигура 21C):
Соединение синтезируют с применением методики, применяемой для 3-аспирин-ГМ, за исключением того, что хлорид O-ацетилсалицилоила заменяют на хлорид бензоила. Выход составляет 58,9%.
Синтез 3,6-ди-аспирин-ГМ·HCl (Фигура 21D):
Триэтиламин (0,70 мл, 5 ммоль) добавляют к гидрохлориду гидроморфона (0,322 г, 1 ммоль) в дихлорметане (15 мл), затем ДМАП (48,9 мг, 0,4 ммоль) и хлорид O-ацетилсалицилоила (0,794 г, 4 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 48 часов. Смесь выливают в этилацетат (100 мл) и промывают водным насыщенным NaHCO3 (30 мл × 3) и насыщенным раствором соли (30 мл). Органический слой сушат над безводным Na2SO4 и концентрируют. Остаток очищают хроматографией на колонке (этилацетат и затем 8% метанол в дихлорметане) и затем далее очищают ПТСХ (8% метанол в дихлорметане). Желаемую фракцию концентрируют и превращают в ее HCl соль добавлением 1N HCl (1 мл). Растворитель выпаривают и к остатку добавляют простой эфир (15 мл). Полученное твердое вещество собирают и ополаскивают простым эфиром (2 мл × 3). Выход составляет 0,203 г (31,4%).
Синтез 6-салицилат-ГМ·HCl (Фигура 21E):
Стадия 1 (3-MOM-ГМ):
0,5M MeONa/MeOH (80 мл, 40 ммоль) добавляют к гидрохлориду гидроморфона (6,436 г, 20 ммоль) в метаноле (50 мл). Растворитель выпаривают, и остаток совместно выпаривают с толуолом (25 мл × 2). MOMCl (1,691 г, 21 ммоль) в хлороформе (5 мл) добавляют к полученному твердому веществу в хлороформе (100 мл) в течение более 5 минут при охлаждении на ледяной бане. Реакционную смесь перемешивают при комнатной температуре в течение ночи. Растворители выпаривают, и полученный остаток очищают на колонке (8% метанол в хлороформе) с получением 5,77 г (87,5%) масла.
Стадия 2 (сукцинимидиловый эфир 2-MOM-салициловой кислоты):
2-MOM салициловую кислоту (3,2 г, 17,6 ммоль) и N-гидроксисукцинимид (NHS, 2,23 г, 19,36 ммоль) растворяют в ТГФ (безводный, 40 мл). Добавляют ДЦК (3,99 г, 19,36 ммоль) одной порцией. Реакционную смесь перемешивают в течение ночи. Твердые вещества отфильтровывают. Фильтрат концентрируют досуха, и остаток перекристаллизовывают из метанола (10 мл). Полученное белое твердое вещество собирают и ополаскивают метанолом (3 мл × 2). Выход составляет 2,599 г (52,8%).
Стадия 3 (3-MOM-6-(2-MOM-салицилат)-ГМ):
1M LiHMDS/ТГФ (3 мл, 3 ммоль) добавляют к 3-MOM-защищенному гидроморфону (0,329 г, 1 ммоль) в ТГФ (безводный, 8 мл) в течение более 5 минут при охлаждении на ледяной бане. Смесь затем перемешивают в течение 20 минут при комнатной температуре. При охлаждении на ледяной бане добавляют сукцинимидиловый эфир 2-MOM-салициловой кислоты (0,838 г, 3 ммоль) одной порцией. Реакционную смесь перемешивают в течение 6 часов. Насыщенный NH4Cl (30 мл) добавляют для гашения реакции. Смесь перемешивают в течение 30 минут и экстрагируют этилацетатом (100 мл). Слой ацетата промывают насыщенным NaHCO3 (30 мл × 2) и насыщенным раствором соли (30 мл), сушат над безводным Na2SO4 и концентрируют. Остаток очищают на колонке (этилацетат и затем 7% метанол в дихлорметане) с получением 100 мг сиропа (20,2%).
Стадия 4 (6-Салицилат-ГМ·HCl):
Защищенный 3-MOM-6-(2-MOM-салицилат)-ГМ (100 мг), полученный на стадии 3, растворяют в метаноле (1 мл). 1,25N HCl/MeOH (3 мл) добавляют к раствору, и реакционную смесь перемешивают в течение 3 часов. Растворители выпаривают, и остаток растворяют в метаноле (0,5 мл). Добавляют простой эфир (15 мл), и полученное твердое вещество собирают фильтрацией и промывают простым эфиром (1 мл × 3). Выход составляет 75 мг (83,7%).
В данном описании применение единственного числа включает множественное число, если четко не указано иначе.
Композиции, пролекарства и способы, описанные здесь, могут быть иллюстрированы следующими вариантами, перечисленными в пронумерованных параграфах, представленных ниже:
В одном типовом варианте, данное изобретение относится к композиции пролекарства, содержащей по крайней мере один конъюгат, где конъюгат содержит по крайней мере один гидроморфон и по крайней мере одну арилкарбоновую кислоту. Далее, композиция пролекарства также может содержать по крайней мере один гидроморфон и по крайней мере одну арилкарбоновую кислоту, химически связанные друг с другом взаимодействием группы карбоновой кислоты арилкарбоновой кислоты с C-6 енольным таутомером гидроморфона. Далее, композиция пролекарства может включать или использовать по крайней мере один гидроморфон и по крайней мере одну арилкарбоновую кислоту, химически связанные друг с другом взаимодействием группы карбоновой кислоты арилкарбоновой кислоты с C-3 гидроксилом гидроморфона. Более того, такие типовые композиции пролекарств также могут содержать или применять по крайней мере один гидроморфон и по крайней мере одну арилкарбоновую кислоту, химически связанные друг с другом взаимодействием группы карбоновой кислоты одной арилкарбоновой кислоты с C-6 енольным таутомером гидроморфона и одной арилкарбоновой кислоты с C-3 гидроксилом гидроморфона. Должно быть понятно, что любой из описанных выше типовых вариантов/композиций может включать или применять по крайней мере одну арилкарбоновую кислоту, содержащую карбоксильную группу, присоединенную к по крайней мере одной арильной группе.
В по крайней мере одном альтернативном варианте таких композиций пролекарств по крайней мере одна арилкарбоновая кислота может быть выбрана из группы, включающей, например, бензоаты и гетероарилкарбоновые кислоты. В других вариантах композиций пролекарств гетероарилкарбоновую кислоту выбирают из группы, включающей пиридин, диазин и триазин. В некоторых вариантах композиций пролекарств, бензоат имеет следующую общую формулу I:

где R1, R2 и R3 независимо выбирают из группы, включающей водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат.
В дополнительных вариантах композиций пролекарств бензоат могут быть выбраны из группы, включающей, например, аминобензоаты, гидроксибензоаты и аминогидроксибензоаты, их смеси и их производные. Более того, композиции пролекарств могут содержать или применять аминобензоат, который выбирают из группы, включающей, например, антранилиновую кислоту, 3-аминобензойную кислоту, 4,5-диметилантранилиновую кислоту, N-метилантранилиновую кислоту, N-ацетилантранилиновую кислоту, фенаминовые кислоты, 2,4-диаминобензойную кислоту (2,4-DABA), 2-ацетиламино-4-аминобензойную кислоту, 4-ацетиламино-2-аминобензойную кислоту и 2,4-диацетиламинобензойную кислоту, их смеси их производные. Более того, композиции пролекарств могут содержать или применять гидроксибензоат, который выбирают из группы, включающей, например, бензойную кислоту, салициловую кислоту, ацетилсалициловую кислоту (аспирин), 3-гидроксибензойную кислоту, 4-гидроксибензойную кислоту, 6-метилсалициловую кислоту, o,м,п-крезотиновую кислоту, анакардиновые кислоты, 4,5-диметилсалициловую кислоту, o,м,п-тимотиновую кислоту, дифлузинал, o,м,п-анизиновую кислоту, 2,3-дигидроксибензойную кислоту (2,3-DHB), α,β,γ-резорциловую кислоту, протокатеховую кислоту, гентизиновую кислоту, пиперонилиновую кислоту, 3-метоксисалициловую кислоту, 4-метоксисалициловую кислоту, 5-метоксисалициловую кислоту, 6-метоксисалициловую кислоту, 3-гидрокси-2-метоксибензойную кислоту, 4-гидрокси-2-метоксибензойную кислоту, 5-гидрокси-2-метоксибензойную кислоту, ванилиновую кислоту, изованилиновую кислоту, 5-гидрокси-3-метоксибензойную кислоту, 2,3-диметоксибензойную кислоту, 2,4-диметоксибензойную кислоту, 2,5-диметоксибензойную кислоту, 2,6-диметоксибензойную кислоту, вератриновую кислоту (3,4-диметоксибензойную кислоту), 3,5-диметоксибензойную кислоту, галлиевую кислоту, 2,3,4-тригидроксибензойную кислоту, 2,3,6-тригидроксибензойную кислоту, 2,4,5-тригидроксибензойную кислоту, 3-O-метилгаллиевую кислоту (3-OMGA), 4-O-метилгаллиевую кислоту (4-OMGA), 3,4-O-диметилгаллиевую кислоту, сиреневую кислоту и 3,4,5-триметоксибензойную кислоту, их смеси и их производные. В других альтернативных вариантах, композиции пролекарств могут содержать или применять аминогидроксибензоат, который выбирают из группы, включающей, например, 4-аминосалициловую кислоту, 3-гидроксиантранилиновую кислоту и 3-метоксиантранилиновую кислоту, их смеси и их производные.
В дополнительных вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которая включает карбоксильную группу, которая связана углеродной связью с арильной группой.
В других вариантах, композиции пролекарств могут содержать или применять по крайней мере, одну арилкарбоновую кислоту, которую выбирают из группы, включающей разветвленные фенилпропионовые кислоты и фенилацетаты, их смеси и их производные. Более того, композиции пролекарств могут содержать или применять фенилацетат, имеющий следующую общую структуру II:

где R1, R2, R3 и R4 независимо выбирают из группы, включающей, например, водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат. В дополнительных вариантах, композиции пролекарств могут содержать или применять фенилацетат, который выбирают из группы, включающей, например, фенилуксусную кислоту (гидратроповую кислоту), 2-гидроксифенилуксусную кислоту, 3-гидроксифенилуксусную кислоту, 4-гидроксифенилуксусную кислоту, гомопротокатеховую кислоту, гомогентизиновую кислоту, 2,6-дигидроксифенилуксусную кислоту, гомованилиновую кислоту, гомоизованилиновую кислоту, гомовалератриновую кислоту, атроповую кислоту, d,l-троповую кислоту, диклофенак, d,l-миндальную кислоту, 3,4-дигидрокси-d,l-миндальную кислоту, ванилил-d,l-миндальную кислоту, изованилил-d,l-миндальную кислоту, ибупрофен, фенопрофен, карпрофен, флурбипрофен, кетопрофен и напроксен, их смеси и их производные.
В некоторых дополнительных вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которая содержит карбоксильную группу, которая связана двухуглеродной связью с арильной группой. Кроме того, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которую выбирают из группы, включающей бензилацетаты и циннаматы, их смеси и их производные. Далее, композиции пролекарств могут содержать или применять по крайней мере, одну арилкарбоновую кислоту которую выбирают из группы, включающей, например, бензилацетаты и циннаматы, имеющие следующую общую формулу III или IV или их сочетания:


где R1, R2, R3 и R4 независимо выбирают из группы, включающей водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат.
В дополнительных вариантах, композиции пролекарств могут содержать или применять бензилацетат, который выбирают из группы, включающей, например, бензилуксусную кислоту, мелилотовую кислоту, 3-гидроксифенилпропановую кислоту, 4-гидроксифенилпропановую кислоту, 2,3-дигидроксифенилпропановую кислоту, d,l-фенилмолочную кислоту, o,м,п-гидрокси-d,l-фенилмолочную кислоту и фенилпировиноградную кислоту, их смеси и их производные. В альтернативных вариантах, композиции пролекарств могут содержать или применять циннамат, который выбирают из группы, включающей, например, коричную кислоту, o,м,п-кумариновую кислоту, 2,3-дигидроксикоричную кислоту, 2,6-дигидроксикоричную кислоту, кофеиновую кислоту, ферулиновую кислоту, изоферулиновую кислоту, 5-гидроксиферулиновую кислоту, синаповую кислоту и 2-гидрокси-3-фенилпропеноевую кислоту, их смеси и их производные.
В некоторых вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которая содержит карбоксильную группу, присоединенную к арильной группе кольца алкильной цепью. В других вариантах, композиции пролекарств могут содержать или применять алкильную цепь, которая содержит один углерод. В других вариантах, композиции пролекарств могут содержать или применять алкильную цепь, которая содержит два углерода. В других вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которая содержит карбоксильную группу, присоединенную к арильной группе алкенильной цепью. В других вариантах, композиции пролекарств могут содержать или применять алкенильную цепь, которая содержит два углерода. В других вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которая содержит одну или более боковых цепей. В дополнительных вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которая содержит одну или более функциональные группы. В альтернативных вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которая содержит по крайней мере одну гетероарилкарбоновую кислоту.
В некоторых вариантах, композиции пролекарств могут содержать или применять гетероарилкарбоновую кислоту, которая имеет, например, одну из следующих общих формул V, VI, VII, VIII, IX, X, XI, XII или XIII или их сочетания:

где R1, R2 и R3 независимо выбирают из группы, включающей водород, гидроксил, амино, амин, амид, тиол, циано, нитро, галоген, имин, алкил, алкокси, арил, алкенил, алкинил, галогеналкил, алкиларил, арилалкил, гетероцикл, арилалкокси, циклоалкил, циклоалкенил, циклоалкинил, карбонил, тиоэфир, селеноэфир, силил, силилокси, сульфонил, фосфонат.
В других вариантах, композиции пролекарств могут содержать или применять гетероарильную группу, которая содержит один гетероатом. В других вариантах, композиции пролекарств могут содержать или применять гетероарилкарбоновую кислоту, то есть, например, по крайней мере один пиридин или производное пиридина. В дополнительных вариантах, композиции пролекарств могут содержать или применять гетероарилкарбоновую кислоту, которую выбирают из группы, включающей, например, никотиновую кислоту (ниацин), изоникотиновую кислоту, пиколиновую кислоту, 3-гидроксипиколиновую кислоту, 6-гидроксиникотиновую кислоту, цитразиновую кислоту, 2,6-дигидроксиникотиновую кислоту, кинуреновую кислоту, ксантуреновую кислоту, 6-гидроксикинуреновую кислоту, 8-метоксикинуреновую кислоту, 7,8-дигидроксикинуреновую кислоту и 7,8-дигидро-7,8-дигидроксикинуреновую кислоту, их смеси и их производные.
В других вариантах, композиции пролекарств могут содержать или применять гетероарильную группу, которая содержит два гетероатома. В других вариантах, композиции пролекарств могут содержать или применять гетероарилкарбоновую кислоту, например, по крайней мере один пиразин, пиримидин, пиридазин или их производные. В других вариантах, композиции пролекарств могут содержать или применять гетероарильную группу, которая содержит три гетероатома. В дополнительных вариантах, композиции пролекарств могут содержать или применять гетероарилкарбоновую кислоту, которая является по крайней мере одной из 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина или их производных. В других вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, содержащую шестичленное кольцо. Более того, композиции пролекарств могут содержать или применять шестичленное кольцо, которое содержит дополнительные замещенные или незамещенные ароматические или алифатические кольца. В других вариантах, композиции пролекарств могут содержать или применять по крайней мере, одну арилкарбоновую кислоту, которая содержит только одну свободную группу карбоновой кислоты. В других вариантах, композиции пролекарств могут содержать или применять по крайней мере одну арилкарбоновую кислоту, которая содержит, например, от 1 до 4 заместителей на арильном кольце.
В других вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в виде конъюгата, который является нейтральным пролекарством. В других вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в форме конъюгата, который является свободной кислотой. В других вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в форме конъюгата, который является свободным основанием. В других вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в форме конъюгата, который является фармацевтически приемлемой анионной или катионной солевой формой или смесью солей. В некоторых вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в форме соли, которую выбирают из группы, включающей, например, ацетат, l-аспартат, безилат, бикарбонат, карбонат, d-камзилат, l-камзилат, цитрат, эдизилат, формиат, фумарат, глюконат, гидробромид/бромид, гидрохлорид/хлорид, d-лактат, l-лактат, d,l-лактат, d,l-малат, l-малат, d-малат, мезилат, памоат, фосфат, сукцинат, сульфат, бисульфат, d-тартрат, l-тартрат, d,l-тартрат, мезотартрат, бензоат, глуцептат, d-глюкуронат, гибензат, изетионат, малонат, метилсульфат, 2-напсилат, никотинат, нитрат, оротат, стеарат, тозилат, тиоцианат, ацефиллинат, ацетурат, аминосалицилат, аскорбат, борат, бутират, камфорат, камфокарбонат, деканоат, гексаноат, холат, ципионат, дихлорацетат, эдентат, этилсульфат, фурат, фузидат, галактарат (мукат), галактуронат, галлат, гентизат, глутамат, глутарат, глицерофосфат, гептаноат (энантат), гидроксибензоат, гиппурат, фенилпропионат, йодид, ксинафоат, лактобионат, лаурат, малеат, миндалят, метансульфонат, миристат, нападизилат, олеат, оксалат, пальмитат, пикрат, пивалат, пропионат, пирофосфат, салицилат, салицилсульфат, субсалицилат, таннат, терефталат, тиосалицилат, триброфенат, валерат, вальпроат, адипат, 4-ацетамидобензоат, камзилат, октаноат, эстолат, эзилат, гликолят, тиоцианат, ундециленат, натрий, калий, кальций, магний, цинк, алюминий, литий, холинат, лизиний, аммоний и трометамин, их смеси и их производные.
В определенных вариантах данного изобретения композиции пролекарств могут разлагаться in vivo с выделением активного гидроморфона, арилкарбоновой кислоты, их производных и их метаболитов. В других вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в виде пролекарства, которое вводят перорально и гидролизуют in vivo с выделением гидроморфона из пролекарства. В дополнительных вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в виде пролекарства, которое демонстрирует отсутствие или ограниченное фармакологическое действие при введении. В других вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в виде пролекарства, которое выделяет гидроморфон так же, как и свободный или немодифицированный гидроморфон при введении в эквимолярных дозах. В других вариантах, композиции пролекарств в соответствии с данным изобретением могут выделять гидроморфон в системный кровоток в пониженных/контролируемых количествах при введении пролекарства путем, отличным от перорального. В других вариантах, композиции пролекарств в соответствии с данным изобретением могут быть в виде пролекарства, которое выделяет гидроморфон контролируемым или замедленным образом при введении.
В определенных вариантах в соответствии с данным изобретением, композиции пролекарств могут быть в виде пролекарств, которые не вызывают или вызывают незначительные побочные эффекты по сравнению с немодифицированным гидроморфоном при введении в эквимолярных дозах. В других вариантах, композиции пролекарств могут быть в виде пролекарств, которые демонстрируют отсутствие или пониженные побочные эффекты, выбранные из, например, головокружения, дурноты, сонливости, тошноты, рвоты, констипации, боли в желудке, сыпи, затрудненного мочеиспускания, затрудненного дыхания, нейровозбуждающего действия или обморока.
В других вариантах в соответствии с данным изобретением, композиции пролекарств не дают высокие концентрации гидроморфона в плазме или крови по сравнению с немодифицированным гидроморфоном при введении в эквимолярных дозах внутривенным или интраназальным способами. В других вариантах, композиции пролекарств не вызывают или снижают эйфорию или подобные эффекты при интраназальном введении. В других вариантах, композиции пролекарств не вызывают или снижают эйфорию или подобные эффекты при внутривенном введении. В альтернативных вариантах, композиции пролекарств не дают быстрый пик концентрации гидроморфона (Cmax) в крови или плазме при пероральном введении. В дополнительных вариантах, композиции пролекарств демонстрируют отложенное Tmax по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах. В других вариантах, композиции пролекарств демонстрируют более низкое значение Cmax по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах. В дополнительных вариантах, композиции пролекарств демонстрируют повышенную относительную биодоступность гидроморфона по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах. В других вариантах, композиции пролекарств демонстрируют более высокое значение Cmax по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах. В альтернативных вариантах, композиции пролекарств имеют более высокое значение ППК по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах. В дополнительных вариантах, композиции пролекарств демонстрируют более высокие значения Cmax и ППК по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах.
В других вариантах в соответствии с данным изобретением композиции пролекарств не высвобождают гидроморфон при физических манипуляциях с композицией. В дополнительных вариантах, композиции пролекарств демонстрируют устойчивость к определенным химическим манипуляциям с целью высвобождения свободного гидроморфона.
В дополнительных вариантах в соответствии с данным изобретением композиции пролекарств не оказывают или оказывают незначительное действие на μ-опиоидные рецепторы. В других вариантах, композиции пролекарств не подвержены или ограниченно подвержены ферментному гидролизу до тех пор, пока они не адсорбируются в кишечнике. В дополнительных вариантах, композиции пролекарств демонстрируют пониженное превращение в гидроморфон-3-глюкуронид (H3G) по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах.
В других вариантах в соответствии с данным изобретением композиции пролекарств предотвращают или снижают вызванную опиоидом констипацию (ВОК) по сравнению с немодифицированным гидроморфоном при пероральном введении в эквимолярных дозах.
В определенных вариантах в соответствии с данным изобретением композиции пролекарств, кроме того, содержат, например, ибупрофен, ацетаминофен или аспирин. В некоторых вариантах данного изобретения, композиции пролекарств содержат или применяют конъюгат, который выбирают из группы, включающей, например, 3-аспирин-гидроморфон, 3,6-диаспирин-гидроморфон, 6-осалицилат-гидроморфон, 3-циннамат-гидроморфон, 6-напроксен-гидроморфон, 3-изониацин-гидроморфон, 3-п-салициловый-гидроморфон, 3-фенамат-гидроморфон, 3-бензоат-гидроморфон и 3,6-ди-бензоат-гидроморфон.
В других вариантах в соответствии с данным изобретением композиции пролекарств имеют пероральную лекарственную форму. В дополнительных вариантах, композиции пролекарства имеют пероральную лекарственную форму, которую выбирают из группы, включающей, например, таблетки, капсулы, каплеты, пастилки, таблетки для рассасывания, порошок, суспензию, сироп, раствор, мягкие желатиновые капсулы, суспензию, подъязычные капли и пероральные тонкие пленки (ПТП). В определенных вариантах, композиции пролекарств имеют пероральную лекарственную форму, которая является твердой лекарственной формой. В других вариантах, композиции пролекарств имеют твердую лекарственную форму и также содержат по крайней мере один наполнитель. В других вариантах, композиции пролекарств содержат наполнитель, который выбирают из группы, включающей, например, антиадгезивы, связующие агенты, покрытия, разрыхлители, наполнители, вкусовые добавки, красители, глиданты, смазывающие агенты, консерванты, сорбенты и подсластители. В дополнительных вариантах, композиции пролекарств составлены в таблетки, капсулы, капсулы с модифицированным высвобождением, мягкие желатиновые капсулы, таблетки с пролонгированным выделением, капсулы с контролируемым высвобождением, суппозитории, порошки для инъекций, пероральные жидкости, сиропы от кашля, чрескожные пленки, суспензии или инъекции.
В других вариантах в соответствии с данным изобретением композиции пролекарства имеют пероральную дозу, которая эквимолярна от около 0,1 мг до около 200 мг немодифицированного гидроморфона. В дополнительных вариантах, композиции пролекарств имеют пероральную дозу, эквимолярную от около 1 мг до около 200 мг немодифицированного гидроморфона. В других вариантах, композиции пролекарств имеют пероральную дозу, эквимолярную от около 2 мг до около 8 мг немодифицированного гидроморфона. В других вариантах, композиции пролекарств имеют пероральную дозу, эквимолярную от около 8 мг до около 60 мг немодифицированного гидроморфона. В дополнительных вариантах, композиции пролекарств имеют пероральную дозу, эквимолярную от около 60 мг до около 200 мг немодифицированного гидроморфона.
Другие варианты в соответствии с данным изобретением относятся к способам лечения пациента, нуждающегося в обезболивающем действии, введением эффективного количества любой композиции пролекарства в соответствии с данным изобретением. Дополнительные варианты в соответствии с данным изобретением относятся к лечению пациента, нуждающегося в подавлении кашля, введением эффективного количества любой композиции пролекарства в соответствии с данным изобретением. В дополнительных вариантах, данное изобретение относится к способу лечения пациента, нуждающегося в терапии наркотической и лекарственной зависимости, введением эффективного количества любой композиции пролекарства в соответствии с данным изобретением. В определенных способах лечения в соответствии с данным изобретением композиции пролекарств имеют пероральную лекарственную форму. В других способах в соответствии с данным изобретением, композиции пролекарства имеют пероральную лекарственную форму, которую выбирают из группы, включающей, например, таблетки, капсулы, каплеты, пастилки, таблетки для рассасывания, порошок, суспензию, сироп, раствор, мягкие желатиновые капсулы, суспензию, подъязычные капли и пероральные тонкие пленки (ПТП). В дополнительных способах лечения в соответствии с данным изобретением композиции пролекарства имеют твердую лекарственную форму. В других вариантах, способы лечения в соответствии с данным изобретением включают композиции пролекарства в твердой лекарственной форме, которые также содержат наполнитель. В дополнительных вариантах, способы лечения в соответствии с данным изобретением включают композиции пролекарства в твердой лекарственной форме, которые также содержат наполнитель, который выбирают из группы, включающей, например, антиадгезивы, связующие агенты, покрытия, разрыхлители, наполнители, вкусовые добавки, красители, глиданты, смазывающие агенты, консерванты, сорбенты и подсластители.
В других вариантах, в способах в соответствии с данным изобретением применяют композиции пролекарства, которые составлены в, например, таблетки, капсулы, капсулы с модифицированным высвобождением, мягкие желатиновые капсулы, таблетки с пролонгированным выделением, капсулы с контролируемым высвобождением, суппозитории, порошки для инъекций, пероральные жидкости, сиропы от кашля, чрескожные пленки, суспензии или инъекции. В других вариантах, в способах в соответствии с данным изобретением применяют композиции пролекарства, которые имеют пероральную дозу, эквимолярную от около 0,1 мг до около 200 мг немодифицированного гидроморфона. В дополнительных вариантах, в способах в соответствии с данным изобретением применяют композиции пролекарства, которые имеют пероральную дозу, эквимолярную от около 2 мг до около 8 мг немодифицированного гидроморфона. В других вариантах, в способах в соответствии с данным изобретением применяют композиции пролекарства, которые имеют пероральную дозу, эквимолярную от около 8 мг до около 60 мг немодифицированного гидроморфона. В других вариантах, в способах в соответствии с данным изобретением применяют композиции пролекарства, которые имеют пероральную дозу, эквимолярную от около 60 мг до около 200 мг немодифицированного гидроморфона.
Дополнительные варианты в соответствии с данным изобретением относятся к способам синтеза любых композиций пролекарств в соответствии с данным изобретением, где синтез включает стадии химического связывания по крайней мере одной арилкарбоновой кислоты с по крайней мере одним гидроморфоном. В других вариантах, способы синтеза любой композиции пролекарства в соответствии с данным изобретением относятся к синтезу, например, 3-аспирин-гидроморфона, 3,6-диаспирин-гидроморфона, 6-салицилат-гидроморфона, 3-циннамат-гидроморфона и 3-бензоат-гидроморфона.
Другие варианты в соответствии с данным изобретением относятся к фармацевтическому набору, содержащему определенное количество отдельных доз композиции пролекарства в соответствии с данным изобретением в упаковке, содержащей фармацевтически эффективное количество по крайней мере одного конъюгата, где конъюгат содержит по крайней мере один гидроморфон и по крайней мере одну арилкарбоновую кислоту. В других вариантах, наборы в соответствии с данным изобретением включают способ лечения или профилактики боли у человека или животного. В дополнительных вариантах, наборы в соответствии с данным изобретением предназначены для лечения детей, пожилых пациентов и/или пациентов среднего возраста. В других вариантах, наборы в соответствии с данным изобретением включают отдельные дозы композиции пролекарства в соответствии с данным изобретением, содержащие по крайней мере около 0,1 мг или выше по крайней мере одного конъюгата в соответствии с данным изобретением. В других вариантах, наборы в соответствии с данным изобретением включают отдельные дозы композиции(ий) пролекарства в соответствии с данным изобретением, содержащие по крайней мере около 1 мг, около 2,5 мг, около 5,0 мг, около 10 мг, около 20 мг, около 50 мг, около 100 мг, около 200 мг, около 500 мг или выше по крайней мере одного конъюгата в соответствии с данным изобретением. В дополнительных вариантах, наборы в соответствии с данным изобретением включают от около 1 до около 90, около 1 до около 60 или около 10 до около 30 отдельных доз по крайней мере одной композиции пролекарства в соответствии с данным изобретением.
Описанное здесь изобретение описано с помощью полных, однозначных, четких и точных терминов, понятных специалистам в данной области техники, для которых оно предназначено, для его применения на практике. Должно быть понятно, что выше представлены предпочтительные варианты изобретения, и в него могут быть внесены модификации, не выходящие за суть или объем изобретения, представленные в формуле изобретения.
Реферат
Изобретение относится к композиции пролекарства для лечения заболеваний, расстройств или состояний, опосредованных связыванием опиоида с рецепторами опиоида, содержащей конъюгат, представляющий собой 3,6-диаспирин-гидроморфон в фармацевтически эффективном количестве, и биологически приемлемый носитель. Указанная композиция проявляет улучшенную биодоступность, меньшую вариабельность в пероральном фармакокинетическом профиле, более низкую пиковую концентрацию в плазме и пониженную возможность передозировки по сравнению с неконъюгированным гидроморфоном. Изобретение также относится к способу лечения пациента, страдающего заболеванием, расстройством или состоянием, опосредованным связыванием опиоида с рецепторами опиоида пациента. 2 н. и 10 з.п. ф-лы, 21 ил., 2 табл., 7 пр.

Комментарии