Назальные фармацевтические композиции и способы их применения - RU2373925C2
Код документа: RU2373925C2
Чертежи

Описание
I. Область, к которой относится изобретение
Настоящее изобретение направлено на назальные фармацевтические композиции, содержащие лекарственное вещество, которое имеет специфический профиль распределения размеров частиц. Такой профиль обеспечивает повышенную биодоступность, улучшенную эффективность или продолжительный терапевтический эффект лекарственного вещества при интраназальном введении. В альтернативном воплощении композиции в соответствии с настоящим изобретением включают беклометазон или его фармацевтически приемлемую производную, которые имеют специфический профиль распределения размеров частиц. Композиция может обеспечиваться в виде водной суспензии, приемлемой для интраназального введения субъекту, который нуждается в этом.
II. Предпосылки создания изобретения
Известно, что размер частиц лекарственного вещества влияет на биодоступность лекарственного средства и его эффективность. Были изучены способы получения тонкоизмельченных лекарственных веществ, а также были предприняты усилия в отношении контроля размера частиц и интервала размера частиц лекарственного вещества в фармацевтических композициях. Однако уровень техники не описывает лекарственных веществ, обладающих специфическими профилями распределения размеров частиц, которые обеспечивают повышенную биодоступность, улучшенную эффективность или длительный терапевтический эффект лекарственного средства при его введении интраназально.
Известно, что кортикостероиды, вводимые путем ингаляции, представляют собой наиболее эффективную систему медикации, используемую для лечения респираторных расстройств или заболеваний, характеризующихся воспалением. Один из таких кортикостероидов, дипропионат беклометазона (BDP), является особенно полезным при лечении или профилактике сезонного или длящегося круглый год ринита, а также назначается для ослабления одного или более симптомов, ассоциированных с сезонной или длящейся круглый год аллергией и неаллергическим (вазомоторным) ринитом. Ринит представляет собой реакцию, которая возникает в глазах, носу и горле, когда раздражаются дыхательные пути, например, запускается высвобождение гистамина. Гистамин вызывает воспаление и выработку жидкости в хрупкой выстилке носовых ходов, синусах и веках. Применение кортикостероидов, таких как беклометазон, может вызвать частичное или полное избавление от симптомов, связанных с ринитом, таких как чихание, закладывание носа, насморк, зуд в носу, воспаление глаз и ушей. Применение беклометазона может также отсрочить повторное появление полипов в носу у индивидуумов, которые подверглись удалению носовых полипов. У тех индивидуумов, у которых полипы возникают повторно, беклометазон может подавлять рост полипов и увеличение их размера.
Подобно большинству кортикостероидов и других лекарственных веществ, BDP является очень слабо растворимым в воде. Когда такие лекарственные вещества вводятся интраназально, то их обычно суспендируют в водном растворе. Однако, когда эти вещества вводятся интраназально с помощью традиционного назального аэрозоля, количества лекарственных веществ, меньшие, чем оптимальные, поглощаются слизистой оболочкой носа (ткань, которая представляет интерес), остальное количество заглатывается или выводится из носовой полости. В некоторых случаях частички, которые являются недостаточно мелкими, удаляются из желудочно-кишечного тракта до их попадания в область, которая преставляет интерес.Невозможность введения оптимальных количеств лекарственных веществ приводит к сниженной биодоступности и эффективности лекарственного средства.
III. Короткое изложение изобретения
Настоящее изобретение направлено на назальную фармацевтическую композицию, содержащую лекарственное вещество, имеющее специфический профиль распределения размеров частиц, который обеспечивает повышенную биодоступность, улучшенную эффективность или длительный терапевтический эффект лекарственного вещества, когда оно вводится интраназально. В частности, в одном альтернативном воплощении композиция в соответствии с настоящим изобретением включает лекарственное вещество (например, активный ингредиент), имеющий следующий профиль распределения размеров частиц: приблизительно 10% частиц лекарственного вещества имеют размер частиц приблизительно 0,75 микрона; приблизительно 25% частиц лекарственного вещества имеют размер частиц меньший, чем 1,5 микрона; приблизительно 50% частиц лекарственного вещества имеют размер частиц, меньший, чем 2 микрона; приблизительно 75% частиц лекарственного вещества имеют размер частиц, меньший, чем 3,5 микрона; приблизительно 90% частиц лекарственного вещества имеют размер частиц, меньший, чем 5 микрон; и больше, чем 90%, или приблизительно 100% частиц лекарственного вещества имеют размер частиц, меньший, чем 10 микрон. В одном предпочтительном воплощении лекарственное вещество представляет собой кортикостероид, предпочтительно беклометазон или его фармацевтически приемлемую производную.
IV. Фигуры
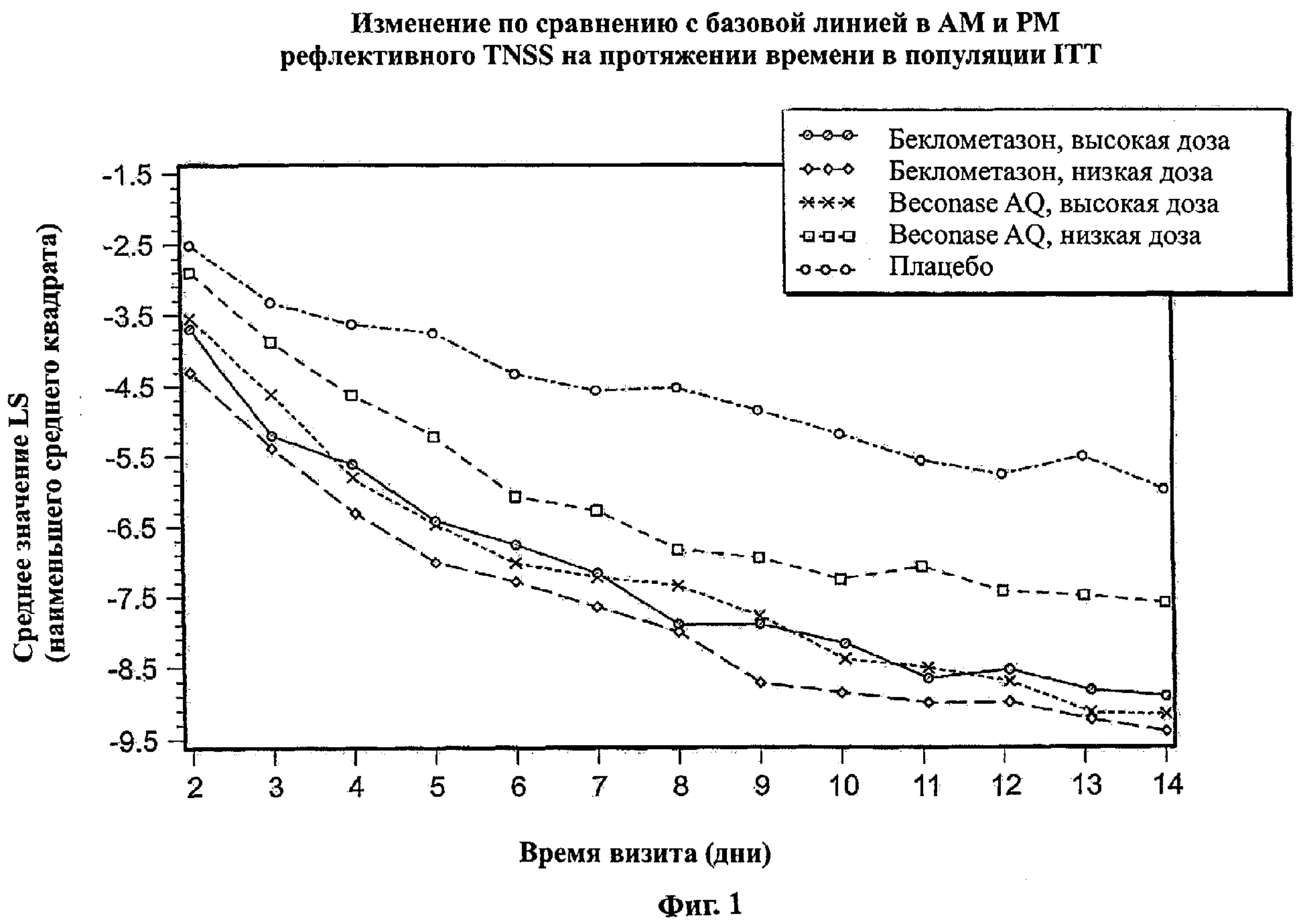
Фигура 1 показывает изменение базовой линии в AM и РМ рефлективном TNSS в течение времени в популяции ITT на протяжении периода изучения 14 дней.
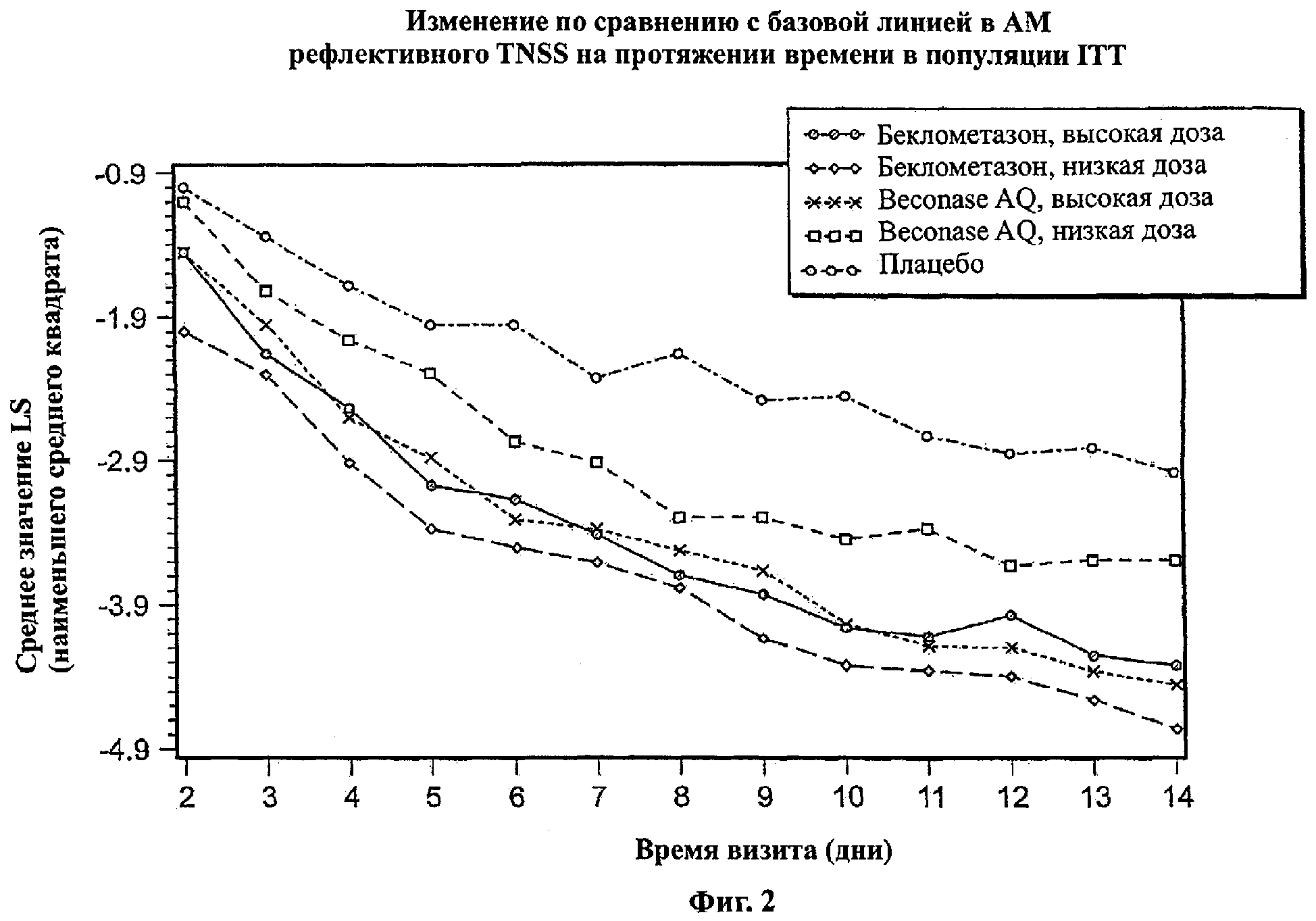
Фигура 2 показывает изменение базовой линии в AM рефлективном TNSS в течение времени в популяции ITT на протяжении периода изучения 14 дней.
Фигура 3 показывает изменение базовой линии в РМ рефлективном TNSS в течение времени в популяции ITT на протяжении периода изучения 14 дней.
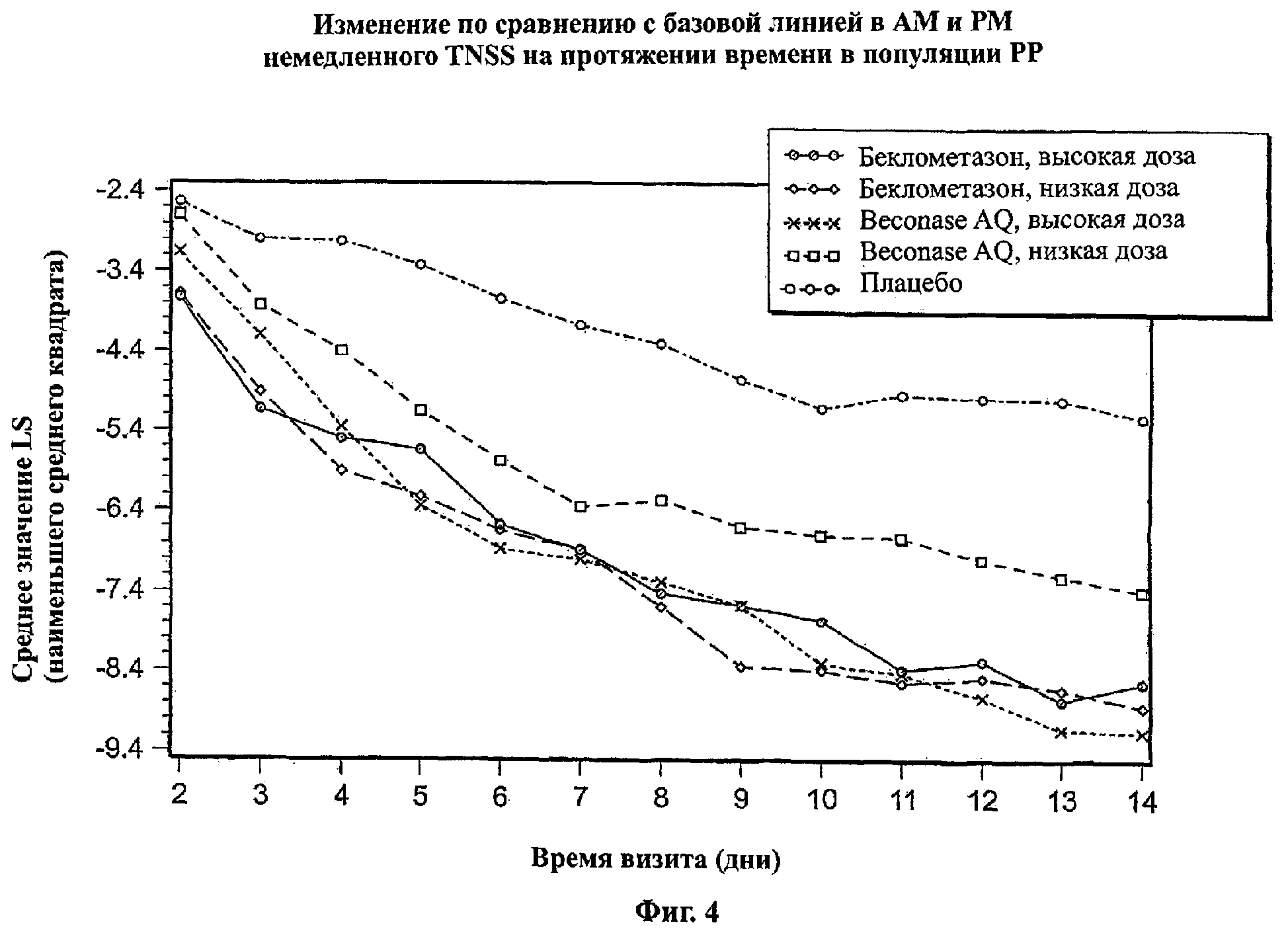
Фигура 4 показывает изменение базовой линии в AM и РМ рефлективном TNSS в течение времени в популяции РР на протяжении периода изучения 14 дней.
V. Подробное описание изобретения
Композиции, которые предлагаются в настоящем изобретении, применяются для лечения, предотвращения и/или облегчения одного или более симптомов медицинского состояния, расстройства или заболевания. Как используется в данной заявке, лечение означает любой способ, с помощью которого один или более симптомов состояния, расстройства или заболевания облегчаются или претерпевают иное благотворное изменение. Лечение также охватывает любое фармацевтическое или медицинское применение композиций в соответствии с настоящим изобретением. Как используется в данной заявке, облегчение симптомов частного расстройства путем введения частной композиции относится к любому облегчению, постоянному либо временному, длительному либо кратковременному, которое может быть приписано или ассоциировано с введением композиции. Как такой, который используется в данной заявке, термин «терапевтически эффективное количество» означает количество лекарственного вещества, достаточное для лечения, предотвращения и/или облегчения одного или более симптомов медицинского состояния, расстройства или заболевания. Оно также может включать безопасное и переносимое количество лекарственного вещества на основании промышленных и/или регуляторных стандартов.
В одном альтернативном воплощении композиции, которые обеспечиваются в данной заявке, используются для лечения, преотвращения и/или облегчения одного или более симптомов респираторного расстройства у индивидуума. В другом альтернативном воплощении настоящее изобретение обеспечивает композицию для лечения, профилактики и/или облегчения одного или более симптомов ринита или других родственных расстройств, при этом композиция включает один или более кортикостероидов, которые имеют специфический профиль распределения размеров чатиц. В альтернативном воплощении лекарственное вещество представляет собой беклометазон или его фармацевтически приемлемую производную. Препочтительно, когда лекарственное вещество представляет собой дипропионат беклометазона. Неожиданно было обнаружено, что лекарственное вещество, имеющее профили распределения размеров частиц в соответствии с изобретением, при введении интраназально субъекту, который в этом нуждается, обеспечивают повышенную биодоступность лекарственного вещества, а также повышенную и длительную эффективность по сравнению с традиционными композициями, содержащими то же лекарственное вещество. Лекарственные вещества для применения в данной заявке включают любое фармацевтическое вещество, имеющее настоящий профиль распределения размеров частиц, и пригодное для лечения, предотвращения и/или облегчения одного или более симптомов медицинского состояния, расстройства или заболевания, когда такое вещество вводится интраназально субъекту, который в этом нуждается.
Способ введения
Настоящие композиции могут быть упакованы для введения любым традиционным способом, предпочтительно в назальном аппликаторе и предпочтительно таким образом, чтобы обеспечить доставку фиксированной дозы лекарственного вещества. Контейнеры для введения в виде аэрозолей для различных типов назальных композиций были известны ранее и существенно все они будут в равной степени приемлемыми для композиций в соответствии с настоящим изобретением, принимая во внимание то, что материалы, из которых изготовлен контейнер, являются совместимыми с композициями. Среда, содержащая лекарственное вещество и другие приемлемые ингредиенты, может содержаться в маленькой бутылочке или подобном контейнере, из которого она может быть распылена в виде тумана, направленного в каждую ноздрю. Используя окружающий воздух в качестве газа-вытеснителя, можно получить бутылочку, изготовленную из гибкого пластика так, что простое сжимание бутылочки по бокам приводит к распылению аэрозоля через форсунку в полость каждой ноздри. Воздух может также служить газом-вытеснителем для насосного распылителя, в котором пользователь манипулирует с небольшой кнопкой насоса, накачивающего воздух в контейнер, и вызывает образование распыленной жидкости, которая испускается при обратном ударе. Альтернативно, бутылочка может быть герметизирована с газом, который является инертным для пользователя и для ингредиентов раствора. Газ может быть растворен под давлением в контейнере или может быть получен при растворении или при реакции твердого материала, который образует газ в качестве продукта растворения или продукта реакции. Типичные газы, которые могут использоваться, включают азот, аргон и двуокись углерода. Кроме того, когда композиции вводятся в виде спрея или аэрозоля, композиция может находится в герметизированном контейнере, содержащем жидкий газ-вытеснитель, включая без ограничения дихлордифторметан или хлортрифторэтилен среди прочих газов-вытеснителей.
В другом альтернативном воплощении для введение в виде аэрозоля композиция в соответствии с настоящим изобретением может быть помещена в приемлемое устройство для распыления, например, в насосное распылительное устройство или подобные ему. Распылительное устройство может быть обеспечено с приемлемыми средствами для доставки водного аэрозоля в ноздрю. Предпочтительно, когда оно обеспечивается со средствами, служащими для доставки существенно фиксированных композиции/впрыска (то есть, на каждую аэрозольную единицу). В одном воплощении устройство вводит отмеренную дозу. Аэрозольная композиция может быть суспендирована или растворена в жидком газе-вытеснителе. Могут присутствовать стабилизирующие и/или суспендирующие агенты и/или сорастворители. В других воплощениях настоящего изобретения композиция в соответствии с изобретением является приемлемой для интраназального введения с помощью насоса для аэрозоля, испускающего отмеренную дозу для индивидуума, который в этом нуждается. В этой связи композиция в соответствии с настоящим изобретением может быть предварительно упакована в бутылочку с насосом для накачивания отмеренной дозы или с дозирующим распылительным насосом.
В другом альтернативном воплощении композиции в соответствии с настоящим изобретением могут вводиться в ноздрю в форме капель или любым другим способом, который приводит к местному применению для слизистой оболочки носа. Форма дозы для интраназального введения может включать растворы, суспензии или эмульсии активного соединения в жидком носителе в форме носовых капель. Приемлемые жидкие носители включают воду, пропиленгликоль и другие фармацевтически приемлемые спирты. Для введения в виде капель композиции могут быть приемлемым образом помещены в контейнер, обеспеченный, например, традиционной пипеткой/устройством для перекрывания, например, включающий пипетку или тому подобное, предпочтительно доставляющий фиксированный объем композиции/капель. Дозированные формы могут быть стерилизованными, если это требуется. Дозированные формы могут также включать вспомогательные вещества, такие как консерванты, стабилизаторы, эмульгаторы или суспендирующие агенты, смачивающие агенты, соли для варьирования осмотического давления или буферы, если это требуется.
В другом альтернативном воплощении композиции в соответствии с настоящим изобретением могут вводиться в форме порошка. Например, порошковые назальные композиции могут непосредственно использоваться в виде порошка для единичной дозированной формы. Если это является желательным, то порошок может помещаться в капсулы, такие как твердые желатиновые капсулы. Содержание капсулы или устрйоства для единичной дозы может вводиться при использовании, например, инсуффлятора. Предпочтительно, когда это обеспечивается при использовании средств, осуществляющих дозирование существенно фиксированного количества композиции/впрыска.
Лекарственное вещество
Настоящее изоретение направлено на композиции для лечения, профилактики или облегчения одного или более симптомов состояния, расстройства или заболевания. В альтернативном воплощении настоящее изобретение направлено на композиции для лечения, профилактики или облегчения одного или более симптомов ринита или любого другого респираторного расстройства. Например, композиции, раскрытые в данной заявке, являются полезными для лечения сезонного аллергического ринита (например, сенной лихорадки) или аллергического и неаллергического (вазомоторного) ринита, длящегося круглый год.
Лекарственные вещества, приемлемые для применения в композициях в соответствии с настоящим изобретением, включают любое фармацевтически приемлемое соединение или любую его производную, включая без ограничения любые соли, сложные эфиры, энол, сложные эфиры энола, кислоты, основания, сольваты или их гидраты. Такие производные могут быть получены специалистом в данной области при использовании известных способов для такой дериватизации. Кроме того, лекарственные вещества для применения в композициях и способах, предлагаемых в данной заявке, включают такие соединения, которые содержат хиральные центры либо (R), либо (S) конфигурации, или их смеси (например, рацемат). Таким образом, лекарственные вещества для применения в композициях, предложенных в данной заявке, включают энантиомерно-чистые соединения, их стереоизомерные или диастереоизомерные смеси. При этом понятно, что хиральные центры лекарственных веществ, предлагаемых в данной заявке, могут подвергаться эпимеризации in vivo. Таким образом, специалист в данной области признает, что введение лекарственного вещества в его (R) форме является эквивалентным для соединений, которые подверглись эпимеризации in vivo, введению соединения в его (S) форме.
Лекарственные вещества, приемлемые для применения в композициях в соответствии с настоящим изобретением, включают без ограничения кортикостероиды, такие как беклометазон и любые его фармацевтически приемлемые производные. Как используется в данной заявке, фармацевтически приемлемые производные беклометазона включают любые соли, сложные эфиры, простые эфиры энола, сложные эфиры энола, кислоты, основания, их сольваты или гидраты. Такие производные могут быть получены специалистом в данной области при использовании известных способов для такой дериватизации. Предпочтительно, когда композиции включают дипропионат беклометазона или его моногидрат. Дипропионат беклометазона имеет химическое наименование 9-хлор-11b, 17,21-тригидрокси-16b-метилпрегна-1,4-диен-3,20-диен-17,21-дипропионат и следующую формулу:

Соединение может представлять собой белый порошок с молекулярным весом 521,25, слабо растворимый в воде (Physicians' Desk Reference. RTM), очень хорошо растворимый в хлороформе и свободно растворимый в ацетоне и спирте.
Профиль распределения размеров частиц
Композиции в соответствии с настоящим изобретением могут включать кортикостероид (например, дипропионат беклометазона), имеющий следующий профиль распределения размеров частиц: приблизительно 10% частиц лекарственного вещества имеют размер частиц приблизительно 0,75 микрона;
приблизительно 25% частиц лекарственного вещества имеют размер частиц меньший, чем 1,5 микрона; приблизительно 50% частиц лекарственного вещества имеют размер частиц, меньший, чем 2 микрона; приблизительно 75% частиц лекарственного вещества имеют размер частиц, меньший, чем 3,5 микрона; приблизительно 90% частиц лекарственного вещества имеют размер частиц, меньший, чем 5 микрон; и больше, чем 90%, или приблизительно 100% частиц лекарственного вещества имеют размер частиц, меньший, чем 10 микрон. Неожиданно было обнаружено, что композиции, содержащие кортикостероид (например, дипропионат беклометазона) и имеющие профиль распределения размеров частиц, попадающий в пределы, приведенных выше интервалов, обеспечивают повышенную биодоступность по сравнению с традиционными композициями, когда вводятся интраназальным путем субъекту, который имеет такую потребность, а также имеют повышенную и длительную эффективность лекарственного средства.
Как используется в данной заявке, размер частиц относится к среднему размеру частиц, как определяется с помощью традиционных методик измерения размеров частиц, которые хорошо известны специалисту в данной области, таких как седиментационный анализ фракционирования потока, фотонкорреляционная спектроскопия или дисковое центрифугирование, среди прочих методик.
В альтернативном воплощении композиция в соответствии с настоящим изобретением включает лекарственное вещество, которое имеет следующий профиль распределения размеров частиц: приблизительно 10% частиц лекарственного вещества имеют размер частиц приблизительно 0,35 микрона;
приблизительно 25% частиц лекарственного вещества имеют размер частиц меньший, чем 0,70 микрона; приблизительно 50% частиц лекарственного вещества имеют размер частиц, меньший, чем 1,25 микрона; приблизительно 75% частиц лекарственного вещества имеют размер частиц, меньший, чем 2,0 микрона; приблизительно 90% частиц лекарственного вещества имеют размер частиц, меньший, чем 3 микрона; и больше, чем 90%, или приблизительно 100% частиц лекарственного вещества имеют размер частиц, меньший, чем 6,5 микрона. Предпочтительно, когда лекарственное вещество представляет собой дипропионат беклометазона.
Композиции в соответствии с настоящим изобретением могут также включать лекарственное вещество, которое имеет следующий профиль распределения размеров частиц: приблизительно 10% частиц лекарственного вещества имеют размер частиц приблизительно 0,75, 0,70, 0,60, 0,55, 0,50, 0,40, 0,35, 0,30, 0,25, 0,20, 0,15, 0,10 или 0,05 микрона; приблизительно 25% частиц лекарственного вещества имеют размер частиц меньший, чем 1,5, 1,45, 1,40, 1,35, 1,30, 1,25, 1,20, 1,15, 1,10, 1,05, 1,0, 0,95, 0,90, 0,85, 0,80, 0,75, 0,70, 0,65, 0,60, 0,55, 0,50, 0,45, 0,40, 0,35, 0,30, 0,25, 0,20, 0,15 или 0,10 микрона; приблизительно 50% частиц лекарственного вещества имеют размер частиц, меньший, чем 2,5, 2,4, 2,3, 2,2, 2,1, 2,0, 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,2, 1,1, 0,9, 0,8, 0,7 или 0,6 микрона. Приблизительно 75% частиц лекарственного вещества имеют размер частиц, меньший, чем 3,5, 3,4, 3,3, 3,2, 3,1, 3,0, 2,9, 2,8, 2,7, 2,6, 2,5, 2,4, 2,3, 2,2, 2,1, 2,0, 1,9, 1,8, 1,7, 1,6, 1,5 или 1,4 микрона; приблизительно 90% частиц лекарственного вещества имеют размер частиц, меньший, чем 5,0, 4,9, 4,8, 4,7, 4,6, 4.5, 4,4, 4,3, 4,2, 4,1, 4,0, 3,9, 3,8, 3,7, 3,6, 3,5, 3,4, 3,3, 3,2, 3,1, 3,0, 2,9, 2,8, 2,7, 2,6, 2,5, 2,4, 2,3, 2,2 или 2,1 микрона; и больше, чем 90%, или приблизительно 100% частиц лекарственного вещества имеют размер частиц, меньший, чем 10, 9,5, 9,0, 8,5, 8,0, 7,5, 6,5, 6,0, 5,5, 5,0, 4,5 или 4,0 микрона.
В одном предпочтительном воплощении настоящее изобретение включает лекарственные вещества, обладающие следующим профилем распределения размеров частиц: приблизительно 10% частиц лекарственного вещества имеют размер частиц приблизительно 0,4 микрона; приблизительно 25% частиц лекарственного вещества имеют размер частиц меньший, чем 0,70 микрона; приблизительно 50% частиц лекарственного вещества имеют размер частиц, меньший, чем 1,3 микрона; приблизительно 75% частиц лекарственного вещества имеют размер частиц, меньший, чем 2,0 микрона; приблизительно 90% частиц лекарственного вещества имеют размер частиц, меньший, чем 3 микрона; и больше, чем 90%, или приблизительно 100% частиц лекарственного вещества имеют размер частиц, меньший, чем 6,5 микрона.
В другом альтернативном воплощении композиция в соответствии с настоящим изобретением включает лекарственное вещество, обладающее следующим профилем распределения размеров частиц: приблизительно 10% частиц лекарственного вещества имеют размер частиц приблизительно 0,60 микрона; приблизительно 25% частиц лекарственного вещества имеют размер частиц меньший, чем 0,90 микрона; приблизительно 50% частиц лекарственного вещества имеют размер частиц, меньший, чем 1,5 микрона; приблизительно 75% частиц лекарственного вещества имеют размер частиц, меньший, чем 2,5 микрона; приблизительно 90% частиц лекарственного вещества имеют размер частиц, меньший, чем 3,5 микрона; и больше, чем 90%, или приблизительно 100% частиц лекарственного вещества имеют размер частиц, меньший, чем 6,0 микрон.
В другом альтернативном воплощении больше, чем 90%, или приблизительно 100% частиц имеют размер частиц меньший, чем 15 микрон, предпочтительно, меньший, чем 10 микрон, более предпочтительно, меньший, чем 8 микрон, наиболее предпочтительно, меньший, чем 7 микрон. В другом предпочтительном воплощении больше, чем 90%, или приблизительно 100% частиц имеют размер частиц в интервале от 4 до 7 микрон или от 5 до 6 микрон. В другом воплощении больше, чем 90%, или приблизительно 100% частиц имеют размер частиц меньший, чем 10 микрон, предпочтительно, меньший, чем 7 микрон, меньший, чем 6 микрон, меньший, чем 5 микрон или меньший, чем 4 микрона.
В одном альтернативном воплощении такие водные суспензионные композиции являются приемлемыми для непосредственного введения субъекту через нос и представляют собой улучшенный способ по сравнению с традиционными методиками для введения лекарственных веществ интраназально, в частности, беклометазона. Так благодаря специфическому профилю распределения размеров частиц лекарственного вещества композиции в соответствии с изобретением обеспечивают повышенную биодоступность лекарственного вещества, а также улучшенную эффективность и/или длительный терапевтический эффект лекарственного вещества.
Композиция в соответствии с настоящим изобретением может обеспечиваться в виде водной суспензии. Как используется в данной заявке, суспензия включает без ограничения смеси мелких частиц твердого вещества, не образующих осадка, в жидкой фазе. В одном воплощении композиция в соответствии с настоящим изобретением представляет собой водную суспензию, содержащую от приблизительно 0,005 мас.% до 10 мас.% лекарственного вещества в пересчете на сухую основу. В альтернативном воплощении лекарственное вещество представляет собой беклометазон.
В другом альтернативном воплощении композиция в соответствии с настоящим изобретением представляет собой водную суспензию, содержащую от приблизительно 0,005 мас.% до приблизительно 5 мас.% или от 0,01 мас.% до приблизительно 2,5 мас.% лекарственного вещества в пересчете на сухую основу. В предпочтительном воплощении композиция представляет собой водную суспензию, содержащую от приблизительно 0,025 мас.% до приблизительно 1,0 мас.% лекарственного вещества в пересчете на сухую основу, которая обладает частным профилем распределения размеров частиц в соответствии с настоящим изобретением, при этом лекарственное вещество предпочтительно представляет собой беклометазон. Еще более предпочительно, когда композиция представляет собой водную суспензию, содержащую от приблизительно 0,04 мас.% до приблизительно 0,05 мас.% лекарственного вещества в пересчете на сухую основу. В предпочтительном воплощении лекарственное вещество представляет собой дипропионат беклометазона.
В препочтительном воплощении композиция в соответствии с изобретением представляет собой водную суспензию, содержащую приблизительно 0,042 мас.% дипропионата беклометазона в пересчете на сухую основу, при этом дипропионат беклометазона имеет следующий интервал профиля распределения размеров частиц: приблизительно 10% частиц лекарственного вещества имеют размер частиц приблизительно 0,35 микрона; приблизительно 25% частиц лекарственного вещества имеют размер частиц меньший, чем 0,65 микрона;
приблизительно 50% частиц лекарственного вещества имеют размер частиц, меньший, чем 1,20 микрона; приблизительно 75% частиц лекарственного вещества имеют размер частиц, меньший, чем 1,9 микрона; приблизительно 90% частиц лекарственного вещества имеют размер частиц, меньший, чем 2,85 микрона; и больше, чем 90%, или приблизительно 100% частиц лекарственного вещества имеют размер частиц, меньший, чем 6 микрон.
В одном альтернативном воплощении назальная композиция в соответствии с настоящим изобретением может включать консервант, суспендирующий агент, смачивающий агент, агент для регулирования тоничности и/или разбавитель. В одном воплощении композиции, предлагаемые в данной заявке, могут включать от приблизительно 0,01 мас.% до приблизительно 90 мас.% или от приблизительно 0,01 мас.% до приблизительно 50 мас.%, или от приблизительно 0,01 мас.% до приблизительно 25 мас.%, или от приблизительно 0,01 мас.% до приблизительно 10 мас.%, или от приблизительно 0,01 мас.% до приблизительно 5 мас.% одного или более фармакологически приемлемых суспендирующих жидкостей, которые являются физиологически приемлемыми при введении интраназально. Фармакологически приемлемые жидкости для применения в данной заявке включают без ограничения полярные растворители, включая без ограничения соединения, которые содержат гидроксильные группы или другие полярные группы. Растворители включают без ограничения воду или спирты, такие как этанол, изопропанол, а также гликоли, включая пропиленгликоль,, полиэтиленгликоль, полипропиленгликоль, гликолевый простой эфир, глицерин и спирты полиоксиэтилена. Полярные растворители также включают протонные растворители, включая без ограничения воду, водные солевые растворы с одной или более фармацевтически приемлемой(мыми) солью(солями), спирты, гликоли или их смеси. В одном альтернативном воплощении вода для применения в настоящих композициях будет соответствовать или превышать приемлемые регуляторные требования для применения в лекарственных средствах, которые вводятся путем ингаляции.
В некоторых воплощениях данной заявки композиции в соответствии с настоящим изобретением имеют значение рН от приблизительно 2,0 до приблизительно 9,0. Необязательно композиции в соответствии с настоящим изобретением могут содержать буфер рН. Например, буфер может содержать любые известные фармакологически приемлемые буферы, которые являются физиологически приемлемыми для интраназального введения. Буфер может прибавляться для поддержания значения рН композиции, например, от приблизительно 3,0 до приблизительно 7,0.
Стерильность или адекватная защита от микроорганизмов может обеспечиваться как часть настоящих композиций. Поскольку определенные композиции в соответствии с настоящим изобретением предназначены для введения интраназально, то является препочтительным, чтобы они были свободными от патогенных организмов. Преимущество стерильных жидких суспензий заключается в том, что они снижают возможность попадания загрязняющих веществ к индивидууму, когда суспензионная композиция вводится интраназально, снижая, таким образом, вероятность оппортунистической инфекции. Процессы, которые можно рассматривать как приемлемые для достижения стерильности, могут включать любые стерилизационные этапы, известные в области техники. В одном воплощении лекарственное вещество (например, беклометазон) получают в стерильных условиях, микронизацию осуществляют в стерильной окружающей среде, смешивание и упаковку осуществляют в стерильных условиях. В альтернативном воплощении композиции в соответствии с настоящим изобретением могут стерильно фильтроваться и вноситься во флаконы, включая флаконы для единичной дозы, обеспечивающие стерильные единичные дозы композиции, которые используются, например, в устройстве для назальных аэрозолей. Каждый флакон с единичной дозой может быть стерильным и приемлемым образом вводится, не затрагивая других флаконов или следующей дозы. В другом альтернативном воплощении один или более ингредиентов в данной композиции могут быть стерилизованы паром, с помощью гамма-радиации или могут быть приготовлены при использовании или смешивании стерильного порошка стероидов и других стерильных ингредиентов в случае, если это является приемлемым. Композиции могут быть получены и подвергнуты обработке в стерильных условиях или могут быть простерилизованы перед упаковыванием или после упаковывания.
В дополнение к или вместо стерилизации композиции в соответствии с настоящим изобретением могут содержать фармацевтически приемлемый консервант для минимизации возможности микробного загрязнения. Кроме того, фармацевтически приемлемый консервант может использоваться в настоящих композициях для увеличения стабильности композиции. Следует заметить, однако, что для безопасности ингаляции должен быть выбран любой консервант, поскольку обрабатываемые ткани могут быть чувствительными к раздражителям. Консерванты, приемлемые для применния в данной заявке, включают без ограничения те, которые защищают раствор от контаминации патогенными частицами, включая фенилэтиловый спирт, хлорид бензалкония, бензойную кислоту или бензоаты, такие как бензоат натрия. Предпочтительно, когда консерванты для применения в настоящих композициях представляют собой хлорид бензалкония или фенилэтиловый спирт.В некоторых воплощениях композиции в соответствии с данным изобретением включают от приблизительно 0,01 мас.% до приблизительно 1,0 мас.% хлорида бензалкония, или от приблизительно 0,01% до приблизительно 1,0% об./мас. фенилэтилового спирта. Консервирующие агенты могут также присутствовать в количестве от приблизительно от приблизительно 0,01% до приблизительно 1,0%, предпочтительно от приблизительно 0,002% до приблизительно 0,02% от общего веса или объема композиции.
Композиции, предлагаемые в данной заявке, могут также содержать от приблизительно 0,01 мас.% до приблизительно 90 мас.% или от приблизительно 0,01 мас.% от приблизительно 50 мас.%, или от приблизительно 0,01 мас.% до приблизительно 25 мас.%, или от приблизительно 0,01 мас.% до приблизительно 10 мас.%, или от приблизительно 0,01 мас.% до приблизительно 1 мас.% одного или более эмульгирующего агента, смачивающего или суспендирующего агента. Такие агенты для применения в данной заявке включают без ограничения жирные эфиры полиоксиэтиленсорбита или полисорбаты, включая без ограничения полиэтиленсорбитмоноолеат (полисорбат 80), полисорбат 20 (полиоксиэтилен (20) сорбитмонолаурат), полисорбат 65 (полиоксиэтилен (20) сорбиттристеарат), полиоксиэтилен (20) сорбитмоноолеат, полиоксиэтилен (20) сорбитмонопальмитат, полиоксиэтилен (20) сорбитмоностеарат; лецитины, альгиновую кислоту; альгинат натрия; альгинат калия; альгинат кальция; альгинат аммония, пропан-1,2-диолальгинат; агар; ирландский мох; камедь плодов рожкового дерева; гуаровую камедь; трагакант; гуммиарабик, ксантановую камедь; караевую камедь; пектин; амидированный пектин; фосфатиды аммония; микрокристаллическую целлюлозу; метилцеллюлозу; гидроксипропилцеллюлозу; гидроксипропилметилцеллюлозу; этилметилцеллюлозу; карбоксиметилцеллюлозу; соли жирных кислот натрия, калия, кальция; моно- и диглицериды жирных кислот; сложные эфиры уксусной кислоты и моно- и диглицериды жирных кислот; сложные эфиры молочной кислоты и моно- и диглицеридов жирных кислот; сложные эфиры уксусной кислоты и моно- и диглицериов жирных кислот; сложные эфиры молочной кислоты и моно- и диглицериов жирных кислот; сложные эфиры лимонной кислоты и моно- и диглицеридов жирных кислот; сложные эфиры винной кислоты и моно- и диглицеридов жирных кислот; сложные эфиры моно- и диацетилвинной кислоты и моно- и диглицеридов жирных кислот; сложные эфиры смешанных уксусной и винной кислоты и моно- и диглицеридов жирных кислот; сложные эфиры сахарозы и жирных кислот; сахарозаглицериды; полиглицериновые сложные эфиры жирных кислот; сложные полиглицериновые эфиры поликонденсированных жирных кислот касторового масла; пропан-1,2-диоловые сложные эфиры жирных кислот; стеароил-2-лактилат натрия; стеароил-2-лактилат кальция; стеароил тартрат; сорбитмоностеарат; сорбиттристеарат; сорбитмонолаурат; сорбит моноолеат; сорбитмонопальмитат; экстракт килайи; сложные эфиры полиглицерина и димеризованных жирных кислот масла соевых бобов; окислительно полимеризованное масло соевых бобов и пектиновый экстракт. В некоторых воплощениях в данной заявке предлагаемые композиции включают полисорбат 80, микрокристаллическую целлюлозу, карбоксиметилцеллюлозу натрия и/или декстрозу.
Композиции в соответствии с настоящим изобретением включают от приблизительно 0,01% до приблизительно 90% или от приблизительно 0,01% до приблизительно 50%, или от приблизительно 0,01% до приблизительно 25%, или от приблизительно 0,01% до приблизительно 10%, или от приблизительно 0,01% до приблизительно 1% одного или более наполнителей и добавок, которые являются фармакологически приемлемыми. Наполнители и добавки обычно не имеют фармакологической активности или, по крайней мере, не имеют нежелательной фармакологической активности. Их концентрация может варьировать в зависимости от выбранного агента, несмотря на то, что присутствие или отсутствие этих агентов или их концентрация не является существенной чертой изобретения. Наполнители и добавки могут включать без ограничения сурфактанты, смачивающие агенты, стабилизаторы, комплексирующие агенты, антиоксиданты или другие известные в области техники добавки. Комлексирующие агенты включают без ограничения этилендиаминтетрауксусную кислоту (ЭДТА) или ее соль, такую как соль динатрия, лимонную кислоту, нитрилтриуксусную кислоту и их соли. В другом воплощении композиции содержат эдетат натрия в концентрации от приблизительно 0,05 мг/мл до приблизительно 0,5 мг/мл или от приблизительно 0,1 мг/мл до приблизительно 0,2 мг/мл. Композиции в соответствии с настоящим изобретением могут также, например, включать от приблизительно 0,001 мас.% до приблизительно 5 мас.% увлажнителя для ингибирования высушивания слизистой оболочки и предотвращения раздражения. Может использоваться любой из разнообразия фармацевтически приемлемых увлажнителей, включая, например, сорбит, пропиленгликоль, полиэтиленгликоль, глицерин или их смеси.
Композиции, предлагаемые в данной заявке, могут также содержать от приблизительно 0,01% до приблизительно или от приблизительно 0,01% до приблизительно 50%, или от приблизительно 0,01% до приблизительно 25%, или от приблизительно 0,01% до приблизительно 10% одного или более растворителей или сорастворителей для увеличения растворимости любого из компонентов настоящей композиции. Растворители или сорастворители для применения в данной заявке включают без ограничения гидроксилированные растворители или другие фармацевтические полярные растворители, такие как спирты, включая изопропиловый спирт, гликоли, такие, как пропиленгликоль, полиэтиленгликоль, полипропиленгликоль, гликолевый эфир, глицерин и спирты полиоксиэтилена. В другом воплощении композиции в соответствии с настоящим изобретением могут включать один или более традиционных разбавителей, известных в области техники. Предпочтительный растворитель представляет собой воду.
Агенты для регулирования тоничности могут включать без ограничения хлорид натрия, хлори калия, хлорид цинка, хлорид кальция и их смеси. Другие агенты, регулирующие осмотическое давление, могут также включать без ограничения маннит, глицерин, декстрозу и их смеси. В альтернативном воплощении композиция в соответствии с изобретением могут содержать от приблизительно 0,01 мас.% до приблизительно 10 мас.% или от приблизительно 1 мас.% до приблизительно 8 мас.%, или от 1 мас.% до приблизительно 6,0 мас.%, препочтительно приблизительно 5 мас.% агента для регуляции осмотического давления. Предпочтительный агент для регуляции тоничности представляет собой безводную декстрозу.
В одном альтернативном воплощении композиции в соответствии с настоящим изобретением являются стабильными. Как используется в данной заявке, стабильность композиций, предлагаемых в данной заявке, относится к продолжительности времени при данной температуре, когда в композиции присутствует больше, чем 80%, 85%, 90% или 95% от исходного количества лекарственного вещества, например, беклометазона. Например, композиции, предлагаемые в данной заявке могут храниться при температуре от приблизительно 15°С до приблизительно 30°С и оставаться стабильными, по крайней мере, 1, 2, 12, 18, 24 или 36 месяцев. Кроме того, композиции могут быть приемлемыми для введения субъекту, который в этом нуждается, после их хранения в течение более чем 1, 2, 12, 18, 24 или 36 месяцев при температуре 25°С. Кроме того, в другом альтернативном воплощении при использовании кинетики Аррениуса установлено, что более чем 80% или более чем 85%, или более чем 90%, или более чем 95% исходного количества лекарственного вещества (например, беклометазона) сохраняется после хранения композиций более чем 1, 2, 12, 18, 24 или 36 месяцев при температуре от приблизительно 15°С до приблизительно 30°С.
Композиции по настоящему изобретению могут быть получены любым традиционным способом путем тщательного перемешивания ингредиентов, описанных в данной заявке при комнатной темпераутре или температуре, которая выше комнатной, для того, чтобы достичь растворения ингредиентов, если это является приемлемым.
Препарат лекарственного вещества, которое имеет профиль распределения размеров частиц в соответствии с настоящим изобретением, может быть получен с помощью традиционных способов, известных в уровне техники или с помощью незначительной модификации таких способов. Например, суспензии лекарственных частиц могут подвергаться быстрому уменьшению размеров частиц при использовании методики струйной мельницы (модель жидкостного дробления при высоком давлении). Другие известные способы для уменьшения размеров частиц в микрометрическом интервале включают механическое дробление, применение энергии ультразвука и других методик.
В другом альтернативном воплощении настоящее изобретение обеспечивает способ лечения ринита, который предусматривает этап введения субъекту, который в этом нуждается, терапевтически эффективного количества композиций, описанных в данной заявке. В одном воплощении способ по настоящему изобретению включает введение субъекту, который в этом нуждается, терапевтически эффективного количества лекарственного вещества, при этом лекарственное вещество представляет собой беклометазон и имеет профиль распределения размеров частиц, описанный в данной заявке. Предпочтительно, когда лекарственное вещество представляет собой дипропионат беклометазона. В некоторых воплощениях субъект представляет собой млекопитающее. В других воплощениях субъект представляет собой человека.
В одном воплощении настоящее изобретение обеспечивает способ лечения ринита, включающий этап введения субъекту, который в этом нуждается, терапевтически эффективного количества предлагаемой композиции, где композиция содержит водную суспензию, включающую от приблизительно 0,005 мас.% до приблизительно 5 мас.% беклометазона, и которая имеет профиль распределения размеров частиц, описанный в данной заявке. В некоторых воплощениях композиция является стерильной, содержит консервант и/или является стабильной.
В других воплощениях настоящее изобретение обеспечивает способ лечения ринита, предусматривающий этап введения композиций, описанных в данной заявке, интраназально субъекту с помощью назального аэрозоля, предпочтительно с помощью насоса для распыления отмеренной дозы. Насос для распыления отмеренной дозы может управляться вручную, так, что каждое приведение насоса в действие обеспечивает доставку одной дозы лекарственного вещества субъекту. В другом воплощении композиция в соответствии с настоящим изобретением может вводиться с помощью назального распылительного насоса или микронизирующего распылительного насоса.
В другом альтернативном воплощении назальный аэрозоль включает отмеренную дозу, аэрозольную единицу, испускаемую ручным аэрозольным насосом (например, отмеривающим микронизирующим насосом), которая включает микрокристаллическую суспензию дипропионата беклометазона, моногидрата, эквивалентную от 0,02 мас.% до приблизительно 2,0 мас.%, предпочтительно от приблизительно 0,10 мас.% до приблизительно 0,05 мас.%, более предпочтительно приблизительно 0,042 мас.% дипропионата беклометазона в пересчете на сухую основу, в водной среде. В другом альтернативном воплощении указанная суспензия включает микрокристаллическую целлюлозу, карбоксиметилцеллюлозу натрия, декстрозу, хлорид бензалкония, полисорбат 80 и 0,25% об./мас. фенилэтилового спирта. Кислота, предпочтительно соляная кислота, может прибавляться для регулирования pH. Значение pH может лежать в пределах от 4,5 до 7,0. После исходного прокачивания (3-4 срабатывания) каждое приведение в действие ручного насоса может доставлять из назального адаптера приблизительно от 10 мг до приблизительно 1000 мг, предпочтительно от приблизительно 100 мг до приблизительно 500 мг, наиболее предпочтительно приблизительно 100 мг суспензии, содержащей дипропионат беклометазона, моногидрат, эквивалентноый количеству от приблизительно 10 мкг до приблизительно 500 мкг или от приблизительно 10 мкг до приблизительно 100 мкг, или от приблизительно 30 мкг до приблизительно 60 мкг, предпочтительно от приблизительно 40 мкг до приблизительно 50 мкг, более предпочтительно приблизительно 42 мкг дипропионата беклометазона в пересчете на сухую основу. Каждая бутылочка, содержащая композиции в соответствии с настоящим изобретением для назального аэрозоля, может обеспечивать приблизительно 20-600 отмеренных доз, предпочтительно от 100 до приблизительно 300 доз, более предпочтительно, по крайней мере, 200 отмеренных доз.
В альтернативном воплощении введение композиций в соответствии с настоящим изобретением может включать 1, 2, 3, 4, 5, 6, 7 или 8 ингаляций настоящей композиции в каждую ноздрю один, два, три, четыре или пять раз в день. Каждая ингаляция может содержать от приблизительно 1 мкг до приблизительно 400 мкг или приблизительно от 1 мкг до приблизительно 100 мкг, предпочтительно от приблизительно 30 мкг до приблизительно 100 мкг, более предпочтительно от приблизительно 30 мкг до приблизительно 80 мкг, или от приблизительно 30 мкг до приблизительно 50 мкг, наиболеее предпочтительно приблизительно 42 мкг. Общая суточная доза лекарственного вещества может включать от приблизительно 10 мкг до приблизительно 4000 мкг, от приблизительно 10 мкг до приблизительно 1000 мкг, от приблизительно 10 мкг до приблизительно 500 мкг, или от приблизительно 100 мкг до прилизительно 900 мкг, предпочтительно от приблизительно 100 мкг до приблизительно 500 мкг, или более предпочтительно от приблизительно 150 мкг до приблизительно 400 мкг.
В другом альтернативном воплощении введение настоящей композиции может включать одну и только одну ингаляцию в каждую ноздрю в день. В одном альтернативном воплощении исходная доза настоящей композиции может включать одну и только одну ингаляцию в каждую ноздрю один раз в день. В другом альтернативном воплощении такая исходная доза является приемлемой для взрослых. Каждая ингаляция может включать от приблизительно 5 мкг до приблизительно 100 мкг, предпочтительно от приблиизительно 30 мкг до 70 мкг, более предпочтительно приблизительно 42 мкг беклометазона в пересчете на сухую основу.
Введение одной и только одной ингаляции в каждую ноздрю является более благоприятным и предпочтительным по сравнению с традиционными режимами в соответствии с уровнем техники, которые требуют больше ингаляций в каждую ноздрю в сутки. Например, другие известные назальные аэрозоли, например, продукты на основе беклометазона, требуют 1 или 2 ингаляций (от 42 до 84 мкг) в каждую ноздрю два раза в сутки (общая доза составляет 168-336 мкг/сутки). В противовес этому, композиции в соответствии с настоящим изобретением могут требовать осуществления одной или толькой одной ингаляции в каждую ноздрю в сутки. Путем снижения дозы или количества ингаляций в сутки индивидууму, вероятно, было бы возможно соблюдать режим или расписание введения регулярных доз для достижения адекватного ослабления и, таким образом, улучшения качества жизни пациента по сравнению с другими традиционными режимами. Кроме того, введение меньшего количества ингаляций обеспечивает индивидууму больше возможности для осуществления других медикаций во время лечения, таких, как, например, введение других стероидов, которые вводятся перорально или в форме ингаляции, снижая, таким образом, вероятность передозировки или перекрестной реакции между лекарственными средствами. Кроме того, обеспечение меньшего количества ингаляций будет снижать вероятность привыкания к лекарственному средству в назальной композиции. Более того, осуществление меньшего количества ингаляций может снизить токсичность и неблагоприятные события, которые ассоциируются с двумя или более ингаляциями конкретного лекарственного вещества в каждую ноздрю в сутки. Индивидуумы, обладающие гиперчувствительностью к двум или более дозам конкретного лекарственного вещества, также получат выгоду от приема одной и только одной дозы в сутки.
Настоящие композиции могут быть упакованы как наборы или системы, которые необязательно содержат другие компоненты, включая инструкции по применению композиций. Изделия, являющиеся полезными для лечения, предотвращения или облегчения одного или более симптомов медицинского состояния, расстройства или заболевания (например, ринита), содержат упаковочный материал и композицию в нем, а также этикетку, указывающую на то, что композиция используется для лечения, предотвращения или облегчения одного или более симптомов заболеваний или расстройств, ассоциированных с нежелательным и/или неконтролируемым ринитом.
VI. Пример
Следующий пример включен только с иллюстративной целью и не предназначен для ограничения объема изобретения.
Двойное слепое, войное холостое рандомизированное, плацебо-контролируемое исследование осуществляли для оценки безопасности и эффективности композиций в соответствии с настоящим изобретением (Dey BD) у подростков и взрослых пациентов с сезонным аллергическим ринитом. Задачами этого исследования было (1) определить безопасность и эффективность Dey BD по сравнению с плацебо на протяжении 2 недель лечения у взрослых и подростков с сезонным аллергическим ринитом (SAR); и (2) установить сравнимость Dey BD с назальным аэрозолем Beconase AQ® в течение 2 недель лечения у взрослых пациентов и подростков. В настоящее время Beconase AQ® является коммерчески доступной от GlaxoSmithKlein.
Как Dey, так и Beconase AQ® включали микрокристаллическую суспензию дипропионата беклометазона, моногидрата, эквивалентную 0,042 мас.% дипропионата беклометазона в пересчете на сухую основу, в водной среде. Однако беклометазон, используемый в назальном аэрозоле Dey BD, был получен и/или закуплен из источника, отличного от такового, который использовался для Beconase AQ®. В противовес этому, оба назальных аэрозоля содержали одинаковые наполнители и добавки в тех же количествах. Кроме того, назальный аэрозоль Dey BD и Beconase AQ® вводили в тех же отмеренных дозах с помощью аэрозольного устройства с ручным насосом. Как для назального аэрозоля Dey BD, так и для Beconase AQ® каждая активация ручного насоса доставляла приблизительно 42 мкг дипропионата беклометазона.
Изучение осуществляли в период аллергического сезона осени 2001 года (местная осенняя пыльца) в США. Длительность исследования составляла 3 недели и исследование состояло из 2 фаз: за базовым периодом скрининга длительностью 1 неделя шла двухнедельная фаза рандомизированного двойного слепого лечения пациентов. Пациентов наблюдали на амбулаторной основе в День - 7, День 7, День 14. Оценки исходных базовых линий осуществляли за одну неделю до рандомизации лечения (День - 7±2 дня). Пациентам сначала присваивали номер, а потом подвергали скринингу на пригодность на основе изучения критериев вступления в исследование и осуществления оценки базовой линии. В случае пригодности пациенты получали оральный стандартный антигистаминовый препарат как экстренную спасательную медикацию и дневник значения общего назального симптома у пациента (TNSS). Пациенты ежедневно регистировали TNSS (сумма признаков и симптомов для выделений из носа, заложенности носа, чихания и зуда в носу) и их ежедневные значения в пределах от 0 до 3, при этом 0 регистрировали в случае отсутствия симптомов, а 3 в случае наличия тяжелых симптомов, а также регистрировали количество принятого перорально антигистаминового средства. Через неделю при наличии заключения базовой оценки пациенты возвращались в место исследования и повторно оценивались на пригодность. Пациенты, которые не заполняли дневников или более не соответствовали критериям включения/исключения, были исключены из исследования.
Для того чтобы быть включенными в исследование, пациенты должны были быть продиагностированы как таковые с SAR и должны были соответствовать следующим критериям включения в исследование:
- по крайней мере, двухгодичная история от слабого до умеренного SAR, вызванного осенней пыльцой;
- индивидуумы в возрасте 12 лет и более;
- подтвержденная IgE-опосредованная гиперчувствительность к местной осенней пыльце в течение последних 12 месяцев (необходим позитивный результат);
- минимальное TNSS 8 и максимальное 12 в течение, по крайней мере, 3 дней во время базового периода, один из которых должен находится в пределах 3 дней от Дня 1;
- при получении иммунотерапии стабильный режим поддержания в течение 30 дней перед включением в исследование;
- хорошее общее состояние здоровья и отсутствие заболеваний или сопутствующего лечения, которое может препятствовать интерпретации результатов исследования;
- письменное согласие/согласование с педиатром; и
- готовность выполнять процедуры исследования.
Пациенты, которые соответствовали всем критериям, были потом грубо отобраны в одну из 5 групп лечения: (1) Dey BD назальный аэрозоль (0,042%), низкая доза - 1 впрыск из бутылочки 1 (Dey BD) в каждую ноздрю, после чего осуществляли 1 впрыск из бутылочки 2 (плацебо) в каждую ноздрю два раза в день (утро и вечер); (2) Dey BD назальный аэрозоль (0,042%), высокая доза - 1 впрыск из бутылочки 1 (Dey BD) в каждую ноздрю, после чего осуществляли 1 впрыск из бутылочки 2 (Dey BD) в каждую ноздрю два раза в день (утро и вечер); (3) Beconase AQ®, низкая доза - 1 впрыск из бутылочки 1 (Beconase AQ®) в каждую ноздрю, после чего осуществляли один впрыск из бутылочки 2 (плацебо) в каждую ноздрю два раза в день (утро и вечер); (4) Beconase AQ®, высокая доза - 1 впрыск из бутылочки 1 (Beconase AQ®) в каждую ноздрю, после чего осуществляли 1 впрыск из бутылочки 2 (Beconase AQ®) два раза в день (утро и вечер); и (5) плацебо - 1 впрыск из бутылочки 1 (плацебо в каждую ноздрю, после чего осуществляли 1 впрыск из бутылочки 2 (плацебо) в каждую ноздрю два раза в день (утро и вечер).
Фаза двойного слепого лечения (Дни с 1 по 14) состояла из двухразовых ежедневных самостоятельных введений (1 впрыск из кажой бутылочки в каждую ноздрю на введение. На День 7 и День 14 (или в более ранний период окончания) пациенты возвращались в место исследования и повергались оценке. Оценки эффективности включали ежедневну суточную рефлективную и немедленную информацию, общие оценки пациента и лечащего врача и применение экстренной спасательной медикации.
Первичной конечной точкой для этого лечения было изменение базовой линии 12-часового (объединенные AM и РМ) рефлективного TNSS в течение 2-недельного периода лечения. Анализ первичной конечной точки представлял собой сравнение Dey BD, высокая доза, против плацебо. TNSS состояло из суммы 12-часовых оценок для выделений из носа, закладывания носа, чихания и зуда в носу, которые регистрировались два раза в день в ежедневной карте TNSS пациента. Базовую линию определяли как среднее значение 12-часового периода изучения (объединенные значения AM плюс РМ) рефлективного TNSS из 7 календарных дней ±2 дня, предшествующих Дню 1.
Вторичные конечные точки для этого исследования были следующими:
- изменение по сравнению с базовой линией объединенных AM плюс РМ 12-часового рефлективного общего TNSS (Дни 2-14) пациентов;
- изменение по сравнению с базовой линией объединенных AM плюс РМ 12-часового рефлективного TNSS в Дни 7 и 14 пациентов;
- изменение по сравнению с базовой линией AM 12-часового рефлективного TNSS пациентов;
- изменение по сравнению с базовой линией РМ 12-часового рефлективного TNSS пациентов;
- изменение по сравнению с базовой линией 1- и 2-недельной постбазовой линии для площади под кривой концентрации (AUC) объединенных значений AM плюс РМ 12-часового рефлективного TNSS пациентов;
- изменение по сравнению с базовой линией 1- и 2-недельной постбазовой линии для AUC AM 12-часового рефлективного TNSS пациентов;
- изменение по сравнению с базовой линией 1- и 2-недельной постбазовой линии для AUC РМ 12-часового рефлективного TNSS пациентов;
- изменение по сравнению с базовой линией объединенных AM плюс РМ немедленного TNSS у пациентов;
- изменение по сравнению с базовой линией AM немедленного TNSS у пациентов;
- изменение по сравнению с базовой линией РМ немедленного TNSS у пациентов;
- общая оценка пациентом изменения в признаках SAR и симптомах;
- общая оценка лечащим врачом изменения в признаках SAR и симптомах;
- применение экстренной спасательной медикации.
Вторичные конечные точки эффективности сравнивали по всем группам лечения.
В отношении эффективности как рефлективного, так и немедленного изменения по сравнению с базовой линией 12-часового периода (объединенных AM плюс РМ индивидуумов) TNSS для первичных переменных на Неделе 1 и Неделе 2 сравнивали между группам при использовании анализа смешанного эффекта вариантной (ANOVA) модели. Площадь под кривой (AUC) 12-часового периода (AM плюс РМ, объединенных и индивидуальных) рефлективного TNSS подсчитывали для периода базовой линии, Недели 1 и Недели 2 (в течение Дней 2-14) постбазовой линии при использовании трапезоидального метода. Изменение по сравнению с базовой линией сравнивали между группам при использовании подобной модели ANOVA. Общую оценку пациентом и лечащим врачом изменения по сравнению с базовой линией в отншении SAR симптомов сравнивали между группами при использовании однонаправленной модели ANOVA. Частота применения экстренной спасательной медикации, а также процент пациентов, для которых была необходима экстренная спасательная медикация, сравнивали межу группами при использовании точного анализа Фишера. Среднее число таблеток экстренной спасательной медикации сравнивали при использовании модели ANOVA. Все статистические анализы осуществляли как для популяции, имеющей намерение лечиться (ITT), так и для популяции в соответствии с прописью. Отсутствующие наблюдения в популяции ITT оценивали при использовании метода последнего наблюдения, перенесенного на другой счет (LOCF). Все выведенные статистические сведения получали против двусторонней альтернативной гипотезы при уровне значимости 0,05.
Общее количество 674 пациента случайно распределяли в 1-5 группы лечения (136 Dey BD, высокая доза, 136 Dey BD, низкая доза, 135 Beconase AQ®, высокая доза, 129 Beconase AQ®, низкая доза или 138 группа плацебо); 661 (98,7%) пациентов заканчивали исследование, а 13 (1,93%) пациентов прерывали исследование. Наиболее частыми причинами прерывания исследования были АЕ и отказ от согласия. Более чем 85% популяции пациентов, были белокожими людьми, более чем 60% были особями женского пола со средним значением возраста в группах, которое колеблется от 33,62 до 36,79 лет, среднее значение определения реакции на введение провокационного антигена колебалось от 8,6 до 9,4 мм. Большинство пациентов имело негативную историю применения беклометазона (среднее значение=82,61-87,60%).
Все группы активного лечения (Dey BD и Beconase AQ®) демонстрировали снижение TNSS в течение 2-недельного периода лечения. Несмотря на то, что проверяли эффективность конечной точки (то есть, 12-часового рефлективного TNSS, изменения в отношении AUC), эффект лечения был высокозначимым, как и дневной эффект (р=0,0000), что свидетельствовало об улучшении в отношении TNSS. Как группы Dey BD, так и группы Beconase®, высокая доза, были такими, которые статистически превосходили плацебо для двух анализов конечных точек как первичной, так и вторичной эффективности, которые представляли собой группы лечения Dey В, высокая доза, и Beconase AQ®, низкая доза. Эффекты суточного лечения (в среднем Дни 2-14) и недельного лечения не были статистически значимыми, что свидетельствовало о том, что группы лечения вели себя подобно на протяжении всего периода лечения, за исключением амплитуды улучшения TNSS. Не было статистической разницы между группами Dey BD и Beconase AQ®, низкая доза, для любого из анализов эффективности конечных точек. Однако группа Dey BD, низкая доза, была определена как такая, которая была последовательно статистически превосходящей группу Beconase AQ®, низкая доза, в отношении ослабления симптомов SAR. Результаты анализов в соответствии со списком популяции были параллельными таковым для популяции ITT для всех переменных эффективности.
Фигура 1 показывает изменение по сравнению с базовой линией в AM и РМ рефлективном TNSS в течение времени в популяции ITT на протяжении периода изучения 14 дней. Фигура 2 показывает изменение по сравнению с базовой линией в AM рефлективном TNSS в течение времени в популяции ITT на протяжении периода исследования 14 дней. Фигура 3 показывает изменение по сравнению с базовой линией в РМ рефлективном TNSS в течение времени в популяции ITT на протяжении периода исследования 14 дней. Фигура 4 показывает изменение по сравнению с базовой линией в AM и РМ рефлективном TNSS в течение времени в популяции РР на протяжении периода исследования 14 дней.
На Фигурах 1-4 эффективность назальных композиций выражали как изменение по сравнению с базовой линией (предварительная обработка) в смешанном значении назальных симптомов (например, выделения из носа, чихание, зуд в носу и закладывание носа), которые указаны как общие значения назальных симптомов (TNSS). Изменение по сравнению с базовой линией в значениях TNSS выражали в абсолютных единицах (либо как процент отличия от базовой линии). Используя анализ вариантной модели (ANOVA), получали значение наименьшего среднего квадрата (значение LS) для базовой линии (позитивное значение) и изменение по сравнению с базовой линией (негативное значение, если симптом был улучшен). Более высокое негативное значение наблюдали в значении LS, наиболее высоким было изменение (улучшение) TNSS.
Таблица 1 показывает распределение размеров частиц беклометазона в Dey BD, размер частиц при этом выражен в микронах. Таблица 2 показывает качественный состав Dey BD.
Таблица 2
Количественный состав композиции назального аэрозоля моногидрата дипропионата беклометазона, 0,042%.
Фигуры и приложения в данной заявке проставлены только для иллюстративных целей. Они не предназначеня для ограничения объема изобретения. Кроме того, при этом понятно, что различные изменения и модификации к представленному воплощению, описанному в данной заявке, будут очевидны для специалиста в данной области. Такие изменения и модификации могут быть осуществлены без отступления от духа и буквы настоящего изобретения и без снижения присущих ему преимуществ. Таким образом, предполагается, что такие изменения и модификации охватываются прилагаемыми пунктами. Также изобретение может приемлемым образом включать, состоять или существенно состоять из элементов или этапов, описанных в данной заявке. Кроме того, изобретение, описанное тут, приемлемым образом может включать или может осуществляться при отсутствии любого элемента или этапа, который специфически не раскрыт в данной заявке. Более того, один или более этапов, описанных в данной заявке, могут осуществляться одновременно с другим этапом.
Реферат
Изобретение относится к химико-фармацевтической промышленности, и касается назальных фармацевтических композиций, предназначенных для лечения аллергического ринита, содержащих беклометазон в виде водной суспензии, обладающих специфическим профилем распределения размеров частиц. Такой профиль обеспечивает повышенную биодоступность, улучшенную эффективность или длительный терапевтический эффект фармацевтической композиции при интраназальном введении. 8 н. и 41 з.п. ф-лы, 2 табл., 4 ил.
Формула
(i) 10% частиц имеют размер 0,3 мкм;
(ii) 25% частиц имеют размер, меньший 0,6 мкм;
(iii) 50% частиц имеют размер, меньший 1,1 мкм;
(iv) 75% частиц имеют размер, меньший 1,8 мкм;
(v) 90% частиц имеют размер, меньший 2,7 мкм;
где композиция является приемлемой для интраназального введения на слизистую носа индивидуума.
(а) предварительно упакованную композицию, которая содержит водную суспензию, содержащую от 0,04 до 0,045 мас.% беклометазона в расчете на сухую основу, где беклометазон имеет следующий профиль распределения размеров частиц:
(i) 10% частиц имеют размер, меньший 0,75 мкм;
(ii) 25% частиц имеют размер, меньший 1,5 мкм;
(iii) 50% частиц имеют размер, меньший 2,0 мкм;
(iv) 75% частиц имеют размер, меньший 3,5 мкм;
(v) 90% частиц имеют размер, меньший 5,0 мкм;
где композиция является приемлемой для интраназального введения на слизистую носа индивидуума.
(i) 10% частиц имеют размер, меньший 0,3 мкм;
(ii) 25% частиц имеют размер, меньший 0,6 мкм;
(iii) 50% частиц имеют размер, меньший 1,1 мкм;
(iv) 75% частиц имеют размер, меньший 1,8 мкм;
(v) 90% частиц имеют размер, меньший 2,7 мкм,
где композиция является приемлемой для интраназального введения на слизистую носа индивидуума.
(i) 10% частиц имеют размер, меньший 0,35 мкм;
(ii) 25% частиц имеют размер, меньший 0,65 мкм;
(iii) 50% частиц имеют размер, меньший 1,20 мкм;
(iv) 75% частиц имеют размер, меньший 1,9 мкм;
(v) 90% частиц имеют размер, меньший 2,85 мкм;
(vi) более 90% частиц, имеют размер, меньший 6,0 мкм.
(i) 10% частиц имеют размер, меньший 0,75 мкм;
(ii) 25% частиц имеют размер, меньший 1,5 мкм;
(iii) 50% частиц имеют размер, меньший 2,0 мкм;
(iv) 75% частиц имеют размер, меньший 3,5 мкм;
(v) 90% имеют размер, меньший 5,0 мкм;
(vi) где композиция включает по меньшей мере один комплексирующий агент, выбранный из группы, включающей этилендиаминтетрауксусную кислоту, лимонную кислоту, нитрилтриуксусную кислоту, их соли и эдентат натрия, причем композиция является приемлемой для интраназального введения на слизистую носа индивидуума.
(i) 10% частиц имеют размер, меньший 0,50 мкм;
(ii) 25% частиц имеют размер, меньший 1,0 мкм;
(iii) 50% частиц имеют размер, меньший 1,5 мкм;
(iv) 75% частиц имеют размер, меньший 2,5 мкм;
(v) 90% частиц имеют размер, меньший4,0 мкм.
(i) 10% частиц имеют размер, меньший 0,40 мкм;
(ii) 25% частиц имеют размер, меньший 0,70 мкм;
(iii) 50% частиц имеют размер, меньший 1,30 мкм;
(iv) 75% частиц имеют размер, меньший 2,0 мкм;
(v) 90% частиц имеют размер, меньший 3,0 мкм.
(i) 10% частиц имеют размер, меньший 0,35 мкм;
(ii) 25% частиц имеют размер, меньший 0,65 мкм;
(iii) 50% частиц имеют размер, меньший 1,20 мкм;
(iv) 75% частиц имеют размер, меньший 1,9 мкм;
(v) 90% частиц имеют размер, меньший 2,85 мкм
(vi) больше 90% частиц имеют размер, меньший 6,0 мкм.
(i) 10% частиц беклометазона имеют размер, меньший 0,3 мкм;
(ii) 25% частиц беклометазона имеют размер, меньший 0,6 мкм;
(iii) 50% частиц беклометазона имеют размер, меньший 1,1 мкм;
(iv) 75% частиц беклометазона имеют размер, меньший 1,8 мкм;
(v) 90% частиц беклометазона имеют размер, меньший 2,7 мкм;
(vi) где композиция дополнительно включает комплексирующий агент и указанная композиция является приемлемой для введения индивидууму интраназально.
(i) 10% частиц имеют размер, меньший 0,3 мкм;
(ii) 25% частиц имеют размер, меньший 0,6 мкм;
(iii) 50% частиц имеют размер, меньший 1,1 мкм;
(iv) 75% частиц имеют размер, меньший 1,8 мкм;
(v) 90% частиц имеют размер, меньший 2,7 мкм.
(a) микрокристаллическая целлюлоза;
(b) карбоксиметилцеллюлоза натрия;
(c) декстроза;
(d) хлорид бензалкония;
(e) полисорбат 80 и
(f) фенилэтиловый спирт.
(i) 10% частиц имеют размер, меньший 0,75 мкм;
(ii) 25% частиц имеют размер, меньший 1,5 мкм;
(iii) 50% частиц имеют размер, меньший 2,0 мкм;
(iv) 75% частиц имеют размер, меньший 3,5 мкм;
(v) 90% частиц имеют размер, меньший 5,0 мкм.
(vi) При этом указанная композиция включает по меньшей мере один комплексирующий агент, выбранный из группы, включающей этилендиаминтетрауксусную кислоту, лимонную кислоту, нитрилтриуксусную кислоту, их соли и эдентат натрия, причем композиция является приемлемой для интраназального введения на слизистую носа индивидуума.
(i) 10% частиц имеют размер, меньший 0,40 мкм;
(ii) 25% частиц имеют размер, меньший 0,70 мкм;
(iii) 50% частиц имеют размер, меньший 1,30 мкм;
(iv) 75% частиц имеют размер, меньший 2,0 мкм;
(v) 90% частиц имеют размер, меньший 3,0 мкм.
(i) 10% частиц имеют размер, меньший 0,35 мкм;
(ii) 25% частиц имеют размер, меньший 0,65 мкм;
(iii) 50% частиц имеют размер, меньший 1,20 мкм;
(iv) 75% частиц имеют размер, меньший 1,9 мкм;
(v) 90% частиц имеют размер, меньший 2,85 мкм;
(vi) больше 90% частиц имеют размер, меньший 6,0 мкм.
(i) облегчения одного или более симптомов сезонного аллергического ринита путем введения индивидууму в каждую ноздрю одного и только одного впрыска композиции, включающей водную суспензию, содержащую от 0,01 до 2,5 мас.% беклометазона в расчете на сухую основу и комплексирующий агент, выбранный из группы, включающей этилендиаминтетрауксусную кислоту, лимонную кислоту, нитрилтриуксусную кислоту, их соли и эдентат натрия, при этом указанный впрыск содержит от 5 до 100 мкг беклометазона.
(i) 10% частиц имеют размер, меньший 0,75 мкм;
(ii) 25% частиц имеют размер, меньший 1,5 мкм;
(iii) 50% частиц имеют размер, меньший 2,0 мкм;
(iv) 75% частиц имеют размер, меньший 3,5 мкм;
(v) 90% частиц имеют размер, меньший 5,0 мкм, причем композиция является приемлемой для интраназального введения индивидууму.
(i) 10% частиц имеют размер, меньший 0,50 мкм;
(ii) 25% частиц имеют размер, меньший 1,0 мкм;
(iii) 50% частиц имеют размер, меньший 1,5 мкм;
(iv) 75% частиц имеют размер, меньший 2,5 мкм;
(v) 90% частиц имеют размер, меньший 4,0 мкм.
(i) 10% частиц имеют размер, меньший 0,40 мкм;
(ii) 25% частиц имеют размер, меньший 0,70 мкм;
(iii) 50% частиц имеют размер, меньший 1,30 мкм;
(iv) 75% частиц имеют размер, меньший 2,0 мкм;
(v) 90% частиц имеют размер, меньший 3,0 мкм.
(i) 10% частиц имеют размер, меньший 0,35 мкм;
(ii) 25% частиц имеют размер, меньший 0,65 мкм;
(iii) 50% частиц имеют размер, меньший 1,20 мкм;
(iv) 75% частиц имеют размер, меньший 1,9 мкм;
(v) 90% частиц имеют размер, меньший 2,85 мкм, больше 90% частиц имеют размер частиц, меньший 6,0 мкм.

Комментарии