Микробиологически стабильная фармацевтическая композиция, включающая электрохимически активированный солевой раствор, и ее применение - RU2554802C2
Код документа: RU2554802C2
Описание
Изобретение относится к фармацевтическим композициям, включающим активный ингредиент и носитель, в которых носитель включает водный электрохимически активированный солевой раствор.
Annolyte® или Imecalyte® - это нейтральный электрохимически активированный солевой раствор, являющийся высокоэффективным дезинфицирующим средством. Такой активированный раствор может быть получен путем электролиза растворов хлорида натрия. Он может применяться в таких областях, как дезинфекция, например, рабочих мест, столов, пола и т.д., для процедур холодной стерилизации, в сельском хозяйстве для удаления микроорганизмов, для мытья и стирки, в плавательных бассейнах и даже для профилактики эпидермофитии. Устройство для производства нейтральных электрохимически активированных солевых растворов описано в ЕР-А-1 728 768, включенном здесь посредством ссылки. Заявитель, однако, не имеет сведений о применении таких растворов в качестве носителей в фармацевтических композициях.
WO 2004/031077 раскрывает устройство для получения биологического раствора путем электролитической обработки водных солевых растворов. Содержимое этого документа включено здесь посредством ссылки.
WO 2005/065388 раскрывает водный раствор с окислительно-восстановительным потенциалом и его применение в качестве дезинфицирующего средства или для лечения ран. Содержимое этого документа включено здесь посредством ссылки.
Предметом данного изобретения является применение водных электрохимически активированных растворов солей, в частности растворов солей гипохлоритов, в качестве носителей в фармацевтических композициях. Фармацевтические композиции предпочтительно включают по крайней мере две отдельных фазы, в которых первая фаза включает активный ингредиент, а вторая фаза включает носитель.
В первом аспекте настоящее изобретение относится к фармацевтической композиции, включающей активный ингредиент и носитель, в которой носитель включает водный электрохимически активированный солевой раствор с содержанием свободного хлора между 1 и 500 мг/л и положительным редокс-потенциалом между +150 и +1350 мВ. Активный ингредиент предпочтительно физически отделяется от носителя, например, активный ингредиент присутствует в фазе, отделенной от электрохимически активированного солевого раствора. Однако, если активный ингредиент достаточно устойчив в присутствии электрохимически активированной соли, фармацевтическая композиция может также состоять из одной фазы, например водного раствора.
В другом аспекте данное изобретение относится к применению водного электрохимически активированного солевого раствора с содержанием свободного хлора между 1 и 500 мг/л и положительным редокс-потенциалом между +150 и +1350 мВ в качестве носителя для производства фармацевтической композиции.
Водный электрохимически активированный раствор имеет содержание свободного хлора (определенное с помощью амперометрического измерения (ДФД) в соответствии с US 4278507, включенным здесь посредством ссылки), обеспечивающего достаточную активность, например дезинфицирующую или противомикробную активность, не оказывающую отрицательного влияния на стабильность композиции. Содержание свободного хлора может быть отрегулировано путем разбавления электрохимически активированных солевых растворов в отношении, например, 1 часть (объемная) солевого раствора к 1 - 250 частей (объемных) физиологически пригодного носителя, такого как вода, буферный или солевой раствор. Предпочтительно содержание свободного хлора составляет от 1 до 500 мг/л, особо предпочтительно от 10 до 400 мг/л, и наиболее предпочтительно от 100 до 350 мг/л.
Редокс-потенциал электрохимически активированного солевого раствора составляет по меньшей мере около +150 мВ, предпочтительно по меньшей мере +200 мВ, более предпочтительно +300 мВ, даже более предпочтительно по меньшей мере +400 мВ, даже более предпочтительно по меньшей мере +500 мВ и вплоть до +1330 мВ, предпочтительно вплоть до +1200 мВ. В некоторых воплощениях редокс-потенциал составляет от +650 мВ до +950 мВ, особенно от +700 до +900 мВ. Электрохимически активированный солевой раствор предпочтительно является раствором гипохлорита щелочного металла, например, раствором гипохлорита лития, натрия или калия. Более предпочтительно раствор является раствором гипохлорита натрия.
Электрохимически активированный солевой раствор обычно имеет pH от 2-8. В некоторых воплощениях pH может быть от 2-5, например, от 2-4, от 2-3 или от 2-2,8. В других воплощениях pH может быть от 5-8, в частности от 5,9 до 7,6 и более конкретно, от 6,7 до 7,4.
Содержание хлората и/или содержание хлорита предпочтительно ниже токсического уровня, например ниже 10 мг/л. Кроме того, раствор предпочтительно свободен от определяемых количеств радикалов, таких как радикалы ОН, и от озона. Кроме того, раствор предпочтительно свободен от ионов тяжелых металлов, например, от ионов Мо.
Активный ингредиент может быть любым медикаментом, пригодным для применения у человека или в ветеринарной медицине, например, выбранным из гидрофильных активных ингредиентов или из липофильных агентов. В некоторых воплощениях предпочтительно, чтобы активный ингредиент был выбран из липофильных или амфифильных ингредиентов, т.е. ингредиентов, имеющих коэффициент распределения бутанол-вода по меньшей мере 0,5, предпочтительно по меньшей мере 1. В других воплощениях активный ингредиент является гидрофильным ингредиентом, таким как полисахарид. Например, активный агент может быть выбран из агентов для лечения глаукомы, например, из простагландинов, таких как латанопрост, бета-блокаторов, таких как тимолол, агентов для снижения повышенного внутриглазного давления, таких как дорзоламид, агентов для лечения синдрома сухого глаза (офтальмологических любрикантов), таких как гидроксипропилметилцеллюлоза (гипромеллоза) и гиалуроновая кислота, и других фармацевтически активных агентов.
Фармацевтическая композиция настоящего изобретения стабилизирована против микробной деградации. Таким образом, композиция пригодна для многоцелевого применения. Композиция для многоцелевого применения может даже не содержать обычных консервантов.
Композиция обладает устойчивостью к микробной деградации предпочтительно в течение 6 месяцев, более предпочтительно по меньшей мере 12 месяцев даже при хранении при комнатной температуре. Предпочтительно противомикробную активность электрохимически активированного солевого раствора можно определить путем измерения c×t концентрации (с) и времени действия (t) продукта в соответствии со способом, описанным Schleupen, GWF, 1996. Предпочтительно значение c×t составляет 1 мг/л×мин или меньше, более предпочтительно 0,5 мг/л×мин или меньше для получения коэффициента снижения 106 против микроорганизмов, таких как Pseudomonas aeruginosa и Legionella pneumophila.
Композиция может быть предназначена для любого типа применения, например, для местного или для системного применения. Например, композиция предназначается для глазного, интраназального, внутриушного, местного, легочного, мукозального, перорального или интраперитонеального применения, например, для применения посредством инъекции. Предпочтительные композиции предназначаются для глазного применения, например для лечения глаукомы или синдрома сухого глаза.
В одном предпочтительном воплощении изобретения фармацевтическая композиция включает одну фазу, включающую как активный ингредиент, так и электрохимически активированную соль. В этом воплощении активный ингредиент является достаточно устойчивым к деградации в присутствии химически активированной соли. Подходящими примерами активных ингредиентов являются полимеры, выбранные из полисахаридов и полимеров поливинилпирролидона. Полисахариды, например, могут быть выбраны из целлюлозы или производных целлюлозы, или глюкозаминогликанов, таких как гепарин, гепаран-сульфат и гиалуроновая кислота. Более предпочтительно, композиция может включать офтальмологический любрикант и носитель, в котором носитель включает водный электрохимически активированный солевой раствор с содержанием свободного хлора, как описано выше, т.е. от 1 до 500 мг/мл, и редокс-потенциалом, как описано выше, т.е. от +150 до +1350 мВ. Офтальмологический любрикант может быть полимером, например, полисахаридом или поливинилпирролидоном, например, целлюлозой или производным целлюлозы, таким как гидроксипропилметилцеллюлоза, или глюкозаминогликаном, таким как гиалуроновая кислота. Фармацевтическая композиция предпочтительно является однородным водным раствором. В данном воплощении предпочтительно, чтобы в композиции не присутствовали другие активные агенты и/или консерванты. Композиция в соответствии с указанным воплощением может применяться для лечения и/или профилактики синдрома сухого глаза.
В другом воплощении композиция предпочтительно образует по меньшей мере две отдельные фазы, в которых активный агент присутствует в первой фазе, а электрохимически активированный солевой раствор присутствует во второй фазе, отделенной от первой фазы. Первая фаза может быть твердой взвешенной фазой, жидкой гидрофобной фазой или твердой или жидкой фазой, имеющей барьер по отношению ко второй фазе, которая находится в водной фазе, включающей носитель. Таким образом, композиция может быть эмульсией, например, микроэмульсией, или липосомальной композицией, или микрокапсулярной композицией, или дисперсией, в которой активный ингредиент может быть эмульгирован или диспергирован факультативно в присутствии носителя, например, липофильного носителя и/или сурфактантов, в водном носителе. Активный агент может, таким образом, быть физически отделенным от электрохимически активированного солевого раствора.
Особо предпочтительными являются микроэмульсии, как описано в ЕР 07 008 347.1, включенном здесь посредством ссылки.
В дополнение к активному агенту и электрохимически активированному солевому раствору, композиция может содержать другие известные ингредиенты, например буферы, адъюванты, вспомогательные агенты, наполнители, разбавители и т.д.
Композиция изобретения может применяться у человека или в ветеринарной медицине.
Еще один аспект данного изобретения относится к применению электрохимически активированного солевого раствора, описанного выше, для очистки контактных линз, например, стеклянных или пластиковых контактных линз. В этом воплощении раствор может не содержать какого-либо активного агента или может включать активный агент, например, полимер, как описано выше.
Еще один аспект данного изобретения относится к применению электрохимически активированного солевого раствор, описанного выше, для промывания полостей организма, например, в виде раствора для интраназального, глазного или внутриушного применения. В этом воплощении раствор может не содержать какого-либо активного агента или может включать активный агент, например полимер, как описано выше.
Далее настоящее изобретение описывается более подробно с помощью следующих примеров.
Пример 1. Приготовление и характеристика микроэмульсий с электрохимически активированным солевым раствором в качестве носителя
1.1. Состав анализируемых рецептур
Готовили следующие микроэмульсии, включающие 0,0050% латанопрост в качестве активного ингредиента. Все проценты являются массовыми.
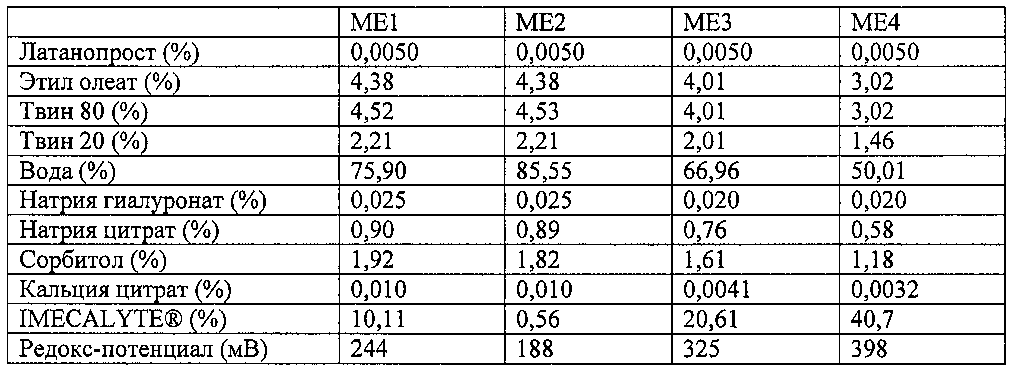
1.2. Стабильность латанопроста в микроэмульсиях IMECALYTE®
Стабильность латанопроста в микроэмульсиях, включающих электрохимически
активированный солевой раствор (IMECALYTE®) в качестве носителя, определяли посредством ВЭЖХ. В качестве сравнения анализировали стабильность латанопроста в растворах IMECALYTE®.
Количество латанопроста (мкг/мл) после хранения при комнатной температуре в течение указанных периодов времени было следующим:

Результаты показали, что латанопрост защищен от деградации, вызванной IMECALYTE® в рецептурах микроэмульсий МЕ1 и МЕ2. В противоположность этому латанопрост был неустойчив в растворах IMECALYTE®. В 0,5% IMECALYTE® значительная деградация была отмечена спустя две недели. В 10% растворе IMECALYTE® латанопрост полностью разрушался за несколько минут.
1.3. Противомикробная активность
Анализировали активность микроэмульсий, содержащих латанопрост против роста микроорганизмов Staphylococcus aureus и Pseudomonas aeruginosa. Исходная концентрация S.aureus составила 2,82×105/мл для МЕ1 и МЕ2, и 1,7×106/мл для МЕ3 и МЕ4. Исходная концентрация P.aeruginosa составила 2,15×106/мл для МЕ1 и МЕ2, и 3,18×105/мл для МЕ3 и 3,18×106/мл для МЕ4.
Спустя 14 суток не было отмечено жизнеспособных микроорганизмов S.aureus и P.aeruginosa (концентрация<10/мл) в МЕ1, МЕ3 и МЕ4. В МЕ2 спустя 28 суток не обнаруживалось организмов S.aureus. Однако в МЕ1 рост P.aeruginosa не был существенно ингибирован.
Результаты примера 1 показали, что активный ингредиент, такой как латанопрост, был защищен от деградации в микроэмульсиях на основе IMECALYTE®. Кроме того, эти микроэмульсии проявляют существенные антибактериальные свойства.
Пример 2. Приготовление и характеристика рецептур гиалуроновой кислоты на основе IMECALYTE®
Были приготовлены следующие рецептуры гиалуроновой кислоты. Все проценты являются массовыми процентами.


Проводили анализ, оказывает ли IMECALYTE® существенное влияние на свойства рецептур, такие как отделение капель. Угол контакта отделенных капель на контрольной бумажной поверхности измеряли немедленно после производства рецептур HS1 и HS2 и после хранения в течение трех месяцев при комнатной температуре. Для сравнения использовали рецептуру гиалуроновой кислоты, соответствующую HS2 (однако без IMECALYTE®).
Были получены следующие результаты:

Кроме того, определяли растекание отделенных капель различных рецептур гиалуроновой кислоты немедленно после производства (t=0) и после хранения в течение трех месяцев при комнатной температуре (t=3 месяца).

Вышеуказанные результаты показали, что IMECALYTE® не оказывает существенного влияния на характеристики отделения капель рецептур гиалуроновой кислоты. Качество отделения и образования капель растворов на основе IMECALYTE® было очень хорошим.
Кроме того, определяли противомикробную активность рецептур гиалуроновой кислоты на основе IMECALYTE®. В качестве анализируемых организмов использовали S.aureus (исходная концентрация 7,27×105мл) и P.aeruginosa (исходная концентрация 1,29×106/мл). С раствором HS1 концентрация жизнеспособных P.aeruginosa была ниже 102/мл спустя 6 часов. Со S.aureus не определялось жизнеспособных микроорганизмов спустя 14 суток. С рецептурой HS2 жизнеспособные микроорганизмы P.aeruginosa не определялись спустя 7 суток. Жизнеспособные микроорганизмы S.aureus не определялись спустя 14 суток.
Вышеуказанные результаты показали, что рецептуры гиалуроновой кислоты на основе IMECALYTE® являются стабильными и обладают противомикробной активностью.
Реферат
Изобретение относится к микробиологически стабильной фармацевтической композиции, включающей активный агент, выбранный из простагландинов, и носитель. Носитель включает водный электрохимически активированный солевой раствор с содержанием свободного хлора от 1 до 500 мг/л и редокс-потенциалом от +150 до +1350 мВ. Активный агент присутствует в фазе, отделенной от электрохимически активированного солевого раствора, причем электрохимически активированный солевой раствор является раствором гипохлорита. Изобретение также относится к применению фармацевтической композиции для лечения и/или профилактики синдрома сухого глаза и для очистки контактных линз. 5 н. и 9 з.п. ф-лы, 5 табл., 2 пр.

Комментарии