Ионофоретическая доставка ротиготина для лечения болезни паркинсона - RU2478383C2
Код документа: RU2478383C2
Описание
Область изобретения
Настоящее изобретение относится к эффективному способу лечения или облегчения симптомов болезни Паркинсона, в котором используют ионофоретическую доставку агониста дофаминовых рецепторов ротиготина (МНН).
Предшествующий уровень техники
Полагают, что болезнь Паркинсона главным образом вызвана дегенерацией дофаминергических нейронов в черном веществе (substantia nigra). Это, в сущности, приводит к потере тонической секреции дофамина и связанной с дофамином модуляции нейрональной активности в хвостатом ядре (caudate nucleus) и, таким образом, к недостатку дофамина в некоторых участках мозга. Возникающий в результате дисбаланс нейромедиаторов ацетилхолина и дофамина в итоге приводит к симптомам, связанным с болезнью. Хотя обычно болезнь Паркинсона и считают расстройством двигательной системы, в настоящее время ее следует рассматривать как более сложное расстройство, которое включает как двигательную систему, так и не связанную с двигательной системой. Это истощающее заболевание характеризуется основными клиническими признаками, включающими тремор, брадикинезию, оцепенелость, дискинезию, нарушения походки и расстройства речи. У некоторых пациентов деменция может сопровождать эти симптомы. Вовлечение вегетативной нервной системы может вызывать ортостатическую гипотензию, пароксизмальные приливы крови, проблемы с терморегуляцией, запор и потерю контроля мочевого пузыря и сфинктера. Психологические расстройства, такие как потеря мотивации и депрессия, также могут сопровождать болезнь Паркинсона.
Болезнь Паркинсона является главным образом болезнью среднего возраста и старше, и она в равной степени поражает и мужчин, и женщин. Наивысшая частота встречаемости болезни Паркинсона находится в возрастной группе старше 70 лет, где болезнь Паркинсона существует у 1,5-2,5% данной популяции. Средний возраст начала заболевания составляет от 58 до 62 лет, и у большинства пациентов болезнь Паркинсона развивается в возрасте от 50 до 79 лет. В одних только Соединенных Штатах имеется приблизительно 800000 человек с болезнью Паркинсона.
Ранняя двигательная недостаточность при болезни Паркинсона может быть обнаружена по начинающейся дегенерации клеток, высвобождающих дофамин из черного вещества (nigral). Такая дегенерация нейронов вызывает дефект в дофаминергическом пути, который связывает черное вещество (substantia nigra) с полосатым телом (striatum). По мере прогрессирования болезни могут развиться стойкие двигательные, вегетативные и психические отклонения, что подразумевает, что имеет место прогрессирующая дегенерация стриарных рецепторных механизмов.
Клинический диагноз болезни Паркинсона основан на присутствии характерных физических симптомов. Как известно, болезнь в начале является постепенной, медленно прогрессирующей и вариабельной в клиническом проявлении. Данные свидетельствуют о том, что перед появлением симптомов содержание дофамина в полосатом теле снижается до уровней на 20% ниже обнаруживаемых у соответствующих по возрасту контролей.
Лечение болезни Паркинсона ограничивалось попыткой использовать, среди прочего, L-допа (леводопа), который все еще является золотым стандартом для терапии болезни Паркинсона. Леводопа проникает через гематоэнцефалический барьер в виде предшественника дофамина и затем превращается в мозге в дофамин. L-допа улучшает симптомы болезни Паркинсона, но может вызывать сильные побочные эффекты. Кроме того, лекарство имеет тенденцию к потере его эффективности после первых двух-трех лет лечения. После пяти-шести лет только у 25-50% пациентов поддерживается улучшение.
Кроме того, основным недостатком используемых в настоящее время терапий болезни Паркинсона является возможное проявление «синдрома колебаний», приводящего к условиям «все или ничего», характеризующимся чередованием периодов «включения» подвижности с дискинезиями и периодов «выключения» с гипокинезией или акинезией. Пациенты, которые демонстрируют непредсказуемые или непостоянные явления «включения-выключения» при пероральной терапии против болезни Паркинсона, имеют предсказуемую благоприятную реакцию на внутривенное введение L-допы и других агонистов дофамина, что свидетельствует о том, что колебания в концентрации лекарства в плазме ответственны за явления «включения-выключения». Частоту колебаний «включения-выключения» также улучшали путем непрерывных инфузий агонистов дофаминовых рецепторов апоморфина и лизурида. Однако этот способ введения является неудобным. Поэтому другие способы введения, обеспечивающие более постоянный уровень в плазме, такие как местное введение, являются полезными и предлагались в прошлом.
Как было упомянуто выше, один подход при лечении болезни Паркинсона включает агонисты дофаминовых рецепторов. Агонисты дофаминовых рецепторов (иногда также называемые дофаминовыми агонистами) представляют собой вещества, которые, являясь структурно отличными от дофамина, связываются с различными подтипами дофаминовых рецепторов и запускают эффекты, которые сравнимы с эффектами дофамина. Ввиду сниженных побочных эффектов полезно, когда эти вещества избирательно связываются с подгруппой дофаминовых рецепторов, например D2-рецепторами.
Одним из агонистов дофаминовых рецепторов, который использовали для лечения симптомов болезни Паркинсона, является ротиготин. Его главным образом тестировали в форме его гидрохлорида. Ротиготин представляет собой международное непатентованное наименование (МНН) соединения (-)-5,6,7,8-тетрагидро-6-[пропил-[2-(2-тиенил)этил]-амино]-1-нафталенол, имеющего структуру, показанную ниже

Ранее было известно введение ротиготина с помощью пассивных трансдермальных терапевтических систем (ТТС). Такие пассивные трансдермальные терапевтические системы для введения ротиготина описаны, например, в WO 94/07568 и WO 99/49852. Однако поток ротиготина, получаемый при использовании этих пассивных трансдермальных терапевтических систем, не всегда является достаточным для всех пациентов.
Другим агонистом дофамина, который использовали при лечении болезни Паркинсона, является R-апоморфин. R-апоморфин представляет собой международное непатентованное наименование (МНН) соединения (R)-5,6,6а,7-тетрагидро-6-метил-4Н-дибензохинол ин-11,12-диол, имеющего структуру, показанную ниже
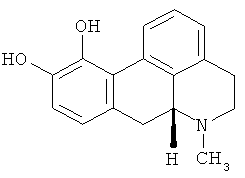
Ранее было описано несколько подходов для разработки системы ионофоретического введения R-апоморфина (см., например, R. van der Geest, М. Danhof, Н.Е. Boddé «lontophoretic Delivery of Apomorphine: In Vitro Optimization and Validation», Pharm. Res. (1997), 14, 1797-1802; M. Danhof, R. van der Geest, T. van Laar, H.E. Boddé «An integrated pharmacokinetic-pharmacodynamic approach to optimization of R-apomorphine delivery in Parkinson's disease», Advanced Drug Delivery Reviews (1998), 33, 253-263). Однако, несмотря на эти усилия, смогли получить только концентрации у нижней границы диапазона терапевтической концентрации от 1,4 до 10,7 нг/мл.
Еще одним антагонистом дофамина является гидрохлорид ропинирола. Ропинирол (МНН) представляет собой (4-[2-дипропиламино)этил]-1,3-дигидро-2Н-индол-2-он), имеющий структуру, показанную ниже

Хотя ионофоретическое введение ропинирола считали осуществимым, оказалось возможным только получение потоков у нижней границы терапевтического диапазона (см. A.Luzardo-Alvarez, М.В.Delgado-Charro, J.Blanco-Méndez, «lontophoretic Delivery of Ropinirole Hydrochloride: Effect of Current Density and Vehicle Formulation», Pharmaceutical Research (2001), 18(12), 1714-1720).
Многим пациентам необходимы концентрации, которые значительно выше, чем концентрации, возможные при ионофоретической доставке апоморфина или ропинирола.
Принимая во внимание широкий ряд симптомов болезни Паркинсона и ее особую тяжесть, существует острая потребность в способе, который позволяет регулировать поток ротиготина через кожу и в то же время обеспечивает постоянную рецепторную стимуляцию дофаминовых рецепторов пациентов с болезнью Паркинсона. Предпочтительно такая система также должна обеспечивать более высокие потоки ротиготина, чем потоки, достигаемые при помощи пассивных трансдермальных систем доставки.
Принимая во внимание удручающий опыт с ионофоретической доставкой апоморфина, неожиданно оказалось, что ионофоретическая доставка ротиготина смогла обеспечить уровни ротиготина в плазме, которые не только являются более высокими, чем уровни при использовании общепринятых систем пассивной диффузии, но и фактически находятся в диапазоне, который обеспечивает доставку фармацевтически эффективных дозировок лекарства. Результаты, полученные при использовании этого изобретения, дают возможность обоснованного предположения того, что может быть обеспечено эффективное лечение болезни Паркинсона. Следует понимать, что термин «лечение» в контексте этой заявки означает указание скорее на лечение или облегчение симптомов болезни Паркинсона, чем на реальное лечение причинного фактора, приводящее к полному исцелению.
Краткое изложение сущности изобретения
В настоящем изобретении предложено применение композиции, включающей ротиготин и по меньшей мере одну хлоридную соль в концентрации от 1 до 140 ммоль/л, где данная композиция имеет рН от 4 до 6,5, для заправки устройства для ионофореза для лечения болезни Паркинсона.
Ионофорез представляет собой введение различных ионов в кожу при помощи электричества. По сравнению с пассивной трансдермальной доставкой ионофорез обеспечивает несколько преимуществ, которые полезны при лечении болезни Паркинсона:
- он позволяет программировать поток с необходимой терапевтической скоростью путем регулирования электрического тока, и
- он обеспечивает быстрое начало или прекращение введения лекарственного средства, если необходимо, просто путем включения или выключения системы ионофоретической доставки.
Так как ионофоретический поток подвержен влиянию нескольких параметров, для достижения оптимального потока важно отдельно оптимизировать эти параметры.
Неожиданно было обнаружено, что при использовании композиции, имеющей рН от 4 до 6,5 и содержащей ротиготин и по меньшей мере одну хлоридную соль в концентрации от 1 до 140 ммоль/л в донорной камере устройства для ионофореза, смогли достичь потоков полностью в пределах терапевтического диапазона.
Снижая концентрацию электролита в донорном отсеке, оказалось возможным достичь целевого ионофоретического потока при более низкой плотности электрического тока или увеличить трансдермальную дозу на единицу площади.
Во время исследований, проведенных для оценки возможности ионофоретической доставки ротиготина, было обнаружено, что растворимость ротиготина снижается при увеличении рН. Однако, к удивлению, было обнаружено, что терапевтически релевантная скорость достигается в интервале рН от 4 до 6,5 при очень низких концентрациях ротиготина.
Для обеспечения оптимального потока через роговой слой (stratum corneum) человека также было необходимо обеспечить достаточную концентрацию ионов СГ для электродной реакции в донорной фазе. Однако поддерживая электродную реакцию, добавление хлоридных солей снижает растворимость ротиготина. Таким образом, оптимальной оказалась концентрация хлоридных солей от 1 до 140 ммоль/л, предпочтительно от 50 до 100 ммоль/л, более предпочтительно от 60 до 80 ммоль/л.
Концентрацию ротиготина можно изменять в соответствии с потребностями пациента и потоком, необходимым для получения терапевтического эффекта при лечении болезни Паркинсона. Однако для оптимального действия предпочтительно использовать по меньшей мере 0,5 мг/мл, более предпочтительно от 0,5 мг/мл до 3 мг/мл.
Все хлоридные соли, которые являются фармацевтически приемлемыми, могут быть использованы в композиции по данному изобретению. В предпочтительном воплощении данного изобретения хлоридная соль выбрана из NaCl, хлорида тетраэтиламмония и хлорида тетрабутиламмония. Хлорид тетраэтиламмония и хлорид тетрабутиламмония особенно предпочтительны, так как они приводят к более высоким потокам ротиготина.
В особенно предпочтительном воплощении данного изобретения композиция, которую используют в качестве донорной фазы устройства для ионофореза, содержит ротиготин в концентрации от 0,5 до 3 мг/мл и по меньшей мере один из хлорида тетраэтиламмония и хлорида тетрабутиламмония в концентрации от 60 до 80 ммоль/л, причем донорная фаза имеет рН от 4,5 до 5,5.
В другом аспекте настоящего изобретения предложен способ лечения болезни Паркинсона, при котором на кожу нуждающегося в этом пациента прикладывают устройство для ионофореза, которое содержит композицию, включающую ротиготин и по меньшей мере одну хлоридную соль в концентрации от 1 до 140 ммоль/л, где данная композиция имеет рН от 4 до 6,5.
Любое общепринятое устройство для ионофореза может быть использовано в данном изобретении. Такие устройства для ионофореза описаны, например, в V.Nair, О.Pillai, R.Poduri, R.Panchagnula, «Transdermal Iontophoresis. Part I: Basic Principles and Considerations» Methods Find. Exp. Clin. Pharmacol. (1999), 21(2), 139-151.
Плотность тока, используемая во время ионофореза, может варьировать в соответствии с нуждами пациента и будет зависеть от устройства для ионофореза и композиции, которые используют. Подходящий электрический ток может быть определен лечащим врачом. В общем, подходящая плотность тока будет находиться предпочтительно в диапазоне от 200 до 500 мкА/см2.
Пример 1
Ионофоретические исследования in vitro по введению ротиготина проводили с использованием трехкамерных проточных диффузионных ячеек, как описано R. van der Geest et al. (R. van der Geest, M. Danhof, H.E. Boddé, «Validation and testing of a new iontophoretic continuous flow through transport cell», J. Control. Release (1998), 51, 85-19). Stratum corneum (SC) человека поместили на обе стороны акцепторного отсека. В качестве поддерживающей мембраны использовали диализную мембрану, имеющую порог отсечения 5000 Да. Объем наружных камер составлял приблизительно 2 мл, тогда как объем акцепторного отсека составлял 0,54 мл. Две наружные камеры содержали серебряную пластинку (анод) или серебро/хлорид серебра (катод) движущие электроны. Донорная фаза состояла из раствора ротиготина, забуференного 5 мМ цитратным буфером (2,1 мМ дигидрата цитрата натрия и 2,9 мМ лимонной кислоты).
Используя такую установку, рН 5 в донорной камере, плотность тока 500 мкА/см2, рН 7,4 в акцепторной камере, температуру 20°С и концентрацию NaCl в донорной камере 70 ммоль/л, измерили поток ротиготина при различных концентрациях лекарства в донорной фазе.
Пример 2
Используя методику, подобную описанной в Примере 1, и концентрацию ротиготина 1,4 мг/мл (3,98 мМ), рН 5 в донорной камере, плотность тока 500 мкА/см2, рН 7,4 в акцепторной камере и температуру 20°С, но замещая хлорид тетраэтиламмония (TEACl) или хлорид тетрабутиламмония (TBACl) на NaCl, оценили влияние различных катионов на поток. Концентрация хлоридных солей в донорном растворе составляла 70 ммоль/л.
Пример 3
Используя подобную методику и те же самые параметры как в Примере 2, оценили влияние снижения рН в акцепторной камере от 7,4 до 6,2 для различных хлоридных солей. Концентрация хлоридных солей в донорном растворе составляла 70 ммоль/л.
Реферат
Группа изобретений относится к медицине и касается применения композиции, включающей ротиготин в концентрации, достаточной для обеспечения потока ротиготина, необходимого для получения терапевтического эффекта, и по меньшей мере одну хлоридную соль в концентрации от 1 до 140 ммоль/л, где данная композиция имеет рН от 4 до 6,5, для заправки устройства для ионофореза для лечения болезни Паркинсона. Группа изобретений обеспечивает поток ротиготина через роговой слой (stratum comeum)человека, который является более высоким, чем поток, получаемый ранее с использованием общепринятых систем пассивной диффузии. 2 н. и 7 з.п. ф-лы, 3 пр.

Комментарии