Комбинация гиалуроновой кислоты и сульфатированного полисахарида - RU2683567C2
Код документа: RU2683567C2
Чертежи


Описание
Область техники
Настоящее изобретение относится к новой комбинации гиалуроновой кислоты или ее соли и сульфатированного полисахарида с низкой молекулярной массой; и к применению указанной комбинации в области против старения и для заживления.
Предшествующий уровень техники
Гиалуроновая кислота (ГК) представляет собой молекулу с наиболее важной ролью в коже. Это действительно главный компонент внеклеточного матрикса. Этот последний относится к набору внеклеточных макромолекул соединительной ткани. Она, в основном, состоит из гликопротеинов, чистых белков, а также гликозаминогликанов. ГК представляет собой линейный несульфатированный гликозаминогликан, состоящий из повторяющихся дисахаридных звеньев, состоящих из D-глюкуроновой кислоты и N-ацетил-D-глюкозамина, соединенных с чередованием β1-3 и β1-4 гликозидных связей между димерами (Tammi R., Agren U.M., Tuhkanen A.L., Tammi M. Hyaluronan metabolism in skin. Progress in Histochemistry & Cytochemistry 29(2):1-81, 1994). В своей нативной форме ГК представляет собой полимер, имеющий очень высокую молекулярную массу в диапазоне от 600000 Да до 3 МДа (Toole BP. Hyaluronan: from extracellular glue to peracellular cue. Nat Rev Cancer 2004, 4:538-539).
С возрастом количество ГК и степень ее полимеризации уменьшаются, что приводит к уменьшению количества воды, удерживаемой во внеклеточном матриксе. Затем кожа подвергается процессу старения, что приводит к увеличению фиброза и к снижению содержания эластиновых волокон. Во время процесса старения наблюдается изменение структуры и функций кожи. Старение является физиологическим по природе, но также может быть фотоиндуцированным, т.е. из-за частого воздействия на кожу солнечных лучей, в частности ультрафиолетового излучения. Основными клиническими признаками старения кожи являются появление линий и глубоких морщин, которые, очевидно, увеличиваются с возрастом. Борозды и морщины являются заметными; кожа становится пустой и теряет упругость; на поверхности кожа теряет сияние.
Сульфатированные полисахариды включают в себя, в частности, сульфатированные фуканы и сульфатированные ульваны, имеющие молекулярную массу от 5 до 25 кДа.
Эти сульфатированные полисахариды с низкой молекулярной массой обладают полезными биохимическими свойствами: ингибированием деградации коллагена и эластина, реструктуризацией, противовоспалительным действием и индукцией продукции ГК.
С возрастом фибробласты входят в стадию старения и их способность пролиферировать значительно уменьшается. Таким образом, обеспечение способности вновь стимулировать пролиферацию этих клеток является одним из способов борьбы со старением кожи.
Кроме того, заживление ран представляет собой сложный и динамичный биологический процесс, который приводит в действие взаимодействие многочисленных локальных и системных факторов в нормальном восстановлении тканей. Заживление включает три взаимосвязанных фазы: гемостаз и воспаление, пролиферацию и ремоделирование (General principles of wound healing. Witte MB, Barbul A. Surg Clin North Am. 1997 Jun; 77(3):509-28.). Пролиферация включает в себя три четко наблюдаемых процесса: грануляцию, стягивание и реэпителизацию.
В процессе грануляции наблюдают пролиферацию и миграцию к раневому ложу клеток, которые будут вовлечены в оставшуюся часть процесса восстановления. Таким образом, там обнаруживают макрофаги, фибробласты и эндотелиальные клетки. Макрофаги постоянно выделяют хемостатические факторы и факторы роста. Фибробласты строят новую клеточную матрицу, необходимую для роста клеток у основания раны. Эта подложка поддерживает миграцию клеток. И, наконец, эндотелиальные клетки вызывают образование зачатков сосудов, их которых будут образовываться новые капилляры, которые будут восстанавливать перфузию и обеспечивать снабжение кислородом и питательными веществами, существенными для метаболической активности клеток в ране.
Стягивание раны является механизмом уменьшения размера раны, и фибробласты играют ведущую роль в этом стягивании.
Реэпителизация состоит в регенерации эпидермиса, который покрывает рану, чтобы сформировать эффективный барьер против внешней среды, который способен пигментироваться и восстанавливать свои сенсорные и иммунные функции. Таким образом, она включает в себя клеточные процессы миграции и пролиферации кератиноцитов, а также дифференциацию этого нового эпителия и восстановление базальной мембраны, которая соединяет дерму и эпидермис. Когда миграция базальных клеток в направлении центра раны приводит к соединению двух краев раны, происходит волна митоза клеток для заполнения пробелов, оставленных миграцией, и обеспечения клеток для эпителиальной ткани в трехмерной регенерации.
Стадии пролиферации кератиноцитов, фибробластов или эндотелиальных клеток можно рассматривать в качестве одного из функциональных явлений, демонстрирующих заживляющую активность активного агента. Увеличение пролиферации фибробластов будет принимать участие в заживлении глубокой раны (достигающей дермы), в то время как усиление пролиферации кератиноцитов участвует в реэпителизации.
Существует потребность в создании новых косметических композиций для борьбы с признаками старения кожи.
Заявитель продемонстрировал синергетический эффект между гиалуроновой кислотой и сульфатированным полисахаридом с низкой молекулярной массой на пролиферацию фибробластов. Эта активность особенно интересна в области борьбы со старением, а также в области регенерации тканей и заживления повреждений кожи.
Подробное описание изобретения
Настоящее изобретение относится к комбинации, содержащей гиалуроновую кислоту или ее соль и сульфатированный полисахарид, имеющий молекулярную массу от 5 до 25 кДа.
В контексте настоящего изобретения термины "гиалуроновая кислота", "фрагменты гиалуроновой кислоты", "ГК" и "гиалуронан" используются взаимозаменяемо для обозначения гиалуроновой кислоты. Когда гиалуроновая кислота находится в форме соли, ее называют гиалуронат.
В конкретном варианте осуществления изобретения комбинация содержит гиалуроновую кислоту или ее соль, имеющую среднюю молекулярную массу (Mw) в диапазоне от 50000 до 750000 Да.
В конкретном варианте осуществления изобретения фрагмент ГК или его соль характеризуется средней молекулярной массой от 60 до 120 кДа, причем эту молекулярную массу измеряют с помощью аналитического метода, сочетающего эксклюзионную хроматографию (SEC, от англ. size-exclusion chromatography) с многоракурсным фотометром для измерения рассеянного света (MALS, от англ. multi-angle light scattering photometer) в сочетании с вискозиметром (VIS, от англ. viscometer) и дифференциальным рефрактометром (RI, от англ. differential refractometer).
В конкретном варианте осуществления это будет гиалуронат натрия.
Молекулярная масса ГК или ее соли может быть измерена с использованием метода Европейской Фармакопеи, который измеряет характеристическую вязкость с помощью капиллярного вискозиметра Уббелоде (см. статью Европейской Фармакопеи 7.6, фармакопейная статья для гиалуроната натрия: 01/2011: 1472). Это значение вязкости затем соотносят со средней молекулярной массой в соответствии с зависимостью Марка-Хаувинка. Этот метод является длительным и требует идеальной воспроизводимости.
В контексте настоящего изобретения среднюю молекулярную массу ГК или ее соли измеряют с помощью метода SEC-MALS-VIS-IR, который представляет собой аналитический метод, сочетающий эксклюзионную хроматографию (SEC) с многоракурсным фотометром для измерения рассеянного света (MALS) в сочетании с вискозиметром (VIS) и дифференциальным рефрактометром (RI). Этот метод позволяет получить среднюю молекулярную массу (Mw).
Эта методика позволяет охарактеризовать молекулярные массы ГК точно и воспроизводимо (Stepan Podzimek & al. Solution of Hyaluronic Acid and Comparison of SEC-MALS-VIS Data with Off-line Capillary Viscometry. Journal of Applied Polymer Science. 2009).
Сочетание эксклюзионной хроматографии (SEC) с детектором (MALS) позволяет после введения полимерного раствора в хроматографическую систему разделить эти полимеры по размеру в хроматографической колонке для измерения этих размеров с помощью рассеяния света и количественно их охарактеризовать, используя дифференциальный рефрактометр или УФ-спектрометр.
- Гиалуроновую кислоту или ее соль растворяют в водном 0,1 М растворе NaCl, затем элюируют на колонке, заполненной шариками из полистирола-дивинилбензола, имеющими калиброванный размер пор. Большие полимерные цепи не проходят через поры и элюируются перед меньшими цепями.
- Детектор MALS измеряет рассеяние падающего света под разными углами. Эти углы позволяют путем экстраполяции измерять R0, который представляет собой рассеяние под углом 0. R0 прямо пропорционален размеру молекулы.
- Si ответ дифференциального рефрактометра пропорционален общей массе Ci полимера, имеющего степень полимеризации i в соответствии с уравнением (1):

где: Si - это, таким образом, ответ дифференциального рефрактометра,
K' - константа, связанная с прибором, и
Ci - общая масса (вес) полимера, имеющего степень полимеризации i
(Ci=Ni×Mi), где Ni - количество цепей с молекулярной массой Mi.
Кроме того, приращение показателя преломления dn/dc - это специфичное значение изучаемого полимера.
Это отношение dn/dc можно измерить в соответствии со следующим протоколом на примере гиалуроната натрия.
а/ Устройство и получение растворов:
Измерения проводят на рефрактометре, таком как модель Brice-Phoenix, имеющем гелий-неоновый лазер (λ равно 633 нм) в качестве источника падающего света.
Различные концентрации изучаемых полимеров готовят независимо друг от друга путем взвешивания (нахождение в растворе составляет 24 часа). Соответствующие показатели преломления (dn) затем измеряют с помощью рефрактометра.
b/ Результат
Результаты представлены в виде графика dn = f (концентрация) (см. фиг. 1). Затем определяют линейную регрессию типа Y = А + В*Х.
В случае гиалуроната натрия определенные значения А и В соответственно составляют А = -2,030 и В = 14927,911.
Таким образом, отношение dn/dc соответствует k × В, где k - константа прибора, которая равна 0,97⋅10-5 в этом примере.
Для гиалуроната натрия dn/dc, таким образом, составляет 0,97⋅10-5 × 14927,911 = 0,145 мл/г.
Следующее уравнение дает взаимосвязь между всеми измеренными параметрами:

где: R0 - отношение Релея при угле рассеяния 0,
K' - константа прибора, и
Ci - общая масса (вес) полимера, имеющего степень полимеризации i (рассчитанная в соответствии с уравнением (1)), введенного раствора,
и Mi - молекулярная масса искомой полимерной цепи.
Средневесовую молекулярную массу Mw можно рассчитать по формуле: Mw=ΣCiMi/ΣCi.
Все молекулярные массы выражены в дальтонах.
Гиалуроновую кислоту или ее соль, предмет настоящего изобретения, можно получить в соответствии с одним из способов, известных специалистам в данной области техники, таких, как те, которые упомянуты в документе ЕР 1987153.
ГК получают, главным образом, в промышленном масштабе с помощью бактериальной ферментации: нити гиалуроновой кислоты синтезируются бактериями.
Таким образом, в конкретном варианте осуществления изобретения нативную ГК, имеющую высокую молекулярную массу в диапазоне обычно от 1 до 2 МДа, получают путем бактериальной ферментации с использованием выбранного штамма бактерий.
Полученный полимер затем можно отделить от бактерий. Затем раствор очищают и гидролизуют с помощью контролируемого кислотного гидролиза до тех пор, пока не будет получена желаемая молекулярная масса.
В случае получения гиалуроната натрия можно осуществить стадию нейтрализации путем добавления NaOH.
Солью гиалуроновой кислоты предпочтительно будет гиалуронат натрия.
В контексте настоящего изобретения сульфатированные полисахариды с низкой молекулярной массой могут быть выбраны из сульфатированных фуканов и сульфатированных ульванов, имеющих молекулярную массу от 5 до 25 кДа.
Сульфатированные фуканы - это полисахариды, содержащие сульфированную L-фукозу. Эти полисахариды можно выделить, в частности, из коричневых водорослей, например, из Fucales или Laminariales.
Сульфатированные ульваны - это сульфатированные анионные полисахариды, содержащие уроновые кислоты (например, глюкуроновую кислоту, идуроновую кислоту) и сахара, которые можно сульфатировать (например, 3-сульфат рамнозы, галактозы, ксилозы, глюкозы), распределенные в повторяющихся звеньях. Основные звенья:
- 3-сульфат ульванобиуроновой кислоты типа А, состоящий из 3-сульфата α-L-рамнозы, связанной с β-D-глюкуроновой кислотой связью типа 1→4, и
- 3-сульфат ульванобиуроновой кислоты типа В, состоящий из 3-сульфата α-L-рамнозы, связанной с α-L-идуроновой кислотой связью типа 1→4.
Ульваны можно получить, в частности, из зеленых водорослей типа ульвы или энтероморфы (Ulva sp. и Enteromorpha sp.).
В соответствии с конкретным вариантом осуществления изобретения сульфатированный фукан с низкой молекулярной массой является таким, как описано в публикации WO 2010/086197.
Можно упомянуть запатентованный коммерческий продукт Ascophyscient® (Algues и Mer), полученный из водоросли Ascophyllum nodosum.
Согласно другому предпочтительному варианту осуществления изобретения сульфатированный ульван с низкой молекулярной массой является таким, как описано в публикации WO 2013/150253.
Можно также упомянуть фракцию QT40®, выпускаемую фирмой Green Tech, на основе определенного олигосахарида из водоросли Ulva lactuca: сульфоолигорамноглюкуронан.
В соответствии с конкретным вариантом осуществления изобретения массовое отношение гиалуроновой кислоты к полисахариду составляет от 0,1 до 10.
В соответствии с другим вариантом осуществления изобретения массовое отношение гиалуроновой кислоты к полисахариду составляет от 0,5 до 5 и предпочтительно от 0,5 и 2.
Настоящее изобретение дополнительно относится к комбинации гиалуроновой кислоты или ее соли и сульфатированного полисахарида с низкой молекулярной массой согласно изобретению (т.е. имеющего молекулярную массу от 5 до 25 кДа) для применения для стимуляции пролиферации фибробластов.
Настоящее изобретение также относится к косметической композиции, содержащей в качестве активного ингредиента против старения комбинацию гиалуроновой кислоты или ее соли и сульфатированного полисахарида, имеющего молекулярную массу в диапазоне от 5 до 25 кДа, и дополнительно содержащей по меньшей мере один косметически приемлемый эксципиент.
Предпочтительно косметически приемлемые эксципиенты подходят для местного применения.
Приемлемые эксципиенты позволяют, в частности, обеспечить хорошую стабильность, приятные текстуру и ощущение. Они также могут быть, например, агентами для приготовления или добавками для известного и обычного использования в косметических средствах: можно упомянуть поверхностно-активные вещества, красители, консерванты, отдушки, пленкообразующие вещества, загустители и т.д.
Композиции против старения могут быть в формах, обычно известных для местного применения на коже, то есть, в частности, в виде кремов, эмульсий, лосьонов, сывороток, масок, филлеров морщин, подводки для глаз и т.п.
Предмет настоящего изобретения направлен на косметическое применение комбинации в соответствии с настоящим изобретением или указанной косметической композиции согласно настоящему изобретению для борьбы с признаками старения кожи. Косметическое применение комбинации в соответствии с изобретением или косметической композиции в соответствии с изобретением более конкретно предназначено для восстановления ткани кожи, для повышения ее плотности и визуального уменьшения заметных морщин и глубоких борозд.
Настоящее изобретение также относится к способу борьбы с признаками старения кожи, включающему введение, предпочтительно местное, эффективного количества комбинации согласно изобретению или косметической композиции согласно изобретению человеку, нуждающемуся в этом.
Другой предмет настоящего изобретения относится к дерматологической композиции, предназначенной для ускорения восстановления кожи, для восстановления целостности и качества кожи, содержащей в качестве дерматологически или косметически активного ингредиента комбинацию гиалуроновой кислоты или ее соли и сульфатированного полисахарида, молекулярная масса которого составляет от 5 до 25 кДа, упомянутого выше, и дополнительно содержащей по меньшей мере один дерматологически или косметически приемлемый эксципиент.
В предпочтительном варианте осуществления изобретения композиция предназначена для местного применения.
Дерматологически (фармацевтически) или косметически совместимые эксципиенты могут представлять собой любой эксципиент из тех, которые известны специалистам в данной области техники для получения композиции для местного применения в форме молочка, крема, бальзама, масла, лосьона, геля, пенного геля, мази, спрея и т.п.
В предпочтительном варианте осуществления композиция будет в виде крема или мази.
В конкретном варианте осуществления изобретения дерматологические и косметические композиции по настоящему изобретению содержат по меньшей мере один другой активный ингредиент.
Этот другой активный ингредиент может быть, в частности, выбран из группы, включающей агенты, предотвращающие старение, заживляющие агенты, смягчающие агенты, противозудные агенты, антиоксиданты, агенты против радикалов, агенты против УФ-излучения, агенты, стимулирующие синтез дермальных макромолекул или энергетический метаболизм, увлажняющие агенты, депигментирующие агенты, антибактериальные агенты, противогрибковые средства, противовоспалительные средства или анестетики.
В соответствии с конкретным вариантом осуществления изобретения композиции согласно настоящему изобретению, предпочтительно косметические, дополнительно содержат ретинальдегид. Этот дополнительный омолаживающий активный агент является непосредственным предшественником ретиноевой кислоты для немедленного эффекта реактивации клеточного метаболизма. Ретинальдегид повышает экспрессию рецепторов ГК, CD44, и индуцирует синтез ГК.
Таким образом, композиция по настоящему изобретению содержит комбинацию гиалуроновой кислоты или ее соли, сульфатированного полисахарида с низкой молекулярной массой и ретинальдегид. Такая комбинация оказывает реструктуризирующий и уплотняющий эффект на дермоэпидермальное соединение и сосочковый слой дермы.
В соответствии с другим вариантом осуществления изобретения композиция будет дополнительно содержать производное токоферола, включая дельта-токоферилглюкопиранозид: его мощные антиоксидантные эффекты защищают кожу и сохраняют ее сияние.
Таким образом, композиция по настоящему изобретению содержит комбинацию гиалуроновой кислоты или ее соли, сульфатированного полисахарида с низкой молекулярной массой и дельта-токоферилглюкопиранозид.
Согласно другому предпочтительному варианту осуществления изобретения другой активный ингредиент будет выбран из заживляющих агентов, успокаивающих агентов и их смесей. Такой активный ингредиент будет предпочтительно использоваться в дерматологических композициях.
И, наконец, еще один предмет настоящего изобретения направлен на комбинацию гиалуроновой кислоты или ее соли и сульфатированного полисахарида с низкой молекулярной массой или на дерматологическую композицию, содержащую эти вещества в соответствии с настоящим изобретением, для применения в качестве лекарственного средства (более конкретно, дерматологического лекарственного средства), предназначенного, в частности, для лечения и заживления поражений кожи.
Настоящее изобретение относится также к применению комбинации гиалуроновой кислоты или ее соли и сульфатированного полисахарида, имеющего молекулярную массу в диапазоне от 5 до 25 кДа, для получения лекарственного средства (в частности, дерматологического лекарственного средства), предназначенного, в частности, для лечения и заживления поражений кожи.
Настоящее изобретение также относится к способу лечения и заживления поражений кожи, включающему введение, предпочтительно местное, эффективного количества комбинации гиалуроновой кислоты или ее соли и сульфатированного полисахарида, имеющего молекулярную массу в диапазоне от 5 до 25 кДа, или дерматологической композиции, содержащей указанные вещества в соответствии с изобретением, человеку, нуждающемуся в этом.
Дерматологические и косметические композиции согласно изобретению предназначены, в частности, для ухода за поврежденной кожей:
- после инвазивных процедур/лечения: хирургических процедур (иссечения, бритья) с или без шовного материала, криотерапии, лазерной абляции, умеренного или сильного пилинга, мезотерапии, кюретажа,
- после травм с поверхностными порезами или ожогами,
- после поверхностных (неинвазивных) процедур, требующих заживляющего продукта, который ускоряет восстановление кожи, для длительного использования (до полного восстановления кожи),
- после умеренных наружных повреждений: поверхностных ссадин, солнечных ожогов.
Лечение поражений кожи и слизистых оболочек в соответствии с изобретением может включать, в частности, лечение порезов, швов, ссадин, царапин, соскобов, рубцов после хирургической операции или после эстетической дерматологической процедуры, поверхностных ожогов, солнечных ожогов.
Настоящее изобретение дополнительно относится к применению косметической композиции по настоящему изобретению для улучшения заживления и восстановления кожи.
Изобретение будет лучше понято при прочтении результатов, представленных ниже, которые иллюстрируют изобретение, не ограничивая его объем.
Краткое описание графических материалов
На фиг. 1 показан показатель преломления dn в зависимости от концентрации С для гиалуроната натрия.
На фиг. 2 показано влияние ГК в соответствии с изобретением (HAF120) при 100 и 1000 мкг/мл, и Ascophyscient® при 10 и 100 мкг/мл на пролиферацию фибробластов. *: р менее 0,05 и **: р менее 0,01. Эксперимент представляет три независимых эксперимента.
На фиг. 3 показано влияние ГК в соответствии с изобретением (HAF120) при 100 мкг/мл, Ascophyscient® при 10 мкг/мл и их комбинации на пролиферацию фибробластов. *: р менее 0,05 и **: р менее 0,01. Эксперимент представляет три независимых эксперимента.
На фиг. 4 показано влияние ГК в соответствии с изобретением (HAF120) при 1000 мкг/мл, Ascophyscient® при 10 мкг/мл и их комбинации на пролиферацию фибробластов. *: р менее 0,05 и **: р менее 0,01. Эксперимент представляет три независимых эксперимента.
ПРИМЕРЫ
Фармакологическая оценка комбинации фрагмента гиалуроната натрия, имеющего среднюю молекулярную массу от 60 до 120 кДа (HAF120), и сульфатированного фукана, имеющего низкую молекулярную массу (5-25 кДа), на пролиферацию фибробластов
Протокол:
Используемый метод заключается во включении нуклеотида, 5-бром-2'-дезоксиуридина (BrdU), аналога тимидина, в ДНК клеток в S-фазе при 37°С. Этот метод дает возможность количественно оценить клетки, у которых развитие клеточного цикла характерно для пролиферирующих клеток (S-фаза или фаза синтеза ДНК).
Нормальные фибробласты человека (NHF, от англ. normal human fibroblasts), выделенные из кожи, являющейся хирургическими отходами, как правило, выращивают в среде Игла, модифицированной по способу Дульбекко (DMEM, от англ. Dulbecco's modified Eagle's medium), с 10% фетальной телячьей сыворотки (FCS, от англ. fetal calf serum). В наших экспериментальных условиях разведения продуктов для тестирования готовят в среде DMEM с 3% FCS.
Из клеток сначала убирали FCS в течение 24 часов, чтобы остановить размножение клеток перед их инкубированием в присутствии молекул, которые будут оценены в течение 44 часов при температуре 37°С в атмосфере 5% CO2.
Включение BrdU, пропорциональное скорости пролиферации клеток, оценивают с помощью системы антител анти-BrdU (Roche Applied Science). Соответствующую оптическую плотность (OD) измеряют при 450 нм. Эти данные, таким образом, пропорциональны скорости пролиферации клеток.
Активные агенты, которые оценивают, являются следующими:
- Положительный контроль: эпидермальный фактор роста (ЭФР) в концентрации 10 нг/мл
- Собственный коммерческий продукт Ascophyscient® (Algues et Mer): 10 и 100 мкг/мл (что соответствует 0,001% и 0,01%, соответственно)
- Гиалуронат натрия 60-120 кДа в соответствии с примером 1: 100 и 1000 мкг/мл (что соответствует 0,01 и 0,1%, соответственно)
- Комбинация, содержащая соответственно Ascophyscient® и гиалуронат натрия 60-120 кДа при следующих соответствующих концентрациях:
- 10 мкг/мл плюс 100 мкг/мл,
- 10 мкг/мл плюс 1000 мкг/мл.
Анализ результатов:
- выражены в виде OD (пропорциональной включению BrdU и, таким образом, скорости пролиферации клеток)
- выражены в виде процента стимуляции:
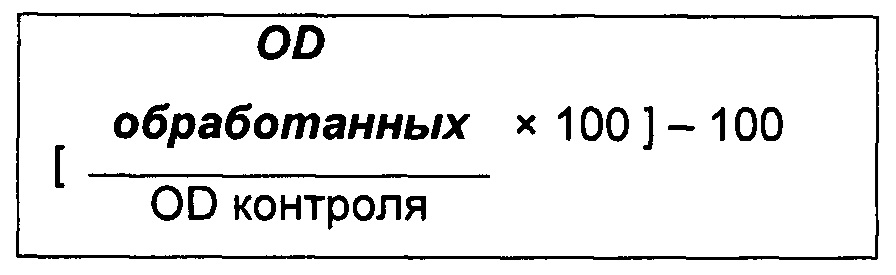
- выражены в виде стандартного отклонения от среднего (SEM, от англ. standard error of the mean):
SEM = стандартное отклонение (SD)/√n
Статистические анализы:
Статистические анализы с использованием непарного двустороннего критерия Стьюдента проводили на исходных значениях OD.
Этот тест дает значения р, характеризующие значимость результатов, полученных для различных условий. Степень значимости устанавливается следующим образом:
важное для р менее 0,05 (*)
очень важное для р менее 0,01 (**)
высоко важное для р менее 0,001 (***)
не важное для р более 0,05
Результаты:
В этих экспериментальных условиях
- Ascophyscient® индуцировал пролиферацию фибробластов очень воспроизводимым и статистически значимым образом, особенно при 100 мкг/мл (фиг. 2).
- один гиалуронат натрия имел умеренный эффект на пролиферацию фибробластов (фиг. 2).
- комбинация этих двух соединений индуцировала пролиферацию фибробластов синергетическим образом (фиг. 3 и 4).
Выводы:
В этих экспериментальных условиях Ascophyscient® индуцировал пролиферацию фибробластов очень воспроизводимым и статистически значимым образом. Комбинация Ascophyscient® с HAF120 индуцировала пролиферацию фибробластов синергетическим образом.
Путем индуцирования пролиферации фибробластов Ascophyscient® и его комбинация с фрагментом гиалуроната натрия 60-120 кДа восстанавливает клеточный метаболизм и участвует в восстановлении кожи и в борьбе со старением.
Иллюстративные композиции
Пример 1

Пример 2:

Реферат
Изобретение относится к косметической промышленности и представляет собой комбинацию для борьбы с признаками старения кожи и для улучшения заживления или восстановления кожи, содержащую гиалуроновую кислоту или ее соль, имеющие средневесовую молекулярную массу в диапазоне от 60 до 120 кДа, и сульфатированный полисахарид, имеющий молекулярную массу в диапазоне от 5 до 25 кДа, выбранный из сульфатированных фуканов. Изобретение обеспечивает индуцирование пролиферации фибробластов синергетическим образом. 5 н. и 8 з.п. ф-лы, 4 ил., 2 пр.

Комментарии