Сериновые протеиназы рыб и их фармацевтическое и косметическое применение - RU2264824C2
Код документа: RU2264824C2
Чертежи


Описание
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в его наиболее широком аспекте касается лечения и предупреждения болезней, в частности фармацевтического и косметического использования сериновых протеиназ рыб. В частности, представлены фармацевтически или косметически активные композиции, содержащие в качестве активного компонента трипсин и/или химотрипсин, выделенный из атлантической трески, и сериновые протеиназы, родственные таким ферментам.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Американские патенты №4801451 и 4963491 раскрывают смесь экзо- и эндопептидаз, выделенных из антарктического криля (Eupasia superba) и использование этой смеси в виде очищенного раствора. Американский патент №4801451 раскрывает использование таких ферментов для удаления чужеродных веществ (гноя) и мертвой ткани из ран. Международная заявка WO 85/04809 раскрывает использование ферментов криля в качестве агента, ускоряющего переваривание. ЕР-А1-0170115 раскрывает использование ферментов криля для растворения сгустков крови.
Однако все эти ссылки раскрывают неочищенные и плохо охарактеризованные вещества. Очищенная пептидаза или смесь очищенных пептидаз желательна для обеспечения фармацевтически пригодного продукта, более того, не раскрыто, где очищенная пептидаза или смесь очищенных пептидаз пригодна для лечения, например, артрита, воспаленных суставов, бурсита, остеоартрита, ревматоидного артрита, септического артрита, флебита, экземы, сыпи, псориаза или инфекционных болезней.
Международная заявка WO 96/24371 раскрывает применение многофункционального протеолитического фермента, полученного из криля, и семейства протеолитических ферментов, полученных из ракообразных и рыб и обладающих значительным структурным сходством с многофункциональным ферментом, полученным из антарктического криля. Эта заявка касается также способов очистки многофункционального фермента и фармацевтического, косметического и другого применения многофункционального фермента. Значительное структурное сходство с многофункциональным ферментом, полученным из антарктического криля, определяется в этой заявке, как приблизительно 70% гомология с многофункциональной гидролазой, полученной из криля. Трипсин и химотрипсин, полученные из трески и раскрытые в этой заявке, имеют менее 70% гомологии с многофункциональным ферментом, полученным из криля. Кроме того, трипсины и химотрипсины, полученные из трески, не являются многофункциональными ферментами. Их основная известная активность заключается в том, что они являются трипсиновыми протеазами и химотрипсиновыми протеазами, соответственно.
Основная цель данного изобретения заключается в представлении использования трипсинов и химотрипсинов трески в фармацевтических композициях и лекарственных препаратах для локального (местного) применения для лечения внутренних болезней и нарушений и косметического использования таких ферментов. Было найдено, что местное применение для лечения локального внутреннего заболевания без фермента, обладающего способностью проникать в открытые раны или слизистую ткань, оказалось чрезвычайно эффективным, как описано в прилагающихся примерах. Это противоречит известным представлениям о соответствующем использовании других ферментов, в соответствии с которыми, например, многофункциональная гидролаза криля инъецируется для лечения различных локальных болей. Другая цель данного изобретения заключается в использовании трипсинов и химотрипсинов трески в фармацевтических композициях или лекарственных препаратах для транспорта других активных соединений белковой или небелковой природы через кожу для местного применения с целью лечения внутренних заболеваний и нарушений. Было найдено, что такие сериновые протеиназы являются фармацевтически чрезвычайно активными против множества болезней.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Первый аспект данного изобретения, соответственно, имеет отношение к сериновой протеиназе рыб, предназначенной для использования в качестве лекарственного препарата. В этом контексте особенно полезные протеиназы включают трипсины и химотрипсины, полученные из трески, а именно атлантической трески.
Другой аспект изобретения касается использования сериновой протеиназы рыб для изготовления лекарственного препарата для лечения и/или предупреждения болезней у человека или животных. Заболевания и нарушения, которые могут быть вылечены или предупреждены, включают боль, острое воспаление, хроническое воспаление, артрит, воспаленный сустав, бурсит, остеоартрит, ревматоидный артрит, подростковый ревматоидный артрит, септический артрит, фибромиалгию, флебит, тендинит, сыпь, псориаз, акне, экзему, лицевую себорейную экзему, экзему рук, лица или шеи, инфекции крайней плоти, эпидермофитию стопы, свищевую инфекцию, инфекционные локальные язвы, пупочные инфекции новорожденных, рубцы, келлоидные рубцы, фурункулы, бородавки и аллергический зуд, геморрои, раны, раневые инфекции, ожоговые раны, грибковую инфекцию и нарушения иммунной системы, включающие аутоиммунные болезни.
Еще один аспект данного изобретения представляет использование сериновой протеиназы рыб для изготовления лекарственных преператов для удаления мертвой или шелушащейся кожи от здоровой кожи и использование сериновой протеиназы рыб для изготовления лекарственных препаратов для лечения и предупреждения заболеваний, в патогенез которых вовлекается рецептор-опосредованное связывание.
Еще один аспект данного изобретения касается фармацевтической и косметической композиций, включающих сериновые протеиназы рыб, и способа лечения и/или предупреждения болезней у человека или животных, способа, включающего введение человеку или животным фармацевтически эффективного количества сериновых протеиназ рыб.
В соответствии с данным изобретением также представлены метод получения в коммерческом масштабе очищенного препарата изоформ трипсина, полученных из трески, метод, включающий следующие стадии: (i) приготовление водного экстракта из внутренних органов трески, (ii) осуществление одного или нескольких этапов хроматографической очистки водного экстракта, включающих этап аффинной хроматографии с использованием аффинного лиганда пара-аминобензамидина, и (iii) десорбция и элюция трипсина, связанного с аффинным лигандом пара-аминобензамидином, и очищенный в коммерческих масштабах препарат трипсина трески.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение представляет использование трипсинов трески и других родственных трипсинов или сериновых протеиназ, например химотрипсинов, полученных из животных, в частности водных животных, а именно рыб, включая треску, для множества медицинских и косметических целей.
Используемый здесь термин "фермент" означает активный фермент, если не определяется иначе. Используемый здесь также термин "трипсин или другие пептидазы" означает пептидазы трипсинового типа (ЕС 3.4.21.4) и все пептидазы, последовательности которых имеют 90% или более гомологию с трипсинами из атлантической трески (Asgeirsson et al., Eur. J. Biochem. 180:85-94, 1989; Gudmundsdottir et al., Eur. J. Biochem. 217:1091-1097, 1993). Используемый здесь также термин "химотрипсин или другие пептидазы" означает все пептидазы химотрипсинового типа (ЕС 3.4.21.1) и все пептидазы, последовательности которых имеют 90% или более гомологию с химотрипсинами А и В из атлантической трески (Asgeirsson and Bjamason, Сотр. Biochem. Physiol. 99B:327-335, 1991; Gudmundsdottir et al., Biochem. and Biophys. Acta 1219:211-214, 1994).
Ферменты согласно данному изобретению пригодны, в частности, для обезболивания, лечения воспаления, острого и хронического воспаления, артрита, воспаленных суставов, бурсита, остеоартрита, ревматоидного артрита, подросткового ревматоидного артрита, септического артрита, фибромиалгии, системной красной волчанки, флебита, экземы, сыпи, псориаза, акне, ран и кандидоза. В приемлемых реализациях трипсин из трески или химотрипсин из трески или смесь этих ферментов применяются локально или местно к пораженному участку в составе фармацевтической композиции, включающей очищенную пептидазу или смесь очищенных пептидаз и фармацевтически приемлемый растворитель или носитель, в частности гидрогель. Кроме того, эти ферменты пригодны для лечения вирусных инфекций, например, герпесных высыпаний, грибковых, бактериальных или паразитарных инфекций, включая колит, язвы, геморрои, рубцевание роговицы, зубной налет и нарушения иммунной системы, включающие аутоиммунные болезни.
Ферменты, которые имеют значительное структурное сходство с трипсином и химотрипсином, полученным из трески, имеют ту же полезность, что и ферменты из трески.
В частности, эти трипсины и химотрипсины пригодны для лечения артрита, воспаленных суставов, бурсита, остеоартрита, ревматоидного артрита, подросткового ревматоидного артрита, септического артрита и флебита. При таком лечении трипсин, или химотрипсин, или смесь обоих ферментов применяется локально или местно на участке с артритом или воспалением в фармацевтической композиции, включающей трипсины, или химотрипсины, или смесь обоих ферментов и фармацевтически приемлемый растворитель или носитель, в частности, но не только, гидрогель. Кроме того, трипсины и химотрипсины, согласно данному изобретению пригодны для лечения вирусных инфекций, например, герпесных высыпаний, грибковых, бактериальных или паразитарных инфекциий, включая колит, язвы, геморрои, рубцевание роговицы, зубной налет, акне, раны, кандидоз и нарушения иммунной системы, включающие аутоиммунные болезни.
Изобретение особенно касается медицинского, фармацевтического и косметического применения трипсинов, полученных из атлантической трески или других животных. Существуют три основных изоформы трипсина в атлантической треске, которые уже очищены и охарактеризованы. Они были названы трипсин I, II и III (Asgeirsson et al., Eur. J. Biochem. 180:85-94, 1989). Трипсины трески имеют N-концевую последовательность I-V-G-G-Y-Q/E-C-E/T-K/R-H-S-Q-A-H-Q-V-S-L-N-S, тогда как трипсины млекопитающих, например бычий трипсин, имеют N-концевую последовательность I-V-G-G-Y-T-C-G-A-N-T-V-P-Y-Q-V-S-L-N-S. Все три изоформы трипсина трески имеют сходную молекулярную массу около 24 кДа.
Изобретение также касается медицинского, фармацевтического и косметического применения химотрипсинов, полученных из атлантической трески или других животных. Существуют две основных изоформы химотрипсина в атлантической треске, которые уже очищены и охарактеризованы. Они были обозначены химотрипсин А и В (Asgeirsson and Bjamason, Сотр. Biochem. Physiol. 99B:327-335, 1991). Химотрипсины трески имеют двойную N-концевую последовательность одной из его активных форм C-G-R/S-P-A-I-S/Q-P-V/Q-I/V-Т-О-Y(А-цепь) и I-V-N-G-E-E-A-V-P-H-S/T-W-S/P/Y-W-Q-V-S-LQ-D/Q (В цепь), тогда как химотрипсины млекопитающих, например бычий химотрипсин А, имеют N-концевые коследовательности C-G-V-P-A-I-Q-P-V-L-S-G-L (А цепь) и I-V-N-G-E-E-A-V-P-G-S-W-P-W-Q-V-S-L-Q-D (В цепь). Обе изоформы химотрипсина трески имеют сходную молекулярную массу около 26 кДа.
Трипсины и химотрипсины трески выделяются и очищаются из внутренних органов трески, за исключением печени, селезенки и икры. Авторы изобретения нашли способы, описанные ниже, которые пригодны для получения трипсинов и химотрипсинов трески в коммерческом масштабе. Ферменты экстрагируют из целых или измельченных внутренних органов путем водной экстракции осторожным перемешиванием при любом соотношении внутренних органов и воды, предпочтительнее соотношение (вес/вес) от 1:1 до 1:10 потрохов к воде. После разделения грубого экстракта и оставшихся потрохов этот экстракт очищают путем осаждения или фильтрации. Очищенный раствор концентрируют предпочтительнее путем ультрафильтрации и/или обычно ионообменной хроматографией, а затем предпочтительнее микрофильтруют для достижения истинного раствора с низким количеством биопримесей, пригодного для проведения колоночной хроматографии, которая может включать несколько стадий. Затем трипсин трески очищают путем проведения аффинной хроматографии, предпочтительнее с помощью бензамидин-аффинной хроматографии, а химотрипсин - путем проведения гидрофобной хроматографии, предпочтительнее с помощью хроматографии на фенил-сефарозе.
Используемое здесь получение трипсинов и химотрипсинов трески в коммерческом масштабе подразумевает способы, которые являются надежными и хорошо воспроизводимыми и позволяют получать продукцию партиями от 1 до 10 г или более, например от 10 до 100 г и более.
Предпочтительный способ применения очищенных ферментов или смеси очищенных ферментов заключается в получении гидрогеля и воды, содержащих от 0 до 85% (объем/объем) многоатомного спирта, например глицерина. Подходящая концентрация активности трипсина составляет от 0,1 до 10000 единиц активности фермента для CBZ-Gly-Pro-Arg-pNA (карбобензокси-Gly-Pro-Arg-n-нитроаналид) на 100 мл конечного препарата гидрогеля и соответствующая концентрация активности химотрипсина составляет от 0,1 до 10000 единиц активности фермента для сукцинил-Ala-Ala-Pro-Phe-pNA на 100 мл конечного препарата гидрогеля.
Изобретение также представляет фармацевтическую композицию, включающую трипсины трески и родственные пептидазы и фармацевтически приемлемый растворитель или носитель.
Изобретение, кроме того, представляет (а) способы лечения и профилактики состояний с использованием эффективных количеств очищенных ферментов, описанных выше, (б) композиции или вещества для применения в таких способах, (в) фармацевтические композиции, содержащие эффективные количества ферментов для применения в таких способах, и (г) использование фермента или ферментной композиции для изготовления лекарственного препарата, применяющегося в таких способах.
Эти способы представляют собой:
лечение или профилактическое предупреждение симптомов, выбранных из группы, состоящей из боли, воспаления, острого и хронического воспаления, артрита, воспаленных суставов, бурсита, остеоартрита, ревматоидного артрита, подросткового ревматоидного артрита, септического артрита, фибромиалгии, системной красной волчанки и флебита, где эффективным количеством является количество, эффективное для лечения или предупреждения;
лечение или профилактическое предупреждение дерматологических показаний, таких как акне, сыпь, псориаз или экзема, включая лицевую себорейную экзему или экзему рук, лица, волосистой части кожи головы или шеи, геморрои и тому подобное, где предпочтительное количество введенных трипсинов трески и родственных пептидаз является таким количеством, которое эффективно для лечения или предупреждения дерматологических состояний;
лечение или профилактическое предупреждение раневой инфекции и обрабатывание ран путем приложения к ране эффективного количества фермента, предупреждающего микробную инфекцию, или благодаря усилению заживления ран путем введения эффективного количества фермента, ингибирующего микробы, достаточного для того, чтобы обработанная рана была значительно освобождена от некротической ткани;
удаление мертвой или шелушащейся кожи со здоровой кожи для улучшения кожного обновления, где предпочтительнее такое количество введенного фермента, которое является эффективным количеством для удаления мертвой кожи;
лечение или профилактическое предупреждение муковисцидоза, рака, например путем введения фермента в количестве, эффективном для лечения рака или для предупреждения или ингибирования опухолевых метастазов, атеросклероза, астмы, септического шока, токсического шокового синдрома, тканевых спаек, например, влагалища сухожилия, брюшных постхирургических или суставных спаек, травм при повторной перфузии, малярии, иммунных нарушений, таких как аутоиммунные болезни, апоптоза, колита и энтерита, например болезни Крона (гранулематозной болезни), где предпочтительнее введение такого количества трипсинов трески и родственных пептидаз, которое эффективно для лечения или предупреждения указанных заболеваний;
лечение или профилактическое предупреждение микробной инфекции, например, вирусной инфекции, такой как герпесная инфекция (например, HSV-1, HSV-2, опоясывающий герпес или герпесная инфекция половых органов), инфекция, вызванная вирусом иммунодефицита человека (ВИЧ), гепатита, гриппа, инфекция, вызванная коронавирусом, цитомегаловирусом, риновирусом или папиллома-вирусом; инфекции, вызывающей желудочно-кишечные заболевания, например язву или диарею; грибковой инфекции, например, системной, кожной, оральной, вагинальной инфекции или грибковой инфекции пищевода, включая, например, дрожжевую инфекцию, которая в свою очередь включает грибковую инфекцию ногтей и инфекцию грибами рода Candida (кандидозы); микробной инфекции глаз, предпочтительнее для глазного применения; бактериальных инфекций, включающих инфекцию Staphylococcus spp., Streptococcus spp., Klebsiella spp., Pseudomonas spp., Neisseria gonorrheae, Haemophilus spp., Chlamydia spp., сифилис и E.coli инфекции, и бактериальных инфекций, вызывающими венерическую язву;
условно-патогенных микробных инфекций у пациентов с нарушенной иммунной системой, где предпочтительным вводимым количеством трипсинов трески является количество, эффективное для лечения или предупреждения микробной инфекции или количество, достаточное для ингибирования клеточно-клеточной или клеточно-вирусной адгезии;
удаление зубного налета, где предпочтительным назначенным количеством фермента является количество, эффективное для удаления зубного налета; и
лизис кровяных сгустков, где предпочтительным количеством фермента является количество, эффективное для лизиса сгустков.
Способ включает применение композиции, содержащей трипсины и/или химотрипсины трески или родственные пептидазы, как описано выше. Композиция изобретения может использоваться также для удаления мертвых или дивергентных клеток.
Изобретение представляет косметические и медицинские композиции для местного применения, включающие очищенные трипсин, химотрипсин трески или другие родственные пептидазы, описанные выше; и композиции в виде геля, крема или суппозитория.
Изобретение также представляет (а) способы лечения или профилактического предупреждения синдромов, связанных с клеточно-клеточной или клеточно-вирусной адгезией, включающие применение трипсинов или химотрипсинов в количестве, эффективном для предотвращения адгезии, или родственных пептидаз, эффективных для удаления или инактивации клеточного или вирусного акцептора или рецепторного компонента адгезии, (б) композиции или вещества для использования в таких способах, (в) фармацевтические композиции, содержащие эффективные количества фермента для использования в таких способах, и (г) использование ферментной композиции для получения лекарственного препарата, применяющегося в таких способах. Обычно эти синдромы включают воспаление, артрит, воспаленные суставы, бурсит, остеоартрит, ревматоидный артрит, подростковый ревматоидный артрит, септический артрит, флебит, экзему, сыпь, псориаз, акне, раны, кандидоз и иммунные нарушения, включая аутоиммунные болезни, шок, опухолевое метастазирование, реакции отторжения трансплантата или микробные инфекции. Предпочтительнее (а) синдром представляет собой микробную инфекцию, иммунные нарушения, муковисцидоз, атеросклероз, рак, астму, септический шок, токсический шоковый синдром, конъюктивит, травму при перфузии и сыпь, и предпочтительнее, чтобы (б) клеточно-поверхностный рецептор, связанный с синдромом клеточно-клеточной или клеточно-вирусной адгезии, представляющий собой рецептор, который, как было показано, расщепляется трипсином трески и включает CD4, CD8, CD54 (ICAM-1), CD31, CD62L, CD 102 (ICAM-2), CD11a/CD18, удалялся или инактивировался с помощью введенного фермента. Предпочтительнее микробная инфекция представляет собой герпесную инфекцию, ВИЧ-инфекцию, гепатит или папиллому; инфекцию, вызывающую колит или диарею; кандидоз, например, оральный, вагинальный кандидоз или кандидоз пищевода; простуду или грипп; инфекции, вызванные Staphylococcus, Streptococcus Klebsiella, Pseudomonas, Haemophilus или E.coli; первичную или вторичную инфекцию проказой; или инфекцию, вызывающую конъюктивит или туберкулез.
В одной реализации изобретение представляет способ ингибирования или профилактического предупреждения передачи патогенного микроба благодаря применению трипсинов или химотрипсинов трески. Предпочтительно, чтобы трипсин или химотрипсин трески прикладывался к участку тела, который включает первичные ворота для инфекции рассматриваемого микроба. В одной предпочтительной реализации для участков тела, вовлеченных в сексуальную активность, используют спрей (опрыскивание), мазь или промывание, например, для предотвращения передачи ВИЧ-инфекции или гепатита. В другой предпочтительной реализации трипсин трески или родственные пептидазы применяют для верхних дыхательных путей, например, с помощью аэрозоля, для того чтобы ингибировать или предотвращать передачу вирусов, вызывающих обычную простуду, например риновирусов или коронавирусов.
В одном аспекте способ экстракорпоральной обработки ткани, жидкости организма или группы клеток для удаления клеточных адгезионных компонентов уменьшает иммунное отторжение ткани, жидкости организма или группы клеток, которые трансплантируются от одного индивидуума другому. Другой аспект состоит в том, что такие обработки удаляют или инактивируют клеточные адгезионные компоненты, находящиеся в обработанной ткани, жидкости организма или группе клеток, вовлеченных в микробную инфекцию.
В лечении или профилактическом предупреждении септического шока или токсического шокового синдрома с помощью трипсинов трески или родственных пептидаз, соответствующие способы применения включают системное применение. Для вагинальных инфекций, связанных с шоком, в качестве способа применения могут использоваться вагинальные промывания, кремы, гели или суппозитории.
В лечении или профилактическом предупреждении сыпи, воспаления, острого и хронического воспаления, артрита, воспаленных суставов, бурсита, остеоартрита, ревматоидного артрита, подросткового ревматоидного артрита, септического артрита, фибромиалгии, системной красной волчанки, флебита с применением трипсинов трески или родственных пептидаз применяют кремы, гели или суппозитории, в частности гидрогели, содержащие глицерин или другие многоатомные спирты.
В лечении или профилактическом предупреждении сыпи, псориаза, акне, экземы, включая лицевую себорейную экзему или экзему рук, лица, волосистой части кожи головы или шеи, инфекции крайней плоти, эпидермофитию стопы, свищевую инфекцию, инфицированные местные язвы, пупочные инфекции новорожденных, рубцы и келлоидные рубцы, фурункулы, бородавки и аллергический зуд, геморрои и тому подобное, раны, раневые инфекции, ожоговые раны, удаление мертвой или шелушащейся кожи от здоровой кожи для улучшения кожного возобновления, грибковую инфекцию, например системную, кожную, оральную, вагинальную или инфекцию пищевода, включая, например, дрожжевую инфекцию, включающую в свою очередь грибковую инфекцию ногтей и инфекции, вызванные грибами рода Candida, и нарушения иммунной системы, включающие аутоиммунные болезни, с применением трипсинов, химотрипсинов трески или родственных пептидаз, применяют кремы, гели или суппозитории, в частности гидрогели, содержащие глицерин или другие многоатомные спирты.
Соответственно, одна из целей данного изобретения состоит в представлении композиции для лечения сыпи, воспаления, острого и хронического воспаления, артрита, воспаленных суставов, бурсита, остеоартрита, ревматоидного артрита, подросткового ревматоидного артрита, септического артрита, фибромиалгии, системной красной волчанки, флебита, сыпи, псориаза, акне, экземы, включая лицевую себорейную экзему или экзему рук, лица, волосистой части кожи головы или шеи, инфекции крайней плоти, эпидермофитию стопы, свищевую инфекцию, инфицированные местные язвы, пупочные инфекции новорожденных, рубцы и келлоидные рубцы, фурункулы, бородавки и аллергический зуд, геморрои и тому подобное, раны, раневые инфекции, ожоговые раны, удаление мертвой или шелушащейся кожи от здоровой кожи для улучшения кожного возобновления, грибковую инфекцию, например системную, кожную, оральную, вагинальную или инфекцию пищевода, включая, например, дрожжевую инфекцию, включающую в свою очередь грибковую инфекцию ногтей и инфекции, вызванные грибами рода Candida, и нарушения иммунной системы, включающие аутоиммунные болезни. Другая цель состоит в представлении способа приготовления композиции для лечения вышеуказанных заболеваний. Третья цель состоит в представлении способа применения вышеуказанной композиции для лечения вышеуказанных заболеваний. Следовательно, в основе изобретения лежат композиции, ферменты, в которых ранее не использовались ферменты, или содержащие лучшие ферменты, в которых ферменты уже использовались ранее.
Вышеуказанные цели достигаются путем использования композиции, содержащей эффективное количество трипсинов и/или химотрипсинов трески, которое способно уменьшать боль, воспаление, артрит, припухлость, отек, псориазную экзему, дерматит, сыпь и/или другие симптомы болезней, указанные в вводной части. Ферменты трески могут быть получены с высоким выходом и относительно простым методом из внутренних органов трески. Было обнаружено, что ферменты трески могут быть очищены в коммерческом масштабе относительно простым методом и с высоким выходом. Очищенный трипсин трески содержит три основных изоформы фермента, а химотрипсин трески содержит две основных изоформы фермента. Один или все изоферменты могут использоваться для целей данного изобретения.
Было установлено, что трипсины и химотрипсины трески данного изобретения эффективно удаляют или инактивируют определенные адгезионные молекулы, находящиеся на поверхности клеток, бактериальные эндотоксины, цитокины, воспалительные медиаторы и матриксные металлопротеиназы (ММР), такие как CD4, CD8, CD54 (ICAM-1), CD31, CD62L, CD 102 (ICAM-2), CD11a/CD18, TNFα, IL-1 и ММР-9, не действуя на жизнеспособность клеток. Наличие этого адгезионного сайта расщепления или инактивации цитокинов, воспалительных медиаторов и матриксных металлопротеиназ, как полагают, представляет, по крайней мере, частичное объяснение эффективности трипсинов и химотрипсинов трески против множества, хотя, вероятно, не всех, симптомов, против которых эффективны трипсины и химотрипсины трески. Так, TNFα вовлечен как при артрите, псориазе, раке, так и при воспалении (см. Cytokines, Eds. Mire-Slui and Thrope, Academic press, 1988, p.350).
Трипсины и химотрипсины трески являются более эффективными, чем традиционные протеазы, по многим аспектам. При сравнении 13 наиболее активных протеаз по их активности в отношении 16 вышеуказанных определенных адгезионных молекул, находящихся на поверхности клеток, бактериальных токсинов, цитокинов, воспалительных медиаторов и ММР, а также их чувствительности к сывороточному ингибированию, было обнаружено, что трипсин и химотрипсин атлантической трески являются гораздо более активными. Протеазы показали 2 балла в диапазоне от высокой до очень высокой активности, 1 балл в диапазоне от низкой до умеренной активности и 0 баллов в диапазоне от очень низкой до отсутствия активности (обратные значения для сывороточного ингибирования активности протеаз). На основе этой схемы трипсин атлантической трески набрал 30 баллов, а химотрипсин атлантической трески набрал 29 баллов, в то время как известные многофункциональные протеазы криля набрали 16 баллов. Бычий трипсин и химотрипсин не набрали баллов в этом отношении. Более того, трипсины и химотрипсины атлантической трески оказались в 2-20 раз более активными, чем их бычьи эквиваленты, при сравнении их активностей с использованием стандартных небольших хромогенных субстратов (Asgeirsson et al., Eur. J. Biochem. 180:85-94, 1989; Asgeirsson and Bjamason, Comp. Biochem. Physiol. 99B:327-335,1991).
Внутренние органы трески являются подходящим источником для трипсинов и химотрипсинов трески данного изобретения. Например, ферменты можно экстрагировать в коммерческом масштабе из замороженных внутренних органов трески, как описано выше. Осветленный и концентрированный экстракт можно произвольно фракционировать с помощью ионообменной хроматографии в коммерческом масштабе, предпочтительнее, чтобы первой стадией была катионообменная хроматография, а затем стадия анионообменной хроматографии для связывания и удаления таким образом родственных сериновых протеаз, например эластаз и сериновых коллагеназ. На следующей и заключительной стадии трипсин трески очищают с помощью аффинной хроматографии в коммерческом масштабе, предпочтительнее используя колоночную аффинную хроматографию с пара-аминобензамидином, а химотрипсин - с помощью гидрофобной колоночной хроматографии, предпочтительнее с использованием фенил-сефарозы.
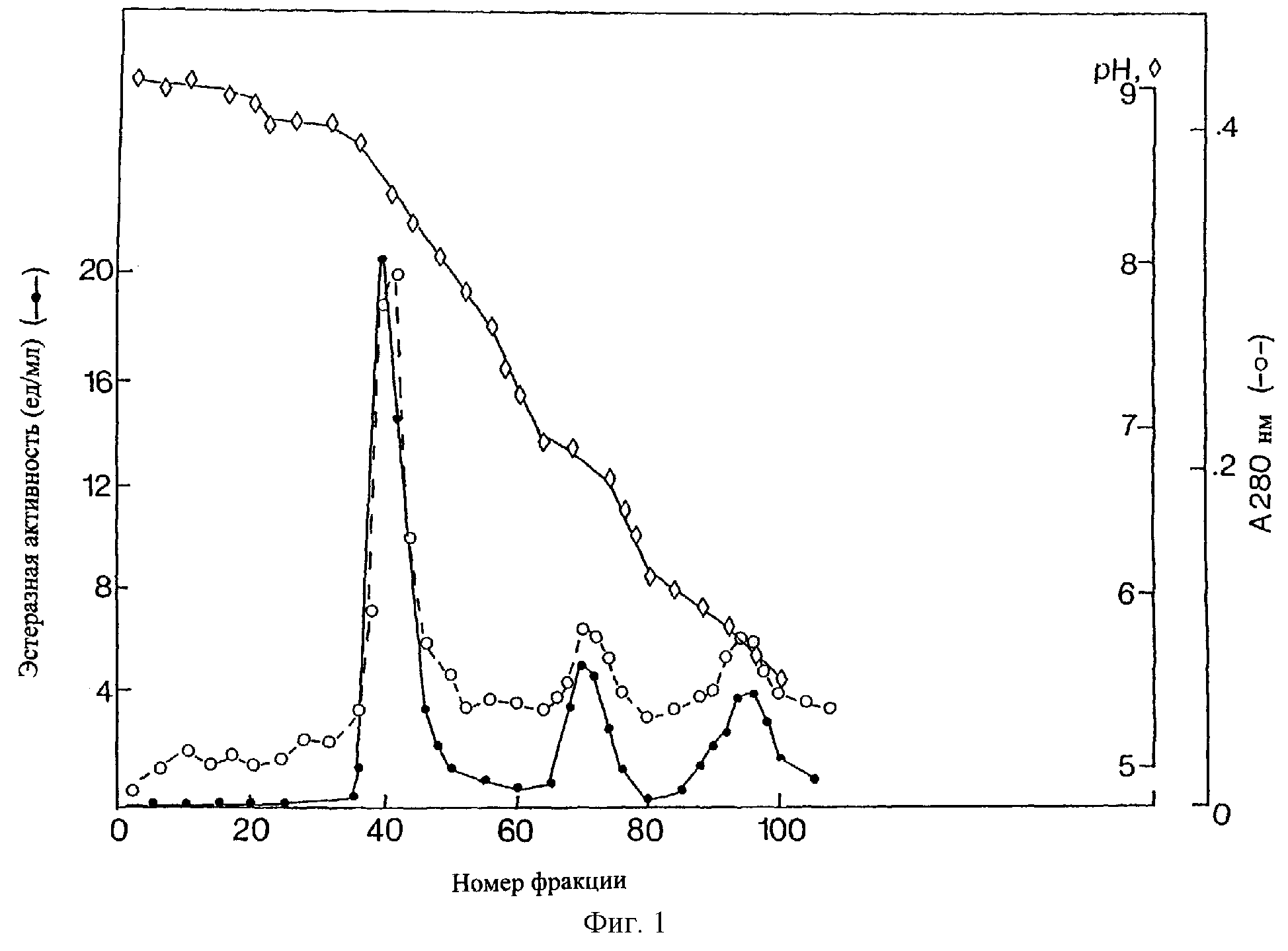
Трипсин трески, использующийся в данном изобретении, можно десорбировать с аффинного матрикса при условиях, которые будут дестабилизировать взаимодействие между ферментом и аффинным лигандом. Такие условия включают использование элюента с высокой концентрацией соли, затем с низким рН, и содержащего предпочтительнее 30% или более глицерина. Элюенту с колонки дают возможность стекать в нейтрализующий буфер для стабилизации трипсина трески после стадии кислой элюции (Asgeirsson et al., Eur. J. Biochem. 180:85-94, 1989). Химотрипсин трески, использующийся в данном изобретении, может высвобождаться с колонки с фенил-сефарозой путем применения условий, которые будут дестабилизировать взаимодействие между ферментом и гидрофобным лигандом. Такие условия включают высокое содержание глицерина в воде или буфере, предпочтительнее 50% и более глицерина в воде или буфере (Asgeirsson and Bjarnason, Comp. Biochem. Physiol. 99B:327-335, 1991). Этими методами трипсины и химотрипсины трески могут быть выделены с чистотой свыше 90%. Полученная таким образом фракция трипсина трески содержит 3 основных формы или изофермента трипсина трески, как продемонстрировано SDS-электрофорезом, который дает одну полосу, изоэлектрическим фокусированием, показывающим три полосы, и хроматографическим фокусированием, которое дает три пика, соответствующих трем изоформам трипсина (Фиг.1). По крайней мере, четыре изоформы трипсина IV дополнительно содержатся в трипсиновой фракции, если не применяется анионообменная хроматография. Они могут быть выделены как подфракции последующей анионообменной хроматографией на Mono Q или ДЕАЕ.
Сериновые протеазы из других источников (не из атлантической трески) можно сравнить с выделенными трипсинами из атлантической трески по молекулярной массе, изоэлектрической точке, аминокислотной последовательности, температурной или рН-стабильности, температурному или рН-максимуму, протеолитической специфичности и кинетическим параметрам или другим характеристикам трипсинов атлантической трески, приведенным в примерах (Asgeirsson et al., Eur. J. Biochem. 180:85-94, 1989). Активность трипсина трески можно измерять с использованием в качестве субстрата тирозин-аргинин-метилового эфира (TAME). Выделенный после очистки на аффинной колонке трипсин трески (90-100% чистоты) будет предпочтительнее иметь специфическую активность, по крайней мере, 140 ед/мг при 25°С и рН 8,1 по сравнению с 60 ед/мг для многофункциональной гидролазы криля. Триптическую активность также можно измерить, используя в качестве субстрата Cbz-Gly-Pro-Arg-пара-нитроанилид (Cbz-GPR-pNA), дающий специфическую активность предпочтительнее, по крайней мере, около 100 ед/мг. Более того, если в качестве субстрата используется Bz-Arg-pNA, то получают константы каталитической эффективности (kcat/Km) 50, 20 и 7 s-1 мМ-1 для трипсинов трески I, II и III, соответственно, по сравнению с 3 s-1мМ-1 для бычьего трипсина (Asgeirsson et al., Eur. J. Biochem. 180:85-94, 1989). Похожие различия прослеживаются и для химотрипсинов трески и бычьего химотрипсина (Asgeirsson and Bjarnason, Comp. Biochem. Physiol. 99B:327-335, 1991).
Молекулярная масса трипсинов трески составляет около 24 кДа, а их изоэлектрические точки - 6,6; 6,2 и 5,5 соответственно для трипсинов I, II и III, и даже меньше для изоформ трипсина IV. Аминокислотные последовательности изоформ трипсина трески могут быть выражены следующей последовательностью, которая содержит точечную вариабельность благодаря множественности изоформ:
I-V-G-G-Y-E-C-T-K/R-H-S-Q-A-H-Q-V-S-L-N-S-G-Y-H-Y/F-C-G-G-S-L-I-N-K/E-D/Q-W-V-V-S-A-A-H-C-Y-K-S-V-L-R-V-R-L-G-E-H-H-I-R-V-N-E-G-T-E-Q-Y/F-I-S-S-S-S-V-I/X-R-H-P-N-Y-S-S-Y-N-I-N/D-N-D-I-M-L-I-K-L-T-K/E-P-A-T-L-N-Q-Y-V-H-A-V-A-L-P-T-E-C-A-A-D-A-T-M-C-T-V-S-G-W-G-N-T-M-S-S-V-A/D-D-G-D-K-L-Q-V/C-L-N/S-L-P-I-L-S-H-A-D-C-A-N-S-Y-G-P-G-M-I-T-Q-S-M-F-C-A-G-Y-L-E-G-G-K-D-S-C-Q-G-D-S-G-G-P-V-V-C-N-G-V-L-Q-G-V-G-V-V-S-W-G-Y-G-C-A-E-R-D-H/N-P-G-V-Y-A-K-V-M/V/C-V-L-S-G-W-V-R-D-T-M-A-N/S-Y, где X означает любую аминокислоту или ее отсутствие и трипсин I трески имеет аминокислоту К в положении 9, тогда как трипсины II и III трески содержат R в том же положении (Gudmundsdottir et al. 1993 и неопубликованные данные).
Как правило, трипсиновые изоформы трески будут достаточно стабильными, так что по крайней мере около 50% ТАМЕ-активности сохранится после инкубации при 5°С в течение 18 часов при рН 7,0 в буферном растворе, содержащем 10 мМ хлорида кальция. Однако только около 10% ТАМЕ-активности сохранится после инкубации при 5°С в течение 18 часов при рН 2,0 (Фиг.2).
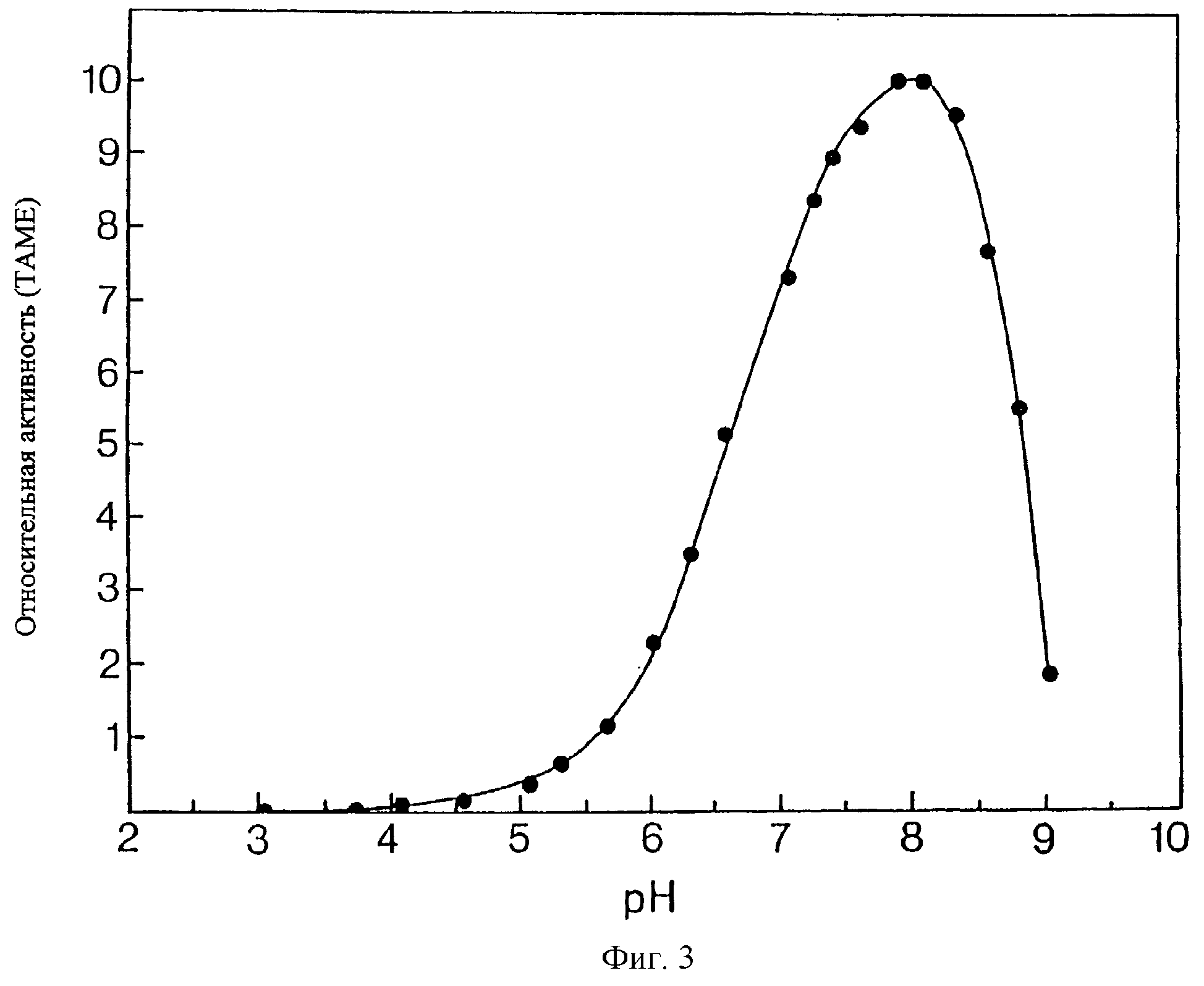
Оптимальное значение рН трипсинов трески для TAME в качестве субстрата находится предпочтительнее между приблизительно 7,0 и 8,7, более предпочтительно около 8,0 (Фиг.3). При использовании TAME в качестве субстрата Km при рН 8,1 и 25°С в присутствии 10 мМ хлорида кальция имеет значение предпочтительно около 0,029 мМ, 0,021 мМ и 0,049 мМ для трипсинов I, II и III, соответственно. Предпочтительнее, чтобы трипсин трески имел температурный максимум активности для TAME в качестве субстрата между 50 и 60°С (Фиг.4).
Трипсины и химотрипсины трески данного изобретения применяются местно, перорально, ректально, вагинально путем введения малых доз (например, в мочевой тракт или в свищи), путем легочного введения с помощью аэрозоля, путем закапывания в глаза или системно, например парентерально, включая, например, внутримышечное, подкожное, внутрибрюшинное, внутриартериальное или внутривенное введение. Ферменты трески применяются в растворе или в комбинации с фармацевтически приемлемым носителем или наполнителем в соответствии со стандартной фармацевтической практикой. Для перорального способа применения ферменты трески используются в форме таблеток, капсул, лепешек, жевательных резинок, пастилок, порошков, сиропов, эликсиров, водных растворов, суспензий и тому подобного. Для парентерального применения обычно приготавливают стерильные растворы ферментов трески с подходящим рН и добавлением буферных веществ. Для внутривенного применения общая концентрация растворенных веществ должна быть такова, чтобы препарат являлся изотоническим. Для глазного применения мази или капли могут наносится с помощью известных специалистам специализированных для глаз систем нанесения, таких как аппликаторы или глазные капельницы. Для легочного применения выбирают растворители и/или носители, которые способствуют образованию аэрозолей. Для местного применения ферменты трески обычно вводятся в гидрогель, содержащий от 0 до 85% глицерина, например от 20 до 30% глицерина, и, возможно, вплоть до 85% глицерина.
Для местной терапии подходящая для введения доза ферментов трески варьирует от 0,01 мкг/см2 до 1 мг/см2, предпочтительнее от 0,1 мкг/см2 до 0,1 мг/см2 (например, гель с содержанием фермента около 0,01 мг/мл). Для систематической терапии обычно выбираются дозы, которые будут поддерживать уровень трипсинов трески в сыворотке от 0,1 мг/100 мл до 100 мг/100 мл, предпочтительнее от 0,5 мг/100 мл до 2 мг/100 мл. При другом способе измерения используются количества для систематического применения предпочтительнее от 0,1 мг/кг до 10 мг/кг, более предпочтительно около 1 мг/кг. Для обработки влагалища и мочевого тракта соответствующие растворы ферментов трески, предназначенные для промывания/инстилляции, имеют в основном концентрации от 1 мкг/мл до 15 мг/мл, предпочтительнее от 100 мкг/мл до 3 мг/мл. Для всех обработок ферментная композиция вводится от 1 до 10 раз в день, предпочтительнее от 2 до 5 раз в день. Эти дозы зависят от множества факторов, включая тип и тяжесть заболевания и возраст, вес и медицинское состояние пациента, которые определяются специалистами. Предполагают, что значительно более высокие дозы можно применять без существенного побочного действия.
Для раневого заживления ферменты трески предпочтительнее следует применять не только при первой перевязке. Предпочтительнее, чтобы трипсин трески наносили по крайней мере, каждый раз во время перевязки раны. Предпочтительнее ферменты трески применять ежедневно или несколько раз в день. В случае дерматологических заболеваний, таких как экзема, псориаз и тому подобное, гидрогель, содержащий трипсины и/или химотрипсины трески, предпочтительнее наносят каждый день, более предпочтительно два раза в день. В случае острого или хронического воспаления, артрита, воспаленных суставов, бурсита, остеартрита и тому подобного трипсины трески предпочтительнее прикладывают каждый день, более предпочтительно два раза в день.
Как показано ниже в многочисленных клинических примерах, гидрогель, содержащий фермент трески данного изобретения, эффективен для лечения или предупреждения воспалительных состояний. Обычно воспаления уменьшаются до приемлемого уровня в пределах 2 или 3 дней от начала лечения. Примеры также показывают, что фермент эффективен для облегчения боли. Снятие боли часто происходит в пределах от 20 минут до 2 часов от начала лечения. Снятие боли не сопровождалось потерей чувствительности в обработанной ткани. Более полное снятие боли, при котором пациент испытывает незначительную боль или чувство болезненности, достигалось часто в течение 1 дня от начала лечения.
Ферменты трески, в соответствии с данным изобретением, применяются в эффективном количестве. Эффективное количество подразумевает количество, эффективное либо для (1) уменьшения симптомов болезни, которую хотят вылечить, либо для (2) индукции фармакологического изменения, относящегося к лечению болезни, которую хотят вылечить, либо для (3) ингибирования или предупреждения инфекции или повторной инфекции инфицирующим агентом, либо для (4) предупреждения появления неинфекционного заболевания (например, которое можно лечить путем блокирования явления клеточной адгезии). Один аспект раневой терапии подразумевает, что эффективное количество представляет собой количество, которое при регулярном применении предупреждает появление инфекции. Другой аспект раневой терапии подразумевает, что эффективное количество представляет собой количество, которое эффективно для уменьшения среднего значения времени, необходимого для заживления раны.
Специалистам известны многочисленные методы определения процента гомологии белков. Предпочтительным методом является использование версии 6.0 компьютерной программы GAP, осуществляющей сравнение последовательностей. Эта программа, которую можно приобрести в Генетической Компьютерной Группе Висконсинского университета, использует метод выравнивания Needelman и Wunsch (J. Mol. Biol. 48, 443 (1970)), переработанный Smith и Waterman (Adv. Appi, Math., 2, 482 (1981)). Другой доступный метод использует компьютерную программу FASTA.
Изобретение далее проиллюстрировано в следующих, не ограничивающих изобретение, примерах и чертежах, где:
На Фиг.1 изображена хроматограмма, полученная после хроматографического фокусирования трипсиновой фракции из атлантической трески на стадии очистки с использованием аффинной колонки с аминобензамидином. Фракцию, элюированную из пара-аминобензамидиновой колонки, подвергали гель-фильтрации на колонке с сефадексом G-25, уравновешенной 25 мМ буфером моноэтаноламин/уксусная кислота с рН 9,4, содержащим 10 мМ хлорида кальция, и затем наносили на колонку с ионообменным материалом РВЕ-94 (Pharmacia), уравновешенную тем же буфером. Колонку затем подвергали элюции Полибуфером 94 (доведенным до рН 5,5 уксусной кислотой), содержащим 10 мМ хлорида кальция. Контролировали активность субстрата TAME (темные кружки), поглощение при 280 нм (светлые кружки) и рН (светлые ромбы). Первая элюированная фракция соответствует трипсину I, вторая фракция - трипсину II и третья фракция - трипсину III;
Фиг.2 демонстрирует влияние рН на стабильность трипсина из атлантической трески, очищенного с помощью n-аминобензамидина, выраженную в виде по остаточной ТАМЕ-активности после инкубации при различных значениях рН и в течение разных периодов времени. Образцы трипсина из атлантической трески инкубировали при 5°С в течение 30 минут (светлые кружки) и 18 часов (темные квадратики) при различных значениях рН. Остаточную активность для субстрата TAME измеряли затем при рН 8,1 и 25°С;
На Фиг.3 представлена зависимость активности трипсина из атлантической трески, очищенного с помощью n-аминобензамидина, от рН, определенную с использованием субстрата TAME. Буферы с конечной концентрацией 0,1 М, представляли собой ацетат (рН 3,0-5,9), Hepes-HCl (pH 6,0-8,0) и глицинат (рН 8,3-9,0), все из которых содержали 10 мМ хлорида кальция; и
Фиг.4 показывает температурную зависимость активности трипсина I из атлантической трески по сравнению с активностью бычьего трипсина, измеренной с использованием субстрата TAME. Ферменты добавляли в предварительно нагретую термостатированную кювету и после короткого периода уравновешивания определяли среднюю скорость гидролиза в течение последующих 3 минут.
ПРИМЕР 1
Приготовление смеси протеаз из трески
Около 100 кг замороженных внутренних органов трески оттаивали и добавляли к четырехкратному объему холодной питьевой воды в резервуар для экстракции и рН подводили от 8 до 9 раствором гидроксида натрия. Смесь перемешивали приблизительно 2-6 часов при 0-5°С. После короткого периода грубой седиментации (приблизительно 30 минут) водный экстракт процеживали от оставшихся нерастворимых внутренностей с помощью насоса и собирали в седиментационном резервуаре. Водный экстракт отстаивали в охлажденном седиментационном резервуаре для осаждения приблизительно от 24 до 60 часов. Супернатант переливали из седиментационного резервуара в резервуар для хранения с использованием насоса. Супернатант концентрировали в 10-20 раз путем ультрафильтрации и диафильтрации до приемлемого уровня ионной силы с проводимостью ниже 3 мсек/см. Получали около 10-15 литров отфильтрованного белкового концентрата.
ПРИМЕР 2
Очистка трипсина трески из концентрированного экстракта внутренностей трески
Около 10 литров отфильтрованного концентрата, полученного в Примере 1, наносили приблизительно по 1 литру на серию непрерывно связанных хроматографических колонок, причем первая содержала катионообменную смолу CM fast flow (Pharmacia, Швеция), вторая - анионообменную смолу ДЭАЭ fast flow (Pharmacia, Швеция) и третья - аффинный лиганд пара-аминобензамидин, связанный с сефарозной смолой (Pharmacia, Швеция). Колонки предварительно уравновешивали приблизительно 10 объемами 25 мМ буфера Трис-HCl, рН 7,8, содержащего 2,5 мМ хлорида кальция (буфер А). Концентрат прокачивали через колонки со скоростью потока приблизительно 100 мл в минуту. После завершения загрузки концентрата на колонки, оставшийся материал вымывали из непрерывной системы колонок приблизительно 8 литрами буфера А.
После завершения промывки аффинную колонку с пара-аминобензамидином отсоединяли от других колонок и промывали приблизительно 5 колоночными объемами 25 мМ буфера Трис-HCl, рН 7,5, содержащего 0,5 М NaCl и 2,5 мМ хлорида кальция. Трипсины трески затем десорбировали с аффинного лиганда и элюировали колонку раствором 25 мМ уксусной кислоты, рН 3,2, содержащим 2,5 мМ хлорида кальция и 30% глицерина. Трипсиновую фракцию из трески собирали в нейтрализующий буфер 200 мМ Трис-HCl, рН 8,5, содержащий 30% глицерина.
Очищенный препарат трипсина трески был гомогенным, как показано SDS-электрофорезом в ПААГ и жидкостной хроматографией быстрого разрешения (FLPC) на Mono Q, и показал 3 изоформы трипсина при изоэлектрическом фокусировании. Ферментный препарат имел активность около 100 ед/мг с использованием Cbz-GPR-pNA в качестве субстрата, как описано выше. Очищенный препарат стерилизовали фильтрацией через 0,22 мкм фильтр и хранили замороженным при -20°С.
ПРИМЕР 3
Альтернативная очистка в коммерческом масштабе трипсина трески из концентрированного экстракта внутренностей трески
Около 10 литров отфильтрованного концентрата, полученного в Примере 1, наносили на аффинный лиганд пара-аминобензамидин, связанный с сефарозной смолой (Pharmacia, Швеция). Колонки предварительно уравновешивали приблизительно 10 колоночными объемами 25 мМ буфера Трис-HCl, рН 7,8, содержащего 2,5 мМ хлорида кальция (буфер А). Концентрат прокачивали через колонки со скоростью потока приблизительно 100 мл в минуту. После завершения загрузки концентрата на колонки оставшийся материал вымывали из непрерывной системы колонок приблизительно 8 литрами буфера А.
Аффинную колонку затем промывали приблизительно 5 колоночными объемами высоко солевого раствора 25 мМ буфера Трис-HCl, рН 7,5, содержащего 0,5 М NaCl и 2,5 мМ хлорида кальция. Трипсины трески затем десорбировали с аффинного лиганда и элюировали колонку раствором 25 мМ уксусной кислоты, рН 3,2, содержащим 2,5 мМ хлорида кальция и 30% глицерина. Трипсиновую фракцию из трески собирали в нейтрализующий буфер, содержащий 200 мМ Трис-HCl, рН 8,5, содержащего 30% глицерина, и эта фракция содержала от 5 до 6 г трипсина.
Очищенный препарат трипсина трески был гомогенным, как показано SDS-электрофорезом в ПААГ, и показал 3 изоформы трипсина при изоэлектрическом фокусировании. Минорную фракцию (<5%) отделяли последующей FLPC хроматографией на Mono Q, и определили, что она содержит, по крайней мере, четыре дополнительных изоформы: трипсин IVa, IVb, IVc и IVd. Ферментный препарат имел активность около 100 ед/мг при использовании в качестве субстрата Cbz-GPR-pNA, как описано выше. Очищенный препарат стерилизовали фильтрацией через 0,22 мкм фильтр, хранили замороженным при -20°С.
ПРИМЕР 4
Приготовление гидрогеля из препарата трипсинов трески
Очищенный препарат трипсина трески, полученный в Примере 2, смешивали с гидроколлоидным гелем, включающим водный гель, содержащий 0,8% (вес/объем) Carbomer 940, 30% глицерина и 0,08% параоксибензоата. Препарат трипсина трески смешивали в соотношении 1:1 с гидрогелем до получения конечной концентрации 1 единица ферментативной активности на мг (ед/мг) полученной смеси гель-фермент (ферментной гидрогелевой мази), причем единица ферментативной активности определялась при использовании в качестве субстрата Cbz-GPR-pNA, как описано выше. Таким образом, полученная ферментная гидрогелевая мазь содержала около 0,01 мг/мл, или 1 ед/мл трипсинов трески, 0,4% Carbomer 940, 20% глицерина и 0,04% параоксибензоата. В последующем эта ферментная гидрогелевая мазь обозначена как Пэнзим 100.
ПРИМЕР 5
Лечение остеоартрита Пэнзимом 100
17 пациентов с артритом, некоторые с острыми и очень тяжелыми симптомами, лечили ферментной гидрогелевой мазью (Пэнзимом 100) из Примера 4. Ферментный гель наносили один или два раза в день, всегда один раз вечером перед сном и в большинстве случаев также утром. Около 5 мл ферментного геля наносили на каждый пораженный участок, например колено, или тазобедренный сустав, или обе кисти. В тяжелых случаях можно наносить большие количества геля. Гель оставляли сушиться приблизительно на 10-30 минут, в зависимости от наносимого количества, имеющегося в распоряжении времени и потребностей пациента. Это высушивание можно ускорять, используя воздушный вентилятор, например фен. Все пациенты избавлялись от симптомов в течение одной недели, большинство же из них в течение 2-4 дней. Пациент №71 не способен был спускаться по лестнице до лечения, но не имел больше проблем после лечения. Эти результаты представлены в следующей Таблице 5.1:
Несколько пациентов (№№19 и 21) оказались в состоянии прекратить лечение и таким образом избавились от болезни совсем или на длительное время, но у большинства из них симптомы сохранялись при контроле с постоянным или прерывистым применением Пэнзима 100.
ПРИМЕР 6
Лечение пациентов, страдающих от тендивита
8 пациентов с тендивитом, некоторые из которых имели очень тяжелые симптомы, вызывающие проблемы с ночным сном, лечили ферментной гидрогелевой мазью (Пэнзимом 100) из Примера 4. Ферментный гель наносили местно на пораженный участок один или два раза в день, около 5-10 мл на каждый пораженный участок, в зависимости от размера участка. Гель оставляли сушиться приблизительно на 10-30 минут, в зависимости от нанесенного количества, имеющегося в наличии времени и потребностей пациента. Все эти пациенты избавлялись от симптомов в течение двух недель, большинство же из них в течение 2-4 дней, а другие болели дольше, особенно пациенты с тендинитом локтя (теннисный локоть или гольфный локоть). Эти результаты представлены в следующей Таблице 6.1:
Все эти пациенты избавились от симптомов совсем и прервали лечение.
ПРИМЕР 7
Лечение фибромиалгии
Двух пациенток, страдающих от тяжелой фибромиалгии, лечили с помощью ферментной гидрогелевой мази (Пэнзима 100) из Примера 4. Ферментный гель наносили местно на пораженный участок один или два раза в день, около 5-10 мл на каждый пораженный участок, в зависимости от размера участка. Гель оставляли сушиться приблизительно на 10-30 минут, в зависимости от нанесенного количества, имеющегося в наличии времени и потребностей пациента. Обе пациентки (№78, Ж-50 и №92, Ж-53) освобождались от симптомов в течение 3 недель. Обе пациентки используют лечение ферментным гелем, когда боль возобновляется.
ПРИМЕР 8
Лечение ревматоидного артрита
5 пациентов с ревматоидным артритом, некоторые имели очень тяжелые симптомы, лечили с помощью ферментной гидрогелевой мази (Пэнзима 100) из Примера 4. Ферментный гель наносили местно на пораженный участок обычно, по крайней мере, два раза в день, около 3-5 мл на каждый пораженный участок, в зависимости от размера участка. Гель оставляли сушиться приблизительно на 15 минут, в зависимости от толщины приложенного геля. Этот период высушивания можно сделать короче с использованием воздушного вентилятора, например фена. Все 5 пациентов освобождались от симптомов в течение 5 дней. Эти результаты просуммированы в следующей Таблице 8.1:
Пациентка №61 не могла вставать с постели и одеваться без помощи до тех пор, пока не начала лечение, но смогла полностью делать это после лечения. Пациент №94 жаловался на боль в груди при дыхании из-за осложнения в связи с плевральной эффузией. Он освободился от этих симптомов после 3 дней лечения Пэнзимом 100. Все эти пациенты контролировали эти симптомы постоянным или прерывистым лечением ферментным гелем.
ПРИМЕР 9
Лечение флебита
5 пациентов с различными формами флебита, такими как тромбофлебит, флеботромбоз, хронический постфлебитный синдром и варикозные вены, во всех случаях в икроножных мышцах, некоторые с очень тяжелыми симптомами, вызывающими боли и трудности при засыпании, лечили ферментной гидрогелевой мазью (Пэнзимом 100) из Примера 4. Ферментный гель наносили местно на икроножную мышцу, по крайней мере, один раз в день, то есть вечером, а в некоторых случаях также и утром, около 5 мл на каждую икроножную мышцу. Гель оставляли сушиться приблизительно на 15 минут. Все 5 пациентов освобождались от симптомов в течение нескольких недель. Эти результаты просуммированы в следующей Таблице 9.1:
У пациента №2 был диагноз - хронический постфлебитный синдром. Пациентка №68 не может спать ночью из-за боли, если она не наносит гель перед тем, как идти спать. Все эти пациенты контролировали симптомы постоянным или прерывистым лечением ферментным гелем.
ПРИМЕР 10
Лечение псориаза
6 пациентов с псориазом, некоторые хронические случаи с очень тяжелыми симптомами, лечили ферментным гелем из Примера 4, но в большинстве случаев псориаза использовали гидрогелевую композицию, названную Пэнзимом 200 с двойной концентрацией трипсина трески или 2 ед/мл, так как Пэнзим 100 (1 ед/мл трипсина трески) давал весьма слабые, а в некоторых случаях неопределенные результаты. Пациенты отмечали существенные улучшения в лечении гелем, содержащим более высокую концентрацию трипсина трески (Пэнзимом 200), по сравнению с гелем, содержащим более низкую концентрацию трипсина (Пэнзимом 100). Комбинация трипсина трески и химотрипсина трески с концентрацией 1 ед/мл для каждого фермента, названная Пэнзим 100-С, также исследованная, давала похожие положительные результаты, как и в случае с Пэнзимом 200. Ферментный гель наносили местно один или два раза в день, всегда вечером перед сном, после чего ферментный гель оставался на коже всю ночь, а в некоторых случаях также и утром после ванны и до одевания. Гель накладывали в виде тонкого слоя или пленки и оставляли сушиться приблизительно на 5 минут. Все 6 пациентов освобождались от симптомов в течение двух недель. В некоторых случаях лечение дополняли обычными методами самолечения, такими как солнечные ванны или обработка УФ-светом. Эти результаты просуммированы в следующей Таблице 10.1:
Пациентка №3 страдала от хронического и очень тяжелого псориаза с 5 лет. Она испробовала все возможные способы лечения, но с ограниченными результатами. Только лечение Пэнзимом 200 дало ей долговременное освобождение от симптомов. Она отмечает, что облегчение стало заметным после 4 дней и полное вылечивание наступило в течение 2-3 недель после начала лечения с одной аппликацией в день перед тем, как идти спать.
У пациента №69, также с тяжелым хроническим псориазом, наблюдалось исчезновение нескольких пятен. Все эти пациенты контролировали симптомы постоянным или прерывистым лечением ферментным гелем.
ПРИМЕР 11
Лечение акне и фурункулов
2 пациентов (№25 - Ж-16, и №63 - М-17), страдающих от акне, и одного пациента, страдающего от фурункулов (№64 - М-22), лечили гидрогелевой мазью, содержащей трипсин трески (Пэнзим 100) из Примера 4. Ферментный гель наносили местно на пораженный участок (лицо) один раз в день, каждый раз около 5 мл. Гель оставляли сушиться приблизительно на 15 минут, после чего его оставляли на коже. Все 3 пациента полностью освободились от симптомов в течение двух недель и использовали лечение ферментным гелем только в том случае, когда симптомы возобновлялись.
ПРИМЕР 12
Лечение экземы, дерматита и других кожных заболеваний
18 пациентов, страдающих от экземы, дерматита и других кожных заболеваний, лечили гидрогелевой мазью, содержащей трипсин трески (Пэнзим 100) из Примера 4. Ферментный гель наносили один раз в день (иногда два раза в день), обычно перед сном. Гель накладывали в виде тонкого слоя или пленки. Высушивание происходило в течение около 5-10 минут. В тяжелых случаях можно прикладывать более высокую концентрацию. Это высушивание можно ускорить, используя воздушный вентилятор, например фен. Все эти пациенты освободились от симптомов в течение одной недели, большинство из них в течение 2-4 дней. Эти результаты просуммированы в следующей Таблице 12.1:
Некоторые из этих пациентов (№№40, 41, 48, 66, 50, 20, 46, 87, 97, 100) оказались в состоянии прервать лечение и, следовательно, избавились от болезни совсем или на длительное время, но другие контролировали симптомы постоянным или прерывистым лечением Пэнзимом 100.
ПРИМЕР 13
Раневое заживление
Двух пациентов (№44 - М-4 и №85 - М-9) с ожогами лечили гидрогелевой мазью с трипсином трески (Пэнзим 100) из Примера 4. У двух других пациентов (№62 - Ж-47 и №96 - М-70) лечили послеоперационные раны, которые не заживали. Ферментный гель накладывали местно на раны, по крайней мере, два раза в день и оставляли на пораженном участке. Все 4 пациента испытали облегчение и заживление их ран произошло в течение 1-3 недель.
ПРИМЕР 14
Лечение химотрипсином трески
Для каждого из Примеров 5-13 ферментный гидрогель, содержащий трипсин трески, заменяли ферментным гидрогелем, содержащим химотрипсин трески, или гидрогелем, содержащим смесь трипсина трески и химотрипсина трески.
Реферат
Изобретение относится к области лекарственных средств и касается применения сериновых протеиназ рыб, выбранных из группы, состоящей из трипсина, химотрипсина и любой их смеси, полученной из трески, или имеющей, по меньшей мере, 90% гомологию по аминокислотной последовательности с трипсином или химотрипсином, выделенными из атлантической трески, в качестве лекарственного средства для лечения и/или предупреждения болезней, в патогенез которых вовлекается рецептор-опосредованное связывание. Также предлагается фармацевтическая композиция для лечения и/или предупреждения болезней у человека или животных, в патогенез которых вовлекается рецептор-опосредованное связывание, содержащая эффективное количество указанной сериновой протеиназы и фармацевтически приемлемый растворитель или носитель, и косметическая композиция для удаления мертвой или шелушащейся кожи со здоровой кожи, содержащая эффективное количество указанной сериновой протеиназы рыб. Техническим результатом является применение сериновых протеиназ для медицинских и косметических целей. 4 н. и 20 з.п. ф-лы, 6 табл., 4 ил.

Комментарии