Новый экстракт семянок silybum marianum и его применения в дерматологии и лечебно-косметических средствах для кожи - RU2746724C2
Код документа: RU2746724C2
Чертежи







Описание
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новому экстракту семянок Silybum marianum (L.) Gaertn., а также к содержащим его фармацевтическим и косметическим композициям, более конкретно, предназначенным для местного нанесения, к его способу получения и его применениям в дерматологии или косметологии, в частности, в лечении угрей, себореи, себорейного дерматита и/или розовых угрей.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Научное название Silybum marianum (L.) Gaertn. обозначает растение, принадлежащее к семейству Asteraceae, которое является однолетним или двухлетним с крепким стеблем, который может достигать вплоть до одного метра в высоту. Его большие, блестящие, чередующиеся листья, лишенные прилистников, покрыты белыми крапинками и окружены твердыми, острыми шипами. Цветки собраны в соцветия, часто одиночные. Они окружены большими, колючими прицветниками с очень острыми концами. Цветки с трубочками и пятью лопастями имеют фиолетово-пурпурный цвет. Плодами являются блестящие семянки с черными или желтыми крапинками, с летучкой на кончике, имеющей зубчатые щетинки, организованные в кольцо у ее основания. Народное название данного растения - молочный чертополох.
Семянка (часто неправильно называемая в литературе «семя») Silybum marianum (L.) Gaertn. и ее препараты традиционно используются перорально в симптоматическом лечении расстройств пищеварительной функции, приписываемых по происхождению печени.
Главным активным ингредиентом семянки Silybum marianum (L.) Gaertn. является силимарин - смесь целого ряда флавонолигнанов (по существу силибин, изосилибин, силихристин и силидианин). Семянки содержат вплоть до 3% по массе силимарина. Они также состоят из масла (20-30% по массе), слизи и белков.
Силимарин был темой многочисленных исследований (in vitro, in vivo и клинических), продемонстрировав его антиоксидантные, защищающие печень, способствующие пищеварению или противовоспалительные свойства.
В настоящее время экстракты семянок Silybum marianum (L.) Gaertn. с высоким содержанием силимарина присутствуют во многих фармацевтических препаратах, предназначенных для лечения разных расстройств печени и желчного пузыря, таких как Легалон®.
Кроме того, силимарин был темой исследования в лечении угрей (Sahib et al. 2012), а также в лечении эритематозно-телеангиэктатических розовых угрей в ассоциации с метилсульфонилметаном (MSM) (Berardesca et al. 2008).
Масло Silybum marianum (L.) Gaertn., богатое омега 6 и витамином Е, используется, главным образом, в приготовлении пищи. Его традиционно получают из семянок посредством холодного прессования.
Исследования по антиоксидантным и гепатозащитным свойствам такого масла молочного чертополоха, вводимого перорально, однако, проводили in vivo на крысах или мышах (Hermenean et al. 2015; Zhu et al. 2014).
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Заявитель неожиданно продемонстрировал то, что экстракт семянок Silybum marianum (L.) Gaertn. с низким содержанием силимарина демонстрировал очень интересные свойства в отношении лечения угрей, себореи, розовых угрей или себорейного дерматита.
Один объект изобретения, следовательно, относится к экстракту семянок Silybum marianum (L.) Gaertn., содержащему меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта для его применения в лечении угрей, себореи, розовых угрей и/или себорейного дерматита.
Другой объект изобретения относится к применению экстракта семянок Silybum marianum (L.) Gaertn., содержащему меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта, для изготовления лекарственного средства, предназначенного для лечения угрей, себореи, розовых угрей и/или себорейного дерматита.
Другой объект изобретения относится к применению Silybum marianum (L.) Gaertn., содержащему меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта, в лечении угрей, себореи, розовых угрей и/или себорейного дерматита.
Другой объект изобретения относится к способу лечения угрей, себореи, розовых угрей и/или себорейного дерматита, включающему введение субъекту, нуждающемуся в этом, эффективного количества экстракта семянок Silybum marianum (L.) Gaertn., содержащего меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта.
Другой объект изобретения относится к экстракту семянок Silybum marianum (L.) Gaertn., содержащему меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта.
Другой объект изобретения относится к экстракту семянок Silybum marianum (L.) Gaertn., содержащему меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта, для его применения в качестве лекарственного средства.
Другой объект изобретения относится к фармацевтической (особенно к дерматологической) или косметической (особенно дермокосметической) композиции, содержащей экстракт семянок Silybum marianum (L.) Gaertn., содержащий меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта, в смеси с по меньшей мере одним фармацевтически или косметически приемлемым эксципиентом.
Другой объект изобретения относится к фармацевтической (особенно к дерматологической) или косметической (особенно дермокосметической) композиции, содержащей экстракт семянок Silybum marianum (L.) Gaertn., содержащий меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта, в смеси с по меньшей мере одним фармацевтически или косметически приемлемым эксципиентом для ее применения в лечении угрей, себореи, розовых угрей и/или себорейного дерматита.
Другой объект изобретения относится к применению фармацевтической (особенно к дерматологической) или косметической (особенно дермокосметической) композиции, содержащей экстракт семянок Silybum marianum (L.) Gaertn., содержащий меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта, в смеси с по меньшей мере одним фармацевтически или косметически приемлемым эксципиентом в лечении угрей, себореи, розовых угрей и/или себорейного дерматита.
Другой объект изобретения относится к способу лечения угрей, себореи, розовых угрей и/или себорейного дерматита, включающему введение субъекту, нуждающемуся в этом, предпочтительно местным путем, эффективного количества фармацевтической (особенно дерматологической) или косметической (особенно дермокосметической) композиции, содержащей экстракт семянок Silybum marianum (L.) Gaertn., содержащий меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта, в смеси с по меньшей мере одним фармацевтически или косметически приемлемым эксципиентом.
Другой объект изобретения относится к способу получения экстракта семянок Silybum marianum (L.) Gaertn., содержащего меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта, включающему стадию экстрагирования масла, полученного из семянок Silybum marianum (L.) Gaertn., экстрагирующим растворителем, содержащим, в частности состоящим из гидротропического водного раствора, субкритической воды или органического растворителя, не смешивающегося с маслом, полученным из семянок Silybum marianum (L.) Gaertn., возможно, в смеси с водой.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем описании растение Silybum marianum (L.) Gaertn. может называться с использованием сокращенного термина Silybum marianum.
Термин «силимарин» согласно настоящему изобретению обозначает очищенный экстракт семянок Silybum marianum (L.) Gaertn., главным образом содержащий (по меньшей мере 95% по массе) смесь следующих четырех флавонолигнанов: силибин, изосилибин, силикристин и силидианин (Kuki et al. 2012). Содержание силимарина меньше, чем 0,2% по его массе означает то, что общее количество компонентов силимарина меньше, чем 0,2% по массе. Такое содержание может быть, в частности, определено посредством ВЭЖХ (высокоэффективная жидкостная хроматография) или СВЭЖХ (сверхэффективная жидкостная хроматография) путем расчета общей площади пиков, соответствующих всем компонентам силимарина, в частности, с использованием стандартного образца силимарина, который может быть приобретен, например, у Sigma Aldrich, для определения положения данных пиков.
Термин «силибин», также именуемый в данной области силибинин, обозначает, согласно настоящему изобретению, четыре диастереоизомера: силибин А, силибин В, 2,3-цис-силибин А и 2,3-цис-силибин В.
Термин «изосилибин» обозначает согласно настоящему изобретению два диастереоизомера: изосилибин А и изосилибин В.
Термин «силикристин» обозначает согласно настоящему изобретению два диастереоизомера: силикристин А и силикристин В.
Термин «приблизительно» обозначает в настоящем изобретении то, что рассматриваемое значение может быть меньше или больше на 10%, в частности, на 5%, в частности, на 1%, чем указанное значение.
Термин «сухой экстракт» обозначает согласно настоящему изобретению экстракт, лишеный экстрагирующего растворителя или просто содержащий его в незначимых следовых количествах. Такой сухой экстракт, таким образом, содержит только вещество, полученное из Silybum marianum (L.) Gaertn. Он также может содержать незначимые следы экстрагирующего растворителя.
Термин «органический растворитель, не смешивающийся с маслом, полученным из семянок Silybum marianum (L.) Gaertn.» согласно настоящему изобретению обозначает органический растворитель, который не способен к смешиванию или просто частично смешивается с маслом, полученным из алкенов Silybum marianum (L.) Gaertn., таким образом, что смесь органических растворителей и масла, полученного из семянок Silybum marianum (L.) Gaertn., дает гетерогенную смесь, в которой можно наблюдать по меньшей мере две отдельные фазы.
Экстракт по изобретению
Экстракт по изобретению представляет собой экстракт семянок Silybum marianum, содержащий меньше, чем 0,2%, предпочтительно меньше, чем 0,1% по массе силимарина по отношению к массе сухого экстракта.
Согласно одному конкретному воплощению экстракт по изобретению содержит по меньшей мере 0,5% по массе, предпочтительно по меньшей мере 1,0% по массе бета-ситостерола по отношению к сухому экстракту. В частности, экстракт по изобретению содержит от 0,5% до 2,5% по массе, в частности, от 1,0% до 2,0% по массе, например, приблизительно 1,5% по массе бета-ситостерола по отношению к массе сухого экстракта. Отношение масс силимарин/бета-ситостерол экстракта по изобретению, в частности, может быть меньше, чем 0,4, в частности, меньше, чем 0,07. Экстракт по изобретению может дополнительно содержать от 2 до 7% по массе, в частности, от 3 до 6% по массе, например, от 3 до 5% по массе стеролов по отношению к массе сухого экстракта.
Термин «стерол» обозначает согласно настоящему изобретению молекулу, имеющую ядро стерана, в котором углерод 3 несет гидроксильную группу ОН, причем данный стеран имеет следующую структуру:
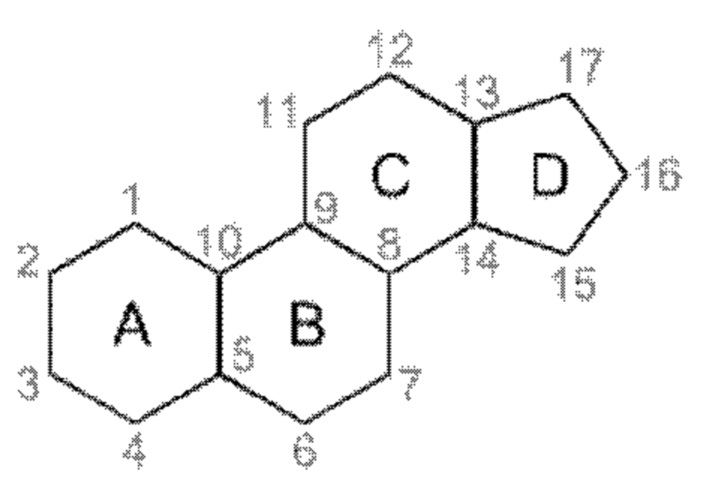
Согласно одному конкретному воплощению экстракт по изобретению содержит по меньшей мере 3% по массе, предпочтительно по меньшей мере 4% по массе свободной линолевой кислоты по отношению к массе сухого экстракта. В частности, экстракт по изобретению содержит от 3% до 15% по массе, в частности, от 4% до 10% по массе, в частности, от 4% до 6% по массе, например, приблизительно 5% по массе свободной линолевой кислоты по отношению к массе сухого экстракта. Экстракт по изобретению может дополнительно содержать от 10% до 70%, в частности, от 10% до 30% по массе, в частности, от 15% до 25% по массе свободных жирных кислот по отношению к массе сухого экстракта.
Термин «жирная кислота» обозначает, согласно настоящему изобретению, карбоновую кислоту R1CO2H, в которой цепь R1 является линейной или разветвленной углеводородной цепью, насыщенной или содержащей двойные С=С связи, причем данная карбоновая кислота содержит от 16 до 22 атомов углерода (включая атом углерода функциональной карбоксильной группы).
Термин «свободная» жирная кислота (включая линолевую кислоту) согласно настоящему изобретению обозначает жирную кислоту, не связанную с другими молекулами (например, с глицерином или его производными с образованием глицеридов, или со спиртом с образованием сложного эфира жирной кислоты).
Согласно другому конкретному воплощению экстракт по изобретению содержит от 0,5% до 2,5% по массе, в частности, от 1,0% до 2,0% по массе, например, приблизительно 1,5% по массе бета-ситостерола по отношению к массе сухого экстракта, и от 3% до 15% по массе, в частности, от 4% до 10% по массе, в частности, от 4% до 6% по массе, например, приблизительно 5% по массе свободной линолевой кислоты по отношению к массе сухого экстракта. Отношение масс силимарин/бета-ситостерол экстракта по изобретению, в частности, может составлять меньше, чем 0,4, в частности, меньше, чем 0,07. Экстракт по изобретению может дополнительно содержать от 2 до 7% по массе, в частности, от 3 до 6% по массе, например, от 3 до 5% по массе стеролов по отношению к массе сухого экстракта, и от 10% до 50%, в частности, от 10 до 30% по массе, в частности, от 15 до 25% по массе свободных жирных кислот по отношению к массе сухого экстракта.
Согласно одному конкретному воплощению экстракт по изобретению содержит по меньшей мере 0,01% по массе, в частности, по меньшей мере 0,05% по массе токоферолов по отношению к массе сухого экстракта. В частности, экстракт по изобретению содержит от 0,01% до 0,5% по массе, в частности, от 0,05% до 0,2% по массе, например, приблизительно 0,1% по массе токоферолов по отношению к массе сухого экстракта. Отношение масс силимарин/токоферолы экстракта по изобретению, в частности, может составлять меньше, чем 1, в частности, меньше, чем 0,1.
Термин «токоферол» обозначает согласно настоящему изобретению α-токоферол, β-токоферол, γ-токоферол и δ-токоферол.
Согласно другому конкретному воплощению экстракт по изобретению содержит от 0,5% до 2,5% по массе, в частности, от 1,0% до 2,0% по массе, например, приблизительно 1,5% по массе бета-ситостерола по отношению к массе сухого экстракта; от 3% до 15% по массе, в частности, от 4% до 10% по массе, в частности, от 4% до 6% по массе, например, приблизительно 5% по массе свободной линолевой кислоты по отношению к массе сухого экстракта; и от 0,01% до 0,5% по массе, в частности от 0,05% до 0,2% по массе, например, приблизительно 0,1% по массе токоферолов по отношению к массе сухого экстракта. Экстракт по изобретению может дополнительно содержать от 2 до 7% по массе, в частности, от 3 до 6% по массе, например, от 3 до 5% по массе стеролов по отношению к массе сухого экстракта и от 10% до 50%, в частности, от 10% до 30% по массе, в частности, от 15% до 25% по массе свободных жирных кислот по отношению к массе сухого экстракта. Отношение масс силимарин/бета-ситостерол экстракта по изобретению может составлять, в частности, меньше, чем 0,4, в частности, меньше, чем 0,07. Отношение масс силимарин/токоферолы экстракта по изобретению может составлять, в частности, меньше, чем 1, в частности, меньше, чем 0,1.
Предпочтительно экстракт по настоящему изобретению будет представлять собой сухой экстракт.
Согласно предпочтительному воплощению экстракт по изобретению подходит для получения посредством способа по изобретению, описанного далее.
Способ получения экстракта по изобретению
Способ получения экстракта по изобретению включает стадию экстрагирования масла, полученного из семянок Silybum marianum (L.) Gaertn., экстрагирующим растворителем, содержащим, в частности, состоящим из гидротропического водного раствора, субкритической воды или органического растворителя, не смешивающегося с маслом, полученным из семянок Silybum marianum (L.) Gaertn., возможно в смеси с водой.
Согласно одному конкретному воплощению органический растворитель содержит, предпочтительно состоит из органического растворителя, не смешивающегося с маслом, полученным из семянок Silybum marianum (L.) Gaertn., возможно в смеси с водой.
Органический растворитель, не смешивающийся с маслом, полученным из семянок Silybum marianum (L.) Gaertn., в частности, может представлять собой C1-С3 спирт.
Внеклеточный растворитель, в частности, может представлять собой С1-С3 спирт, возможно в смеси с водой.
Термин «С1-С3 спирт» согласно настоящему изобретению означает спирт R2OH, в котором цепь R2 является насыщенной, линейной или разветвленной углеводородной цепью, содержащей от 1 до 3 атомов углерода. Он может состоять из метанола, этанола, н-пропанола или изопропанола, в частности, метанола, этанола или изопропанола. Предпочтительно он будет представлять собой изопропанол.
Органический растворитель, не смешивающийся с маслом, полученным из семянок Silybum marianum (L.) Gaertn., в частности, С1-С3 спирт, такой как метанол, этанол или изопропанол, может использоваться в смеси с водой, в частности при отношении объемов органический растворитель/вода от 80/20 до 100/0, в частности, от 85/15 до 95/5, в частности, приблизительно 90/10.
Экстракционный растворитель может, в частности, быть выбран из метанола, смеси метанол/вода, этанола, смеси этанол/вода, изопропанола и смеси изопропанол/вода.
Согласно предпочтительному воплощению экстрагирующий растворитель будет представлять собой метанол, смесь этанол/вода при отношении объемов приблизительно 90/10 или смесь изопропанол/вода при отношении объемов приблизительно 90/10, предпочтительно смесь изопропанол/вода при отношении объемов приблизительно 90/10.
Стадия экстрагирования масла, получаемого из семянок Silybum marianum, будет проводиться, в частности, смешиванием масла, получаемого из семянок Silybum marianum, с экстрагирующим растворителем в течение 1-12 ч и, в частности, при температуре от 15 до 25°С, в частности, приблизительно 20°С. Количество экстрагирующего растворителя, используемого для осуществления данной экстракции, преимущественно будет составлять от 0,5 до 3 г, в частности, от 1 до 3 г для 1 г масла, полученного из семянок Silybum marianum (L.) Gaertn.
Тогда в конце данной экстракции будет получена экстракционная фаза и липидная. Экстракционная фаза будет преимущественно отделена от липидной фазы и извлечена до высушивания, частичного или полного, в частности в вакууме, для большего или меньшего удаления экстрагирующего растворителя и получения либо сухого экстракта при полном удалении растворителя, либо концентрированного экстракта, который разводят в остаточном растворителе.
Масло, получаемое из семянок Silybum marianum, преимущественно может быть получено экстракцией из семянок Silybum marianum (L.) Gaertn. (семянки могут быть целыми или разделенными на части), в частности, посредством прессования, преимущественно посредством холодного прессования (т.е. без нагревания, при температуре окружающей среды).
Согласно одному воплощению по изобретению способ по изобретению будет включать следующие две последовательные стадии:
(i) экстрагирование масла из семянок Silybum marianum (L.) Gaertn. и
(ii) экстрагирование масла, полученного из семянок Silybum marianum (L.) Gaertn., экстрагирующим растворителем, содержащим, в частности состоящим из гидротропического водного раствора, субкритической воды или органического растворителя, не смешивающегося с маслом, полученным из экстракта семянок Silybum marianum (L.) Gaertn., возможно в смеси с водой.
Согласно предпочтительному воплощению по изобретению способ по изобретению будет включать следующие последовательные стадии:
(i) возможно экстрагирование масла из семянок Silybum marianum (L.) Gaertn. и
(ii) экстрагирование масла, полученного из семянок Silybum marianum (L.) Gaertn., экстрагирующим растворителем, содержащим, в частности состоящим из гидротропического водного раствора, субкритической воды или органического растворителя, не смешивающегося с маслом, полученным из экстракта семянок Silybum marianum (L.) Gaertn., возможно в смеси с водой,
(iii) извлечение экстракционной фазы, полученной на стадии (ii), и
(iv) частичная или полная сушка экстракционной фазы с получением концентрированного или сухого экстракта по изобретению.
Стадия (i) будет преимущественно проводиться холодным прессованием семянок Silybum marianum (L.) Gaertn., целых или разделенных на части.
Стадия (ii) будет преимущественно проводиться с использованием экстрагирующего растворителя, как определено выше, и, в частности, выбранного из метанола, смеси метанол/вода, этанола, смеси этанол/вода, изопропанола и смеси изопропанол/вода.
Органический растворитель, не смешивающийся с маслом, полученным из семянок Silybum marianum (L.) Gaertn., в частности, С1-С3 спирт, такой как метанол, этанол или изопропанол, может использоваться в смеси с водой, в частности при отношении объемов органический растворитель/вода от 80/20 до 100/0, в частности, от 85/15 до 95/5, в частности, приблизительно 90/10. Преимущественным экстрагирующим растворителем является смесь изопропанол/вода при отношении объемов приблизительно 90/10.
Стадию экстракции (ii) можно проводить смешиванием масла, полученного из семянок Silybum marianum, с экстрагирующим растворителем в течение 1-12 ч и, в частности, при температуре от 15 до 25°С, в частности, при приблизительно 20°С. Количество экстракционного растворителя, используемого для проведения данной экстракции будет преимущественно составлять от 0,5 до 3 г, в частности, от 1 до 3 г для 1 г масла, полученного из семянок Silybum marianum (L.) Gaertn. Данная стадия экстракции (ii) делает возможным получение в конце интересующей экстракционной фазы и липидной фазы.
Стадия (iii) будет преимущественно проводиться посредством отделения экстракционной фазы от липидной фазы.
Стадия (iv) будет преимущественно проводиться в вакууме.
Фармацевтическая или косметическая композиция по изобретению Фармацевтическая или косметическая композиция по изобретению содержит экстракт по изобретению, как определено выше, в смеси с по меньшей мере одним фармацевтически или косметически приемлемым эксципиентом. Она предпочтительно состоит из местной композиции.
В настоящем изобретении термин «фармацевтически или косметически приемлемый» обозначает то, что является пригодным в приготовлении фармацевтической или косметической композиции, которое, в общем, является безопасным, нетоксичным и ни биологически, ни иным образом нежелательным, и которое является приемлемым для фармацевтического или косметического применения и, в частности, дерматологического или дермо-косметического, в частности, посредством местного применения.
Композиции по изобретению преимущественно предназначены для местного применения, в частности, на коже.
Композиции по изобретению, таким образом, могут быть представлены в формах, которые обычно известны для местного введения, т.е., в частности, лосьонов, пен, гелей, дисперсий, эмульсий, спреев, сывороток, масок или кремов, с подходящими эксципиентами, в частности, для проникновения через кожу для того, чтобы улучшать свойства и доступность активного ингредиента. Преимущественно это будет крем.
Данные композиции обычно содержат, помимо экстракта по настоящему изобретению, физиологически приемлемую среду, обычно на основе воды или растворителя, например, спиртов, простых эфиров или гликолей. Они также могут содержать поверхностно-активные вещества, комплексообразующие агенты, консерванты, стабилизаторы, эмульгаторы, загустители, гелеобразующие агенты, увлажнители, мягчители, микроэлементы, незаменимые масла, отдушки, красители, матирующие агенты, химические или минеральные фильтры, увлажнители, минеральные воды и т.д.
Согласно одному конкретному воплощению композиция по настоящему изобретению содержит по меньшей мере один фармацевтически или косметически приемлемый эксципиент, выбранный из матирующих агентов, увлажнителей и их смесей. Согласно другому воплощению композиция по настоящему изобретению содержит по меньшей мере один матирующий агент и/или по меньшей мере один увлажнитель, возможно с по меньшей мере одним химическим или минеральным фильтром (УФ (ультрафиолет) фильтр).
Увлажнитель увеличивает содержание влаги в коже и сохраняет ее мягкой и гладкой. Он может представлять собой, например, мочевину, аминокислоту, глицерол (также именуемый глицерин), пропиленгликоль, бутиленгликоль, сорбит, ксилит, мальтит, маннит, полидекстрозу, коллаген, эластин, гиалуроновую кислоту и ее соли (такие как натриевые или калиевые соли), пектин, желатин, хитозан, алоэ древовидное, мед или их смесь.
Матирующий агент представляет собой ингредиент, который делает кожу матовой, который предотвращает ее блеск. Он может представлять собой, например, тальк, диоксид кремния, рисовую пудру или их смесь, а именно - в микронизированной форме.
УФ фильтр представляет собой соединение, которое блокирует или поглощает ультрафиолетовый (УФ) свет, а именно для того, чтобы защитить кожу от солнечного УФ. Он может представлять собой, например, фильтр УФ А, фильтр УФ В, фильтр широкого спектра или их смесь.
Согласно другому конкретному воплощению композиция по изобретению содержит в качестве фармацевтически или косметически приемлемого эксципиента изопропанол, полиэтиленгликоль (ПЭГ) или их смесь. По существу преимущественно композиция по настоящему изобретению будет содержать, в частности, состоять из экстракта по изобретению, изопропанола и полиэтилен гликоля (ПЭГ). Данная композиция также может содержать экстракт по изобретению, изопропанол, полиэтиленгликоль (ПЭГ) и по меньшей мере один ингредиент, выбранный из матирующих агентов, увлажнителей, фильтров УФ и их смесей. Данная композиция также может содержать экстракт по изобретению, изопропанол, полиэтиленгликоль (ПЭГ), по меньшей мере один матирующий агент и/или по меньшей мере другой увлажнитель и, возможно, по меньшей мере один химический или минеральный фильтр (фильтр УФ). Матирующие агенты, увлажнители м фильтры УФ являются такими, как определено выше.
Отношение масс изопропанол/ПЭГ преимущественно будет составлять от 1/2 до 2/1, в частности, от 1/1,5 до 1,5/1, в частности, будет составлять приблизительно 1/1.
В частности, полиэтиленгликоль может иметь среднюю молекулярную массу, составляющую от 200 до 600 г/моль, в частности, от 200 до 500 г/моль, в частности, от 200 до 400 г/моль, например, от 250 до 350 г/моль, в частности приблизительно 300 г/моль. Таким образом, он, в частности, может представлять собой ПЭГ 300.
Данные композиции могут дополнительно содержать другие активные ингредиенты, приводящие к взаимодополняющему или, возможно, синергическому эффекту.
Преимущественно композиции по настоящему изобретению будут содержать по меньшей мере 0,001% по массе, а именно: от 0,001 до 15% по массе, от 0,001 до 10% по массе или от 0,001 до 5% по массе, в частности, от 0,01 до 15% по массе, от 0,01 до 10% по массе или от 0,01 до 5% по массе, предпочтительно от 0,1 до 10% по массе, а именно - от 0,1 до 5% по массе экстракта по изобретению по отношению к общему объему композиции.
Предпочтительно композиция по изобретению, как определено выше, не будет содержать какое-либо растительное масло, а именно - любое масло.
Терапевтические применения
Экстракты по изобретению и содержащие их фармацевтические композиции подходят для применения в лечении угрей (например, юношеских угрей, также известных как угри подростков, или угрей взрослых, которые могут быть кистозными), себореи, себорейного дерматита и/или розовых угрей, предпочтительно посредством местного нанесения, в частности, на кожу.
ГРАФИЧЕСКИЕ МАТЕРИАЛЫ
На Фиг. 1А, 1Б и 1В представлены, соответственно, хроматограмма СВЭЖХ силимарина (Sigma Aldrich), экстракта I семянок Silybum marianum по изобретению и экстракта А семянок Silybum marianum согласно предшествующему уровню техники, полученному согласно Протоколу 1.
На Фиг. 2А, 2Б и 2В представлены, соответственно, хроматограмма СВЭЖХ метанольного экстракта М по изобретению, экстракта Е этанолом 90 по изобретению и экстракта I изопропанолом 90 по изобретению, полученных согласно Протоколу 2.
На Фиг. 3А, 3Б и 3В представлены, соответственно, хроматограмма СВЭЖХ линолевой кислоты экстракта I семянок Silybum marianum по изобретению и экстракта А семянок Silybum marianum согласно предшествующему уровню техники, полученных согласно Протоколу 2.
На Фиг. 4А, 4Б и 4В представлена, соответственно, область 10-28 мин (соответствующая области жирных кислот и стеролов) хроматограммы ГХ-МС экстракта Е этанолом 90 по изобретению, метанольного экстракта М по изобретению и экстракта I изопропанолом 90 по изобретению, полученных согласно Протоколу 3.
На Фиг. 5А, 5Б и 5В представлена, соответственно, область 22-28 мин (соответствующая области стеролов) хроматограмм на Фиг. 4А, 4Б и 4В.
На Фиг. 6А, 6Б и 6В представлена, соответственно, область 10-22 мин (соответствующая области жирных кислот) хроматограмм на Фиг. 4А, 4Б и 4В.
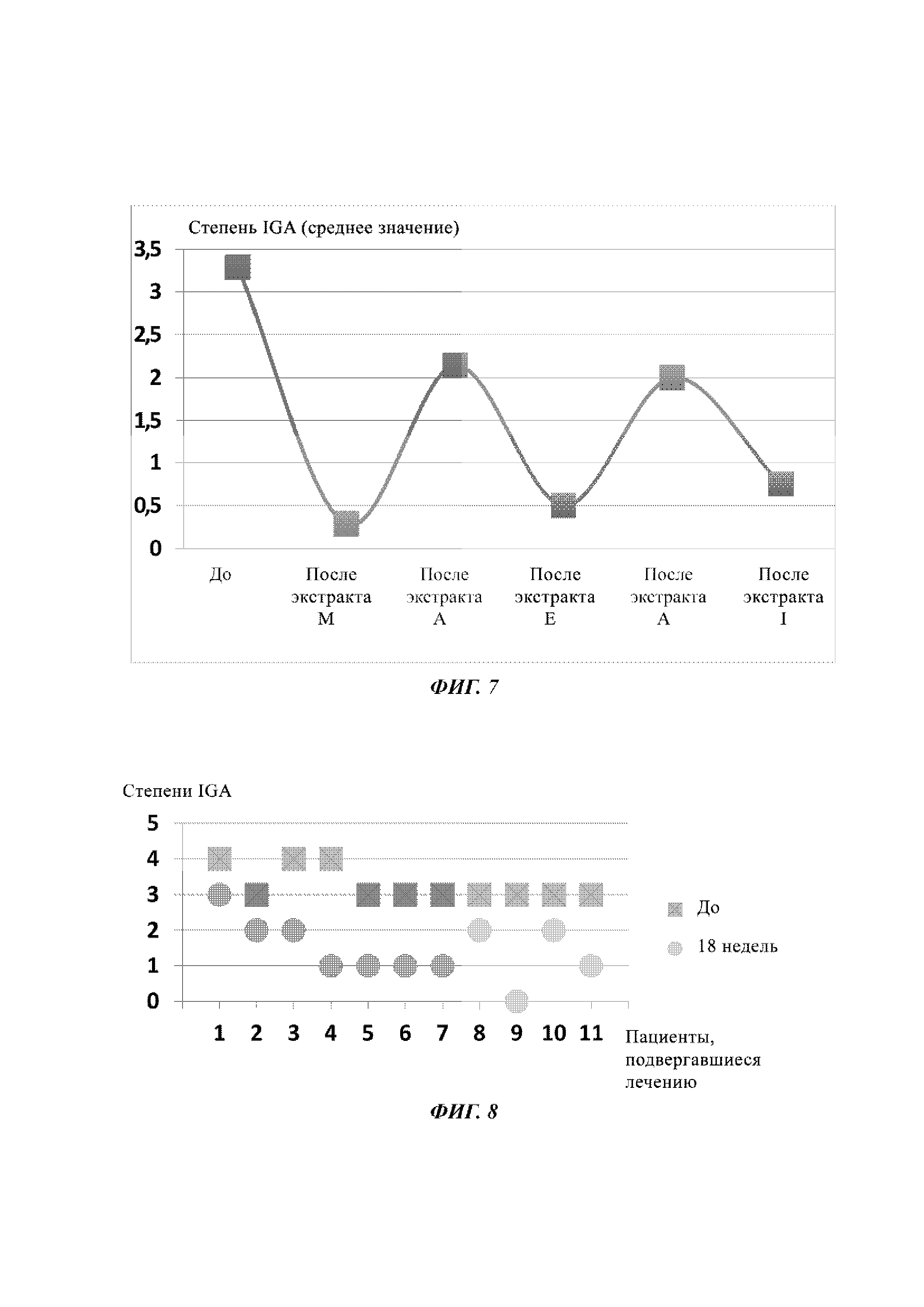
На Фиг. 7 показан средний терапевтический эффект на 7 пациентах, страдающих от угрей, определенный способом IGA после последовательного лечения экстрактами семянок Silybum marianum по изобретению, бедными силимарином (экстракты I, М и Е) и экстрактами семянок Silybum marianum согласно предшествующему уровню техники, богатыми силимарином (экстракт А).
На Фиг. 8 показан терапевтический эффект у 11 пациентов, страдающих от угрей взрослых, определенный способом IGA после лечения экстрактом семянок Silybum marianum по изобретению.
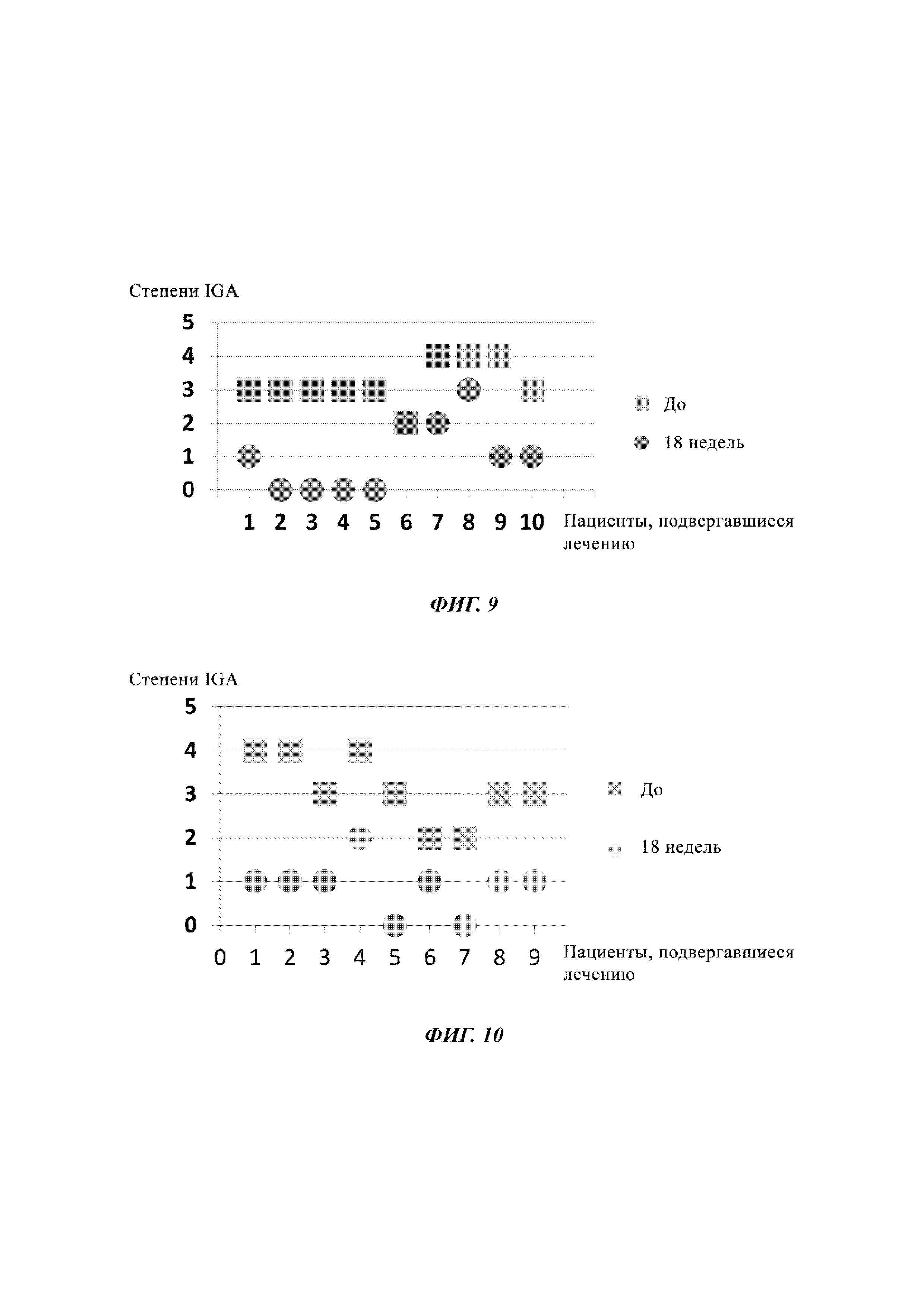
На Фиг. 9 показан терапевтический эффект у 10 пациентов, страдающих от угрей подростков, определенный способом IGA после лечения экстрактом семянок Silybum marianum по изобретению.
На Фиг. 10 показан терапевтический эффект у 9 пациентов, страдающих от розовых угрей с себореей, определенный способом IGA после лечения экстрактом семянок Silybum marianum по изобретению.
На Фиг. 11 представлено среднее ингибирование (кратность) двух генов себогенных ферментов - FADS2 и SCD1 - экстрактом семянок Silybum marianum по изобретению и экстрактом семянок Silybum marianum согласно предшествующему уровню техники.
ПРИМЕРЫ
1. Приготовление экстракта
Способ А: способ согласно предшествующему уровню техники, дающий экстракт А, имеющий высокое содержание силимарина:
• экстракция семянок Silybum marianum 96%-ным этанолом в течение 1 ч с обратным холодильником с использованием 10 мл этанола на грамм семянок,
• фильтрование смеси,
• извлечение этанольной фазы, и
• выпаривание растворителя.
Способ Б: способ по изобретению, дающий экстракт изопропанолом 90 (экстракт I), имеющий низкое содержание силимарина:
• холодное прессование семянок Silybum marianum с получением масла из семянок Silybum marianum,
• экстракция масла, полученного из семянок Silybum marianum, смесью изопропанол/вода (90/10 об./об.) с использованием 1 грамма смеси изопропанол/вода на грамм масла в течение 2 часов при 20°,
• извлечение изопропанольной фазы, и
• выпаривание растворителя.
Метанольный экстракт (экстракт М) и экстракт этанолом 90 (экстракт Е) получали аналогичным образом, заменяя смесь изопропанол/вода (90/10 об./об.) метанолом и смесью этанол/вода (90/10 об./об.) соответственно. Экстракция масла, полученного из семянок Silybum marianum, проводится, соответственно, 3 объемами метанола и 3 объемами смеси этанол/вода (90/10 об./об.) для 1 объема масла в течение 2 часов при 20°С.
Эти разные экстракты характеризовали СВЭЖХ (сверхвысокоэффективная жидкостная хроматография) или ГХ-МС (газовая хроматография-масс-спектрометрия) согласно протоколам, подробно описанным далее.
Протоколы оценки полученных экстрактов:
Протокол 1: оценка содержания силимарина посредством СВЭЖХ

- Стандарт силимарина: приготовить раствор силимарина, содержащий 5 мг в 10 мл смеси метанол/вода (60:40) (об./об.).
- Образец:
• Экстракт А: приготовить раствор, содержащий 100 мг экстракта, подлежащего анализу, в 10 мл смеси метанол/дихлорметан (70:30) (об./об.)
• Экстракты М, Е, I: нагревать сухой экстракт, подлежащий анализу, до 35°С при перемешивании, пока не получается прозрачный, гомогенный раствор. Аккуратно взвесить 200 мг (ре) (с допустимой погрешностью) экстракта, солюбилизировать его в 10 мл смеси метанол/дихлорметан, обеспечивая общую солюбилизацию экстракта, и гомогенизировать раствор. Данная смесь варьирует от отношения метанол/дихлорметан (1:1) (об./об.) до чистого метанола.

- Колонка: Acquity ВЕН Shield С18 150 мм × 2,1 мм - 1,7 мкм (Waters)
- Подвижная фаза:


- Градиент:

- Температура колонки: 40°С
- Скорость тока: 0,4 мл/мин
- Выявление: 287 нм
- Объем инъекции: 1 мкл
Протокол 2: оценка содержания линолевой кислоты посредством СВЭЖХ

- Стандарт линолевой кислоты: приготовить раствор линолевой кислоты, содержащий 10 мг в 10 мл смеси метанол/дихлорметан (1:1) (об./об.).
- Образец:
• Экстракты М, Е, I: Нагреть сухой экстракт, подлежащий анализу, до 35°С при перемешивании, пока не получается прозрачный, гомогенный раствор. Аккуратно взвесить 50 мг (ре) экстракта, солюбилизировать его в 1 мл смеси метанол/дихлорметан, обеспечивая общую солюбилизацию экстракта, и гомогенизировать раствор. Данная смесь варьирует от отношения метанол/дихлорметан (1:1) (об./об.) до чистого метанола.

- Колонка: Acquity ВЕН Shield С18 150 мм × 2,1 мм - 1,7 мкм (Waters)
- Подвижная фаза:


- Градиент:

- Температура колонки: 40°С
- Скорость тока: 0,4 мл/мин
- Выявление: 215 нм
- Инъекционный объем: 1 мкл
Протокол 3: оценка содержания жирных кислот и стерола посредством ГХ-МС

- Нагреть сухой экстракт, подлежащий анализу, до 35°С при перемешивании, пока не получается прозрачная, гомогенная жидкость
- Солюбилизировать 20 мг экстракта в 800 мкл смеси метанол/дихлорметан (1:1) (об./об.)
- Добавить 200 мкл дериватизирующего агента - N,O-бис(триметилсилил)трифторацетамид (BSTFA) плюс триметилхлорсилан (TMCS) (99:1) (Supelco - Sigma Aldrich)
- Перемешивать в течение 1 минуты с использованием вибромешалки.

- Колонка: DB-5ms (Agilent technologies); 30 м × 0,25 мм; 0,25 мкм
- Инъекция: Т равна 300°С; Режим - деление; отношение деления -100:1
- Печь: температурный градиент (°С):



- Скорость тока газа-носителя: 1 мл/мин
- Выявление: МС-ЭУ (масс-спектрометрия с ионизацией электронным ударом); Т - 300°С; время сканирования 0,2 с; исходная масса при полном сканировании - 40; конечная масса при полном сканировании - 600
- Инъекционный объем: 1 мкл.
Результаты:
Экстракт А семянок Silybum marianum согласно предшествующему уровню техники, богатый силимарином, по существу содержит компоненты силимарина, имеющие время удерживания от 6 до 14 минут при разделении СВЭЖХ (см. Фиг. 1В и 1А).
Экстракт I семянок Silybum marianum по изобретению, бедный силимарином, главным образом, содержит вещества, имеющие время удерживания от 13 до 30 минут при разделении СВЭЖХ (см. Фиг. 1Б).
Способ А, таким образом, благоприятствует экстракции полярных соединений и, в частности, флавонолигнанов силимарина, тогда как способ Б благоприятствует экстракции липофильных соединений, таких как свободные жирные кислоты, стеролы, токоферолы и другие неполярные соединения.
Содержание силимарина экстрактов А и I определяли посредством СВЭЖХ после калибровки с использованием растворов имеющегося в продаже стандарта силимарина (Sigma Aldrich) (см. Фиг. 1).
Экстракт А содержит 28% по массе силимарина.
Экстракт I содержит 0,06% по массе силимарина.
Содержание свободных жирных кислот (и, более конкретно, линолевой кислоты) и стерола (и, более конкретно, β-ситостерола) в экстракте I определяли посредством СВЭЖХ (см. Фиг. 3Б) и посредством ГХ (см. Фиг. 4В, 5В и 6В):

Авторы изобретения смогли определить то, что результаты СВЭЖХ (см. Фиг. 2) и ГХ (см. Фиг. 4, 5 и 6) 3 экстрактов семянок по изобретению, полученных метанольной экстракцией (экстракт М), экстракцией этанолом 90 (экстракт Е) и экстракцией изопропанолом 90 (экстракт I), являются аналогичными.
Заключение:
Разные анализы, проведенные СВЭЖХ и ГХ-МС, позволили продемонстрировать следующие характеристики.
• «Хроматограммы силимарина» (см. Фиг. 1): сравнение данных хроматограмм демонстрирует то, что:


• «Хроматограмма линолевой кислоты» (см. Фиг. 3): линолевой кислотой является пик в 7,742 мин. Отмечается то, что этанольный экстракт семянок согласно предшествующему уровню техники (экстракт А) практически лишен линолевой кислоты, в отличие от экстракта изопропанолом 90 по изобретению (экстракт I).
• Кроме того, авторы изобретения также смогли продемонстрировать то, что профили СВЭЖХ (см. Фиг. 2) и ГХ (см. Фиг. 4, 5 и 6) 3 экстрактов семянок по изобретению, полученных метанольной экстракцией, экстракцией этанолом 90 и экстракцией изопропанолом 90 (экстракты М, Е и I), являются очень сходными.
2. Композиции по изобретению
Экстракты, полученные в Примере 1, готовили с содержанием 7% (масс/об.) в смеси изопропанол/ПЭГ 300 (полиэтиленгликоль 300) (1:1) (масс/масс). Образующиеся композиции использовали в разных клинических исследованиях (см. Примеры 3-6 далее) посредством местного нанесения на кожу.
Экстракты по настоящему изобретению также могут быть приготовлены, например, в виде сыворотки согласно следующему препарату:

3. Сравнительное клиническое исследование в лечении угрей
Семь пациентов, страдающих от угрей, последовательно лечили композициями из Примера 2, содержащими экстракт семянок Silybum marianum по изобретению, бедный силимарином (экстракт I, М или Е), или экстракт семянок Silybum marianum согласно предшествующему уровню техники, богатый силимарином (экстракт А), согласно следующей схеме:
- фаза 1: 18-недельное лечение композицией, содержащей экстракт М семянок Silybum marianum по изобретению, бедный силимарином (5,64 плюс/минус 0,01 мкг/г), с последующей
- фазой 2: 12-недельное лечение композицией, содержащей экстракт А семянок Silybum marianum согласно предшествующему уровню техники, богатый силимарином (23,21 плюс/минус 2,03 мкг/г), с последующей
- фазой 3: 18-недельное лечение композицией, содержащей экстракт Е семянок Silybum marianum по изобретению, бедный силимарином, с последующей
- фазой 4: 6-недельное лечение композицией, содержащей экстракт А семянок Silybum marianum согласно предшествующему уровню техники, богатый силимарином, с последующей
- фазой 5: 6-недельное лечение композицией, содержащей экстракт I семянок Silybum marianum по изобретению, бедный силимарином.
Анализ полученных терапевтических эффектов проводили согласно способу IGA (общая оценка исследователем) анализа общего клинического состояния, принятому FDA (Управление по контролю качества пищевых продуктов и лекарственных средств США), и он применялся экспертом по клинической дерматологии (Guidance for Industry Acne Vulgaris: Developing Drugs for Treatment).
При применении такого способа наблюдаются следующие степени IGA, приписываемые согласно тяжести угрей:

Средние результаты, полученные для семи пациентов, показаны на Фиг. 7.
На данной Фиг. показано то, что во время первой фазы лечения экстрактом семянок Silybum marianum по изобретению, бедным силимарином, наблюдается заметное улучшение клинического состояния угрей, соответствующее «успеху» согласно критериям FDA, с заметной стабильностью эффекта в свете исключительной продолжительности (18 недель) лечения.
При переходе ко второй фазе лечения экстрактом семянок Silybum marianum согласно предшествующему уровню техники, богатым силимарином, наблюдается потеря эффективности с возвращением поражений, соответствующая «неуспеху» согласно критериям FDA.
Такие же наблюдения делали на протяжении последующих фаз 3, 4 и 5.
Данные клинические наблюдения ясно показывают то, что наблюдаемый клинический терапевтический эффект не ассоциирован с силимарином, так как композиции, содержащие чрезвычайно малые концентрации силимарина, оказывают заметный клинический терапевтический эффект, тогда как композиции, содержащие высокие концентрации силимарина, имеют тенденцию к ухудшению клинического состояния, вызывая рецидив.
Таким образом, лечение экстрактом семянок Silybum marianum согласно предшествующему уровню техники, богатым силимарином, вызывает ухудшение клинического состояния, тогда как лечение экстрактом семянок Silybum marianum по изобретению, бедным силимарином, обеспечивает заметное улучшение.
Следовательно, наблюдаемые клинические результаты демонстрируют то, что эффективность лучше с экстрактами по изобретению, содержащими пренебрежимо малое количество силимарина, по сравнению с экстрактами согласно предшествующему уровню техники, богатыми силимарином, которые приводят к возвращению угрей.
4. Клиническое исследование по лечению угрей взрослых
Одиннадцать пациентов, страдающих от угрей взрослых, лечили в течение 18 недель композицией из Примера 2, содержащей экстракт семянок Silybum marianum по изобретению, бедный силимарином.
Анализ полученных терапевтических эффектов проводили так же, как и в Примере 3, согласно способу IGA (общая оценка исследователем) анализа общего клинического состояния, принятому FDA (Управление по контролю качества пищевых продуктов и лекарственных средств США), и он применялся экспертом по клинической дерматологии (Guidance for Industry Acne Vulgaris: Developing Drugs for Treatment).
Полученные результаты показаны на Фиг. 8 и в таблице, приведенной ниже:

Данные результаты демонстрируют заметное улучшение клинического состояния угрей взрослых с уменьшением на две степени в 7 из 11 случаев, соответствуя «успеху» согласно критериям FDA, а также заметную стабильность эффекта в свете исключительной продолжительности (18 недель) лечения.
Данные клинические наблюдения демонстрируют несомненный клинический терапевтический эффект экстракта по изобретению на угри взрослых.
5. Клиническое исследование при лечении угрей подростков
Десять пациентов-подростков (15-18-летних), страдающих от угрей подростков, лечили в течение 18 недель композицией из Примера 2, содержащей экстракт семянок Silybum marianum по изобретению, бедный силимарином.
Анализ полученных терапевтических эффектов проводили так же, как и в Примере 3, согласно способу IGA (общая оценка исследователем) анализа общего клинического состояния, принятому FDA (Управление по контролю качества пищевых продуктов и лекарственных средств США), и он применялся экспертом по клинической дерматологии (Guidance for Industry Acne Vulgaris: Developing Drugs for Treatment).
Полученные результаты показаны на Фиг. 9 и в таблице, приведенной ниже:


Данные результаты демонстрируют заметное улучшение клинического состояния угрей подростков с уменьшением на две степени в 8 из 10 случаев, соответствуя «успеху» согласно критериям FDA, а также заметную стабильность эффекта в свете исключительной продолжительности (18 недель) лечения.
Данные клинические наблюдения демонстрируют несомненное клиническое терапевтическое влияние экстракта по изобретению на угри подростков.
6. Клиническое исследование при лечении розовых угрей, возможно с себореей
Девять пациентов, страдающих от розовых угрей, возможно с себореей, лечили в течение 18 недель композицией из Примера 2, содержащей экстракт семянок Silybum marianum по изобретению, бедный силимарином.
Анализ полученных терапевтических эффектов проводили так же, как и в Примере 3, согласно способу IGA (общая оценка исследователем) анализа общего клинического состояния, принятому FDA (Управление по контролю качества пищевых продуктов и лекарственных средств США) для угрей и адаптированному для розовых угрей экспертом по клинической дерматологии (Guidance for Industry Acne Vulgaris: Developing Drugs for Treatment).
Полученные результаты показаны на Фиг. 10 и в таблице, приведенной ниже:


Данные результаты демонстрируют заметное улучшение клинического состояния розовых угрей для всех пациентов, а также заметную стабильность эффекта в свете исключительной продолжительности (18 недель) лечения. Это общее улучшение соответствует заметному влиянию на разные клинические параметры данного состояния (Wilkin et al. 2004): сосудистый, воспалительный, папулопустулярный компонент и, кроме того, на себорейные компоненты, воплощающие в данных случаях себорейный дерматит (SD) типа «смешанного дерматита лица». Данный себорейный дерматит ассоциирован с поражениями розовыми угрями в типичных для данного состояния местах, т.е. на выпуклостях лица, и с поражениями себорейным дерматитом в областях складок, как описано В. Cribier в

Данные клинические наблюдения демонстрируют несомненный клинический терапевтический эффект экстракта по изобретению на розовые угри, возможно с себореей.
7. Сравнительное исследование in vitro
В данном исследовании изопропанольные экстракты семянок Silybum marianum в концентрации 0,03% (масс/об.) в культуральной среде тестировали in vitro на культуре первичных человеческих себоцитов (Zenbio, Inc. Research Triangle Park, NC) в течение 3 последовательных суток (с заменой среды каждые сутки), т.е. экстракт семянок Silybum marianum по изобретению и экстракт А семянок Silybum marianum согласно предшествующему уровню техники. Клетки отбирали, и РНК выделяли через 24 ч после последней обработки.
Анализ ПЦР (полимеразная цепная реакция) сделал возможным измерение уровня экспрессии двух генов себогенных ферментов - FADS2 и SCD1. Эти два фермента участвуют в синтезе специфических липидов секрета сальных желез, и известно то, что их ингибирование индуцирует уменьшение активности сальных желез. Средние результаты ингибирования (кратность изменения) этих двух генов по отношению к растворителю (изопропанол, концентрация которого в культуральной среде составляет 1%), полученные по меньшей мере из 5 экспериментов, показаны на Фиг. 11, причем 2-кратное ингибирование рассматривается как значимое.
Данные результаты, таким образом, демонстрируют то, что экстракт семянок Silybum marianum по изобретению, бедный силимарином, значимо ингибирует экспрессию этих двух генов, в отличие от экстракта семянок Silybum marianum согласно предшествующему уровню техники, богатого силимарином.
Библиографические ссылки
Berardesca et al. "Combined effects of silymarin and methylsulfonylmethane in the management of rosacea: clinical and instrumental evaluation" Journal of Cosmetic Dermatology 2008, 7, 8-14 Cribier B. Dermatoses faciales, страница 861 в Dermatologie et IST, 5th edition Elsevier Masson 2009
"Guidance for Industry Acne Vulgaris: Developing Drugs for Treatment" Draft guidance, U.S. Department of Health and Human Services Food and Drug Administration Center for Drug Evaluation and Research (CDER), September 2005.
Hermenean et al. "Antioxidant and hepatoprotective activity of milk thistle (Silybum marianum L. Gaertn.) seed oil" Open Life Sci. 2015, 10(1), 225-236.
Kuki et al. "Identification of Silymarin Consituents: An Improved HPLC-MS Method" Chromatographia 2012, 75:175-180.
Sahib et al. "Effects of Oral Antioxidants on Lesion Counts Associated with Oxidative Stress and Inflammation in Patients with Papulopustular Acne" J. Clin. Exp. Dermatol. Res. 2012, 3:5.
Wilkin et al. "Standard grading system for rosacea: Report of the National Rosacea Society Expert Committee on the Classification and Staging of Rosacea" J. Am. Acad. Dermatol. 2004, 50:907-12.
Zheng et al. "Application of response surface methodology to optimize microwave-assisted extraction of silymarin from milk thistle seeds" Sep. Purif. Technol. 2009, 70:34-40.
Zhu et al. "Silybum marianum oil attenuates oxidative stress and ameliorates mitochondrial dysfunction in mice treated with D-galactose" Pharmacogn Mag. 2014, 10 (Suppl. 1), S92-S99.
Реферат
Группа изобретений относится к дерматологической и косметической отраслям промышленности, а именно к экстракту для лечения угрей, себореи, розовых угрей и/или себорейного дерматита. Предлагается экстракт семянок Silybum marianum (L.) Gaertn. для лечения угрей, себореи, розовых угрей и/или себорейного дерматита, содержащий меньше чем 0,2% по массе силимарина по отношению к массе сухого экстракта и полученный способом, включающим следующие последовательные стадии: (i) прессование семянок Silybum marianum (L.) Gaertn. с получением масла; (ii) экстрагирование масла, полученного из семянок Silybum marianum (L.) Gaertn. на стадии (i), экстрагирующим растворителем, выбранным из субкритической воды и С1-С3спирта, необязательно в смеси с водой, с получением экстракционной фазы и липидной фазы; (iii) извлечение экстракционной фазы, полученной на стадии (ii), и (iv) частичная или полная сушка экстракционной фазы с получением концентрированного или сухого экстракта. Фармацевтическая композиция для лечения угрей, себореи, розовых угрей и/или себорейного дерматита содержит экстракт в смеси с по меньшей мере одним фармацевтически приемлемым эксципиентом. Вышеописанный экстракт и композиция на его основе обладают повышенной эффективностью в лечении угрей, себореи, розовых угрей и/или себорейного дерматита. 2 н. и 10 з.п. ф-лы, 11 ил., 3 табл., 3 пр.

Комментарии