Ингибитор гепараназной активности - RU2503454C1
Код документа: RU2503454C1
Чертежи







Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к наружному препарату для кожи, содержащему в качестве активного ингредиента циклическое карбоксамидное производное формулы (I), и, в частности, к ингибитору гепараназы, который, когда используется как косметическое средство, ингибирует активность гепараназы в коже, ингибирует изменение кожи, происходящее в силу недостаточности регуляции факторов роста, путем сохранения гепарансульфата и создает условия сохранения кожи молодой, причем в то же время также обнаруживает отбеливающее действие.
Уровень техники
В последние годы продолжают продвигаться исследования по противодействию старению. Соматическое старение является основной причиной старения кожи с макроскопической точки зрения, но другие причины, такие как окисление, сухость и солнечный свет (ультрафиолетовое излучение) также являются непосредственными факторами, связанными со старением кожи. Известно, что специфическое явление старения кожи ассоциируется с повреждением клеток из-за снижения количества мукополисахаридов, включая гиалуроновую кислоту, реакцией сшивания коллагена и ультрафиолетовым излучением.
Значительная часть исследований также проводится с целью ингибирования или улучшения в отношении, например, кожных морщин, мелких морщин и обвисания, вызванных повреждением кожи или старением кожи из-за воздействия ультрафиолетового излучения. В результате показана эффективность промотирования выработки гиалуроновой кислоты (JP 2001-163794A - патентный документ 1), подавления выработки и активации металлопротеиназ матрикса (ММР) (JP 2000-503660X - патентный документ 2), промотирования выработки коллагена и ингибирования эстеразной активности (JP-Н11-335235В - патентный документ 3), подавления ангиогенеза (WO 03/084302A -патентный документ 4) и подавления лимфангиэктазии (K. Kajiya et al., Am. J. Pathol., 2006, 169(4): 1496-1503 - непатентный документ 1).
Такие исследования в основном разделяются на усилия по предотвращению и улучшению в отношении мелких морщин сосредоточением на эпидермисе или эпидермальных клетках, и усилия по предотвращению и улучшению в отношении крупных морщин сосредоточением на подавлении изменений в дерме, в том числе, изменений кровеносных сосудов или лимфатических сосудов. Распространение изменений в эпидермисе до дермы ведет к изменению дермы, в том числе, кровеносных сосудов и лимфатических сосудов, и гепараназа неоднозначно вовлечена в этот процесс. Действительно, было показано, что существенное действие против морщин можно достичь путем нанесения на модель мелких морщин ингибитора гепараназы (PCT/JP 2009/-56717).
Документы известного уровня техники
Патентные документы
Патентный документ 1: JP 2001-163794A
Патентный документ 2: JP 2000-503660X
Патентный документ 3: JP-H11-335235 В
Патентный документ 4: WO 03/084302A
Патентный документ 5: DE 2746550A
Патентный документ 6: JP 29011297 В
Патентный документ 7: JP 2008-303186A
Патентный документ 8: JP 2004-526758X
Непатентные документы
Непатентный документ 1: K. Kajiya et al., Am. J. Pathol., 2006, 169(4): 1496-1503
Непатентный документ 2: I. Viodavsky et al., Semin. Cancer Biol., 2002, 12(2): 121-129
Раскрытие изобретения
Проблемы, решаемые изобретением
Целью изобретения является поиск нового лекарственного средства, которое эффективно для предотвращения и подавления старения кожи с точки зрения связи между гепараназой и старением кожи, а также средства для отбеливания кожи, которое эффективно для предотвращения и подавления пигментации, в том числе, пятен на коже, веснушек и утраты чистоты кожи.
Способы решения проблем
В результате кропотливого исследования авторы настоящего изобретения обнаружили, что некоторое циклические карбоксамидные производные ингибируют гепараназную активность и в результате эффективно предотвращают или подавляют старение или пигментацию.
Таким образом, настоящая заявка представляет изобретение, описанное ниже.
(1) Ингибитор гепараназной активности, включающий в качестве активного ингредиента циклическое карбоксамидное производное, представленное формулой (I)

в которой
n равен целому числу от 1 до 3,
R1 представляет собой водород или углеводородную группу С 1-6, необязательно замещенную гидроксилом,
Х представляет собой -CH2- или группу, представленную -N(R2)-, где R2представляет собой водород или углеводородную группу С1-6, необязательно замещенную гидроксилом,
или его соль.
(2) Ингибитор гепараназной активности по (1), в котором в формуле (1) n=1.
(3) Ингибитор гепараназной активности по (1), при этом циклическое карбоксамидное производное представляет собой одно или несколько соединений, выбранных из группы, состоящей из 2-имидазолидинона, 1-(2-гидроксиэтил)-2-имидазолидинона и 1-(2-гидроксиэтил)-2-пирролидона.
(4) Средство против морщин, включающее в качестве активного ингредиента ингибитор гепараназной активности по любому из (1)-(3).
(5) Средство против крупных морщин, включающее в качестве активного ингредиента ингибитор гепараназной активности по любому из (1)-(3).
(6) Средство для отбеливания кожи, включающее в качестве активного ингредиента ингибитор гепараназной активности по любому из (1)-(3).
Действие изобретения
Так как ингибитор гепараназной активности по изобретению может эффективно ингибировать гепараназную активность, его можно использовать в качестве активного ингредиента в средстве против морщин, например, для предупреждения или подавления образования морщин (особенно, крупных морщин) и также соответственно использовать в качестве средства для отбеливания кожи, которое эффективно для предупреждения или подавления пигментации, в том числе, пятен на коже, веснушек и утраты чистоты кожи.
Краткое описание чертежей
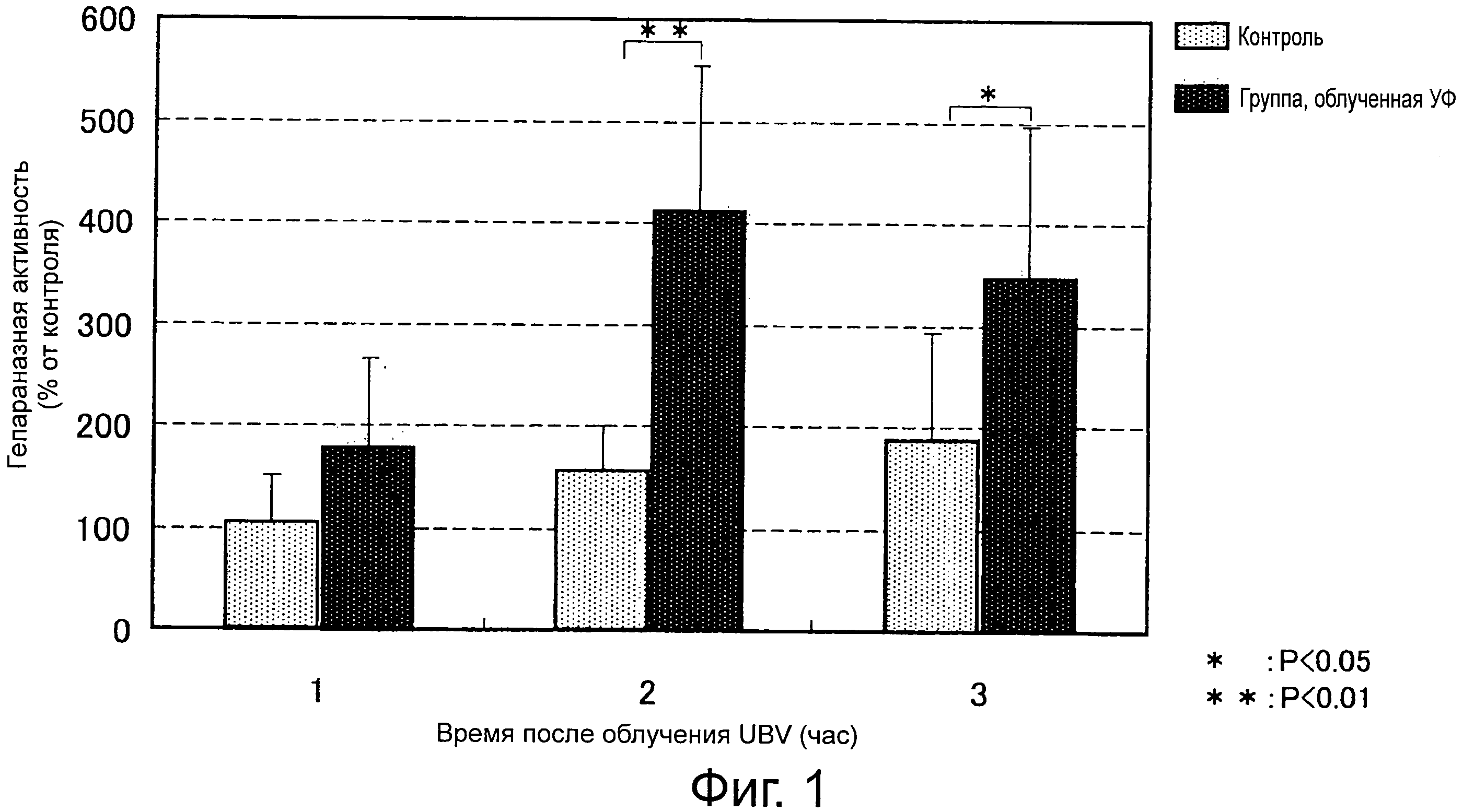
Фиг.1 представляет собой диаграмму, показывающую различие в гепараназной активности в зрелых кератиноцитах человека в условиях воздействия ультрафиолетового излучения и его отсутствия.
Фиг.2 представляет собой ряд иммуноокрашенных изображений для гепараназы и гепарансульфата в облученных и необлученных ультрафиолетовым излучением участках нормальной ткани ягодиц человека.
Фиг.3а и 3b представляют собой схематические диаграммы моделей псевдокожи, где (а) показывает «модель с разложившимся гепарансульфатом», которая не содержит гепарансульфат на базальном мембранном слое (гепарансульфат (-)), в то время как (b) показывает «нормальную модель», которая содержит гепарансульфат на базальном мембранном слое (гепарансульфат (+)).
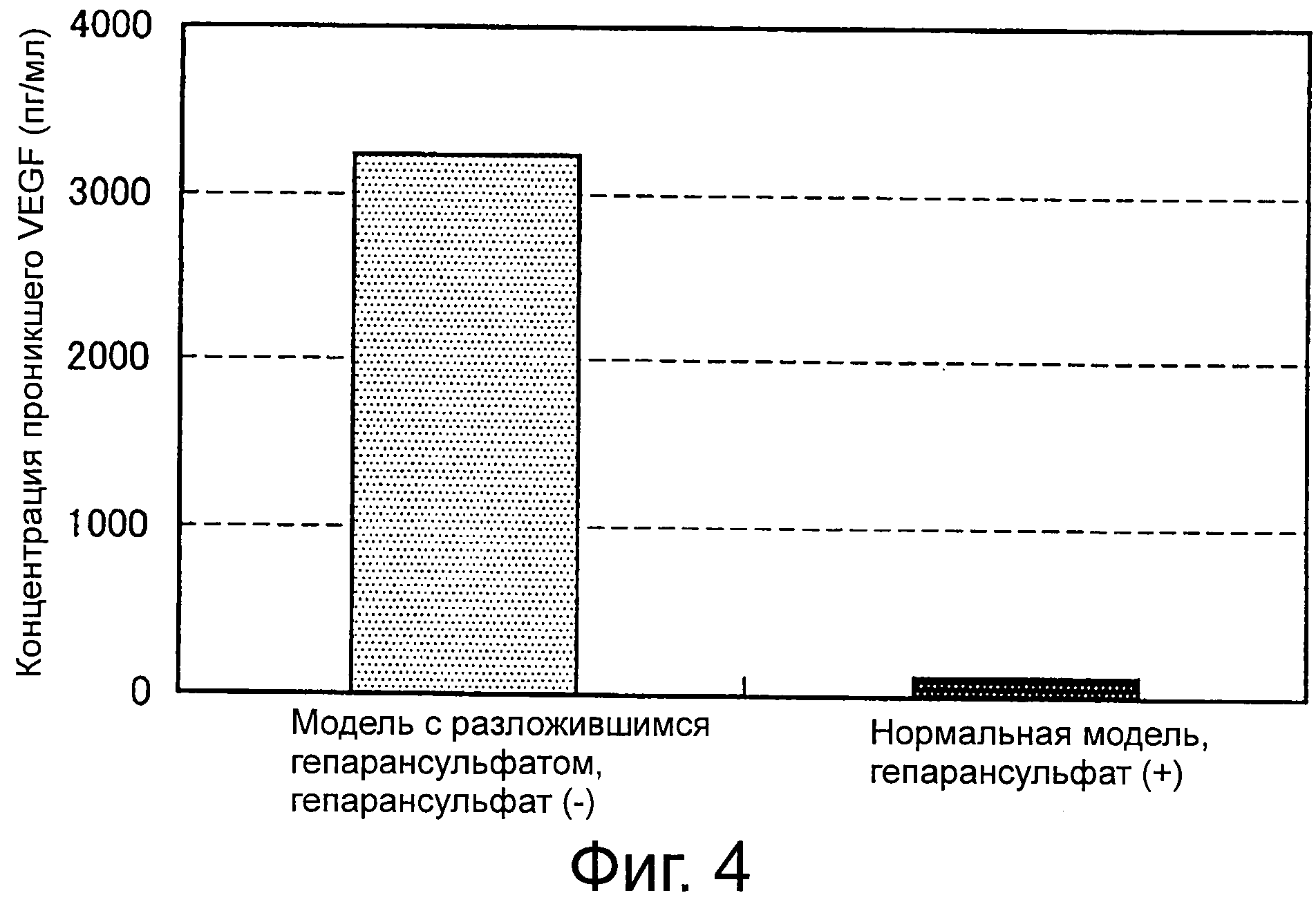
Фиг.4 представляет собой диаграмму, показывающую результаты оценки проникновения VEGF с использованием моделей псевдокожи на фиг.3а и 3b.
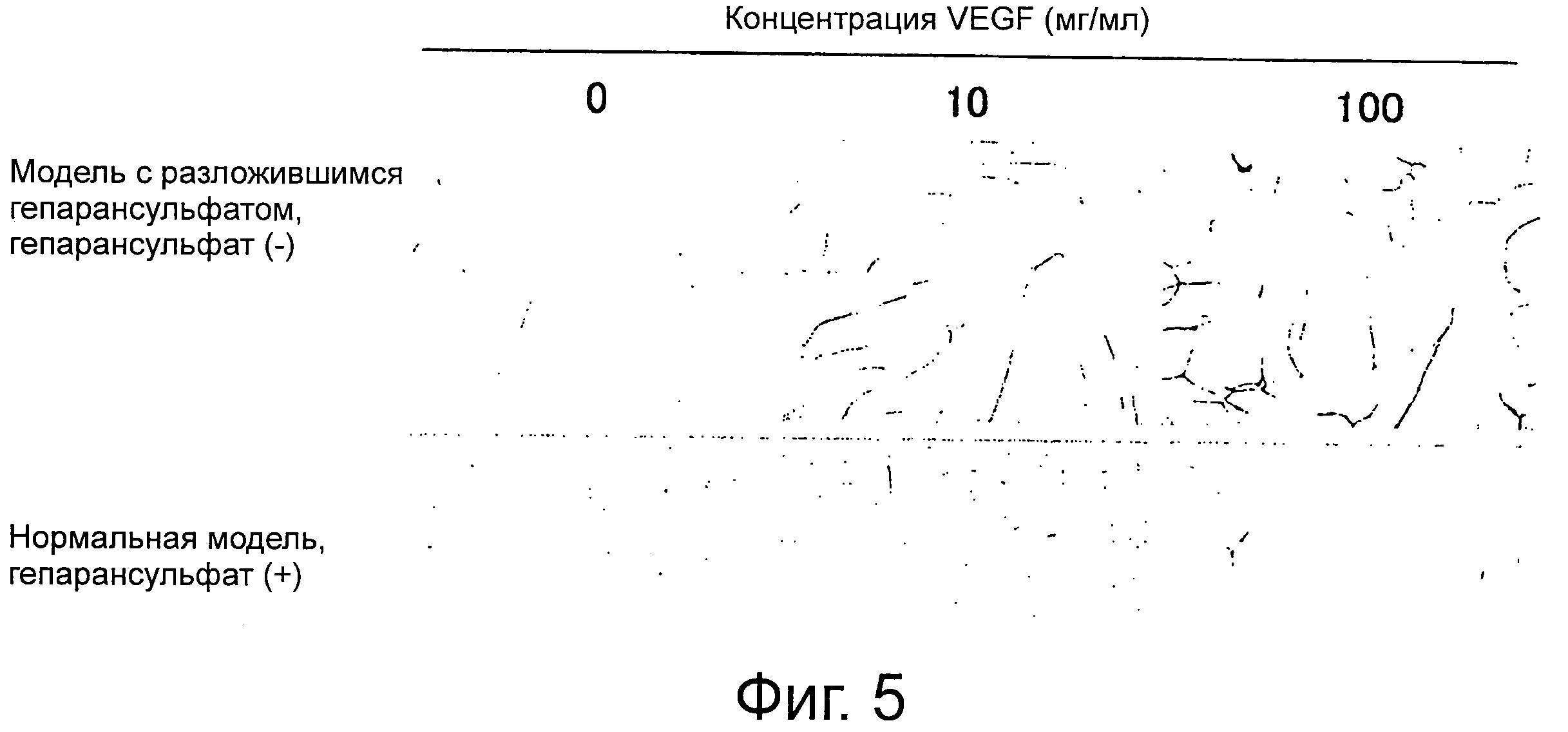
Фиг.5 представляет собой ряд фотографий, показывающих результаты оценки ангиогенеза с использованием моделей псевдокожи на фиг.3а и 3b.
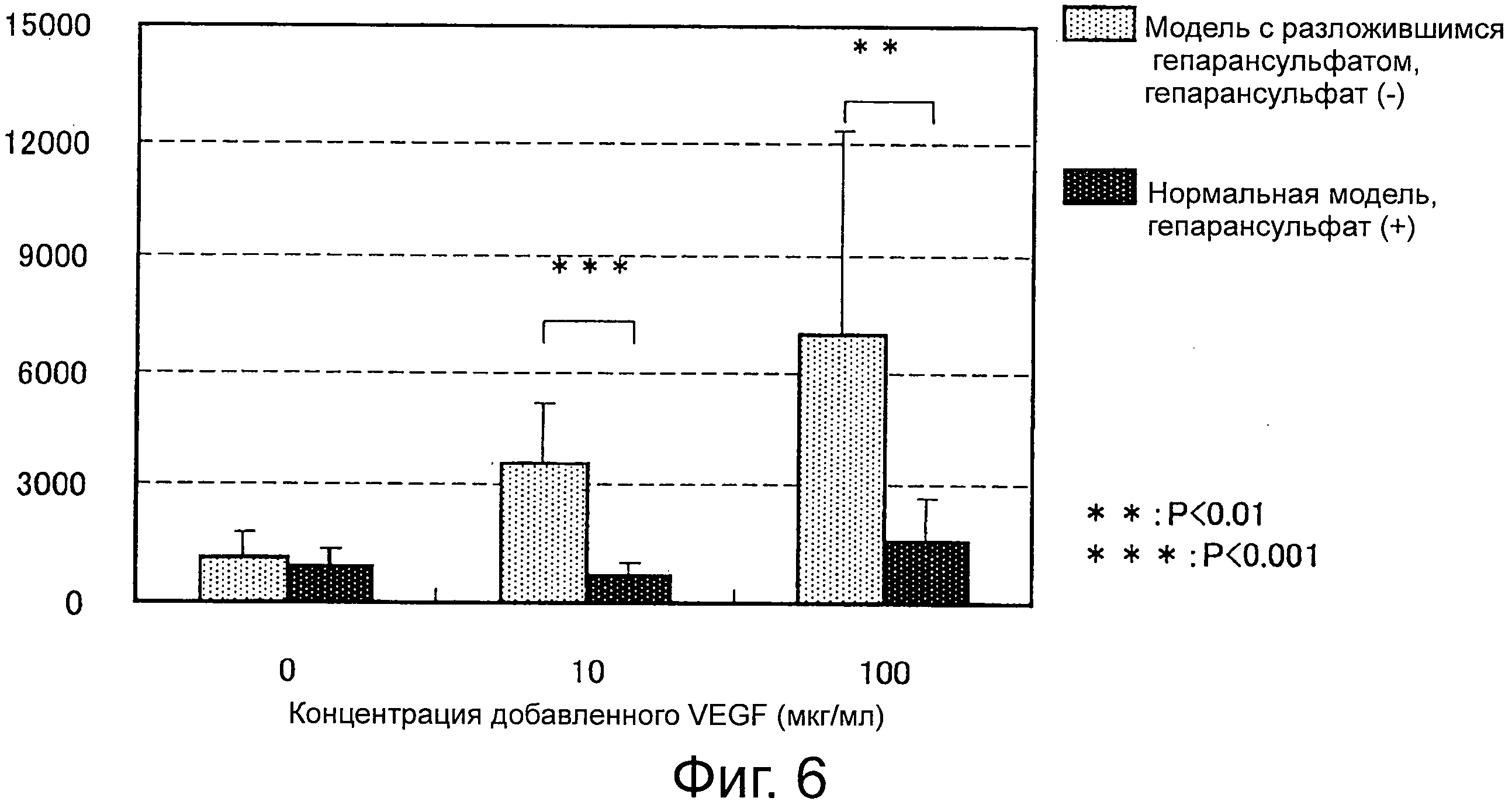
Фиг.6 представляет собой диаграмму, показывающую результаты анализа площади кровеносных сосудов на фотографии на фиг.5.
Фиг.7 представляет собой ряд фотографий внешнего вида моделей меланоцитсодержащей кожи (MEL-FT, получены MatTeK, США).
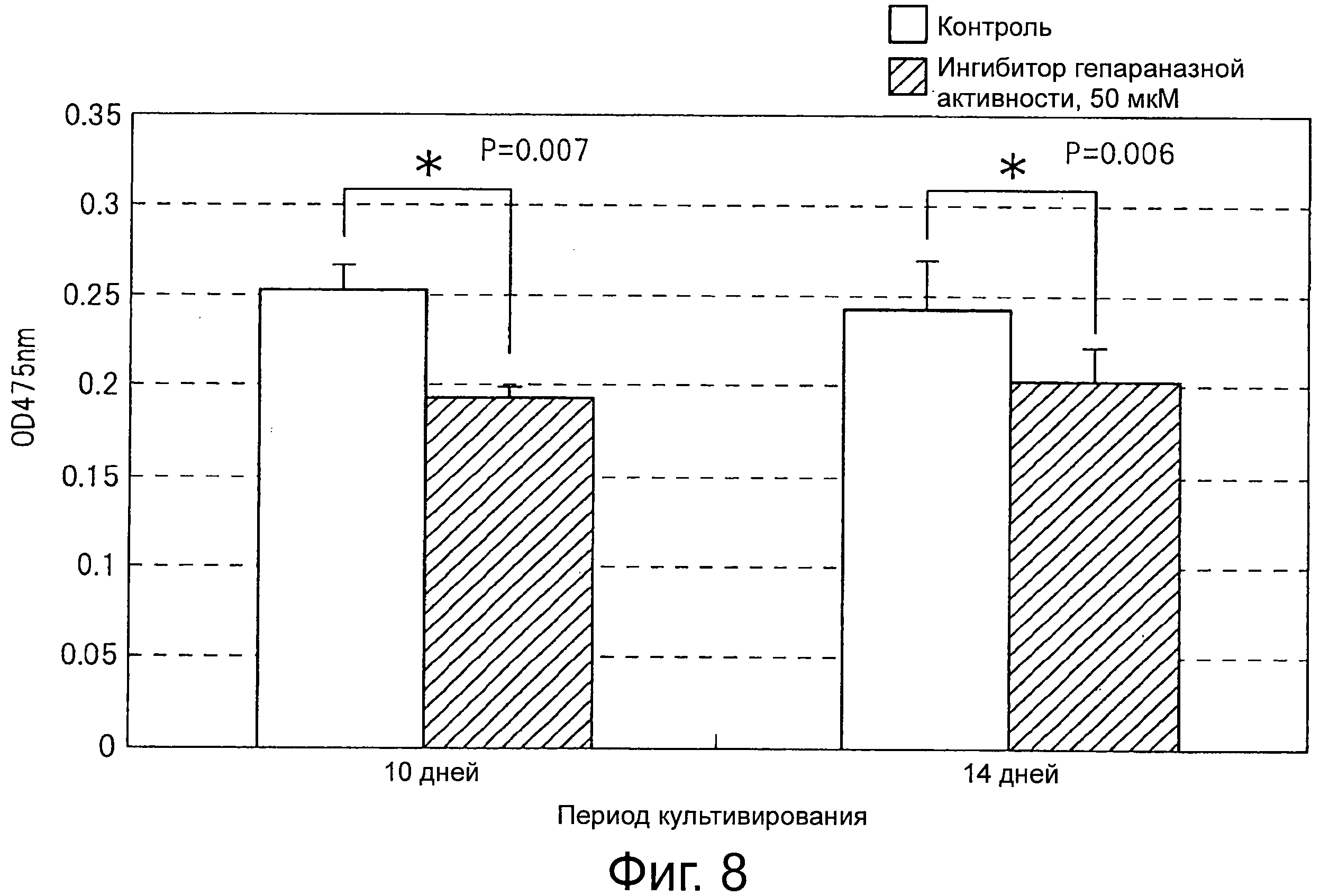
Фиг.8 представляет собой диаграмму, показывающую результаты сравнения содержания меланина в эпидермисе для различных моделей кожи.
Фиг.9 показывает результаты иммунного окрашивания для перлекана и гепарансульфата в старческих пигментных пятнах и в окружающей нормальной ткани.
Фиг.10 показывает результаты иммунного окрашивания с антителами против CD31 в качестве маркера кровеносных сосудов вместе с результатами анализа изображений.
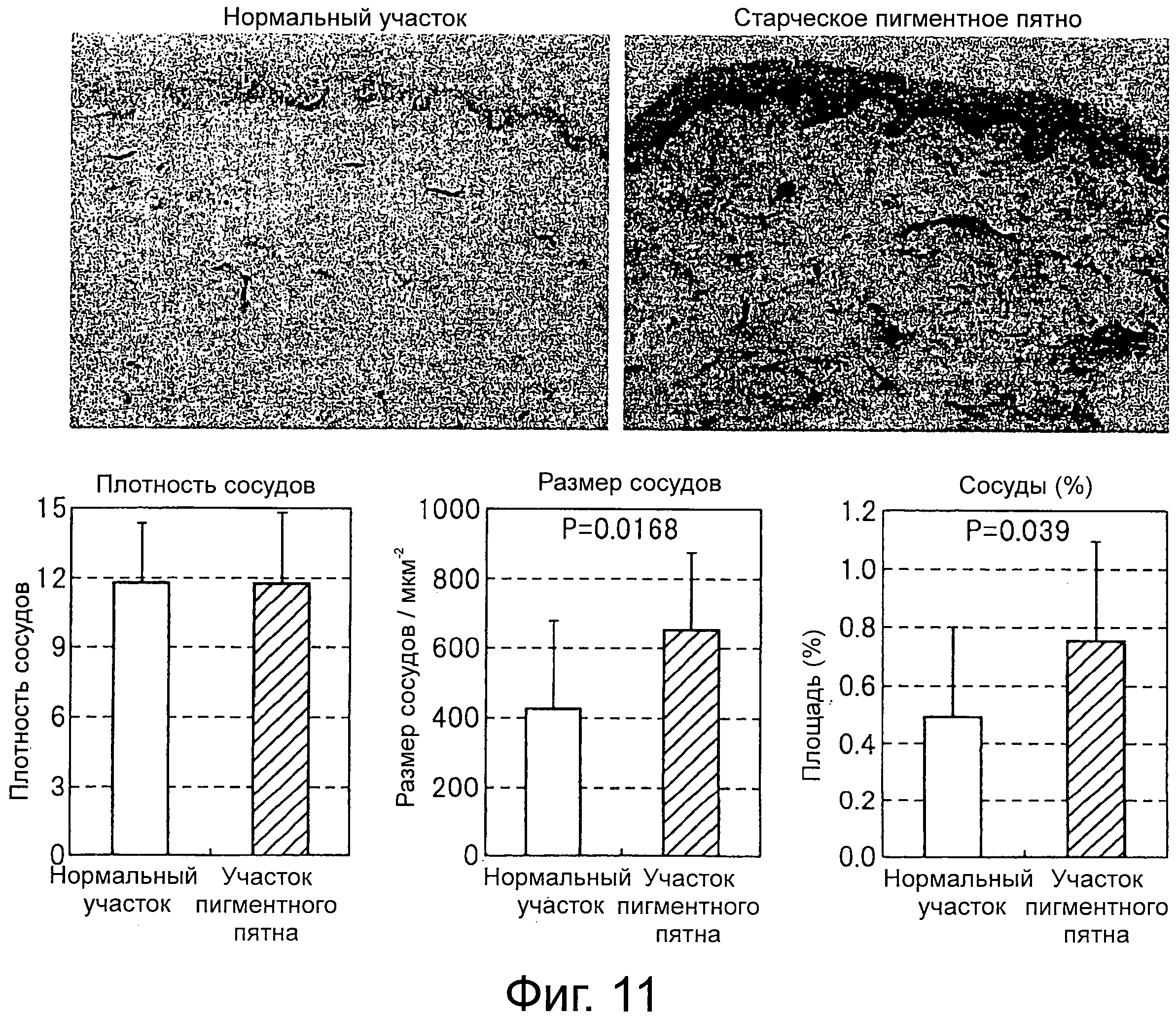
Фиг.11 показывает результаты иммунного окрашивания с антителами против LYVE-1 в качестве маркера лимфатических сосудов вместе с результатами анализа изображений.
Фиг.12 показывает результаты анализа связывания bFGF in situ со старческой пигментированной тканью, и
фиг.13 показывает результаты анализа связывания bFGF in situ с себорейной пигментированной тканью.
Осуществление изобретения
Гепараназа присутствует в различных клетках как фермент, который специфически разрушает цепи гепарансульфата в различных типах гепарансульфатпротеогликанов. В коже она вырабатывается эпидермальными кератиноцитами, составляющими эпидермис, и фибробластами, или сосудистыми эндотелиальными клетками дермы. Также известно, что ее выработка возрастает в различных типах раковых клеток, и также предполагается связь с раковой злокачественностью. Известно, что повышенная выработка гепараназы в раковых клетках повышает метастазирование и повышает индуцибельность ангиогенеза (см. I. Viodavsky et al., Semin. Cancer Biol., 2002, 12(2): 121-129 - непатентный документ 2).
Гепарансульфатпротеогликаны обладают способностью вызывать внеклеточное накопление гепарансульфатсвязывающих факторов роста (например, bFGF, HGF, VEGF и HB-EGF). Перлекан представляет собой тип гепарансульфатпротеогликана, который также присутствует в эпидермальной базальной мембране на границе между эпидермисом и дермой, и в коже, гепарансульфатсвязывающне факторы роста связываются с эпидермальной базальной мембраной, регулируя миграцию факторов роста между эпидермисом и дермой. Кроме того, перлекан в эпидермальной базальной мембране также регулирует факторы роста для эпидермальных базальных клеток, связывающихся с базальной мембраной, и как показано, необходим для соответствующего роста и дифференцировки эпидермиса.
Следовательно, разрушение гепарансульфатных цепей перликана путем активации или ускоренной экспрессии гепараназы нарушает высвобождение накопленных факторов роста и регуляцию факторов роста в эпидермисе и дерме, что ведет к недостаточной регуляции дифференцировки и роста эпидермиса и толщины дермиса и к промотированию образования морщин. Иными словами, подавление гепараназной активности подавляет высвобождение факторов роста, что сопровождается разложением гепарансульфата и способствует подавлению миграции факторов роста между эпидермисом и дермой.
В результате скрининга на показатель гепараназной активности было обнаружено, что некоторые циклические карбоксамидные производные существенно подавляют гепараназную активность. Некоторые соединения известны как циклические карбоксамидные производные, и, например, они известны для применения в качестве увлажняющих средств для кожи (DE 274655A - патентный документ 5), для применения в качестве соединений, промотирующих проникновение (JP 2901297 В - патентный документ 6), и для применения в качестве промоторов образования ороговевшей оболочки и созревания (JP 2008-303186 A - патентный документ 7). Однако на известном уровне техники совершенно неизвестно, что циклические карбоксамидные производные обнаруживают ингибирующее действие на гепараназную активность.
Как подробно поясняется в примерах, авторы настоящего изобретения показали, что облучение культивированных зрелых кератиноцитов ультрафиолетовыми лучами приводит к активации гепараназы зрелых кератиноцитов (см. фиг.1). Также показано, что облучение человеческой кожи ультрафиолетовыми лучами повышает количество гепараназы в эпидермисе и снижает количество гепарансульфата в базальной мембране (см. фиг.2). Посредством этого показано, что гепараназная активность имеет место не только на моделях тонких морщин, но также за счет ультрафиолетовых лучей.
Кроме того, так как гепарансульфат базальной мембраны разлагается при активации гепараназы, авторы настоящего изобретения получили, как модель псевдокожи, нормальную модель, содержащую гепарансульфат в базальной мембране, и модель с разложившимся гепарансульфатом, не содержащую гепарансульфат в базальной мембране, и оценили проникновение VEGF и ангиогенез. В результате было показано, что на модели с разложившимся гепарансульфатом проникновение VEGF возрастает и ангиогенез индуцируется (см. фиг.3-6).
Yano et al. ранее показали, что вызванная ультрафиолетовыми лучами индукция ангиогенеза в дерме и изменение дермы являются важными для образования крупных морщин (JP 2004-526758 X - патентный документ 8), и обнаружили, что гепараназа является ферментом, сложным образом связанным не только с мелкими морщинами, но также и с крупными морщинами. Иными словами, ингибирование гепараназной активности эффективно не только для предупреждения образования мелких морщин, но также и крупных морщин из-за длительного воздействия солнечного света. В данном случае термин «крупные морщины» используется для обозначения крупных глубоких морщин в направлении, перпендикулярном стороне мышцы, которые образуются в углах глаз и в носогубной складке не только в эпидермисе, но также и в дерме.
При первичной оценке с использованием гепараназной активности в качестве показателя, как подробно описано в следующих далее примерах, биотинилированный гепарансульфат иммобилизуют в 96 лунках, после чего дают возможность гепараназе действовать в присутствии лекарственного средства, и уменьшение количества биотинилированного гепарансульфата используют для оценки гепараназной активности, с помощью реакции с меченным пероксидазой авидином и окрашивания. Лекарственные средства, которые обнаруживают ингибирующее действие на гепараназную активность при первичной оценке, затем оценивают на воспроизводимость и зависимость от концентрации во вторичной системе оценки. Таким путем обнаружено, что циклические карбоксамидные производные ингибируют гепараназную активность.
Термин «против старения», используемый в данном описании, обозначает предупреждение и улучшение в отношении морщин, обвисания и отвердевания кожи путем подавления изменения кожи, вызванного гепарансульфатсвязывающими факторами роста из-за разложения гепарансульфата протеогликана в базальной мембране в результате старения или фотостарения, и, особенно, подавление эпидермальных анормальностей дифференцировки, ангиогенеза дермы, лимфангиэктазии и разрушения эластина для сохранения эластичной, молодой и здоровой кожи.
Кроме того, как подробно описано в примерах, авторы настоящего изобретения также определили, что в старческой пигментированной ткани степень разложения гепарансульфата базальной мембраны больше, чем в коже, подвергнутой воздействию света. Разложение гепарансульфата ведет к утрате регуляции сосудистого эпителиального фактора роста A (VEGF-A), экспрессируемого в эпидермисе, за счет чего происходят изменения в кровеносных сосудах дермы и лимфатических сосудах, вызывая воспаление и активацию меланоцитов, которая промотирует хранение меланина в меланосомах. Кроме того, недостаточная регуляция фактора роста фибробластов 7 (FGF-7), экспрессируемого в дерме, ведет к ускоренной доставке меланосом из меланоцитов в эпидермальные клетки. Иными словами, полагают, что разложение гепарансульфата, которое сопровождает активацию гепараназы, ведет к активации меланоцитов из-за воспаления и к ускоренной доставке меланосом из-за утраты регуляции FGF-7, что приводит к синергичному сосредоточению меланосом в кератиноцитах. Следовательно, ингибитор гепараназной активности применим не только для предотвращения и подавления появления морщин, но также в качестве средства для отбеливания кожи для предотвращения и подавления пигментации, в том числе, пятен на коже, утраты чистоты кожи и веснушек.
Используемый в данном описании термин «отбеливание» обозначает подавление потемнения кожи, вызываемого накоплением меланосом в кератиноцитах, сопровождающим разложение гепарансульфата в базальной мембране, причем посредством этого происходит улучшение, например, в отношении пятен на коже, веснушек и утраты чистоты кожи. Если не указано иное, термин «способ отбеливания» используется согласно изобретению в косметическом смысле, но он также может использоваться в медицинском смысле.
Ингибитор гепараназной активности по изобретению также может быть использован для лечения, улучшения или предупреждения других состояний или симптомов, связанных с гепараназной активностью. «Состояния или симптомы, связанные с гепараназной активностью» могут представлять собой пролиферацию раковых клеток или метастазирование или ангиогенез. Таким образом, лекарственную композицию, содержащую ингибитор гепараназной активности по изобретению, также можно использовать для подавления пролиферации раковых клеток или метастазирования или для подавления ангиогенеза.
Когда циклическое карбоксамидное производное формулы (I) по изобретению представляет собой известное вещество, его можно легко синтезировать известным способом или просто закупить как коммерческий продукт, или если оно представляет собой новое соединение, например, его можно легко синтезировать способом, известным специалистам в данной области техники.
Циклическое карбоксамидное производное по настоящему изобретению, представленное формулой (I), также можно превратить известным способом в неорганическую соль или органическую соль. Не имеется особых ограничений в отношении солей, используемых для изобретения, и их примеры включают неорганические соли, такие как гидрохлориды, соли серной кислоты, соли фосфорной кислоты, соли бромоводородной кислоты, натриевые соли, калиевые соли, магниевые соли, кальциевые соли и аммониевые соли. Органические соли включают соли уксусной кислоты, соли молочной кислоты, соли малеиновой кислоты, соли фумаровой кислоты, соли винной кислоты, соли лимонной кислоты, соли метансульфоновой кислоты, соли п-толуолсульфоновой кислоты, соли триэтаноламина, соли диэтаноламина и соли аминокислот.
Ингибитор гепараназной активности по настоящему изобретению может содержать один тип циклического карбоксамидного производного формулы (I) или одну его соль, но он также может содержать два или больше циклических карбоксамидных производных формулы (I) или их солей, в любой желательной комбинации и соотношении.
Содержание циклического карбоксамидного производного формулы (I) или его соли в ингибиторе гепараназной активности по настоящему изобретению особо не ограничивается до тех пор, пока оно представляет собой количество, достаточное для эффективного проявления ингибирования гепараназной активности, и его можно соответствующим образом выбрать согласно поставленной цели ингибитора гепараназной активности. Однако, как правило, доля циклического карбоксамидного производного формулы (I) или его соли относительно всего ингибитора гепараназной активности предпочтительно обычно составляет по меньшей мере 0,0001 мас.%, и в особенности по меньшей мере 0,0001 мас.%, и, как правило, не превышает 1 мас.%, и, в особенности, не превышает 0,2 мас.%. Когда используют два или больше циклических карбоксамидных производных формулы (I) или их солей, общее количество должно удовлетворять интервалу, указанному выше.
Также ингибитор гепараназной активности по изобретению может дополнительно, кроме циклического карбоксамидного производного формулы (I) или его соли, содержать любые другие желательные компоненты до тех пор, пока ингибирующее действие на гепараназную активность циклического карбоксамидного производного формулы (I) или его соли существенно не ухудшается. Другие компоненты включают другие соединения с ингибирующим действием на гепараназную активность (другие активные компоненты) или медицински приемлемые носители и/или адъюванты. Такие другие компоненты могут использоваться по одному или два или больше в любой желательной комбинации и соотношении.
Ингибитор гепараназной активности по настоящему изобретению можно получить обычным способом, и как компонент для наружного препарата для кожи, одно или несколько циклических карбоксамидных производных формулы (I) или их солей даже можно получить отдельно, но при необходимости соответственно могут добавляться компоненты, обычно используемые в наружных препаратах для кожи, таких как содержащие квазилекарственные средства косметические препараты или фармацевтические препараты, в том числе, масла, поверхностно-активные вещества, порошки, красители, вода, спирты, загустители, хелатирующие агенты, силиконы, антиоксиданты, поглотители ультрафиолетового излучения, увлажняющие вещества, ароматические вещества, различные лекарственные компоненты, антисептические средства, регуляторы рН, нейтрализаторы.
Способ введения и лекарственная форма ингибитора гепараназной активности по изобретению не ограничиваются и могут быть выбраны в соответствии с поставленной целью. Примеры способов введения включают местное введение (например, нанесение на кожу), пероральное введение, парентеральное введение (например, внутривенное введение и интраперитонеальное введение) и т.п.., но для применения как средства против старения предпочтительно получают наружный препарат для кожи. Лекарственная форма для местного введения (материал для нанесения на кожу) может представлять собой форму, когда систему раствора, солюбилизированную систему, эмульгированную систему, систему диспергируемого порошка, двухслойную систему вода/масло, трехслойную систему вода/масло/порошок или подобную систему получают в виде пластыря, мази, крема, латекса, туалетной воды, геля или аэрозоля. Для перорального введения она может быть представлена в форме твердого препарата, такого как таблетка, таблетка с покрытием, таблетка с покрытием из сахара, гранулы, порошок, капсула (например, твердая или мягкая желатиновая капсула), или жидкого препарата (раствора или суспензии), такого как внутреннее жидкое лекарственное средство или сироп. Для парентерального введения такая форма может представлять собой инъекцию или подобную форму.
Ингибитор гепараназной активности по настоящему изобретению также может содержать, кроме циклического карбоксамидного производного формулы (I) или его соли, один или несколько других желательных компонентов до тех пор, пока ингибирующее действие на гепараназную активность циклического карбоксамидного производного формулы (I) или его соли существенно не ухудшается. Не существует особых ограничений для таких других компонентов, и их можно соответственно выбрать согласно цели, лекарственной форме и способу введения лекарственной композиции, но в качестве примеров можно упомянуть медицински приемлемые носители и/или адъюванты. Примеры адъювантов включают разбавители, связующие вещества, разрыхлители, загустители, диспергирующие вещества, ускорители повторного поглощения, корригент вкуса, буферирующие вещества, поверхностно-активные вещества, вспомогательные растворители, консерванты, эмульгаторы, вещества, способствующие изотоничности, стабилизаторы и регуляторы рН.
В качестве примера, когда ингибитор гепараназной активности по изобретению должен использоваться как наружный препарат для кожи, при необходимости соответственно могут быть добавлены компоненты, обычно используемые в наружных препаратах, такие как отбеливающие средства для кожи, увлажняющие вещества, антиоксиданты, масляные компоненты, поглотители ультрафиолетового излучения, поверхностно-активные вещества, загустители, спирты, порошковые компоненты, красители, водные компоненты, вода или различные питательные препараты для кожи. Кроме того, также могут быть добавлены соответствующие количества хелатообразователей с ионами металлов, таких как динатрийэдетат, тринатрийэдетат, цитрат натрия, полифосфат натрия, метафосфат натрия, или глюконовая кислота, антисептические средства, такие как метилпарабен, этилпарабен или бутилпарабен, кофеин, таннин, верапамил, транэксамовая кислота и ее производные, экстракт из корня солодки, лекарственные средства, такие как глабридин, горячий водный экстракт плодов хеномелес китайской, галеновые препараты, ацетат токоферола, глицирризиновая кислота и ее производные или соли, отбеливающие средства для кожи, такие как витамин С, аскорбатфосфат магния, глюкозидаскорбат, арбутин или койевая кислота, сахариды, такие как глюкоза, фруктоза, манноза, сахароза или трегалоза, производные витамина А, такие как ретиноевая кислота, ретинол, ацетат ретинола или пальмитат ретинола.
Однако такие компоненты не ограничиваются указанными выше. Такие компоненты также могут использоваться в соответствующих смесях согласно прописям для предписанных лекарственных форм.
Лекарственная форма наружного препарата для кожи по настоящему изобретению особо не ограничивается и, например, может представлять собой любую желательную форму, такую как раствор, солюбилизированная система, эмульсия, диспергируемый порошок, двухслойная система вода-масло, трехслойная система вода-масло-порошок, мазь, гель, аэрозоль или подобную форму. Форма для использования также особо не ограничивается, и может быть использована любая желательная форма, такая как туалетная вода, эмульсия, крем, эссенция, желе, гель, мазь, косметическая маска, тональный крем или подобная форма.
Ингибитор гепараназы по настоящему изобретению можно наносить на кожу для использования косметическим способом для предупреждения образования крупных морщин и/или для уменьшения и устранения образовавшихся морщин. Способ и дозировка наружного препарата для кожи по изобретению, используемые в способе для украшения, особо не ограничиваются и соответственно могут быть установлены в зависимости от лекарственной формы или состояния кожных морщин, которые обрабатывают, но обычно подходящую дозу, например, от 0,1 мл до 1 мл на см3, втирают непосредственно в кожу или пропитывают марлю и применяют к коже несколько (1-5) раз в день.
Настоящее изобретение поясняется конкретными примерами, причем должно быть понятно, что указанные примеры предназначены только для пояснения, и что изобретение может включать любые желательные модификации, которые входят в объем формулы изобретения.
Настоящее изобретение теперь будет пояснено подробнее с обращением к примерам, причем следует иметь в виду, что изобретение не ограничивается указанными примерами.
Примеры
1. Оценка, основанная на степени ингибирования гепараназной активности
Клетки А431 (клетки эпителиальной карциномы человека) культивируют в содержащей 10% сыворотки DMEM (модифицированная по способу Дульбекко среда Игла). Культивированные клетки солюбилизируют в буфере для лизиса (50 мМ трис, 0,5% Triton Х-100, 0,15 М хлорида натрия, рН 4,5) и собирают скребком и затем пипетируют и оставляют стоять на льду в течение 30 минут. За этим следует центрифугирование при 10000 об/мин в течение 10 минут для удаления нерастворимой части, и супернатант извлекают как клеточный экстракт.Количество белка в клеточном экстракте измеряют с помощью набора для анализа белка ВСА (ВСА Protein Assay Kit, PIERCE, CA46141).
Затем экстракт клеток А431 разбавляют до 500 мкг/мл буфером для анализа (50 мМ HEPES, 50 мМ ацетата натрия, 150 мМ хлорида натрия, 9 мМ хлорида кальция, 0,1% BSA). Затем испытываемое соединение растворяют в ДМСО и добавляют к разбавленному клеточному экстракту в количествах 0,0005 мас.%, 0,005 мас.% и 0,05 мас.%, перемешивают, и получают испытываемые растворы (конечная концентрация ДМСО 5%). Контрольный раствор получают, смешивая ДМСО с разбавленным клеточным экстрактом до конечной концентрации 5%, и испытываемый раствор и контрольный раствор высевают на биотинилированный планшет с иммобилизованным гепарансульфатом в количестве 100 мкл/лунка. После взаимодействия при 37ºС в течение 2 часов и промывки PBS-T 3 раза добавляют разведенный 10000 крат HPR-авидин (Vector, A-2004)/PBS-T в количестве 100 мкл/лунка, и реакцию продолжают при 37ºС в течение 1 часа. После дополнительной промывки PBS-T 3 раза добавляют реагент ТМВ (BIO-RAD, 172-1066) в количестве 100 мкл/лунка, проводят реакцию, прекращают реакцию IN серной кислотой, и измеряют поглощение при 475 нм (OD475).
Также ДМСО добавляют к серийным разведениям, полученным с буфером для анализа с вышеуказанным экстрактом клеток А431 (концентрации клеточного экстракта 500 мкг/мл, 50 мкг/мл, 5 мкг/мл, 0,5 мкг/мл) до конечной концентрации 5% без добавления испытываемого соединения, и получают смесь (раствор для калибровочной кривой). Раствор для калибровочной кривой подвергают обработке той же процедурой, какая описана выше, от высевания на биотинилированный планшет с иммобилизованным гепарансульфатом, и измеряют OD475.
Затем строят калибровочную кривую для концентрации белка на основании величины OD475 раствора для калибровочной кривой, и полученную калибровочную кривую используют для вычисления концентрации белка в каждом испытываемом растворе, полученном добавлением испытываемого соединения в различных концентрациях. Концентрацию белка вычисляют таким же образом для контрольного раствора. Степень ингибирования гепараназной активности каждым испытываемым раствором определяют из отношения концентрации белка в каждом испытываемом растворе и концентрации белка в контрольном растворе (%).
Подробности, касающиеся данной процедуры, описаны в патенте Японии №2003-502054.
Ингибирующее действие на гепараназную активность различных циклических карбоксамидных производных проверяют с помощью указанной процедуры. Результаты приводятся в таблице 1. Из таблицы 1 видно, что каждое циклическое карбоксамидное производное 2-имидазолидинон, 1-(2-гидроксиэтил)-2-имидазолидинон и 1-(2-гидроксиэтил)-2-пирролидон показывает степень ингибирования 37,64% при добавлении в концентрации 0,0005% и 94,74% при добавлении в концентрации 0,05%, и, следовательно, эффективно ингибирует гепараназную активность.
2. Оценка изменения гепараназной активности под действием ультрафиолетового излучения
Зрелые кератиноциты человека культивируют в нормальной среде для кератиноцитов. Культуральную среду временно размещают в PBS и затем облучают UVB 50 мДж, и после культивирования в течение 1 часа, 2 часов и 4 часов клетки солюбилизируют в буфере для лизиса и используют в качестве испытываемых растворов в группе ультрафиолетового излучения. Также среду временно размещают в PBS без облучения ультрафиолетовым светом для использования в качестве контрольного раствора. Испытываемые растворы и контрольный раствор используют для одинаковой обработки, как в примере 1, и измеряют OD475. Гепараназную активность оценивают так же, как в примере 1, на основании полученных величин OD475. Результаты приводятся на фиг.1. Видно, что гепараназа существенно активируется в группе ультрафиолетового излучения по сравнению с необлученным контролем.
Иммунное окрашивание гепараназы и гепарансульфата в коже человека, облученной ультрафиолетовым светом
Ягодицы человека (20-летнего возраста) облучают ультрафиолетовыми лучами 2MED, и через 2 суток облученный участок и окружающую необлученную кожу ягодицы берут на биопсию, и получают парафиновый блок методом АМеХ. Получают 3-мкм срез ткани, и осуществляют иммунное окрашивание гепараназы и гепарансульфата. Полученное при иммунном окрашивании изображение показано на фиг.2. Количество гепараназы в облученном ультрафиолетовыми лучами участке явно возросло, а количество гепарансульфата уменьшилось по сравнению с необлученным участком.
Оценка проникновения VEGF и ангиогенеза с гепарансульфатом и без него
После нагревания и растворения 2 мг гепарансульфата и 10 мг агарозы в 1 мл PBS (1% раствор агарозы) полученный раствор наносят на вставку (24-луночный Transwell, Coming, Inc.), и получают слой, содержащий гепарансульфат. Такой же процедурой, за исключением того, что используют одну агарозу без использования гепарансульфата, получают в качестве контроля слой, не содержащий гепарансульфат. Таким образом, выбирают внутреннюю часть вставки для стороны эпидермиса, слой - в качестве базальной мембраны и лунку для стороны дермы, и получают модель псевдокожи (фиг.3, a, b).
Полученную модель псевдокожи можно использовать как систему оценки для оценки проникновения VEGF и ангиогенеза, основываясь на присутствии или отсутствии гепарансульфата на слое, выбранном в качестве базальной мембраны (далее в данном описании называемом «слой базальной мембраны»). В последующем пояснении модель псевдокожи, содержащая гепарансульфат в слое базальной мембраны, называется «нормальной моделью», и модель псевдокожи, не содержащая гепарансульфат в слое базальной мембраны, называется «моделью с разложившимся гепарансульфатом».
Сначала для оценки проникновения VEGF со стороны эпидермиса (внутренняя часть вставки) каждой модели добавляют водный раствор 10 мкг/мл VEGF и оставляют стоять в течение 3 часов при комнатной температуре, и определяют концентрацию VEGF в лунке на дерме с помощью набора для ELISA VEGF (S&D Systems). Результаты приводятся на фиг.4. Проникновение VEGF существенно меньше на нормальной модели по сравнению с моделью с разложившимся гепарансульфатом.
Затем для оценки ангиогенеза со стороны эпидермиса (внутренняя часть вставки) каждой модели добавляют водный раствор 100 мкг/мл VEGF, и помещают в набор для ангиогенеза (Kurabo Industries, Ltd.) для культивирования на 11 суток, после чего получают фотографии культуры на оптическом микроскопе. Полученное изображение показано на фиг.5. На модели с разложившимся гепарансульфатом наблюдают заметный ангиогенез в зависимости от концентрации, в то время как на нормальной модели ангиогенез не наблюдают.
Используют программу для анализа набора для ангиогенеза (Kurabo Industries, Ltd.) для анализа площади кровеносных сосудов на изображении на фиг.5. Результаты приводятся на фиг.6. На модели с разложившимся гепарансульфатом наблюдают заметное возрастание площади кровеносных сосудов по сравнению с нормальной моделью, что показывает существенный ангиогенез.
3. Оценка отбеливающего действия ингибитора гепараназы
Используют содержащую меланоциты модель кожи для проверки отбеливающего действия ингибитора гепараназы 1-[4-(1Н-бензимидазол-2-ил)фенил]-3-[4-(1Н-бензимидазол-2-ил)фенил)мочевины.
Культивирование содержащей меланоциты модели кожи (MEL-FT, изготовитель MatTeK, США) инициируют в специальной среде (MEL-FT-NMM-113, изготовитель MatTeK, США). Со второго дня культивирования добавляют ДМСО к контрольной группе и группе с 1-[4-(1Н-бензимидазол-2-ил)фенил]-3-[4-(1Н-бензимидазол-2-ил)фенил)мочевиной до конечной концентрации 50 мкМ в группе с ингибитором гепараназы, и продолжают культивирование с заменой среды каждый 2 или 3 дня. На 10-ый и 14-ый дни культивирования берут образцы модели кожи и делают фотографии внешнего вида, посредством чего находят, что цвет в группе с ингибитором гепараназы несколько светлее по сравнению с контрольной группой.
Затем берут образец одного эпидермиса модели кожи, добавляют 300 мкл 0,2 N раствора гидроксида натрия, и смесь перемешивают и оставляют стоять в течение 24 часов при комнатной температуре и затем греют в течение 30 минут при 95°C для завершения солюбилизации эпидермиса. Когда содержание меланина в эпидермисе проверяют путем измерения поглощения солюбилизированного раствора при 475 нм, группа с ингибитором гепараназы явно имеет существенно меньшую величину OD475, т.е., содержание меланина меньше по сравнению с контрольной группой.
Фиг.7 показывает фотографию внешнего вида модели кожи MEL-FT. Отчетливо видна белизна в группе с ингибитором гепараназы на 10-ый и 14-ый дни культивирования. Фиг.8 показывает сравнительные результаты для содержания меланина в эпидермисе для каждой модели кожи. На 10-ый и 14-ый дни культивирования величина поглощения при 475 нм как индикатор меланина в группе с ингибитором гепараназы в основном низкая. Таким образом показано, что ингибитор гепараназы имеет отбеливающее действие.
4. Иммунное окрашивание лиофилизованной ткани человека
Из кусочка лиофилизованной ткани старческого пигментного пятна и окружающей нормальной ткани готовят свежий гистологический срез, и получают полоски 8 мкм. 8-мкм полоски ткани фиксируют холодным ацетоном и сушат, и удаляют ОСТ с помощью PBS. После дезактивации эндогенной пероксидазы обработкой 3% пероксидом водорода ее подвергают блокаде 10% сывороткой здоровой козы, и проводят реакцию с первичными антителами и вторичными антителами, указанными в таблице 2, в указанном порядке. Меченную HRP ткань 5 раз промывают PBS и затем окрашивают АЕС. Окрашенную ткань тщательно промывают в проточной воде и затем инкапсулируют с использованием водорастворимого заливочного средства.
5. Анализ bFGF in situ
После связывания 25 мкг bFGF с 200 мкл набухшей гепаран-сефарозы (CL-6B; Pharmacia Biotech) его вводят в реакцию с NH2-реакционноспособным биотином (Dojindo molecular tech.), растворенным в ДМСО в течение 5 минут при комнатной температуре, затем смесь промывают 800 мкл буфера для промывки (20 ммоль/л HEPES, рН 7,4, 400 ммоль/л NaCl), и дважды элюируют 200 мкл буфера для элюирования (20 ммоль/л HEPES, рН 7,4, 0,2% BSA, 3 моль/л NaCl) для извлечения биотинилированного bFGF с высокой концентрацией соли. Затем его помещают в колонку Ultra free C3LGC (Amicon) и 3 раза промывают PBS, и получают биотинилированный bFGF (0,25 г/л).
Полоски ткани в парафине (участки старческой ткани с себорейным кератозом и окружающей нормальной тканью), нарезанные по 5 мкм, депарафинируют ксилолом и затем обменивают с этанолом (100% → 70%), и инактивируют эндогенную пероксидазу обработкой 3% водным пероксидом водорода. Затем их промывают буфером с рН 5 (содержащим 0,5 М NaCl) и буфером с рН 10 (содержащим 0,5 М NaCl) для высвобождения эндогенных гепарансульфатсвязывающих факторов. Блокировку выполняют 10% сывороткой с последующим взаимодействием с биотинилированным bFGF (10 нмоль/л) при комнатной температуре в течение 1 часа и промывкой PBS 3 раза. Затем следует взаимодействие с меченным пероксидазой стрептавидином (Nichirei, Япония) при комнатной температуре в течение 15 минут, промывка PBS 3 раза и окрашивание DAB. Окрашенную ткань тщательно промывают проточной водой, и после окрашивания ядер гематоксилином и выполнения обмена с этанолом (70% → 100%) и замещения ксилола ее инкапсулируют.
6. Анализ изображения кровеносных сосудов и лимфатических сосудов
Ткань, окрашенную CD31 и окрашенную LYVE1, фотографируют 3 раза на срез, и вычисляют число окрашенных кровеносных сосудов и лимфатических сосудов и площадь путем анализа с использованием WinROOF (Mitani Corporation). Кроме того, с помощью анализа изображения также вычисляют общую площадь дермы в папиллярном слое дермы, и вычисляют плотность и размеры кровеносных сосудов или лимфатических сосудов.
Фиг.9 показывает результаты иммунного окрашивания для перлекана и гепарансульфата в старческих пигментных пятнах и в окружающей нормальной ткани. Базальная мембрана окрашивается как перлеканом, так и гепарансульфатом в нормальной ткани, но окрашивается только путем окрашивания перлекана в старческой пигментированной ткани, в то время как окрашивание гепарансульфата заметно уменьшается. Такие результаты показывают, что гепарансульфат существенно разлагается в участках старческих пигментных пятен.
Фиг.10 показывает результаты иммунного окрашивания антителами против CD31 как маркера кровеносных сосудов вместе с результатами анализа изображения. Число, толщину и площадь окрашенных CD31 кровеносных сосудов вычисляют с помощью программы анализа изображений WinROOF для каждого окрашенного изображения, и анализируют изменение в кровеносных сосудах в участках старческих пигментных пятен и участках окружающей нормальной ткани. Находят, что размеры кровеносных сосудов и площади кровеносных сосудов значительно выше в участках старческих пигментных пятен. Такие результаты показывают, что в участках старческих пигментных пятен происходит васкуляризация.
Фиг.11 показывает результаты иммунного окрашивания антителами против LYVE1 как маркера лимфатических сосудов вместе с результатами анализа изображения. Число, толщину и площадь окрашенных LYVE1 лимфатических сосудов вычисляют с помощью программы анализа изображений WinROOF для каждого окрашенного изображения, и анализируют изменение в лимфатических сосудах в участках старческих пигментных пятен и участках окружающей нормальной ткани. Находят, что размеры лимфатических сосудов и площади лимфатических сосудов значительно выше в участках старческих пигментных пятен. Такие результаты показывают, что в участках старческих пигментных пятен происходит лимфангиэктазия.
Фиг.12 показывает результаты анализа связывания bFGF in situ старческой пигментированной тканью. В данном случае видно, что базальная мембрана окрашена в коричневый цвет в нормальной ткани, окружающей старческие пигментные пятна, что указывает на связывание bFGF, в то время как окрашивания базальной мембраны в участках старческих пигментных пятен не видно, т.е., bFGF не способен связываться, что приводит к выводу, что связывание bFGF больше невозможно из-за разложения гепарансульфата.
Фиг.13 показывает результаты анализа связывания bFGF in situ себорейной пигментированной тканью. В данном случае видно, что базальная мембрана окрашена в коричневый цвет в нормальной ткани, окружающей себорейные пигментные пятна, что указывает на связывание bFGF, в то время как окрашивания базальной мембраны в участках себорейных пигментных пятен не видно, т.е., bFGF не способен связываться, что приводит к выводу, что связывание bFGF больше невозможно из-за разложения гепарансульфата.
Промышленная применимость
Так как ингибитор гепараназной активности по настоящему изобретению может эффективно ингибировать гепараназную активность, его можно использовать в качестве активного ингредиента в средстве против морщин, например; для предупреждения или подавления образования морщин (в частности, крупных морщин) или для предупреждения или подавления пигментации, включая пятна на коже, веснушки или утрату чистоты кожи.
Реферат
Изобретение относится к области фармацевтики и косметологии и касается ингибитора гепараназной активности, включающего в качестве активного ингредиента циклическое карбоксамидное производное, представленное формулой (I) или его соли, который может использоваться в качестве средства против морщин или для отбеливания кожи. 4 н. и 2 з.п. ф-лы, 13 ил., 2 табл., 6 пр.
Формула

в которой n равен целому числу от 1 до 3,
R1 представляет собой водород или углеводородную группу С1-6, необязательно замещенную гидроксилом,
X представляет собой -СН2- или группу, представленную -N(R2)-, где R2 представляет собой водород или углеводородную группу С1-6, необязательно замещенную гидроксилом,
или его соль.

Комментарии