Гели на основе гиалуроновой кислоты, включающие обезболивающие агенты - RU2496474C2
Код документа: RU2496474C2
Чертежи
Описание
Перекрестная ссылка на родственные заявки на изобретения
В этой заявке на изобретение заявлен приоритет предварительной заявки на патент США номер 61/085956, поданной 4 августа 2008 года, предварительной заявки на патент США номер 61/087934, поданной 11 августа 2008 года, предварительной заявки на патент США номер 61/096278, поданной 11 сентября 2008 года, не предварительной заявки на патент США номер 12/393768, поданной 26 февраля 2009 года, и не предварительной заявки на патент США номер 12/393884, поданной 26 февраля 2009 года, полное содержание которых включено здесь путем ссылки.
Область изобретения
Настоящее изобретение в общем относится к инъецируемым наполнителям мягких тканей и более конкретно относится к основанным на гиалуроновой кислоте кожным и подкожным наполнителям, включающим обезболивающий агент.
Предшествующий уровень техники
Общеизвестно, что по мере старения людей на лице начинают отражаться эффекты силы тяжести, солнечного воздействия и многолетних движений лицевой мускулатуры, таких как улыбка, нахмуривание бровей, жевание и прищуривание глаз. Нижележащие ткани, которые придают коже молодой внешний вид, начинают разрушаться, часто приводя в результате к морщинкам от смеха, морщинкам от улыбки, эффекту "гусиных лапок" и лицевым морщинам, которые часто называются "эффектами старения".
В попытках лечить или корректировать эффекты старения разработаны наполнители мягких тканей, способствующие заполнению лицевых линий и складок и восстановлению утраты объема ткани вследствие утраты жира. Наполнители мягких тканей, таким образом, временно восстанавливают более мягкий более молодой внешний вид.
В идеале, наполнители мягких тканей являются стойкими, мягкими, сглаженными и имеют естественный внешний вид, будучи имплантированными в кожу или под кожу. Кроме того, наполнители мягких тканей легко имплантировать пациенту с использованием иглы тонкого калибра и они требуют низкой силы выталкивания для инъекции. Идеальные наполнители также могут не вызывать неблагоприятных побочных действий и могут быть инъецированы с минимальным дискомфортом для пациента или при отсутствии дискомфорта.
Основанные на коллагене наполнители мягких тканей разработаны около 20 лет назад, и в течение некоторого времени наполнители, основанные на бычьем коллагене, представляли собой единственные кожные наполнители, которые одобрены U.S. Food and Drug Administration (FDA) (Управлением no санитарному надзору за качеством пищевых продуктов и медикаментов). Поскольку эти кожные наполнители основаны на бычьем материале, один из основных недостатков заключается в потенциальных аллергических реакциях у пациентов. Полагают, что приблизительно 3-5% людей проявляют серьезные аллергические реакции на бычий коллаген, таким образом требуя осторожного тестирования перед использованием этих наполнителей в отношении любого конкретного лица. Дополнительно к аллергическим реакциям основанные на коллагене наполнители быстро деградируют после инъекции и требуют частых введений для поддержания более гладкого, более молодого внешнего вида.
В феврале 2003 года композиции наполнителей на основе человеческого коллагена получили одобрение FDA. Эти коллагены обеспечивают преимущество, заключающееся в значительно уменьшенном риске аллергических реакций. Тем не менее, несмотря на уменьшенную частоту аллергических реакций, наполнители на основе человеческого коллагена все же страдают от быстрой деградации инъецированного продукта.
Поиск наполнителей, которые не вызывают аллергические реакции и поддерживают более гладкий более молодой внешний вид, привел к разработке продуктов, на основе гиалуроновой кислоты (ГК). В декабре 2003 года первый наполнитель на основе ГК был одобрен FDA. За ним быстро последовала разработка других наполнителей на основе ГК.
ГК, также известный как гиалуронан, представляет собой встречающийся в природе водорастворимый полисахарид, в частности глюкозаминогликан, который представляет собой основной компонент внеклеточного матрикса и широко распространен в животных тканях. ГК обладает превосходной биосовместимостью и не вызывает аллергические реакции после имплантации пациенту. Дополнительно, ГК обладает способностью связываться с большими количествами воды, превращая ее в превосходный агент, придающий объем мягким тканям.
Разработка наполнителей на основе ГК, которые демонстрируют идеальные свойства in vivo, а также идеальную хирургическую применимость, как оказалось, является трудной. Например, наполнители на основе ГК, которые демонстрируют желаемые свойства стабильности in vivo, могут быть настолько вязкими, что инъекция через иглы с тонким калибром, является трудной. Наоборот, наполнители на основе ГК, которые относительно легко инъецировать через иглы с тонким калибром, часто обладают относительно более плохими свойствами стабильности in vivo.
Один из способов преодоления этой проблемы заключается в применении перекрестно-сшитых наполнителей на основе ГК. Перекрестно-сшитая ГК образуется путем взаимодействия свободной ГК с перекрестно сшивающим агентом в подходящих условиях реакции. Хорошо известны способы получения наполнителей мягких тканей на основе ГК, включающих перекрестно-сшитую и свободную ГК.
Предложено включать некоторые терапевтические агенты, например обезболивающие агенты, такие как лидокаин, в инъецируемые композиции на основе ГК. К сожалению, инъецируемые композиции на основе ГК, которые включают лидокаин, во время способа приготовления, склонны частичной или почти полной деградации перед инъекцией, в особенности во время стадий высокотемпературной стерилизации и/или при помещении на хранение на любой значительный промежуток времени.
Задача композиций мягкого наполнителя на основе ГК и способов их получения и применения, как описано, заключаются в том, чтобы предложить наполнители мягких тканей, которые не вызывают аллергические реакции у пациентов, являются биосовместимыми и стабильными и применимы in vivo, и включают один или более чем один локальный обезболивающий агент.
Краткое изложение сущности изобретения
Описание настоящего изобретения относится к наполнителям мягких тканей, например кожным и подкожным наполнителям на основе гиалуроновой кислоты (ГК) и фармацевтически приемлемых солей ГК, например гиалуроната натрия (NaГК). Композиции на основе ГК, описанные в данном документе, включают терапевтически эффективное количество по меньшей мере одного обезболивающего агента. В одном из воплощений, например, обезболивающий агент представляет собой лидокаин. Композиции на основе ГК по настоящему изобретению, включающие по меньшей мере один обезболивающий агент, обладают улучшенной стабильностью, по сравнению с обычными композициями на основе ГК, включающими, например лидокаин, будучи подверженными способам стерилизации, таким как автоклавирование и/или при хранении в течение длительных периодов времени при температуре окружающей среды. Также предложены способы получения таких композиций на основе ГК, а также продукты, полученные при помощи таких способов.
В данном документе описаны композиции наполнителей для мягких тканей, где указанные композиции в общем содержат: компонент гиалуроновой кислоты (ГК), перекрестно-сшитый перекрестно сшивающим агентом, выбранным из группы, состоящей из 1,4-бутандиолдиглицидильного эфира (БДДЭ), 1,4-бис(2,3-эпоксипропокси)бутана, 1,4-бисглицидилоксибутана, 1,2-бис(2,3-эпоксипропокси)этилена и 1-(2,3-эпоксипропил)-2,3-эпоксициклогексана, и 1,4-бутандиолдиглицидильного эфира; и по меньшей мере один обезболивающий агент комбинированный с перекрестно-сшитым компонентом ГК.
В еще одном воплощении по меньшей мере один обезболивающий агент представляет собой лидокаин. В еще одном воплощении количество обезболивающего агента представлено в концентрации от приблизительно 0,1% до приблизительно 5,0 масс.% композиции. В еще одном воплощении обезболивающий агент представлен в концентрации от приблизительно 0,2% до приблизительно 1,0 масс.% композиции. В одном из воплощений, обезболивающий агент представляет собой лидокаин и представлен в концентрации приблизительно 0,3 масс.% композиции.
В еще одном воплощении композиция наполнителя мягких тканей обладает силой выталкивания от приблизительно 10 Н до приблизительно 13 Н, например, при скорости приблизительно 12,5 мм/минуту. В еще одном воплощении композиция обладает вязкостью от приблизительно 5 Па*с до приблизительно 450 Па*с, например измеренной при приблизительно 5 Гц.
В одном из воплощений компонент ГК представляет собой гель, например, когезионный гидратированный гель. В одном из воплощений компонент ГК представляет собой перекрестно-сшитый гель ГК, имеющий не больше чем приблизительно от 1% до приблизительно 10% свободной ГК. Для задач данного описания свободная ГК включает действительно не сшитую перекрестной связью ГК, а также в незначительной степени сшитые перекрестной связью цепи и фрагменты ГК, все из которых представлены в растворимой в воде форме.
В других воплощениях компонент ГК содержит больше чем приблизительно 10%, например, больше чем приблизительно 15%, например, до или больше чем приблизительно 20% свободной ГК.
В еще одном воплощении компонент ГК представляет собой гель, содержащий частицы перекрестно-сшитой ГК в относительно текучей среде свободной ГК. В некоторых воплощениях компонент ГК имеет средний размер частиц больше чем приблизительно 200 мкм, например, больше чем приблизительно 250 мкм.
В данном документе дополнительно описана композиция наполнителя мягких тканей, содержащая: компонент ГК, перекрестно сшитый с 1,4-бутандиолдиглицидильным эфиром (БДДЭ), где указанный ГК компонент обладает степенью перекрестного сшивания меньше чем приблизительно 5%, например приблизительно 2%, и обезболивающий агент, имеющий концентрацию от приблизительно 0,1% до приблизительно 5,0 масс.% композиции наполнителя мягких тканей, где обезболивающий агент представляет собой лидокаин.
В данном документе дополнительно описаны способы приготовления композиции наполнителя мягких тканей, где в способах осуществляют стадии: получения компонента ГК, перекрестно-сшитого с помощью по меньшей мере одного перекрестно-сшивающего агента, выбранного из группы, состоящей из 1,4-бутандиолдиглицидильного эфира (БДДЭ), 1,4-бис(2,3-эпоксипропокси)бутана, 1,4-бисглицидилоксибутана, 1,2-бис(2,3-эпоксипропокси)этилена и 1-(2,3-эпоксипропил)-2,3-эпоксициклогексана и 1,4-бутандиолдиглицидильного эфира или их комбинаций; доведения pH указанного ГК компонента к pH больше приблизительно 7,2; и добавления раствора, содержащего по меньшей мере один обезболивающий агент, к компоненту ГК, имеющему доведенный pH, с получением композиции наполнителя на основе ГК.
В еще одном воплощении композицию стерилизуют, например, путем автоклавирования, с образованием стерилизованной композиции, и где стерилизованная композиция стабильна при температуре окружающей среды в течение по меньшей мере приблизительно 6 месяцев, например, по меньшей мере 9 месяцев, по меньшей мере приблизительно 12 месяцев или больше.
В еще одном воплощении доведенный pH составляет больше приблизительно 7,5. В еще одном воплощении в способе дополнительно осуществляют стадию гомогенизации компонента ГК во время или после стадии добавления раствора содержащего по меньшей мере один обезболивающий агент. В еще одном воплощении на стадии гомогенизации композицию подвергают смешиванию с контролируемым усилием сдвига.
В еще одном воплощении на стадии получения компонента ГК осуществляют получение сухого свободного материала NaГК и гидратирования сухого свободного материала NaГК в щелочном растворе с получением щелочного свободного геля NaГК. В еще одном воплощении щелочной свободный гель NaГК имеет pH больше чем приблизительно 8,0. ГВ еще одном воплощении pH составляет больше чем приблизительно 10.
В еще одном воплощении компонент ГК содержит больше чем приблизительно 20% свободной ГК и перекрестно-сшитый фрагмент компонента ГК имеет степень перекрестного сшивания меньше чем приблизительно 6% или меньше чем приблизительно 5%.
В еще одном воплощении композиция наполнителя мягких тканей имеет природу в виде частиц, которой содержит частицы перекрестно-сшитой ГК диспергированные в текучей растворимой среде ГК. В некоторых воплощениях средний размер таких частиц составляет по меньшей мере приблизительно 200 мкм, и в других воплощениях средний размер таких частиц составляет по меньшей мере приблизительно 250 мкм.
В данном документе дополнительно описана композиция наполнителя мягких тканей, содержащая: компонент гиалуроновой кислоты (ГК), перекрестно сшитый с помощью 1,4-бутандиолдиглицидильного эфира (БДДЭ), где указанный ГК компонент обладает степенью перекрестного сшивания меньше чем приблизительно 5%, и обезболивающий агент, имеющий концентрацию от приблизительно 0,1% до приблизительно 5,0 масс.% композиции наполнителя мягких тканей, где обезболивающий агент представляет собой лидокаин.
В конкретном воплощении изобретения дополнительно описан способ приготовления композиции наполнителя мягких тканей, при котором осуществляют стадии: получения безводного свободного материала NaГК и гидратирования безводного свободного материала №ГК в щелочном растворе с получением щелочного свободного геля NaГК; перекрестного сшивания свободного геля NaГК с помощью БДДЭ с образованием перекрестно-сшитой щелочной композиции ГК со степенью перекрестного сшивания меньше чем приблизительно 5% и pH больше приблизительно 7,2; добавления раствора, содержащего лидокаин HCl к компоненту ГК, имеющему доведенный pH, с получением указанной композиции наполнителя на основе ГК; гомогенизации композиции наполнителя на основе ГК, таким образом, с образованием гомогенизированной композиции наполнителя на основе ГК; и стерилизации гомогенизированной композиции наполнителя на основе ГК, таким образом с образованием стерилизованной композиции наполнителя на основе ГК, где композиция наполнителя мягких тканей имеет размер частиц больше чем приблизительно 200 мкм, например размер частиц больше чем приблизительно 250 мкм.
Краткое описание графических материалов
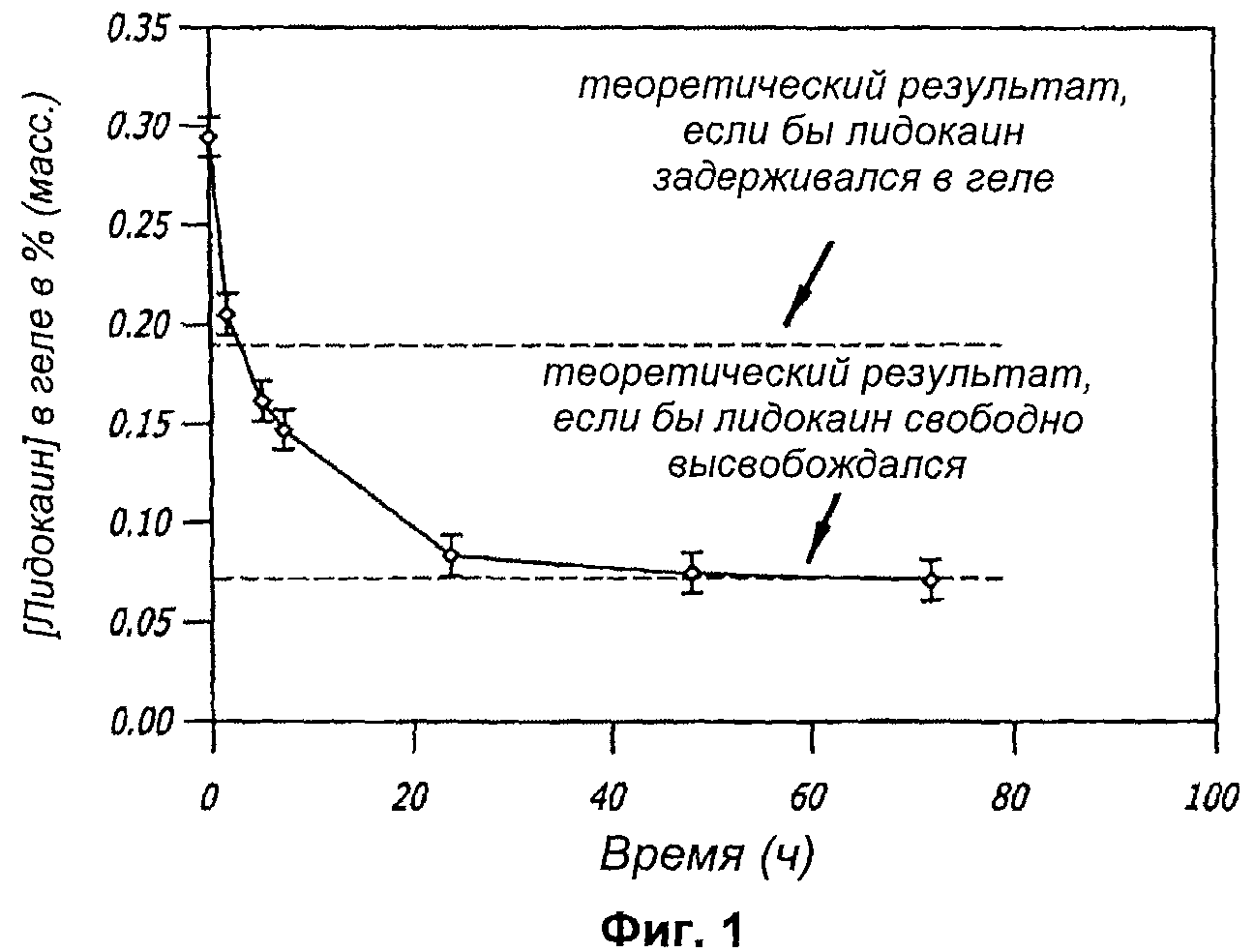
Фиг.1 графически иллюстрирует концентрацию лидокаина в гелевой форме Образца 5 в примере 4, приготовленной при помощи способа в соответствии с тестом 2 в зависимости от времени.
Определения
Предполагается, что некоторые термины, используемые в описании, относятся к следующим определениям, как подробно изложено ниже. Когда определение терминов отклоняется от обычно используемого значения этого термина, тогда, если не указано иное, заявитель имеет намерение использовать приведенные ниже определения.
Используемый в данном документе термин "стабильный при автоклавировании" или "стабильный к автоклавированию" описывает продукт или композицию, устойчивую к деградации, таким образом, что продукт или композиция содержит по меньшей мере один, и предпочтительно все из следующих аспектов после эффективной автоклавируемой стерилизации: прозрачность, pH, силу выталкивания и/или реологические характеристики, концентрацию гиалуроновой кислоты (ГК), стерильность, осмолярность и концентрацию лидокаина.
Используемый в данном документе термин "высокомолекулярная ГК" описывает вещество ГК, имеющее молекулярную массу по меньшей мере от приблизительно 1,0 миллион Дальтон (м.м. ≥106 Да или 1 МДа) до приблизительно 4,0 МДа. Например, высокомолекулярная ГК в композиции по настоящему изобретению может иметь молекулярную массу приблизительно 2,0 МДа. В еще одном примере высокомолекулярная ГК может иметь молекулярную массу приблизительно 2,8 МДа.
Используемый в данном документе термин "низкомолекулярная ГК" описывает вещество ГК, имеющее молекулярную массу меньше чем приблизительно 1,0 МДа. Низкомолекулярная ГК может иметь молекулярную массу от приблизительно 200000 Да (0,2 МДа) до меньше чем приблизительно 1,0 МДа, например от приблизительно 300000 Да (0,3 МДа) до приблизительно 750000 Да. (0,75 МДа).
Используемый в данном документе термин "степень перекрестного сшивания" относится к межмолекулярным соединениям, сшивающим индивидуальные молекулы полимера ГК или мономерные цепи в прочную структуру, или, как раскрыто в данном документе, композицию наполнителя мягких тканей. Кроме того, степень перекрестного сшивания для задач настоящего описания дополнительно определяется как процент массовой доли перекрестно-сшивающего агента к мономерным единицам ГК в перекрестно-сшитом фрагменте композиции на основе ГК. Она измеряется массовой долей мономеров ГК относительно перекрестно-сшивающего агента (мономеры ГК: перекрестно-сшивающий агент).
Используемый в данном документе термин "свободная ГК" относится к индивидуальным молекулам полимера ГК, которые не являются перекрестно-сшитыми или в незначительной степени перекрестно-сшиты (очень низкая степень перекрестного сшивания) с сильно перекрестно-сшитой (высокая степень перекрестного сшивания) макромолекулярной структурой, составляющей композицию наполнителя мягких тканей. Свободная ГК, как правило, остается растворимой в воде. Свободная ГК альтернативно может быть определена как "не являющаяся перекрестно сшитой" или как в незначительной степени перекрестно сшитый компонент макромолекулярной структуры, составляющей композицию раскрытого здесь наполнителя мягких тканей.
Используемый в данном документе термин "когезионный" представляет собой способность композиции на основе ГК сохранять свою форму и препятствовать деформации. На когезионность среди прочих факторов влияет доля молекулярной массы исходной свободной ГК, степень перекрестного сшивания, количество остаточной свободной ГК после перекрестного сшивания и pH композиции на основе ГК. Когезионная композиция на основе ГК противостоит фазовому разделению при тестировании в соответствии со способом, раскрытым здесь в примере 1.
Подробное описание изобретения
Описание настоящего изобретения в общем относится к наполнителям мягких тканей, например кожным и подкожным наполнителям на основе гиалуроновой кислоты (ГК) и фармацевтически приемлемых солей ГК, например гиалуронате натрия (NaГК). В одном из аспектов композиции на основе ГК, описанные в данном документе, включают терапевтически эффективное количество по меньшей мере одного обезболивающего агента, например, лидокаина. Композиции на основе ГК по настоящему изобретению, включающие по меньшей мере один обезболивающий агент, обладают улучшенной стабильностью по сравнению с обычными композициями на основе ГК, включающими, например лидокаин, будучи подверженными высоким температурам и давлениям, например таким, какие возникают во время способов стерилизации теплом и/или под давлением, например, автоклавирование, и/или например во время хранения при температуре окружающей среды в течение длительного периода времени.
Стабильные композиции сохраняют по меньшей мере один из или все из следующих аспектов после эффективной стерилизации путем автоклавирования и/или при длительном хранении: прозрачность, pH для применения пациентом, сила выталкивания и/или реологические характеристики, концентрация ГК, стерильность, осмолярность и концентрация лидокаина. Также предложены методы или способы приготовления таких композиций на основе ГК, а также продукты, полученные при помощи таких методов или способов.
Используемый в данном документе термин "гиалуроновая кислота (ГК)" может относиться к любой из ее гиалуронатных солей, и включает гиалуронат натрия (NaГК), гиалуронат калия, гиалуронат магния, гиалуронат кальция и их комбинации, но не ограничивается ими.
Как правило, концентрация ГК описанной здесь композиции предпочтительно составляет по меньшей мере 10 мг/мл и до приблизительно 40 мг/мл. Например, концентрация ГК в некоторых из композиций находится в диапазоне от приблизительно 20 мг/мл до приблизительно 30 мг/мл. Кроме того, например, в некоторых воплощениях композиции имеют концентрацию ГК приблизительно 22 мг/мл, приблизительно 24 мг/мл, приблизительно 26 мг/мл, или приблизительно 28 мг/мл.
Дополнительно, концентрация одного или более чем одного обезболивающего агента представляет собой количество, эффективное для уменьшения боли, которую испытывают при инъекции композиции. По меньшей мере одно обезболивающее средство для местного введения может быть выбрано из группы амбукаина, амоланона, амилокаина, беноксината, бензокаина, бетоксикаина, бифенамина, бупивакаина, бутакаина, бутамбена, бутаниликаина, бутетамина, бутоксикаина, картикаина, хлорпрокаина, кокаэтилена, кокаина, циклометикаина, дибукаина, диметисоквина, диметокаина, диперодона, дициклонида, экгонидина, экгонина, этилхлорида, этидокаина, бета-эукаина, эупроцина, феналкомина, формокаина, гексилкаина, гидрокситетракаина, изобутил лара-аминобензоата, лейцинокаина мезилата, левоксадрола, лидокаина, мепивакаина, меприлкаина, метабутоксикаина, метилхлорида, миртекаина, наепаина, октакаина, ортокаина, оксетазаина, парэтоксикаина, фенакаина, фенола, пиперокаина, пиридокаина, полидоканола, прамоксина, прилокаина, прокаина, пропанокаина, пропаракаина, пропипокаина, пропоксикаина, псевдококаина, пиррокаина, ропивакаина, салицилового спирта, тетракаина, толикаина, тримекаина, золамина и их солей. В одном из воплощений по меньшей мере один обезболивающий агент представляет собой лидокаин, такой как в форме лидокаина HCl. Описанные в данном документе композиции могут иметь концентрацию лидокаина от приблизительно 0,1% до приблизительно 5 масс.% композиции, например от приблизительно 0,2% до приблизительно 1,0 масс.% композиции. В одном из воплощений композиция имеет концентрацию лидокаина приблизительно 0,3 масс.% (масс.%) композиции. Концентрация лидокаина в описанной в данном документе композиции может быть терапевтически эффективной, означая, что концентрация подходит для обеспечения терапевтической пользы, не причиняя пациенту вред.
В одном из аспектов изобретения предложен способ приготовления композиции на основе ГК, включающей эффективное количество лидокаина, где в способе готовят композицию предшественника, дополнительно содержащую перекрестно-сшитый гель на основе ГК, к ней добавляют раствор, содержащий лидокаин, например, в форме лидокаина HCl, и гомогенизируют смесь с получением когезионной по меньшей мере частично перекрестно-сшитой композиции на основе ГК, включающей лидокаин, которая стабильна при автоклавировании. Когезионный перекрестно-сшитый гель на основе ГК включает не больше чем от приблизительно 1% до приблизительно 10 масс/об.% свободной ГК или в незначительной степени сшитого вещества свободной ГК.
Не желая быть связанными какой-либо теорией, полагают, что высокая когезионная способность композиции предшественника в некоторых воплощениях изобретения действует таким образом, чтобы частично или полностью предупреждать или препятствовать какому-либо разрушению или деградации перекрестно-сшитой ГК в композиции при добавлении лидокаина.
Полагают, что такая деградация может в основном возникать поскольку множество, возможно большинство перекрестно-сшитых гелей на основе ГК обычно готовят таким образом, что получают гели, которые не достаточно когезионны для предупреждения такой деградации при добавлении лидокаина. В настоящее время обнаружили, что добавление лидокаина к в достаточной мере когезионным композициям на основе ГК не вызывает существенной или значительной деградации композиции, и композиции сохраняют свою целостность с точки зрения реологии, вязкости, внешнего вида и других характеристик даже при хранении в течение длительного периода времени, например, в течение периода времени по меньшей мере приблизительно от 6 месяцев до года или более, и даже после того, как их подвергают процедурам стерилизации, например автоклавированию.
Неожиданно обнаружили, что препараты перекрестно-сшитых композиций на основе ГК, включающих лидокаин, могут быть приготовлены согласно изобретению, чтобы получить стабильные при стерилизации инъецируемые композиции ГК/лидокаин.
В данном документе дополнительно описан способ получения стабильных композиций на основе ГК, содержащих эффективное количество лидокаина, путем приготовления когезионной перекрестно-сшитой композиции предшественника на основе ГК, добавления к композиции предшественника хлоргидрата лидокаина с образованием гелевой смеси ГК/лидокаин, и гомогенизации смеси с получением перекрестно-сшитой композиции на основе ГК, которая стабильна при автоклавировании.
В некоторых воплощениях композиция предшественник представляет собой гель, который содержит менее приблизительно 1% растворимой в жидкости формы свободной ГК. В других воплощениях композиция предшественника содержит не более от 1 об.% до 10 об.% свободной ГК.
Композиция предшественник может содержать первый компонент, включающий в относительно-высокой степени перекрестно-сшитые частицы ГК по существу в твердой фазе, и второй компонент, содержащий свободную или в относительно меньшей степени перекрестно-сшитую ГК по существу в жидкой фазе, в которой диспергированы в относительно высокой степени перекрестно-сшитые частицы. Композиция может включать от приблизительно 10 об.% до приблизительно 20 об.% или больше свободной ГК.
В некоторых воплощениях свободная ГК составляет меньше чем 20 масс.% композиции. Например, свободная ГК составляет меньше чем 10 масс.% компонента ГК. В еще одном примере вторая порция составляет от приблизительно 1% до приблизительно 10 масс.% компонента ГК.
Например, композиция, предшественник может содержать когезионный гель на основе ГК.
В других воплощениях свободная ГК составляет больше чем приблизительно 20 масс.% компонента ГК.
В некоторых воплощениях композиции по настоящему изобретению имеют природу частиц и содержат частицы в относительно высокой степени перекрестно-сшитой ГК, диспергированной в среде со свободной ГК. В некоторых воплощениях средний размер таких частиц перекрестно-сшитой ГК составляет по меньшей мере приблизительно 200 мкм или по меньшей мере приблизительно 250 мкм. Такие композиции в виде частиц, как правило, менее когезионны по сравнению иным образом похожими композициями, в которых отсутствуют различимые частицы, или имеют частицы, имеющие средний размер меньше чем 200 мкм.
Например, в некоторых воплощениях композиция предшественник может быть получена путем прессования массы в относительно высокой степени перекрестно-сшитого геля на основе ГК через решето или сито с получением в относительно высокой степени перекрестно-сшитых частиц ГК, имеющих в общем однородный размер и форму. Эти частицы затем смешивают с веществом носителя, например количеством свободной ГК с получением геля.
Кроме того, предложен способ получения композиции на основе ГК, включающей эффективное количество лидокаина, где в способе готовят композицию предшественник, включающий по существу имеющий нейтральный pH по меньшей мере частично перекрестно-сшитый гель на основе ГК, и доводят pH геля до значения больше чем приблизительно 7,2, например, от приблизительно 7,5 до приблизительно 8,0. В способе дополнительно осуществляют стадию комбинирования раствора, содержащего лидокаин, например, в форме лидокаина HCl, со слегка щелочным гелем после доведения pH и получения композиции на основе ГК, включающей лидокаин, которая стабильна при автоклавировании.
Еще в одном способе получения стабильной композиции на основе ГК, содержащей эффективное количество лидокаина, как описано, в общем осуществляют стадии: получения очищенного материала NaГК, например в форме волокон; гидратирования материала; и перекрестного сшивания гидратированного материла с подходящим перекрестно-сшивающим агентом с образованием перекрестно-сшитого геля на основе ГК. В способе дополнительно осуществляют стадии нейтрализации и набухания геля, и добавления к гелю раствора, содержащего лидокаин, предпочтительно кислой соли хлоргидрата лидокаина, с образованием геля ГК/лидокаин. Дополнительно в способе осуществляют гомогенизацию геля ГК/лидокаин и упаковку гомогенизированного геля ГК/лидокаин, например, в шприцы для дозирования. Шприцы затем стерилизуют путем автоклавирования при эффективной температуре и давлении. В соответствии с описанием настоящего изобретения упакованные и стерилизованные когезионные гели NaГК/лидокаин проявляют улучшенную стабильность по сравнению с композициями на основе ГК, включающими лидокаин, которые изготовлены с использованием обычных способов.
Полагают, что продукты и композиции по настоящему изобретению являются стерильными при воздействии температур по меньшей мере от приблизительно 120°C до приблизительно 130°C и/или давлений по меньшей мере от приблизительно 12 фунтов на квадратный дюйм (PSI) (82,7 кПа) до приблизительно 20 ф./кв.дюйм (137,9 кПа) во время автоклавирования в течение периода по меньшей мере приблизительно от 1 минуты до приблизительно 15 минут.
Продукты и композиции по настоящему изобретению также остаются стабильными при хранении в течение длительных периодов времени при комнатной температуре. Предпочтительно, композиции по настоящему изобретению остаются стабильными в течение периода по меньшей мере приблизительно двух месяцев, или по меньшей мере приблизительно шести месяцев, или по меньшей мере приблизительно 9 месяцев, или по меньшей мере приблизительно 12 месяцев, или по меньшей мере приблизительно 36 месяцев, при температурах по меньшей мере приблизительно 25°С. В конкретном воплощении композиции стабильны при температуре до приблизительно 45°С в течение периода по меньшей мере двух месяцев.
Способ получения включает, в одном из воплощений, исходную стадию получения неочищенного вещества ГК в форме безводных волокон или порошка ГК. Неочищенное вещество ГК может представлять собой ГК, ее соли и/или смеси. В предпочтительном воплощении вещество ГК содержит волокна или порошок NaГК, и еще более предпочтительно, NaГК из бактериального источника. В некоторых аспектах описания настоящего изобретения вещество ГК может быть получено из животного. Вещество ГК может представлять собой комбинацию неочищенных веществ, включающих ГК и по меньшей мере один другой полисахарид, например глюкозаминогликан (ГАГ).
В некоторых воплощениях вещество ГК в композиции почти полностью содержит или состоит из высокомолекулярной ГК. То есть, почти 100% вещества ГК в композиции по настоящему изобретению может представлять собой высокомолекулярную ГК, как определено выше. В других воплощениях вещество ГК в композиции содержит комбинацию высокомолекулярной ГК и относительно низкомолекулярной ГК, как определено выше.
Вещество ГК в композиции может содержать от приблизительно 5% до приблизительно 95% высокомолекулярной ГК с балансом вещества ГК, включающим низкомолекулярную ГК. В типичном воплощении изобретения отношение высокомолекулярной к низкомолекулярной ГК составляет по меньшей мере приблизительно и предпочтительно больше чем 2 (масс.≥2), где высокомолекулярная ГК имеет молекулярную массу больше 1,0 МДа.
Специалисту в данной области техники понятно, что выбор высоко- и низкомолекулярного вещества ГК и их относительные проценты или отношения зависят от желаемых характеристик, например силы выталкивания, модуля упругости, модуля вязкости и фазового угла, выраженного как отношение модуля вязкости к модулю упругости, когезионности и т.д. конечного основанного на ГК продукта. Дополнительную информацию, которая может быть полезна для понимания этого и других аспектов настоящего изобретения, смотри в Lebreton, публикация заявки на патент США №2006/0194758, полное описание которой включено в данный документ путем ссылки.
Гели на основе ГК могут быть приготовлены в соответствии с описанием настоящего изобретения сначала путем очистки сухого или неочищенного вещества ГК, обладающего желаемым отношением высокой/низкой молекулярной массы. Эти стадии в общем включают гидратирование сухих волокон ГК или порошка с желаемым отношением высокой/низкой молекулярной массы, например с использованием чистой воды, и фильтрования материала для удаления крупных чужеродных частиц и/или других примесей. Фильтрованное гидратированное вещество затем сушат и очищают. Высоко и низкомолекулярная ГК могут быть очищены раздельно, или могут быть смешаны вместе, например, в желаемом отношении непосредственно перед перекрестным сшиванием.
В одном из аспектов настоящего описания чистые безводные волокна ГК гидратируют в щелочном растворе с получением свободного щелочного NaГК геля. Любой подходящий щелочной раствор может быть использован для гидратирования NaГК на этой стадии, например водные растворы, содержащие гидроксид натрия (NaOH), гидроксид калия (КОН), бикарбонат натрия (NaHCO3), гидроксид лития (LiOH) и т.п., но не ограничиваясь ими. В еще одном воплощении подходящий щелочной раствор представляет собой водные растворы, содержащие NaOH. Получающийся в результате щелочной гель имеет pH больше 7,5. pH получающегося в результате щелочного геля может составлять больше чем 9, или больше чем 10, или больше чем 12, или больше чем 13.
Следующая стадия в способе приготовления включает стадию перекрестного сшивания гидратированного щелочного геля NarK с помощью подходящего перекрестно сшивающего агента. Перекрестно-сшивающий агент может представлять собой любой агент, который, как известно, подходит для перекрестного сшивания полисахаридов, и их производных посредством их гидроксильных групп.Подходящие перекрестно-сшивающие агенты включают 1,4-бутандиолдиглицидильный эфир (или 1,4-бис(2,3-эпоксипропокси)бутан или 1,4-бисглицидилоксибутан, все из которых в общем известны как БДДЭ), 1,2-бис(2,3-эпоксипропокси)этилен и 1-(2,3-эпоксипропил)-2,3-эпоксициклогексан, но не ограничиваются ими. Применение больше чем одного перекрестно-сшивающего агента или отличающегося перекрестно-сшивающего агента не исключается из объема настоящего описания. В одном из аспектов настоящего описания описанные в данном документе гели ГК перекрестно-сшиты с использованием БДДЭ.
Стадия перекрестного сшивания может быть осуществлена с использованием любых средств, известных специалистам в данной области техники. Специалистам в данной области техники понятно то, как оптимизировать условия перекрестного сшивания в соответствии с природой ГК, и как осуществлять перекрестное сшивание в оптимизированной степени.
"Степень перекрестного сшивания" для задач настоящего описания определяется как выраженное в процентах массовое отношение перекрестно-сшивающего агента к ГК-мономерным единицам в перекрестно-сшитом фрагменте композиции на основе ГК. Ее измеряют по массовому отношению мономеров ГК к перекрестно-сшивающему агенту (мономеры ГК: перекрестно-сшивающий агент).
Степень перекрестного сшивания в компоненте ГК композиций по настоящему изобретению составляет по меньшей мере приблизительно 2% и до приблизительно 20%.
В некоторых воплощениях степень перекрестного сшивания составляет от приблизительно 4% до приблизительно 12%. В некоторых воплощениях степень перекрестного сшивания составляет меньше чем приблизительно 6%, например меньше чем приблизительно 5%.
В других воплощениях степень перекрестного сшивания составляет больше чем 5%, например от приблизительно 6% до приблизительно 8%.
В некоторых воплощениях компонент ГК способен абсорбироваться по меньшей мере приблизительно однократно его массе в воде. При нейтрализации и набухании перекрестно-сшитый компонент ГК и вода, абсорбированная перекрестно-сшитым компонентом ГК, находятся в массовом отношении приблизительно 1:1. Образующиеся в результате гидратированные основанные на ГК гели обладают свойством, заключающимся в том, что они высококогезионные.
Гели на основе ГК в соответствии с некоторыми воплощениями изобретения могут обладать достаточной когезионностью, таким образом, что гели не будут претерпевать значительное фазовое разделение после центрифугирования геля при 2000 об./мин в течение 5 минут. В еще одном воплощении гели обладают свойством, заключающемся в том, что они способны абсорбировать воду по меньшей мере однократно их массе и обладают достаточной когезионностью, такой что после набухания в воде при массовом отношении гель/вода приблизительно 1:1, гели сохраняют свою целостность, например будучи подверженными центрифугированию.
Гидратированные перекрестно-сшитые гели ГК могут набухать с получением желаемой когезионности. Эта стадия может быть осуществлена путем нейтрализации перекрестно-сшитого гидратированного геля ГК, например путем добавления водного раствора, содержащего кислоту, такую как HCl. Гели затем набухают в забуференном фосфатом физиологическом растворе (PBS) в течение достаточного периода времени и при низкой температуре.
В одном из воплощений образующиеся в результате набухшие гели высококогезионны при отстутствии видимых отдельных частиц, например при отстутствии отдельных частиц, наблюдаемых невооруженным глазом. В предпочтительном воплощении гели не имеют визуально отдельными частицами при увеличении меньше чем 35Х.
Гели в настоящее время очищают при помощи обычных способов, таких как диализ или спиртовое осаждение, для выделения перекрестно-сшитого вещества для стабилизации pH вещества и для удаления любого непрореагировавшего перекрестно-сшивающего агента. Дополнительное количество воды или слегка щелочного водного раствора может быть добавлено для доведения концентрации NaГК в композиции к желаемому уровню.
pH очищенных, по существу рН-нейтральных перекрестно-сшитых гелей ГК предпочтительно доводят для того, чтобы гель стал слегка щелочным, таким образом, чтобы гели имели pH больше чем приблизительно 7,2, например от приблизительно 7,5 до приблизительно 8,0. Эта стадия может быть осуществлена при помощи любых подходящих способов, например путем добавления к гелям подходящего количества разведенной NaOH, KOH, NaHCO3или LiOH или любой другой щелочной молекулы, раствора и/или буферной композиции, известной специалистам в данной области техники.
Эффективное количество лидокаина, такого как лидокаин HCl, затем добавляют к очищенным когезионным гелям NaГК. Например в некоторых воплощениях лидокаин HCl получают в порошкообразной форме, которую солюбилизируют с использованием воды для инъекции (ВДИ). Гели сохраняют нейтральными при помощи буфера или путем доведения pH при помощи разведенной NaOH для того, чтобы конечная композиция ГК/лидокаин имела желаемый по существу нейтральный pH. Предпочтительно, конечные композиции наполнителя на основе ГК, включающие лидокаин, имеют концентрацию лидокаина от по меньшей мере приблизительно 0,1% до приблизительно 5%, например приблизительно 2 масс.% композиции, или в еще одном примере приблизительно 0,3%.
После добавления лидокаин HCl, или альтернативно, во время добавления лидокаин HCl, гели или композиции ГК/лидокаин гомогенизируют для получения высокогомогенных когезионных гелей ГК/лидокаин, обладающих желаемой целостностью и стабильностью. Предпочтительно, на стадии гомогенизации осуществляют смешивание, перемешивание или измельчение гелей с контролируемой силой сдвига с получением по существу гомогенных смесей.
Описанные в данном документе композиции ГК/лидокаин демонстрируют вязкость, которая зависит от свойств композиции и присутствия по меньшей мере одного обезболивающего агента. Вязкость композиции ГК/лидокаин может составлять от приблизительно 50 Па*с до приблизительно 450 Па*с. В других воплощениях вязкость может составлять от приблизительно 50 Па*с до приблизительно 300 Па*с, от приблизительно 100 Па*с до приблизительно 400 Па*с, или от приблизительно 250 Па*с до приблизительно 400 Па*с, или от приблизительно 50 Па*с до приблизительно 250 Па*с.
После гомогенизации композиции ГК/лидокаин вводят в шприцы и стерилизуют. Щприцы, полезные в соответствими с описанием настоящего изобретения, включают любой шприц, известный в области техники, который способен доставлять вязкие заполняющие кожу композиции. Шприцы как правило имеют внутренний объем от приблизительно 0,4 мл до приблизительно 3 мл, более предпочтительно от приблизительно 0,5 мл до приблизительно 1,5 мл или от приблизительно 0,8 мл до приблизительно 2,5 мл. Этот внутренний объем ассоциируется с внутренним диаметром шприца, который играет ключевую роль для силы выталкивания, необходимой для инъекции обладающих высокой вязкостью заполняющих кожу композиций. Внутренние диаметры как правило составляют от приблизительно 4 мм до приблизительно 9 мм, более предпочтительно от приблизительно 4,5 мм до приблизительно 6,5 мм или от приблизительно 4,5 мм до приблизительно 8,8 мм. Кроме того, силы выталкивания, необходимые для доставки композиции ГК/лидокаин из шприца, зависят от калибра иглы. Калибры обычно используемых игл включают калибры от приблизительно 18G до приблизительно 40G, более предпочтительно от приблизительно 25G до приблизительно 33G или от приблизительно 16G до приблизительно 25G. Специалист в данной области техники может определить правильные размеры шприца и калибр иглы, требующийся для достижения конкретных требований силы выталкивания.
Силы выталкивания, демонстрируемые описанными здесь композициями ГК/лидокаин, с использованием описанных выше размеров игл, достигаются при скоростях инъекций, которые комфортны для пациента. Термин комфортный для пациента используется для определения скорости инъекции, которая не повреждает или вызывает избыточную боль у пациента после инъекции в мягкую ткань. Специалисту в данной области техники понятно, что используемый здесь термин комфортабельный включает не только комфорт пациента, но также комфорт и способность лечащего врача или медицинского работника инъецировать композиции ГК/лидокаин. Хотя определенные силы выталкивания могут быть достигнуты с использованием композиций ГК/лидокаин, описанных в настоящем изобретении, специалисту в данной области техники понятно, что высокие силы выталкивания могут привести к утрате контроля во время инъекции, и что такая утрата контроля может привести в результате к дополнительной боли у пациента. Силы выталкивания композиций ГК/лидокаин по настоящему изобретению может составлять от приблизительно 8 H до приблизительно 15 H, или более предпочтительно от приблизительно 10 H до приблизительно 13 H, или от приблизительно 11 H до приблизительно 12 H.
Используемый в данном документе термин "стерилизация" включает любой способ, известный в области техники, который эффективно убивает или устраняет заразные агенты, предпочтительно по существу не изменяя деградацию композиций ГК/лидокаин.
Один из предпочтительных способов стерилизации заполненных шприцев осуществляют путем автоклавирования. Автоклавирование может быть осуществлено путем применения комбинации нагревания, давления и влажности к образцу, нуждающемуся в стерилизации. Множество различных температур стерилизации, давлений и времен цикла может быть использовано для этой стадии. Например, заполненные шприцы могут быть стерилизованы при температуре по меньшей мере от приблизительно 120°C до приблизительно 130°C или больше. Влажность может использоваться или не использоваться. Давление, применяемое в некоторых воплощениях в зависимости от температуры, используемой в способе стерилизации. Цикл стерилизации может составлять по меньшей мере от приблизительно 1 минуты до приблизительно 20 минут или больше.
Еще один способ стерилизации включает применение газообразных частиц, которые, как известно, убивают или устраняют заразные агенты. Предпочтительно этиленоксид используют в качестве стерилизующего газа и, как известно в области техники, полезен в стерилизации медицинских устройств и продуктов.
В еще одном способе стерилизации применяют источник излучения, который, как известно в области техники, убивает или устраняет заразные агенты. Пучок излучения направлен на шприц, содержащий раствор ГК/лидокаин, и длина волны энергии убивает или устраняет нежелаемые заразные агенты. Предпочтительная используемая энергия включает ультрафиолетовое (УФ), гамма излучение, видимый свет, микроволны или любая другая длина волны или пучок длин волн, которые убивают или устраняют нежелательные заразные агенты, предпочтительно по существу без изменения деградации композиции ГК/лидокаин.
Кроме того описаны способы получения основанных на ГК композиций, в общем при которых осуществляют стадии получения перекрестно-сшитого геля на основе ГК без обезболивающего средства (далее иногда геля-предшественника), доведения pH геля-предшественника с получением геля, имеющего pH от приблизительно 7,2 до 8,0, и добавления подходящего количества лидокаина или другого обезболивающего агента к гелю с приведенным pH с получением композиции на основе ГК, которая включает обезболивающий агент. В одном из воплощений гель-предшественник представляет собой высоко когезионный гель, содержащий не больше чем приблизительно 10 об.% свободной ГК. В еще одном воплощении гель предшественник представляет собой относительно менее когезионный гель, содержащий по меньшей мере от 10% до приблизительно 20 об.% свободной ГК.
Пример 1 Способ тестирования когезионности геля
Следующие тесты могут быть осуществлены для доказательства когезионности основанной на ГК гелевой композиции для задач настоящего описания.
Сначала 0,2 г или 0,4 г тестируемой гелевой композиции помещают в стеклянный шприц. Затем 0,2 г или больше фосфатного буфера добавляют в шприц и смесь тщательно перемешивают в течение приблизительно 1 часа с получением гомогенной смеси. Затем, гомогенизированную смесь центрифугируют в течение 5 мин при 2000 об./мин для удаления воздушных пузырьков и для того, чтобы обеспечить декантацию любых частиц. Шприц затем хранят в вертикальной позиции, и одну каплю красителя эозина размещают на поверхности геля при помощи шприца и иглы 18G. Через 10 мин краситель медленно диффундирует через гель.
После разбавления геля, гомогенизации и декантирования гель с относительно низкой когезионностью демонстрирует фазовое разделение (верхняя разбавленная менее вязкая фаза без частиц и нижняя фаза, состоящая из декантированных частиц, которые видны невооруженным глазом или под микроскопом). В тех же самых условиях высококогезионный гель демонстрирует по существу отсутствие фазового разделения, и предупреждается диффузия красителя в когезионную композицию. С другой стороны, относительно менее когезионный гель демонстрирует ясное разделение фаз.
Пример 2 Синтез наполнителя мягкой ткани с лидокаином
Волокна или порошок NaГК гидратируются в щелочном растворе, например водном растворе, содержащем NaOH. Смесь перемешивают при температуре окружающей среды, приблизительно 23°C, с образованием по существу гомогенного щелочного геля ГК.
Перекрестно-сшивающий агент БДДЭ разбавляют в водном растворе и добавляют к щелочному гелю ГК. Смесь гомогенизируют в течение нескольких минут.
Альтернативно, БДДЭ может быть добавлен непосредственно к волокнам ГК (сухое состояние) в начале процесса перед гидратацией. Реакция перекрестного сшивания затем начинает протекать относительно медленно при температуре окружающей среды, обеспечивая еще более хорошую гомогенность и эффективность перекрестного сшивания. Смотри, например, Piron et al., патент США №6921819, который включен в данный документ путем ссылки, как если бы он представлял собой часть настоящего описания.
Образующуюся в результате смесь перекрестно-сшитого геля ГК затем нагревают при приблизительно 50°C в течение приблизительно 2,5 часов. Материал представляет собой в высокой степени перекрестно-сшитый гель ГК/БДДЭ (аспект=твердый гель). Этот перекрестно-сшитый гель затем нейтрализуют подходящим кислым раствором. Нейтрализованный гель ГК затем набухает в фосфатном буфере при холодной температуре, например температуре приблизительно 5°C, с получением высоко когезионного геля ГК. В этом конкретном примере забуференный фосфатом физиологический раствор содержит воду для инъекции (ВДИ), двузамещенный фосфорнокислый натрий и монозамещенный фосфорнокислый натрий. После нейтрализации и набухания перекрестно-сшитый компонент ГК и вода, абсорбированная перекрестно-сшитым компонентом ГК, находятся в массовом отношении приблизительно 1:1.
Когезионный набухший гель ГК затем подвергают механическому перемешиванию и заполняют в диализные мембраны и подвергают диализу против фосфатного буфера. Гель ГК заполняют в диализные мембраны и подвергают диализу против фосфатного буфера в течение до нескольких дней с регулярными заменами ванны для удаления непрореагировавшего перекрестно-сшивающего агента для стабилизации pH, делая его близким к нейтральному (pH=7,2) и для обеспечения правильной осмолярности геля ГК. Осмолярность образующегося в результате когезионного геля ГК составляет от приблизительно 200 мОсмоль до приблизительно 400 мОсмоль, наиболее предпочтительно приблизительно 300 мОсмоль.
После диализа образующийся в результате когезионный гель ГК имеет по существу нейтральный pH, предпочтительно приблизительно 7,2, и отсутствие видимых частиц в жидких средах при наблюдении под увеличением меньше чем приблизительно 35Х.
Лидокаин хлоргидрат (лидокаин HCl) в порошковой форме сначала солюбилизируют в ВДИ и фильтруют через фильтр 0,2 мкм. Разведенный раствор NaOH добавляют к когезионному гелю ГК для достижения слегка основного pH (например, pH от приблизительно 7,5 до приблизительно 8). Раствор лидокаина HCl затем добавляют к слегка основному гелю для достижения конечной желаемой концентрации, например концентрации приблизительно 0,3% (масс). Достигаемая в результате pH смеси ГК/лидокаин затем составляет приблизительно 7 и концентрация ГК составляет приблизительно 24 мг/мл. Механическое перемешивание осуществляют для достижения подходящей гомогенности в стандартном реакторе, оборудованном соответствующим механизмом перемешивания.
Если желательно, то подходящее количество свободного геля ГК может быть добавлено к гелевой смеси ГК/лидокаин, обеспечивая преимущество, увеличивающее кинетику доставки лидокаина. Например, волокна свободной ГК набухают в фосфатном буферном растворе для получения гомогенного вязко-эластичного геля. Этот свободный гель ГК затем добавляют к перекрестно-сшитому гелю ГК/лидокаин (например, при приблизительно 5% масс). Образующийся в результате гель затем заполняют в готовые к заполнению стерильные шприцы и автоклавируют при достаточных температурах и давлениях для стерилизации в течение по меньшей мере приблизительно 1 минуты.
После автоклавирования конечный продукт ГК/лидокаин упаковывают и продают лечащим врачам. Продукт, изготовленный в соответствии с этим способом, демонстрирует одно или более чем одно определенное здесь свойство стабильности. Например, автоклавированный продукт ГК/лидокаин обладает вязкостью, когезионностью и силами выталкивания, которые являются приемлемыми. Никакой деградации гелевого продукта ГК/лидокаин не обнаруживают во время тестирования продукта после хранения продукта в течение нескольких месяцев.
Пример 3 Свойства наполнителей мягких тканей
Свойства композиций ГК/лидокаин, изготовленных в соответствии с описанными здесь способами, представлены в нижеприведенной Таблице 1. Например силы выталкивания измеряли с использованием INSTRON® Advanced Materials Testing System Model 5564 (Instron, Norwood, MA) с использованием программного обеспечения BLUEHILL® версия 2.11 (Instron, Norwood, MA).
Для обеспечения того, чтобы спецификации продукта поддерживались в течение срока годности композиции, проводили множество исследований. Дополнительно содержание 2,6-диметиланилина измеряли для подтверждения того, что деградация лидокаина отсутствует.
В Таблице 2 приведено обобщение результатов тестирования стабильности для композиций, изготовленных в соответствии с описанным в данном документе.
Обнаружено, что в момент 9 месяцев (с даты изготовления) композиция продолжает удовлетворять спецификациям продукта.
Пример 4 Кинетика высвобождения
В следующем примере проиллюстрирована кинетика высвобождения лидокаина из когезионных гелей ГК в соответствии с описанием настоящего изобретения. Задача Примера заключается в том, чтобы продемонстрировать то, что лидокаин, содержащийся в гелях ГК в соответствии с описанием настоящего изобретения, свободно высвобождается из гелей после введения в кожу.
Диализ осуществляли для различных периодов времени (приблизительно 10 г геля помещали в небольшой контейнер для диализа затем погружали в 30 г воды). После прекращения каждого диализа в заданный момент времени гель гомогенизировали при помощи шпателя, и количество лидокаина определяли при помощи УФ метода. Конечную концентрацию в ванне для диализа соответствовала теоретической концентрации лидокаина, что указывало на свободное высвобождение лидокаина из геля.
В Таблице 3 проиллюстрирована концентрация лидокаина в % (масс), корректировка значения и определение % высвобожденного лидокаина. Дополнительно, Фиг.9 графически иллюстрирует результаты, указанные в нижеприведенной Таблице 3. На Фиг.9 указана теоретическая равновесная концентрация лидокаина, которая может существовать в том случае, если лидокаин останется в геле или если он полностью высвободится. В соответствии с проиллюстрированным здесь графически данные свидетельствуют о том, что лидокаин свободно высвобождается из геля.
Фиг.1 демонстрирует, что профиль концентрации лидокаина в течение времени достигает равновесия, которое соответствует свободному высвобождению лидокаина. Препарат композиции на Фиг.1 представляет собой когезионный перекрестно-связанный гель ГК. Композиция имеет концентрацию ГК приблизительно 24 мг/мл, приблизительно 6% перекрестного связывания, G' приблизительно 170 и отношение ГК с высокой молекулярной массой к ГК с низкой молекулярной массой ГК от приблизительно 95% к 5% до приблизительно 100% высокомолекулярной ГК. Это исследование in vitro демонстрирует, что лидокаин свободно высвобождается из геля, а не задерживается в геле после имплантации.
Хотя изобретение описано и проиллюстрировано с некоторой степенью конкретики, понятно, что настоящее описание приведено только для примера, и что к многочисленным изменениям комбинаций и перегруппировок частей можно прибегнуть специалистам в данной области техники, не отступая от объема изобретения, как изложено далее.
Если не указано иное, то следует понимать, что все числа, выражающие количества ингредиентов, свойства, такие как молекулярная масса, условия реакции и т.д. используемые в описании и формуле изобретения модифицируемы во всех случаях термином "приблизительно." Соответственно, если не указано иное, то числовые параметры, приведенные выше в описании и в формуле изобретения, представляют собой приближения, которые могут варьировать в зависимости от желаемых свойств, которых пытаются достичь при помощи настоящего изобретения. Как минимум, и не будучи попыткой ограничить заявку на изобретение доктриной эквивалентов объему формулы изобретения, каждый числовой параметр следует по меньшей мере рассматривать в свете множества приведенных значимых цифр и путем применения обычных способов округления. Не смотря на то, что числовые диапазоны и параметры, приведенные в широком объеме изобретения, представляют собой приближения, числовые значения, представленные в конкретных примерах, приведены по возможности макимально точными. Тем не менее, любое числовое значение по своей природе содержит некоторые погрешности, обязательно возникающие в результате стандартного отклонения, обнаруживаемого в соответствующих им тестирующих измерениях.
Если здесь не указано иное или явно не противоречит по контексту, то термины "a," "an", "the" и близкие объекты ссылки, используемые в контексте описания изобретения (в особенности в контексте следующей формулы изобретения), следует рассматривать, как охватывающие единичное и множество. Перечисление здесь диапазонов значений всего лишь предназначено для того, чтобы служить как метод условного обозначения для индивидуальной ссылки на каждое отдельное значение, оказывающееся в пределах диапазона. Если здесь не указано иное, то каждое индивидуальное значение включено в описание таким образом, как если бы оно было здесь приведено индивидуально. Все описанные здесь способы могут быть осуществлены в любой подходящей последовательности, если не указано иное или явно не противоречит по контексту. Предполагается, что применение любого и всех примеров, или приведенных здесь иллюстративных оборотов (например, "такой как") служит лишь для более хорошего освещения изобретения и не накладывает ограничения на заявленный иным образом объем изобретения. Никакие обороты в описании не следует рассматривать как указывающие на какой-либо не заявленный элемент, необходимый для практической реализации изобретения.
Раскрытую в данном документе группировку альтернативных элементов или воплощений изобретения не следует рассматривать как ограничения. Каждый член группы может быть упомянут и заявлен индивидуально или в любой комбинации с другими членами группы или другими обнаруженными здесь элементами. Полагают, что один или более чем один член группы может быть включен в или исключен из группы по причинам удобства и/или патентоспособности. Когда возникает любое из таких включений или исключений, тогда описание по-видимому содержит модифицированную группу, таким образом удовлетворяя письменному описанию всех групп Маркуша, используемых в формуле изобретения.
В данном документе описаны некоторые воплощения этого изобретения, включающие наилучший известный авторам изобретения способ осуществления изобретения. Безусловно, вариации этих описанных воплощений понятны специалисту в данной области техники, при прочтении предшествующего описания. Автор изобретения ожидает, что специалист в данной области техники использует такие вариации как подходящие, и авторы изобретения предполагают, что изобретение может реализовываться на практике иначе, чем конкретно описано в данном документе. Соответственно, изобретение включает все модификации и эквиваленты объекта, перечисленные в формуле изобретения, которые допустимы в соответствии с действующим законодательством. Кроме того, изобретением охвачена любая комбинация вышеописанных элементов во всех возможных их вариациях, если здесь не указано иное или если иным образом не противоречит контексту.
Кроме того, многочисленные ссылки сделаны на патенты и печатные публикации в этом описании. Каждая из вышеприведенных ссылок и печатных публикаций индивидуально включена в данный документ путем ссылки.
Раскрытые в данном документе конкретные воплощения могут быть дополнительно ограничены в формуле изобретения с использованием оборотов "состоящий из" или/и "по существу состоящий из". Когда используется в формуле изобретения, как заявленный или как добавленный путем внесения изменений "состоящий из" исключает любой элемент, стадию или ингредиент, не указанный в формуле изобретения. Переходный термин "по существу состоящий из" огранивает объем формулы изобретения определенными материалами или стадиями и материалами и стадиями, которые материально не влияют на основные и новые характеристики. Заявленные таким образом воплощения изобретения по существу или прямо описаны и разрешены в данном документе.
В завершение, должно быть понятно, что раскрытые в данном документе воплощения изобретения представляют собой иллюстрации принципов настоящего изобретения. Другие модификации, которые могут быть использованы, находятся в объеме изобретения. Таким образом, в качестве примера, но не ограничения, альтернативные конфигурации настоящего изобретения могут быть использованы в соответствии с сущностью изобретения. Соответственно, настоящее изобретение не ограничивается теми, которые точно представлены и описаны.
Реферат
Изобретение относится к медицине. Описаны наполнители мягких тканей, например кожные и подкожные наполнители, основанные на гиалуроновых кислотах и их фармацевтически приемлемых солях. Описана композиция на основе гиалуроновой кислоты, которая включает терапевтически эффективное количество по меньшей мере одного обезболивающего агента, например лидокаина, а также дополнительно включает не сшитую перекрестно гиалуроновую кислоту. Композиция на основе гиалуроновой кислоты, включающая лидокаин, обладает улучшенной стабильностью по сравнению с обычными композициями, включающими лидокаин, например, будучи подверженными способам стерилизации или при хранении в течение длительных периодов времени. Также описаны способы получения композиций на основе гиалуроновой кислоты. 3 н. и 9 з.п. ф-лы, 1 ил., 3 табл., 4 пр.
Формула
получение компонента ГК (гиалуроновой кислоты), перекрестно сшитого с помощью по меньшей мере одного перекрестно сшивающего агента, выбранного из группы, состоящей из 1,4-бутандиолдиглицидильного эфира (БДДЭ), 1,4-бис(2,3-эпоксипропокси)бутана, 1,4-бисглицидилоксибутана, 1,2-бис(2,3-эпоксипропокси)этилена и 1-(2,3-эпоксипропил)-2,3-эпоксициклогексана или их комбинаций; где компонент ГК дополнительно включает не сшитую перекрестно ГК в концентрации по меньшей мере примерно 10% от массы компонента ГК, доведение pH указанного компонента ГК до pH больше приблизительно 7,2; и
добавление раствора, содержащего по меньшей мере один обезболивающий агент, к указанному компоненту ГК, имеющему указанный доведенный pH, с получением композиции наполнителя мягких тканей на основе ГК.
получение сухого не сшитого перекрестно вещества NaГК и гидратирование указанного сухого не сшитого перекрестно вещества NaГК в щелочном растворе с получением щелочного не сшитого перекрестно геля NaГК;
перекрестное сшивание указанного не сшитого перекрестно геля NaГК с БДДЭ с образованием перекрестно сшитой щелочной композиции ГК со степенью перекрестного сшивания менее 5% и pH выше приблизительно 7,2;
добавление по меньшей мере 10% не сшитой перекрестно ГК от массы композиции;
добавление раствора, содержащего лидокаин HCl, к указанному компоненту ГК, имеющему указанный доведенный pH, с получением указанной композиции наполнителя на основе ГК;
гомогенизация указанной композиции наполнителя на основе ГК с получением гомогенизированной композиции наполнителя на основе ГК и
стерилизация указанной гомогенизированной композиции наполнителя на основе ГК с получением стерилизованной композиции наполнителя на основе ГК;
Документы, цитированные в отчёте о поиске
Способ получения содержащих альгинат пористых формованных изделий

Комментарии