Композиция, включающая экзосому, полученную из стволовых клеток, для индукции адипогенной дифференцировки, регенерации жировой ткани, отбеливания кожи или коррекции морщин - RU2710373C2
Код документа: RU2710373C2
Чертежи























Описание
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к композиции для индукции дифференцировки стволовых клеток в адипоциты и/или регенерации жировых тканей с использованием экзосомы, полученной из стволовых клеток, содержащей вещество, индуцирующее дифференцировку в адипоциты. Кроме того, настоящее изобретение относится к косметической композиции для отбеливания кожи, коррекции морщин или регенерации кожи, содержащей экзосому, полученную из стволовых клеток.
УРОВЕНЬ ТЕХНИКИ
В качестве терапевтического способа регенерации жировых тканей существует способ применения терапевтического агента, содержащего стволовые клетки, которые культивируют в матриксе, содержащем гидрогель и позволяющем трехмерный рост клеткам жировой ткани. После культивирования ткани в гидрогеле, позволяющем трехмерный рост, клетки могут начать выделять фактор роста и внеклеточный матрикс. Тем не менее, для применения терапевтического агента в инъекционной форме затруднительно удалять гидрогель, имеющий вид пленки, из контейнера для культивирования и обрабатывать ткань лиазами. Для преодоления этих трудностей был разработан терапевтический способ регенерации тканей путем трансплантации собственной жировой ткани или прямой трансплантации стволовых клеток.
В случае трансплантации собственной жировой ткани в способе используют части тела оперируемого субъекта. Следовательно, способ не вызывает проблем, связанных с иммунным отторжением тканей, и иммунный ответ не наблюдается. Тем не менее жировая ткань высоко зависима от кислорода и взаимодействует с соседними клетками, обладая при этом большим количеством окружающих кровяных сосудов. Трансплантированная жировая ткань практически неспособна образовывать кровеносные сосуды, и поэтому этот способ имеет недостатки. Например, по причине гипоксии может быть вызван клеточный апоптоз или клеточный некроз, и субъекту может потребоваться несколько процедур, так как степень приживления трансплантата невелика.
Ранее стволовые клетки часто использовались для восстановления поврежденных при хирургической операции или медикаментозном лечении тканей. Например, для трансплантации стволовых клеток используют биополимеры, такие как гиалуроновая кислота и коллаген. Так как стволовые клетки могут дифференцироваться в различные клетки, включая адипоциты, такие стволовые клетки имеют широкий диапазон применений. Тем не менее, так как уровень выживаемости и степень приживления трансплантата при помещении клеток в организм являются низкими, эффективность снижается. Также существует риск того, что недиффиренцированные стволовые клетки могут образовывать опухоли.
В настоящее время способ дифференцировки стволовых клеток в адипоциты для регенерации тканей в общем включает обработку стволовых клеток материалами, индуцирующими дифференцировку, такими как инсулин, дексаметазон, изобутилметилксантин и т.д., и их культивирование в течение длительного времени. Тем не менее, вышеперечисленные материалы, индуцирующие дифференцировку стволовых клеток, являются дорогими и неэффективны при дифференцировке только одним составляющим. Таким образом, они имеют недостатки. Например, их необходимо обрабатывать смесью различных веществ, и эффективность клеточной дифференцировки является низкой. Это вызывает трудности.
С другой стороны, известны попытки использовать культуральный раствор, полученный при культивировании стволовых клеток, в качестве косметического средства. Обычно для культивирования стволовых клеток используют культуральную среду, содержащую необходимое для роста количество антибиотиков и сыворотки. В большинстве культуральных растворов стволовых клеток, используемых в качестве косметических композиций, используют нормальную культуральную среду, а косметическая композиция включает липосомы, заключающие в себя культуральный раствор стволовых клеток (см. корейские патенты №1237430; 1047873). Кроме того, была разработана косметическая композиция, в которой используют культуральную среду, полученную без составляющих, не разрешенных в качестве исходных ингредиентов для косметических средств, и косметическая композиция, содержащая бессывороточную культуральную среду, и тому подобные (см. корейские патенты №1413686; 1108847).
Культуральные среды представляют собой вещества, содержащие белки, аминокислоты, гормоны и факторы роста для клеточной пролиферации. Среды получают очень технически сложным путем и поставляют. Однако, поскольку клеточная культуральная среда, антибиотики и сыворотка имеют риски и не признаны безопасными, они следует использовать только в исследовательских целях, и их применение в отношении организма человека запрещено. Компоненты, включенные в культуральную среду, такие как холинхлорид, натриевая соль гипоксантина, тимидин, путресцин дигидрохлорид, азотнокислое железо, L-глютамин и тому подобные, не разрешены в качестве исходных ингредиентов для косметических композиций. Следовательно, использование такой культуральной среды не подходит для целей косметической композиции. Как таковая, культуральная среда содержит различные белки, цитокины, факторы роста и тому подобные, выделяемые стволовыми клетками. Напротив, они также содержат компоненты, такие как продукты отходов, выделяемые во время роста клеток, антибиотики, добавляемые для предотвращения заражения, или сыворотка животных, и т.д. Следовательно, они обладают высокой вероятностью вызывать различные риски при применении на коже.
Компоненты культуральных растворов стволовых клеток, подходящие для применения в косметической области, ограничены. Кроме того, во время заключения в липосомы возможны повреждения составляющих культурального раствора и его заражение, и поэтому требуется дополнительная обработка культурального раствора при заключении в липосомы. Следовательно, техника заключения культуральных растворов стволовых клеток в липосомы, включая использование липидов для увеличения скорости абсорбции культуральных растворов кожей, имеет свои ограничения при использовании в косметической области.
Чтобы восполнить недостатки данных культуральных растворов стволовых клеток, были разработаны техники применения экзосом, полученных из стволовых клеток. Стволовые клетки обычно культивируют в среде, содержащей антибиотики и сыворотку. Био-наночастицы, выделяемые различными клетками и присутствующие в многоклеточных организмах, включая человека, могут быть классифицированы на экзосомы и микровезикулы в зависимости от их размера и различий в секреторном механизме. Известно, что экзосомы, представляющие собой везикулы с мембранной структурой, выделяемые различными типами клеток, играют различные роли. Например, их роли включают перенос компонентов мембраны, белков, РНК, и т.д., путем связывания с другими клетками и тканями. Большинство секретом, включая экзосомы, получают из супернатанта клеточных культур. Следовательно, в условиях используемого в настоящее время способа выделения полученных из клеток экзосом сложно полностью очищать экзосомы по причине присутствия белков в среде или сыворотке на стадии выделения секретом, включая экзосомы.
Соответственно, авторы настоящего изобретения выделили экзосомы из стволовых клеток и обнаружили, что экзосомы, полученные из стволовых клеток, обладают эффектами дифференцировки стволовых клеток, регенерации жировой ткани, отбеливания, коррекции морщин и регенерации кожи.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Одним из аспектов настоящего изобретения является получение композиции для индукции дифференцировки в адипоциты или регенерации жировых тканей. Композиция может в качестве активного ингредиента включать экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты.
Другим аспектом настоящего изобретения является получение косметической композиции, содержащей композицию для индукции дифференцировки в адипоциты или регенерации жировых тканей. Косметическая композиция в качестве активного ингредиента может включать экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты.
Еще одним аспектом настоящего изобретения является получение композиции среды для индукции дифференцировки в адипоциты или регенерации жировых тканей. Композиция среды в качестве активного ингредиента может включать экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты.
Еще одним аспектом настоящего изобретения является получение инъекционной формы препарата, содержащей композицию для индукции дифференцировки в адипоциты или регенерации жировых тканей. Инъекционная форма препарата в качестве активного ингредиента может включать экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты, и гидрогель.
Еще одним аспектом настоящего изобретения является получение косметической композиции для отбеливания кожи, коррекции морщин или регенерации кожи. Косметическая композиция в качестве активного ингредиента может включать экзосому, полученную из пролиферирующих стволовых клеток.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном варианте осуществления настоящего изобретения предложена композиция для индукции дифференцировки в адипоциты или регенерации жировых тканей. Композиция в качестве активного ингредиента может включать экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты.
При использовании в настоящем описании «стволовые клетки, дифференцирующиеся в адипоциты» относятся к стволовым клеткам, дифференцирующимся в адипоциты, например, из стволовых клеток, полученных из жировой ткани (ASC). Пример стволовых клеток, полученных из жировой ткани, представлен на Фиг. 1. Из них могут быть выделены экзосомы, содержащие генетическую информацию, белки и факторы роста.
В частности, когда стволовые клетки дифференцируются в адипоциты, их формы явственно меняются, и в этот момент выделяют экзосомы. Следовательно, это отличается от выделения экзосом из недифференцированных стволовых клеток.
Экзосомы относятся к полученным из клеток коммуникационным везикулам, содержащим клеточно-специфические компоненты, играющие роль в межеклеточной коммуникации путем слияния с клеткой-получателем. В одном из вариантов осуществления экзосомы имеют эндоцитозное происхождение и представляют собой везикулы, вовлеченные в межклеточную коммуникацию, выделяемые клеткой и содержащие клеточно-специфические компоненты, такие как липиды, генетический материал и белки.
Экзосомы могут быть получены способом выделения экзосом, известным в области техники, или посредством следующих стадий, например, 1) культивирования стволовых клеток в культуральной среде, и затем субкультивирования в бессывороточной и не содержащей антибиотиков среде; 2) сбора супернатанта клеточной культуры; 3) центрифугирования собранного супернатанта клеточной культуры; и 4) отделения и очистки экзосом, но не ограничиваясь им.
Стволовые клетки, дифференцирующиеся в адипоциты, могут представлять собой стволовые клетки костного мозга, стволовые клетки пуповинной крови или стволовые клетки, полученные из жировой ткани, и могут представлять собой стволовые клетки, полученные у человека, животных или растений, но не ограничиваясь перечисленным.
Экзосомы могут добавляться к стволовым клеткам в концентрации от 1 до 150 мкг на 1 мл композиции для индукции дифференцировки в адипоциты или регенерации жировых тканей, конкретнее, в концентрации от 5 до 150 мкг, более конкретно, в концентрации от 10 до 150 мкг, даже более конкретно, в концентрации от 20 до 130 мкг, и еще более конкретно, в концентрации от 20 до 100 мкг, но не ограничиваясь перечисленным.
При использовании в настоящем описании, термин «индукция дифференцировки в адипоциты» относится к индукции стволовых клеток к дифференцировке в адипоциты.
Композиция в качестве активного ингредиента может включать экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты в соответствии с одним из вариантов осуществления настоящего изобретения. Композиция способна дифференцировать стволовые клетки в адипоциты. Следовательно, композиция может использоваться в качестве композиции для индукции дифференцировки в адипоциты.
При использовании в настоящем описании термин «регенерация жировых тканей» относится к регенерации жировых тканей путем восстановления поврежденных жировых тканей или стимуляции развития недостающих жировых тканей.
Кроме того, композиция способна регенерировать жировые ткани. Следовательно, композиция может использоваться в качестве композиции для регенерации жировых тканей.
Композиция для индукции дифференцировки в адипоциты или регенерации жировых тканей в соответствии с другим вариантом осуществления настоящего изобретения может использоваться в качестве фармацевтической композиции. В частности, фармацевтическая композиция может содержаться в количестве от 0,001 до 10 масс. частей из расчета на 100 масс. частей всей композиции.
Фармацевтическая композиция в соответствии с вышеприведенным вариантом осуществления может быть в виде различных пероральных или парентеральных лекарственных форм. Лекарственные формы могут быть изготовлены с использованием разбавителя или вспомогательного вещества, такого как общепринятые наполнители, утяжелители, связывающие вещества, смачивающие вещества, разрыхлители, поверхностно-активные вещества и тому подобные. Твердые лекарственные формы для перорального введения включают таблетки, пилюли, порошки, гранулы, капсулы и тому подобные. Такие твердые лекарственные формы могут быть получены путем смешивания по меньшей мере одного соединения с по меньшей мере одним вспомогательным веществом, например, крахмалом, карбонатом кальция, сахарозой или лактозой, желатином и тому подобными. Помимо простых вспомогательных веществ, могут быть использованы смазочные вещества, такие как стеарат магния, тальк и тому подобные. Жидкие лекарственные формы для перорального введения включают суспензию, жидкость для приема внутрь, эмульсию, сироп и тому подобные. Помимо общепринятых простых разбавителей, таких как вода и жидкий парафин, жидкие лекарственные формы могут также включать различные вспомогательные вещества, например, смачивающие вещества, подсластители, вкусовые добавки, консерванты и тому подобные. Лекарственные формы для парентерального введения включают стерильные водные растворы, неводные растворители, суспензии, эмульсии, лиофилизированные лекарственные формы и суппозитории.
Для фармацевтической композиции в соответствии с вышеприведенным вариантом осуществления в качестве неводных растворителей и суспендирующих агентов могут быть использованы растительное масло, такое как пропиленгликоль, полиэтиленгликоль и оливковое масло, и инъекционный эфир, такой как этилолеат и тому подобные. В качестве основы для суппозитория могут использоваться Витепсол, макрогол, твин 61, какао-масло, лаурин, глицерин, желатин и тому подобные.
Лекарственные формы фармацевтической композиции в соответствии с вышеприведенным вариантом осуществления могут быть в любой фармацевтически приемлемой форме, или она может быть использована в отдельности или в подходящей комбинации с другими фармацевтически активными соединениями. Соль соединения экзосомы не ограничена конкретно при условии, что они являются фармацевтически приемлемыми. Соль включает, например, соли соляной кислоты, серной кислоты, азотной кислоты, фосфорной кислоты, фтороводородной кислоты, бромводородной кислоты, муравьиной кислоты, уксусной кислоты, винной кислоты, молочной кислоты, лимонной кислоты, фумаровой кислоты, яблочной кислоты, янтарной кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты, толуолсульфоновой кислоты, нафталинсульфоновой кислоты и тому подобные.
Фармацевтическая композиция в соответствии с вышеприведенным вариантом осуществления может вводиться парентерально или перорально, в зависимости от назначения, и может вводиться один раз или несколько раз в сутки, по мере необходимости, таким образом, чтобы вводимое количество составляло от 0,1 до 500 мг, от 1 до 100 мг на кг. Эффективная дозировка для конкретного пациента различается в зависимости от массы тела пациента, возраста, пола, состояния здоровья, режима питания, периода введения, режима введения, скорости экскреции, тяжести заболевания и тому подобного.
В соответствии с общепринятым способом, фармацевтические композиции в соответствии с вышеприведенными вариантами осуществления могут быть использованы путем выполнения их в любой форме, подходящей для лекарственной формы, включающей пероральные композиции, такие как порошки, гранулы, таблетки, капсулы, суспензии, эмульсии, сиропы, аэрозоли и тому подобные, препараты для наружного применения, такие как мази, кремы и тому подобные, суппозитории и стерилизованные инъекционные растворы.
Фармацевтические композиции в соответствии с вышеприведенными вариантами осуществления могут быть введены млекопитающим, таким как крысы, мыши, сельскохозяйственные животные, люди и тому подобные, используя различные пути, такие как парентеральный, пероральный и тому подобные, и, хотя можно предполагать все пути введения, предпочтительно они могут быть введены перорально, ректальной или внутривенной, внутримышечной, подкожной, внутриматочной или интрацеребровентрикулярной инъекцией.
Фармацевтическая композиция для индукции дифференцировки в адипоциты или регенерации жировых тканей может дополнительно включать материалы, индуцирующие дифференцировку, такие как инсулин, дексаметазон, дегидроэпиандростерон (ДГЭА), гистамин и изобутилметилксантин, и т.д., для дифференцировки стволовых клеток в адипоциты, но не ограничиваясь перечисленным.
В другом варианте осуществления настоящего изобретения предложена косметическая композиция для индукции дифференцировки в адипоциты или регенерации жировых тканей, которая может включать в качестве активного ингредиента экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты. Косметическая композиция может стимулировать регенерацию жировых тканей путем индукции дифференцировки в адипоциты.
Экзосомы могут содержаться в косметической композиции в концентрации от 1 до 150 мкг на 1 мл косметической композиции, конкретнее, в концентрации от 5 до 150 мкг, более конкретно, в концентрации от 10 до 150 мкг, даже более конкретно в концентрации от 20 до 130 мкг, и еще более конкретно в концентрации от 20 до 100 мкг, но не ограничиваясь перечисленным.
Косметическая композиция в соответствии с вышеуказанным вариантом осуществления может содержать адъюванты, общепринятые в косметологии или дерматологии, такие как жировые вещества, органические растворители, солюбилизаторы, загустители, желирующие агенты, смягчители, антиоксиданты, суспендирующие агенты, стабилизаторы, пенообразующие агенты, отдушки, поверхностно-активные вещества, воду, ионогенные или неионогенные эмульгаторы, наполнители, связывающие агенты, хелатообразующие агенты, консерванты, витамины, блокаторы, смачивающие вещества, эфирные масла, красители, пигменты, гидрофильные или липофильные активные агенты, липидные везикулы или любой другой ингредиент, общепринятый в косметике. Такие адъюванты добавляют в количествах, общепринятых в косметической или дерматологической областях.
Внешняя форма косметической композиции в соответствии с вышеуказанным вариантом осуществления содержит косметически или дерматологически приемлемую среду или основание. Косметическая композиция может быть в любой форме, подходящей для наружного применения. Например, косметическая композиция может быть выполнена в форме растворов, гелей, твердых веществ, пасты, безводных продуктов, эмульсий, полученных диспергированием масляной фазы в водной фазе, суспензий, микроэмульсий, микрокапсул или ионогенных (липосомы) и неионогенных диспергирующих везикулы агентов, и эти композиции могут быть изготовлены в соответствии с общепринятым в области техники способом.
Косметическая композиция в соответствии с вышеприведенным вариантом осуществления предпочтительно применяют в форме, абсорбируемой кожей, с использованием микроиглы и т.д., но не ограничиваясь этим.
Косметическая композиция для индукции дифференцировки в адипоциты или регенерации жировых тканей может включать в качестве активного ингредиента экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты. Косметическая композиция может дополнительно включать материалы, индуцирующие дифференцировку, такие как инсулин, дексаметазон, дегидроэпиандростерон (ДГЭА), гистамин и изобутилметилксантин, и т.д., для дифференцировки стволовых клеток в адипоциты, но не ограничиваясь перечисленным.
В еще одном варианте осуществления настоящего изобретения предложена композиция среды для дифференцировки стволовых клеток, содержащая экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты, и индуцирующая дифференцировку стволовых клеток в адипоциты.
Экзосома может содержаться в композиции среды для дифференцировки стволовых клеток в концентрации от 1 до 150 мкг на 1 мл композиции среды для дифференцировки стволовых клеток, конкретнее, в концентрации от 5 до 150 мкг, более конкретно в концентрации от 10 до 150 мкг, даже более конкретно в концентрации от 20 до 130 мкг, и еще более конкретно в концентрации от 20 до 100 мкг, но не ограничиваясь перечисленным.
Композиция среды для дифференцировки стволовых клеток может дополнительно включать культуральную среду стволовых клеток, но не ограничиваясь этим.
Композиция среды для дифференцировки стволовых клеток может дополнительно включать материалы, индуцирующие дифференцировку, такие как инсулин, дексаметазон, дегидроэпиандростерон (ДГЭА), гистамин и изобутилметилксантин, и т.д., для дифференцировки стволовых клеток в адипоциты, но не ограничиваясь перечисленным.
В еще одном варианте осуществления настоящего изобретения предложена инъекционная форма препарата, содержащая композицию для индукции дифференцировки в адипоциты или регенерации жировых тканей. Инъекционная форма препарата в качестве активного ингредиента может включать экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты; и гидрогель.
Экзосома может содержаться в инъекционной форме препарата в концентрации от 1 до 150 мкг на 1 мл, конкретнее, в концентрации от 5 до 150 мкг, более конкретно в концентрации от 10 до 150 мкг, даже более конкретно в концентрации от 20 до 130 мкг, и еще более конкретно в концентрации от 20 до 100 мкг, но не ограничиваясь перечисленным.
Гидрогель может представлять собой по меньшей мере один гидрогель, такой как желатин, альгинат, хитозан, фибрин, эластин, гиалуроновая кислота, коллаген, метилцеллюлоза, или гидрогель на основе коллагена и метил целлюлозы, но не ограничиваясь перечисленным.
Инъекционная форма препарата может представлять собой инъекционную форму препарата для индукции дифференцировки в адипоциты или регенерации жировых тканей, но не ограничиваясь перечисленным. То есть при введении инъекционной формы препарата по настоящему изобретению животному посредством инъекции могут проявляться эффекты индукции дифференцировки в адипоциты или регенерации жировых тканей.
В одном из вариантов осуществления настоящего изобретения гидрогель был получен путем добавления порошка метилцеллюлозы к раствору коллагена. А именно, порошок метилцеллюлозы добавляли к раствору коллагена в 0,02 Н уксусной кислоте с концентрацией 3 мг/мл, так что конечная концентрация метилцеллюлозы составила 6 масс. %. Затем смесь перемешивали при 4°C в течение 1 часа с получением гидрогеля на основе коллагена и метилцеллюлозы.
В одном из вариантов осуществления настоящего изобретения инъекционная форма препарата была получена путем внесения экзосом, полученных из стволовых клеток, дифференцирующихся в адипоциты, в гидрогель на основе коллагена и метилцеллюлозы. А именно, экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты, вносили в гидрогель до конечной концентрации 50 мкг/мл, и затем диспергировали в гидрогеле путем раскапывания пипеткой.
Инъекционная форма препарата в соответствии с вышеприведенным вариантом осуществления может быть введена млекопитающим, таким как крысы, мыши, сельскохозяйственные животные, люди и тому подобные, перорально, ректальной или внутривенной, внутримышечной, подкожной, внутриматочной или интрацеребровентрикулярной инъекцией.
В одном из вариантов осуществления настоящего изобретения экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты, в сравнении с экзосомами, полученными из пролиферирующих стволовых клеток, демонстрируют превосходный уровень экспрессии биоактивных факторов, оказывающих воздействие на дифференцировку в адипоциты (Фиг. 4 и 5).
В другом варианте осуществления настоящего изобретения в эксперименте по дифференцировке стволовых клеток в адипоциты добавляли экзосому, полученную из стволовых клеток, дифференцирующихся в адипоциты, в соответствии с настоящим изобретением, к экзосоме, полученной из пролиферирующих стволовых клеток, в качестве контроля. На этих примерах было подтверждено, что при использовании экзосом в соответствии с настоящим изобретением адипоциты дифференцировали на уровне, схожим с уровнем для стволовых клеток, культивируемых в дифференцирующей среде, на седьмой день, и, соответственно, синтезировали жиры. Однако для стволовых клеток, обработанных экзосомами, полученными из пролиферирующих стволовых клеток, было подтверждено, что эти стволовые клетки только пролиферировали, без дифференцировки в адипоциты (Фиг. 6 и 7).
В еще одном варианте осуществления настоящего изобретения инъекционная форма препарата, в которой экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты в соответствии с настоящим изобретением, находились в гидрогеле на основе коллагена/метилцеллюлозы, продемонстрировала превосходный эффект в отношении регенерации жировых тканей по сравнению с инъекционной формой препарата, переносимой экзосомами, полученными из пролиферирующих стволовых клеток (Фиг. 9 и 10).
Композиция для дифференцировки стволовых клеток и регенерации жировой ткани в соответствии с вышеприведенным вариантом осуществления включает экзосомы, содержащие генетическую информацию, белки и факторы роста адипоцитов, связанные с дифференцировкой в адипоциты. Следовательно, композиция может эффективно использоваться для дифференцировки стволовых клеток, так как нет необходимости добавлять сложные и различные факторы роста для дифференцировки. Стволовые клетки дифференцируются в адипоциты посредством экзосом, полученных из стволовых клеток, дифференцирующихся в адипоциты по настоящему изобретению, оказывая таким образом положительный эффект на регенерацию жировых тканей при применении in vivo. Экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты по настоящему изобретению представляют собой материал, полученный из клеток, и поэтому являющийся биологически совместимым, что минимизирует побочные эффекты существующих агентов для клеточной терапии. Кроме того, экзосома сама по себе может выполнять роль носителя, что облегчает применение компонентов, переносимых ей, в организме человека. Таким образом, экзосома может применяться в качестве стимулятора дифференцировки клеток, инъекционной формы препарата для регенерации тканей, наполнителя для косметических целей, препарата для тканевой инженерии и тому подобного.
В другом варианте осуществления настоящего изобретения предложена косметическая композиция, содержащая в качестве активного ингредиента экзосому, полученную из стволовых клеток, и более конкретно, косметическая композиция для отбеливания кожи, коррекции морщин или регенерации кожи, содержащая в качестве активного ингредиента экзосому, полученную из стволовых клеток.
Экзосома, полученная из стволовых клеток в бессывороточной, не содержащей антибиотиков среде, содержит производные внеклеточного матрикса, а также коллаген и факторы роста, которые эффективны для регенерации кожи и могут, следовательно, эффективно применяться для улучшения состояния кожи.
В вышеприведенном варианте осуществления термин «стволовые клетки» относится к пролиферирующим стволовым клеткам. Из них возможно выделение экзосом, содержащих генетическую информацию стволовых клеток, белки и факторы роста.
Стволовые клетки могут представлять собой стволовые клетки костного мозга, стволовые клетки пуповинной крови или стволовые клетки, полученные из жировой ткани, и могут представлять собой стволовые клетки человека, животных или растений, но не ограничиваясь перечисленным.
При использовании в настоящем описании термин «стволовые клетки, полученные из жировой ткани человека» относится к стволовым клеткам, полученным из адипоцитов человека. Из них возможно выделение экзосом, содержащих генетическую информацию, белки и факторы роста стволовых клеток.
Способ выделения экзосом может осуществляться посредством любого известного в области техники способа, но не ограничиваясь им. В одном из вариантов осуществления настоящего изобретения экзосомы выделяли во время процесса субкультивирования стволовых клеток, полученных из жировой ткани человека. А именно, стволовые клетки, полученные из жировой ткани человека (пассажи 3-7), культивировали в нормальной культуральной среде (среда Игла, модифицированная Дульбекко, ДМЕМ, содержащая 10% фетальной бычьей сыворотки, 1% пенициллина/стрептомицина). Затем за 24 часа до выделения экзосом клеточную культуральную среду заменяли средой ДМЕМ, представляющей собой бессывороточную и не содержащую антибиотиков среду, не содержащую фенолового красного, и затем выдерживали в течение 24 часов. По истечении 24 часов супернатант клеточной культуры собирали. Собранный супернатант клеточной культуры центрифугировали при 300×g в течение 10 минут для удаления клеток, и затем центрифугировали при 2000×g в течение 30 минут для удаления продуктов выделения клеток. Затем клетки концентрировали путем центрифугирования при 5000×g в течение 60 минут с помощью центрифужной пробирки, оборудованной фильтром, задерживающим молекулы, имеющие молекулярную массу 3000. Супернатант, полученный после концентрирования, смешивали с реагентом для выделения экзосом в соотношении 1:0,5 и хранили при 4°C в течение одних суток. Получали экзосомальный осадок центрифугированием при 10000×g в течение 60 минут, затем фильтровали через 0,22 мкм фильтр и промывали натрий-фосфатным буфером (PBS). Промытый экзосомальный осадок центрифугировали при 10000×g в течение 60 минут и ресуспендировали в PBS (Фиг. 1). После сбора супернатанта к стволовым клеткам добавляли нормальную культуральную среду и культивировали. Эту процедуру повторяли до седьмого пассажа стволовых клеток. Косметическую композицию получали с использованием экзосом, выделенных во время процесса пролиферации стволовых клеток до седьмого пассажа.
Экзосома может содержаться в концентрации от 1 до 150 мкг на 1 мл косметической композиции в косметической композиции для отбеливания кожи, коррекции морщин или регенерации, конкретнее, в концентрации от 5 до 150 мкг, более конкретно в концентрации от 10 до 150 мкг, даже более конкретно в концентрации от 20 до 130 мкг, и еще более конкретно в концентрации от 20 до 100 мкг, но не ограничиваясь перечисленным.
В одном варианте осуществления настоящего изобретения экзосомы, полученные из стволовых клеток жировой ткани человека, использовались в концентрации, составляющей 10, 30 или 50 мкг/мл. Кроме того, были подтверждены превосходное заживление ран у фибробластов крайней плоти человека (Фиг. 18), превосходный уровень синтеза коллагена (Фиг. 19) и снижение синтеза меланина (Фиг. 20).
Экзосома может содержаться в косметической композиции в форме липосомы, заключающей в себя экзосому, путем заключения экзосомы в липосому, но не ограничиваясь этим. В некоторых вариантах осуществления экзосома может находиться в любой форме, при условии что она подходит для использования в косметической композиции. Также возможно использовать экзосому самостоятельно, без ее заключения в липосому.
Когда экзосому используют в форме, заключенной в липосому, экзосома может содержаться в количестве от 0,1 до 10,0 масс. %, более конкретно в количестве от 0,1 до 1,0 масс. % относительно общей массы липосомы, но не ограничиваясь перечисленным.
Липосома, заключающая экзосому, может содержаться в количестве от 0,001 до 10,0 масс. %, конкретнее, в количестве от 0,001 до 1,0 масс. %, более конкретно в количестве от 0,01 до 1,0 масс. %, и еще более конкретно в количестве от 0,01 до 0,1 масс. % относительно общей массы всей косметической композиции, но не ограничиваясь перечисленным.
В одном из вариантов осуществления настоящего изобретения 3 масс. % лецитина диспергировали в водной фазе, содержащей 0,01 масс. % экзосом, полученных из стволовых клеток, при комнатной температуре (например, 15°C), а затем образовывали эмульсию с обратными мицеллами (вода/диоксид углерода, полученный при низкой температуре) с использованием сверхкритического диоксида углерода. Затем реакцию останавливали и испаряли сверхкритический диоксид углерода при пониженном давлении для удаления фазы сверхкритического диоксида углерода, получая таким образом полученную при низкой температуре суспензию липосом, заключающих в себя экзосомы. Косметическая композиция была получена таким образом, что полученные липосомы, заключающие в себя экзосомы, содержались в количестве 5 масс. % относительно общей массы всей косметической композиции.
В общепринятой технологии использовали культуральный раствор, полученный во время культивирования стволовых клеток, полученных из жировой ткани человека. Однако вышеприведенный вариант осуществления отличается от нее тем, что экзосому в виде нано-везикулы, присутствующую в культуральном растворе, выделяют и очищают для применения в качестве косметического ингредиента, без применения культурального раствора как такового. Когда экзосомы стволовых клеток выделяют и очищают, связанные с регенерацией белки, коллагеновые производные и различные факторы роста, содержащиеся в экзосомах, могут быть эффективно использованы таким образом, что они исключают вмешательство компонентов среды. Следовательно, проблемы, вызываемые компонентами среды, включая антибиотики и сыворотку, могут быть решены.
Экзосома в соответствии с вышеприведенным вариантом осуществления содержит генетическую информацию, белки и факторы роста стволовых клеток, и экзосома сама по себе может служить в качестве носителя. Экзосома, состоящая из липидов размером приблизительно от 50 до 150 нм, является биологически совместимой, так как представляет собой материал, полученный из клетки, и имеет высокую степень абсорбции клетками. Следовательно, она обладает теми преимуществами, что в отличие от общепринятой технологии не требует дополнительных процессов для заключения культурального раствора в липосому, а также она может быть легко применяться на коже.
Кроме того, косметическая композиция, содержащая экзосомы, полученные из стволовых клеток в соответствии с вышеприведенным вариантом осуществления, может использоваться в качестве препарата для улучшения внешнего вида шрамов. Поскольку полученные из стволовых клеток экзосомы содержат белки и факторы роста, индуцирующие пролиферацию и дифференцировку, а также регенерацию кожи, они могут применяться к старым ранам и постугревым рубцам для уменьшения образования рубцов или улучшения их внешнего вида. Следовательно, при использовании в качестве препарата для коррекции рубцовой ткани, она может применяться в форме спреев, гелевых мазей и пластырей, содержащих экзосому, полученную из стволовых клеток, и т.д.
Кроме того, в еще одном варианте осуществления настоящего изобретения предложена фармацевтическая композиция, содержащая в качестве активного ингредиента экзосому, полученную из стволовых клеток, более конкретно, фармацевтическая композиция для регенерации кожи, содержащая в качестве активного ингредиента экзосому, полученную из стволовых клеток. Соответственно, косметическая композиция для регенерации кожи, содержащая в качестве активного ингредиента экзосому, полученную из стволовых клеток, в соответствии с одним из вариантов осуществления настоящего изобретения, может быть использована в качестве фармацевтической композиции.
Стволовые клетки могут представлять собой стволовые клетки костного мозга, стволовые клетки пуповинной крови или стволовые клетки, полученные из жировой ткани, и могут представлять собой стволовые клетки человека, животных или растений. Например, данные стволовые клетки могут представлять собой стволовые клетки, полученные из жировой ткани человека, но не ограничены перечисленным.
В одном из вариантов осуществления настоящего изобретения при исследовании размера экзосомы, полученной из пролиферирующих стволовых клеток жировой ткани человека (Stem-EXO), размер составил приблизительно 69 нм, что подтверждает, что данная экзосома меньше, чем экзосома, полученная из эпидермальных кератиноцитов человека (K-ЕХО), или экзосома, полученная из фибробластов крайней плоти человека (F-EXO) (Фиг. 13).
В другом варианте осуществления настоящего изобретения при сравнении и анализе биоактивных факторов, задействованных в коррекции морщин, отбеливании и регенерации кожи, присутствующих в Stem-EXO, К-ЕХО и F-EXO, было подтверждено, что моноцитарный хемоаттрактантный белок-1, -3 (МСР-1, -3), хемокиновый лиганд-5 (CCL-5) и ингибитор коллагеназы (тканевый ингибитор металлопротеиназы-1 (TIMP-1)), относящиеся к механизмам, связанным со стимуляцией синтеза коллагена и ингибированием его распада, интерлейкин-6, -8 (IL-6, -8), связанный с отбеливанием, фактор роста гепатоцитов (HGF), ингибитор-1 активатора плазминогена (РАI-1), ангиогенин и ангиопоэтин-1, связанные с регенерацией кожи и ангиогенезом, оверэкспрессировались в Stem-EXO по сравнению с K-ЕХО и/или F-EXO (Фиг. 15, 16 и 17).
В еще одном варианте осуществления настоящего изобретения исследовали ранозаживляющий эффект Stem-Exo на фибробластах крайней плоти человека. В результате, при использовании Stem-EXO в концентрации 10, 30 и 50 мкг/мл, она продемонстрировала превосходный эффект в отношении миграции фибробластов крайней плоти по сравнению с K-ЕХО или F-EXO, демонстрируя таким образом превосходный ранозаживляющий эффект (Фиг. 18).
В еще одном варианте осуществления настоящего изобретения был подтвержден эффект Stem-EXO в отношении коррекции морщин. В результате, синтез коллагена повышался при повышении используемой концентрации Stem-EXO. В частности, Stem-EXO продемонстрировала исключительно превосходную скорость синтеза коллагена по сравнению с K-ЕХО или F-EXO в концентрации 50 мкг/мл, что подтверждает превосходный эффект в отношении коррекции морщин (Фиг. 19).
В еще одном варианте осуществления настоящего изобретения исследовали ингибирующий эффект Stem-EXO на синтез меланина. В результате, при использовании Stem-EXO на меланоме мыши в концентрации 10, 30 и 50 мкг/мл, было подтверждено снижение синтеза меланина, что подтверждает исключительно превосходный отбеливающий эффект (Фиг. 20).
ПОЛОЖИТЕЛЬНЫЕ ЭФФЕКТЫ
Экзосомы в соответствии с вариантами осуществления настоящего изобретения демонстрируют превосходную степень экспрессии биоактивных факторов, оказывающих воздействие на дифференцировку в адипоциты, и обладающие эффектом дифференцировки стволовых клеток в адипоциты. Соответственно, настоящее изобретение может применяться в качестве агентов, индуцирующих дифференцировку стволовых клеток, инъекционных форм препаратов для регенерации тканей, наполнителей для косметических целей, препаратов для тканевой инженерии и т.д. Кроме того, экзосомы в соответствии с вариантами осуществления настоящего изобретения представляют собой экзосомы, выделяемые во время пролиферации стволовых клеток, и содержат гены, белки, факторы роста и тому подобные, связанные с пролиферацией клеток, дифференцировкой и регенерацией стволовых клеток, и, следовательно, могут стимулировать регенерацию кожи без других добавок, таких как активаторы клеток или факторы роста. Кроме того, экзосомы представляют собой очищенные компоненты, не включающие антибиотики, сыворотки или вредные факторы культурального раствора, и, таким образом, могут быть преодолены проблемы, связанные с косметикой на основе клеточных культур. Кроме того, экзосомы представляют собой полученные из клеток липидные носители, что позволяет им превосходно проникать в клетки и быть высокоэффективными при доставке эффективных факторов. Соответственно, настоящее изобретение может применяться в функциональных косметических композициях, обладающих функциями отбеливания кожи, коррекции морщин и регенерации кожи, и в препаратах для улучшения внешнего вида шрамов в косметических целях, и т.д.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фиг. 1 представляет собой схематическую диаграмму экзосом, полученных из стволовых клеток, дифференцирующихся в адипоциты, и их применение.
Фиг. 2 представляет собой схематическую диаграмму способа выделения экзосом из стволовых клеток, дифференцирующихся в адипоциты.
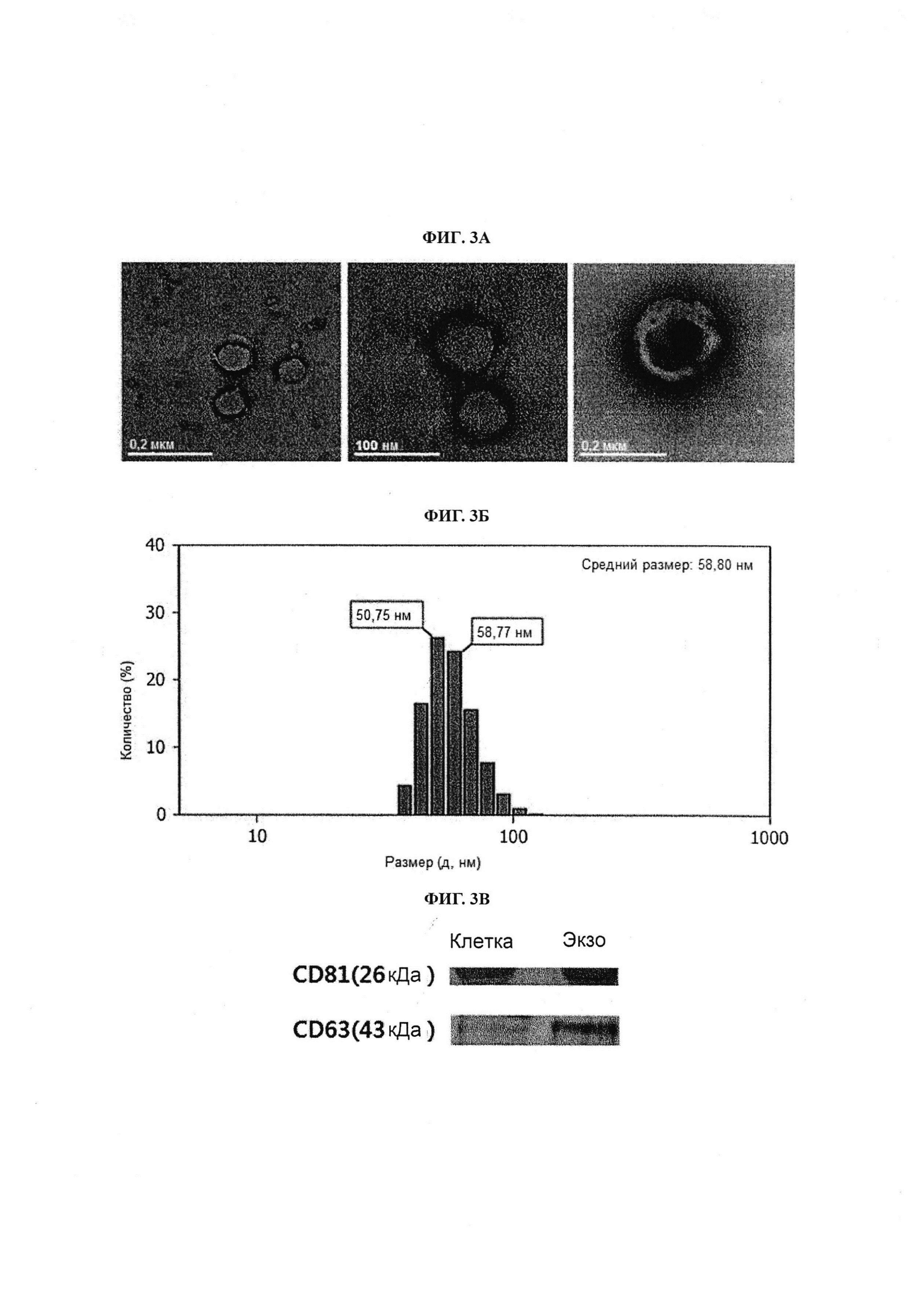
Фиг. 3А-3В демонстрируют диаграммы, иллюстрирующие характеристики экзосом, полученных из стволовых клеток, дифференцирующихся в адипоциты; А: структура и форма экзосом (трансмиссионный электронный микроскоп), Б: размер экзосомы (анализатор наночастиц, динамическое рассеяние света), В: белок-маркер, присутствующий на поверхности мембраны экзосомы (вестерн-блоттинг).
Фиг. 4А-4В демонстрируют диаграммы, иллюстрирующие связанные с липидами биоактивные факторы в экзосомах посредством микроматричного анализа; А: экзосомы, полученные из пролиферирующих стволовых клеток (hASC-EXO), Б: экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты (D-ЕХО), В: матрица для адипокинов.
Фиг. 5 демонстрирует диаграмму, иллюстрирующую степень экспрессии факторов, оказывающих воздействие на дифференцировку в адипоциты; экзосомы, полученные из пролиферирующих стволовых клеток (hASC-EXO), и экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты (D-EXO).
Фиг. 6 демонстрирует результат индукции дифференцировки стволовых клеток, полученных из жировой ткани человека, в адипоциты; А: стволовые клетки человека, полученные из жировой ткани (hASC), Б: положительный контроль (DM), экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты (D-EXO), и экзосомы, полученные из пролиферирующих стволовых клеток (hASC-EXO).
Фиг. 7 демонстрирует результат окраски масляным красным О стволовых клеток, индуцированных к дифференцировке в адипоциты; А: стволовые клетки, полученные из жировой ткани человека (hASC), Б: положительный контроль (DM), экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты (D-ЕХО), и экзосомы, полученные из пролиферирующих стволовых клеток (hASC-EXO).
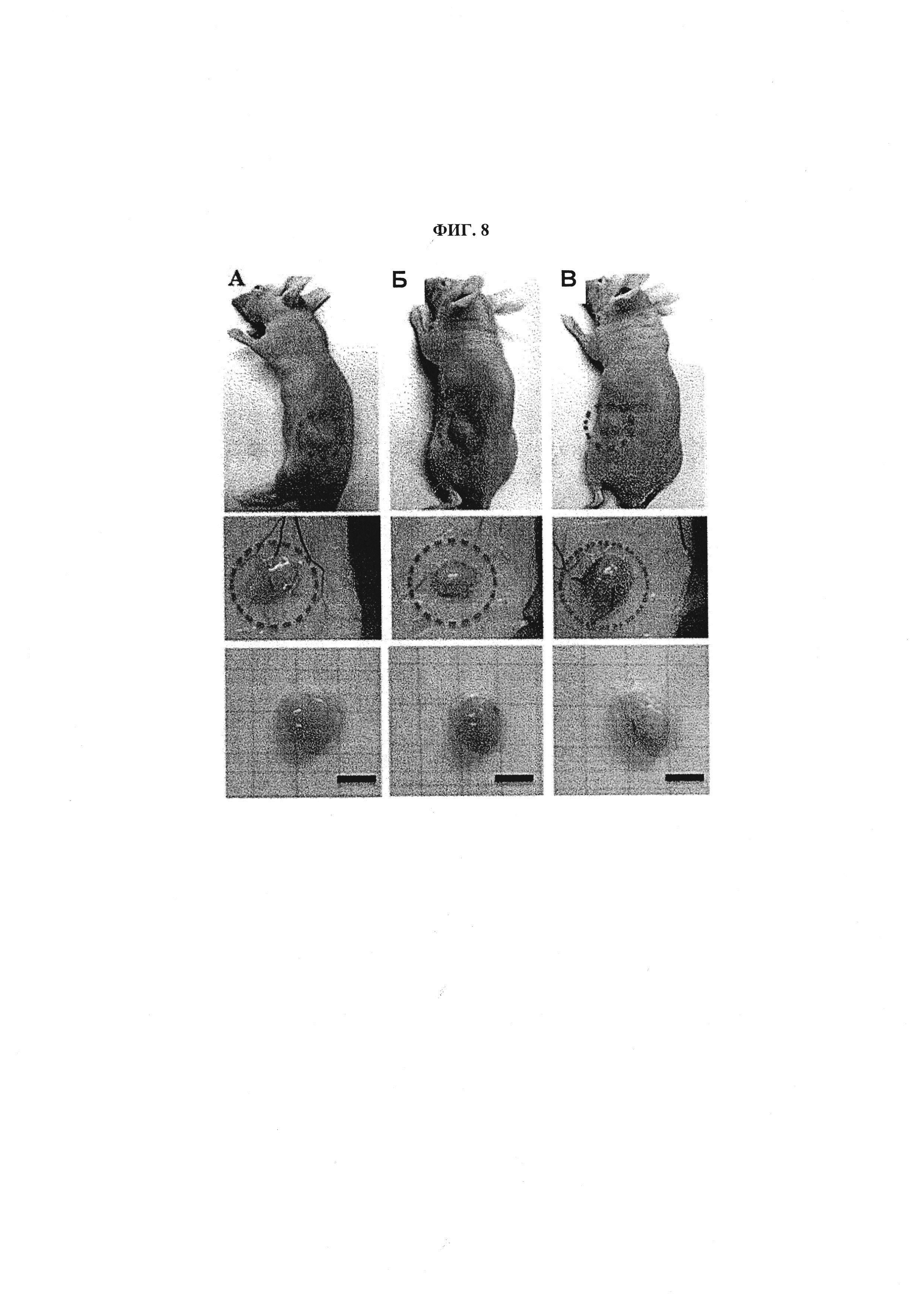
Фиг. 8 демонстрирует результат стимуляции образования жировых тканей в течение 3 недель путем внесения экзосом в гидрогель, полученный смешиванием коллагена и метилцеллюлозы, и подкожного введения экзосом бестимусным мышам в качестве моделей; А: гидрогель на основе коллагена/метилцеллюлозы (Gel), Б: гидрогель, несущий экзосомы, полученные из пролиферирующих стволовых клеток (hASC-EXO), В: гидрогель, несущий экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты (D-EXO).
Фиг. 9 демонстрирует результат окраски гематоксилин-эозином гелей, подкожно введенных бестимусным мышам. Один гель не несет экзосом (Gel), и остальные гели несут экзосомы, полученные из пролиферирующих стволовых клеток (hASC-EXO), и экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты (D-EXO), соответственно. А, В, Д: 40-кратное увеличение; Б, Г, Е: 100-кратное увеличение.
Фиг. 10 демонстрирует результат окраски масляным красным O гелей, подкожно введенных бестимусным мышам в качестве моделей. Один гель не несет экзосом (Gel), и остальные гели несут экзосомы, полученные из пролиферирующих стволовых клеток (hASC-EXO), и экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты (D-EXO), соответственно.
Фиг. 11 представляет собой схематическую диаграмму способа выделения экзосом из пролиферирующих стволовых клеток, полученных из жировой ткани человека.
Фиг. 12 демонстрирует изображения стволовых клеток, полученных из жировой ткани человека, эпидермальных кератиноцитов человека и фибробластов крайней плоти человека, полученные при помощи микроскопа.
Фиг. 13А-13В демонстрируют диаграммы, иллюстрирующие характеристики экзосом, полученных из стволовых клеток жировой ткани человека (Stem-Exo). Экзосомы, полученные из кератиноцитов человека (K-Ехо) и из фибробластов крайней плоти человека (F-Exo) использовались в качестве контролей. Проиллюстрированы структура и форма экзосом (трансмиссионный электронный микроскоп), и размер экзосом (анализатор наночастиц, динамическое рассеяние света) показаны соответственно; A: Stem-Exo (масштабные метки обозначают 50 нм (черная), 100 нм (белая), соответственно), Б: K-Ехо (масштабные метки обозначают 50 нм (черная), 100 нм (белая), соответственно) и В: F-Exo (масштабные метки обозначают 50 нм (черная) и 200 нм (белая), соответственно).
Фиг. 14А-14Г демонстрируют диаграммы, демонстрирующие сравнение уровней экспрессии биоактивных факторов, содержащихся в экзосомах, полученных из стволовых клеток жировой ткани человека (Stem-EXO), экзосомах, полученных из эпидермальных кератиноцитов человека (K-ЕХО), и экзосомах, полученных из фибробластов человека (F-EXO), посредством микроматричного анализа; А: таблица микроматричного анализа, Б: результат микроматричного анализа, В и Г: графики, демонстрирующие сравнительные уровни экспрессии биоактивных факторов.
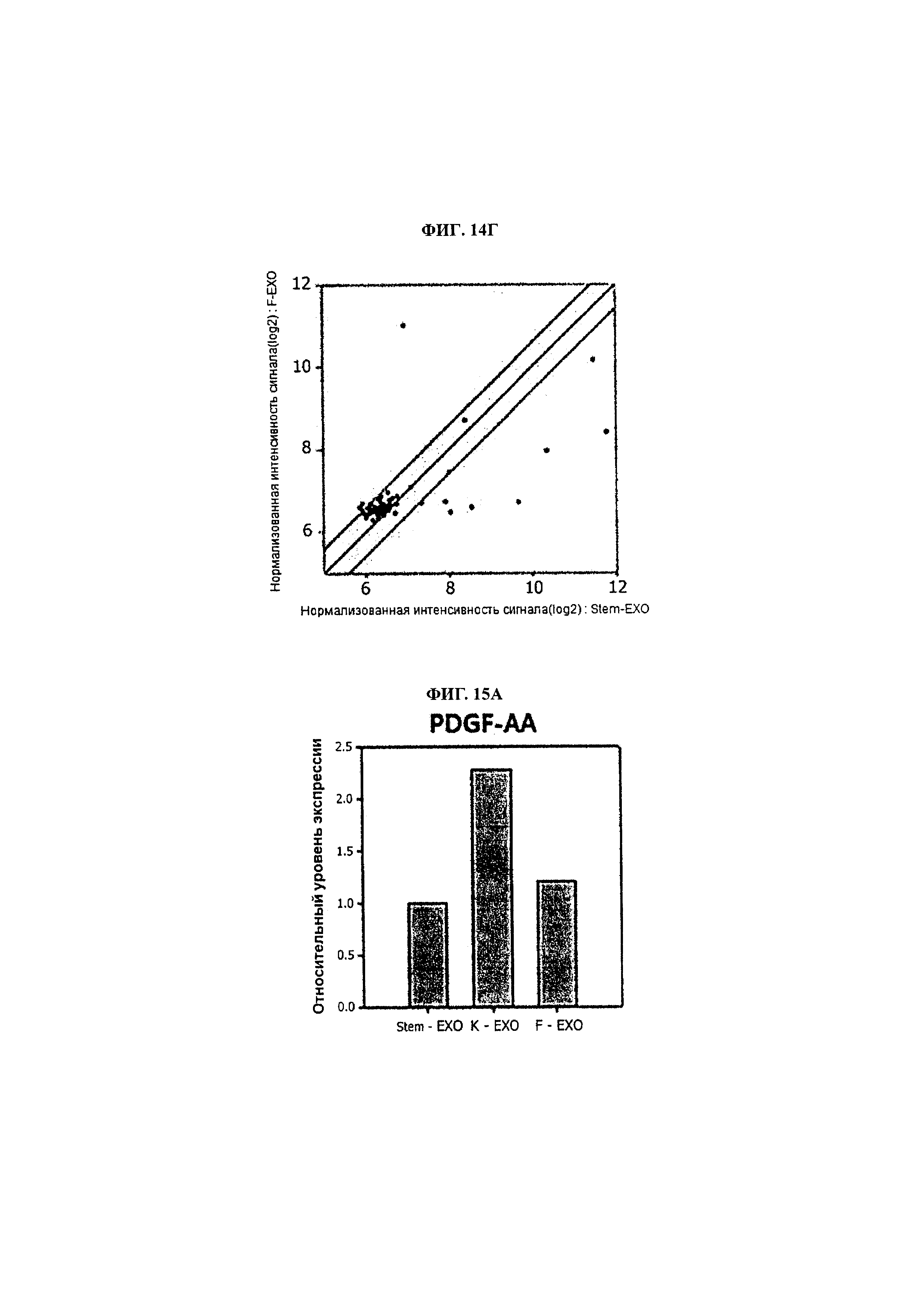
Фиг. 15А-15И демонстрируют графики, иллюстрирующие уровень экспрессии в экзосомах биоактивного фактора (A: PDGF-AA, Б: PDGF-AB, В: PDGF-BB, Г: FGF-6, Д: МСР - Е: МСР-3, Ж: эотаксин, З: CCL-5, И: TIMP-1), связанного с эффектом коррекции морщин, посредством микроматричного анализа; Stem-EXO: экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека, K-ЕХО: экзосомы, полученные из эпидермальных кератиноцитов человека, F-EXO: экзосомы, полученные из фибробластов крайней плоти человека.
Фиг. 16А-16Г демонстрируют графики, иллюстрирующие уровень экспрессии в экзосомах биоактивного фактора (А: TGF-бета, Б: TNF-альфа, В: IL-6, Г: IL-8), связанного с отбеливающим эффектом, посредством микроматричного анализа; Stem-EXO: экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека, K-ЕХО: экзосомы, полученные из эпидермальных кератиноцитов человека, F-EXO: экзосомы, полученные из фибробластов крайней плоти человека.
Фиг. 17А-17Е демонстрируют графики, иллюстрирующие уровни экспрессии в экзосомах биоактивного фактора (A: EGF, Б: HGF, В: РАI-1, Г: VEGF, Д: ангиогенин, Е: ангиопоэтин-1), связанного с регенерацией кожи и ангиогенезом, посредством микроматричного анализа; Stem-EXO: экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека, K-ЕХО: экзосомы, полученные из эпидермальных кератиноцитов человека, F-EXO: экзосомы, полученные из фибробластов крайней плоти человека.
Фиг. 18А-18Б демонстрируют диаграммы, иллюстрирующие воздействие экзосом, полученных из стволовых клеток жировой ткани человека (Stem-EXO), на миграцию фибробластов человека; GM: культуральная среда стволовых клеток (среда для выращивания), SFM: бессывороточная среда, Stem-EXO: экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека, K-ЕХО: экзосомы, полученные из эпидермальных кератиноцитов человека, F-EXO: экзосомы, полученные из фибробластов крайней плоти человека.
Фиг. 19 демонстрирует график, иллюстрирующий воздействие экзосом, полученных из стволовых клеток жировой ткани человека (Stem-EXO), на синтез коллагена фибробластами человека; SFM: бессывороточная среда, Stem-EXO: экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека, K-ЕХО: экзосомы, полученные из эпидермальных кератиноцитов человека, F-EXO: экзосомы, полученные из фибробластов крайней плоти человека.
Фиг. 20 демонстрирует график, иллюстрирующий воздействие экзосом, полученных из стволовых клеток жировой ткани человека (Stem-EXO), на синтез меланина меланоцитами мыши; GM: культуральная среда стволовых клеток (среда для выращивания), SFM: бессывороточная среда, Stem-EXO: экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека, K-ЕХО: экзосомы, полученные из эпидермальных кератиноцитов человека, F-EXO: экзосомы, полученные из фибробластов крайней плоти человека.
ПРИМЕРЫ
Здесь и далее предпочтительные варианты осуществления представлены для облегчения понимания сущности настоящего изобретения, но варианты осуществления представлены только с иллюстративной целью. Кроме того, специалистам в данной области очевидно, что в объеме и техническом замысле настоящего изобретения могут быть получены различные модификации и альтернативные формы, и что такие модификации и альтернативные формы находятся в объеме изобретения.
Пример 1 Экзосомы. полученные из стволовых клеток, дифференцирующихся в адипоциты
Пример 1-1: Выделение экзосом
Для выделения экзосом из стволовых клеток, дифференцирующихся в адипоциты, была индуцирована дифференцировка в адипоциты путем культивирования стволовых клеток в дифференцирующей среде.
Дифференцировка в адипоциты подтверждалась при образовании капель жира в цитоплазме, при этом популяция стволовых клеток постепенно становилась неоднородной. Дифференцирующую культуральную среду стволовых клеток заменяли бессывороточной средой и выдерживали в течение 48 часов, и собирали клеточный супернатант. Собранный клеточный супернатант центрифугировали при 300×g в течение 10 минут для удаления клеток, и затем центрифугировали при 2000×g в течение 30 минут для удаления продуктов выделения клеток.
После чего клетки концентрировали центрифугированием при 5000×g в течение 60 минут с использованием центрифужной пробирки (отсекаемая молекулярная масса составляла 3000, пробирка amicon), оборудованной фильтром, задерживающим молекулы, имеющие молекулярную массу 3000. Супернатант, полученный после концентрации, смешивали с реагентом для выделения экзосом в соотношении 1:0,5, и хранили при 4°C в течение одних суток. После чего клетки центрифугировали при 10000×g в течение 60 минут с получением экзосомального осадка, затем фильтровали через фильтр (спин-колонка для экзосом), задерживающий молекулы, имеющие молекулярную массу 3000, и промывали натрий-фосфатным буфером (PBS). Промытый экзосомальный осадок центрифугировали при 10000×g в течение 60 минут и ресуспендировали в PBS (Фиг. 2).
Пример 1-2: Микроскопическое исследование экзосом
Размер и форму экзосом, полученных в Примере 1-1, подтверждали с использованием трансмиссионного электронного микроскопа и динамического рассеяния света, и поверхностный белок экзосом подтверждали с использованием вестерн-блоттинга, обнаруживающего специфический белок для мембранной поверхности экзосом.
В результате выделенные экзосомы, как продемонстрировано на Фиг. 3А, подтверждали трансмиссионным электронным микроскопом, и их подтвержденный размер составил в среднем приблизительно от 50,75 до 58,77 нм, как продемонстрировано на Фиг. 3Б. Кроме того, как продемонстрировано на Фиг. 3В, на поверхности мембран экзосом присутствует специфический для экзосом белок-маркер, обнаруженный реакцией на антитела.
Пример 1-3: Исследование белков и биоактивных факторов, связанных с адипоцитной дифференцировкой, в экзосомах
Для анализа связанных с липидами биоактивных факторов в экзосомах, полученных из стволовых клеток, дифференцирующихся в адипоциты, и экзосомах, полученных из пролиферирующих стволовых клеток, использовали микроматричный анализ. Микроматричный анализ проводили посредством реакции антиген-антитело и измеряли степень интенсивности флуоресценции (стрептавидин-Су3) с помощью лазерного сканера (GenePix 4000 В).
Кроме того, среди факторов,. выявленных с помощью микроматричного анализа, было подтверждено наличие макрофагального колониестимулирующего фактора (MCSF), фактора некроза опухоли-α (TNF-α), лептина, инсулина, ангиопоэтина-1 (ANGPT1) и адипонектина с молекулярной массой 30 кДа (Acrp30), все из которых представляют собой биоактивные факторы, оказывающие воздействие на дифференцировку в адипоциты, и в этой связи проводили сравнение их относительных уровней экспрессии в экзосомах, полученных из стволовых клеток, дифференцирующихся в адипоциты, и из пролиферирующих стволовых клеток.
В результате, как продемонстрировано на Фиг. 4А-4В и в Таблице 1, было подтверждено наличие в экзосомах, полученных из пролиферирующих стволовых клеток (hASC-EXO) и экзосомах, полученных из стволовых клеток, дифференцирующихся в адипоциты (D-EXO), различных типов связанных с липидами биоактивных факторов, и было также подтверждено существенное различие в уровнях экспрессии биоактивных факторов, оказывающих воздействие на дифференцировку в адипоциты (Фиг. 5).

Пример 1-4: Индукция адипоцитной дифференцировки с использованием экзосом
С целью индуцировать адипоцитную дифференцировку стволовых клеток с использованием экзосом применяли композиции сред, каждая из которых содержала культуральную среду экзосом, полученных из пролиферирующих стволовых клеток и экзосом, полученных из стволовых клеток, дифференцирующихся в адипоциты. Композиции сред использовали путем добавления экзосом к культуральной среде стволовых клеток в концентрации 30, 50 и 100 мкг/мл. После обработки каждой композицией среды культивируемых стволовых клеток, полученных из жировой ткани человека (hASC), композиции сред заменяли каждые 3 дня в течение 14 дней.
Стволовые клетки, культивированные в среде Игла, модифицированной Дульбекком (ДМЕМ), содержащей 5% фетальной бычьей сыворотки, 1 мкм дексаметазона, 1 мкг/мл инсулина, 100 мкМ индометацина, 0,5 мМ 3-изобутил-1-метилксантина, использовали в качестве положительного контроля. Стволовые клетки, обработанные экзосомами, полученными из пролиферирующих стволовых клеток, использовали в качестве положительного контроля. Затем у стволовых клеток, в которых была индуцирована дифференцировка в адипоциты, анализировали форму клеток и определяли, была ли осуществлена дифференцировка, используя микроскоп и окраску масляным красным O в течение 14 дней.
В результате при использовании экзосом, полученных из стволовых клеток, дифференцирующихся в адипоциты (D-EXO), уровень дифференцировки стволовых клеток в адипоциты был схож с уровнем для положительного контроля (DM) на седьмой день (Фиг. 6), и, соответственно, был подтвержден синтез жира (Фиг. 7). Однако в случае стволовых клеток, обработанных экзосомами, полученными из пролиферирующих стволовых клеток (hASC-EXO), было подтверждено, что осуществлялась только пролиферация без дифференцировки в адипоциты.
Пример 1-5: Косметическая композиция, содержащая экзосомы. полученные из стволовых клеток, дифференцирующихся в адипоциты
В соответствии с Примером 1-1 была получена липосома, заключающая в себя экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты. А именно, 3 масс. % лецитина диспергировали в водной фазе, содержащей 0,01 масс. % экзосом, полученных из стволовых клеток, дифференцирующихся в адипоциты, при комнатной температуре (15°C), и затем получали эмульсию с обратными мицеллами (вода/диоксид углерода, полученный при низкой температуре) с использованием сверхкритического диоксида углерода. После чего реакцию останавливали, испаряли сверхкритический диоксид углерода при пониженном давлении для удаления фазы сверхкритического диоксида углерода, и получали полученную при низкой температуре суспензию липосом, заключающих в себя экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты. В данном примере температура проведения реакции составляла 4°C или ниже.
Косметическая композиция, полученная с использованием липосом, заключающих в себя экзосомы, имела состав, представленный в Таблице 2 ниже.

Пример 1-6: Индукция регенерации жировой ткани с использованием экзосом. полученных из стволовых клеток, дифференцирующихся в адипоциты
Для подтверждения воздействия, оказываемого на регенерацию жировой ткани при введении в организм экзосом, полученных из стволовых клеток, дифференцирующихся в адипоциты, экзосомы, полученные из пролиферирующих стволовых клеток и экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты, независимо вносили в гидрогель на основе коллагена/метилцеллюлозы.
А именно, гидрогель получали добавлением порошка метилцеллюлозы к раствору коллагена с образованием гидрогеля на основе коллагена/метилцеллюлозы. То есть, порошок метилцелюлозы добавляли к раствору коллагена в 0,02 Н уксусной кислоте с концентрацией 3 мг/мл, так что конечная концентрация метилцеллюлозы составляла 6 масс. %, и затем перемешивали смесь при 4°C в течение 1 часа с получением геля. Полученный таким образом гидрогель на основе коллагена/метилцеллюлозы содержал экзосомы, полученные из пролиферирующих стволовых клеток, или экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты. А именно, экзосомы вносили в гидрогель на основе коллагена/метилцеллюлозы до конечной концентрации 50 мкг/мл, и затем диспергировали в гидрогеле путем раскапывания пипеткой. Затем гидрогель, содержащий экзосомы, подкожно вводили бестимусным мышам и проводили наблюдение в течение 3 недель. Гидрогель, не содержащий экзосом, использовали в качестве отрицательного контроля, а гидрогель, содержащий экзосомы, полученные из пролиферирующих стволовых клеток (hASC-EXO), использовали в качестве положительного контроля (Фиг. 8). Три недели спустя осуществляли окраску гематоксилин-эозином и масляным красным O для подтверждения регенерации жировых тканей в трансплантированном гидрогеле.
В результате в геле, содержащем экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты (D-EXO) (Фиг. 9), наблюдалось большое количество клеток мыши, а также большое число адипоцитов, в которых синтезировался жир (Фиг. 10), по сравнению с отрицательным и положительным контролями. Исходя из этих результатов можно сделать вывод, что экзосомы, полученные из стволовых клеток, дифференцирующихся в адипоциты, или гидрогель на основе коллагена/метилцеллюлозы, несущий экзосомы, были исключительно эффективны в отношении индукции регенерации жировых тканей.
Пример 2 Экзосомы. полученные из пролиферирующих стволовых клеток
Пример 2-1: Выделение экзосом из пролиферирующих стволовых клеток, полученных из жировой ткани человека
Экзосомы выделяли во время пролиферации стволовых клеток, полученных из жировой ткани человека, до седьмого пассажа. То есть экзосомы выделяли из пролиферирующих стволовых клеток жировой ткани человека.
А именно, стволовые клетки человека, полученные из жировой ткани (пассажи 3-7) культивировали в нормальной культуральной среде (среда Игла, модифицированная Дульбекком (ДМЕМ), содержащая 10% фетальной бычьей сыворотки, 1% пенициллина/стрептомицина). Затем за 24 часа до выделения экзосом клеточную культуральную среду заменяли средой ДМЕМ, представляющей собой бессывороточную и не содержащую антибиотиков среду, не содержащую фенолового красного, и затем выдерживали в течение 24 часов. По истечении 24 часов супернатант клеточной культуры собирали. Собранный супернатант клеточной культуры центрифугировали при 300×g в течение 10 минут для удаления, и затем центрифугировали при 2000×g в течение 30 минут для удаления продуктов выделения клеток. Затем клетки концентрировали путем центрифугирования при 5000×g в течение 60 минут с помощью центрифужной пробирки, оборудованной фильтром, задерживающим молекулы, имеющие молекулярную массу 3000 (отсекаемая молекулярная масса составляла 3000, пробирка amicon). Супернатант, полученный после концентрирования, смешивали с реагентом для выделения экзосом в соотношении 1:0,5, и хранили при 4°C в течение одних суток. Получали экзосомальный осадок центрифугированием при 10000×g в течение 60 минут, затем фильтровали через 0,22 мкм фильтр (спин-колонка для экзосом) и промывали натрий-фосфатным буфером (PBS). Промытый экзосомальный осадок центрифугировали при 10000×g в течение 60 минут и ресуспендировали в PBS (Фиг. 11). После сбора супернатанта к стволовым клеткам добавляли нормальную культуральную среду и культивировали. Эту процедуру повторяли до седьмого пассажа стволовых клеток. Экзосомы, выделенные во время пролиферации стволовых клеток до седьмого пассажа, использовали в следующих экспериментах. Чтобы сравнить эффективность экзосом, полученных из стволовых клеток жировой ткани человека, экзосомы выделяли из эпидермальных кератиноцитов человека и фибробластов крайней плоти человека таким же образом, как и в вышеприведенном способе (Фиг. 12).
Пример 2-2: Микроскопическое исследование экзосом
Размеры и формы экзосом, полученных из стволовых клеток жировой ткани человека (Stem-Exo), экзосом, полученных из эпидермальных кератиноцитов человека (K-Ехо), и экзосом, полученных из фибробластов крайней плоти человека (F-EXO), в соответствии с Примером 2-1 подтверждали с использованием трансмиссионного электронного микроскопа и динамического рассеяния света.
В результате, форму каждой полученной экзосомы подтверждали с использованием трансмиссионного электронного микроскопа. Кроме того, размеры экзосом, полученных из стволовых клеток жировой ткани человека, экзосом, полученных из эпидермальных кератиноцитов человека, и экзосом, полученных из фибробластов крайней плоти человека, составили приблизительно 69 нм, приблизительно 79,7 нм и приблизительно 94,6 нм, соответственно, и размер экзосом, полученных стволовых клеток жировой ткани человека (Stem-Exo), был наименьшим (Фиг. 13А-13В).
Пример 2-3: Анализ белков и биоактивных Факторов, связанных с коррекцией морщин, отбеливанием и регенерацией кожи, в экзосомах
Для сравнения и анализа биоактивных факторов, связанных с коррекцией морщин, отбеливанием и регенерацией кожи, в экзосомах, полученных из стволовых клеток жировой ткани человека (Stem-Exo), экзосомах, полученных из эпидермальных кератиноцитов человека (K-Ехо), и экзосомах, полученных из фибробластов крайней плоти человека (F-EXO), осуществляли микроматричный анализ. Микроматричный анализ проводили посредством реакции антиген-антитело и измеряли степень интенсивности флуореценции (стрептавидин-Су3) посредством лазерного сканера (GenePix 4000 В).
Посредством микроматричного анализа было подтверждено наличие 9 биоактивных факторов, оказывающих воздействие на коррекцию морщин (PDFG-AA, PDGG-AB, PDGF-BB, FGF-6, МСР-1, МСР-3, эотаксина, CCL-5, TIMP-1), 4 биоактивных факторов, связанных с отбеливанием (TGF-бета, TNF-альфа, IL-6, IL-8), и 6 биоактивных факторов, связанных с регенерацией кожи и ангиогенезом (EGF, HGF, PAI-I, VEGF, ангиогенина, ангиопоэтина-1), и в этой связи проводили сравнение относительных уровней экспрессии каждого биоактивного фактора в экзосомамах, полученных из стволовых клеток жировой ткани человека, и экзосомах, полученных из эпидермальных кератиноцитов человека и из фибробластов крайней плоти человека (Фиг. 14). Фиг. 14В и 14Г демонстрируют относительные уровни экспрессии биоактивных факторов, где горизонтальная ось обозначает экзосомы из стволовых клеток жировой ткани человека, и вертикальная ось обозначает экзосомы из эпидермальных кератиноцитов и экзосомы фибробластов, соответственно. Кроме того, верхняя линия и нижняя линия по отношению к серединной линии в центре обозначают полуторакратное увеличение/уменьшение по отношению к референсному значению, соответственно. Фиг. 15А-15И демонстрируют биоактивные факторы, связанные с эффектом экзосом в отношении коррекции морщин, Фиг. 16А-16Г демонстрируют биоактивные факторы, связанные с отбеливающим эффектом экзосом, и Фиг. 17А-17Е демонстрируют биоактивные факторы, связанные с эффектом экзосом в отношении регенерации кожи и ангиогенеза.
В результате, как продемонстрировано на Фиг. 15, 16 и 17, было подтверждено наличие в экзосомах, полученных из стволовых клеток жировой ткани человека (Stem-Exo), экзосомах, полученных из эпидермальных кератиноцитов человека (K-Ехо), и экзосомах, полученных из фибробластов крайней плоти человека (F-EXO), различных типов биоактивных факторов. А именно, было подтверждено, что моноцитарный хемоаттрактантный белок-1, -3 (МСР-1, -3), хемокиновый лиганд-5 (CCL-5) и ингибитор коллагеназы (тканевый ингибитор металлопротеиназы-1 (TIMP-1)), относящиеся к механизмам, связанным со стимуляцией синтеза коллагена и ингибированием его распада, интерлейкин-6, -8 (IL-6, -8), связанный с отбеливанием, фактор роста гепатоцитов (HGF), ингибитор активатора плазминогена-1 (РАI-1), ангиогенин и ангиопоэтин-1, связанные с регенерацией кожи и ангиогенезом, оверэкспрессировались в экзосомах, полученных из стволовых клеток жировой ткани человека (Stem-EXO), по сравнению с K-ЕХО и/или F-EXO (Фиг. 15, 16 и 17).
Пример 2-4: Воздействие на миграцию фибробластов крайней плоти человека при использовании экзосом, полученных из пролиферирующих стволовых клеток жировой ткани человека
Для исследования воздействия экзосом, полученных из пролиферирующих стволовых клеток жировой ткани человека, на миграцию фибробластов крайней плоти человека, использовали композиции сред, каждая из которых содержала экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека (Stem-EXO), экзосомы, полученные из эпидермальных кератиноцитов человека (K-ЕХО), и экзосомы, полученные из фибробластов крайней плоти человека (F-EXO). Каждую из композиций сред получали путем добавления Stem-EXO к бессывороточной среде ДМЕМ в концентрациях 10, 30 и 50 мкг/мл, и добавления K-ЕХО и F-EXO к бессывороточной среде ДМЕМ в концентрации 50 мкг/мл, соответственно. Среду ДМЕМ, содержащую 10% сыворотки, использовали в качестве положительного контроля, и бессывороточную среду ДМЕМ использовали в качестве отрицательного контроля. Фибробласты крайней плоти человека метили зеленым флуоресцентным красителем, затем высевали в 24-луночный планшет с плотностью 1×105 клеток/лунка, и культивировали в культуральной среде (ДМЕМ, содержащей 10% фетальной бычьей сыворотки, 1% пенициллина/стрептомицина) в течение 72 часов. После культивирования в центре нижней части планшета, к которому прикреплялись клетки, с помощью стерилизованного желтого наконечника наносили раны с искусственно единообразными промежутками, и наносили на клетки композиции сред, каждая из которых содержала экзосомы.
В результате, клетки, обработанные средой, содержащей Stem-EXO, по истечении 24 часов демонстрировали более высокую степень миграции по сравнению с клетками, обработанными отрицательным контролем, K-ЕХО и F-EXO, и эта тенденция была еще более выраженной для среды, содержащей Stem-EXO в концентрации 30 и 50 мкг/мл. По истечении 48 часов миграция бурно осуществлялась в среде, содержащей 10, 30 и 50 мкг/мл Stem-EXO, демонстрируя лучший (например, более быстрый, приводящий к меньшему количеству шрамов или меньшему изменению цвета) ранозаживляющий эффект по сравнению со средами, содержащими K-ЕХО и F-EXO (Фиг. 18А и 18Б).
Таким образом, экзосомы, полученные из стволовых клеток жировой ткани человека (Stem-Exo), демонстрировали превосходный эффект в отношении миграции фибробластов крайней плоти человека по сравнению с K-ЕХО или F-EXO.
Пример 2-5: Эффект экзосом, полученных из пролиферирующих стволовых клеток жировой ткани человека, в отношении коррекции морщин
Для исследования воздействия экзосом, полученных из стволовых клеток жировой ткани человека, на синтез коллагена фибробластами крайней плоти человека, использовали композиции сред, каждая из которых содержала экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека (Stem-EXO), экзосомы, полученные из эпидермальных кератиноцитов человека (K-ЕХО), и экзосомы, полученные из фибробластов крайней плоти человека (F-EXO). Каждую из композиций сред получали добавлением Stem-EXO к бессывороточной культуральной среде ДМЕМ в концентрациях 10, 30 и 50 мкг/мл, и добавлением K-ЕХО и F-EXO к бессывороточной культуральной среде ДМЕМ в концентрации 50 мкг/мл, соответственно. Бессывороточную среду ДМЕМ использовали в качестве отрицательного контроля. Фибробласты крайней плоти человека высевали в 48-луночный планшет с плотностью 5×104 клеток/лунка, и культивировали в культуральной среде (ДМЕМ, содержащей 10% фетальной бычьей сыворотки, 1% пенициллина/стрептомицина) в течение 72 часов, затем промывали PBS и наносили на клетки композиции сред, каждая из которых содержала экзосомы.
После завершения культивирования собирали культуральный раствор из каждой лунки, центрифугировали при 25°C при 3000 об/мин в течение 10 минут, и затем отбирали супернатант и использовали для экстракции и количественной оценки растворимого коллагена. Каждую лунку планшета, из которой удалили культуральный раствор, промывали PBS. Затем клетки отделяли от нижней части каждой лунки с помощью трипсина (трипсин-ЭДТА), и измеряли количество клеток.
Набор для исследования коллагена Sircol (Biocolor, Великобритания) использовали для количественной оценки растворимого коллагена. Полученный таким образом супернатант обрабатывали буфером Трис-HCl (pH 7,6), смешанным с полиэтиленгликолем, и выдерживали при 4°C в течение 12 часов или дольше. После чего результат центрифугировали при 12000 об/мин в течение 10 минут для концентрирования коллагена. После удаления супернатанта к коллагеновому осадку добавляли 1 мл предоставленного красителя для адсорбции коллагеном (окрашивающий реагент Sircol), и затем культивировали при встряхивании в течение 30 минут. Неадсорбировавшийся краситель удаляли центрифугированием при 12000 об/мин в течение 10 минут и промывали осадок кислотно-солевым буфером. Затем краситель, адсорбированный коллагеном, растворяли посредством применения щелочного реагента, и измеряли поглощение при длине волны 555 нм. Величину поглощения подставляли в уравнение стандартной кривой для рассчета количества растворимого коллагена в лунках, к которым добавлялись Stem-EXO, K-ЕХО, F-EXO и отрицательный контроль, соответственно. Калиброванное количество коллагена подставляли в уравнение для расчета скорости синтеза.
В результате, скорость синтеза растворимого коллагена для группы, обработанной Stem-EXO, увеличивалась в зависимости от использованной концентрации экзосом по сравнению с отрицательным контролем (0,138 мкг). В частности, для группы, обработанной Stem-EXO в концентрации 50 мкг/мл, количество синтезированного коллагена составило 2,59 мкг, что было существенно выше по сравнению с таким же количеством K-ЕХО (1,4 мкг) или F-EXO (0,8 мкг). Следовательно, можно предположить, что экзосомы, полученные из стволовых клеток жировой ткани человека, обладают эффектом стимуляции синтеза коллагена фибробластами крайней плоти человека (Фиг. 19).
Пример 2-6: Ингибирующий эффект экзосом, полученных из пролиферирующих стволовых клеток жировой ткани человека, на синтез меланина на меланоме мыши
Отбеливающий эффект экзосом, полученных из стволовых клеток жировой ткани человека (Stem-EXO), и экзосом, полученных из эпидермальных кератиноцитов человека (K-ЕХО), и экзосом, полученных из фибробластов крайней плоти человека (F-EXO), в качестве контролей, определяли относительно степени ингибирования синтеза меланина меланомой мыши. Клетки меланомы представляют собой клетки, получаемые из меланомы мыши и выделяющие пигмент меланин, называемый «меланин». Клетки меланомы высевали с плотностью 1×105 клеток/лунка в 96-луночный планшет для прикрепления клеток, и затем культивировали в течение 3 суток путем замещения культуральной среды средой, содержащей Stem-EXO, K-ЕХО и F-EXO, соответственно. По истечении 3 суток среду собирали и центрифугировали при 4500 об/мин в течение 10 минут, и измеряли поглощение при 405 нм для расчета количества меланина, выделенного клетками. Клетки, прикрепленные к планшету, удаляли с помощью трипсина (трипсин-ЭДТА), и измеряли количество клеток с последующим центрифугированием для извлечения клеток. Клетки однократно промывали PBS и центрифугировали с получением клеточных осадков. К клеточным осадкам добавляли 1 мл 1 Н раствора гидроксида натрия (NaOH), содержащего 10% диметилсульфоксида (ДМСО), для растворения меланина, при 80°C в течение 2 часов, результат добавляли в 96-луночный планшет и измеряли поглощение при 405 нм. Количественную оценку меланина проводили с использованием измеренных значений поглощения, и нормализовывали к концентрации белка в образце для определения концентрации синтезированного меланина.
Экзосомы, полученные из стволовых клеток жировой ткани человека, использовали на клетках меланомы в концентрации 10, 30 и 50 мкг/мл, и исследовали уровень синтеза меланина. В результате было подтверждено, что синтез меланина был уменьшен для всех концентраций экзосом, полученных из стволовых клеток (Фиг. 20).
Пример 2-7: Косметические композиции, содержащие экзосомы. полученные из пролиферирующих стволовых клеток жировой ткани человека
В соответствии с Примером 2-1 была получена липосома, заключающая в себя экзосомы, полученные из пролиферирующих стволовых клеток жировой ткани человека.
А именно, 3 масс. % лецитина диспергировали в водной фазе, содержащей 0,01 масс. % экзосом, полученных из пролиферирующих стволовых клеток, при комнатной температуре (15°C), а затем получали эмульсию с обратными мицеллами (вода/диоксид углерода, полученный при низкой температуре) с использованием сверхкритического диоксида углерода. Затем реакцию останавливали и испаряли сверхкритический диоксид углерода при пониженном давлении для удаления фазы сверхкритического диоксида углерода, получая таким образом полученную при низкой температуре суспензию липосом, заключающих в себя экзосомы, полученные из пролиферирующих стволовых клеток. В данном примере температура проведения реакции составляла 4°C или ниже.
Косметическая композиция, полученная с использованием липосом, заключающих в себя экзосомы, имела состав, представленный в Таблице 3 ниже.

Пример препарата 1: Получение смягчающей кожу косметической воды (лосьон для кожи)
Смягчающая кожу косметическая вода (лосьон для кожи), полученная с использованием липосом, заключающих в себя экзосомы, полученные из пролиферирующих стволовых клеток, полученных способом согласно Примеру 2-7, имела состав, представленный в Таблице 4 ниже.

Пример препарата 2: Получение питательной косметической воды (лосьон в виде молочка)
Питательная косметическая вода (лосьон в виде молочка), полученная с использованием липосом, заключающих в себя экзосомы, полученные из пролиферирующих стволовых клеток, полученных способом согласно Примеру 2-7, имела состав, представленный в Таблице 5 ниже.

Реферат
Группа изобретений относится к биотехнологии, а именно к композиции для индукции дифференцировки стволовых клеток в адипоциты. Композиция для индукции дифференцировки стволовых клеток в адипоциты для регенерации жировых тканей содержит в качестве ингредиента экзосомы, полученные из стволовых клеток, полученных из жировой ткани и дифференцирующихся в адипоциты, где экзосомы характеризуются тем, что содержат макрофагальный колониестимулирующий фактор (MCSF), фактор некроза опухоли-α (TNF-α), лептин, инсулин, ангиопоэтин-1 (ANGPT1) и адипонектин с молекулярной массой 30 кДа (Acrp30). Группа изобретений относится также к инъекционной форме препарата, содержащей указанную композицию. Использование данной группы изобретений позволяет применять данную композицию в качестве агентов, индуцирующих дифференцировку стволовых клеток, инъекционных форм препаратов для регенерации тканей путем экспрессии экзосомами биоактивных факторов, оказывающих воздействие на дифференцировку в адипоциты. 2 н. и 4 з.п. ф-лы, 20 ил, 5 табл., 2 пр.

Комментарии