Пероксидные композиции и способы и аппликаторы для их применения - RU2711662C2
Код документа: RU2711662C2
Чертежи


















Описание
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Варианты реализации данного описания касаются композиции, содержащей пероксид водорода и спирт. В некоторых вариантах реализации, пероксид водорода представляет собой стабилизированный пероксид водорода. В некоторых вариантах реализации, пероксид водорода может быть пероксидом водорода стандартного сорта, для пищевых продуктов, для химического синтеза, полупроводниковой чистоты, высококачественным пероксидом водорода, для антибактериального применения, для питьевой воды, для использования в фармацевтике, или для косметических целей. В некоторых вариантах реализации, спирт может быть выбран из первичного спирта, вторичного спирта, третичного спирта или их комбинации. В некоторых вариантах реализации, спирт может быть выбран из 2-пропанола, метанола, бутанола, 1-пропанола, пентанола, гексанола, октанола, нонанола, деканола, 2-пентанола, 2-бутанола, бензилового спирта, этанола, их изомеров или их комбинации. В некоторых вариантах реализации, пероксид водорода присутствует в количестве до около 50% композиции. В некоторых вариантах реализации спирт присутствует в количестве, достаточном для снижения поверхностного натяжения композиции. В некоторых вариантах реализации, спирт присутствует в количестве до около 5% композиции. В некоторых вариантах реализации, композиция представляет собой раствор. В некоторых вариантах реализации, композиция представляет собой гелевую композицию. В некоторых вариантах реализации, композиция содержит два или больше отдельных компонентов, которые могут быть смешаны перед, в момент, или незадолго до времени применения.
Некоторые варианты реализации касаются композиции для местного применения, содержащей до около 50% перекиси водорода и до 5% 2-пропанола. В некоторых вариантах реализации, пероксид водорода представляет собой стабилизированный пероксид водорода. В некоторых вариантах реализации, композиция для местного применения дополнительно содержит стабилизатор. Стабилизатор может быть выбран из станната, пирофосфата натрия, органофосфоната, нитрата, фосфорной кислоты, коллоидного силиката, любого стабилизатора, известного из уровня техники, или их комбинации. В некоторых вариантах реализации, 2-пропанол присутствует в количестве, достаточном для снижения поверхностного натяжения, в то же время минимизируя растекание композиции на не требующую обработки кожу при нанесении на целевое поражение. Композиция может быть стабильной на протяжении по меньшей мере двух лет при 5 °C, по меньшей мере одного года при 30 °C, по меньшей мере 6 месяцев при 40 °C, или их комбинации.
В некоторых вариантах реализации, композиция для местного применения содержит около 45% стабилизированного пероксида водорода для косметических целей и около 5% 2-пропанола, и при этом композиция для местного применения имеет поверхностное натяжение от около 42 мН•м-1 до около 55 мН•м-1 при 37 °C. В некоторых вариантах реализации, композиция для местного применения содержит около 40% стабилизированного пероксида водорода для косметических целей и около 5% 2-пропанола, и при этом композиция для местного применения имеет поверхностное натяжение от около 42 мН•м-1 до около 55 мН•м-1 при 37 °C. В некоторых вариантах реализации, композиция для местного применения содержит около 32,5% стабилизированного пероксида водорода для косметических целей и около 5% 2-пропанола, и при этом композиция для местного применения имеет поверхностное натяжение от около 42 мН•м-1 до около 55 мН•м-1 при 37 °C. В некоторых вариантах реализации, композиция для местного применения содержит около 25% стабилизированного пероксида водорода для косметических целей и около 5% 2-пропанола, и при этом композиция для местного применения имеет поверхностное натяжение от около 42 мН•м-1 до около 55 мН•м-1 при 37 °C.
Некоторые варианты реализации касаются композиции, содержащей пероксид водорода и модификатор поверхностного натяжения. В некоторых вариантах реализации, модификатор поверхностного натяжения представляет собой агент, стабильный в композициях, содержащих пероксид водорода в концентрациях, раскрытых в вариантах реализации настоящего изобретения. В некоторых вариантах реализации, модификатор поверхностного натяжения присутствует в количестве, достаточном для повышения терапевтической эффективности композиции. В некоторых вариантах реализации, модификатор поверхностного натяжения присутствует в количестве, достаточном для модификации поверхностного натяжения при поддержании стабильности композиции, достаточной для использования в качестве коммерчески жизнеспособной композиции. В некоторых вариантах реализации, модификатор поверхностного натяжения представляет собой спирт. В некоторых вариантах реализации, модификатор поверхностного натяжения представляет собой 2-пропанол.
Варианты реализации настоящего изобретения также описывают способ лечения кожного состояния, включающий введение композиции, содержащей до около 50% пероксида водорода и спирт, нуждающемуся в этом субъекту. Кожное состояние может быть вирусно-индуцированным или не-вирусно-индуцированным новообразованием или пролиферацией кожной ткани. Кожное состояние может быть доброкачественным новообразованием, предраком или злокачественной опухолью. Кожное состояние может быть воспалительным состоянием. Кожное состояние может быть гиперпролиферативным состоянием. Кожное состояние может быть старением, включая внутренне обусловленные изменения (например, хронологические) и изменения, вызванные внешними воздействиями (например, фотостарение, изменения, индуцированные воздействием ультрафиолетовых лучей), пигментные изменения, тонкие морщинки и преждевременное появление морщин на лице. В некоторых вариантах реализации, кожное состояние может быть выбрано из поражений, индуцированных вирусом папилломы человека, например, бородавки, обыкновенные бородавки, ладонно-подошвенные бородавки, плоские бородавки, периодические бородавки, не поддающиеся лечению бородавки, бородавки, лечение которых ранее не проводилось, бородавки, связанные с верруциформной эпидермодисплазией, аногенитальные бородавки, остроконечная кондилома, цервикальные дисплазии или неоплазии, например, цервикальная интраэпителиальная неоплазия (CIN); поражения, вызванные герпесвирусом, включая индуцированные герпевирусами человека (вирусами простого герпеса) HHV-1 (HSV-1), HHV-2 (HSV-2), HHV-3 (вирус varicella-zoster) например, ветряную оспу, опоясывающий герпес, опоясывающий лишай; поражения, индуцированные поксвирусом, например, контагиозный моллюск, контагиозный пустулезный дерматит; мозоль (callus), кожные рога, ороговевшей мозоли, мягкие бородавки, фиброэпителиальные полипы, узловатая почесуха Гайда, старческие кератозы, плоскоклеточная карцинома, плоскоклеточная карцинома in situ, кератоакантома, базальноклеточная карцинома, кожные лимфомы и доброкачественные лимфоцитарные инфильтраты и гиперплазии кожи, светлоклеточная акантома, крупноклеточная акантома, эпидермолитическая акантома, порокератоз, гиперкератоз, фолликулярный кератоз, лихеноидный кератоз, акантоз, черный акантоз, папулезный сливающийся папилломатоз, невусы, включая, например, дермальные невусы, эпидермальные невусы, сложные невусы, ILVEN (воспалительные линейные бородавчатые эпидермальные невусы), сальный невус, фолликулярный кератоз, и т.п.; угри, например, комедоны, воспалительные угри, папулезные угри, пустулезные угри, кистозные угри; кисты, например, эпидермоидные кисты, милиум, атеромы, фолликулярные кисты, пролиферирующие кисты, дермоидные кисты, пилонидальные кисты, апокринные кисты, экзокринные кисты, кисты сальной железы, слизистые кисты, миксоидные кисты, ганглиевые кисты, синовиальные кисты, кисты пушковых волос, стеатоцистома, гидроцистома; неоплазии придатков, например, трихофолликулома, фиброфолликулома, перифолликулярная фиброма, триходискома, сальный невус, хондроидная сирингома, трихоэпителиома, трихобластома, десмопластическая трихоэпителиома, пиломатриксома (pilomatricoma), пиломатрикальная карцинома, трихолеммома, трихолеммальная карцинома, опухоль фолликулярной воронки, трихоаденома (tricoadenoma), пролиферирующая волосяная опухоль, сальная гиперплазия, сальная аденома, сальная эпителиома, сальная карцинома, сирингома, порома, гидраденома, апокринная гидраденома, спираденома, цилиндрома, эккринный невус (эккринная гамартома), папиллярная аденома, папиллярная аденокарцинома; доброкачественные меланоцитарные пролиферации или неоплазмы, например, веснушки, пятна цвета кофе с молоком, меланоз Беккера, лентигиноз, солнечный лентигиноз, простое лентиго, мукозальные меланоцитарные поражения, монгольские пятна, невус Ота, голубой невус, обычные приобретенные меланоцитарные невусы (новоклеточный невус, ʺродимые пятнаʺ), врожденные невусы, плоская родинка, рецидивные невусы; сосудистые и периваскулярные неоплазмы и реактивные гиперплазии например, гемангиомы, сенильные гемангиомы, мишенеподобные гемосидеротические гемангиомы, пучковые капиллярные ангиомы, гемангиоэндотелиомы, ангиолимфоидная гиперплазия с эозинофилией (ALHE), гломусные опухоли (гломангиомы), гемангиоперицитомы; кожные нервные и нейроэндокринные неоплазии, например, нейромы, шванномы, нейрофибромы, опухоль периневрия, миксома периневрия, нейротекеома, зернисто-клеточная опухоль; фиброзные и фиброгистиоцитарные пролиферации, например, мягкие бородавки, фиброэпителиальные полипы, фибромы, фиброзные папулы, ангиофибромы, перламутровые папулы полового члена, околоногтевые фибромы, дерматофибромы, фиброкератомы, склеротические или плеоморфные фибромы, соединительнотканные невусы; кожные шрамы, гиперплазии, келоиды, розовые угри, кожные грибковые, дерматофитные и плесневые инфекции, онихомикоз, гиперпигментация, преждевременные морщины, псориаз, злокачественная меланома, себорейный кератоз, варианты себорейного кератоза, включая, например, черный папулезный дерматоз, обратный фолликулярный кератоз/кератома, бородавчатый дискератоз/бородавчатая дискератома, бородавчатый акрокератоз, «штукатурный» кератоз; или их комбинация.
Некоторые варианты реализации описывают способ лечения бородавок, включающий введение композиции, содержащей до около 50% пероксида водорода и спирт, нуждающемуся в этом субъекту.
Некоторые варианты реализации описывают способ лечения себорейного кератоза, включающий введение композиции, содержащей до около 50% пероксида водорода и спирт, нуждающемуся в этом субъекту. В некоторых вариантах реализации, спирт присутствует в количестве, способном снижать поверхностное натяжение композиции. В некоторых вариантах реализации, спирт присутствует в количестве, способном повышать смачиваемость поверхности кожи или поражения кожи. В некоторых вариантах реализации, спирт присутствует в количестве, способном повышать проницаемость композиции в кожу субъекта и/или кожное поражение. В некоторых вариантах реализации, спирт присутствует в количестве, способном увеличивать клиническую эффективность композиции. В некоторых вариантах реализации, спирт присутствует в количестве, способном увеличивать клиническую эффективность композиции при поддержании стабильности, достаточной для коммерчески жизнеспособной композиции.
Некоторые варианты реализации настоящего изобретения касаются композиции раствора для местного применения, содержащей до около 50% пероксида водорода и спирт. В некоторых вариантах реализации, раствор состоит из двух или больше частей, которые должны быть смешаны во время применения или непосредственно перед ним.
Некоторые варианты реализации настоящего изобретения касаются гелевой композиции, содержащей до около 50% пероксида водорода, спирт, и гелеобразующий агент. В некоторых вариантах реализации, гелевая композиция состоит из двух или больше частей, которые могут быть смешаны во время применения или непосредственно перед ним.
Некоторые варианты реализации настоящего изобретения описывают композицию, состоящую по существу из до около 50% пероксида водорода и спирта. Некоторые варианты реализации настоящего изобретения описывают композицию, состоящую из до около 50% пероксида водорода и спирта. В некоторых вариантах реализации, спирт представляет собой первичный спирт, вторичный спирт, третичный спирт, или их комбинацию. В некоторых вариантах реализации, спирт не является 1-пропанолом, этанолом, бутанолом, пентанолом, гексанолом, октнолом, нонанолом, деканолом, 2-бутанолом, 2-пентанолом или бензиловым спиртом. В некоторых вариантах реализации, спирт представляет собой 2-пропанол.
Некоторые варианты реализации настоящего изобретения касаются устройств для введения композиций по вариантам реализации настоящего изобретения. В некоторых вариантах реализации, устройства могут включать аппликатор, предназначенный для безопасной и эффективной доставки композиций в соответствии с вариантами реализации настоящего изобретения на целевой (участок) кожи пациента. Некоторые варианты реализации настоящего изобретения включают аппликатор, предназначенный для хранения и дозирования композиции для местного применения, содержащей агент, выбранный из едкого вещества, нестабильного вещества или их комбинации, причем аппликатор содержит хрупкую ампулу, содержащую находящееся в ней вещество, корпус аппликатора содержит размещенную в нем хрупкую ампулу; втулка аппликатора находится в жидкостном сообщении с корпусом аппликатора; на проксимальном конце втулки аппликатора расположен кончик; и фильтр расположен между хрупкой ампулой и кончиком. В некоторых вариантах реализации, композиция для местного применения содержит от около 25% до около 50% пероксида водорода и до 5% 2-пропанола. В некоторых вариантах реализации, агент содержит от около 25% пероксида водорода до около 50% пероксида водорода. В некоторых вариантах реализации, хрупкая ампула дополнительно содержит до 5% 2-пропанола. В некоторых вариантах реализации, корпус аппликатора дополнительно содержит дополнительный ингредиент композиции для местного применения, размещенный внутри него, причем агент высвобождается из хрупкой ампулы в результате разрушения хрупкой ампулы и смешивается с дополнительным ингредиентом в корпусе аппликатора перед нанесением композиции для местного применения. В некоторых вариантах реализации, композиция для местного применения высвобождается из хрупкой ампулы в результате разрушения хрупкой ампулы и протекает через корпус аппликатора, фильтр, и вытекает из аппликатор через кончик. В некоторых вариантах реализации, аппликатор дополнительно содержит зону давления, расположенную на внешней поверхности корпуса аппликатора, для указания участка корпуса аппликатора, к которому должно быть приложено давление для раздавливания хрупкой ампулы.
Некоторые варианты реализации касаются аппликатора, предназначенного для хранения и дозирования композиции для местного применения, содержащей от около 25% до около 50% пероксида водорода и до 5% 2-пропанола, причем аппликатор содержит хрупкую ампулу с находящейся в ней композицией для местного применения, корпус аппликатора содержит размещенную в нем хрупкую ампулу, втулка аппликатора находится в жидкостном сообщении с корпусом аппликатора, кончик расположен на проксимальном конце корпуса аппликатора; и фильтр расположен между хрупкой ампулой и кончиком. В некоторых вариантах реализации, хрупкая ампула сформована из по меньшей мере одного материала из стекла, пластика, боросиликатного стекла, боросиликатного стекла типа 1, и окрашенного стекла. В некоторых вариантах реализации, корпус аппликатора сформован из полипропилена, полиэтилена высокой плотности, полиэтилена низкой плотности, поливинилхлорида, полиэтилена, или их комбинации. В некоторых вариантах реализации, фильтр предназначен для задерживания осколков раздавленной хрупкой ампулы и пропускания композиции для местного применения. В некоторых вариантах реализации, фильтр сформован из по меньшей мере одного материала из полипропилена, полиэтилена высокой плотности, полиэтилена низкой плотности, полиэтилена, полистирола, керамического материала, пеноматериала, песка, диатомовой земли и бумажных волокон.
Некоторые варианты реализации касаются способа лечения кожного состояния, включающего введение композиции для местного применения, содержащей до 50% пероксида водорода и до 5% 2-пропанола, используя аппликатор, содержащий хрупкую ампулу с находящейся внутри нее композицией для местного применения, корпус аппликатора содержит размещенную в нем хрупкую ампулу, втулка аппликатора находится в жидкостном сообщении с корпусом аппликатора, на проксимальном конце втулки аппликатора расположен кончик, и фильтр расположен между хрупкой ампулой и кончиком. В некоторых вариантах реализации, введение композиции для местного применения включает приложение надавливающего усилия к внешней поверхности корпуса аппликатора для дозирования композиции. В некоторых вариантах реализации, введение композиции для местного применения включает введение в контакт кончика с целевым поражением, вызванным кожным состоянием, причем композиция для местного применения дозируется через кончик на участок целевого поражения. В некоторых вариантах реализации, введение композиции для местного применения дополнительно включает приложение давления к зоне давления, расположенной на внешней поверхности корпуса аппликатора, вызывающего разрушение хрупкой ампулы. В некоторых вариантах реализации, введение композиции для местного применения включает действие, вызывающее разрушение хрупкой ампулы и высвобождение композиции для местного применения через кончик; и введение в контакт кончика с целевым поражением, вызванным кожным состоянием.
В некоторых вариантах реализации, аппликатор может содержать хрупкую ампулу, предназначенную для хранения композиций в соответствии с вариантами реализации настоящего изобретения, размещенную внутри корпуса аппликатора. В некоторых вариантах реализации, ампула может быть сформована из стекла или других подобных хрупких материалов, таких как боросиликатное стекло. В некоторых вариантах реализации, корпус аппликатора может быть сформован из различных гибких материалов, включая, без ограничений, полиэтилен высокой плотности (ПЭВП), полиэтилен низкой плотности (ПЭНП) или их различные комбинации или смеси. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения могут быть высвобождены из ампулы путем приложения давления вручную (например, ʺсдавливанияʺ) к корпусу аппликатора в направлении к ампуле, достаточного для того, чтобы вызвать разрушение ампулы. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения, высвобождающиеся из ампулы, могут проходить через фильтр, предназначенный для задерживания стеклянных осколков разбитой ампулы и пропускания композиций в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, по меньшей мере одна часть аппликатора может содержать гидрофобный материал, такой как фильтр и/или кончик. В некоторых вариантах реализации, гидрофобный материал состоит из полиэфирных полимеров или сополимеров, акриловой смолы, модифицированной акриловой смолы (например, модакриловой), полипропилена, полиэтилена или их комбинаций или смесей. Неограничительные примеры гидрофобных материалов могут также включать материалы, содержащие, имеющие покрытия из, и/или модифицированные силанами, алкилсиланами, фторалкилсиланами, силиконом, их комбинациями, и их производными. В некоторых вариантах реализации, гидрофобные части аппликатора могут выполнять функции препятствования, уменьшения, ограничения, предотвращения и/или предотвращения в значительной степени вытекания композиций в соответствии с вариантами реализации настоящего изобретения, высвобождающихся из ампулы, через части аппликатора и/или из кончика аппликатора. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения могут вытекать через фильтр и из аппликатора через кончик аппликатора для нанесения на кожу пациента. В некоторых вариантах реализации, кончик может включать распушенный участок, сформированный из волокон различных химически совместимых и нереакционноспособных материалов, таких как нейлон.
ОПИСАНИЕ ФИГУР
Фигура 1 изображает среднее кумулятивное количество пероксида водорода, высвобождаемой на единицу площади через силиконовую мембрану (мкг/см2) после нанесения всех композиций, содержащих 40% мас./мас. пероксида водорода. Каждая точка временной зависимости представляет собой среднее значение ± стандартное отклонение (SD) (n=5-6).
Фигура 2 изображает среднее кумулятивное количество пероксида водорода, высвобождаемой на единицу площади через силиконовую мембрану (мкг/см2) после нанесения композиций 40% мас./мас. пероксида водорода, содержащих 1-пропанол. Каждая точка временной зависимости представляет собой среднее значение ± SD (n=5-6).
Фигура 3 изображает среднее кумулятивное количество пероксида водорода, высвобождаемой на единицу площади через силиконовую мембрану (мкг/см2) после нанесения композиций 40% мас./мас. пероксида водорода, содержащих 2-пропанол. Каждая точка временной зависимости представляет собой среднее значение ± SD (n=5-6).
Фигура 4 изображает установившийся режим высвобождения пероксида водорода, рассчитанный между 0,5 и 4 ч (мкг/см2/ч) после нанесения композиций пероксида водорода с разными уровнями содержания пропанола. Каждая точка данных представляет собой среднее значение ± SD, n=5-6.
Фигура 5 изображает разность при установившемся режиме высвобождения пероксида водорода (Поток [1-пропанол] - Поток [2-пропанол]) для 5, 10, 15 и 20% мас./мас. (1-пропанол и 2-пропанол).
Фигура 6 изображает среднее поверхностное натяжение (мН/м) разных анализируемых композиций пероксида водорода, содержащих 1- или 2-пропанол.
Фигура 7 изображает шкалу оценок и описания для балльной оценки улучшения состояния бородавок (Wart Improvement Assessment) и балльной оценки тяжести бородавок (Wart Severity Assessment).
Фигура 8 изображает средний балл улучшения состояния (при лечении) бородавок по посещениям.
Фигура 9 изображает среднее изменение значения базовой линии при оценке тяжести бородавок по посещениям.
Фигура 10 изображает окислительно-восстановительный потенциал (мВ) всех композиций 40% мас./мас. пероксида водорода, содержащих 1- и 2-пропанол, в присутствии кожи и без нее, в моменты времени t=0, 1, 6 и 24 ч. Каждая точка временной зависимости представляет собой среднее значение ± диапазон предельных значений, n=3.
Фигура 11 изображает окислительно-восстановительный потенциал (мВ) композиций 40% мас./мас. пероксида водорода, содержащих 5% мас./мас. 1- или 2-пропанола, с кожей и без нее, в моменты времени t=0, 1, 6 и 24 ч. Каждая точка временной зависимости представляет собой среднее значение ± диапазон предельных значений, n=3.
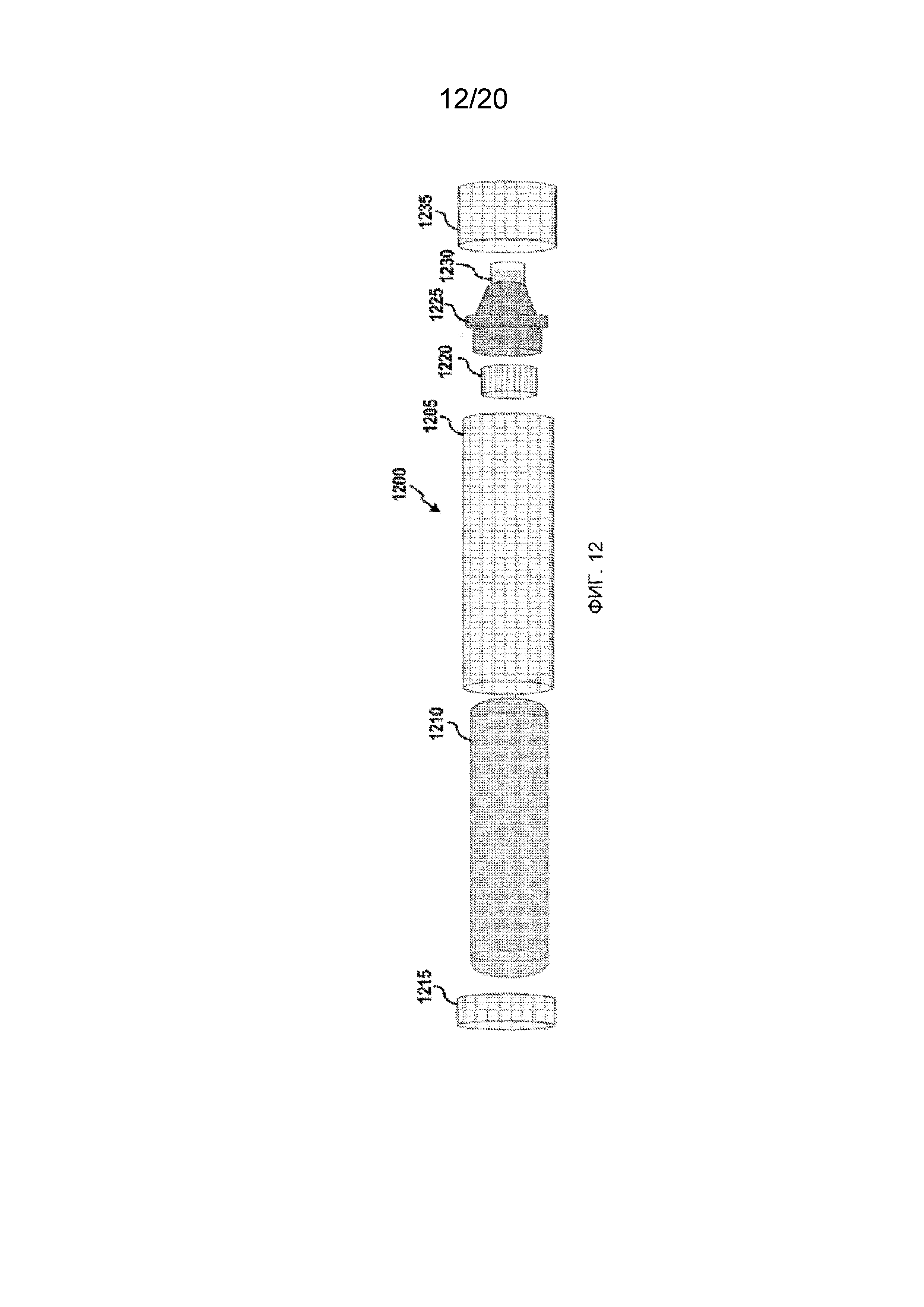
Фигура 12 изображает иллюстративный пример аппликатора в соответствии с первым вариантом реализации.
Фигуры 13A-13C изображают иллюстративный пример аппликатора в соответствии со вторым вариантом реализации.
Фигуры 14A и 14B изображают различные виды иллюстративного примера корпуса аппликатора в соответствии с некоторыми вариантами реализации.
Фигура 15 изображает иллюстративный пример торцевой крышки аппликатора в соответствии с некоторыми вариантами реализации.
Фигура 16 изображает иллюстративный пример перфорированного распушеннего кончика (или ʺвтулки аппликатораʺ) в соответствии с некоторыми вариантами реализации.
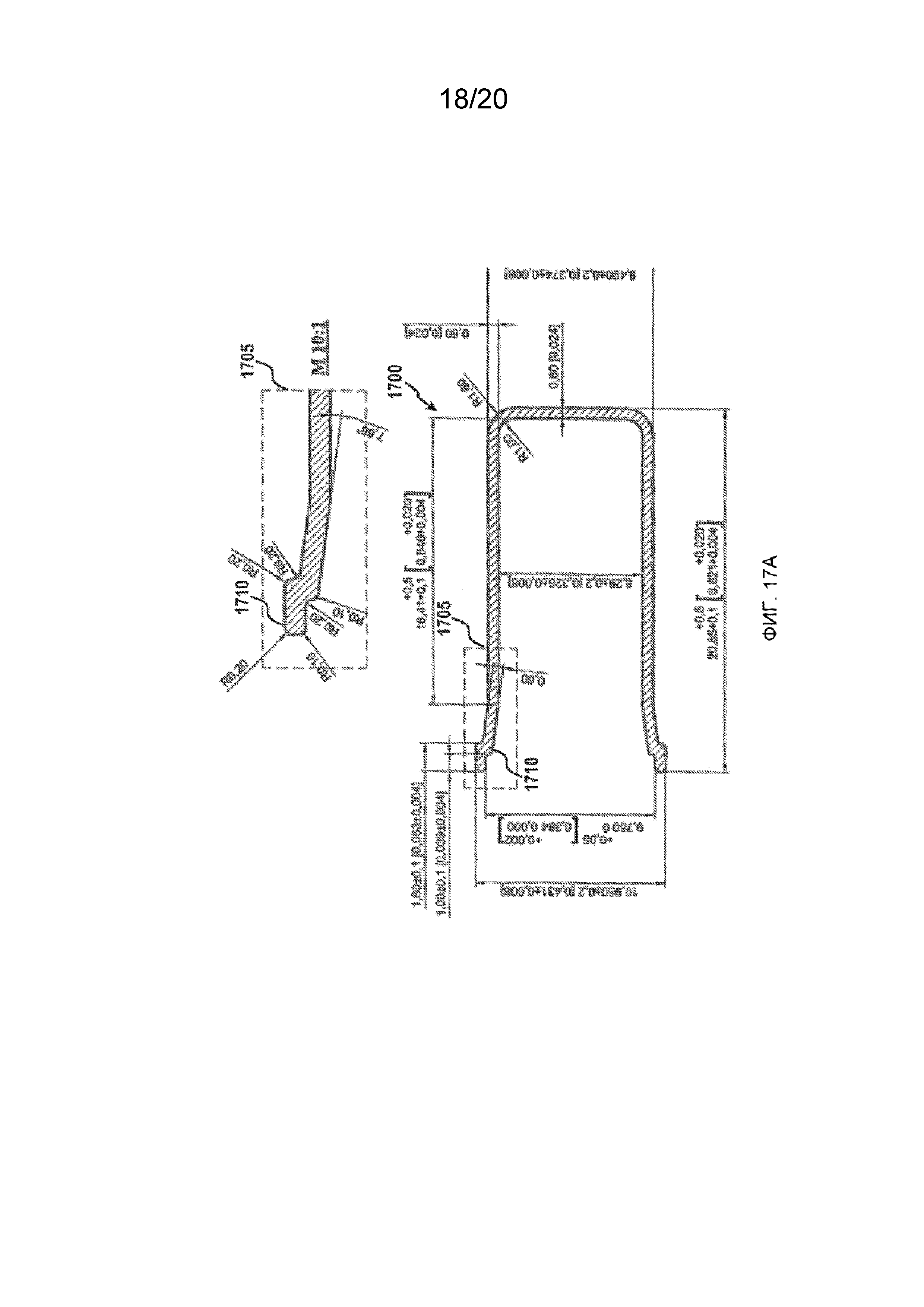
Фигуры 17A и 17B изображают иллюстративный пример защитного колпачка в соответствии с первым вариантом реализации.
[1] Фигуры 18A и 18B изображают иллюстративный пример защитного колпачка в соответствии со вторым вариантом реализации.
ДЕТАЛЬНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Перед описанием композиций и способов по настоящему изобретению укажем, что следует понимать, что данное изобретение не ограничено конкретно описанными процессами, композициями или методиками, которые могут меняться. Также следует понимать, что терминология, использованная в описании, предназначена только для описания конкретных версий или вариантов реализации, и не должна ограничивать объем настоящего изобретения, который будет ограничиваться только прилагаемой формулой изобретения. Если не указано иное, все технические и научные термины, используемые в данном документе, имеют значения, общеизвестные рядовым специалистам в данной области техники. Хотя любые способы и материалы, аналогичные или эквивалентные описанным в данном документе могут быть использованы в практике или при тестировании вариантов реализации настоящего изобретения, здесь описаны предпочтительные способы, устройства и материалы. Все публикации, упоминаемые в данном документе, включены в качестве ссылок в полном объеме. Ничто в данном документе не должно истолковываться как допущение, что изобретение не имеет права предвосхищать такое раскрытие на основании предшествующего изобретения.
[2] Следует отметить, что существительное в единственном числе подразумевает также и множественное число, если из контекста однозначно не следует иное. Таким образом, например, ссылка на ʺкожное поражениеʺ указывает на одно или более кожных поражений и их эквивалентов, известных квалифицированным специалистам в данной области техники, и т.д.
В используемом в данном документе значении, термин ʺоколоʺ означает плюс или минус 10% от численного значения, с которым он используется. Поэтому, около 50% означает диапазон значений 45%-55%.
ʺВведениеʺ, при использовании в сочетании с лекарственным средством, означает введение лекарственного средства непосредственно в или на ткань-мишень или введение лекарственного средства субъекту, в результате которого лекарственное средство положительно влияет на ткань, на которую оно нацелено. Таким образом, в используемом в данном документе значении, термин ʺвведениеʺ, при использовании в сочетании с лекарственным средством, может включать, без ограничений, доставку лекарственного средства субъекту системно, например, путем внутривенной инъекции, в результате которой лекарственное средство достигает ткани-мишени. Введение композиции или лекарственного средства может осуществляться, например, с помощью инъекции, перорального введения, местного применения, или этими способами в комбинации с другими известными методами. Такие комбинированные методы могут включать нагревание, облучение, ультразвук и использование агентов доставки. Предпочтительно, введение представляет собой самовведение, когда лекарственное средство или композиция вводится самим субъектом. Альтернативно, введение субъекту может осуществляться поставщиком медицинских услуг.
ʺОбеспечениеʺ, при использовании в сочетании с лекарственным средством, означает введение лекарственного средства непосредственно в или на ткань-мишень, или введение лекарственного средства субъекту, в результате которого лекарственное средство положительно воздействует на ткань, на которую оно нацелено.
Термин ʺживотноеʺ, в используемом в данном документе значении, включает, без ограничений, людей и не являющихся человеком прозвоночных, таких как дикие, домашние и сельскохозяйственные животные.
Термин ʺпациентʺ или ʺсубъектʺ, в используемом в данном документе значении, обозначает животное, в частности, человека, страдающего от нежелательной болезни или состояния, поддающихся лечению лекарственным средством и/или композициями, описанными в данном документе.
Термин ʺулучшаетʺ используется для указания того, что варианты реализации, предусматриваемые в данном документе, изменяют характеристики и/или физические признаки ткани, по отношению к которой терапевтическая композиция доставляется, наносится или вводится. Термин ʺулучшаетʺ может также быть использован в сочетании с болезненным состоянием таким образом, чтобы при ʺулучшенииʺ болезненного состояния симптомы или физические характеристики, ассоциированные с болезненным состоянием, уменьшались, ослабевали или исчезали.
Термин ʺингибированиеʺ обычно относится к предотвращению начала проявления симптомов, облегчению симптомов, или устранению болезни, состояния или расстройства.
ʺНеобязательныйʺ или ʺнеобязательноʺ означает, что описанные далее событие или обстоятельство могут произойти или не произойти, и что описание включает случаи, когда указанное событие происходит, и случаи, когда оно не происходит.
В используемом в данном документе значении, ʺкомнатная температураʺ означает температуру в помещении от около 20°C до около 25°C (68-77 °F).
В описании заявки используются различные термины, такие как ʺпервичныйʺ, ʺвторичныйʺ, ʺпервыйʺ, ʺвторойʺ и т.п. Эти термины являются словами, используемыми для удобства различения разных элементов, и такие термины не являются ограничительными в отношении возможного использования разных элементов.
ʺФармацевтически приемлемыйʺ, ʺфизиологически переносимыйʺ и их грамматические варианты, по отношению к композициям, носителям, разбавителям и реагентам или другим ингредиентам композиции, могут использоваться взаимозаменяемо и указывают на то, что материалы могут быть введены без возникновения нежелательных физиологических эффектов, таких как сыпь, жжение, раздражение или другие нежелательные эффекты, с интенсивностью, непереносимой для реципиента.
В используемом в данном документе значении, термин ʺкосметически приемлемыйʺ и его грамматические варианты, по отношению к композициям, носителям, разбавителям и реагентам или другим ингредиентам композиции, указывает, что используемые материалы и готовая композиция не являются раздражающими или иначе вредными для пациента в общем и для кожи в частности, и предпочтительно, создают приятные ощущения и хорошо переносятся по показателям общего вида, pH, цвета, запаха и текстуры (ощущений на ощупь), и что они не являются, например, неприемлемо липкими (клейкими), жирными или сушащими, и что они легко намазываются, впитываются в кожу с приемлемой скоростью впитывания, и в общем обладают увлажняющей способностью.
В используемом в данном документе значении, термин ʺлекарственное средствоʺ означает агент, используемый для лечения, борьбы, облегчения, предотвращения или улучшения нежелательного состояния или болезни субъекта. В частности, варианты реализации, описанные в данном документе, могут касаться лечения различных кожных болезней, состояний или расстройств или их симптомов, включая, без ограничений, доброкачественные пролиферации, неоплазмы, предопухолевые состояния или злокачественные опухоли кожи. Кожное состояние может быть вирусно-индуцированным или не-вирусно-индуцированным ростом или пролиферацией кожной ткани. Кожное состояние может быть воспалительным состоянием. Кожное состояние может быть гиперпролиферативным состоянием. Кожное состояние может быть старением, включая изменения, вызванные внутренними факторами и внешними воздействиями (например, фотостарение (изменения, индуцированные воздействием ультрафиолетовых лучей)), пигментные изменения, мелкие морщинки и преждевременное появление морщин на лице. В некоторых вариантах реализации, кожное состояние может быть выбрано из поражений, индуцированных вирусом папилломы человека, например, таких как бородавки, обыкновенные бородавки, ладонно-подошвенные бородавки, плоские бородавки, периодические бородавки, не поддающиеся лечению бородавки, бородавки, лечение которых ранее не проводилось, бородавки, связанные с верруциформной эпидермодисплазией, аногенитальные бородавки, остроконечная кондилома, цервикальные дисплазии или неоплазии, например, цервикальная интраэпителиальная неоплазия (CIN); поражений, вызванных герпесвирусом, включая индуцированные HHV-1 (HSV-1), HHV-2 (HSV-2), HHV-3 (вирус varicella zoster) например, ветряная оспа, опоясывающий герпес, опоясывающий лишай; поражений, индуцированных поксвирусом например, контагиозный моллюск, контагиозный пустулезный дерматит; мозоль, кожные рога, ороговевшей мозоли, мягкие бородавки, фиброэпителиальные полипы, узловатая почесуха Гайда, старческие кератозы, плоскоклеточная карцинома, плоскоклеточная карцинома in situ, кератоакантома, базальноклеточная карцинома, кожные лимфомы и доброкачественные лимфоцитарные инфильтраты и гиперплазии кожи, светлоклеточная акантома, крупноклеточная акантома, эпидермолитическая акантома, порокератоз, гиперкератоз, фолликулярный кератоз, лихеноидный кератоз, акантоз, черный акантоз, папулезный сливающийся папилломатоз, невусы, включая например, дермальные невусы, эпидермальные невусы, сложные невусы, ILVEN (воспалительные линейные бородавчатые эпидермальные невусы), сальный невус, фолликулярный кератоз, и т.п.; угри, например, комедоны, воспалительные угри, папулезные угри, пустулезные угри, кистозные угри; кисты, например, эпидермоидные кисты, милиум, атеромы, фолликулярные кисты, пролиферирующие кисты, дермоидные кисты, пилонидальные кисты, апокринные кисты, экзокринные кисты, кисты сальной железы, слизистые кисты, миксоидные кисты, ганглиевые кисты, синовиальные кисты, кисты пушковых волос, стеатоцистома, гидроцистома; неоплазии придатков например, трихофолликулома, фиброфолликулома, перифолликулярная фиброма, триходискома, сальный невус, хондроидная сирингома, трихоэпителиома, трихобластома, десмопластическая трихоэпителиома, пиломатрикома, пиломатрикальная карцинома, трихолеммома, трихолеммальная карцинома, опухоль фолликулярной воронки, трикоаденома, пролиферирующая волосяная опухоль, сальная гиперплазия, сальная аденома, сальная эпителиома, сальная карцинома, сирингома, порома, гидраденома, апокринная гидраденома, спираденома, цилиндрома, эккринный невус (эккринная гамартома), папиллярная аденома, папиллярная аденокарцинома; доброкачественные меланоцитарные пролиферации или неоплазмы, например, веснушки, пятна цвета кофе с молоком, меланоз Беккера, лентигиноз, солнечный лентигиноз, простое лентиго, мукозальные меланоцитарные поражения, монгольские пятна, невус Ота, голубой невус, обычные приобретенные меланоцитарные невусы (новоклеточный невус, ʺродимые пятнаʺ), врожденные невусы, плоская родинка, рецидивные невусы; сосудистые и периваскулярные неоплазмы и реактивные гиперплазии например, гемангиомы, сенильные гемангиомы, мишенеподобные гемосидеротические гемангиомы, пучковые капиллярные ангиомы, гемангиоэндотелиомы, ангиолимфоидная гиперплазия с эозинофилией (ALHE), гломусные опухоли (гломангиомы), гемангиоперицитомы; кожные нервные и нейроэндокринные неоплазмы, например, нейромы, шванномы, нейрофибромы, опухоль периневрия, миксома периневрия, нейротекеома, зернисто-клеточная опухоль; фиброзные и фиброгистиоцитарные пролиферации, например, мягкие бородавки, фиброэпителиальные полипы, фибромы, фиброзные папулы, ангиофибромы, перламутровые папулы полового члена, околоногтевые фибромы, дерматофибромы, фиброкератомы, склеротические или плеоморфные фибромы, соединительнотканные невусы; кожные шрамы, гиперплазии, келоиды, розовые угри, кожные грибковые, дерматофитные и плесневые инфекции, онихомикоз, гиперпигментация, преждевременное появление морщин на лиц, псориаз, злокачественная меланома, себорейный кератоз, варианты себорейного кератоза, включая, например, черный папулезный дерматоз, обратный фолликулярный кератоз/кератома бородавчатый дискератоз/бородавчатая дискератома, бородавчатый акрокератоз, «штукатурный» кератоз; или их комбинация.
В используемом в данном документе значении, термин ʺстабилизированный пероксид водородаʺ относится к пероксиду водорода, содержащему стабилизатор или смесь стабилизаторов, пригодных для разбавления пероксида водорода до концентрации, которая может быть включена в стабильную коммерческую композицию для местного применения при кожных поражениях для лечения кожных состояний, описанных в данном документе. В некоторых вариантах реализации, пероксид водорода может быть получен из коммерческого источника. Количество и тип стабилизатора (стабилизаторов), используемых в композиции пероксида водорода, могут быть патентованной собственностью и/или коммерческой тайной коммерческого источника. В некоторых вариантах реализации, стабилизированный пероксид водорода представляет собой пероксид водорода высокой концентрации. Хотя чистые пероксид водорода высокой концентрации типично являются стабильными, стабилизаторы могут быть использованы в композициях пероксида водорода, обычно, полученных из коммерческих источников, для стабилизации разбавленных вариантов ʺвысококонцентрированнойʺ композиции пероксида водорода. Некоторые композиции пероксида водорода содержат стабилизаторы в концентрации (общей и/или по отдельности), достаточной для обеспечения стабилизации разбавленного пероксида водорода для конкретных областей применения или в конкретных отраслях промышленности. В некоторых вариантах реализации, стабилизированный пероксид водорода имеет разрешение Управления по контролю за пищевыми продуктами и медикаментами США (Food and Drug Administration, FDA) на местное применение для людей. В некоторых вариантах реализации, стабилизированная пероксид водорода имеет файл нормативно-справочной информации FDA и была допущена FDA для местного применения у людей.
В используемом в данном документе значении, термин ʺклиническая эффективностьʺ относится к способности ингредиента или композиции вызывать желательный эффект. Например, в некоторых вариантах реализации, желательный эффект может включать, без ограничений, снижение поверхностного натяжения композиции, повышение смачиваемости поверхности кожи или поражения кожи, повышение проницаемости композиции в кожу субъекта, кожное поражение или неровности поверхности, включая бороздки, выпячивания и неровности кожи или поражения кожи, уменьшение размера поражения-мишени, улучшение формы и/или внешнего вида поражения-мишени, улучшение поражения-мишени или обрабатываемого участка и/или удаление поражения-мишени, или их комбинацию.
Термины ʺтерапевтически эффективныйʺ или ʺэффективныйʺ, в используемом в данном документе значении, могут использоваться взаимозаменяемо и относятся к количеству терапевтической композиции в соответствии с вариантами реализации, описанными в данном документе. Например, терапевтически эффективное количество композиции представляет собой количество композиции и, в частности, активного ингредиента, такого как пероксид водорода, которое обычно обеспечивает достижение желательного эффекта.
ʺТерапевтически эффективное количествоʺ или ʺэффективное количествоʺ композиции представляет собой количество, необходимое или достаточное для достижения желательного результата. Активность, предусматриваемая вариантами реализации настоящего изобретения, включает медико-терапевтическую, косметико-терапевтическую и/или профилактическое лечение, в зависимости от необходимости. Конкретная доза соединения, введенного в соответствии с вариантами реализации настоящего изобретения для достижения терапевтических и/или профилактических эффектов будет, конечно, определяться конкретными обстоятельствами случая, включая, например, введенное соединение, путь введения и состояние, лечение которого проводится. Однако, эффективное для введения количество может быть определено специалистом-практиком или производителем или пациентом с учетом соответствующих обстоятельств, включая состояние, лечение которого проводится, выбор соединения для введения и выбранный путь введения, и поэтому вышеуказанные диапазоны дозировок не должны каким-либо образом ограничивать объем изобретения. Терапевтически эффективное количество соединения в соответствии с вариантами реализации настоящего изобретения типично представляет собой количество, которое при введении в композиции с физиологически переносимым вспомогательным веществом, является достаточной для достижения эффективной системной концентрации или местной концентрации в или на ткани для достижения желательного терапевтического или клинического результата.
Термины ʺлечитьʺ, ʺполучающий лечениеʺ или ʺлечениеʺ, в используемом в данном документе значении, относится к терапевтическому лечению, косметическому лечению и/или профилактическим или предупредительным мерам, целью которых является предотвращение или замедление (ослабление) нежелательного физиологического состояния, расстройства или болезни, или достижение благоприятных или желательных клинических результатов. В целях данного описания, благоприятные или желательные клинические результаты включают, без ограничений, облегчение симптомов; ослабление тяжести состояния, расстройства или болезни; стабилизация (т.е., отсутствие ухудшения) показателей состояния, расстройства или болезни; задержка начальных проявлений или замедление прогрессирования состояния, расстройства или болезни; улучшение показателей состояния, расстройства или болезни; и ремиссия (частичная или полная), детектируемая или недетектируемая, или коррекция или улучшение состояния, расстройства или болезни. Лечение включает достижение клинически значимого отклика без чрезмерных уровней побочных эффектов.
В используемом в данном документе значении, термин ʺсостоит изʺ или ʺсостоящий изʺ означает, что композиция или способ включают только элементы, стадии или ингредиенты, конкретно указанные в конкретном заявляемом варианте реализации или пункте формулы.
В используемом в данном документе значении, термин ʺсостоящий по существу изʺ или ʺсостоит по существу изʺ означает, что композиция или способ включают только указанные материалы или стадии, и те, которые существенно не влияют на основные и новые характеристики заявляемого изобретения.
В общем, термин ʺтканьʺ относится к любому скоплению клеток схожей специализации, которые вместе выполняют определенную функцию.
Себорейный кератоз (СК) представляет собой одну из наиболее распространенных кожных опухолей у человека. Такие доброкачественные эпителиальные кожные опухоли наиболее часто встречаются у особ пожилого возраста, их распространенность увеличивается с возрастом, и они поражают мужчин и женщин около в равных пропорциях. Новообразования могут быть одиночными или возникать в больших количествах и типично имеют вид хорошо разграниченных, приподнятых или ʺналепленныхʺ папул или бляшек, которые могут различаться по окраске, например, от телесного цвета до оттенков желтого, серого, коричневого или черного. Несмотря на свою доброкачественность, они часто причиняют беспокойство пациентам с косметической точки зрения, иногда требуют определения отличия от других доброкачественных или злокачественных кожных опухолей, и могут становиться симптоматическими. Они могут вызывать зуд, раздражение, кровоточить, и могут быть болезненными при травмах, особенно если они расположены в местах, подверженных трению и травмам, таких как линия пояса и линии бретелей бюстгальтера.
Пациенты могут стремиться к лечению СК по косметическим причинам, особенно когда они являются большими, пигментированными, и/или в случае присутствия множественных поражений, или просто потому, что поражения обычно ассоциируются с пожилым возрастом. Однако, удаление может иметь медицинские показания, для поражений, которые становятся раздраженными, зудящими, воспаленными или болезненными, или для поражений, которые, по мнению врача. требуют гистологического подтверждения диагноза.
Существуют многочисленные хирургические варианты лечения СК, которые включают изобилие деструктивных/абляционных модальностей, таких как, например, криотерапия жидким азотом, фульгурация, лазеры с различными длинами волн (абляционные и неабляционные), радиочастотная абляция, дермабразия, и хирургическое удаление путем выскабливания или хирургического иссечения. Существует, однако, заметная нехватка проведенных под надежным контролем клинических испытаний по сравнению эффективности, осложнений и частоты случаев осложнений таких методов лечения. Существует большое разнообразие применяемых практикующими врачами способов, использующих все эти методики (например, различия во времени контакта и методе замораживания поражения жидким азотом) с меняющимися в широких пределах результатами. Ни один из этих методов лечения, в действительности, не был одобрен Управлением по контролю за пищевыми продуктами и медикаментами США (FDA) для лечения себорейного кератоза. Хотя эти способы могут обеспечивать показатели эффективности лечения, многие из них требуют специальной подготовки и использования дорогого оборудования, они являются болезненными и могут требовать анестезии и/или обезболивания, и они часто дают осложнения в виде значительных неблагоприятных косметических результатов. Широко распространены как гипопигментация, так и гиперпигментация, которые могут быть преходящими, но часто являются постоянными, а также рубцевание на месте проведения лечения, и типичные постхирургические риски кровотечения и инфекции увеличивают риск того, что результат лечения этих поражений может быть хуже самой болезни.
Предпринимались многочисленные попытки местного лечения СК, однако ни один их методов местного лечения не продемонстрировал постоянной эффективности. Например, было обнаружено, что лактат аммония является неэффективным. Другие примеры включают нанесение мази кальципотриена, крема тазаротена, крема имиквимода, и Vanicream® раз в сутки в течение 16 недель, которые все показали свою неэффективность. В одном отчете о недокументированном использовании тазаротена 0,1% при нанесении два раза в сутки сообщалось при эффективность только у 7/15 (47%) субъектов, и курс лечения был осложнен ʺощущениями жжения, зуда и покраснениемʺ. Сообщалось о местном применении мази витамина D3 при использовании один или два раза в сутки на протяжении в среднем 7,3 месяцев (в интервале 3-12 месяцев), которое продемонстрировало 80% или больше улучшения поражений только у 30% пациентов. Таким образом, в данной области существует потребность в безопасном и эффективном местном лечении себорейного кератоза.
Бородавки (веррука) представляют собой вирусно-индуцированные поражения, вызываемые субтипами семейства вирусов кожных папиллом человека (ВПЧ). Типы ВПЧ представляют собой подгруппу большой группы семейства ДНК папилломавирусов, способных инфицировать людей и вызыватьь кожные поражения. ВПЧ являются повсеместными в окружающей среде и инфицирование чаще всего происходит в результате прямого контакта с особами, переносящими вирус, с клиническими проявлениями (заметные поражения) или на субклинической стадии, косвенно через контакт с зараженными поверхностями, или путем аутоинокуляции вируса с единичного поражения на прилегающую неинфицированную кожу. Кожные проявления инфекции ВПЧ включают обыкновенные бородавки (verruca vulgaris), ладонно-подошвенные бородавки, мозаичные бородавки, плоские бородавки, бугорки туберкулезного происхождения и другие. Субтипы семейства ВПЧ также являются этиологическими факторами орофарингеальных, аногенитальных, ларингеальнх бородавок, папиллом, дисплазий (например, CIN (цервикальная интраэпителиальная неоплазия) карциномы in situ, карцином, и кожных поражений, наблюдаемых при верруциформной эпидермодисплазии. Обыкновенные бородавки типично представляют собой гиперкератотические экзофитные куполообразные папулы или узелки (типично ассоциированные с ВПЧ типа 1, 2 или 4) и чаще всего расположены на пальцах (включая околоногтевые и подногтевые участки), тыльные поверхности рук, места, предрасположенные к травмам (например, колени, локти), но могут возникать с практически любой другой анатомической локализацией. В некоторых вариантах реализации, кожное состояние может быть доброкачественным новообразованием, предраком или злокачественной опухолью. Кожное состояние может быть воспалительным состоянием. Кожное состояние может быть гиперпролиферативным состоянием. Кожное состояние может быть старением, включая изменения, вызванные внутренними факторами и внешними воздействиями (например, фотостарение (изменения, индуцированные воздействием ультрафиолетовых лучей)), пигментные изменения, мелкие морщинки и преждевременное появление морщин на лице.
Остроконечные бородавки, более известные как генитальные бородавки, типично связаны с ВПЧ типа 6 и 11, 16, 18, и многочисленными другими субтипами (например, 33, 35, 39, 40, 43, 45, 51-56, 58 и другие), и в одном поражении может присутствовать множество субтипов. Остроконечные бородавки типично присутствуют в виде от одиночных до множественных мясистых, мягких, веррукозных папул, которые могут быть куполообразными, нитевидными, грибовидными, ʺрыхлымиʺ (cauliflower-like), или образовывать сливающиеся бляшки. Они типично расположены в аногенитальной области (например, в области пениса, вульвы, влагалища, шейки матки, промежности и перианально), и могут появляться на слизистой оболочке ротоглотки, гортани и даже трахеи, и редко на других участках кожи (например, туловища, конечностей). Поражения типично являются доброкачественными, но некоторые субтипы ВПЧ ассоциированы с риском потенциальной злокачественности (например, субтипы ВПЧ 16, 18) и могут приводить к кожным карциномам или карциномам in-situ, таким как бовеноидный папулез или гигантская остроконечная кондилома (Buschke-Lowenstein tumor), и дисплазиям или неоплазиям шейки матки, например, цервикальной интраэпителиальной неоплазии (CIN).
У иммунокомпетентных индивидуумов, многие обычные кожные поражения, ассоциированные с инфекцией ВПЧ (например, бородавки и кондиломы), самопроизвольно рассасываются в течение менее чем двух лет. Однако, бородавки могут быть большими и/или косметически неприглядными (например, на лице, руках), распространяться на отдаленые анатомические области путем аутоинокуляции, быть болезненными (например, при травмировании или на подощках), и бородавки без лечения создают значительный резервуар инфекции ВПЧ в популяции.
В настоящее время не существует специфических антивирусных терапий для лечения кожной инфекции ВПЧ. Существующие терапии, таким образом, направлены или на прямое физическое разрушение поражений с помощью локально деструктивных способов воздействия, таких как криотерапия, электрохирургия, выскабливание, лазерная терапия, применение кислот (например, салициловой кислоты, трихлоруксусной кислоты); локально цитотоксических терапий, таких как подофиллин для местного применения, кантаридин, или 5-фторурацил для местного применения или в очаге поражения, или блеомицин; местной иммуномодулирующей терапии (например, имиквимод для местного применения, антиген Candida в очаге поражения, дибутиловый эфир квадратной кислоты для местного применения, циметидин перорально), или на хирургическое удаление поражения. Различные виды таких терапий также доступны в виде отпускаемых без рецепта (OTC) средств для лечения бородавок в низких концентрациях (например, препараты салициловой кислоты для местного применения; наборы для "замораживания" в домашних условиях). Хотя такие способы могут обеспечивать показатели эффективности лечения в некоторых случаях, многие из них требуют многократных посещений врача, специальной подготовки и использования дорогого оборудования; они являются болезненными и могут потребовать анестезии и/или обезболивания, и они могут давать осложнения в виде нежелательных косметических результатов, включая рубцевание в месте лечения, и типичные постхирургические риски кровотечения и инфекции. Ни одна из терапий не является стабильно эффективной во всех случаях и, фактически, практикующие врачи используют все эти методики по разному, с большими различиями в результатах. Рецидивы представляют собой обычное явление и для достижения значительного улучшения часто необходимо использование нескольких способов лечения в комбинациях. Таким образом, в данной области существует большая неудовлетворенная потребность в безопасном и эффективном местном способе лечения кожных поражений, ассоциированных с инфекцией ВПЧ, например, бородавок и кондилом.
Моллюски представляют собой вирусно-индуцированные поражения, вызываемые субтипами вирусов контагиозного моллюска (ВКМ) семейства ДНК поксвирусов. Существует четыре субтипа ВКМ, (ВКМ 1-4), причем ВКМ-1 является наиболее распространенным и ВКМ-2 чаще всего встречается у взрослых. Как и ВПЧ, ВКМ распространены повсеместно в окружающей среде и инфицирование чаще всего происходит в результате прямого контакта с особами-переносчиками вируса, имеющими клинические проявления (очевидные поражения) или находящимися на субклинической стадии, опосредованно через зараженные поверхности, или путем аутоинокуляции вируса из индивидуального поражения на прилегающую неинфицированную кожу. Инфекция наиболее распространена в педиатрической популяции, у сексуально активных взрослых, и у лиц с ослабленным иммунитетом. Поражения контагиозного моллюска типично телесного цвета, представляют собой куполообразные с пупкообразным вдавлением (ʺс ямочкойʺ) папулы, которые могут быть расположены по одной или кластерами и типично расположены в паху или на конечностях, хотя могут возникать на любых участках кожи. Индивидуальные поражения могут спонтанно рассасываться в течение периода от нескольких недель до нескольких месяцев, однако, естественное развитие инфекции от появления первого поражения до рассасывания последнего поражения может занимать от шести месяцев до пяти лет или больше.
В настоящее время не существует одобренных Управлением по контролю за пищевыми продуктами и медикаментами США методов лечения контагиозного моллюска. В настоящее время не существует специфических антивирусных терапий для лечения кожной инфекции ВКМ. Существующие методы лечения, таким образом, направлены или на прямое физическое разрушение поражений локально деструктивными методами лечения, такими как криотерапия, электрохирургия, выскабливание, лазерная терапия, иссечение поражения, например, с помощью иглы (препарирование иглой ʺneedle-prickingʺ), нанесение кислот или едких веществ (например, салициловой кислоты, гидроксида калия); локально цитотоксические терапии, такие как (использование) подофиллина для местного применения, кантаридина; местная иммуномодулирующая терапия (например, имиквимод для местного применения, антиген Candida в место поражения, азотная кислота, циметидин перорально), или на хирургическое удаление поражения. Хотя эти способы могут обеспечивать показатели эффективности лечения в некоторых случаях, многие из них требуют многократных посещений врача, специальной подготовки и использования дорогого оборудования; они могут быть болезненными и могут требовать анестезии и/или обезболивания, и могут вызывать беспокойство и быть психологически травмирующими, особенно в педиатрической возрастной группе. Эти методы лечения могут давать осложнения в виде нежелательных косметических результатов, включая пигментные изменения (как гиперпигментация, так и гипопигментация), рубцевание в месте лечения, кровотечение и инфекция. Ни один из методов лечения не является стабильно эффективным во всех случаях и, фактически, разные практикующие врачи по разному применяют способы с использованием всех этих методик с большими различиями в результатах. Часто для достижения значительно улучшения необходимо комбинированное использование нескольких методов лечения, включая лечение лежащих в их основе местных состояний, таких как атопический дерматит, который имеет тенденцию к предрасположенности к моллюску и распространению поражений. Таким образом, в данной области существует большая неудовлетворенная потребность в безопасном и эффективном (местном) способе лечения кожных поражений, ассоциированных с инфекцией ВКМ.
Пероксид водорода (H2O2) представляет собой соединение, повсеместно распространенной в окружающей среде. Она является простейшим пероксидом и сильным окислителем, широко используемым в бесчисленных бытовых товарах, включая бесхлорные отбеливатели, чистящие продукты общего назначения и дезинфицирующие средства, использовалась в качестве окислительного компонента в красителях для волос, и использовалась в продуктах для гигиены полости рта и системах отбеливания зубов на протяжении многих лет. В промышленности, она используется для обработки сточных вод и, в вісоких концентрациях, используется при отбеливании бумаги, целлюлозы и материалов, используемых в текстильном производстве. Клинически, в дополнение к ее использованию в качестве средства для местного применения в полости рта, как было указано выше, пероксид водорода широко применяется при низких концентрациях (например, 3%-6%) в качестве средства для орошения ран и антисептического/дезинфицирующего средства местного действия, и используется в медицине с момента ее введения в клиническую практику Ричардсоном (Richardson) в 1858 г.
Пероксид водорода является важным окислителем в биологических системах. Локальные нежелательные эффекты реакционноспособных форм кислорода на кожу смягчаются присутствием комплексной защитной системы антиоксидантов, которая включает ферменты, такие как каталаза, глутатионпероксидаза, супероксиддисмутаза, тиоредоксинредуктаза, липоамин, липидпероксидаза и другие, а также неферментные компоненты, включая аскорбиновую кислоту, ураты и мочевую кислоту, токоферол, глутатион, убихиноны, убихинол и другие водорастворимые группы. Местное применение пероксида водорода в сверхфизиологических концентрациях может подавлять антиокислительные защитные системы кожи, позволяя пероксиду водорода действовать не только путем прямого окисления органических тканей, генерирования реакционноспособных форм кислорода и локального перекисного окисления липидов, но также путем генерирования локальных концентраций кислорода, являющихся токсичными для аномальных клеток поражений (например, себорейного кератоза, бородавки, остроконечной кондиломы, контагиозного моллюска).
Неожиданно было обнаружено, что как поражения, вызванные себорейным кератозом, так и поражения, вызванные обыкновенной бородавкой (простой бородавкой), демонстрируют клинический отклик после применения композиций в соответствии с вариантами реализации настоящего изобретения. В определенных случаях, выведение поражения кожи наблюдалось после единственного применения. В других случаях, например, при поражениях большей глубины или больших по размеру поражениях, два или больше сеансов применения могут потребоваться для клинического отклика. В качестве типичных примеров полезных эффектов данного способа лечения укажем, что клинический отклик достигается без необходимости обезболивания, без причинения боли, и без индуцирования значительных нежелательных явлений и нежелательных косметических результатов, часто наблюдающихся при других способах лечения, таких как, например, пигментные изменения (таких как гипопигментация или гиперпигментация), рубцевание в месте лечения, кровотечение или инфекция.
Варианты реализации настоящего изобретения в общем касаются композиций, содержащих пероксид водорода и модификатор поверхностного натяжения. В некоторых вариантах реализации, модификатор поверхностного натяжения представляет собой агент, стабильный в композициях, содержащих пероксид водорода в концентрациях, раскрытых в вариантах реализации настоящего изобретения. В некоторых вариантах реализации, модификатор поверхностного натяжения присутствует в количестве, достаточном для повышения терапевтической эффективности композиции. В некоторых вариантах реализации, модификатор поверхностного натяжения присутствует в количестве, достаточном для повышения терапевтической эффективности композиции при поддержании стабильности композиции. В некоторых вариантах реализации, модификатор поверхностного натяжения присутствует в количестве, достаточном для повышения терапевтической эффективности композиции при поддержании стабильности композиции, достаточной для использования в качестве коммерчески жизнеспособной композиции. В некоторых вариантах реализации, модификатор поверхностного натяжения представляет собой спирт. Варианты реализации настоящего изобретения касаются композиций, содержащих пероксид водорода и спирт. В некоторых вариантах реализации, пероксид водорода может быть пероксидом водорода стандартного сорта, для пищевых продуктов, для химического синтеза, полупроводниковой чистоты, высококачественной пероксидю водорода, для антибактериального применения, для питьевой воды, для использования в фармацевтике или для косметических целей. В некоторых вариантах реализации, спирт может быть выбран из первичного спирта, вторичного спирта, третичного спирта или их комбинации. В некоторых вариантах реализации, спирт может быть выбран из, без ограничений, низкомолекулярного спирта, такого как метанол, этанол, бутанол, 1-пропанол, пентанол, гексанол, октнол, нонанол, деканол, 2-бутанол, 2-пропанол, 2-пентанол, бензиловый спирт, их изомеров, или их комбинации. В некоторых вариантах реализации, спирт не является 1-пропанолом, этанолом, пропанолом, бутанолом, пентанолом, гексанолом, октнолом, нонанолом, деканолом, 2-бутанолом, 2-пентанолом или бензиловым спиртом. В некоторых вариантах реализации, спирт представляет собой 2-пропанол (также называемый изопропиловым спиртом). В некоторых вариантах реализации, другие летучие вещества, такие как, например, ацетаты, такие как этил- и бутилацетат (летучие вещества, используемые в лаках для ногтей), циклометикон (летучий силикон, который может быть включен в систему эмульгатора), могут использоваться в комбинации с или вместо спирта. Варианты реализации настоящего изобретения также включают композицию, состоящую по существу из пероксида водорода и спирта. Некоторые варианты реализации касаются композиции, состоящей из пероксида водорода и спирта. Некоторые варианты реализации касаются композиции, содержащей пероксид водорода и 2-пропанол. Некоторые варианты реализации касаются композиции, состоящей по существу из пероксида водорода и 2-пропанола. Некоторые варианты реализации касаются композиции, состоящей из пероксида водорода и 2-пропанола.
В некоторых вариантах реализации, пероксид водорода присутствует в количестве до около 50% композиции. В некоторых вариантах реализации, композиция содержит пероксид водорода в количестве от около 0,5% до около 99,9%, от около 10% до около 99,9%, от около 20% до около 99,9%, от около 30% до около 99,9%, от около 40% до около 99,9%, от около 50% до около 99,9%, от около 60% до около 99,9%, от около 70% до около 99,9%, от около 80% до около 99,9%, от около 90% до около 99,9%, от около 0,5% до около 70%, от около 5% до около 70%, от около 10% до около 70%, от около 15% до около 70%, от около 20% до около 70%, от около 25% до около 70%, от около 30% до около 70%, от около 35% до около 70%, от около 40% до около 70%, от около 45% до около 70%, от около 50% до около 70%, от около 55% до около 70%, от около 60% до около 70%, от около 65% до около 70%, до около 50%, от около 0,5% до около 50%, от около 5% до около 50%, от около 10% до около 50%, от около 15% до около 50%, от около 20% до около 50%, от около 23,5% до около 50%, от около 25% до около 50%, от около 30% до около 50%, от около 35% до около 50%, от около 40% до около 50%, или от около 45% до около 50%. В некоторых вариантах реализации, пероксид водорода может присутствовать в количестве около 0,5%, 5%, 10%, 15%, 20%, 23,5%, 25%, 30%, 32,5%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, или в интервале между любыми двумя из этих значений.
В некоторых вариантах реализации, пероксид водорода может быть стабилизированным пероксидом водорода. В некоторых вариантах реализации, пероксид водорода может быть пероксидом водорода стандартного сорта, для пищевых продуктов, для химического синтеза, полупроводниковой чистоты, высококачественным пероксидом водорода, для антибактериального применения, для питьевой воды, для использования в фармацевтике или для косметических целей. В некоторых вариантах реализации, пероксид водорода может быть стабилизированым для использования в фармацевтике пероксидом водорода. В некоторых вариантах реализации, пероксид водорода может быть стабилизированным для косметических целей пероксидом водорода. В некоторых вариантах реализации, пероксид водорода представляет собой пероксид водорода ʺSuper Dʺ 50% фирмы FMC/PeroxyChem для косметических целей. В некоторых вариантах реализации, пероксид водорода представляет собой пероксид водорода ʺHigh-Test Hydrogen Peroxideʺ фирмы FMC/PeroxyChem, содержащую стабилизированную 50%, 70% и 90% пероксид водорода. В некоторых вариантах реализации, пероксид водорода представляет собой Peroxal 50 CG фирмы Arkema. В некоторых вариантах реализации, исходный пероксид водорода имеет концентрацию, достаточную для разбавления до величины концентрации около 23% пероксида водорода или выше в композициях, описанных в данном документе. В некоторых вариантах реализации, стабилизированный пероксид водорода содержит стабилизаторы в концентрации, достаточной для предотвращения разложения/деградации пероксида водорода при ее разбавлении до концентрации около 23% пероксида водорода или выше в композициях, описанных в данном документе. В некоторых вариантах реализации, стабилизированный пероксид водорода содержит стабилизаторы в концентрации, достаточной для предотвращения разложения/деградации модификатора поверхностного натяжения (например, спирта, такого как 2-пропанол) при ее разбавлении до концентрации около 23% пероксида водорода или выше в композициях, описанных в данном документе. В некоторых вариантах реализации, стабилизированный пероксид водорода содержит стабилизаторы в концентрации, достаточной для обеспечения стабильности композиции, которая должна быть упакована в пригодную систему упаковки, контейнер или аппликатор, и пригодной для коммерческого использования, как предусматривается в вариантах реализации, описанных в данном документе. Например, в некоторых вариантах реализации, способ приготовления композиции может включать стадию или стадии разбавления стабилизированного пероксида водорода до, например, 45%, или 40% или 32,5%, или 25%, в готовой композиции. При таком сценарии, исходная композиция пероксида водорода должна иметь достаточно высокую концентрацию для разбавления, например, до 45%, или 40%, или 32,5%, или 25%, путем добавления воды, такой как деионизированная вода, и дополнительного вспомогательного вещества или вспомогательных веществ, таких как модификатор поверхностного натяжения, такой как спирт (например, 2-пропанол и т.п.), как описано в вариантах реализации настоящего изобретения, чтобы она была в достаточной степени стабилизирована для гарантирования срока хранения, пригодного для получения коммерчески жизнеспособной композиции.
Пероксид водорода представляет собой соединение, имеющее высокую склонность к разложению в присутствии растворенных примесей, преимущественно, катионов переходных металлов, и смеси на основе пероксида водорода могут быть нестабильными, со снижением концентрации пероксида водорода со временем вследствие каталитического разложения. Примеси, вызывающие разложение пероксида водорода, типично содержатся в воде, используемой для разбавления маточной водной композиции пероксида водорода до желательной концентрации, или в дополнительных эксципиентах, добавляемых в композицию (например, 2-пропаноле). Различные факторы могут влиять на стабильность пероксида водорода в растворах, включая, например, температуру, концентрацию пероксида водорода, значение pH и присутствие примесей, обладающих эффектом разложения. Было обнаружено, что в некоторых вариантах реализации для ограничения влияния таких факторов разложения на стабильность, стабилизированная композиция, обладающая коммерческой ценностью для лечения разнообразных кожных состояний, описанных в данном документе, например, себорейного кератоза, бородавок, остроконечной кондиломы, контагиозного моллюска, может быть получена путем тщательного подбора концентраций 2-пропанола и стабилизированного (например, для косметических целей) водного раствора пероксида водорода высокой концентрации (например, 50%). Соответственно, в некоторых вариантах реализации, композиция может содержать стабилизатор или комбинацию стабилизаторов. Продукты на основе пероксида водорода из разных источников могут отличаться из-за использования фирменных смесей стабилизаторов, уникальных для каждой компании и для каждой линейки продуктов в каждой компании, и могут существенно влиять на стабильность и характеристики готового продукта. Уровни содержания каждого отдельного стабилизатора могут меняться от значений выше 0 мг/мл до тысяч мг/л, и в каждом случае зависят от марки пероксида водорода, концентрации пероксида и выбора используемых стабилизаторов. В некоторых вариантах реализации, пероксид водорода поставляется фирмами FMC Industrial Chemicals®(в настоящее время - PeroxyChem, LLC.), Sigma Corporation®, Arkema Incorporated® и т.п. В некоторых вариантах реализации, пероксид водорода поставляется фирмой PeroxyChem, LLC. В некоторых вариантах реализации, пероксид водорода представляет собой пероксид водорода ʺSuper Dʺ 50% для косметических целей фирмы FMC/PeroxyChem. Обычные стабилизаторы, используемые в композициях пероксида водорода, могут включать станнат (например, коллоидный станнат, станнат натрия), пирофосфат натрия, органофосфонаты, нитрат, фосфорную кислоту, коллоидный силикат, любой другой стабилизатор, известный из уровня техники, или их комбинацию. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от выше 0 ppm (млн-1) до около 5000 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от выше 0 ppm до около 3000 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 70 ppm до около 5000 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 70 ppm до около 3000 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 70 ppm до около 2700 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 270 ppm до около 5000 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 300 ppm до около 5000 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 270 ppm до около 3000 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 300 ppm до около 3000 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 300 ppm до около 2700 ppm. В некоторых вариантах реализации, каждый стабилизатор может иметь концентрацию от около 270 ppm до около 2700 ppm.
Пероксид водорода в композициях в соответствии с вариантами реализации настоящего изобретения может быть заменена на или скомбинирована с другими пероксидами. Другие пероксиды могут включать, без ограничений, пероксид натрия, пероксид калия и супероксид калия, пероксид лития, пероксид бария, пероксид кальция, пероксид магния, пероксид цинка, трет-бутилгидропероксид, перуксусную кислоту, дибензилпероксид, пероксид бензоила, пероксид лауроила или их комбинацию.
Вода, органические растворители, такие как спирты, поверхностно-активные вещества и другие агенты могут изменять поверхностное натяжение композиций, фармацевтических композиций, и особенно растворов. Однако, мало известно о влиянии низких концентраций спиртов или других летучих веществ на смачиваемость нормальной кожи при нанесении смесей спирт/вода, и отсутствуют сообщения о влиянии разных концентраций спиртов или других летучих веществ при их включении в композиции, содержащие пероксид водорода, на смачиваемость нормальной кожи или о смачиваемости аномальной или имеющей поражения кожи - такой как кожи, пораженной себорейным кератозом, бородавками, остроконечной кондиломой, контагиозным моллюском или другими вирусно-индуцированными или не-вирусно-индуцированными кожными новообразованиями или поражениями, включая кожные состояния, перечисленные в данном документе. Без ограничений теорией, считается, что включение спирта в стабилизированный раствор пероксида может выполнять несколько важных функций: Включение низкой концентрации спирта, например, менее 15% 2-пропанола, может обеспечить возможность включения терапевтически эффективной концентрации пероксида водорода (например, от 25% до 45% пероксида водорода), причем пероксид водорода может иметь концентрацию, достаточную для достижения желательного терапевтического эффекта на кожные поражения, и спирт присутствует в количестве, достаточном для снижения поверхностного натяжения композиции и для повышения смачиваемости поверхности поражения кожи, обеспечивая распространение композиций по поверхности и в неровностях поверхности очага поражения. Однако, вторичные спирты (например, изопропанол (ИПС)), как ожидается, являются по своей природе менее стабильными при высоких концентрациях пероксида водорода, чем первичные спирты (см. ниже), то есть, ожидается, что 2-пропанол будет легче окисляться при высоких концентрациях пероксида водорода, чем 1-пропанол, и включение низких концентраций вторичного спирта (ИПС), при концентрациях, достаточных для выполнения вышеуказанных требований (снижение поверхностного натяжения/увеличение смачиваемости поражения кожи/поддержание или повышение терапевтической эффективности) и обеспечения возможности создания стабильной коммерчески жизнеспособной композиции, было сложной задачей.
Неожиданно было обнаружено, что 2-пропанол, в количестве, которое может быть достаточным для снижения поверхностного натяжения композиции, может увеличивать смачиваемость поверхности кожных поражений, и может поддерживать или усиливать терапевтический эффект композиции на состояния, являющиеся предметом данной заявки, может быть стабильно включен в высококонцентрированный раствор пероксида водорода. Как было отмечено выше, ожидается, что изопропанол, представляющий собой вторичный спирт, будет окисляться легче, чем 1-пропанол, являющийся первичным спиртом, в присутствии высоких концентраций пероксида водорода. Механизм окисления спиртов в высоких концентрациях пероксида водорода заключается, во-первых, в образовании гидроксильных радикалов в результате разложения пероксида водорода. Этот процесс может быть ускорен в присутствии каталитических металлов или других катализаторов, таких как те, которые могут быть введены при добавлении вспомогательных веществ и/или примесей (преимущественно, катионы переходных металлов). Гидроксильный радикал будет затем оттягивать атом водорода от углерода, соседнего с кислородом в молекуле спирта, приводя к образованию углеродного радикала. В случае изопропанола, он представляет собой вторичный радикал, стабилизированный электронами кислорода и обоих метильных групп, соседних с углеродом. Для 1-пропанола, он представляет собой первичный радикал, имеющий только одну соседнюю алкильную группу, который является менее стабильным и образуется с большим трудом. Этот промежуточный продукт теряет атом водорода гидроксильной группы с образованием кетона или альдегида и альдегид, пропаналь в случае 1-пропанола, может быть далее окислен до пропионовой кислоты. В препаратах перекисей водорода высокой чистоты и с высокой степенью стабилизации или с высокими концентрациями стабилизаторов (и с более низкими концентрациями катализатора/примесей), разложение пероксида может быть замедлено и, таким образом разложение входящего в состав композиции спирта может замедляться. Однако, без очевидного присутствия катализатора, разложение пероксида происходит медленно. Кажущася скорость реакции может описываться сложным уравнением, включающим концентрации любого следового катализатора (например, каталитического металла), пероксида и спирта, но если рассматривать только спирт, то вторичный спирт окисляется легче, чем первичный. Однако, было неожиданно обнаружено, что при использовании стабилизированной композиции пероксида водорода (например, ʺSuper Dʺ фирмы FMC/PeroxyChem), включение низких концентраций вторичного спирта 2-пропанола (ИПС) в стабильную коммерчески жизнеспособную композицию становится действительно возможным. Дополнительно и важно, что первичные спирты, такие как 1-пропанол, как известно, провоцируют кожную эритему (покраснение) и раздражение кожи и могут вызывать ʺэффект прилива кровиʺ при нанесении на кожу вследствие образования альдегидных промежуточных продуктов разложения первичного спирта. Алкогольдегидрогеназа (ADH), присутствующая в коже, воздействует на, и разрушает, первичные спирты, такие как 1-пропанол, но не влияет на вторичные спирты, такие как 2-пропанол. Таким образом, только первичные спирты, которые могут окисляться до соответствующих альдегидов алкогольдегидрогеназой (ADH), присутствующей в кожа, а не вторичные (или третичные) спирты, вызывают такую реакцию кожной эритемы по этому важному механизму. Благодаря включению в композицию вторичного спирта, такого как 2-пропанол (а не первичного спирта, такого как 1-пропанол), можно избежать появления или ослабить кожные эритематозные реакции, вызываемые или обостряемые ADH-катализируемыми альдегидными промежуточными продуктами.
Таким образом, неожиданно было обнаружено, что добавление низких концентраций спирта, такого как описанные в вариантах реализации настоящего изобретения, и в частности, 2-пропанола, к пероксида водорода повышает смачиваемость поражения кожи. Дополнительно, кожные поражения, по своей природе, могут иметь трещинки и/или впячивания или неровности поверхности, которые могут затрусутокть проникновение пероксида водорода. Соответственно, в некоторых вариантах реализации, композиция может содержать пероксид водорода и модификатор поверхностного натяжения. В некоторых вариантах реализации, модификатор поверхностного натяжения может быть спиртом. Спирт может присутствовать в количестве, достаточном для снижения поверхностного натяжения композиции до уровня, который эффективно повышает проникновение композиции в такие трещинки и/или впячивания поражения кожи, увеличивает площадь поверхности реакции и повышает терапевтическую эффективность и/или клинический отклик поражения кожи на терапевтическую композицию. В некоторых вариантах реализации, композиция дополнительно содержит другой модификатор поверхностного натяжения. В некоторых вариантах реализации, модификатор поверхностного натяжения может быть выбран из, без ограничений, поверхностно-активного вещества, например, анионного или неионного поверхностно-активного вещества, водорастворимого поверхностно-активного вещества, такого как полисорбат, SLS (лаурилсульфат натрия), полипропиленгликоль (PPG) стеарат, такой как Arlamol, ПЭГ (полиэтиленгликоль) стеарат, стеарет (steareth), цетеарет (ceteareth), полиоксилстеарат и т.п., или их комбинация. Модификатор поверхностного натяжения может присутствовать в количестве, достаточном для снижения поверхностного натяжения композиции до уровня, который эффективно повышает проникновение композиции в трещинки, впячивания и/или неровности поверхности поражения кожи, увеличивает площадь поверхности реакции, и повышает терапевтическую эффективность и/или клинический отклик поражения кожи на терапевтическую композицию,, или обеспечивает комбинацию таких эффектов.
В частности, неожиданно было обнаружено, что 2-пропанол представляет собой особенно эффективный спирт для включения в композиции, описанные в данном документе. Фактически, было неожиданно обнаружено, что 2-пропанол является более пригодным и эффективным спиртом в композициях, описанных в данном документе, чем 1-пропанол. 1-Пропанол обеспечивает выделение пероксида водорода, может снижать поверхностное натяжение композиции для увеличения проникновения композиции в кожу и, как ожидалось, является более стабильным (т.е. менее склонным к окислению) в композициях, содержащих высокие концентрации пероксида водорода. Фактически, при сравнении с 2-пропанолом, 1-пропанол действительно, в некоторых концентрациях, обеспечивает повышенное выделение или повышенную скорость выделения пероксида водорода, и может снижать поверхностное натяжение в большей степени (по весовому соотношению). Однако, неожиданно было обнаружено, что несмотря на свои кажущиеся потенциально желательными эффекты, 1-пропанол является в действительности менее эффективным спиртом, чем 2-пропанол, в композициях в соответствии с вариантами реализации, раскрытыми в данном документе. Не желая ограничиваться теорией, укажем, что, как считается, (i) несмотря на существование тенденции к выделению композициями, содержащими 1-пропанол, больших количеств пероксида водорода, когда 1-пропанол присутствует в более высоких концентрациях, композиции, содержащие 2-пропанол, эффективно выделяют пероксид водорода и демонстрируют более постоянное значение скорости выделения в диапазоне желательных концентраций в вариантах реализации, описанных в данном документе; (ii) хотя 1-пропанол может снижать поверхностное натяжение композиции пероксида водорода в большей степени, по весовому соотношению, чем 2-пропанол, снижение поверхностного натяжения, индуцируемое 1-пропанолом в композициях в соответствии с предпочтительными вариантами реализации, является чрезмерным и субоптимальным, поскольку он может индуцировать настолько большое снижение, что композиция будет нежелательно растекаться за пределы целевого поражения или участка на прилегающую не имеющую поражений кожу, приводя к нежелательным эффектам, таким как раздражение и эритема, в результате, по меньшей мере частично, образования нежелательных альдегидных промежуточных продуктов, как было описано выше; и (iii) хотя теоретически, как было описано, следовало бы ожидать, что первичный спирт, 1-пропанол, будет демонстрировать большую стабильность в высококонцентрированных композициях пероксида водорода, чем вторичный спирт (т.е. 2-пропанол), 1-пропанол проявляет более высокую склонность к окислению пероксидом водорода в высококонцентрированных композициях пероксида водорода в соответствии с предпочтительными вариантами реализации, чем 2-пропанол и, фактически, является менее стабильным. Таким образом, включение 2-пропанола в композиции, описанные в данном документе, обеспечивает значительные преимущества по сравнению с использованием 1-пропанола, включая, без ограничений, получение терапевтически эффективной композиции, являющейся более стабильной, что приводт к улучшенной клинической эффективности композиции, меньшей тенденции к растеканию от предполагаемого места применения и, таким образом, более благоприятному профилю безопасности.
Количество спирта в композиции может также быть ограничено концентрацией пероксида в композиции. Например, если желательной является высокая концентрация пероксида, концентрация спирта может потребовать обязательного снижения для поддержания высокой концентрации пероксида в композиции. В некоторых вариантах реализации, спирт может присутствовать в количестве, достаточном для снижения поверхностного натяжения композиции, для усиления проникновения композиции в трещинки и/или впячивания поражения кожи, увеличения площади поверхности реакции и повышения терапевтической эффективности и/или клинического отклика поражения кожи на терапевтическую композицию. В некоторых вариантах реализации, композиция не распространяется нежелательно на прилегающую не имеющую поражений кожу, как могло бы происходить при слишком большом количестве спирта или слишком большом снижении величины поверхностного натяжения. В некоторых вариантах реализации, композиция не раздражает окружающую не имеющую поражений кожу. В некоторых вариантах реализации, композиция не вызывает эритемы на окружающей не имеющей поражений кожи. Эритема и раздражение окружаюшей не имеющей поражений кожи могут быть вызваны образованием раздражающих индуцирующих эритему промежуточных продуктов, таких как альдегиды, которое может быть вызвано разрушением субоптимальных спиртов в композиции (например, первичных спиртов, таких как 1-пропанол).
В некоторых вариантах реализации, композиция содержит модификатор поверхностного натяжения. В некоторых вариантах реализации, модификатор поверхностного натяжения представляет собой спирт. В некоторых вариантах реализации, модификатор поверхностного натяжения присутствует в количестве, достаточном для снижения поверхностного натяжения композиции пероксида водорода и воды. В некоторых вариантах реализации, композиция содержит спирт в количестве, достаточном для снижения поверхностного натяжения композиции пероксида водорода и воды. В некоторых вариантах реализации, спирт представляет собой первичный спирт, вторичный спирт, третичный спирт, или их комбинацию. В некоторых вариантах реализации, вторичный спирт представляет собой 2-пропанол. Без спирта, такого как 2-пропанол, для снижения поверхностного натяжения, композиция пероксид водорода-вода может оставаться на поверхности поражения, без проникновения в поражение и/или неровности поверхности, неоднородности, трещинки поражения. В некоторых вариантах реализации, модификатор поверхностного натяжения может присутствовать в количестве, достаточном для снижения поверхностного натяжения композиции до уровня, который эффективно повышает проникновение композиции в такие трещинки и/или впячивания поражения кожи, увеличивать площадь поверхности реакции, повышать терапевтическую эффективность и/или клинический отклик поражения кожи на терапевтическую композицию, в то же время минимизируя раздражение окружающей кожи, или обеспечивает любую комбинацию этих эффектов. Кроме этого, спирты, чрезмерно снижающие поверхностное натяжение композиции пероксида водорода, могут приводить к риску легкого растекания с места применения на прилегающую не имеющую поражений кожу, вызывая снижение активности в требуемом месте и нежелательное раздражение и другие нежелательные эффекты на окружающей не имеющей поражений коже.
В некоторых вариантах реализации, спирт в композициях в соответствии с вариантами реализации настоящего изобретения может быть заменен на другие летучие агенты. Такие летучие агенты могут включать, без ограничений, летучие вещества, такие как ацетаты, например, этилацетат и бутилацетат (летучие вещества, используемые в лаках для ногтей), циклометикон (летучий силикон, который может быть включен в систему эмульгатора), и различные другие летучие вещества в дополнение к указанным и описанным в данном документе, которые будут очевидными для квалифицированных специалистов в данной области техники на основании предшествующего описания. Такие дополнительные летучие агенты могут быть использованы в комбинации с, или вместо спирта.
В некоторых вариантах реализации, спирт может быть выбран из первичного спирта, вторичного спирта, третичного спирта или их комбинации. В некоторых вариантах реализации, спирт может включать метанол, этанол, бутанол, 1-пропанол, пентанол, гексанол, октнол, нонанол, деканол, 2-бутанол, 2-пропанол, 2-пентанол, бензиловый спирт, их изомер или их комбинацию. В некоторых вариантах реализации, спирт представляет собой 2-пропанол. Хотя варианты реализации настоящего изобретения могут относиться, в частности, к 2-пропанолу, квалифицированному специалисту в данной области техники будет понятно, что другие спирты и/или летучие вещества, такие как, без ограничений, описанные выше, могут быть использованы вместо 2-пропанола в таких вариантах реализации.
2-Пропанол (также называемый изопропиловым спиртом) представляет собой химическое соединение с молекулярной формулой C3H8O или C3H7OH. Он представляет собой бесцветное горючее химическое соединение с сильным запахом. Он является простейшим примером вторичного спирта, в котором атом углерода спирта присоединен к двум другим атомам углерода, что иногда записывается как (CH3)2CHOH. Он представляет собой структурный изомер пропанола. 2-Пропанол спешивается с водой, спиртом, эфиром и хлороформом. Он растворяет этилцеллюлозу, поливинилбутираль, многие масла, алкалоиды, камеди и природные смолы. Он нерастворим в солевых растворах. В отличие от этанола или метанола, 2-пропанол может быть выделен из водных растворов путем добавления соли, такой как хлорид натрия, сульфат натрия, или любая из нескольких других неорганических солей, поскольку спирт намного менее растворим в солевых растворах, чем в не содержащей соли воде. 2-Пропанол имеет много медицинских и фармацевтических применений и типично используется для местного применения в концентрациях от около 60% до около 70% в воде в качестве местного дезинфицирующего средства и в концентрациях от около 60% до около 75% об./об. раствора в гелях в качестве средства для дезинфекции рук. 2-Пропанол также используется в качестве средства, способствующего обезвоживанию, при лечении/предотвращении отита наружного уха ("ухо плавца") в концентрации до 95%.
В некоторых вариантах реализации, спирт присутствует в количестве до около 0,1%, до около 0,25%, до около 0,5%, до около 1%, до около 2%, до около 2,5%, до около 3%, до около 4%, до около 5%, до около 8%, до около 10%, до около 14%, до около 15%, до около 20%, или до около 25% композиции. Применение низких концентраций спирта, например, 2-пропанола, как описано в вариантах реализации настоящего изобретения, позволяет использовать стабилизированные пероксида водорода с терапевтическими высокими концентрациями (такими как более 23%) пероксида водорода, таким образом, чтобы стабилизаторы в пероксида водорода были способны поддерживать химическую стабильность композиции без воздействия на них со стороны спирта (и его примесей). В некоторых вариантах реализации, спирт может составлять до около 25% композиции. В некоторых вариантах реализации, спирт может присутствовать в количестве от около 0,05% до около 25%, от около 0,5% до около 25%, от около 1% до около 25%, от около 2,5% до около 25%, от около 5% до около 25%, от около 10% до около 25%, от около 15% до около 25%, или от около 20% до около 25%, от около 0,05% до около 15%, от около 0,5% до около 25%, до около 5%, от около 0,01% до около 5%, от около 0,1% до около 5%, от около 0,5% до около 5%, от около 1% до около 5%, от около 1,5% до около 5%, от около 2% до около 5%, от около 2,5% до около 5%, от около 3% до около 5%, от около 3,5%, до около 5%, от около 4% до около 5%, от около 4,5% до около 5% и т.п. В некоторых вариантах реализации, спирт может присутствовать в количестве около 0,01%, 0,1%, 0,25%, 0,5%, 0,75%, 1%, 2%, 2,5%, 3%, 4% 5%, 10%, 15%, 20%, 25%, или в интервале между любыми двумя из этих значений. В некоторых вариантах реализации, композиция содержит около 40% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция содержит около 45% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция содержит около 35% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция содержит около 32,5% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция содержит около 25% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция содержит около 40% пероксида водорода и около 2,5% спирта. В некоторых вариантах реализации, композиция содержит около 45% пероксида водорода и около 2,5% спирта. В некоторых вариантах реализации, композиция содержит около 35% пероксида водорода и около 2,5% спирта. В некоторых вариантах реализации, композиция содержит около 32,5% пероксида водорода и около 2,5% спирта. В некоторых вариантах реализации, композиция содержит около 25% пероксида водорода и около 2,5% спирта. В некоторых вариантах реализации, композиция содержит около 40% пероксида водорода и около 2% спирта. В некоторых вариантах реализации, композиция содержит около 45% пероксида водорода и около 2% спирта. В некоторых вариантах реализации, композиция содержит около 35% пероксида водорода и около 2% спирта. В некоторых вариантах реализации, композиция содержит около 32,5% пероксида водорода и около 2% спирта. В некоторых вариантах реализации, композиция содержит около 25% пероксида водорода и около 2% спирта. В некоторых вариантах реализации, спирт представляет собой 2-пропанол.
В некоторых вариантах реализации, композиция состоит по существу из пероксида водорода в количестве до около 50% и спирта. В некоторых вариантах реализации, композиция состоит по существу из около 40% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит по существу из около 45% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит по существу из около 35% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит по существу из около 32,5% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит по существу из около 25% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит из пероксида водорода в количестве до около 50% и спирта. В некоторых вариантах реализации, композиция состоит из около 40% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит из около 45% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит из около 35% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит из около 32,5% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, композиция состоит из около 25% пероксида водорода и около 5% спирта. В некоторых вариантах реализации, спирт представляет собой 2-пропанол.
В некоторых вариантах реализации, спирт понижает поверхностное натяжение композиции. В некоторых вариантах реализации, спирт увеличивает проникновение пероксида водорода в дефекты кожи субъекта, такие как неровности, трещинки и неоднородности кожи или поражения кожи. В некоторых вариантах реализации, спирт обезжиривает кожу субъекта или кожное поражение субъекта, тем самым обеспечивая лучшее проникновение пероксида водорода в кожу субъекта или кожное поражение. В некоторых вариантах реализации, спирт увеличивает смачиваемость поверхности кожи, включая смачиваемость кожного новообразования или поражения.
В некоторых вариантах реализации, спирт повышает эффективную концентрацию пероксида водорода при введении. Пероксид водорода является бактерицидной, вирулицидной, спороцидной и фунгицидной, и может быть стерилизующим средством в различных концентрациях и при различных временах контакта. В некоторых вариантах реализации, пероксид водорода присутствует в концентрации, достаточной для создания вирулицидного эффекта. В некоторых вариантах реализации, пероксид водорода имеет достаточное время контакта с кожей или кожным поражением для проявления ею своих эффектов бактерицидного, вирулицидного, спороцидного, фунгицидного или стерилизующего средства. В некоторых вариантах реализации, пероксид водорода имеет достаточное время контакта с кожей или кожным поражением для проявления ею вирулицидных эффектов. Без ограничений теорией, спирт может повышать эффективную концентрацию пероксида водорода при его испарении после нанесения, и может увеличивать окислительную и/или бактерицидную активность композиции. Дополнительно, повышенная проницаемость композиции может увеличивать площадь поверхности или время контакта раствора с кожей или кожным поражением и приводить к усиленному действию в качестве бактерицида или стерилизующего средства.
В некоторых вариантах реализации, композиция может быть введена местно. В некоторых вариантах реализации, композиция может быть раствором. В некоторых вариантах реализации, композиция может быть гелевой композицией. В некоторых вариантах реализации, раствор или гелевая композиция могут состоять из двух или больше частей, которые должны быть смешаны в момент или непосредственно перед моментом введения. В некоторых вариантах реализации, композиция может быть кремом, лосьоном, жидкой мазью, пенкой, трансдермальным пластырем, порошком, твердым веществом, лентой, пастой или тинктурой. В некоторых вариантах реализации, способы лечения, описанные в вариантах реализации настоящего изобретения, требуют только одного применения композиции в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, способы лечения, описанные в вариантах реализации настоящего изобретения, требуют двух или больше применений композиции в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, способы лечения, описанные в вариантах реализации настоящего изобретения, требуют многократного применения композиции в соответствии с вариантами реализации настоящего изобретения.
В некоторых вариантах реализации, композиция может дополнительно содержать фармацевтически приемлемый эксципиент. В некоторых вариантах реализации, композиция может дополнительно содержать мягчитель, эмульгатор, гелеобразующий агент, добавку, или их комбинацию. В некоторых вариантах реализации, добавка может быть выбрана из консервантов, стабилизаторов эмульсии, регуляторов pH, хелатирующих агентов, модификаторов вязкости, антиоксидантов, поверхностно-активных веществ, детергентов, мягчителей, замутнителей, агентов кондиционирования кожи, буферов, или их комбинации.
[3] Некоторые варианты реализации настоящего изобретения касаются гелевой композиции, содержащей пероксид водорода, и гелеобразующий агент. В некоторых вариантах реализации, гелевая композиция может дополнительно содержать спирт. В некоторых вариантах реализации, гелевая композиция может дополнительно содержать фармацевтически приемлемый эксципиент. В некоторых вариантах реализации, гелеобразующий агент может быть выбран из Carbopol ETD 2020, Carbopol 980 NF, Carbopol 974P, Carbopol Ultrez 10 и т.п. В некоторых вариантах реализации, гелеобразующий агент может быть высокомолекулярными сшитыми сополимерами акриловой кислоты и гидрофобного сомономера или сополимера (например, Pemulen TR-1); Polycarbophil AA-1; ПВП (поливинилпирролидоном); Eudragit; полоксамером ; Sepineo; бентонитом; аэросилом (силикаты); гиалуроновыми кислотами; сшитыми гиалуроновыми кислотами; их комбинацией, или их составным или химическим эквивалентом, обладающим свойствами, требующимися для композиции в соответствии с вариантами реализации, описанными в данном документе. В некоторых вариантах реализации, гелевая композиция содержится в двух частях и смешивается во время применения или непосредственно перед ним. Например, пероксид водорода и 2-пропанол (первая часть) могут содержаться отдельно от гелеобразующего агента (вторая часть) до времени применения или непосредственно перед ним. В качестве другого примера, пероксид водорода, 2-пропанол и гелеобразующий агент могут быть разделены все на три части и смешиваться во время применения или непосредственно перед ним. Могут быть предусмотрены дополнительные части для дополнительных вспомогательных веществ, или такие вспомогательные вещества могут быть включены в существующие части. В момент или непосредственно перед моментом применения, многокомпонентная гелевая композиция может быть смешана и нанесена местно на кожу в виде единой гелевой композиции.
[4] Некоторые варианты реализации касаются гелевой композиции, которая может подаваться в аппликатор, в котором смешиваются два или больше компонентов гелевой композиции во время применения или непосредственно перед ним. В некоторых вариантах реализации, секция гелевой композиции аппликатора содержит по меньшей мере один хрупкий отсек (например, гелеобразующий агент в основном отсеке аппликатора, с пероксидом в стеклянной ампуле внутри этого отсека или рядом с ним). Некоторые типичные примеры аппликаторов могут включать шприцеподобные аппликаторы или ʺдвухкамерныеʺ аппликаторы, которые могут непосредственно смешивать (например, ʺвихревое смешениеʺ) два или больше компонентов, которые должны содержаться в отдельных отсеках для поддержания стабильности, но которые могут быть смешаны во время применения или непосредственно перед ним.
В некоторых вариантах реализации, композиция дополнительно содержит буфер. В некоторых вариантах реализации, буфер может быть выбран из триэтаноламина, буферов с низкими значениями pH, такими как ацетат, цитрат, фосфат натрия, глицин, хлористый водород, цитрат и фосфат, глицин и хлористый водород и т.п., или их комбинации. В некоторых вариантах реализации, буфер может присутствовать в количестве от около 0,001% до около 15%. В некоторых вариантах реализации, буфер присутствует в количестве около 0,001%, 0,01%, 0,05%, 0,1%, 0,5%, 1%, 5%, 10%, 15%, или в интервале между любыми двумя из этих значений. В некоторых вариантах реализации, буфер присутствует в любом количестве, необходимом для оптимального регулирования pH композиции.
В некоторых вариантах реализации, композиция имеет поверхностное натяжение от около 15 мН•м-1 до около 80 мН•м-1 при комнатной температуре. В некоторых вариантах реализации, композиция имеет поверхностное натяжение от около 20 мН•м-1 до около 80 мН•м-1, от около 30 мН•м-1 до около 80 мН•м-1, от около 40 мН•м-1 до около 80 мН•м-1, от около 50 мН•м-1 до около 80 мН•м-1, от около 35 мН•м-1 до около 80 мН•м-1, от около 35 мН•м-1 до около 70 мН•м-1, от около 35 мН•м-1 до около 60 мН•м-1, от около 35 мН•м-1 до около 50 мН•м-1 при 37 °C, от около 40 мН•м-1 до около 80 мН•м-1, от около 40 мН•м-1 до около 70 мН•м-1, от около 40 мН•м-1 до около 60 мН•м-1, от около 40 мН•м-1 до около 50 мН•м-1, от около 45 мН•м-1 до около 80 мН•м-1, от около 45 мН•м-1 до около 70 мН•м-1, от около 45 мН•м-1 до около 60 мН•м-1, или от около 45 мН•м-1 до около 50 мН•м-1 при комнатной температуре. В некоторых вариантах реализации, композиция имеет поверхностное натяжение около 15 мН•м-1, около 20 мН•м-1, около 30 мН•м-1, около 36 мН•м-1, около 41 мН•м-1, около 48 мН•м-1, около 54 мН•м-1, около 75 мН•м-1, около 40 мН•м-1, около 50 мН•м-1, около 60 мН•м-1, около 70 мН•м-1, около 80 мН•м-1, или в интервале между любыми двумя из этих значений, при комнатной температуре. В некоторых вариантах реализации, композиция имеет поверхностное натяжение от около 42 мН•м-1 до около 55 мН•м-1 при комнатной температуре. В некоторых вариантах реализации, композиция имеет поверхностное натяжение от около 42 мН•м-1 до около 50 мН•м-1 при комнатной температуре.
В некоторых вариантах реализации, композиция имеет поверхностное натяжение от около 15 мН•м-1 до около 80 мН•м-1 при 37 °C. В некоторых вариантах реализации, композиция имеет поверхностное натяжение от около 20 мН•м-1 до около 80 мН•м-1, от около 30 мН•м-1 до около 80 мН•м-1, от около 40 мН•м-1 до около 80 мН•м-1, от около 50 мН•м-1 до около 80 мН•м-1, от около 35 мН•м-1 до около 80 мН•м-1, от около 35 мН•м-1 до около 70 мН•м-1, от около 35 мН•м-1 до около 60 мН•м-1, от около 35 мН•м-1 до около 50 мН•м-1 при 37 °C, от около 40 мН•м-1 до около 80 мН•м-1, от около 40 мН•м-1 до около 70 мН•м-1, от около 40 мН•м-1 до около 60 мН•м-1, от около 40 мН•м-1 до около 50 мН•м-1, от около 45 мН•м-1 до около 80 мН•м-1, от около 45 мН•м-1 до около 70 мН•м-1, от около 45 мН•м-1 до около 60 мН•м-1, или от около 45 мН•м-1 до около 50 мН•м-1 при 37 °C. В некоторых вариантах реализации, композиция имеет поверхностное натяжение около 15 мН•м-1, около 20 мН•м-1, около 30 мН•м-1, около 36 мН•м-1, около 41 мН•м-1, около 48 мН•м-1, около 54 мН•м-1, около 75 мН•м-1, около 40 мН•м-1, около 50 мН•м-1, около 60 мН•м-1, около 70 мН•м-1, около 80 мН•м-1, или в интервале между любыми двумя из этих значений при 37 °C. В некоторых вариантах реализации, композиция имеет поверхностное натяжение от около 42 мН•м-1 до около 55 мН•м-1 при 37 °C. В некоторых вариантах реализации, композиция имеет поверхностное натяжение от около 42 мН•м-1 до около 50 мН•м-1 при 37 °C.
В некоторых вариантах реализации, композиция, содержащая 40% пероксида водорода, имеет поверхностное натяжение от около 35 мН•м-1 до около 60,3 мН•м-1 при 37 °C. В некоторых вариантах реализации, композиция, содержащая 40% пероксида водорода, может иметь поверхностное натяжение около 60,3 мН•м-1 при 37 °C. Композиция, содержащая 40% пероксида водорода и 2,5% 2-пропанола, может иметь поверхностное натяжение около 54,1 +/- 0,8 мН•м-1 при 37 °C. Композиция, содержащая 40% пероксида водорода и 5% 2-пропанола, может иметь поверхностное натяжение около 48,3 +/- 0,7 мН•м-1 при 37 °C. Композиция, содержащая 40% пероксида водорода и 10% 2-пропанола, может иметь поверхностное натяжение около 41,1 +/- 0,6 мН•м-1 при 37 °C. Композиция, содержащая 40% пероксида водорода и 15% 2-пропанола, может иметь поверхностное натяжение около 35,9 +/- 0,6 мН•м-1 при 37 °C.
В некоторых вариантах реализации, композиция имеет pH от около 1,5 до около 7,0. В некоторых вариантах реализации, pH может иметь значение от около 1,5 до около 3,5, от около 1,5 до около 5,0, от около 1,5 до около 4,0, от около 1,7 до около 3,7, от около 2,0 до около 5,0, от около 2,0 до около 4,0, от около 2,0 до около 2,8, от около 2,5 до около 4,0, от около 2,5 до около 4,5, от около 2,5 до около 5,0, от около 2,7 до около 3,83, от около 2,7 до около 4,0, от около 2,8 до около 4,0, от около 2,83 до около 3,83, от около 3,0 до около 7,0, от около 4,0 до около 7,0, от около 5,0 до около 7,0, или от около 6,0 до около 7,0. В некоторых вариантах реализации, значение pH может составлять около 1,5, 1,7, 2,0, 2,5, 2,7, 2,8, 2,83, 3,0, 3,3, 3,5, 3,7, 3,83, 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, или находиться в интервале между любыми двумя из этих значений.
В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения являются стабильными на протяжении периода времени до около четырех недель при комнатной температуре. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения являются стабильными на протяжении периода времени до около 15 минут, около 30 минут, около 1 часа, около 2 часов, около 3 часов, около 4 часов, около 5 часов, около 6 часов, до около 12 часов, до около 24 часов, до около 1 недели, до около 2 недель, до около 3 недель, до около 1 месяца, до около 6 недель, до около 2 месяцев, до около 3 месяцев, до около 4 месяцев, до около 6 месяцев, до около 8 месяцев, до около 10 месяцев, до около 12 месяцев, до около 18 месяцев, до около 2 лет, до около 2,5 лет, или до около 3 лет, при комнатной температуре. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения являются стабильными на протяжении периода времени до около четырех недель, до около шести недель, до около восьмим недель, до около трех месяцев, до около 6 месяцев, до около 8 месяцев, или до около года при 40 °C. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения являются стабильными на протяжении периода времени до около четырех недель, до около 6 недель, до около 1 месяца, до около 2 месяцев, до около 3 месяцев, до около 4 месяцев, до около 6 месяцев, до около 8 месяцев, до около 10 месяцев, до около 12 месяцев, до около 18 месяцев, до около 2 лет, до около 2,5 лет, или до около 3 лет при 30 °C. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения являются стабильными на протяжении периода времени до около четырех недель, до около 1 месяца, до около 6 недель, до около 2 месяцев, до около 3 месяцев, до около 4 месяцев, до около 6 месяцев, до около 8 месяцев, до около 10 месяцев, до около 12 месяцев, до около 18 месяцев, до около 2 лет, до около 2,5 лет, или до около 3 лет при 25 °C. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения являются стабильными на протяжении периода времени до около четырех недель, до около 6 недель, до около 1 месяца, до около 2 месяцев, до около 3 месяцев, до около 4 месяцев, до около 6 месяцев, до около 8 месяцев, до около 10 месяцев, до около 12 месяцев, до около 18 месяцев, до около 2 лет, до около 2,5 лет, или до около 3 лет при 5 °C.
В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения удовлетворяют требованиям к стабильности, установленным Международной конференцией по гармонизации технических требований к регистрации фармацевтических продуктов, предназначенных для применения человеком (International Conference of Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use) в Согласованном трехстороннем руководстве Международной конференции по гармонизации - Испытания на стабильность новых лекарственных субстанций и продуктов Q1A(R2) (ICH Harmonised Tripartite Guideline: Stability Testing of New Drug Substances and Products Q1A(R2)), текущая редакция Стадии (Step) 4, от 6 февраля 2003 г., которое в полном объеме включено в данный документ в качестве ссылки.
В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения могут также быть введены в комбинации с другими способами, которые механически, физически или химически усиливают проникновение активного вещества в поражение. Такие способы могут включать снятие слоев кожи клейкой лентой, деструктивные/абляционные методики, такие как, например, криотерапия жидким азотом, фульгурация, лазеры с различными длинами волн (абляционные и неабляционные), радиочастотная абляция, дермабразия, и частичное или полное хирургическое удаление выскабливанием или хирургическим иссечением, использование абляционного или химического агента с отшелушивающим действием, или иные способы возмущения поверхности, или уменьшения толщины или размера или общего объема, или увеличения площади поверхности поражения. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения могут быть введены в комбинации с другими активными ингредиентами, такими как, например, адъюванты, ингибиторы или другие совместимые лекарственные средства или соединения, когда такая комбинация кажется желательной или предпочтительной для достижения желательных эффектов способов, описанных в данном документе. Любой другой известный способ лечения может быть использован в комбинации с композицией для лечения кожных болезней, раскрытой в данном документе. Например, композиция может быть введена в комбинации с активным фармацевтическим агентом, используемым для лечения кожных состояний, описанных в данном документе. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения могут быть введены до, совместно с, или после введения другого соединения для лечения поражения. В некоторых вариантах реализации, композиция дополнительно содержит активный при местном применении фармацевтический агент, используемый для лечения кожных состояний, описанных в данном документе. В качестве примера, способ лечения себорейного кератоза может включать введение ингенола мебутата субъекту и затем введение композиции в соответствии с вариантами реализации настоящего изобретения. В качестве другого примера, способ лечения бородавок может включать нанесение утром салициловой кислоты на поражение особы, нуждающейся в этом, и введение вечером композиции в соответствии с вариантами реализации настоящего изобретения в поражение особы, нуждающейся в этом. В качестве другого примера, способ лечения бородавок, себорейного кератоза, остроконечной кондиломы, моллюсков или мягких бородавок может включать введение ретиноида для местного применения в поражение нуждающейся в этом особы в течение ряда дней, и введение композиции в соответствии с вариантами реализации настоящего изобретения в поражение нуждающейся в этом особы после проведения в течение ряда дней предварительного курса лечения местным агентом. Другие возможные примеры могут быть легко представлены специалистом, знающим современный уровень техники. Другое активное вещество или процедура могут быть введены или проведены до, после или совместно с композициями в соответствии с вариантами реализации настоящего изобретения.
Варианты реализации настоящего изобретения также касаются способа лечения кожного состояния, включающего введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. В некоторых вариантах реализации, композиция может быть введена раз в сутки, два раза в сутки, раз в неделю, раз в две недели, три раза в неделю, через сутки, ежемесячно, раз в два месяца, раз в три месяца или в соответствии с указаниями, приведенными на упаковке или данными врачем, для достижения желательного клинического результата. Кожное состояние может иметь инфекционную этиологию. Кожное состояние может быть вирусно-индуцированным или не-вирусно-индуцированным новообразованием или пролиферацией кожной ткани. Кожное состояние может быть доброкачественным новообразованием, предраком или злокачественной опухолью. Кожное состояние может быть воспалительным состоянием. Кожное состояние может быть гиперпролиферативным состоянием. Кожное состояние может быть старением, включая изменения, вызванные внутренними факторами и внешними воздействиями (например, фотостарение (изменения, индуцированные воздействием ультрафиолетовых лучей)), пигментные изменения, мелкие морщинки и преждевременное появление морщин на лице. В некоторых вариантах реализации, кожное состояние может быть выбрано из поражений, индуцированных вирусом папилломы человека, например, таких как бородавки, обыкновенные бородавки, периодические бородавки, не поддающиеся лечению бородавки, бородавки, лечение которых ранее не проводилось, ладонно-подошвенные бородавки, плоские бородавки, бородавки, связанные с верруциформной эпидермодисплазией, аногенитальные бородавки, остроконечная кондилома, цервикальные дисплазии или неоплазии, например, цервикальная интраэпителиальная неоплазия (CIN); поражения, вызванные герпесвирусом включая индуцированные HHV-1 (HSV-1), HHV-2 (HSV-2), HHV-3 (вирус varicella zoster) например, ветряная оспа, опоясывающий герпес, опоясывающий лишай; поражения, индуцированные поксвирусом например, контагиозный моллюск, контагиозный пустулезный дерматит, мозоль, кожные рога, ороговевшей мозоли, мягкие бородавки, фиброэпителиальные полипы, узловатая почесуха Гайда, старческие кератозы, плоскоклеточная карцинома, плоскоклеточная карцинома in situ, кератоакантома, базальноклеточная карцинома, кожные лимфомы и доброкачественные лимфоцитарные инфильтраты и гиперплазии кожи, светлоклеточная акантома, крупноклеточная акантома, эпидермолитическая акантома, порокератоз, гиперкератоз, фолликулярный кератоз, лихеноидный кератоз, акантоз, черный акантоз, папулезный сливающийся папилломатоз, невусы, включая например, дермальные невусы, эпидермальные невусы, сложные невусы, ILVEN (воспалительные линейные бородавчатые эпидермальные невусы), сальный невус, фолликулярный кератоз, и т.п.; угри, например, комедоны, воспалительные угри, папулезные угри, пустулезные угри, кистозные угри; кисты, например, эпидермоидные кисты, милиум, атеромы, фолликулярные кисты, пролиферирующие кисты, дермоидные кисты, пилонидальные кисты, апокринные кисты, экзокринные кисты, кисты сальной железы, слизистые кисты, миксоидные кисты, ганглиевые кисты, синовиальные кисты, кисты пушковых волос, стеатоцистома, гидроцистома; неоплазии придатков например, трихофолликулома, фиброфолликулома, перифолликулярная фиброма, триходискома, сальный невус, хондроидная сирингома, трихоэпителиома, трихобластома, десмопластическая трихоэпителиома, пиломатрикома, пиломатрикальная карцинома, трихолеммома, трихолеммальная карцинома, опухоль фолликулярной воронки, трикоаденома, пролиферирующая волосяная опухоль, сальная гиперплазия, сальная аденома, сальная эпителиома, сальная карцинома, сирингома, порома, гидраденома, апокринная гидраденома, спираденома, цилиндрома, эккринный невус (эккринная гамартома), папиллярная аденома, папиллярная аденокарцинома; доброкачественные меланоцитарные пролиферации или неоплазмы, например, веснушки, пятна цвета кофе с молоком, меланоз Беккера, лентигиноз, солнечный лентигиноз, простое лентиго, мукозальные меланоцитарные поражения, монгольские пятна, невус Ота, голубой невус, обычные приобретенные меланоцитарные невусы (новоклеточный невус, ʺродимые пятнаʺ), врожденные невусы, плоская родинка, рецидивные невусы; сосудистые и периваскулярные неоплазмы и реактивные гиперплазии например, гемангиомы, сенильные гемангиомы, мишенеподобные гемосидеротические гемангиомы (hobnail hemangiomas, targeted hemosiderotic hemangiomas), пучковые капиллярные ангиомы, гемангиоэндотелиомы, ангиолимфоидная гиперплазия с эозинофилией (ALHE), гломусные опухоли (гломангиомы), гемангиоперицитомы; кожные нервные и нейроэндокринные неоплазмы, например, нейромы, шванномы, нейрофибромы, опухоль периневрия, миксома периневрия, нейротекеома, зернисто-клеточная опухоль; фиброзные и фиброгистиоцитарные пролиферации, например, мягкие бородавки, фиброэпителиальные полипы, фибромы, фиброзные папулы, ангиофибромы, перламутровые папулы полового члена, околоногтевые фибромы, дерматофибромы, фиброкератомы, склеротические или плеоморфные фибромы, соединительнотканные невусы; кожные шрамы, гиперплазии, келоиды, розовые угри, кожные грибковые, дерматофитные и плесневые инфекции, онихомикоз, гиперпигментация, псориаз, злокачественная меланома, себорейный кератоз, варианты себорейного кератоза, включая, например, черный папулезный дерматоз, обратный фолликулярный кератоз/кератома бородавчатый дискератоз/бородавчатая дискератома, бородавчатый акрокератоз, «штукатурный» кератоз; или их комбинация.
В некоторых вариантах реализации, способ лечения кожного состояния дополнительно включает стадию очистку места проведения лечения перед введением композиции. В некоторых вариантах реализации, очистка места проведения лечения включает обезжиривание места проведения лечения перед введением композиции. В некоторых вариантах реализации, очистка места проведения лечения включает нанесение по меньшей мере 70% 2-пропанола на кожу, подлежащую лечению, перед введением композиции. Обезжиривание места проведения лечения может включать нанесение спирта на кожу, например, путем растирания, массажа, размещения, растирания щеткой, соскабливания, вытирания, промакивания, или иного введения кожи в контакт со спиртом.
В некоторых вариантах реализации, способ лечения кожного состояния дополнительно включает стадию санации места проведения лечения субъекта. В некоторых вариантах реализации, санация может включать механическое, химическое, или физическое скобление, абляцию, истончение, кюретаж, разрушение, удаление, иссечение или иное возмущающее воздействие на поверхность кожи или поражение, требующее лечения, включая уменьшение толщины и/или уменьшение объема поражения. В некоторых вариантах реализации, стадия санации проводится до, после и/или совместно с введением композиций в соответствии с вариантами реализации настоящего изобретения, в место проведения лечения.
В некоторых вариантах реализации, спирт может быть выбран из первичного спирта, вторичного спирта, третичного спирта или их комбинации. Спирт может быть выбран из метанола, этанола, бутанола, 1-пропанола, пентанола, гексанола, октанола, нонанола, деканола, 2-бутанола, 2-пропанола, 2-пентанола, 2-гексанола, бензилового спирта, их изомеров, или их комбинации. В некоторых вариантах реализации, обезжиривание кожи может включать нанесение на кожу другого известного обезжиривающего агента, такого как этилацетат, бутилацетат и т.п., например, путем растирания, массажа, размещения, растирания щеткой, соскабливания, вытирания, промакивания, или иного введения кожи в контакт с агентом. В некоторых вариантах реализации, очистка кожи включает нанесение раствора антисептика на кожу или кожное поражение, требующее лечения. В некоторых вариантах реализации, антисептик представляет собой повидон, йод, хлоргексидин, детергент, мыло и т.п.
Некоторые варианты реализации касаются способа лечения бородавок, включающего введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. В некоторых вариантах реализации, композиция содержит спирт и до около 50% пероксида водорода. В некоторых вариантах реализации, бородавки могут быть обработаны с использованием любого из способов лечения, описанных в данном документе. Некоторые варианты реализации касаются способа улучшения внешнего вида бородавок, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. Некоторые варианты реализации касаются способа улучшения внешнего вида бородавок, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. Некоторые варианты реализации касаются способа облегчения состояния, например, сморщивания, уменьшения размера и/или уменьшения высоты бородавки, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. В некоторых вариантах реализации, лечение бородавок ранее не проводилось. В некоторых вариантах реализации, бородавка, не получавшая ранее лечения, может быть обработана с использованием любого из способов лечения, описанных в данном документе. Некоторые варианты реализации касаются способа улучшения внешнего вида бородавок, лечение которых ранее не проводилось, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. Некоторые варианты реализации касаются способа улучшения внешнего вида бородавок, лечение которых ранее не проводилось, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. Некоторые варианты реализации касаются способа облегчения состояния, например, сморщивания, уменьшения размера и/или уменьшения высоты бородавки, не получавшей ранее лечения, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. В некоторых вариантах реализации, бородавки представляют собой не поддающиеся лечению бородавки. Не поддающиеся лечению бородавки могут включать бородавки, резистентные к, или не поддающиеся или частично реагирующие на другие терапии, бородавки, с трудом поддающиеся лечению, или бородавки, расположенные в анатомически труднодоступных местах. В некоторых вариантах реализации, не поддающиеся лечению бородавки могут включать подошвенные бородавки, околоногтевые бородавки, подногтевые бородавки и т.п. В некоторых вариантах реализации, не поддающиеся лечению бородавки могут быть расположены на любой поверхности тела. В некоторых вариантах реализации, не поддающиеся лечению бородавки могут быть обработаны с использованием любого из способов лечения, описанных в данном документе. Некоторые варианты реализации касаются способа улучшения внешнего вида не поддающихся лечению бородавок, включающего введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. Некоторые варианты реализации касаются способа улучшения внешнего вида не поддающихся лечению бородавок, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. Некоторые варианты реализации касаются способа облегчения состояния, например, сморщивания, уменьшения размера и/или уменьшения высоты не поддающейся лечению бородавки, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. В некоторых вариантах реализации, композиция содержит около 25% пероксида водорода и 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 32,5% пероксида водорода и 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 40% пероксида водорода и 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 45% пероксида водорода и 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит до около 50% пероксида водорода и 2-пропанол.
Некоторые варианты реализации касаются способа лечения себорейного кератоза, включающего введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. В некоторых вариантах реализации, композиция содержит спирт и до около 50% пероксида водорода. В некоторых вариантах реализации, композиция содержит около 45% пероксида водорода и 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 40% пероксида водорода и 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 35% пероксида водорода и около 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 32,5% пероксида водорода и около 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 25% пероксида водорода и около 5% 2-пропанола.
Некоторые варианты реализации касаются способа лечения мягких бородавок, включающий введение композиции в соответствии с вариантами реализации настоящего изобретения нуждающемуся в этом субъекту. В некоторых вариантах реализации, композиция содержит спирт и до около 50% пероксида водорода. В некоторых вариантах реализации, композиция содержит около 45% пероксида водорода и 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 40% пероксида водорода и 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 35% пероксида водорода и около 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 32,5% пероксида водорода и около 5% 2-пропанола. В некоторых вариантах реализации, композиция содержит около 25% пероксида водорода и около 5% 2-пропанола.
Некоторые варианты реализации настоящего изобретения касаются способа лечения кожного состояния, включающего (i) местное введение первой дозы композиции, содержащей до около 50% пероксида водорода и спирт; и (ii) местное введение одной или нескольких последующих доз композиции. В некоторых вариантах реализации, применение первой дозыи одной или нескольких последующих доз включает один сеанс применения. В некоторых вариантах реализации, последующая доза вводится немедленно после введения первой дозы. В некоторых вариантах реализации, последующая доза вводится по меньшей мере через около 0,5 минут после первой дозы. В некоторых вариантах реализации, последующая доза вводится по меньшей мере через около 1 минуту, по меньшей мере около 1,5 минуты, по меньшей мере около 2 минуты, по меньшей мере около 5 минут, по меньшей мере около 10 минут, по меньшей мере около 15 минут, по меньшей мере около 20 минут, по меньшей мере около 25 минут, по меньшей мере около 30 минут, или по меньшей мере около 1 час после первой дозы. В некоторых вариантах реализации, может быть введена одна последующая доза, две последующие дозы, три последующие дозы, четыре последующие дозы, пять последующих доз, шесть последующих доз, семь последующих доз, восемь последующих доз, девять последующих доз или десять последующих доз в каждом сеансе применения. Каждая очередная последующая доза может быть введена немедленно после введения предыдущей дозы, через по меньшей мере около 1 минуту, по меньшей мере около 1,5 минуты, по меньшей мере около 2 минуты, по меньшей мере около 5 минут, по меньшей мере около 10 минут, по меньшей мере около 15 минут, по меньшей мере около 20 минут, по меньшей мере около 25 минут, по меньшей мере около 30 минут или по меньшей мере один час после предыдущей дозы.
В некоторых вариантах реализации, композиция для местного применения может быть введена в эффективной дозе. В некоторых вариантах реализации, эффективная доза может составлять от около 0,0025 миллилитра до около 3 миллилитров композиций в соответствии с вариантами реализации настоящего изобретения, включая около 0,0025 миллилитра, около 0,01 миллилитра, около 0,025 миллилитра, около 0,05 миллилитра, около 0,075 миллилитра, около 0,1 миллилитра, около 0,15 миллилитра, около 0,5 миллилитра, около 1 миллилитра, около 1,5 миллилитра, около 2 миллилитра (millimeters), около 2,5 миллилитра, около 3 миллилитра, их комбинацию, или любое количество, обеспечивающее клинический эффект на поражение. В некоторых вариантах реализации, эффективная доза пропорциональна размеру поражения. В некоторых вариантах реализации, эффективная доза композиции составляет менее чем около 0,1 миллилитра на поражение. В некоторых вариантах реализации, эффективная доза может составлять около 3 миллилитра композиций в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, эффективн доза может составлять от около 2 миллилитров до около 3 миллилитров композиций в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, эффективная доза может составлять от около 2 миллилитров до около 5 миллилитров композиций в соответствии с вариантами реализации настоящего изобретения.
В некоторых вариантах реализации, местное применение первой дозы и последующих доз включает введение композиции в кожу путем массажа в течение по меньшей мере около 5 секунд, по меньшей мере около 10 секунд, по меньшей мере около 15 секунд, по меньшей мере около 20 секунд, по меньшей мере около 25 секунд, по меньшей мере около 30 секунд, по меньшей мере около 35 секунд, по меньшей мере около 40 секунд, по меньшей мере около 45 секунд, по меньшей мере около 50 секунд, по меньшей мере около 55 секунд, по меньшей мере около 1 минуты, по меньшей мере около 2 минут, по меньшей мере около 3 минут, по меньшей мере около 4 минут, или по меньшей мере около 5 минут, по меньшей мере около 10 минут, по меньшей мере около 15 минут, по меньшей мере около 20 минут по меньшей мере около 25 минут, или по меньшей мере около 30 минут для каждой дозы. В некоторых вариантах реализации, композиция представляет собой раствор. В некоторых вариантах реализации, композиция представляет собой гель. В некоторых вариантах реализации, массаж включает втирание, манипулирование, разминание, надавливание, или иные действия, обеспечивающие введение композиции в кожу. В некоторых вариантах реализации, композиция наносится и вводится при массировании в кожу с помощью аппликатора. В некоторых вариантах реализации, композиция наносится и вводится при массировании в кожу по меньшей мере 1 раз, по меньшей мере 2 раза, по меньшей мере 3 раза, по меньшей мере 4 раза, по меньшей мере 5 раз, по меньшей мере 6 раз, по меньшей мере 7 раз, по меньшей мере 8 раз, по меньшей мере 9 раз, или по меньшей мере 10 раз в каждом сеансе применения. В некоторых вариантах реализации, сеанс применения, в ходе которого вводится композиция, может повторяться раз в сутки, два раза в сутки, раз в неделю, раз в две недели, три раза в неделю, через сутки, ежемесячно, раз в два месяца, раз в три месяца, раз в шесть месяцев или в соответствии с указаниями, приведенными на упаковке или данными врачем для достижения желательного клинического результата.
В некоторых вариантах реализации, композиция вводится поставщиком медицинских услуг. В некоторых вариантах реализации, композиция вводится в условиях медицинского учреждения. В некоторых вариантах реализации, композиция самостоятельно вводится нуждающимся в этом субъектом. В некоторых вариантах реализации, композиция вводится лицом, осуществляющим уход за субъектом. В используемом в данном документе значении, поставщик медицинских услуг может включать доктора, медсестру, помощника врача, младшую медсестру, фельдшера, или любого профессионала, работающего во врачебном кабинете, больнице или клинике. В условиях медицинского учреждения, в используемом в данном документе значении, относится к врачебному кабинету, больнице, условиям амбулаторного учреждения или клинике. Лицо, осуществляющее уход за субъектом, может включать родителей, медсестру, друга, члена семьи, профессионального медика, или любую особу, помогающую при введении композиции нуждающемуся в этом субъекту.
В некоторых вариантах реализации, способ дополнительно включает местное введение субъекту второй композиции, содержащей пероксид водорода и спирт, как описано в вариантах реализации выше, после начального лечения поставщиком медицинских услуг. В некоторых вариантах реализации, вторая композиция представляет собой композицию, предоставляемую для использования в домашних условиях. В некоторых вариантах реализации, вторая композиция отпускается без рецепта. В некоторых вариантах реализации, вторая композиция отпускается по рецепту. В некоторых вариантах реализации, вторая композиция может содержать более низкую концентрацию пероксида водорода, чем при начальном лечении, проводимом для субъекта. В некоторых вариантах реализации, вторая композиция может содержать такую же концентрацию пероксида водорода, как при начальном лечении, проводимом для субъекта. В некоторых вариантах реализации, вторая композиция содержит до около 50% пероксида водорода и спирт. В некоторых вариантах реализации, вторая композиция содержит около 45% пероксида водорода и 5% спирта. В некоторых вариантах реализации, вторая композиция содержит около 40% пероксида водорода и 5% спирта. В некоторых вариантах реализации, вторая композиция содержит около 35% пероксида водорода и 5% спирта. В некоторых вариантах реализации, вторая композиция содержит около 32,5% пероксида водорода и 5% спирта. В некоторых вариантах реализации, вторая композиция содержит около 25% пероксида водорода и 5% спирта. В некоторых вариантах реализации, спирт представляет собой 2-пропанол. В некоторых вариантах реализации, вторая композиция может вводиться субъектом самостоятельно. В некоторых вариантах реализации, вторая композиция может вводиться через по меньшей мере около 1 сутки, по меньшей мере около 2 суток, по меньшей мере около 3 суток, по меньшей мере около 1 неделю, по меньшей мере около 2 недели, по меньшей мере около 3 недели, по меньшей мере около 4 недели, по меньшей мере около 5 недель, по меньшей мере около 6 недель, по меньшей мере около 7 недель, или с интервалом, необходимым для поддержания клинического эффекта или до исчезновения поражения, после начального лечения специалистом по медицинскому обеспечению. В некоторых вариантах реализации, вторая композиция может быть введена раз в сутки, два раза в сутки, раз в неделю, раз в две недели, через сутки, ежемесячно, раз в два месяца, раз в три месяца, раз в шесть месяцев, или в соответствии с указаниями, приведенными на упаковке или данными врачем для достижения клинически желательного результата.
Некоторые варианты реализации настоящего изобретения касаются способа лечения кожного состояния у субъекта, включающего местное введение субъект композиции, предоставляемой для использования в домашних условиях, содержащей пероксид водорода и спирт, как описано выше. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, отпускается без рецепта. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, отпускается по рецепту. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, содержит около 50% пероксида водорода и спирт. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, содержит около 45% пероксида водорода и 5% спирта. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, содержит около 40% пероксида водорода и 5% спирта. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, содержит около 35% пероксида водорода и 5% спирта. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, содержит около 32,5% пероксида водорода и 5% спирта. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, содержит около 25% пероксида водорода и 5% спирта. В некоторых вариантах реализации, спирт представляет собой 2-пропанол. Такие композиции, предоставляемые для использования в домашних условиях, могут быть введены после посещения специалиста по медицинскому обеспечению. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, может быть введена после начального лечения специалистом по медицинскому обеспечению. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, может содержать более низкую концентрацию пероксида водорода, чем при начальном лечении, проводимом для субъекта. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, может содержать такую же концентрацию пероксида водорода, как при начальном лечении, проводимом для субъекта. Композиция, предоставляемая для использования в домашних условиях, может вводиться субъектом самостоятельно. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, может вводиться через по меньшей мере около 1 сутки, по меньшей мере около 2 суток, по меньшей мере около 3 суток, по меньшей мере около 1 неделю, по меньшей мере около 2 недели, по меньшей мере около 3 недели, по меньшей мере около 4 недели после начального лечения специалистом по медицинскому обеспечению. В некоторых вариантах реализации, композиция, предоставляемая для использования в домашних условиях, может быть введена раз в сутки, два раза в сутки, раз в неделю, раз в две недели, через сутки, ежемесячно, раз в два месяца, раз в три месяца, раз в шесть месяцев, или в соответствии с указаниями, приведенными на упаковке или данными врачем для достижения клинически желательного результата.
Варианты реализации настоящего изобретения также охватывают устройства для введения композиций пероксида водорода в соответствии с вариантами реализации настоящего изобретения (см., например, Фигуры 12-16 и связанное с ними описание). В некоторых вариантах реализации, композиция, содержащая пероксид водорода и спирт, как описано в вариантах реализации настоящего изобретения, может быть введена с использованием любого аппликатора для местного применения, известного из уровня техники. В некоторых вариантах реализации, композиция, содержащая пероксид водорода и спирт, как описано в вариантах реализации настоящего изобретения, может быть введена с использованием губки, тампона, тупфера с аппликатором из пеноматериала, ватного шарика, щетки, тканого или нетканого материала, роликового аппликатора, марли, ручки-аппликатора, перчатки и т.п. В некоторых вариантах реализации, аппликатор может дозировать композиции в соответствии с вариантами реализации настоящего изобретения через кончик, который является распушенным, абсорбирующим и/или достаточно твердым для приложения давления к поражению. В некоторых вариантах реализации аппликатор представляет собой аппликатор с кончиком из спеченного полимерного материала. В некоторых вариантах реализации, аппликатор является стойким к, совместимым с, или инертным по отношению к высококонцентрированным растворам пероксидов. В некоторых вариантах реализации, аппликатор способен дозировать раствор с контролируемым объемным расходом, чтобы помочь ограничить применение активного вещества представляющим интерес поражением и уберечь окружающую нормальную кожу. В некоторых вариантах реализации, раствор может быть введен с использованием устройства, содержащего раствор пероксида водорода отсеке, из которого раствор дозируется на или через кончик аппликатора при необходимости. В некоторых вариантах реализации, аппликатор может содержать материал, предназначенный для стирания поражения кожи или место обработки до, после или во время введения композиции. В некоторых вариантах реализации, аппликатор представляет собой аппликатор в форме "козьей ножки". В некоторых вариантах реализации, аппликатор представляет собой распушенный аппликатор в форме "козьей ножки". В некоторых вариантах реализации, распушенный аппликатор в форме "козьей ножки" состоит из ПЭВП (полиэтилен высокой плотности), нейлона и адгезива. В некоторых вариантах реализации, раствор наносят раз в сутки, два раза в сутки, раз в неделю, раз в две недели, три раза в неделю, через сутки, ежемесячно, раз в два месяца, раз в три месяца или в соответствии с указаниями, приведенными на упаковке или данными врачем или поставщиком услуг для достижения желательного клинического результата.
В некоторых вариантах реализации, способ лечения кожного состояния включает введение композиции в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, введение композиции в соответствии с вариантами реализации настоящего изобретения включает введение в контакт места обработки с кончиком аппликатора, причем аппликатор включает размещенную внутри него хрупкую ампулу, содержащую композицию, корпус аппликатора содержит размещенную в нем хрупкую ампулу, втулка аппликатора находится в жидкостном сообщении с корпусом аппликатора, кончик расположен на проксимальном конце втулки аппликатора, и фильтр расположен между хрупкой ампулой и кончиком. В некоторых вариантах реализации, введение композиции для местного применения включает контроль скорости подачи композиции для местного применения из кончика путем изменения надавливающего усилия, приложеного к внешней поверхности корпуса аппликатора. В некоторых вариантах реализации, введение композиции для местного применения включает введение в контакт кончика с целевым поражением, вызванным кожным состоянием причем композиция для местного применения дозируется через кончик на целевое поражение. В некоторых вариантах реализации, введение композиции для местного применения дополнительно включает приложение давления к зоне давления, расположенной на внешней поверхности корпуса аппликатора, вызывающего разрушение хрупкой ампулы. В некоторых вариантах реализации, введение композиции для местного применения включает действие, вызывающее разрушение хрупкой ампулы и высвобождение композиции для местного применения через кончик; и введение в контакт кончика с целевым поражением, вызванным кожным состоянием.
Некоторые варианты реализации настоящего изобретения касаются набора для лечения кожного состояния, включающий контейнер, включающий отсек, содержащий пероксид водорода, отсек, содержащий 2-пропанол, и инструкции по применению. Некоторые варианты реализации касаются набора для лечения кожного состояния, включающего контейнер, содержащий пероксид водорода и 2-пропанол, и инструкции по применению. В некоторых вариантах реализации, набор дополнительно содержит аппликатор. В некоторых вариантах реализации, набор может включать два или больше аппликаторов. Например, в некоторых вариантах реализации, набор может содержать много аппликаторов, когда требуется проведение лечения нескольких поражений (например, в отпускаемом без рецепта наборе или наборе для многократного применения врачем) или если набор дополнительно содержит композицию, предоставляемую для использования в домашних условиях композиции для многократного применения. В некоторых вариантах реализации, набор может содержать аппликатор с хрупкой стеклянной ампулой, содержащей раствор пероксида водорода и спирт. В некоторых вариантах реализации, набор может содержать аппликатор с хрупкой стеклянной ампулой, содержащей раствор пероксида водорода, причем аппликатор также содержит отсек со спиртом, таким как, без ограничений, 2-пропанол, в корпусе аппликатора. В некоторых вариантах реализации, аппликатор может дополнительно содержать отсек, содержащий гелеобразующий агент. В некоторых вариантах реализации, набор может содержать два или больше контейнеров с композицией пероксида водорода для местного применения. В некоторых вариантах реализации, два или больше контейнеров композиции пероксида водорода для местного применения могут содержать композиции пероксида водорода с одинаковыми концентрациями пероксида водорода. В некоторых вариантах реализации, два или больше контейнерой композиций пероксида водорода для местного применения могут содержать композиции пероксида водорода с разными концентрациями пероксида водорода. Например, в некоторых вариантах реализации, набор может содержать один контейнер с 40% пероксида водорода и 5% 2-пропанола для применения врачем в учреждении, и другие контейнеры с другими концентрациями (например, более слабыми концентрациями) пероксида водорода, предназначенные для использованием пациентом в домашних условиях для последующего нанесения на место поражения. В некоторых вариантах реализации, набор может включать два или больше контейнеров для одноразового использования с композицией перекиси водорода для местного применения с множеством аппликаторов. В некоторых вариантах реализации, набор может включать контейнер, содержащий многодозовые контейнеры с композицией пероксида водорода для местного применения со множеством аппликаторов. Кожное состояние может быть вирусно-индуцированным или не-вирусно-индуцированным новообразованием или пролиферацией кожной ткани. Кожное состояние может быть доброкачественным новообразованием, предраком или злокачественной опухолью. Кожное состояние может быть воспалительным состоянием. Кожное состояние может быть гиперпролиферативным состоянием. Кожное состояние может быть старением, включая изменения, вызванные внутренними факторами и внешними воздействиями (например, фотостарение (изменения, индуцированные воздействием ультрафиолетовых лучей)), пигментные изменения, мелкие морщинки и преждевременное появление морщин на лице. В некоторых вариантах реализации, кожное состояние может быть выбрано из поражений, таких как индуцированные вирусом папилломы человека, например, бородавки, обыкновенные бородавки, ладонно-подошвенные бородавки, плоские бородавки, периодические бородавки, не поддающиеся лечению бородавки, бородавки, лечение которых ранее не проводилось, бородавки, связанные с верруциформной эпидермодисплазией, аногенитальные бородавки, остроконечная кондилома, цервикальные дисплазии или неоплазии, например, цервикальная интраэпителиальная неоплазия (CIN); поражения, вызванные герпесвирусом включая индуцированные HHV-1 (HSV-1), HHV-2 (HSV-2), HHV-3 (вирус varicella zoster) например, ветряная оспа, опоясывающий герпес, опоясывающий лишай; поражения, индуцированные поксвирусом например, контагиозный моллюск, контагиозный пустулезный дерматит; мозоль, кожные рога, ороговевшей мозоли, мягкие бородавки, фиброэпителиальные полипы, узловатая почесуха Гайда, старческие кератозы, плоскоклеточная карцинома, плоскоклеточная карцинома in situ, кератоакантома, базальноклеточная карцинома, кожные лимфомы и доброкачественные лимфоцитарные инфильтраты и гиперплазии кожи, светлоклеточная акантома, крупноклеточная акантома, эпидермолитическая акантома, порокератоз, гиперкератоз, фолликулярный кератоз, лихеноидный кератоз, акантоз, черный акантоз, папулезный сливающийся папилломатоз, невусы, включая например, дермальные невусы, эпидермальные невусы, сложные невусы, ILVEN (воспалительные линейные бородавчатые эпидермальные невусы), сальный невус, фолликулярный кератоз, и т.п.; угри, например, комедоны, воспалительные угри, папулезные угри, пустулезные угри, кистозные угри; кисты, например, эпидермоидные кисты, милиум, атеромы, фолликулярные кисты, пролиферирующие кисты, дермоидные кисты, пилонидальные кисты, апокринные кисты, экзокринные кисты, кисты сальной железы, слизистые кисты, миксоидные кисты, ганглиевые кисты, синовиальные кисты, кисты пушковых волос, стеатоцистома, гидроцистома; неоплазии придатков например, трихофолликулома, фиброфолликулома, перифолликулярная фиброма, триходискома, сальный невус, хондроидная сирингома, трихоэпителиома, трихобластома, десмопластическая трихоэпителиома, пиломатрикома, пиломатрикальная карцинома, трихолеммома, трихолеммальная карцинома, опухоль фолликулярной воронки, трикоаденома, пролиферирующая волосяная опухоль, сальная гиперплазия, сальная аденома, сальная эпителиома, сальная карцинома, сирингома, порома, гидраденома, апокринная гидраденома, спираденома, цилиндрома, эккринный невус (эккринная гамартома), папиллярная аденома, папиллярная аденокарцинома; доброкачественные меланоцитарные пролиферации или неоплазмы, например, веснушки, пятна цвета кофе с молоком, меланоз Беккера, лентигиноз, солнечный лентигиноз, простое лентиго, мукозальные меланоцитарные поражения, монгольские пятна, невус Ота, голубой невус, обычные приобретенные меланоцитарные невусы (новоклеточный невус, ʺродимые пятнаʺ), врожденные невусы, плоская родинка, рецидивные невусы; сосудистые и периваскулярные неоплазмы и реактивные гиперплазии например, гемангиомы, сенильные гемангиомы, мишенеподобные гемосидеротические гемангиомы (hobnail hemangiomas, targeted hemosiderotic hemangiomas), пучковые капиллярные ангиомы, гемангиоэндотелиомы, ангиолимфоидная гиперплазия с эозинофилией (ALHE), гломусные опухоли (гломангиомы), гемангиоперицитомы; кожные нервные и нейроэндокринные неоплазмы, например, нейромы, шванномы, нейрофибромы, опухоль периневрия, миксома периневрия, нейротекеома, зернисто-клеточная опухоль; фиброзные и фиброгистиоцитарные пролиферации, например, мягкие бородавки, фиброэпителиальные полипы, фибромы, фиброзные папулы, ангиофибромы, перламутровые папулы полового члена, околоногтевые фибромы, дерматофибромы, фиброкератомы, склеротические или плеоморфные фибромы, соединительнотканные невусы; кожные шрамы, гиперплазии, келоиды, розовые угри, кожные грибковые, дерматофитные и плесневые инфекции, онихомикоз, гиперпигментация, преждевременное появление морщин на лиц, псориаз, злокачественная меланома, себорейный кератоз, варианты себорейного кератоза, включая, например, черный папулезный дерматоз, обратный фолликулярный кератоз/кератома бородавчатый дискератоз/бородавчатая дискератома, бородавчатый акрокератоз, «штукатурный» кератоз; или их комбинация. В некоторых вариантах реализации, аппликатор может быть выбран из губки, тампона, тупфера с аппликатором из пеноматериала, ватного шарика, щетки, тканого или нетканого материала, роликового аппликатора, марли, ручки-аппликатора и т.п. В некоторых вариантах реализации, аппликатор является распушенным, абсорбирующим и/или достаточно твердым для приложения давления к поражению. В некоторых вариантах реализации аппликатор представляет собой аппликатор с кончиком из спеченного полимерного материала. В некоторых вариантах реализации, аппликатор является стойким к, совместимым с, или инертным по отношению к высококонцентрированным растворам пероксидов. В некоторых вариантах реализации, аппликатор способен дозировать раствор с контролируемым объемным расходом, для того чтобы способствовать ограничению нанесения активного вещества поражением, представляющим интерес, и уберечь окружающую нормальную кожу. В некоторых вариантах реализации, раствор может быть введен с использованием устройства, содержащего раствор пероксида водорода в отсеке, дозирующего раствор на или через кончик аппликатора при необходимости. В некоторых вариантах реализации, аппликатор может содержить материал, предназначенный для истирания поражения кожи или места обработки перед или во время введения композиции. В некоторых вариантах реализации, аппликатор представляет собой аппликатор в форме "козьей ножки". В некоторых вариантах реализации, аппликатор представляет собой распушенный аппликатор в форме "козьей ножки". В некоторых вариантах реализации, распушенный аппликатор в форме "козьей ножки" состоит из ПЭВП (полиэтилен высокой плотности), ПЭНП (полиэтилен низкой плотности), нейлона, адгезива, или любой их комбинации. В некоторых вариантах реализации, контейнер может быть выбран из флакона, ампулы, банки, бутылки, медицинской пробирки, шприца, или любого другого контейнера для хранения жидкостей. В некоторых вариантах реализации, отсек может быть выбран из флакона, пробирки, ампулы, банки, бутылки, медицинской пробирки, шприца, или любого другого контейнера для хранения жидкостей. В некоторых вариантах реализации, контейнер может быть изготовлен из стекла, боросиликатного стекла, боросиликатного стекла типа I, окрашенного или иного светозащитного стекла, янтарного окрашенного стекла, янтарного боросиликатного стекла типа I, ПЭВП, тефлона (Teflon®), силикона, ABS (акрилонитрил-бутадиен-стирольного сополимера), или другого совместимого полимера или материала. В некоторых вариантах реализации, набор может включать стеклянный флакон или бутылку, содержащие раствор пероксида водорода и спирт, размещенный внутри них. В некоторых вариантах реализации, стеклянный флакон или бутылка могут представлять собой стеклянный флакон или бутылку из янтарного стекла. В некоторых вариантах реализации, набор может содержать флакон или бутылку, по меньшей мере частично сформованные из ПЭВП, содержащие раствор пероксида водорода и спирт, размещенный внутри них. В некоторых вариантах реализации, контейнер может быть сформован из материала, имеющего низкую реакционную способность по отношению к пероксиду. В некоторых вариантах реализации, отсек может включать материал, имеющий низкую реакционную способность по отношению к пероксиду. В некоторых вариантах реализации, пероксид водорода представляет собой стабилизированный пероксид водорода. В некоторых вариантах реализации, спирт, такой как, без ограничений, 2-пропанол, присутствует в количестве менее чем около 25%. В некоторых вариантах реализации, набор может быть предназначен для использования поставщиком медицинских услуг. В некоторых вариантах реализации, набор может быть предназначен для использования нуждающимся в этом субъектом. В некоторых вариантах реализации, набор может быть доступен только по рецепту. В некоторых вариантах реализации, набор может отпускаться без рецепта для использования нуждающимся в этом субъектом.
Фигура 12 изображает иллюстративный пример аппликатора, выполненного в соответствии с первым вариантом реализации. Как показано на Фигуре 12, аппликатор 1200 может включать корпус аппликатора 1205. В некоторых вариантах реализации, трубка аппликатора 1205 может быть закрыта на своем дистальном конце торцевой крышкой 1215. В некоторых вариантах реализации, корпус аппликатора 1205 и/или торцевая крышка 1215 могут быть сформованы из различных гибких материалов, включая, без ограничений, гибкие полимерные материалы. Неограничительные примеры гибких полимерных материалов могут включать полипропилен (ПП), полиэтилен высокой плотности (ПЭВП) или полиэтилен низкой плотности (ПЭНП), поливинилхлорид (ПВХ), полиэтилен (ПЭ), их производные, и любую их комбинацию. В некоторых вариантах реализации, корпус аппликатора 1205 может иметь в общем удлиненную форму. В некоторых вариантах реализации, корпус аппликатора 1205 может иметь в общем цилиндрическую форму. Корпус аппликатора 1205 может иметь различную длину в соответствии с некоторыми вариантами реализации, включая примернр 80 миллиметров, около 90 миллиметров, около 98 миллиметров, около 99 миллиметров, около 100 миллиметров, около 110 миллиметров, около 120 миллиметров, около 130 миллиметров, около 140 миллиметров, около 150 миллиметров, от около 80 миллиметров до около 100 миллиметров, от около 80 миллиметров до около 150 миллиметров, от около 90 миллиметров до около 100 миллиметров, от около 100 миллиметров до около 120 миллиметров, от около 100 миллиметров до около 150 миллиметров, и любые значения или диапазоны значений между любыми из этих значений (включая конечные точки). Корпус аппликатора 1205 может иметь различные наружные размеры в соответствии с некоторыми вариантами реализации, включая около 5 миллиметров, около 7 миллиметров, около 9 миллиметров, около 10 миллиметров, около 12 миллиметров, около 15 миллиметров, около 18 миллиметров, около 20 миллиметров, от около 5 миллиметров до около 7 миллиметров, от около 5 миллиметров до около 10 миллиметров, от около 7 миллиметров до около 10 миллиметров, от около 9 миллиметров до около 15 миллиметров, от около 10 миллиметров до около 15 миллиметров, от около 5 миллиметров до около 20 миллиметров, от около 10 миллиметров до около 20 миллиметров, и любые значения или диапазоны значений между любыми из этих значений (включая конечные точки).
В некоторых вариантах реализации, ампула 1210, предназначенная для хранения композиции в соответствии с вариантами реализации настоящего изобретения, может быть размещена в полости, сформованной в корпусе аппликатора 1205. В некоторых вариантах реализации, ампула 1210 может быть хрупкой, например, предназначенной для разбивания, фрагментирования, разламывания, раздрабливания или иного разрушения в ответ на приложение к ней достаточного давления. Например, достаточное давление может быть приложено вручную, например, путем приложения усилия рукой (например, сдавливания или нажатия) к корпусу аппликатора 1205 в направлении к ампуле 1210 в той области корпуса аппликатора, где размещена ампула. Таким образом, усилие, прикладываемое к корпусу аппликатора 1205, может передаваться ампуле 1210 и ампула может разламываться в ответ на приложение к ней достаточной силы. В некоторых вариантах реализации, ампула 1210 может быть сформована из различных хрупких материалов, включая стекло, пластик, полимерный материал, боросиликатное стекло, боросиликатное стекло типа I, окрашенное стекло и любую их комбинацию. В некоторых вариантах реализации, ампула 1210 может включать один или более участков с пониженной прочностью для облегчения разрушения ампулы 1210. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения могут быть едкими и/или могут реагировать с материалами аппликатора 1200 или окружающей средой. В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения могут быть деградировать или иначе подвергаться воздействию загрязняющих веществ и/или контактов с окружающей средой. Соответственно, хранение композиций в соответствии с вариантами реализации настоящего изобретения с использованием одной или более ампул 1210 может защищать материалы и/или композиции аппликатора 1200 в соответствии с вариантами реализации настоящего изобретения от деградации до их высвобождения из ампулы. Благодаря использованию ампул 1210, аппликатор 1200 может, в числе прочего, обеспечивать надежное и стабильное хранение композиций в соответствии с вариантами реализации настоящего изобретения и других компонентов до момента осуществления доставки.
Композиции в соответствии с вариантами реализации настоящего изобретения, содержащиеся в ампуле 1210, могут высвобождаться в корпусе аппликатора 1205 в результате разламывания ампулы 1210. Ампула 1210 может быть предназначена для удерживания различных объемов композиций в соответствии с вариантами реализации настоящего изобретения, включая около 0,1 миллилитра, около 0,2 миллилитра, около 0,5 миллилитра, около 1 миллилитр, около 1,5 миллилитра, около 2 миллилитра, около 2,4 миллилитра, около 3 миллилитра, около 3,2 миллилитра, около 4 миллилитра, около 5 миллилитров, около 10 миллилитров, около 20 миллилитров, около 30 миллилитров, около 50 миллилитров, около 100 миллилитров, около 500 миллилитров, от около 0,1 миллилитра до около 3 миллилитров, от около 0,1 миллилитра до около 4 миллилитров, от около 0,1 миллилитра до около 5 миллилитров, от около 0,1 миллилитра до около 10 миллилитров, от около 0,1 миллилитра до около 100 миллилитров, от около 0,1 миллилитра до около 500 миллилитров, от около 1 миллилитра до около 3 миллилитров, от около 1 миллилитра до около 4 миллилитров, от около 1 миллилитра до около 5 миллилитров, от около 1 миллилитра до около 100 миллилитров, от около 1 миллилитра до около 500 миллилитров, от около 2 миллилитров до около 3 миллилитров, от около 2 миллилитров до около 4 миллилитров, от около 2 миллилитров до около 5 миллилитров, от около 2 миллилитров до около 10 миллилитров, от около 3 миллилитров до около 4 миллилитров, от около 3 миллилитров до около 5 миллилитров, от около 3 миллилитров до около 10 миллилитров, от около 3 миллилитров до около 100 миллилитров, от около 4 миллилитров до около 5 миллилитров, от около 4 миллилитров до около 10 миллилитров, от около 4 миллилитров до около 100 миллилитров, от около 5 миллилитров до около 10 миллилитров, от около 5 миллилитров до около 100 миллилитров, от около 100 миллилитров до около 500 миллилитров, и любые значения или диапазоны значений между любыми из этих значений (включая конечные точки). В некоторых вариантах реализации, ампула 1210 может быть предназначена для удерживания эффективной дозы композиций в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, ампула 1210 может быть предназначена для удерживания эффективной дозы композиций в соответствии с вариантами реализации настоящего изобретения, достаточной для обработки одного поражения или участка кожи. В некоторых вариантах реализации, ампула 1210 может быть предназначена для удерживания эффективной дозы композиций в соответствии с вариантами реализации настоящего изобретения, достаточной для обработки множества поражений или участков кожи. В некоторых вариантах реализации, эффективная доза может составлять от около 0,0025 миллилитра до около 3 миллилитров композиций в соответствии с вариантами реализации настоящего изобретения, включая около 0,0025 миллилитра, около 0,01 миллилитра, около 0,025 миллилитра, около 0,05 миллилитра, около 0,075 миллилитра, около 0,1 миллилитра, около 0,15 миллилитра, около 0,5 миллилитра, около 1 миллилитр, около 1,5 миллилитра, около 2 миллиметра, около 2,5 миллилитра, около 3 миллилитра, их комбинацию, или любое количество, проявляющее клинический эффект воздействия на поражения. В некоторых вариантах реализации, эффективная доза пропорциональна размеру поражения. В некоторых вариантах реализации, эффективная доза композиции составляет менее чем около 0,1 миллилитра на поражение. В некоторых вариантах реализации, эффективная доза может составлять около 3 миллилитра композиций в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, эффективная доза может составлять от около 2 миллилитров до около 3 миллилитров композиций в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, эффективная доза может составлять от около 2 миллилитров до около 5 миллилитров композиций в соответствии с вариантами реализации настоящего изобретения.
Хотя на Фигуре 12 изображена только одна ампула 1210, варианты реализации не ограничены в этом отношении, поскольку аппликатор 1200 может содержать множество ампул. Например, аппликатор 1200 может содержать множество ампул 1210 для множества доз композиций в соответствии с вариантами реализации настоящего изобретения. В другом случае, аппликатор 1200 может содержать множество ампул 1210, содержащих разные композиции. В некоторых вариантах реализации, аппликатор 1200 может включать отсек (не показан), содержащий первую композицию (например, гелеобразующий агент, пероксид водорода) и одну или несколько ампул 1210, содержащих одну или более вторых композиций (например, 2-пропанол, композиции в соответствии с вариантами реализации настоящего изобретения). Например, одна или более стенок могут разделять корпус аппликатора на один или более отсеков. В некоторых вариантах реализации, отсек или его часть (например, участок стенки, образующей отсек в корпусе аппликатора 1205) может быть разрушен путем приложения к отсеку достаточного усилия. В некоторых вариантах реализации, одна или более первых композиций могут быть расположены в корпусе аппликатора 1205 таким образом, чтобы одна или более вторых композиций, размещенных в одной или более ампулах 1210 и/или одном или более отсеках, могли вступать в контакт с одной или более вторыми композициями в результате высвобождения одной или более вторых композиций. Неограничительные примеры первой композиции могут включать спирт (например, 2-пропанол) или гелеобразующий агент, и неограничительные примеры второй композиции могут включать композицию едкого вещества, такого как раствор пероксида водорода. В некоторых вариантах реализации, различные композиции (например, одна или несколько первых композиций и одна или более вторых композиций) могут быть смешаны до или одновременно с их применением.
В некоторых вариантах реализации, втулка аппликатора 1225 может находиться в жидкостном сообщении с корпусом аппликатора 1205 на проксимальном конце аппликатора 1200. Втулка аппликатора 1225 может быть предназначена для приема композиции в соответствии с вариантами реализации настоящего изобретения, вытекающей из корпуса аппликатора 1205 в результате высвобождения композиций в соответствии с вариантами реализации настоящего изобретения из ампулы 1210. В некоторых вариантах реализации, по меньшей мере часть втулки аппликатора 1225 может быть размещена внутри корпуса аппликатора 1205. В некоторых вариантах реализации, втулка аппликатора 1225 может быть неподвижно прикреплена к корпусу аппликатора 1205, например, с помощью адгезивов, притертого соединения, запрессовывания, резьбового соединения и т.п. В некоторых вариантах реализации, наружная часть втулки аппликатора 1225 может быть неподвижно прикреплена к внутренней части проксимального конца корпуса аппликатора 1205. В некоторых вариантах реализации, втулка аппликатора 1225 может образовывать герметичное соединение с корпусом аппликатора 1205 с помощью притертого соединения, адгезивов, резьбового соединения и т.п. В некоторых вариантах реализации, втулка аппликатора 1225 может быть сформована из полимерного материала, включая, без ограничений, ПЭ, ПП, ПЭВП и ПЭНП. В некоторых вариантах реализации, защитный колпачок 1235 может быть предназначен для закрывания втулки аппликатора 1225 на проксимальном конце аппликатора 1200.
В некоторых вариантах реализации, фильтр 1220 может быть размещен внутри аппликатора 1200 между ампулой 1210 и проксимальным концом аппликатора 1200. В некоторых вариантах реализации, фильтр 1220 может быть размещен в дистальной части втулки аппликатора 1225, обращенной к ампуле 1210. Фильтр 1220 может быть предназначен для задерживания кусочков разбитой ампулы 1210, в то же время позволяя вытекать композиции в соответствии с вариантами реализации настоящего изобретения. Фильтр 1220 может быть сформован из различных материалов, включая любой материал, способный отделять осколки ампулы от композиции в соответствии с вариантами реализации настоящего изобретения. Неограничительные примеры материалов фильтра 1220 могут включать различные полимерные материалы, ПЭ, ПП, ПЭВП, ПЭНП, полистирол (PS), уголь, пеноматериал, керамику, песок, диатомовую землю (DE), бумажные волокна и любую их комбинацию. В некоторых вариантах реализации, материал фильтра 1220 может быть выбран таким образом, чтобы обеспечивать определенную скорость потока композиций в соответствии с вариантами реализации настоящего изобретения через фильтр.
В некоторых вариантах реализации, аппликатор 1200 может включать кончик 1230, расположенный в его проксимальной части. В некоторых вариантах реализации, кончик 1230 может быть неподвижно размещен в центральном канале втулки аппликатора 1225. Кончик 1230 может быть предназначен для облегчения нанесения композиций в соответствии с вариантами реализации настоящего изобретения на кожу пациента. В некоторых вариантах реализации, кончик 1230 может быть сформован из абсорбирующего материала или материала со значительной поглощающей способностью. В некоторых вариантах реализации, кончик 1230 может быть выполнен в виде спеченного кончика из полимерного материала. В некоторых вариантах реализации, кончик 1230 может быть выполнен в форме "козьей ножки". В некоторых вариантах реализации, кончик 1230 может быть выполнен в виде распушенного кончика, который, например, может включать и/или может быть сформован из распушенного материала, включая, без ограничений, пучки, сформованные их волокон различных материалов. В некоторых вариантах реализации, распушенный кончик может быть сформован путем прикрепления распушенного материала к кончику 1230. В некоторых вариантах реализации, кончик 1230 может быть сформован из различных материалов, которые являются нереакционноспособными или иначе химически совместимыми с композициями в соответствии с вариантами реализации настоящего изобретения. В некоторых вариантах реализации, кончик 1230 может быть сформован из различны биосовместимых материалов. В некоторых вариантах реализации, кончик 1230 может быть сформован из различных материалов, включая, без ограничений, целлюлозу, нейлон, вискозный шелк, полиэфир, тефлон, их волокна, изготовленные из них распушенные материалы, и любую их комбинацию.
В некоторых вариантах реализации, кончик 1230 может быть неподвижно закреплен в аппликаторе 1200, например, во втулке аппликатора 1225, например, с помощью адгезивов, притертого соединения, резьбового соединения, защелки, запрессовывания и т.п. В некоторых вариантах реализации, аппликатор 1200 может быть выполнен с возможностью замены кончика 1230 во время или после каждого использования. В некоторых вариантах реализации, предусмотрена возможность замены ампулы 1210 в аппликаторе 1200. Например, оператор может снять торцевую крышку 1215, удалить осколки разбитой ампулы 1210, и вставить новую ампулу с такой же и/или другой композицией в соответствии с вариантами реализации настоящего изобретения. Таким образом, аппликатор 1200 может быть использован многократно и/или для лечения множества кожных состояний (т.е., отдельных поражений, бородавок или других кожных образований) у одного пациента. В некоторых вариантах реализации, аппликатор 1200 может быть аппликатором для одноразового применения. В некоторых вариантах реализации, аппликатор для одноразового применения предназначен для утилизации после одноразового применения.
В некоторых вариантах реализации, композиции в соответствии с вариантами реализации настоящего изобретения могут высвобождаться из ампулы 1210 и вытекать через корпус аппликатора 1205 (включая любые его камеры), фильтр 1220, втулку аппликатора 1225, и из аппликатора через кончик 1230. В некоторых вариантах реализации, корпус аппликатора 1205 и/или кончик 1230 может быть предназначен для того, чтобы позволить оператору контролировать поток композиции едкого вещества из аппликатора 1200. В неограничительном примере, после высвобождения композиции в соответствии с вариантами реализации настоящего изобретения из ампулы 1210, оператор может инициировать вытекание композиций в соответствии с вариантами реализации настоящего изобретения из аппликатора 1200 путем сдавливания корпуса аппликатора 1205, тем самым создавая в нем давление, достаточное для выдавливания композиции в соответствии с вариантами реализации настоящего изобретения через кончик 1230. В некоторых вариантах реализации, прижимание кончика 1230 к коже пациента может создавать капиллярный эффект, достаточный для того, чтобы композиции в соответствии с вариантами реализации настоящего изобретения, высвобождающиеся из ампулы 1210 и находящиеся в контакте с кончиком, вытекали через кончик и из аппликатора 1200. В некоторых вариантах реализации, оператор может контролировать скорость вытекания, изменяя величину усилия, используемого для сдавливания с боков корпуса аппликатора 1205 и/или прижимания кончика 1230 к коже пациента. В некоторых вариантах реализации, аппликатор 1200 может включать приводной механизм (не показан), предназначенный для принудительного дозирования композиций в соответствии с вариантами реализации настоящего изобретения из аппликатора.
В некоторых вариантах реализации, по меньшей мере одна часть аппликатора может содержать гидрофобный материал, такой как фильтр 1220 и/или кончик 1230. В некоторых вариантах реализации, гидрофобный материал состоит из полиэфирных полимеров или сополимеров, акрилового полимера, модифицированного акрилового полимера (например, модакрила), полипропилена, полиэтилена или их комбинации или смеси. В некоторых вариантах реализации, например, фильтр может содержать смесь полипропилена и полиэфирных полимеров или сополимеров. Неограничительные примеры гидрофобных материалов могут также включать материалы, содержащие, имеющие покрытие из, и/или модифицированные силанами, алкилсиланами, фторалкилсиланами, силиконом, их комбинациями, и их производными. В некоторых вариантах реализации, материалам, используемым для изготовления аппликатора и его частей в соответствии с некоторыми вариантами реализации, описанными в данном документе, могут быть приданы гидрофобные свойства путем нанесения покрытия или иного включения в них гидрофобного материала. В некоторых вариантах реализации, гидрофобные части аппликатора могут выполнять функцию препятствования, уменьшения, предотвращения и/или предотвращения в значительной степени вытекания композиций в соответствии с вариантами реализации настоящего изобретения, высвобождающихся из ампулы, через части аппликатора и/или из кончика аппликатора.
В некоторых вариантах реализации, аппликатор 1200 может быть выполнен таким образом, чтобы композиции в соответствии с вариантами реализации настоящего изобретения, высвобождающиеся из ампулы 1210, не могли самотеком доставляться из аппликатора 1200 без приложения оператором давления к аппликатору, например, путем сдавливания или иного приложения силы к корпусу аппликатора 1205. В некоторых вариантах реализации, потребность в действии оператора (т.е., прикладывании давления к аппликатору 1200) может усиливаться за счет использования гидрофобных материалов в соответствии с некоторыми вариантами реализации. В некоторых вариантах реализации, аппликатор 1200 может быть выполнен таким образом, чтобы пустое пространство могло образовываться внутри корпуса аппликатора 1205 позади объема композиций в соответствии с вариантами реализации настоящего изобретения, высвобождающегося из ампулы 1210, например, когда аппликатор ориентирован вертикально, по существу вертикально, или частично вертикально. В некоторых вариантах реализации, пустое пространство может выполнять роль вакуума, препятствуя, уменьшая, ограничивая, предотвращая и/или по существу предотвращая вытекание композиций в соответствии с вариантами реализации настоящего изобретения, высвобождающихся из ампулы 1210, из аппликатора 1200. Таким образом, гидрофобная часть аппликатора 1200 и/или пустое пространство, образующееся внутри корпуса аппликатора 1205, может выполнять функцию предотвращения утечки композиций в соответствии с вариантами реализации настоящего изобретения из аппликатора после высвобождения композиций в соответствии с вариантами реализации настоящего изобретения из хрупкой ампулы 1210, включая случаи, когда аппликатор находится в положении, способствующем дозированию композиций в соответствии с вариантами реализации настоящего изобретения, таком как вертикальное или по существу вертикальное положение.
Аппликатор 1200 может быть предназначен для хранения, дозирования и применения любых композиций в соответствии с вариантами реализации настоящего изобретения, как части способа лечения любых состояний, раскрытых в данном документе. Например, аппликатор 1200 может быть предназначен для хранения, дозирования и применения композиции для местного применения, содержащей 2-пропанол и до около 50% пероксида водорода. В некоторых вариантах реализации, композиция для местного применения может представлять собой любую композицию, описанную в вариантах реализации настоящего изобретения.
Фигуры 13A-13C изображают первый вид сбоку с пространственным разделением деталей, второй вид сбоку с пространственным разделением деталей, и поперечное сечение, соответственно, иллюстративного примера аппликатора в соответствии со вторым вариантом реализации. Как показано на Фигурах 13A-13C, аппликатор 1300 может включать корпус аппликатора 1305, имеющий ампулу 1310, размещенную внутри его внутренней полости. Проксимальный конец корпуса аппликатора 1305 может быть закрыт защитным колпачком 1325, например, когда аппликатор 1300 не используется. Дистальный конец корпуса аппликатора 1305 может быть закрыт торцевой крышкой 1315, неподвижно прикрепленной к нему, например, с помощью адгезивов, притертого соединения, соединения на защелке и т.п. Перфорированный распушенный кончик 1330 может быть размещен по меньшей мере частично внутри корпуса аппликатора 1305 на его проксимальном конце. В некоторых вариантах реализации, перфорированный распушенный кончик 1330 может быть образован из или по существу из втулки аппликатора 1225 и кончика 1230, как изображено на Фигуре 12. В некоторых вариантах реализации, перфорированный распушенный кончик 1330 может быть неподвижно прикреплен к корпусу аппликатора 1330, например, с помощью адгезивов, притертого соединения, резьбового соединения, защелки и т.п. В некоторых вариантах реализации, фильтр 1335 может быть размещен внутри перфорированного распушенного кончика 1330.
В некоторых вариантах реализации, (поверхность) захвата 1320 может быть расположена на наружной части корпуса аппликатора 1305 на его проксимальном конце. В некоторых вариантах реализации, поверхность захвата 1320 может быть предназначена для улучшения способности оператора удерживать рукой аппликатор 1300 и управлять им. В некоторых вариантах реализации, поверхность захвата 1320 может быть сформована из различны полимерных материалов, включая, без ограничений, пеноматериал, резиновый материал, пластический материал, термопластический материал или другие материалы, известные рядовым специалистам в данной области техники, или любую их комбинацию. В некоторых вариантах реализации, поверхность захвата 1320 может быть предназначена для улучшения размещения руки, повышения комфортности оператора, уменьшения усталости руки и т.п., при использовании аппликатора 1300. В некоторых вариантах реализации, по меньшей мере часть поверхности захвата 1320 может включать профилированные, изогнутые, вогнутые или другие неплоские поверхности, предназначенные для облегчения точного контроля аппликатора 1300 со стороны оператора. В некоторых вариантах реализации, поверхность захвата 1320 может включать по меньшей мере одно приспособление, препятствующее проворачиванию вокруг оси, предназначенное для уменьшения или предотвращения проворачивания или поворота аппликатора 1300 в руке оператора при его использовании. В некоторых вариантах реализации, поверхность захвата 1320 может включать по меньшей мере одно приспособление, препятствующее проворачиванию вокруг оси, предназначенное для уменьшения или предотвращения проворачивания или поворота аппликатора 1300 при его размещении на поверхности, например, прилавке, столе, подставке для инструментов и т.п. В некоторых вариантах реализации, поверхность захвата 1320 может быть нанесена формованием на внешнюю поверхность корпуса аппликатора 1305. В некоторых вариантах реализации, поверхность захвата 1320 может быть выполнена в виде отдельного элемента, который может быть надет на, или иначе присоединен к аппликатору 1300 или закреплен на нем.
В некоторых вариантах реализации, зона давления 1345 может быть размещена на корпусе аппликатора 1305. В некоторых вариантах реализации, зона давления 1345 может включать помеченный участок, предназначенный для того, чтобы указывать оператору оптимальную область на трубке аппликатора 1305 для прикладывания давления для раздавливания ампулы 1310. В некоторых вариантах реализации, зона давления 1345 может быть предназначена для размещения пальцев и/или большого пальца пользователя для улучшения захвата и/или сдавливания трубки аппликатора 1305 для раздавливания ампулы 1310. В некоторых вариантах реализации, зона давления 1345 может включать помеченный участок, образованный одним или несколькими выступающими элементами. В некоторых вариантах реализации, зона давления 1345 может быть сформована из материалов, которые наносятся формованием на наружную поверхность корпуса аппликатора 1305. В некоторых вариантах реализации, зона давления 1345 может включать отпечатанный и/или выступающий элемент, размещенный на ярлыке, закрепленном на внешней поверхности корпуса аппликатора 1305. В некоторых вариантах реализации, зона давления 1345 может быть предназначена для концентрирования давления, прикладываемого оператором для раздавливания ампулы 1310. В некоторых вариантах реализации, зона давления 1345 может быть предназначена для указания положения непосредственно или по существу непосредственно над одним или несколькими элементами концентрирования усилия (не показаны), размещенными внутри корпуса аппликатора 1305, предназначенными для концентрирования давления, прикладываемого оператором для раздавливания ампулы 1310. В некоторых вариантах реализации, элементы концентрирования усилия могут включать один или несколько подпорок, сформованных из различных материалов, таких как пластический материал. В некоторых вариантах реализации, аппликатор 1300 не содержит элементов концентрирования усилия. В некоторых вариантах реализации, давление пальца является достаточным для раздавливания ампулы 1310. В некоторых вариантах реализации, зона давления 1345 может быть сформована из более гибкого материала, чем другие участки трубки аппликатора 1305 для облегчения передачи давления от руки оператора, сдавливающей трубку аппликатора 1305, к ампуле 1310. В варианте реализации, в котором аппликатор 1300 включает множество ампул 1310 и/или один или несколько отсеков (не показан), аппликатор может содержать множество зон давления 1345, предназначенных для указания оптимального участка приложения давления для раздавливания каждого отсека и/или ампулы.
В некоторых вариантах реализации, ампула 1310 может быть неподвижно размещена внутри корпуса аппликатора 1305. Например, в некоторых вариантах реализации, ампула может быть неподвижно размещена внутри корпуса аппликатора 1305 таким образом, чтобы ампула не сдвигалась или по существу не сдвигалась в продольном направлении внутри корпуса аппликатора 1305 или не сдвигалась в проксимальном направлении далее определенного положения внутри корпуса аппликатора. В некоторых вариантах реализации, размер и/или форма ампулы 1310 могут быть выполнены такими, чтобы они соответствовали размеру и/или форме корпуса аппликатора 1305 (например, внутренним размерам корпуса аппликатора), так чтобы ампула удерживалась на месте в корпусе аппликатора благодаря притертому соединению. В некоторых вариантах реализации, корпус аппликатора 1305 может иметь переменные внутренние размеры, так чтобы ампула 1310 могла удерживаться только в определенной части корпуса аппликатора. В некоторых вариантах реализации, внутренняя поверхность корпуса аппликатора 1305 может включать бугорки, ребра, выступы, или другие конструктивные элементы, предназначенные для удерживания ампулы 1310 на месте и/или для предотвращения движения ампулы в продольном направлении внутри корпуса аппликатора. В некоторых вариантах реализации, опорный элемент 1340 может быть размещен внутри корпуса аппликатора для удерживания ампулы 1310 на месте и/или для предотвращения движения ампулы в продольном направлении внутри корпуса аппликатора 1305. В некоторых вариантах реализации, опорный элемент 1340 может включать один или несколько упоров или выступов (например, ребра, бугорки и т.п.), размещенных внутри и/или образованных частями корпуса аппликатора 1305. В некоторых вариантах реализации, опорный элемент 1340 может быть предназначен для размещении ампулы в положении для раздавливания оператором. Например, опорный элемент 1340 может быть предназначен для удерживания (ампулы) в области, соответствующей зоне давления 1345.
В некоторых вариантах реализации, аппликатор 1300 может включать один или несколько элементов для проведения санации (не показаны), размещенных на внешней части аппликатора, например, на корпусе аппликатора 1305, торцевой крышке 1315, и/или защитном колпачке 1325. Один или несколько элементов для проведения санации могут быть предназначены для механического или физического скобления, абляции, истончения, кюретажа, разрушения, удаления, иссечения или иного санирующего воздействия на участок кожи пациента, такой как участок кожи, имеющий поражение, бородавку, себорейный кератоз, или другие кожные образования. В некоторых вариантах реализации, один или несколько элементов для проведения санации могут быть предназначены для возмущающего воздействия на поверхность, уменьшения размера, уменьшения толщины и/или уменьшения объема поражения или другого кожного образования. В некоторых вариантах реализации, один или несколько элементов для проведения санации могут включать абразивный элемент, тонкую иглу, кончик, кюретку, или любой другой элемент и/или конструкцию, пригодные для проведения санации или иного воздействия на поражение или другое кожное образование. В таких вариантах реализации, оператор может использовать один или несколько элементов для проведения санации для очистки или иного воздействия на поражение или другое кожное образование до, после, и/или во время применения композиций в соответствии с вариантами реализации настоящего изобретения с помощью аппликатора 1300.
[5] Фигуры 14A и 14B изображают различные виды корпуса аппликатора в соответствии с некоторыми вариантами реализации. Как показано на виде сбоку A на Фигуре 14A, аппликатор 1400 может включать корпус 1405, имеющий расположенную на нем зону давления 1445. Как изображено на виде изнутри B Фигуры 14A, корпус аппликатора 1400 может включать опорный элемент 1440, расположенный в нем. Торцевая крышка 1415 может быть предназначена для соединения, включая съемное соединение, с дистальным концом 1420 корпуса аппликатора 1400. Фигура 14B изображает вид сбоку A и вид сверху B корпуса аппликатора, имеющего область захвата 1425.
[6] Фигура 15 изображает иллюстративный пример торцевой крышки аппликатора в соответствии с некоторыми вариантами реализации. В частности, Фигура 15 изображает вид сбоку A, вид сверху B, и вид изнутри сбоку C торцевой крышки 1500. Фигура 16 изображает перфорированный распушенный кончик (или ʺвтулку аппликатораʺ) в соответствии с некоторыми вариантами реализации. Более конкретно, Фигура 16 изображает внутренний вид сбоку A, вид сбоку B, и вид сверху C перфорированного распушенного кончика 1600. Как показано на виде сбоку B Фигуры 16, перфорированный распушенный кончик 1600 может включать распушенный участок 1605 и участок питающего отверстия 1610.
Фигура 17A изображает внутренний вид сбоку защитного колпачка 1700 в соответствии с некоторыми вариантами реализации, включая выносной элемент 1705 с дистальной частью 1710 защитного колпачка. Фигура 17B изображает защитный колпачок 1700, размещенный на участке корпуса аппликатора 1710 и закрывающий кончик 1720 аппликатора в соответствии с некоторыми вариантами реализации. Фигуры 18A и 18B изображают вид сбоку и внутренний вид, соответственно, аппликатора 1800 в соответствии с некоторыми вариантами реализации. Как показано на Фигуре 18A, аппликатор 1800 может включать корпус аппликатора 1805, закрытый защитным колпачком 1810. Фигура 18B изображает внутренний вид защитного колпачка 1810, имеющего ребро 1815, выступающее от его внутренней поверхности. Когда защитный колпачок 1810 соединен с корпусом аппликатора 1805, ребро 1815 может входить в зацепление с или прилегать к перфорированному распушенному кончику 1820. В некоторых вариантах реализации, ребро 1815 может затыкать, блокировать, или иначе закрывать одно или несколько отверстий в перфорированном распушенном кончике 1820, предотвращая, например, вытекание жидкости из перфорированного распушенного кончика. Хотя варианты реализации, изложенные в данном документе, описаны с использованием термина ʺсодержащийʺ, все ранее описанные варианты реализации также включают композиции и способы, состоящие только из перечисленных ингредиентов или стадий, или состоящие по существу из перечисленных ингредиентов или стадий и, необязательно, дополнительных ингредиентов или стадий, которые существенно не влияют на основные и новые свойства композиции или способа.
Данное описание и варианты реализации, иллюстрирующие способ и используемые материалы, будут лучше понятны из следующих неограничительных примеров.
ПРИМЕР 1
Поражение кожи, вызванное себорейным кератозом (СК) у женщины в возрасте 76 лет с типом кожи 1 по Фицпатрику, обрабатывали раствором, содержащим 40% стабилизированного пероксида водорода и 5% 2-пропанола. После очистки кожи 70% 2-пропанолом, раствор пероксида водорода наносили местно на поражение себорейным кератозом с помощью распушенного аппликатора в форме "козьей ножки". Используя сильное надавливание и методику нанесения, соответствующую размеру целевого поражения, раствор наносили в течение приблизительно 20-30 секунд. Приблизительно через 1-2 минуты, процесс нанесения повторяли. Эту последовательность повторяли до проведения 4 процедур нанесения. Процедура не вызывала боли или ощущения дискомфорта. Контрольный осмотр через неделю показал, что поражение СК рассасывается. Контрольный осмотр через 3 недели после обработки показал, что поражение рассасывается, но не исчезло полностью. Второй сеанс обработки, идентичный первому, проводили через 3 недели после первой обработки. Контрольный осмотр через 5 недель и 8 недель после второго сеанса обработки показал, что поражение полностью рассосалось без признаков рецидива поражения и без нежелательных косметических последствий (например, рубцевания или изменения пигментации (гиперпигментации или гипопигментации)). Субъект остался очень доволен результатами.
ПРИМЕР 2
Поражение, вызванное себорейным кератозом (СК) у женщины в возрасте 65 лет с типом кожи 4 по Фицпатрику, обрабатывали раствором, содержащим 32,5% стабилизированного пероксида водорода и 5% 2-пропанола. После очистки кожи 70% 2-пропанолом, раствор наносили местно на поражение себорейным кератозом с помощью распушенного аппликатора в форме "козьей ножки". Используя сильное надавливание и методику нанесения, соответствующую размеру целевого поражения, раствор наносили в течение приблизительно 20-30 секунд. Приблизительно через 1-2 минуты процесс нанесения повторяли. Эту последовательность повторяли до проведения 4 процедур нанесения. Процедура не вызывала боли или ощущения дискомфорта. Контрольный осмотр через 3 недели после обработки показал, что поражение полностью рассосалось без признаков рубцевания или изменения пигментации (гиперпигментации или гипопигментации). Субъект остался очень доволен результатами. Контрольный осмотр через 11 недель после обработки не выявил рецидивов поражения и нежелательных косметических последствий.
ПРИМЕР 3
Поражение, вызванное себорейным кератозом (СК), у мужчины в возрасте 73 лет с типом кожи 3 по Фицпатрику, обрабатывали раствором, содержащим 25% стабилизированного пероксида водорода и 5% 2-пропанола. После очистки кожи 70% 2-пропанолом, раствор наносили местно на поражение себорейным кератозом с помощью распушенного аппликатора в форме "козьей ножки". Используя сильное надавливание и методику нанесения, соответствующую размеру целевого поражения, раствор наносили в течение приблизительно 20-30 секунд. Приблизительно через 1-2 минуты процесс нанесения повторяли. Эту последовательность повторяли до проведения 4 процедур нанесения. Процедура не вызывала боли или ощущения дискомфорта. Контрольный осмотр через 3 недели после обработки показал, что поражение улучшается, но полностью не рассосалось. Второй сеанс обработки, идентичный первому, проводили через 3 недели после первой обработки. Контрольный осмотр через 1 неделю после второго сеанса обработки показал, что поражение СК полностью рассосалось, без признаков рубцевания или изменения пигментации (гиперпигментации или гипопигментации). Контрольный осмотр через 8 недель после второго сеанса обработки (11 недель после первой обработки) не выявил рецидивов поражения и нежелательных косметических последствий. Субъект остался очень доволен результатами.
ПРИМЕР 4
Обыкновенную бородавку на щеке белого мужчины в возрасте 56 лет (тип кожи 2 по Фицпатрику) обрабатывали раствором, содержащим 40% пероксида водорода (FMC/PeroxiChem ʺSuper Dʺ), и 5% 2-пропанола (Spectrum Chemical, соответствует требованиям Фармакопеи США). После очистки кожи 70% 2-пропанолом, раствор наносили местно на поражение себорейным кератозом с помощью распушенного аппликатора в форме "козьей ножки". Используя сильное надавливание и методику нанесения, соответствующую размеру целевого поражения, раствор наносили в течение приблизительно 20-30 секунд. Приблизительно через 1-2 минуты процесс нанесения повторяли. Эту последовательность повторяли до проведения 4 процедур нанесения. Процедура не вызывала боли или ощущения дискомфорта. На протяжении нескольких последующих дней поражение демонстрировало образование поверхностной корки и слабую эритему (покраснение). Контрольный осмотр через 2 недель после обработки показал, что бородавка полностью рассосалась, без эритемы и без признаков рубцевания или изменения пигментации (гиперпигментации или гипопигментации). Контрольный осмотр через 8 недель после обработки не выявил рецидивов поражения и нежелательных косметических последствий. Субъект остался очень доволен результатами.
ПРИМЕР 5
Были проведены рандомизированные двойные слепые исследования с контролем по плацебо с параллельными группами с 22 субъектами, для оценки эффективности местного применения 40% раствора пероксида водорода и 5% 2-пропанола при нанесении раз в неделю (максимум 4 нанесения) на обыкновенные бородавки, лечение которых ранее не проводилось, на конечностях (не околоногтевые или подногтевые) по сравнению с аналогичным раствором носителя для местного применения. Протокол лечения включал (1) очистку целевой бородавки протиранием тампоном/салфеткой, смоченными 70% 2-пропанолом; (2) смачивание предоставленного аппликатора количеством исследуемого лекарственного средства, достаточным для увлажнения целевой бородавки тонким слоем; (3) нанесение исследуемого лекарственного средства на целевую бородавку в течение приблизительно 10 секунд, используя сильное надавливание и круговые движения; (4) поглощение избытка исследуемого лекарственного средства чистой поглощающей салфеткой (или эквивалентом) для минимизации воздействия на нормальную окружающую кожу; (5) повторение процедуры нанесения 3 раза после периода ожидания, равного около 20 секунд после каждого нанесения. После завершения третьего нанесения на целевую бородавку исследуемого лекарственного средства, целевую бородавку не беспокоили до прекращения всех визуально заметных реакций, если они были. Приблизительно через 10 минут, все остатки исследуемого лекарственного средства собирали впитывающим средством и целевую бородавку подсушивали без протирания или растирания. 17 субъектов завершили все четыре процедуры обработки раз в неделю. Все субъекты хорошо переносили процедуру, без жалоб на нежелательные реакции, и местные кожные реакции описывались как отсутствующие или слабые. Хотя после завершения этих предварительных исследований ни одно из бородавчатых поражений не рассосалось полностью (4 дозы раз в неделю) - ожидалось, что некоторые из бородавчатых поражений продемонстрируют улучшение, но полное исцеление поражения может потребовать более четырех сеансов лечения (например, до 10 или до 30 сеансов лечения или больше) -что является обычным при местном лечении бородавок - (например, отпускаемая без рецепта салициловая кислота для ежедневного применения) или потребует более частого применения, чем раз в неделю (например, два раза в неделю или ежедневно) -было продемонстрировано статистически значимое улучшение поражений и получено подтверждение концепции. Субъекты продемонстрировали статистически значимое улучшение тяжести бородавок, определяемой с использованием средних значений по балльной шкале оценки улучшения бородавок (Wart Improvement Assessment score) во время посещений врача (Фигура 8) и средней величины изменений базовых значений по балльной шкале оценки тяжести бородавок (Wart Severity Assessment score) во время посещений врача (Фигура 9). На Фигуре 7 приведено описание балльной шкалы оценки улучшения бородавок и балльной шкале оценки тяжести бородавок.
ПРИМЕР 6
Были проведены исследования in vitro высвобождения лекарственного средства и in vitro проницаемости через кожу. Было приготовлено тринадцать композиций 40 % мас./мас. пероксида водорода с использованием маточного раствора стабилизированного пероксида водорода ʺSuper Dʺ 50% FMC/PeroxyChem в качестве источника пероксида, с разными уровнями содержания 1- и 2-пропанола для проведения оценки, как указано в Таблице 1.
Таблица 1
Были проведены исследования in vitro высвобождения лекарственного средства (на основании рекомендаций SUPAC) для 13 композиций. Жидкостью-приемником был фосфатно-солевой буфер (PBS), синтетической мембраной был силикон (выбранный после предварительных исследований пригодности), и объем отбираемых образцов составлял 1 мл, при пополнении 1 мл. Моментами времени, в которые проводились измерения, были 0 мин, 0,5 ч, 1 ч, 2 ч, 4 ч, 6 ч и 8 ч. Фигура 1 изображает среднее кумулятивное количество пероксида водорода, высвобождаемой на единицу площади после нанесения всех композиций. Фигуры 2 и 3 сравнивают выделение пероксида водорода между композициями, содержащими 1- и 2-пропанол, соответственно, демонстрируя, что, в общем, увеличение содержания 1-пропанола или 2-пропанола в композициях приводит к увеличению количества пероксида водорода, высвобождаемой через силиконовую мембрану.
Хотя, в общем, большее количество пероксида водорода высвобождается после нанесения композиций, содержащих 1-пропанол, по сравнению с 2-пропанолом, в пересчете на массовое соотношение, эта тенденция наиболее заметна в композициях 1-пропанола и в композициях с более высокими концентрациями спиртов - начиная с концентраций спирта выше приблизительно 5% - и наблюдалась в значительно большей степени с увеличением концентрации спирта до 10%, 15% и 20%. Этот эффект проиллюстрирован на Фигуре 4, которая показывает установившийся режим высвобождения пероксида водорода между 0,5 ч и 4 ч для разных концентраций 1-пропанола и 2-пропанола, и на Фигуре 5, которая показывает разницу в высвобождении пероксида водорода в установившимся режиме между композициями, содержащими 1-пропанол и 2-пропанол в количествах 5-20% мас./мас. Для композиций, содержащих 1-пропанол, наблюдается увеличение высвобождения пероксида водорода при установившемся режиме (на протяжении периода времени от 0,5 до 4 ч) с увеличением содержания 1-пропанола, однако для композиций, содержащих 2-пропанол, высвобождение пероксида водорода в установившемся режиме, по-видимому, остается по существу постоянным для исследованных концентраций 2-пропанола.
Неожиданно, и важно, что этот эффект более высокой скорости выделения (0,5-4 ч) пероксида водорода из композиций 1-пропанола по сравнению с соответствующими композициями 2-пропанола, меняется на обратный при более низких концентрациях спиртов, например, ниже приблизительно 5% спирта, и скорость выделения пероксида водорода из композиций 2-пропанола при более низких концентрациях спирта (например, <5%) превышает скорость выделения пероксида водорода из композиций, содержащих 1-пропанол. Таким образом, в диапазоне более низких концентраций спирта, включаемого в композиции в соответствии с предпочтительным вариантом реализации, что является наиболее желательным, поскольку снижение до минимума концентрации добавляемого спирта может минимизировать потенциальные примеси, вводимые в пероксидную композицию, было неожиданно обнаружено, что 2-пропанол может быть предпочтительным по сравнению с 1-пропанолом. Не желая ограничиваться теорией, укажем, что, по-видимому, скорость выделения пероксида водорода при более низких концентрациях 2-пропанола выше чем для 1-пропанола.
ПРИМЕР 7
Оценка окисления путем измерения окислительно-восстановительного потенциала: Оценку окисления (путем измерения окислительно-восстановительного потенциала) проводили для 13 приготовленных композиций 40% мас./мас. пероксида водорода, описанных в Таблице 1, с кожей и без нее, в моменты времени t=0, 1, 6 и 24 ч (выполняли n=3 повторных измерений). Данные об окислительно-восстановительных потенциалах для каждой из 13 композиций, приведенные в Таблице 1 выше, представлены графически на Фигуре 10.
Если для композиций, содержащих менее чем 5% мас./мас. пропанола, данные не были статистически значимыми, то для композиций, содержащих от 5% до 20% мас./мас. пропанола, более высокие (более положительные) окислительно-восстановительные потенциалы были определены для композиций, содержащих 1-пропанол, по сравнению с 2-пропанолом. Таким образом, 1-пропанол при включении в композиции пероксида водорода в данном диапазоне концентраций (т.е., 40%), будет иметь более высокую склонность к окислению, чем 2-пропанол при включении в такие же композиции пероксида водорода. Аналогичная тенденция наблюдается в присутствии кожи, причем разность окислительно-восстановительных потенциалом между композициями, содержащими 1-пропанол и 2-пропанол, сохраняется неизменной. Данные, полученные в результате исследований по исследованию окислительно-восстановительного потенциала композиций 40% мас./мас. пероксида водорода, содержащих 5% мас./мас. 1- или 2-пропанола, в присутствии кожи и без нее, проиллюстрированы на Фигуре 11. Таким образом, хотя теоретически можно ожидать, что вторичные спирты, (например, 2-пропанол) по своей природе являются менее стабильными в высоких концентрациях пероксида водорода, чем первичные спирты, этот неожиданный результат, фактически, демонстрирует, что 2-пропанол является менее склонным к окислению, чем 1-пропанол, в этих вариантах реализации, и включение 2-пропанола в такие растворы будет предпочтительным.
ПРИМЕР 8
Анализ поверхностного натяжения проводили для 13 композиций 40% пероксида водорода с разными концентрациями 1-пропанола или 2-пропанола из Таблицы 1 при 37°C (с двумя параллельными измерениями) с использованием тензиометра Kruss и методики пластинки Вильгельми. Калибровка системы с использованием деионизированной воды продемонстрировала результаты с отклонениями не более 1,0 мН/м от литературных данных при 37°C (ок. 70 мН/м). Для каждого образца использовали время проведения эксперимента 30 минут и результат рассчитывали как среднее для 10 последних определений.
Анализ образцов проводили с двумя параллельными измерениями при 37 ± 0,5°C с использованием уровня доверительной вероятности ± 1,4%. В тех случаях, когда результаты двух параллельных измерений выходили за пределы этого интервала, проводили третье измерение и итоговый результат рассчитывали по 2 ближайшим индивидуальным результатам. Все данные представлены в Таблице 2 ниже и проиллюстрированы на Фигуре 6.
Таблица 2
Данные демонстрируют, что, в общем, включение 1-пропанола или 2-пропанола снижает поверхностное натяжение исследуемой композиции пероксида водорода, и что этот эффект понижения поверхностного натяжения является около пропорциональным концентрации добавленного 1-пропанола или 2-пропанола. Теоретически, с точки зрения поверхностного натяжения, любой из них может считаться полезным для включения в варианты реализации, раскрытые в данном документе.
Однако, эффект понижения поверхностного натяжения пероксидных композиций 1-пропанолом является более сильным, чем у 2-пропанола, так что в предпочтительных вариантах реализации композиции, содержащие 1-пропанол, будут иметь значительно более низкое поверхностное натяжение, чем соответствующие композиции с 2-пропанолом, и будут иметь значительно меньшую вероятность растекания за пределы области нанесения и поражения на окружающую не имеющую поражений кожу, тем самым снижая эффективность лекарственного средства и выступая в качестве субстрата алкогольдегидрогеназы (ADH) в коже, что приводит к усилению раздражения, эритемы, и нежелательным кожным эффектам, раздражающим окружающую кожу. В данных иллюстративных исследованиях и примерах использовался 40% пероксид водорода, но за счет изменения концентрации спиртового компонента (например, 2-пропанола) в других композициях пероксида водорода в соответствии с вариантами реализации, описанными в данном документе (например, с концентрациями пероксида водорода 25%, 32,5%, 40%, 42,5%), можно легко определить оптимальную концентрацию спирта, которая обеспечит оптимальное снижение поверхностного натяжения, достижение желательного клинического эффекта и снижение до минимума риска нежелательных местных кожных эффектов.
ПРИМЕР 9
Готовили растворы с использованием стабилизированного пероксида водорода (Peroxal CG 50®Arkema, Inc.) и 99%-го 2-пропанола (Spectrum Chemical, соответствует требованиям Фармакопеи США) для получения композиции, содержащей 40% стабилизированного пероксида водорода и 5% 2-пропанола, и композиции, содержащей 25% стабилизированного пероксида водорода и 5% 2-пропанола. Растворы помещали (для проведения испытаний) на стабильность во флаконы из янтарного боросиликатного стекла типа I с закручивающимися крышечками и выдерживали при 25 °C/60% относительной влажности (RH); 40 °C/75% RH; и 5°C (в холодильнике). Растворы 25% стабилизированной H2O2/5% изопропилового спирта (ИПС) оставались стабильными (ʺin specificationʺ (в указанных в спецификации пределах) в соответствии с Согласованном трехстороннем руководстве Международной конференции по гармонизации - Испытания на стабильность новых лекарственных субстанций и продуктов Q1A(R2)ʺ, текущая редакция Стадии 4, от 6 февраля 2003 г.) при 40°C в течение 6 месяцев, и как при 25 °C, так и при 5°C в течение 24 месяцев. Растворы 40% стабилизированной H2O2/5% ИПС оставались стабильными (ʺв указанных в спецификации пределахʺ в соответствии с Согласованном трехстороннем руководстве Международной конференции по гармонизации - Испытания на стабильность новых лекарственных субстанций и продуктов Q1A(R2)ʺ, текущая редакция Стадии 4, от 6 февраля 2003 г.) при 40°C в течение 6 месяцев, при 25°C и 5°C в течение 24 месяцев.
ПРИМЕР 10
Готовили растворы с использованием стабилизированного пероксида водорода (Peroxal CG 50®Arkema, Inc.) и 2-пропанола 99% (Spectrum Chemical, соответствует требованиям Фармакопеи США) для приготовления композиции, содержащей 40% стабилизированного пероксида водорода и 15% 2-пропанола, и композиции, содержащей 25% стабилизированного пероксида водорода и 15% 2-пропанола. Растворы помещали (для проведения испытаний) на стабильность во флаконы из янтарного боросиликатного стекла типа I с закручивающимися крышечками и выдерживали при 25 °C/60% относительной влажности (RH); 40 °C/75% RH; и 5°C (в холодильнике). Растворы 25% стабилизированной H2O2/15% ИПС оставались стабильными (ʺв указанных в спецификации пределахʺ в соответствии с Согласованном трехстороннем руководстве Международной конференции по гармонизации - Испытания на стабильность новых лекарственных субстанций и продуктов Q1A(R2)ʺ, текущая редакция Стадии 4, от 6 февраля 2003 г.) при 40°C в течение 6 месяцев, и как при 5 °C, так и при 25 °C, в течение 24 месяцев. Растворы 40% стабилизированной H2O2/15% ИПС оставались стабильными (ʺв указанных в спецификации пределахʺ в соответствии с Согласованном трехстороннем руководстве Международной конференции по гармонизации - Испытания на стабильность новых лекарственных субстанций и продуктов Q1A(R2)ʺ, текущая редакция Стадии 4, от 6 февраля 2003 г.) при 40°C в течение 6 месяцев, и как при 5 °C, так и при 25°C в течение 24 месяцев.
ПРИМЕР 11
Готовили растворы с использованием стабилизированного пероксида водорода (FMC/PeroxyChem ʺSuper D 50%ʺ (FMC/PeroxyChem) и 2-пропанола 99% (Spectrum Chemical, соответствует требованиям Фармакопеи США) для приготовления композиции, содержащей 45% стабилизированного пероксида водорода и 5% 2-пропанола. Растворы помещали (для проведения испытаний) на стабильность во флаконы из янтарного боросиликатного стекла типа 1 в климатические камеры и выдерживали при 25 °C/60% относительной влажности (RH), 40 °C/75% RH, и 5°C (в холодильнике). Растворы 45% стабилизированной H2O2/5% ИПС оставались стабильными (ʺв указанных в спецификации пределахʺ в соответствии с Согласованном трехстороннем руководстве Международной конференции по гармонизации - Испытания на стабильность новых лекарственных субстанций и продуктов Q1A(R2)ʺ, текущая редакция Стадии 4, от 6 февраля 2003 г.) при 40°C в течение 6 месяцев, и как при 5 °C, так и при 25 °C, в течение 12 месяцев.
ПРИМЕР 12
Готовили растворы с использованием стабилизированного пероксида водорода (FMC/PeroxyChem ʺSuper D 50%ʺ (FMC/PeroxyChem) и 2-пропанола 99% (Spectrum Chemical, соответствует требованиям Фармакопеи США) для приготовления композиции, содержащей 40% стабилизированного пероксида водорода и 5% 2-пропанола. Аликвоты растворов помещали в запаиваемые раздавливаемые стеклянные ампулы. Растворы/ампулы помещали (для проведения испытаний) на стабильность в камеры и выдерживали в условиях 25 °C/60% относительной влажности (RH); 40 °C/75% RH; и 5°C (в холодильнике). Растворы 40% стабилизированной H2O2/5% ИПС оставались стабильными (ʺв указанных в спецификации пределахʺ в соответствии с Согласованном трехстороннем руководстве Международной конференции по гармонизации - Испытания на стабильность новых лекарственных субстанций и продуктов Q1A(R2)ʺ, текущая редакция Стадии 4, от 6 февраля 2003 г.) как при 5 °C, так и при 25 °C, в течение 12 месяцев до настоящего времени.
ПРИМЕР 13
Готовили растворы с использованием стабилизированного пероксида водорода (FMC/PeroxyChem ʺSuper D 50%ʺ (FMC/PeroxyChem, Inc.) и 2-пропанола 99% (Spectrum Chemical, соответствует требованиям Фармакопеи США) для приготовления композиции, содержащей 40% стабилизированного пероксида водорода и 5% 2-пропанола. Готовили растворы и аликвоты помещали во флаконы из янтарного боросиликатного стекла типа I с закручивающимися крышечками. Растворы помещали (для проведения испытаний) на стабильность в камеры и выдерживали в условиях 25 °C/60% относительной влажности (RH) и 5°C (в холодильнике). Растворы 40% стабилизированной H2O2/5% ИПС оставались стабильными (ʺв указанных в спецификации пределахʺ в соответствии с Согласованном трехстороннем руководстве Международной конференции по гармонизации - Испытания на стабильность новых лекарственных субстанций и продуктов Q1A(R2)ʺ, текущая редакция Стадии 4, от 6 февраля 2003 г.) при 25°C и 5°C в течение 12 месяцев до настоящего времени.
ПРИМЕР 14
Были приготовлены следующие композиции с использованием стабилизированного пероксида водорода (Peroxal CG 50®Arkema, Inc.), 2-пропанола 99% (Spectrum Chemical, соответствует требованиям Фармакопеи США), содержащие от около 44% до около 46% (мас./мас.) стабилизированного пероксида водорода, 0% или 5% 2-пропанола (как указано в Таблице 3) и гелеобразующий агент, содержащий Carbopol ETD 2020, Carbopol 974P, или Carbopol Ultrez 10, в концентрациях, указанных в Таблице 3. Динатрия ЭДТА также включали во все композиции в качестве хелатирующего агента, и pH доводили до величины от около pH 3,5 до около pH 4,0. Для максимального увеличения уровня содержания перекиси водорода в гелевых композициях, стадию регулировки pH (с использованием 1% и 10% триэтиламина) проводили после приготовления композиций и поэтому количественный состав (% мас./мас.) в Таблице 3 представляет собой фактические концентрации композиций, помещенных на испытания на стабильность.
Композиции помещали (для проведения испытаний) на стабильность в камеры и выдерживали при 25 °C/60% относительной влажности (RH); 40 °C/75% RH; и 5°C (в холодильнике). Гелевые композиции стабилизированного пероксида водорода, указанные выше, анализировали на стабильность и на основании определений выделения пероксида водорода, pH, и вязкости по Брукфильду было показано, что через t=6 недель Carbopol ETD, Carbopol 974 P и Carbopol Ultrez 10 2020 обеспечивали поддержание концентраций пероксида водорода и их химической и физической стабильности. Стабильность на протяжении данного периода времени является достаточным показателем стабильности для двухкомпонентной гелевой композиции (или трех- или более компонентной композиции с дополнительными вспомогательными веществами, такими как изопропиловый спирт), смешиваемой во время применения или непосредственно перед ним, в которой, например, пероксид водорода и гелеобразующий агент хранятся в отдельных отсеках (например, разделены хрупкой (перегородкой), в отдельных флаконах, в отдельных шприцах) и объединяются или смешиваются при необходимости.
ПРИМЕР 15
Были проведены рандомизированные двойные слепые интраиндивидуальные исследования с контролем по носителю для определения безопасности, переносимости и эффективности растворов пероксида водорода/2-пропанола у субъектов с себорейным кератозом. Главной целью этого исследования была оценка эффективности трех разных растворов пероксида водорода/5% 2-пропанола (25% H2O2, 32,5% H2O2, и 40% H2O2) при нанесении на поражения на спине, вызванные себорейным кератозом (СК), по сравнению с соответствующим носителем. Вторичные цели включали оценку безопасности и переносимости растворов активного вещества при местном нанесении субъектам с СК. Тридцать два субъекта завершили исследования и были включены в анализы эффективности. Все субъекты имели стабильный клинически типичный СК, с соответствующими поражениями СК на спине.
Субъекты были рандомизированы по исследуемым лекарственным средствам (индивидуально определенное исследуемое лекарственное средство для каждого отдельного поражения), и исследуемые лекарственные средства наносили на назначенные поражения поражения, причем каждое отдельное поражение обрабатывали разными исследуемыми лекарственными средствами в 1 сутки. При последующем контроле через 3 недели после начального применения лекарственного средства, для каждого отдельного поражения, которое не рассосалось полностью, проводилась повторная обработка путем нанесения исследуемого лекарственного средства. Проводилось наблюдение за субъектами для оценки эффекта лечения на протяжении в общей сложности 78 дней после второго применения исследуемого лекарственного средства.
Статистически значимые отличия в эффективности активного средства по сравнению с носителем были впервые обнаружены для 40% раствора начиная с 29 суток, через семь дней после второго сеанса обработки. Показатели длины наибольшей оси, длины перпендикулярной оси и высоты поражения все демонстрировали статистически значимое улучшение по сравнению с носителем. Композиции всех концентраций в общем хорошо переносились, наблюдались только слабое ʺжжениеʺ в момент нанесения раствора и слабые доза-ассоциированные преходящие местные кожные реакции (например, отек, эритема) во время нанесения раствора. Не наблюдалось долговременных пигментных изменений.
ПРИМЕР 16
Проводили рандомизированные двойные слепые исследования с контролем по плацебо с параллельными группами с использованием композиций (i) 40% мас./мас. пероксида водорода и 5% 2-пропанола, (ii) 32,5% мас./мас. пероксида водорода и 5% 2-пропанола, и (iii) раствор носителя для лечения поражений, вызванных себорейным кератозом, на теле и конечностях пациентов. Главной целью этих исследований была оценка соотношения доза-отклик для композиций с 2 концентрациями пероксида водорода и их соответствующего носителя при нанесении на поражения, вызванные СК, на теле/конечностях. Дополнительной целью была оценка безопасности и эффективности композиций с 2 концентрациями пероксида водорода и их соответствующего носителя при местном нанесении до 2 раз на поражения, вызванные СК, на теле/конечностях. Исследователи идентифицировали по четыре подходящих поражения, вызванных СК, у каждого субъекта. Каждое выбранное поражение обрабатывали максимум два раза. Для каждого субъекта, четыре выбранных поражения находились все на теле/конечностях. Кожу пациента сначала очищали 70% 2-пропанолом, и тонкую пленку композиции пероксида водорода наносили местно на поражение (поражения) на теле/конечностях, вызванные себорейным кератозом, с помощью распушенного аппликатора в форме "козьей ножки". Используя сильное надавливание и методику нанесения, соответствующую размеру целевого поражения (например, касательно-роликовый аппликатор для поражений меньшего размера; втирание круговыми движениями для поражений большего размера), наносили раствор в течение приблизительно 20-30 секунд. Исследователь принимал меры по минимизации воздействия на окружающую нормальную кожу. В процессе нанесения, избыток исследуемого лекарственного средства удаляли с окружающей нормальной кожи с помощью чистой впитывающей салфетки. Исследователь следил за тем, чтобы выбранное поражение было увлажнено исследуемым лекарственным средством по истечении 20-30 секунд и оставлял выбранное поражение в покое приблизительно на 1-2 минуты. Эту последовательность действий повторяли до 4 раз с перерывом на 1-2 минуты между процедурами нанесения. Контрольный осмотр проводили многократно, включая моменты времени через 1 и 3 недели после обработки. При необходимости, второй сеанс обработки, идентичный первому, проводили через 3 недели после первой обработки. Проводили оценку поражений для определения их клинического отклика через 12 недель после последней обработки. Сто шестьдесят девять субъектов завершили исследования. Первичная конечная точка, средний по индивидуальным субъектам процент выбранных поражений, признанных удаленными по шкале PLA (оценка поражений врачем) при последнем посещении врача, составляла 45,1% для 40% мас./мас. пероксида водорода и 5% 2-пропанола, и 26,8% для 32,5% мас./мас. пероксида водорода и 5% 2-пропанола, по сравнению с 4,8% для носителя. Значительно большее по сравнению с носителем улучшение для обоих композиций наблюдалось при первой оценке результатов, причем зависимость от дозы была заметной при каждом посещении. Местные кожные реакции были преимущественно слабыми. Результаты этих исследований подтверждают, что местное нанесение растворов как 40% H2O2, так и 32,5% H2O2 на вызванные СК поражения с использованием предписанного метода и композиции обладают потенциалом к безопасному и эффективному удалению вызванных СК поражений без необходимости в обезболивании и/или анестезии, и с минимальным риском гипопигментации, гиперпигментации, или рубцевания.
ПРИМЕР 17
Были проведены рандомизированные двойные слепые исследования с контролем по плацебо с параллельными группами с использованием композиций (i) 40% мас./мас. пероксида водорода и 5% 2-пропанола, (ii) 32,5% мас./мас. пероксида водорода и 5% 2-пропанола, и (iii) раствора носителя для лечения поражений, вызванных себорейным кератозом, на лице пациентов. Главной целью этих исследований была оценка соотношения доза-отклик для композиций с двумя концентрациями пероксида водорода и их соответствующего носителя при нанесении на поражения, вызванные СК, на лице. Дополнительной целью была оценка безопасности и эффективности композиций с двумя концентрациями пероксида водорода и их соответствующего носителя при местном нанесении до двух раз на поражения, вызванные СК, на лице. Исследователь идентифицировал по одному подходящему поражению, вызванному СК, на лице каждого субъекта. Выбранное поражение обрабатывали максимум два раза. Защитная композиция на основе масла (такая как 100% медицинский вазелин) необязательно наносилась вдоль глазничного валика и у медиального или латерального углов глазной щели; осторожно растягивали кожу периорбитальной области большим и указательным пальцем во время нанесения вазелина для растягивания каких-либо периорбитальных морщин (например, ʺгусиных лапокʺ) и обеспечения полного покрытия кожи у основания морщин для уменьшения вероятности просачивания исследуемого лекарственного средства в направлении к глазу. Субъектов дополнительно инструктировали держать впитывающий тампон в соответствующей области глаза для поглощения любого избытка исследуемого лекарственного средства, которое может растекаться от выбранного поражения, и держать оба глаза закрытыми на протяжении всей процедуры нанесения исследуемого лекарственного средства. Кожу пациента сначала очищали 70% 2-пропанолом, и тонкий слой композиции пероксида водорода наносили местно на поражение (поражения), вызванные себорейным кератозом, на лице пациента с помощью распушенного аппликатора в форме "козьей ножки". Используя сильное надавливание и методику нанесения, соответствующую размеру целевого поражения (например, касательно-роликовый аппликатор для поражений меньшего размера; втирание круговыми движениями для поражений большего размера), наносили раствор в течение приблизительно 20-30 секунд. Исследователь принимал меры к тому, чтобы минимизировать воздействие на окружающую нормальную кожу. В процессе нанесения, избыток исследуемого лекарственного средства удаляли с окружающей нормальной кожи с помощью чистой впитывающей салфетки. Исследователь следил за тем, чтобы выбранное поражение было увлажнено исследуемым лекарственным средством по истечении 20-30 секунд и оставлял выбранное поражение в покое на приблизительно 60 секунд. Эта последовательность действий повторялась до 4 раз с перерывом на 1-2 минуту между нанесениями. Контрольный осмотр проводили в несколько моментов времени, включая через 3 недели после обработки. При необходимости, второй сеанс обработки, идентичный первому, проводили через 3 недели после первой обработки. Проводили оценку поражений для определения их клинического отклика через 12 недель после последней обработки. Сто шестнадцать субъектов завершили исследования. Первичной конечной точкой было попарное сравнение между носителем и каждой из групп активного лекарственного средства, основанное на среднем отклонении от базового значения по шкале PLA (оценка поражения врачем) при каждом посещении врача после базовой линии с использованием метода ковариационного анализа (ANCOVA). Значительно большее по сравнению с носителем улучшение наблюдалось для обоих композиций начиная с первой процедуры оценки, причем зависимость от дозы была заметной при каждом посещении. Местные кожные реакции были преимущественно слабыми. Результаты этих исследований подтверждают, что местное нанесение обоих растворов, как 40% H2O2, так и 32,5% H2O2, на вызванные СК поражения на лице с использованием предписанного метода и композиции, обладает потенциалом безопасного и эффективного удаления вызванного СК поражения без необходимости обезболивания и/или анестезии, и с минимальным риском гипопигментации, гиперпигментации или рубцевания.
ПРИМЕР 18
Белому мужчине в возрасте 60 лет с типом кожи III по Фицпатрику проводили нанесение раствора для местного применения, содержащего 40% H2O2 и 5% изопропилового спирта (ИПС) на выглядящий клинически типичным яйцевидный себорейный кератоз в правой височной области размером 18,7×24,0 мм. Перед началом нанесения раствора наносили вазелин с помощью аппликатора с ватным кончиком на область, окружающую кератозное поражение, для предотвращения растекания раствора по статическим и динамическим морщинам на лице и более надежного удерживания раствора на поражении.
Раствор наносили, как описано: выбранное поражение тщательно очищали протиранием с приложением силы с помощью аппликатора с ватным кончиком, смоченным 70% изопропиловым спиртом (ИПС). Следили за тем, чтобы не подносить флаконы с ИПС и раствором H2O2 к лицу субъекта. После очистки поражения, аппликатор, представляющий собой нейлоновый распушенный аппликатор в форме "козьей ножки", смачивали количеством раствором исследуемого лекарственного средства на основе пероксида/ИПС, достаточным для смачивания выбранного поражения тонким слоем. Используя давление от среднего до сильного и методику нанесения, соответствующую размеру выбранного поражения, наносили раствор круговыми движениями в количестве, достаточном покрытия всей поверхности поражения (себорейный кератоз) в течение приблизительно 30 секунд. Принимали меры по минимизации воздействия на окружающую нормальную кожу. В процессе нанесения избыток исследуемого лекарственного средства удаляли с окружающей нормальной кожи с помощью чистой впитывающей салфетки, промакивая избыточное количество. Поражение затем оставляли в покое приблизительно на 1-2 минуты. Раствор оставался в области нанесения на кожное поражение. Приблизительно через 1-2 минуты, процесс нанесения повторяли до тех пор, пока раствор пероксида/ИПС не наносили на поражение в общей сложности 4 раза.
Процедура переносилась хорошо и без осложнений. Максимальный дискомфорт был описан как ʺжжениеʺ, достигавшее максимального значения ʺоколо 1ʺ (слабое) по 5-балльной шкале (0-4). При завершении сеанса нанесения, область нанесения демонстрировала реакцию ʺповерхностного отбеливанияʺ, которая распространялась только на область нанесения раствора, с минимальной сопутствующей эритемой. Раствор на стекал с поражения и не наблюдалось отбеливания или любых нежелательных эффектов за пределами области нанесения. При опросе приблизительно через 20 минут после последнего нанесения было отмечено, что ощущение дискомфорта уже полностью прекратилось (было оценено как "0/4"). Оценка через около 75 минут после последнего нанесения показала почти полное рассасывание реакции ʺповерхностного отбеливанияʺ.
На протяжении нескольких последующих дней происходило образование поверхностной корки на обработанном участке и на протяжении нескольких следующих недель поражение сошло путем отшелушивания без осложнений. Контрольный осмотр через 38 дней после начального нанесения показал полное заживление области обработки с почти полным рассасыванием первичного подвергнутого обработке поражения, за исключением маленького участка у нижнего края первичной области нанесения. Этот участок обработали снова в указанный момент времени в соответствии с описанным выше способом, по той же процедуре, с таким же откликом, и без осложнений. Снова происходило образование поверхностной корки на обработанном участке, которая сошла в течение ʺоколо неделиʺ по словам субъекта. Последующий контроль через 31 сутки после второй обработки показал полное удаление поражения с прекрасным косметическим результатом. Субъект остался очень доволен результатами. Долгосрочный контроль через 193 суток после первой обработки (155 дней после второй обработки) показал отсутствие рецидива исходного поражения, вызванного СК, и сохранение отличных косметических результатов.
ПРИМЕР 19
Будут проведены интраиндивидуальные исследования с контролем по носителю биодоступности раствора пероксида водорода и 2-пропанола для местного применения, который был введен в условиях максимального использования субъектам с клинически типичным себорейным кератозом на спине. Главной целью этих исследований будет оценка относительной биодоступности раствора 40% пероксида водорода/5% 2-пропанола при местном введении в условиях максимального использования субъектам с себорейным кератозом (СК) на теле, лице и конечностях. Дополнительной целью будет оценка безопасности раствора 40% пероксида водорода/5% 2-пропанола при местном введении в условиях максимального использования субъектам с себорейным кератозом на теле, лице и конечностях. Ожидается, что каждый субъект будет иметь 10 поражений, вызванных СК, на теле, лице и конечностях, для проведения лечения и оценки. По меньшей мере одно выбранное поражение у каждого субъекта будет находиться на лице. В ходе проведения исследований, исследователь идентифицирует 10 подходящих поражений, вызванных СК, на теле, лице и конечностях каждого субъекта. Каждое выбранное поражение, вызванное СК, будет обработано один раз (первый) раствором носителя для получения образцов крови для фармакокинетического анализа до проведения лечения, и затем, через одну неделю, композицией активного вещества.
Образцы крови для фармакокинетического (ФК) анализа пероксида водорода будут отобраны в моменты времени от 0 часов (непосредственно перед нанесением исследуемого лекарственного средства) до по меньшей мере около 6 часов после завершения нанесения исследуемого лекарственного средства. Образцы для ФК анализа будут отобраны в одно и то же время суток во избежание осложнений, ассоциированных с какими-либо потенциальными циркадными изменениями уровней эндогенного пероксида водорода в плазме. Исследователь будет проводить измерения клинических параметров поражений, включая размеры поражения (т.е., длину и ширину), для каждого выбранного поражения во время Посещения 1. Будет проведен статистический анализ и относительная биодоступность будет рассчитана для раствора активного вещества по сравнению с раствором носителя. Статистический анализ может включать дисперсионный анализ (ANOVA) ФК параметров Cmax, AUC0-t, и AUC0-∞. Данные Cmax и AUC0-t будут преобразованы в значения натуральных логарифмов перед проведением анализа.
Предполагается достижение главной цели этих исследований - оценки относительной биодоступности раствора 40% пероксида водорода/5% 2-пропанола при местном введении в условиях максимального использования субъектам с себорейным кератозом (СК) на теле, лице и конечностях. Предполагается, что не будет обнаружено измеримых уровней пероксида водорода в крови в данных условиях максимального использования. Предполагается достижение дополнительной цели - оценки безопасности раствора 40% пероксида водорода/5% 2-пропанола при местном введении в условиях максимального использования субъектам с себорейным кератозом на теле, лице и конечностях. Предполагается, что исследуемый раствор окажется безопасным для использования при местном введении в данных условиях максимального использования.
ПРИМЕР 20
Был получен аппликатор, содержащий композицию раствора для местного применения, содержащего 40% пероксида водорода и 5% изопропилового спирта, размещенную в хрупкой ампуле, размещенной в корпусе аппликатора, для лечения пациента с поражениями, вызванными себорейным кератозом, на лице, теле и конечностях. Поражение очищают протиранием салфеткой с 70% изопропиловым спиртом перед обработкой. Аппликатор активируют путем сдавливания корпуса аппликатора снаружи большим и указательным пальцами для разламывания хрупкой ампулы и высвобождения раствора. Аппликатор необходимо держать на расстоянии от пациента во время активирования упаковки. После активирования аппликатора, колпачок снимают, и кончик смачивают путем осторожного сдавливания снаружи корпуса аппликатора до увлажнения кончика количеством раствора, достаточным для смачивания поражения тонким слоем.
Прикладывая требуемое давление, раствор наносят на поражение круговыми движениями в течение от 20 до 30 секунд. Во время нанесения, любой избыток раствора необходимо удалять с окружающей кожи с помощью чистой впитывающей салфетки.
Обработанное поражение оставляют в покое приблизительно на 1 минуту и затем обработку повторяют. Эта процедура может быть повторена до 4 раз, пока поражение (поражения) не будут полностью насыщены раствором.
После завершения обработки каждого выбранного поражения, поражение (поражения) должны оставаться в покое до полного высыхания раствора. Обработанные поражения можно промакивать, не вытирая, впитывающей салфеткой для того, чтобы обработанное поражение было сухим к моменту ухода пациента.
Если поражение (поражения) не будет удалено полностью через приблизительно три недели, дополнительная обработка (обработки) могут быть проведены в соответствии с первоначальной процедурой.
ПРИМЕР 21
Аппликатор будет иметь корпус аппликатора, сформованный из ПЭВП, ПЭНП, или смеси ПЭВП/ПЭНП, с размещенной в нем ампулой из боросиликатного стекла. Ампула содержит дозу композиции 40% мас./мас. пероксида водорода и 5% 2-пропанола для разового нанесения. Оператор держит аппликатор в руке аналогично пишущим приспособлениям. Оператор помещает указательный палец на первую зону давления, расположенную на внешней поверхности корпуса аппликатора, и напротив него большой палец на вторую зону давления, расположенную по существу с противоположной стороны корпуса аппликатора. Оператор сдавливает корпус аппликатора своими указательным и большим пальцами с достаточным усилием для раздавливания ампулы, размещенной внутри корпуса аппликатора между первой зоной давления и второй зоной давления. Оператор смещает положение руки на аппликаторе вниз к области захвата на проксимальной части корпуса аппликатора. Оператор выдавливает композицию для ее выделения на нейлоновом распушенном кончике аппликатора в форме "козьей ножки", который находится в жидкостном сообщении с трубкой аппликатора, путем сдавливания участка поверхности захвата своими пальцами.
Фильтр, сформованный из ПЭНП, покрытого силиконовым материалом, предназначенным для придания гидрофобных свойств фильтру, размещен внутри аппликатора для задерживания осколков раздавленной ампулы. Фильтр препятствует вытеканию композиции, пока оператор не прикладывает давление к корпусу аппликатора. Оператор контролирует скорость вытекания из аппликатора на выбранное место применения (например, кожное поражение) путем изменения давления, приложенного к участку поверхности захвата. Оператор затем обрабатывает выбранное поражение или поражения.
Хотя настоящее изобретение было описано весьма детально со ссылками на определенные предпочтительные варианты его реализации, возможны другие варианты. Поэтому сущность и объем прилагаемой формулы изобретения не должны ограничиваться описанием и предпочтительными вариантами, содержащимися в данном описании изобретения.
Реферат
Изобретение относится к фармацевтической промышленности и представляет собой композицию для местного применения для лечения кожного состояния, содержащую от около 25 мас./мас.% до около 50 мас./мас.% пероксида водорода и от около 1 мас./мас.% до около 5 мас./мас.% 2-пропанола. Изобретение обеспечивает повышение уровня высвобождения пероксида водорода, состав по изобретению менее подвержен окислению, то есть является более стабильным и обладает выраженным эффектом уменьшения поверхностного натяжения. 4 н. и 26 з.п. ф-лы, 18 ил., 3 табл., 21 пр.
Формула
Документы, цитированные в отчёте о поиске
Терапевтическая композиция для лечения кожных заболеваний, содержащая органосилановые четвертичные соединения и пероксид водорода

Комментарии