Новые расширяющиеся сополимеры - RU2785346C1
Код документа: RU2785346C1
Чертежи
Описание
Настоящее изобретение относится к новой расширяемой полимеризуемой композиции/ продукту полимеризации указанной расширяемой полимеризуемой композиции, а также к способу получения продукта полимеризации. Изобретение также относится к герметику, адгезиву, покрытию, связующему или зубной пломбе, содержащей указанную расширяемую полимеризуемую композицию, а также к применению указанной расширяемой полимеризуемой композиции в качестве/в герметиках, адгезивах, покрытиях, связующих или зубных пломбах.
Объемная усадка, которая происходит в процессе полимеризации, часто игнорируется и в значительной степени недопредставлена в литературе. Усадка при полимеризации происходит в результате изменения расстояния сцепления от расстояний Ван-дер-Ваальса в мономере (3,4 Å) до ковалентных расстояний в полимере (1,5 Å). Значения усадки при полимеризации могут составлять до 50% для поликонденсационной полимеризации или до 2-5% для полимеризации с раскрытием кольца.
Основой большого количества используемых в настоящее время полимеризуемых композиций преимущественно являются эпоксиды. Такие композиции на основе эпоксидов демонстрируют объемную усадку во время полимеризации, приводящую к расслоению, растрескиванию и образованию пустот в смоле. Кроме усадки эпоксидные полимеры также имеют другие известные недостатки, включая высокое поглощение влаги и ограниченную стабильность при более высоких температурах.
Для того чтобы найти решение этой проблемы, были разработаны различные стратегии по уменьшению объемной усадки во время полимеризации. Эти стратегии основаны главным образом на трех подходах: (А) изменение условий полимеризации (фотополимеризация или термически отвержденные полимеры), (В): добавление наполнителей или добавок, и (С): изменение структуры мономера или олигомера.
Например, спироортосоединения (соединения SOC) были представлены как мономеры с исключительно высоким объемным расширением при полимеризации (Т. Takata, Т. Endo: Recent advances in the development of expanding monomers: Synthesis, polymerization and volume change. Prog. Polym. Sci 1993, 18(5), 839-870). Однако соединения SOC имеют недостаток чувствительности к воде. Другим потенциальным вопросом, связанным с промышленным применением, является тот факт, что синтез многочисленных спироортомономеров в литературе включает различные соединения, которые запрещены REACH (регистрация, оценка, разрешение и ограничение химических веществ).
Другим набором соединении, которые, как сообщалось, приводят к увеличению объема после отверждения, являются фенолытые смолы на основе бензоксазина (Н. Ishida, Н. Y. Low: A Study on the Volumetric Expansion of Benzoxazine-Based Phenolic Resin. Macromolecules 1997, 30, 1099-1106). Различные мономеры бензоксазина могут быть получены из бисфенольных звеньев (чаще всего бисфенол А), формальдегида и первичных аминов. Однако наблюдалось огромное различие между различными бензоксазинами на основе амина в их характеристиках объемного расширения. Даже если поли(бензоксазин) может преодолеть многие недостатки, описанные для полимеров на основе эпоксидов, способы получения поли(бензоксазина) требуют высоких температур и полученные полимеры, как правило, являются хрупкими, таким образом, ограничивая их спектр применения.
Увеличение объема при полимеризации циклических карбонатов, содержащих норборненовые звенья (NBC), с инициатором на основе амина было сообщено Murayama (М. Murayama: Anionic R1ng-Opening Polymerization of a Cyclic Carbonate having a Norbornene Structure with Amine Initiators. Macromolecules 1998, 31, 919-923). Сообщалось, что полимеризация чистого NBC приводит к расширению на 8,2%.
Cho и его коллеги изучали влияние на усадку включения различных лактамов в эпоксидные смолы во время сополимеризации (L.W. Chen, С.Н. Twu, C.S. Cho: Physical properties and shrinkation of epoxy resins hesed with lactams. /. Polifm. Res. 1997, 4, 65-72). Усадка уменьшалась с увеличением содержания лактама и с увеличением размера лактамного кольца.
Кроме того, сообщалось, что полиуретановые акрилаты с различными количествами стеариновых спиртов влияют на объемную усадку (L. Qin, J. Nie, Y. He: Synthesis and properties of polyurethane acrylate modified by different contents of stearyl alcohol. /. Coat. Technol. Res. 2015, 12, 197-204). В частности, полиуретановые акрилаты, модифицированные более высоким содержанием стеаринового спирта, демонстрируют меньшую объемную усадку.
Поскольку усадка полимеризации непосредственно связана с превращением реакционноспособных двойных связей, было показано, что новые фотополимеризуемые составы на основе диметилакрилатных мономеров с объемными группами заместителей демонстрируют более низкую усадку при полимеризации (J. Ge, М. Tmjillo, J. Stansbury: Synthesis and photopolymerization of low shrinkage metacrylate monomers containing bulkly substituent groups. Dent. Mater. 2005, 21, 1163-1169).
Nie и его коллеги изучали влияние температуры на объемную усадку во время фотополимеризапии диметакрилата три(этиленгликоля) (В. Lu, P. Xiao, М. Sun, J. Nie: Reducing volume shrinkage by low-temperature photopolymerization. /. Appl. Polym. Sci. 2007, 104, 1126-1130). Они обнаружили, что оптимальная температура для фотоотверждения составляет 40°С, поскольку общая конверия после реакции в темноте была аналогична конверсии, наблюдаемой при комнатной температуре, при этом усадка была значительно ниже, что являлось преимуществом.
Другое исследование показало, что усадка при фотополимеризации (мет)акрилатных покрытий зависит от преобразования двойной связи и концентрации двойных связей: мономер в основном отвечал за усадку из-за присущей ему высокой концентрации двойных связей (Y. Jian, Y. Не, Т. Jiang, С.Li, W. Yang, J. Nie: Volume shrinkage of UV-curable coating composition investigated by real-time laser reflection method. /. Coat. Technol. Res. 2013, 10, 231-237).
Другой подход связан с использованием преполимеров для предотвращения усадки по объему. Синтез новых типов гиперразветвленных сложных полиэфиров с гибкой этоксилированной структурой бисфенола А и концевыми гидроксильными группами был сообщен Serra и коллегами (Т. Li, Н. Qin, Y. Liu, Y. Zhong, Y. Yu, A. Serra: Hyperbranched polyester as additives in filled and unfilled epoxy-novolac systems. Polymer 2012, 53(25), 5864-5872).
Влияние наполнителя TiO2 на объемную усадку композитов эпоксидной смолы было изучено Томасом и коллегами (J. Parameswaranpillai, A. George, J. Pionteck, S. Thomas: Investigation of Cure Reaction, Rheology, Volume Shrinkage and Thermomechanical Properties of Nano-TiO2 Filled Epoxy/DDS Composites. /. Polym. 2013,183463:1-183463:17).
Существует потребность в альтернативных или улучшенных расширяемых полимеризуемых композициях, которые обеспечивают полимеры, имеющие улучшенное и настраиваемое поведение по расширению во время полимеризации.
Задачей настоящего изобретения является получение новой расширяемой полимеризуемой композиции на основе бензоксазинов, демонстрирующей улучшенные свойства расширения, в частности, демонстрирующей высокие, регулируемые и воспроизводимые степени расширения во время полимеризации. Еще одной задачей настоящего изобретения является получение новой расширяемой полимеризуемой композиции на основе бензоксазинов, в результате чего полимеры имеют широкий спектр применения.
Эти цели достигаются с помощью новой расширяемой полимеризуемой композиции, содержащей по меньшей мере один бензоксазин и по меньшей мере один циклический карбонат.
Настоящее изобретение основано на неожиданно обнаруженном факте того, что сополимеризация мономеров бензоксазина с циклическими карбонатными мономерами приводит к появлению новых сополимеров, имеющих непредсказуемо высокие степени расширения, при этом свойства (например, твердость/ хрупкость, твердость/мягкость, каучукоподобие) полученных сополимеров могут быть легко и воспроизводимо настроены/ скорректированы в зависимости от соотношения эквивалентов бензоксазина/эквивалентов циклического карбоната, присутствующих в композиции и сополимере, соответственно. Таким образом, новые сополимеры обеспечивают значительные преимущества по сравнению с расширяемыми полимерами, известными в данной области техники. Кроме того, полученные новые расширяемые полимеризуемые композиции и поли(бензоксазин)-сополи(циклический карбонат) -полимеры обладают большим потенциалом для обеспечения широкого спектра применений. Как будет описано более подробно ниже, сополимер может быть получен сополимеризацией бензоксазинов и циклических карбонатов при температуре, достаточной для инициирования сополимеризации, при этом оба типа мономеров подвергаются полимеризации с раскрытием кольца.
Об этих неожиданных выводах свидетельствуют экспериментальные данные, приведенные в приведенных ниже примерах. Результаты, представленные в экспериментальных данных, показывают, что для большинства сополимеров, которые были протестированы, наблюдались степени расширения более 25% или даже более 30%. Насколько известно авторам изобретения, такие высокие степени расширения никогда не сообщались до сих пор для расширяемых полимеров, таким образом, они превышают степени расширения известных расширяемых полимеров более чем на 300%.
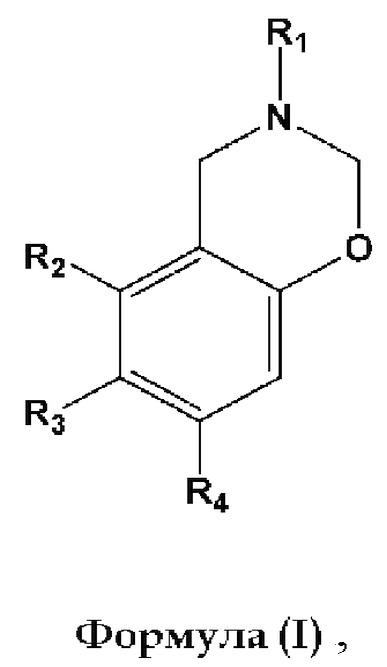
В одном аспекте настоящего изобретения по меньшей мере один бензоксазин, содержащийся в расширяемой полимеризуемой композиции, представляет собой соединение общей формулы (I):
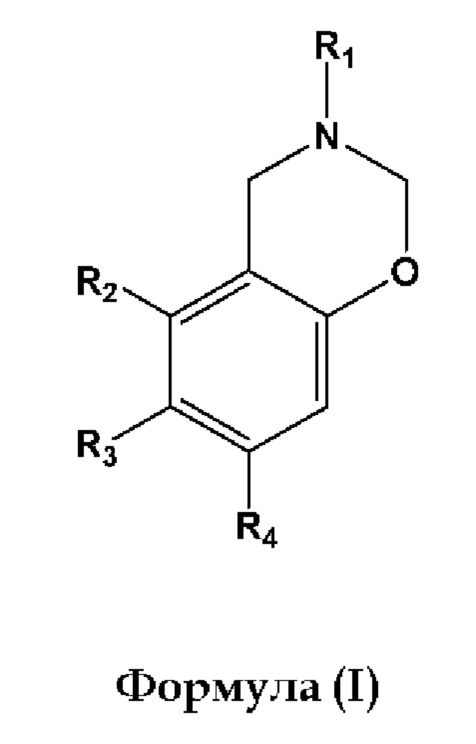
где R1, R2, R3 и R4 каждый независимо представляет собой Н, СН3, С2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкенильными или алкинильными группами, алкарильными группами, гетероалкильными группами, гетероарильными группами, гидроксигруппами, дисульфидами, сульфонатами, простыми эфирными группами, тиолоэфирными группами, сложноэфирными группами, карбоксильными группами, аминогруппами, амидными группами, азидами или бензоксазинами, и R2 может быть связан с R3 с образованием циклического заместителя на бензольном кольце, или R3 может быть связан с R4 с образованием циклического заместителя на бензольном кольце.
Термин «алкил», используемый в настоящем документе, относится к прямым или разветвленным углеводородным цепям, имеющим определенное количество атомов углерода. Например, «С2-С15 прямой, разветвленный или циклический алкил», указанный в формуле изобретения, относится к прямой, разветвленной или циклической алкильной группе, содержащей по меньшей мере 2 и не более 15 атомов углерода. Алкильные группы, имеющие прямую цепь, предпочтительно представляют собой С2-С9 алкил. Подходящие разветвленные алкильные цепи, которые предпочтительно представляют собой С3-С7 алкил, представляют собой, например, заместители композиции изопропил, изобутил, неопентил и (1'-метил)-гексил. Подходящие циклические алкильные цепи, которые предпочтительно представляют собой С4-C12 алкил, представляют собой, например, заместители композиции циклобутил, циклогексил и адамантил.
Как упоминалось выше, прямой, разветвленный или циклический алкил С2-С15 необязательно замещен одним или более заместителями, независимо выбранными из группы, состоящей из галогена, алкенильных или алкинильных групп, алкарильных групп, гетероалкильных групп, гетероарильных групп, гидроксигрупп, дисульфидов, сульфонатов, простых эфирных групп, тиолоэфирных групп, сложноэфирньгх групп, карбоксильных групп, аминогрупп, амидных групп, азидов или бензоксазинов.
Термин "галоген" в данном контексте означает галогены хлор, бром, фтор или йод, где хлор и бром являются предпочтительными, а также псевдогалогеньг CN, N3, OCN, NCO, CNO, SCN, NCS, SeCN, где N3, NCO и SCN являются предпочтительными.
Термин «алкенил», как используется в настоящем документе, относится к алкильным цепям, содержащим указанное количество атомов углерода и содержащим по меньшей мере одну углерод-углеродную двойную связь, где алкил определен, как описано выше, и может представлять собой прямую или разветвленную углеводородную цепь или может иметь кольцевые замыкания. Например, С2-С25 алкенил означает алкенил, содержащий по меньшей мере 2 и не более 25 атомов углерода и содержащий по меньшей мере одну двойную связь. Предпочтительными являются прямые алкенильные цепи. Примеры "алкенила", используемые в настоящем документе, включают, но не ограничиваются ими, 2-пропенил, Z- или Е-пропенил, бутадиенил, изопенил и циклопропенилэтил, а также Z- или Е-деценил и Е-октадец-9-енил.
Термин «алкинил», как используется в настоящем документе, относится к алкильным цепям, содержащим указанное количество атомов углерода и содержащим по меньшей мере одну углерод-углеродную тройную связь, где алкил определен, как описано выше, и может представлять собой прямую или разветвленную углеводородную цепь или может иметь кольцевые замыкания. Например, С2-С12 алкинил означает алкинил, содержащий по меньшей мере 2 и не более 12 атомов углерода и содержащий по меньшей мере одну тройную связь. Типичные примеры алкинила включают, но не ограничиваются ими, 1-пропинил, 2-пропинил, 3-бутинил и 2-пентинил, а также 1-додепинил.
Используемый в настоящем документе термин «алкарил» относится к группе формулы алкилен-арил или арилен-алкил. В частности, алкарил относится к арильной группе, присоединенной к бензоксазиновому кольцу через алкиленовую группу. В данном контексте термин «арил» относится к ароматическому карбоциклическому кольцу, содержащему определенное количество атомов углерода. Например, C5-С6 арил относится к ароматическому кольцу, содержащему по меньшей мере 5 и не более 6 атомов углерода. Термин «арил» также относится к мультициклической группе, имеющей более одного ароматического кольца, такого как С10-С14 арил. Типичные примеры арила включают, но не ограничиваются ими, циклопентадиенил, фенил, нафтил, антрацит, фенантрил. Типовые алкарильные группы имеют от 7 до 16 атомов углерода и включают, но не ограничиваются ими, бензил, фенилэтил и изопропилбензил.
Термин «гетероалкил», используемый в настоящем документе, относится к «алкильной» группе, в которой по меньшей мере один атом углерода заменен на гетероатом (например, атом О, N или S). Гетероалкил может представлять собой, например, первичные, вторичные и третичные амины, линейные, разветвленные и циклические тиоэфиры, первичные тиолы, линейные, разветвленные и циклические простые эфиры, а также карбоновые кислоты и полученные из них сложные эфиры.
Согласно некоторым вариантам реализации "гетероалкил" может представлять собой 2-8-членнъгй гетероалкил, что указывает на то, что гетероалкил содержит от 2 до 8 атомов, выбранных из группы, состоящей из углерода, кислорода, азота и серы. Согласно другим вариантам реализации гетероалкил может представлять собой 2-6-членную, 4-8-членную или 5-8-членную гетероалкильную группу (которая может содержать, например, 1 или 2 гетероатома, выбранных из группы кислорода и азота).
Используемый здесь термин «гетероарил» относится к ароматическим группам, имеющим один или более гетероатомов (О, S или N). Предпочтительные гетероарильные остатки имеют 5 или 6 кольцевых членов и включают остатки, полученные из фурана, имидазола, триазола, изотиазола, изоксазола, оксадиазола, оксазола, пиразина, пиразола, пиридазина, пиридина, пиримидина, пирролина, тиазола, тиофена, триазола и тетразола. Мультициклическая группа, имеющая один или более гетероатомов, где по меньшей мере одно кольцо группы является гетероароматическим, также называется «гетероарилом»; примером являются гетероарильные группы, имеющие от 7 до 10 членов колец, включая те, которые получены из индола, хинолина, изохинолина и тетрагидрохинолина.
Термины «гидрокси», «дисульфиды», «сульфонаты», «тиоэфир», «простой эфир», «сложный эфир» и «карбоновая кислота» являются общепризнанными в данной области техники. Иллюстративные дисульфиды включают, но не ограничиваются ими, метилдисульфанил, этилдисульфанил, фенилдисульфанил и бензилдисульфанил. Типовые сульфонаты включают, но не ограничиваются ими, мезилат, тозилат, метансульфонат натрия, метансульфонат калия и 2-метилбензолсульфонат натрия. Иллюстративные простые эфирные группы включают, но не ограничиваются ими, метокси, этокси, бензокси и фенокси. Иллюстративные тиоэфирные группы включают, но не ограничиваются ими, метилтиил, этилтиил и фенилтиил. Типовые сложноэфирные группы включают, но не ограничиваются ими, формиаты, ацетаты, пропаноаты, фталаты и бензоаты. Типовые группы карбоновых кислот включают, но не ограничиваются ими, муравьиные кислоты, уксусные кислоты, бензойные кислоты, фталевые кислоты и жирные кислоты, такие как декановые кислоты и дека-10'-еновая кислота.
Термины «амин» и «амино» известны в данной области техники и относятся к первичным, вторичным и третичным аминам, включая, но не ограничиваясь ими, этиламин, бензиламин, этилендиамин, изофорон диамин, диэтилентриамин, трет-бутиламин и триэтиламин.
Используемый в настоящем документе термин «амид» представляет собой молекулу, имеющую по меньшей мере одну идентифицируемую амидную группу. Типовые амиды включают, но не ограничиваются ими, ацетамидометил, пропионамидометил и бензамидометил.
Используемый в настоящем документе термин «азид» относится к любой группе, содержащей фрагмент N3. Иллюстративные азиды включают, но не ограничиваются ими, (4Н-1,2,3-триазол-4-ил)метил, (5-метил-4Н-1,2,3-триазол-4-ил)метил, (5-этил-4Н-1,2,3-триазол-4-ил)метил и (5-фенил-4Н-1,2,3-триазол-4-ил)метил, а также азидометил, азидоэтил, азидопропил, 4-азидофенил и 4-азидо бензил.
В настоящем документе термин «бензоксазин» относится к соединениям и полимерам, содержащим характерное бензоксазиновое кольцо. Иллюстративные заместители бензоксазина включают, но не ограничиваются ими, (2Н-бензо [е][1,3]оксазин-3(4Н)-ил)метил, (5,6,7-триметил-2Н-бензо [е][1,3]оксазин-3(4Н)-ил)метил, (7-амино-5-азидо-6-гидрокси-2Н-бензо [е][1,3]оксазин-3(4Н)-ил)метил и 2-((2Н-бензо[е][1,3]оксазин-3(4Н)-ил)метил)бензил. Например, в основе синтеза мономеров бензоксазина формулы (I), где один из R1, R2, R3 и R4 представляет собой С2-С15 прямой, разветвленный или циклический алкил, замещенный бензоксазином, может лежать симметричное бисфенольное соединение или дигидроксибензольное соединение.
Термин «замещенный» относится к химическому соединению, замещенному одним или более заместителями. Термин «необязательно замещенный», относящийся к химическому объекту, означает, что химический объект может быть замещен или не замещен, т.е. включены обе ситуации. Термин «один или более заместителей» относится к количеству заместителей от одного до максимального количества возможных заместителей, в зависимости от количества доступных сайтов замещения.
Согласно некоторым вариантам реализации R2 может быть связан с R3 с образованием циклического заместителя на бензольном кольце. Согласно другим вариантам реализации R3, может быть связан с R4 с образованием циклического заместителя на бензольном кольце. Иллюстративные циклические заместители включают, но не ограничиваются ими, 3-аллил-1,3-оксазинан-5,6-диил, 3-аллил-4-метил-1,3-оксазинан-5,6-диил, циклогексан-1,2-пиил и бетол-1,2-диил. Например, путем связывания R2 с R3 или путем связывания R3 с R4 может быть образован циклический заместитель в форме 4 -, 5- или 6-членного алкильного кольца.
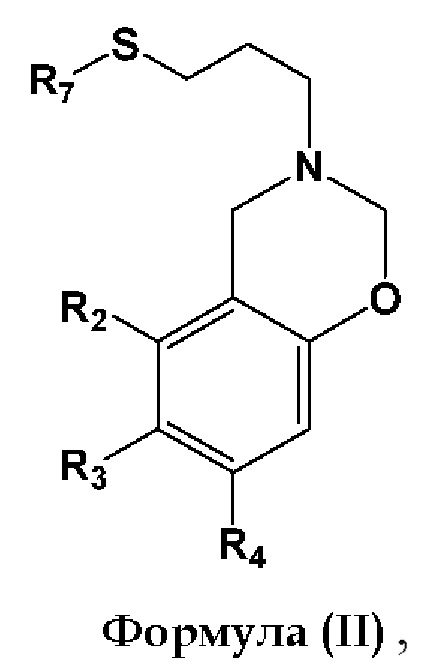
В другом аспекте, бензоксазиновые звенья, содержащиеся в композиции, представляют собой бензоксазиновые звенья, которые являются сшиваемыми друг с другом. Предпочтительно, бензоксазины являются сшиваемыми путем сшивки тиол-ен. В некоторых вариантах реализации сшиваемый бензоксазин представляет собой соединение общей формулы (II):
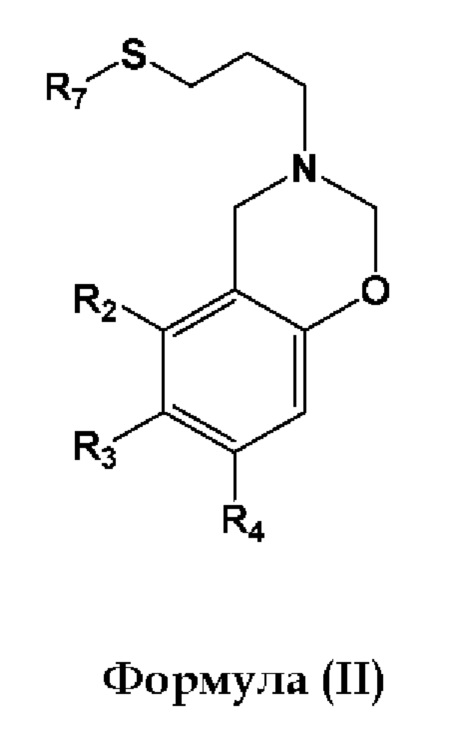
где R2, R3 и R4 каждый независимо представляет собой Н, СН3, C2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкенильными или алкинильными группами, алкарильными группами, гетероалкильными группами, гетероарильными группами, гидроксигруппами, дисульфидами, сульфонатами, эфирными группами, тиоэфирными группами, сложноэфирными группами, карбоксильными группами, аминогруппами, амидными группами, азидами или бензоксазинами, и R2 может быть связан с R3 с образованием циклического заместителя на бензольном кольце, или R3 может быть связан с R4 с образованием циклического заместителя на бензольном кольце, при условии, что R2, R3 и/или R4 содержит по меньшей мере одну ненасыщенную связь, например, олефиновую связь, и R7 представляет собой С2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкарильными группами, гетероалкильными группами, гетероарильными группами, гидроксигруппами, дисульфидами, сульфонатами, простыми эфирными группами, тиоэфирными группами, сложноэфирными группами, группами карбоновых кислот, аминогруппами, амидными группами и азидами, при условии, что R7 содержит по меньшей мере одну тиольную группу для обеспечения (УФ-опосредованного) сшивки тиол-ен.
УФ-опосредованное поперечное сшивание мономеров, содержащих доступные алкеновые и тиольные функциональные группы, посредством реакций тиол-ен (также известных как «клик-химия тиол-ен») хорошо известно специалистам в данной области техники и часто используется в синтезе поперечно-сшитых трехмерных сетей. В настоящем изобретении бензоксазиновые звенья могут быть поперечно сшиты посредством инициированной УФ-излучением клик-реакции тиол-ен перед сополимеризалией. Сополимеризацию сшитых бензоксазиновых звеньев и циклических карбонатных звеньев, в которых происходит расширение полученного сополимера, осуществляют путем подачи тепла при температуре, достаточной для инициирования сополимеризации, которая в случае настоящего изобретения составляет, например, до 140°С.
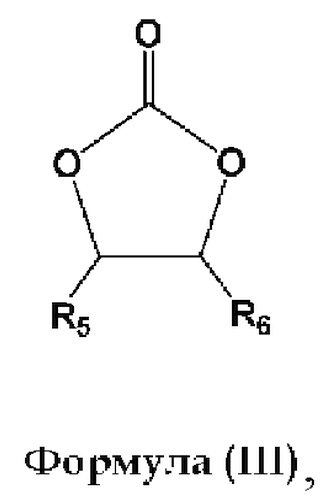
По меньшей мере один циклический карбонат может представлять собой соединение общей формулы (III):
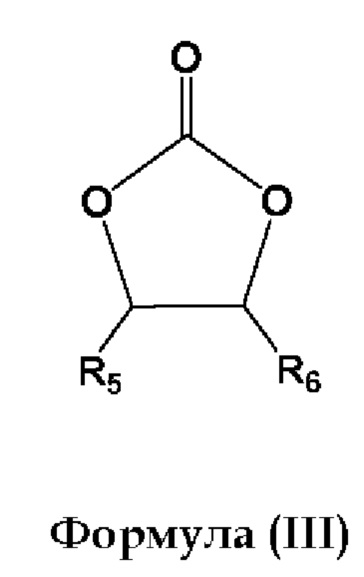
где R5 и R6 каждый независимо представляет собой Н, СН3, С2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкенилом, гетероалкильными группами и гидроксигруппами. Согласно предпочтительным вариантам реализации циклический карбонат представляет собой этиленкарбонат или пропиленкарбонат, предпочтительно этиленкарбонат.
Согласно конкретным вариантам реализации бензоксазин может быть получен из дигидроксибензола или бисфенола. Предпочтительно дигидроксибензол представляет собой гидрохинон, и бисфенол выбран из группы, состоящей из бисфенола А, бисфенола F, бисфенола S, бисфенола М, бисфенола Z и бисфенола АР. Примеры таких бензоксазинов приведены в экспериментальной части в примерах ниже.
Соотношение эквивалентов бензоксазина к эквивалентам циклических карбонатов в композиции предпочтительно составляет от 99:1 до 1:99; более предпочтительно соотношение эквивалентов бензоксазина к эквивалентам циклических карбонатов в композиции составляет от 99:1 до 30:70. В зависимости от соотношения, характеристики (например, твердый/ хрупкий, твердый/ мягкий, каучукоподобный) продукта полимеризации, полученные после полимеризации композиции согласно настоящему изобретению, можно регулировать/настраивать.
Согласно другим вариантам реализации композиция дополнительно содержит по меньшей мере один реакционноспособный разбавитель. Согласно конкретным вариантам реализации реакционноспособный разбавитель присутствует в количестве от 20% до 60% по массе от массы бензоксазина. В конкретных вариантах реализации реакционноспособный разбавитель выбран из группы, состоящей из 3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазина, 3-аллил-5-метил-3,4-дигидро-2Н-бензо[е][1,3]оксазина, 3-аллил-6-октил-3,4-дигидро-2Н-бензо[е][1,3]оксазина и 3-аллил-6-нонил-3,4-дигидро-2Н-бензо[е][1,3]оксазина.
Настоящее изобретение также относится к продукту полимеризации расширяемой полимеризуемой композиции согласно настоящему изобретению, которая описана в настоящем документе.
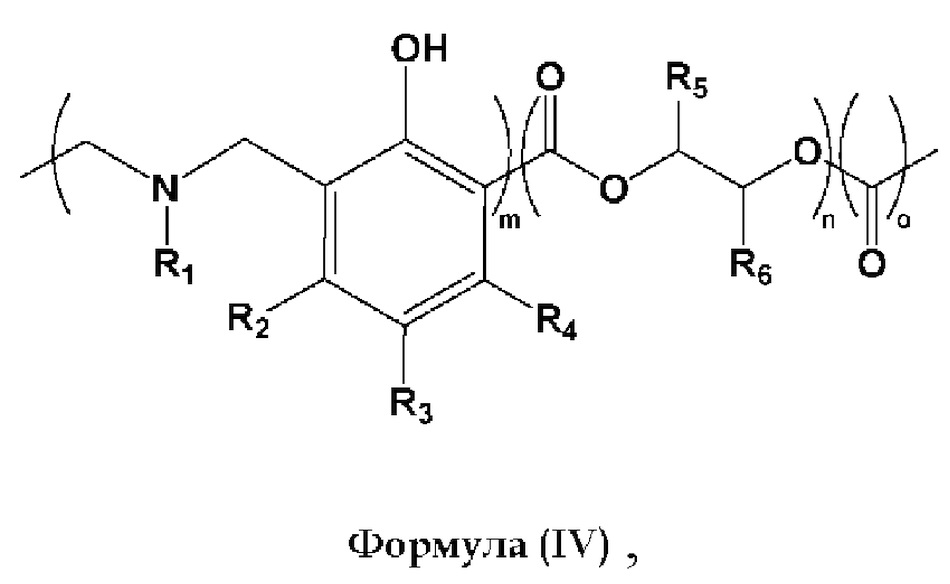
Согласно некоторым вариантам реализации продукт полимеризации согласно изобретению содержит поли(бензоксазин)-сополи(циклический карбонат) общей формулы (IV):
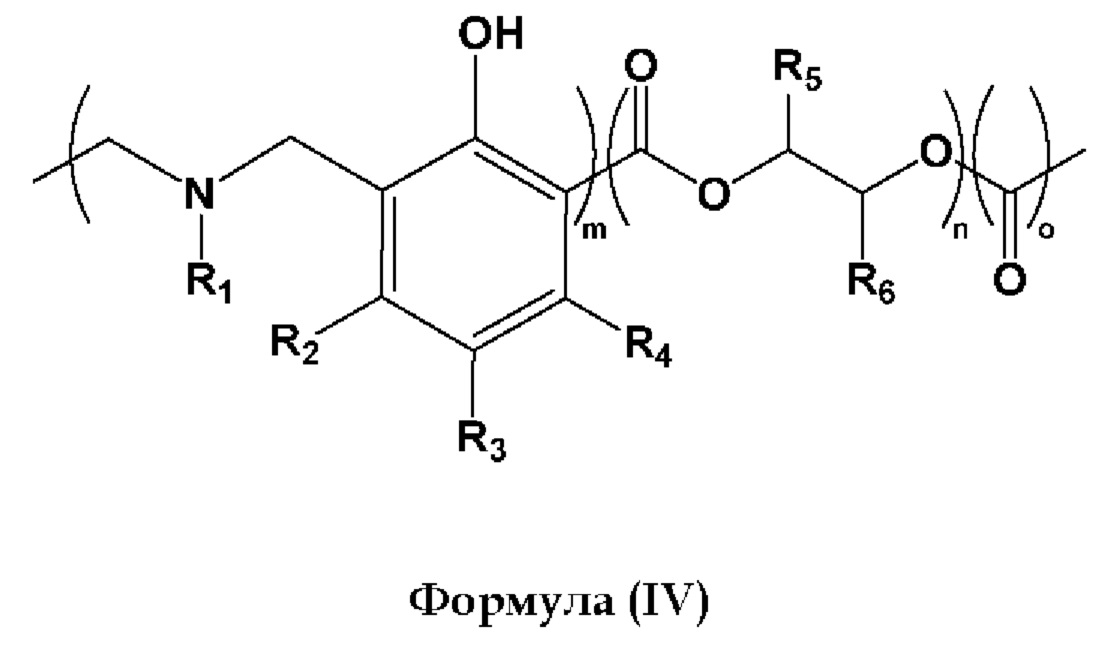
где
R1, R2, R3 и R4 каждый независимо представляет собой Н, СН3, С2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкенильными или алкинильными группами, алкарильными группами, гетероалкильными группами, гетероарильными группами, гидроксигруппами, дисульфидами, сульфонатами, простыми эфирными группами, тиоэфирными группами, сложноэфирными группами, группами карбоновых кислот, аминогруппами, амидными группами, азидами или бензоксазином, и R2 может быть связан с R3 с образованием циклического заместителя на бензольном кольце, или R3 может быть связан с R4 с образованием циклического заместителя на бензольном кольце;
R5 и R6 каждый независимо представляет собой Н, СН3, С2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкенилом, гетероалкильными группами и гидроксигруппами;
m представляет собой целое число от 10 до 10'000
n представляет собой целое число от 10 до 6'700;
о представляет собой целое число от 0 до 1'000.
Во время сополимеризации оба типа мономеров, т.е. мономеры бензоксазина и циклические карбонатные мономеры, подвергаются кольцевой полимеризации, как показано ниже:
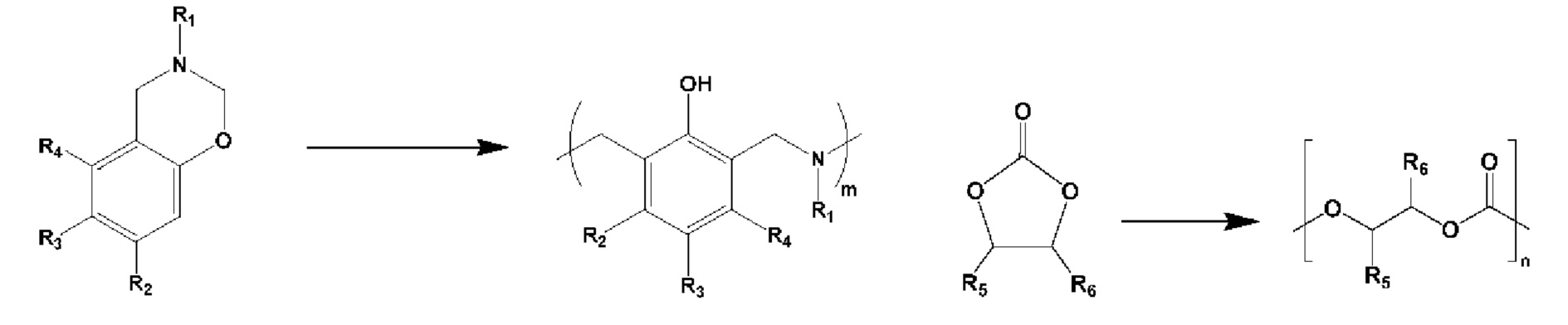
Стадия сополимеризации для получения поли(бензоксазин)-сополи(циклический карбонат) вышеупомянутой общей формулы (IV) изображена ниже:
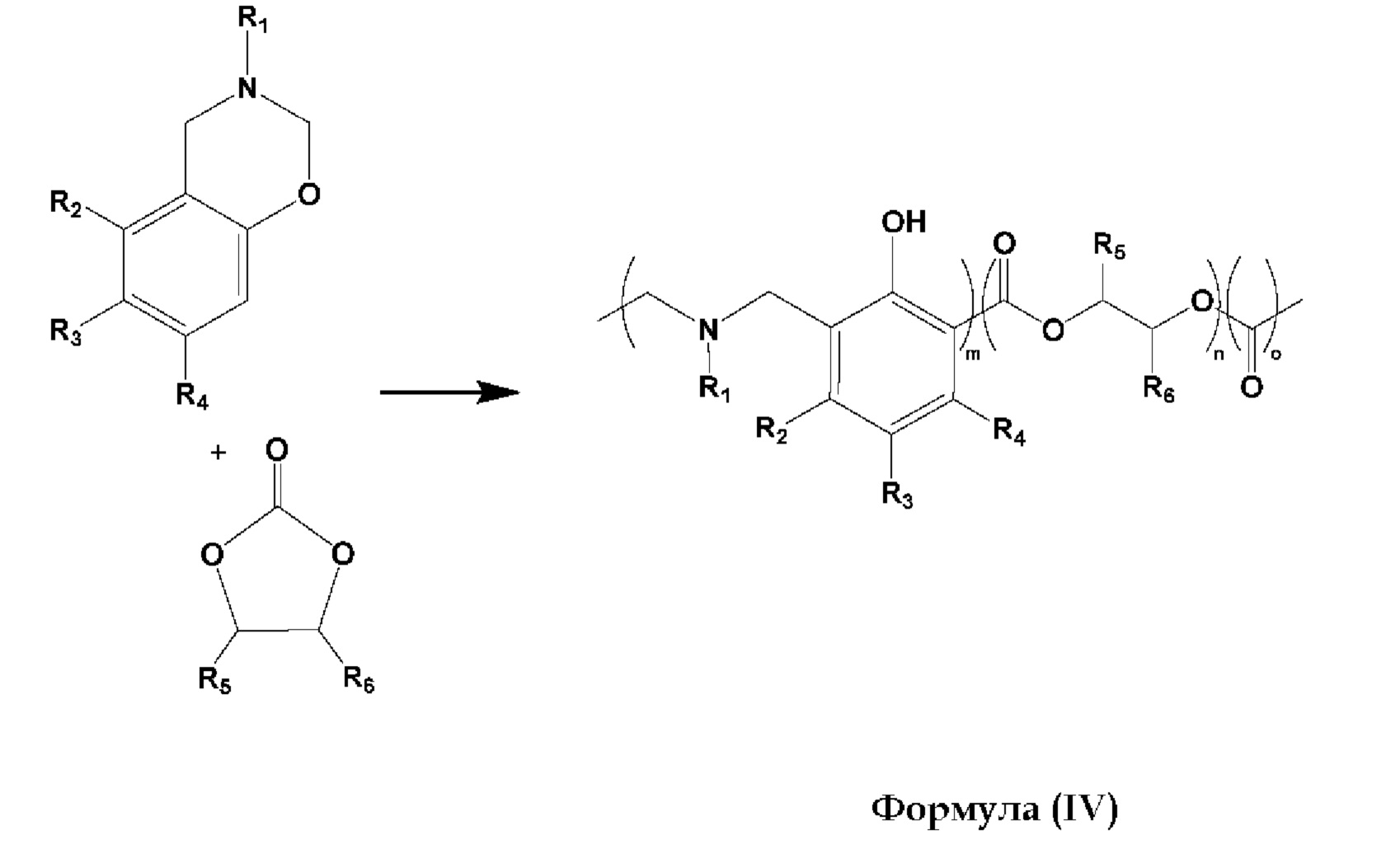
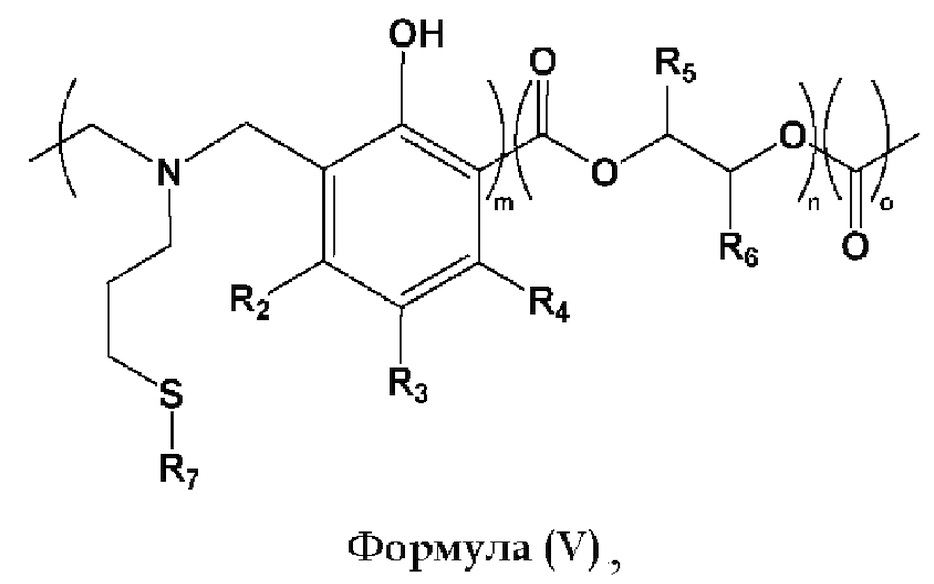
Согласно некоторым вариантам реализации продукт полимеризации согласно настоящему изобретению содержит поли(бензоксазин)-сополи(циклический карбонат) общей формулы (V):
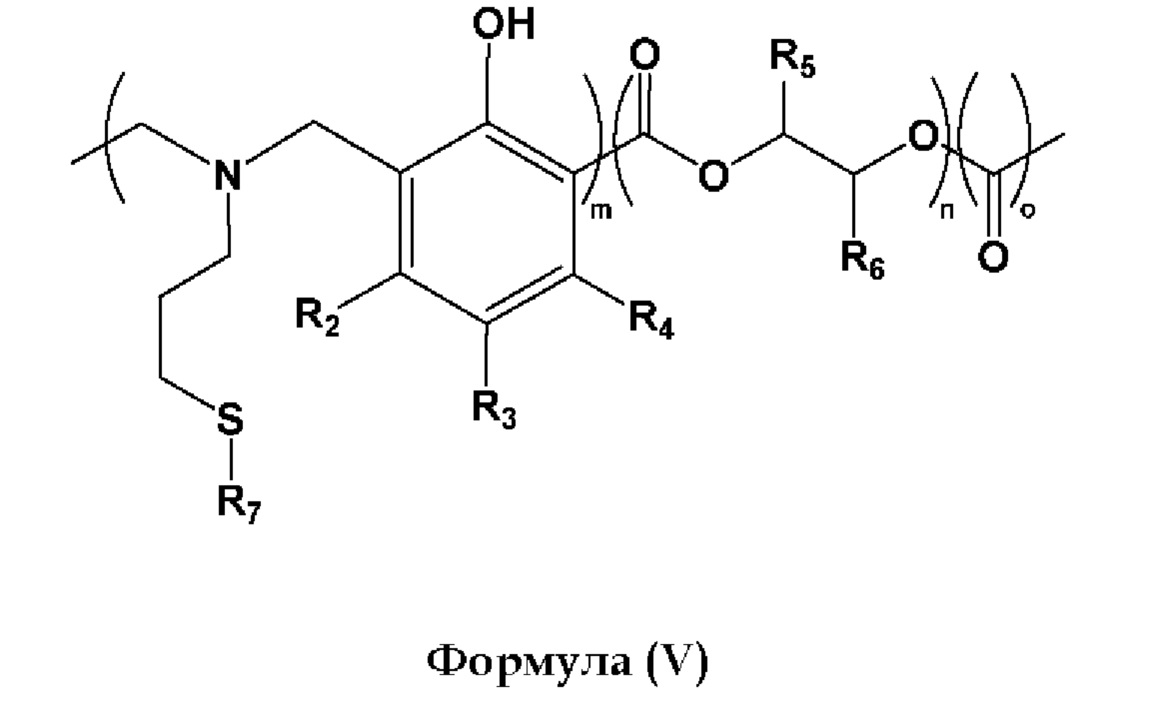
где
R2, R3 и R4 каждый независимо представляет собой Н, СН3, C2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкенильными или алкинильными группами, алкарильными группами, гетероалкильными группами, гетероарильными группами, гидроксигруппами, дисульфидами, сульфонатами, простыми эфирными группами, тиоэфирными группами, сложноэфирными группами, карбоксильными группами, аминогруппами, амидными группами, азидами или бензоксазином, и R2 может быть связан с R3 с образованием циклического заместителя на бензольном кольце, или R3 может быть связан с R4 с образованием циклического заместителя на бензольном кольце, при условии, что R2, R3 и/или R4 содержит по меньшей мере одну ненасыщенную связь;
R7 представляет собой С2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкарильными группами, гетероалкильными группами, гетероарильными группами, гидроксигруппами, дисульфидами, сульфонатами, простыми эфирными группами, тиоэфирными группами, сложноэфирными группами, группами карбоновых кислот, аминогруппами, амидными группами и азидами, при условии, что R7 содержит по меньшей мере одну тиольную группу, для обеспечения возможности (УФ-опосредованной) сшивки тиол-ен.
R5 и R6 каждый независимо представляет собой Н, СН3, С2-С15 прямой, разветвленный или циклический алкил, необязательно замещенный галогенами, алкенилом, гетероалкильными группами и гидроксигруппами;
m представляет собой целое число от 10 до 10'000;
n представляет собой целое число от 10 до 6'700;
о представляет собой целое число от 0 до 1000.
Двухстадийная полимеризация для получения поли(бензоксазин)-сополи(циклический карбонат) вышеупомянутой общей формулы (V) изображена ниже:
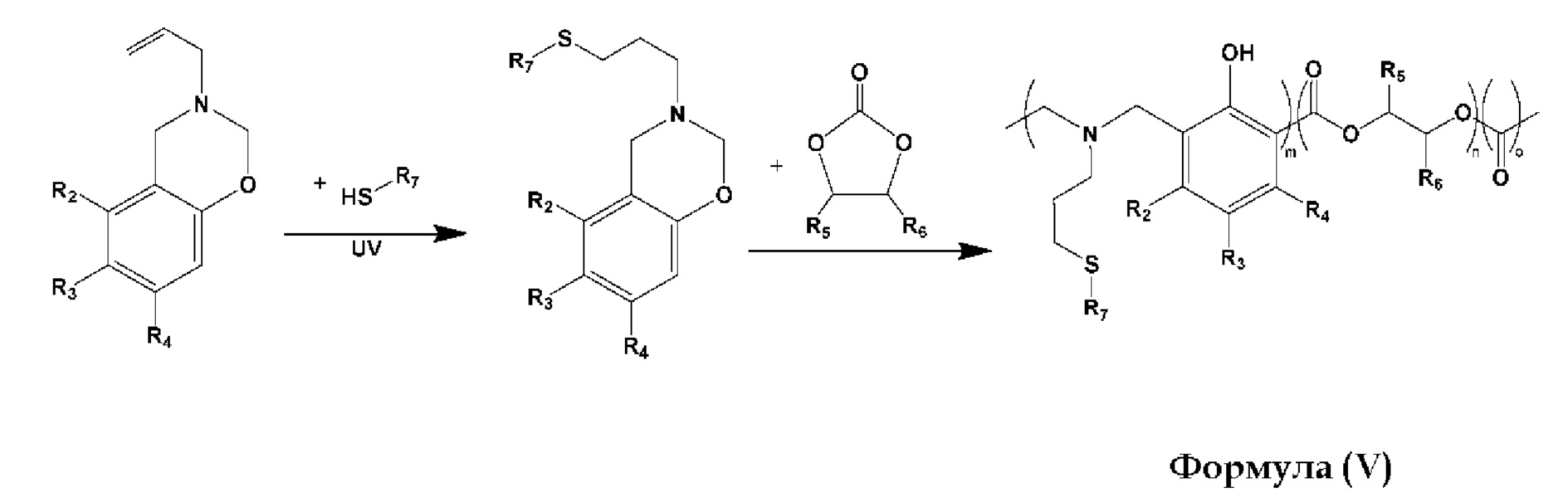
Согласно этим вариантам реализации перед сополимеризацией сшитых бензоксазиновых звеньев и циклических карбонатов сначала производят сшивку бензоксазиновых звеньев с помощью инициируемой УФ-излучением клик-реакции тиол-ен. Сополимеризацию, в ходе которой происходит расширение полученного сополимера, осуществляют путем подачи тепла при температуре, достаточной для инициирования сополимеризации, которая в случае настоящего изобретения, например, составляет до 140°С.
Согласно дополнительному аспекту настоящее изобретение также относится к герметику, адгезиву, покрытию, связующему агенту или зубной пломбе, содержащей расширяемую полимеризуемую композицию, как описано в настоящем документе. В еще одном аспекте настоящее изобретение также относится к применению расширяемой полимеризуемой композиции, описанной в настоящем документе, в качестве/в герметиках, клеях, покрытиях, связующих агентах или зубных пломбах. Например, расширяемая полимеризуемая композиция может быть применена в строительной промышленности, например, в качестве литейных композиций и герметиков; в литейной промышленности, например, в качестве связующих веществ и формовочных смесей; в промышленности по изготовлению покрытий, например, для покрытия объектов; в деревообрабатывающей промышленности, например, для приготовления изделий из прессованной древесины; в автомобильной промышленности; в электронной промышленности, например, в качестве изоляционных материалов; в клеевой промышленности; и в области медицинских/стоматологических изделий, например, стоматологических пломб.
Согласно дополнительному аспекту настоящее изобретение относится к предварительно отвержденной, расширяемой полимеризуемой композиции, полученной путем сшивания сшиваемых бензоксазинов, содержащейся в расширяемой полимеризуемой композиции, как описано в настоящем документе. В дополнительном аспекте настоящее изобретение также относится к применению этой предварительно отвержденной, расширяемой полимеризуемой композиции в качестве расширяемого наполнительного элемента для заполнения пространств в устройствах, где отвержденная, расширяемая композиция имеет заранее определенную форму, в частности, но не ограничиваясь ими, стержни, палочки, цилиндры или строительные блоки, где отвержденная, расширяемая композиция демонстрирует объемное расширение во время сополимеризации при тепловом воздействии. Согласно конкретным вариантам реализации объемное расширение предварительно сформированной и отвержденной композиции может приводить к геометрическому выравниванию с подлежащим заполнению пространством. Указанные предварительно определенные формы отвержденной, расширяемой полимеризуемой композиции могут иметь размеры в милли-, санти- или метровом диапазоне. В частности, указанная предварительно отвержденная, расширяемая полимеризуемая композиция может быть использована в качестве опорного и фиксирующего элемента для обмоток электрических машин или может служить в качестве изолирующего барьера обмотки для электрического оборудования. То есть, за счет объемного расширения происходит точное геометрическое выравнивание полученного расширенного сополимера с окружающим материалом и компенсирует усадочные и сборочные допуски этих материалов, что обеспечивает превосходную стабильность и, кроме того, изолирующие свойства и посадочную опору обмоток или слоистых электромагнитных материалов (см. также главу 4 нижеприведенных примеров заявок).
В еще одном аспекте настоящее изобретение также относится к способу изготовления продукта полимеризации, включающему стадию нагрева расширяемой полимеризуемой композиции, описанной в настоящем документе, до температуры, достаточной для инициирования сополимеризации. Температура, при которой инициируют сополимеризацию, предпочтительно находится в диапазоне 70 - 200°С, более предпочтительно в диапазоне 70 - 150°С и наиболее предпочтительно в диапазоне 70 - 120°С.
В конкретных вариантах реализации способа получения продукта полимеризации способ включает стадии:
a.) обеспечение полимеризуемой композиции по п.п. 3 или 4, содержащей сшиваемые бензоксазины и циклические карбонаты,
b.) предварительное отверждение полимеризуемой композиции путем сшивки сшиваемых бензоксазинов, и
c.) нагревание предварительно отвержденной полимеризуемой композиции до температуры, достаточной для инициирования сополимеризации сшитых бензоксазинов и циклических карбонатов.
Таким образом, как описано выше, стадия b.) предварительного отверждения расширяемой полимеризуемой композиции может быть осуществлена путем УФ-опосредованного сшивания сшиваемых бензоксазиновых мономеров, содержащих доступные алкеновые и тиольные функциональные группы, посредством тиоло-еновых реакций перед стадией сополимеризации с), на которой происходит расширение поли(бензоксазин)-сополи(циклический карбонат). На стадии сополимеризации с.) применяется нагревание при температуре, достаточной для инициирования сополимеризации. Температура, при которой инициируют сополимеризацию, предпочтительно находится в диапазоне 70-200°С, более предпочтительно в диапазоне 70-150°С и наиболее предпочтительно в диапазоне 70-120°С. Этот двухстадийный процесс, включающий стадию предварительного отверждения b.), за которой следует стадия сополимеризации/ расширения с), является особенно подходящим для применения в строительной и литейной промышленности, поскольку он обеспечивает легкую и удобную обработку/расположение предварительно отвержденной, соответственно предварительно сформированной, но еще не расширенной композиции. Например, предварительно отвержденная композиция, которая уже имеет желаемую форму, может быть помещена в отверстие, подлежащее герметизации; на следующем этапе применение нагревания инициирует сополимеризацию и расширение полученного сшитого полимера поли(бензоксазин)-сополи(циклический карбонат).
Настоящее изобретение дополнительно продемонстрировано и проиллюстрировано следующими примерами, но не ограничивается ими.
На фиг.1 главы 3.1 ниже показан тиол-еновый предварительно отвержденный, но не сополимеризованный образец (справа) и тиол-еновый предварительно отвержденный и сополимеризованный образец (слева), причем оба образца приготовлены с помощью расширяемой полимеризуемой композиции согласно настоящему изобретению.
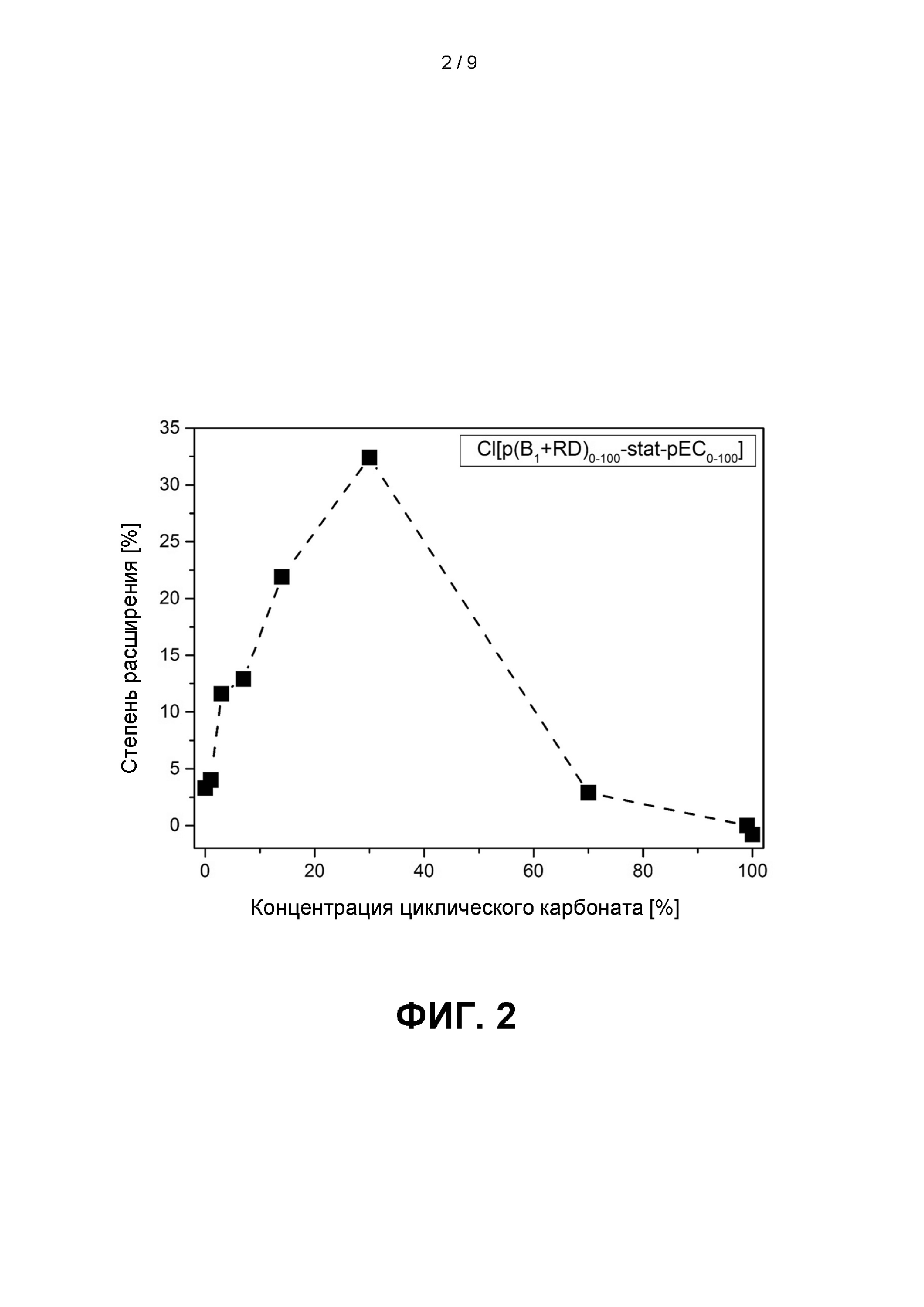
Фиг. 2 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B1+RD)0-100-stat -pEC0-100]; см. главу 3.В.1 ниже.
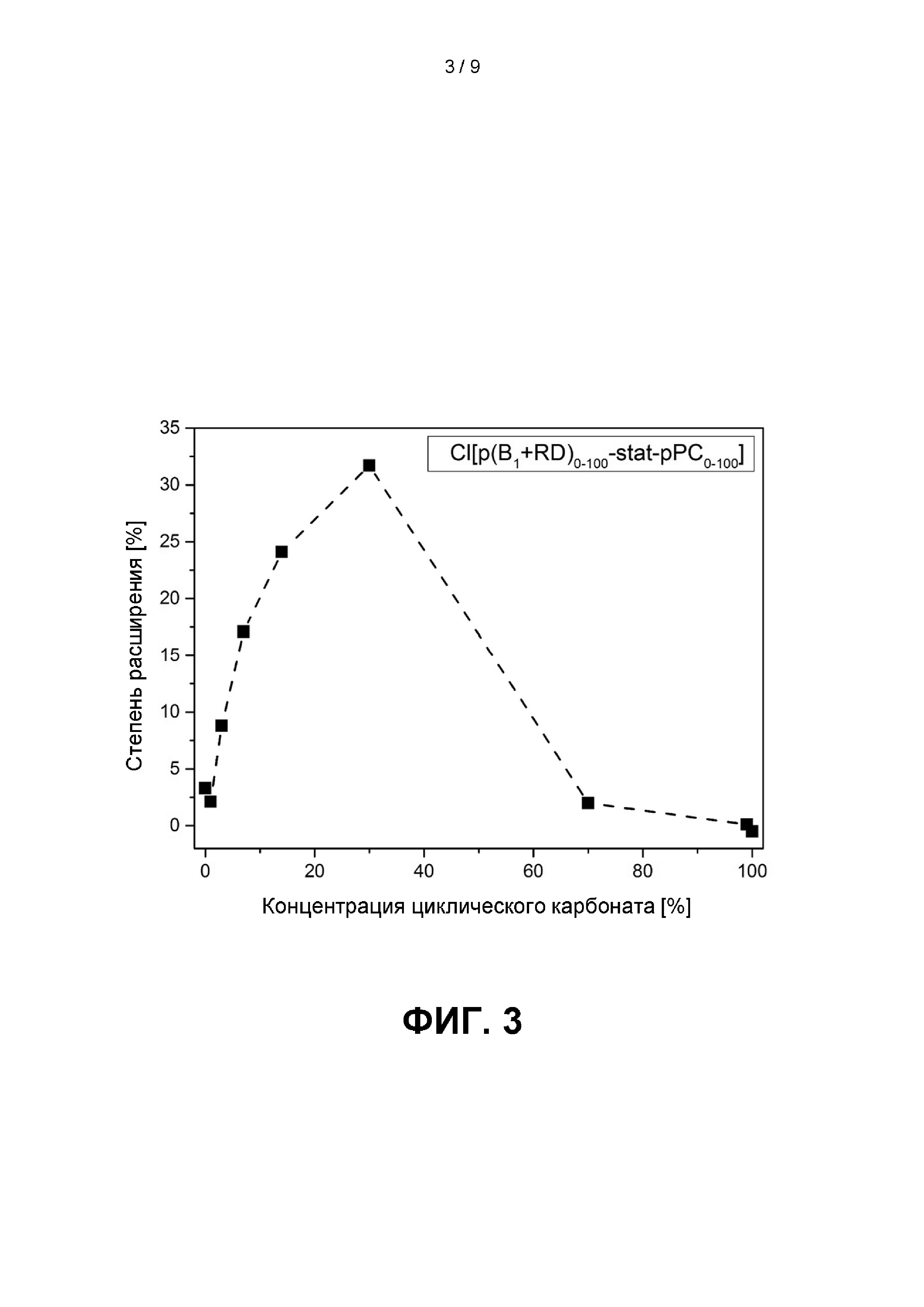
Фиг. 3 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B1+RD)0-100-stat -pPC0-100]; см. главу 3.В.2. ниже.
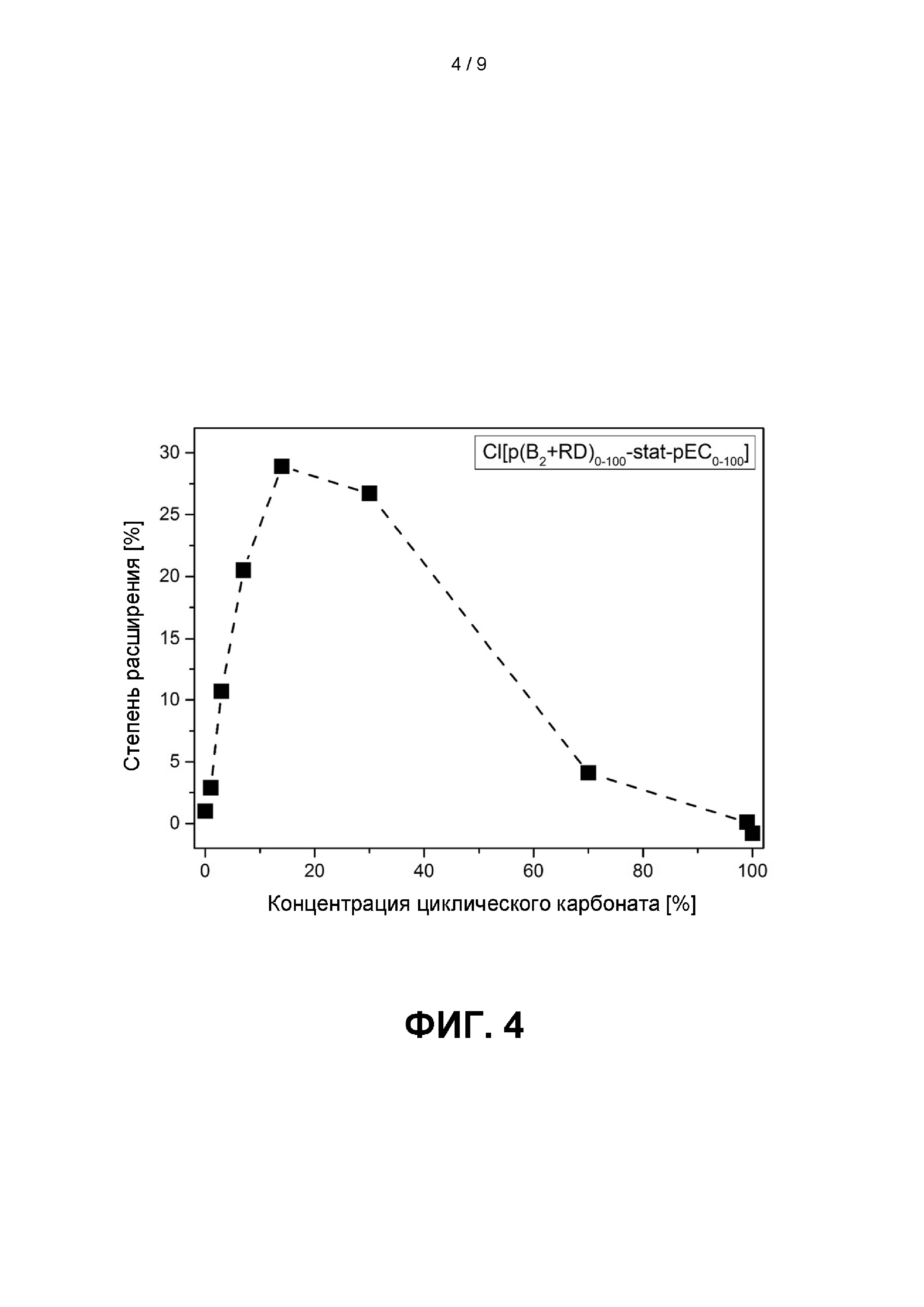
Фиг. 4 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B2+RD)0-100-stat -рЕС0-100]; см. главу 3.В.3. ниже.
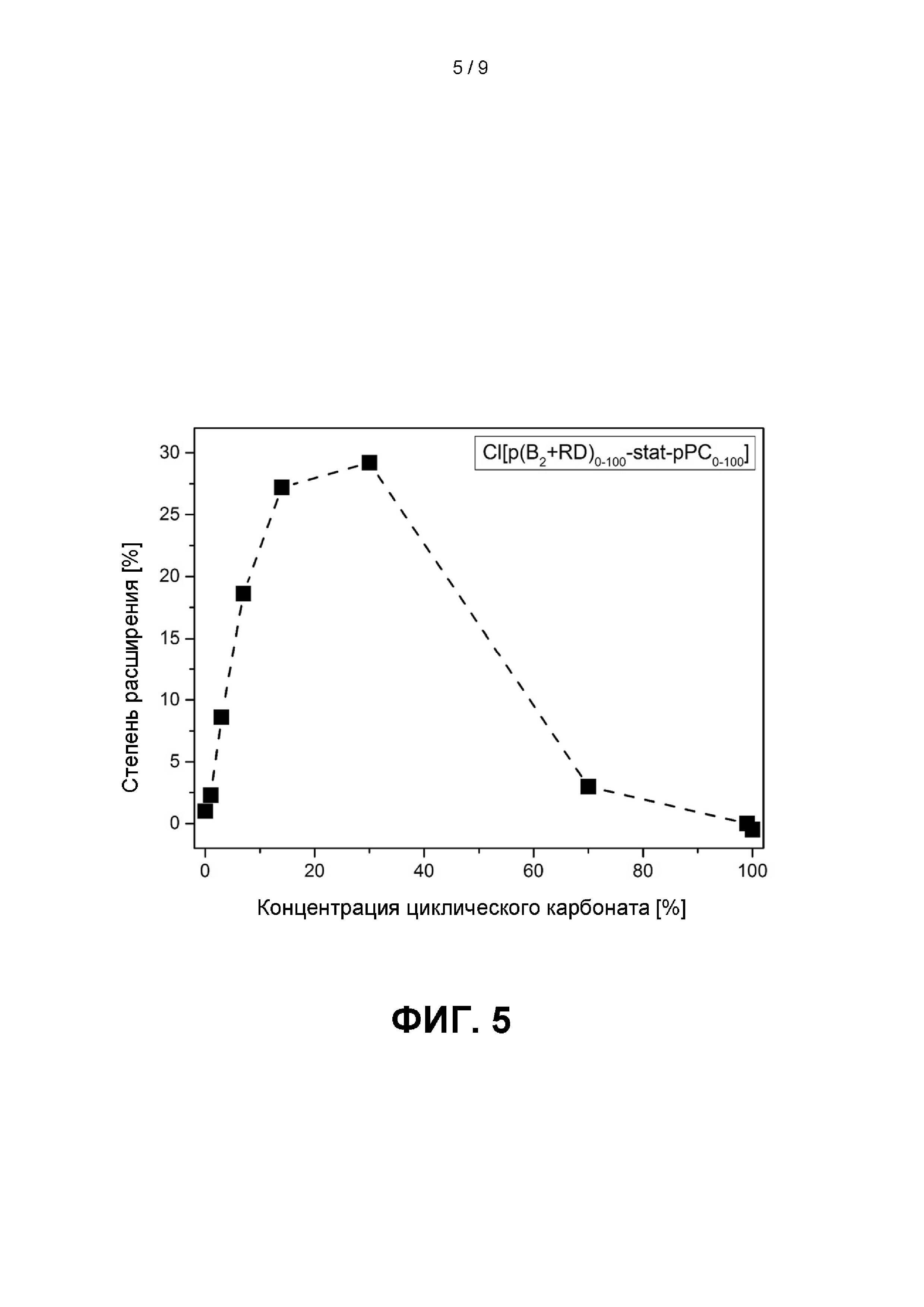
Фиг. 5 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B2+RD)0-100-stat -pPC0-100]; см. главу 3.В.4. ниже.
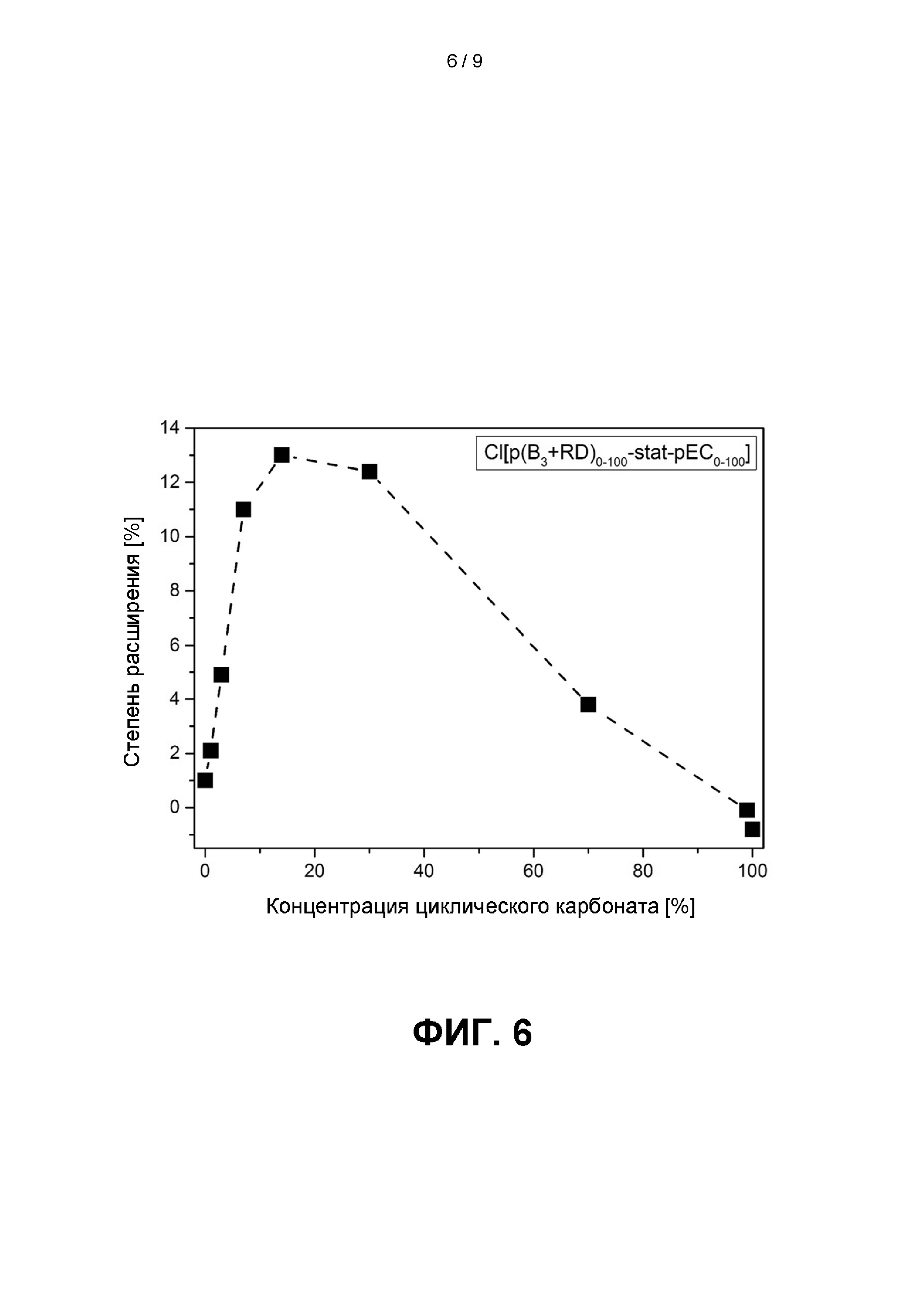
Фиг. 6 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B3+RD)0-100-stat -рЕС0-100]; см. главу 3.В.3. ниже.
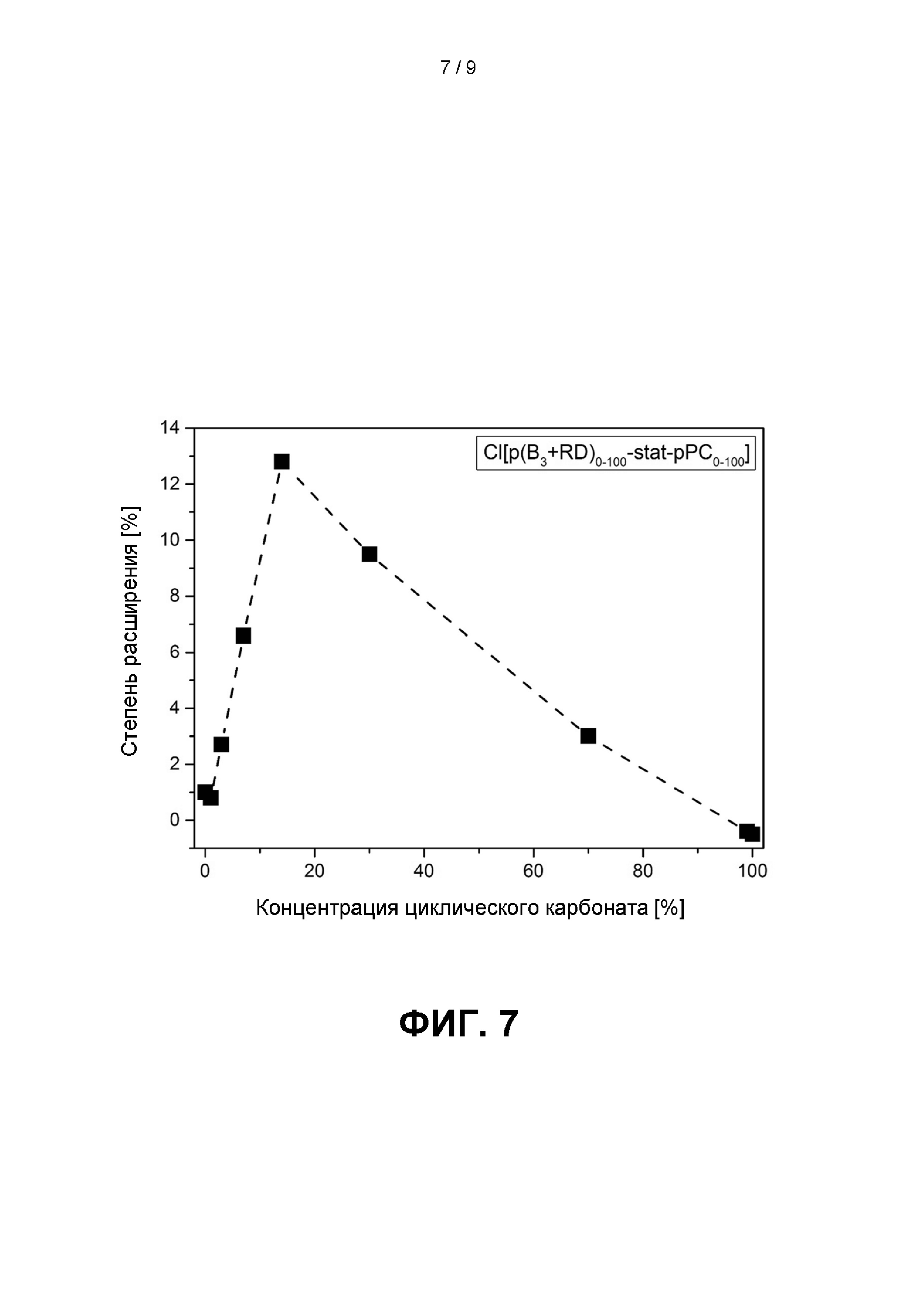
Фиг. 7 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B3+RD)0-100-stat -рРС0-100]; см. главу 3.В.6. ниже.
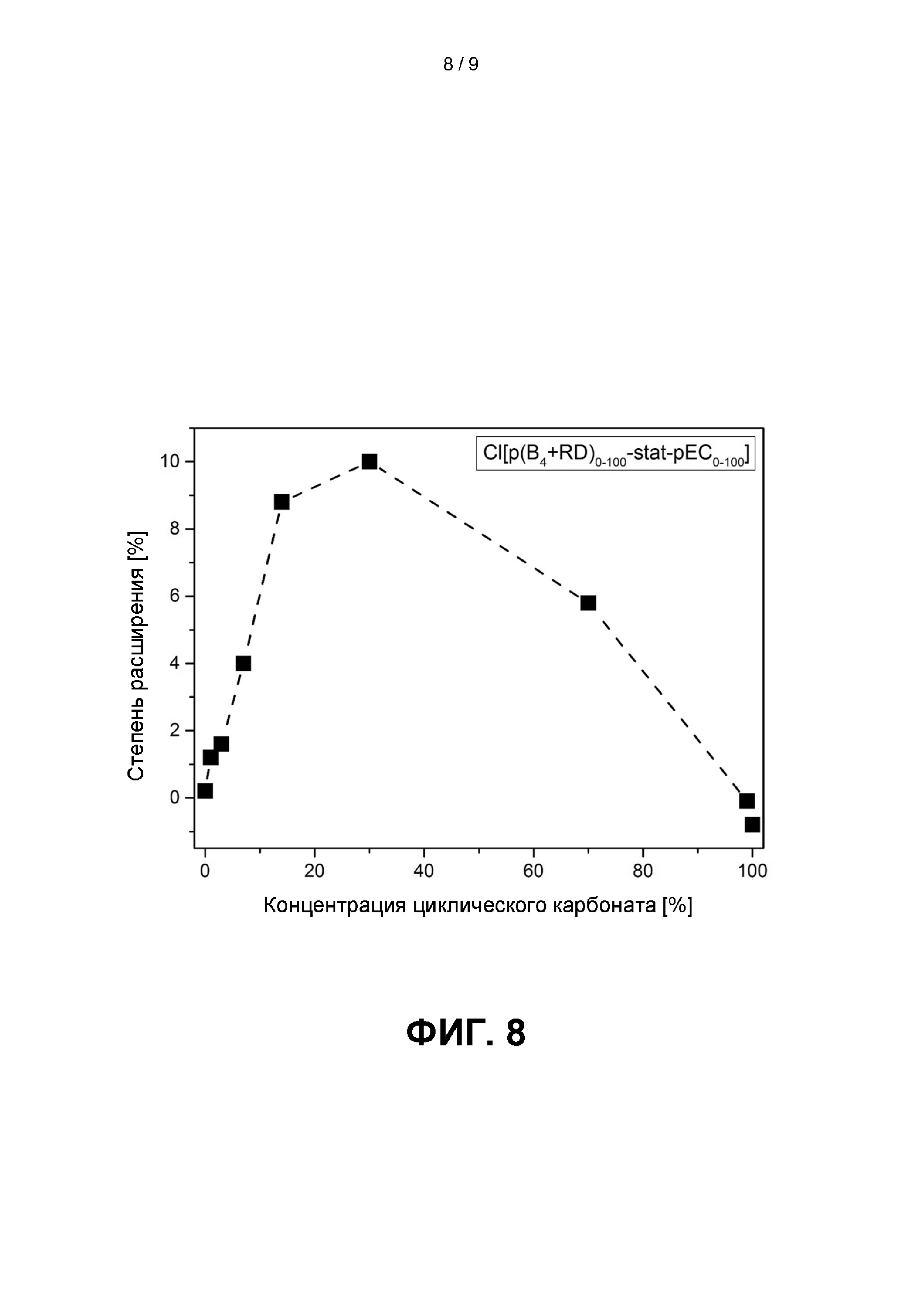
Фиг. 8 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B4+RD)0-100-stat -рЕС0-100]; см. главу 3.В.7. ниже.
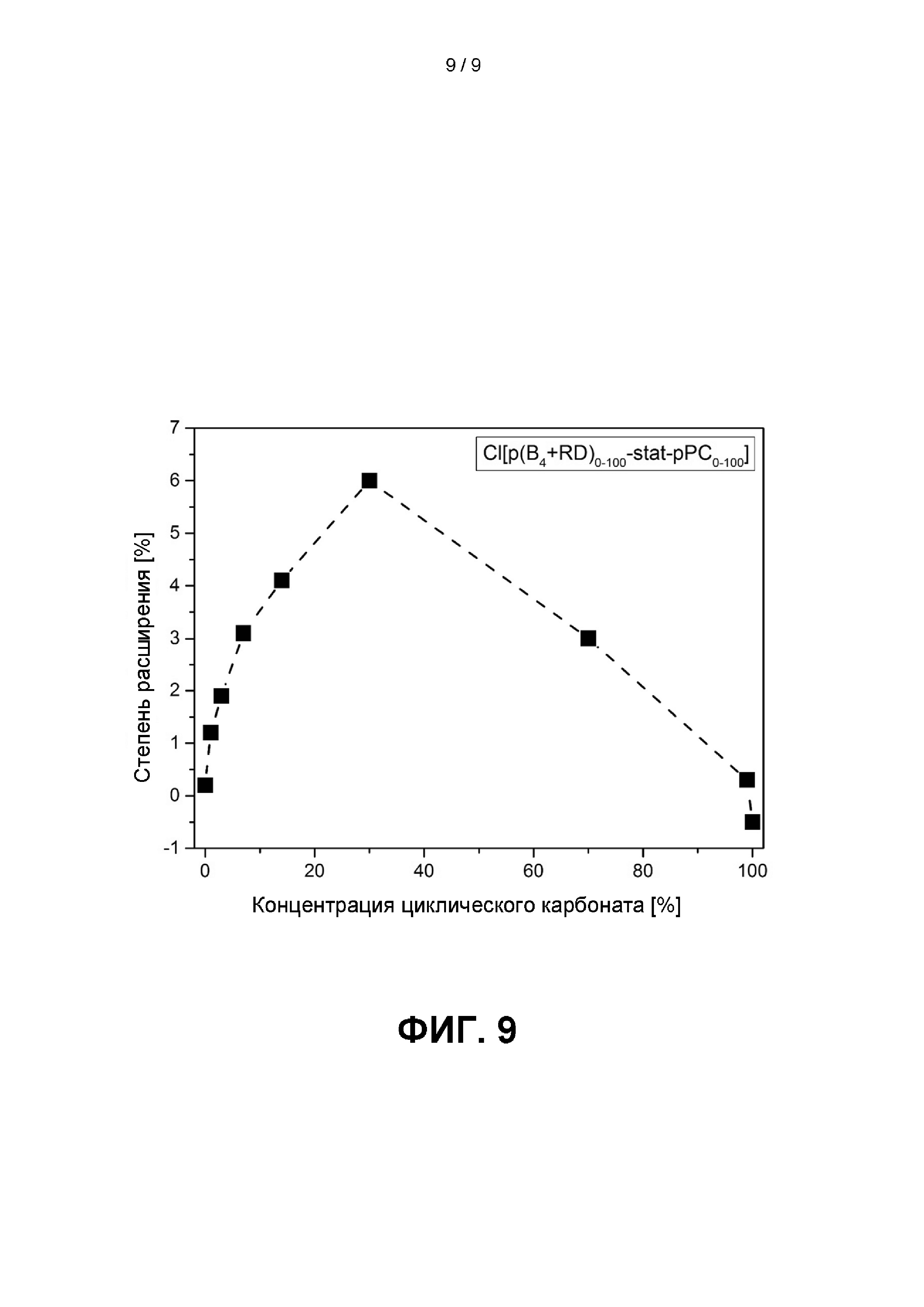
Фиг.9 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B4+RD)0-100-stat -pPC1-100]; см. главу 3.В.8. ниже.
ЭКСПЕРИМЕНТАЛЬНЫЕ ДАННЫЕ и ПРИМЕРЫ
1 А. Материалы и методы
1.А.1 Материалы
Бисфенол А (97%), гидрохинон (97%), параформальдегид (95%), фенол (>99%), м-крезол (>98%), 4-октилфенол (99%), 4-нонилфенол (>90%), сульфат натрия (>99%), этиленкарбонат (98%), пропиленкарбонат (99,7%) и диэтиловый эфир (>98%) были приобретены у компании Sigma-Aldrich Chemie GmbH (Вена, Австрия). Бисфенол F (>99%), бисфенол S (>98%), пентаэритритол тетракис(3-меркаптопропионат) (>90%) были приобретены у TCI (Tokyo Chemical Industry Co., Ltd.; Австрия, Вена). Аллиламин (>98%) был приобретен у Thermo Fisher GmbH (Карлсруэ, Германия). Этил-2,4,6-триметилбензоилфенилфосфинат (>95%) был приобретен у ABCR GmbH (Карлсруэ, Германия). Все вещества использовали без дополнительной очистки.
1.А.2 Методы
Измерение степени расширения - Измерение плотности
Измерения плотности проводили с использованием набора для измерения плотности Mettler Toledo. Плотность образца рассчитывается с помощью гидростатического баланса в воде, определяющего подъем образцов в и из растворителя.
Степени расширения определяли количественно путем измерения плотности мономеров/прекурсоров, с одной стороны, и вспененных полимеров - с другой. Степень расширения рассчитывали по следующей формуле:
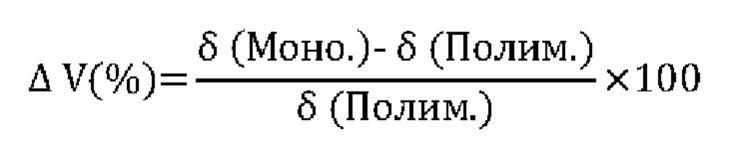
Измерения FTIR,1Н-ЯМР и13С-ЯМР
Спектры FTIR-ATR регистрировали на приборе Bruker Alpha Р, оснащенном детектором DTGS (спектральный диапазон от 4000 до 800 см-1). Блок ATR оснащен алмазным кристаллом. Спектры FTIR были измерены в режиме пропускания и получены из порошкообразных образцов или жидких пленок.
ЯМР-спектры регистрировали на спектрометре Bruker Ultrashield 300 WB 300 МГц. Пик растворителя CDCl3 служил эталоном спектров (7,26 ppm для1Н и 77,0 ppm для13С). Остаточный пик растворителя ДМСО использовали для сравнения спектров с 2,50 (1H) и 39,5 (13С) ppm. Формы пиков индицируются следующим образом: s (синглет), d (дублет), t (триплет), m (мультиплет).
2.А. Синтез мономеров
2.А.1 6,6'-(пропан-2,2-диил)бис(3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазин)
(сокращение: B1):
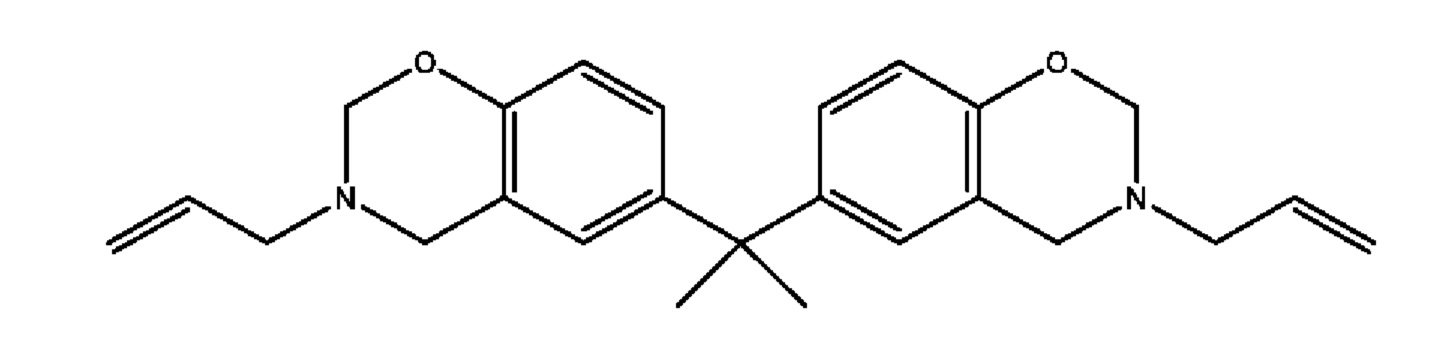
К смеси бисфенола А (0,15 моль, 34,3 г) и аллиламина (0,30 моль, 17,1 г) небольшими порциями добавляют параформальдегид (0,62 моль, 18,6 г) в течение 30 мин, охлаждая на ледяной бане для поддержания температуры ниже 10°С. Затем добавляют пара-толуолсульфоновую кислоту (2,90 ммоль, 0,50 г), поднимают температуру до 90°С и смесь перемешивают в течение 3 ч. Полученную реакционную смесь растворяли в 500 мл диэтилового эфира. Раствор в эфире промывают водой (3 порции по 500 мл) для удаления любого непрореагировавшего формальдегида, бисфенола А или аллиламина и сушат над сульфатом натрия. Растворитель упаривают при пониженном давлении и продукт сушат в вакуумной печи.
1H-ЯМР (300 МГц, CDCl3): δ (ppm) = 6,86 (2Н, m), 6,72 (2Н, m), 6,62 (2Н, m), 5,80 (2Н, m), 5,12 (4Н, m), 4,74 (4Н, s), 3,85 (4Н, s), 3,31 (2Н, d), 1,51 (6Н, s).
13С-ЯМР (75 МГц, CDCl3): δ (ppm) = 151,9, 143,8, 135,1, 126,3, 122,5, 119,2, 118,3, 115,8, 81,9, 54,5, 50,3, 41,7, 31,1.
FTIR (ATR): v (см-1) = 3074, 2964, 2894, 2825, 1611, 1495, 1330, 1226, 1187, 1115, 987, 928, 814.
2.A.2 Бис(3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазин-6-ил)метан
(сокращение: В2);
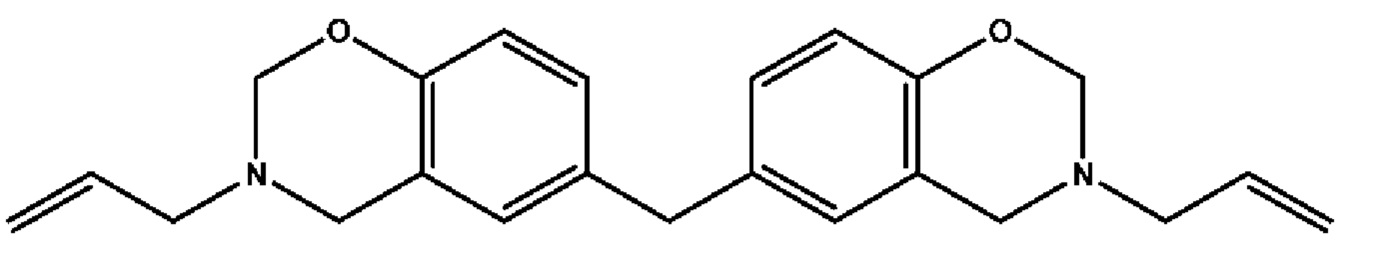
К смеси бисфенола F (0,15 моль, 29,7 г) и аллиламина (0,30 моль, 17,1 г) небольшими порциями добавляют параформальдегид (0,62 моль, 18,6 г) в течение 30 мин, охлаждая на ледяной бане для поддержания температуры ниже 10°С. Затем добавляют пара-толуолсульфоновую кислоту (2,90 ммоль, 0,50 г), поднимают температуру до 90°С и смесь перемешивают в течение 3 ч. Полученную реакционную смесь затем растворяют в 500 мл диэтилового эфира. Раствор в эфире промывают водой (3 порции по 500 мл) для удаления любого непрореагировавшего пара-формальдегида, бисфенола F или аллиламина и сушат над сульфатом натрия. Растворитель упаривают при пониженном давлении и продукт сушат в вакуумной печи.
1Н-ЯМР (300 МГц, CDCl3): δ (ppm) = 6,83 (2Н, m), 6,67 (2Н, m), 6,60 (2Н, m), 5,79 (2Н, m), 5,10 (4Н, m), 4,73 (4Н, s), 3,84 (4Н, s), 3,66 (2Н, s), 3,30 (2Н, d).
13С-ЯМР (75 МГц, CDCl3): δ (ppm) = 152,5, 135,3, 133,7, 128,2, 127,7, 120,1, 118,4, 116,5, 82,5, 55,6, 49,8,40,5.
FTIR (ATR): v (см-1) = 3074, 2972, 2917, 2863, 1740, 1619, 1493, 1436, 1368, 1211, 1109, 987, 928, 811.
2.А.3 6,6'-сульфонилбис(3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазин)
(сокращение: В3);
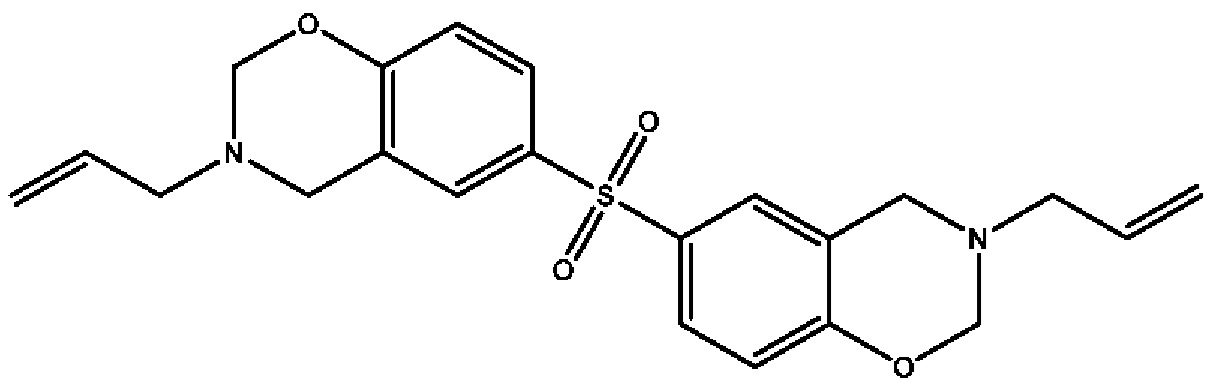
К смеси параформальдегида (0,62 моль, 18,6 г) и аллиламина (0,30 моль, 17,1 г) небольшими порциями добавляют бисфенол S (0,15 моль, 39,3 г) в течение 30 мин при перемешивании при 60°С. Затем добавляют пара-толуолсульфоновую кислоту (2,90 ммоль, 0,50 г), повышают температуру до 90°С и смесь перемешивают в течение 3 ч. Полученную реакционную смесь затем растворяют в 500 мл хлороформа. Раствор промывают водой (3 порции по 500 мл) для удаления любого непрореагировавшего пара-формальдегида, бисфенола S или аллиламина и сушат над сульфатом натрия. Растворитель упаривают при пониженном давлении и продукт сушат в вакуумной печи.
1Н-ЯМР (300 МГц, CDCl3): δ (ppm) = 7,83 (2Н, m), 7,68 (2Н, m), 5,90 (2Н, m), 5,21 (4Н, m), 4,81 (4Н, s), 4,07 (4Н, s), 3,32 (4Н, d).
13С-ЯМР (75 МГц, ДМСО):δ6 (ppm) = 163,4, 135,4, 134,9, 130,4, 128,2, 122,2, 118,5, 117,2, 55,1, 49,8.
FTIR (ATR): v (см-1) = 3072, 2958, 2007, 2850, 1683, 1577, 1484, 1440, 1287, 1442, 1081, 991, 916, 822.
2.А.4 2,9-диаллил-1,2,3,8,9,10-гексагидробензо[2,1-е:3,4-е']бис([1,3]оксазин)
(сокращение: В4);
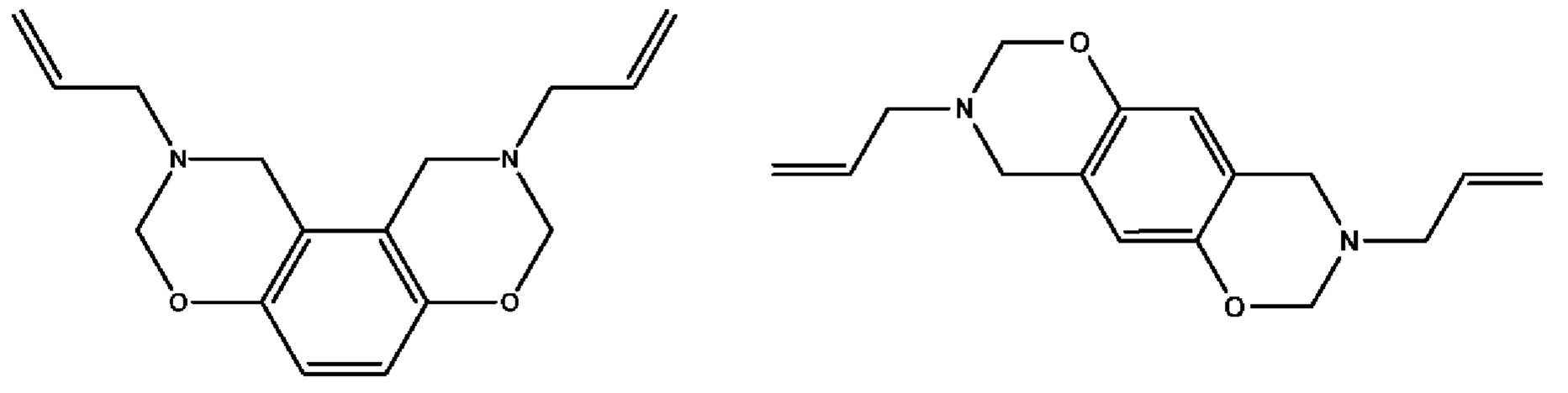
К смеси гидрохинона (0,15 моль, 16,5 г) и аллиламина (0,30 моль, 17,1 г) небольшими порциями добавляют параформальдегид (0,62 моль, 18,6 г) в течение 30 мин, охлаждая на ледяной бане для поддержания температуры ниже 10°С. Затем добавляют пара-толуолсульфоновую кислоту (2,90 ммоль, 0,50 г), поднимают температуру до 90°С и смесь перемешивают в течение 3 ч. Полученную коричневую реакционную смесь растворяли в 500 мл диэтилового эфира. Раствор в эфире промывают водой (3 порции по 500 мл) для удаления любого непрореагировавшего пара-формальдегида, гидрохинона или аллиламина и сушат над сульфатом натрия. Растворитель упаривают при пониженном давлении и продукт сушат в вакуумной печи.
1Н-ЯМР (300 МГц, CDCl3): δ (ppm) = 6,61 (2Н, m), 6,43 (2Н, m), 6,92 (2Н, d), 5,87 (2Н, m), 5,18 (4Н, m), 4,92 (4Н, s), 4,75 (4Н, s), 3,78 (4Н, s), 3,68 (4Н, s), 3,36 (4Н, d), 3,14 (4Н, d).
13С-ЯМР (75 МГц, ДМСО): δ (ppm) = 150,3, 147,7, 135,0, 118,4, 117,9, 117,5, 117,0, 116,4, 115,6, 115,0, 114,4, 113,0, 81,6, 67,1, 55,8, 54,5, 49,7, 46,6.
FTIR (ATR): v (см-1) = 3076, 2970, 2850, 1740,1475,1366, 1230,1117, 985, 916, 805.
2.А.5 3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазин (реакционноспособный разбавитель)
(сокращение: НД):
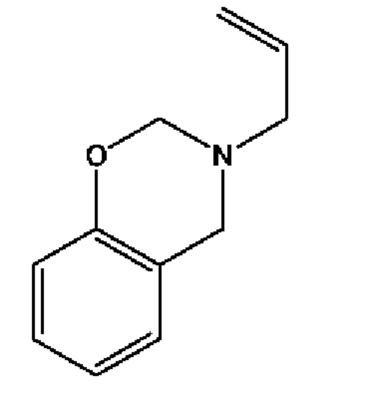
К смеси фенола (0,30 моль, 28,2 г) и аллиламина (0,30 моль, 17,1 г) небольшими порциями добавляют параформальдегид (0,62 моль, 18,6 г) в течение 30 мин, охлаждая на ледяной бане для поддержания температуры ниже 10°С. Затем добавляют пара-толуолсульфоновую кислоту (2,90 ммоль, 0,50 г), поднимают температуру до 90°С и смесь перемешивают в течение 3 ч. Полученную коричневую реакционную смесь затем растворяют в 500 мл диэтилового эфира. Раствор в эфире промывают водой (3 порции по 500 мл) для удаления любого непрореагировавшего пара-формальдегида, фенола или аллиламина и сушат над сульфатом натрия. Растворитель упаривают при пониженном давлении и продукт сушат в вакуумной печи.
1Н-ЯМР (300 МГц, CDCl3): δ (ppm) = 7,02 (1Н, m), 6,87 (1Н, m), 6,78 (1Н, m), 6,69 (1Н, m), 5,81 (1Н, m), 5,14 (2Н, m), 4,79 (2Н, s), 3,91 (2Н, s), 3,30 (2Н, d).
13С-ЯМР (75 МГц, CDCl3): δ (ppm) = 158,1, 134,4, 130,1, 129,7, 127,6, 121,0, 117,2, 111,9, 85,4, 58,5, 56,9.
FTIR (ATR): v (см-1) = 3072, 2970, 2841, 1740,1576,1487, 1364,1219,1107, 991, 922, 850, 754.
2. А.6 3-аллил-5-метил-3,4-дигидро-2Н-бензо[е][1,3]оксазин
(реакционноспособный разбавитель)
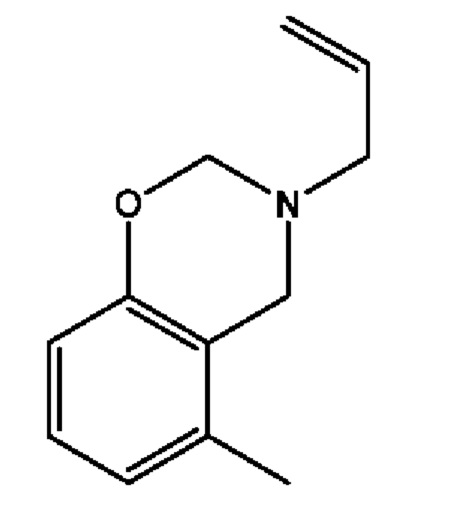
(сокращение; RD-A):
К смеси м-крезола (0,30 моль, 32,4 г) и аллиламина (0,30 моль, 17,1 г) небольшими порциями добавляют пара -формальдегид (0,62 моль, 18,6 г) в течение 30 мин, охлаждая на ледяной бане для поддержания температуры ниже 10°С. Затем добавляют пара-толуолсульфоновую кислоту (2,90 ммоль, 0,50 г), поднимают температуру до 90°С и смесь перемешивают в течение 3 ч. Полученную коричневую реакционную смесь затем растворяют в 500 мл диэтилового эфира. Раствор в эфире промывают водой (3 порции по 500 мл) для удаления любого непрореагировавшего формальдегида, м-крезола или аллиламина и сушат над сульфатом натрия. Растворитель упаривают при пониженном давлении и продукт сушат в вакуумной печи.
1Н-ЯМР (300 МГц, CDCl3): δ (ppm) = 6,72 (1Н, m), 6,64 (1Н, m), 6,53 (1Н, m), 5,82 (1Н, m), 5,10 (2Н, m), 4,81 (2Н, s), 3,86 (2Н, s), 3,08 (2Н, d), 2,17 (3Н, s).
13С-ЯМР (75 МГц, CDCl3): δ (ppm) = 157,9, 133,4, 130,2, 127,4, 122,2, 121,5, 118,3, 114,2, 82,1, 56,3, 49,4, 21,2.
FTIR (ATR): v (см-1) = 2956, 2843,1615, 1578,1505,1445, 1420,1279,1241,1109, 990, 921, 860.
2.А.7 3-аллил-6-окгил-3,4-дигидро-2Н-бензо[е][1,3]оксазин
(реакционноспособный разбавитель)
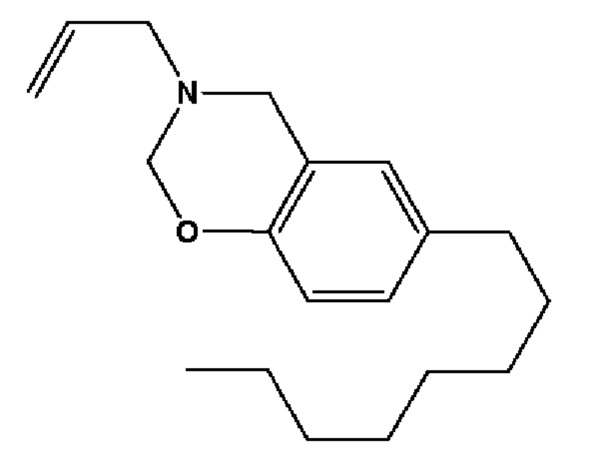
(сокращение; RD-B);
К смеси 4-октилфенола (0,30 моль, 61,8 г) и аллиламина (0,30 моль, 17,1 г) небольшими порциями добавляют параформальдегид (0,62 моль, 18,6 г) в течение 30 мин, охлаждая на ледяной бане для поддержания температуры ниже 10°С. Затем добавляют пара-толуолсульфоновую кислоту (2,90 ммоль, 0,50 г), поднимают температуру до 90°С и смесь перемешивают в течение 3 ч. Полученную коричневую реакционную смесь затем растворяют в 500 мл диэтилового эфира. Раствор в эфире промывали водой (3 порции по 500 мл) для удаления любого непрореагировавшего пара-формальдегида, 4-октилфенола или аллиламина и сушили над сульфатом натрия. Растворитель упаривают при пониженном давлении и продукт сушат в вакуумной печи.
1Н-ЯМР (300 МГц, CDCl3): δ (ppm) = 6,81 (1Н, d,3JH,Н = 6,65 Гц), 6,64 (1Н, s), 6,60 (1Н,3JH,H = 6,65 Гц), 5,85 (1Н, m), 5,12 (2Н, m), 4,84 (2Н, s), 3,88 (2Н, s), 3,21 (2Н, d), 2,41 (2Н, t), 1,48 (2Н, m), 1,19 (10Н, m), 0,79 (2Н, m).
13С-ЯМР (75 МГц, CDCl3): δ (ppm) = 152,0, 135,3, 135,1, 127,6, 127,2, 118,1, 116,2, 82,0, 54,6, 49,7, 35,3, 31,9, 31,7, 29,5, 29,4, 29,3, 22,7,14,1.
FTIR (ATR): v (см-1) = 2923, 2852, 1499, 1217, 1117, 988, 919, 820.
2.А.8 3-аллил-6-нонил-3,4-дигидро-2Н-бензо[е][1,3]оксазин
(реакционноспособный разбавитель)
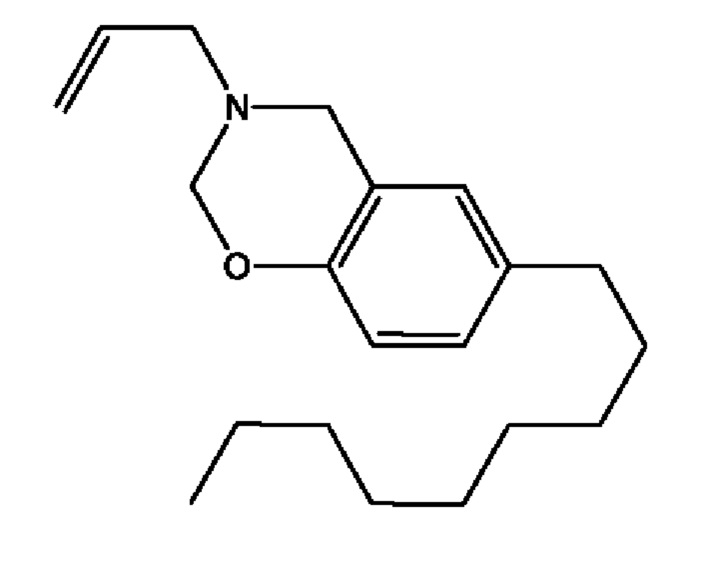
(сокращение: RD-C):
К смеси 4-нонилфенола (0,30 моль, 66,1 г) и аллиламина (0,30 моль, 17,1 г) небольшими порциями добавляют параформальдегид (0,62 моль, 18,6 г) в течение 30 мин, охлаждая на ледяной бане для поддержания температуры ниже 10°С. Затем добавляют пара-толуолсульфоновую кислоту (2,90 ммоль, 0,50 г), поднимают температуру до 90°С и смесь перемешивают в течение 3 ч. Полученную коричневую реакционную смесь затем растворяют в 500 мл диэтилового эфира. Раствор в эфире промывали водой (3 порции по 500 мл) для удаления любого непрореагировавшего пара-формальдегида, 4-нонилфенола или аллиламина и сушили над сульфатом натрия. Растворитель упаривают при пониженном давлении и продукт сушат в вакуумной печи.
1Н-ЯМР (300 МГц, CDCl3): δ (ppm) = 6,89 (1H, d), 6,82 (1H, s), 6,55 (1H,), 5,76 (1H, m), 5,01 (2Н, m), 4,66 (2Н, s), 3,85 (2Н, s), 3,21 (2Н, d), 2,99 (2Н, m), 1,91 (2Н, m), 1,13 (2Н, m), 1,08 (2Н, m), 0,99 (4Н, m), 0,67 (4Н, m), 0,53 (3Н, m).
13С-ЯМР (75 МГц, CDCl3): δ (ppm) = 136,7, 126,6, 125,9, 125,7, 119,2, 118,0, 116,4, 82,8, 57,3, 53,0, 36,4, 32,0, 31,5, 29,8, 29,4, 29,1, 22,5, 14,6.
FTIR (ATR): v (см-1) = 2957, 2851,1500, 1378, 1230, 1122, 988, 822, 820, 748.
2.B. Синтез гомополимеров (сравнительные примеры)
2.В1. Гомополимеризация сшитых бензоксазинов (сравнительные примеры)
Сокращенное название для сшитых (Cl) сополимеров бензоксазина Bn и реакционноспособного разбавителя RD выглядит следующим образом: Cl[p(Bn+RD)100].
В качестве тетратиола 4SH используют пентаэритритол тетракис(3-меркаптопропионат).
В качестве фотоинициатора PI используют этил(2,4,6-триметилбетоил)фенилфосфиновый этиловый эфир.
2.В1.1. Пример 1 (сравнительный); Сшитые сополимеры 6,6'-(пропан-2,2-диил)бис(3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазина) и 3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазина
(сокращение: Cl[p(B1+RD)100]):
Эфират трифторида бора (1,10 ммоль, 156 мг) добавляют к 4SH (3,1 ммоль, 1,51 г). Смесь добавляют к жидкой смеси B1 (8,1 ммоль, 3,16 г), RD (13,8 ммоль, 2,41 г) и PI (0,1 ммоль, 31,6 мг). С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризации B1 и RD.
FTIR (ATR): v (см-1) = 3011, 2968, 2919, 1740, 1625, 1438, 1364, 1215, 1117, 911.
2.B1.2. Пример 2 (сравнительный): Сшитые сополимеры бис(3-аллил-3,4-дигидро-2Н-бензо [е][1,3]оксазин-6-ил) метана и 3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазина
(сокращение; Cl[p(B2+RD)100]):
Эфират трифторида бора (1,10 ммоль, 156,1 мг) добавляют к 4SH (3,1 ммоль, 1,51 г). Смесь добавляют к жидкой смеси В2 (8,1 ммоль, 2,94 г), RD (10,3 ммоль, 1,80 г) и PI (0,1 ммоль, 31,6 мг). С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризации В2 и RD.
FTIR (ATR): v (см-1) = 3017, 2968, 2860, 1740, 1440, 1368, 1226, 1054, 869.
2.В1.3. Пример 3 (сравнительный): Сшитые сополимеры 6,6'-сульфонилбис(3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазина) и 3-аллил-3,4-дигидро-2Н-бензо[е][1,3]-оксазина
(сокращение: Cl[p(B3+RD)100]):
Эфират трифторида бора (1,10 ммоль, 156,1 мг) добавляют к 4SH (3,1 ммоль, 1,51 г). Смесь добавляют к жидкой смеси В3 (8,1 ммоль, 3,34 г), RD (10,3 ммоль, 1,80 г) и PI (0,1 ммоль, 31,6 мг). С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризации В3 и RD.
FTIR (ATR): v (см-1) = 2921, 2853, 1683, 1578, 1458, 1290, 1098, 911
2.B1.4. Пример 4 (сравнительный): Сшитые сополимеры 2,9-диаллил-1,2,3,8,9,10-гексагидробензо [2,1-е: 3,4-е']бис([1,3]оксазина и 3-аллил-3,4-дигидро-2Н-бензо[е][1,3]оксазина
(сокращение: Cl[p(B4+RD)100]):
Эфират трифторида бора (1,10 ммоль, 156,1 мг) добавляют к 4SH (3,1 ммоль, 1,51 г). Смесь добавляют к жидкой смеси В4 (12,1 ммоль, 3,29 г), RD (9,8 ммоль, 2,66 г) и PI (0,1 ммоль, 31,6 мг). С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризации В4 и RD.
FTIR (ATR): v (см-1) = 3017, 2970,1740, 1640, 1444, 1368, 1219, 911.
2.В2. Гомополимеризация циклических карбонатов (сравнительные примеры)
2.B2.1. Пример 5 (сравнительный): Поли(этиленкарбонат)
(сокращение: рЕС):
Эфират трифторида бора (1,86 ммоль, 265 мг) добавляют к расплаву этиленкарбоната (ЕС) (0,10 моль, 8,8 г). Реакционную смесь нагревают до 100°С в течение ночи без перемешивания. Через 24 ч получают твердый полимер.
FTIR (ATR): v (см-1) = 3007, 2970, 2878, 1744, 1442, 1364, 1219, 1048, 879.
2.В2.2. Пример 6 (сравнительный): Поли(пропиленкарбонат)
(сокращение: рРС):
Эфират трифторида бора (1,9 ммоль, 265 мг) добавляют к пропиленкарбонату (PC) (0,10 моль, 10,2 г). Реакционную смесь нагревают до 100°С в течение ночи без перемешивания. Через 24 ч получают твердый полимер.
FTIR (ATR): v (см-1) = 2988, 2923, 1789, 1485, 1379, 1180, 1040, 885, 773.
2.С. Синтез сополимеров (примеры согласно настоящему изобретению)
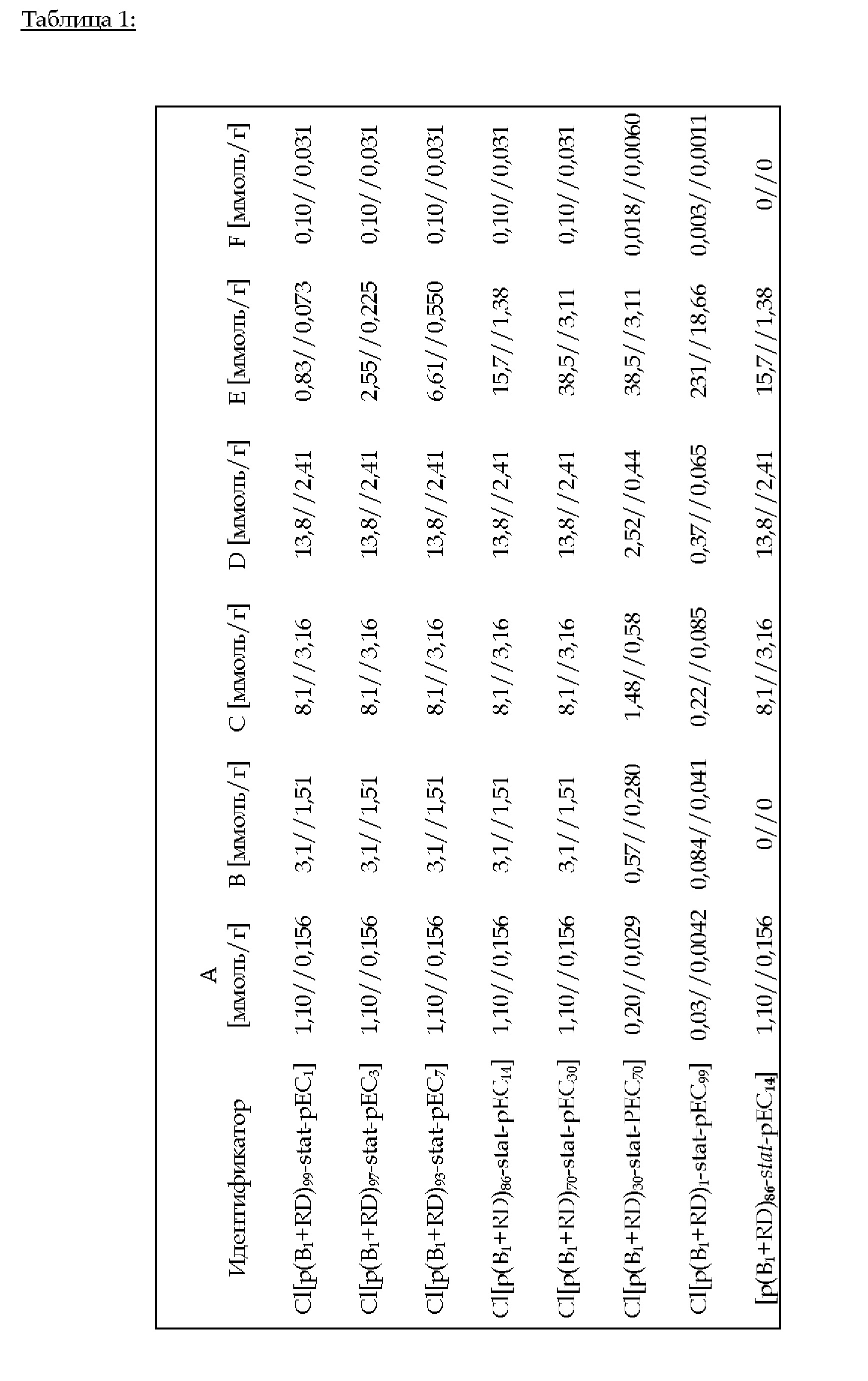
2.С.1. Пример 7 (изобретение): Cl[p(B1+RD)i-stat-pEC100-i] (i = 99, 97, 93, 86,70, 30,1) и [p(B1+RD)i-stat-pEC100-i] (i = 86)
Эфират трифторида бора (количество: А) добавляют к 4SH (количество: В). Смесь добавляют к жидкой смеси B1 (количество: С), RD (количество: D), ЕС (количество: Е) и PI (количество: F) - см. таблицу 1 ниже. С помощью УФ-излучения проводят предварительное тиол-еновое отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой сополимеризации B1, RD и ЕС. В случае [p(B1+RD)86-stat-pEC14] не добавляют ни 4SH, ни PI; УФ-освещение не применяли.
FTIR (ATR): v (см-1) = 3074, 2964, 2825, 1809, 1593, 1493, 1344, 1222, 1120, 1073, 922, 816, 754.
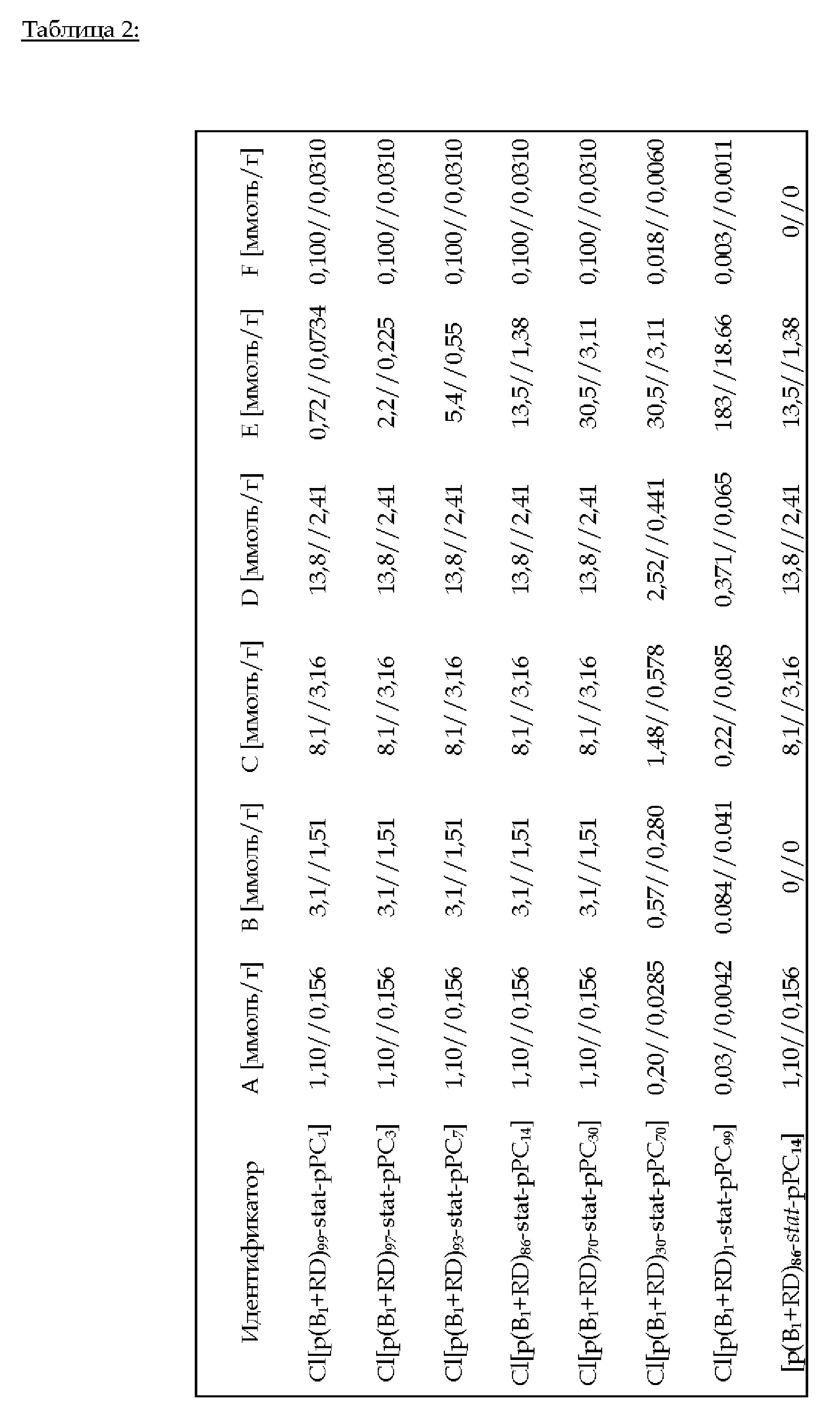
2.С.2. Пример 8 (изобретение): Cl[p(B1+RD)i-stat-pPC100-i] (i = 99, 97, 93, 86, 70, 30,1) и [p(B1+RD)i-stat-pPC100-i] (i = 86)
Эфират трифторида бора (количество: А) добавляют к 4SH (количество: В). Смесь добавляют к жидкой смеси B1 (количество: С), RD (количество: D), PC (количество: Е) и PI (количество: F) - см. таблицу 2 ниже. С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой сополимеризации B1, RD и PC. В случае [p(B1+RD)86-stat-pPC14] не добавляли ни 4SH, ни PI; УФ-освещение не применяли.
FTIR (ATR): v (см-1) = 2968, 2925, 2821, 1740, 1591, 1493, 1366, 1236, 1132, 987, 911, 820, 754.
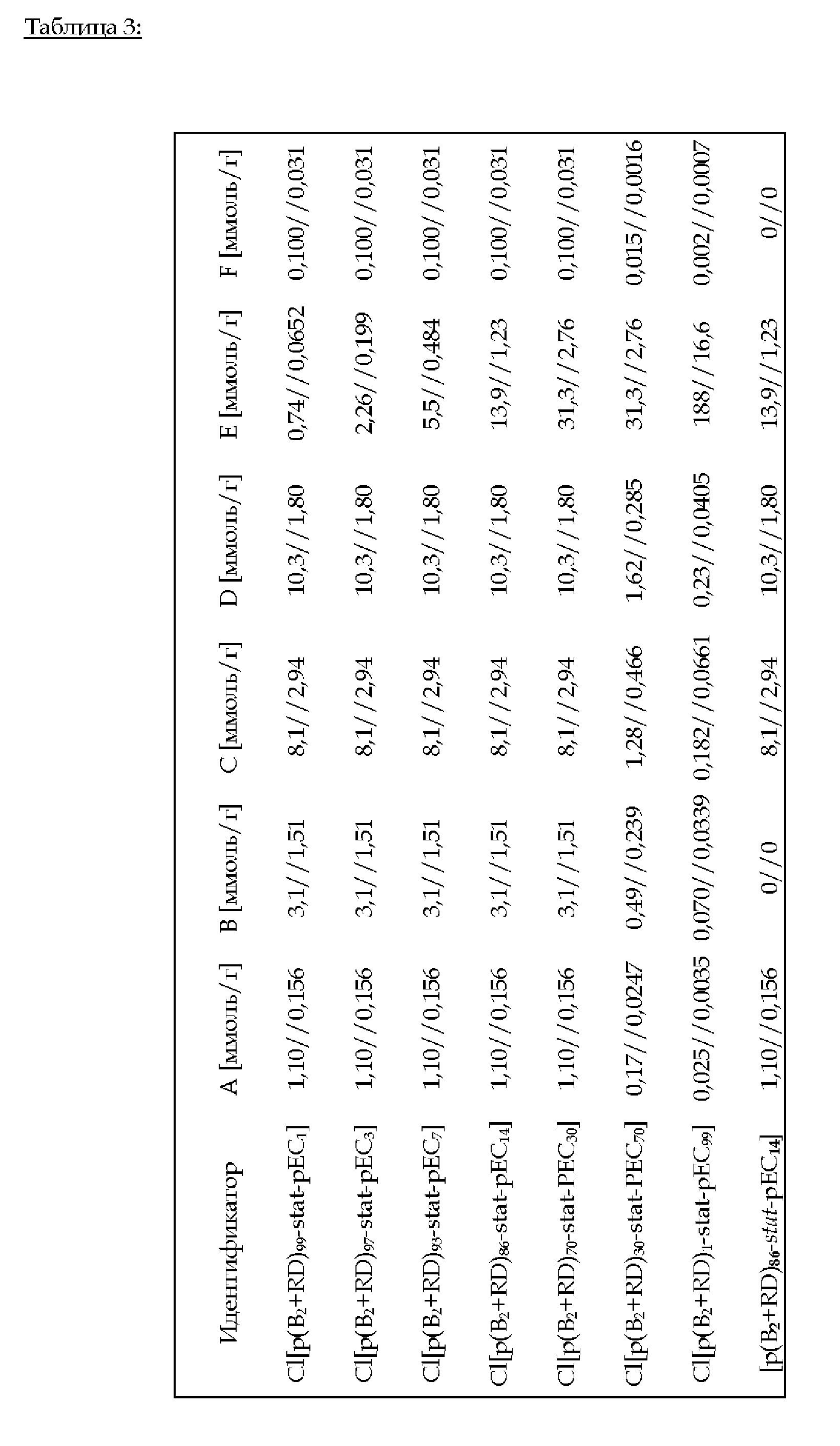
2.С.3. Пример 9 (изобретение): Cl[p(B2+RD)i-stat-pEC100-i] (i = 99, 97, 93, 86, 70, 30,1) и [p(B2+RD)i-stat-pEC100-i] (i = 86)
Эфират трифторида бора (количество: А) добавляют к 4SH (количество: В). Смесь добавляют к жидкой смеси В2 (количество: С), RD (количество: D), ЕС (количество: Е) и PI (количество: F) - см. таблицу 3 ниже. С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризапии В2, RD и ЕС. В случае [p(B2+RD)86-stat-pEC14] не добавляли ни 4SH, ни PI; УФ-освещение не применяли.
FTIR (ATR): v (см-1) = 3005, 2968, 2926, 1736, 1594, 1438, 1364, 1230, 1236, 987, 920, 811.
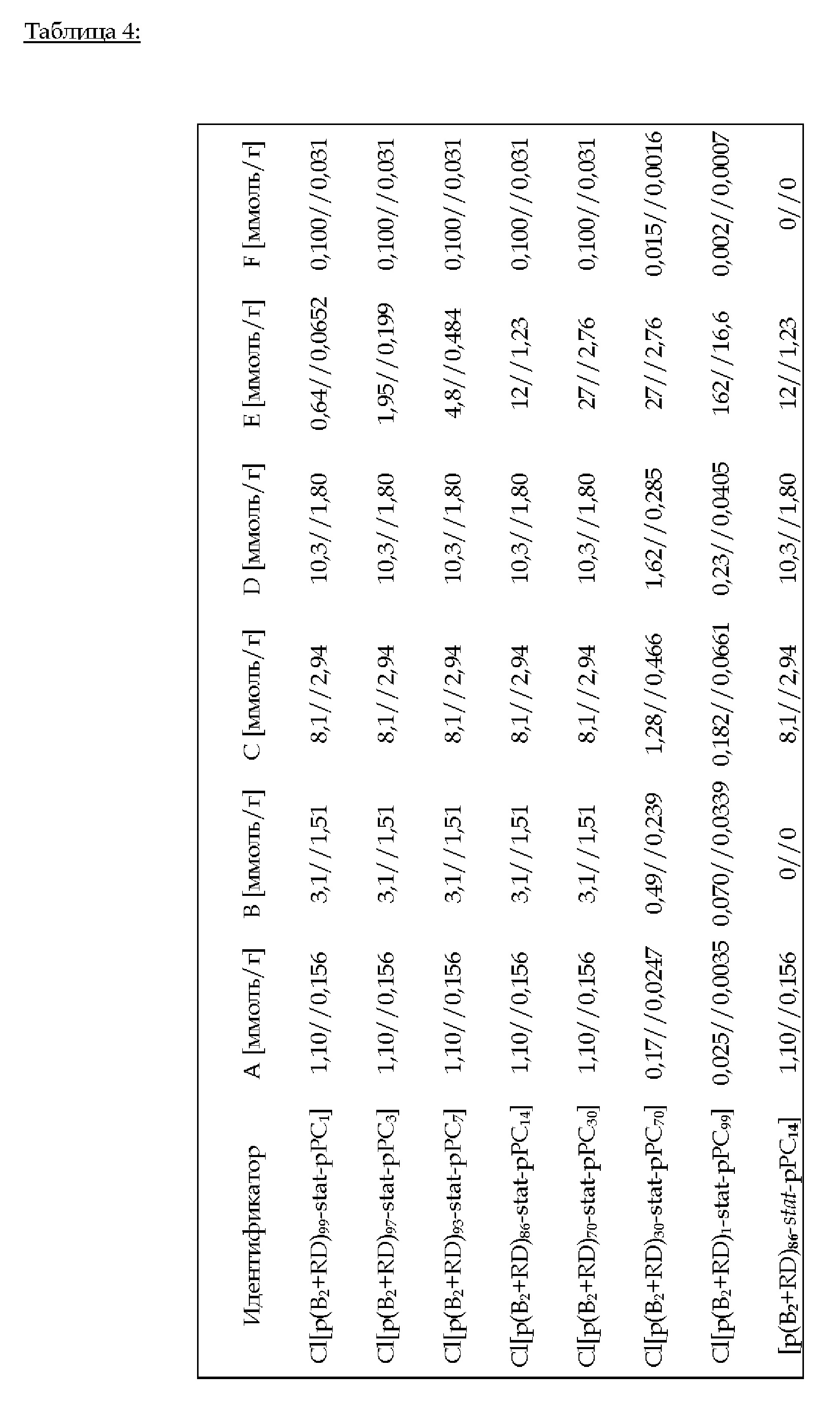
2.С.4. Пример 10 (изобретение): Cl[p(B2+RD)i-stat-pPC100-i] (i = 99, 97, 93, 86,70, 30,1) и [p(B2+RD)i-stat-pPC100-i] (i = 86)
Эфират трифторида бора (количество: А) добавляют к 4SH (количество: В). Смесь добавляют к жидкой смеси Б2 (количество: С), RD (количество: D), PC (количество: Е) и PI (количество: F) - см. таблицу 4 ниже. С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризапии В2, RD и PC. В случае [p(B2+RD)86-stat-pPC14] не добавляли ни 4SH, ни PI; УФ-освещение не применяли.
FTIR (ATR): v (см-1) = 3070, 2923, 2839, 1797, 1736, 1591, 1493, 1354, 1246, 1117, 991, 926, 765.
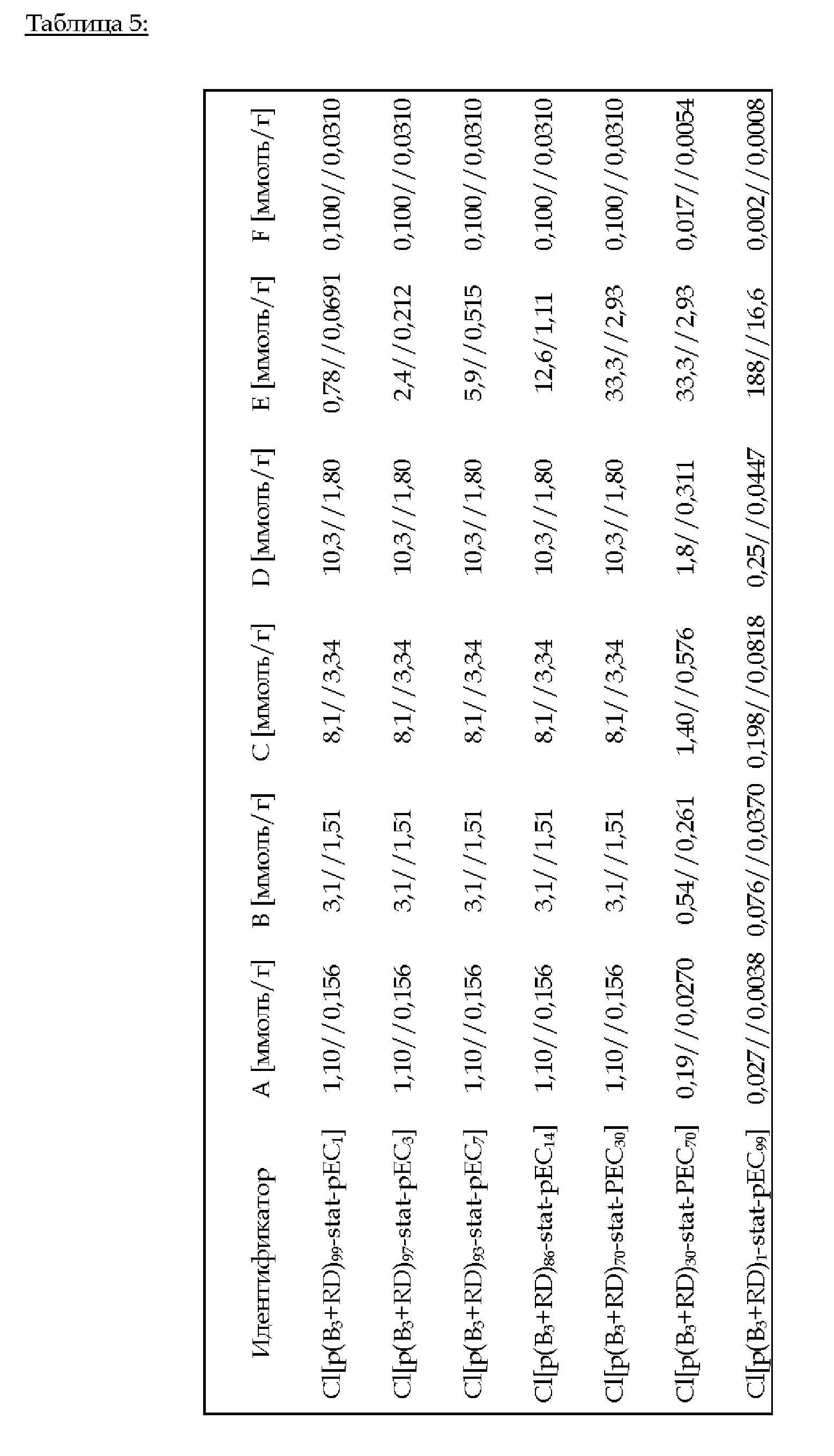
2.С.5. Пример 11 (изобретение): Cl[p(B3+RD)i-stat-pEC100-i] (i = 99, 97, 93, 86, 70, 30, 1)
Эфират трифторида бора (количество: А) добавляют к 4SH (количество: В). Смесь добавляют к жидкой смеси В3 (количество: С), RD (количество: D), ЕС (количество: Е) и PI (количество: F) - см. таблицу 5 ниже. С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризации В3, RD и ЕС.
FTIR (ATR): v (см-1) = 3004, 2919, 2815, 1729, 1592, 1452, 1252, 1136, 999, 920.
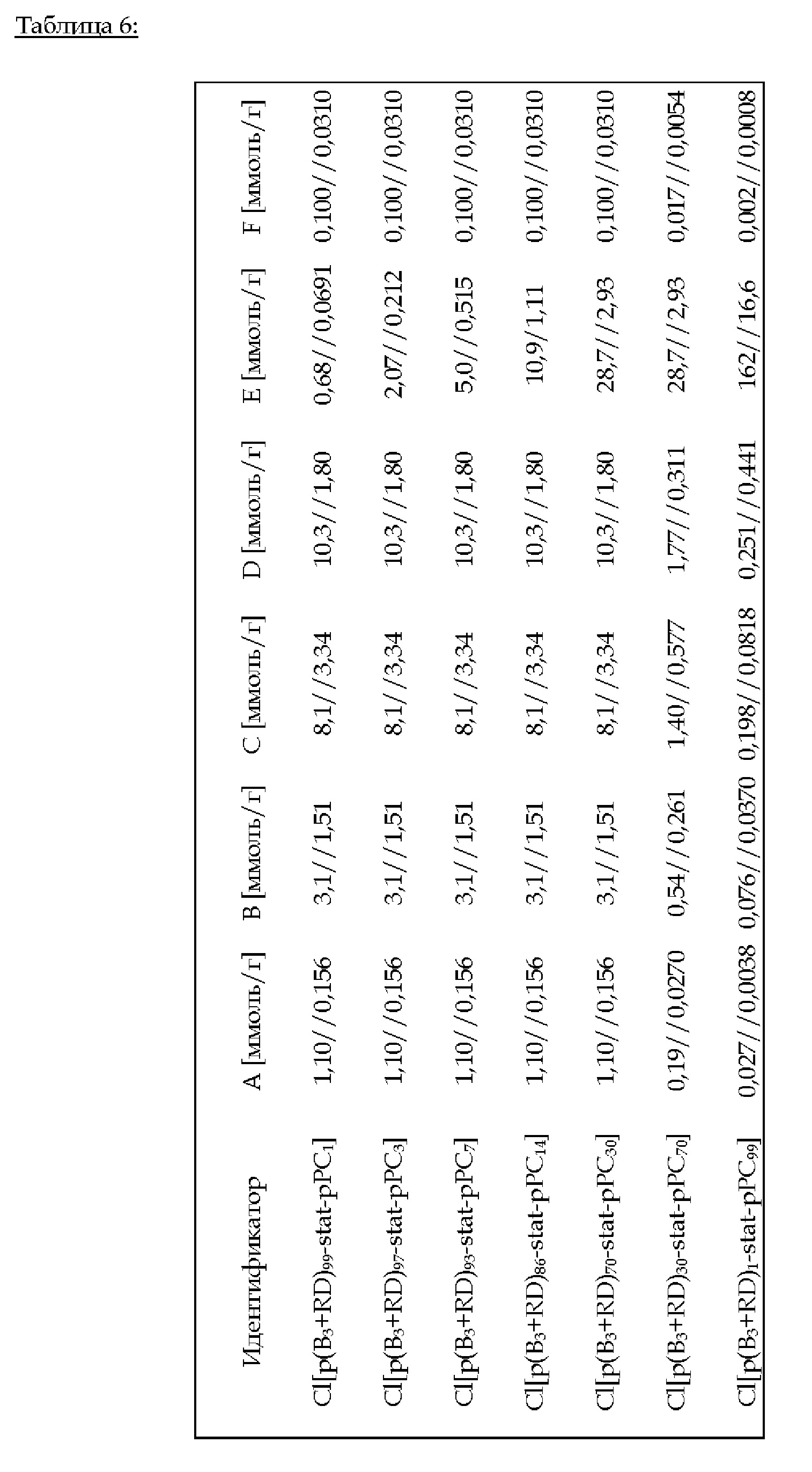
2.С.6. Пример 12 (изобретение): Cl[p(B3+RD)i-stat-pPC100-i] (i = 99, 97, 93, 86, 70, 30, 1)
Эфират трифторида бора (количество: А) добавляют к 4SH (количество: В). Смесь добавляют к жидкой смеси В3 (количество: С), RD (количество: D), PC (количество: Е) и PI (количество: F) - см. таблицу 6 ниже. С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризапии В3, RD и PC.
FTIR (ATR): v (см-1) = 3076, 2925, 2815, 1730, 1595, 1460, 1256, 1142, 971, 916, 756.
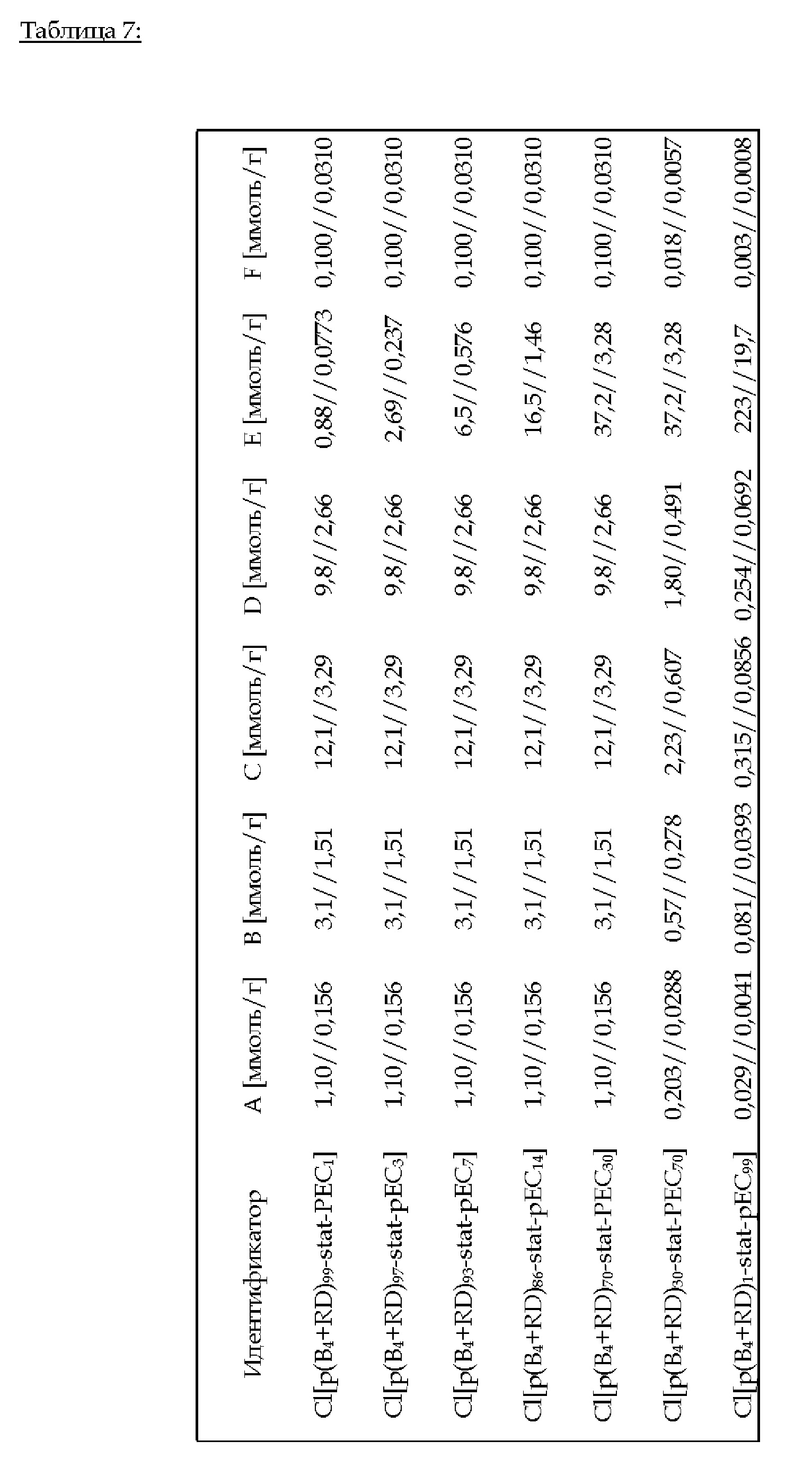
2.С.7. Пример 13 (изобретение): Cl[p(B4+RD)i-stat-pEC100-i] (i = 99, 97, 93, 86, 70, 30, 1)
Эфират трифторида бора (количество: А) добавляют к 4SH (количество: В). Смесь добавляют к жидкой смеси В4 (количество: С), RD (количество: D), ЕС (количество: Е) и PI (количество: F) - см. таблицу 7 ниже. С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризации В4, RD и ЕС.
FTIR (ATR): v (см-1)=2998, 2917, 1762, 1638, 1622, 1479, 1391, 1156, 1052, 969, 716.
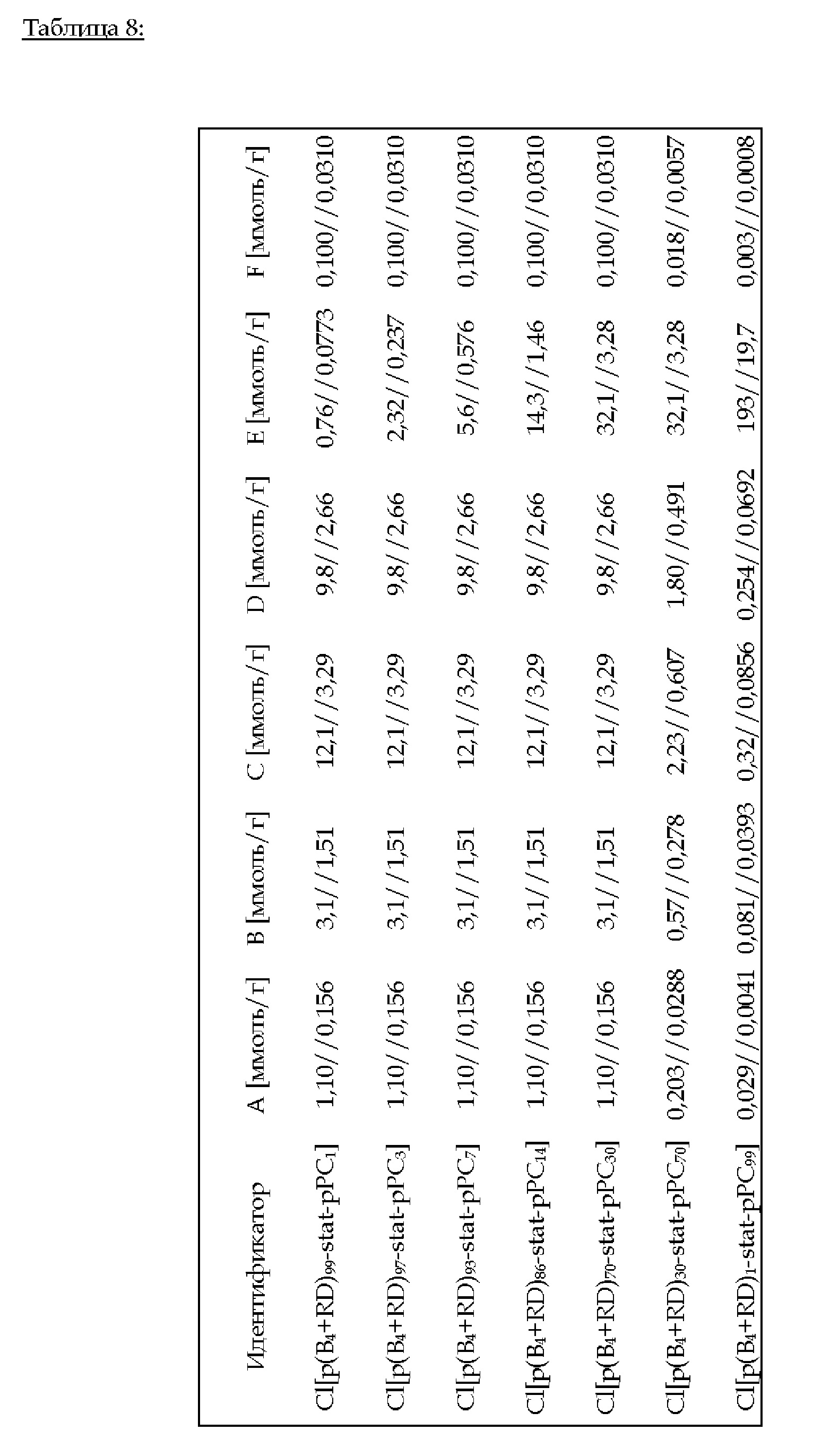
2.С.8. Пример 14 (изобретение); Cl[p(B4+RD)i-stat-pPC100-i] (i = 99, 97, 93, 86, 70, 30, 1)
Эфират трифторида бора (количество: А) добавляют к 4SH (количество: В). Смесь добавляют к жидкой смеси В4 (количество: С), RD (количество: D), PC (количество: Е) и PI (количество: F) - см. таблицу 8 ниже. С помощью УФ-излучения проводят тиол-еновое предварительное отверждение в течение 15 мин. Последующее нагревание до 100°С в течение 24 ч приводит к катионной кольцевой полимеризации В4, RD и PC.
FTIR (ATR): v (см-1) = 3070, 2928, 2854, 1740, 1640, 1617, 1436, 1354, 1217, 1130, 936.
3. Расширение
3.А Визуальное представление сополимера согласно изобретению
Для визуальной демонстрации влияния расширения при отверждении образцы готовили следующим образом: Эфират трифторида бора (1,1 ммоль, 0,156 г) добавляли к 4SH (3,1 ммоль, 1,51 г). Смесь добавляли к жидкой смеси B1 (8,1 ммоль, 3,16 г), RD (13,8 ммоль, 2,41 г), PC (15,7 ммоль, 1,38 г) и PI (0,10 ммоль, 0,031 г) и выливали в круглую форму. С использованием УФ-излучения проводили предварительное тиол-еновое отверждение в течение 15 мин. Впоследствии образец был разделен на две части. Одну часть нагревали до 100°С в течение 24 ч для обеспечения катионной сополимеризации B1, RD и PC с раскрытием кольца; другую часть выдерживали без дополнительного отверждения.
Фиг. 1 иллюстрирует тиол-еновый предварительно отвержденный, но не сополимеризованный образец (меньшая часть справа) и тиол-еновый предварительно отвержденный и сополимеризованный образец (большая часть слева).
3.В. Степень расширения
Степень расширения количественно определяли путем измерения плотности гомополимеров (см. выше сравнительные примеры 1-6), с одной стороны, и сополимеров согласно настоящему изобретению (см. выше примеры 7-14 согласно настоящему изобретению) - с другой. Степень расширения измеряли и рассчитывали, как описано выше в главе 1.А.2 «Методы». Степени расширения приведены в таблицах 10-17 ниже в главах 3.В.1 - 3.В.8 и дополнительно проиллюстрированы на прилагаемых фиг.2-9.
В то время как сравнительные примеры были включены в отдельные таблицы в главах 3.В.1 - 3.В.8., НЕсополимеризованные конгенеры, а именно гомополимеры полибензоксазина, с одной стороны, а также поли(циклические карбонатные) гомополимеры, с другой стороны, были перечислены в таблице 9 ниже, чтобы можно было составить представление о степенях расширения, достижимых для образцов из уровня техники:
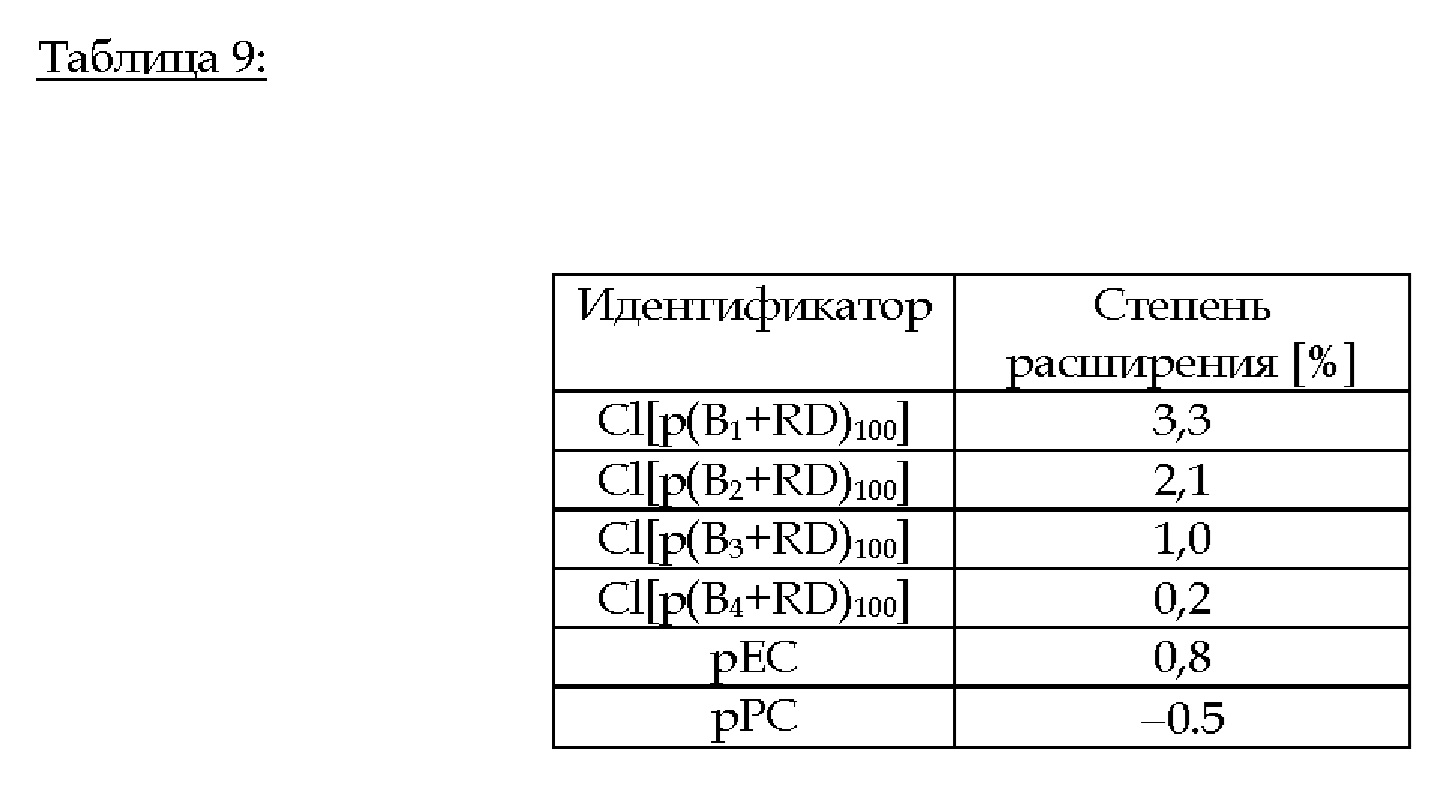
3.В.1. Cl[p(B1+RD)i-stat -рЕС100-i] (i = 100, 99, 97, 93, 86, 70, 30,1, 0) и [p(B1+RD)i-stat-pEC100-i] (i = 86)
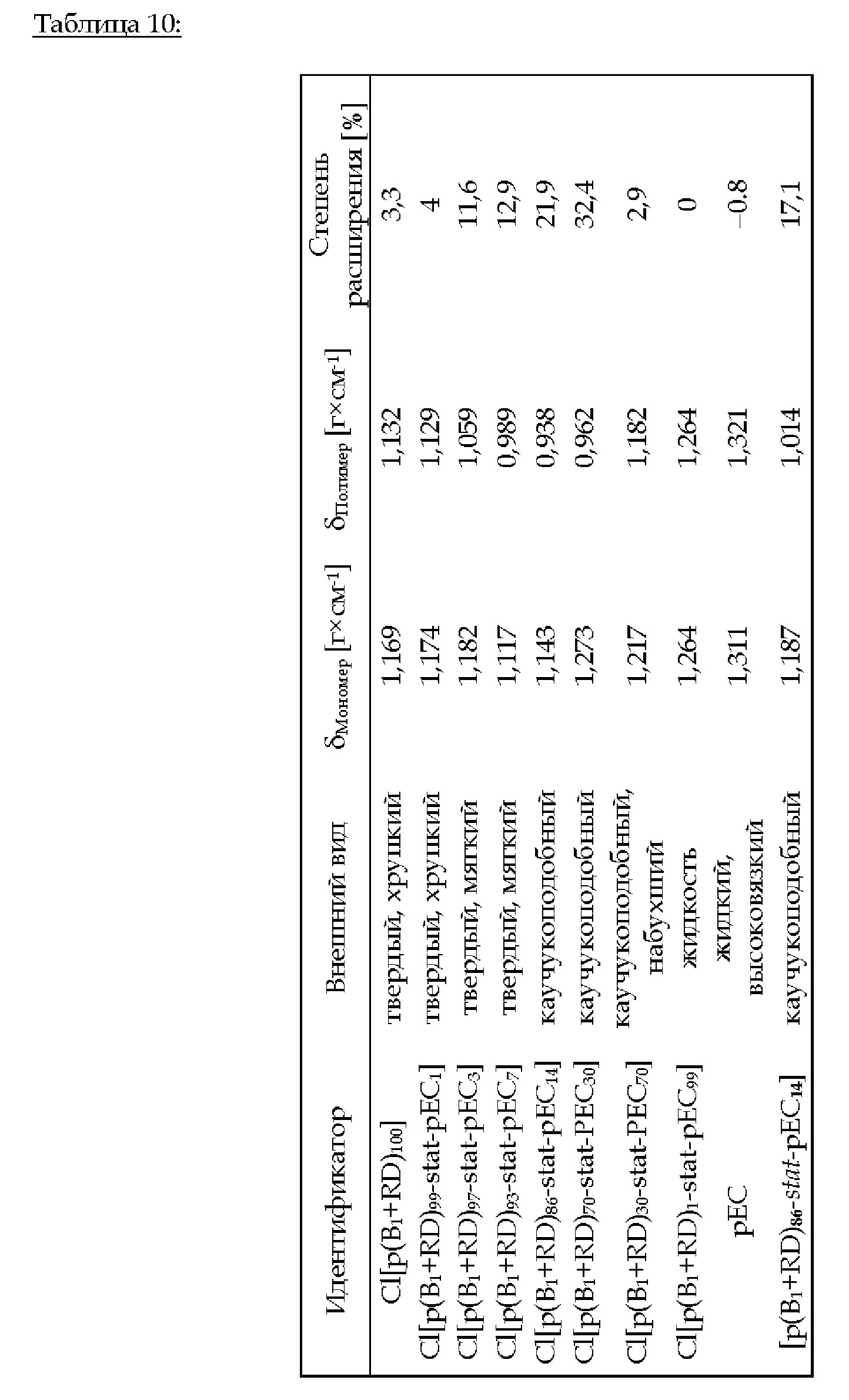
Фиг. 2 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B1+RD)0-100-stat -рЕС0-100].
3.В.2. Cl[p(B1+RD)i-stat -pPC100-i] (i = 100, 99, 97, 93, 86, 70, 30,1, 0) и [p(B1+RD)i-stat-pPC100-i] (i = 86)
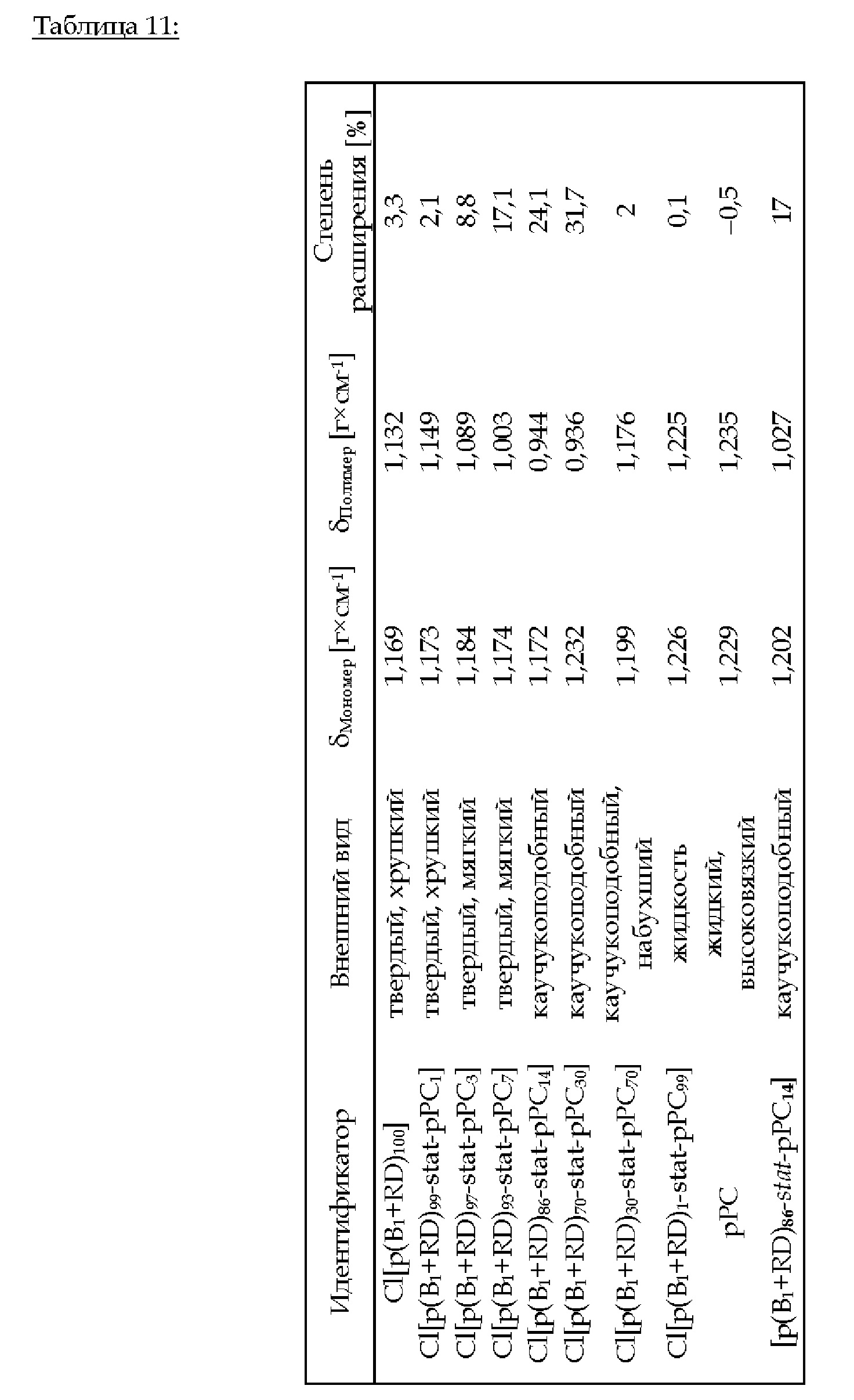
Фиг. 3 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B1+RD)0-100-stat -рРС0-100].
3.В.3. Cl[p(B2+RD)i-stat -рЕС100-i] (i = 100, 99, 97, 93, 86, 70, 30,1, 0) и [p(B2+RD)i-stat-pEC100-i] (i = 86)
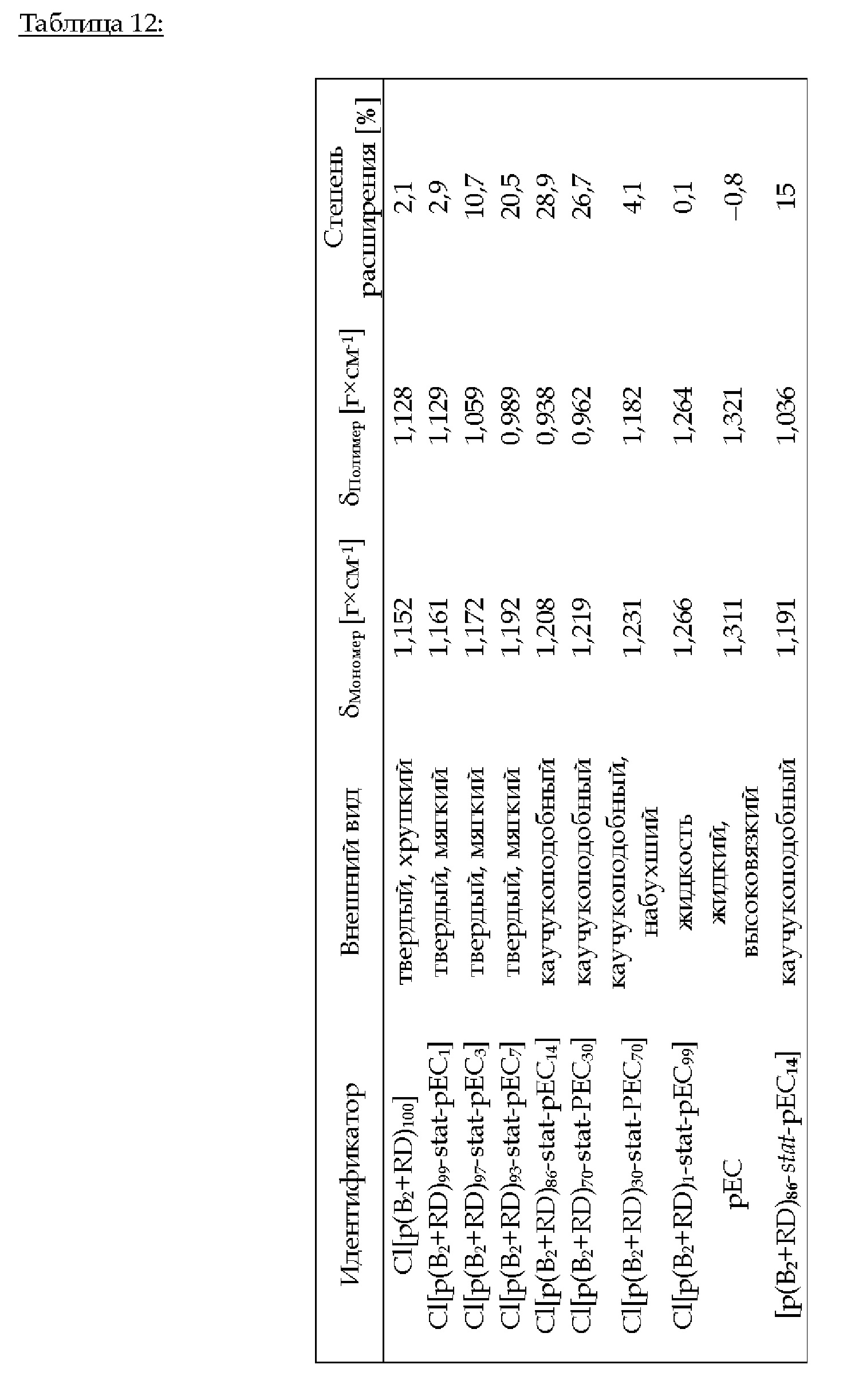
Фиг. 4 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B2+RD)0-100-stat -рЕС0-100].
3.В.4. Cl[p(B2+RD)i-stat -pPC100-i] (i = 100, 99, 97, 93, 86, 70, 30,1, 0) и [p(B2+RD)i-stat-pPC100-i] (i = 86)
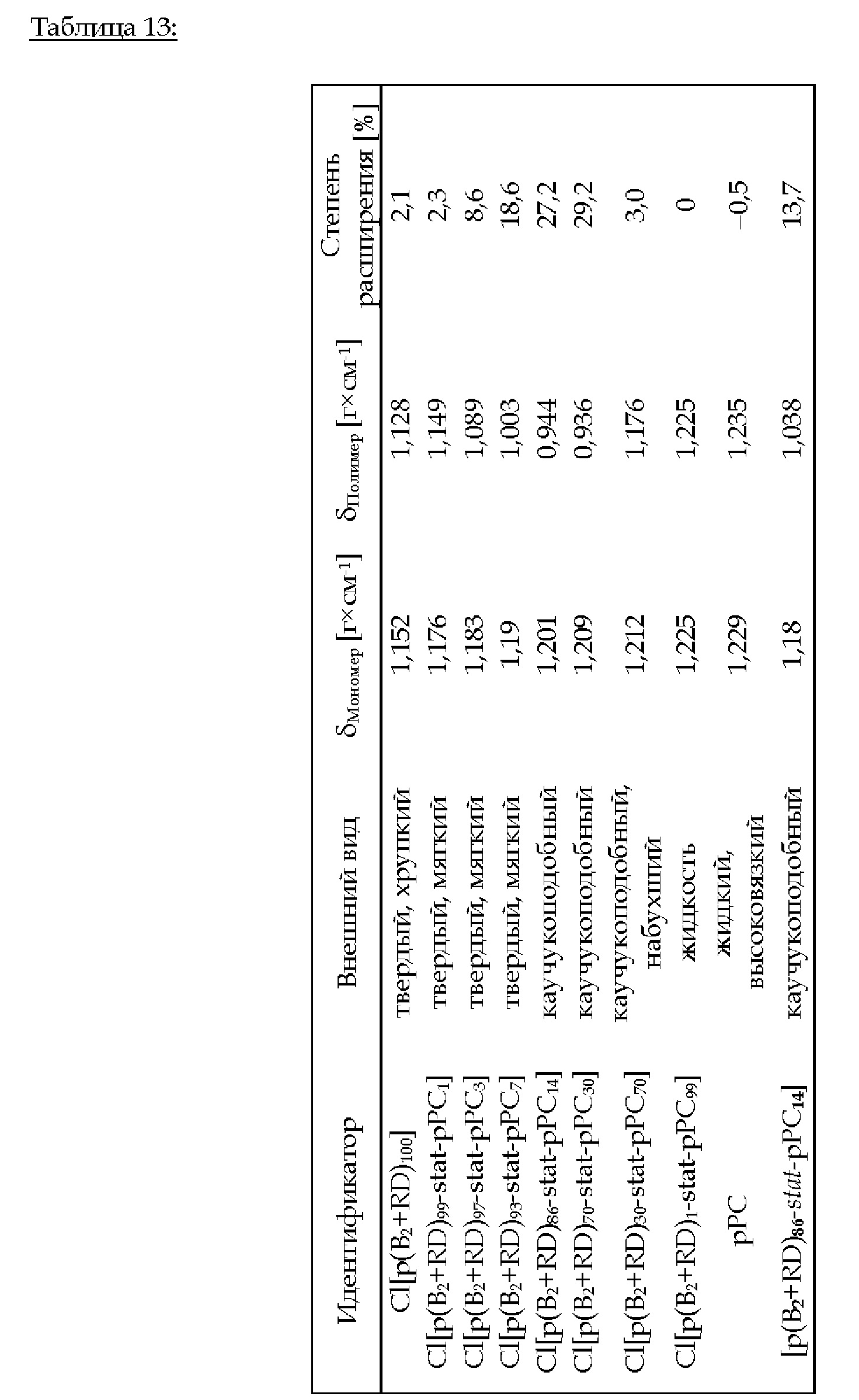
Фиг. 5 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B2+RD)0-100-stat -рРС0-100].
3.В.5. Cl[p(B3+RD)i-stat-pEC100-i] (i = 100, 99, 97, 93, 86, 70, 30,1, 0)
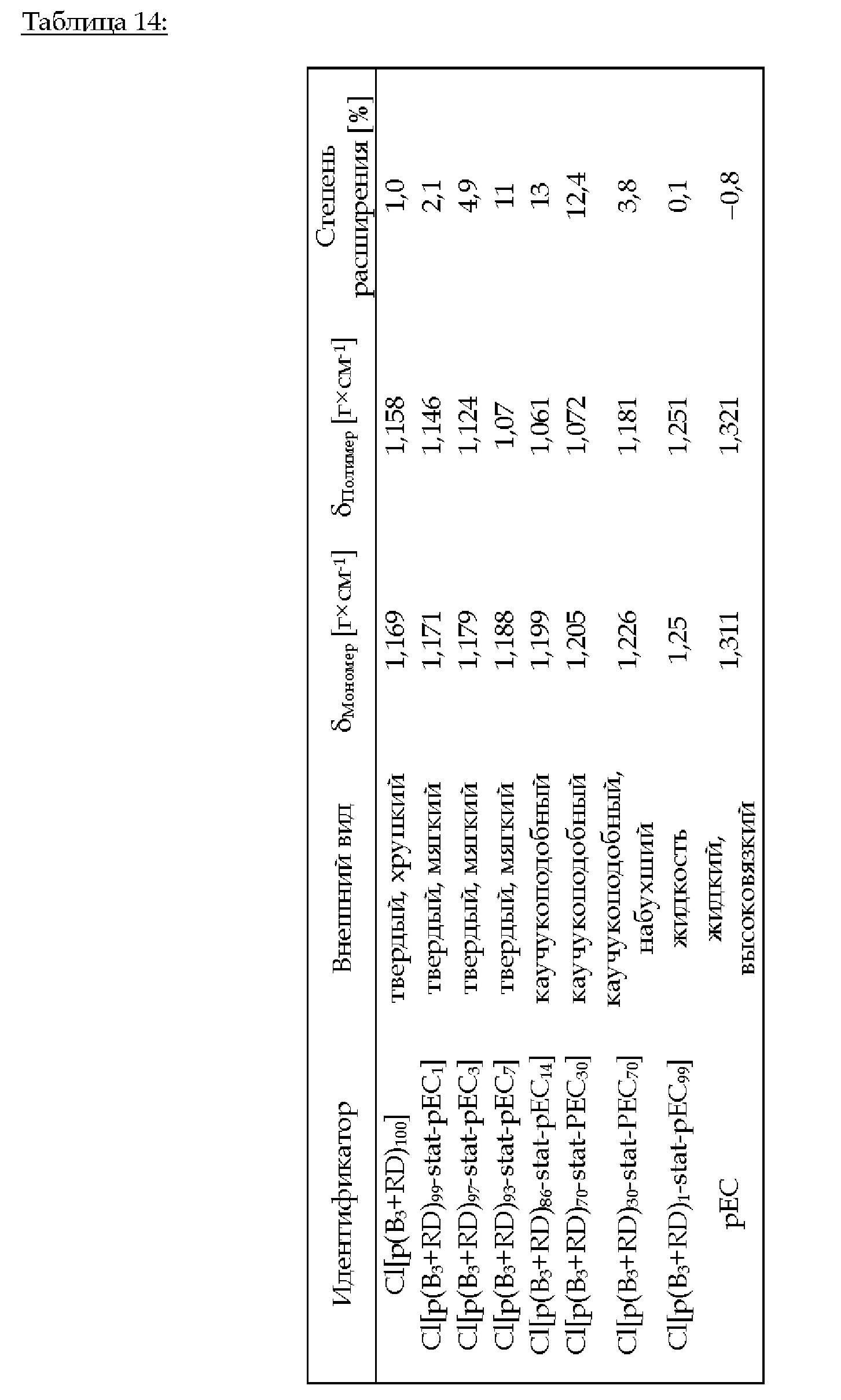
Фиг. 6 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B3+RD)0-100-stat -рЕС0-100].
3.В.6. Cl[p(B3+RD)i-stat-pPC100-i] (i = 100, 99, 97, 93, 86, 70, 30,1, 0)
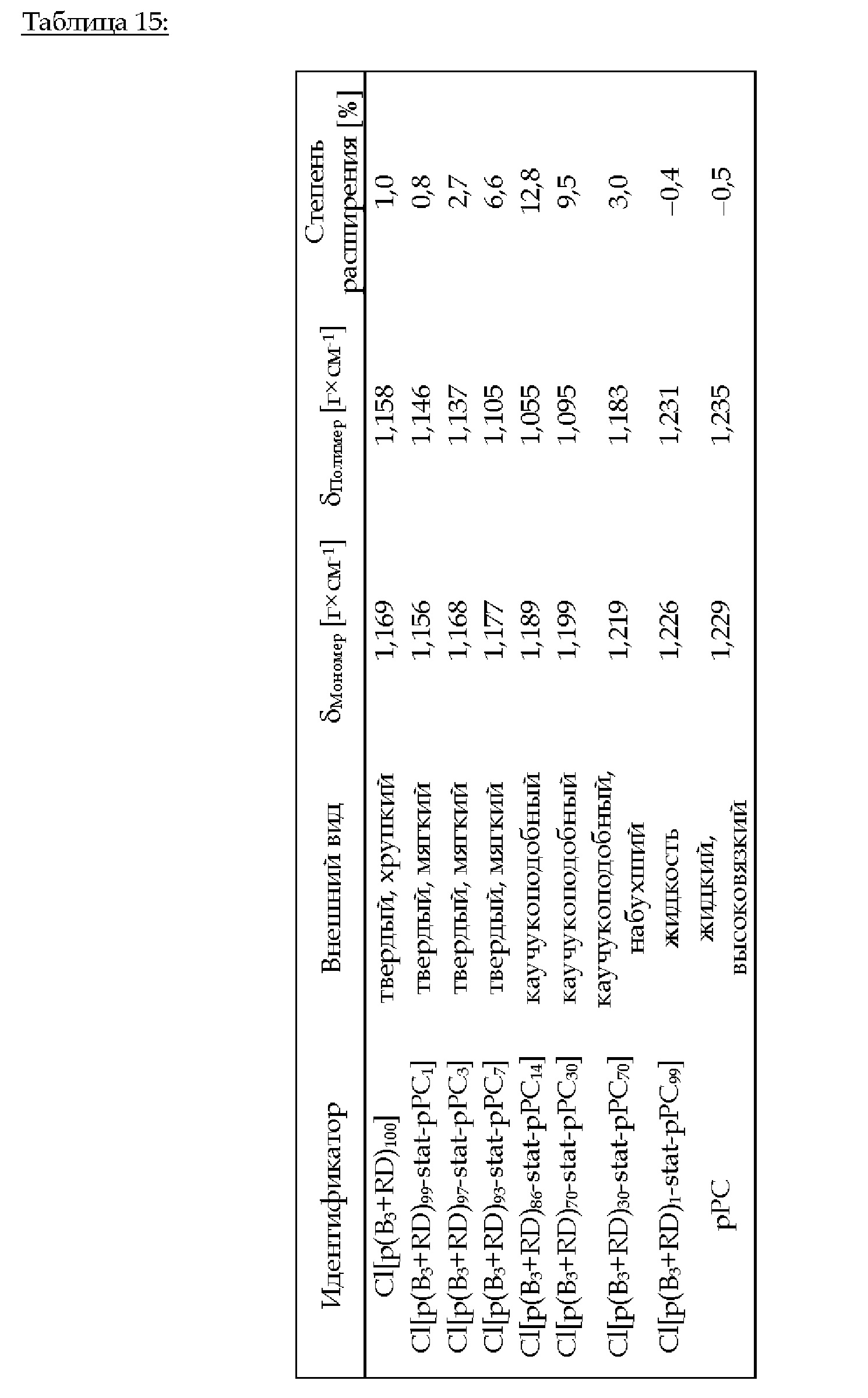
Фиг. 7 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B3+RD)0-100-stat -рРС0-100].
3.В.7. Cl[p(B4+RD)i-stat-pEC100-i] (i = 100, 99, 97, 93, 86, 70, 30,1, 0)
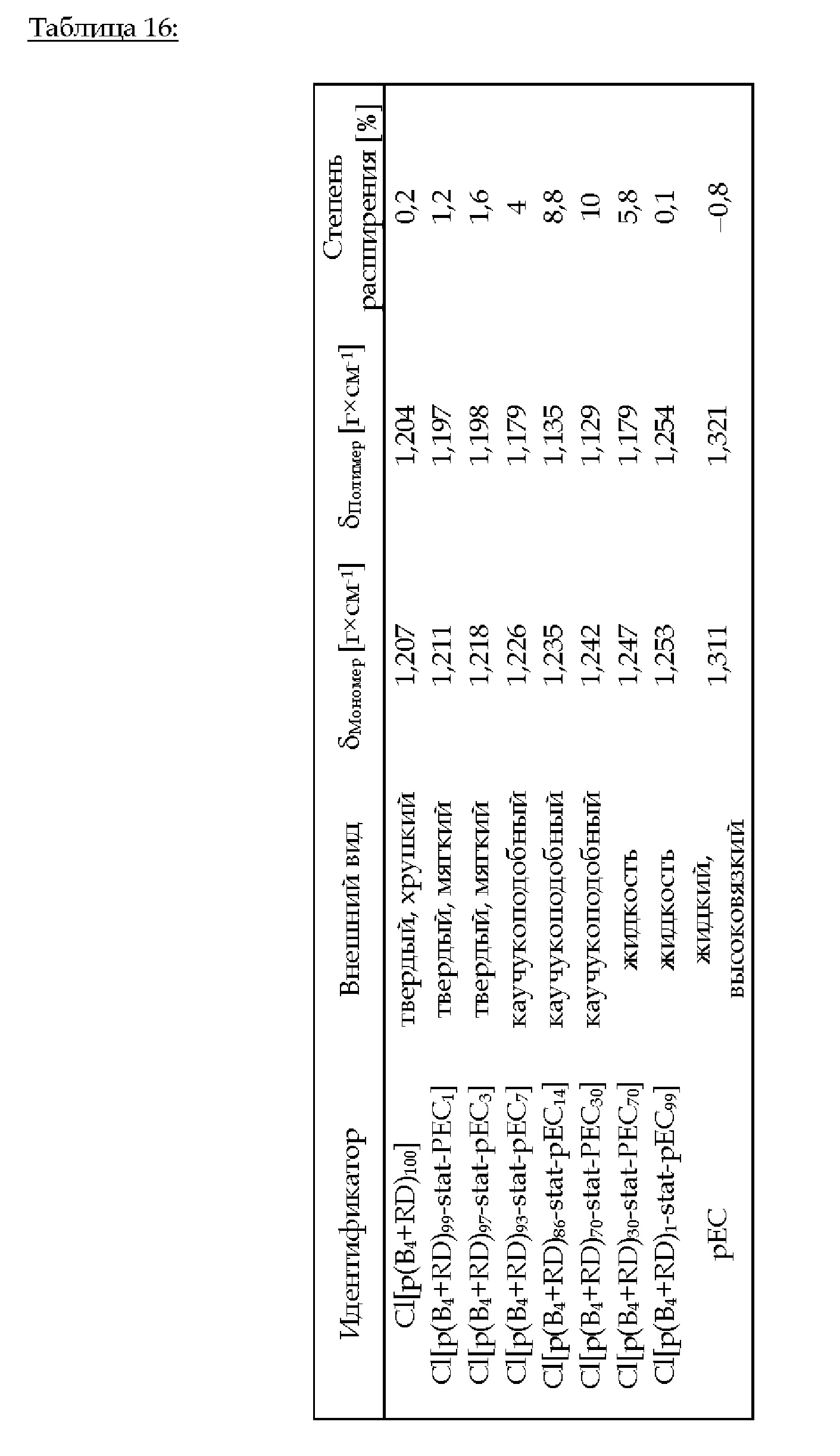
Фиг. 8 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B4+RD)0-100-stat -рЕС0-100].
3.В.8. Cl[p(B4+RD)i-stat-pPC100-i] (i = 100, 99, 97, 93, 86, 70, 30,1, 0)
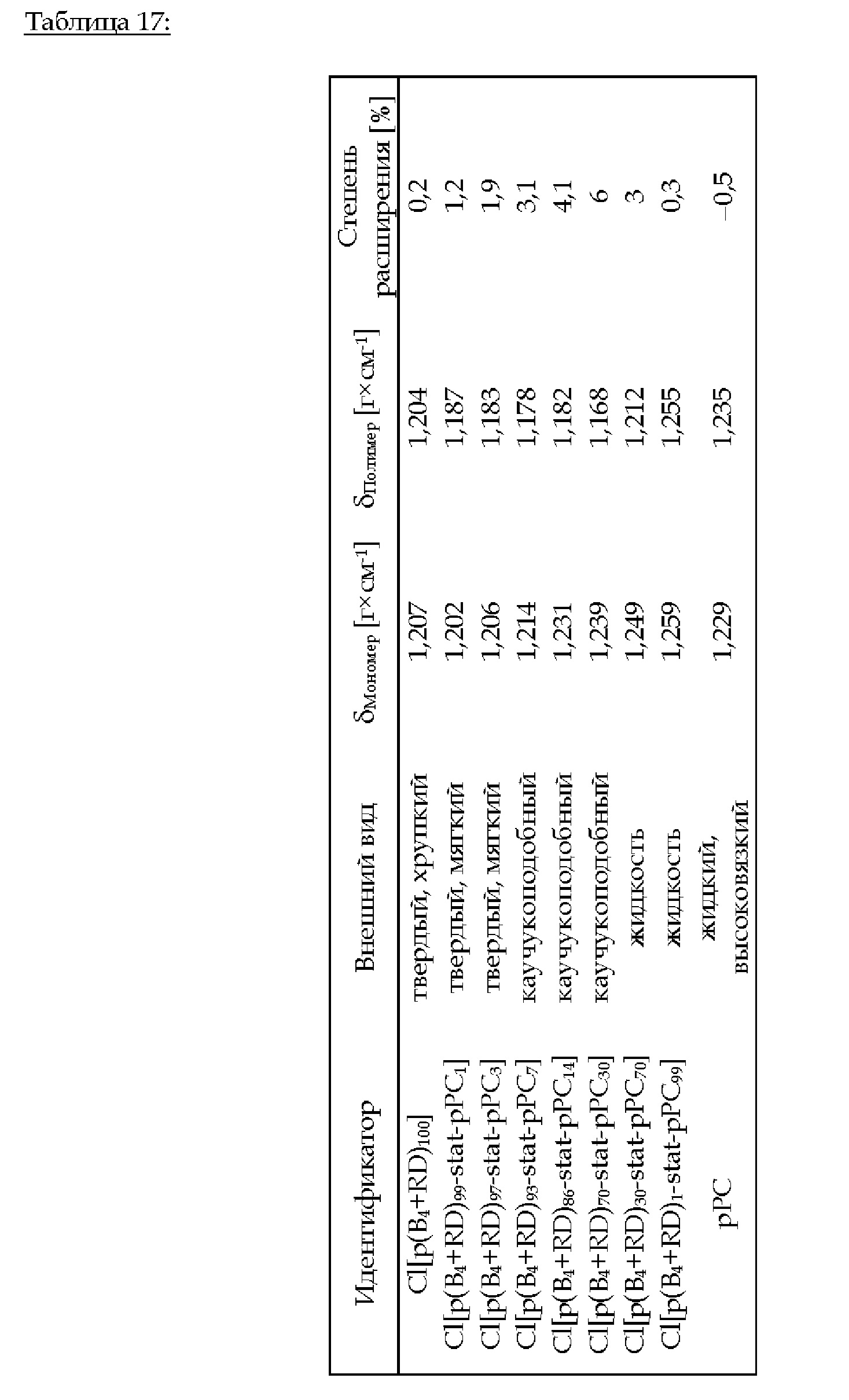
Фиг. 9 иллюстрирует степень расширения в [%] в зависимости от концентрации циклического карбоната в сополимере Cl[p(B4+RD)0-100-stat -рРС0-100].
3.С ЗАКЛЮЧЕНИЕ
Бензоксазины и циклические карбонаты могут быть сополимеризованы в соответствии с механизмами раскрытия кольца. На этом этапе отверждения состав демонстрирует объемное расширение до более чем 30 об. %. Примечательно, что соответствующие гомополимеры демонстрируют объемное расширение только в низкой степени (в случае поли(бензоксазина)) или вообще не имеют объемного расширения (в случае поли(циклического карбоната)). Такое поведение составов, содержащих бензоксазины и циклические карбонаты, отличается от многих других мономерных составов, которые демонстрируют усадку на стадии отверждения. Степень объемного расширения может быть адаптирована в диапазоне от 0 до более чем 30 об. % путем тщательного выбора количества и типов бензоксазинов и циклических карбонатов. Соответственно, механические свойства соответствующих сополимеров также могут варьироваться от высокохрупких до каучукоподобных типов.
Состав, содержащий бензоксазины и циклические карбонаты, от жидкого до полутвердого; его вязкость можно регулировать путем добавления реакционноспособных разбавителей, например реакционноспособных разбавителей на основе бензоксазина. Следовательно, смеси, не содержащие растворителей, можно поддерживать. Таким образом, эти составы можно использовать в качестве покрытий и адгезивов, которые расширяются во время реакции отверждения, что приводит к образованию пустотных и не содержащих трещин покрытий, которые не отслаиваются от подложки, к которой они были приклеены. Если бензоксазины содержат дополнительные функциональные группы, такие как олефиновые звенья, которые обеспечивают поперечное сшивание с помощью реакций, таких как клик-реакция тиол-ен, состав может быть предварительно отвержден таким образом, что поперечное сшивание выполняется перед сополимеризацией с раскрытием кольца. Одним из возможных методов для этой стратегии является добавление радикальных фотоинициаторов и применение УФ-облучения, так что сшивание может быть выполнено при комнатной температуре, в то время как индуцируемая температурой сополимеризация, открывающая кольцо, еще не началась. С помощью этой стратегии могут быть получены твердые образцы с индивидуальной геометрией, которые могут быть вставлены в полости, в которых они показывают геометрическое выравнивание (например, полное заполнение полости) при воздействии температурных раздражителей.
4. Примеры применения
4,1. Пример применения 1
Отвержденный образец композиции Cl[p(B2+RD)93 -stat-pEC7] и размеры в санти- и дециметровом диапазоне, например, 11,8 × 3,9 × 0,95 см, можно использовать в качестве материала для поддержки и фиксации обмоток электрических машин. Этот образец вставляется в полость с немного большими размерами, чем размеры образца, например, 12 × 4 × 1 см. Затем применяют нагревание, и образец объемно расширяется за счет полимеризации с раскрытием кольца. За счет объемного расширения происходит точное геометрическое выравнивание образца со стенками полости, что придает отличную стабильность и, кроме того, изолирующие свойства, так как между образцом и стенками полости не образуются трещины или пустоты.
4,2. Пример применения 2
Предварительно отвержденный образец композиции Cl[p(B2+RD)86-stat -рРС14] и размеры в милли-, санти- или метровом диапазоне в форме, например, готовых стержней, стиков, цилиндров или прокладок, может быть использован в качестве материала для поддержки и фиксации в изолирующих барьерных системах высоковольтной обмотки электрооборудования, которое изолировано от жидкости или газа. Этот образец вставляется в изолирующие барьерные системы с другим традиционным изоляционным материалом. Затем в процессе высушивания применяют нагревание, и образец расширяется объемно за счет полимеризации с раскрытием кольца. Благодаря объемному расширению происходит точное геометрическое выравнивание образца с окружающим материалом и компенсирует усадочные и сборочные допуски этих материалов, что обеспечивает превосходную стабильность и, кроме того, изолирующие свойства и формирует посадочную опору, например, обмоток или слоистых электромагнитных материалов.
Реферат
Изобретение относится к группе изобретений: расширяемая полимеризуемая композиция; варианты поли(бензоксазин)-сополи(циклического карбонатного) продукта полимеризации; герметик, клей, покрытие, связующий агент или зубная пломба; варианты применения расширяемой полимеризуемой композиции; варианты способов получения поли(бензоксазин)-сополи(циклического карбонатного) продукта полимеризации; предварительно отвержденная расширяемая полимеризуемая композиция; применение предварительно отвержденной расширяемой полимеризуемой композиции. Расширяемая полимеризуемая композиция, применяемая для получения поли(бензоксазин)-сополи(циклического карбонатного) продукта полимеризации. Данная композиция содержит по меньшей мере один бензоксазин и по меньшей мере один циклический карбонат. Бензоксазиновые звенья, содержащиеся в композиции, представляют собой бензоксазиновые звенья, которые являются сшиваемыми друг с другом. Герметик, клей, покрытие, связующий агент или зубная пломба содержат данную расширяемую полимеризуемую композицию. Расширяемая полимеризуемая композиция содержит по меньшей мере один бензоксазин и по меньшей мере один циклический карбонат, где расширяемая композиция демонстрирует объемное расширение во время сополимеризации при нагревании. Способ получения поли(бензоксазин)-сополи(циклического карбонатного) продукта полимеризации включает стадию нагревания расширяемой полимеризуемой композиции до температуры, достаточной для инициирования сополимеризации. Способ получения поли(бензоксазин)-сополи(циклического карбонатного) продукта полимеризации включает стадию нагревания расширяемой полимеризуемой композиции, содержащей по меньшей мере один бензоксазин и по меньшей мере один циклический карбонат, до температуры, достаточной для инициирования сополимеризации. Предварительно отвержденная расширяемая полимеризуемая композиция, применяемая для получения поли(бензоксазин)-сополи(циклического карбонатного) продукта полимеризации получена путем сшивания сшиваемых бензоксазинов, содержащихся в расширяемой полимеризуемой композиции. Предварительно отвержденная расширяемая полимеризуемая композиция применяется в качестве расширяемого наполнительного элемента для заполнения пространств в устройствах, где указанная предварительно отвержденная расширяемая композиция имеет заранее определенную форму и где отвержденная расширяемая композиция демонстрирует объемное расширение во время сополимеризации при нагревании. Технический результат – получение новой расширяемой полимеризуемой композиции на основе бензоксазинов, демонстрирующей улучшенные свойства расширения, в частности демонстрирующей высокие, регулируемые и воспроизводимые степени расширения во время полимеризации. 10 н. и 24 з.п. ф-лы, 9 ил., 17 табл., 14 пр.
Формула




Комментарии