Электропреобразовательная ячейка - RU2186442C2
Код документа: RU2186442C2
Чертежи





Описание
Изобретение относится к области электрохимического преобразования с использованием, например, электрохимических ячеек.
Потребность в создании экологически чистых средств транспорта, выравнивания уровня нагрузки электрических установок, также как многих других электрохимических применений, способствовали проведению исследований новых электрохимических ячеек. Плотность энергии, стоимость, срок службы, эффективность перезарядки, надежность, воздействие на окружающую среду и ремонтопригодность могут служить некоторыми из факторов, которые нужно учитывать при создании аккумулятора, подходящего для практического использования во многих применениях.
Способность преобразовывать химическую энергию в электрическую и обратно хорошо известна почти два столетия. Однако некоторые области применения, такие как электрические транспортные средства, предъявляют требования плотности энергии, относящиеся к плотности энергии, экономичности и увеличению срока службы, которые трудно удовлетворить при производстве коммерчески практичных ячеек, которые удобны в эксплуатации и надежны. Например, высокая теоретическая плотность энергии (см. обсуждение этого термина ниже) может в некоторых случаях быть связана с увеличением веса компонентов, тем самым снижая теоретические преимущества.
Автором было установлено, что с использованием группы окислительно-восстановительных соединений бора может быть создана электрохимическая ячейка со сбалансированными характеристиками, такими как располагаемая энергия, плотность энергии, капитальные и эксплуатационные затраты, эффективность перезарядки, надежность, воздействие на окружающую среду, ремонтопригодность и долговечность.
Соответственно в одном из аспектов изобретение в основном относится к электрохимической накопительной среде, которая содержит носитель, смешанный с восстановленным борсодержащим составом (предпочтительно бороводородом), причем восстановленное соединение является окисляемым до окисленного борсодержащего соединения (предпочтительно бората или полиборатов в неводных системах с использованием галогенсодержащего восстановителя, может быть получен трихлорид бора) одновременно с генерированием электрического тока, когда накопительная среда находится в электрическом контакте с электродом, который проводит ток, генерируемый при окислении. Носителем может быть водный или неводный раствор, например жидкость, которая растворяет восстановленное соединение и вступает в контакт с электродом так, чтобы восстановленное борсодержащее соединение могло доставлять электроны на электрод непосредственно, а не косвенно через стабильный промежуточный компонент, такой как водород. Предпочтительные неводные жидкости включают безводный аммиак, диметилформамид, диметилсульфоксид, амины, неаминовые органические основания, спирты, алкен карбонаты и гликоли; конкретные жидкости включают трипропиламин, пиридин, хинолин, триэтаноламин, моноэтаноламин, этиленгликоль, пропиленгликоль, метанол, этиловый спирт, карбонат этилена и карбонат пропилена. Неводный раствор может включать сжижающий агент или агент, усиливающий проводимость, например этилендиаминтетрауксусную кислоту, крон-эфиры, криптаты и четвертичные соли аммония.
В другом аспекте изобретения накопительную среду размещают в качестве анода аккумулятора, который включает анод и катод, имеющие возможность электрической связи. Восстановленное соединение имеет возможность окисления до окисленного борсодержащего соединения одновременно с разрядом аккумулятора, например, когда восстановленное соединение вступает в контакт с электродом и доставляет к нему электроны. Окислителем может быть доступный воздух, или аккумулятор может включать окислитель, например О2; соединения, которые содержат кислород и галоген; и Х2, где Х - галоген. Предпочтительными окислителями являются: перхлорат (ClO4-), хлорат (СlO3-), хлорит (СlO2-), гипохлорит (ОСl-), хлор (С12), бром (Вr2), бромат (ВrО3-), иодат (IO3-) или другие сопоставимые соединения галоген/кислород. Другими предпочтительными окислителями являются те, которые содержат элементы, которые могут легко переходить между двумя или больше состояниями окисления, в общем случае начиная с более высокого состояния. Эти соединения могут быть или растворимыми или нерастворимыми в среде носителя, и их можно использовать в виде раствора, суспензии, пасты, геля или любой другой желательной формы. Предпочтительные окислители включают: a) [Mn(VII)O4]- (например, перманганат натрия); b) [Fe(VI)O4]-2 (например, натрий феррат); с) Се(IV)ОН(NО3)3 (основной нитрат церия); d) [Се(IV)(NО3)6]-2 (например, нитрат церия аммония); е) [Fe(III)(CN)4]-3 (феррицианид); f) [Cr(VI)O4]-2 (хромат); g) [Sn(IV)О3]-2 (станнат); h) [Вi(V)О3]- (висмутат); i) Mn(IV)O2; j) Аg(I)2O; k) Аg(II)O; 1) Ce(IV)O2; m) Pb(IV)O2; n) Ni(III)О(ОН); о) Ni(IV)O2; p) Co(III)O(OH); q) [N(V)О3]- (например, нитрат аммония, нитрат натрия, нитрат лития, нитрат кальция); r) [NO2]- (например, нитрит натрия); s) [S2O8]-2 (например, пероксидисульфат натрия или аммония); соединения, которые содержат Cu(III), Tl(III), Hg(II), Se(VI) или Te(VI); или u) R(NO2)n-, где R - алкиловая, ариловая или арилалкиловая органическая группа и n=1-6 (например, моно- или поли-, или пернитроорганические соединения). Валентности приведены для характеристики понимания характера окислителей, но необязательно как ограничение формулы изобретения. Другими окислителями являются тринитробензойная кислота, гексанитробензол или тринитробензол.
Анолит и католит аккумулятора можно разделять мембраной с избирательной проницаемостью, такой как анионная мембрана, катионная мембрана или биполярная мембрана. Катод может представлять собой катод с чередующимся поглощением и выделением воздуха, например, с католитом, который может окисляться воздухом (например, в основном растворе), чтобы выработать агент, который затем окисляет бороводород до бората с генерированием электрического тока, предпочтительно в цикле, который включает регенерацию католита после того, как он генерировал электричество при окислении бороводорода, и таким образом допускать многократное использование. Например, католит может содержать иодат (IO3); феррицианид и ферроцианид; хромат и Сr+3; марганец с валентностями +2 и +3; олово с валентностями +2 и +4; кобальт с валентностями +2 и +3; катализатор, чтобы помочь переокислению окислителя воздухом до более высокого состояния окисления.
Аккумулятор может включать отдельную от катодного отсека камеру, в которой происходит переокисление католита. Аккумулятор может включать две части, одна из которых осуществляет чередующиеся поглощения и выделение воздуха, а другая часть содержит католит, который может окисляться воздухом и который может затем окислять бороводо-род до бората с генерированием электрического тока с использованием косвенно воздуха. Аккумулятор может также включать биполярный электрод. Он может иметь внешние резервуары для хранения анолита, католита или и анолита и католита. Ячейка для генерирования электричества путем окисления бороводорода может быть физически отделена от ячейки для получения бороводорода из бората или она может быть той же самой ячейкой, которая используется для получения бороводорода из боратов. По меньшей мере, с одним источником реагента может быть соединен контроллер, чтобы регулировать перенос реагента к аноду или катоду, и контрольное устройство, которое определяет характеристику аккумулятора и подает сигнал на контроллер в соответствии с контролируемыми значениями характеристики. Например, по меньшей мере один датчик реагирует на характеристику, которую выбирают из ORP, проводимости, напряжения, тока и выходной мощности, ионной концентрации, рН, показателя преломления, колориметрической, COD, мутности, плотности, чтобы генерировать входной сигнал. Входной сигнал передается на электронный процессор, процессор соединяется с контроллером, который управляет потоком в аккумуляторный отсек.
Электрод аккумулятора может включать проводящую подложку, такую как нержавеющая сталь с покрытием. Электроды, которые являются особенно полезными (например, чтобы избежать выделения водорода) включают: а) сплав висмута, таллия, кадмия, олова, галлия, свинца или индия; b) ртуть или ртуть, амальгамированную с другими металлами, или ртутное покрытие на проводящей подложке; с) теллур или теллуриды. Электрод может включать дополнительные материалы, чтобы улучшить коррозионную стойкость или другие свойства электрода. Возможен биполярный электрод, который имеет две стороны, причем одна из сторон покрыта указанным веществом, а вторая сторона покрыта материалом с низким кислородным перенапряжением, таким как золото или окись иридия; в качестве альтернативы вторая сторона представляет собой стандартный электрод с чередующимся поглощением и выделением воздуха. Биполярный электрод содержит лист из проводящего материала, такого как нержавеющая сталь или медь, покрытая золотом, или другой подходящий металл. Электрод может иметь гладкую поверхность или развитую поверхность большой площади пенометалла или трубок, цилиндров, волокон или другой геометрической формы, порошка с покрытием или без покрытия, катализированную или некатализированную.
Такие аккумуляторы, как описано выше, могут быть выполнены в виде герметичной ячейки определенного физического размера, формы и диапазона напряжения, в соответствии с требованиями относительно формы и функционирования, соответствующими стандартному аккумулятору для потребительского электронного или электрического прибора, например пуговичному аккумулятору для слухового аппарата; ААА; АА; А; В; С; D; 9-вольтовому аккумулятору; компьютерному аккумулятору; аккумулятору сотового телефона. Аккумулятор отличается тем, что вырабатывает напряжение и ток, подходящие для зажигания и работы стартера в транспортном средстве, приводимом в движение двигателем внутреннего сгорания, или он может подходить для установки на транспортном средстве, которое частично или полностью использует электричество для приведения в движение это транспортное средство. Аккумулятор может также быть пригоден для накопления электричества в таких применениях, как выравнивание уровня нагрузки электрического оборудования и других средств накопления электричества. Этот аспект изобретения также демонстрирует возможность генерировать ток через какое-то время при соединении аккумулятора с нагрузкой. В этом случае ток генерируется посредством окисления восстановленного борсодержащего соединения. Аккумулятор может также перезаряжаться, для чего прикладывают электрический потенциал к аноду, чтобы восстановить анион бороводорода из аниона бората. В качестве альтернативы, разрядившийся раствор анолита можно заменить на анолит, который содержит анион бороводорода, пригодный для окисления до аниона бората.
Другой аспект изобретения демонстрирует синтез иона борана (предпочтительно бороводорода) посредством электрического восстановления иона бората, например, как способ перезарядки аккумулятора. Синтез может контролироваться с помощью датчика, который генерирует электрический сигнал, представляющий характеристику, выбираемую из ORP, проводимости, напряжения, тока и мощности на входе, ионной концентрации, рН, показателя преломления, колориметрической, COD, мутности и плотности, указанный сигнал передается к электронному процессору. Процессор соединяется с контроллером, который управляет потоком в аккумуляторный отсек, который соединяется с регулируемым потоком в каждый отсек, например, посредством насосов, клапанов и других подходящих средств передачи. Обычно борат и ион бороводорода находятся в водном носителе. Катод ячейки может представлять собой электрод с высоким водородным перенапряжением, причем восстановление ионов бората выполняется путем подачи потенциала на электрод, который может состоять из сплава висмута, таллия, кадмия, олова, свинца, галлия и индия. В качестве альтернативы, электрод для подачи потенциала может состоять из ртути или ртути, амальгамированной с другими металлами, или ртутного покрытия на проводящей подложке. Электрод может также содержать теллур или теллуриды. Такие электроды замедляют выделение газообразного водорода при протекании тока. Можно добавлять электродные добавки для улучшения таких характеристик, как коррозионная стойкость. Можно образовывать другие сильно восстановленные соединения (в дополнение к бороводороду). В числе борсодержащих соединений находятся несколько высших боранов В2 Н7-, В3Н8-. Эти бораны могут связываться с амином или с азотным/водородным составом, таким как аммиак или гидразин, например, для получения ВН3•NН3 или ВН3•N2Н4. Можно также образовывать неборсодержащие материалы, которые представляют интерес, например соединения, которые содержат металлы или соединения водных и/или неводных систем. Как прежде, в этом способе можно использовать биполярный электрод; можно также использовать мембрану с избирательной проницаемостью, например анионную мембрану, катионную мембрану с избирательной проницаемостью, например анионную мембрану, катионную мембрану или биполярную мембрану. Кислород может выделяться из анода при образовании бороводорода в католите. Окисленные соединения могут образовываться в качестве продукта в анодной камере. Небороводородные бораны могут образовываться посредством добавления к католиту аддуктов частичного восстановления или других аддуктов, таких как ион цианистого калия, амидные ионы, галогенные ионы и псевдогалоидные соединения.
Еще в одном аспекте изобретение в основном представляет перенос аниона бороводорода от точки порождения до точки потребления посредством приложения электрического потенциала к раствору окисленного бороводорода в точке порождения, чтобы произвести бороводород в первой ячейке и перенос раствора бороводорода в точку потребления, куда бороводород подают для окисления во второй ячейке. Отработанный раствор, который содержит окисленный бороводород, может также транспортироваться от точки потребления до места порождения и прикладывать электрический потенциал к отработанному раствору в точке порождения для образования бороводорода в первой ячейке. Возникающий в результате бороводород можно использовать как описано выше. В качестве альтернативы его можно соединять с водой, чтобы генерировать водород посредством восстановления воды, например, катализируемой присутствием соединений переходных металлов, таких как соединения кобальта (II) (например, гидроксид кобальта (II)). Водород может собираться и транспортироваться к точке потребления водорода, например, промышленному потребителю водорода. Раствор окисленного бороводорода можно транспортировать обратно к точке порождения, чтобы снова использовать для получения бороводорода.
Эту систему можно использовать с ячейками, которые выполняются в соответствии с требованиями установки на транспортном средстве, в котором частично или полностью используется электричество для приведения в движение транспортного средства. Их также можно использовать для накопления электричества в таких применениях, как выравнивание уровня полезной нагрузки электрических установок общего пользования и других средств накопления электричества. Короче говоря, этот аспект характеризует собой систему транспортировки бороводорода как способ передачи энергии к заданному местоположению, например систему транспортировки и распределения бороводорода, такую, что средства передвижения, которые работают на бороводороде, можно заправлять свежим бороводородом и сливать бораты. Раствор бората преобразуют в раствор бороводорода с помощью ячейки для синтеза бороводорода, для перезарядки аккумулятора, посредством электрического восстановления иона бората.
Система с выгодой использует очень высокую энергию пар электродов на основе использования бороводородов у анода. Кроме того, система является универсальной, потому что реагенты можно использовать в самых разнообразных химических условиях для вторичных и для первичных источников тока. Термин "вторичные" связан со способностью к перезарядке ячейки, а "первичный" связан с системой, в которой первоначальные реагенты используют только однократно и не восстанавливаются реакцией зарядки. Другой особенностью, которая обеспечивает эксплуатационную гибкость, является растворимость реагентов в воде или других растворителях, которая допускает конфигурации, в которых реагенты прокачиваются через ячейку или сохраняются неподвижными в пасте или геле, или растворе.
Реагенты можно варьировать, включая широкое множество окислителей для катода аккумулятора, в том числе кислород, который можно получать из окружающего воздуха. Эта гибкость допускает много конфигураций, характеризуемых продолжительным сроком службы при малой мощности до высокой мощности при продолжительном сроке службы, как это необходимо. Способность сохранять жидкое топливо вне ячейки является ключевой для обеспечения системы с большим диапазоном, в которой площадь электрода не зависит от общей сохраненной энергии, например, в таких применениях, как выравнивание уровня нагрузки электростанций и автомобильный транспорт. Израсходованную жидкость можно быстро поменять на новую жидкость вместо того, чтобы реально перезаряжать систему с использованием электричества.
Термин "электропреобразовательная ячейка" включает в себя понятие, относящееся к преобразованию или электричества в химический продукт, или химического продукта в электричество, а также к работе в качестве первичного источника тока, вторичного источника тока, топливной ячейки или ячейки синтеза или любой комбинации вышеупомянутых ячеек.
Ячейка относится к любой электрохимической системе, которая производит или потребляет электричество и/или производит и потребляет химические продукты. Аккумулятор относится к любой комбинации ячеек, которую используют для выработки электричества. Первичный источник тока относится к ячейке, спроектированной для выработки электричества, причем без возможности перезаряда. Вторичный источник - это ячейка, которая может вырабатывать электричество и может перезаряжаться. Топливная ячейка - это ячейка, которая генерирует электричество посредством потребления "топлив", таких как водород, гидразин или метанол с кислородом, и обычно производит электричество, пока подают топлива, но не реверсирует свою функцию для перезарядки или выработки материалов, которые она использовала. Как отмечено, понятие "электропреобразовательная ячейка" относится к ячейкам, определенным ниже, которые имеют возможность функционирования в одном или больше из нескольких режимов.
В нижеследующих уравнениях, ссылки на напряжение (Е0 или Е1/2) подразумевают нормальные условия и предусмотрены только для вычислений. Ячейки, которые эксплуатируют при условиях (включая концентрации, температуры и давления), которые отличаются от стандартных, показывают различные напряжения. Ничто связанное с указанным напряжением не следует рассматривать как ограничение широкого разнообразия комбинаций ячеек и аккумуляторов, предусматриваемого электропреобразовательной ячейкой, и не подразумевает фактического достижения указанного напряжения. Е0 относится к напряжению полной реакции, а Е1/2 относится к половинной реакции, которая происходит в одной части ячейки, в то время как другая половинная реакция также должна происходить в ячейке.
Понятие "электрод" является очень широким термином и относится к проводящему материалу, который проводит электроны в ячейку или из нее. И аноды, и катоды являются электродами. Биполярные электроды (одна сторона которых является анодом, а противоположная сторона является катодом в смежной ячейке) являются электродами. Электроды могут быть твердыми или жидкими. Электроды с чередующимся поглощением и выделением воздуха также должны взаимодействовать с газом. В последние годы используются самые разнообразные электроды. Электроды могут быть простыми, как лист стали, или могут представлять собой "пенометалл" или коллоид или порошок. Электроды могут быть практически любой формы, включая листы (пластины), трубки, цилиндр, кубы, сферы или любой иной формы, которую можно разработать для данной цели. Они могут иметь такие характеристики, как пористые, не имеющие пор, проточные, продувочные и так далее. В то время как любые типы электродов используют в электропреобразовательных ячейках, чтобы получить желательный результат, ни один из них специально не требуется, чтобы использовать электрохимический процесс так, как показано в данном изобретении. Следовательно, при любом упоминании электродов любую конфигурацию электродов, которая используется в реальном аккумуляторе или ячейке на основе химических преобразований, описываемых в настоящем изобретении, следует рассматривать как пример осуществления данного изобретения.
Когда ячейка работает на разрядку и таким образом вырабатывает электричество, электрод, который взаимодействует с "топливом", которое окисляется, называется анодом. Жидкость в этой камере называют анолитом. Другая половина ячейки имеет электрод, называемый катодом, и раствор в этой камере называют католитом. В ячейке без барьера для поддержки различных химических процессов (свинцово-кислотный аккумулятор) анолит и католит представляют собой одно и то же (в свинцово-кислотном аккумуляторе это серная кислота) и их часто просто называют электролитом. В любом случае термин электролит, который используется здесь, относится к любой проводящей жидкости или суспензии в любой функции.
Когда аккумулятор перезаряжается, электричество вводится в ячейки. При этих условиях функции компонентов являются обратными, и анод теперь становится катодом и наоборот.
При альтернативной терминологии анод разражающейся ячейки определяется как отрицательный электрод. Электроны вытекают из этой стороны аккумулятора и проходят через нагрузку к положительной стороне аккумулятора. Во время перезарядки электроны текут к отрицательному электроду, и это обозначение не изменяется в зависимости от того, заряжается ли аккумулятор или разряжается.
Для энергии используют единицу ватт-час (Вт•ч) или киловатт-час (кВт•ч), или килоджоуль (кДж). Для мощности используют единицу ватт (Вт) или киловатт (кВт). Плотность энергии относится к количеству энергии, получаемой из определенного объема ячейки или материала, выраженному, например, как ватт-часы на литр (Вт•ч/л) или в киловаттах на литр (кВт/л). Удельная энергия относится к энергии, получаемой из определенной массы ячейки или материала, выраженной как ватт-часы на килограмм (Вт•ч/кг) или киловатты на килограмм (кВт/кг). Плотность энергии и удельная энергия связаны между собой через плотность материала или системы. Удельная мощность относится к количеству мощности, получаемой на единицу веса, обычно в Вт/кг. Разбрызгиватель представляет собой устройство, которое облегчает контакт между газом и жидкостью, например устройство с мелкими порами, которое разбивает поток газа в очень мелкие пузыри, чтобы получить очень высокую площадь поверхности раздела с жидкостью.
Изобретатель использует единицу его собственного определения: Вольт-Фарадей (В-Ф). Эта единица В-Ф получается путем умножения напряжения реакции на число электронов, которые участвуют в реакции. Это представляет собой быстрый способ определения доступных энергий для аккумуляторов. Таким образом, 37,31 В-Ф равняется одному киловатт-часу (1000 ватт-часов); один В-Ф равняется 26,8 ватт-часам.
Во многих примерах изобретатель вычисляет теоретическую плотность энергии или теоретическую удельную энергию. Их используют для целей сравнения, и не следует рассматривать их как достижимые в любой реальной системе аккумулятора. Не следует также рассматривать любое такое число, как требование к какому-либо примеру осуществления электропреобразовательной ячейки. При теоретических вычислениях не принимаются во внимание никакие контейнеры, электроды, насосы или любые вспомогательные механизмы, которые могут потребоваться для изготовления реальной ячейки. Такие вычисления полезны для прогнозирования того, обеспечит ли конкретный химический процесс теоретическую возможность достижения некоторой цели.
Другие примеры осуществления будут очевидны для специалистов из нижеследующего описания предпочтительных примеров осуществления и из формулы изобретения.
Фиг. 1-8 (то есть фиг.8А-8Г) представляют собой схемы электрохимических ячеек.
Ключевая половинная реакция, которая определяет топливную сторону (анод или отрицательный электрод) ячейки, основана на ионах бороводорода. Реакция
представляет собой
BH4- + 8OH--->BO2- + 6H2O + 8e-, E1/2=1,24 B. (1)
Уравнение (1) выше написано для водной системы, но неограничено такой системой. Один пример осуществления электропреобразовательной ячейки использует электрод с чередующимся поглощением и выделением
воздуха, чтобы обеспечить реакцию другой половины ячейки, обеспечивающей получение полной ячейки. Эта реакция имеет вид:
2O2 + 4H2O + 8e--->8OH-, E1/2=0,401 B. (2)
Результирующую реакцию для уравнений (1) и (2) находят посредством сложения двух реакций, чтобы получить
BH4- +
2O2--->BO2- + 2H2O, E1/2=1,641 B. (3)
Ион бороводорода стабилизируют ионами гидроксида. Раствор может
выделять газообразный водород, если его катализируют или подкисляют. Следовательно, в приложениях аккумуляторов следует избегать состояний с выделением газа. Выделение газообразного водорода
нежелательно, потому что это может в некоторых обстоятельствах понижать получаемую энергию и быть причиной ряда других нежелательных характеристик такой ячейки, как здесь описано. Следовательно,
материалы, которые должны быть в контакте с раствором бороводородистого натрия, следует выбирать так, чтобы избежать реакций с выделением газа. Другими факторами, которые нужно учитывать, являются рН
и присутствие материала, который может катализировать разложение бороводорода. Присутствие иона, ионов, например, гидроксида (высокое значение рН) является желательным, и экзогенные ионы гидроксида
(такие, как гидроксид натрия) будут обычно добавлять в таких переменных количествах, как это необходимо для устойчивой системы и желательных проводимостей для любого данного применения. Другие
материалы можно добавлять, чтобы усилить проводимость или другие свойства ячейки.
Свободная энергия Гиббса, упоминаемая как "дельта G" для уравнения (3), составляет 1270 кДж/моль реагентов. Кислород получают из воздуха, и молекулярный вес бороводородистого натрия равен 37,83 г на моль (можно использовать любую бороводородную соль, такую как соль лития или аммония и т.д., как источник бороводорода с соответствующими поправками на характер каждого материала). Следовательно, энергия, доступная из одного фунта бороводородистого натрия, составляет 15200 кДж/фунт или 33500 кДж/кг. Бороводородистый натрий растворим в воде до приблизительно 44% весовых, и, следовательно, насыщенный раствор этой соли содержал бы 14700 кДж/кг или, так как плотность этого раствора равна 1,25 г/мл, энергия, доступная из раствора, должна быть равна 18400 кДж/л. Чтобы преобразовывать эти выражения тепловой энергии в электрические выражения, один киловатт-час равняется 3600 кДж, так что более чем 5,11 кВт•ч на литр должно быть доступно при кпд 100% (в единицах, которые использует Консорциум Перспективных Аккумуляторов: 5110 ватт-часов/литр). При более высоких температурах возможны большие растворимости бороводородов, и должны быть доступны даже более высокие энергии. В безводном аммиаке растворимость выше, и должны быть доступны даже более высокие запасенные энергии, если это необходимо.
В качестве более быстрого способа расчета изобретатель использует введенную им единицу Вольт-Фарадей, в дальнейшем В-Ф, которая определяется путем умножения напряжения ячейки на число электронов в реакции. Этот способ допускает быструю сортировку по доступным энергиям различных пар. Один киловатт-час равняется 37, 31 В-Ф. В качестве иллюстрации вышеупомянутая система в уравнении (3) дала бы 1,641 В•8=13,128 В-Ф на моль реагентов. Это равняется 347,0 В-Ф/кг или для раствора 44% с плотностью 1,25 равняется 190,9 В-Ф/л или 5,11 кВт•ч/л, так же, как рассчитано выше.
В качестве энергетического сравнения, теоретическая энергия, получаемая от литра бензина, составляет приблизительно 33000 кДж. Литр раствора бороводорода содержит приблизительно 56% теоретической энергии, получаемой от галлона бензина. Если принять, что электрохимическая ячейка и электродвигатель могут преобразовывать энергию в механическое движение при кпд в 2, 5-3 раза больше кпд двигателя внутреннего сгорания, то дальность и мощность того же самого порядка, которые доступны в стандартных автомобилях, будут обеспечены для автомобиля, который оборудуют такой основанной на бороводороде ячейкой, как описано здесь.
При энергетических плотностях, доступных для растворов бороводорода, электрическое устройство теоретически может запасать один
гигаватт-час (109 ватт-часов) электричества в резервуаре емкостью 473,1765 м3. Электрический автомобиль нормального веса, в котором используют кондиционирование воздуха,
теоретически может пройти более чем 482,8 км с резервуаром емкостью 113,5 или 132,5 литров. Данный прогноз дает благоприятный результат сравнения со стандартными свинцово-кислотными аккумуляторами,
основанными на реакции
Pb+PbO2+2H2SO4-->2PbSO4+2H2O, E0=2,0 B, (4)
которая дает 4 В-Ф (это 2-электронная
реакция) для 642 г реагентов (не учитывая требуемую воду) или 6,23 В-Ф на килограмм или только 167 Вт•ч/кг. Исключительно на основе теоретической химии, бороводородная система может
обеспечивать значительно больше энергии, чем свинцово-кислотная система.
В качестве еще одной точки сравнения, современной промежуточной задачей для разработки перспективного аккумулятора, установленной Консорциумом Перспективных Аккумуляторов США (USABC), является достижение плотности энергии между 100 Вт• ч/л и 135 Вт•ч/л и удельной энергии между 80 и 100 Вт•ч/кг. Долгосрочной задачей для аккумулятора, который используют в электрическом транспортном средстве, должно быть достижение 200 Вт•ч/кг.
Одно из преимуществ использования жидкого топлива (анода) и электролита состоит в том, что можно удалить твердые реагенты, которые обычно имеют форму пластин. Так как электроды должны представлять собой только коллекторы электронов, можно получить относительно простую и прочную конструкцию. Более высокие напряжения можно получить посредством последовательного соединения необходимого числа ячеек; в качестве альтернативы, другой способ достижения последовательного соединения состоит в том, чтобы использовать то, что известно, как биполярные электроды. В некоторых примерах осуществления электропреобразовательной ячейки биполярные электроды могут представлять собой простые листы соответствующего проводника. В других аккумуляторах, где электрод является также топливом, обычно получают более сложную конструкцию.
Дополнительно площадь электрода можно определить таким образом, чтобы получить необходимую для данного применения мощность. Если для данного применения требуется дополнительная энергия, можно увеличивать размер хранилища для источника бороводорода вместо того, чтобы увеличивать площадь электрода. В перезаряжаемой ячейке, которая использует раствор бороводорода, можно использовать внешний резервуар хранения подходящего размера, чтобы обеспечить желательные требования к результирующему накоплению энергии. Эта характерная черта особенно полезна для выравнивания уровня нагрузки электрооборудования общего пользования, электрических автомобилей и аварийных применений электричества, таких как освещение или источники бесперебойного питания (ИБП), которые используют в компьютерной промышленности, если назвать только некоторые из них. В ячейке, где бороводород представляет собой пасту или гель или вообще не является текучим, такой как ячейке для таких применений, как источники питания компьютеров, для игрушек, сотовых телефонов и т. д. , размер камеры можно увеличить, чтобы хранить большее количество бороводорода и тем самым увеличить запасенную энергию.
Все чертежи являются концептуальными, представлены не в масштабе и предназначены только для иллюстративных целей.
На фиг.1 показана основная ячейка без движущихся частей и с электродом с чередующимся поглощением и выделением воздуха. В основном можно использовать известные электроды с чередующимся поглощением и выделением воздуха или электроды, которые будут разработаны в будущем, если они химически совместимы с выбранной системой электролита. Как можно заметить, две половинные реакции одновременно происходят в соответствующих камерах, которые разделяют ионообменной мембраной с избирательной проницаемостью. Известны коммерчески доступные мембраны, которые позволяют проходить сквозь них некоторым типам ионов, помещаемые между отсеками катода и анода. В конфигурации с чередующимся поглощением и выделением воздуха ионоселективная мембрана необходима, чтобы предотвратить саморазряд ячейки, как это происходит со многими электродами с чередующимся поглощением и выделением воздуха, которые должны иметь большую площадь поверхности и катализаторы, чтобы поддерживать реакции с достаточно высокими скоростями, чтобы обеспечить приемлемые токи. Коммерчески доступные мембраны являются подходящими для использования в электропреобразовательной ячейке. По существу мембрана может быть или катионной, допуская только перенос катионов (натрий, Na+ в данном случае). Или они могут быть анионными, которые допускают перенос иона гидроксида, но не бороводорода. Биполярные мембраны также можно использовать в соответствующей конструкции, если это необходимо. Перенос иона бората (продукта разрядки) можно допустить в неперезаряжаемой системе или перезаряжаемой системе, которая способна извлекать борат из обоих жидкостных резервуаров. Ячейка функционирует с любым типом мембраны, и конкретное применение определяет соответствующие подходящие мембраны. В некоторых случаях можно обходиться без мембраны, если бороводород по существу не растворяют, но взвешивают в среде, которая предотвращает перенос бороводорода к катоду с чередующимся поглощением и выделением воздуха. В данном примере осуществления бороводородную "пасту" или "гель" изготавливают путем взвешивания порошка в материале, который дает низкую растворимость бороводорода. Можно также добавлять проводящий состав, чтобы повысить общую проводимость. Эти ячейки можно изготовить так, чтобы создать аккумуляторы почти любого размера и емкости для данного применения. Их можно перезаряжать при использовании соответствующих электродов, как определено далее в данном описании.
На фиг.2 изображен тот же тип ячейки, как на фиг.1, но вместо использования электрода с чередующимся поглощением и выделением воздуха в ячейке запасают окислитель. Эта конфигурация значительно понижает теоретическую удельную энергию, но все еще дает подходящие удельные энергии. Пример осуществления на фиг.2 можно использовать там, где требуется герметичная ячейка или нет доступного воздуха. Большая часть первичных источников тока, которые изготавливают в настоящее время и которые включают типы С или D, или АА, или ААА, или аккумуляторы пуговичного типа для слуховых аппаратов (среди многих других), относится к этой категории. При правильном конструировании эти ячейки можно выполнить с возможностью перезаряда. Электропреобразовательная ячейка может работать как нормальный первичный источник тока или как первичный источник тока с прокачиванием бороводорода через анод и прокачиванием окисляющего раствора через катод.
Вообще окислитель, который используют в катодном отсеке, будет содержать кислород в форме, обеспечивающей реакцию с бороводородом согласно уравнению (1), для получения боратов и электричества. Результирующее напряжение зависит от выбора окислителя.
Например, в водной системе сильно растворимым источником кислорода является хлорат или перхлорат
натрия. В преимущественно основных условиях ячейки половинная реакция имеет вид (для хлората)
ClO3- + 3H2O + 6e--->Cl- +
6OH-, E1/2=0,62 B. (5)
Если 4 части уравнения (5) добавляют к 3 частям уравнения (1), получают следующее результирующее уравнение
3BH4- + 4ClO3--->3BO2- + 4Cl- + 6H2O, E0=1,86 B. (6)
Доступная энергия равна 1,86•
24= 44,64 В-Ф на три моля бороводорода и четыре моля хлората. Если принять, что используют соль натрия, то полная масса этого количества равна 539,25 г. Это равняется 82,78 В-Ф/кг, что равняется 2,22
кВт•ч/кг. При 40% концентрации и плотности 1,25 плотность энергии приближается к 1,1 кВт•ч/л, что в основном пригодно для современных герметичных аккумуляторов.
Нет
необходимости, чтобы окислитель доставлял кислород. Можно применять другие химические процессы. В основных водных системах бораты будут доминировать в продуктах. Так что даже если в качестве
окислителя используют галоид, такой как хлор, результирующая реакция представляет собой
BH4- + 4Cl2 + 8OH--->BO2- + 8Cl- + 6H2. (7)
Фиг.3 показывает поток через конфигурацию бороводородной системы с электродом с чередующимся поглощением и выделением воздуха.
Дополнительные окислители, которые подходят для конфигурации типа первичного источника тока, проточного или нет, включают следующие соединения или их растворы: галогеноокиси, такие как соли хлоратов, перхлорат, броматы, иодаты, гипохлораты и т.д. Типичными соединениями являются соли, такие как перхлорат лития или раствор гипохлорита натрия. Хотя перхлорат аммония проявляет низкую растворимость в воде, он вполне растворим в безводном аммиаке.
Ионы переходных металлов в высших состояниях окисления
Перманганаты и манганаты. Можно использовать Mn(VI),
Mn(VII) или Mn(IV) (такие, как двуокись марганца), ферраты (Fe(VI) или Fe(III)) или хроматы (Cr(VI)), окиси никеля (Ni(III)), олово (Sn(IV)), окиси серебра и т.д. Необходимо действовать с
осторожностью, чтобы гарантировать, что выбранный материал не катализирует разложение бороводорода как в уравнении (15), или гарантировать, что не допускается прямой контакт между материалом и
бороводородом, если каталитическое действие возможно. Типичные соединения включают перманганат натрия, феррат натрия, феррицианид калия, хромат натрия, станнат натрия и т.д.
Галогены или межгалоидные соединения. Эти материалы при растворении в водном основании образуют соли галогеноокиси.
Соли нитратов и нитритов, такие как нитрат аммония или нитрит натрия. Эти соединения хорошо растворимы в воде и исключительно растворимы в безводном аммиаке.
Нитроорганические соединения; нитробензойная или динитро- или тринитробензойная кислоты проявляют хорошую растворимость в растворах гидроксида, и они образуют соответствующий амин и спирт (то есть нитробензойная кислота образует аминофенол).
Пероксидисулъфаты. Можно использовать пероксидисульфаты, такие как пероксидисульфат аммония или натрия. Так как этот анион не переносит кислород, но только принимает электроны, кислород для образования боратов поступает из гидроксида, который необходимо также сделать доступным для реакции. По причине неустойчивости пероксидов в основном растворе это рекомендуют для необычных применений.
Напряжение для ячеек, которые используют материалы из вышеупомянутого списка или другие материалы, может варьироваться в широких пределах. При использовании таких соединений, как ферраты или пероксидисульфаты, или галогеноокиси, результирующее напряжение на зажимах ячейки может превышать 3 В. Такие системы помогают поддерживать высокие плотности энергии. Некоторые из таких систем подходят также для вторичных ячеек, где восстановленное вещество можно повторно окислять электролитическим способом. Как правило, в такой вторичной ячейке можно повторно окислять галогеноокиси, ионы переходных металлов, пероксидисульфаты и некоторые органонитраты.
На фиг. 3 раствор в резервуаре 1 прокачивают через ячейку 2 и сливают в резервуар 3, в то время как электричество выводят из ячейки 2. Скорость нагнетания можно изменять, чтобы учитывать изменяющиеся требования к ячейке и таким образом обеспечивать широкий диапазон уровней мощности для заданной площади электрода в ячейке. Резервуар 4 и насос 5 устанавливают на стороне катода аккумулятора, и они согласуют потоки, чтобы поддерживать достаточную концентрацию ионов вблизи электродов, чтобы поддерживать выходную мощность. Расход может дополнительно управляться компьютером (микросхемой). Данные от датчиков через устройства ввода-вывода, которые контролируют такие условия, как ORP или проводимость или другие параметры, могут представлять собой входные данные, которые определяют результирующий поток.
В этой конфигурации, также как во многих других становится очевидной обеспечиваемая гибкость. Она имеет свойства как аккумулятора, так и топливного элемента. Это очень важно для таких применений, как выравнивание уровня нагрузки электрооборудования или электрические транспортные средства, для которых может потребоваться совершать дальние поездки без перезарядок. Но возможность перезарядки при необходимости сохранена. В типичном топливном элементе продуктами обычно являются вода и (иногда в зависимости от топлива) диоксид углерода или азот. В топливном элементе их по существу следует рассматривать как электрохимические продукты сгорания, и продукты не имеют никакой ценности для регенерации первоначальных реагентов. В электропреобразовательной ячейке продукт разряда является пригодным для извлечения бороводорода. Хотя воду можно повторно преобразовать обратно в водород и кислород для топливного элемента и бороводород характеризует собой метод сохранения газообразного водорода (как обсуждено позже в этом описании), фактически происходит реакция в соответствии с уравнением (1). Если бороводород катализировать, чтобы выделить его газообразный водород, то необходима ячейка, которая имеет анод, который может катализировать окисление водорода до воды. Теоретическое напряжение реакции в этом случае равно только 1,23 В, и теоретическая плотность энергии падает до приблизительно 3,8 кВт•ч/л. Боратный продукт все равно необходимо перезаряжать в отдельной ячейке при более высоком напряжении, и результирующий кпд цикла системы выделения полезного электричества падает по меньшей мере на 43% (1,23 В/1,65 В~ 75%, и так как 75% - максимальный кпд и зарядки и разрядки, то 75%•75%~ 57%: 100%-57%= 43%). Следовательно, понятно, что электропреобразовательная ячейка представляет собой не просто топливный элемент или его вариант, но действительно новый подход в электрохимической технологии.
Если используют катионную мембрану, необходимый ион гидроксида для анолита можно добавлять в форме гидроксида. Этот способ понижает полную удельную энергию. Однако некоторое количество гидроксида должно быть доступно, чтобы способствовать кинетике двух половинных реакций, даже если не происходит никакого результирующего потребления. Анионная или биполярная мембрана позволяет гидроксиду, который производится согласно уравнению (2), проходить и быть доступным для реакции (1). По мере разрядки ячейки масса электролитов растет благодаря впуску кислорода. Эту массу главным образом перемещают от катода к анодному отсеку. Ее можно также физически доставлять с помощью насоса или перелива из катодного отсека в анодный отсек. Если используют катионную или биполярную мембрану, то переносят ионы натрия из анодного отсека в катодный отсек, чтобы поддержать равновесие заряда во время разрядки. По этой причине резервуары для содержания отработанных растворов должны быть больше, чем резервуары хранения для свежих растворов, чтобы разместить дополнительную массу. Во время перезарядки реакции реверсируются. Отдельную ячейку для перезарядки предусматривают в качестве дополнительной возможности. Это позволяет оптимизировать электроды для различных химических функций, которые они выполняют во время разрядки и перезарядки. Дополнительно можно поддерживать такие условия, чтобы во время перезарядки происходил соответствующий массоперенос, так чтобы по многим циклам не было никакого результирующего перемещения гидроксида или воды. Однако благодаря открытому и гибкому характеру системы новое заполнение или простое добавление желательных компонентов устраняет любые нарушения баланса, которые могут иногда происходить.
В конфигурации по фиг.3, хотя ячейку можно перезаряжать с помощью электричества, ячейку можно также перезаряжать посредством опорожнения резервуара 2 через отверстие 9 и заполнения заново резервуара 1 через отверстие 8 свежим раствором бороводорода. Для электрического автомобиля это эквивалентно "заправке" в пути. Таким образом, благодаря этой особенности, вместо того, чтобы ограничиваться уровнем мощности перезарядки, который диктует доступная мощность, можно поменять жидкости. Отработанную жидкость можно затем перезаряжать во внешней ячейке, чтобы восстановить бороводород электрически. Этот раствор можно затем продавать другим автомобилистам. Станция по существу берет плату за электричество плюс прибыль, а не за бороводород сам по себе. Малогабаритное устройство регенерации можно также установить дома у владельца транспортного средства, где в любое время можно было бы осуществить один или два избыточных заряда бороводорода, если владелец не имел времени ожидать очередной перезарядки.
Следует отметить, что электрохимический синтез бороводорода из раствора бората представляет собой новый способ синтеза для производства бороводорода. Следовательно, любые ссылки на перезарядку ячейки также относятся к примеру осуществления изобретения, в котором ячейку эксплуатируют с целью производства бороводородов. Для повышения кпд такое регенерирование предпочтительно использует электрод с высоким водородным перенапряжением. Система со сниженными требованиями к проектированию показана на фиг.4 и 5, где ячейка перезарядки (5) представляет собой отдельную ячейку от ячейки заряжания. Следует отметить, что эта ячейка перезарядки эквивалентна ячейке для производства бороводородов. Следовательно, любые примеры осуществления, которые относятся к ячейке перезарядки, относятся также к ячейке электрохимического синтеза. Таким образом, электроды заряда и разряда необходимо оптимизировать для их соответствующих функций. В других отношениях на фиг.4 показана та же самая система, как и на фиг.3, с отдельной ячейкой для перезарядки.
На фиг. 5 показана ячейка, в которой вторичный электролит циркулирует мимо воздушного разбрызгивателя. Использование вторичного электролита позволяет избежать использования электрода с чередующимся поглощением и выделением воздуха, который должен действовать и как электрод, и как воздушный распылитель. Воздух разбрызгивают в электролит, и он окисляет соединение, которое затем направляется к катоду, где соединение восстанавливается. Восстановленное соединение затем возвращается в камеру разбрызгивания для повторного окисления и, таким образом, завершения цикла. В этом применении можно использовать любую электрохимическую пару, которую можно окислять воздухом и которая затем реагирует в катодной камере, чтобы обеспечить источник окисления для бороводорода. В этом способе, чтобы максимизировать напряжение ячейки, необходимо выбирать пару с потенциалом, по возможности близким к кислороду.
Пример последовательности реакций для конфигурации с
разбрызгиванием по фиг.5 представляет собой следующее:
I-
+6OH-->IO3-+3H2O+6e-, E1/2=0,26 B. (8)
Так как уравнение (8) имеет более низкий потенциал, чем уравнение (2) (потенциал
окисления кислорода в основном растворе), результирующая реакция, которая показана ниже, происходит в камере, где допустим воздух:
2I-+3O2-->2IO3-, E0=0,15 B. (9)
Этой реакции могут способствовать катализаторы, которые помещают в разбрызгиватель и/или непосредственно в камеру раствора. Катализаторы могут
быть гомогенными или гетерогенными, как желательно, чтобы максимизировать кпд системы. Способность воздуха окислять данное соединение определяют рН и концентрации так же, как катализаторы, температура
и давление. Следовательно, при надлежащих условиях некоторые пары могут быть окисляемыми, даже если стандартные потенциалы указывают на то, что это невозможно. Следует использовать электрохимические
процедуры и диаграммы, такие как диаграммы Пурбе или диаграммы площади преобладания. Следует отметить, что часто промежуточным звеном в таких реакциях служит ион пероксида, и это ограничивает
фактическую окислительную способность воздуха. Однако в других растворителях, таких как аммиак, образование пероксида является более обычным и доступными для использования становятся совершенно другие
пары.
Для этой функции подходит меньшее количество материалов, чем для использования в основной ячейке, так как материал должен быть восстановлен кислородом. Можно использовать пары Fe(III)/Fe(II) (включенные в комплексы для растворимости в основной среде или поддающейся перекачке насосом кашице) и другие переходные металлы, хромат/Сr(III), Мn(II)/Мn(III), Sn(IV)/Sn(II), Со(II)/Со(III), которые катализируют активированным древесным углем в камере разбрызгивания. Можно также использовать пару хлорат/хлорит и т.д.
Раствор, который образуется согласно
уравнению (9), можно затем передавать в катодную камеру, и в электропреобразовательной ячейке происходит результирующая реакция (для пары иодат/иодид):
3BH4-
+4IO3--->3BO2-+4I-+6H2O, E0=1,50 B. (10)
Так как раствор постоянно рециркулируется, только
малое количество жидкости - которое достаточно только, чтобы обеспечить максимальные расходы, - должно находиться в резервуаре 4. Результирующая реакция по-прежнему та же, что и в реакции (3), за
исключением того, что напряжение реакции равно 1,50 В вместо 1,65 В. Использование этого специфического посредника приводит к потере приблизительно 9% доступной энергии по причине уменьшения выходного
напряжения. Эта энергия, конечно, выделяется как теплота в реакции (9) и равна потерянным 0,15 В.
Этот пример осуществления изобретения полезен в ситуациях, где желательна конструкция с чередующимся поглощением и выделением воздуха с высокой удельной энергией, но также желательна и система с очень высокой пиковой мощностью. В конфигурациях с чередующимся поглощением и выделением воздуха на фиг.3 и 4 пиковая мощность ограничена (среди других факторов) площадью поверхности электрода с чередующимися поглощением и выделением воздуха. Так как возможны конструктивные и стоимостные ограничения на использование электрода с непосредственным чередующимся поглощением и выделением воздуха, этот пример реализации допускает конструкцию с очень высокой скоростью впуска воздуха (он может даже быть сжатым), чтобы обеспечить высокую мощность. Другое преимущество для этой конфигурации состоит в существенно сниженном времени срабатывания. Поскольку и анолит и католит можно запасать в их соответствующих резервуарах, когда быстро необходим высокий расход мощности (например, нажимают педаль акселератора в электрическом автомобиле), можно быстро увеличивать подачу обеих жидкостей в ячейку. Этот пример осуществления также полезен, когда биполярная ячейка и система с результирующим потреблением воздуха желательны вместе. Этот пример осуществления устраняет потребность распределять воздух по всем катодам в биполярной ячейке.
Другой пример осуществления электропреобразовательной ячейки состоит в использовании основной системы ячейки как на фиг.3 или 4, которая имеет электрод с прямым чередующимся поглощением и выделением воздуха для обеспечения большей части энергии при самом высоком кпд, а также другой системы как на фиг.5, которая использует камеру разбрызгивания, для окисления другого соединения, чтобы обеспечить необходимую пиковую мощность. В этом примере осуществления изобретения устройство разбрызгивания (4), как показано на фиг. 5, может (но не обязательно должно) быть меньше, чем устройство воздушного электрода. Проектировщик может тогда избежать создания очень большой площади поверхности воздушного электрода, который должен самостоятельно выполнять всю работу. Результатом является в целом меньшая система с эквивалентной эффективностью (удельная энергия против удельной мощности). Раствор бороводорода для питания двух ячеек при необходимости можно извлекать из одного и того же резервуара или различных резервуаров.
В этих примерах осуществления изобретения можно использовать второй комплект электродов для перезарядки, чтобы перезаряжать жидкость. Возможность слива резервуара 2 и заполнения резервуара 1 по-прежнему может быть реализована в этом примере осуществления изобретения.
Дополнительная гибкость, которую предлагает эта система, состоит в том, что в любой проточной ячейке с переменными выходными мощностями и расходами обычно весь бороводород в растворе не преобразуют полностью, когда он проходит через ячейку. Следовательно, даже если резервуар 1 может быть почти пуст, в качестве аварийного запаса можно накачивать использованную жидкость из резервуара 2 в резервуар 1 (через ячейку перезарядки, если она присутствует, или только через трубку), чтобы обеспечить аварийный запас. Так как концентрация бороводорода является низкой, следует ожидать пониженной эффективности, но и при этих условиях автомобилист сможет добраться до станции перезарядки.
Дополнительное преимущество этих конфигураций состоит в том, что определение остающейся энергии является просто функцией от того, сколько свежего раствора остается в резервуаре 1. Точное измерение энергии, оставленной в многочисленных аккумуляторах, является более трудным.
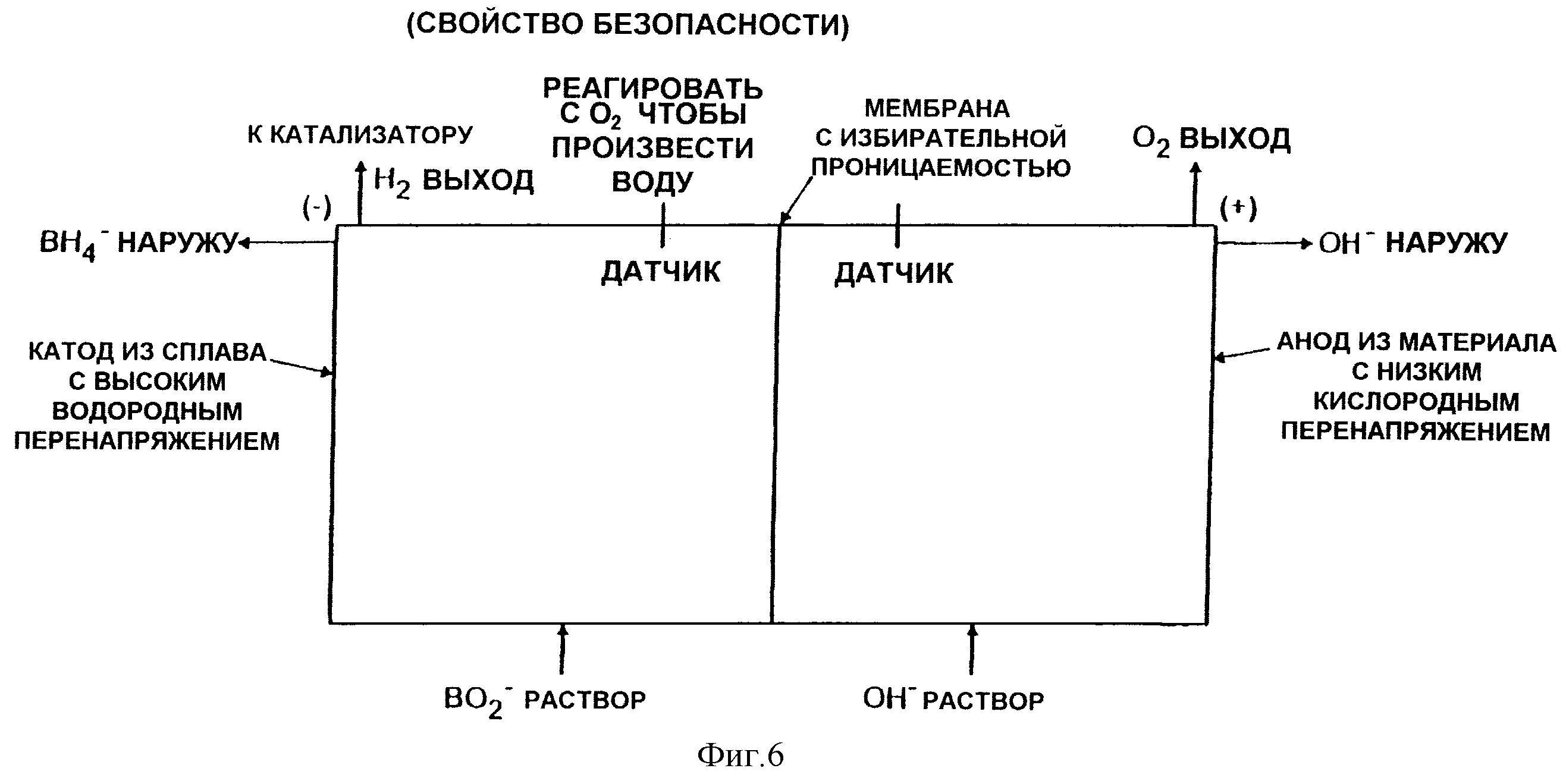
На фиг. 6 показана ячейка перезарядки. Хотя эта ячейка может фактически быть той же самой ячейкой, что и ячейка 2, гибкость, которую допускает эта система, позволяет использовать две
отдельные ячейки. Во время перезарядки уравнение (3) реверсируется для выработки бороводорода и газообразного кислорода следующим образом:
BO2-+2H2
O-->BH4-+2O2, E0=-1,65 B. (11)
Отрицательное напряжение указывает, что электричество необходимо подавать, чтобы вести реакцию в
показанном направлении. Нужно выполнить некоторые важные условия для обеспечения эффективного протекания реакции. При таком отрицательном напряжении легче диссоциировать воду на водород и кислород. К
счастью, кислород является желательным продуктом. Выделение газов из физических электродов является процессом, который чрезвычайно зависит и от состава, и от физических свойств электрода. Выделение
кислорода из основного раствора воды происходит в соответствии с реверсированием уравнения (2):
8OH--->2O2+4H2O+8e-, E1/2=-0,401
B. (12)
При рассмотрении приведенного выше обсуждения теоретических напряжений следует учитывать, что фактическое напряжение, которое необходимо для выделения свободного газа, выше, чем
теоретическое. Разность между теоретическим напряжением и фактическим требуемым напряжением определяется как перенапряжение. В случае выделяющего кислород электрода этот потенциал определяется как
кислородное перенапряжение. Аналогично для водородного электрода это называется водородным перенапряжением. Перенапряжение зависит и от выделяемых газов и от материала электрода. Высокие плотности
тока и более низкие температуры способствуют более высокому перенапряжению.
Электрод с низким кислородным перенапряжением желателен, чтобы максимизировать кпд реакции (12). Материалами с низким кислородным перенапряжением являются золото, окись иридия, двуокись марганца среди других, которые известны в промышленности. Эти электроды можно выполнить из базового металла, например из нержавеющей стали, и покрыть желательным материалом.
Производство бороводорода требует обращения реакции (1), которое имеет вид
BO2-+6H2O+8e--->BH4-+8OH-, E1/2=-1,24 B (13)
При таком отрицательном напряжении выделять водород из воды более
благоприятно следующим образом:
2H2O+2e--->H2+2OH-, E1/2=-0,8277 B. (14)
Если реакция (14) происходит вместо реакции
(13), ячейка не будет перезаряжаться и энергия пропадет впустую. Следовательно, чтобы обеспечить, чтобы происходила реакция (13), для стороны перезарядки ячейки необходим электрод с высоким водородным
перенапряжением. При таких условиях восстановления можно получить различные восстановленные соединения бора. Необходимо перенапряжение, равное по меньшей мере разности в напряжениях между реакциями
(13) и (14), 0,4123 В, и более высокие значения перенапряжения желательны, чтобы минимизировать реакцию (14) в максимально возможной степени.
Мягкие металлы имеют тенденцию к высоким водородным перенапряжениям. Ртуть, например, используют многие десятилетия, чтобы извлечь металлический натрий {E1/2=-2,7 В) из водных растворов, чтобы произвести гидроксид натрия. Ртуть, конечно, является жидкостью, а также имеет ограничения, относящиеся к окружающей среде. Однако жидкая ртуть или ртутное покрытие на поверхности другого металла обеспечило бы протекание реакции (14) с высоким кпд и рассматривается как пример осуществления электропреобразовательной ячейки. Другие мягкие металлы в твердом состоянии также входят в объем изобретения. Они включают висмут, свинец, олово, таллий, кадмий, галлий и индий, но не ограничены ими. Различные сплавы этих металлов проявляют очень высокое перенапряжение. Теллур отравляет способность электрода образовывать газообразный водород, и его можно включать как свободный элемент или как теллурид других металлов, перечисленных выше. Разнообразные комбинации доступных сплавов позволяют проектировщикам выбрать материал, основываясь на водородном перенапряжении, коррозионной стойкости к различным окружающим средам, стоимости, механических качествах и других параметрах. Как легко заметить, оптимальная ячейка перезарядки должна иметь большую площадь поверхности (и, следовательно, низкую плотность тока) анода, который покрывают золотом или окисью иридия. Катод должен иметь меньший (с более высокой плотностью тока) электрод, который покрывают мягким металлическим сплавом. Хотя можно сконструировать одиночную ячейку, которая может эффективно заряжаться и разряжаться, однако электропреобразовательная ячейка дает проектировщику свободу использования и других вариантов (свободу выбора между двумя ячейками или одной) для создания решения, соответствующего конкретным условиям использования.
Следует отметить, что любой перезаряжаемый аккумулятор представляет электрохимический синтез реагентов. Бороводородные соли являются полезными химическими веществами, и их широко используют в химической промышленности как восстановители. Себестоимость производства современными способами высока, так как бороводород производят с помощью реакции гидрида натрия или с трехфтористым бором, или с борными эфирами органических спиртов. При этом производят большие количества побочных продуктов, которые необходимо отделять от бороводорода. В противовес этому производство бороводорода и электричества из дешевых боратов и даже буры представляет значительное улучшение в издержках производства и может даже подстегнуть "бороводородную экономику", в которой возникает инфраструктура для распределения, например, энергии для электроустановок общего пользования или, например, водорода на очистительный завод (бороводород выделяет газообразный водород при различных условиях), или раствора бороводорода к транспортным средствам как легко поддающегося перекачке насосом и хранимого раствора бороводорода.
Электроды, которые делают из этих сплавов, и реакция (13) представляют новые материалы для использования в электрохимическом синтезе бороводородов.
Эти электроды можно также использовать при любом восстановлении, в котором необходимо высокое водородное перенапряжение.Такие материалы, как титан, ванадий, другие переходные металлы, так же как редкоземельные металлы, можно восстанавливать из водных растворов с помощью этих электродов как катодов при операциях типа электрохимической металлизации. Способы производства этих материалов обычно зависят от восстановления безводных хлоридов с таким активным металлом, как магний или натрий. Ванадий восстанавливают из окисей и алюминия в реакции термитного типа. Все эти способы дороги и имеют проблемы при извлечении металла из матрицы расплавленных солей. Эти электроды можно также использовать в любом электрохимическом синтезе, в котором желателен высокий восстановительный потенциал. Органические соединения можно восстанавливать электрически, например с дешевой водой как источником протонов.
Синтез бороводорода из боратов является сравнительно чистым и эффективным. Продуктами являются кислород и бороводород. Присутствует малое количество гидроксида, но это полезно, поскольку основные состояния стабилизируют раствор. Для энергии и большинства других использований гидроксид можно оставлять. Если необходимо восстановление сухого продукта, его можно отделять от бороводорода одним из нескольких существующих способов.
Доступность бороводорода позволяет перекачивать растворы из одного местоположения в другое, где его можно преобразовать обратно в
электричество. Бороводород может также быть очень безопасным и дешевым способом транспортировки водорода. Например, нефтеперерабатывающие заводы в настоящее время часто являются чистыми потребителями
водорода. Раствор бороводорода можно транспортировать (с помощью трубопровода, барж, железных и автомобильных дорог и т. д.) к месту, где нужен водород. Если раствор подкисляют или катализируют
катализатором из переходного металла, такого как кобальт, выделяется водород:

В реакции (15) выделяются большие количества водорода. Если 44% по весу раствор бороводорода подкисляют, один литр раствора выделяет приблизительно 116,3 г водорода. Это количество водорода больше, чем доступное из других источников водорода. Даже криогенный жидкий водород имеет плотность только 70 г на литр. Водород, сжатый до 41,4 МПа, имеет плотность только 36 г на литр. Если водород запасают в таких сплавах, как сплавы редкоземельные металлы - никель, то запасают приблизительно 1% весового водорода. При этом плотность сплава дает плотности немного выше, чем у жидкого водорода, но меньше, чем в растворе бороводорода. В любом случае сплавы очень дороги и их не так легко обрабатывать, как жидкость. Раствор бороводорода также более просто и более безопасно обрабатывать, чем жидкий водород или водород высокого давления.
Еще более высокая плотность доступна, если бороводород обрабатывают как твердое тело или как поддающуюся перекачке насосом суспензию, или более высокотемпературный раствор с приблизительно от 80 до 90% весовых. Таким образом, доступно удвоение количества водорода более чем до 200 г на литр. Это соответствует 2240 л водорода из одного литра доставленного материала. (На месте добавляют некоторое количество воды). Это дает более чем 2,24 м3 водородного газа из одного литра материала. Чтобы сохранять газообразный водород при этой плотности, необходима система, которая работает при почти 227,5 МПа (это давление является типичным для давления, которое развивается внутри ствола винтовки во время выстрела).
Отработанная жидкость представляет собой раствор бората, который можно послать обратно в устройство регенерации и преобразовать обратно в бороводород посредством регулирования рН в случае необходимости и электролиза в ячейке, чтобы синтезировать бороводород, и тем самым по существу обеспечивают замкнутую систему с электричеством и водой как реагентами и водородом и кислородом как продуктами. Необходимая для этого энергия предпочтительна по сравнению с транспортировкой электричества на большое расстояние ввиду потерь в линии. Она также конкурентоспособна с преобразованием сначала бороводорода в электричество и использованием этого электричества, чтобы генерировать водород, так как доступные ячейки электролиза работают с кпд только приблизительно от 70 до 75%. Следовательно, если цель транспортировки состоит в том, чтобы фактически закончить газообразным водородом как исходным сырьем, то приемлема прямая каталитическая реакция по уравнению (15). Если цель транспортировки состоит в передаче электричества, как конечного продукта, то преобразование бороводорода в электропреобразовательной ячейке согласно уравнению (1) является более подходящим.
Как упомянуто ранее, некоторые применения могут потребовать работы при более высоких напряжениях, чем напряжение на выводах ячейки. Если желательна биполярная ячейка, ее можно сделать с использованием химических процессов согласно данному изобретению, как схематично показано на фиг.7. Ячейку можно использовать или благодаря ее способности генерировать электричество, или как устройство для синтеза бороводородов. На фиг.7 биполярное устройство состоит из биполярного электрода, анолита, мембраны с избирательной проницаемостью, католита. Данную последовательность затем повторяют. Каждая такая последовательность представляет собой ячейку (электроды на двух концах являются не биполярными, но обычными с только одной поверхностью в контакте с электролитом). Аккумулятор может быть герметичным и может быть перезаряжаемым или нет, как это желательно. Аккумулятор может быть проточным, который требует, чтобы трубопровод распределял электролит в каждую камеру. Если он является электродом с непосредственно чередующимся поглощением и выделением воздуха, то необходимо также распределять воздух в каждую катодную камеру.
Во всех показанных электродах, в отличие от многих стандартных электродов, сам электрод не является частью электрохимического процесса, и материалы, из которых изготовлен электрод, не изменяются в химическом составе. В результате повышается срок службы электрода и облегчается конструирование. Даже если материалы электрода могут способствовать протеканию химического процесса, который имеет место, сам электрод не изменяется.
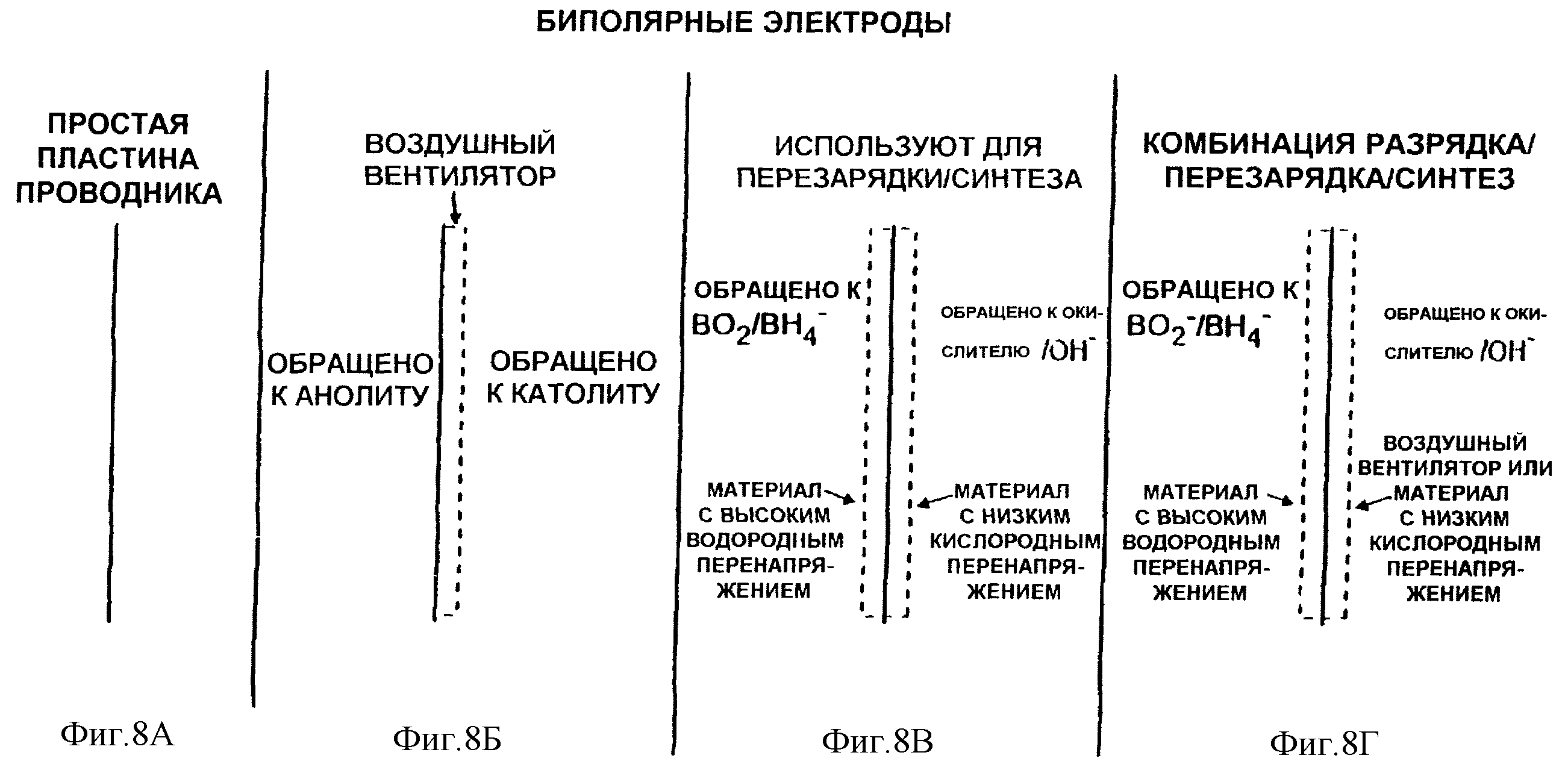
На фиг.8А-8Г показаны различные типы биполярных электродов, которые полезны в различных применениях. Эти электроды ни в коем случае не ограничивают имеющихся возможностей. На фиг.8А показана простая пластина, которая действует только как электронный коллектор. Ее можно использовать в конфигурации, как показано на фиг.5, где воздух разбрызгивают в отдельную камеру, и эту жидкость доставляют в каждую катодную камеру. Раствор бороводорода распределяют в каждую анодную камеру при использовании системы. Герметичная система, как показано на фиг.2, может быть выполнена биполярным способом с электродом, показанным на фиг.8А.
На фиг.8Б одна сторона электрода показана как вентилятор. Эти электроды требуют большой площади поверхности, их обычно катализируют, и они также требуют пространства для католита.
На фиг.8В показан биполярный электрод, который больше оптимизирован для ячейки перезарядки или ячейки, которую выполняют для производства бороводородов. Этот электрод покрывается материалом с высоким водородным перенапряжением на стороне ячейки, поверхность которой обращена к раствору бората/бороводорода. Другая сторона электрода имеет покрытие материалом с низким кислородным перенапряжением на стороне, которая обращена к окислительной стороне ячейки. Этот электрод подходит для ячеек перезарядки, как показано на фиг.4 и 5, или в качестве электрода для ячейки 2 на фиг.5, или в качестве электрода для производства бороводородов.
Электрод на фиг.8Г представляет собой комбинированный электрод для использования в конфигурациях с прямым чередующимся поглощением и выделением воздуха. Одну сторону можно покрыть материалом с высоким водородным перенапряжением и обратить к раствору бората/бороводорода. Другая сторона имеет электрод с чередующимся поглощением и выделением воздуха. Этот электрод можно использовать в биполярной конфигурации ячейки 2 по фиг.3 и 4. Его можно также использовать в ячейке перезарядки 5 по фиг.4 и 5. Так как эта ячейка перезарядки (5) является также ячейкой синтеза для производства бороводородов, этот электрод подходит также для производства бороводородов.
Дополнительная эксплуатационная гибкость объясняется тем, что многие бороводородные соли в значительной степени растворимы в других растворителях помимо воды. Например, растворимость бороводородистого натрия в диметилформамиде при 20oС составляет приблизительно 18% весовых. Она растет при более высоких температурах. Если ячейка должна функционировать в окружающей среде, которая не подходит для воды, вместо нее можно использовать этот растворитель. Как упомянуто выше, бороводородистый натрий очень хорошо растворим в безводном аммиаке. Эта система допускает очень низкие температуры эксплуатации и высокие удельные энергии. Эта система также позволяет, например, использовать чрезвычайно высокую растворимость таких материалов, как нитрат аммония, как высококонцентрированный окислитель, как католит.
Комплексообразующие реагенты (такие, как крон-эфиры) или другие реагенты, которые увеличивают растворимость бороводорода в любом данном растворителе, также можно использовать, и они рассматриваются как подходящие под область охвата данного изобретения.
Хотя мембраны с избирательной проницаемостью допускают перенос неионных материалов через мембрану осмотическим давлением, в одну и ту же ячейку можно ввести две различные системы растворителей. Например, диметилформамид/бороводородный раствор может быть анолитом, а водный раствор гидроксида натрия может быть католитом.
В еще одном примере осуществления изобретения мембрану с избирательной проницаемостью можно удалить, и ячейку могут образовать две жидкости, которые не растворимы друг в друге, но каждая может растворять необходимый электролит. Например, бороводородистый натрий, который растворяют в воде, служит анолитом. Галоид, такой как хлор, который растворяют в таком растворителе, как хлороформ, может быть католитом. Катализатор фазового превращения (такой, как галогенная соль четвертичного аммония, R4N+X-) для переноса хлорида через барьер служит как вариант, чтобы обеспечить проводимость.
Другие примеры осуществления охватываются формулой изобретения.
Реферат
Изобретение относится к области электрохимического преобразования. Техническим результатом изобретения является создание электрохимической ячейки с улучшенными эксплуатационными характеристиками. Согласно изобретению окислительно-восстановительные соединения бора могут использоваться для электрохимических ячеек для аккумулятора или систем накопления энергии, которые характеризуются благоприятными характеристиками удельной энергии, плотности энергии, капитальных и эксплуатационных затрат, эффективности перезарядки, безопасности, воздействия на окружающую среду, ремонтопригодности и долговечности. 7 с. и 89 з.п.ф-лы, 8 ил.

Формула
39. Аккумулятор по одному из пп. 28-38, отличающийся тем, что содержит две части, в одной из которых размещен прямой вентилятор, а в другой - католит с возможностью окисления воздухом и последующего окисления бороводорода до бората с генерированием электрического тока.

Комментарии