Смесь металлоценилфталоцианинов, металлоценилфталоцианины, способ их получения, оптический носительинформации - RU2301810C2
Код документа: RU2301810C2
Описание
Настоящее изобретение относится к металлоценилфталоцианинам, их смесям, способам их получения и к их применению для оптической записи.
Изобретение относится к области записи на оптические носители информации, предпочтительно к носителям однократной записи. Информацию с их помощью хранят благодаря разнице оптических свойств красителя в содержащих и не содержащих запись точках. Такие носители информации известны, например, под названием систем "ОЗМЧ" (однократная запись - многократное чтение) и дополнительно подразделяются, например, на "компакт-диски типа CD-R" и "диски типа DVD-R".
Применение красителей, которые поглощают излучение в ближней инфракрасной области спектра (БИК область спектра), для записи информации в системах ОЗМЧ описано, например, М.Emmelius в Angewandte Chemie, номер 11, сс.1475-1502 (1989). Лазерный луч способен вызвать изменения поглощения, необходимые для записи информации в цифровой форме в таких носителях информации посредством физических (например, за счет сублимации или диффузии) или химических изменений (например, как в цветной фотографии, изомеризация или термическое разложение красителя).
Замещенные фталоцианины представляют класс красителей, имеющих важное значение для применения в таких системах ОЗМЧ, поскольку они характеризуются сильным поглощением в БИК в интервале от 700 до 900 нм, когда соответствующим образом замещены, независимо от центрального атома металла, который обычно присутствует.
Предусмотренный для использования записывающий слой должен удовлетворять очень важным требованиям, таким как высокий показатель преломления и низкая поглощающая способность при длине волны лазерного луча, высокий контраст нанесенных пит (микроскопических углублений), однородность пит при различных длинах пит, высокая светопрочность при дневном свете и при маломощном лазерном излучении (считывание) и одновременно с тем обладание высокой чувствительностью к интенсивному лазерному излучению (запись), высокая долговременная стабильность, низкий уровень помех, высокая разрешающая способность, и в качестве особенно важного свойства очень малые систематическое и случайное отклонения ("дрожание") длины питов от номинального значения при оптимальной мощности излучения во время записи.
Поскольку записывающий слой обычно наносят из раствора, например в виде покрытия, нанесенного по методу центрифугирования, красители должны быть дегкорастворимыми в обычных растворителях, например так, как изложено в ЕР-А 511598 (независимо от существующих при этом различий между полярными и неполярными растворителями).
Используемые для оптической записи полимерные или олигомерные фталоцианины, т.е. соединения, включающие по меньшей мере по два фталоцианиновых звена, которые обычно соединены между собой посредством одинарной связи или атома, или молекулы, служащей в качестве мостика, известны. Так, например, в JP-A 59073994 описаны полимерные материалы-носители сигналограммы, у которых имеются макроциклы, образованные фталоцианинами в главной цепи.
В JP-А 59229396 описаны материалы-носители сигналограммы, включающие олигомеры красителей, у которых по меньшей мере по две молекулы, например фталоцианинов, включающих ванадий или оксид ванадия, VO, в качестве центрального атома, соединены между собой группой -СОО или звеном, содержащим по меньшей мере две группы -СОО.
В JP-A 62059285 описаны фталоцианиновые соединения формулы Рс-(CONH-L-OH)n, где Рс обозначает фталоцианиновый радикал, содержащий центральный атом, например Co(II), L обозначает С1-С5алкилен, а n обозначает число, которое больше или равно единице, которые могут быть полимеризованы полиприсоединением или реакцией поликонденсации.
В GB-A 2259517 описаны полимерные фталоцианины формулы (Q-X-)qPc(-X-Q-Y)p, где Х обозначает О, S, Se, Те, NH, N-алкил или N-арил, Q обозначает углеродный атом или ароматический или гетероциклический радикал, Y обозначает реакционноспособную группу, которая может образовывать мостик, а р≥2, q≥0,16≥(p+q).
Точно так же известны фталоцианиновые соединения, содержащие в качестве заместителя по меньшей мере по одному ферроценовому звену. Так, например, в J.Organomet.Chem. 468(1-2) (1994) 205-212 описан 1,1",1"",1"""-(29Н,31H-фталоцианин-2,9,16,23-тетраил)тетракисферроцен, в Chin.Chem.Lett. 4(4) (1993) 339-342 описан [1-(11-ферроценилундецил)-1′-[4-[4-[[9,16,23-трис(2,2-диметилпропокси)-29H,31H-фталоцианин-2-ил]окси]фенокси]бутил]-4,4′-бипиридиний(2-)-N29,N30,N31, N32]цинкдибромид, в New J.Chem. 21(2) (1997) 267-271 описан 1,1"-[[9,23-бис(додецилтио)-29H,31H-фталоцианин-2,16-диил]бис(нитрилометилидин)]бисферроцен, а в J.Organomet.Chem. 541(1-2) (1997) 441-443 описан синтез [Cp(dppe)Fe-CN-MnPc]2O (где dppe обозначает 1,2-этандиилбис(дифенилфосфин); Ср обозначает циклопентадиенил; Рс обозначает фталоцианин).
В J.Chem.Soc., Chem.Commun. 1995, 1715-1716 описано получение жидкокристаллических ферроценилфталоцианинов реакцией ферроценкарбонилхлорида с не содержащим металла фталоцианином, несущим в качестве заместителя гидроксильную группу, с получением соответствующего сложноэфирного соединения.
В Inorg.Chem. 37 (1998) 411-417 описан синтез бис(ферроценкарбоксилато)(фталоцианинато)кремния, причем ферроценовое звено связано с центральным атомом.
В WO-A 9723354 описаны оптические материалы-носители сигналограммы на основе фталоцианинов, включающих ферроценовые звенья, в качестве заместителей связанные помимо прочего с центральный атомом.
В WO-A 0009522 описан металлоценилфталоцианин или его комплекс с двухвалентным металлом или оксометаллом, галометаллом или гидроксиметаллом, у которого по меньшей мере одно из четырех фенильных колец фталоцианина в качестве заместителя несет по меньшей мере один металлоценовый радикал, связанный посредством мостикового звена Е, где Е состоит из цепи с по меньшей мере двумя атомами или группой атомов, выбранной из ряда, включающего -СН2-, -С(=O)-, -СН(С1-С4 алкил)-, -C(C1-С4алкил)2-, -NH-, -S-, -О- и -СН=СН-.
Применение компакт-диска типа CD-R в качестве носителя для архивирования и резервного копирования компьютерных данных во все большей степени требует более высоких скоростей записи. С другой стороны, когда его необходимо использовать в качестве носителя звуковой информации, требуются низкие (1х) скорости. Это ведет к потребности в постоянной повторной оптимизации записывающих слоев для достижения таких широкодиапазонных характеристик (до последнего времени 1х-8х, в настоящее время 1х-16х, в будущем 24х и выше), что предъявляет сверхвысокие требования к предусмотренным для применения записывающим слоям. Известно, что записывающие слои, включающие фталоцианины, демонстрируют хорошие показатели при промежуточных скоростях (2х-8х), но менее благоприятные параметры при 1х по контрасту и отклонению по длине пит и возвышений от номинальных значений, а также по их случайным отклонениям ("дрожание").
Понятие "контраст" относится к разнице между отражениями пита и возвышения или соответствующей модулирующей амплитуды высокочастотного сигнала. Понятие "дрожание" относится конкретно к временному дефекту изменения сигнала, которое может быть обусловлено тем, что пит оказывается слишком коротким или слишком длинным. Так, например, в компакт-диске типа CD-R длину питов или возвышений можно варьировать в интервале от 3Т до 11T, где 1T=231,4 нс при скорости 1,2 м/с (1х). Когда, например, длина пита 3Т оказывается чрезмерно малой или чрезмерно большой, это может привести к увеличенному числу ЧБЛО (т.е. частоты блоков с ошибками, которая относится к числу физических ошибок, имеющихся на компакт-диске) и, таким образом, к пониженному качеству. В соответствии с применяемым стандартом ЧБЛО должна быть меньше 220 в секунду, а в соответствии с существующими рыночными требованиями даже меньше чем от 10 до 20 в секунду. Требования, которым должен удовлетворять носитель информации, и применяемые стандарты (сформулированные в настоящее время в "Оранжевой книге") специалистам в данной области техники известны, вследствие чего дополнительные пояснения по этой теме являются лишними.
Для устранения вышеупомянутых затруднений, связанных с фталоцианинами, были внесены различные предложения. В частности, были предприняты попытки понизить их относительно высокую температуру разложения в сравнении с красителями других классов, в частности с цианинами.
Так, например, в DE-A 4112402 в качестве записывающего слоя предлагается смесь фталоцианина с цианином (в качестве светопоглощающего элемента), которая поглощает излучение в диапазоне вышеупомянутых длин волн. Однако и в этом случае повторное считывание также приводит к деструкции поглотителя света, вследствие чего целевые свойства не достигаются. Кроме того, известно, что цианиновые красители светопрочностью не обладают, поэтому обычно к ним необходимо добавлять стабилизатор.
В заявке ЕР-А 600427 описан оптический носитель информации, записывающий слой которого включает фталоцианин и добавку, например ферроценовое производное, ацетилацетонат металла или противоударную добавку. В соответствии с этой заявкой введение указанных добавок повышает качество записи. Однако недостатками являются применение дополнительного вещества в форме добавки и затруднения при рекуперации красителя, остающегося во время получения записывающего слоя, поскольку активное вещество необходимо либо удалить, либо вновь отрегулировать его концентрацию для возможности повторного использования.
В JP-A 8-118800 описаны оптические носители информации, записывающие слои которых включают азосоединение, замещенное ферроценовым звеном. Описаны также смеси этих азосоединении, помимо прочего с фталоцианинами и пентаметинцианинами. При этом недостаток состоит в том, что с использованием только либо азосоединения, либо фталоцианинов удовлетворительный записывающий слой получить невозможно.
В заявке WO 0009522, которая уже обсуждалась выше, описаны металлоценилфталоцианины, которые можно использовать в качестве материалов-носителей сигналограммы в оптических носителях информации и которые без дополнительных добавок, предпочтительно когда их применяют в компакт-дисках типа CD-R, обладают существенно улучшенными широкодиапазонными характеристиками (1х-8х) в сравнении с достижимыми при современном состоянии в данной области техники и демонстрируют превосходные характеристики записи и воспроизведения при длине волны полупроводникового лазера (770-790 нм). Более того, эти соединения обуславливают возможность усовершенствованного способа рекуперации красителя, используемого при получении записывающего слоя.
Однако известные до сих пор материалы-носители сигналограммы не в состоянии полностью удовлетворить повышенным требованиям при очень высоких скоростях записи. Так, в частности, установлено, что для разных интервалов скорости записи оптимальна разная толщина записывающего слоя. В то время как при низких скоростях записи (1х-2х) решающим параметром обычно является неудовлетворительно низкий контраст (I11), который может быть улучшен благодаря относительно толстому слою, при более высоких скоростях записи (>4х) решающим параметром обычно является чрезмерное дрожание при коротких питах или возвышениях (в частности L3T), которое может быть уменьшено благодаря относительно тонкому записывающему слою. С другой стороны, при наличии тонкого слоя требуется, что нежелательно, повышенная мощность для записи при данной скорости записи, что вновь ограничивает максимально достижимую скорость записи при данной мощности лазера.
Следовательно, существует потребность в усовершенствованных материалах-носителях сигналограммы, которые могут удовлетворить всем необходимым техническим требованиям в широком диапазоне, т.е. как при низких (1х-2х), так и очень высоких (>12х) скоростях записи и при той же толщине слоя, и запись на которых возможна также при сравнительно низкой мощности лазера, т.е. которые обладают высокой чувствительностью. Более того, по производственным причинам необходимо добиваться качества в широком диапазоне не только при конкретной толщине слоя, а в максимально возможном интервале толщин, а именно, требуется "технологическое окно". Адекватным мерилом размера технологического окна служит оптическая плотность записывающего слоя. Соответственно необходимо располагать материалами-носителями сигналограммы, которые обладают очень большим положительным численным значением ширины технологического окна, тогда как отрицательное численное значение означает отсутствие такой толщины слоя, при которой в широком диапазоне могут быть удовлетворены все технические требования.
Таким образом, объектом настоящего изобретения является создание новых широкодиапазонных материалов-носителей сигналограммы, обеспечивающих наличие большого технологического окна, т.е. усовершенствованного позитивного технологического окна, и обладающих высокой чувствительностью. Так, в частности, необходимо иметь возможность изготовления оптических носителей информации, характеризующихся малой толщиной слоя, повышенной пригодностью для повторного использования и повышенными скоростями записи, от выше 32х до по меньшей мере 40х.
Соответственно созданы заявленные смеси, металлоценилфталоцианиновые соединения, разработаны способы их получения и их применения, а также оптические носители информации, включающие эти смеси или соединения.
В частности, по настоящему изобретению предлагаются смеси металлоценилфталоцианинов, которые могут быть приготовлены реакцией смеси А, включающей
(а) от 1 до 99 мас.%, предпочтительно от 50 до 95 мас.%, фталоцианина формулы I

где M1 обозначает атом двухвалентного металла, металлоксогруппу, металлгалогруппу, металлгидроксильную группу или два водородных атома, где с атомом двухвалентного металла, металлоксогруппой, металлгалогруппой или металлгидроксильной группой может быть связан один или два лиганда, Х обозначает атом галогена, такого как хлор, бром или иод, предпочтительно хлор или бром,
Y1 обозначает -OR1, -OOC-R2, -NHR1, -N(R1)R2, -SR1, предпочтительно -OR1,
Y2 обозначает -CHO, -СН(OR3)OR4, -CH=N-OH, -CH=N-OR3, -CH=N-NHR5, -CH=N-N(R3)R5, -CH2OH, -(CH2)2-20OH, -СН2OR3, -СН2OOC-R3, -СО-R3, -СООН или -COOR3,
R1-R5 каждый независимо друг от друга может обозначать незамещенный или замещенный атомом галогена-, гидрокси-, С1-С20алкокси-, C1-С20 алкиламино- или С2-С20диалкиламинозамещенный С1-С20алкил, который может прерываться -О-, -S- или -NR11-, где R11 может обозначать C1-С6алкил,
и R1 и R2 каждый может также обозначать С5-С20циклоалкил, С2-С20алкенил, C5 -С12циклоалкенил, С2-С20алкинил, С6-С18арил или С7-С18аралкил,
х обозначает рациональное число от 0 до 8, предпочтительно от 0 до 5, особенно предпочтительно от 0 до 3,
y1 обозначает рациональное число от 0 до 6, предпочтительно целое число от 1 до 6, особенно предпочтительно от 3 до 5, в особенности 4,
y2 обозначает рациональное число от 0 до 4, предпочтительно от 0 до 2, особенно предпочтительно от 0 до 1, где (х+y1+y2)≤ 16, а
R15 может обозначать гидроксилсодержащий радикал, карбоксилсодержащий радикал или радикал, содержащий остаток хлорангидрида кислоты, предпочтительно -СН2OH, -СН(Ме)ОН, -СООН, -COCl, и
(б) от 99 до 1 мас.%, предпочтительно от 50 до 5 мас.%, фталоцианина формулы II

с металлоценовым производным в присутствии катализатора.
В качестве атома двухвалентного металла можно использовать катионы двухвалентных переходных металлов, в частности катионы меди, цинка, никеля, палладия, платины, марганца или кобальта, предпочтительно палладия или меди. В качестве металлоксогруппы можно использовать VO, MnO или TiO.
В качестве металлгалогруппы можно использовать Al-Cl, Al-Br, Al-F, Al-I, Ga-Cl, Ga-F, Ga-I, Ga-Br, In-Cl, In-F, In-I, In-Br, Tl-Cl, Tl-F, Tl-I, Tl-Br, Fed или RuCl, или CrCl2, SiCl2, SiBr2, SiF2, Sil2, ZrCb, GeCl2, GeBr2, GeI2, GeF2, SnCl2, SnBr2, SnI2, SnF2, TiCl2, TiF2, TiBr2.
В качестве металлгидроксильной группы можно использовать MnOH, Si(OH)2, Ge(OH)2, Zr(OH)2, Mn(OH)2, AlOH или Sn(OH)2.
С1-С20алкил представляет собой, например, метил, этил, н-, изопропил, н-, втор-, изо-, трет-бутил, н-, неопентил, гексил, гептил, октил, нонил, децил, ундецил, до децил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, нонадецил, эйкозил, предпочтительно
С1-С12алкил, такой как метил, этил, н-, изопропил, н-, втор-, изо-, трет-бутил, н-, неопентил, гексил, гептил, октил, нонил, децил, ундецил, додецил или, в частности, разветвленный С3-С12алкил, такой как изопропил, втор-, изо-, трет-бутил, неопентил, 1,2-диметилпропил, 1,3-диметилбутил, 1-изопропилпропил, 1,2-диметилбутил, 1,4-диметилпентил, 2-метил- 1-изопропилпропил, 1-этил-3-метилбутил, 3-метил-1-изопропилбутил, 2-метил-1-изопропилбутил и 1-трет-бутил-2-метилпропил, и C1-С6алкил, такой как метил, этил, н-, изопропил, н-, втор-, изо-, трет-бутил, н-, неопентил, н-гексил, 2,2-диметилгексил, особенно предпочтительно С1-С4алкил, такой как метил, этил, н-, изопропил, н-, втор-, изо-, трет-бутил и 2,4-диметил-3-пентил.
С5-С20циклоалкил представляет собой, например, циклопентил, циклогексил, циклогептил, циклооктил, циклононил, циклодецил, циклоундецил, циклододецил, циклотридецил, циклотетрадецил, циклопентадецил, циклогексадецил, циклогептадецил, циклооктадецил, циклононадецил, циклоэйкозил, предпочтительно С5-С8 циклоалкил, такой как циклопентил, циклогексил, циклогептил, циклооктил или бициклоалкил, такой как

где Хр, Yp и Zp каждый независимо друг от друга может обозначать атом водорода или галогена, метил или этил, а каждый с Rp1 no Rp6 независимо друг от друга может обозначать С1-С4алкил, который может быть незамещенным или галозамещенным. Предпочтительные бициклоалкильные радикалы представляют собой, например, производные, такие как

Получение фталоцианинов, несущих такие бициклоалкильные лиганды, подробно описано в US 6348250, вследствие чего дополнительные подробности по этой теме в настоящем описании являются лишними.
С2-С20алкенил представляет собой, например, этенил, н-, изопропенил, н-, втор-, изо-, трет-бутенил, н-, неопентенил, гексенил, гептенил, октенил, ноненил, деценил, ундеценил, додеценил, тридеценил, тетрадеценил, пентадеценил, гексадеценил, гептадеценил, октадеценил, нонадеценил или эйкозенил, предпочтительно С2-С6алкенил, такой как этенил, н-, изопропенил, н-, втор-, изо-, трет-бутенил, н-, неопентенил и н-гексенил, особенно предпочтительно С2-С4алкенил, такой как этенил, н-, изопропенил, н-, втор-, изо- и трет-бутенил.
С5-С12циклоакенил представляет собой, например, циклопентенил, циклогексенил, циклогептенил, циклооктенил, циклононенил, циклодеценил, циклоундеценил, циклододеценил, предпочтительно С5-С8циклоалкенил, такой как циклопентенил, циклогексенил, циклогептенил, циклооктенил.
С2-С20алкинил представляет собой, например, этинил, н-, изопропинил, н-, втор-, изо-, трет-бутинил, н-, неопентинил, гексинил, гептинил, октинил, нонинил, децинил, ундецинил, додецинил, тридецинил, тетрадецинил, пентадецинил, гексадецинил, гептадецинил, октадецинил, нонадецинил или эйкозинил, предпочтительно С2-С6алкинил, такой как этинил, н-, изопропинил, н-, втор-, изо-, трет-бутинил, н-, неопентинил и н-гексинил, особенно предпочтительно С2-С4 алкинил, такой как этинил, н-, изопропинил, н-, втор-, изо- и трет-бутинил.
С6-С18арил представляет собой, например, фенил, 1-, 2-нафтил, инденил, азуленил, аценафтиленил, флуоренил, фенантренил, антраценил или трифенилен, предпочтительно фенил.
С7-С18аралкил представляет собой, например, бензил, фенетил или фенил(СН2)3-12-, предпочтительно бензил.
С1-С20алкокси представляет собой, например, метокси, этокси, н-, изопропокси, н-, втор-, изо-, трет-бутокси, н-, неопентокси, гексокси, гептокси, октокси, нонокси, децокси, ундецокси, додецокси, тридецокси, тетрадецокси, пентадецокси, гексадецокси, гептадецокси, октадецокси, нонадецокси или эйкозокси, предпочтительно C1-С6алкоксигруппу, такую как метокси, этокси, н-, изопропокси, н-, втор-, изо-, трет-бутокси, н-, неопентокси, н-гексокси и 2,2-диметилгексокси, особенно предпочтительно С1-С4алкоксигруппу, такую как метокси, этокси, н-, изопропокси, н-, втор-, изо- и трет-бутокси.
С1-С20 алкиламиногруппа представляет собой, например, метиламино-, этиламино-, н-, изопропиламино-, н-, втор-, изо-, трет-бутиламино-, н-, неопентиламино-, гексиламино-, гептиламино-, октиламино-, нониламино-, дециламино-, ундециламино-, додециламино-, тридециламино-, тетрадециламино-, пентадециламино-, гексадециламино-, гептадециламино-, октадециламино-, нонадециламино- или эйкозиламиногруппу, предпочтительно C1-С6алкиламиногруппу, такую как метиламино-, этиламино-, н-, изопропиламино-, н-, втор-, изо-, трет-бутиламино-, н-, неопентиламино- и н-гексиламино-, особенно предпочтительно С1-С4алкиламиногруппу, такую как метиламино-, этиламино-, н-, изопропиламино-, н-, втор-, изо- или трет-бутиламиногруппу.
С2-С20диалкиламиногруппа представляет собой, например, диметиламино-, диэтиламино-, н-, изодипропиламино-, н-, втор-, изо-, трет-дибутиламино-, н-, неодипентиламино-, дигексиламино-, дигептиламино-, диоктиламино-, динониламино-, дидециламино-, диундециламино-, дидодециламино-, дитридециламино-, дитетрадециламино-, дипентадециламино-, дигексадециламино-, дигептадециламино-, диоктадециламино-, динонадециламино- или диэйкозиламиногруппу, предпочтительно C1-С6алкиламиногруппу, такую как диметиламино-, диэтиламино-, н-, изодипропиламино-, н-, втор-, изо-, трет-дибутиламино-, н-, неодипентиламино-и н-дигексиламиногруппа, особенно предпочтительно С1-С4алкиламиногруппу, такую как диметиламино-, диэтиламино-, н-, изодипропиламино-, н-, втор-, изо- и трет-дибутиламиногруппа.
В качестве фосфорсодержащего С1-С4алкила предпочтение отдают использованию метилена, этилена, пропилена или бутилена, замещенного дифенилфосфиновыми радикалами, например -СН2-PAr2 или -СН(Ме)-PAr2, где Ar обозначает незамещенный или замещенный фенил.
В качестве диарилфосфинов можно использовать, например, дифенилфосфин и замещенные дифенилфосфины.
Процесс в соответствии с изобретением обычно проводят этерификацией смеси А посредством металлоценового производного в присутствии катализатора, реакцией смеси А с металлоценовым производным, предпочтительно с производным, выбранным из группы, включающей гидроксилсодержащие металлоцены, карбоксилсодержащие металлоцены и металлоцены, включающие остаток хлорангидрида кислоты, предпочтительно из группы, включающей металлоценкарбонилхлориды CpM2Cp′-COCl, металлоценкарбоновые кислоты CpM2Cp′-COOH, где Ср обозначает


Особое предпочтение отдают использованию смеси А, в которой R15обозначает гидроксилсодержащий радикал, а металлоцен несет карбоксилсодержащий радикал или радикал, включающий остаток хлорангидрида кислоты. Такое же предпочтение отдают варианту, в котором R15обозначает карбоксилсодержащий радикал или радикал, включающий остаток хлорангидрида кислоты, а металлоцен представляет собой гидроксилсодержащий радикал.
Эту реакцию также можно проводить по методу, который известен, путем конденсации двух гидроксилсодержащих радикалов с получением простого эфира или конденсацией одного гидроксилсодержащего радикала с аминсодержащим радикалом с получением уретана.
В предпочтительном варианте по аналогичным методам могут быть получены другие вышеописанные возможные радикалы для R15.
Исходные соединения I и II, если они включают ОН-содержащий заместитель, обычно могут быть получены восстановлением соответствующих формильных соединений, предпочтительно соответствующего альдегида, например по способу, описанному в WO 98/14520. В предпочтительном варианте восстановление альдегида проводят с использованием комплексного гидрида металла, такого как боргидрид натрия. В особенно предпочтительном варианте такое восстановление проводят с использованием комплексного гидрида металла на инертном материале носителя, таком как цеолит, ускоритель фильтрования, силикат, оксид алюминия (продукт "Alox"), а в еще более предпочтительном варианте-с использованием боргидрида натрия на продукте Alox. Карбоксильная группа может быть получена по методу, который известен, окислением соответствующего формильного соединения, и при необходимости его можно превращать в соответствующий хлорангидрид кислоты.
Сами формильные соединения получают, например, по методу, также описанному в WO 98/14520, реакцией фталоцианинов III

известных, например, из ЕР-В 373643, по методу Вильсмайера, предпочтительно с оксихлоридом фосфора/диметилформамидом или оксихлоридом фосфора/N-метилформанилидом.
Соответствующие галоидированные соединения с I по III (в случае, когда х не обозначает 0) получают, например, галоидированием соответствующих формильных соединений с последующим восстановлением и получением соответствующих спиртовых соединений V.
Галоидирование можно проводить по обычным методам, как это изложено в ЕР-А 513370 или ЕР-А 519419, например смешением целевых фталоцианинов с бромом в органическом растворителе, таком как насыщенный углеводород, простой эфир и галоидированный углеводород, или как при осуществлении способа, описанного в ЕР-А 703281, в двухфазной системе, включающей воду и галоидированный ароматический растворитель, который практически не смешивается с водой, при необходимости с нагреванием. Такое галоидирование может быть с равным успехом проведено только после реакции смеси А с металлоценовыми производными.
В качестве металлоценкарбонильных соединений предпочтение отдают использованию ферроценкарбоновой кислоты и производных, таких как эфиры и галоидангидриды, предпочтительно ферроценкарбоновой кислоты,
Металлоценкарбонильные соединения обычно технически доступны или могут быть получены по известным методам, как это изложено в Org. Synthesis 56 (1977) 28-31. Ферроценовые производные также могут быть получены по методам, описанным в "Synthesis of Substituted Ferrocenes and Other π-Cyclopentadienyl-Transition Metal Compounds, Org.Reactions 17, 1969, 1/154, 21/3, 99/100". Конкретно вышеупомянутая ферроценилуксусная кислота может быть получена следующим синтетическим путем:
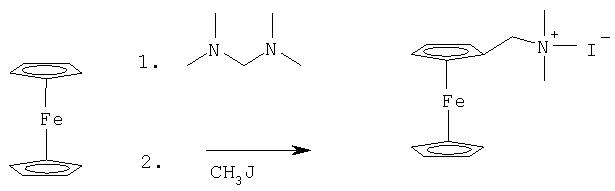
Org. Syn. 40, 1960, 31/3, 45/6, 52; J. Chem. Soc.,1958, 656-660
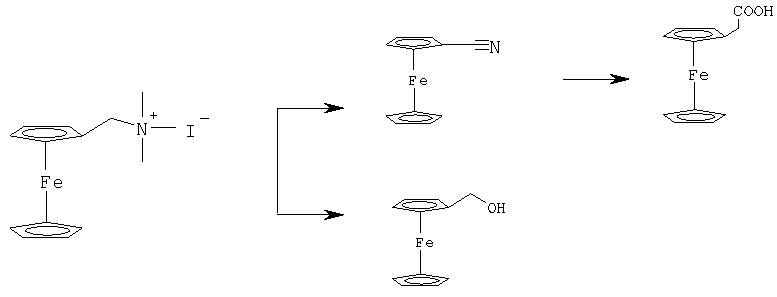
Org. Syn. 40, 1960, 31/3, 45/6, 52; J. Org. Chem. 23, 1958, 653-655
Другие ферроценовые производные, такие как ферроценилмасляная кислота и ферроценоилпропионовая кислота, описаны, например, в J.Am.Chem.Soc. 79, 3420-3424 (1957); Docl.Acad.Nauk SSSR 118, 1958, 512/4; Proc.Acad.Sci. USSR Chem-Sect. 118, 1958, 81/3; US 3,222,373.
Бифункциональные ферроценовые производные, такие как ферроцендикарбоновая кислота и 1,1'-бисгидроксиметилферроцен, можно также вводить в качестве мостика между двумя фталоцианиновыми звеньями. Процесс получения, например, ферроцендикарбоновой кислоты проводят по методу, аналогичному описанному в J.Polymer Sci., 54, 651 (1961); 1,1′-бисгидроксиметилферроцен технически доступен (например, на фирме ALDRICH под №37,262-5, регистрационный №1291-48-1 CHEMCATS).
Молярное соотношение между металлоценкарбонильным соединением и смесью А обычно зависит от целевой степени этерификации и молярного соотношения фталоцианинов I и II. Предпочтение отдают интервалу от 5:1 до 0,5:1, особенно предпочтительно от 2:1 до 1:1.
Эту реакцию обычно проводят в растворителе. В качестве растворителей используют, например, апротонные органические растворители, такие как пиридин, хлорбензол, толуол, ксилол, тетрагидрофуран, хлороформ, метиленхлорид, этилацетат и их смеси.
Предпочтение отдают использованию смесей растворителей, включающих относительно низкокипящий полярный растворитель и относительно высококипящий неполярный растворитель, в частности когда проводят катализируемую кислотой этерификацию с использованием карбоновой кислоты или эфира карбоновой кислоты (переэтерификация). В зависимости от растворимости используемого ферроценового производного можно также обойтись без добавления полярного растворителя.
Затем в предпочтительном варианте во время проведения реакции относительно низкокипящий полярный растворитель отгоняют из реакционной смеси совместно с образующейся в результате реакции водой (или спиртом).
Массовое соотношение между полярным и неполярным растворителями обычно находится в интервале от 10:1 до 1:10, предпочтительно от 4:1 до 1:1.
Массовое соотношение между смесью растворителей и смесью А обычно находится в интервале от 2:1 до 50:1, предпочтительно от 5:1 до 20:1.
В качестве катализаторов для этой реакции предпочтение отдают использованию кислот, которые обычно применяют для этерификации спиртов карболовыми кислотами или для этерификации двух спиртовых компонентов.
Ими служат, например:
минеральные кислоты, такие как H2SO4, HCl, HBr, HClO4, Н3PO4,
ароматические сульфоновые кислоты формулы Ar-SO3H, например п-толуолсульфоновая кислота,
кислоты Льюиса, такие как FeCl3, AlCl3, ZnCl2, TiOR4 (где R обозначает C1-С6алкил), дибутилоловооксид, диоктилоловооксид.
В зависимости от катализатора количество катализатора обычно находится в интервале от 0,01 до 20 мас.% в пересчете на используемую смесь А. В случаях сильных минеральных кислот и кислот Льюиса обычно оказываются достаточными количества от 0,1 до 1 мас.%.
Реакционная температура обычно находится в интервале от 0°С до температуры кипения реакционной смеси под давлением окружающей среды, предпочтительно от комнатной температуры (20°С) до 130°С. Реакционная температура обычно зависит от используемого растворителя или выбранного состава смеси растворителей.
Если основываться на проведенных к настоящему времени наблюдениях, то для успешного выполнения изобретения реакционное давление решающего значения не имеет. Его целесообразно выбирать в интервале от 70 кПа до 5 МПа, предпочтительно от 90 до 120 кПа.
В предпочтительном варианте реакцию проводят в атмосфере инертного газа, такого как азот и благородный газ, в частности неон или аргон.
Смеси по изобретению могут быть также приготовлены восстановлением формильных соединений, которые могут быть получены из фталоцианинов III по методу, описанному в WO 98/14520, например посредством натрийборгидрида, с получением соответствующих спиртовых соединений, последующей этерификацией этих последних металлоценильным радикалом, а затем, если необходимо, галоидированием продуктов.
По другому варианту выполнения настоящего изобретения предлагаются смеси в соответствии с изобретением, которые включают следующие основные компоненты:
(а) от 1 до 99 мас.%, предпочтительно от 20 до 95 мас.%, особенно предпочтительно от 40 до 90 мас.%, еще более предпочтительно от 50 до 80 мас.%, металлоценилфталоцианина IV или его комплекса металла с двухвалентным металлом, оксометаллом, галометаллом или гидроксиметаллом, в котором по меньшей мере одно из четырех фенильных колец фталоцианина в качестве заместителя несет по меньшей мере один металлоценовый радикал, связанный посредством мостикового звена Е, где Е включает цепь из по меньшей мере двух атомов или атомных групп, выбранных из ряда, включающего -СН2-, -С(=O)-, -СН(С1-С4алкил)-, -С(С1-С4алкил)2-, -NH-, -S- и -О-, или смеси разных металлоценилфталоцианинов IV,
и
(б) от 99 до 1 мас.%, предпочтительно от 80 до 5 мас.%, особенно предпочтительно от 60 до 10 мас.%, еще более предпочтительно от 50 до 20 мас.%, металлоценилфталоцианинового соединения, выбранного из группы, включающей фталоцианиновые соединения V, содержащие по два фталоцианиновых звена, связанных посредством одинарной связи или мостикового атома, или молекулы; фталоцианиновые соединения VI, содержащие по три фталоцианиновых звена, связанных в каждом случае посредством одинарной связи и/или мостикового атома, или молекулы; и фталоцианиновые соединения VII, содержащие по четыре фталоцианиновых звена, связанных в каждом случае посредством одинарной связи и/или мостикового атома, или молекулы.
Предпочтительные металлоценилфталоцианины IV или их комплексы металлов представляют собой продукты, отвечающие формуле IVa:
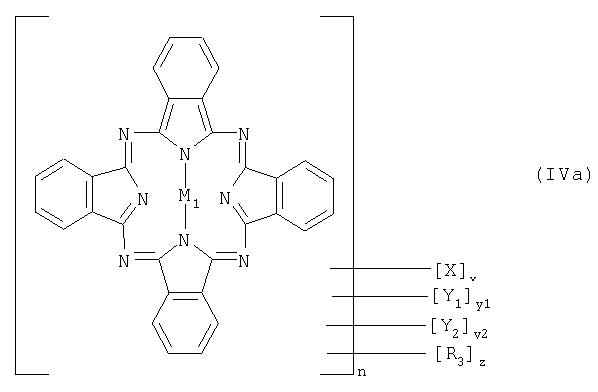
где R3 обозначает

предпочтительно

где R4 и R5 каждый независимо друг от друга может обозначать водородный атом или С1-С4алкил,
n обозначает число от 1 до 4,
R6 и R7 каждый независимо друг от друга обозначает атом водорода или галогена, такого как фтор, хлор, бром или иод, С1-С4алкил, C1-С4алкокси, амино-С1-С4алкил, диарилфосфин или фосфорсодержащий С1-С4алкил, такой как -СН2-PAr2 и -СН(Ме)-PAr2, где Ar обозначает незамещенный или замещенный фенил, R8 может обозначать -O-R9-, -C(=O)-O-R9 или -O-C(=O)-R9-, где R9 может обозначать одинарную связь, С1-С4алкилен или С2-С4алкенилен, M2 обозначает двухвалентный переходный металл, R12 обозначает водородный атом или метил, a R13 обозначает одинарную связь, -СН2-, -СН2СН2-, -СН=СН-, -СН2-С(=O)- или -СН2 СН2-С(=O)-,
z обозначает число от 1 до 4, предпочтительно от 1 до 3, особенно предпочтительно от 1 до 2, где (х+y1+у2+z)≤16,
и один или два лиганда могут быть связаны с атомом двухвалентного металла, металлоксогруппой, металлгалогруппой или металлгидроксильной группой, а Е обозначает, как дополнительно указано выше, молекулярную цепь, выбранную из ряда, включающего -СН2-, -С(=O)-, -СН(С1-С4алкил)-, -С(С1-С4алкил)2-, -NH-, -S- и -О-.
Рациональные или нецелочисленные значения z, x, y1 и у2 (а также приведенных ниже символов с а2 по а8) показывают, что содержится смесь по меньшей мере двух разных соединений IV, причем молярное соотношение между обоими соединениями приводит к соответствующему рациональному числу. Так, например, значение z, равное 1,5, означает, по-видимому, что соединение формулы IV, в которой z обозначает 1, и другое соединение формулы IV, в которой z обозначает 2, находятся в молярном соотношении 1:1.
Можно также отметить то, что общей формуле отвечают соответствующие структурные изомеры, характеризующиеся другим положениям замещения в фенильных кольцах, но в интересах простоты они не представлены.
Эти два замечания применимы ко всем формулам, приведенным в данной заявке на патент.
Особенно предпочтительные металлоценилфталоцианины отвечают формуле IVb

где х обозначает число от 2,6 до 3,0, предпочтительно от 2,7 до 2,9, в частности 2,8, или формуле IVc (нижняя формула на с.19 оригинала)

где х обозначает число от 0 до 0,5, предпочтительно 0.
Предпочтение отдают также смесям разных металлоценилфталоцианинов IV, включающим
(а) от 60 до 95 мол.%, предпочтительно от 80 до 95 мол.%, соединения IVd
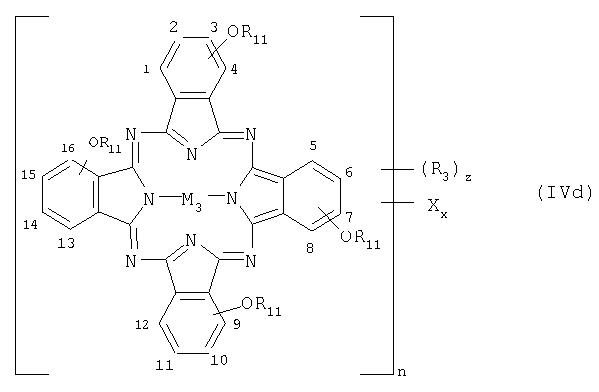
включающего один радикал R3 (z обозначает 1),
(б) от 5 до 20 мол.%, предпочтительно от 5 до 10 мол.%, соединения IVd, включающего два радикала R3(z обозначает 2) и
(в) от 0 до 25 мол.%, предпочтительно от 0 до 10 мол.%, соединения IVe

где каждый из радикалов -OR11, R3 и R14, которые одинаковы, Х и М3 имеют те же значения в формулах IVd и IVe, а в противном случае имеют те значения, которые указаны выше, причем суммарное количество в мол.% дополняют до 100%.
Более того, особое предпочтение отдают смесям разных металлоценилфталоцианинов IV, включающим
(а) от 60 до 95 мол.%, предпочтительно от 80 до 95 мол.%, соединения IVd, у которого R11 обозначает С1-С12алкил, М3 обозначает атом палладия или меди,a z обозначает 1,
(б) от 5 до 20 мол.%, предпочтительно от 5 до 10 мол.%, соединения IVd, включающего два радикала R3 (z обозначает 2)
и
(в) от 0 до 25 мол.%, предпочтительно от 0 до 10 мол.%, соединения IVe, у которого R14 обозначает -СНО, -CH2OH, -COOH, -СН2OC(O)-С1-С4алкил или ацеталь, а z может обозначать 1 или 2, где каждый из радикалов -OR11, R3 и R14, которые одинаковы, Х и М3 в формулах IVd и IVe имеет одни и те же значения, а в противном случае имеют те значения, которые указаны выше, причем суммарное количество в мол.% дополняют до 100%.
По еще одному варианту выполнения настоящего изобретения предлагаются металлоценилфталоцианиновые соединения, выбранные из группы, включающей фталоцианиновые соединения V, содержащие по два фталоцианиновых звена, связанных посредством одинарной связи или мостикового атома, или молекулы; фталоцианиновые соединения VI, содержащие по три фталоцианиновых звена, связанных в каждом случае посредством одинарной связи и/или мостикового атома, или молекулы; и фталоцианиновые соединения VII, содержащие по четыре фталоцианиновых звена, связанных в каждом случае посредством одинарной связи и/или мостикового атома, или молекулы.
Металлоценилфталоцианины V, VI и VII и более высокомолекулярные олигомеры могут быть представлены формулой VIII

где Рс обозначает фталоцианин или его комплекс металла с двухвалентным металлом, оксометаллом, галометаллом, гидроксиметаллом или 2 водородными атомами, а понятия "двухвалентный металл", "оксометалл" и т.д. имеют указанные выше значения,
Ха, Ya, Za, Ma и -L- обозначают заместители на периферийном углеродном скелете, в частности Ха обозначает атом галогена, Ya обозначает замещенный или незамещенный алкокси, алкиламиногруппу или алкилтио, Za обозначает формильную, карбонильную, гидроксиметильную или карбоксильную группу,
Ма обозначает заместитель, включающий по меньшей мере один металлоценовый радикал, -L- обозначает одинарную связь, -(СН2)а7-, где а7 обозначает 1, 2, 3 или 4, остаток простого эфира, такой как -О- или -(СН2)а7-O-(СН2)а8-, где а8 обозначает 1, 2, 3 или 4, сложноэфирную группу, амидную группу или двухвалентную металлоценильную группу, а
а1 обозначает 1, 2, 3, 4, 5, 6, 7. 8, 9 или 10,
а2 обозначает рациональное число от 0 до 8, предпочтительно от 0 до 5, особенно предпочтительно от 0 до 3,
а3 обозначает рациональное число от 0 до 6, предпочтительно целое число от 1 до 6, особенно предпочтительно от 3 до 5, еще более предпочтительно 4,
а4 обозначает рациональное число от 0 до 4, предпочтительно от 0 до 2, особенно предпочтительно от 0 до 1,
а5 обозначает рациональное число от 0 до 4, предпочтительно от 0 до 2,
а6 обозначает рациональное число от 1 до 4, предпочтительно от 1 до 3, где (а2+а3+а4+а5+а6)≤16 и 1<(а4+а5+а6)≤4.
Особенно предпочтительные олигомерные фталоцианины формул с V по VII и другие олигомеры, включающие больше четырех фталоцианиновых звеньев, отвечают формуле IX
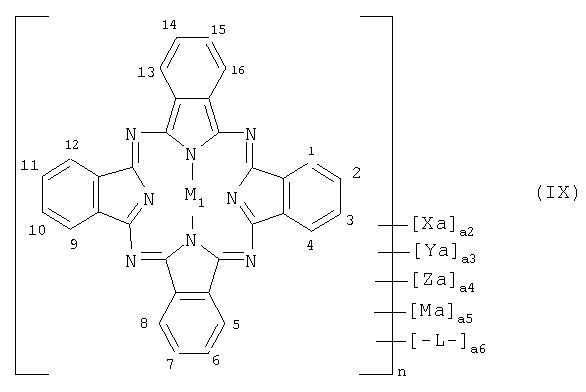
где
M1 имеет приведенные выше значения,
Ха обозначает атом галогена, такого как хлор, бром и иод, предпочтительно атом хлора или брома, Ya в предпочтительном варианте обозначает -OR1, -OOC-R2, -NHR1, -N(R1)R2, -SR1, предпочтительнее -OR1,
Za в предпочтительном варианте обозначает -СНО, -СН((OR3)OR4, -CH=N-OH, -CH=N-OR3, -CH=N-NHR5, -СН=N-N(R3)R5, -СН2OH, -(СН2)2-2-ОН, -CH2 OR3, -СН2OOC-R3, -СО-R3, -СООН или -COOR3,
Ма в предпочтительном варианте обозначает

L в предпочтительном варианте обозначает -Е2- или

где М2 и М3 каждый обозначает атом двухвалентного переходного металла, предпочтительно железа,
E1, Е2, Е3 каждый независимо друг от друга обозначает -R8(CH2)1-20R9-, -R8(COO)1-20R9-, -R8OR9-, -R8(CONR10)1-20R9-, предпочтительно -(CH2)1-8-, -(CH2)1-8(COO)1-8-, -(CH2)1-8O(CH2)1-8-, -(CH2)1-8(CONH)1-8- или -CONH-,
R1-R7 имеют указанные выше значения, R8 и R9 каждый независимо друг от друга обозначает одинарную связь, незамещенный или гало-, О-, С1-С4алкил-, С1-С4алкокси- или C1-С4алкиламинозамещенный С1-С20алкилен или С2-С20алкенилен, который может прерываться группой -О-, -СО-, -S-, -NR10-,
R10 может обозначать Н или C1-С6алкил,
R11 обозначает Н, С5-С20Циклоалкил, С2-С20алкенил, С5-С12циклоалкенил, C2-С20алкинил, С6-С18арил или С7-С18аралкил.
По еще одному особенно предпочтительному варианту предлагаются олигомерные металлоценилфталоцианины IX, предпочтительно димерные (предпочтительно для соединения V), тримерные (предпочтительно для соединения VI) и тетрамерные (предпочтительно для соединения VII) фталоцианины, у которых в предпочтительном варианте M1 обозначает Pd или Cu, Ха обозначает Cl или Br, Ya обозначает -ОСН(СНМе2)2, Ма обозначает -CH2OC(=O)Fc (Fc обозначает незамещенное ферроценовое звено, -FeCp2), a L обозначает -СН2-, -CH2ОСН2- или -CH2OC(=O)FcC(=O)OCH2-,
а2 обозначает число от 0 до 4, а3 обозначает число от 2 до 6, особенно предпочтительно 4, а4 обозначает число от 0 до 2, а5 обозначает число от 0 до 3, а6 обозначает число от 1 до 3, где сумма а5+а6 меньше или равна 3, a Ya, Ma и L в предпочтительном варианте присоединены в положениях 1, 4, 5, 8, 9, 12, 13, 16 фталоцианинового скелета формулы IX.
Особенно предпочтительными фталоцианинами формул IX и с V по VII являются:

причем мостиковые звенья в этих формулах соединяют друг с другом отдельные фталоцианиновые звенья, т.е. в частности -СН2 -О-СН2- и -CH2-, и в предпочтительном варианте мостиковые звенья L относительно алкоксигруппы (Ya) находятся в пара-положении.
В особенно предпочтительном варианте выполнения настоящего изобретения предлагается новое соединение формулы VIII или более конкретной формулы IX, в которых а1 обозначает 1, а2 обозначает ноль, Ya обозначает 2, 4-диметил-3-пентилокси, а3 обозначает 4, а4 обозначает ноль, а5 обозначает ноль, а6 обозначает 1, а L обозначает -СН2-О-СН2-, и которое отвечает конкретной формуле Ixa

где

В особенно предпочтительном варианте выполнения настоящего изобретения предлагается новое соединение формулы VIII или более конкретной формулы IX, в которых а1 обозначает 2, а2 обозначает ноль, Ya обозначает 2, 4-диметил-3-пентилокси, а3 обозначает 4, а4 обозначает ноль, а5 обозначает 1, Ма обозначает -CH2-OCO-FeCp2, а6 обозначает 1, а L обозначает -СН2-О-СН2-, и которое отвечает конкретной формуле IXb

где


В еще одном особенно предпочтительном варианте выполнения настоящего изобретения предлагается новое соединение формулы VIII или более конкретной формулы IX, в которой а1 обозначает 3, а2 обозначает ноль, Ya обозначает 2,4-диметил-3-пентилокси, а3 обозначает 4, а4 обозначает ноль, а5 обозначает 0, а6 обозначает 2, а L обозначает -СН2-О-СН2-, и которое отвечает конкретной формуле IXc

где

В другом особенно предпочтительном варианте выполнения настоящего изобретения предлагается новое соединение формулы VIII или более конкретной формулы IX, в которых а1 обозначает 3, а2 обозначает ноль, Ya обозначает 2,4-диметил-3-пентилокси, а3 обозначает 4, а4 обозначает ноль, а5 обозначает 1, Ма обозначает -CH2-OCO-FeCp2, а6 обозначает 2, а L обозначает -СН2-О-СН2-, и которое отвечает конкретной формуле IXd

где


В еще одном особенно предпочтительном варианте предлагаются смеси, включающие металлоценилфталоцианин IV и по меньшей мере один металлоценилфталоцианин IX, у которых M1 обозначает Pd, а каждый из Х и Ха обозначает Br, -L- обозначает -СН2- или -СН2ОСН2-, каждый из х и а2 обозначает число от 2 до 3, предпочтительно от 2,5 до 3, каждый из у и а3 обозначает 4, а каждый из z и а6 меньше или равен до 2, где предпочтительное содержание металлоценилфтало цианина или металлоценилфталоцианинов IX составляет от 10 до 30 мас.% в пересчете на всю смесь.
По другому особенно предпочтительному варианту предлагаются смеси, включающие металлоценилфталоцианин IV и по меньшей мере один металлоценилфталоцианин IX, у которых M1 обозначает Cu, -L- обозначает -СН2- или -СН2OCH2 -, каждый из х и а2 обозначает число от 0 до 0,3, особенно предпочтительно 0, каждый из Х и Ха обозначает Br, каждый из у и а3 обозначает 4, а каждый из z и а6 меньше или равен до 3, где предпочтительное содержание металле ценилфталоцианина или металлоценилфталоцианинов IX составляет от 20 до 50 мас.%, особенно предпочтительно от 30 до 50 мас.%, в пересчете на всю смесь.
Более того, объектом настоящего изобретения является способ приготовления смеси по изобретению реакцией смеси А, включающей
(а) от 99 до 1 мас.% фталоцианина формулы I и
(б) от 1 до 99 мас.% фталоцианина формулы II с металлоценовым производным в присутствии катализатора.
Кроме того, по настоящему изобретению предлагаются предпочтительный способ получения нового металлоценилфталоцианинового соединения IV или соединений с V по VIII их выделением из продукта взаимодействия, полученного согласно вышеописанному способу, по методу, который известен, и их выделение.
По другому варианту предлагается применение соединений или смесей по изобретению, или соединений или смесей, приготовленных согласно способам по изобретению, при изготовлении оптического носителя информации.
По другому варианту предлагается оптический носитель информации, включающий прозрачную подложку, записывающий слой на этой подложке, отражающий слой на записывающем слое и, если необходимо, защитный слой на отражающем слое, где этот записывающий слой включает смесь в соответствии с изобретением или соединение в соответствии с изобретением, или соединение или смесь, приготовленную по способу в соответствии с изобретением.
По еще одному варианту предлагается применение оптического носителя информации в соответствии с изобретением для оптической записи, хранения и воспроизведения информации, для изготовления дифракционно-оптических элементов или для хранения голограмм.
При необходимости оптический носитель информации по изобретению может включать больше одного записывающего слоя и/или больше одного отражающего или частично отражающего (полупрозрачного) слоя.
Подложка, которая служит в качестве опоры для нанесенных на нее слоев, обычно полупрозрачна (т.е. обладает прозрачностью Т по меньшей мере 10%) или, что предпочтительно, прозрачна (Т≥ 90%). Толщина этой опоры может составлять от 0,01 до 10 мм, предпочтительно от 0,1 до 5 мм.
В предпочтительном варианте записывающий слой находится между прозрачной подложкой и отражающим слоем. Толщина записывающего слоя обычно составляет от 10 до 1000 нм, предпочтительно от 50 до 500 нм, особенно предпочтительно находится в зоне 100 нм, например от 80 до 150 нм. Поглощение записывающего слоя при максимуме поглощения обычно находится в интервале от 0,1 до 2,0, предпочтительно от 0,5 до 2,0. В еще более предпочтительном варианте толщину этого слоя выбирают обычным путем как функцию соответствующего показателя преломления в незаписанном и записанном состояниях при длине волны считывания таким образом, чтобы усиливающая интерференция обуславливала незаписанное состояние и в отличие от этого ослабляющая интерференция обуславливала записанное состояние или наоборот.
В предпочтительном варианте отражающий слой, толщина которого обычно составляет от 10 до 150 нм, обладает высокой отражающей способностью (R≥70%) и низкой прозрачностью (Т≤10%).
В предпочтительном варианте самый верхний слой, например, в зависимости от многослойной структуры, отражающий слой или записывающий слой, дополнительно снабжен защитным слоем, толщина которого обычно находится в интервале от 0,1 до 1000 мкм, предпочтительно от 0,1 до 50 мкм, а особенно предпочтительно от 0,5 до 15 мкм. Этот защитный слой может также служить связующим слоем для второго слоя подложки, который на него наносят, в предпочтительном варианте обладает толщиной от 0,1 до 5 мм и состоит из того же материала, что и опорная подложка.
В предпочтительном варианте при записывающей длине волны используемого лазера отражающая способность носителя информации в целом составляет по меньшей мере 60%, особенно предпочтительно по меньшей мере 65%.
Приемлемыми подложками являются, например, стекла, минералы, керамика, а также термореактивные и термопластичные полимеры. Предпочтительными подложками являются стекла, а также гомополимеры и сополимеры. Приемлемые полимеры представляют собой, например, термопластичные поликарбонаты, полиамиды, сложные полиэфиры, полиакрилаты и полиметакрилаты, полиуретаны, полиолефины, поливинилхлорид, поливинилиденфторид, полиимиды, термореактивные сложные полиэфиры и эпоксидные смолы. Подложка может быть выполнена из чистого материала или дополнительно включает обычные добавки, например поглотители УФ-лучей или красители, как это предлагается в JP 04/167239, в качестве средств защиты записывающего слоя от светового излучения. В этом последнем случае может оказаться целесообразным добавление красителя в материал опорной подложки для достижения максимума поглощения, который гипсохромно сдвинут по меньшей мере на 10 нм, предпочтительно по меньшей мере на 20 нм относительно максимума красителя записывающего слоя.
В предпочтительном варианте подложка прозрачна в по меньшей мере части диапазона от 600 до 830 нм, вследствие чего при длине волны записи или считывания она пропускает по крайней мере 90% падающего света. У предпочтительной подложки со снабженной покрытием стороны имеется спиральная направляющая канавка, причем глубина канавки обычно составляет от 50 до 500 нм, ширина канавки обычно равна от 0,2 до 0,8 мкм, а радиальное расстояние между смежными канавками обычно находится в пределах от 0,4 до 1,6 мкм, особенно предпочтительны глубина канавки от 100 до 300 нм и ширина канавки от 0,3 до 0,6 мкм.
Вместо подложки канавка может также находиться, как это изложено в ЕР-А 392531, на самом записывающем слое.
Записывающий слой состоит исключительно или по существу из одного или нескольких фталоцианинов в соответствии с изобретением. Однако для дополнительного повышения стабильности возможно добавление в обычных количествах известных стабилизаторов, например дитиолата никеля, описанного в JP 04/025493, в качестве светостабилизатора. При необходимости можно также добавлять дополнительные красители, но целесообразно в количествах не больше 50 мас.%, предпочтительно не больше 10 мас.% в пересчете на записывающий слой. Поскольку преимущества носителей информации по изобретению зависят от фталоцианинов по изобретению, любой добавляемый целесообразный краситель характеризуется максимумом поглощения, гипсохромно сдвинутым относительно максимума для фталоцианина по изобретению, а количество добавляемого красителя должно быть настолько малым, чтобы его вклад в общее поглощение записывающего слоя в диапазоне от 600 до 830 нм не превышал 20%, предпочтительно не превышал 10%. Однако в особенно предпочтительном варианте никакого дополнительного красителя не добавляют.
Отражающими материалами, приемлемыми для получения отражающего слоя, являются, в частности, металлы, которые хорошо отражают лазерное излучение, используемое для записи и воспроизведения, например металлы третьей, четвертой и пятой основных групп и переходных групп Периодической таблицы элементов. Особенно эффективными металлами являются Al, In, Sn, Pb, Sb, Bi, Cu, Ag, Au, Zn, Cd, Hg, Sc, Y, La, Ti, Zr, Hf, V, Nb, Та, Сг, Mo, W, Fe, Co, Ni, Ru, Rh, Pd, Os, Ir, Pt и лантанидные металлы - Се, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb и Lu, а также их смеси и сплавы. По причинам высокой отражающей способности и простоте изготовления особое предпочтение отдают отражающему слою из алюминия, серебра, меди, золота или их сплавов.
Приемлемыми материалами для защитного слоя являются главным образом синтетические полимеры, которые могут быть нанесены в виде тонкого слоя либо непосредственно на подложку с помощью связующих слоев, либо самого верхнего слоя. Целесообразно выбирать механически и термически стабильные полимеры, которые обладают хорошими поверхностными свойствами и могут быть дополнительно модифицированы, например, печатью на них. Возможно применение как термореактивных полимеров, так и термопластичных полимеров. Предпочтение отдают радиационно отвержденным (например, с помощью УФ-излучения) защитным слоям, которые особенно просты и экономичны в получении. Известно большое число радиационно отверждаемых материалов. Примерами радиационно отверждаемых мономеров и олигомеров служат акрилаты и метакрилаты диодов, триолов и тетролов, полиимиды ароматических тетракарбоновых кислот и ароматических диаминов, содержащие С1-С4алкильные группы в по меньшей мере двух орто-положениях относительно аминогруппы, и олигомеры, содержащие диалкилмалеимидильные группы, например диметилмалеимидильные группы.
Носители информации по изобретению могут также иметь дополнительные слои, такие как интерференционные слои. Возможно также изготовление носителей информации, обладающих множеством записывающих слоев (например, двумя записывающими слоями). Структура и применение таких материалов специалистам в данной области техники известны. Если используют интерференционные слои, предпочтение отдают интерференционным слоям, которые находятся между записывающим слоем и отражающим слоем и/или между записывающим слоем и подложкой и состоят из диэлектрического материала, например из TiO2, Si3N4, ZnS или силиконовых смол, как это изложено в ЕР-А 353393.
Носители информации по изобретению могут быть изготовлены по методам, которые известны, с использованием применяемых для этой цели функциональных материалов и различных технологий нанесения покрытия.
Приемлемыми методами нанесения покрытия являются, например, окунание, полив, покраска, ракельное нанесение покрытия и метод нанесения покрытия центрифугированием, а также методы осаждения из паровой фазы, которые осуществляют под высоким вакуумом. Когда, например, применяют методы полива, обычно используют растворы в органических растворителях. Когда используют растворители, в предпочтительном варианте необходимо убедиться в том, что применяемые подложки нечувствительны к этим растворителям. Особое преимущество красителей по изобретению состоит в том, что они легко растворимы либо в виде чистых соединений, либо в виде смесей только небольшого числа компонентов в менее полярных растворителях, благодаря чему можно обойтись без агрессивных растворителей, таких как ацетон и сложные изомерные смеси. Приемлемые методы нанесения покрытия и растворители описаны, например, в ЕР-А 401791.
В предпочтительном варианте записывающий слой наносят с использованием раствора красителя по методу нанесения покрытия центрифугированием. Растворители, которые, как было установлено, могут быть использованы для этой цели, представляют собой, в частности, спирты, такие как 2-метоксиэтанол, циклопентанол, изопропанол, изобутанол, диацетоновый спирт, н-бутанол и амиловый спирт, предпочтительно циклопентанол, диацетоновый спирт или амиловый спирт, или предпочтительно фторированные спирты, такие как 2,2,2-трифторэтанол и 2,2,3,3-тетрафтор-1-пропанол, а также циклогексан, метилциклогексан, 2, 6-диметил-4-гептанон и диизобутилкетон или их смеси, предпочтительно амиловый спирт и 2,6-диметил-4-гептанон. Предпочтение отдают также смесям дибутилового эфира с 2,6-диметил-4-гептаноном или -гептанолом.
Особое предпочтение отдают также введению добавок, таких как поверхностно-активные вещества и закалочные среды, в частности пероксидные закалочные среды, особенно предпочтительно гидрохинонмонометиловый эфир, который обычно используют в количествах, выражаемых в частях на миллион, например в интервале от 1 до 10 част./млн.
В предпочтительном варианте металлический отражающий слой наносят напылением или осаждением из паровой фазы под пониженным давлением. Благодаря хорошей адгезии к подложке для нанесения металлического отражающего слоя особенно предпочтительна технология напыления. Эта технология всесторонне описана как в учебниках (например, J.L.Vossen и W.Kern, "Thin Film Processes", Academic Press, 1978), так и в литературе, посвященной данной области техники (например, в ЕР-А 712904), вследствие чего в изложении в настоящем описании дополнительных подробностей необходимости нет.
Структура носителя информации по изобретению обычно зависит главным образом от метода считывания; известные функциональные принципы состоят в определении изменения пропускания или, предпочтительно, отражения.
Если материал-носитель сигналограммы создают с расчетом на определение изменения отражения, существует возможность применять, например, следующие структуры: прозрачная подложка/записывающий слой (один или несколько слоев)/отражающий слой и, если это приемлемо, защитный слой (необязательно прозрачный) или подложка (необязательно прозрачная)/отражающий слой/записывающий слой и, если это приемлемо, прозрачные защитные слои. В первом случае свет приходит со стороны подложки, тогда как во втором случае излучение приходит со стороны записывающего слоя или, если имеется, защитного слоя. В обоих случаях фотоприемник находится с той же стороны, что и источник света. Для применения в соответствии с изобретением обычно предпочтительна первая структура материала-носителя сигналограммы.
Если материал-носитель сигналограммы создают с расчетом на определение изменения пропускания света, возможна, например, следующая альтернативная структура: прозрачная подложка/записывающие слои (один или несколько слоев) и, если это приемлемо, прозрачный защитный слой. Свет для записи или для считывания может приходить либо со стороны подложки, либо со стороны записывающего слоя или, если имеется, защитного слоя, причем в этом случае фотоприемник всегда находится с противоположной стороны.
Следовательно, по еще одному варианту выполнения настоящего изобретения предлагается оптический носитель информации, включающий металлоценилфталоцианин по изобретению или смесь таких соединений, или металлоценилфталоцианин, полученный в соответствии с изобретением.
По предпочтительному варианту предлагается оптический носитель информации, включающий прозрачную подложку, записывающий слой на этой подложке, отражающий слой на записывающем слое и, если это необходимо, последний защитный слой, где записывающий слой включает металлоценилфталоцианин в соответствии с изобретением или полученный в соответствии с изобретением, или смесь таких соединений.
В предпочтительном варианте запись (регистрирование, ввод) и считывание информации осуществляют с помощью лазерного луча. Приемлемыми лазерами являются, в частности, технические полупроводниковые диодные лазеры, например GaAsAl, InGaAlP, GaAs или GaN лазерные диоды, длина волны которых составляет 635, 650, 670, 680, 780 или 830 нм, или от 390 до 430 нм, или газовые/ионные лазеры, например He/Ne, Kr, HeCd или Ar лазеры, длина волны которых составляет 602, 612, 633, 647 или 442 и 457 нм.
В предпочтительном варианте запись осуществляют созданием питов варьируемой длины с помощью лазерного луча с модулированной длительностью импульса, сфокусированного на записывающий слой. Выбранная скорость записи зависит от конфигурации фокусировки и мощности лазера и может находиться, например, в интервале от 0,01 до 100 м/с, предпочтительно от 1 до 50 м/с (соответственно от 1х до 40х) или даже выше, например от 1х до 48х.
В предпочтительном варианте считывание информации осуществляют локализованным определением отражения или пропускания с использованием лазерного излучения малой мощности и фотодетектора. Особенно предпочтительно иметь возможность применять лазерное излучение с длиной волны, используемой для записи, благодаря чему отсутствует необходимость применения второго лазерного прибора. Таким образом, в предпочтительном варианте запись и считывание информации осуществляют при одинаковой длине волны. Во время считывания мощность применяемого лазера обычно уменьшают по сравнению с лазерным излучением, используемым для записи, например до уровня от одной десятой до одной пятнадцатой. В случаях материалов-носителей сигналограмм, применяемых в соответствии с изобретением, информация может быть считана один или несколько раз. В предпочтительном варианте приемлемые фотодетекторы включают PBY и AV фотодиоды, а также ПЗС (прибор с зарядной связью).
По другому варианту предлагаются записывающие слои, включающие соединения по изобретению или их смеси, а также предлагаются оптические носители информации, которые изготавливают с их использованием и для модификации спектральных свойств или цвета дополнительно включают добавки, такие как стабилизаторы и красители, причем предпочтительное содержание добавок находится в интервале от 0,001 до 20 мас.% в пересчете на записывающий слой.
Такие красители специалистам в данной области техники известны, например из EP-A 376327, и включают, например, цианины, кумарины, алантоиновые красители, азокрасители, в частности

тиазиновые красители, трифенилметановые красители, акридины, оксазины, бисазокрасители, в частности
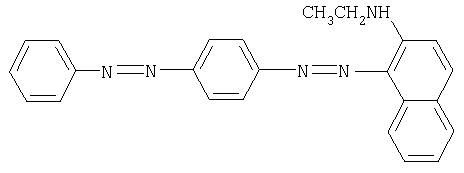
ксантены и дипирометены, которые известны из EP-A 822544.
Фталоцианины по изобретению обуславливают возможность хранения информации с высокими надежностью и стабильностью и обладают очень хорошей механической и термической стойкостью, а также проявляют высокую светопрочность и резкие края пит. Особенно выгодными свойствами являются высокое соотношение сигнал-помехи и высокая оптическая разрешающая способность, которые позволяет добиться свободных от дефектов записи и считывания сигналов даже при высокой скорости (≥4х) и одновременно с этим слабого дрожания. Носитель по изобретению представляет собой, в частности, оптический носитель информации типа ОЗМЧ. Его можно использовать, например, в качестве компакт-диска для воспроизведения на проигрывателе, в виде средств хранения информации для компьютеров и видеомагнитофонов/видеопроигрывателей, в виде идентификационной карты и пропуска или для изготовления дифракционно-оптических элементов, например голограмм.
Следовательно, еще одним объектом изобретения является применение носителя информации по изобретению для оптической записи, хранения и воспроизведения информации, для изготовления дифракционно-оптических элементов или для хранения голограмм. В предпочтительном варианте запись и воспроизведение осуществляют в диапазоне длин волн от 400 до 500 нм или, что особенно предпочтительно, от 600 до 830 нм.
По еще одному варианту выполнения настоящего изобретения предлагается применение смесей по изобретению и новых соединений формул с IXa по IXd при изготовлении средств для оптической записи со скоростью записи, превышающей или равной 8х, предпочтительно превышающей или равной 16х, особенно предпочтительно превышающей или равной 32х, а еще более предпочтительно превышающей или равной 48х.
Благодаря применению красителей по изобретению преимущество носителей информации по изобретению состоит в наличии однородных аморфных и слаборассеивающих записывающих слоев, край полосы поглощения которых в твердой фазе характеризуется крутым наклоном. Другими преимуществами являются высокая светопрочность при дневном свете и при воздействии лазерного излучения малой удельной мощности в сочетании с высокой чувствительностью к лазерному излучению высокой удельной мощности, постоянство ширины дорожки при записи, хорошая термостойкость и стабильность при хранении, а также, в частности, высокая оптическая разрешающая способность и очень слабое дрожание.
Примеры
Пример 1: 97 г тетра(α-2,4-диметил-3-пентилокси)фталоцианина меди ("вещество 1", полученное так, как изложено в ЕР 712904) совместно с 95 г N-метилформанилида вводят в 170 г хлорбензола. После нагревания смеси до 50°С в течение 4-часового периода при температуре от 48 до 52°С дозируют 107 г оксихлорида фосфора. Далее при этой температуре реакционную смесь перемешивают в течение 18 ч. После завершения реакции смесь выливают в приготовленный раствор 550 г ацетата натрия в 450 мл деионизированной воды. Реакционный сосуд ополаскивают примерно 100 мл хлорбензола. Образовавшуюся смесь (эмульсию) интенсивно перемешивают в течение 30 мин, а затем дают постоять в течение 1 ч с выключенной мешалкой, в результате чего фазы разделяются. После отделения водной фазы хлорбензольную фазу дважды промывают с использованием каждый раз 200 мл воды и под пониженным давлением обезвоживают. Хлорбензолом объем раствора доводят до 600 мл, а затем добавляют 100 г силикагеля 60. Приготовленную суспензию перемешивают при 25°С в течение одного часа и в дальнейшем фильтруют. Остаток промывают 4 раза с использованием каждый раз по 200 мл хлорбензола.
Объединенные хлорбензольные фильтраты подвергают дистилляции под пониженным давлением до остатка в 300 мл, который затем выливают в 3,5 л метанола при 25°С. Образовавшуюся суспензию охлаждают до 10°С и фильтруют. Полученный фильтровальный пирог 3 раза промывают с использованием каждый раз по 250 мл метанола, после чего 4 раза с использованием каждый раз по 500 мл деионизированной воды. В результате сушки в сушильном шкафу получают 88 г смеси моноформил-, диформил- и триформилтетра(α-2,4-диметил-3-пентилокси)фталоцианина меди ("вещество 2"), обладающего следующими свойствами: УФ/ВИД: ε=160000 л·моль-1·см-1; λмакс=712 нм (в N-МП) ВЭЖХ (площадь): исходный материал < 0,2%; моноальдегид: 68%; ди- + триальдегид: 32%
Пример 2: 88 г "вещества 2", полученного в примере 1, растворяют в 300 г тетрагидрофурана (ТГФ). После добавления 18 г метанола в течение 30-минутного периода с равномерной скоростью при 20°С дозируют суспензию 2,5 г боргидрида натрия в 30 г ТГФ.
Далее смесь перемешивают в течение еще трех часов при температуре от 20 до 25°С. После завершения этой реакции избыток NaBH4 устраняют добавлением 2,5 г безводной уксусной кислоты.
Затем реакционную смесь осветляют фильтрованием через слой 90 г силикагеля (Becosorb 1000)/ТГФ. Силикагелевый слой дважды промывают с использованием каждый раз по 90 г ТГФ и объединенные фильтраты подвергают дистилляции до остаточного объема в 300 мл.
Концентрированный раствор в течение 3-часового периода выливают с равномерной скоростью в 3,5 л воды при 25°С с одновременным интенсивным перемешиванием, полученную в виде продукта суспензию фильтруют и фильтровальный пирог промывают дейонизированной водой.
В результате сушки в сушильном шкафу при 70°С и под давлением 100 мбар получают 86 г смеси моно(гидроксиметил)-, ди(гидроксиметил)- и три(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианина меди (вещество 3), обладающего следующими свойствами: УФ/ВИД: λмакс =719 нм (в N-МП).
Когда в качестве исходного материала в примере 1 используют тетра(α-2,4-диметил-3-пентилокси)фталоцианин палладия (полученный согласно изложенному в ЕР-А 712904) с применением аналогичного метода может быть приготовлена смесь моно(гидроксиметил)-, ди(гидроксиметил)- и три(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианинов палладия.
Пример 3: 50 г вещества 3 из примера 2 вводят в 310 г толуола и перемешивают при 25°С до перехода в раствор всего твердого вещества. Далее добавляют суспензию 31 г ферроценкарбоновой кислоты в 650 г безводного ТГФ. Затем в перемешиваемую реакционную смесь в качестве катализатора вводят 0,2 г 98%-ной серной кислоты.
Реакционную смесь нагревают до кипения (примерно 74°С) и посредством колонки Вигре из реакционной смеси с равномерной скоростью в течение трехчасового периода отгоняют ТГФ. Одновременно с этим удаляют образовавшуюся во время реакции воду. Внутренней температуре дают возможность повыситься от исходных 74 до 100°С. При этой температуре дистилляцию прерывают и смесь кипятят с обратным холодильником в течение дополнительных трех часов. Затем дистилляцию возобновляют и отгонкой ТГФ в течение часового периода внутреннюю температуру повышают до 107°С. Далее реакционную смесь охлаждают до 25°С и для удаления избытка ферроценкарбоновой кислоты фильтруют через вакуум-фильтр. Остаток на фильтре дважды промывают с использованием каждый раз по 25 г толуола. В объединенные толуольные фильтраты вводят 50 г силикагеля (Becosorb 1000) и 5 г активированного угля, при 25°С смесь перемешивают в течение одного часа, фильтруют через вакуум-фильтр и остаток промывают 4 раза с использованием каждый раз по 100 мл толуола. Объединенные фильтраты подвергают дистилляции при 250 мбар до остатка в 175 г, охлаждают до комнатной температуры и для осаждения конечного продукта вводят в 1600 мл смеси метанола с 5 об.% воды при температуре от 0 до 5°С. После перемешивания в течение одного часа смесь фильтруют и фильтровальный пирог промывают три раза 140 мл холодного метанола (содержащего 5 об.% воды) и затем три раза 140 мл воды. В результате сушки в вакуумном сушильном шкафу при 80°С и 130 мбар получают продукт, обладающий следующими свойствами:
λмакс=713,5 нм (в дибутиловый эфире);
колонка ВЭЖХ: колонка С 18 с обращенной фазой подвижная фаза: градиент метанола и тетрагидрофурана детектор: 319 нм.
(а) основные компоненты: ферроценоилзамещенный моно(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианин меди из примера 2.
(б) димеры и тримеры проявляются в виде группы неразрешенных пиков после фрагментов мономеров.
Общее содержание димерных и тримерных фталоцианиновых производных (ЖХ площадь): 36%.
Когда в качестве исходного материала используют смесь моно(гидроксиметил)-, ди(гидроксиметил)- и три(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианинов палладия, которая может быть приготовлена так, как изложено в примере 2, с применением аналогичного метода может быть приготовлена смесь ферроценилзамещенных и/или этерифицированных моно(гидроксиметил)-, ди(гидроксиметил)- и три(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианинов палладия, а также их димеров и тримеров.
Когда в качестве исходных материалов используют смесь моно(гидроксиметил)-, ди(гидроксиметил)- и три(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианинов палладия, которая может быть приготовлена так, как изложено в примере 2, и вещество 2 из примера 2 в соотношении, например, 1:1, с применением аналогичного метода может быть приготовлена смесь ферроценилзамещенных и/или этерифицированных моно(гидроксиметил)-, ди(гидроксиметил)- и три(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианинов палладия и меди, а также их димеров и тримеров.
Пример 3а): 50 г бромированного моно(гидроксиметил)тетра(α -2,4-диметил-3-пентилокси)фталоцианина палладия (полученного так, как изложено в примере 2 из WO 00/09522) вводят в 310 г толуола и перемешивают при 25°С до перехода в раствор всего твердого вещества. Далее добавляют суспензию 17,2 г ферроценкарбоновой кислоты в 650 г безводного ТГФ. Затем в перемешиваемую реакционную смесь в качестве катализатора вводят 0,3 г 98%-ной серной кислоты. Реакционную смесь нагревают до кипения (примерно 74°С) и из реакционной смеси с равномерной скоростью в течение трехчасового периода отгоняют ТГФ. Одновременно с этим удаляют образовавшуюся во время реакции воду. Внутренней температуре дают возможность повыситься от исходных 74 до 113°С. Далее реакционную смесь охлаждают до 25°С и для удаления избытка ферроценкарбоновой кислоты фильтруют через вакуум-фильтр. Остаток на фильтре дважды промывают с использованием каждый раз по 25 г толуола. В объединенные толуольные фильтраты вводят 50 г силикагеля (Becosorb 1000) и 5 г активированного угля, при 25°С смесь перемешивают в течение одного часа, фильтруют через вакуум-фильтр и остаток промывают 4 раза с использованием каждый раз по 100 мл толуола. Объединенные фильтраты подвергают дистилляции при 250 мбар до остатка в 180 г, охлаждают до комнатной температуры и для осаждения конечного продукта вводят в 1800 мл ацетонитрила при температуре от 0 до 5° С. После перемешивания в течение одного часа смесь фильтруют и фильтровальный пирог промывают три раза 140 мл холодного ацетонитрила и затем три раза 140 мл воды. В результате сушки в вакуумном сушильном шкафу при 80°С и 130 мбар получают продукт, обладающий следующими свойствами: λмакс=712,5 нм (в дибутиловом эфире); колонка ВЭЖХ: колонка С18 с обращенной фазой подвижная фаза: градиент метанола/тетрагидрофурана детектор: 319 нм.
Димеры и тримеры проявляются в виде группы неразрешенных пиков после фрагментов мономерных соединений (мономеры идентичны образцу, полученному в примере 8 заявки WO 00/09522).
Общее содержание димерных и тримерных фталоцианиновых производных (ЖХ площадь): 17%.
Когда в качестве исходных материалов используют небромированный моно(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианин (полученный так, как изложено в ЕР-А 712904) с применением аналогичного метода может быть приготовлена смесь ферроценилзамещенных и/или этерифицированныхмоно(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианинов палладия и их димеров и тримеров.
Пример 3b): эксперимент примера 3 повторяют с использованием 1,2 г п-толуолсульфоновой кислоты вместо 0,2 г серной кислоты.
В результате получают продукт, обладающий следующими свойствами:
λмакс=713 нм (в дибутиловом эфире, ДБЭ);
димеры и тримеры: 32% по площади ЖХ.
Пример 4: 0,5 г (3,5 ммоль) гипохлорита кальция и 15 мл воды загружают в 25-миллилитровую круглодонную колбу и при одновременном охлаждении (0-5°С) в атмосфере инертного газа (азот) добавляют 1,5 мл уксусной кислоты. После перемешивания в течение от 2 до 3 мин получают светло-желтый раствор. В этот раствор при температуре от 0 до 5°С добавляют 3,0 г (2,4 ммоль) продукта, который описан в примере 3, в 60 мл дихлорметана. Далее смесь перемешивают при комнатной температуре в течение еще 3 ч. Реакционную смесь последовательно промывают 10%-ным раствором NaHCO3 и дважды водой, затем сушат над MgSO4, фильтруют и очищают посредством экспресс-хроматографии. Очищенный продукт растворяют в 20 мл ТГФ и осаждают добавлением воды (300 мл). Полученный таким путем зеленый осадок отфильтровывают, затем дважды промывают водой и сушат в течение ночи при 60°С/160 мбар. В результате получают 2,01 г (65%-ный выход от теоретического) хлорированной смеси ферроценилзамещенных моно(гидроксиметил)-, ди(гидроксиметил)- и три(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианинов меди, обладающих следующими свойствами: УФ/ВИД: λмакс=716,5 нм (EtOH), содержание хлора составляет 1,97%, содержание железа равно 5,1%.
ТГА (термогравиметрический анализ): точка перегиба на кривой разложения = 257°С.
Пример 5: в 250-миллилитровой круглодонной колбе, снабженной магнитной мешалкой и средством создания азотной атмосферы, в смесь 0,6 г (4,2 ммоль) гипохлорита кальция, 15 мл воды и 1,5 мл уксусной кислоты при температуре от 0 до 5°С добавляют 10 г (9,4 ммоль) продукта, который описан в примере 1, в 135 мл хлорбензола. Зеленый раствор перемешивают при комнатной температуре в течение 3 ч.
В дальнейшем смесь обрабатывают так, как изложено в примере 4. В результате получают 8,17 г (79%-ный выход от теоретического) хлорированной смеси моноформил-, диформил- и триформилтетра(α-2, 4-диметил-3-пентилокси)фталоцианинов меди, обладающей следующими свойствами: λмакс=714 нм (EtOH), содержание хлора =2,1%, ИК: полоса С=0 при 1636 см-1.
Пример 6: раствор концентрацией 2,5 мас.% "вещества 6а" (полученного так, как изложено в примерах с 1 по 3, но с использованием N-метилформанилида и POCl3 в количествах, уменьшенных на 15% в сравнении с использованными в примере 1, NaBH4 в количестве, уменьшенном на 15% в сравнении с использованными в примере 2) (при содержании олигомера 32 мас.%) в смеси трет-амилового спирта и 2,6-диметил-4-гептанона (в соотношении 90:10) фильтруют через тефлоновый фильтр, обладающий отверстиями размером 0,2 мкм, и наносят на поверхность диска толщиной 1,2 мм с нарезанной канавкой (глубина канавки: 225 нм, ширина канавки: 575 нм, шаг канавки: 1,6 мкм) по методу нанесения покрытия центрифугированием при скорости вращения 500 об/мин. Избыток раствора удаляют центрифугированием путем повышения скорости вращения. Далее равномерно нанесенный слой сушат при 70°С в конвекционном сушильном шкафу в течение 20 мин. С помощью спектрофотометра в оптической области спектра определяют характеристики спектра поглощения, причем длина волны максимума поглощения (λмакс) составляет 732 нм. В дальнейшем с помощью установки для нанесения покрытий по методу напыления в вакууме (Swivel, Balzers) на полученный записывающий слой наносят слой серебра толщиной 60 нм. Затем по методу нанесения покрытия центрифугированием на него наносят защитный слой толщиной 8 мкм из отверждаемого УФ-излучением фотополимера (650-020 из DSM). Изготовленный таким образом диск тестируют с помощью промышленного испытательного прибора (Pulstec OMT 2000) при скорости записи 4х (4,8 м/с) и устанавливают, что оптимальная мощность записи в соответствии с "Оранжевой книгой" (Optimum Power Control and Recording Conditions) составляет 13,8 мВт. Полученные результаты представлены в приведенной ниже таблице А.
Пример 7: эксперимент примера 6 повторяют с использованием "вещества 6б", полученного так, как изложено в примерах с 1 по 3, но, в отличие от примера 3, реакцию останавливают по прошествии 3 ч выдержки при 100°С и внутренней температуре не позволяют повышаться дальше уровня 100°С (содержание олигомера: 41 мас.%). В этом случае устанавливают, что максимум поглощения (λмакс) приходится на 733,3 нм, а оптимальная мощность записи составляет, как установлено, 13,1 мВт. Результаты, полученные в примерах 6 и 7, сведены в таблицу А.
Пример 8: раствор концентрацией 2,5 мас.% соединения, аналогичного "соединению 6а", которое описано в примере 6, но обладающий содержанием олигомера 30%, в смеси трет-амилового спирта и 2,6-диметил-4-гептанона (в соотношении 90:10) фильтруют через тефлоновый фильтр, обладающий отверстиями размером 0,2 мкм, и наносят на поверхность диска толщиной 1,2 мм с нарезанной канавкой (глубина канавки: 225 нм, ширина канавки: 575 нм, шаг канавки: 1,6 мкм) по методу нанесения покрытия центрифугированием при скорости вращения 500 об/мин. Избыток раствора удаляют центрифугированием путем повышения скорости вращения. Далее равномерно нанесенный слой сушат при 70°С в конвекционном сушильном шкафу в течение 20 мин. С помощью спектрофотометра при длине волны 680 нм определяют оптическую плотность слоя красителя (Dr.Schenk). В дальнейшем с помощью установки для нанесения покрытий по методу напыления в вакууме (Swivel, Balzers) на полученный записывающий слой наносят слой серебра толщиной 60 нм. Затем по методу нанесения покрытия центрифугированием на него наносят защитный слой толщиной 8 мкм из отверждаемого УФ-излучением фотополимера (650-020 из DSM).
Этот процесс изготовления повторяют при разных скоростях вращения на стадии нанесения покрытия по методу центрифугирования с получением дисков, обладающих различными оптическими плотностями. На изготовленных таким путем дисках с помощью промышленных пишущих CD-ROM при различных скоростях записи (от 1х до 12х) записывают информацию. В дальнейшем с помощью полностью автоматизированной системы для испытания компакт-дисков (CD-Cats SA3, Audio Development) для каждой скорости записи и каждой оптической плотности определяют динамические параметры сигналов и сравнивают с техническими требованиями в "Оранжевой книге". Все диски, которые полностью удовлетворяют техническим требованиям при всех скоростях записи, находятся в пределах "технологического окна". И наоборот, диски, у которых по меньшей мере один параметр не соответствует техническим требованиям, находятся вне этого окна. Ширину "технологического окна" определяют по разнице между наивысшими и самыми низкими значениями оптической плотности дисков, охватываемых "технологическим окном". В связи с этим оптическую плотность (ОПП) определяют как в 1000 раз превышающую поглощение при 680 нм (фотометр Dr.Schenk). Так, например, технологическое окно может простираться от ОПП 295 до ОПП 310 и, таким образом, характеризоваться шириной 15. Чем шире "технологическое окно", тем более толерантен процесс изготовления высококачественных дисков.
Для скоростей от 1x (Philips) до 8х (Теас) установленная ширина "технологического окна" составляет 9, тогда как для скоростей от 1x (Philips) до 12х (Plextor) установленная ширина окна равна 2.
Пример 9: эксперимент примера 8 повторяют с использованием соединения, аналогичного "соединению 6а", которое описано в примере 6, но с содержанием олигомера 37%. Ширина "технологического окна" составляет 16 для скорости от 1x до 8х и 13 для скорости от 1x до 12х (см.таблицу Б).
Пример 10: 25 г вещества, которое описано в примере 3, вводят в колонку для препаративной хроматографии [длина секции разделения: 1,2 м, диаметр: 5 см, силикагель 60 (фирма Merck), элюент: толуол] и элюируют посредством толуольного раствора. Фракции, включающие мономеры, димеры и более высокомолекулярные олигомеры, собирают по отдельности и в дальнейшем элюаты выпаривают. Осадок сушат в течение 12 ч при 60°С/165 мбар.
Длины волн максимума поглощения (20 мг/л в трет-амиловом спирте, d=0,5 см) и содержание (мас.%) связанного железа во фракциях представлены в таблице В.
Димеры состоят главным образом из фталоцианинов следующего состава

где


"Более высокомолекулярные олигомеры" представляют собой по существу тримерные соединения плюс меньшие количества тетрамеров и более высокомолекулярных олигомеров. Основная часть этой фракции состоит по существу из следующих компонентов:
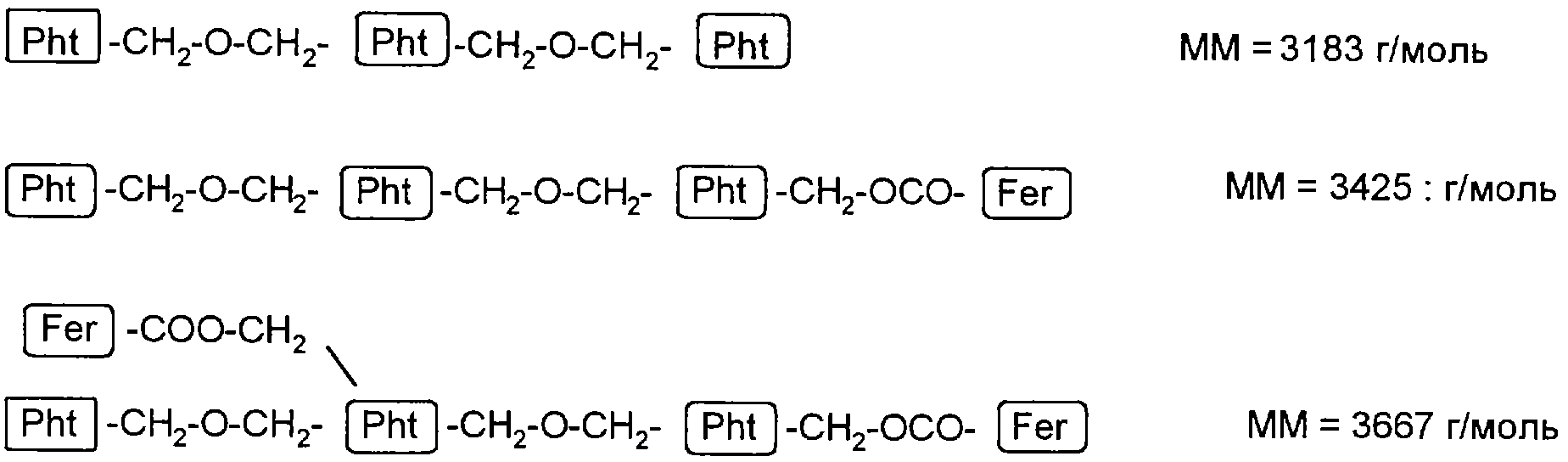
Слой вещества, которое описано в примере 3а, нанесенный аналогичным путем, характеризуется максимумом поглощения 0,58Å при λ=730 нм и поглощением 0.131Å при 780 нм.
Пример 12: 25 г вещества, которое описано в примере 3а, разделяют на фракции по методу, аналогичному использованному в примере 10. Фракцию, включающую мономеры, выбрасывают, а фракцию, включающую димеры и олигомеры, собирают и сушат. Раствор концентрацией 2 мас.% (в трет-амиловом спирте) этого вещества наносят на стеклянную подложку по методу, аналогичному использованному в примере 11, и в диапазоне длин волн видимого света 400-800 нм определяют характеристики спектра поглощения. Максимум поглощения этого вещества, включающего димеры и более высокомолекулярные полимеры, определяют как λ=737 нм в отличие от смеси, которая описана в примере 6, у которой этот параметр определяют равным 732 нм.
Пример 13: компоненты смеси ферроценоилзамещенных и/или этерифицированных медьмоно(гидроксиметил)-, -ди(гидроксиметил)- и -три(гидроксиметил)тетра(α-2,4-диметил-3-пентилокси)фталоцианиновых мономеров и олигомеров, которые описаны в примере 3, разделяют в колонке для препаративной хроматографии так, как изложено в примере 10. В дальнейшем с помощью ДСК (Mettler-Toledo Star-System, 45 мин при 35°С, от 35 до 450°С при 4°С/мин, Tiegel HP плакированный золотом 50 1) и ТГА (Mettler-Toledo Star System, от 35 до 420°С при 10°С/мин, N2 200 мл/мин, Tiegel из оксида алюминия 50 1) определяют термодинамические свойства высушенных фракций. Кривая ДСК проходит полого до примерно 200°С. Точки плавления (эндотермического) не отмечают. Специфический для фракции пик экзотермического разложения проявляется в интервале от 180 до 320°С, причем начальная температура мономеров превышает, а конечная температура оказывается ниже аналогичных температур у димеров, более высокомолекулярных олигомеров и смеси (см. таблицу Г).
Соответствующие данные ТГА для фракций, включающих смеси мономеров/димеров в соотношении 1:1 (смесь А) и смеси мономеров/более высокомолекулярных олигомеров (смесь Б) представлены в таблице Д.
Пример 14: раствор концентрацией 2 мас.% (в трет-амиловом спирте) вещества, которое описано в примере 3, наносят на стеклянную подложку с помощью метода нанесения покрытия центрифугированием и сушат при 70°С в сушильном шкафу в течение 20 мин. Слой красителя (зеленый) накрывают второй стеклянной подложкой. Затем обе стеклянные подложки скрепляют между собой с помощью металлического зажима. Пять таких образцов нагревают в печи до 240°С. Далее один из образцов извлекают и температуру повышают до 245°С, извлекают другой образец, температуру повышают до 250°С и т.д. Визуальное инспектирование холодных образцов показывает, что в интервале от 250 до 255°С слой красителя обесцвечивается (окраска меняется с зеленой на желтую). Фотометрическое определение спектра поглощения подтверждает, что в интервале от 245 до 260°С полоса поглощения длинных волн постепенно исчезает, причем наибольшее ослабление происходит в интервале от 250 до 255°С.
Вещество, описанное в примере За, проявляет аналогичные свойства обесцвечивания, но полоса поглощения исчезает при 255°С.
Пример 15: растворы концентрацией 2 мас.% (в трет-амиловом спирте) каждого из веществ, которые описаны в примере 3 и примере 3а, наносят по методу нанесения покрытия центрифугированием на гладкую (свободную от канавок) поликарбонатную дисковую подложку и сушат при 70°С в сушильном шкафу в течение 20 мин. В дальнейшем с помощью спектрометра (ЕТА Optik) в диапазоне от 390 до 1000 нм определяют характеристики спектров отражения и спектра пропускания слоя красителя, и по ним определяют комплексный показатель преломления (n-ik) в этом спектре и толщину слоя. Полученные значения при длинах волн 780 нм, (nмакс) и (kмакс) представлены в таблице Е.
Пример 16: 25 г вещества, которое описано в примере 3, разделяют на фракции по методу, аналогичному использованному в примере 10. Фракцию, включающую мономеры, выбрасывают, а фракцию, включающую димеры и более высокомолекулярные олигомеры, собирают и сушат. В дальнейшем ее используют для изготовления диска по методу, аналогичному использованному в примере 8. Установлено, что диски хорошего качества могут быть изготовлены при толщине слоя, которая меньше примерно на 10%.
Пример 17: с использованием раствора концентрацией 2 мас.% вещества, которое описано в примере 3, в смеси трет-амилового спирта и 2,6-диметил-4-гептанона (в соотношении 90:10), который предварительно фильтруют через 0, 2-микрометрический тефлоновый фильтр, по методу, аналогичному описанному в примере 6, на технологической линии (Steag) изготавливают диски типа CD-R (74-минутные) [глубина канавки: 212 нм, ширина канавки (полувысота): 565 нм, наклон стенки: 63°, отражатель: 70 нм Ag, защитный слой: 8 мкм]. Процесс центрифугирования проводят таким образом, чтобы оптическая плотность записывающего слоя составляла 360 ед. (фотометр ETA-Optik).
С применением различных промышленных устройств для записи на компакт-дисках типа CD-R (Philips CDD3600, Yahama 8424RW, Теас R558S, Panasonic CW7503, Plextor 8220, Plextor 12432, Sanyo 12x, Yahama 2100 16х) при различных скоростях записи, от 1х до 16х (Audio Tracks), на дисках производят запись и анализируют с помощью испытательной системы CDA SL100 (CD Associates). Результаты: все испытанные диски удовлетворяют техническим требованиям "Оранжевой книги".
Пример 18: с использованием раствора концентрацией 3 мас.% вещества, которое описано в примере 3а, в смеси дибутилового эфира и 2,6-диметил-4-гептанона (в соотношении 97:3), который предварительно фильтруют через 0,2-микрометрический тефлоновый фильтр, по методу, аналогичному описанному в примере 17, на технологической линии (Steag) изготавливают диски типа CD-R (74-минутные) и их испытывают. Результаты: все испытанные диски удовлетворяют техническим требованиям "Оранжевой книги".
Пример 19: для определения свойств при высоких скоростях записи на дисках, изготовленных аналогично примеру 17, в лабораторной системе (непромышленной) при различных скоростях (16х, 24х, 32х) с применением различных мощностей лазерного излучения и стратегий записи (определены в "Оранжевой книге", часть II, том 2, Multi-Speed CD-R) осуществляют запись и в дальнейшем проводят испытание. Установлены следующие оптимальные параметры записи или значения дрожания (дрожание в % от IT в среднем составляет от 3Т до 11T) (см.таблицу Ж).
Пример 20: с использованием раствора концентрацией 3 мас.% вещества, которое описано в примере 3, в смеси дибутилового эфира и 2,6-диметил-4-гептанона (в соотношении 97:3), который предварительно фильтруют через 0,2-микрометрический тефлоновый фильтр, аналогично примеру 96 изготавливают диски. На случайно выбранном диске в промышленной испытательной системе (Pulstec DUU 1000) со скоростью 48 м/с (40х) (Θ=-0,5ТΔР/Ропт=10%) осуществляют запись и в дальнейшем проводят испытания. Результаты сведены в таблицу 3 (по поводу значений параметров следует обращаться к "Оранжевой книге", часть II, том 2, Multi-Speed CD-R).
Пример 21: 2,75 мас.% вещества, которое описано в примере 3, и 0,25 мас.% вещества А растворяют в растворительной смеси дибутилового эфира и 2,6-диметил-4-гептанона (в соотношении 97:3). Раствор фильтруют через 0,2-микрометрический тефлоновый фильтр, а затем используют для изготовления дисков, обладающих записывающим слоем, который по внешнему виду бесцветен (с металлическим блеском), по методу, аналогичному использованному в примере 17. Идентичного эффекта добиваются с использованием 2,70 мас.% вещества, которое описано в примере 3а, и 0,3 мас.% вещества Б.

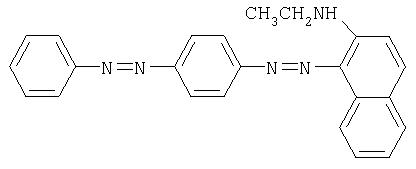
Пример 22: раствор, удаленный центрифугированием во время процесса центрифугирования при изготовлении дисков аналогично примеру 17, собирают в закрытый контейнер. По прошествии 24-часового технологического периода этот контейнер заменяют и раствор анализируют фотометрически и газовой хроматографией. После добавления тех количеств обоих растворительных компонентов, которые требуются для восстановления целевых концентраций, раствор возвращают в технологическую линию. Периодически проверяют качество дисков. После 10 циклов никаких изменений качества не обнаруживают.
Точно так же без ухудшения качества осуществляют 10 циклов возврата в технологический процесс, проводимый аналогично примерам 18 и 20.
Реферат
Описаны смеси металлоценилфталоцианинов, которые готовят реакцией смеси, включающей два фталоцианина (I) и (II) с металлоценовым производным в присутствии катализатора, а также олигомерные металлоценилфталоцианины, способ их получения, и оптический носитель информации, включающий в записывающий слой смесь по любому пп.1 или 2 или соединение по пп.3-10.

где M1 - Cu, Zn, Ni, Pd, Pt, Mn, Co, VO, MnO, TiO или H2, X - Cl, Br, Y1, Y2, R15принимают значения, указанные в п.1. 6 н. и 5 з.п. ф-лы, 8 табл.
Формула

















Комментарии