Многокартриджное устройство для введения жидкости - RU2438719C2
Код документа: RU2438719C2
Чертежи

















Описание
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА СВЯЗАННЫЕ ЗАЯВКИ
Настоящая заявка заявляет приоритет 35 U.S.C. § 119(е) предварительной заявки США серийный № 60/787616, поданной 30 марта 2006, описание которой таким образом включено в настоящее описание в виде ссылки.
Кроме того, сделаны перекрестные ссылки на патент США № 6939324, озаглавленный FLUID DELIVERY AND MEASUREMENT SYSTEMS AND METHODS; публикацию патентной заявки № US 2005/0119618, озаглавленную HYDRAULICALLY ACTUATED PUMP FOR LONG DURATION MEDICAMENT ADMINISTRATION; и заявку США № 11/219944, озаглавленную FLUID DELIVERY AND MEASUREMENT SYSTEMS AND METHODS, описание каждой из которых таким образом включено в настоящее описание в виде ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее описание относится в общем к устройствам для введения жидкости и главным образом к устройствам для введения жидкости, способным вводить один или более лекарственные препараты пациенту с получением длительного базального введения и/или болюсного введения каждого лекарственного препарата.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Устройства для введения жидкости, такие как, например, амбулаторные инфузионные насосы, разрабатывали для введения жидких лекарственных препаратов пациенту. Множество таких насосов или устройств для введения лекарственных средств способны обеспечивать и непрерывное введение («базальное введение») и кратковременные выбросы заранее определенного количества лекарственного средства («болюсное введение»), по требованию. Во множестве случаев требуется осуществлять базальное введение лекарственного средства, которое может также быть дополнено болюсным введением. Например, инсулин для лечения диабета, а также обезболивание, контролируемое пациентом, для лечения хронической боли может вводиться и с непрерывной базальной скоростью введения, а также посредством введения болюсного количества. Множество таких устройств для введения лекарственных средств являются компактными и могут фиксироваться пользователем или пациентом во время применения и впоследствии удаляться, когда лечение заканчивается.
Было осуществлено множество попыток обеспечить непрерывное или почти непрерывное базальное введение таких лекарственных препаратов с использованием различных насосных систем. Точность скорости базального введения часто варьируется, когда объем вводимого лекарственного средства небольшой. Множество устройств для введения жидкости включают резервуар, который содержит жидкий лекарственный препарат, и в них используются различные механические, газовые или электромеханические насосные или дозирующие методики для введения лекарственного препарата пациенту через иглу или другой катетер, введенные транскутанно или через кожу пациента.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение включает одну или более характеристики, указанные в приложенной формуле изобретения, или следующие характеристики или их комбинации.
В соответствии с одним аспектом описания обеспечивают устройство для введения жидкости для введения первого лекарственного препарата и второго лекарственного препарата. Устройство для введения жидкости может функционировать с обеспечением базального введения первого лекарственного препарата и/или базального введения второго лекарственного препарата. Кроме того, устройство для введения жидкости может действовать, обеспечивая болюсное введение первого лекарственного препарата и/или болюсное введение второго лекарственного препарата. Иными словами, предусматривается любая комбинация базального и/или болюсного введения каждого из первого и второго лекарственных препаратов.
Различные конфигурации базального приводного механизма устройства для введения жидкости могут обеспечивать базальное введение первого и/или второго лекарственного препарата. Например, один базальный приводной механизм может обеспечивать базальное введение только первого лекарственного препарата, только второго лекарственного препарата или и первого и второго лекарственных препаратов. В случае когда базальный приводной механизм обеспечивает базальное введение только одного из первого и второго лекарственных препаратов, второй базальный приводной механизм устройства для введения жидкости может обеспечивать базальное введение другого лекарственного препарата.
Сходным образом, различные болюсные приводные механизмы устройств для введения жидкости могут обеспечивать болюсное введение первого и/или второго лекарственного препарата. Например, один болюсный приводной механизм может обеспечивать болюсное введение только первого лекарственного препарата, только второго лекарственного препарата или и первого и второго лекарственных препаратов. В случаях, когда болюсный приводной механизм обеспечивает болюсное введение только одного из первого и второго лекарственных препаратов, второй болюсный приводной механизм устройства для введения жидкости может обеспечивать болюсное введение другого лекарственного препарата.
В соответствии с другим аспектом настоящего описания устройство для введения жидкости может включать одну или более иглы в жидкостной связи с первым и вторым резервуарами, содержащими первый и второй лекарственные препараты. Например, первая игла может быть в жидкостной связи с резервуаром, содержащим первый лекарственный препарат, тогда как вторая игла может быть в жидкостной связи с резервуаром, содержащим второй лекарственный препарат. Такие иглы могут быть разнесены друг от друга или расположены на противоположных концах устройства для введения жидкости для существенного предотвращения какого-либо смешивания первого и второго лекарственных препаратов во время введения. Кроме того, одна игла может содержать плечо введения (для подкожного введения в кожу пациента), которое длиннее плеча введения другой иглы. В таком случае один из первого и второго лекарственных препаратов будет вводиться глубже под кожу, чем другой из первого и второго лекарственных препаратов. Введение лекарственных препаратов на различную глубину также может существенно предотвращать какое-либо смешивание первого и второго лекарственных препаратов.
В соответствии с еще одним аспектом настоящего описания может быть обеспечена единственная игла, которая находится в жидкостной связи с каждым резервуаром для первого и второго лекарственных препаратов. Такая игла может быть «вилкообразной» и включать первое плечо поглощения для жидкостной связи с резервуаром, содержащим первый лекарственный препарат, и второе плечо поглощения для жидкостной связи с резервуаром, содержащим второй лекарственный препарат. Каждое из первого и второго плечей поглощения иглы могут быть в жидкостной связи с плечом введения иглы, так что первый и второй лекарственные препараты могут смешиваться друг с другом в плече введения иглы перед введением пациенту.
Иллюстративно, устройство для введения жидкости по настоящему описанию может включать наружный корпус, первый резервуар в корпусе, выполненный для содержания первого лекарственного препарата, и второй резервуар в корпусе, выполненный для содержания второго лекарственного препарата. Устройство для введения жидкости может, кроме того, включать иглу, имеющую первый конец, выполненный с возможностью жидкостной связи с первым резервуаром, и второй конец, выполненный выступающим из оболочки наружу. Альтернативно, игла может включать третий конец, выполненный с возможностью жидкостной связи со вторым резервуаром, содержащим второй лекарственный препарат. Устройство для введения жидкости может, кроме того, включать вторую иглу, имеющую первый конец, выполненный с возможностью жидкостной связи со вторым резервуаром, и второй конец, выполненный выступающим из оболочки наружу. Первая игла может быть расположена на первом конце корпуса, тогда как вторая игла может быть расположена на втором конце корпуса. Кроме того, плечо введения первой иглы может быть длиннее, чем плечо введения второй иглы.
Кроме того, иллюстративно, устройство для введения жидкости может включать базальный приводной механизм для получения базального введения первого лекарственного препарата. Такой же базальный приводной механизм также может обеспечивать базальное введение второго лекарственного препарата. Альтернативно, второй базальный приводной механизм может обеспечивать базальное введение второго лекарственного препарата. В любом случае базальный приводной механизм может включать цилиндрическую пружину, базальный пусковой поршень и резервуар гидравлической жидкости. Кроме того, устройство для введения жидкости может включать первую насосную камеру, связанную с первым лекарственным препаратом в жидкостной связи с резервуаром гидравлической жидкости первого базального приводного механизма посредством первого дросселя. Сходным образом, вторая насосная камера, ассоциированная со вторым лекарственным препаратом, может быть в жидкостной связи с резервуаром гидравлической жидкости второго базального приводного механизма посредством второго дросселя.
Далее иллюстративно, первый вводящий поршень устройства для введения жидкости может быть расположен в первом жидкостном резервуаре для оказания воздействия на первый лекарственный препарат в первом жидкостном резервуаре. Подобным образом, второй вводящий поршень может быть расположен во втором жидкостном резервуаре для оказания воздействия на второй лекарственный препарат во втором жидкостном резервуаре.
Устройство для введения жидкости может, кроме того, включать болюсный приводной механизм для обеспечения болюсного введения первого лекарственного препарата. Такой же болюсный приводной механизм также может обеспечивать болюсное введение второго лекарственного препарата. Альтернативно, второй болюсный приводной механизм может обеспечивать болюсное введение второго лекарственного препарата. В любом случае болюсный приводной механизм может включать защелку и болюсный поршень, связанный с защелкой. Насосная камера устройства для введения жидкости ассоциирована с первым жидкостным резервуаром, и болюсный поршень располагается в болюсном жидкостном резервуаре в жидкостной связи с насосной камерой.
В соответствии с другим аспектом настоящего описания способ введения первого и второго лекарственных препаратов из устройства для введения жидкости включает введение первой базальной дозы первого лекарственного препарата и введение второй базальной дозы второго лекарственного препарата. Первое базальное введение может быть приблизительно равным второму базальному введению. Альтернативно, первое базальное введение может быть больше, чем второе базальное введение.
Иллюстративно, введение первого лекарственного препарата может включать активацию первого базального приводного механизма и введение второго лекарственного препарата может подобным образом включать активацию первого базального приводного механизма. Альтернативно, введение второго лекарственного препарата может включать активацию второго базального приводного механизма, отличного от первого базального приводного механизма.
Способ может, кроме того, включать введение первой болюсной дозы первого лекарственного препарата и введение второй болюсной дозы второго лекарственного препарата. Первое болюсное введение может быть таким же, как второе болюсное введение. Альтернативно, первое болюсное введение может быть большим, чем второе болюсное введение.
Иллюстративно, введение первой болюсной дозы может включать активацию первого болюсного приводного механизма и введение второй болюсной дозы может включать активацию первого болюсного приводного механизма. Альтернативно, введение второй болюсной дозы может включать активацию второго болюсного приводного механизма, отличного от первого болюсного приводного механизма.
В соответствии с еще одним аспектом настоящего описания другой способ введения первого и второго лекарственных препаратов из устройства для введения жидкости включает (i) выталкивание гидравлической жидкости из резервуара гидравлической жидкости в первую насосную камеру для воздействия на первый подвижный барьер, (ii) выталкивание гидравлической жидкости из резервуара гидравлической жидкости во вторую насосную камеру для воздействия на второй подвижный барьер, (iii) оказание силы на первый поршень для выталкивания, по меньшей мере, части первого лекарственного препарата через отверстие первого жидкостного резервуара, и (iv) оказание силы на второй поршень для выталкивания, по меньшей мере, части второго лекарственного препарата через отверстие второго жидкостного резервуара.
Иллюстративно, выдавливание гидравлической жидкости из резервуара гидравлической жидкости может включать приложение пружинной силы к поршню в резервуаре гидравлической жидкости. Выдавливание гидравлической жидкости из резервуара гидравлической жидкости может, кроме того, включать выталкивание гидравлической жидкости из резервуара гидравлической жидкости через дроссель и в первую и вторую насосные камеры.
Устройства для введения жидкости, описанные в настоящем описании, могут быть использованы для введения большого множества лекарственных средств, фармацевтических веществ и лекарственных препаратов и других компонентов, применимых для лечения заболеваний и патологических состояний. В одном варианте осуществления изобретения устройства для введения, описанные в настоящем описании, включают, или созданы, или адаптированы к содержанию заранее выбранных лекарственных препаратов в соответствующих резервуарах. В одном аспекте заранее выбранные лекарственные препараты используют для лечения диабета и/или диабетических состояний. В другом аспекте заранее выбранные лекарственные препараты используют для лечения бактериальных инфекций и/или других заболеваний, ассоциированных с патологическими популяциями клеток. В другом аспекте заранее выбранные лекарственные препараты используют для лечения заболеваний, ассоциированных с дисфункциями нейромедиаторов, включая, но не ограничиваясь, заболевания, которые лечатся допамином и/или соединениями, которые действуют как агонисты допамина и/или антагонисты допамина.
Вышеуказанные и другие свойства настоящего описания далее будут очевидны из следующего описания и приложенных чертежей.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Подробное описание особенно относится к сопутствующим чертежам, в которых:
фиг. 1-5b являются схемами, показывающими двухкартриджные устройства для введения лекарственных средств по настоящему описанию, которые обеспечивают базальное введение и первого и второго лекарственного препарата и которые обеспечивают болюсное введение и первого и второго лекарственных препаратов;
фиг. 6-7 являются схемами, показывающими дополнительные устройства для введения лекарственных средств по настоящему описанию, которые обеспечивают базальное введение только первого лекарственного препарата и болюсное введение первого и второго лекарственных препаратов;
фиг. 8-9 являются схемами, дополнительно показывающими дополнительные устройства для введения лекарственных средств по настоящему описанию, которые обеспечивают базальное введение первого и второго лекарственных препаратов, при этом обеспечивая болюсное введение только второго лекарственного препарата;
фиг. 10-11 являются схемами, показывающими дополнительные устройства для введения лекарственных средств по настоящему описанию, которые обеспечивают базальное введение первого и второго лекарственных препаратов, при этом обеспечивая болюсное введение или первого или второго лекарственных препаратов;
фиг. 12-13 являются схемами, показывающими дополнительные устройства для введения лекарственных средств по настоящему описанию, которые обеспечивают болюсное введение первого и второго лекарственных препаратов, при этом не обеспечивая базальное введение или первого или второго лекарственных препаратов;
фиг. 14 является схемой другого устройства для введения лекарственных средств по настоящему описанию, которое обеспечивает болюсное введение только первого лекарственного препарата и базальное введение только второго лекарственного препарата;
фиг. 15 является схемой другого устройства для введения лекарственных средств по настоящему описанию, которое обеспечивает баллоноподобный резервуар для базальной жидкости, связанный с каждым из первого и второго лекарственных препаратов, и альтернативный базальный приводной механизм, связанный с соответствующими резервуарами базальной жидкости;
фиг. 16 является схемой другого устройства для введения лекарственных средств по настоящему описанию, подобного устройству, показанному на фиг. 15 и обеспечивающему единственный альтернативный базальный приводной механизм и баллоноподобный резервуар базальной жидкости для обеспечения базального введения каждого из первого и второго лекарственных препаратов;
фиг. 17 является схемой другого устройства для введения лекарственных средств по настоящему описанию, сходного с устройством, показанным на фиг. 1, где вводящий поршень, ассоциированный с каждым из первого и второго лекарственных средств фиг. 1, замещен гибкой деталью;
фиг. 18 является схемой конфигурации иглы по настоящему описанию, включающей первую и вторую иглы, имеющие вводящие плечи различной длины для введения первого и второго лекарственных препаратов на различную глубину под кожу пациента; и
фиг. 19 является схемой в целом «вилкообразной» иглы для жидкостной связи с резервуаром каждого из первого и второго лекарственных препаратов.
ПОДРОБНОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Глядя сначала на фиг. 1-5b, обеспечивают различные устройства для введения жидкости или лекарственных средств 10, 110, 210, 310, 410 и 450. Каждое из этих устройств для введения лекарственных средств 10, 110, 210, 310, 410 и 450 способно вводить первый лекарственный препарат 20 постоянно непрерывно или базальным введением или инфузией, а также одномоментное количество первого лекарственного препарата 20 для получения кратковременного пульсового или болюсного введения или инфузии. Кроме того, каждое из устройств для введения лекарственных средств 10, 110, 210, 310, 410 и 450 способно обеспечить и базальное введение второго лекарственного препарата 22, и болюсное введение второго лекарственного препарата 22. Средства, посредством которых каждое устройство вводит первый и второй лекарственные препараты, обсуждаются ниже.
Необходимо принимать во внимание, что устройства для введения жидкости, описанные в настоящем описании, каждое включают внешний или наружный корпус (не показано). Структуры, показанные на фиг. 1-17, следовательно, обычно содержатся в таком корпусе. Иллюстративно, корпус может включать различные кнопки или рукоятки, которые включает потребитель или пациент, которые активируют базальный или болюсный приводные механизмы, описанные в настоящем описании. Кроме того, как обсуждается более детально ниже, иглы 32, 34 каждого устройства для введения жидкости, показанного на фиг. 1-17, подвижны между первым, неактивированным, положением (не показано), когда вся игла содержится в наружном корпусе и/или во внешней кнопке наружного корпуса, и вторым, активированным, положением. Во втором, активированном, положении (показанном на фиг. 1-17) игла опускается так, что одна часть иглы находится в жидкостной связи с резервуаром, содержащим первый и второй лекарственные препараты 20, 22, и вторая часть иглы, например, расположена вне наружного корпуса устройства для подкожного введения пациенту. Иллюстративно, игла выполнена для, в целом, одновременного введения в один из жидкостных резервуаров (или пробку, связанную с каждым резервуаром) и пациенту. Иными словами, движение иглы из неактивированного положения в активированное положение обычно одновременно помещает первый конец иглы в жидкостную связь с ассоциированным жидкостным резервуаром, при этом вводя второй конец иглы пациенту.
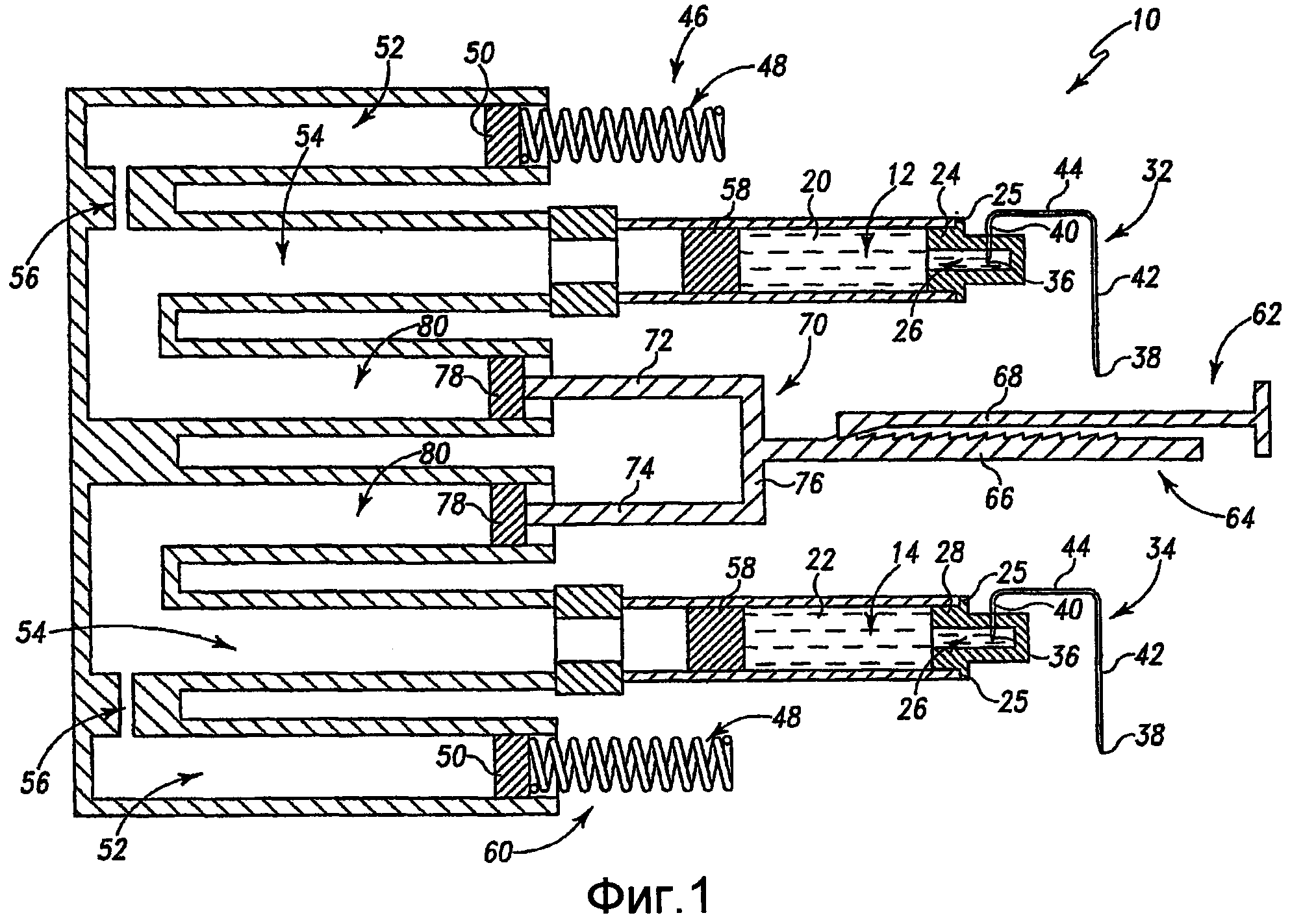
Глядя на фиг. 1, устройство для введения лекарственного средства 10 включает первый резервуар лекарственного средства, или картридж, 12 и второй резервуар лекарственного средства, или картридж, 14. По существу, устройство для введения лекарственных средств 10 (а также другие устройства для введения лекарственных средств, описанные в настоящем описании) может расцениваться как двухкартриджное устройство. Иллюстративно, первый лекарственный препарат 20 содержится в первом резервуаре 12, тогда как второй лекарственный препарат 22 содержится во втором резервуаре 14. Первая перегородка или заглушка 24 частично помещается во внутреннюю камеру первого резервуара 12, так что часть первой заглушки 24 выступает из проксимального конца 25 первого резервуара 12. Первая заглушка 24 включает полую камеру 26 в жидкостной связи с первым резервуаром 12. Подобным образом, вторая заглушка 28 частично помещается во внутреннюю камеру второго резервуара 14, так что часть второй заглушки 28 выступает из проксимального конца 25 второго резервуара 14. Вторая заглушка 28 подобным образом включает полую камеру 26 в жидкостной связи со вторым резервуаром 14. Иллюстративно, первая и вторая заглушки 24, 28, каждая могут быть сделаны из резины. Однако в рамках настоящего описания первая и вторая заглушки 24, 28 могут быть сделаны из других подходящих материалов.
Первая и вторая иглы 32, 34 устройства для введения лекарственных средств 10 каждая включают первый конец 36 и второй конец 38. Первый конец 36 каждой иглы 32, 34 проходит через наружную стенку соответствующей первой и второй заглушек 24, 28 для расположения в полой камере каждой заглушки 24, 28. Второй конец каждой иглы 32, 34 обеспечивают для подкожного введения пациенту с целью введения пациенту первого и второго лекарственных препаратов 20, 22. Иллюстративно, первая и вторая иглы 32, 34 показаны как J-образные, так что каждая игла 32, 34 включает плечо потребления 40 и плечо введения 42, которые обычно параллельны друг другу, и поперечное плечо 44, соединяющее плечи потребления и введения 40, 42 вместе. Каждое плечо 40, 42, 44 каждой иглы 32, 34 выполнено трубчатым для получения в целом непрерывного J-образного канала для возможности прохождения соответствующих первого и второго лекарственных препаратов 20, 22 из первого конца 36 каждой иглы 32, 34 во второй конец 38 каждой иглы 32, 34.
Как показано на фиг. 1, плечи 40, 42 каждой иглы 32, 34 имеют различную длину. В рамки настоящего описания, однако, включают иглы 32, 34, имеющие плечи 40, 42, 44 различной или одинаковой длины. Также в рамки настоящего описания включают конструкции игл, где один конец иглы располагается или может быть расположен в полой камере 26 одной из заглушек 24, 28 и где другой конец иглы может быть подкожно введен пациенту. Кроме того, в рамки настоящего описания включают другие инфузионные устройства для введения пациенту лекарственных препаратов 20, 22 из их соответствующих резервуаров 12, 14. Например, просвет и набор игл, набор катетеров-канюль и/или микроигла или совокупность микроигл, соединенных одним или более просветами, могут быть использованы вместо игл 32, 34. Кроме того, каждый из жидкостных резервуаров 12, 14 может включать отверстие, через которое в каждой камере вытесняются лекарственные препараты 20, 22. Обычный специалист в области техники понимает, что множество устройств могут быть использованы для подачи лекарственных препаратов в организм. Соответственно, настоящее описание не ограничивает типы устройств для инфузии или инъекции, показанные в настоящем описании.
Снова глядя на фиг.1, устройство для введения лекарственных средств 10 включает первый базальный приводной механизм 46, который обеспечивает пациенту базальное введение первого лекарственного препарата 20. Первый базальный пусковой механизм 46 включает спиральную пружину 48, прикрепленную к базальному пусковому поршню 50. Базальный пусковой поршень 50 расположен во внутренней камере базального жидкостного резервуара 52. Базальный пусковой поршень 50 является подвижным относительно стенок жидкостного резервуара 52. Насосная камера 54 находится в жидкостной связи с базальным жидкостным резервуаром 52 через соединительный канал или дроссель 56. Пружина 48 оказывает обычно постоянное воздействие на базальный пусковой поршень 50 для осуществления давления на гидравлическую жидкость в базальной жидкостной камере 52.
Приводной или вводящий поршень 58 устройства для введения лекарственных средств 10 расположен во внутренней камере резервуара 12 и действует как разделяющий или подвижный барьер между первым лекарственным препаратом, содержащимся в первом резервуаре 12, и гидравлической жидкостью, содержащейся в насосной камере 56. Иллюстративно, гидравлическая жидкость, содержащаяся в насосной камере 54 и базальном жидкостном резервуаре 52, представляет собой масло (не показано) или особенно кремниевое масло. Однако эти камеры могут быть наполнены другими несжимаемыми жидкостями, например, такими как описанные в публикации патентной заявки США US2005/0119618, описание которой таким образом включено в виде ссылки в настоящее описание.
В рабочем состоянии цилиндрическая пружина 48 первого базального приводного механизма 46 медленно распрямляется для осуществления смещения базального ведущего поршня 50, таким образом оказывая давление на гидравлическую жидкость в базальном жидкостном резервуаре 52 и насосной камере 54. Такое увеличение давления жидкости в насосной камере 54 сдвигает вводящий поршень 58 вправо (как видно в расположении на фиг. 1). Такое движение поршня 50 вызывает выталкивание некоторого количества первого лекарственного препарата 20 из резервуара 12 через иглу 32 и введение пациенту. Действие такого базального приводного механизма обсуждается более детально в публикации патентной заявки США № US 2005/0119618.
Устройство для введения лекарственных средств 10, кроме того, включает второй базальный приводной механизм 60, который обеспечивает базальное введение пациенту второго лекарственного препарата 22. Второй базальный приводной механизм 60 является таким же или сходным с первым базальным приводным механизмом 46. По существу, такие же ссылочные номера использованы для обозначения подобных компонентов. Например, второй базальный приводной механизм 60 включает цилиндрическую пружину 48, прикрепленную к базальному пусковому поршню 50. Базальный жидкостный резервуар 52 второй базальной системы находится в жидкостной связи с насосной камерой 54 через соединительный канал или дроссель 56. Подобным образом, жидкостный резервуар 52, насосный резервуар 54 и дроссель 56, ассоциированные со вторым лекарственным препаратом, каждый наполнены маслом, таким как, например, кремниевое масло. Кроме того, второй базальный приводной механизм 60 действует так же или подобно первому базальному пусковому механизму 46 для проталкивания второго лекарственного препарата 22 из второго резервуара 14 через иглу 34 и пациенту.
Как обсуждается выше, устройство для введения жидкости 10 включает два отдельных базальных пусковых механизма 46, 60 для обеспечения базального введения каждого из первого и второго лекарственных препаратов 20, 22. В рабочем состоянии единственная кнопка или рукоятка может быть активирована пользователем для запуска и первого и второго пусковых механизмов 46, 60 одновременно. Конечно, также отдельные рукояти могут быть использованы для независимого запуска каждого из пусковых механизмов 46, 60. Иллюстративно, такие кнопка(и) или рукоятка(и) могут быть расположены на или в наружном корпусе (не показано) устройства для введения жидкости 10 для активации пользователем или пациентом.
Глядя далее на фиг. 1, единственный болюсный приводной механизм 62 используется для обеспечения болюсного введения каждого из первого и второго лекарственных препаратов 20, 22. Болюсный приводной механизм 62 включает храповый механизм 64, имеющий зубчатую рейку 66 и защелку 68, находящуюся в зацеплении с зубцами зубчатой рейки 66. Зубчатая рейка 66 соединена с узлом двухголовчатого поршня 70, включая первое и второе плечи 72, 74, расположенные напротив друг друга через поперечное плечо 76, соединенное и с первым и со вторым плечами 72, 74. Иллюстративно, зубчатая рейка 66 храпового механизма 64 соединена с поперечным плечом 76. Болюсный приводной поршень 78 соединен с каждым из первого и второго плечей 72, 74 узла двухголовчатого поршня 70. Каждый из поршней 78 расположен во внутренней камере одного или пары резервуаров болюсного введения 80. Резервуары болюсного введения 80 находятся в жидкостной связи с их соответствующими насосными камерами 54.
В рабочем состоянии сила, прилагаемая к зубчатой рейке 66 продвигает узел двухголовчатого поршня 70 проталкивать жидкость из каждого болюсного жидкостного резервуара 80 в соответствующую насосную камеру 54 для движения соответствующего приводного поршня, таким образом вызывая болюсное введение и первого и второго лекарственных препаратов 20, 22 из соответствующих первого и второго резервуаров лекарственных средств 12, 14. Кнопка болюсного активатора может быть связана с зубчатой рейкой 66 так, что, когда потребитель нажимает на кнопку болюсного активатора, зубчатая рейка 66 продвигается на заранее определенное расстояние. Альтернативно, такая кнопка болюсного активатора может быть соединена с защелкой 68, так что, когда потребитель нажимает на кнопку болюсного активатора, защелка 68 продвигается на заранее определенное расстояние и способствует тому, что зубчатая рейка 66 также проходит такое же заранее определенное расстояние. При таком расположении может быть использован вторичный механизм для отведения назад защелки 68 относительно зубчатой рейки 66 в активированное положение, так что защелка 68 может быть снова выдвинута для получения другого болюсного введения. В любом случае защелка 68 запора 64 предотвращает движение зубчатой рейки 66 назад после выдвижения вперед. Кроме того, защелка 68 запора 64 предотвращает движение зубчатой рейки 66 назад из-за любого повышения давления жидкости, вызванного, например, движением жидкости из резервуаров базальной жидкости 52 в насосные камеры 54.
Как описано выше, устройство для введения жидкости 10 включает два отдельных жидкостных резервуара 12, 14, содержащие различные лекарственные препараты 20, 22. Иллюстративно, обеспечивают отдельные иглы 32, 34 для введения пациенту каждого лекарственного препарата 20, 22. Однако в рамки настоящего описания включают отдельную иглу для введения каждого из первого и второго лекарственных препаратов 20, 22. Такие варианты осуществления изобретения обсуждаются более детально ниже.
Далее глядя на фиг. 2, устройство для введения жидкости 110 является сходным с устройством для введения жидкости 10, описанным выше. По существу, такие же ссылочные номера используют для обозначения тех же или сходных компонентов. Устройство для введения жидкости 110 включает первый болюсный поршень 178, расположенный в первом болюсном резервуаре 180. Болюсный поршень 178 крупнее, чем болюсный поршень 78. Специфически, первый болюсный поршень 178 имеет диаметр D1, который больше, чем диаметр D2 второго болюсного поршня 78. По существу, болюсный поршень 178 имеет большую площадь поверхности, чем второй болюсный поршень 78. Различие в размерах между первым и вторым болюсными поршнями 78, 178 обеспечивает различное болюсное введение (например, количество или дозу вводимого лекарственного препарата) каждого из первого и второго лекарственных препаратов 20, 22 в ответ на движение узла двухголовчатого поршня 70.
Иными словами, согласованное движение поршней 78, 178 способствует перемещению различного количества жидкости из соответствующих болюсных резервуаров 80, 180 и действию на приводной поршень 58, связанный с каждым из первого и второго резервуаров 12, 14. Это вызывает приложение большего давления на поршень 58, ассоциированный с резервуаром 12, относительно давления, связанного с резервуаром 14. Это в свою очередь вызывает введение большего болюса первого лекарственного препарата 20 относительно болюсного введения второго лекарственного препарата 22. Следовательно, возрастающее движение узла двухголовчатого поршня 70 болюсного приводного механизма 62 вызовет введение пациенту большего количества первого лекарственного препарата, чем второго лекарственного препарата 22.
Во множестве обстоятельств, например, может быть предпочтительно вводить первое количество первого лекарственного препарата со вторым количеством второго лекарственного препарата. Варьирование размера болюсного приводного поршня, следовательно, позволяет варьировать соотношение двух вводимых лекарственных препаратов при болюсном введении. Иными словами, в рамках настоящего описания находится варьирование размера болюсных поршней устройства для введения жидкости, раскрытого в настоящем описании, с целью достижения любого желаемого соотношения болюсного введения между двумя лекарственными препаратами, вводимыми пациенту.
Как обсуждается более детально ниже, размер иных компонентов, связанных с устройством для введения жидкости (например, пусковых поршней, дросселей и др.), также может варьироваться с целью исходного введения первого лекарственного препарата с иной скоростью, чем второго лекарственного препарата. Также любой из этих размеров может быть изменен с целью получения желаемого соотношения между скоростью базального введения первого и второго лекарственных препаратов.
Глядя далее на фиг. 3, обеспечивают другое устройство для введения жидкости 210. Также устройство для введения жидкости 210 подобно устройствам 10, 110, описанным выше. По существу, подобные ссылочные номера использованы для обозначения подобных компонентов. Устройство для введения жидкости 210 включает первый болюсный приводной механизм 280 и второй болюсный приводной механизм 282. Каждый из первого и второго болюсных приводных механизмов 280, 282 включает запор 64, имеющий зубчатую рейку 66 и защелку 68, соединенную с зубцами зубчатой рейки 66. Каждый болюсный приводной механизм 280, 282, кроме того, включает поршень 78, соединенный с одним концом каждой зубчатой рейки 66 и расположенный во внутренней камере соответствующего болюсного жидкостного резервуара 80. По существу, характеристики болюсного введения каждого лекарственного препарата 20, 22 осуществляются независимо отдельными болюсными приводными механизмами 280, 282.
В рабочем состоянии болюсные пусковые механизмы 280, 282, могут, следовательно, быть активированы независимо для раздельного движения каждой из зубчатых реек 66 отдельных болюсных пусковых механизмов 280, 282, позволяя потребителю обеспечивать одно болюсное введение одного из лекарственных препаратов 20, 22 без осуществления болюсного введения другого лекарственного препарата 20, 22. Например, активация потребителем первого болюсного приводного механизма 280 обеспечивает болюсное введение только первого лекарственного препарата 20, тогда как активация второго болюсного приводного механизма 282 обеспечивает болюсное введение только второго лекарственного препарата 22. Конечно, болюсные пусковые механизмы 280, 282 также могут быть активированы отдельным активатором (не показано), которые способны продвигать каждую зубчатую рейку 186 одновременно.
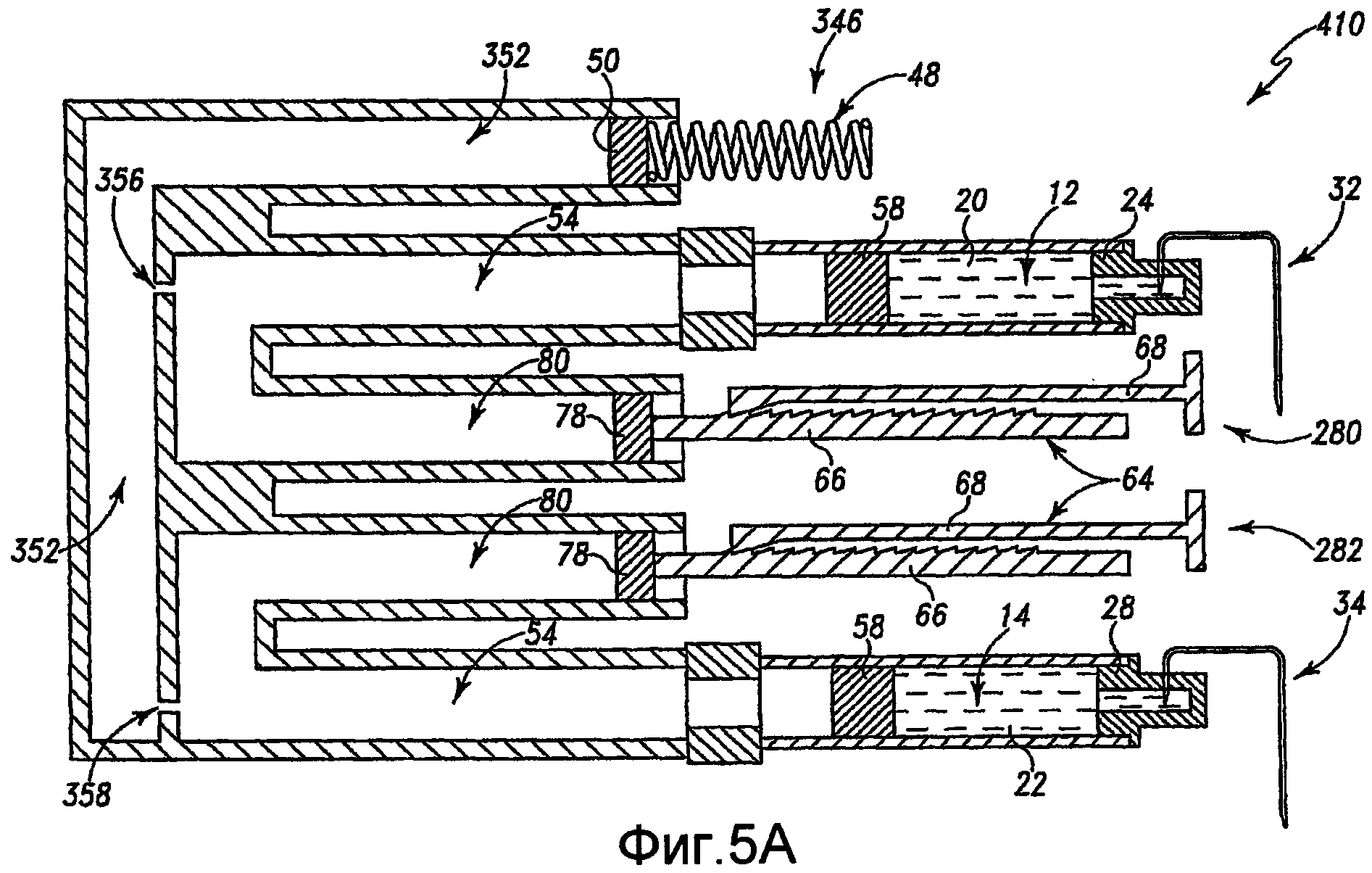
Далее глядя на фиг. 4, обеспечивают устройство для введения жидкости 310. Устройство для введения 310 подобно устройствам для введения 10, 110 и 210, описанным выше. По существу, подобные ссылочные номера использованы для обозначения подобных компонентов. Устройство для введения жидкости 310 включает единственный базальный приводной механизм 346, имеющий цилиндрическую пружину 48 и базальный приводной поршень 50. Базальный жидкостный резервуар 352 находится в жидкостной связи и с соответствующими насосными камерами 54, связанными с каждым из первого и второго резервуаров 12, 14 для лекарственных средств. Иллюстративно, первый дроссель 356 расположен между жидкостным резервуаром 352 и насосной камерой 54, ассоциированной с первым резервуаром 12. Второй дроссель 358 расположен между жидкостным резервуаром 352 и насосной камерой 54, связанной со вторым резервуаром 14. Иллюстративно, первый дроссель 356 расположен выше второго дросселя 358. В рамках настоящего описания, однако, обеспечено сходное устройство для введения жидкости, где дроссель, связанный со вторым лекарственны препаратом, расположен выше дросселя, связанного с первым лекарственным препаратом, или альтернативно, где два дросселя находятся параллельно друг другу. Иными словами, положение или расположение дросселя, ассоциированного с каждым из первого и второго базальных пусковых механизмов, при желании может быть изменено.
Единственный базальный приводной механизм 346 устройства для введения жидкости 310 обеспечивает базальное введение и первого и второго лекарственных препаратов 20, 22. Таким образом, активация приводного механизма 346 для обеспечения возможности цилиндрической пружине 48 продвигать базальный приводной поршень 50 вызывает также продвижение пусковых поршней 58. Иллюстративно, размеры (включая диаметр, или ширину, или длину) каждого из дросселей 356, 358, насосных камер 54, поршней 58 и резервуаров 12, 14 показаны обычно одинаковыми. По существу, скорость базального введения первого и второго лекарственных препаратов 20, 22 обычно является одинаковой или сходной. Однако необходимо понимать, что варьируя одно или более измерения одного ли более вышеупомянутых компонентов, связанных с любым лекарственным препаратом 20, 22, можно обеспечить устройство для введения жидкости, которое способно вводить первый лекарственный препарат 20 с первой скоростью базального введения, тогда как второй лекарственный препарат 22 вводят со второй базальной скоростью, отличной от первой базальной скорости введения. В таком случае обеспечивают такие различные скорости базального введения с применением единственного базального приводного механизма.
В соответствии с другим аспектом настоящего описания устройство для введения жидкости (не показано), сходное с устройством для введения жидкости 310 фиг. 4, может подобным образом включать отдельный базальный приводной механизм для обеспечения базального введения каждого из первого и второго лекарственных препаратов 20, 22. Однако такое устройство для введения жидкости может включать базальный жидкостный резервуар в связи с отдельной насосной камерой посредством отдельного дросселя. Хвостовой конец обычно вилкообразного поршня (не показано) может быть получен с отдельной насосной камерой, тогда как каждое разнесенное плечо вилкообразного поршня может располагаться в жидкостных резервуарах 12, 14, содержащих соответствующие лекарственные препараты 20, 22.
По существу, приводной механизм действует, выталкивая гидравлическую жидкость, такую как, кремниевое масло, например, из базального жидкостного резервуара, через дроссель, и в насосную камеру для действия на конец Y-образного поршня. Такое воздействие вилкообразного поршня способствует тому, что поршень выталкивает первый и второй лекарственные препараты 20, 22 из резервуаров 12, 14. В такой системе для введения жидкости отдельный болюсный приводной механизм может также активировать болюсное введение каждого из первого и второго лекарственных препаратов. Кроме того, плечи поршня, имеющие различный размер или различную площадь сечения относительно друг друга, обеспечивают различное базальное введение и различное болюсное введение двух лекарственных препаратов 20, 22.
Иллюстративно, устройство для введения жидкости 310, показанное на фиг. 4, включает отдельный болюсный приводной механизм 62, сходный с таковым, показанным на фиг. 1 и 2, для обеспечения болюсного введения и первого и второго лекарственных препаратов 20, 22. Однако может быть обеспечено устройство для введения жидкости, такое как устройство для введения жидкости 410, показанное на фиг. 5а, которое включает отдельный базальный приводной механизм 346, показанный на фиг. 4, и отдельные болюсные приводные механизмы 280, 282, сходные с таковыми, показанными на фиг. 3.
Кроме того, устройство для введения жидкости 450, показанное на фиг. 5b, сходно с устройством для введения жидкости 410, показанным на фиг. 5а. Например, устройство 450 подобным образом включает отдельный базальный приводной механизм 346 и обеспечивает базальное введение каждого из первого и второго лекарственных препаратов 20, 22, тогда как два отдельных болюсных приводных механизма 280, 282 обеспечивают болюсное введение каждого из первого и второго лекарственных препаратов 20, 22. Иллюстративно, однако два дросселя 356, 357 жидкостно связывают базальный жидкостный резервуар 352 с насосной камерой 54, связанный с первым резервуаром 12. Обеспечивают отдельный дроссель 358 между базальным жидкостным резервуаром 352 и насосной камерой 54, связанный со вторым резервуаром 14. Двойные дроссели 356, 357 допускают вход дополнительной гидравлической жидкости (не показано) из базального жидкостного резервуара 352 в насосную камеру 54, ассоциированную с первым резервуаром 12. По существу, на приводной поршень 58, связанный с первым резервуаром 12, оказывается большее давление, чем таковое, которое оказывается на приводной поршень 58, связанный со вторым резервуаром 14. Это в свою очередь вызывает большее базальное введение (т.е. большую скорость введения) первого лекарственного препарата 20 относительно базального введения второго лекарственного препарата 22. Могут быть обеспечены другие системы, включая любое количество дросселей, соединяющих жидкостный резервуар 352 с любой из насосных камер 54.
Как обсуждается выше, каждое из устройств для введения жидкости 10, 110, 210, 310, 410 и 450 способно обеспечивать и базальное введение и болюсное введение первого лекарственного препарата 20, а также и базальное введение и болюсное введение второго лекарственного препарата 22. Такая функция может быть осуществлена посредством различных комбинаций различных свойств этих устройств 10, 110, 210, 310, 410 и 450. Например, устройство для введения жидкости 10 включает два отдельных базальных приводных механизма и отдельный болюсный приводной механизм, способные обеспечивать болюсное введение каждого из первого и второго лекарственных препаратов 20, 22. Устройство для введения жидкости 210 по фиг. 3, с другой стороны, включает два отдельных базальных приводных механизма и два отдельных болюсных приводных механизма. Устройство для введения жидкости 310 по фиг. 4 включает только один базальный приводной механизм и один болюсный приводной механизм, тогда как устройства для введения жидкости по фиг. 5а и 5b включают отдельный базальный приводной механизм и два отдельных болюсных приводных механизма.
Как отмечено выше, устройство для введения жидкости 110 по фиг. 2 иллюстрирует различие размеров между площадью поверхности болюсных приводных поршней 178, 78, ассоциированных с каждым из первого и второго резервуаров 12, 14 с целью обеспечения различного болюсного введения каждого из первого и второго лекарственных препаратов 20, 22 с использованием отдельного болюсного приводного механизма 62. Как было упомянуто ранее, измерение(я) многих других компонентов различных устройств для введения жидкости 10, 110, 210, 310, 410 и 450 может варьироваться с целью получения устройства, где базальное и/или болюсное введение первого и второго лекарственных препаратов 20, 22 отличаются друг от друга.
Далее глядя на фиг. 6 и 7, обеспечивают устройства для введения жидкости 510 и 610. Устройства для введения жидкости 510, 610 являются сходными по природе с устройствами для введения жидкости, описанными выше на фиг. 1-5b. По существу, сходные ссылочные номера использованы для обозначения подобных компонентов. Каждое из устройств для введения жидкости 510 и 610 обеспечивает базальное введение только одного лекарственного препарата, иллюстративно, первого лекарственного препарата 20. Иными словами, ни одно из устройств для введения жидкости 510, 610, показанных на фиг. 6 и 7, не обеспечивает базальное введение второго лекарственного препарата 22. Однако обеспечивают болюсное введение каждого лекарственного препарата 20, 22. Такая конструкция может быть полезной для применения различных комбинаций первого и второго лекарственных препаратов, где базальное введение является необходимым только для одного лекарственного препарата, но где желательно болюсное введение каждого лекарственного препарата. Конечно, устройства для введения жидкости 510, 610 могут вместо этого быть выполнены с возможностью обеспечения базального введения только второго лекарственного препарата 22.
Глядя сначала на фиг. 6, устройство для введения жидкости 510 включает только один базальный приводной механизм 46 для обеспечения базального введения первого лекарственного препарата 20. Устройство для введения жидкости 510, кроме того, включает один болюсный приводной механизм 62 для обеспечения болюсного введения каждого из первого и второго лекарственных препаратов 20, 22. Устройство для введения жидкости 610 по фиг. 7 включает один базальный приводной механизм 46 для обеспечения базального введения первого лекарственного препарата 20. Устройство для введения жидкости 610, кроме того, включает первый болюсный приводной механизм 280 для обеспечения болюсного введения первого лекарственного препарата 20 и второй болюсный приводной механизм 282 для обеспечения болюсного введения второго лекарственного препарата 22. Конечно, размер(ы) множества компонентов устройств для введения жидкости 510, 610 может варьироваться с целью получения устройства, где болюсное введение первого и второго лекарственных препаратов 20, 22 отличается друг от друга.
Далее глядя на фиг. 8 и 9, обеспечивают устройства 710 и 810. Каждое из устройств для введения жидкости 710, 810 является подобным устройствам для введения жидкости, описанным выше. По существу, сходные ссылочные номера использованы для обозначения подобных компонентов. Устройства для введения жидкости 710, 810, показанные на фиг. 8 и 9, каждое обеспечивают базальное введение первого и второго лекарственных препаратов 20, 22, при этом обеспечивая болюсное введение только второго лекарственного препарата 22. Функции болюсного введения не обеспечиваются для первого лекарственного препарата 20. Конечно, устройства для введения жидкости 710, 810 могут быть модифицированы для обеспечения болюсного введения только первого лекарственного препарата 20. Такая конфигурация может быть полезной, где желательно базально вводить два различных лекарственных препарата, при этом обеспечивая болюсное введение только одного из двух лекарственных препаратов.
Сначала глядя на фиг. 8, устройство для введения жидкости 710 включает первый базальный приводной механизм 46 для обеспечения базального введения первого лекарственного препарата 20 и второй базальный приводной механизм 60 для обеспечения базального введения второго лекарственного препарата 22. Единственный механизм болюсного введения 282 обеспечивает болюсное введение второго лекарственного препарата 22. Иллюстративно, резервуар болюсной жидкости 80 находится в жидкостной связи с насосной камерой 54, связанной со вторым резервуаром 14. По существу, продвижение зубчатой рейки 66 приводного болюсного механизма 282 для продвижения болюсного приводного поршня 78 оказывает давление на приводной поршень 58 для продвижения приводного поршня 58 и для введения болюсного количества второго лекарственного препарата 22 через иглу 34.
Подобно устройству для введения жидкости 710, устройство для введения жидкости 810, показанное на фиг. 9, обеспечивает базальное введение первого и второго лекарственных препаратов 20, 22, при этом обеспечивая болюсное введение только второго лекарственного препарата 22. Базальное введение и первого и второго лекарственных препаратов 20, 22 обеспечивают посредством использования единственного базального приводного механизма 846. Первый дроссель 856 жидкостно соединяет первый жидкостный резервуар 52 и насосную камеру 54, связанную с первым резервуаром 12, тогда как второй дроссель 858 жидкостно соединяет резервуар базальной жидкости 52 и насосную камеру 54, связанную со вторым резервуаром 14.
Далее иллюстративно, базальный приводной механизм 846 расположен между насосными камерами 54 и первым и вторым резервуарами 12, 14 лекарственных средств, содержащими первый и второй лекарственные препараты 20, 22. По существу, ни один из дросселей 856, 858 не расположен выше или ниже другого. Тогда как предусматривают единственный базальный приводной механизм 846, кроме того, в рамках настоящего описания для устройства 810 для введения жидкости также предусматривается, например, включение единственного базального приводного механизма 346, показанного на фиг. 4 и 5. Болюсный приводной механизм 282 устройства 810 для введения жидкости обеспечивает болюсное введение только второго лекарственного препарата 22. Конечно, размер(ы) множества компонентов устройств 710, 810 для введения жидкости может варьироваться с целью обеспечения устройства, где базальное введение первого и второго лекарственных препаратов 20, 22 отличается друг от друга.
Далее глядя на фиг. 10 и 11, обеспечивают устройства для введения жидкости 910, 1010 по настоящему описанию. Устройства 910, 1010 являются сходными с устройствами для введения жидкости, описанными выше. По существу, подобные ссылочные номера использованы для обозначения подобных компонентов. Каждое из устройств для введения жидкости 910, 1010 обеспечивает только базальное введение и первого и второго лекарственных препаратов 20, 22. Следовательно, сначала глядя на фиг. 10, устройство для введения жидкости 910 включает первый и второй базальные пусковые механизмы 46, 60, связанные с соответствующими первым и вторым резервуарами 12, 14 для обеспечения независимого базального введения каждого из первого и второго лекарственных препаратов 20, 22. Болюсная функция и для первого и для второго лекарственных препаратов 20, 22 не обеспечивается. Иллюстративно, устройство для введения жидкости 910, показанное на фиг. 10, обеспечивает базальное введение первого и второго лекарственных препаратов 20, 22 с использованием отдельных базальных приводных механизмов 46, 60. Однако единственный базальный приводной механизм 846 может быть использован для обеспечения базального введения первого и второго лекарственных препаратов 20, 22, как показано, например, устройством для введения жидкости 1010 на фиг. 11. Также функцию болюсного введения не обеспечивают для устройства 1010 фиг. 11. Конечно, размер(ы) множества компонентов устройств для введения жидкости 910, 1010 может варьироваться с целью обеспечения устройства, где базальное введение первого лекарственного препарата 20 отличается от базального введения второго лекарственного препарата 22.
Далее глядя на фиг. 12 и 13, обеспечивают устройства для введения жидкости 1110, 1210 по настоящему описанию. Устройства 1110, 1210 являются подобными устройствам для введения жидкости, описанным выше. По существу, сходные ссылочные номера используют для обозначения подобных компонентов. Каждое из устройств для введения жидкости 1110, 1210 обеспечивает только болюсное введение и первого и второго лекарственных препаратов 20, 22 и не обеспечивает базального введения и первого и второго лекарственных препаратов 20, 22. Следовательно, сначала глядя на фиг. 12, устройство для введения жидкости 1110 включает один болюсный приводной механизм 62, ассоциированный с каждым из соответствующих первого и второго резервуаров 12, 14, для обеспечения болюсного введения каждого из первого и второго лекарственных препаратов 20, 22. Функция базального введения и для первого и для второго лекарственных препаратов 20, 22 не обеспечивается. Далее глядя на фиг. 13, устройство для введения жидкости 1210 включает первый и второй болюсные приводные механизмы 280, 282, связанные с соответствующими первым и вторым резервуарами 12, 14 для обеспечения отдельного болюсного введения каждого из первого и второго лекарственных препаратов 20, 22. Также не обеспечивают функции базального введения для каждого из первого или второго лекарственных препаратов 20, 22. Конечно, размер(ы) множества компонентов устройств для введения жидкости 1110, 1210 может варьироваться для обеспечения устройства, где болюсное введение первого лекарственного препарата 20 отличается от болюсного введения второго лекарственного препарата 22. Например, размер или диаметр одного или обоих болюсных поршней 78 может варьироваться, как показано в устройстве для введения жидкости 450 по фиг. 5b.
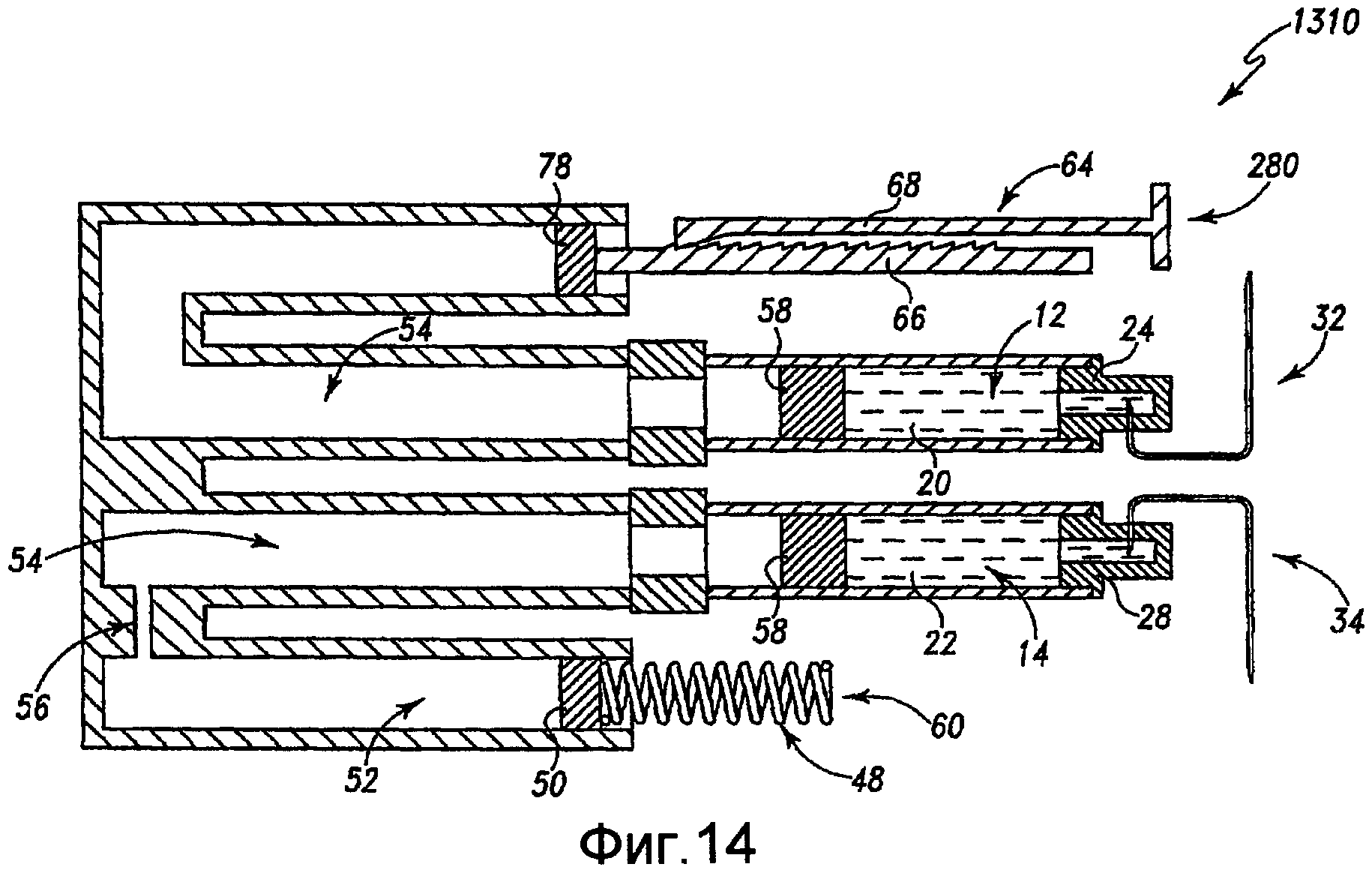
Далее глядя на фиг. 14, устройство для введения жидкости 1310 обеспечивает базальное введение второго лекарственного препарата 22 и болюсное введение первого лекарственного препарата 20. Иллюстративно, базальное введение первого лекарственного препарата 20 не обеспечиваются, тогда как не обеспечивается болюсного введения для второго лекарственного препарата 22. Такая конфигурация может быть полезной, где желательно только базальное введение первого лекарственного препарата, тогда как желательно только дополнительное болюсное введение второго лекарственного препарата. В рамках настоящего описания обеспечивают устройство для введения жидкости, способное обеспечивать базальное введение только первого лекарственного препарата 20, при этом, например, обеспечивая болюсное введение только второго лекарственного препарата 22. Иллюстративно, устройство для введения жидкости 1310, показанное на фиг. 14, включает болюсный приводной механизм 280, связанный с первым резервуаром 12, и базальный приводной механизм 60, связанный со вторым жидкостным резервуаром 14.
Устройства для введения жидкости 10, 110, 210, 310, 410, 510, 550, 610, 710, 810, 910, 1010, 1310 и 1410, описанные выше, каждое включают один или более резервуары базальной жидкости 52, 352, жидкостно связанные с одной или более насосными камерами 54 дросселем, таким как дроссели 56, 356, 357, 358, 856, 858. Иллюстративно, жидкостные резервуары 52, 352 каждый определяют внутреннюю камеру, где соответствующий базальный приводной поршень 50 определенного базального приводного механизма располагается во внутренней камере. Однако также могут быть обеспечены другие различные резервуары базальной жидкости, которые находятся в жидкостном взаимодействии с одной или более насосными камерами. Например, глядя на фиг. 15 и 16, обеспечивают устройства для введения жидкости 1410 и 1510, где каждое включает гибкий, типа баллона резервуар для введения жидкости 1452, содержащий в себе гидравлическую жидкость, такую как масло.
Глядя в особенности на фиг. 15, обеспечивают два отдельных резервуара для введения жидкости 1452, каждый из которых связан с одним из первого и второго резервуаров 12, 14. Далее обеспечивают альтернативный базальный приводной механизм 1446 для проталкивания жидкости из соответствующего базального жидкостного резервуара 1452 через дроссель 56 и в насосную камеру 54. Иллюстративно, каждый базальный приводной механизм 1446 включает шарнирно сочлененный пластинчатый элемент 1450, соединенный с соответствующим гибким базальным жидкостным резервуаром 1452. Шарнирно сочлененный пластинчатый элемент 1450 может сжиматься пружиной 1460 или иной наружной силой с целью проталкивания гидравлической жидкости из резервуара 1452 через дроссель и в насосную камеру 54 для продвижения приводного поршня 58 и обеспечения, например, базального введения первого лекарственного препарата 20. Тогда как описаны шарнирно сочлененный пластинчатый элемент 1450 и пружина 1460, кроме того, в рамках настоящего описания также предусматривается обеспечение другого подходящего приводного механизма для сжатия гибкого резервуара базальной жидкости 1452.
Как показано на фиг. 15, первый и второй базальные пусковые механизмы 1446, 1460 действуют, прессуя соответствующий гибкий резервуар базальной жидкости 1452 с целью обеспечения базального введения каждого из первого и второго лекарственных препаратов 20, 22. Альтернативно, единственный базальный приводной механизм 1446 устройства для введения жидкости 1510, показанного на фиг. 16, действует, обеспечивая базальное введение и первого и второго лекарственных препаратов 20, 22.
Иллюстративно, любое из устройств для введения жидкости, описанных в настоящем описании, может включать базальный и/или болюсный приводные механизмы, включая шарнирно сочлененную оболочку и прессуемый жидкостный резервуар, такой как показанный на фиг. 15 и 16. Также в рамках настоящего описания включены другие подходящие приводные механизмы для продвижения жидкости через дроссель. Например, газовый приводной механизм может создавать газ, такой как кислород, например, который оказывает воздействие на любой поршень, такой как базальный и болюсный приводной поршень, описанные в настоящем описании, или который оказывает воздействие на гибкую мембрану для проталкивания гидравлической жидкости через дроссель для последующего продвижения вводимого лекарственного препарата. Альтернативно, такая гибкая мембрана может непосредственно проталкивать лекарственный препарат через иглу или другое такое инфузионное устройство. Кроме того, могут быть обеспечены сжимаемые пружиной кривошип, парная роликовая установка или другой механизм для проталкивания гидравлической жидкости (например, из жидкостного резервуара) через дроссель и в насосную камеру для оказывания посредством этого давления на подвижный барьер в камере для введения лекарственного средства для выталкивания, по меньшей мере, некоторого количества жидкости из камеры для введения лекарственного средства через отверстие камеры для введения лекарственного средства.
Далее глядя на фиг. 17, обеспечивают устройство для введения жидкости 1610. Устройство для введения жидкости 1610 сходно с устройствами для введения жидкости, описанными выше. По существу, подобные ссылочные номера используют для обозначения подобных компонентов. Гибкий компонент 1658 устройства для введения жидкости 1610 заменяет приводной поршень 58 по предыдущим вариантам осуществления изобретения. Гибкий компонент 1658 способен деформироваться в ответ на давление, оказываемое на него гидравлической жидкостью, проталкиваемой в насосную камеру 54 из любого резервуара базальной жидкости 52 через дроссель 56 или из резервуара болюсной жидкости 80. Деформация гибкого компонента 1658 в резервуаре 12 проталкивает первый лекарственный препарат 20 в резервуаре 12 через иглу 32.
Иллюстративно, гибкий компонент 1658, а также поршень 58, описанный в предыдущих вариантах осуществления изобретения, действуют как барьерные механизмы между одним из лекарственных препаратов 20, 22 и гидравлической жидкостью, оказывающей давление на барьерный механизм. Хотя поршень 58 и гибкий компонент 1658 особым образом описаны в настоящем описании, в рамки настоящего описания включают другие подходящие барьерные механизмы, разделяющие лекарственный препарат 20, 22 и гидравлическую жидкость. По меньшей мере, часть таких барьерных механизмов способна двигаться во внутренней камере жидкостного резервуара относительно наружных стенок жидкостного резервуара с целью проталкивания лекарственного препарата из жидкостного резервуара. Различные другие барьерные механизмы описаны более детально в патенте США № 6969324 и публикации патентной заявки США № US2005/0119618, описание которых таким образом включено в виде ссылки в настоящее описание.
Каждое из устройств для введения жидкости, описанных выше, включает первую иглу 32 в жидкостной связи с резервуаром 12, содержащим первый лекарственный препарат 20, и вторую иглу 34 в жидкостной связи с резервуаром 14, содержащим второй лекарственный препарат 22. Такие отдельные иглы 32, 34 могут быть разнесены друг от друга на желаемое расстояние с целью предотвращения какого-либо смешивания или соединения первого и второго лекарственных препаратов 20, 22 при введении пациенту лекарственных препаратов подкожно. Часто желательно, например, предотвращать какое-либо смешивание двух различных лекарственных препаратов перед введением, во время введения и после введения пациенту лекарственных препаратов, например, если и когда могут быть проблемы совместимости между двумя лекарственными препаратами. По существу, иглы 32, 34 могут быть расположены на противоположных концах соответствующего устройства для введения жидкости с целью увеличения расстояния между двумя лекарственными препаратами, при введении каждого пациенту.
Кроме того, или в качестве альтернативы, может быть обеспечена первая игла 32 с плечом введения 142, которое существенно длиннее, чем плечо введения 42 второй иглы 34, например, как показано на фиг. 18. По существу, плечо введения 142 первой иглы 32 вставляют под кожу пациента на большую глубину, чем плечо введения 42 второй иглы 34. В таком случае первый лекарственный препарат 20 вводят под кожу пациенту на иную глубину, чем глубина, на которую вводят под кожу второй лекарственный препарат 22. Путем варьирования глубины, на которую конец введения игл 32, 34 вводят пациенту, может быть по существу предотвращено смешивание первого и второго лекарственных препаратов 20, 22 при введении пациенту.
Иллюстративно, следовательно, отдельные иглы 32, 34 могут быть использованы для отдельного введения первого и второго лекарственных препаратов 20, 22. В обстоятельствах, когда могут быть проблемы совместимости между двумя лекарственными препаратами 20, 22, иглы 32, 34 могут быть разнесены друг от друга на подходящее расстояние для существенного предотвращения какого-либо смешивания лекарственных препаратов 20, 22 во время или после введения пациенту лекарственных препаратов 20, 22. Кроме того, или в качестве альтернативы, иглы 32, 34 могут быть введены пациенту на различную глубину для дополнительного предотвращения какого-либо смешивания лекарственных препаратов 20, 22 во время или после введения лекарственных препаратов 20, 22.
Снова глядя на фиг. 18, обеспечивают заглушку иглы 200, которая иллюстративно охватывает в себе обе иглы 32, 34. По существу, активация заглушки иглы 200 потребителем или пациентом активирует обе иглы 32, 34 одновременно. Иллюстративно, в рабочем состоянии иглы 32, 34 расположены в первом, неактивированном, положении (не показано), посредством чего потребляющее плечо 40 каждой иглы 32, 34 разносится от соответствующих заглушек 24, 28. Кроме того, плечо введения 142, 42 каждой иглы 32, 34 содержится в наружной оболочке (не показано) устройства для введения жидкости. С целью перемещения игл в активированное положение потребитель нажимает кнопку 200 для опускания каждой иглы 32, 34, так что плечо потребления 40 каждой иглы 32, 34 прокалывает соответствующую заглушку 24, 28 и приходит в жидкостную связь с внутренней камерой 26, содержащей соответствующие первое и второе лекарственные препараты 20, 22, как показано на фиг. 1-17, например. Кроме того, в активированном положении дистальный конец 38 плеча введения 142, 42 каждой иглы 32, 34 простирается за наружную оболочку вводящего устройства для подкожного размещения у пациента. Хотя на фиг. 18 показана одиночная заглушка иглы 200, в рамки настоящего описания включают отдельные кнопки крышки иглы, связанные с каждой иглой 32, 34, так что иглы 32, 34 могут быть активированы отдельно.
Далее глядя на фиг. 19, обычно обеспечиваются Y-образная игла 232, и она может быть использована с одним или более устройствами для введения, описанными в настоящем описании. Иллюстративно, игла 232 включает единственное плечо введения 242, первое плечо потребления 244, отнесенное от и иллюстративно параллельное плечу введения 242, и второе плечо потребления 246, отнесенное от и иллюстративно также параллельное плечу введения 242. Соответствующее первое и второе поперечное или соединительное плечо 248, 250 соединяет каждое из плеч потребления 244, 246 с плечом введения 242. Игла 232 выполнена трубчатой для получения непрерывного канала, простирающегося через каждое из плечей 242, 244, 246, 248, 250. В активированном положении первый конец 36 каждого плеча потребления 244, 246 проходит через наружную стенку соответствующей первой и второй заглушек 24, 28 различных устройств для введения жидкости, описанных в настоящем описании. По существу, первый конец 36 каждого плеча потребления 244, 246 расположен в полой камере 26 каждой заглушки 24, 28, когда игла 232 находится в активированном положении. Второй конец плеча введения 242 иглы 232 обеспечивают для подкожного введения пациенту с целью введения пациенту первого и второго лекарственных препаратов 20, 22.
Иллюстративно, игла 232 позволяет смешивать первый и второй лекарственные препараты 20, 22 друг с другом перед введением пациенту. Например, первый лекарственный препарат 20 может входить в плечо потребления 244 иглы 232 и проходить по поперечному плечу 248 в плечо введения 242. Второй лекарственный препарат 22 может подобным образом входить в плечо потребления 246 иглы 232 и проходить по поперечному плечу 250, смешиваясь с первым лекарственным препаратом 20, в плече введения 242. Игла 232 может быть использована с различными устройствами для введения, где первый и второй лекарственные препараты, содержащиеся в таких устройствах для введения, совместимы друг с другом и могут быть смешаны перед введением пациенту. Конечно, при отдельных базальных и болюсных механизмах введения могут быть обстоятельства, где только один лекарственный препарат 20 или только второй лекарственный препарат 22 будет вводиться через иглу 232.
Тогда как Y-образная игла 232 описана в настоящем описании для использования с совместимыми лекарственными препаратами, способными для смешивания, необходимо понимать, что могут быть использованы другие подходящие иглы, которые позволяют лекарственным препаратам смешиваться друг с другом после выхода из жидкостных резервуаров, в которых каждый хранится. Например, необходимо понимать, что Y-образные охватывают Т-формы. Кроме того, иллюстративно, на фиг. 19 показана заглушка 252 как покрывающая и сохраняющая иглы 232 в неактивированном положении до нажатия или активации кнопки 252 потребителем или пациентом. Кроме того, при нажатии на заглушку 252 игла 232 может быть выдвинута в активированное положение для возможности поступления жидкости из первого и второго резервуаров 12, 14 в соответствующие плечи потребления 244, 246.
В соответствии с одним аспектом настоящего описания устройство для введения жидкости может включать множество резервуаров для лекарственных средств для содержания и введения множества различных лекарственных препаратов. Например, тогда как устройства для введения жидкости, описанные выше и показанные на фиг. 1-17, включают первый и второй лекарственные препараты 20, 22, содержащиеся в первом и втором резервуарах 12, 14, в рамки настоящего описания включают устройство для введения жидкости, имеющее третий лекарственный препарат, содержащийся в третьем резервуаре. Отдельный или общий базальный приводной механизм может быть связан с третьим резервуаром, содержащим третий лекарственный препарат, тогда как отдельный или совместный болюсный приводной механизм также может быть связан с третьим резервуаром, содержащим третий лекарственный препарат. Кроме того, совместная или отдельная игла также может быть связана с каждым из первого, второго и третьего лекарственных препаратов для введения каждого лекарственного препарата отдельно или вместе. Подобным образом, в рамках настоящего описания включают устройство для введения жидкости, имеющее более чем три лекарственных препарата, каждый содержащийся в отдельных жидкостных резервуарах.
В соответствии с другим аспектом настоящего описания устройства для введения, описанные в настоящем описании, являются относительно компактными, портативными и могут быть фиксированы потребителем или пациентом во время применения и впоследствии сняты, когда лечение заканчивается. Конечно, другие такие непортативные и неснимаемые устройства для введения включены в рамки настоящего описания также.
В соответствии с еще одним аспектом настоящего описания устройство для введения жидкости, описанное в настоящем описании, выполнено с возможностью введения двух различных лекарственных препаратов 20 и 22. В одном варианте осуществления изобретения первый и второй лекарственные препараты 20, 22 выбирают как предназначенные для лечения двух различных заболеваний, которые могут возникнуть в совместном патологическом состоянии. В другом варианте осуществления изобретения первый и второй лекарственные препараты 20, 22 выбирают как предназначенные для лечения двух различных симптомов, которые могут присутствовать при отдельном заболевании. В другом варианте осуществления изобретения первый и второй лекарственные препараты 20, 22 выбирают как предназначенные для лечения того же заболевания и/или симптома, где такая комбинация таких двух или более лекарственных препаратов может быть предусмотрена или желательна.
В другом варианте осуществления изобретения первый и второй лекарственные препараты 20, 22 выбирают как предназначенные для лечения патологического состояния, когда, например, один из первого или второго лекарственных препаратов 20, 22 вызывает нежелательные или неблагоприятные побочные эффекты или другие нежелательные явления и другой из первого и второго лекарственных препаратов 20, 22 опосредует, облегчает или смягчает такие побочные эффекты или нежелательные явления.
В другом варианте осуществления изобретения первый и второй лекарственные препараты 20, 22 выбирают как адаптированные для лечения патологического состояния, где эффективность или действие одного из первого или второго лекарственного препарата 20, 22 усиливается или улучшается путем совместного введения другого из первого или второго лекарственных препаратов 20, 22. Усиление эффективности может быть аддитивным или синергичным или может исправлять или опосредовать сенсибилизацию, десенсибилизацию или переносимость, которые могут сопровождать применение одного из первого или второго лекарственных препаратов 20, 22. Принимают во внимание, что такое усиление или улучшение может приводить к снижению общего количества лекарственного препарата, чья эффективность или действие усиливаются.
Понимают, что устройства, описанные в настоящем описании, могут позволить совмещать два лекарственных препарата, которые иным образом не могут быть введены в одной лекарственной форме обычными средствами. Например, определенные пары лекарственных препаратов могут не быть доступными в обычных лекарственных формах из-за химической несовместимости, различных требований к стабильности, различных требований к рецептированию и других параметров оптимизации, необходимых для эффективности. Кроме того, определенные пары лекарственных препаратов могут не иметь возможности существования в обычных стандартных лекарственных формах из-за необходимости гибкого изменения соотношения первого и второго лекарственных препаратов. Предполагают, что обычные лекарственные формы потребуют фиксированного соотношения. Кроме того, определенные пары лекарственных препаратов могут не иметь возможности существования в обычных стандартных лекарственных формах из-за сложной схемы введения, требующей изменять введение в течение заранее определенного периода времени. Также необходимо понимать, что хотя выше описывают пары лекарственных средств, такие аспекты применяются равным образом в вариантах осуществления изобретения устройств для введения, описанных в настоящем описании, которые созданы для введения трех или более лекарственных препаратов.
В одном варианте осуществления изобретения устройства, описанные в настоящем описании, выполнены с возможностью введения лекарственных препаратов для лечения диабета, включая диабет I и II типа, симптомов диабета и диабетических состояний.
В одном варианте осуществления изобретения первым или вторым лекарственным препаратом является инсулин или аналог инсулина, и другим лекарственным препаратом 20, 22 является лекарственное средство, выбираемое для улучшения действия или уменьшения профиля побочных эффектов инсулина или аналога инсулина. Необходимо понимать, что первый и второй лекарственные препараты 20, 22 могут каждый относиться к инсулину или его аналогу. Например, как используется в настоящем описании, аналоги инсулина включают проинсулин, преинсулин и инсулины, которые модифицированы различными аминокислотами, такими как вставки, делеции и замещения. Устройства, описанные в настоящем описании, включают различные варианты, такие как присутствие или отсутствие болюсного и/или базального введения, относительный размер болюсного введения и относительная скорость базального введения и другие характеристики. Соответственно, в некоторых вариантах осуществления устройств инсулин или аналог инсулина является первым лекарственным препаратом 20, тогда как в других вариантах осуществления инсулин или аналог инсулина является вторым лекарственным препаратом 22. Соответственно, как используется на всем протяжении описания, первый лекарственный препарат 20 и второй лекарственный препарат 22 могут быть взаимозаменены с определением лекарственного препарата для различных конфигураций и вариантов осуществления устройств, описанных в настоящем описании.
В другом варианте осуществления изобретения и естественные и синтетические инсулины и аналоги инсулина могут быть использованы в качестве первого и второго лекарственных препаратов 20, 22. В одном аспекте используемые инсулины имеют естественное происхождение, такие как естественные инсулины и их аналоги, включая, но не ограничиваясь, полученные с использованием рекомбинантных методик из других организмов, таких как бактерии. В другом аспекте используемыми инсулинами являются синтетические инсулины, или модифицированные инсулины, включая модификации аминокислотной цепи, такие как вставки, делеции и замены в последовательности инсулина. Иллюстративно, инсулинами являются инсулин Лизпро, инсулин Аспарт, инсулин Гларгин, инсулин Детемир и подобные. Кроме того, инсулины включают, но не ограничиваются, вставки аминокислот, делеции аминокислот и замены аминокислот от человека и других источников. Понимают, что такие модификации могут быть сделаны в А- или В-цепи. Иллюстративно, инсулины могут быть включены в настоящее описание в качестве лекарственных препаратов 20, 22, где Asp28 на В цепи замещен, например, Pro28 или Lys28; где Lys29 в В-цепи замещен Pro29 или Glu29; где В-цепь продлена, например, Arg31 или Arg31-Arg32; где Asn21 на А-цепи замещен, например, Gly21; где Asn3 на В-цепи замещен, например, Lys3; и подобные модификации.
В другом аспекте инсулины, используемые в качестве лекарственных препаратов в настоящем описании, являются инсулинами промежуточного действия, включая, но не ограничиваясь, HUMULIN L, HUMULIN N, NOVOLIN N, NOVOLIN R и подобные. В другом аспекте инсулины, используемые в качестве лекарственных препаратов в настоящем описании, являются инсулинами быстрого действия, включая, но не ограничиваясь, APIDRA, HUMALOG HUMULIN R, NOVOLIN R, NOVOLOG и подобные. В другом аспекте инсулины, используемые в качестве лекарственных препаратов в настоящем описании, являются инсулинами длительного действия, включая, но не ограничиваясь, HUMULIN U, LANTUS и подобные. В другом аспекте инсулины, используемые в качестве лекарственных препаратов в настоящем описании, являются смесями различных инсулинов, включая, но не ограничиваясь, HUMALOG MIX 75/25, HUMULIN 50/50, HUMULIN 70/30, NOVOLIN 70/30, NOVOLOG MIX 70/30 и подобные.
В одном варианте оба лекарственных препарата 20, 22 являются инсулинами. Принимают во внимание, что более различные смеси инсулинов могут вводиться определенным пациентам с использованием вариантов, где первый лекарственный препарат 20 является одним инсулином и второй лекарственный препарат 22 является другим инсулином. Понимают, что могут быть выбраны инсулины, чтобы соответствовать нуждам различных субпопуляций пациентов, для которых легкодоступные заранее смешанные инсулины являются менее желательными, или где смешивание инсулинов нежелательно. В другом аспекте первым инсулином является инсулин длительного действия, такой как HUMULIN U, LANTUS и подобные, и вторым инсулином является инсулин средней или короткой продолжительности действия, как описано в настоящем описании. В одной конфигурации устройство выбирают так, что оба и первый и второй лекарственные препараты 20, 22 являются преимущественно или исключительно вводимыми пациенту болюсно, скорее, чем базально. При такой конфигурации понимают, что, например, инсулин длительного действия может вводиться в виде болюсного количества один раз в день и инсулин короткой или средней продолжительности действия вводят в болюсном количестве перед приемом пищи. В одном варианте предусматривают, что инсулин короткого или промежуточного действия может вводиться базально, или в другом варианте инсулин короткого или промежуточного действия может вводиться базально в течение укороченного периода времени в соответствии со временем приема пищи.
В альтернативном варианте осуществления изобретения другой лекарственный препарат 20, 22 может быть включен для увеличения эффективности, улучшения действия или снижения профиля побочных эффектов инсулина или аналога инсулина, используемого в качестве лекарственного препарата. Механизмами для такого увеличения эффективности инсулина или улучшения действия могут быть любые, включая улучшение продукции эндогенного инсулина, снижение инсулинорезистентности или нечувствительности к инсулину, улучшение утилизации инсулина и глюкозы периферическими тканями, увеличение потребления глюкозы периферическими тканями, снижение количества или замедление скорости продукции эндогенного сахара в определенных органах, включая, но не ограничиваясь, печень, снижение количества или замедление скорости абсорбции сахара в желудочно-кишечном тракте и подобное.
В одной конфигурации другие лекарственные препараты представляют собой инкретин, инкретиномиметик или аналог инкретина, такие как глюкагоноподобный пептид (GLP), аналог GLP-1, экзенатид (BYETTA, Amylin, Lilly), Экзендин-4 и подобные. Инкретиномиметики и/или аналоги инкретина могут действовать аналогично глюкагоноподобному пептиду -1 (GLP-1), естественному пептиду, который усиливает секрецию инсулина в ответ на повышение уровня глюкозы плазмы, могут быть включены в качестве вспомогательных лекарственных средств. Понимают, что система GLP-1 увеличивает секрецию инсулина только в присутствии повышенного уровня глюкозы плазмы, избегая несоответствующих высоких уровней инсулина во время голодания. Принимают во внимание, что инкретины могут усиливать глюкозозависимую секрецию инсулина и проявлять другие антигипергликемические действия после их высвобождения в циркуляцию. Инкретины также могут сглаживать пиковые уровни глюкагона сыворотки во время периодов гипергликемии после приема пищи, не вмешиваясь в высвобождение глюкагона в ответ на гипогликемию. Инкретины также могут иметь полезные вторичные эффекты снижения скорости опустошения желудка и снижения потребления пищи, уменьшая потенциальную тяжесть гипергликемических явлений после приема пищи. В одном варианте осуществления изобретения устройства, описанные в настоящем описании, включают суточную дозу BYETTA в диапазоне от около 5 до около 10 микрограмм. В вышеуказанной конфигурации принимают во внимание, что устройства могут быть выбраны так, чтобы иметь отдельную иглу для каждого из резервуаров, содержащих лекарственные препараты 20, 22, так что в или необязательно около места инъекции не возникает существенного смешивания двух лекарственных препаратов.
В другой конфигурации другим лекарственным препаратом является пептид амилин, такой как прамлинтид (SIMLYN, Amylin). Понимают, что дефицит инсулина может сопутствовать дефициту амилина. Амилин может оказывать моделирующий эффект на поглощение глюкозы из желудка в кровь, замедление и ведение притока глюкозы из пищи, регуляцию секреции глюкагона поджелудочной железой и, следовательно, регуляцию продукции глюкозы печенью. В вышеуказанной конфигурации принимают во внимание, что могут быть выбраны устройства, которые содержат отдельные иглы для каждого из резервуаров, содержащих лекарственные препараты 20, 22, так что в или необязательно около мест инъекции не возникает существенного смешивания двух лекарственных препаратов.
В другой конфигурации другим лекарственным препаратом является бигуанид или комбинация бигуанидов. В одном иллюстративном аспекте бигуанидом является метформин (GLUCOPHAGE, FORTAMET, RIOMET). В другом иллюстративном аспекте бигуанид является ингибитором продукции глюкозы печенью. В другом аспекте бигуанид является ингибитором поглощения глюкозы в желудочно-кишечном тракте. Принимают во внимание, что бигуаниды могут увеличивать эффективность инсулинотерапии путем снижения продукции глюкозы печенью, снижения поглощения глюкозы в кишечнике и/или увеличения периферического потребления и утилизации глюкозы. В одном варианте фармацевтически приемлемые соли таких лекарственных препаратов включают в устройства, описанные в настоящем описании.
В другой конфигурации другим лекарственным препаратом является ингибитор глюкозидазы, такой как акарбоза (PRECOSE, Bayer) и подобные. Принимают во внимание, что ингибиторы глюкозидазы могут увеличивать эффективность инсулинотерапии путем замедления гидролиза комплексных углеводов до глюкозы в поджелудочной железе и/или кишечнике.
В другой конфигурации другим лекарственным препаратом являются препараты сульфонилмочевины, такие как амарил глимепирид (AMARYL, Aventis), глибурид (DIABETA, Aventis), глипизид (GLUCOTROL, Pfizer) и подобные стимуляторы секреции инсулина. Принимают во внимание, что препараты сульфонилмочевины могут увеличивать эффективность инсулинотерапии путем, например, увеличивания количества секреции эндогенного инсулина из бета-клеток поджелудочной железы. Кроме того, препараты сульфонилмочевины могут увеличивать эффективность инсулинотерапии путем увеличения чувствительности периферических тканей к инсулину.
В другой конфигурации другим лекарственным препаратом является меглитинид, такой как репаглинид (PRANDIN, Novo Nordisk), натеглинид (STARLIX, Novartis) и подобные стимуляторы секреции инсулина. Принимают во внимание, что меглитиниды могут увеличивать эффективность инсулинотерапии путем увеличения количества секреции эндогенного инсулина, например, из бета-клеток поджелудочной железы путем блокады АТФ-зависимых калиевых каналов.
В другой конфигурации другим лекарственным препаратом является агонист рецептора, активируемого пролифератором пероксисом (PPAR), такого как PPARγ. В одном варианте осуществления изобретения агонист PPARγ представляет собой тиазолидиндионовые препараты, повышающие чувствительность к инсулину (TZD), включая, но не ограничиваясь, пиоглитазон (ACTOS, Takeda), AVANDAMET (GlaxoSmithKline), малеат розиглитазона (AVANDIA, GlaxoSmithKline), фонформин, буформин и подобные. Принимают во внимание, что TZD препараты, повышающие чувствительность к инсулину, и другие агонисты PPARγ могут увеличивать эффективность инсулинотерапии путем снижения инсулинорезистентности или нечувствительности периферических тканей и печени, приводя к увеличению инсулинозависимого использования глюкозы и снижению выброса глюкозы печенью. Принимают во внимание, что соединения, которые также не имеют PPARα связывающего действия, могут быть преимущественно включены в устройства, описанные в настоящем описании.
В другой конфигурации предусматриваются смеси других лекарственных препаратов. Иллюстративно, смесь может состоять из TZD препарата, увеличивающего чувствительность к инсулину, или агониста PPARγ и бигуанида, такого как метформин, смешанный с малеатом розиглитазона (AVANDAMET, GlaxoSmithKline), и подобные смеси. Принимают во внимание, что другие лекарственные средства, которые снижают глюконеогенез в печени, могут быть включены отдельно или в комбинации с TZD. Также понимают, что другие лекарственные средства, которые снижают абсорбцию глюкозы в кишечнике, могут быть включены отдельно или в комбинации с TZD. Также принимают во внимание, что другие лекарственные средства, которые улучшают чувствительность к инсулину путем увеличения периферического потребления и утилизации глюкозы, могут быть включены отдельно или в комбинации с TZD. Кроме того, смесь может состоять из миметика инкретина или аналога инкретина и бигуанида или сульфонилмочевины, например экзенатид, смешанный и метформином или глимепиридом, и подобные смеси. Кроме того, смесь может состоять из бигуанида и сульфонилмочевины, например метформин, смешанный с глипизидом (METAGLIP, Bristol Meyers Squibb), и подобные смеси.
В другой конфигурации другим лекарственным препаратом является сахарид, такой как глюкагон или его аналог. Принимают во внимание, что при введении инсулина с помощью устройств, описанных в настоящем описании, может быть желательно или необходимо смягчать и/или уменьшать эффект введения инсулина, который может приводить к гипогликемии или гипогликемическому состоянию. Кроме того, принимают во внимание, что введение такого сахарида может регулироваться базальными функциями устройств, описанных в настоящем описании, или альтернативно, болюсными функциями устройств, описанных в настоящем описании. Например, в одном иллюстративном варианте осуществления изобретения при развитии гипогликемии или гипогликемического состояния пациент, получающий лечение, может начать болюсное введение сахарида. Понимают, что начало гипогликемии или гипогликемического состояния может быть определено с использованием любого обычного метода мониторирования уровня глюкозы крови, включая, но не ограничиваясь, полоски для глюкозы крови и подобные. В одном варианте начало гипогликемии или гипогликемического состояния может быть определено пациентом во время физической нагрузки и/или опыта в распознавании определенных симптомов, указывающих на такую гипогликемию или гипогликемическое состояние. Кроме того, принимают во внимание, что при другой конфигурации нежелательно иметь какой-либо постоянный уровень введения глюкагона, и, следовательно, один вариант такого варианта осуществления изобретения включает болюсное введение сахарида в качестве первичного или единственного пути введения.
В другой конфигурации другой лекарственный препарат представляет собой инсулиноподобный фактор роста (IGF) 1 или 2 или его аналог или производное. Принимают во внимание, что IGF-1 и/или IGF-2 могут вводиться с инсулином или его аналогами для уменьшения гипогликемии и/или гипогликемических состояний, которые могут быть вызваны отдельным введением инсулина. IGF-1 и IGF-2 связываются с рецепторами инсулина, но с гораздо меньшим сродством, чем инсулин, например в 10 раз или даже 100 раз меньшим сродством, чем инсулин. Без связи с теорией, предполагают, что совместное введение IGF-1 или IGF-2 или их аналога или производного может снижать чувствительность к инсулину и, следовательно, может снижать возможность развития гипогликемии и/или гипогликемических состояний, вызванных введением инсулина. Понимают, что IGF-1 и IGF-2 могут быстро связываться со связывающими белками при введении. Соответственно, в настоящем описании также предусматриваются конъюгаты лигандов IGF-1 и IGF-2 и их аналоги. Такие конъюгаты лигандов могут увеличивать общую биодоступность IGF-1 и IGF-2 или их аналогов, которые вводят, как описано в настоящем описании.
В другой конфигурации другим лекарственным препаратом является С-пептид или его аналог. Понимают, что в продукции и метаболизме эндогенного инсулина проинсулин производится в β-клетках и при высвобождении расщепляется пептидазами с высвобождением фрагмента С-пептида. Наконец, карбоксипептидаза Е дает зрелый инсулин путем усечения конца В-цепи. Принимают во внимание, что С-пептид может вводиться совместно с инсулином или любым его аналогом или производным в качестве второго лекарственного препарата. Без связи с теорией предполагают, что С-пептид является применимым в регуляции метаболизма глюкозы и также в других биологически важных процессах, и, следовательно, полное или практически полное замещение эндогенного инсулина экзогенными источниками может приводить к нежелательному уровню С-пептида. Например, нейропатия является совместно существующим состоянием, которое может сопровождать диабет или другие диабетические состояния или состояния с нарушенной регуляцией глюкозы. Следовательно, предполагают, что введение С-пептида может лечить нейропатию, снижать прогрессирование нейропатии или замедлять или останавливать развитие нейропатии. Принимают во внимание, что устройства, описанные в настоящем описании, могут приводить к большей приверженности пациента к лечению, чем обычные методы, включая обычные методы, которые включают введение С-пептида путем инъекции.
В одном аспекте С-пептид или его аналог или производное вводят пациенту в соотношении около 1:1 на молярной основе относительно инсулина, таким образом отражая эндогенное состояние здоровых пациентов. В другом аспекте С-пептид, его аналог или производное вводят пациенту в соотношении менее чем 1:1 на молярной основе относительно инсулина. В таком последнем варианте осуществления изобретения понимают, что может не быть необходимости в поддержании уровня С-пептида таким же высоким, как инсулина. Кроме того, понимают, что введение С-пептида может приводить к эффекту плато, и, соответственно, необходимость пациента в С-пептиде может снижаться с течением времени. Следовательно, в таком другом аспекте С-пептид или его аналог или производное вводят пациенту в соотношении около 4:5, около 3:4, около 2:3 или около 1:2 на молярной основе по сравнению с инсулином.
Кроме того, понимают, что хотя в вышеуказанных вариантах осуществления изобретения, где вторым лекарственным препаратом является С-пептид или его аналог или производное, может вводиться с использованием любого из устройств, описанных в настоящем описании, в одном варианте выбирают устройства, которые содержат единственную иглу, где оба лекарственных препарата 20, 22 смешиваются перед введением. В другом варианте выбирают устройства, которые содержат две или более иглы, где по меньшей мере две из таких игл расположены проксимально относительно другой, позволяя обоим лекарственным препаратам 20, 22 смешиваться непосредственно или вскоре после введения в место попадания пациенту.
В другой конфигурации первый и второй лекарственные препараты 20, 22 оба являются противоинфекционными средствами. В одном аспекте противоинфекционными веществами являются антибактериальные вещества, такие как пенициллины и связанные соединения, включая карбацефемы, карбапенемы, цефалоспорины и подобные, монобактамы, полипептиды, аминогликозиды, гликопептиды, ванкомицины, макролидные антибиотики, включая эритромицин, хинолоны, сульфонамиды, тетрациклины и подобные.
Иллюстративные аминогликозиды, которые могут быть включены в устройства, описанные в настоящем описании, включают, но не ограничиваются, амикацин, гентамицин, канамицин, неомицин, нетилмицин, стрептомицин, тобрамицин и подобные. Иллюстративные карбацефемы включают лоракарбеф и подобные. Иллюстративные карбапенемы включают эртапенем, имипенем, циластатин, меропенем и подобные. Иллюстративные цефалоспорины включают цефалоспорины первого, второго, третьего и четвертого поколения, такие как цефадроксил, цефазолин, цефалексин, цефаклор, цефамандол, цефакситин, цефпрозил, цефуроксим, цефиксим, цефдинир, цефдиторен, цефлперазон, цефотаксим, цефподоксим, цефтазидим, цефтибутен, цефтизоксим, цефтриаксон, цефепим и подобные.
Иллюстративные макролиды, которые могут быть включены в устройства, описанные в настоящем описании, включают, но не ограничиваются, азитромицин, кларитромицин, диритромицин, эритромицин, рокситромицин, тролеандомицин и подобные. Иллюстративные гликопептиды, которые могут быть включены в устройства, описанные в настоящем описании, включают тейкопланин, ванкомицин и подобные. Иллюстративные пенициллины включают амоксициллин, ампициллин, азлоциллин, кабенициллин, клоксациллин и подобные, и монобактамы включают азтреонам и подобные. Иллюстративные полипептиды включают бацитрацин, колистин, полимиксин В и подобные.
Иллюстративные хинолоны включают ципрофлоксацин, эноксацин, гатифлоксацин, левофлоксацин, моксифлоксацин и подобные. Иллюстративные сульфонамиды включают мафенид, сульфацетамид, сульфаметизол, сульфасалазин, сульфизоксазол, триметоприм, бактрим и подобные. Иллюстративные тетрациклины включают демеклоциклин, доксификлин, миноциклин, окситетрациклин, тетрациклин и подобные. Еще другие иллюстративные антибиотики, которые могут быть включены в устройства, описанные в настоящем описании, включают, но не ограничиваются, арсфенамин, хлорамфеникол, флорамфеникол, клиндамицин, этамбутол, фосфомицин, фурзолидон, изониазид, линехолид, метронидазол, нитрофурантоин, рифампин, спектиномицин, телитромицин и подобные.
В другом варианте осуществления изобретения первый и второй лекарственные препараты 20, 22 являются агонистами или антагонистами рецепторов нейромедиаторов. В одном иллюстративном аспекте первый лекарственный препарат является допамином или агонистом рецепторов допамина и второй лекарственный препарат является антагонистом рецепторов допамина. Иллюстративные агонисты и антагонисты рецепторов допамина описаны в международной заявке РСТ серийный № PCT/US2004/043145, описание которой включено в настоящее описание в виде ссылки полностью. В одном аспекте агонист допамина является селективным в отношении рецептора допамина D1. В другом аспекте антагонист допамина является селективным в отношении рецептора допамина D2. Принимают во внимание, что совместное введение антагониста рецептора допамина D2 может усиливать или улучшать эффективность или общую пользу агониста рецептора допамина, включая агонист рецептора допамина D1. Также принимают во внимание, что совместное введение антагониста рецептора допамина D2может снижать, облегчать или смягчать побочные эффекты, связанные с агонистом рецепторов допамина, включая агонист рецептора допамина D1.
Иллюстративные антагонисты рецептора допамина D2, которые могут быть включены в устройства, описанные в настоящем описании, включают, но не ограничиваются, соединения по формулам:

и их фармацевтически приемлемые соли, где R представляет собой водород или С1-С4 алкил; R1 представляет собой водород, ацил, такой как С1-С4 алканоил, бензоил, пивалоил и подобные, или необязательно замещенную фенильную или фенокси-защищенную группу, такую как пролекарство и подобное; Х представляет собой водород, фтор, хлор, бром, йод или группу по формуле -OR8, где R8представляет собой водород, С1-С4 алкил, ацил, такой как С1-С4 алканоил, бензоил, пивалоил и подобные, или необязательно фенильную или фенокси-защищенную группу, с условием, что, когда Х является группой по формуле -OR8, группы R1 и R8 могут необязательно быть взяты вместе с образованием -СН2- или -(СН2)2- группы, таким образом, представляя собой метилендиокси или этилендиокси функциональную группу; RА, R2, R3, R4, R5, R6, и R7каждую независимо выбирают из водорода, С1-С4 алкила, фенила, фтора, хлора, брома, йода и группы -OR9, где R9 представляет собой водород, ацил, такой как С1-С4 алканоил, бензоил, пивалоил и подобные или необязательно замещенную фенильную или фенокси-защищенную группу; и RВ выбирают из водорода, С1-С4 алкила, фенила, фтора, хлора, брома, йода и группы -OR9, где R9 представляет собой водород, ацил, такой как С1-С4 алканоил, бензоил, пивалоил и подобные, -OR1 и Х, как определено выше, и необязательно замещенной фенильной или фенокси-защищенной группы, с условием, что, по меньшей мере, один RВ представляет собой -OR1.
Иллюстративные антагонисты рецепторов допамина D2, которые могут быть включены в устройства, описанные в настоящем описании, включают, но не ограничиваются, антипсихотические средства, иллюстративно выбираемые из типичных и атипичных семейств антипсихотических средств. Принимают во внимание, что атипичные нейролептики могут часто быть ассоциированы с менее выраженными экстрапирамидными симптомами, особенно дистониями, и менее частыми и меньшими увеличениями концентрации пролактина сыворотки, ассоциированного с терапией. В одном аспекте типичные нейролептические средства включают фенотиазины и нефенотиазины, такие как локсапин, молиндон и подобные. В другом аспекте атипичные нейролептические вещества включают клозапиноподобные вещества и другие, включая арипипразол, рисперидон (3-[2-[4-(6-фтор-1,2-бензизоксазол-3-ил)пиперидино]этил]-2-метил-6,7,8,9-тетрагидро-4Н-пиридо-[1,2-а]пиримидин-4-он), амисульпирид, сертиндол (1-[2-[4-[5-хлор-1-(4-фторфенил)-1Н-индол-3-ил]-1-пиперидинил]этил]имидазолидин-2-он) и подобные. Фенотиазины включают, но не ограничиваются, хлорпромазин, флуфеназин, мезоридазин, перфеназин, прохлорперазин, тиоридазин и трифторперазин. Нефенотиазины включают, но не ограничиваются, галоперидол, пимозид и тиотиксен. Другие клозапиноподобные вещества включают, но не ограничиваются, оланзапин (2-метил-4-(4-метил-1-пиперазинил)-10Н-тиено[2,3-b][1,5]бензодиазепин), клозапин (8-хлор-11-(4-метил-1-пиперазинил)-5Н-дибензо[b,e][1,4]диазепин), кветиапин (5-[2-(4-дибензо[b,f][1,4]тиазепин-11-ил-1-пиперазинил)этокси]этанол), ципразидон (5-[2-[4-(1,2-бензоизотиазол-3-ил)-1-пиперазинил]этил]-6-хлор-1,3-дигидро-2Н-индол-2-он) и подобные. Принимают во внимание, что другие типичные и атипичные нейролептические средства могут быть использованы в качестве антагонистов рецепторов допамина, описанных в настоящем описании. Также принимают во внимание, что могут быть использованы различные комбинации типичных и атипичных нейролептических средств.
Устройства, описанные в настоящем описании, могут быть созданы для введения суточных дозировок различных первых и вторых лекарственных препаратов 20, 22 на биоэквивалентном уровне, сравнимом с обычными формами лекарственных средств. Иллюстративно, метформин может быть введен со скоростью, которая коррелирует с обычной пероральной дозировкой 500, 850, 1000 или 2000 мг/сутки. Необходимо понимать, что количество, вводимое парентеральным путем, описанным в настоящем описании для различных устройств, часто будет по существу ниже, чем эквивалентная пероральная лекарственная форма. Например, метформин может быть введен с пульсовым или болюсным профилем введения со скоростью, соответствующей значениям, которые не превосходят пиковые концентрации в плазме (Сmax), наблюдаемые для пероральной лекарственной формы, например в диапазоне от около 0,5 до около 4 мкг/мл. Альтернативно, метформин может быть введен с непрерывным или базальным профилем введения со скоростью менее чем Сmax и соответствующей среднему значению площади под кривой (AUC), например в диапазоне от около 4 до около 10 мкг·ч/мл. Эти и другие значения для метформина, а также для других первых и вторых лекарственных препаратов 20, 22, описанных в настоящем описании, обнаруживают при и/или обычным образом получают из значений, представленных для обычных лекарственных форм таких лекарственных препаратов и Physicians Desk Reference, Thompson PDR, Montvale NJ (59th edition, 2005), описание которого включено в настоящее описание в виде ссылки.
Предполагают, что устройства, описанные в настоящем описании, могут быть особенно соответствующими для базального введения или, альтернативно, болюсного введения с более частыми и низкими дозами, лекарственных препаратов, которые вводят обычно один или два раза в сутки из-за особенностей рецептирования, удобства или плохой ожидаемой приверженности пациента к лечению. Соответственно устройства, описанные в настоящем описании, могут быть созданы для введения фармакокинетических профилей (РК) лекарственных препаратов, которые невозможны с обычными лекарственными формами. Например, профиль РК пик-впадина, обычно сопровождающий введение один раз в сутки, может быть преобразован в профиль РК постоянного высвобождения низкого уровня или более низкого пик-большая впадина более частого пульсового профиля РК.
Существует множество преимуществ настоящего описания, возникающих из различных характеристик прибора и способов, описанных в настоящем описании. Отмечают, что альтернативные варианты осуществления прибора и способов по настоящему описанию могут не включать все характеристики, уже описанные, все еще имея преимущество из, по меньшей мере, нескольких преимуществ таких характеристик. Обычный специалист в области техники может легко разработать свои собственные оснащения прибора и способ, который включает одну или более характеристики настоящего описания и попадает в рамки и тенденцию настоящего описания.
Реферат
Варианты устройства относятся к медицинской технике. Устройство содержит корпус, первый резервуар с первым лекарственным препаратом; второй резервуар со вторым лекарственным препаратом; первый приводной механизм для базальной доставки, имеющий первый резервуар гидравлической жидкости; первую насосную камеру в жидкостной связи с первым резервуаром гидравлической жидкости первого приводного механизма для базальной доставки через первый ограничитель потока. Первая насосная камера выполнена с возможностью связи с первым резервуаром, чтобы обеспечивать базальную доставку первого лекарственного препарата во время использования. Второй приводной механизм для базальной доставки в пределах корпуса имеет второй резервуар гидравлической жидкости. Вторая насосная камера находится в жидкостной связи со вторым резервуаром через второй ограничитель потока. Вторая насосная камера выполнена с возможностью обеспечить базальную доставку второго лекарственного препарата во время использования. Игла имеет первый конец, выполненный с возможностью жидкостной связи с первым резервуаром, и второй конец, выполненный с возможностью простираться наружу от корпуса. Раскрыт второй вариант устройства, отличающийся наличием привода для болюсной доставки. Технический результат состоит в повышении точности базального введения лекарственных препаратов. 2 н. и 17 з.п. ф-лы, 19 ил.
Формула
корпус,
первый резервуар в пределах корпуса, выполненный с возможностью содержать первый лекарственный препарат;
второй резервуар в пределах корпуса, выполненный с возможностью содержать второй лекарственный препарат;
первый приводной механизм для базальной доставки в пределах корпуса, имеющий первый резервуар гидравлической жидкости;
первую насосную камеру в жидкостной связи с первым резервуаром гидравлической жидкости первого приводного механизма для базальной доставки через первый ограничитель потока, причем первая насосная камера выполнена с возможностью связи с первым резервуаром, чтобы обеспечивать базальную доставку первого лекарственного препарата во время использования;
второй приводной механизм для базальной доставки в пределах корпуса, имеющий второй резервуар гидравлической жидкости;
вторую насосную камеру в жидкостной связи со вторым резервуаром гидравлической жидкости второго приводного механизма для базальной доставки через второй ограничитель потока, причем вторая насосная камера выполнена с возможностью связи со вторым резервуаром, чтобы обеспечить базальную доставку второго лекарственного препарата во время использования; и
иглу, имеющую первый конец, выполненный с возможностью жидкостной связи с первым резервуаром, и второй конец, выполненный с возможностью простираться наружу от корпуса.
корпус;
первый резервуар в пределах корпуса, выполненный с возможностью содержать первый лекарственный препарат;
второй резервуар в пределах корпуса, выполненный с возможностью содержать второй лекарственный препарат;
приводной механизм для базальной доставки в пределах корпуса, имеющий резервуар гидравлической жидкости;
первую насосную камеру в жидкостной связи с резервуаром гидравлической жидкости приводного механизма для базальной доставки через первый ограничитель потока, причем первая насосная камера выполнена с возможностью связи с первым резервуаром, чтобы обеспечивать базальную доставку первого лекарственного препарата во время использования; и
вторую насосную камеру в жидкостной связи с резервуаром гидравлической жидкости приводного механизма для базальной доставки через второй ограничитель потока, причем вторая насосная камера выполнена с возможностью связи со вторым резервуаром, чтобы обеспечивать базальную доставку вторых лекарственных препаратов во время использования.

Комментарии