Наконечники и системы каналов и способы их использования - RU2752587C2
Код документа: RU2752587C2
Чертежи







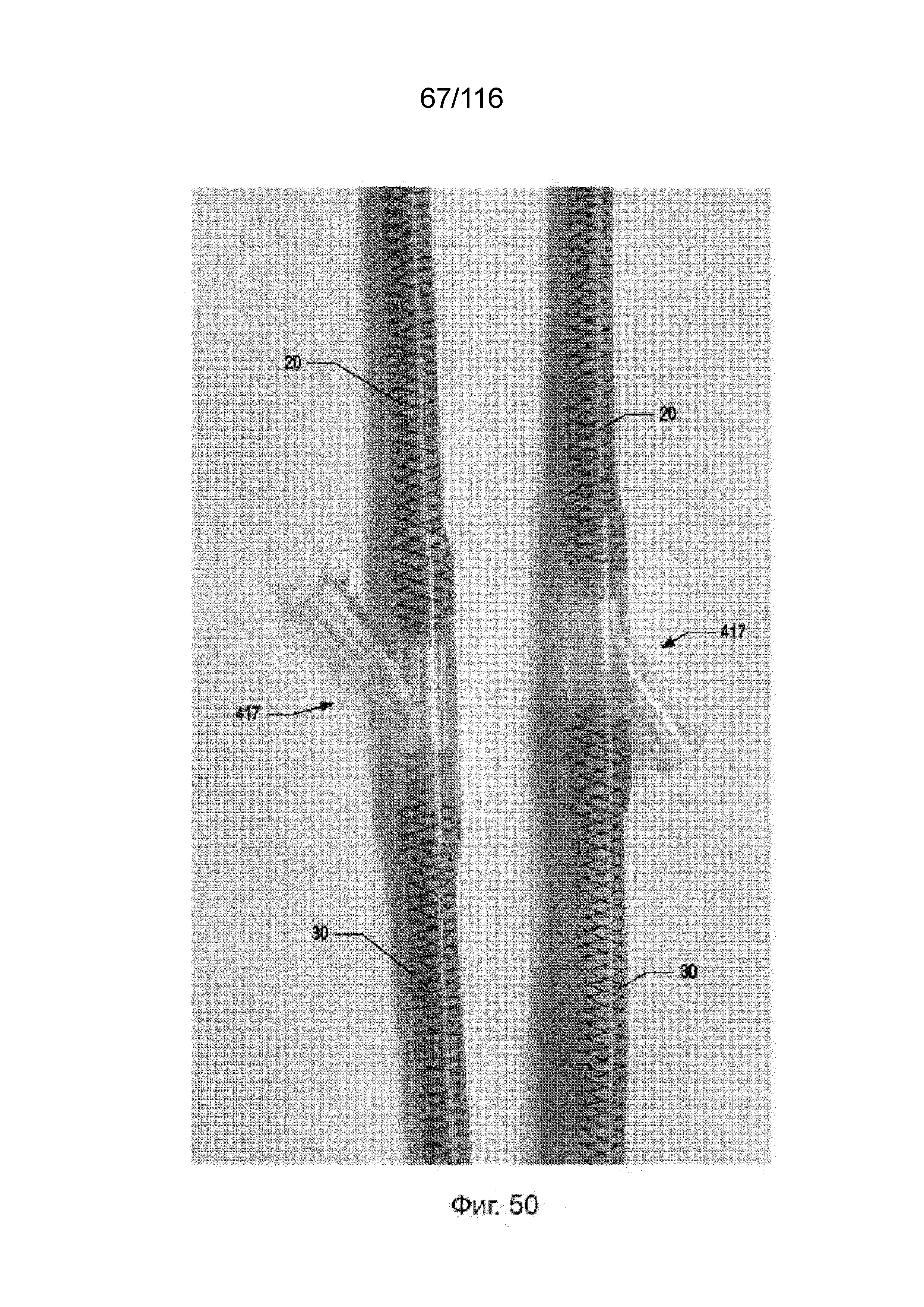




Описание
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] В настоящей заявке заявлен приоритет на основании предварительной заявки США № 61/329,930 под названием «Conduit Fluid Inflow tip», поданной 29 апреля 2016 г. и предварительной заявки США № 62/467,651 под названием «Conduit Outflow Tip and Cage Device», поданной 6 марта 2017 г; обе из которых включены в настоящий документ посредством ссылки в полном объеме.
ОБЛАСТЬ ТЕХНИКИ
[2] Настоящее изобретение относится к перфузионной системе, которая содержит насос, каналы, блок управления и источник питания, благодаря чему система может использоваться по различным клиническим показаниям. Кроме того, настоящее изобретение относится к различным приточным и выводным каналам, наконечникам каналов и несущим конструкциям для использования с перфузионной системой. В частности, устройства, описанные в настоящем документе, могут быть полезны для устойчивого увеличения общего диаметра и диаметра просвета вен и артерий у пациентов, нуждающихся в месте сосудистого доступа для гемодиализа, шунтирующем имплантате или другом типе операции или процедуры, в которой необходим больший диаметр вен или артерий. Описанные в настоящем документе устройства, способы и системы также могут быть полезны для увеличения венозного оттока нижних конечностей и снижения венозного давления нижних конечностей у пациентов с венозной гипертензией нижних конечностей, в том числе у пациентов с нарушением окраски и изъязвлением кожи. Раскрытые устройства, способы и системы, кроме того, могут быть полезны для обеспечения повышенного местного кровотока к нуждающимся в нем органам и тканям, например, нижним конечностям пациентов с заболеванием периферических артерий (peripheral arterial disease, PAD).
УРОВЕНЬ ТЕХНИКИ
[3] В США имеется более 650 000 пациентов с хроническим заболеванием почек (chronic kidney disease, CKD), при ежегодном добавлении новых 100 000 пациентов с CKD. Существует прогноз четырехпроцентного ежегодного прироста для преобладающего населения из-за факторов высокого кровяного давления, диабета и старения населения.
[4] Гемодиализ является предпочтительным вариантом лечения более чем для 90% пациентов с CKD в США. Без гемодиализа или другой формы почечной заместительной терапии большинство пациентов с CKD умерли бы. Типичный пациент с CKD, подвергающийся гемодиализу, должен иметь возможность подключения сосудистой системы к установке для гемодиализа два-три раза в неделю. Для гемодиализа существуют три общеизвестных варианта места сосудистого доступа. Предпочтительным вариантом места доступа является артериовенозная фистула (arteriovenous fistula, AVF), которая представляет собой прямое хирургическое соединение между артерией и веной, предпочтительно в запястье, или, альтернативно, в предплечье или плече. Другим вариантом места доступа является артериовенозный имплантат (arteriovenous graft, AVG), который представляет собой хирургически созданную связь между артерией и веной с использованием вставленного синтетического канала, предпочтительно в предплечье, или, альтернативно, в плече, грудной клетке, паху или ноге. Последним основным вариантом места доступа является катетер, введенный в крупную вену в шее, груди, ноге или другом анатомическом местоположении.
[5] Пациенты с AVF имеют меньшую заболеваемость, меньшую смертность и более низкую стоимость лечения по сравнению с пациентами с AVG или катетером; поэтому AVF является предпочтительной формой сосудистого доступа для гемодиализа. Пациенты с AVG или катетером имеют значительно более высокие показатели инфицирования и смерти, чем пациенты с AVF, при этом пациенты с катетером имеют худшие результаты. Кроме того, пациенты, имеющие AVG или катетер, имеют более высокую среднюю стоимость лечения, при этом пациенты с катетером несут самые высокие затраты. Если для пациента приемлема AVF, запястье или предплечье обычно предпочтительнее, чем AVF в плече, из-за более высоких скоростей ишемии рук и, как правило, более коротких и более глубоких сегментов вен плеча. Один общепринятый принцип, который соблюдают при создании мест сосудистого доступа AVF и AVG, заключается в том, чтобы начать как можно дальше и сохранить более ближние вены для создания места сосудистого доступа позже. Это означает, что доступ начинают с запястья для пациентов с AVF и с предплечья для пациентов с AVG. Однако меньший диаметр самых дальних вен часто снижает успех хирургии сосудистого доступа в этих местах.
[6] К сожалению, примерно для 85 процентов пациентов AVF в запястье неприемлема, в основном, из-за слишком малых диаметров вены и артерии. Кроме того, около 50-60 процентов всех созданных AVF не могут быть использованы без дополнительных хирургических и интервенционных процедур из-за случая, обычно называемого «неудачей созревания», который взаимосвязан с небольшим диаметром вен и артерией. Доступность вен и артерий с более крупными диаметрами взаимосвязана с более высокой степенью приемлемости AVF, более низкими показателями созревания, более быстрым созреванием AVF и пролонгированной степенью первичной и вторичной проходимости.
[7] В настоящее время существует несколько вариантов постоянного или устойчивого увеличения диаметра вены или артерии. Все современные способы используют механические способы расширения, такие как баллонная ангиопластика, которая может привести к повреждению вен или артерий. Поскольку необходимо, чтобы пациент имел периферические вены и артерии определенного размера для того, чтобы врач мог создать AVF, желательно иметь способ и систему для постоянного и устойчивого увеличения размера или диаметра периферических вен или артерий.
[8] Примерно 7 миллионов человек в США страдают от хронической венозной недостаточности и гипертензии, которые могут прогрессировать до венозных язв. Язва нижних конечностей является наиболее распространенной формой хронической раны с оценочной распространенностью у 1% населения США. Около 2,5 миллионов человек в США имеют изъязвление нижних конечностей, и около 600 000 человек ежегодно обращаются за лечением венозной язвы нижних конечностей в США. Ожидается, что заболеваемость венозными изъязвлениями возрастет по мере старения населения.
[9] При обследовании пациентов с венозной язвой 81% пациентов сообщили о неблагоприятном влиянии на мобильность, 56% сообщили о том, что тратят до 8 часов в неделю на лечение язвы, 68% сообщили об отрицательном эмоциональном воздействии, включая страх, социальную изоляцию, гнев, депрессию и негативную самооценку. При обследовании 80% пациентов не работают за пределами дома; и из 20% занятых, изъязвление ног взаимосвязано с потерей времени работы, потерей работы и неблагоприятным воздействием на финансы.
[10] Венозная гипертензия и изъязвление нижних конечностей являются дорогостоящими для лечения и налагают существенное бремя на поставщиков и системы медицинских услуг. В исследовании 78 пациентов с венозной язвой в Кливлендской клинике размер медианной язвы составлял 2,8 см2 (среднее значение=9,4 см2) и 5% имели двусторонние язвы. Среднее время заживления язвы составляло 77 дней (среднее значение=108 дней), а средняя стоимость лечения составляла 2400 долларов в месяц. Средняя общая стоимость лечения до заживления язвы составила 9685 долларов США на одного пациента. Для пациентов, которым требуется более года для заживления, средняя общая стоимость на одного пациента составляла 18 534 доллара США.
[11] В большинстве случаев венозная гипертензия и изъязвление являются результатом недостаточности клапана сердца, с осложнением в виде тромбоза глубоких вен, или неизвестной причины. В значительном меньшем числе случаев венозная гипертензия и изъязвление возникают из-за обструкции бедренной или тазовой вены с осложнением в виде тромбоза глубоких вен, повреждения вен или компрессии наружных вен. Хроническое воздействие на ткань локализованной венозной гипертензии приводит к расширению капилляров с повышенной проницаемостью и утечкой плазмы и эритроцитов, захвату и активации лейкоцитов в капиллярных сосудах, а также высвобождению свободных радикалов и других токсичных продуктов, таких как факторы некроза опухоли и коллагеназы, которые могут способствовать гибели клеток и повреждению тканей. Утечка фибриногена в окружающие ткани связывает или «захватывает» факторы роста и цитокины, и делает их недоступными для поддержания и восстановления целостности тканей.
[12] Венозная гипертензия нижних конечностей клинически выглядит как покраснение и обесцвечивание ног, отек, боль, отек, зуд, шелушение, выделения и липодерматосклероз. Язвы обычно развиваются по медиальной части ноги, имеют неровные границы и могут быть связаны с сильной болью. Венозные язвы часто осложняются бактериальной суперинфекцией. Артериальное кровообращение обычно достаточное. Современные методы лечения венозной гипертензии нижних конечностей и язвы часто неадекватны. Пациентам, в основном, предлагается паллиативное лечение с целью заживления язв и предотвращения рецидивов, включая инвазивный уход за раной, компрессионную терапию для снижения венозного давления нижней конечности и увеличения венозного оттока, удаление или иссечение вены нижней конечности и пересадку кожи. Тем не менее, современные методы лечения часто не могут излечить язвы, и частота рецидивов для излеченных язв высока.
[13] В настоящее время существуют небольшие «сердечные насосы»; однако такие насосы являются дорогостоящими и не предназначены для использования в конечности, и не подходят по размерам, или для вариантов использования, описанных в настоящем документе. Таким образом, существует неудовлетворенная клиническая потребность в системах, компонентах, способах и устройствах перекачивания, которые могут увеличивать диаметр периферических вен и артерий при разумной цене, среди других клинических показаний. Кроме того, существует потребность в системах, компонентах, способах и устройствах перекачивания, которые могут увеличить венозный отток нижней конечности, уменьшить венозную гипертензию нижних конечностей и залечить венозные язвы. Некоторые медицинские процедуры и медицинские устройства основаны на системе насосов и каналов для перемещения различных текучих сред, таких как кровь, в пациента и из него. Различные исследования показали, что конфигурация приточного канала и наконечника приточного канала непосредственно влияет на характеристики потока текучей среды, поступающей в приточный канал перфузионной системы. Различные исследования показали, что конфигурация выводного канала и наконечника выводного канала непосредственно влияет на характеристики потока текучей среды, выходящей из выводного канала перфузионной системы. Когда каналы используют для перекачивания крови из пациента и обратно, существует риск тромбообразования, вызванного зонами низкого и высокого напряжения сдвига стенки (wall shear stress, WSS) в потоке, а также связанный с ним риск случаев тромбоэмболии. Например, вполне понятно, что зоны с низким значением WSS могут вызывать агрегацию тромбоцитов, тогда как зоны с высоким значением WSS могут вызывать активацию тромбоцитов. Зоны очень высокого значения WSS могут также представлять риск гемолиза. Например, зона WSS, превышающего 150 Па, вероятно, может привести к гемолизу.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[14] Настоящая заявка относится к перфузионным системам, включая перфузионные системы с широкими рабочими диапазонами, низкой себестоимостью (cost-of-goods-sold, COGS) и промежуточным сроком службы. Указанные перфузионные системы предназначены для использования в различных клинических ситуациях и для различных клинических показаний, как описано в настоящем документе.
[15] Перфузионные системы, описанные в настоящем документе, могут быть использованы для увеличения диаметра вен и артерий, предпочтительно периферических вен и артерий. Система будет действовать для перемещения крови таким образом, чтобы вызвать увеличение диаметра вены или артерии. Это может быть достигнуто путем выпуска («толкания») крови в вену или артерию, или путем удаления («вытягивания») крови из вены или артерии. Посредством любого способа система увеличивает поток крови в сосуде, что в конечном итоге приводит к устойчивому увеличению диаметра сосуда. Таким образом, система (и, в частности, насос) использует механические средства для активации путей биологической реакции, что приводит к расширению вен или артерий и модификациям в структуре расширенных стенок артерий и вен, что иногда называют «сосудистым ремоделированием». Система содержит перфузионный насос, каналы для переноса или транспортирования крови в перфузионный насос и из него, систему управления для мониторинга перфузионного насоса и изменения режима работы перфузионного насоса, и источник питания. Таким образом, система содержит группу элементов, которые могут, например, сообщаться по текучей среде с артерией на одном конце, и сообщаться по текучей среде с веной на другом конце, причем при включении кровь перекачивается с такой скоростью, что напряжение сдвига стенки (WSS) на эндотелии вены, артерии или их обоих повышается в течение периода времени, достаточного для устойчивого расширения вены или артерии. Может быть использован любой из множества насосов и насосных систем, при условии, что поток крови через насосную систему можно регулировать, чтобы обеспечить желаемое увеличение диаметра кровеносного сосуда.
[16] Перфузионные системы, описанные в настоящем документе, могут быть использованы для увеличения венозного возврата нижних конечностей, снижения венозной гипертензии нижних конечностей и заживления венозных язв. Система будет действовать для перемещения крови из вены в пораженной нижней конечности, такой как бедренная, подкожная вена или подвздошная вена, в место в венозном кровообращении, так что отток венозной крови от нижней конечности к сердцу улучшается. Места для возврата в венозном кровообращении включают яремную вену, подмышечную вену, подключичную вену, плечеголовную вену, полую верхнюю вену и правое предсердие. Система содержит перфузионный насос, один или более каналов для переноса или транспортирования крови в перфузионный насос и из него, систему управления для мониторинга перфузионного насоса и изменения режима работы перфузионного насоса, и источник питания. Таким образом, система содержит группу элементов, которые могут, например, сообщаться по текучей среде на одном конце с периферической веной и сообщаться по текучей среде с периферической, центральной веной или правым предсердием на другом конце, посредством чего при включении кровь накачивается с такой скоростью, чтобы венозное кровяное давление снижалось в подвергаемой лечению нижней конечности в течение периода времени, достаточного для того, чтобы вызвать частичное или полное заживление венозной язвы. Может быть использован любой из множества насосов и насосных систем, при условии, что поток крови через насосную систему можно регулировать, чтобы обеспечить желаемый эффект.
[17] Могут быть использованы различные типы перфузионных насосов, включая насосы вытеснительного типа и ротационные насосы, причем предпочтительными являются насосы ротационного типа. В одном варианте реализации изобретения система с ротационным перфузионным насосом содержит насос, имеющий корпус, образующий впуск для приема крови и выпуск для выпуска крови. Корпус насоса спроектирован и рассчитан на размещение вращающейся крыльчатки, подвешенной на опорах. Корпус насоса может иметь первую опору, расположенную ближе к впускной части корпуса, и вторую опору, расположенную ближе к выпускной части корпуса. Кровь поступает во вращающуюся крыльчатку и выходит из нее, благодаря чему крыльчатка увеличивает скорость выхода крови. Указанная увеличенная скорость получается или передается как повышенное давление, когда кровь замедляется в диффузоре насоса, который заканчивается в выпускном отверстии насоса.
[18] В других вариантах реализации изобретения могут использоваться различные типы ротационных перфузионных насосов. Например, можно использовать осевой проточный насос, смешанный проточный насос или, предпочтительно, центробежный перфузионный насос. Кроме того, могут использоваться различные опоры крыльчатки насоса, включая, но не ограничиваясь ими, магнитные опоры, гидродинамические опоры и, предпочтительно, поворотные (контактные) типы. Аналогичным образом могут использоваться различные типы диффузоров насоса, включая, но не ограничиваясь ими, коллекторный диффузор или, предпочтительно, спиральный диффузор.
[19] В одном варианте реализации изобретения центробежный перфузионный насос с поворотными опорами содержит корпус насоса, образующий впускное отверстие насоса, имеющее приточный диффузор, для приема крови и направления крови на крыльчатку, при этом корпус насоса имеет верхнее посадочное место и верхнюю поворотную опору, проходящую от верхней части корпуса к впускному отверстию, и нижнее посадочное место и нижнюю поворотную опору, проходящую от нижней части корпуса во внутреннее пространство корпуса. Насос также содержит крыльчатку, подвешенную внутри корпуса, причем крыльчатка дополнительно имеет опорный просвет для установки оси крыльчатки. Ось крыльчатки имеет первый конец для фиксации в верхней поворотной опоре, вблизи впускной части, и второй конец для фиксации в нижней поворотной опоре, вблизи выпускной части. В одном варианте реализации изобретения по меньшей мере один конец оси крыльчатки является выпуклым, и конец по меньшей мере одной поворотной опоры является вогнутым. В другом варианте реализации изобретения по меньшей мере один конец оси крыльчатки является вогнутым, и конец по меньшей мере одной поворотной опоры является выпуклым. В другом варианте реализации изобретения оба конца оси крыльчатки являются вогнутыми, и обе поворотные опоры являются выпуклыми. В другом варианте реализации изобретения оба конца оси крыльчатки являются выпуклыми, и обе поворотные опоры являются вогнутыми. Крыльчатка может содержать множество конструкций в виде ребер или лопастей, предназначенных для контакта и ускорения крови в спирали. Например, крыльчатка образует множество лопастей на верхней поверхности крыльчатки, проходящих радиально от центра крыльчатки к внешнему краю крыльчатки. Лопасти ускоряют кровь от центрального впуска крыльчатки к ее периферийному выпуску. В другом варианте крыльчатка не содержит лопастей или ребер, но содержит устройства для перемещения или продвижения крови. Крыльчатка необязательно содержит по меньшей мере один промывной просвет, прорезь или канал, проходящий, в основном, параллельно центральной оси крыльчатки от нижней поверхности через крыльчатку до верхней поверхности. В некоторых вариантах реализации изобретения, просвет предназначен для предотвращения застоя крови под крыльчаткой и вокруг нижней поворотной опоры.
[20] Перфузионный насос содержит двигатель, предпочтительно электрический, предназначенный для приведения в действие крыльчатки. В одном варианте реализации изобретения перфузионный насос содержит приводной двигатель, имеющий по меньшей мере один магнит, механически прикрепленный к крыльчатке, и по меньшей мере один якорь, механически прикрепленный к корпусу. Якорь возбуждает электродвижущую силу по меньшей мере в одном магните, прикрепленном к крыльчатке. Двигатель насоса может представлять собой бесщеточный моментный двигатель постоянного тока (direct current, DC) с осевым зазором, с бессенсорным коммутированием обратной электродвижущей силы (back electromotive force, back-EMF). В двигателе может использоваться спеченный сплав неодима, железа и бора (NdFeB) для магнитов в крыльчатке и трехфазная плоская катушка со схемой «тороид» в статоре. Двигатель может иметь соотношение размеров, как у диска, с очень малой длиной в осевом направлении по сравнению с его диаметром.
[21] В одном варианте реализации изобретения перфузионная система содержит центробежный перфузионный насос с рабочим диапазоном примерно от 50 миллилитров в минуту (мл/мин) до 1500 мл/мин. Система также содержит корпус насоса, образующий впускное отверстие насоса для приема крови и направления крови на крыльчатку. Корпус насоса имеетверхнююповоротную опору, проходящую от верхней части корпуса к впускному отверстию, и нижнюю поворотную опору, проходящую от нижней части корпуса во внутреннее пространство корпуса. Насос также содержит крыльчатку, подвешенную внутри корпуса, причем первый зазор между крыльчаткой и верхней частью корпуса находится в первом диапазоне примерно от 0,05 мм до 0,2 мм.
[22] Крыльчатка содержит ось крыльчатки, имеющую первый конец для фиксацииверха оси, и второй конец для фиксации низа оси, и множество лопастей на верхней поверхности крыльчатки, проходящих в радиальном направлении от центра крыльчатки, при этом лопасти служат для принудительной подачи крови, принятой на впуске, через корпус насоса и к выпуску. Крыльчатка также содержит по меньшей мере один просвет, проходящий параллельно центральной оси крыльчатки от нижней поверхности через крыльчатку до верхней поверхности.
[23] Насос дополнительно содержит по меньшей мере один магнит, механически соединенный с крыльчаткой, и электродвигатель для магнитного взаимодействия по меньшей мере с одним магнитом, причем электродвигатель вращает по меньшей мере один магнит и крыльчатку. В других вариантах реализации изобретения насос также содержит ферромагнитную опорную пластину для магнитного взаимодействия по меньшей мере с одним магнитом.
[24] Перфузионная система имеет один или более каналов, включая первый (приточный) канал, имеющий два конца, первый конец, который сообщается по текучей среде с определенным местом в сосудистой системе и получает кровь из этого места, и второй конец, который сообщается по текучей среде с насосом. Приточный канал доставляет кровь в насос. Перфузионная система имеет второй (выводной) канал, имеющий два конца, первый конец, который сообщается по текучей среде с насосом и получает кровь из насоса, и второй конец, который сообщается по текучей среде с некоторым местом в сосудистой системе и доставляет кровь к этому месту.
[25] В некоторых вариантах реализации изобретения каналы перфузионной системы имеют по отдельности длину от 2 см до 110 см и общую длину между 4 см и 220 см, и могут быть отрезаны врачом до требуемой длины, в том числе во время имплантации насосной системы. Каждый канал имеет внутренний диаметр от 2 см до 10 мм и предпочтительно от 3 см до 5 мм. Каналы могут быть выполнены по меньшей мере частично из полиуретана (например, Pellethane ® или Carbothane®), поливинилхлорида, полиэтилена, силиконового эластомера, политетрафторэтилена (polytetrafluoroethylene, PTFE), вспененного политетрафторэтилена (expanded polytetrafluoroethylene, ePTFE), полиэтилентерефталата (polyethylene terephthalate, PET, например Dacron) и их комбинаций. Каналы могут дополнительно содержать эластичный резервуар.
[26] Каналы, целиком или частично, могут быть упрочнены оплеточным или спирально навитым материалом с памятью формы, таким как нитинол или другой саморасширяющийся или радиально расширяющийся материал, такой как нержавеющая сталь. Для насосных систем, предназначенных для лечения венозной гипертензии и венозных язв нижних конечностей, канал, который передает кровь из вены нижней конечности в насосную часть насосной системы, может дополнительно содержать дальний сегмент из ePTFE или Dacron, так что этот сегмент может сообщаться по текучей среде с веной нижней конечности посредством хирургического анастомоза. Этот сегмент из ePTFE или Dacron может дополнительно содержать наружное упрочнение, такое как дополнительный материал ePTFE или Dacron, или саморасширяющийся или радиально расширяющийся материал, такой как нитинол или нержавеющая сталь. Указанное наружное упрочнение может иметь форму спирали или оплетки, или может содержать более полную периферийную и равномерную несущую конструкцию, или может быть выполнено другим способом, который препятствует спадению, сжатию или сближению стенок, когда давление внутри каналов является низким или меньшим атмосферного давления. Каналы могут иметь скошенные концы, которые сообщаются по текучей среде с сосудистой системой. Концы могут быть скошены под углом от 10 градусов до 80 градусов. Один или более каналов могут иметь одно или более отверстий или фенестраций в стенках дальних концов, когда они выполнены с возможностью размещения в просвете кровеносного сосуда или другом внутрисосудистом положении. Каналы могут быть прикреплены к насосу с помощью радиально сжимающих соединителей.
[27] В другом варианте реализации изобретения перфузионная система, содержащая центробежный перфузионный насос, дополнительно содержит корпус насоса, образующий впускное отверстие насоса для приема крови и направления крови на крыльчатку. Корпус насоса имеетверхнююповоротную опору, проходящую от верхней части корпуса к впускному отверстию, и нижнюю поворотную опору, проходящую от нижней части корпуса во внутреннее пространство корпуса. Насос также содержит крыльчатку, подвешенную внутри корпуса, причем первый зазор между крыльчаткой и верхней частью корпуса находится в первом диапазоне примерно от 0,05 мм до 0,2 мм.
[28] Крыльчатка содержит ось крыльчатки, имеющий первый конец для фиксации верха оси, и второй конец для фиксации низа оси, и множество лопастей на верхней поверхности крыльчатки, проходящих в радиальном направлении от центра крыльчатки, при этом лопасти служат для принудительной подачи крови, принятой на впуске, через корпус насоса и к выпуску. Крыльчатка также содержит по меньшей мере один просвет, проходящий параллельно центральной оси крыльчатки от нижней поверхности через крыльчатку до верхней поверхности.
[29] Насос дополнительно содержит по меньшей мере один магнит, механически соединенный с крыльчаткой, и электродвигатель для магнитного взаимодействия по меньшей мере с одним магнитом, причем электродвигатель вращает по меньшей мере один магнит и крыльчатку. Перфузионный насос также содержит по меньшей мере один канал, имеющий конец, сообщающийся с впуском насоса или выпуском насоса, и дальний конец, служащий для введения в кровеносный сосуд. Дальний конец содержит конический, не скошенный дальний наконечник, образующий, как правило, круглое торцевое отверстие, коаксиальное с центральной продольной осью дальнего конца. Дальний конец также содержит первое множество боковых отверстий, симметрично расположенных по окружности дальнего наконечника, причем первое множество боковых отверстий является ближним относительно круглого торцевого отверстия, и они ориентированы под углом относительно центральной продольной оси. Дальний наконечник также содержит второе множество боковых отверстий, расположенных по окружности дальнего наконечника.
[30] В некоторых вариантах реализации изобретения каналы перфузионных систем также содержат один или более боковых каналов, сообщающихся с каналами. Перфузионные системы также содержат одну или несколько выполненных с возможностью крепления манжет каналов для присоединения по меньшей мере одного канала.
[31] В одном варианте реализации изобретения перфузионная система содержит перфузионный насос и систему управления для мониторинга перфузионной системы и изменения режима работы перфузионного насоса, чтобы поддерживать увеличенное значение «срезающего давления» на стенку сосуда (WSS) в артерии или вене, сообщающейся по текучей среде с перфузионным насосом. Система управления дополнительно выполнена с возможностью поддержания среднего значения WSS внутри вены в диапазоне от 0,76 до 23 паскалей (Па) или предпочтительно в диапазоне от 2,5 до 10 Па. В другом варианте реализации изобретения система управления отслеживает и поддерживает увеличенную среднюю скорость крови внутри артерии или вены, сообщающейся по текучей среде с перфузионным насосом. В данном варианте реализации изобретения система управления выполнена с возможностью поддержания средней скорости крови внутри артерии или вены в диапазоне от 10 см/с до 120 см/с или предпочтительно в диапазоне от 25 см/с до 100 см/с. В любом варианте реализации изобретения перфузионная система выполнена с возможностью поддержания повышенного среднего напряжения сдвига стенки или увеличенной средней скорости крови в течение по меньшей мере 1 дня, 7 дней, 10 дней, 14 дней, 28 дней, 42 дней, 56 дней, 84 дней или 112 дней. В контексте настоящего документа термин «скорость» может относиться к скорости крови независимо от компонента направления или вектора.
[32] Перфузионная система имеет систему управления для достижения и поддержания требуемой скорости потока, которая может дополнительно содержать устройство управления для приема информации и управления работой перфузионной системы. Как минимум, система управления может быть управляемой вручную для регулировки частоты вращения двигателя. В качестве альтернативы может быть использована автоматическая (т. е. «разумная») система управления. Необязательно, система управления содержит датчики, которые могут находиться в насосе, каналах или в сосудистой системе пациента. В одном варианте реализации изобретения устройство управления может измерять частоту вращения двигателя на основе переходов через нулевое значение волны обратной EMF. Указанные переходы через нулевое значение указывают на реверсирование магнитного полюса крыльчатки. При такой конфигурации частоту вращения двигателя регулируют посредством широтно-импульсной модуляции (pulse width modulation, PWM) входного напряжения, а крутящий момент регулируют посредством PWM входного тока. Устройство управления может также отслеживать другие переменные состояния двигателя насоса, такие как ток и напряжение, по которым можно оценивать и регулировать как скорость потока через перфузионную систему, так и WSS в периферическом кровеносном сосуде.
[33] Устройство управления предпочтительно содержит «процессор», который содержит измерительный блок, блок обработки данных и блок питания для привода и управления двигателем насоса. Процессор подает питание на обмотки двигателя и управляет частотой вращения двигателя, анализируя обратную EMF в обмотках двигателя, а также информацию от дополнительных датчиков. Процессор может выполнять алгоритмы управления, зашифрованные на машиночитаемом носителе. Перфузионная система содержит кабель для электрического подключения устройства управления к насосу и дополнительным датчикам. Перфузионная система также содержит источник питания, который в некоторых вариантах реализации изобретения может быть встроен в устройство управления. В некоторых вариантах реализации изобретения источник питания для перфузионной системы может представлять собой мобильное устройство (например, перезаряжаемая батарея или топливный элемент) или стационарное устройство (например, базовый блок питания, подключенный к сети переменного тока).
[34] Система управления может получать информацию от различных источников. Электроника привода двигателя в устройстве управления может измерять по меньшей мере один из параметров: частоту вращения двигателя, входную мощность или ток, необходимый для работы насоса. В других вариантах реализации изобретения система управления содержит датчики в перфузионном насосе или каналах, которые измеряют по меньшей мере один из параметров: скорость крови, скорость кровотока, сопротивление кровотоку в периферическом кровеносном сосуде, кровяное давление, индекс пульсации и их комбинации. В других вариантах реализации изобретения система управления содержит датчики в сосудистой системе пациента, которые измеряют по меньшей мере один из параметров: скорость крови, скорость кровотока, кровяное давление, индекс пульсации, диаметр сосуда и их комбинации.
[35] В некоторых вариантах реализации изобретения система управления может оценивать и поддерживать необходимый и повышенный уровень WSS в заданном сосуде или передающей артерии или вене, используя информацию от устройства управления и/или датчиков, такую как частота вращения двигателя, входная мощность двигателя, производительность насоса, статический напор насоса, давление вблизи соединения выводного канала и заданного сосуда, падение давления на кровеносном сосуде и их комбинации. Для настоящей заявки «заданный сосуд», «заданный кровеносный сосуд», «заданная вена» или «заданная артерия» относится к определенному сегменту артерии или вены, предназначенному для лечения, для достижения устойчивого увеличения общего диаметра и просвета, когда узел насоса-канала имплантирован, настроен и эксплуатируется таким образом, чтобы обеспечить постоянное увеличение общего диаметра и диаметра просвета.
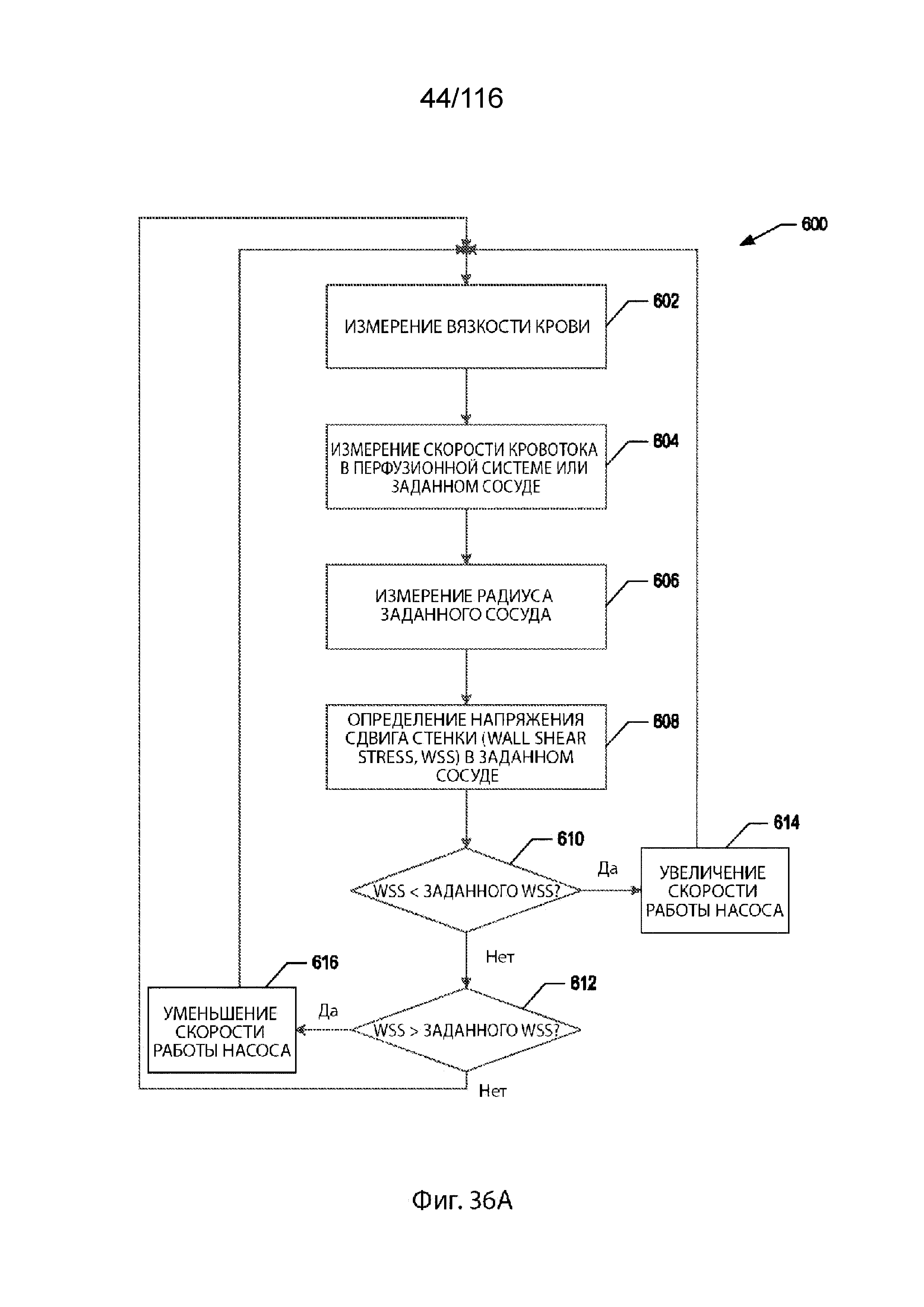
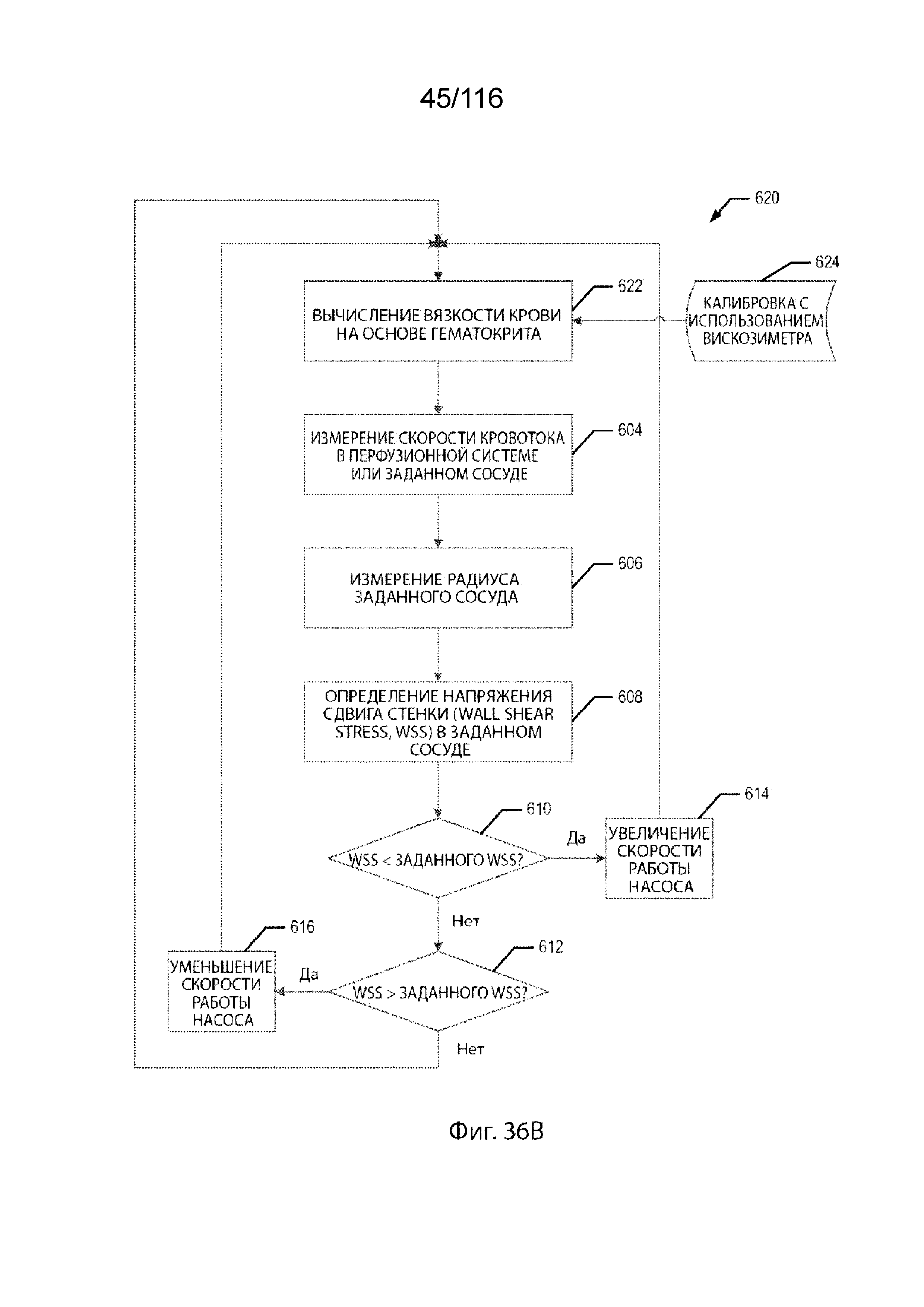
[36] Для автоматического управления работой перфузионной системы могут быть использованы различные способы управления системой. В одном варианте реализации изобретения способ определения и регулирования WSS в кровеносном сосуде включает в себя этапы измерения вязкости крови, измерения скорости кровотока в перфузионной системе или в кровеносном сосуде и измерения радиуса кровеносного сосуда. Этапы также включают в себя определение WSS в кровеносном сосуде по измеренной вязкости крови, измеренной скорости потока и радиусу кровеносного сосуда, сравнение определенного значения WSS с заданным опорным значением и регулирование скорости работы перфузионного насоса, когда определенное значение WSS не приближается к заданному опорному значению. Эти этапы повторяют до тех пор, пока определенное значение WSS не приблизится к заданному опорному значению.
[37] В другом варианте реализации изобретения способ вычисления и регулирования WSS в кровеносном сосуде включает в себя этапы оценки вязкости крови, измерения скорости кровотока в перфузионной системе или в кровеносном сосуде и измерения радиуса кровеносного сосуда. Этапы также включают в себя определение WSS по вычисленной вязкости крови, измеренной скорости кровотока и радиусу кровеносного сосуда, сравнение определенного значения WSS с заданным опорным значением и регулирование скорости работы перфузионного насоса, когда определенное значение WSS не приближается к заданному опорному значению. Эти этапы повторяют до тех пор, пока определенное значение WSS не приблизится к заданному опорному значению.
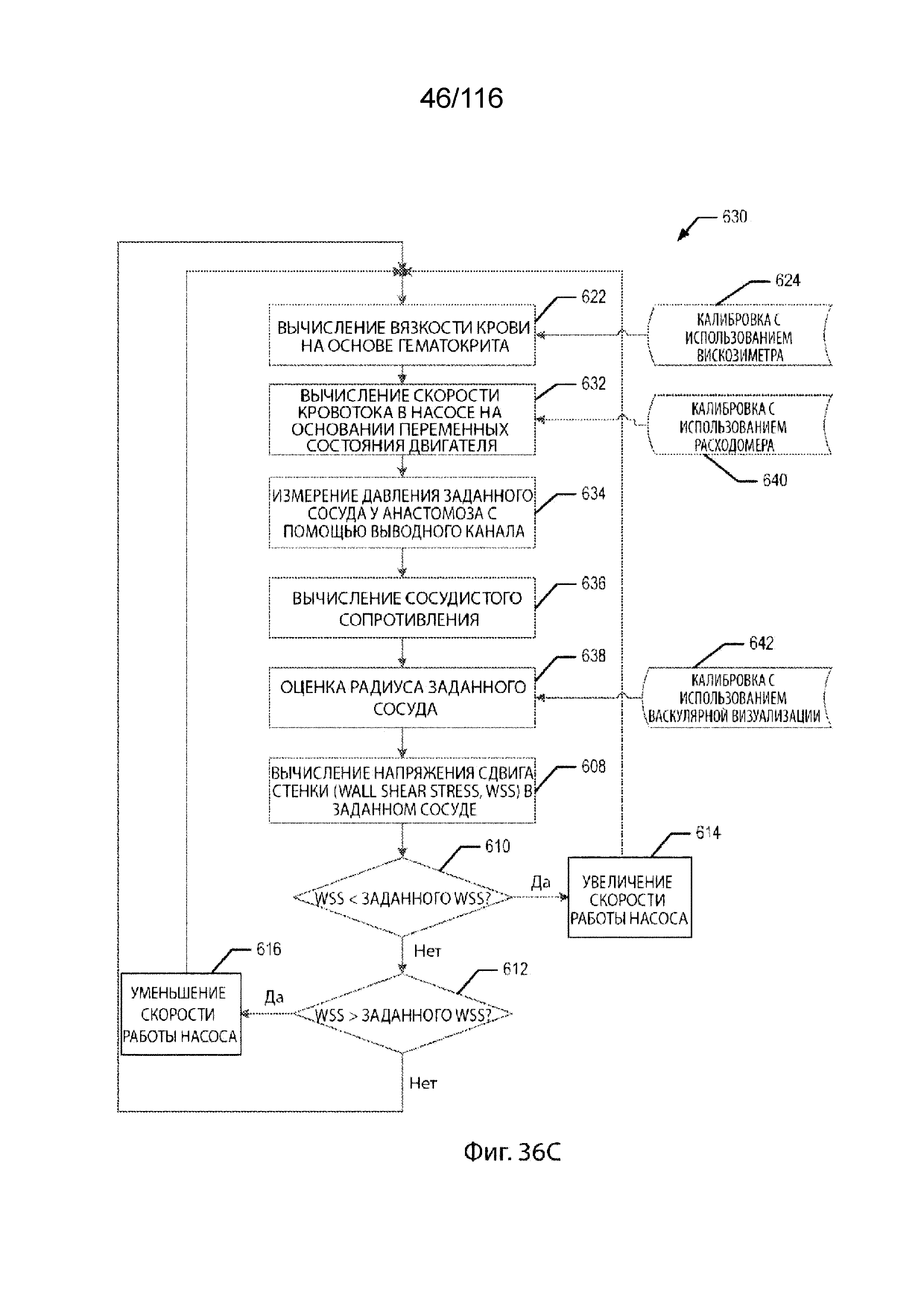
[38] В одном варианте реализации изобретения способ оценки и регулирования WSS в кровеносном сосуде включает в себя этапы оценки вязкости крови, измерения по меньшей мере одной переменной состояния двигателя перфузионной системы, выбранной из напряжения, тока или скорости работы насоса, и оценки скорости кровотока в перфузионной системе. Этапы также включают в себя измерение давления в кровеносном сосуде, определение сосудистого сопротивления кровеносного сосуда по расчетной скорости кровотока и измеренному давлению в кровеносном сосуде, оценку радиуса кровеносного сосуда. Этапы дополнительно включают в себя определение WSS по вычисленной вязкости крови, вычисленной скорости кровотока и радиусу кровеносного сосуда, сравнение определенного значения WSS с заданным опорным значением и регулирование скорости работы насоса, когда определенное значение WSS не приближается к заданному опорному значению. Эти этапы повторяют до тех пор, пока определенное значение WSS не приблизится к заданному опорному значению.
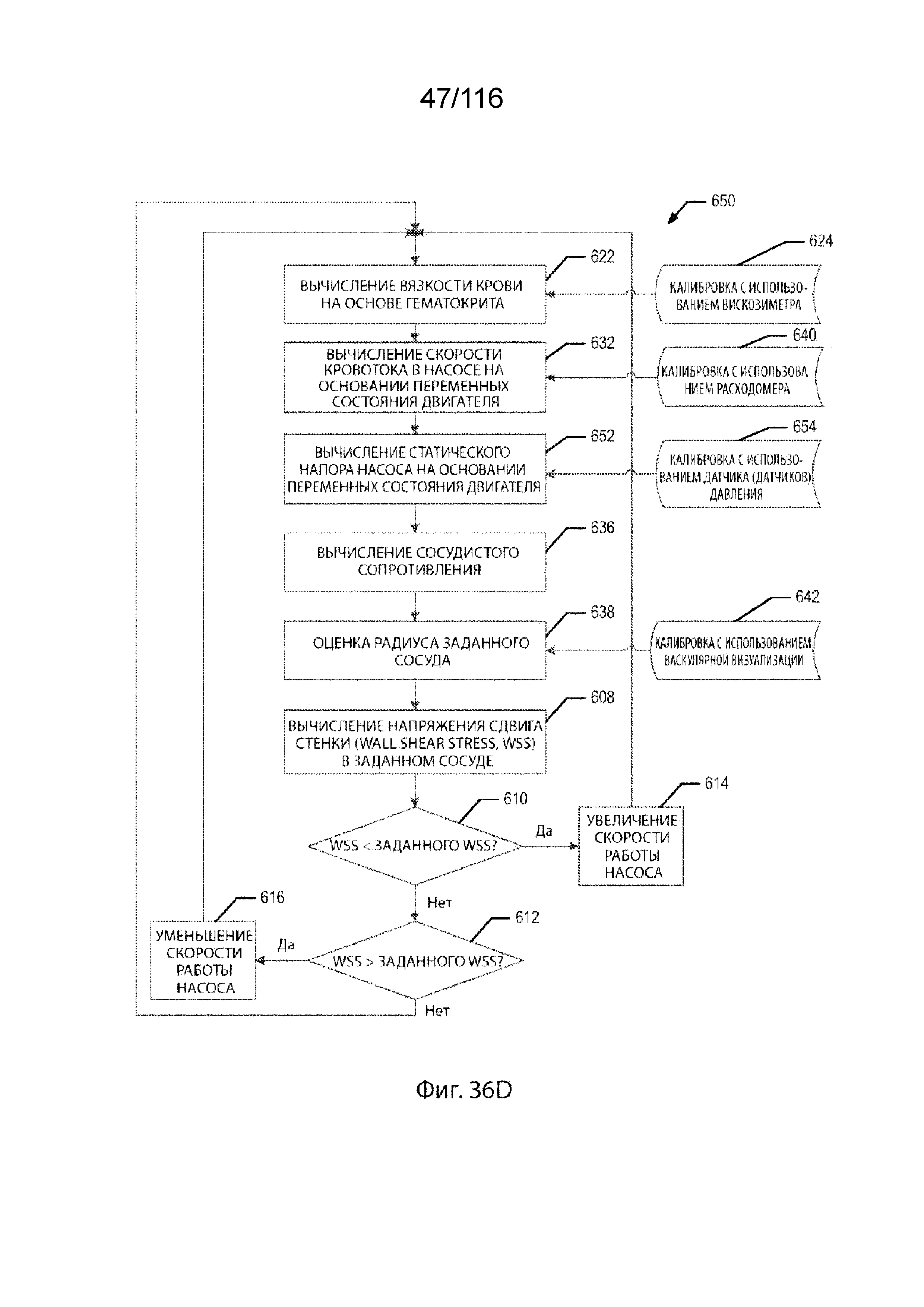
[39] В другом варианте реализации изобретения способ оценки и регулирования WSS в кровеносном сосуде с использованием перфузионной системы включает в себя этапы оценки вязкости крови, измерения по меньшей мере одной переменной состояния двигателя перфузионной системы, выбранной из напряжения, тока или скорости работы насоса и оценки скорости кровотока и статического напора в перфузионной системе. Этапы также включают в себя вычисление сосудистого сопротивления кровеносного сосуда по вычисленной скорости кровотока и вычисленному статическому напору, оценку радиуса кровеносного сосуда и определение WSS по вычисленной вязкости крови, вычисленной скорости кровотока и вычисленному радиусу кровеносного сосуда. Этапы дополнительно включают в себя сравнение определенного значения WSS с заданным опорным значением и регулирование скорости работы насоса, когда определенное значение WSS не приближается к заданному опорному значению. Эти этапы повторяют до тех пор, пока определенное значение WSS не приблизится к заданному опорному значению.
[40] В одном варианте реализации изобретения способ оценки и регулирования WSS в кровеносном сосуде с использованием перфузионной системы включает в себя этапы оценки по меньшей мере одного элемента, выбранного из группы, состоящей из вязкости крови, скорости кровотока, статического напора в перфузионной системе и радиуса кровеносного сосуда, с измерением по меньшей мере одной переменной состояния двигателя перфузионной системы, выбранной из группы, состоящей из напряжения, тока и скорости работы насоса, и определения WSS в кровеносном сосуде. Этапы также включают сравнение определенного значения WSS с заданным опорным значением и регулирование скорости работы насоса, когда определенное значение WSS не приближается к заданному опорному значению. Эти этапы повторяют до тех пор, пока определенное значение WSS не приблизится к заданному опорному значению.
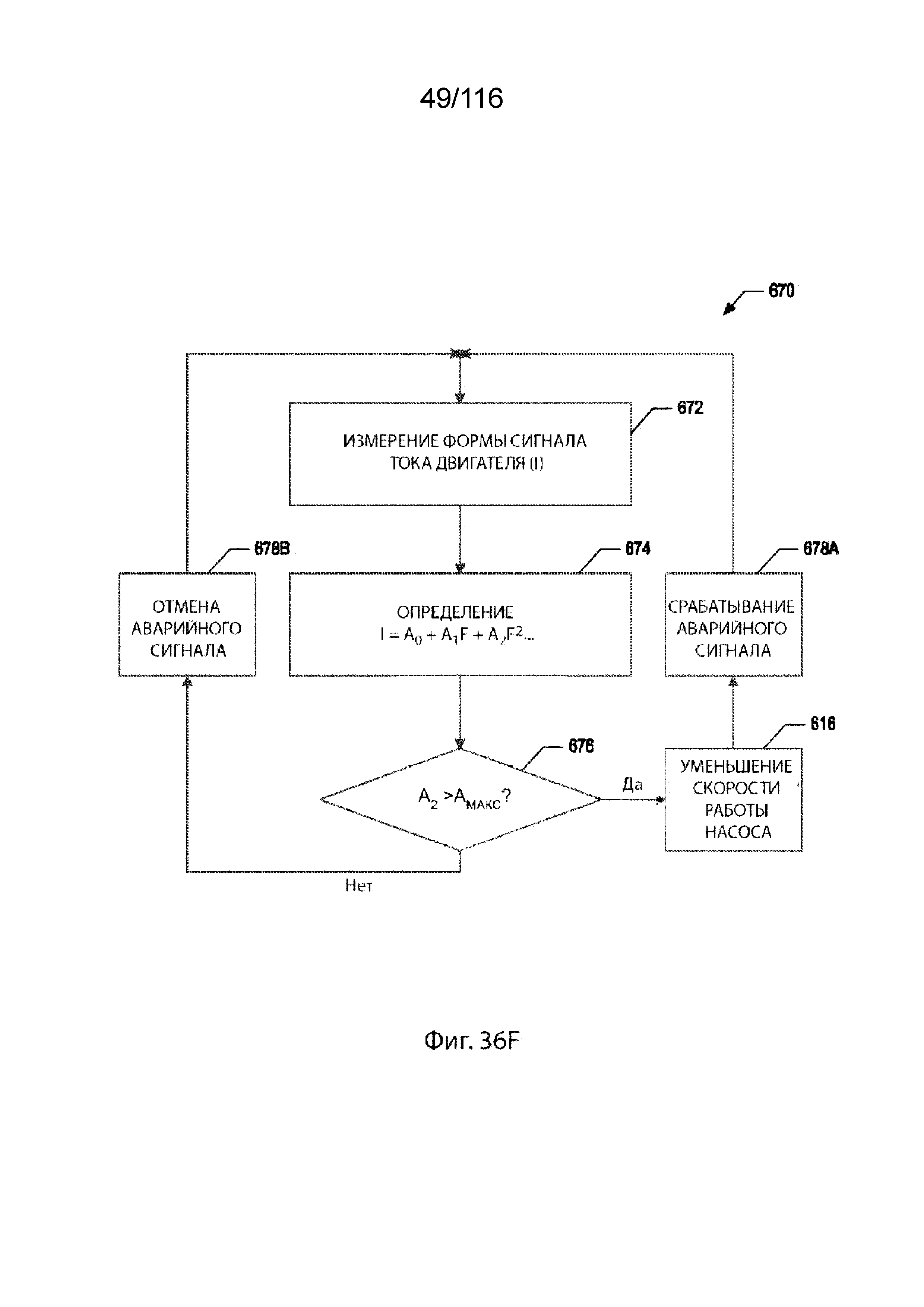
[41] В еще одном варианте реализации изобретения бессенсорный способ недопущения спадения или сближения стенок кровеносных сосудов или предсердной камеры, сообщающихся по текучей среде с перфузионной системой, при обнаружении надвигающегося спадения на впуске в перфузионную систему включает этапы измерения тока двигателя перфузионного насоса и постоянного вычисления представления спектрального анализа тока двигателя перфузионного насоса в виде ряда Фурье. Этапы также включают обеспечение индикации регистрации того, когда амплитуда второго члена гармоники ряда Фурье превышает опорное значение, и уменьшение скорости работы насоса, когда амплитуда второго члена гармоники ряда Фурье превышает опорное значение. Этапы повторяют до тех пор, пока амплитуда второго члена гармоники не опустится ниже эталонного значения.
[42] В другом варианте реализации изобретения перфузионная система содержит перфузионный насос и систему управления для мониторинга перфузионной системы и изменения режима работы перфузионного насоса для поддержания снижения венозного кровяного давления в подвергаемой лечению нижней конечности. Перфузионный насос также выполнен с возможностью поддержания площади просвета приточного канала и сообщающегося по текучей среде сегмента периферической вены при изменении положения тела, например, изменении из положения стоя до положения лежа. В одном варианте реализации изобретения система управления отслеживает кровяное давление в вене нижней конечности, сообщающейся по текучей среде с приточным каналом перфузионной системы, и регулирует скорость работы насоса для поддержания давления вены в требуемом диапазоне, который является достаточно низким, чтобы обеспечить адекватный венозный возврат через перфузионную систему, одновременно не допуская спадения, сближения или выпадения стенок вены. В данном варианте реализации изобретения система управления выполнена с возможностью поддержания давления в сегменте вены нижней конечности рядом с приточным каналом в диапазоне от 5 мм рт. ст. до 100 мм рт. ст. или предпочтительно в диапазоне от 10 мм рт. ст. до 50 мм рт. ст. или в диапазоне от 10 мм рт. ст. до 25 мм рт. ст. В любом варианте реализации изобретения перфузионная система выполнена с возможностью, в основном, поддержания указанного диапазона давления в сегменте вены нижней конечности в течение по меньшей мере 7 дней, 28 дней, 56 дней, 112 дней, 224 дней или 356 дней.
[43] Перфузионная система имеет систему управления, в основном, для достижения и поддержания требуемого диапазона давления сегмента вены нижней конечности, которая может дополнительно содержать устройство управления для приема информации и управления работой насоса перфузионной системы. Как минимум, система управления может быть управляемой вручную для регулировки частоты вращения двигателя. В качестве альтернативы может быть использована автоматическая (т. е. «разумная») система управления. Необязательно, система управления содержит датчики, которые могут находиться в насосе, каналах или сосудистой системе пациента. Датчики, включая, но не ограничиваясь ими, датчики положения, могут находиться в разных местах на пациенте или внутри него. Устройство управления может измерять частоту вращения двигателя на основе переходов через нулевое значение волны обратной EMF. Указанные переходы через нулевое значение указывают на реверсирование магнитного полюса крыльчатки. Частота вращения двигателя регулируется посредством PWM входного напряжения, а крутящий момент регулируется посредством PWM входного тока. Устройство управления также отслеживает другие переменные состояния двигателя насоса, такие как ток и напряжение, по обеим из которых можно оценивать и регулировать скорость потока через перфузионную систему. Устройство управления предпочтительно содержит память, процессор для управления частотой вращения двигателя насоса, анализа информации, поступающей от электроники привода двигателя и дополнительных датчиков, и выполнения команд, зашифрованных на машиночитаемом носителе. Перфузионная система содержит кабель для электрического подключения устройства управления к насосу и дополнительным датчикам. Перфузионная система также содержит источник питания, который в некоторых вариантах реализации изобретения может быть встроен в устройство управления. В некоторых вариантах реализации изобретения источник питания для перфузионной системы может представлять собой мобильное устройство (например, перезаряжаемая батарея или топливный элемент) или стационарное устройство (например, базовый блок питания, подключенный к сети переменного тока).
[44] Система управления может получать информацию от различных источников. Электроника привода двигателя в устройстве управления может измерять по меньшей мере один из параметров: частоту вращения двигателя, входную мощность или ток, необходимый для работы насоса. В других вариантах реализации изобретения система управления содержит датчики в перфузионном насосе или каналах, которые измеряют по меньшей мере один из параметров: скорость крови, скорость кровотока, кровяное давление, положение тела и их комбинации. В других вариантах реализации изобретения система управления содержит датчики в сосудистой системе пациента, которые измеряют по меньшей мере один из параметров: скорость крови, скорость кровотока, кровяное давление и их комбинации.
[45] Для автоматического управления работой перфузионной системы могут быть использованы различные способы управления системой. В одном варианте реализации изобретения способ уменьшения давления сегмента вен нижней конечности включает в себя этапы оценки положения тела и регулировки скорости работы насоса в зависимости от положения тела. В другом варианте реализации изобретения способ уменьшения давления сегмента вены нижней конечности включает этапы оценки положения тела, измерения кровяного давления в приточном канале или сегменте вены, сообщающемся по текучей среде с приточным каналом, и регулировки скорости работы насоса в зависимости от положения тела и кровяного давления в приточном канале или сегменте вены, сообщающемся по текучей среде с приточным каналом. В другом варианте реализации изобретения способ снижения давления сегмента вены нижней конечности включает этапы измерения по меньшей мере одной переменной состояния двигателя перфузионной системы, выбранной из группы, состоящей из напряжения, тока и скорости работы насоса, и настройки скорости работы перфузионной системы для обеспечения по меньшей мере определенного минимального потока крови через перфузионную систему. В другом варианте реализации изобретения способ снижения давления сегмента вены нижней конечности включает в себя этапы измерения кровотока через перфузионную систему и настройку скорости работы перфузионной системы для обеспечения по меньшей мере определенного минимального потока крови через перфузионную систему.
[46] В еще одном варианте реализации изобретения бессенсорный способ недопущения коллапса или сближения стенок сегмента вены нижней конечности, сообщающейся по текучей среде с перфузионной системой, при обнаружении надвигающегося спадения вены или приточного канала на впуске в перфузионную систему или вблизи него, включает этапы измерения тока двигателя перфузионного насоса и постоянного вычисления представления спектрального анализа тока двигателя перфузионного насоса в виде ряда Фурье. Этапы также включают обеспечение индикации регистрации того, когда амплитуда второго члена гармоники ряда Фурье превышает опорное значение, и уменьшение скорости работы насоса, когда амплитуда второго члена гармоники ряда Фурье превышает опорное значение. Этапы повторяют до тех пор, пока амплитуда второго члена гармоники не опустится ниже эталонного значения.
[47] В некоторых других вариантах реализации изобретения системы и способы, описанные в настоящем документе, могут быть зашифрованы на машиночитаемом носителе, который может работать с помощью устройства обработки данных. Какие-либо опорные значения или заранее установленные стандарты, используемые системами и способами, могут храниться в базе данных или другом подходящем носителе данных.
[48] Изобретение также относится к различным наконечникам каналов. В одном варианте реализации изобретения наконечник приточного канала содержит трубчатый корпус, имеющий ближний конец и дальний конец, причем трубчатый корпус образует просвет между ближним концом и дальним концом. Ближний конец образует кольцевой зубец по внешней поверхности наконечника приточного канала, а дальний конец образует кольцевой фланец по окружности трубчатого корпуса и дальнего отверстия. Дальнее отверстие дополнительно содержит дальнюю торцевую поверхность, имеющую по меньшей мере один выступающий участок и по меньшей мере один углубленный участок.
[49] В некоторых вариантах реализации изобретения наконечник приточного канала выполнен по существу из металла или металлического сплава. Наконечник приточного канала может дополнительно содержать антитромботическое покрытие, включая покрытие, содержащее гепарин. Кроме того, дальнее отверстие может быть образовано дальней торцевой поверхностью, которая имеет вид полной дуги от наружной поверхности наконечника приточного канала до внутренней поверхности наконечника канала. В другом аспекте дальнее отверстие содержит две выступающие зоны и две углубленные зоны. В качестве альтернативы, дальняя торцевая поверхность может иметь в основном волнообразную конфигурацию. В одном аспекте поверхность дальнего конца имеет профиль, обычно определяемый синусоидальной функцией.
[50] В других аспектах ближний конец образует другой кольцевой зубец. Другой кольцевой зубец расположен дистально от кольцевого зубца. Кроме того, другой кольцевой зубец проходит от продольной оси наконечника приточного канала под углом, большим, чем угол кольцевого зубца.
[51] Настоящее изобретение также относится к внутрисосудистому наконечнику выводного канала. В одном варианте реализации изобретения наконечник канала содержит трубчатый корпус, имеющий ближний конец и дальний конец, причем трубчатый корпус образует просвет между ближним концом и дальним концом.
[52] В другом варианте реализации изобретения наконечник выводного канала выполнен с возможностью введения в периферийную вену, причем наконечник выводного канала содержит, в основном, трубчатую структуру, имеющую внесосудистый приточный патрубок, сообщающийся по текучей среде с внутрисосудистым патрубком. Приточный патрубок пересекается с внутрисосудистым патрубком под косым углом и создает поток крови, подобный струе, в котором скорость крови, выходящей из дальнего конца приточного патрубка во внутрисосудистый патрубок, больше, чем скорость крови, поступающей в ближний конец приточного патрубка. В одном аспекте внесосудистый приточный патрубок содержит фитинг с кольцевыми зубцами на ближнем конце. В данном варианте реализации наконечника выводного канала стеноз внутри наконечника формируют намеренно для создания струйного потока, который увеличивает WSS в выводном кровеносном сосуде непосредственно ниже по потоку, что вызывает сосудистое ремоделирование и парадоксальным образом способствует расширению сосудов. Этот способ имитирует механизм постстенотического расширения (post-stenotic dilation, PSD), часто наблюдаемый в атеросклеротических артериях (Ojha, 1990). В опубликованных исследованиях Ojha in vitro с использованием модели пульсирующего потока, стеноз с уменьшением площади на 65% вызывал увеличение среднего WSS от значения 1 Па выше по потоку от стеноза до значения 2,3 Па между 3 и 5 диаметрами сосудов ниже по потоку от стеноза.
[53] Настоящее изобретение также относится к узлу внутрисосудистого приточного канала, который содержит каркасную конструкцию, имеющую одно или более удлиненных ребер, проходящих дистально от зоны, ближней (по направлению к стороне насоса) относительно собранного наконечника канала и окружающей собранный наконечник канала. В одном варианте реализации изобретения каркасная конструкция проходит дистально от кольцевой или кольцеобразной структуры на ближнем конце каркаса до дальнего конца каркаса. В другом варианте реализации изобретения каркасная конструкция проходит дистально от кольцевой или кольцеобразной структуры на ближнем конце каркаса до кольцевой или кольцеобразной структуры на дальнем конце каркаса. В одном аспекте каркас также содержит дальнее кольцо, взаимодействующее с дальним концом одного или более удлиненных ребер. Удлиненные ребра, содержащие дальнее кольцо в некоторых вариантах реализации изобретения, могут быть перемещены по продольной оси каркасной конструкции, чтобы растягивать или сужать каркасную конструкцию.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
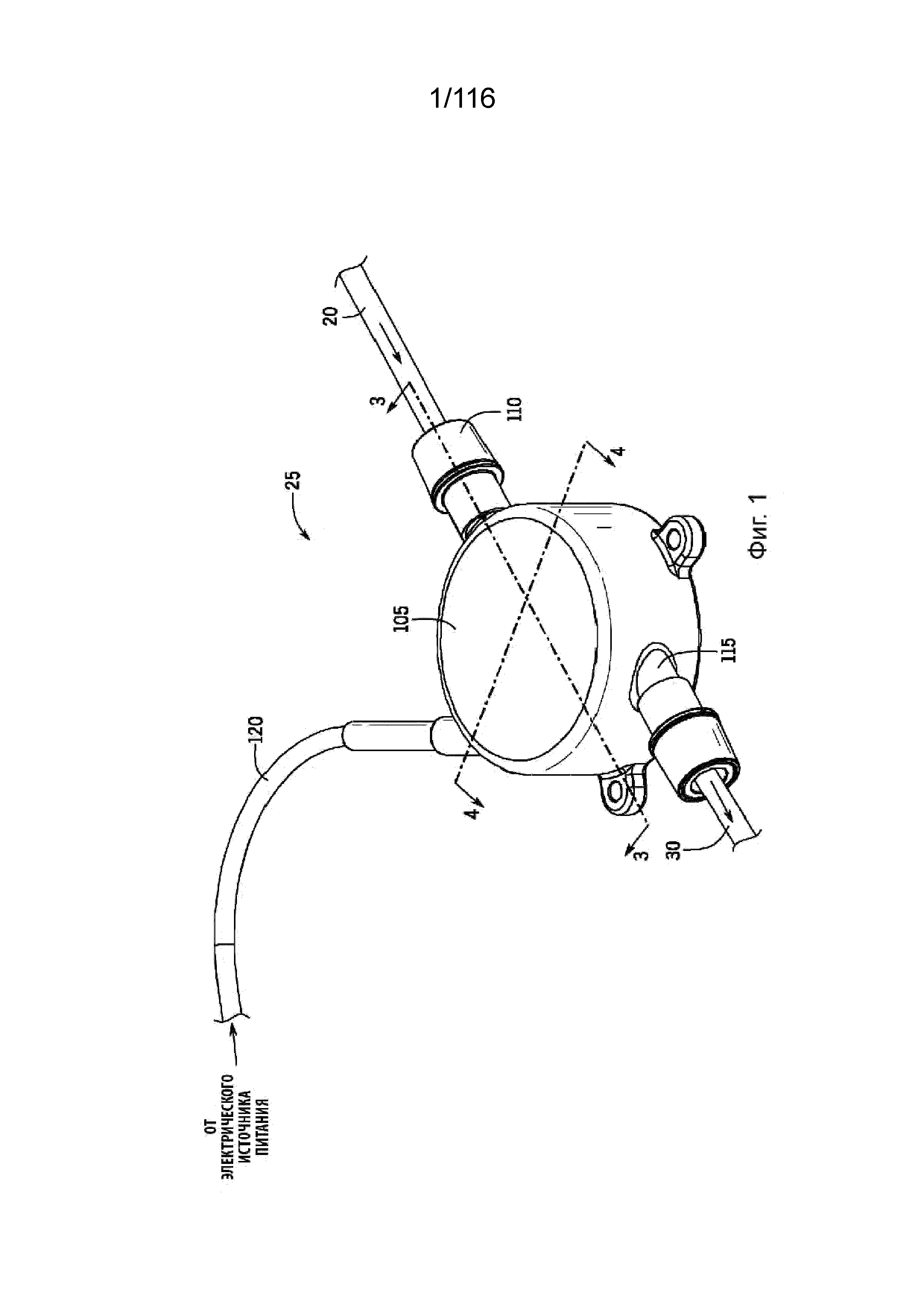
[54] На фиг. 1 представлен вид в изометрии насоса.
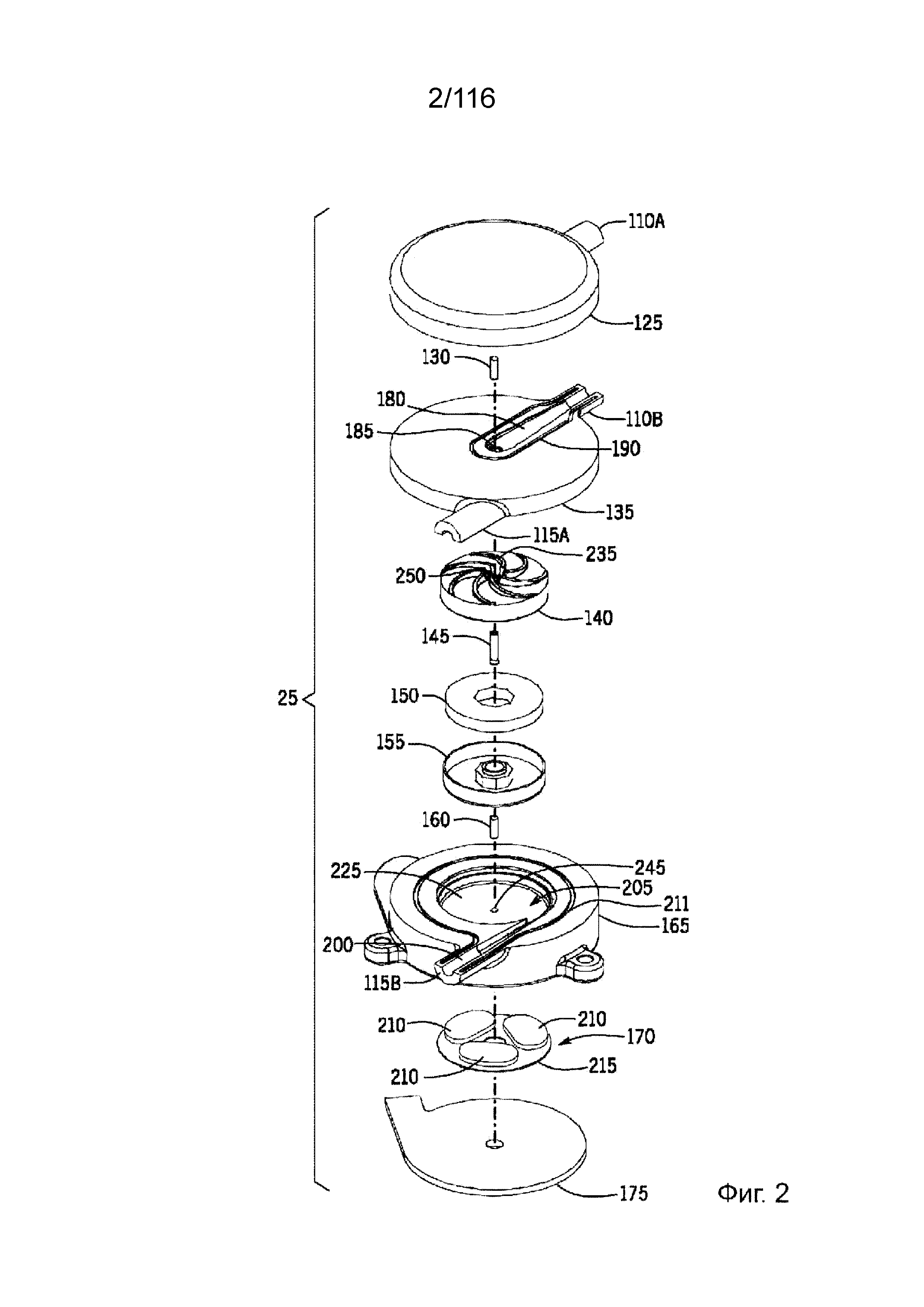
[55] На фиг. 2 представлен вид в изометрии насоса в разобранном состоянии, показывающий компоненты, содержащиеся в корпусе, указанном на фиг. 1.
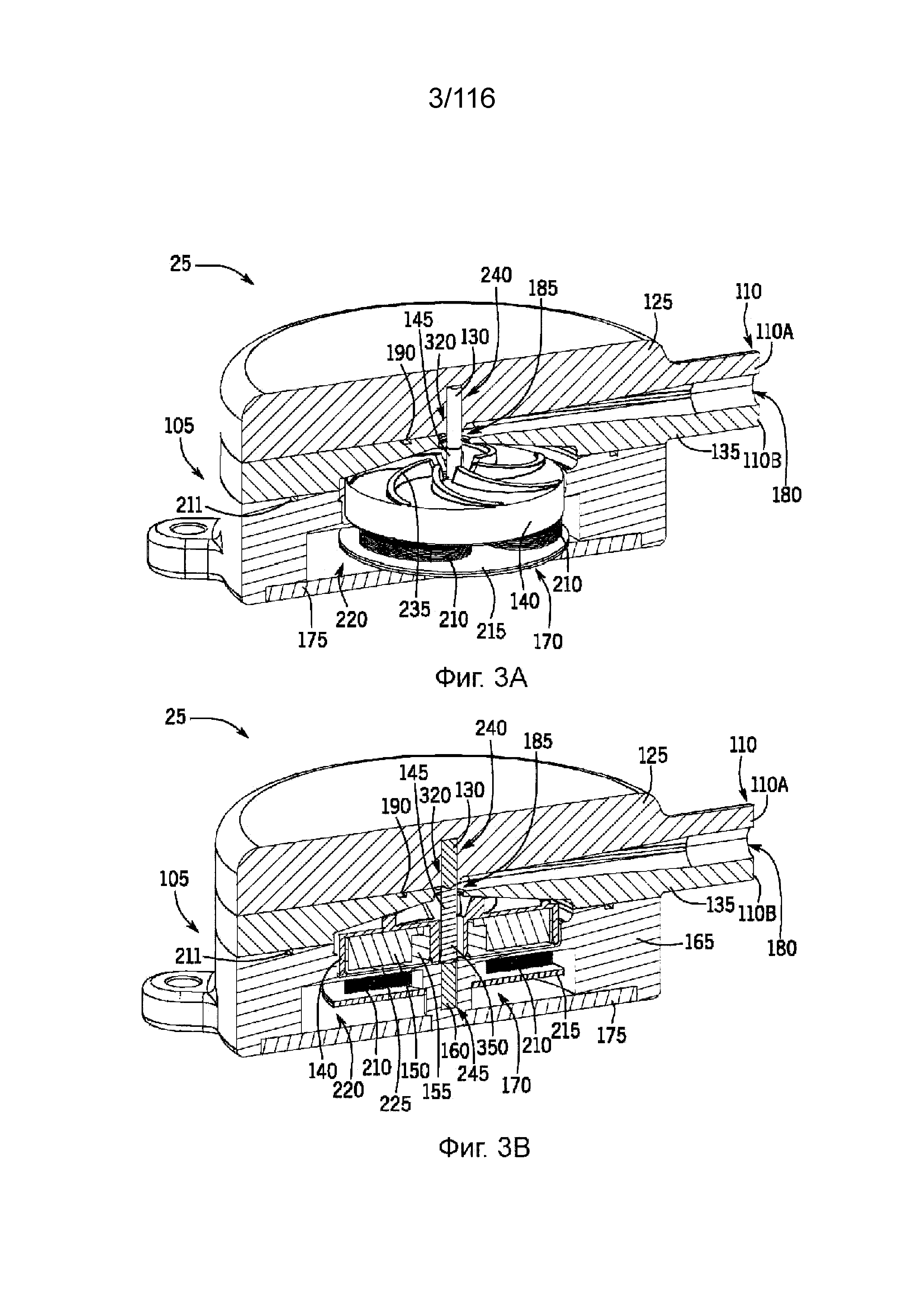
[56] На фиг. 3A и 3B приведены, соответственно, виды сбоку с частичным и полным разрезом насоса по линии 3-3 на фиг. 1.
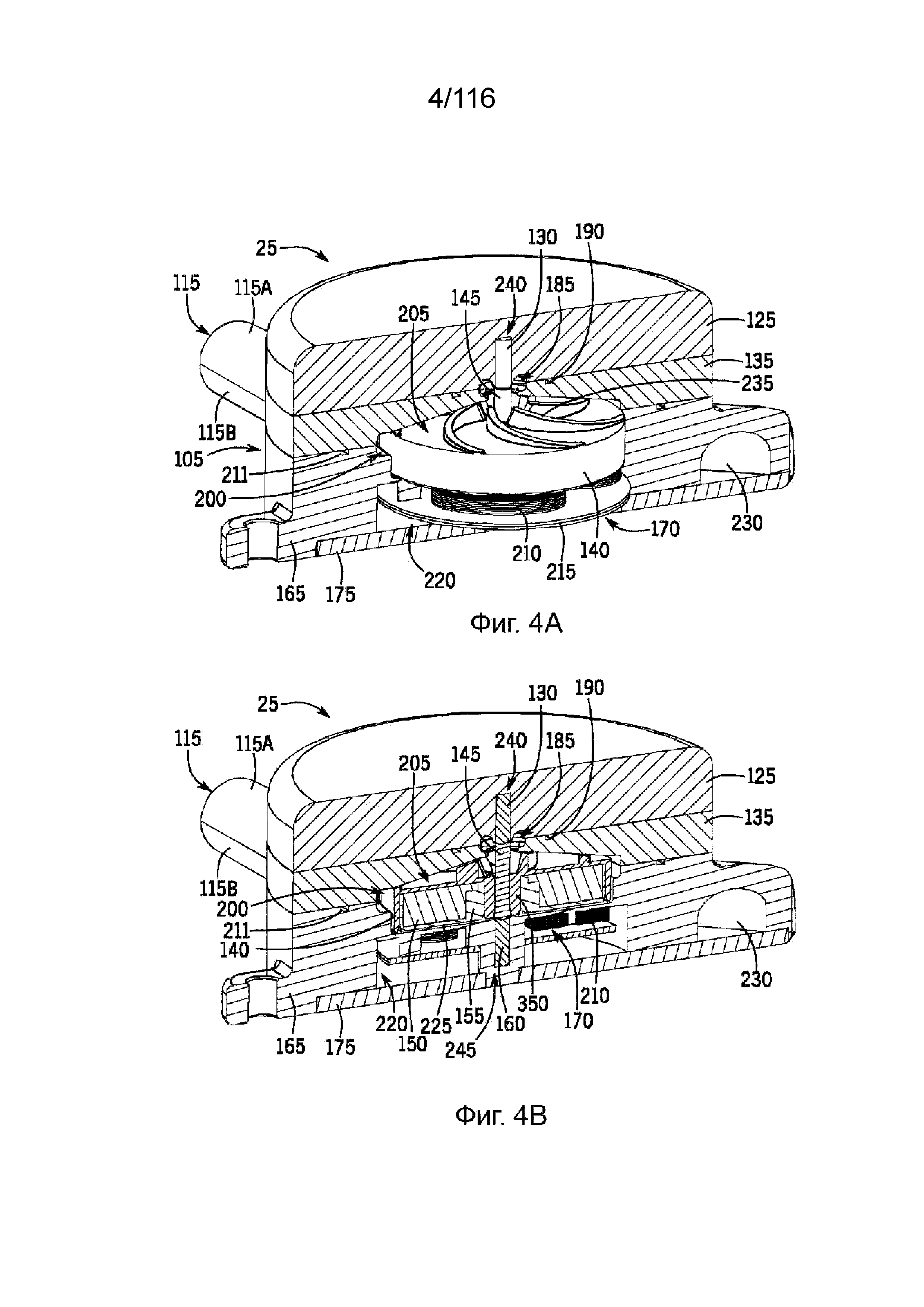
[57] На фиг. 4A и 4B приведены, соответственно, виды сбоку с частичным и полным разрезом насоса по линии 4-4 на фиг. 1.
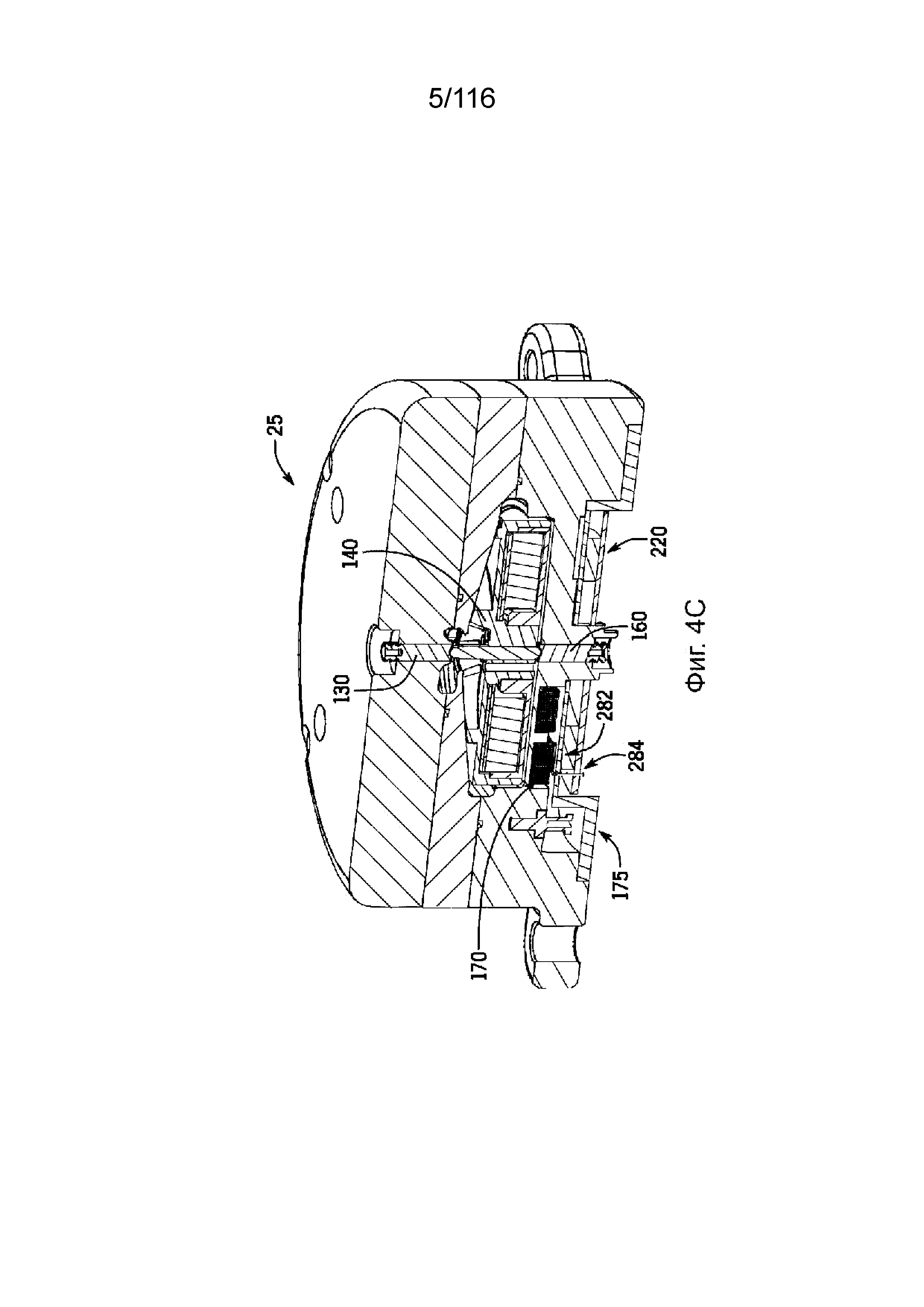
[58] На фиг. 4C приведен вид сбоку в разрезе другого варианта реализации насоса.
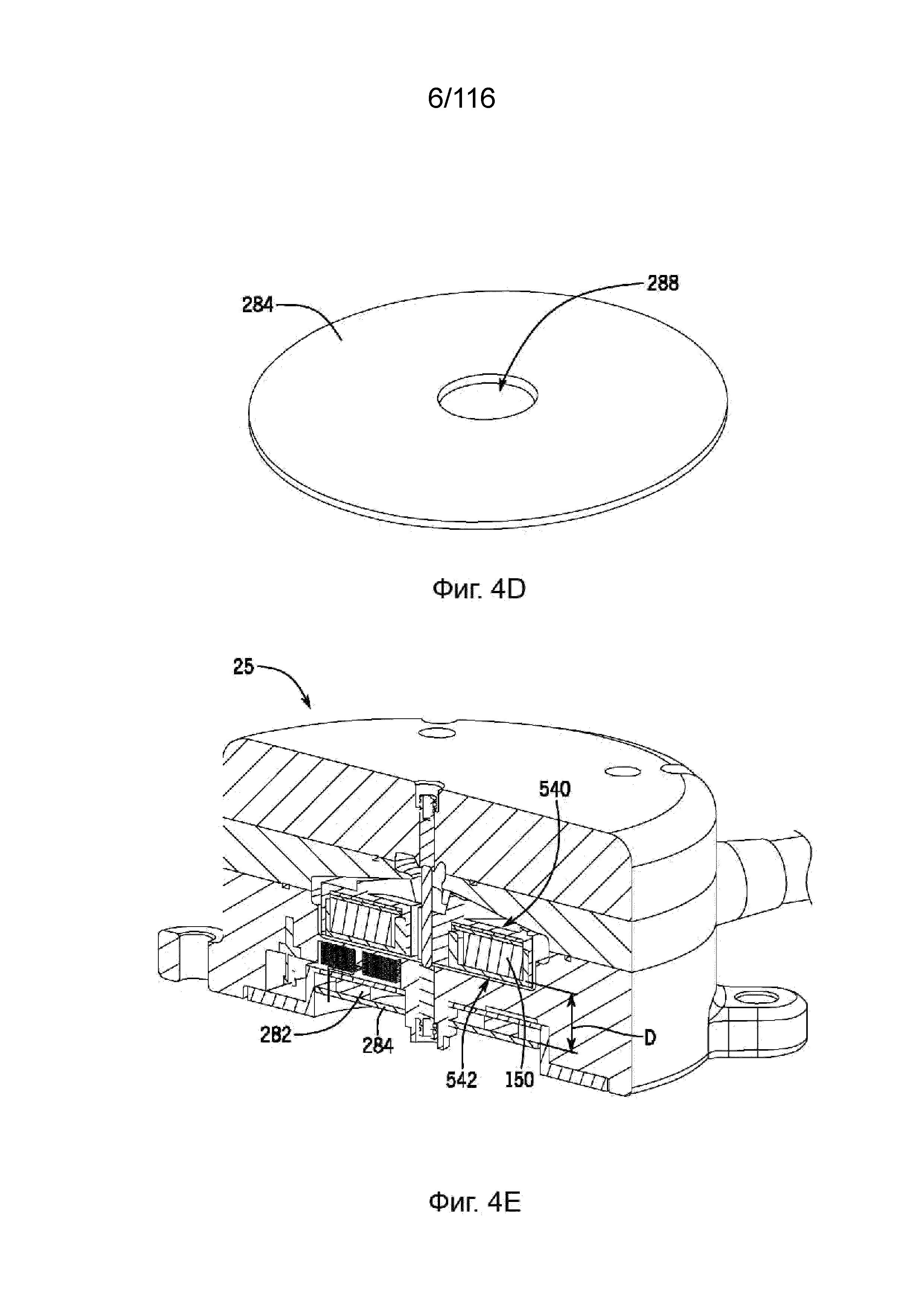
[59] На фиг. 4D приведен вид в перспективе опорной пластины согласно одному варианту реализации изобретения.
[60] На фиг. 4E приведен вид сбоку в разрезе насоса согласно одному варианту реализации изобретения.
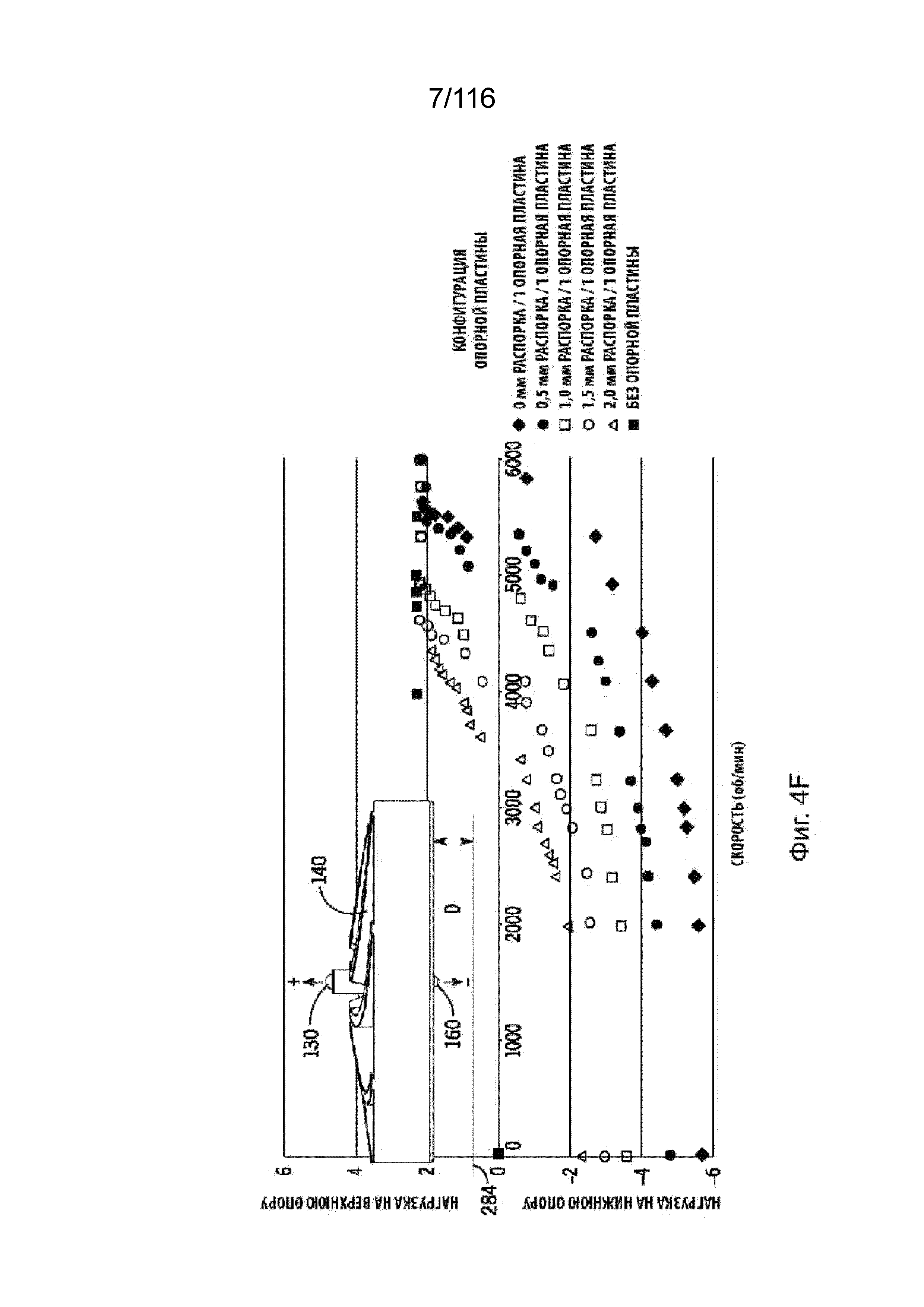
[61] На фиг. 4F приведен график и иллюстрация, изображающая нагрузки на верхней и нижней опорах, в зависимости от расположения опорной пластины согласно одному варианту реализации изобретения.
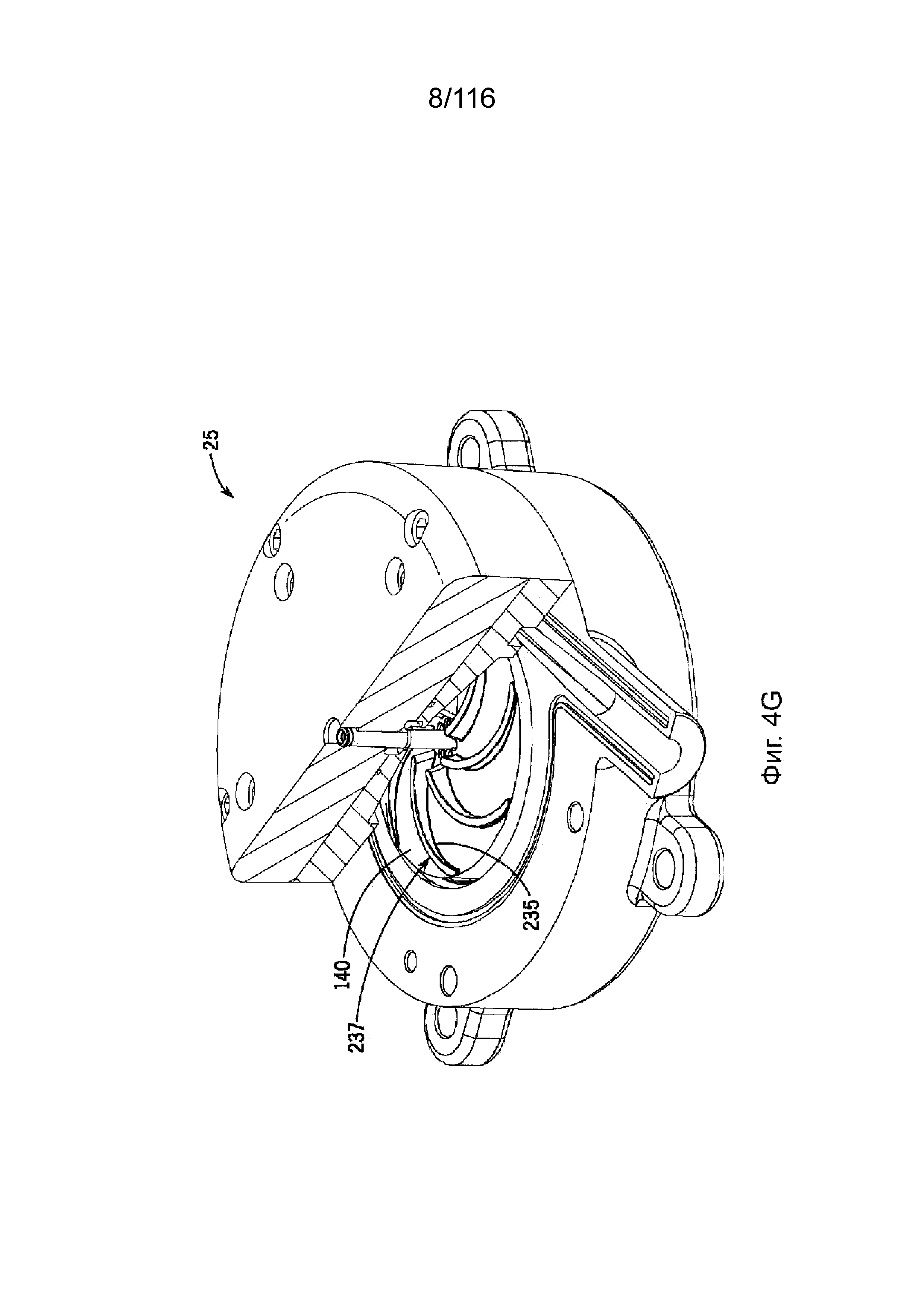
[62] На фиг. 4G приведен вид с частичным разрезом перфузионного насоса, иллюстрирующий площадь поверхности крыльчатки, которая обеспечивает гидродинамическую опору согласно одному варианту реализации изобретения.
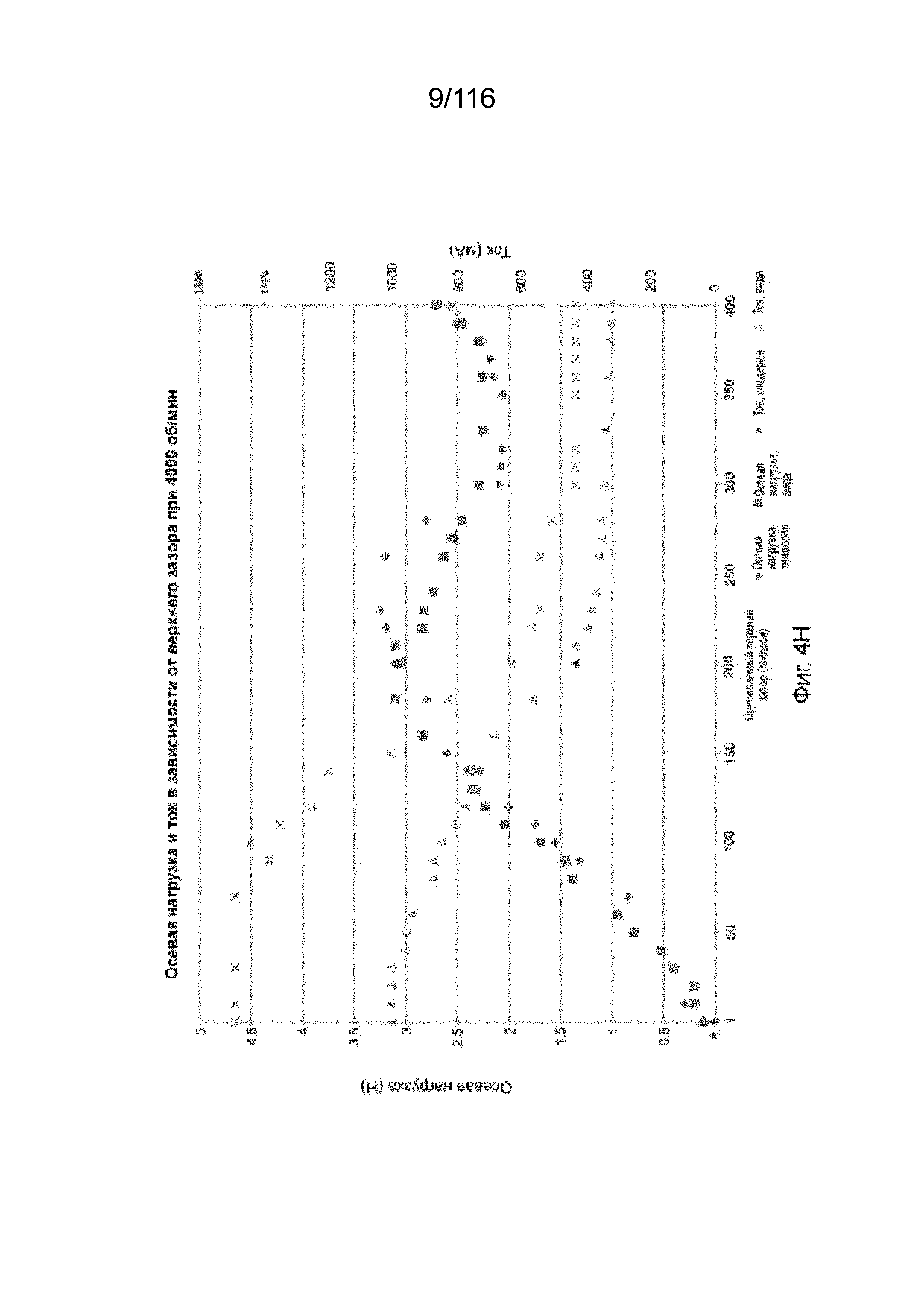
[63] [0063] На фиг. 4H приведен график, изображающий осевую нагрузку на верхней опоре в зависимости от верхнего зазора между крыльчаткой и верхним корпусом, при насосе, работающем с частотой вращения 4000 об/мин.
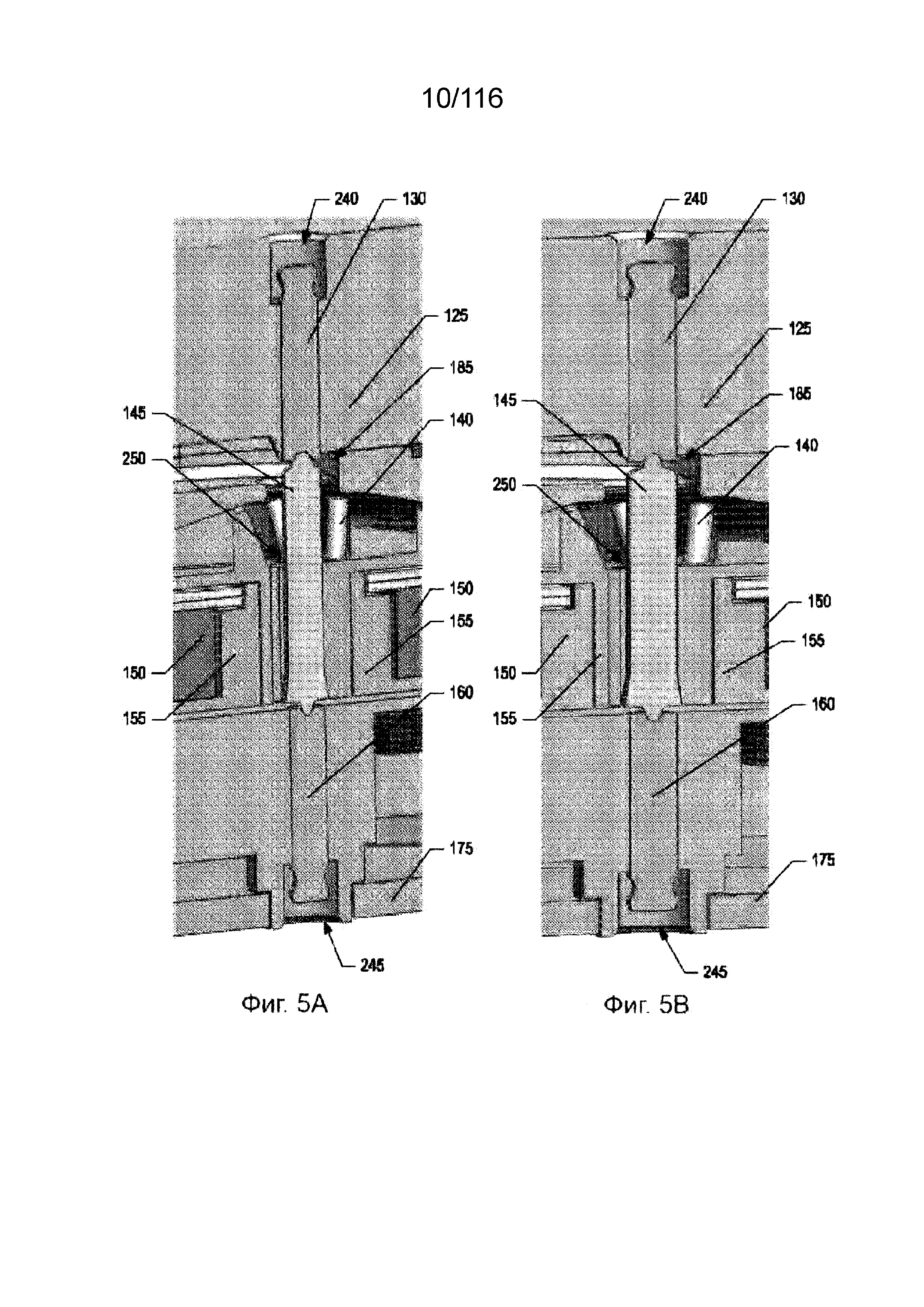
[64] На фиг. 5A-B приведены увеличенные изображения в области оси вращения по фиг. 3B и 4B.
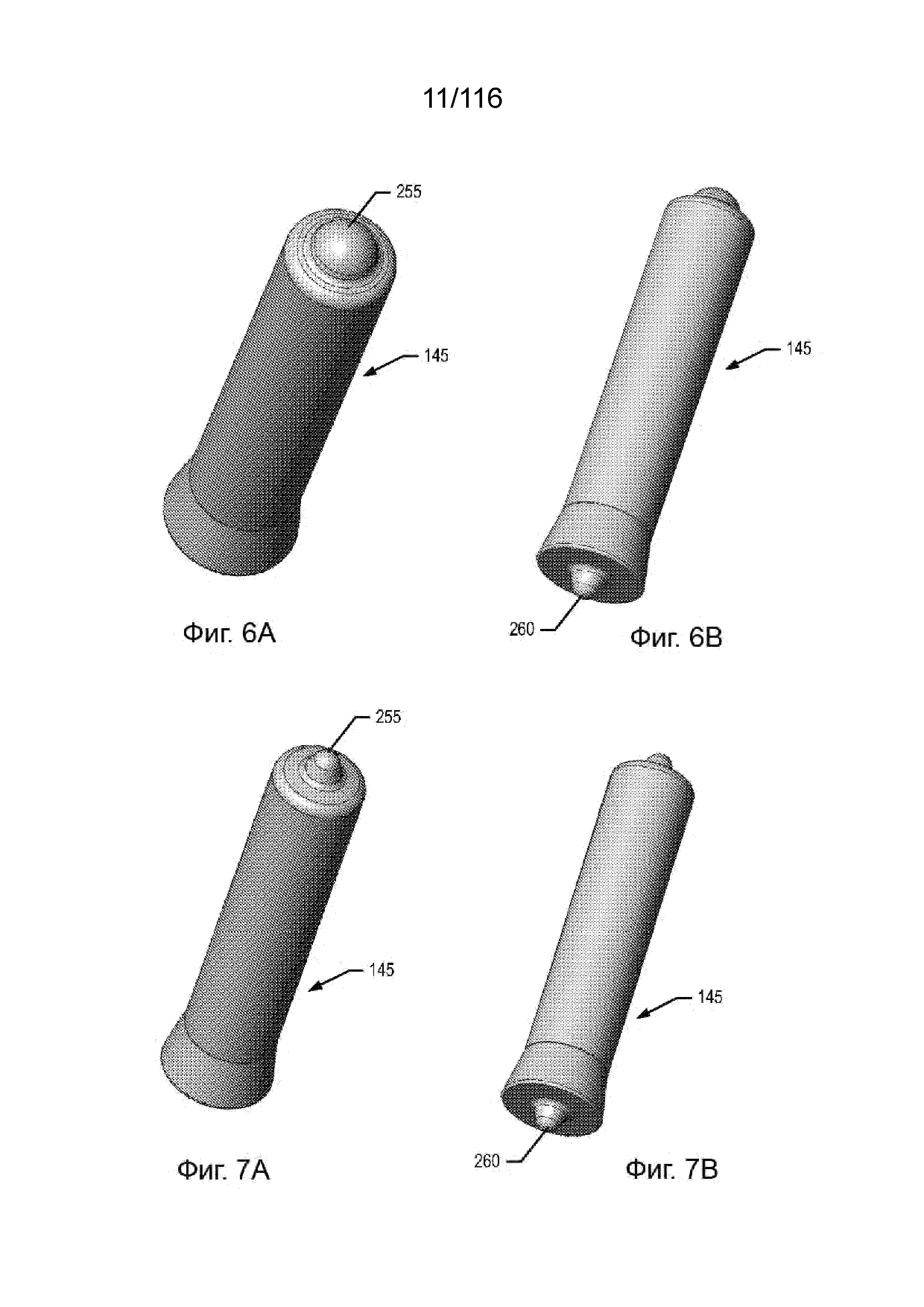
[65] На фиг. 6A-B, соответственно, приведены виды сверху и снизу в изометрии оси крыльчатки.
[66] На фиг. 7A-B, соответственно, приведены виды сверху и снизу в изометрии оси крыльчатки.
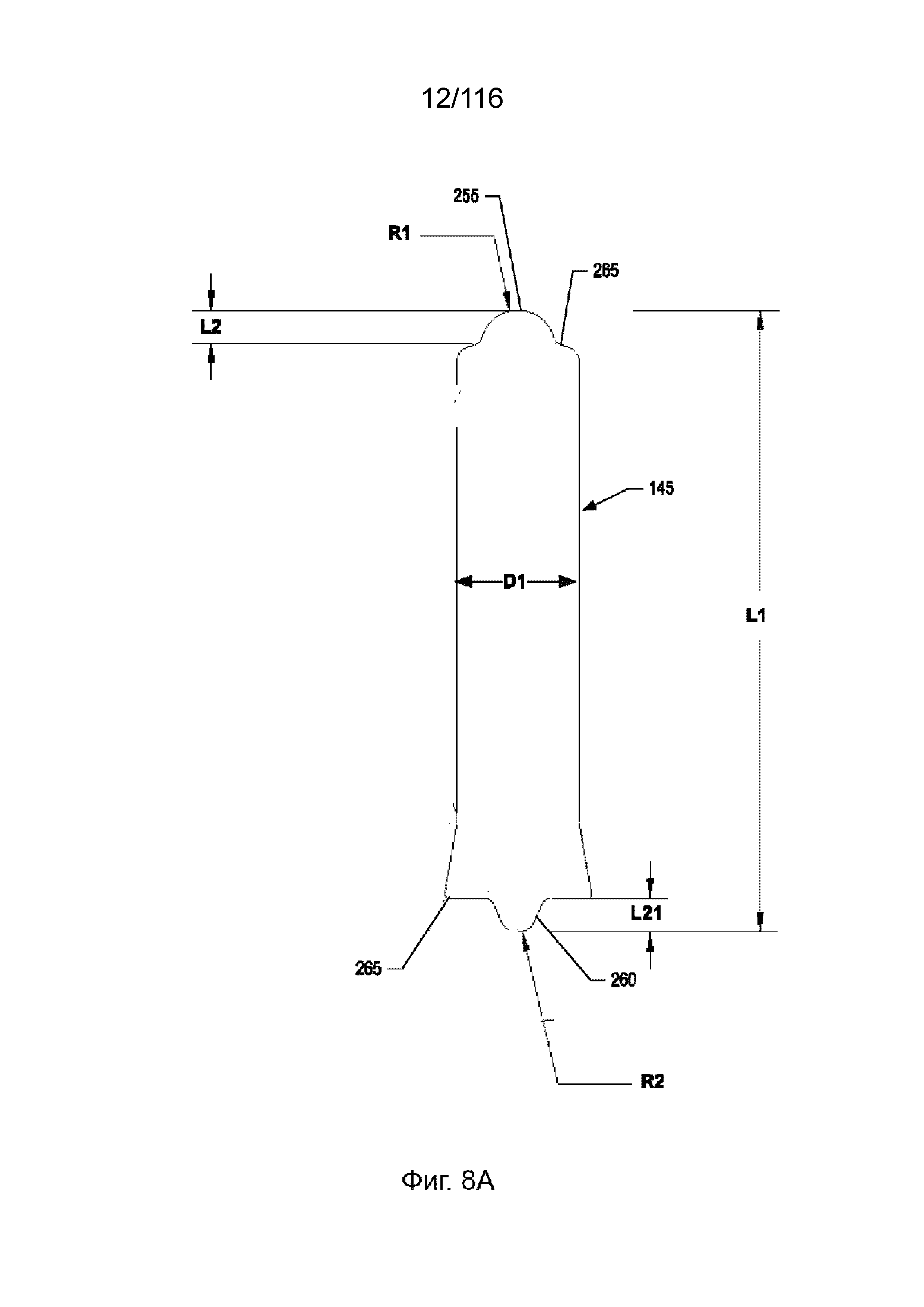
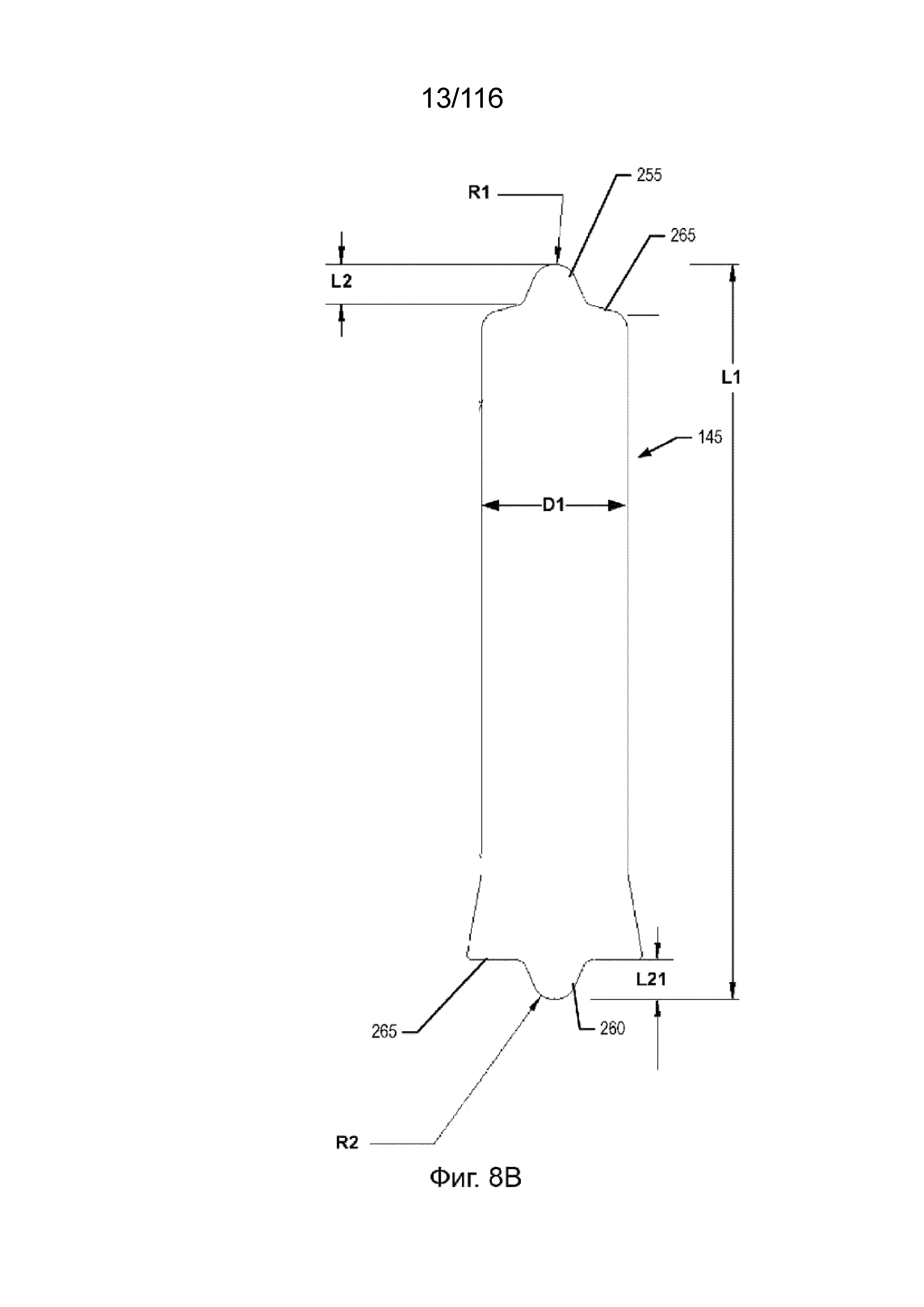
[67] На фиг. 8A-B приведены виды сбоку вариантов реализации оси крыльчатки.
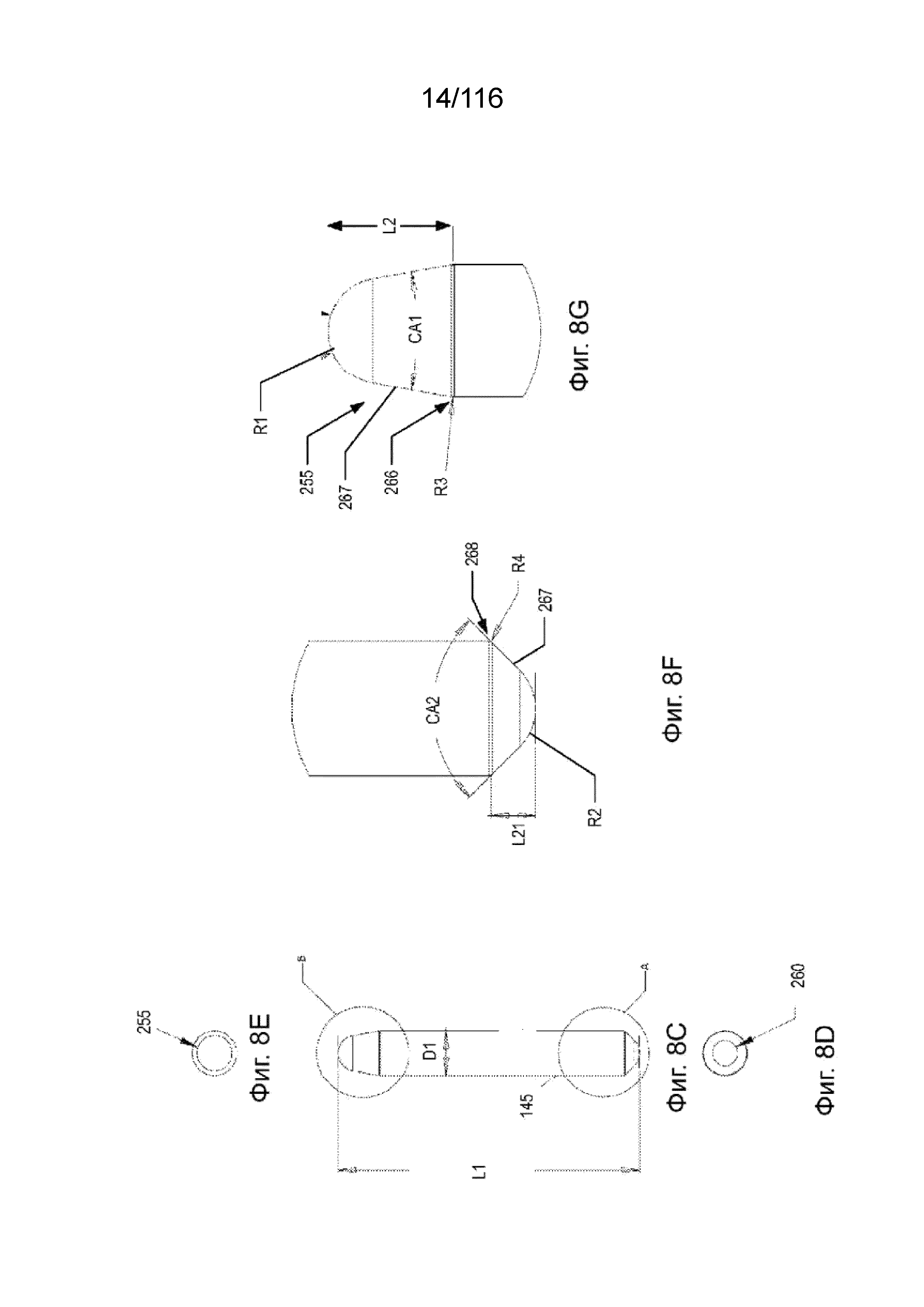
[68] На фиг. 8C приведен вид сбоку варианта реализации оси крыльчатки.
[69] На фиг. 8D-E приведены, соответственно, верхняя и нижняя поверхность варианта реализации оси крыльчатки.
[70] На фиг. 8F-G приведены виды в увеличенном масштабе верха и низа осей, соответственно, для варианта реализации оси крыльчатки.
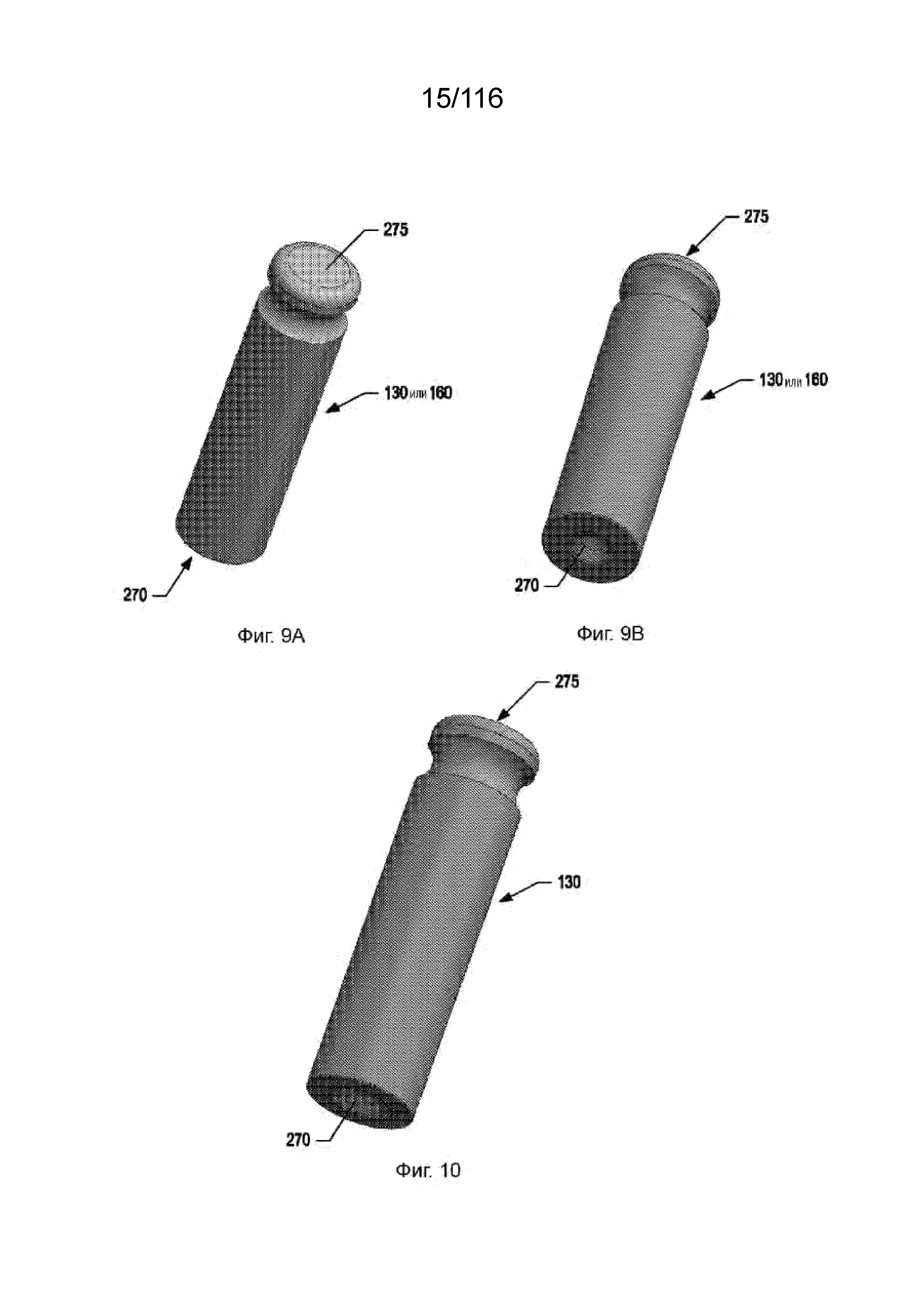
[71] На фиг. 9A-B приведены, соответственно, виды противоположных концов типичного опорного штифта используемого для каждого конца оси крыльчатки для поддержки и обеспечения вращения оси крыльчатки.
[72] На фиг. 10 приведен вид варианта реализации верхнего опорного штифта.
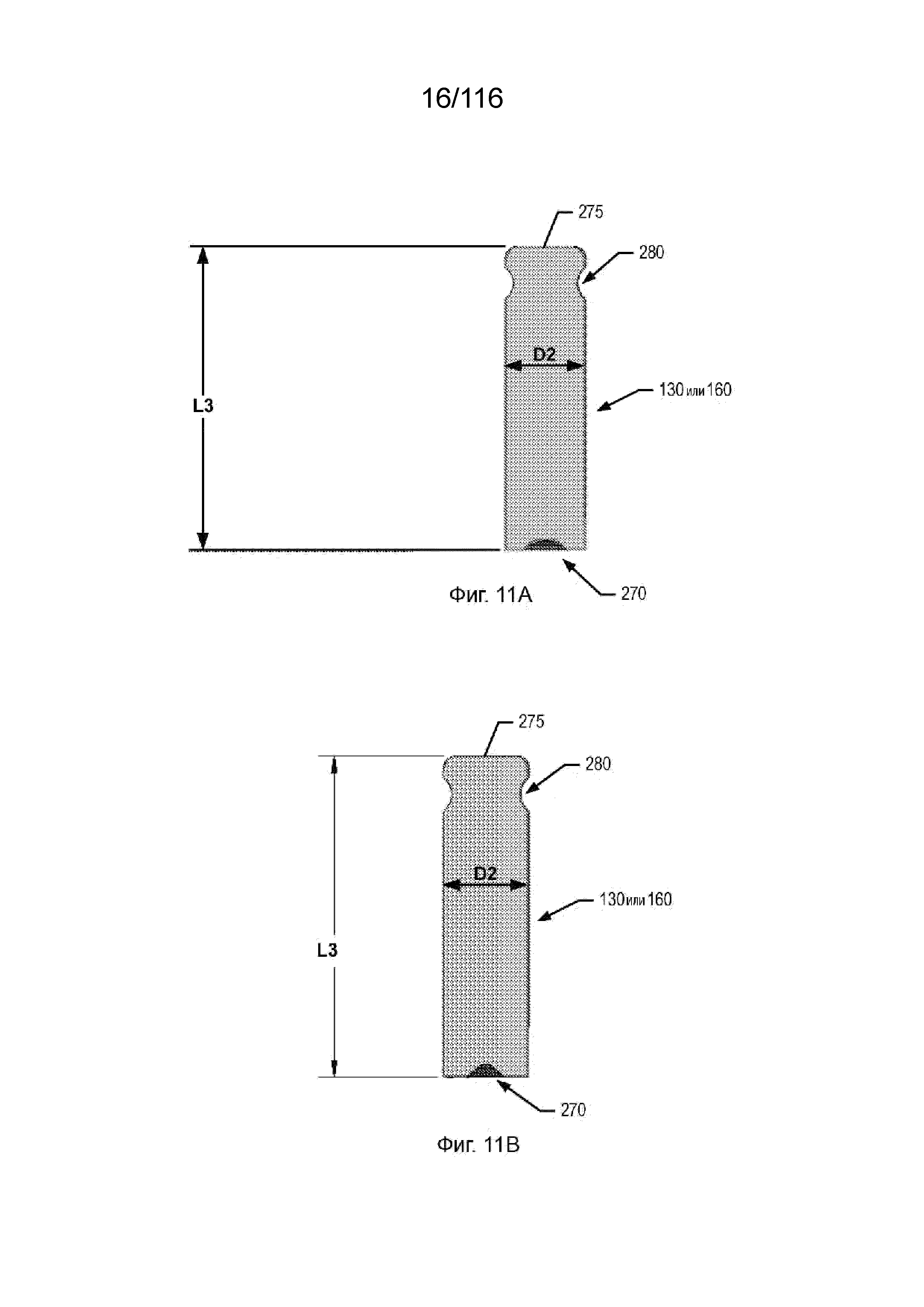
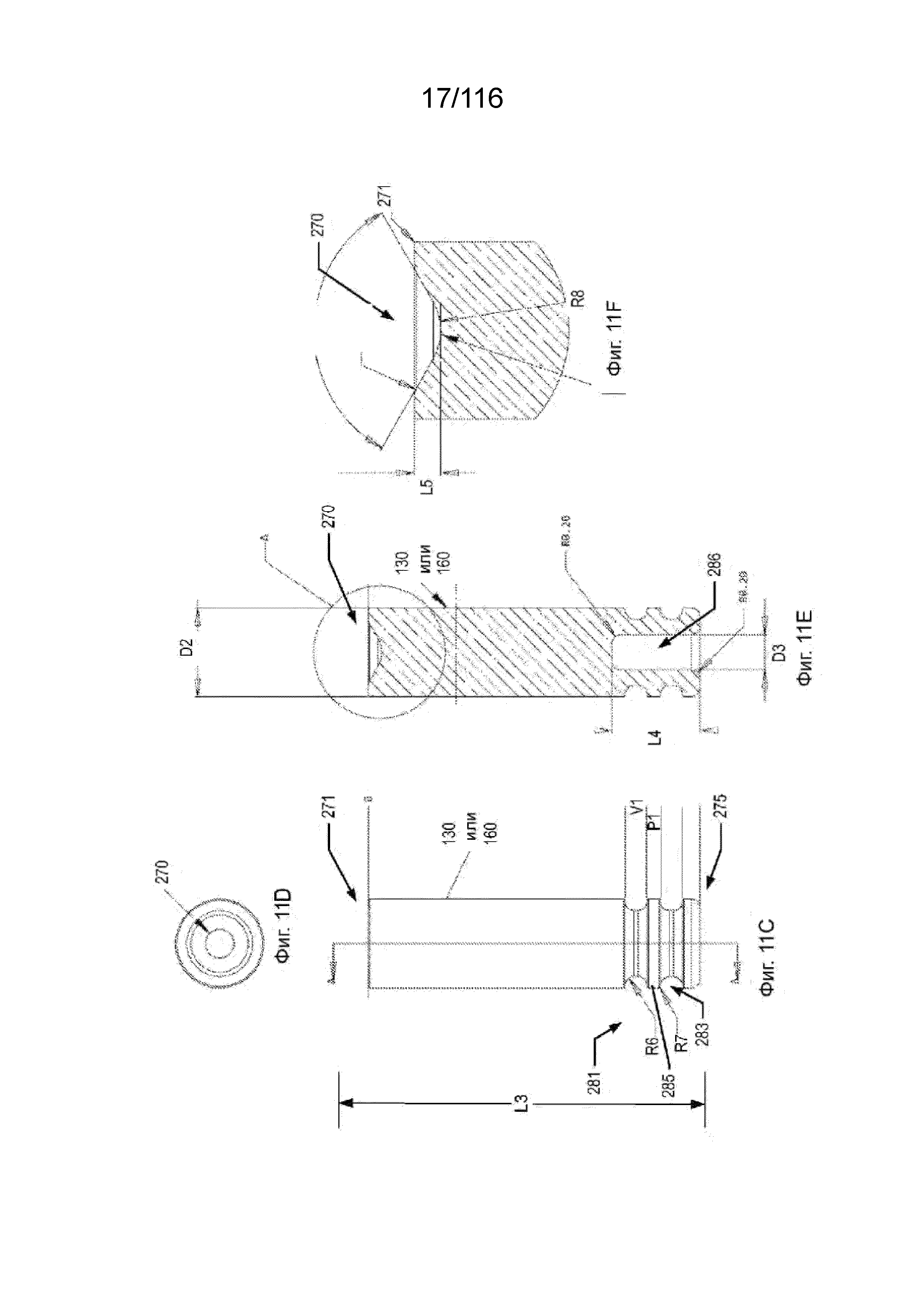
[73] На фиг. 11A-B приведены виды сбоку вариантов реализации типичного опорного штифта.
[74] На фиг. 11C приведен вид сбоку типичного опорного штифта.
[75] На фиг. 11D приведен вид сверху одного конца типичного опорного штифта.
[76] На фиг. 11E-F приведены виды поперечных разрезов типичного опорного штифта и опорной поверхности, соответственно, типичного опорного штифта по линии сечения A-A на фиг. 11C.
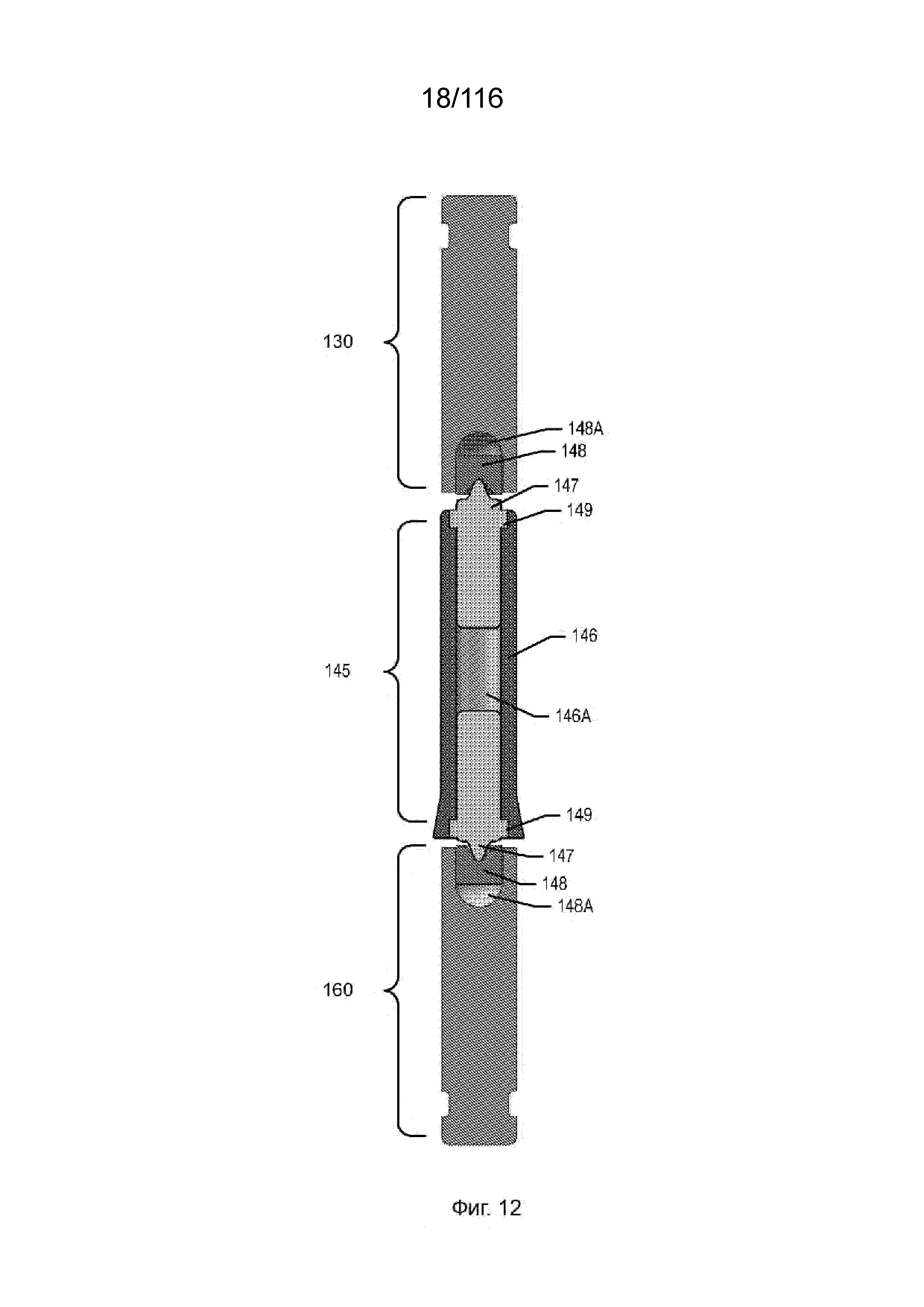
[77] На фиг. 12 приведен продольный разрез узла типичного опорного штифта.
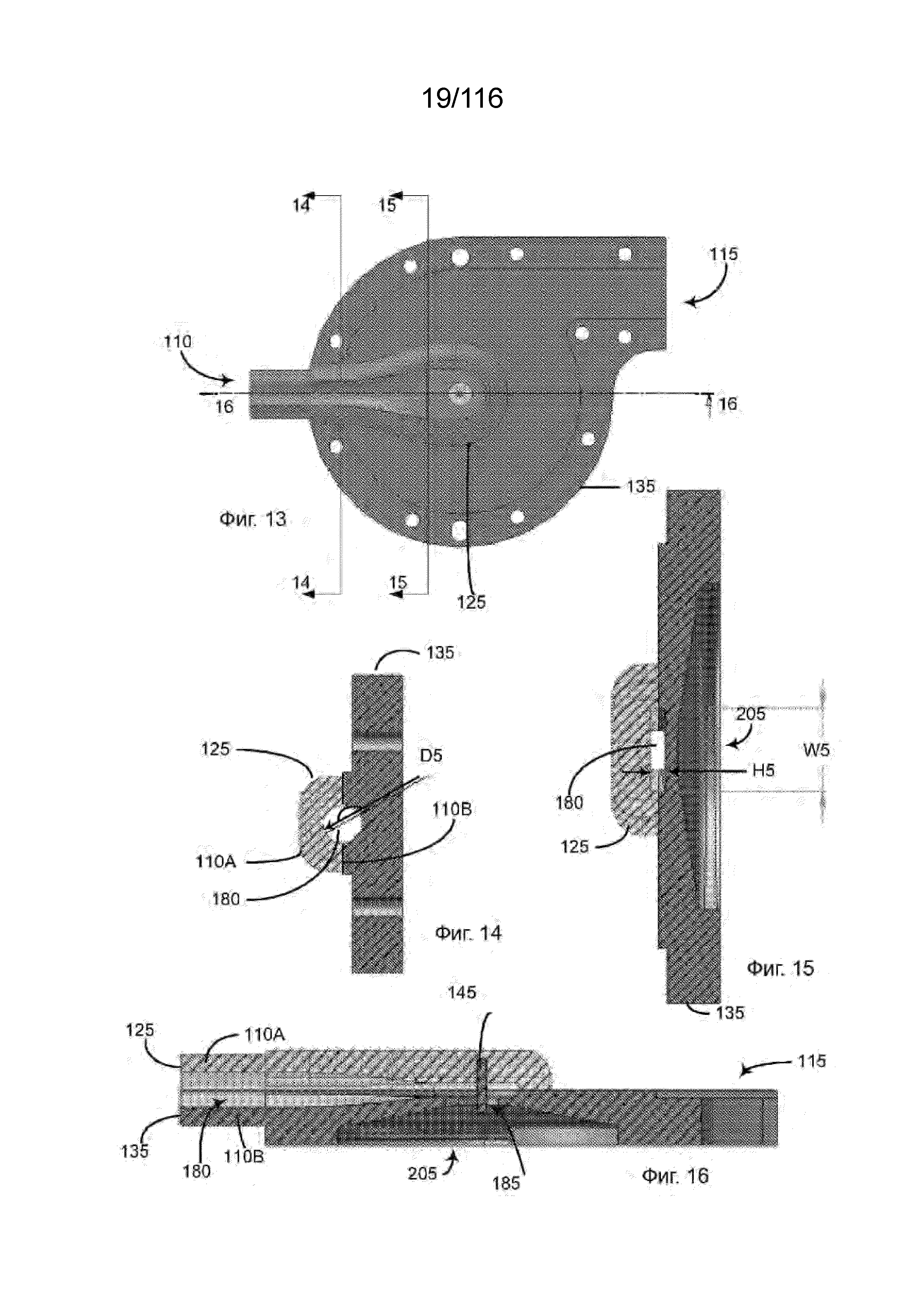
[78] На фиг. 13 приведен вид сверху впускной крышки и корпуса крыльчатки.
[79] На фиг. 14-16 приведены, соответственно, поперечные разрезы по линиям сечения 14-14, 15-15, и 16-16 на фиг. 13.
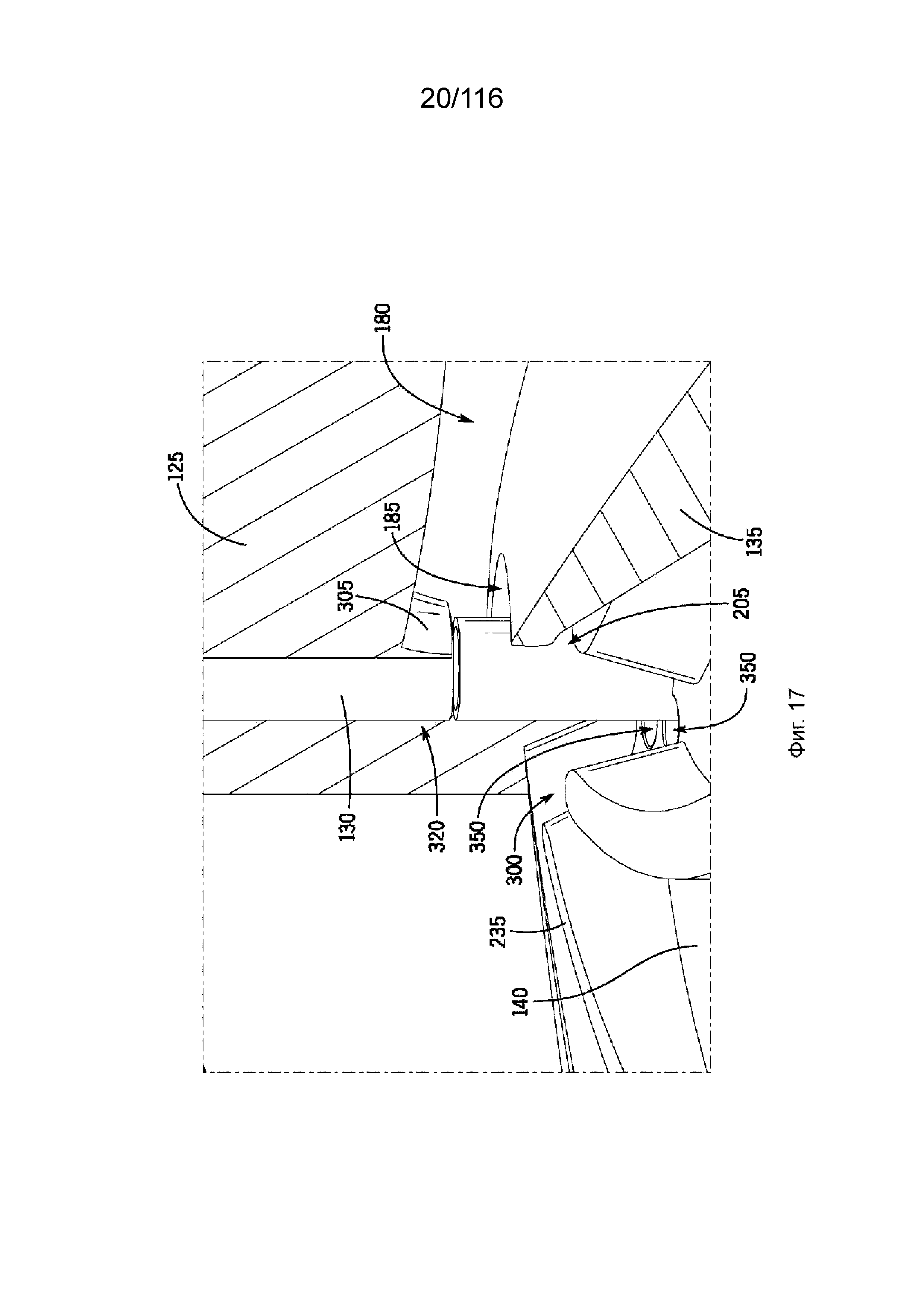
[80] На фиг. 17 представлен вид в изометрии с частичным разрезом впускного отверстия камеры крыльчатки.
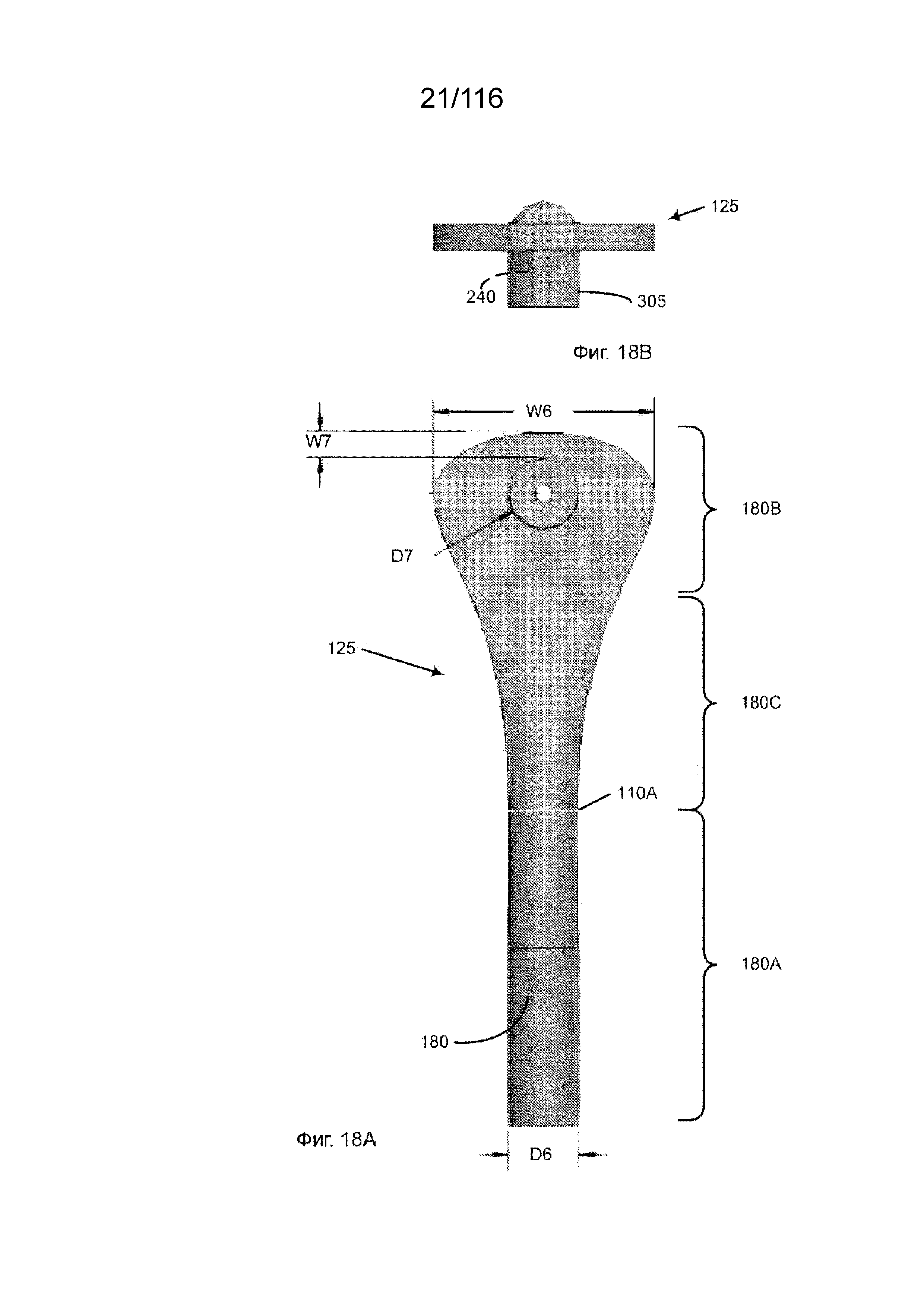
[81] На фиг. 18A и 18B приведены, соответственно, вид сверху части впускной крышки, образующей впускной канал, и ее вид с торца.
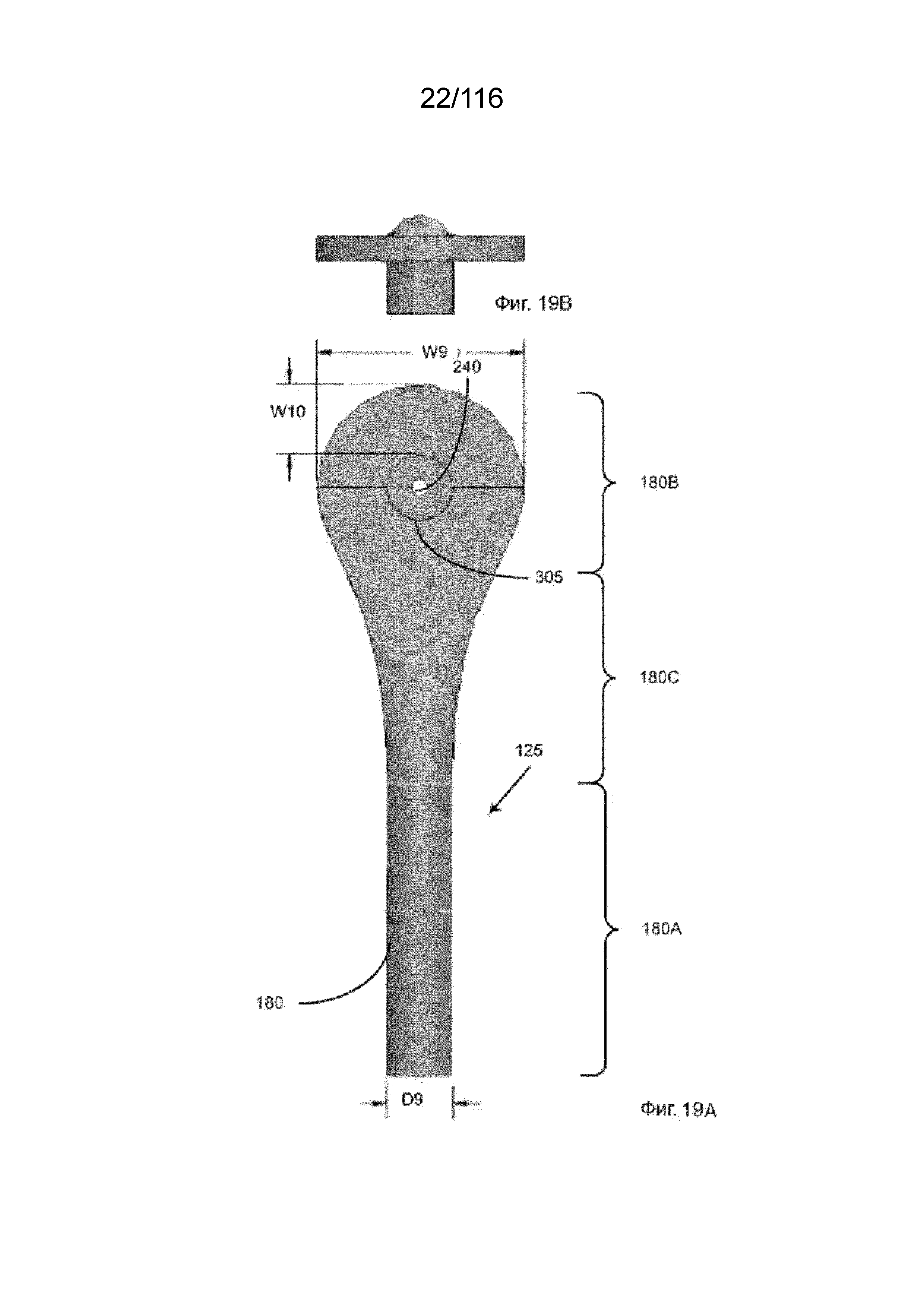
[82] На фиг. 19A и 19B представлены те же виды в перспективе, что и на фиг. 18A и18B, но для другого варианта реализации изобретения.
[83] На фиг. 20A и 20B представлены те же виды в перспективе, что и на фиг. 18A и18B, но для другого варианта реализации изобретения.
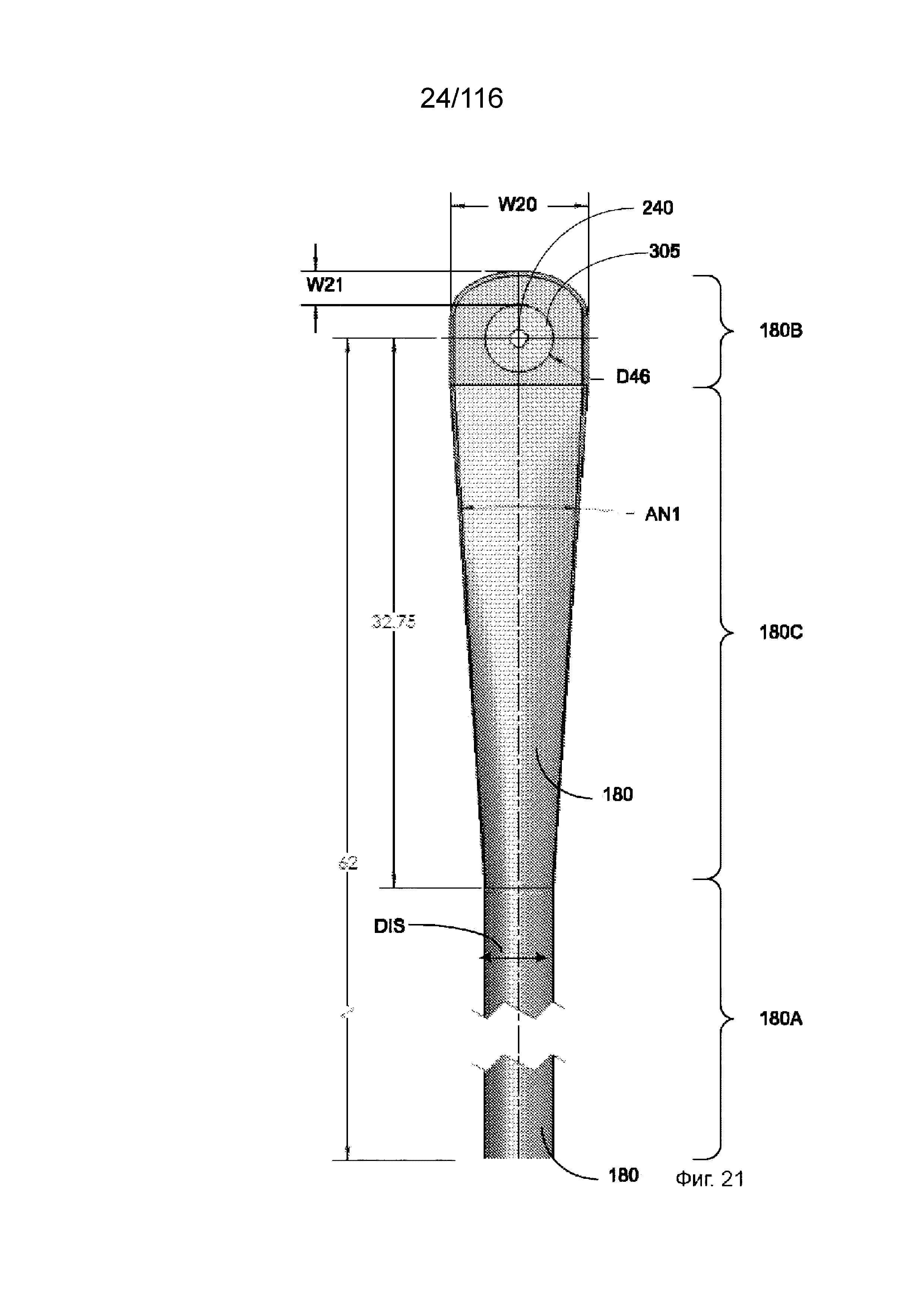
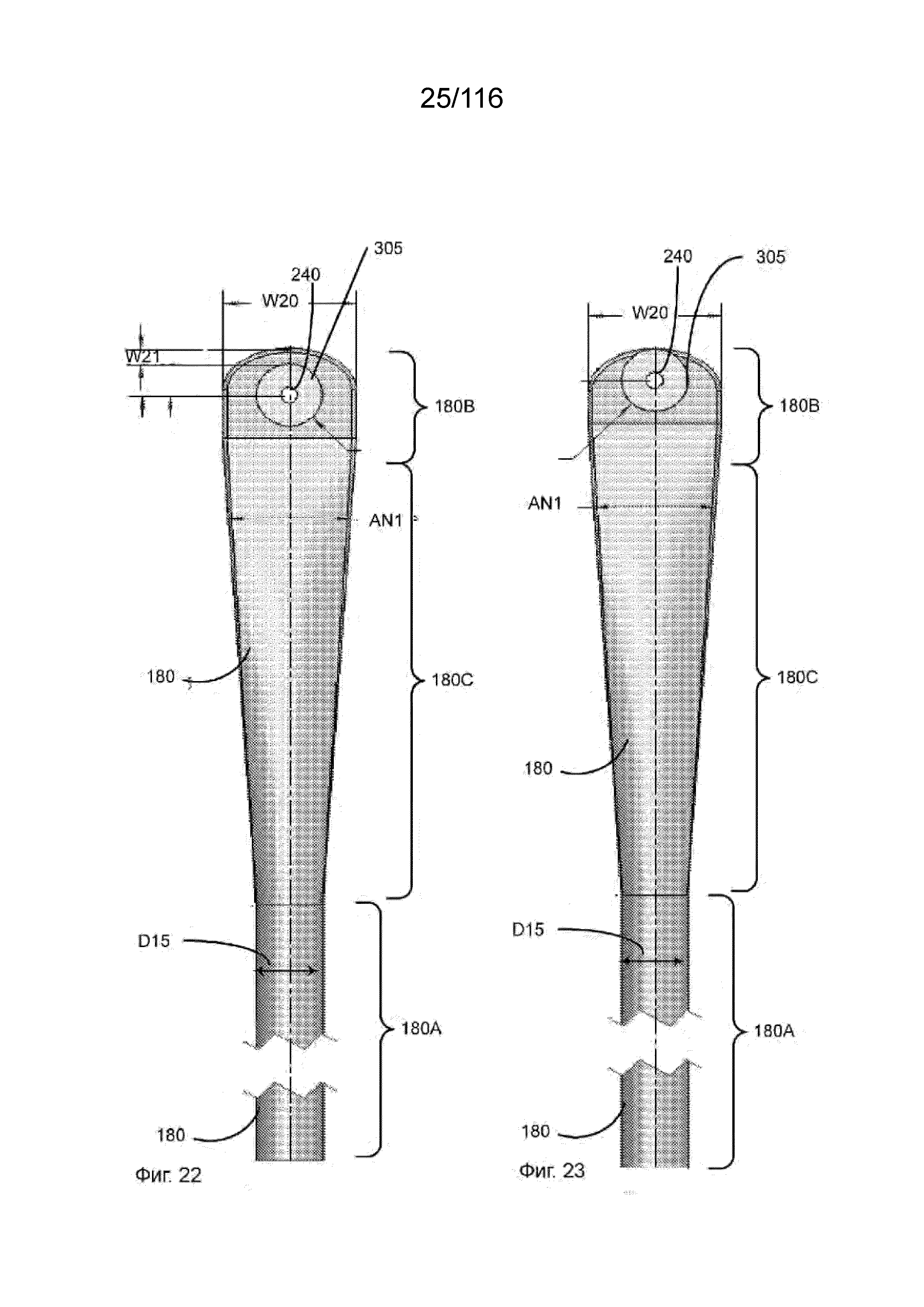
[84] На фиг. 21-23 представлены те же виды в перспективе, что и на фиг. 18A, за исключением трех предыдущих вариантов реализации изобретения.
[85] На фиг. 24A и 24B представлены, соответственно, виды сверху и сбоку другого варианта реализации впускной крышки и впускного канала, аналогичных описанным на фиг. 21, за исключением того, что дополнительно включен дугообразный клиновидный участок.
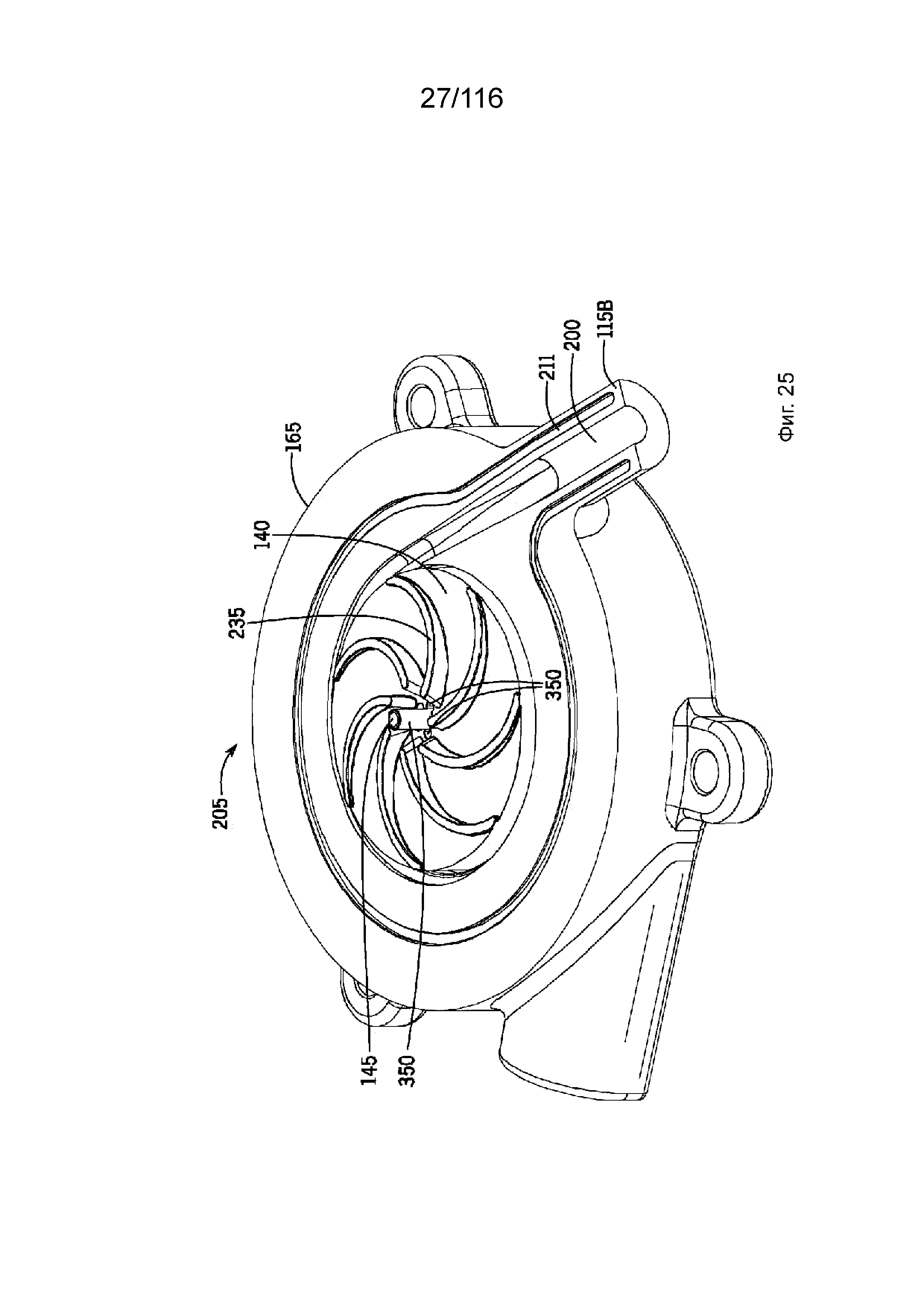
[86] На фиг. 25 представлен вид в изометрии насоса с удаленным верхним корпусом крыльчатки для показа крыльчатки, занимающей камеру крыльчатки.
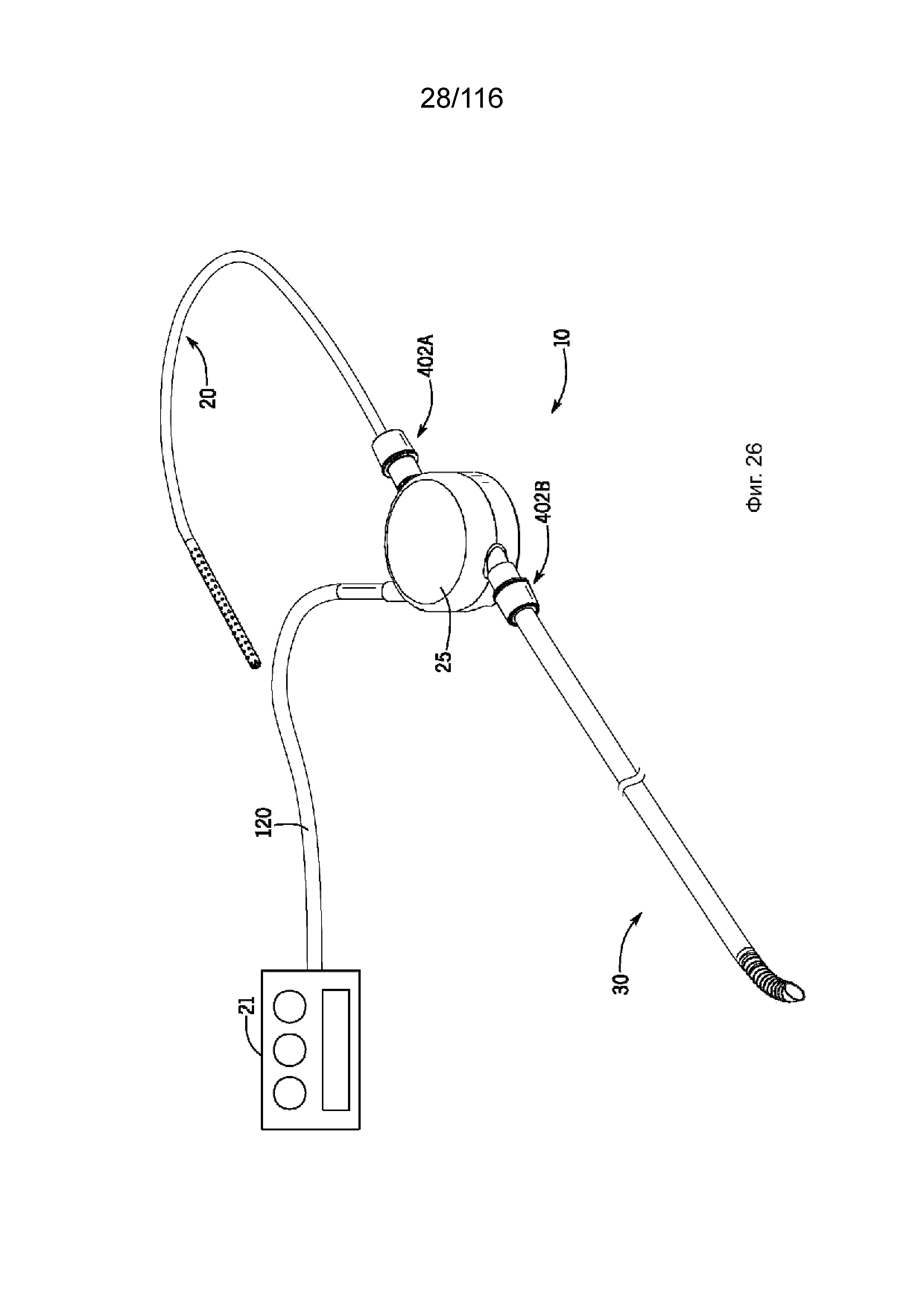
[87] На фиг. 26 приведен вид в перспективе перфузионной системы согласно одному варианту реализации изобретения.
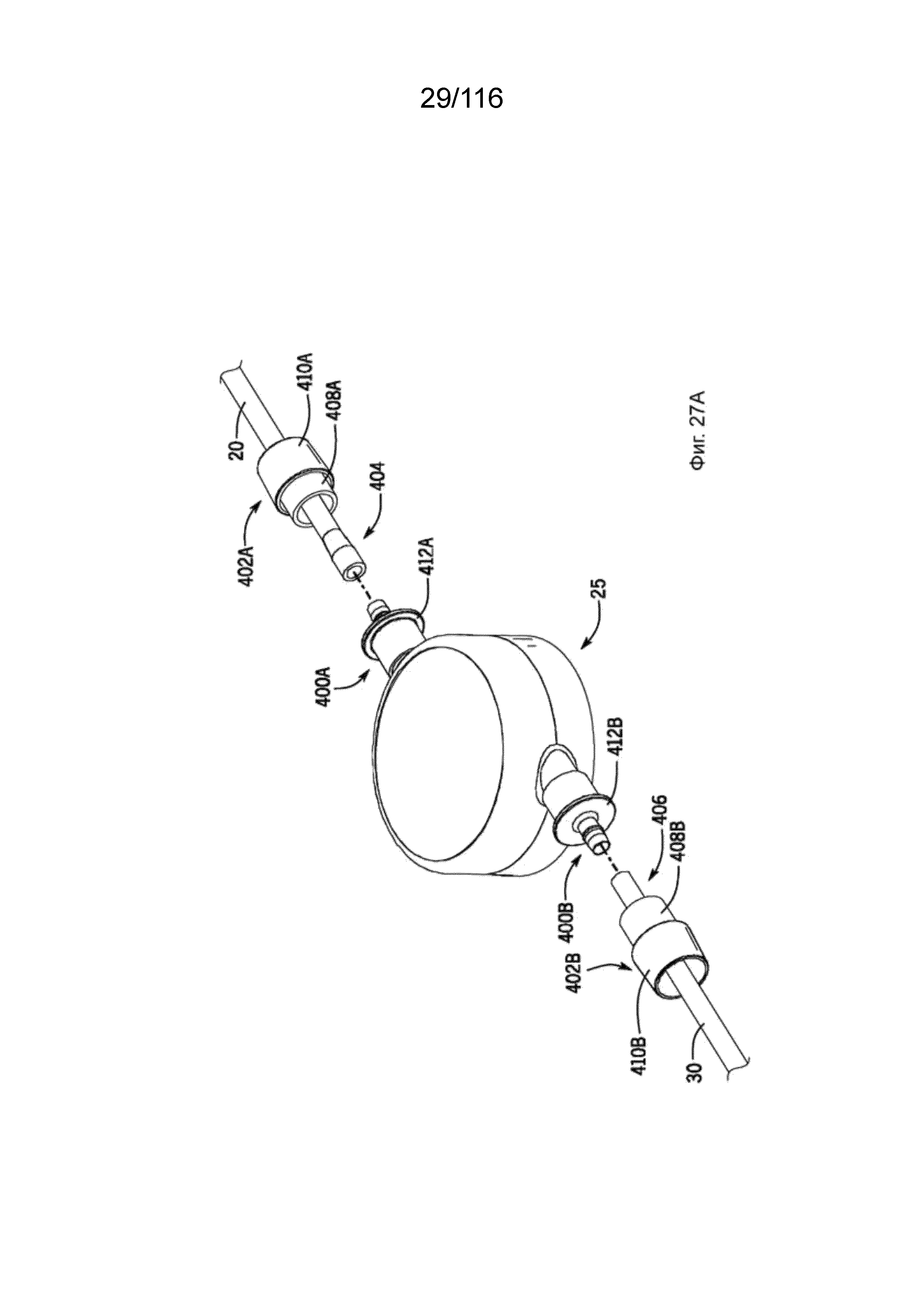
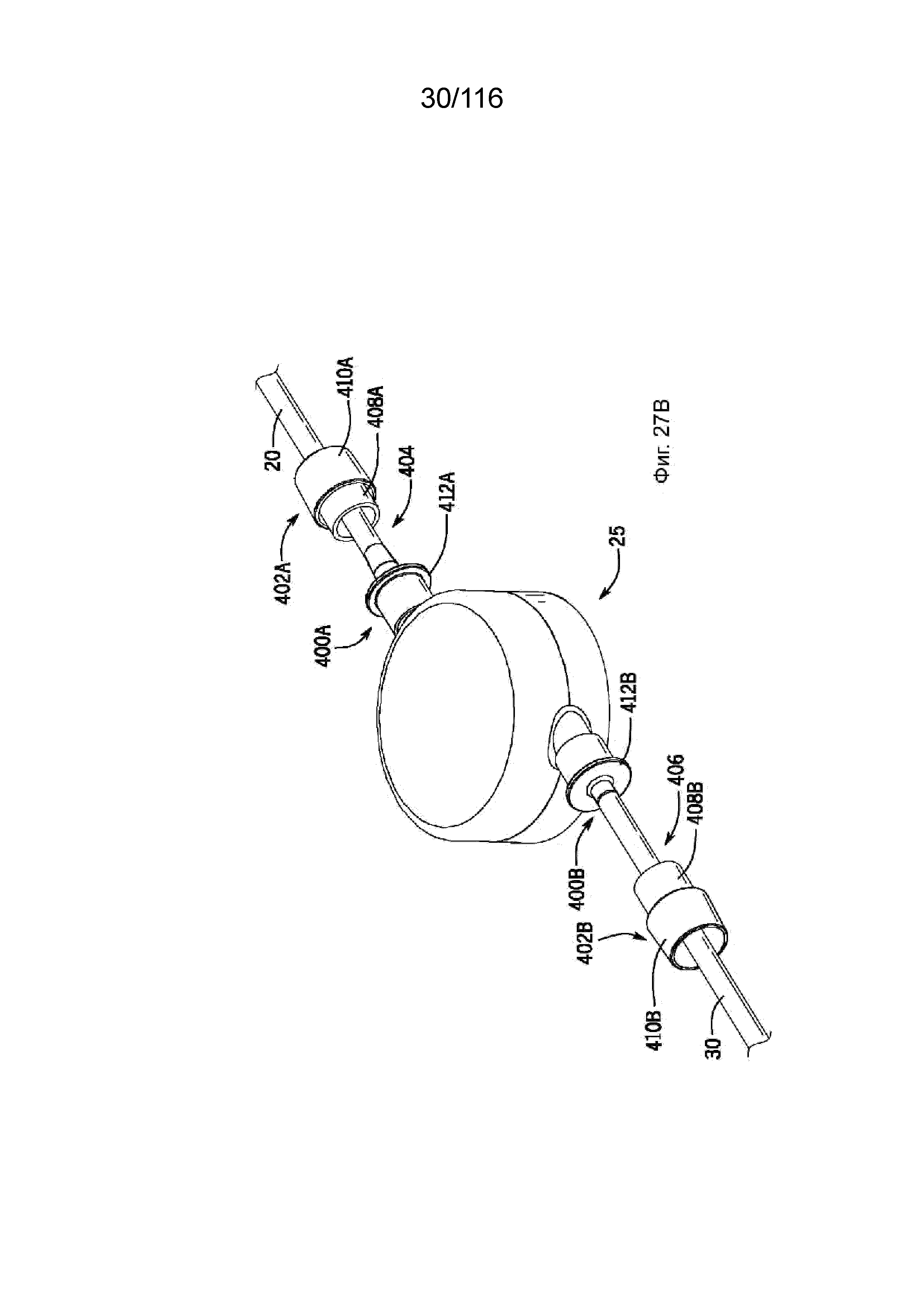
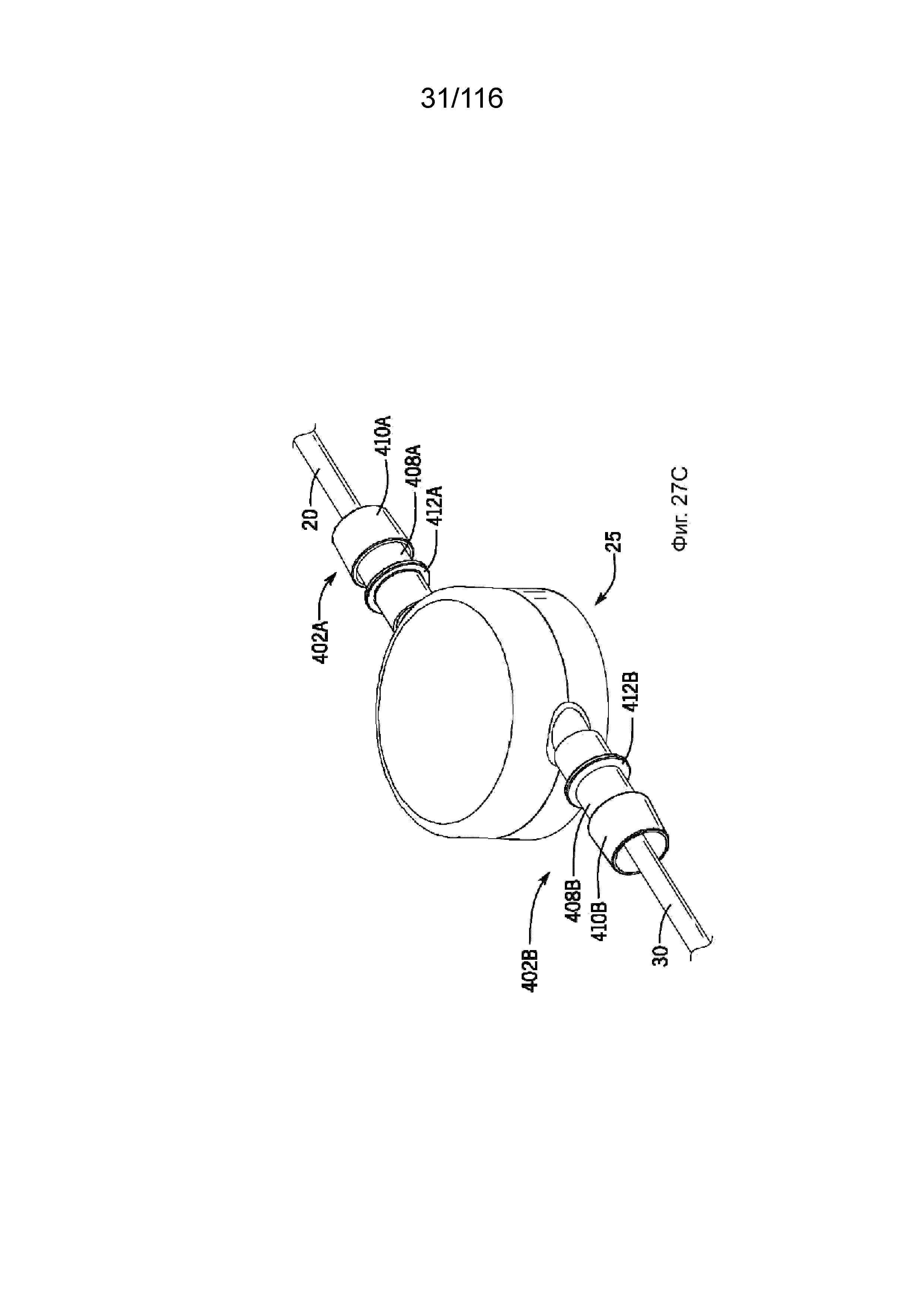
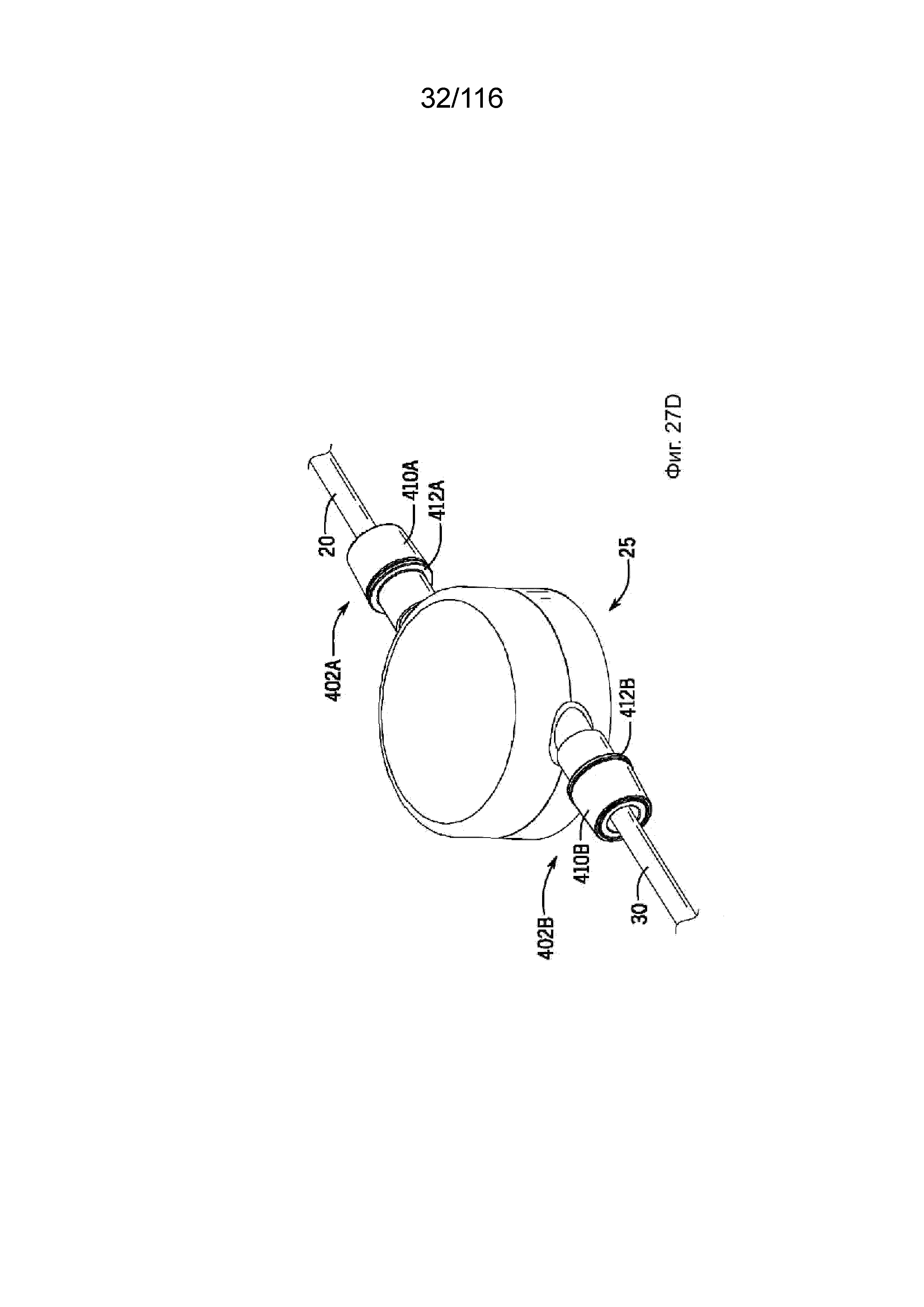
[88] На фиг. 27A-27D приведены виды в перспективе соединения между насосом и каналами согласно одному варианту реализации изобретения.
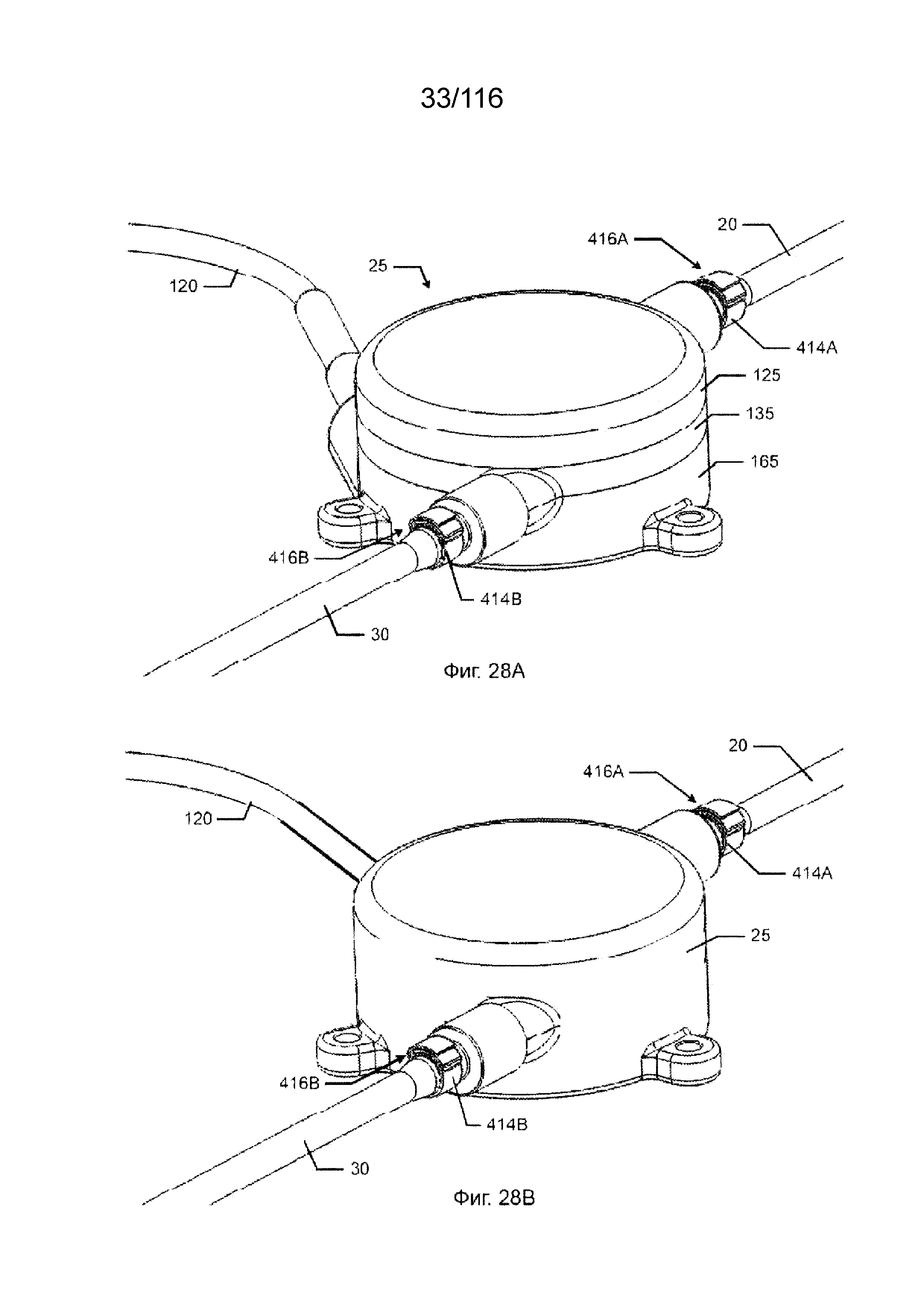
[89] На фиг. 28A и 28B приведены виды в перспективе соединения между насосом и каналами согласно одному варианту реализации изобретения.
[90] На фиг. 29A и 29B приведены виды в перспективе соединения между насосом и каналами, которые содержат боковой канал, согласно одному варианту реализации изобретения.
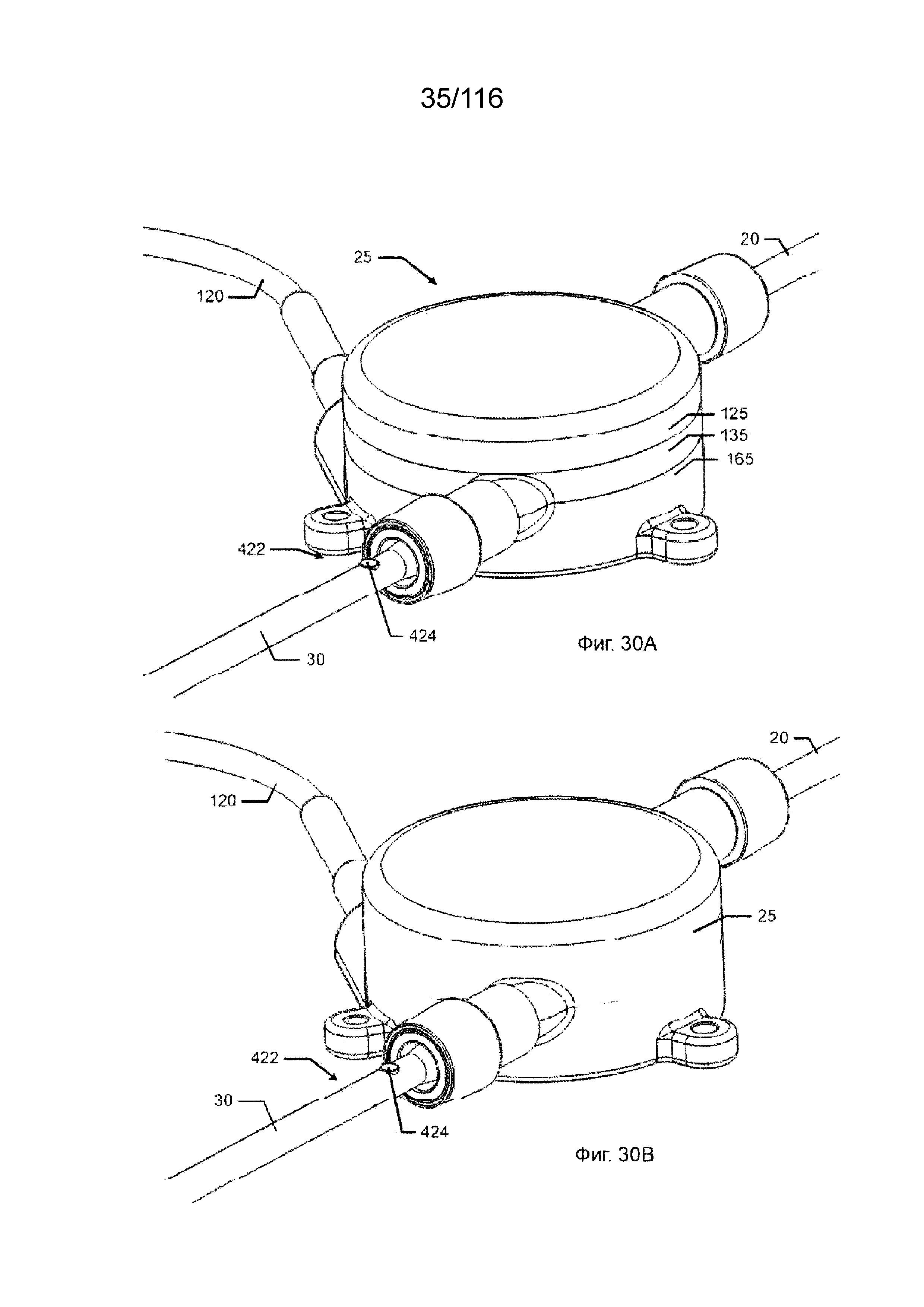
[91] На фиг. 30A и 30B приведены виды в перспективе соединения между насосом и каналами, которое содержит перегородку, согласно одному варианту реализации изобретения.
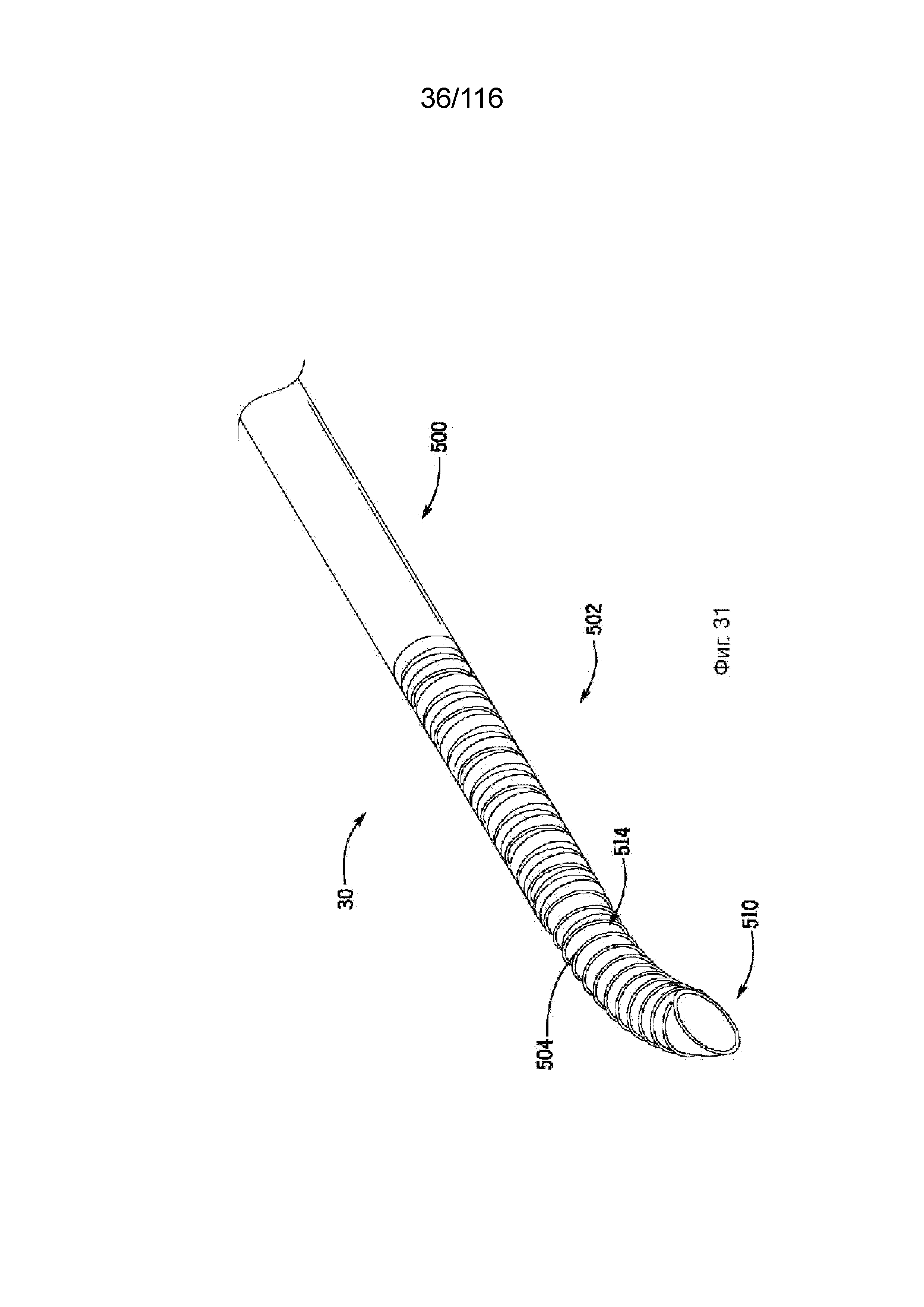
[92] На фиг. 31 приведен вид дальнего участка выводного канала согласно одному варианту реализации изобретения.
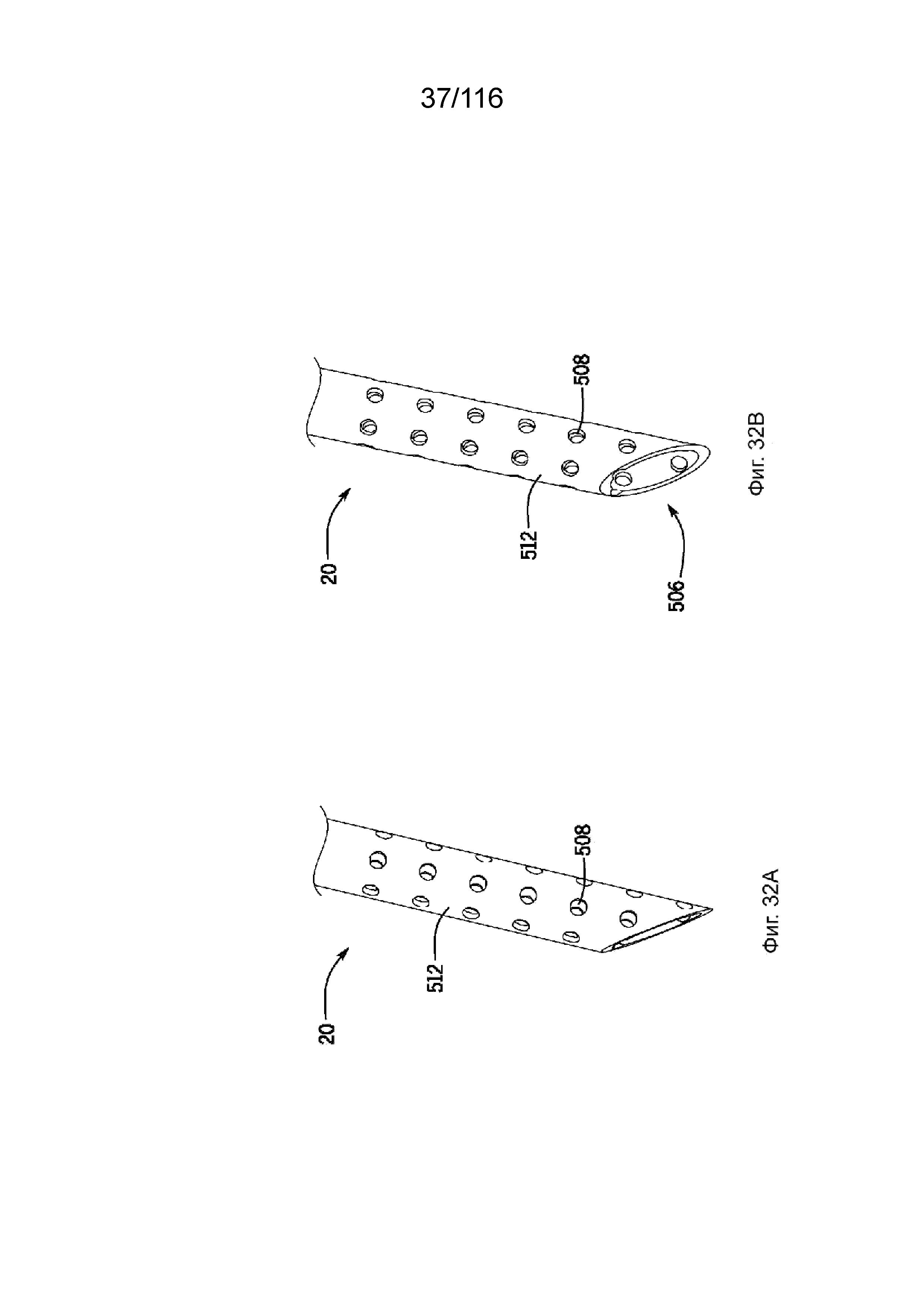
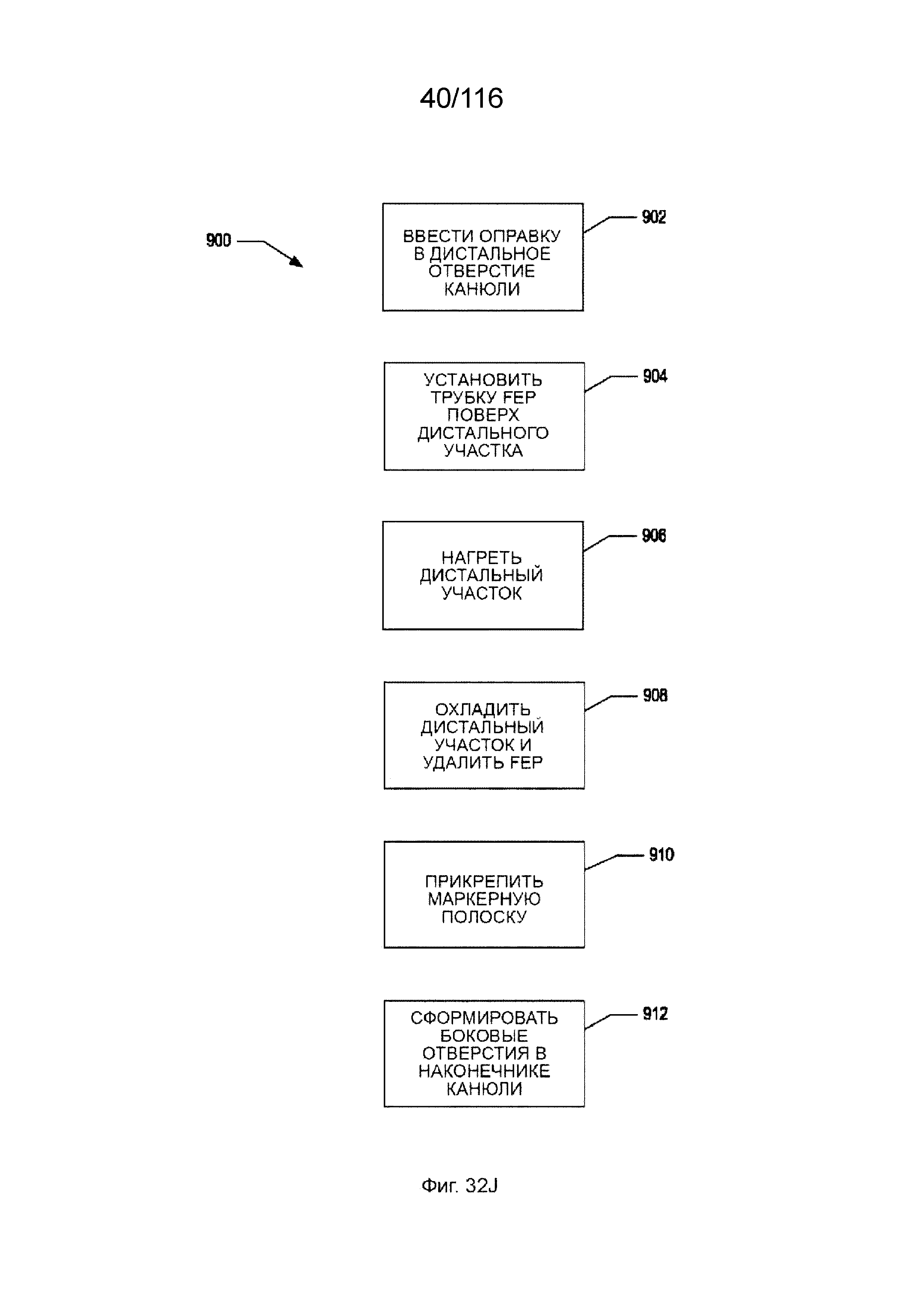
[93] На фиг. 32A и 32B приведены виды внутрисосудистого участка приточного канала согласно одному варианту реализации изобретения.
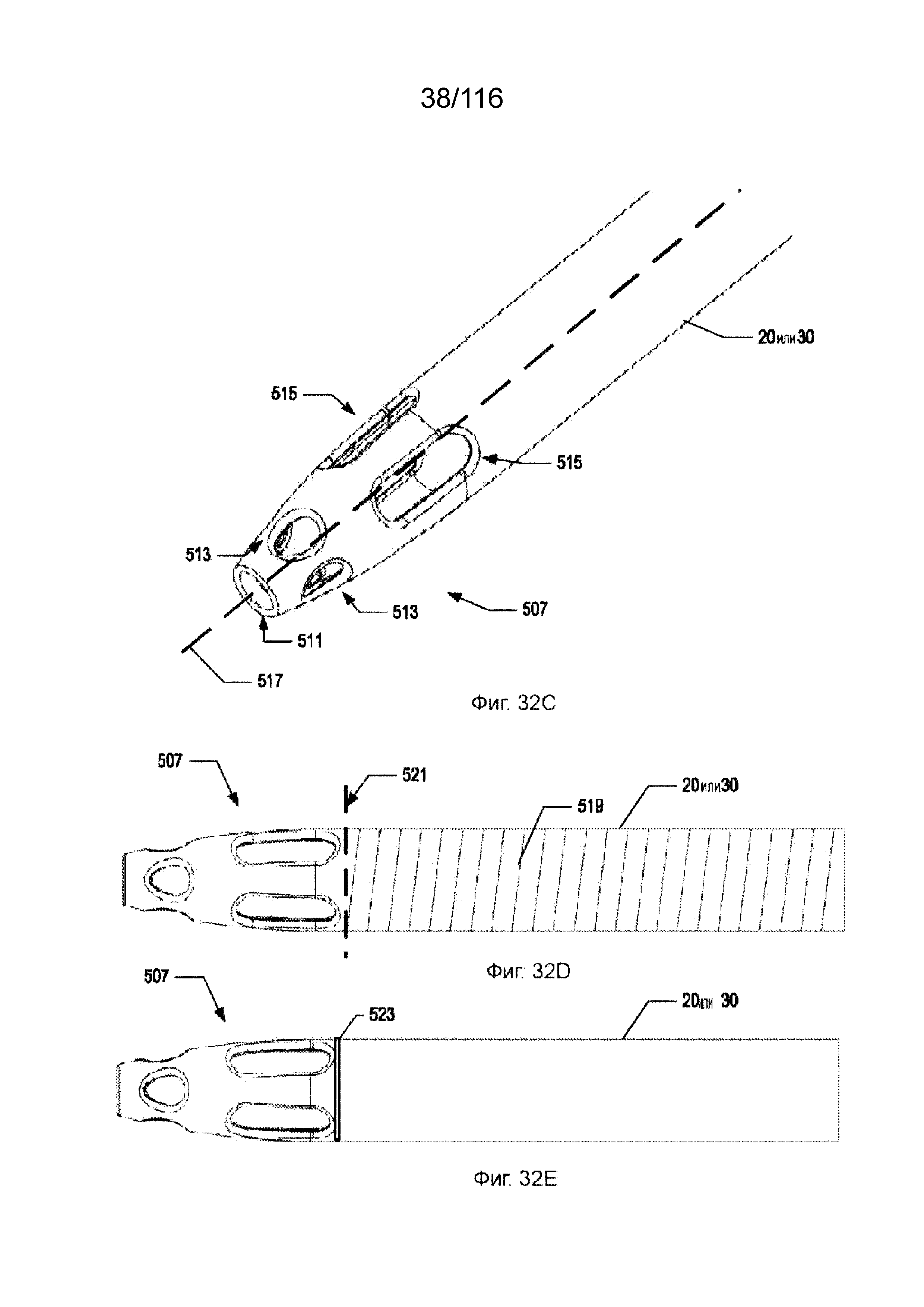
[94] На фиг. 32C приведен вид внутрисосудистого участка приточного или выводного канала согласно одному варианту реализации изобретения.
[95] На фиг. 32D приведен вид сверху внутрисосудистого участка приточного или выводного канала и упрочняющей спирали канала согласно одному варианту реализации изобретения.
[96] На фиг. 32E приведен вид сверху внутрисосудистого участка приточного или выводного канала и маркерной полоски согласно одному варианту реализации изобретения.
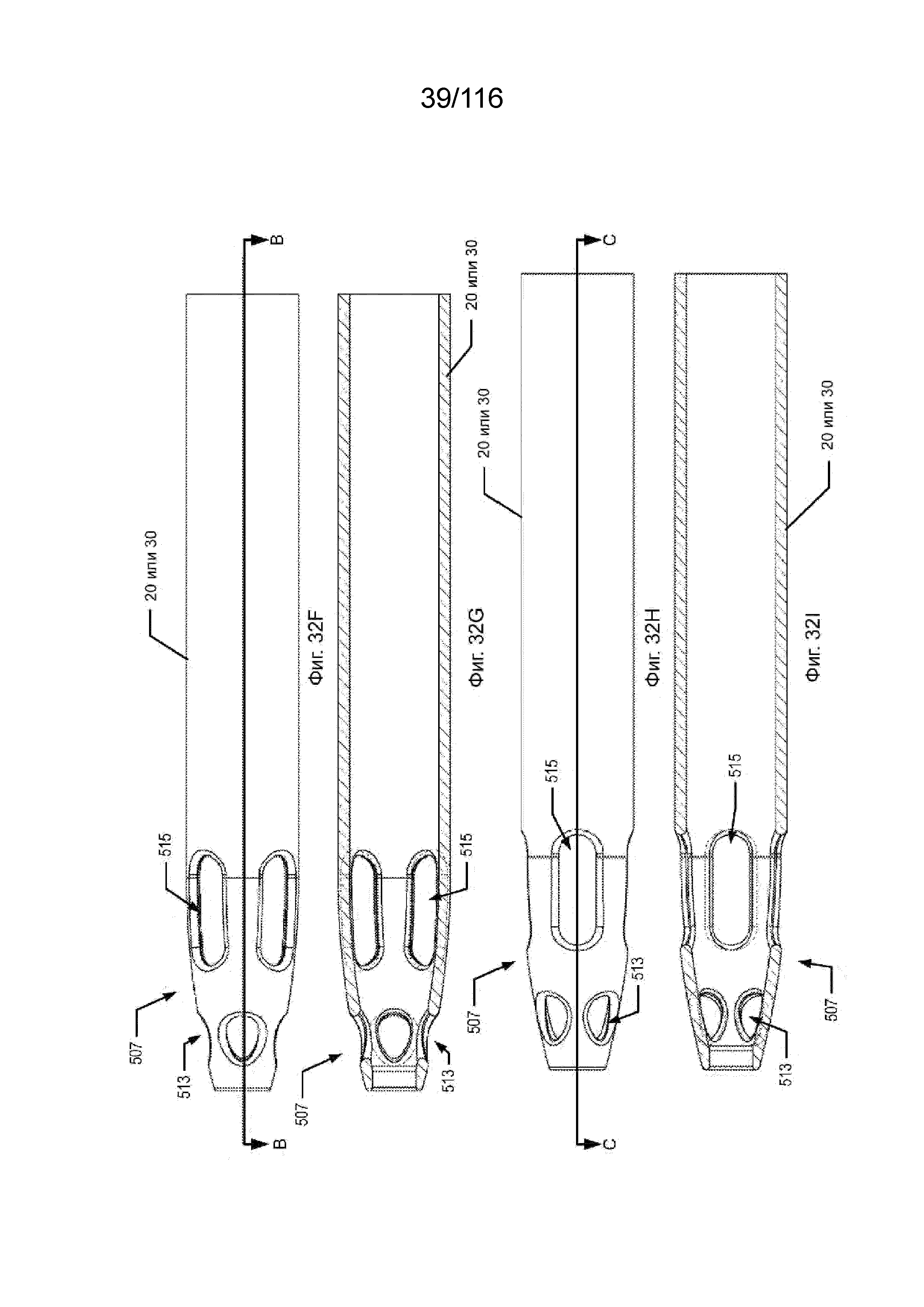
[97] На фиг. 32F приведен вид внутрисосудистого участка приточного или выводного канала согласно одному варианту реализации изобретения.
[98] На фиг. 32G приведен вид поперечного разреза внутрисосудистого участка приточного или выводного канала по фиг. 32F по линии B-B, согласно одному варианту реализации изобретения.
[99] На фиг. 32H приведен вид сверху внутрисосудистого участка приточного или выводного канала согласно одному варианту реализации изобретения.
[100] На фиг. 32I приведен вид поперечного разреза внутрисосудистого участка приточного или выводного канала по фиг. 32H по линии C-C, согласно одному варианту реализации изобретения.
[101] На фиг. 32J приведена схема последовательности этапов для способа изготовления наконечника канюли согласно одному варианту реализации изобретения.
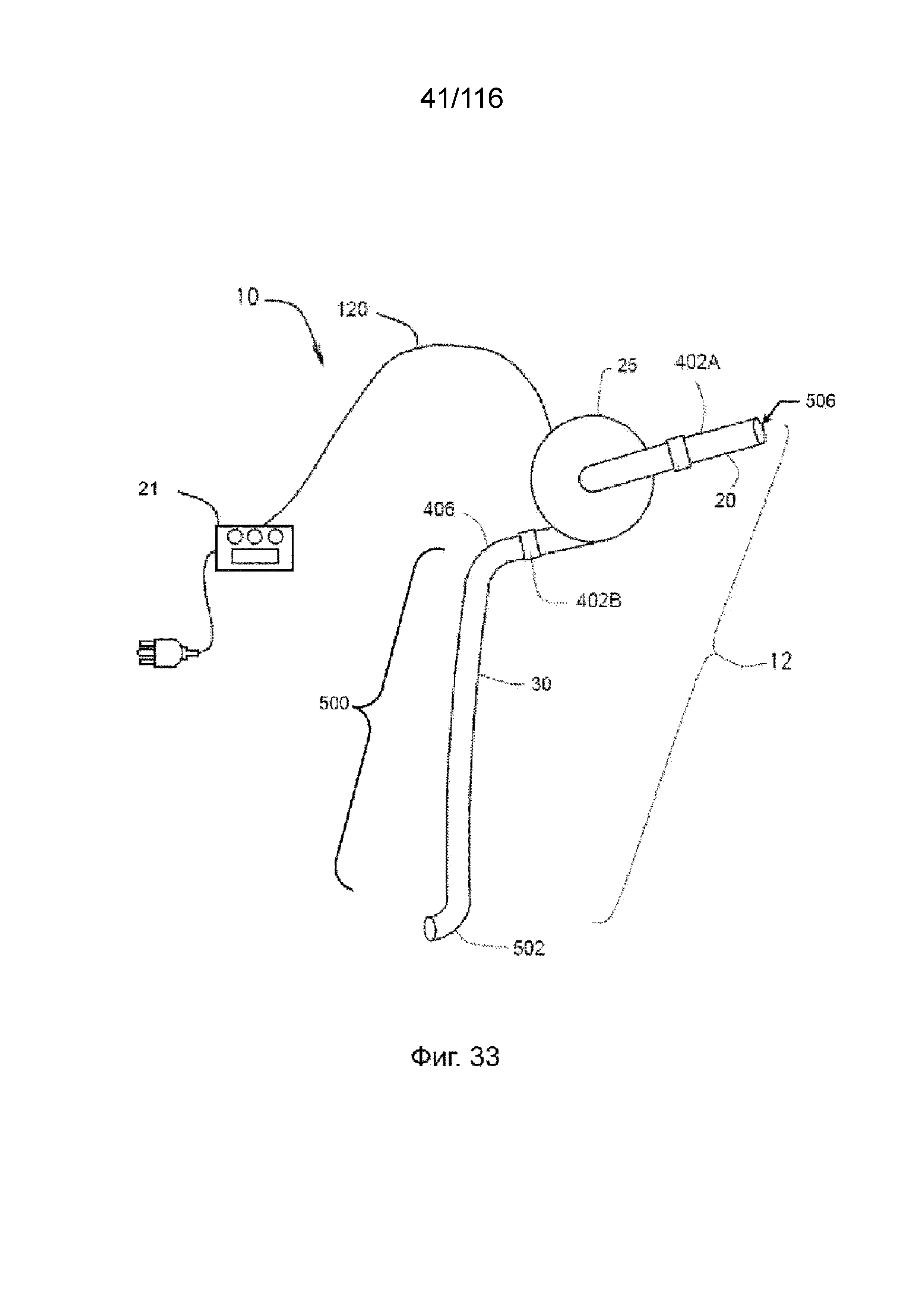
[102] На фиг. 33 приведен схематический вид насосной системы согласно одному варианту реализации изобретения.
[103] На фиг. 34 приведен схематический вид насосной системы согласно другому варианту реализации изобретения.
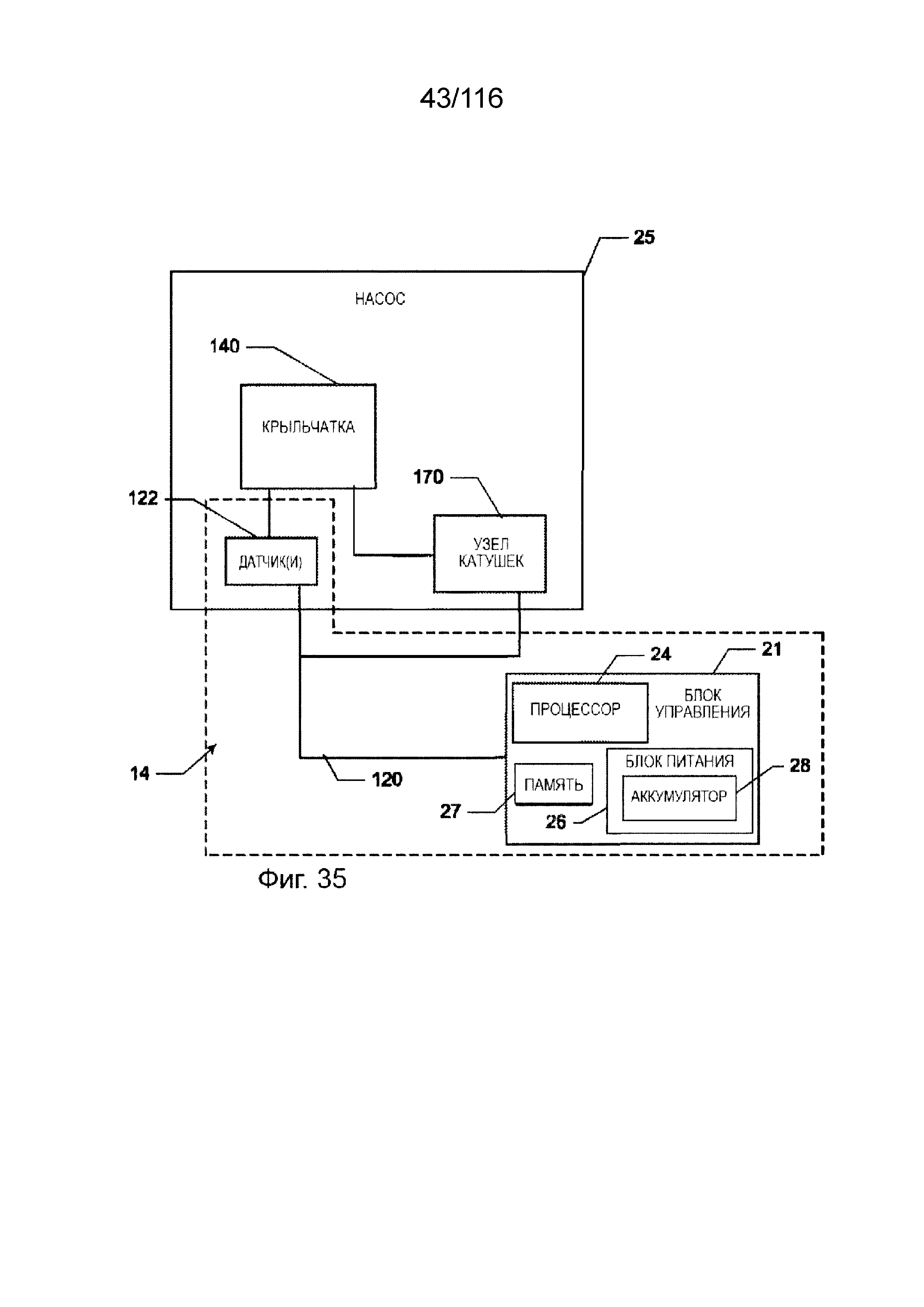
[104] На фиг. 35 приведен схематический вид системы управления согласно одному варианту реализации изобретения.
[105] На фиг. 36A-36D приведены схемы последовательности способов для системы управления, согласно некоторым вариантам реализации изобретения.
[106] На фиг. 36E приведен график давлений анастомоза и скоростей кровотока для модели in vitro насосной системы согласно одному варианту реализации изобретения.
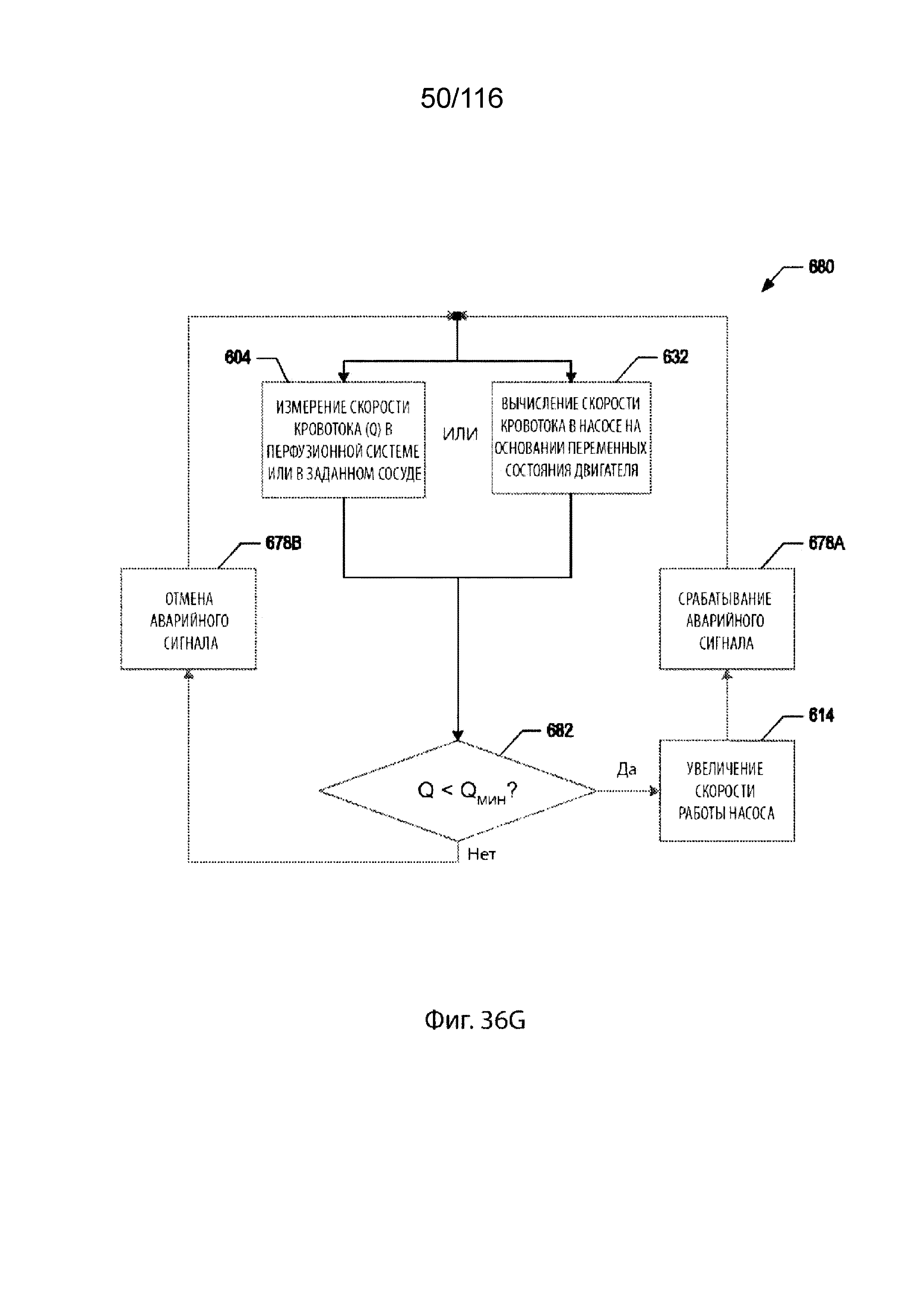
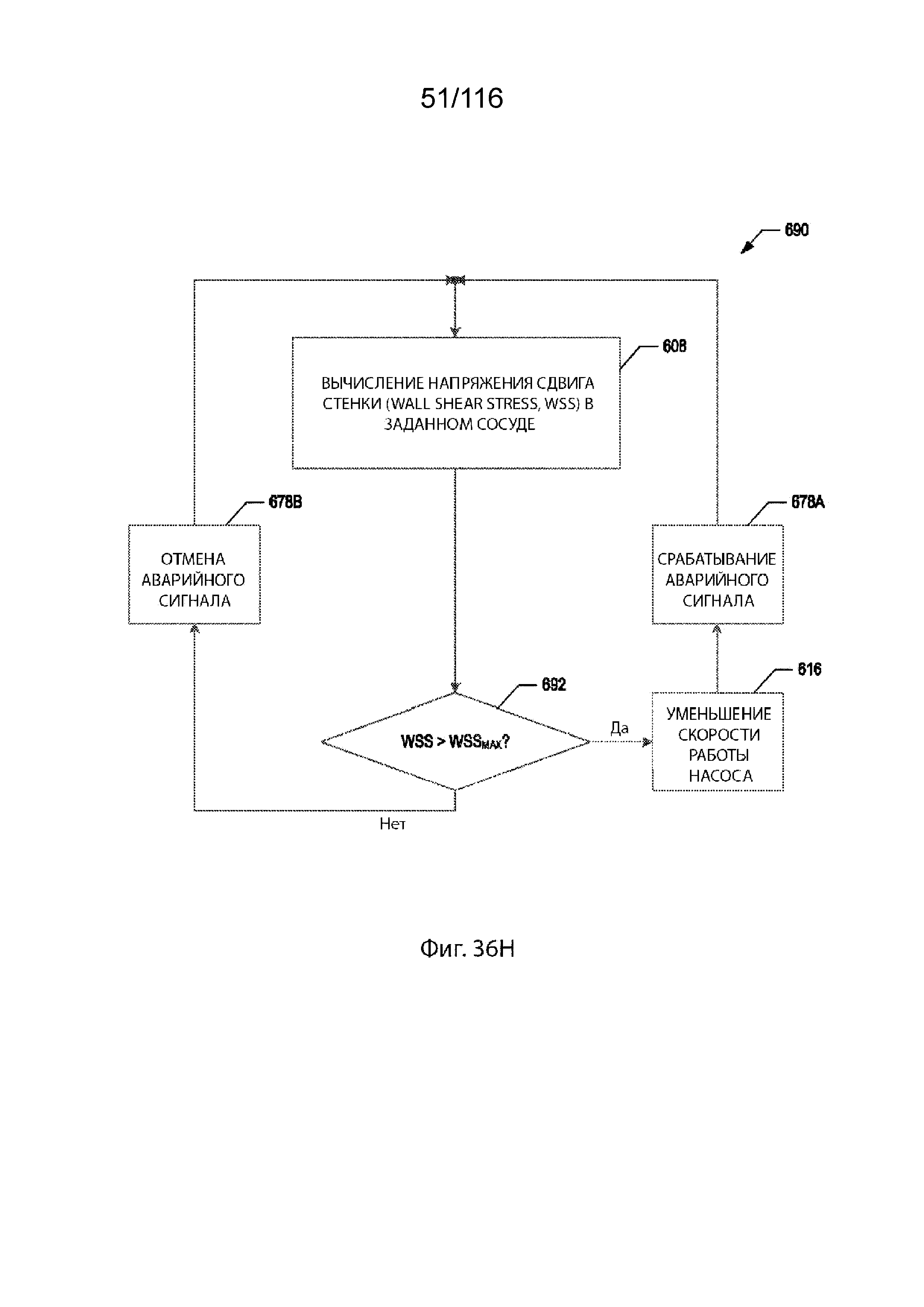
[107] На фиг. 36F-36H приведены схемы последовательности способов для системы управления, согласно некоторым вариантам реализации изобретения.
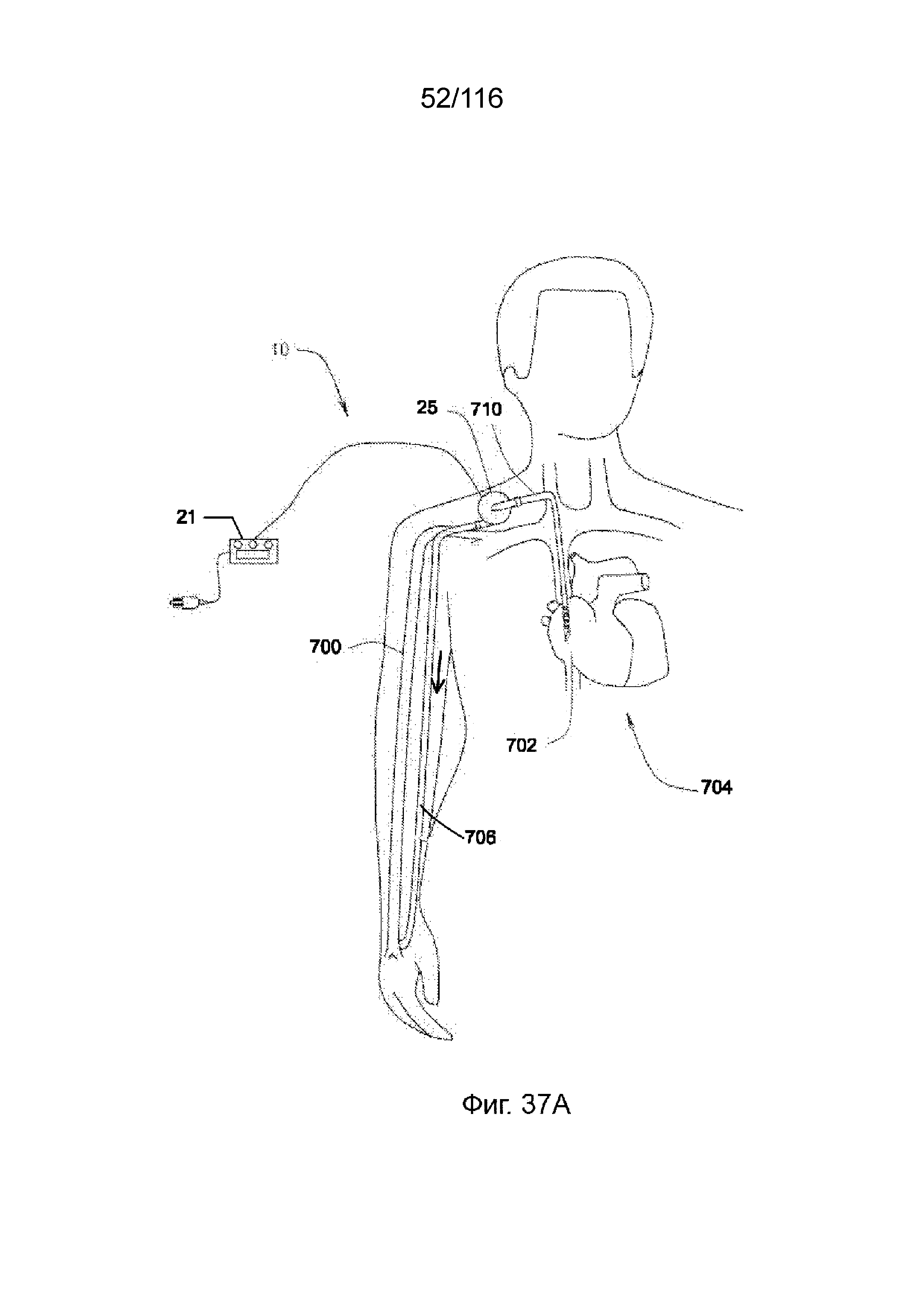
[108] На фиг. 37A приведен вид насосной системы, используемой в системе кровообращения пациента, согласно одному варианту реализации изобретения.
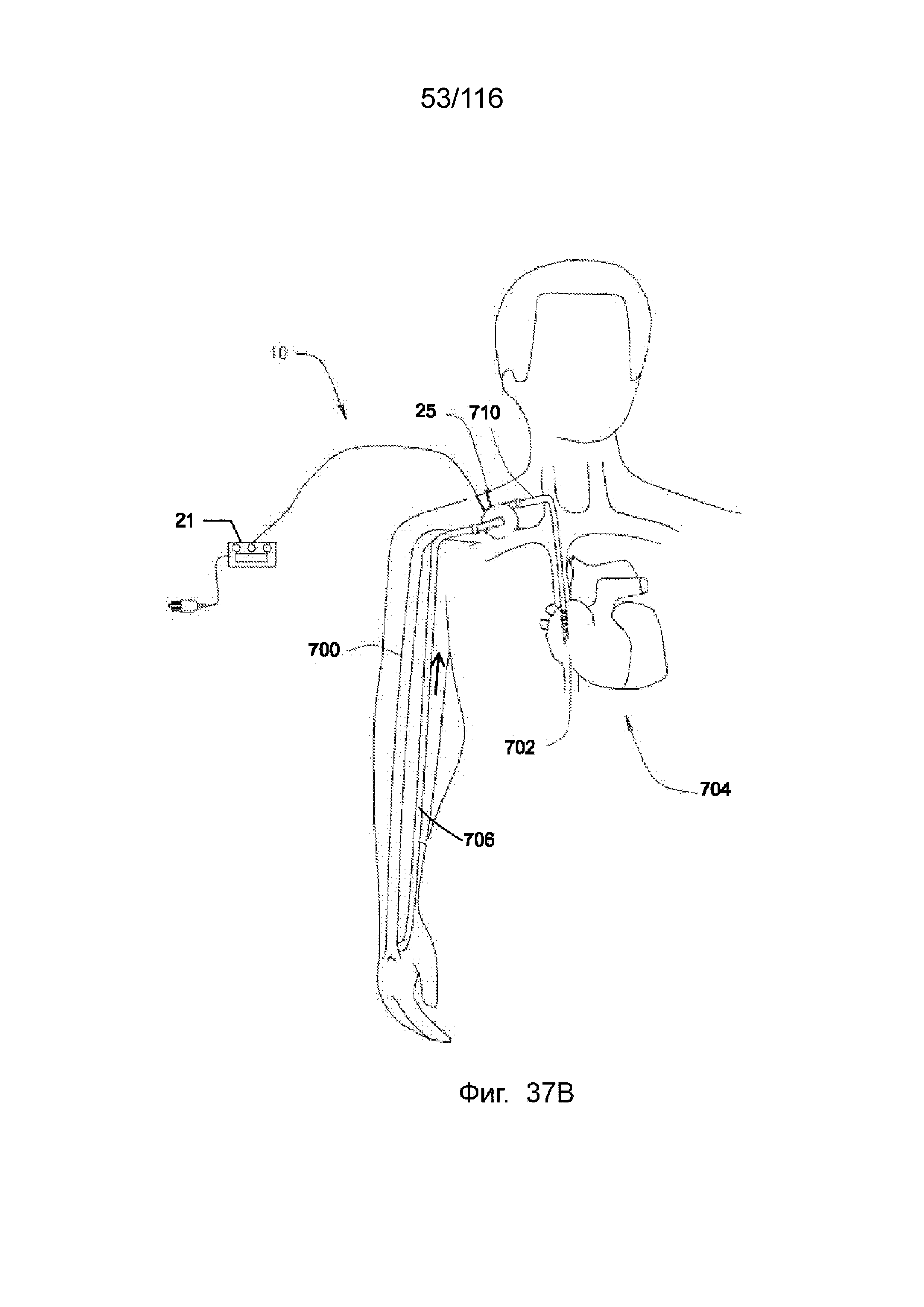
[109] На фиг. 37B приведен вид насосной системы, используемой в системе кровообращения пациента, согласно второму варианту реализации изобретения.
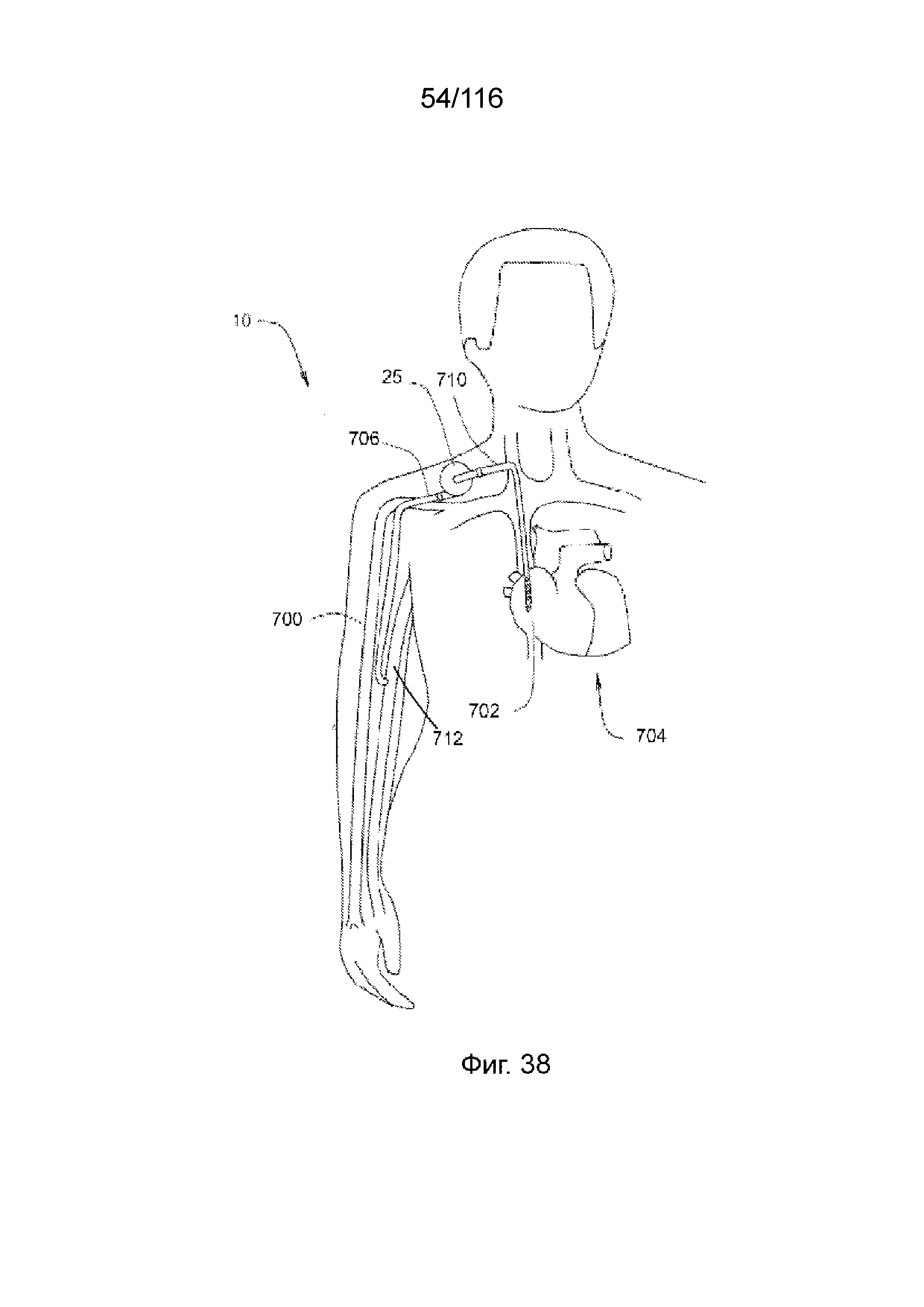
[110] На фиг. 38 приведен схематический вид насосной системы, используемой в системе кровообращения пациента, согласно третьему варианту реализации изобретения.
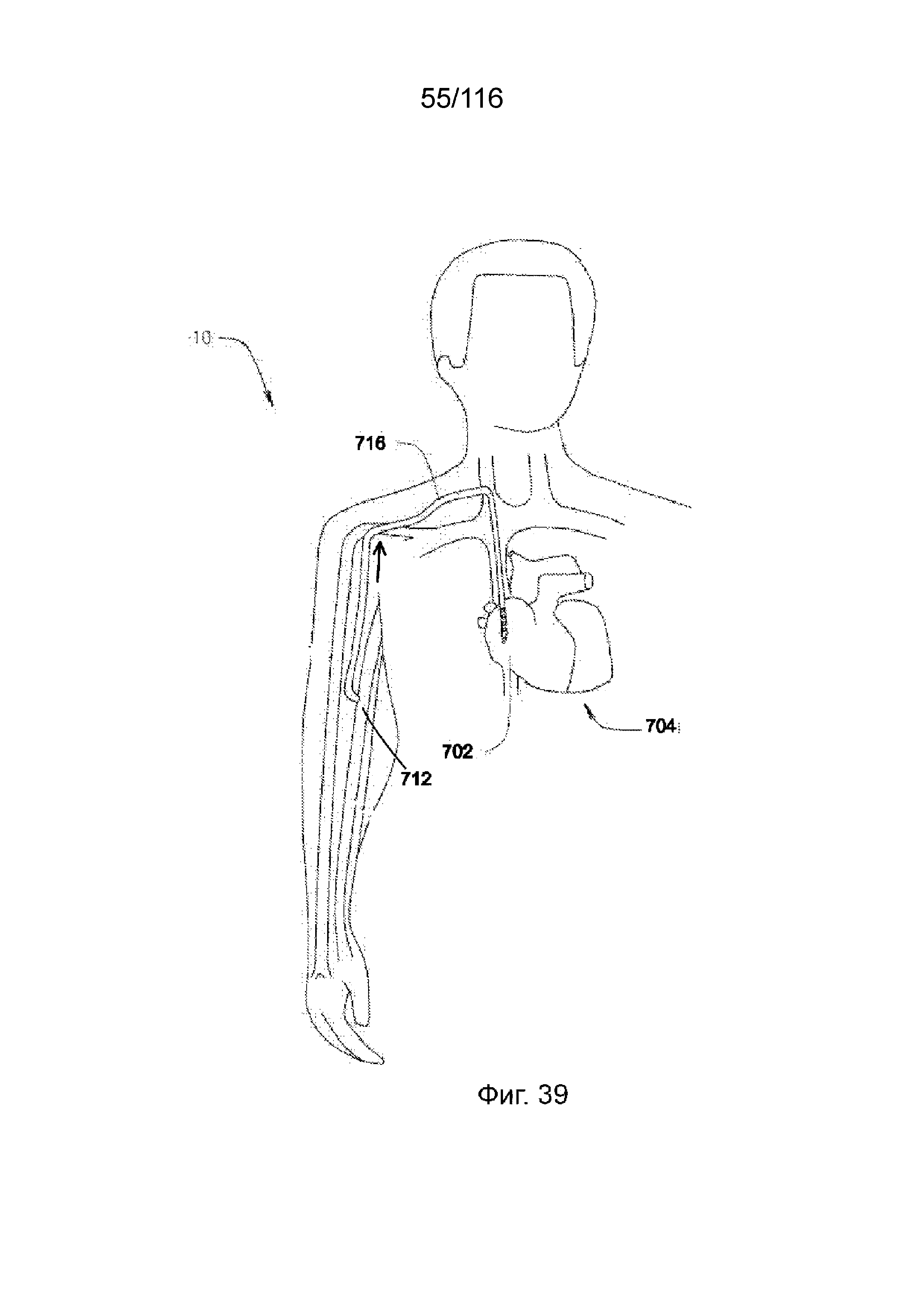
[111] На фиг. 39 приведен схематический вид системы без насоса, используемой в системе кровообращения пациента, согласно четвертому варианту реализации изобретения.
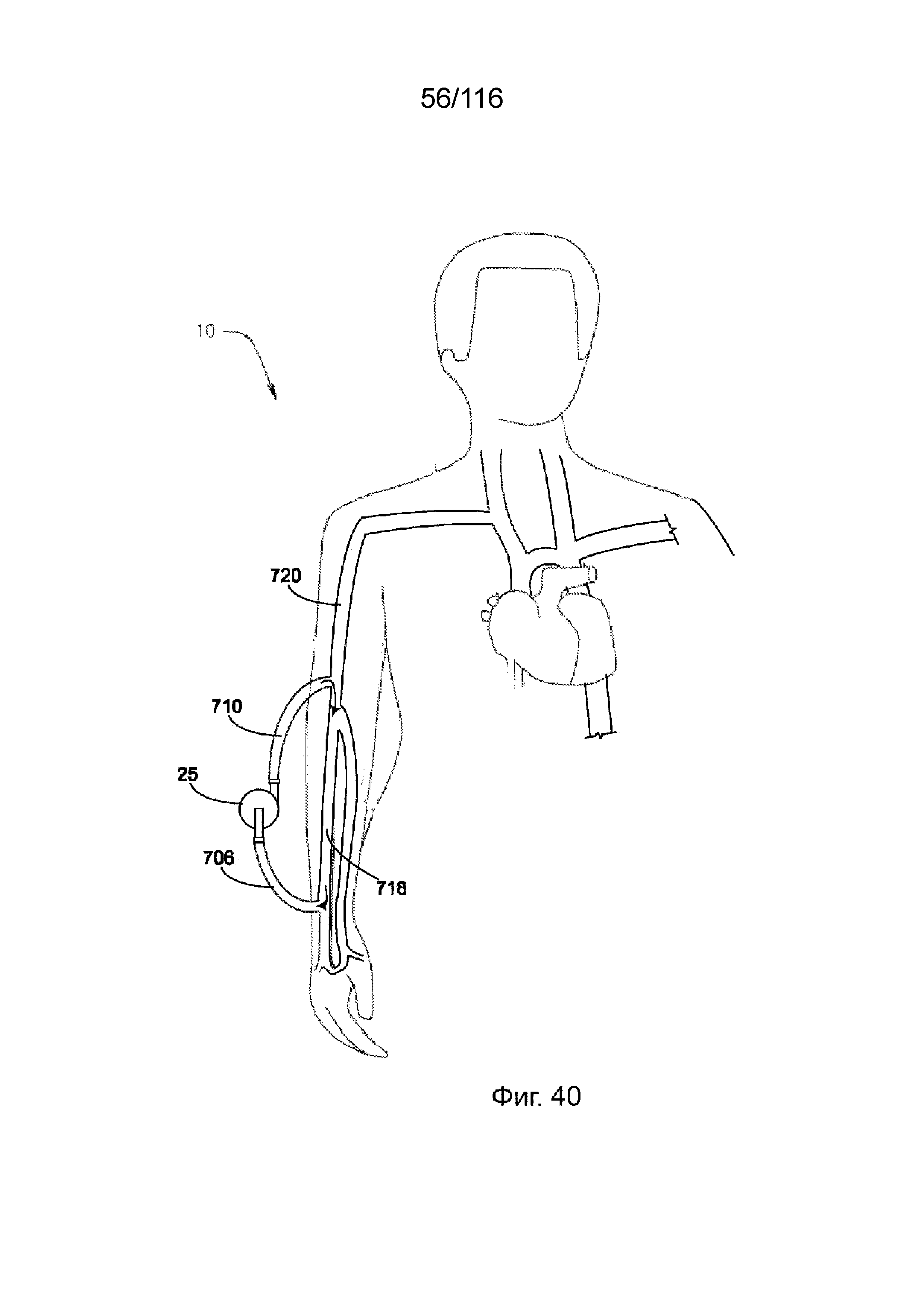
[112] На фиг. 40 приведен схематический вид насосной системы, используемой в системе кровообращения пациента, согласно пятому варианту реализации изобретения.
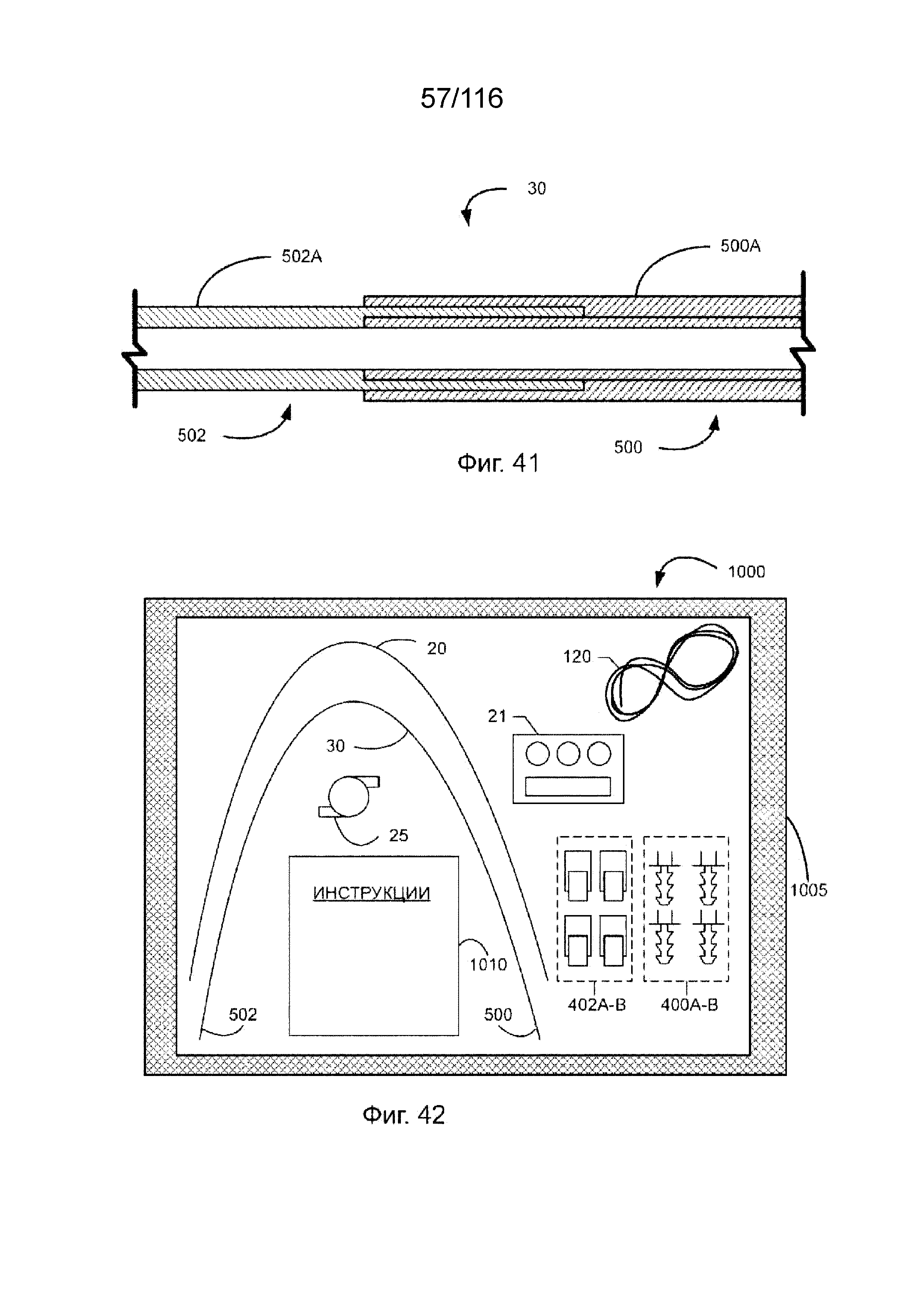
[113] На фиг. 41 приведен продольный разрез соединения между ближним сегментом и дальним сегментом.
[114] На фиг. 42 приведен вид сверху медицинского комплекта.
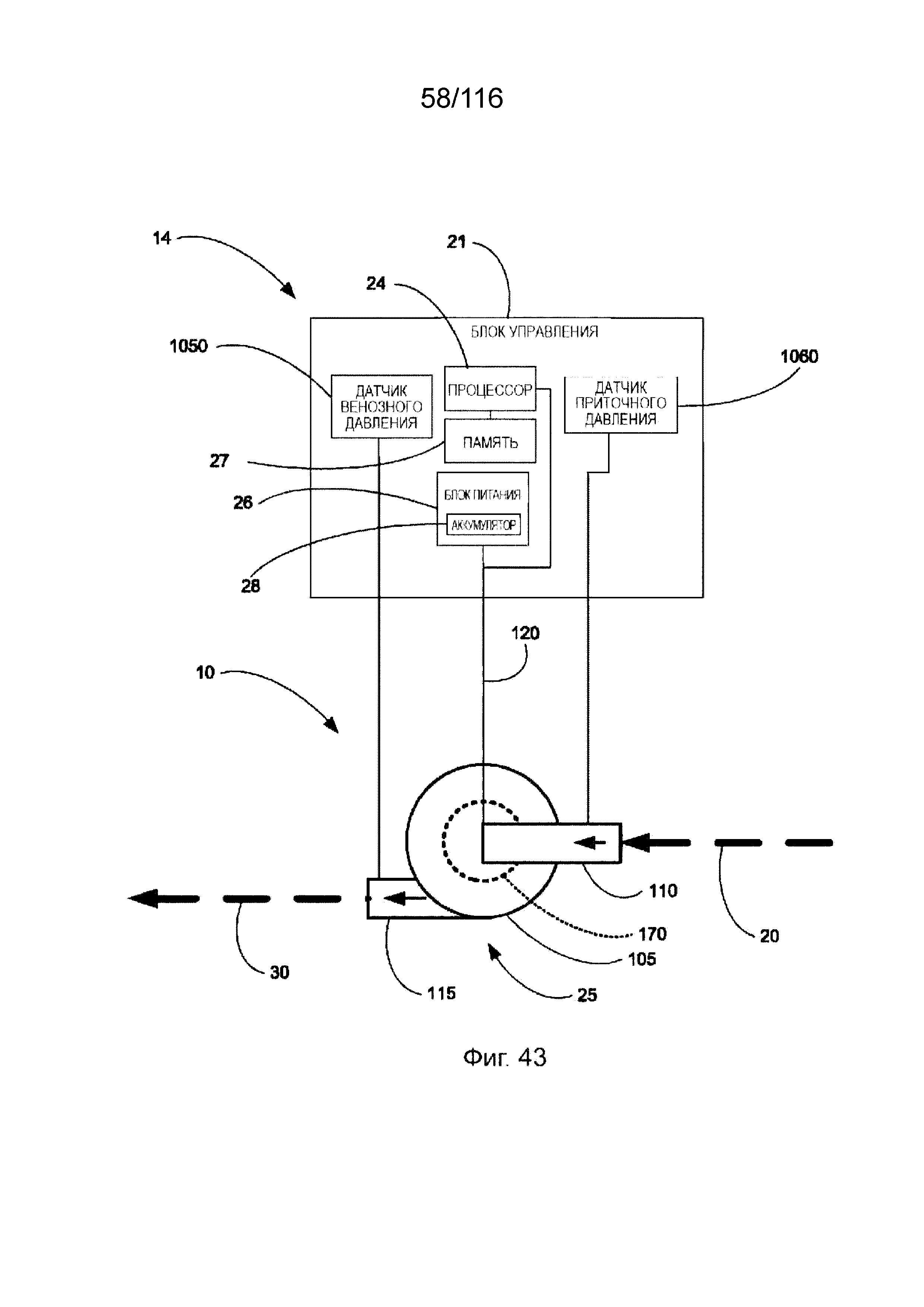
[115] На фиг. 43 приведена принципиальная схема насосной системы, регулируемой в соответствии с венозным давлением.
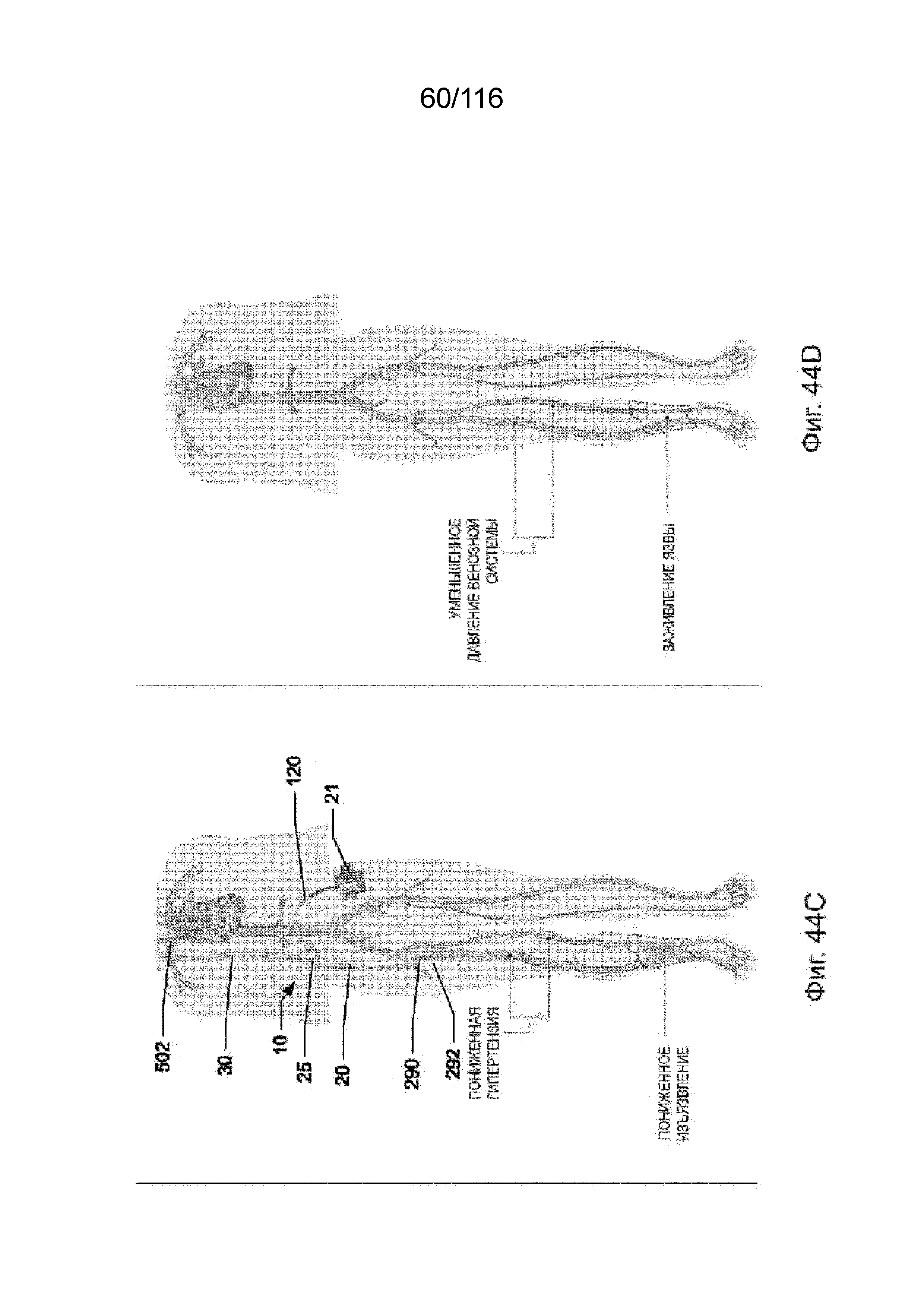
[116] На фиг. 44A-D приведены схематические виды насосной системы, используемой в венозной системе нижней конечности пациента для лечения венозной гипертензии и венозной язвы.
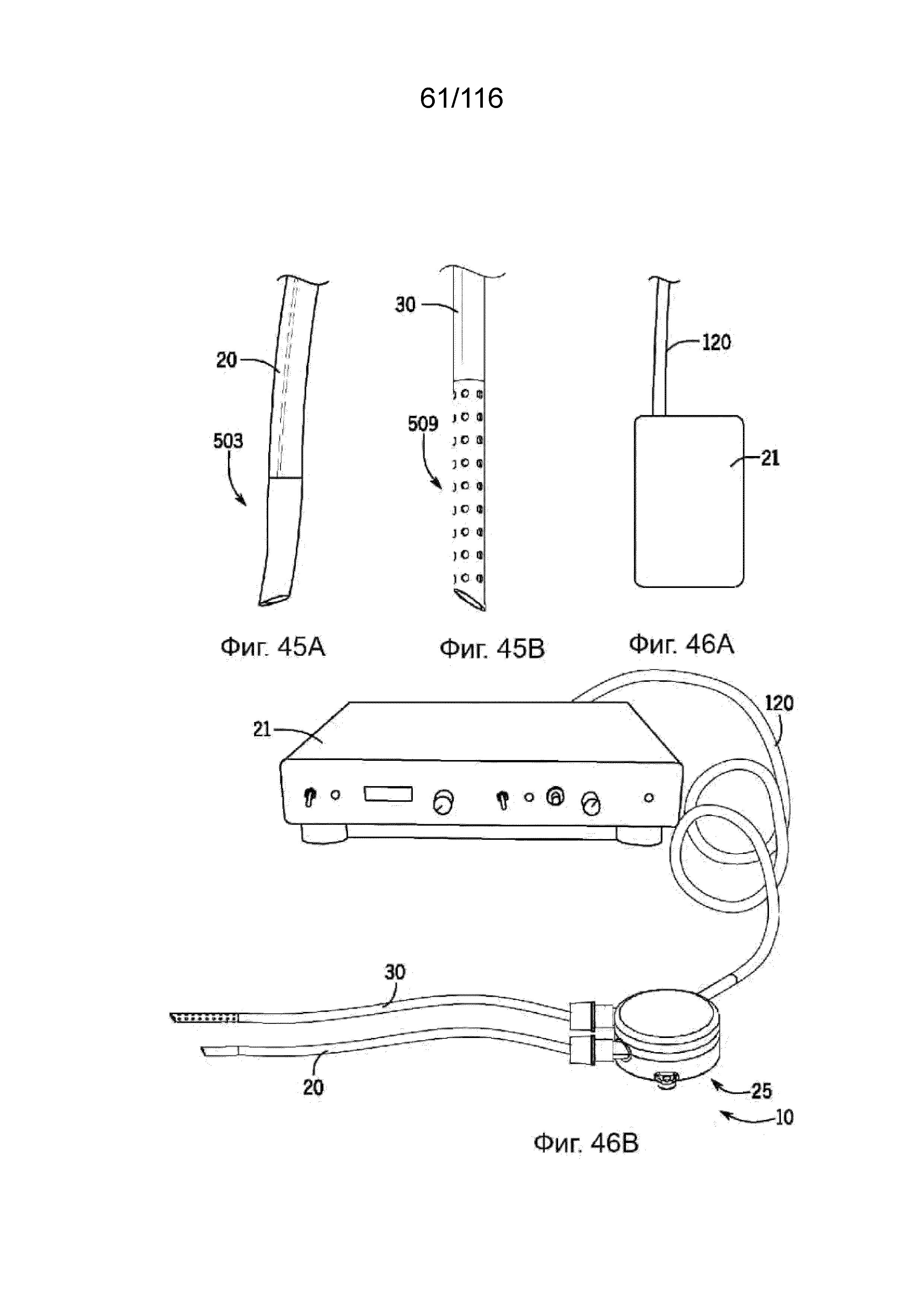
[117] На фиг. 45A приведена иллюстрация участка канала, выполненного с возможностью сообщения по текучей среде с сосудистой системой посредством хирургического анастомоза.
[118] На фиг. 45B приведена иллюстрация участка канала, выполненного с возможностью введения в просвет участка сосудистой системы.
[119] На фиг. 46A-B приведены иллюстрации носимого устройства управления и стационарного или устанавливаемого на столе устройства управления, соответственно.
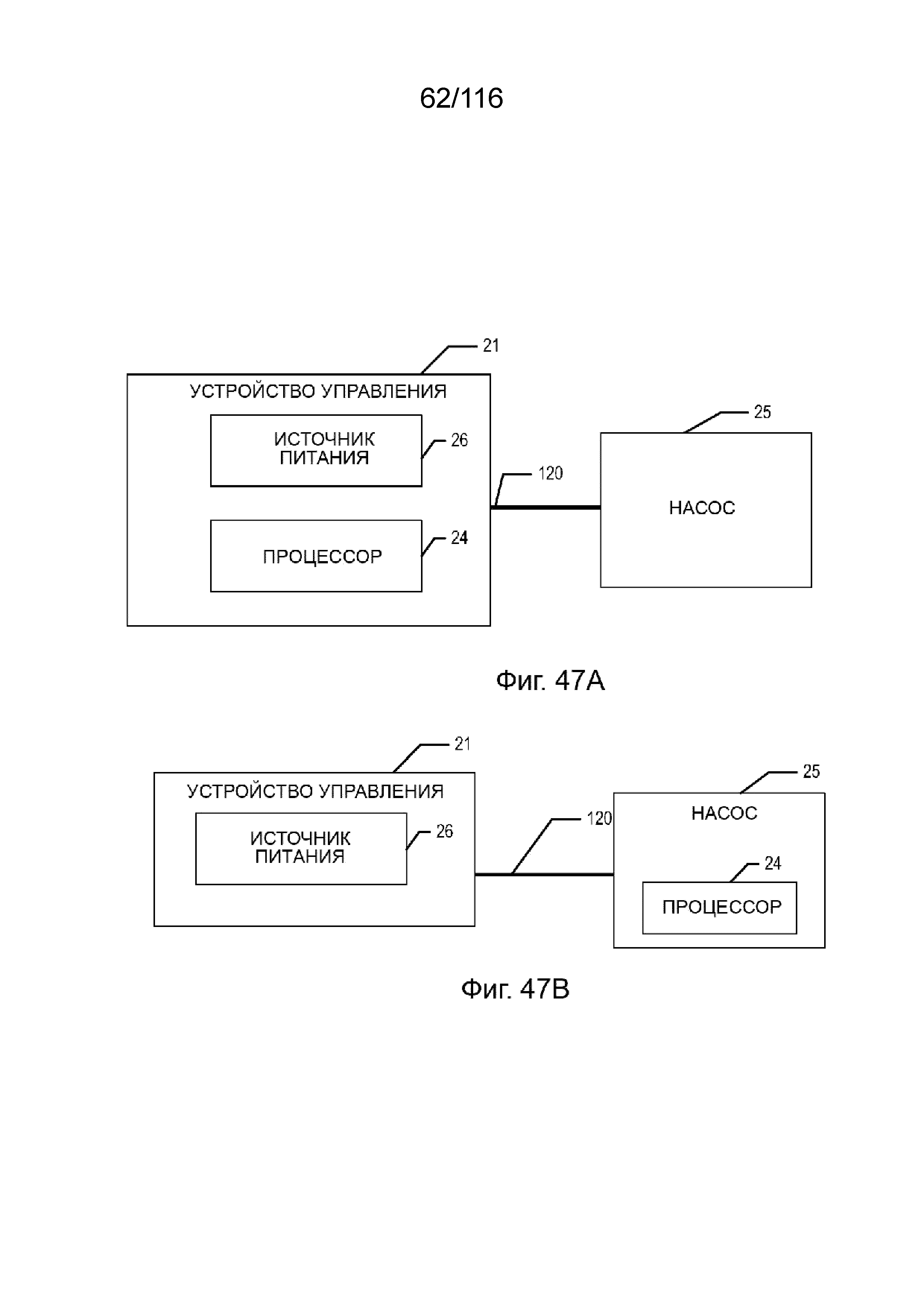
[120] На фиг. 47A-B приведены принципиальные схемы некоторых вариантов реализации устройства управления и перфузионного насоса, на которых процессор с приводом от двигателя может быть расположен в устройстве управления или в корпусе перфузионного насоса.
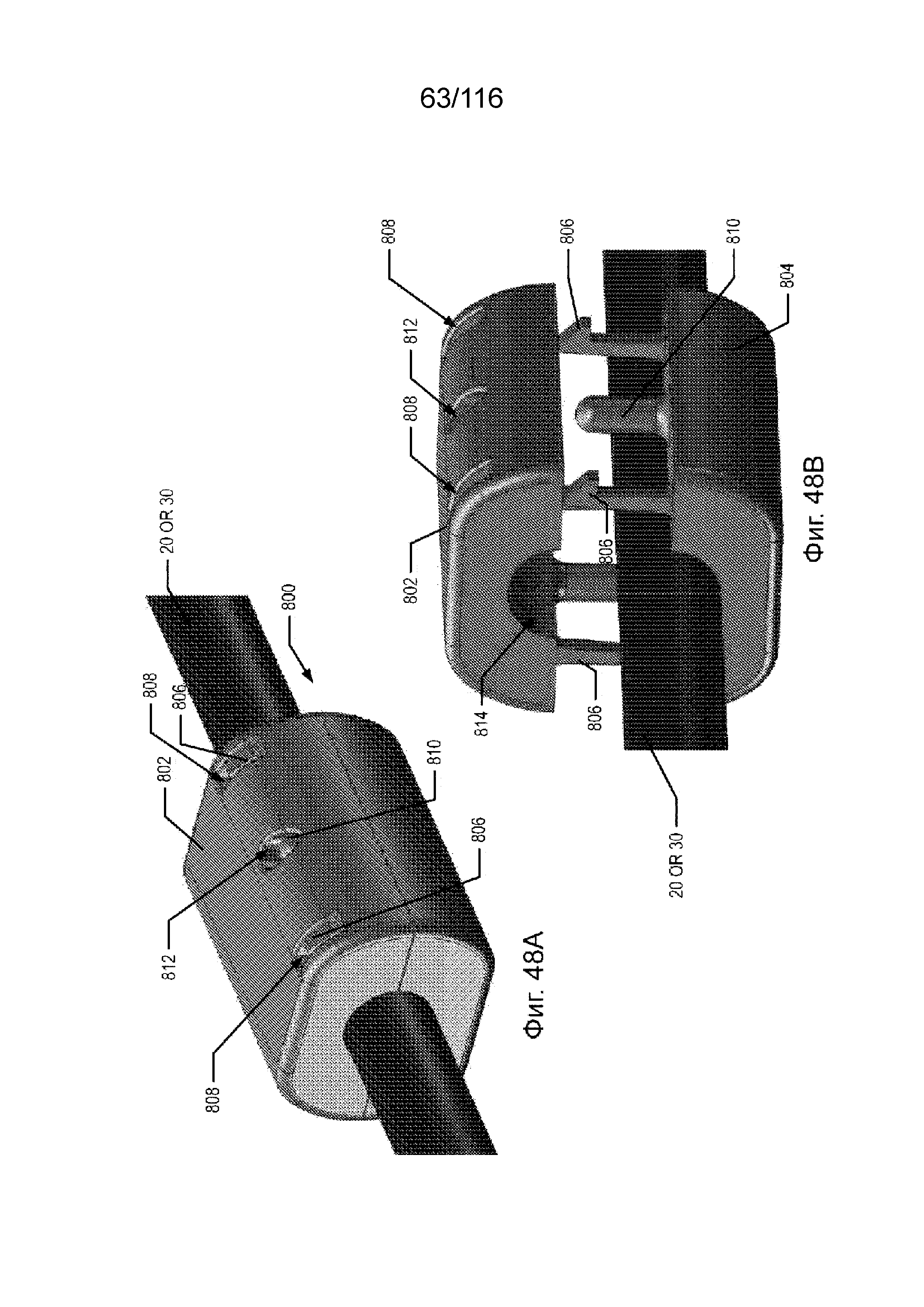
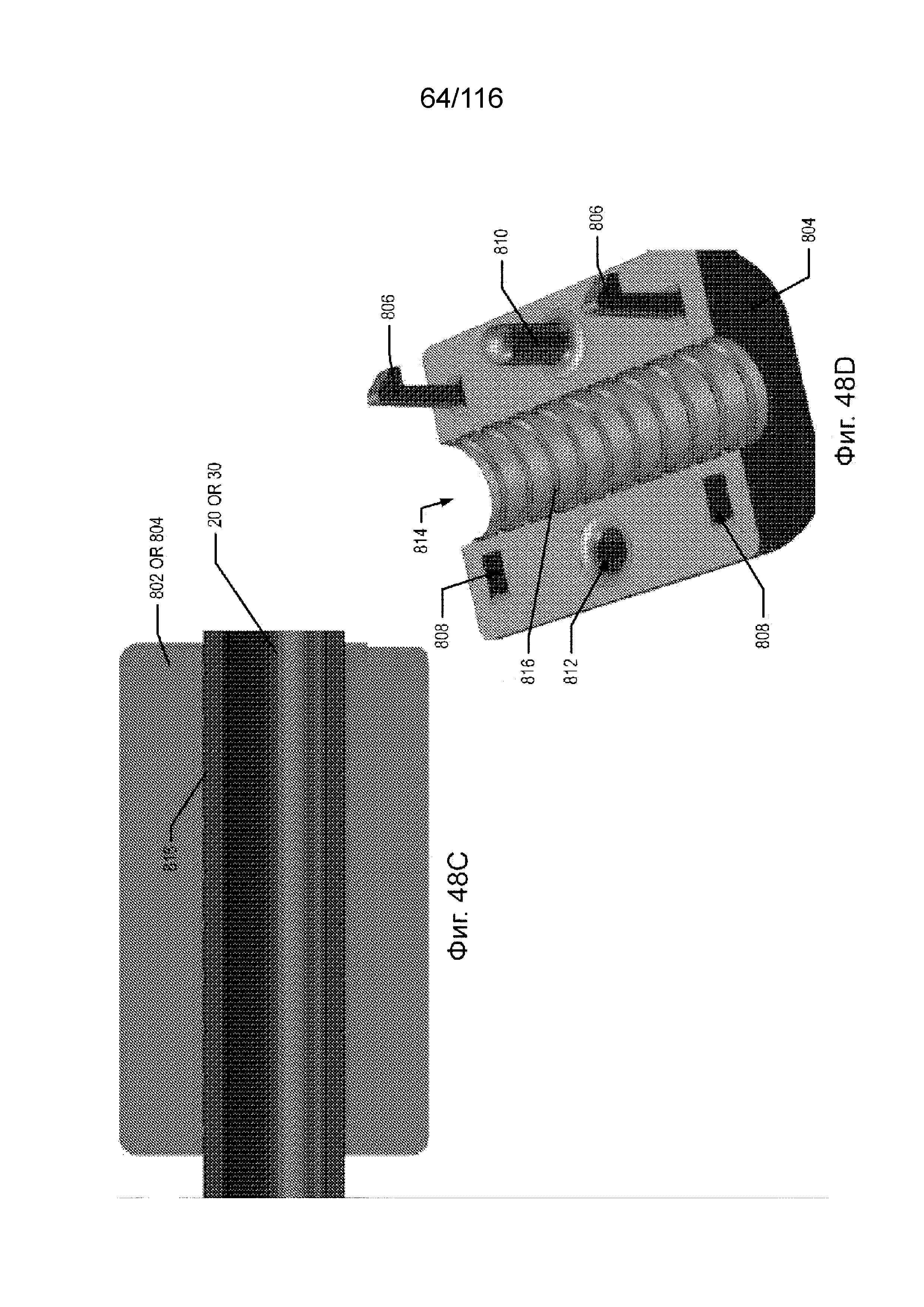
[121] На фиг. 48A-D представлены виды в перспективе участка устройства манжеты, который может быть прикреплен к наружной поверхности сегмента канала.
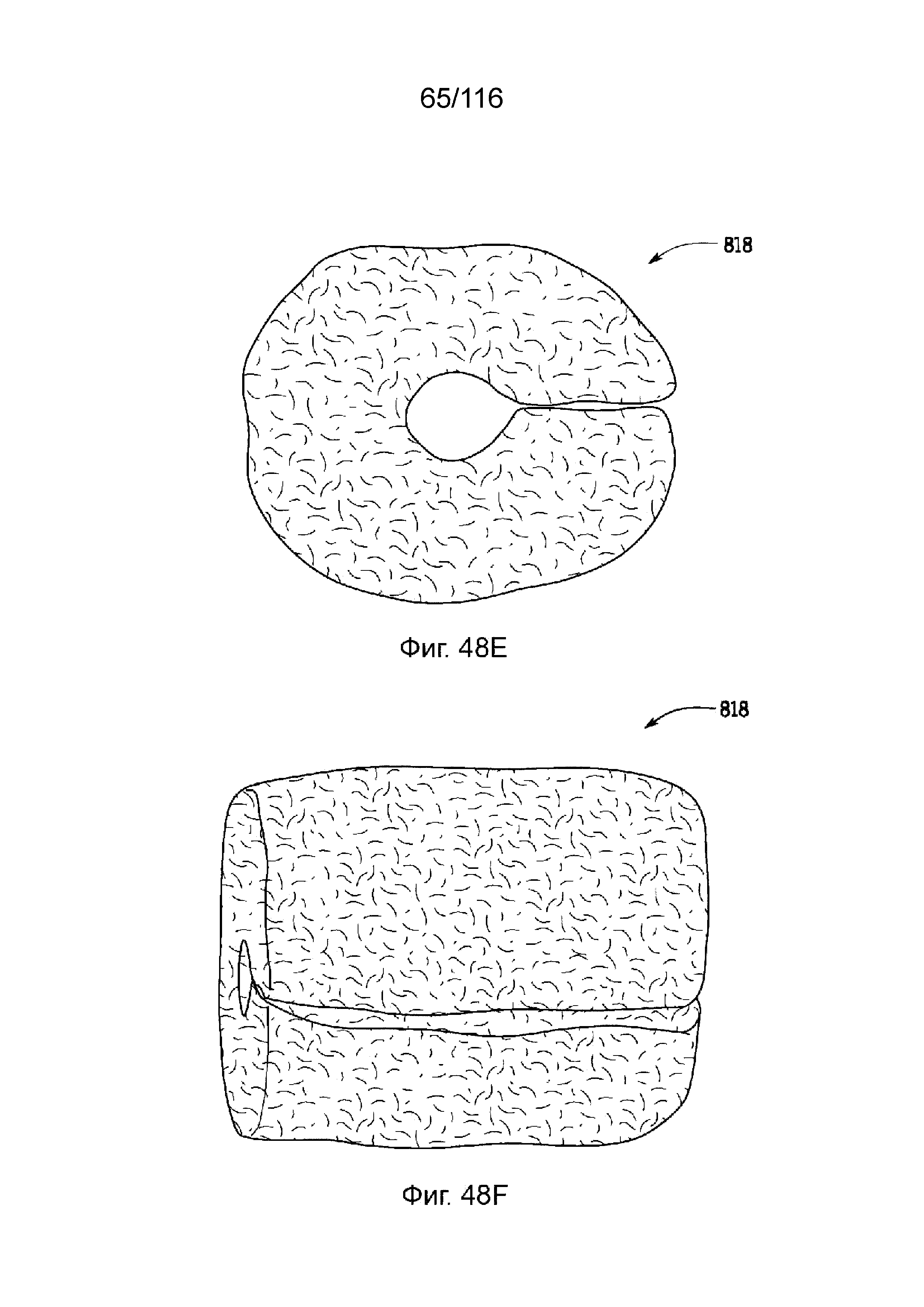
[122] На фиг. 48E-F представлены эскизы устройства манжеты, которое может быть прикреплено к наружной поверхности сегмента канала.
[123] На фиг. 49A-B представлены ангиограмма и результаты гистологического исследования из изучения применимости in vivo системы AFE (Arteriovenous Fistula Eligibility, приемлемости артериовенозной фистулы).
[124] На фиг. 50 приведена фотография бокового канала, собранного с приточным и выводным каналами согласно одному варианту реализации изобретения.
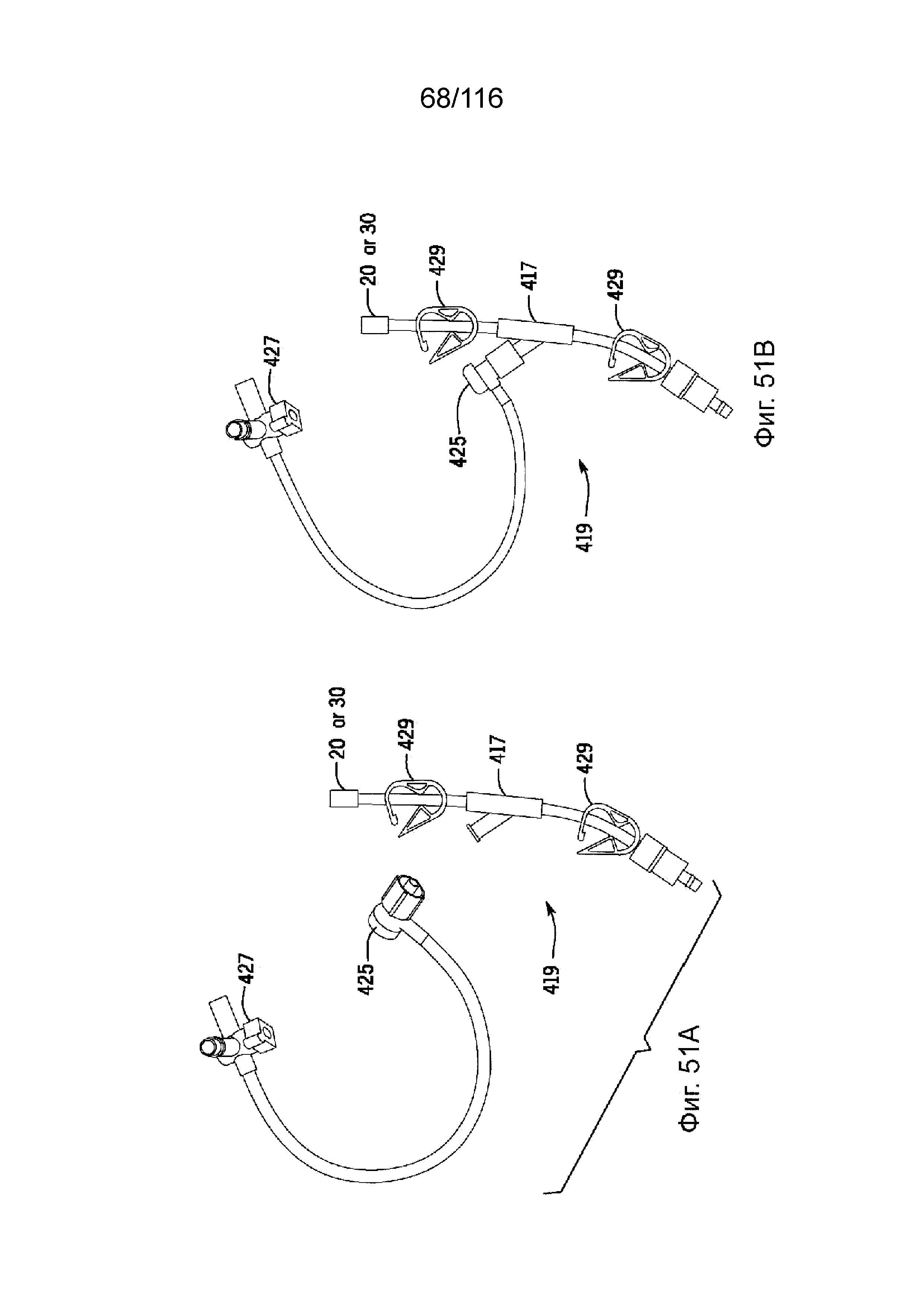
[125] На фиг. 51A-B приведены иллюстрации не смонтированного и смонтированного «готового для доступа» узла бокового канала, соответственно, согласно одному варианту реализации изобретения.
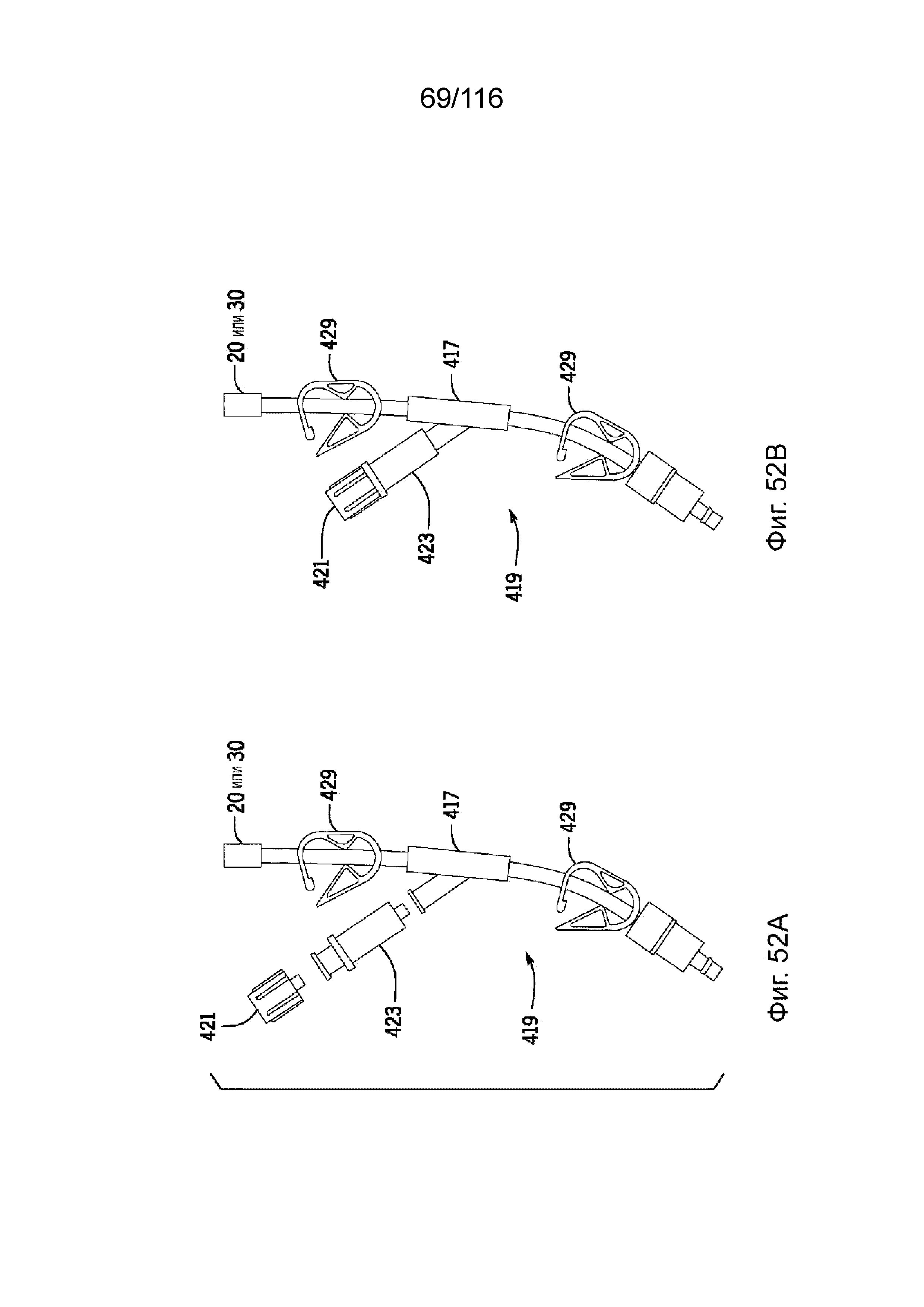
[126] На фиг. 52A-B приведены иллюстрации не смонтированного и смонтированного «готового для доступа» узла бокового канала, соответственно, согласно другому варианту реализации изобретения.
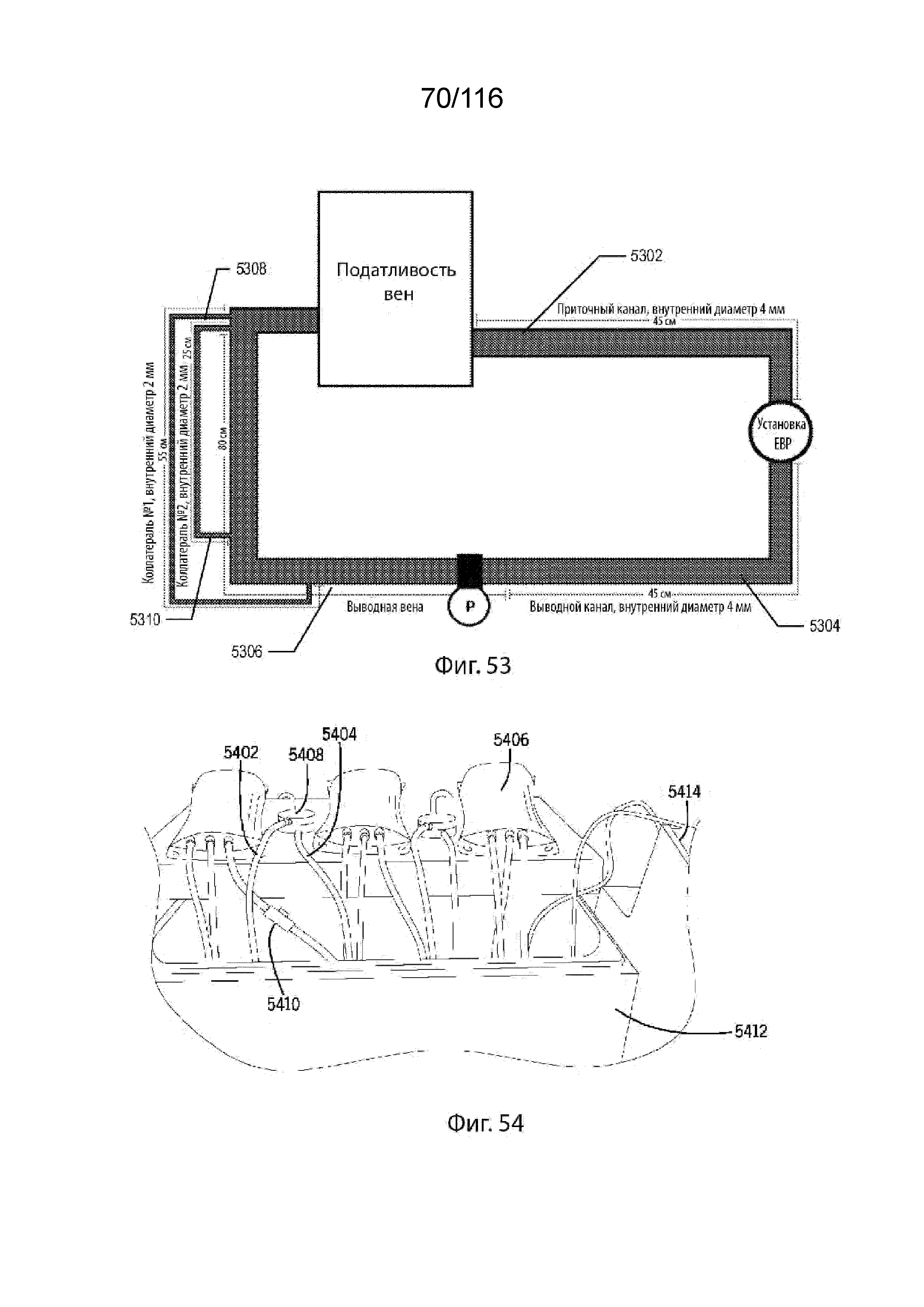
[127] На фиг. 53 приведена иллюстрация имитационного контура кровообращения, используемого во время различных исследований и экспериментов согласно одному варианту реализации изобретения.
[128] На фиг. 54 приведена иллюстрация экспериментальной системы кровообращения, используемой во время различных исследований и экспериментов согласно одному варианту реализации изобретения.
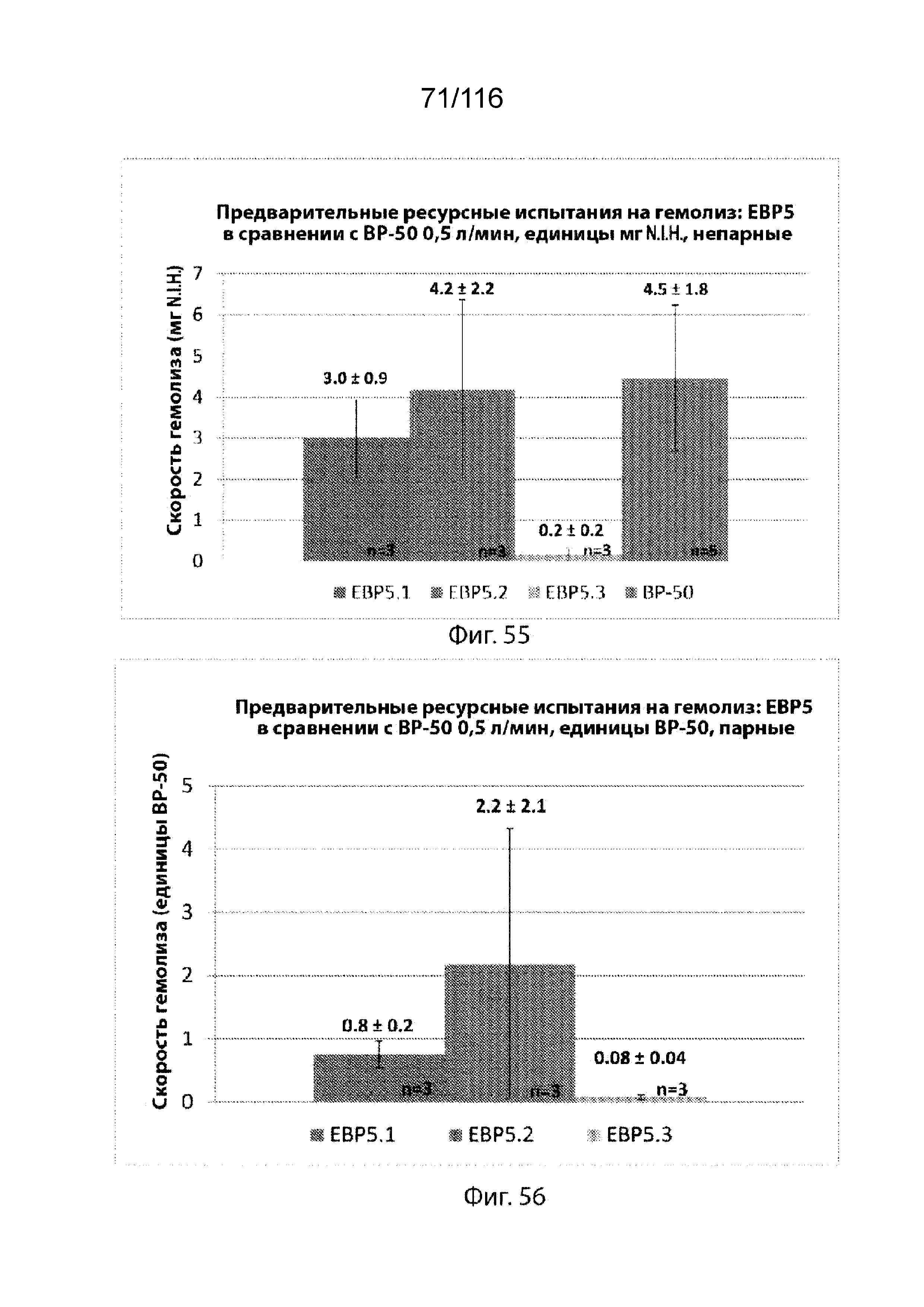
[129] На фиг. 55 приведен график, изображающий непарные результаты для испытательных насосных установок по сравнению с BP-50 в зависимости от мг N.I.H. (нормализованный по миллиграммам индекс гемолиза National Institute of Health, Национального института здравоохранения США).
[130] На фиг. 56 приведен график, изображающий парные результаты испытаний на гемолиз с использованием испытательных насосных установок в зависимости от единиц BP-50.
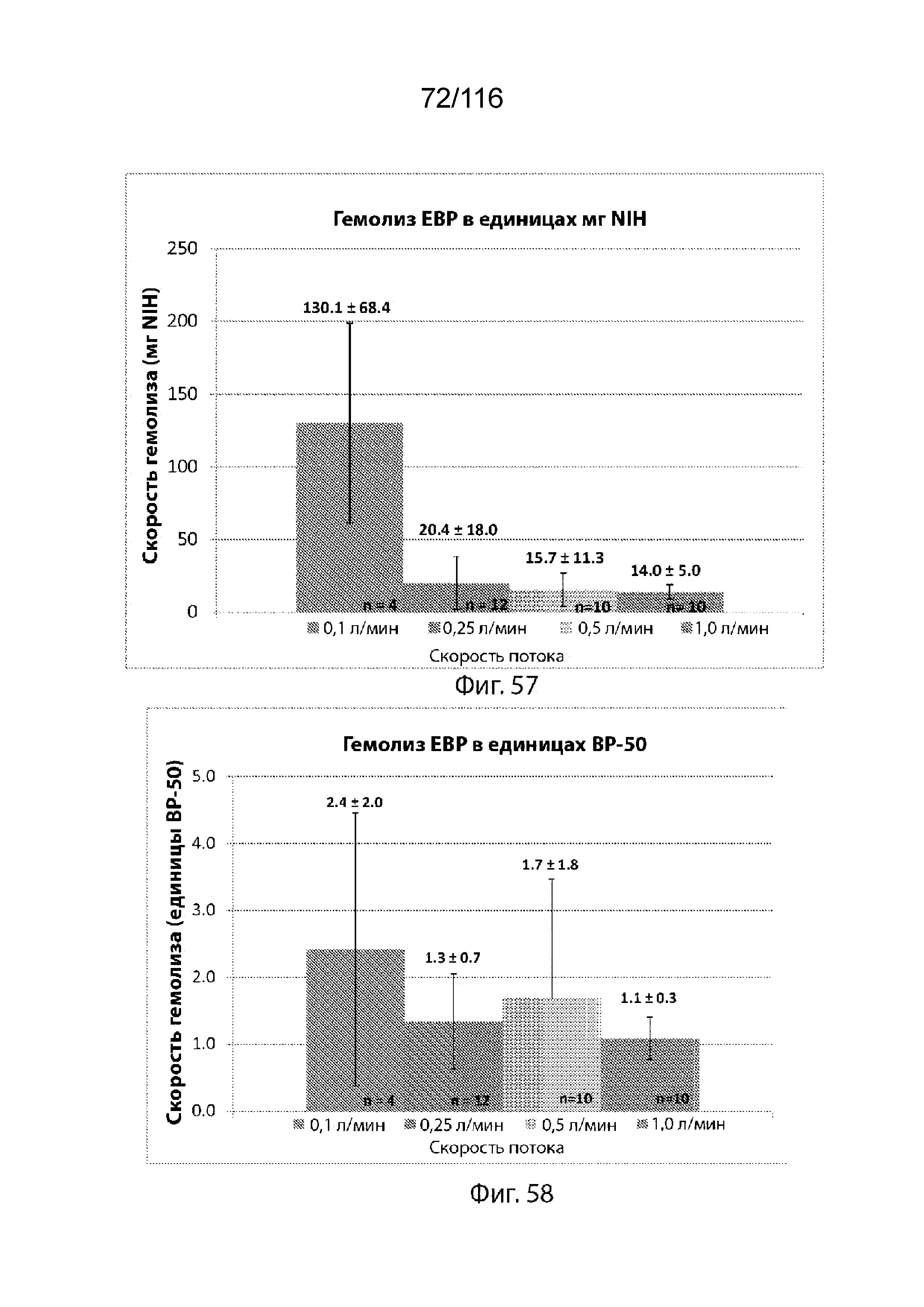
[131] На фиг. 57 приведена схема, изображающая испытания на гемолиз насоса при различных скоростях потока, выраженных в единицах мг NIH, согласно одному варианту реализации изобретения.
[132] На фиг. 58 приведена схема, изображающая испытания на гемолиз насоса при различных скоростях потока, выраженных в единицах BP-50, согласно одному варианту реализации изобретения.
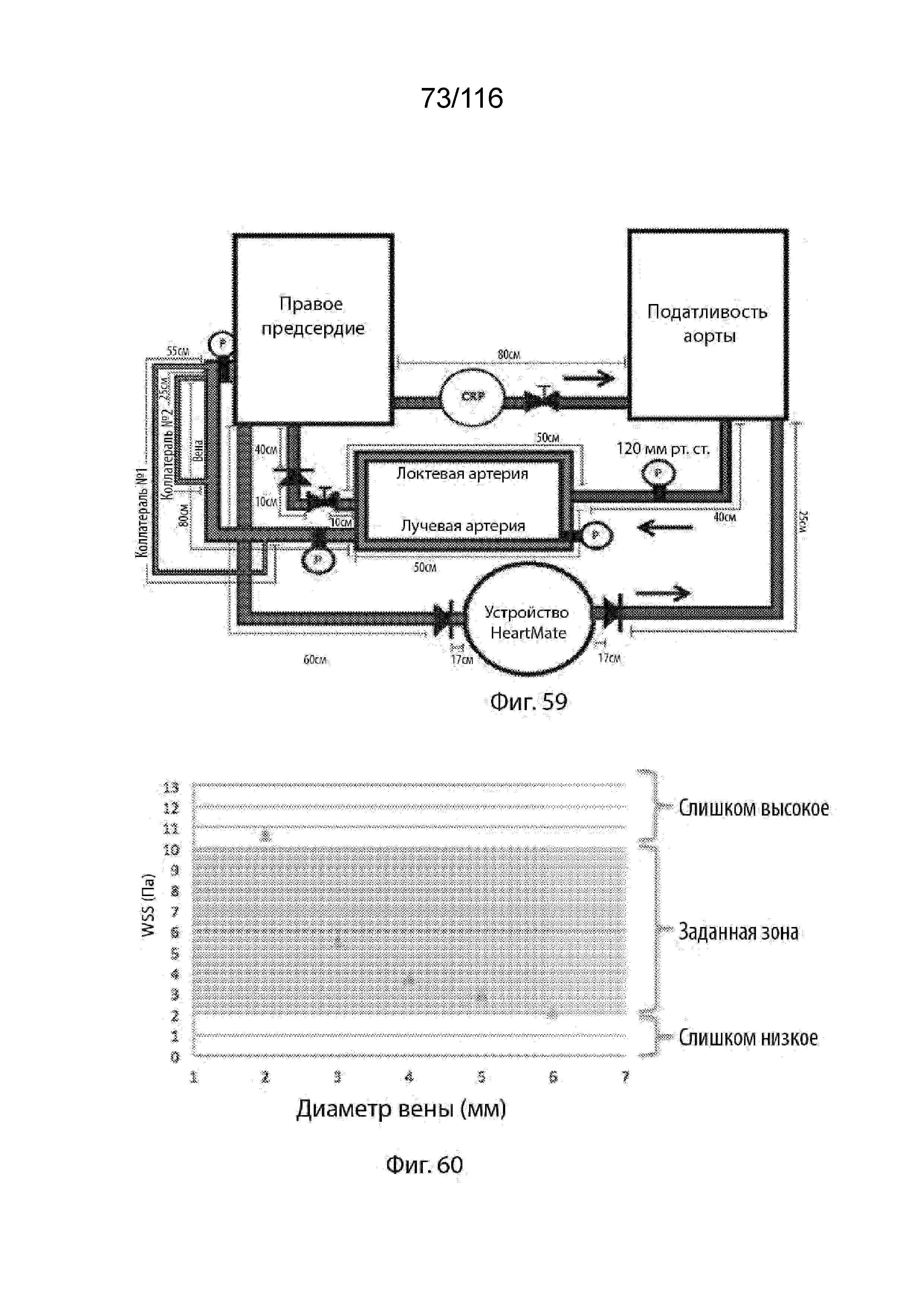
[133] На фиг. 59 приведен имитационный испытательный контур для имитационного контура AVF предплечья, согласно одному варианту реализации изобретения.
[134] На фиг. 60 приведен график, изображающий дозы WSS в зависимости от диаметра вены, согласно одному варианту реализации изобретения.
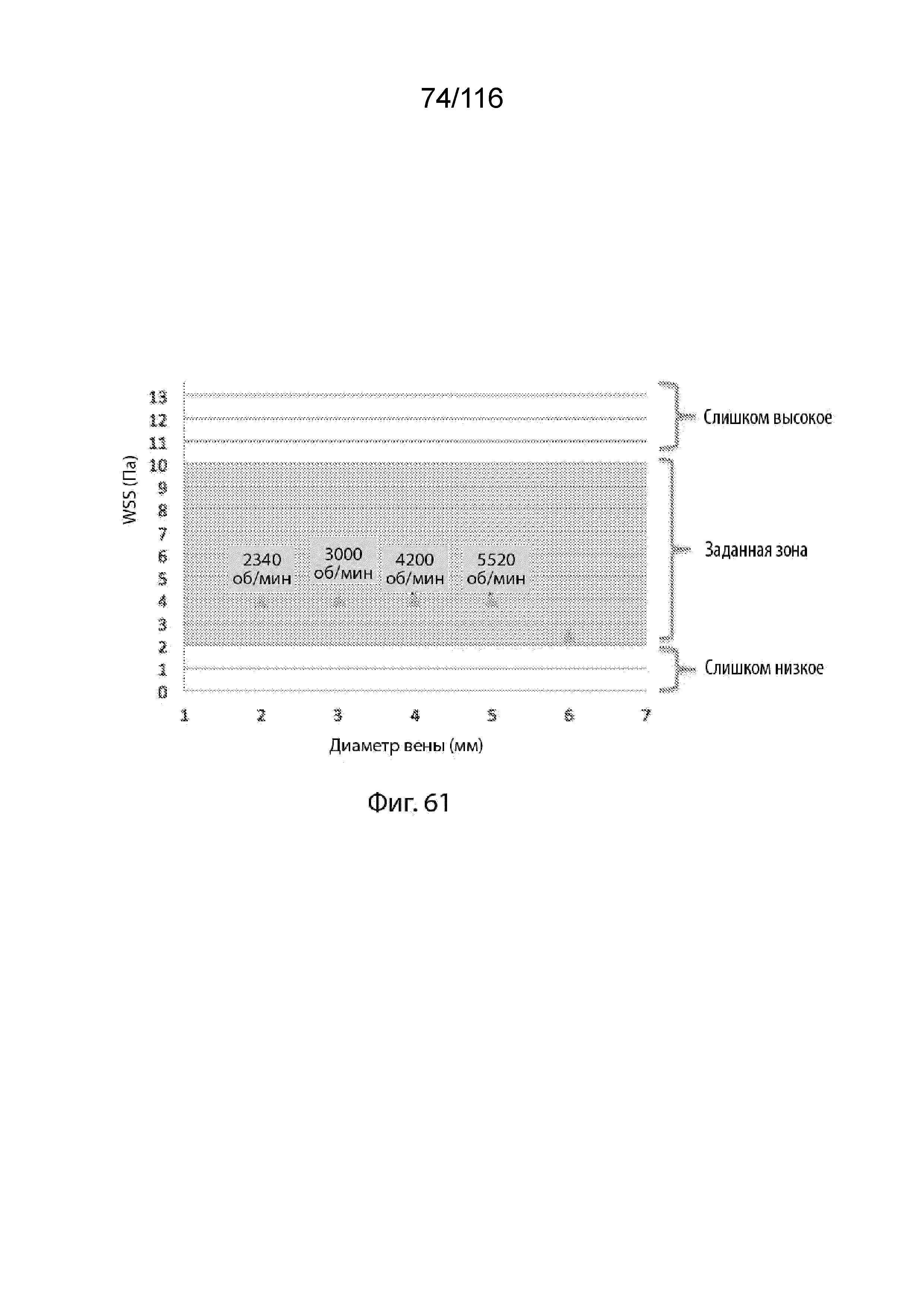
[135] На фиг. 61 приведен график, изображающий дозы WSS в зависимости от диаметра вены, согласно другому варианту реализации изобретения.
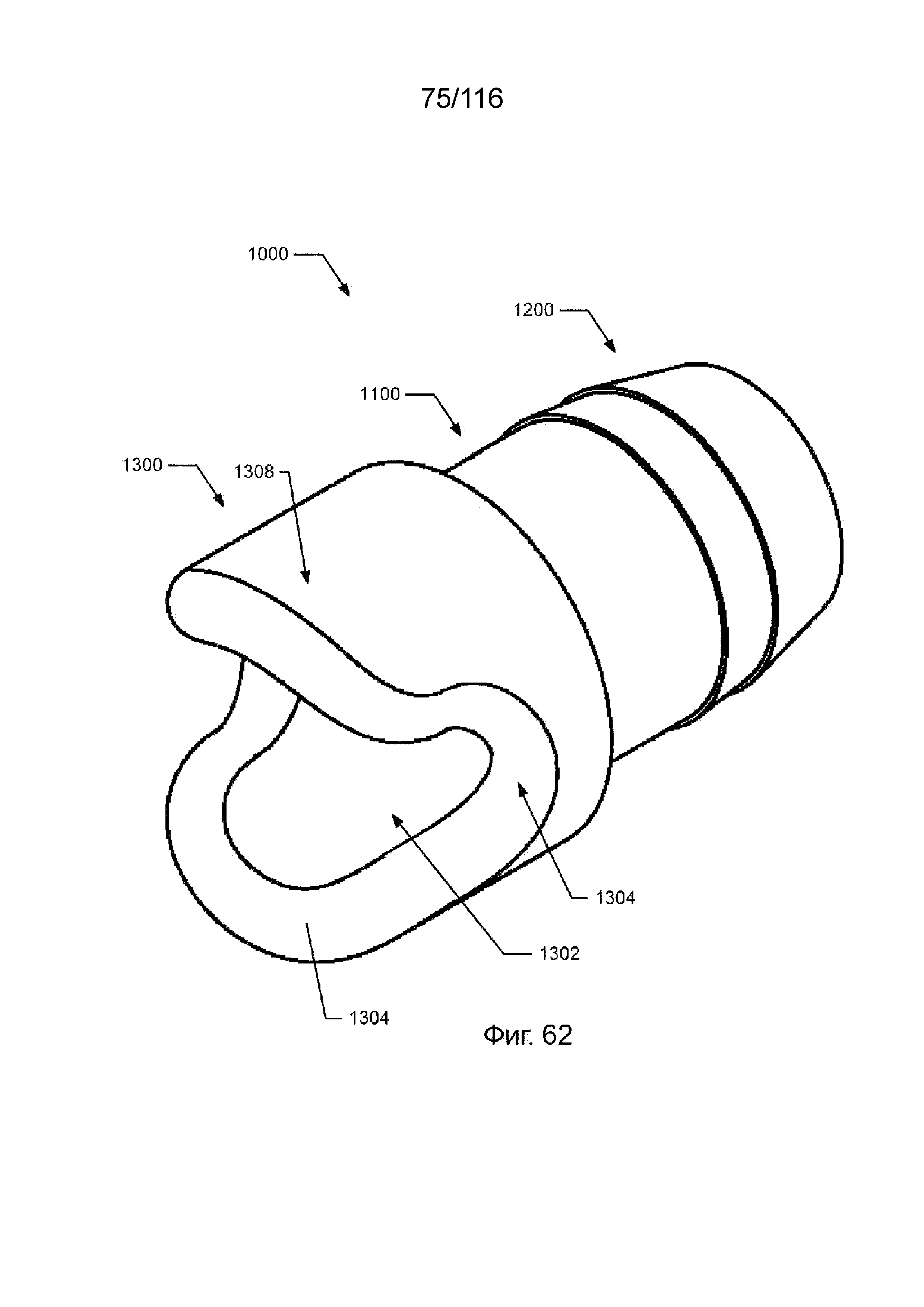
[136] На фиг. 62 приведен вид в перспективе наконечника приточного канала согласно одному варианту реализации изобретения.
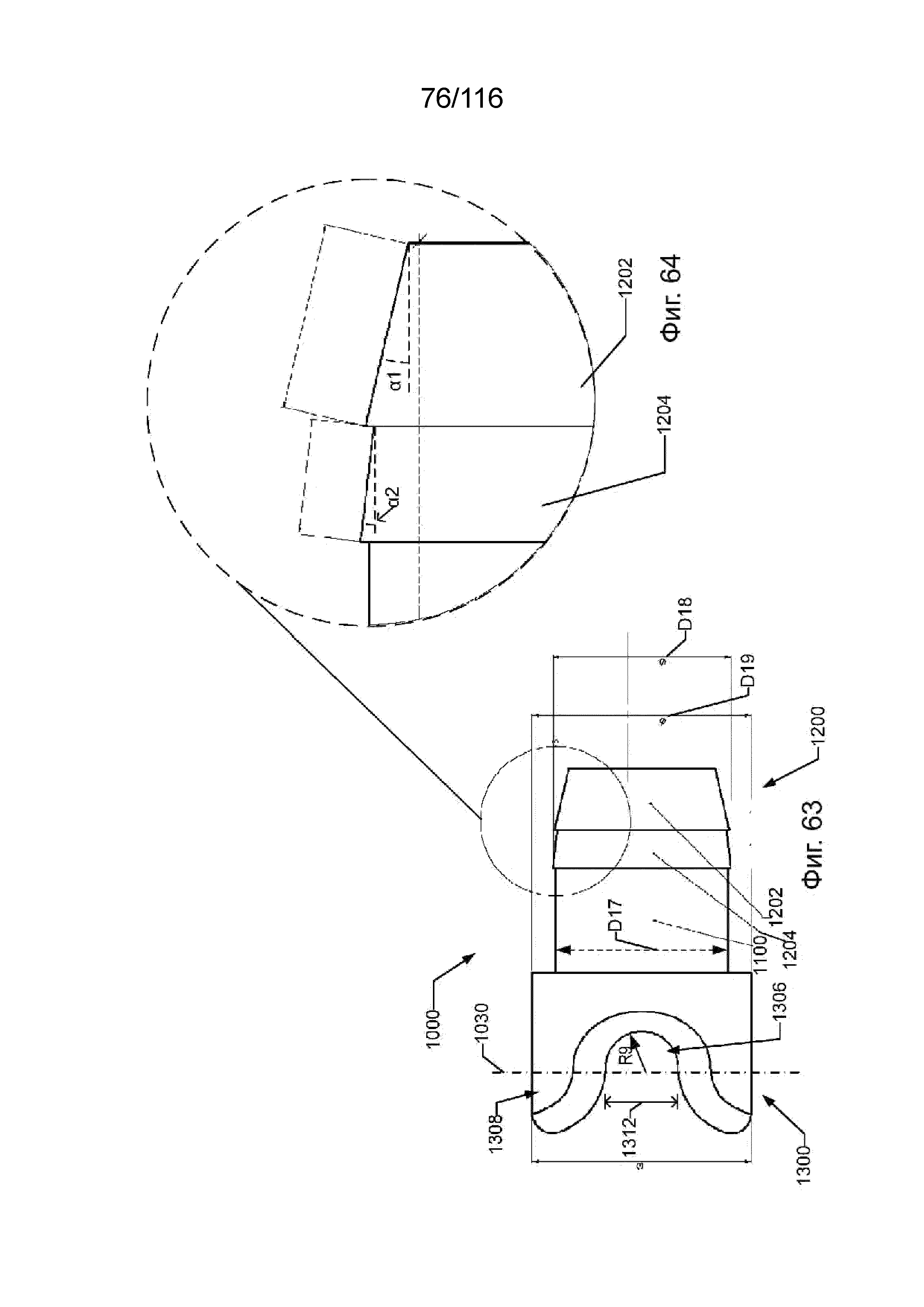
[137] На фиг. 63 приведен вид сбоку наконечника приточного канала согласно одному варианту реализации изобретения.
[138] На фиг. 64 приведен вид в увеличенном масштабе ближнего конца наконечника приточного канала согласно одному варианту реализации изобретения.
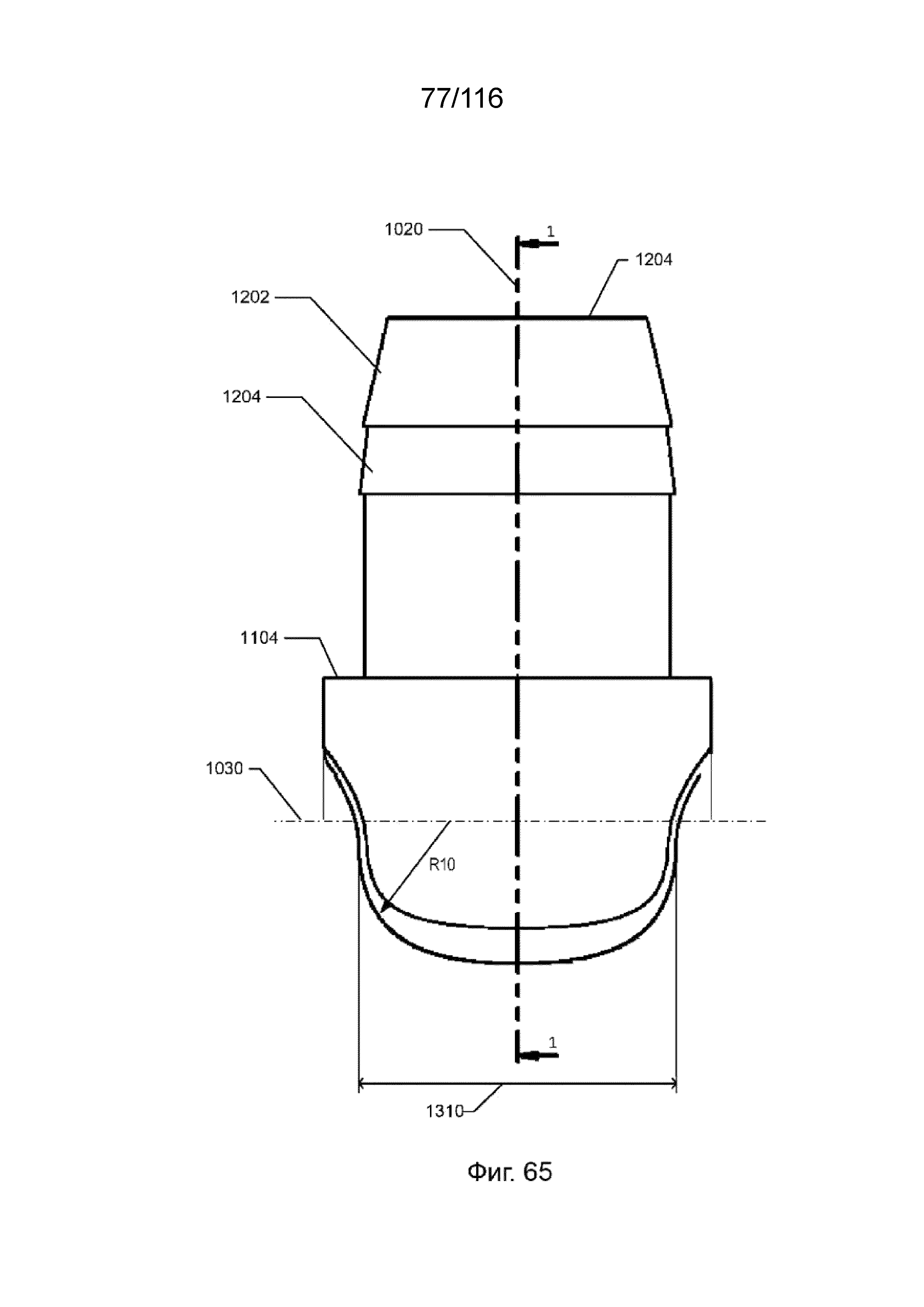
[139] На фиг. 65 приведен вид сбоку наконечника приточного канала согласно одному варианту реализации изобретения.
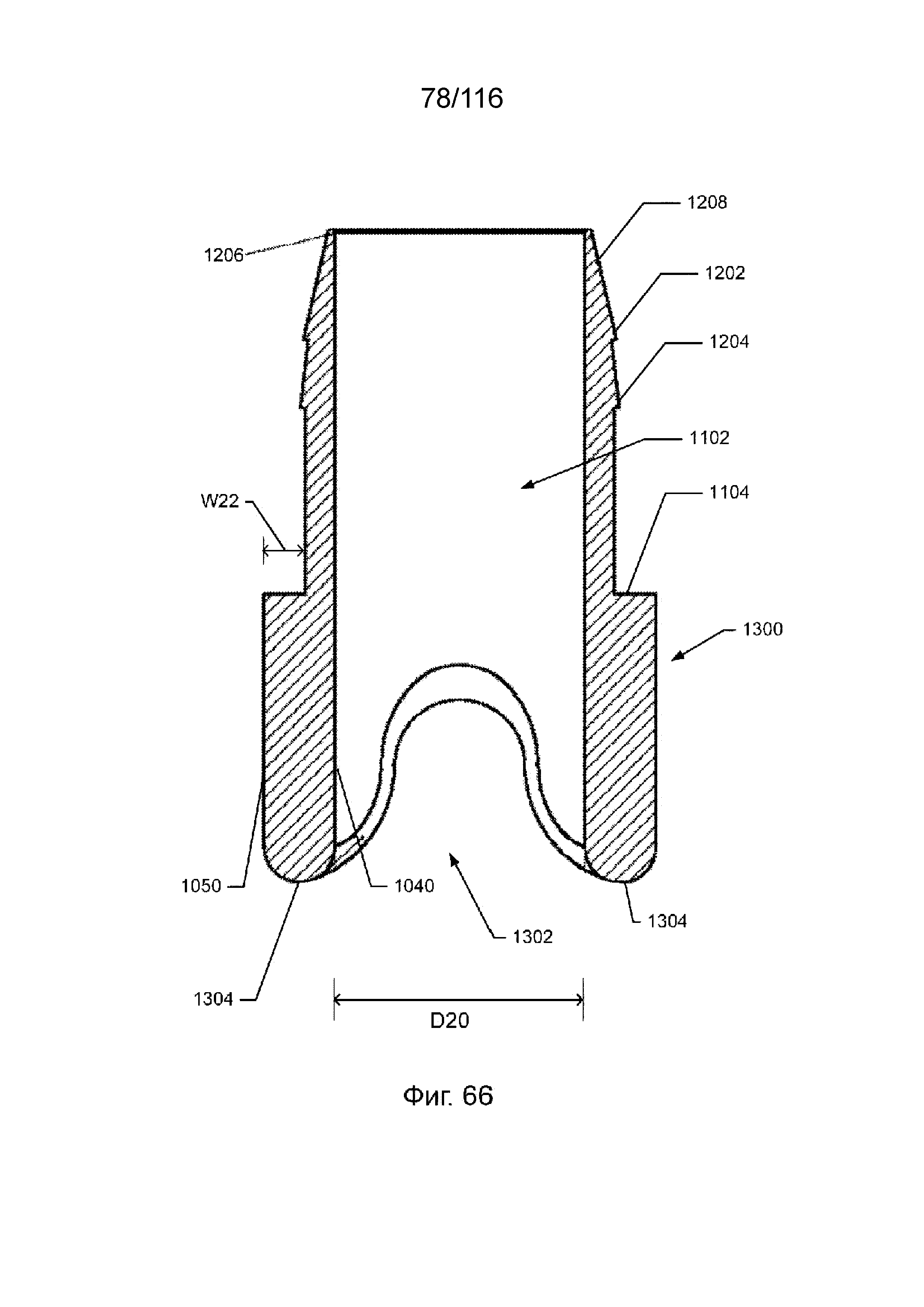
[140] На фиг. 66 приведен вид поперечного разреза наконечника приточного канала, показанного на фиг. 65, по плоскости 1-1, проходящей через продольную ось.
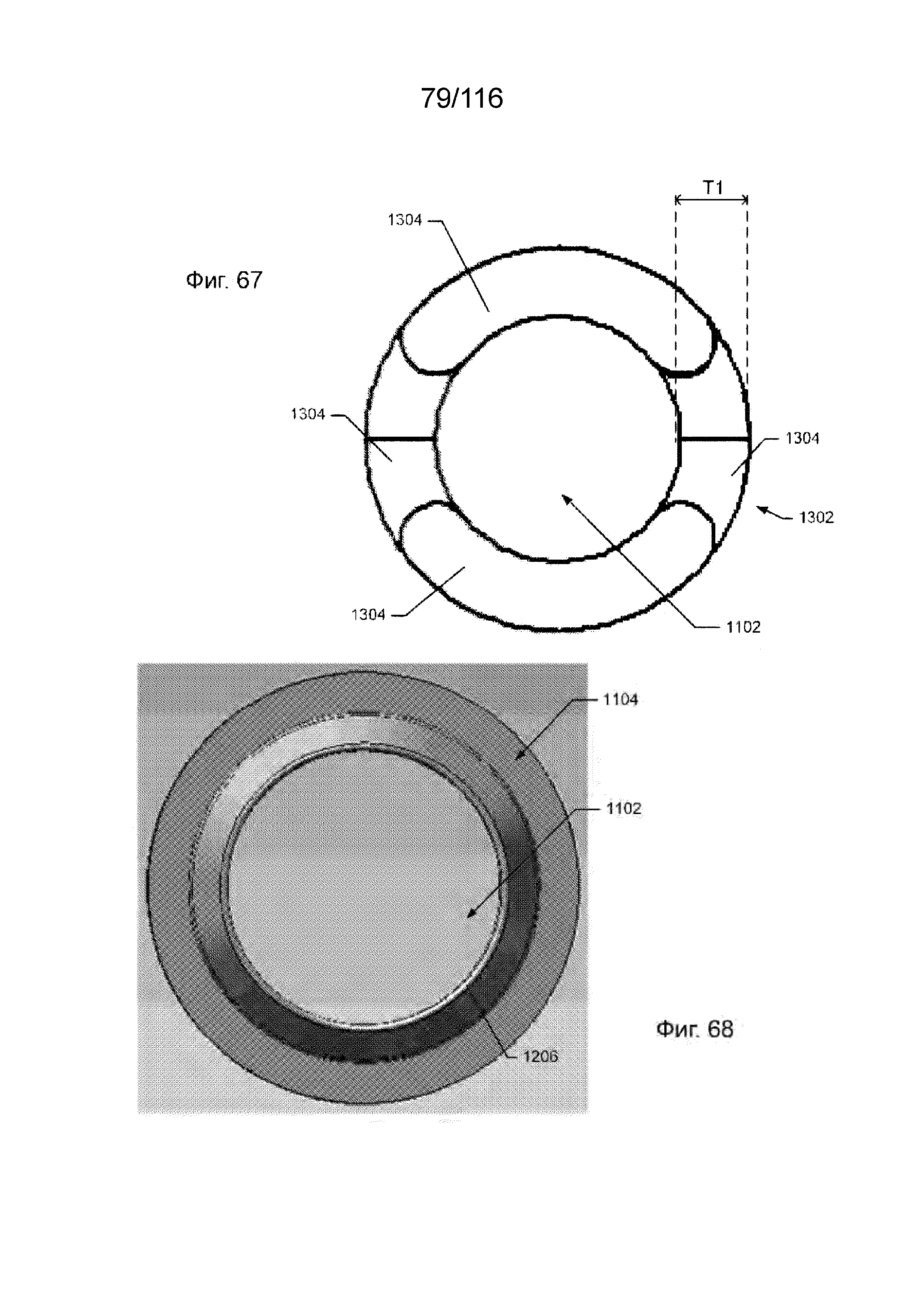
[141] На фиг. 67 приведен вид с торца дальнего конца наконечника приточного канала согласно одному варианту реализации изобретения, если смотреть по продольной оси.
[142] На фиг. 68 приведен вид с торца ближнего конца наконечника приточного канала согласно одному варианту реализации изобретения, если смотреть по продольной оси.
[143] На фиг. 69 приведен вид в перспективе наконечника приточного канала согласно одному варианту реализации изобретения.
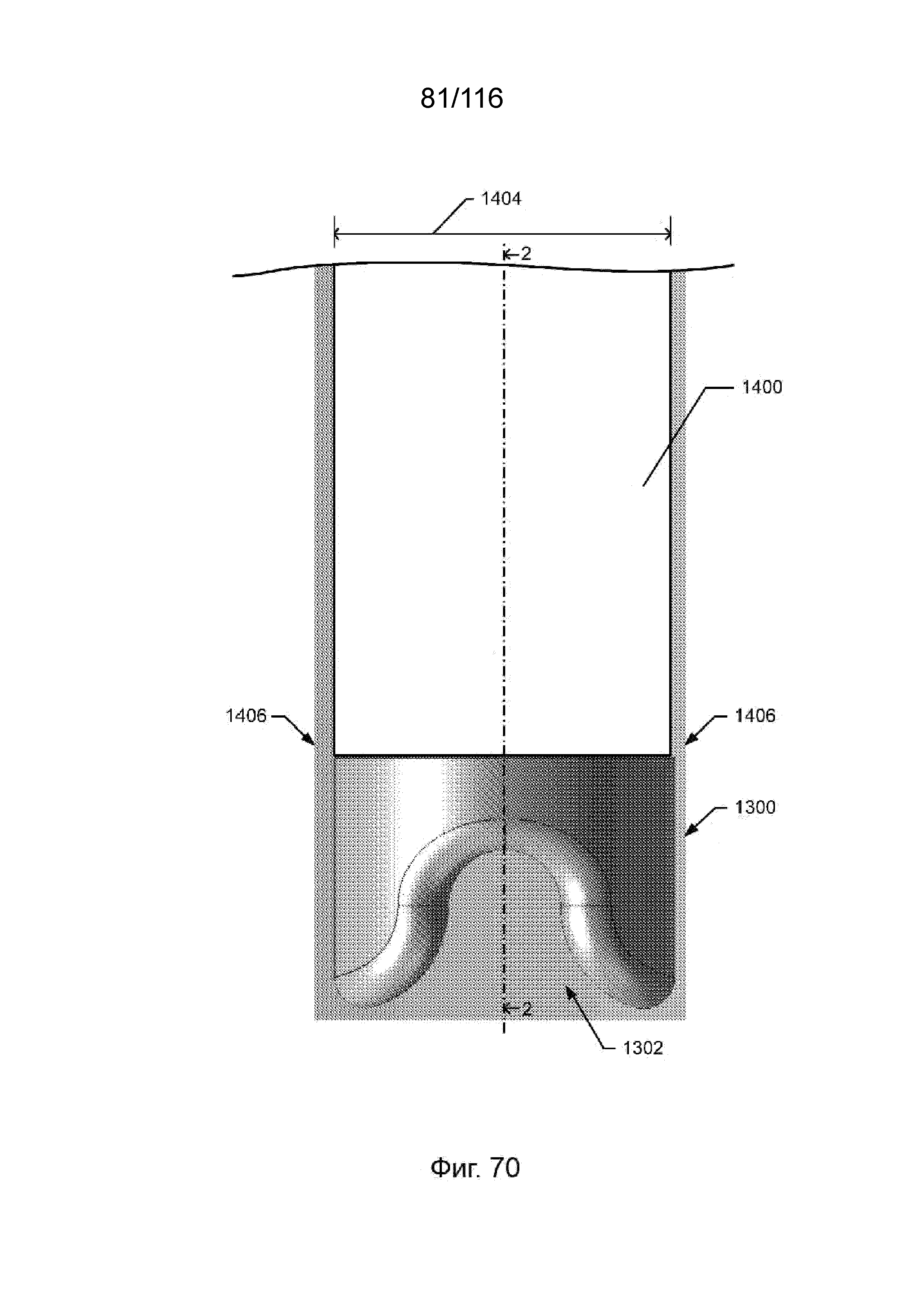
[144] На фиг. 70 приведен вид в перспективе наконечника приточного канала, во взаимодействии с каналом, согласно одному варианту реализации изобретения.
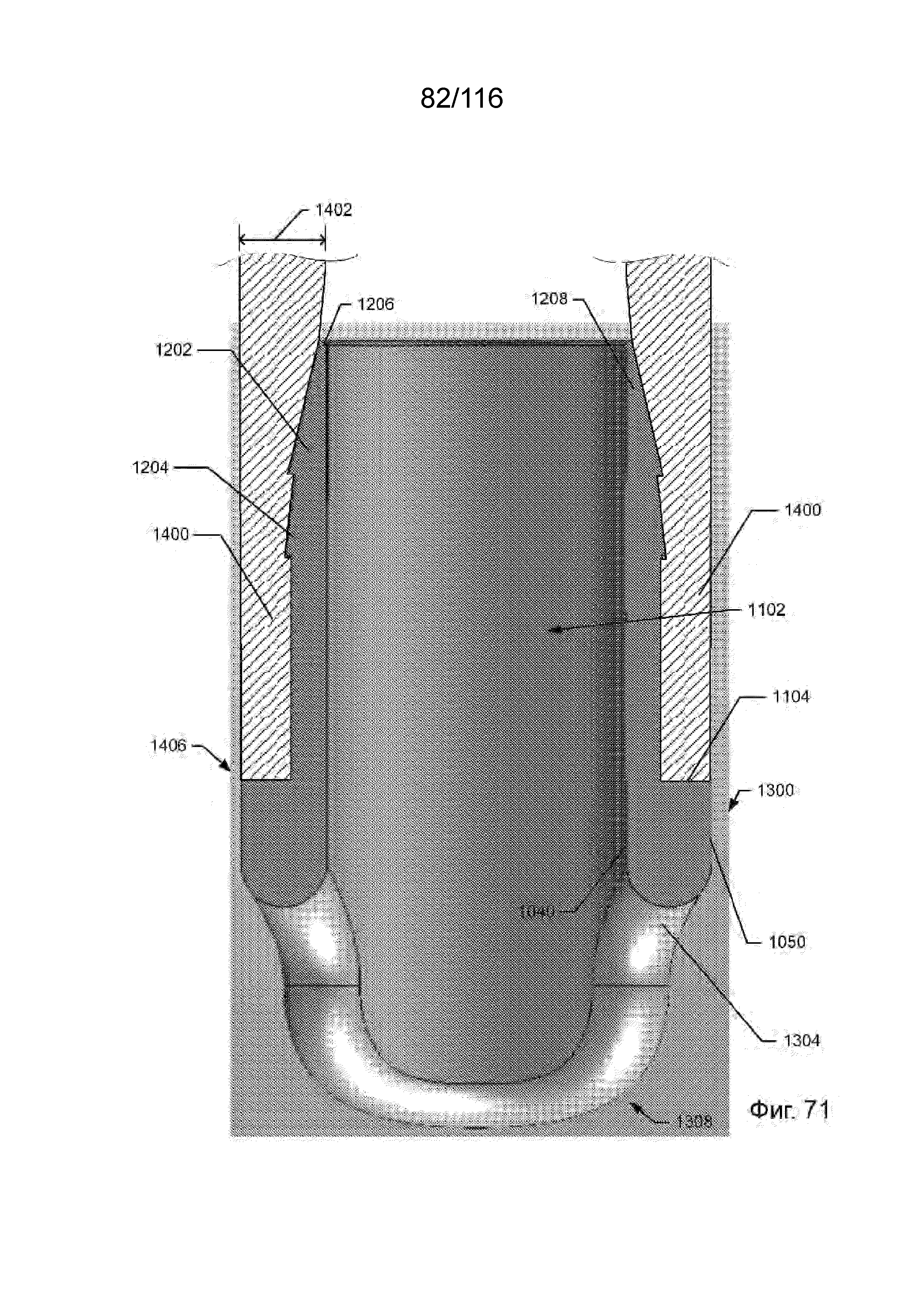
[145] На фиг. 71 приведен вид поперечного разреза наконечника приточного канала и канала, показанного на фиг. 70, в плоскости 2-2, проходящей через продольную ось.
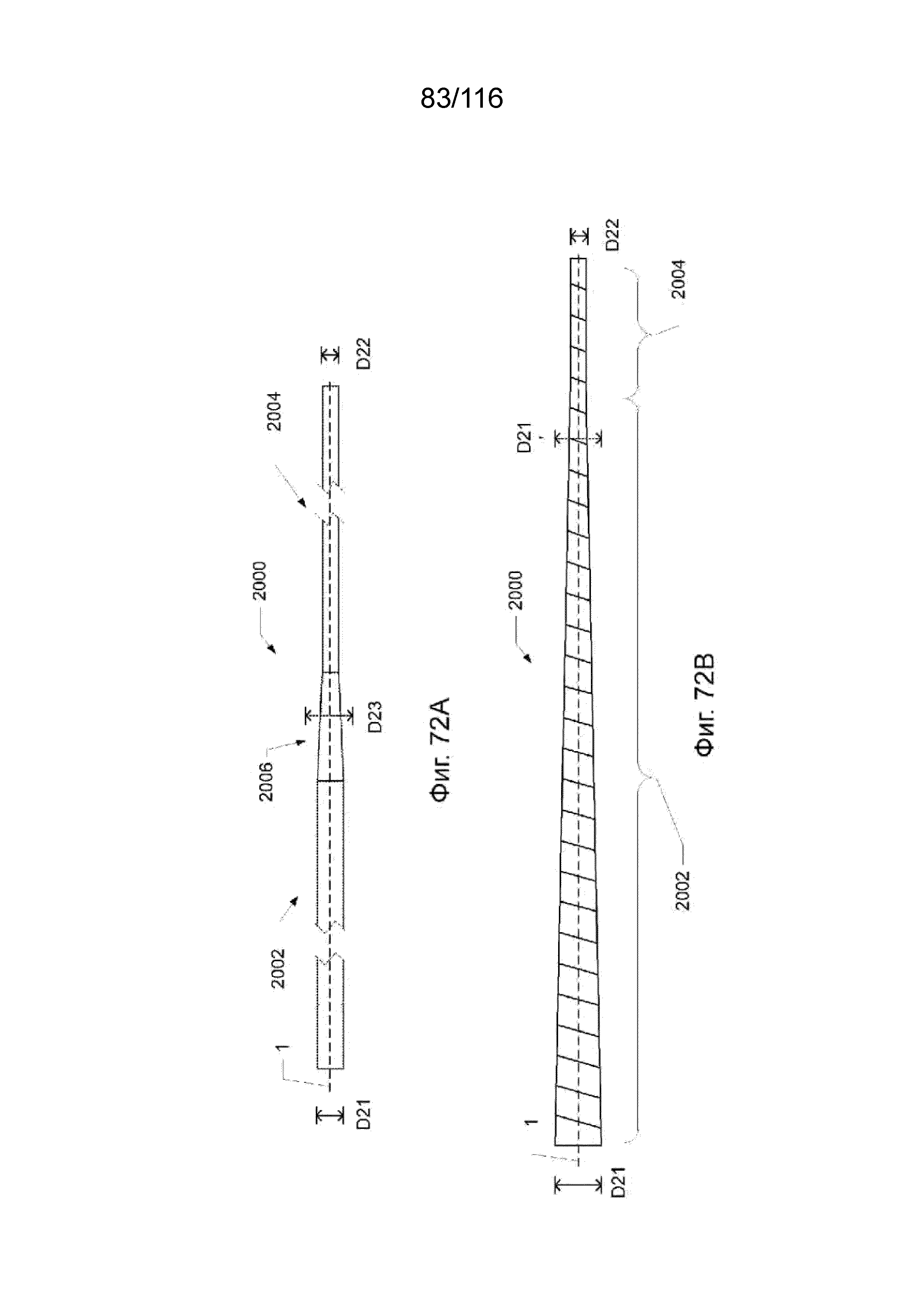
[146] На фиг. 72A приведен вид сверху наконечника выводного канала для линейного наконечника выводного канала согласно другому варианту реализации изобретения.
[147] На фиг. 72B приведен вид сверху наконечника выводного канала для линейного наконечника выводного канала согласно другому варианту реализации изобретения.
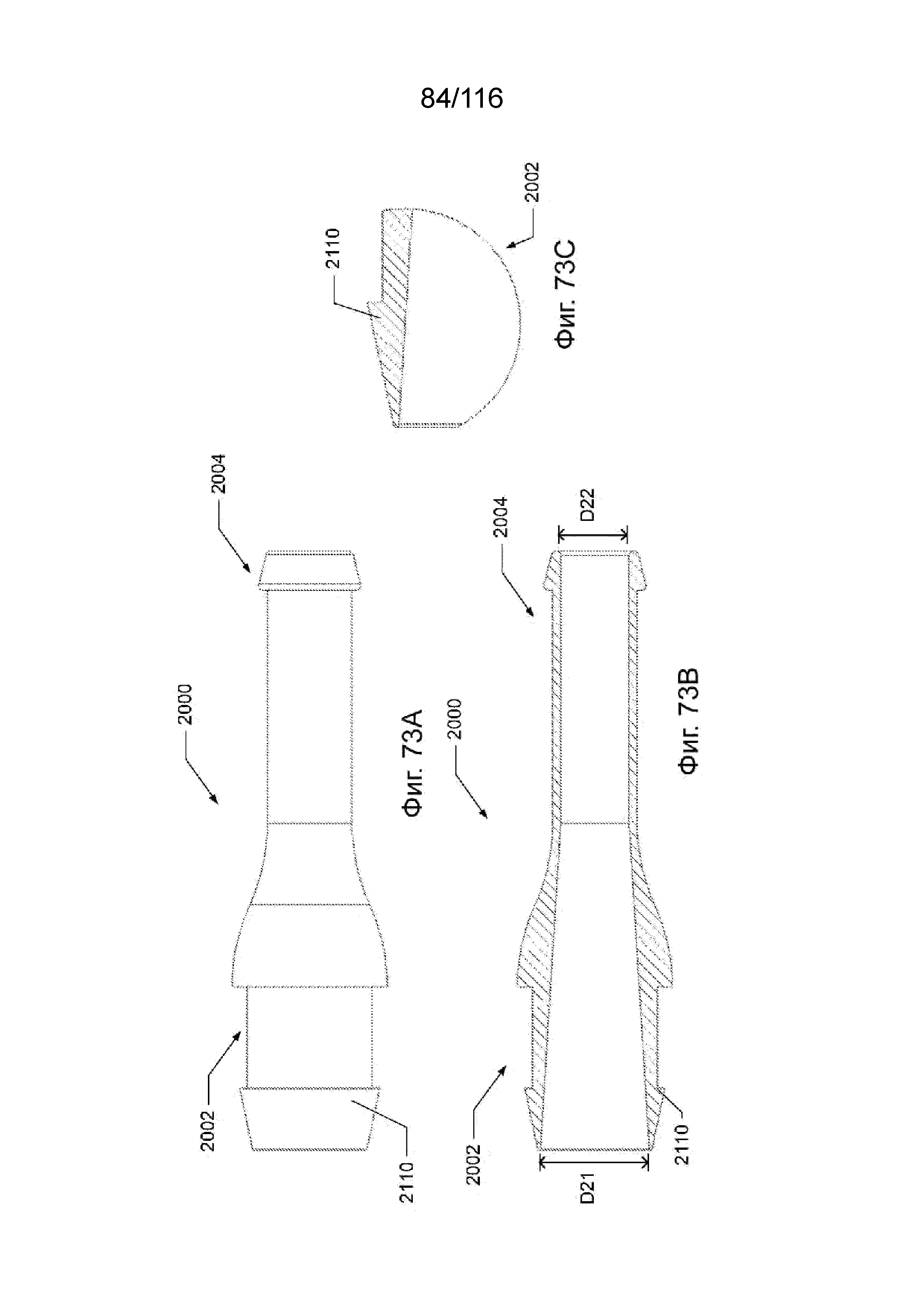
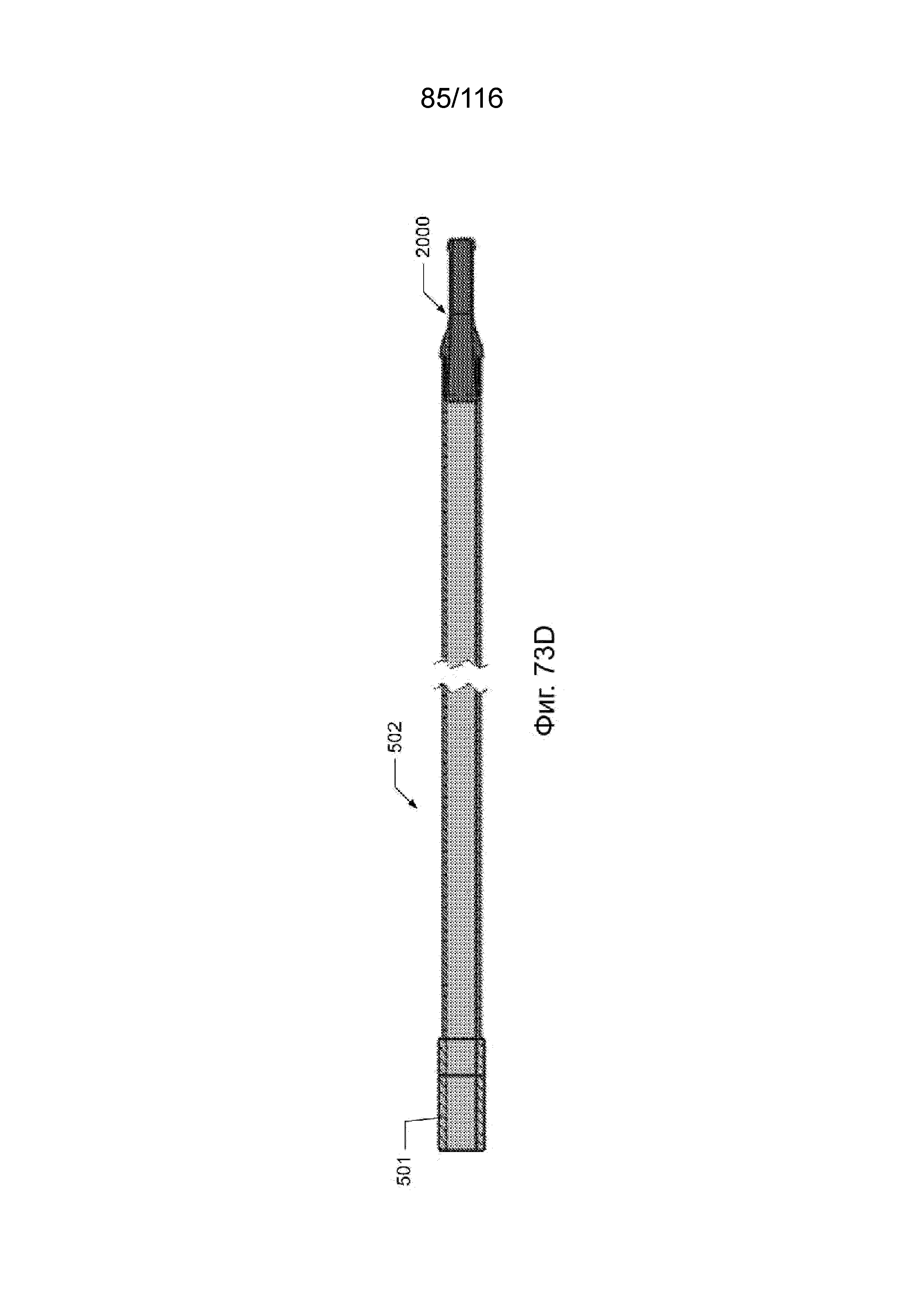
[148] На фиг. 73A приведен вид сбоку наконечника выводного канала для линейного наконечника выводного канала согласно другому варианту реализации изобретения.
[149] На фиг. 73B приведен вид поперечного разреза наконечника выводного канала для линейного наконечника выводного канала по фиг. 73A, если смотреть по оси симметрии.
[150] На фиг. 73С приведен выносной вид поперечного разреза участка ближнего конца наконечника выводного канала для линейного наконечника выводного канала по фиг. 73A, если смотреть по оси симметрии.
[151] На фиг. 73D приведен вид сверху наконечника выводного канала для линейного наконечника выводного канала по фиг. 73A во взаимодействии с выводным каналом, согласно одному варианту реализации изобретения.
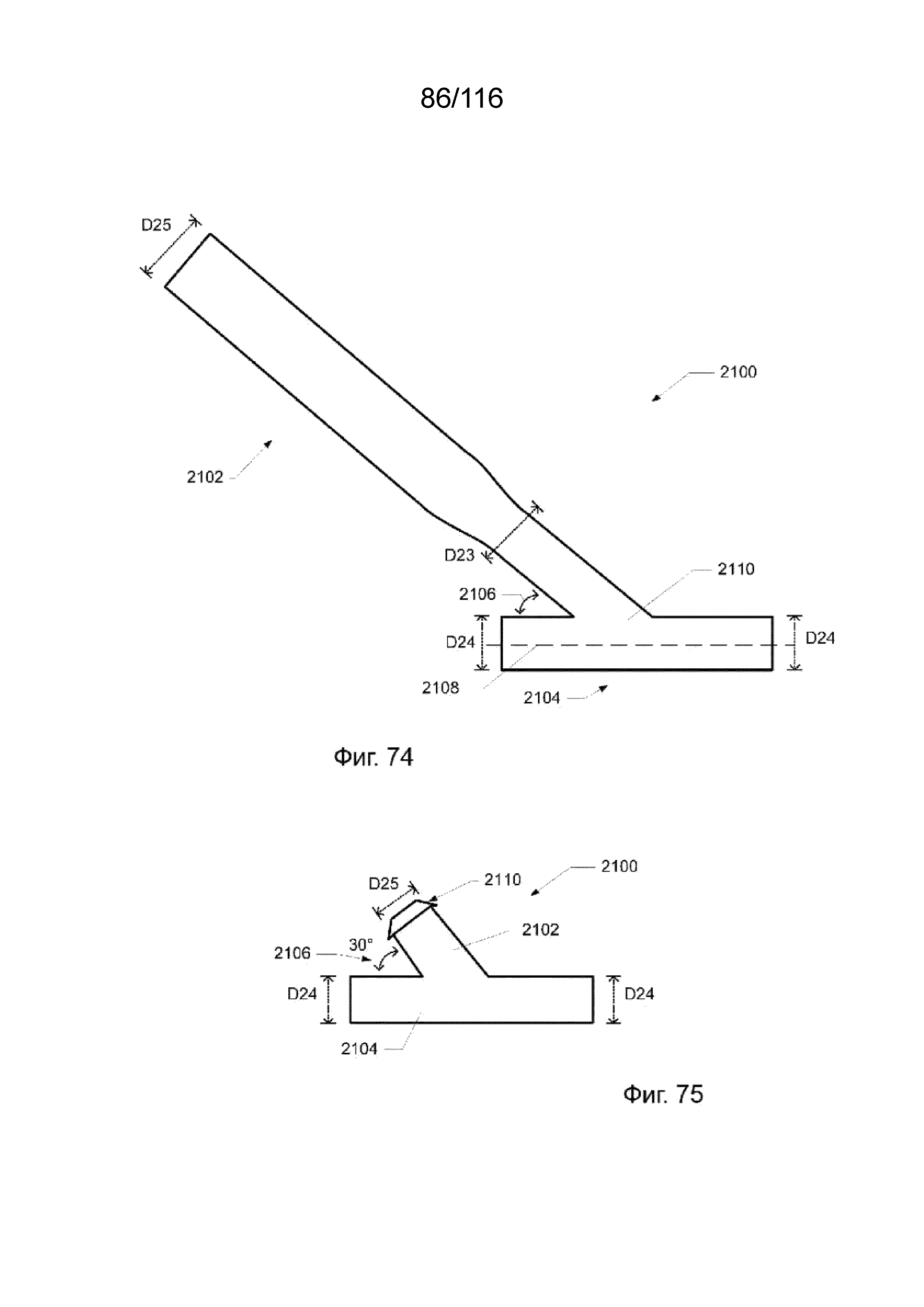
[152] На фиг. 74 приведен вид сверху выводного Т-образного наконечника согласно одному варианту реализации изобретения.
[153] На фиг. 75 приведен вид сверху выводного Т-образного наконечника согласно другому варианту реализации изобретения.
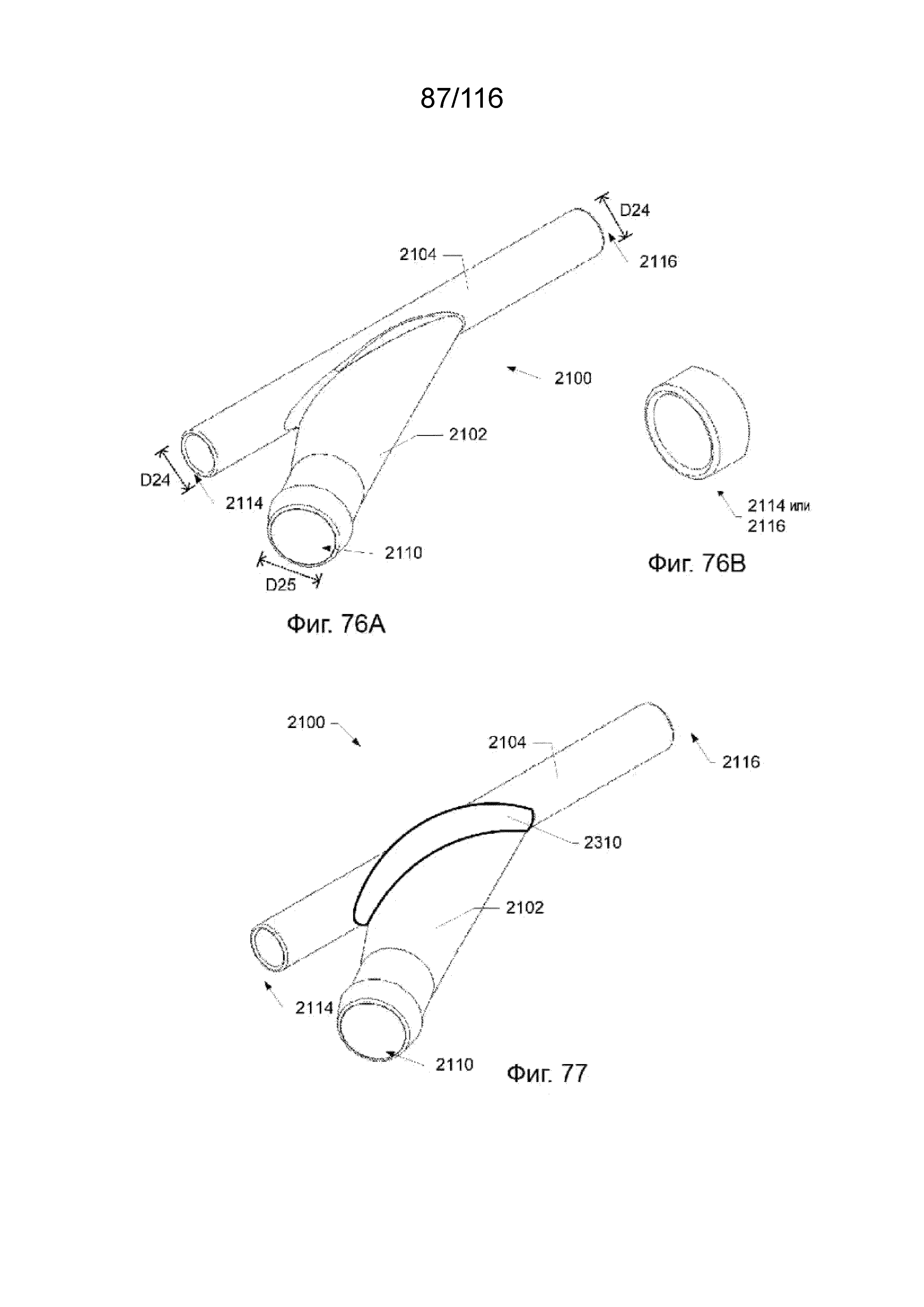
[154] На фиг. 76A приведен вид в перспективе выводного Т-образного наконечника согласно одному варианту реализации изобретения.
[155] На фиг. 76B приведен выносной вид в перспективе выводного Т-образного наконечника по фиг. 76A на ближнем или дальнем конце внутрисосудистого патрубка, согласно одному варианту реализации изобретения.
[156] На фиг. 77 приведен вид в перспективе выводного Т-образного наконечника согласно другому варианту реализации изобретения.
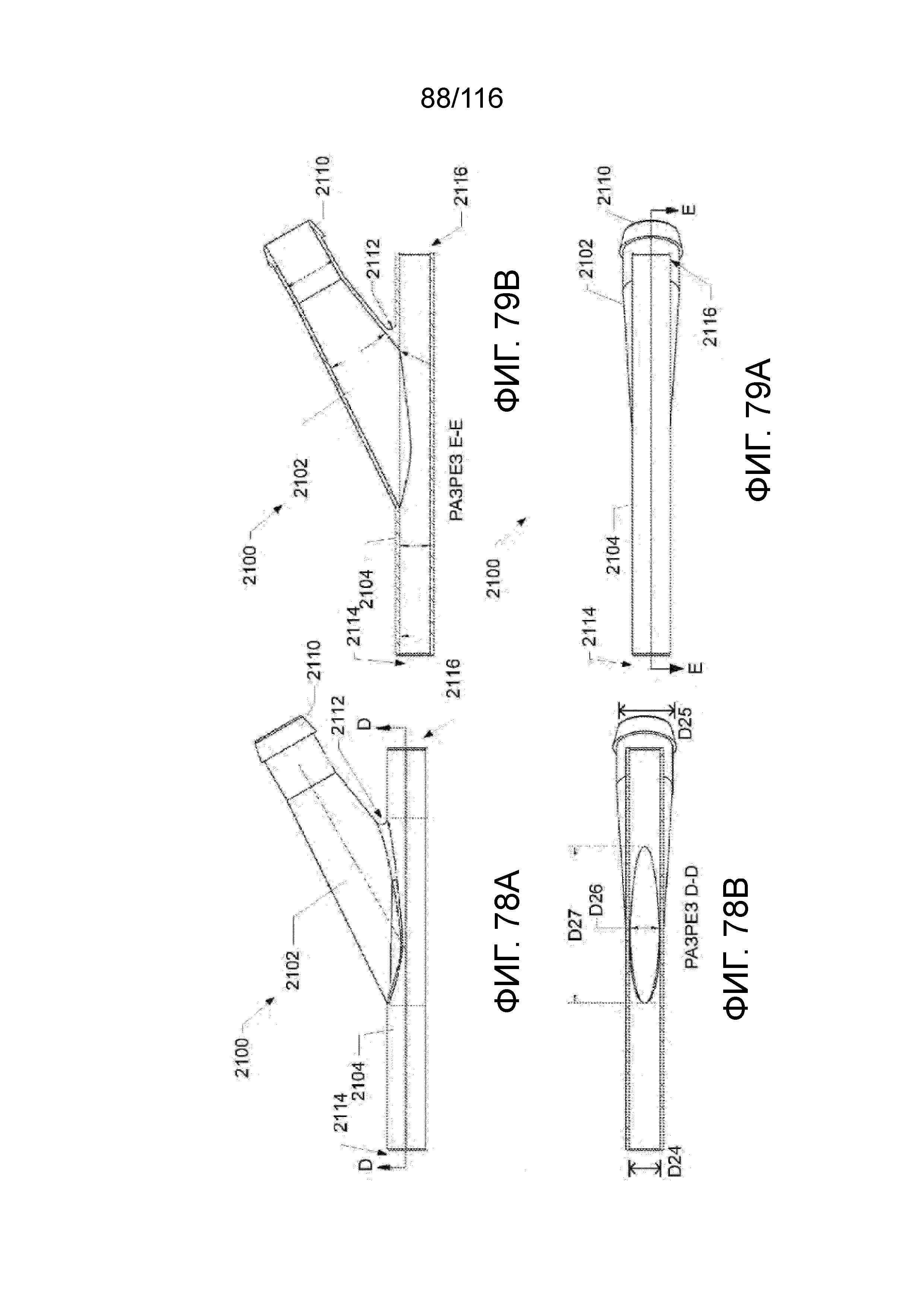
[157] На фиг. 78A приведен вид сверху выводного Т-образного наконечника согласно одному варианту реализации изобретения.
[158] На фиг. 78B приведен вид снизу частичного разреза Т-образного наконечника по фиг. 78A, если смотреть по линии D-D.
[159] На фиг. 79A приведен вид снизу выводного Т-образного наконечника согласно одному варианту реализации изобретения.
[160] На фиг. 79B приведен вид сбоку с частичным разрезом выводного Т-образного наконечника по фиг. 79B, если смотреть по линии E-E.
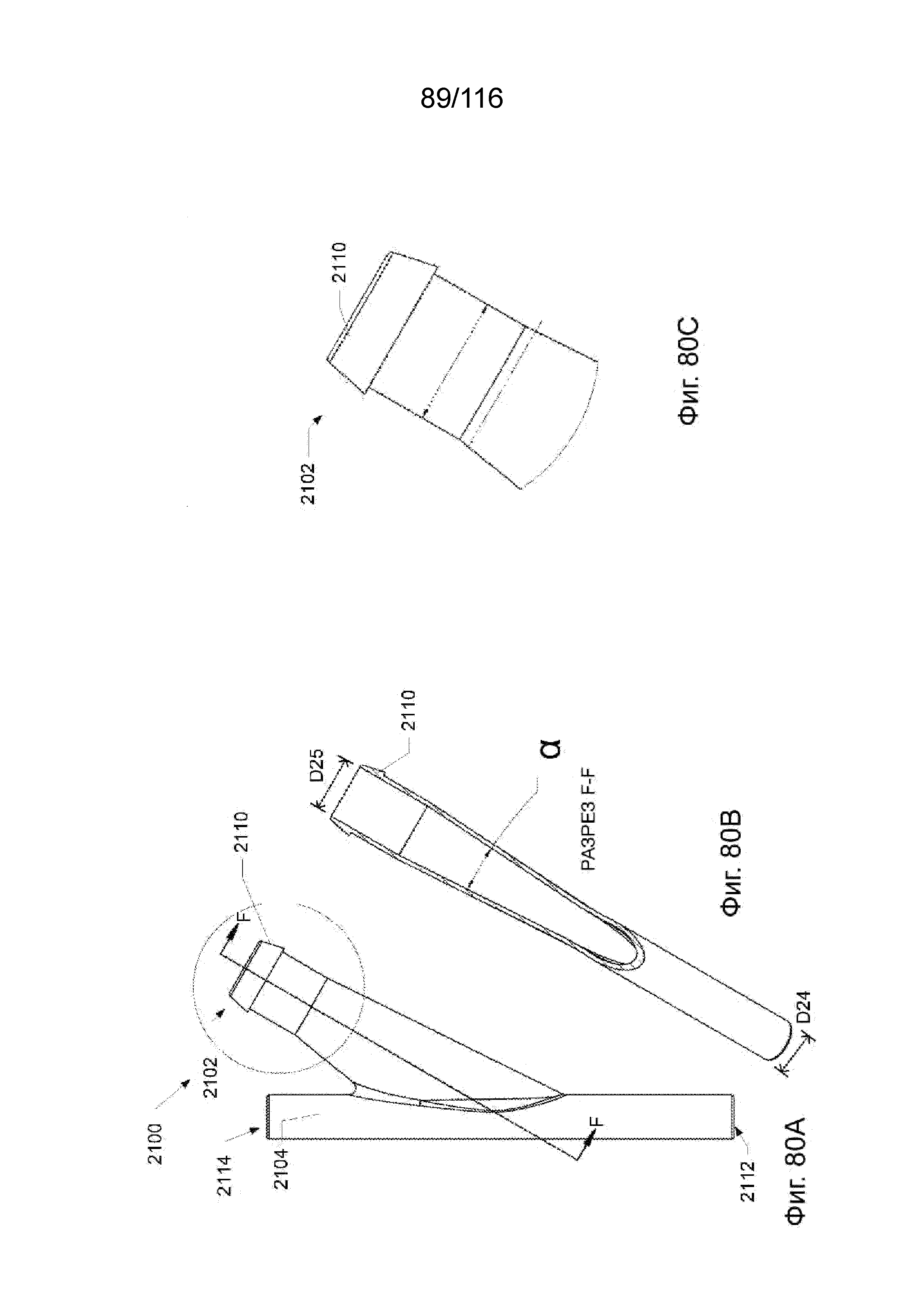
[161] На фиг. 80A приведен вид сбоку выводного Т-образного наконечника согласно одному варианту реализации изобретения.
[162] На фиг. 80B приведен вид частичного разреза выводного Т-образного наконечника по фиг. 80A, если смотреть по линии F-F.
[163] На фиг. 80C приведен вид в увеличенном масштабе патрубка приточного канала выводного Т-образного наконечника по фиг. 80A.
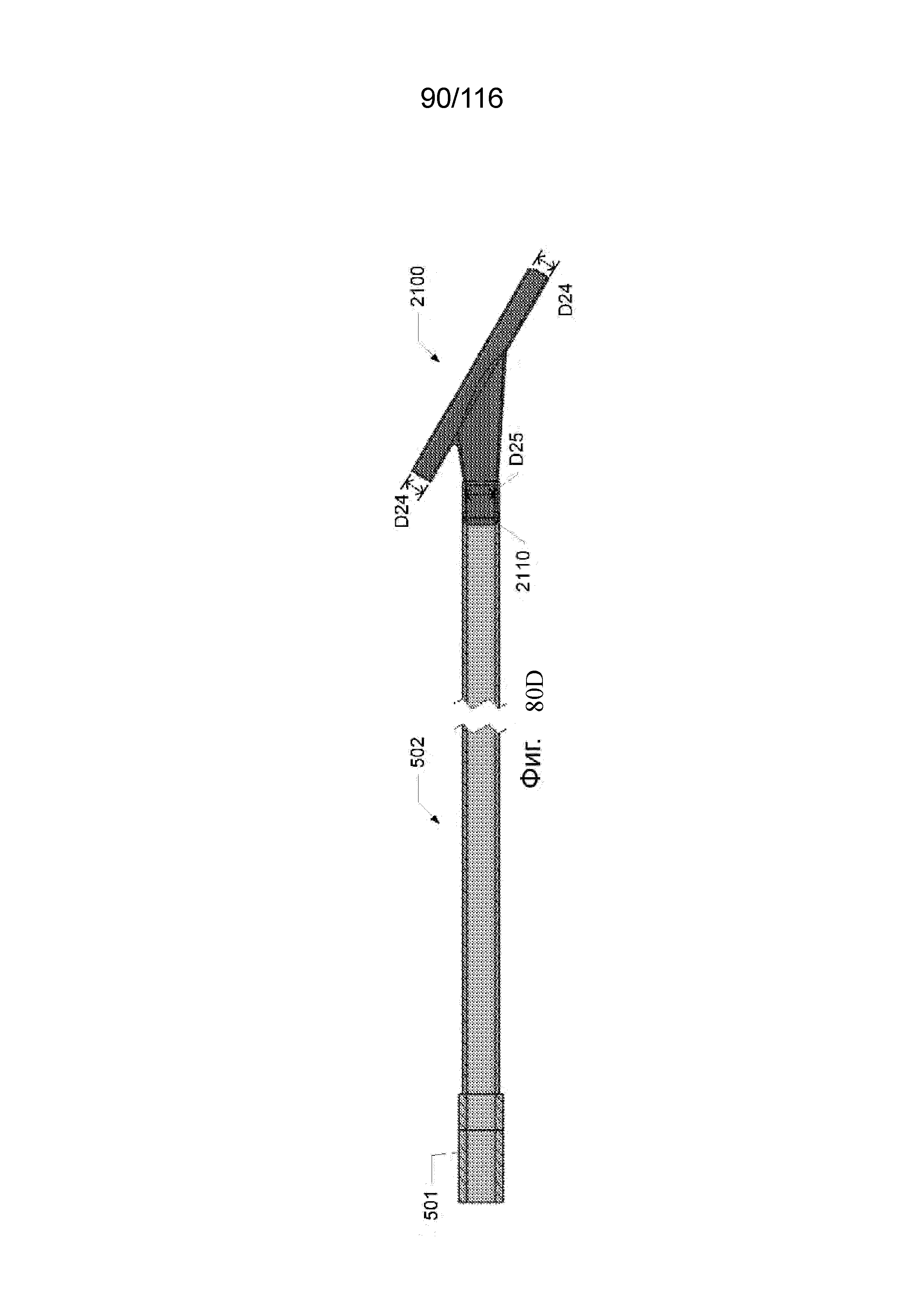
[164] На фиг. 80D приведен вид сверху выводного Т-образного наконечника по фиг. 80A в сборе с выводным каналом или дальним выводным сегментом.
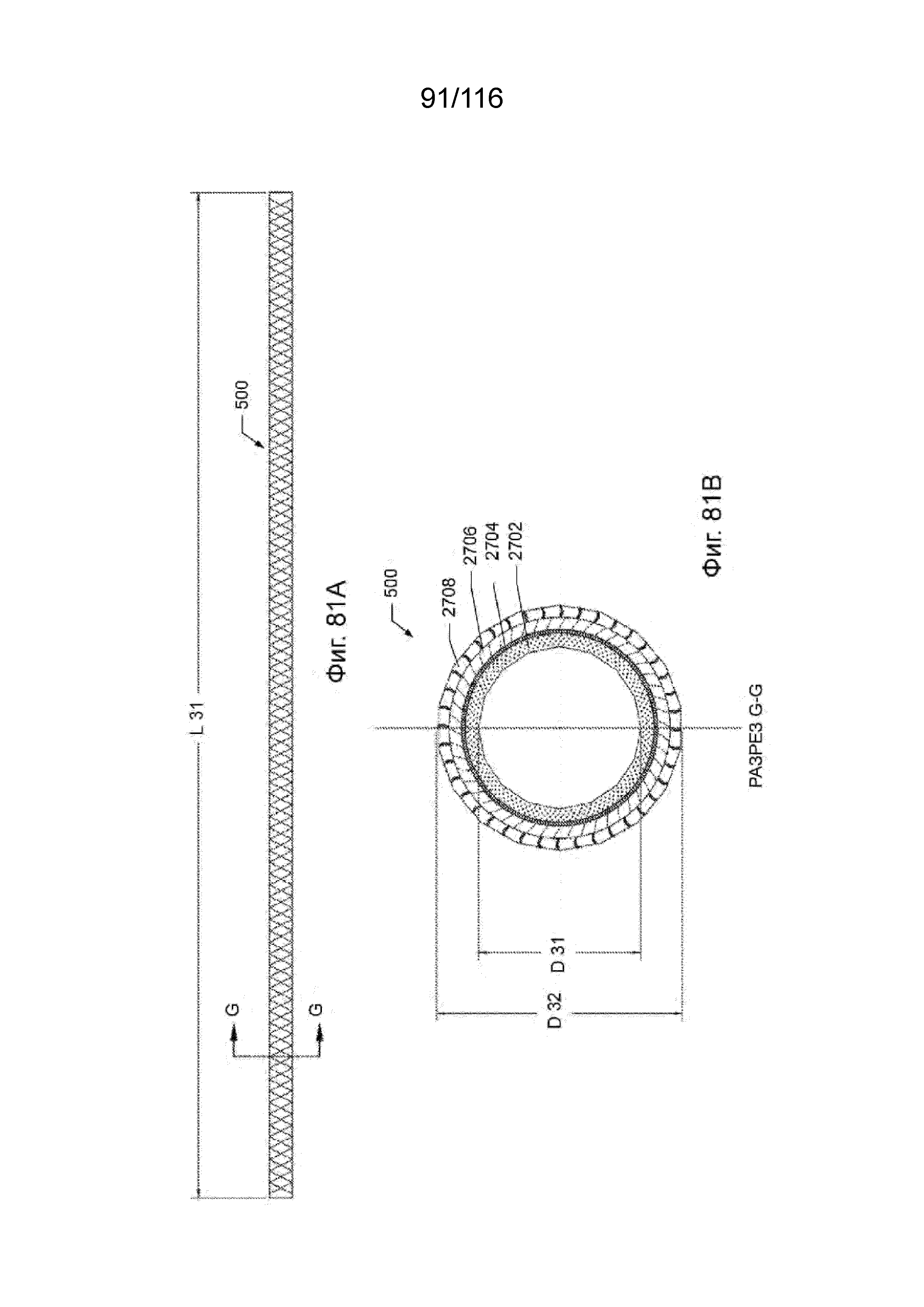
[165] На фиг. 81A приведен вид сверху ближнего сегмента канала согласно одному варианту реализации изобретения.
[166] На фиг. 81B приведен вид поперечного разреза ближнего сегмента канала по FIG. 81A, если смотреть по линии G-G.
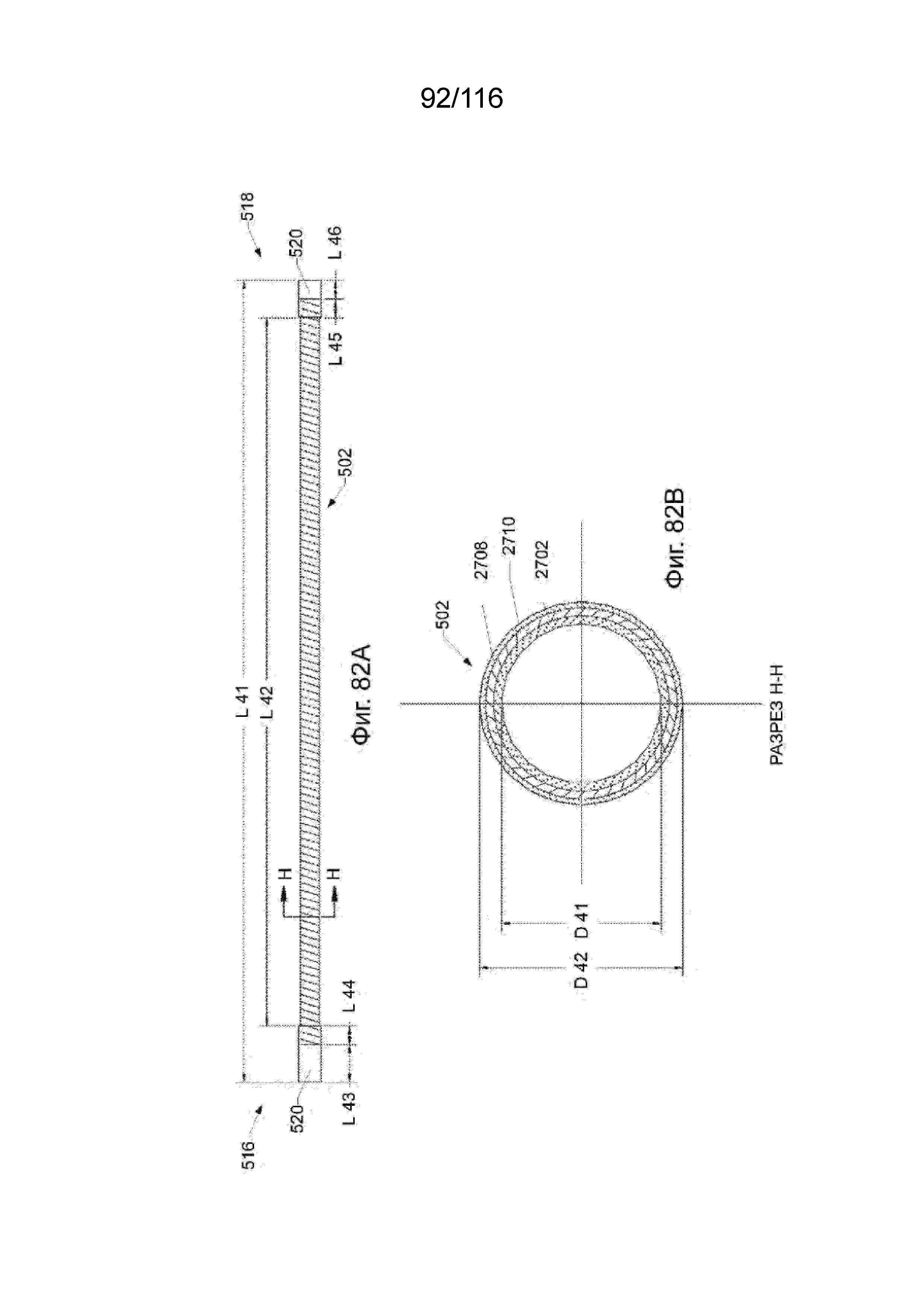
[167] На фиг. 82A приведен вид сверху дальнего сегмента канала согласно одному варианту реализации изобретения.
[168] На фиг. 82B приведен вид поперечного разреза дальнего сегмента канала по FIG. 82A, если смотреть по линии H-H.
[169] На фиг. 83 приведен вид сверху выводного канала согласно одному варианту реализации изобретения, содержащего ближний сегмент канала, соединенный с дальним сегментом канала, который соединен с линейным наконечником выводного канала.
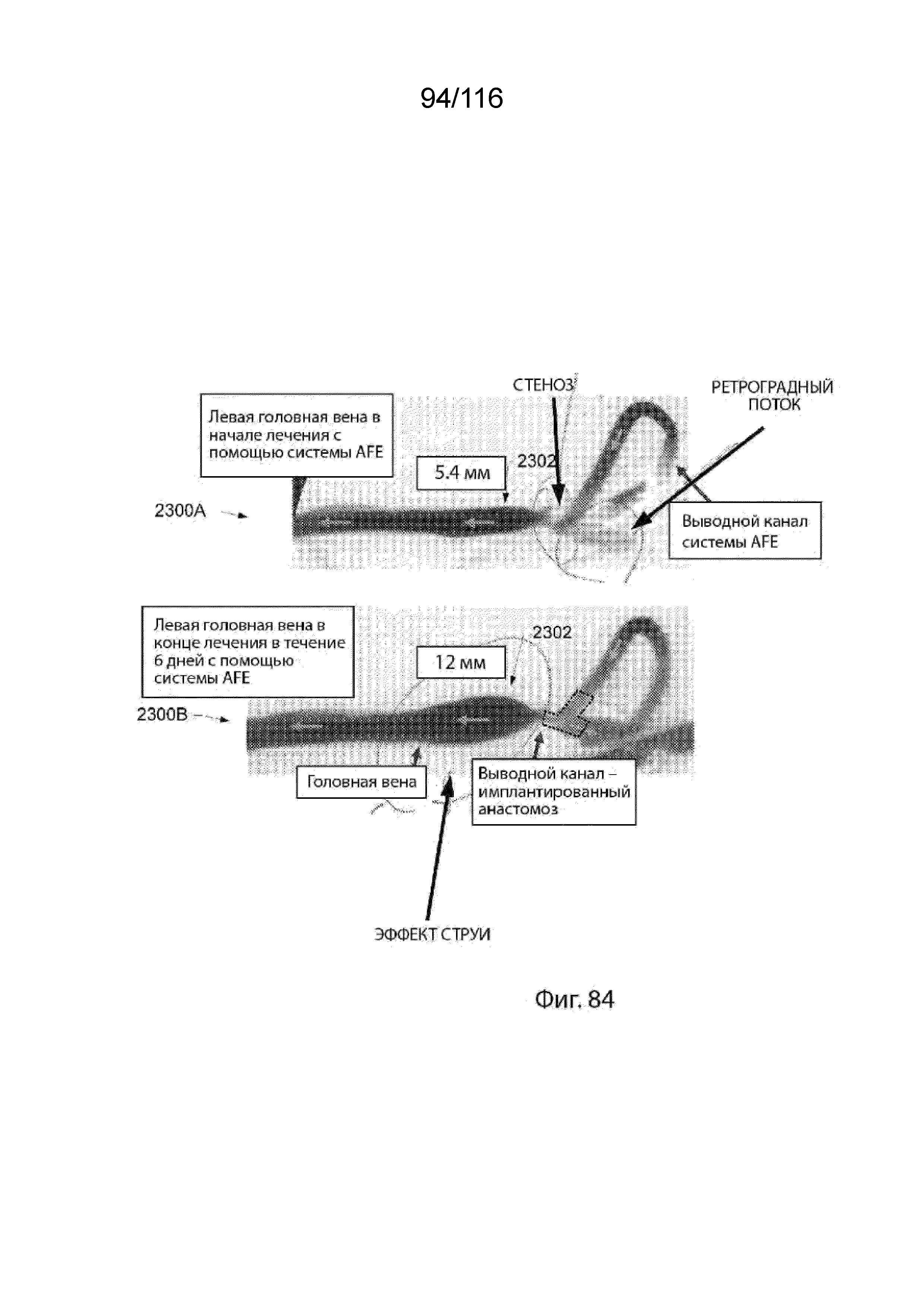
[170] На фиг. 84 приведены ангиографические изображения расширенной овечьей головной вены после лечения с использованием системы AFE с вариантом реализации выводного канала, содержащего дальний сегмент из ePTFE, соединенный с веной.
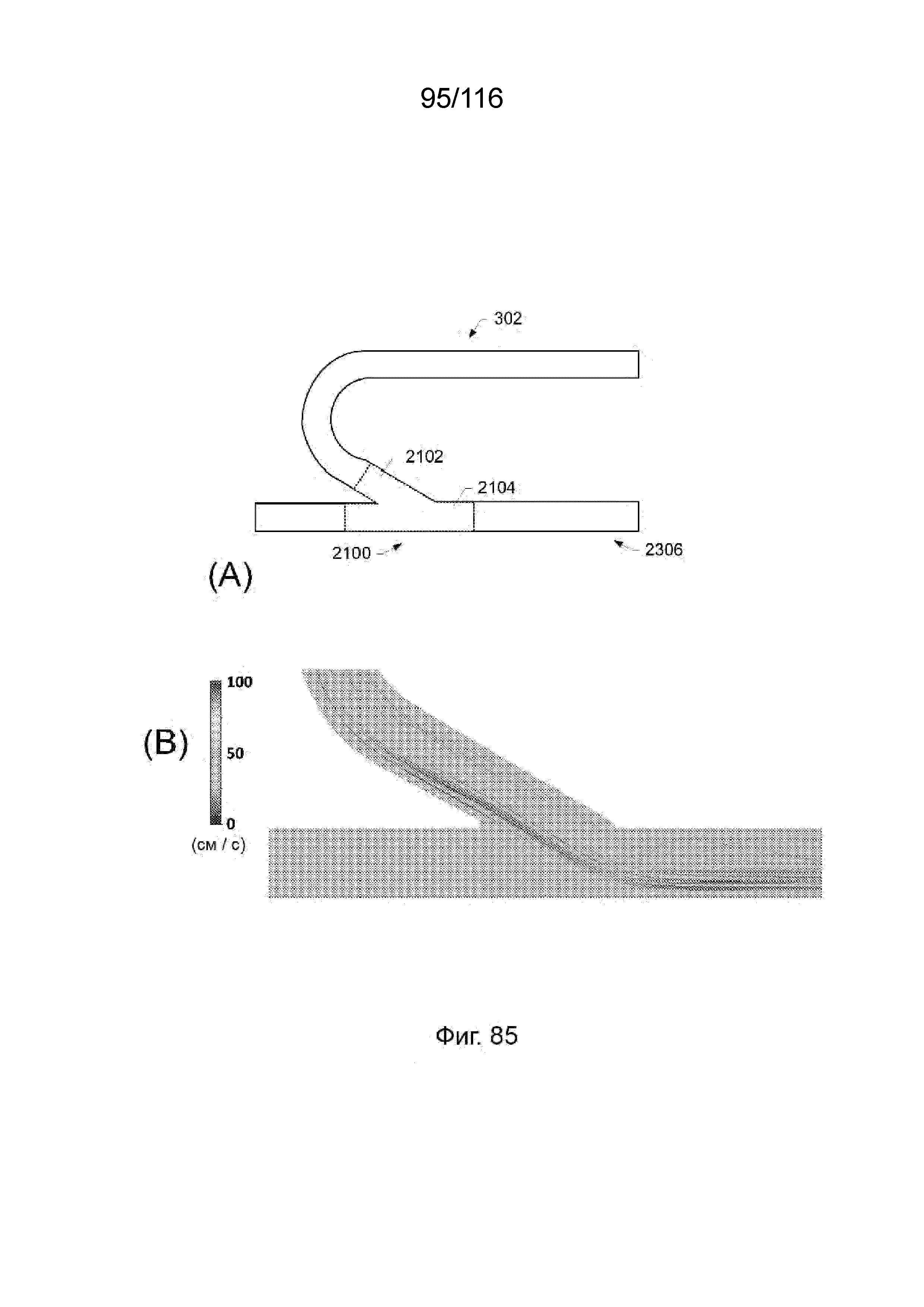
[171] На фиг. 85 А-В приведена схема и изображение вычисляемой динамики текучей среды (computational fluid dynamics, CFD), изображающее скорость вдоль линии тока в кровеносном сосуде, содержащем Т-образный наконечник выводного канала.
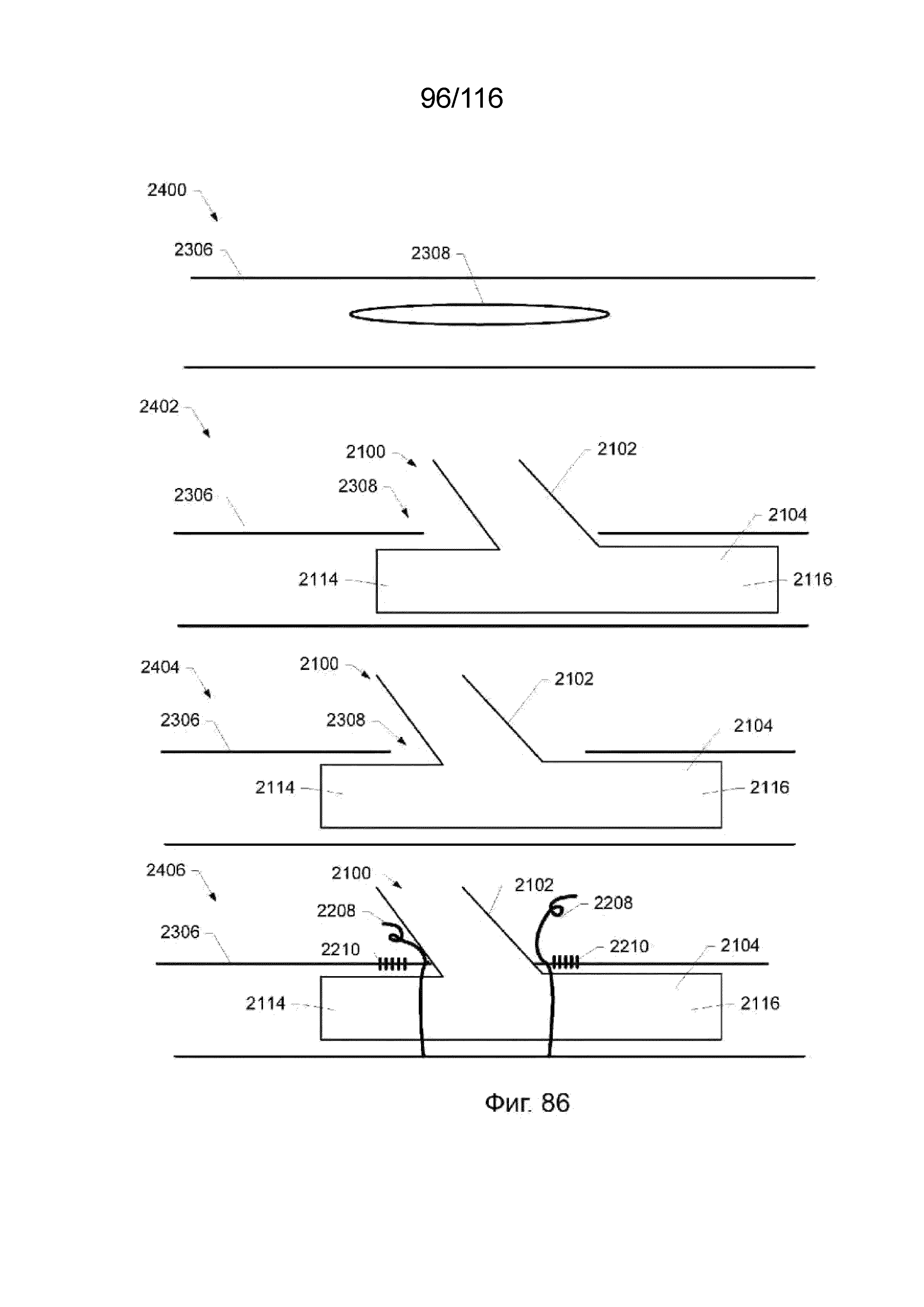
[172] На фиг. 86 изображен способ имплантации Т-образного наконечника выводного канала согласно одному варианту реализации изобретения.
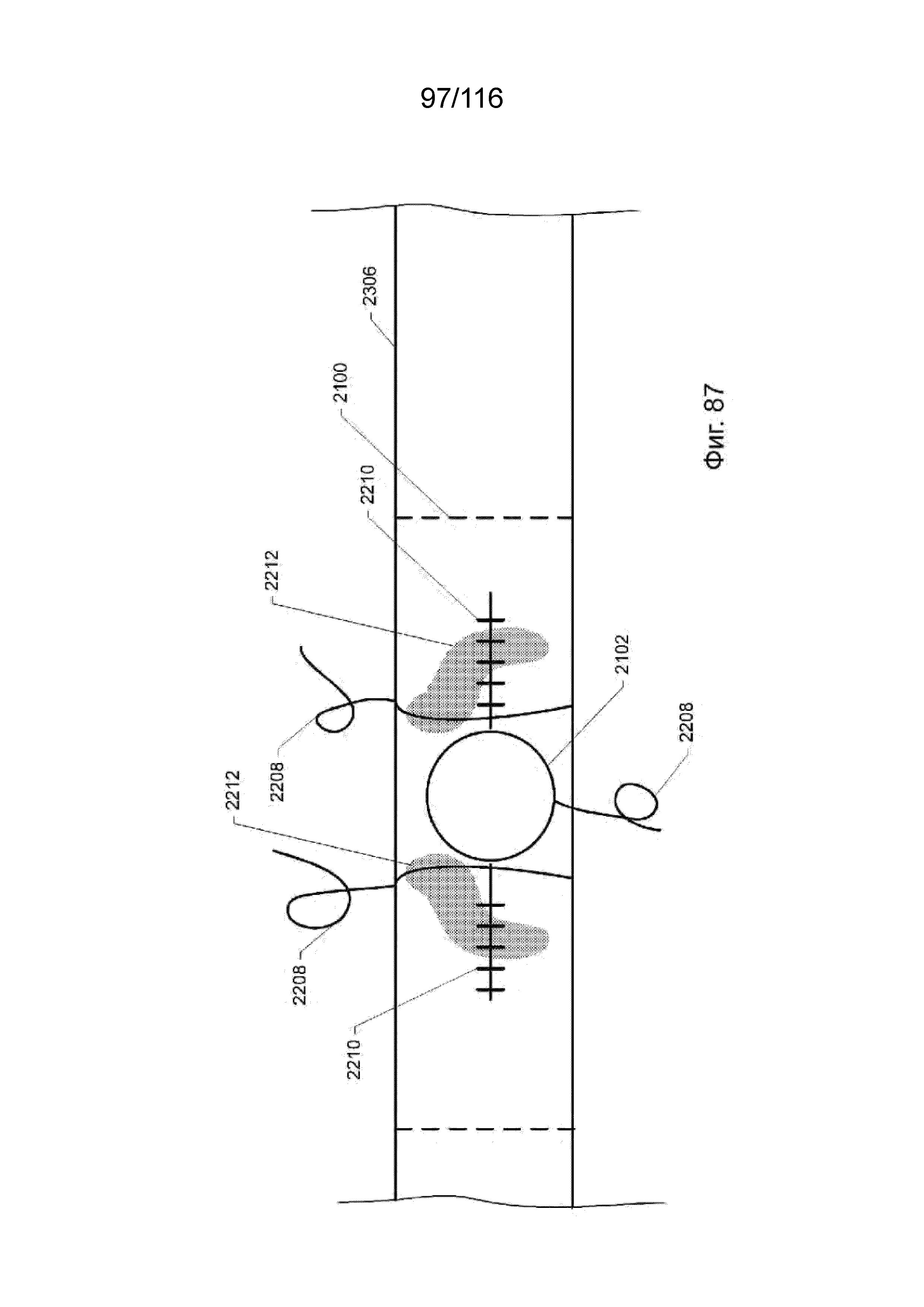
[173] На фиг. 87 приведен вид сверху Т-образного наконечника выводного канала, имплантированного в кровеносный сосуд, согласно одному варианту реализации изобретения.
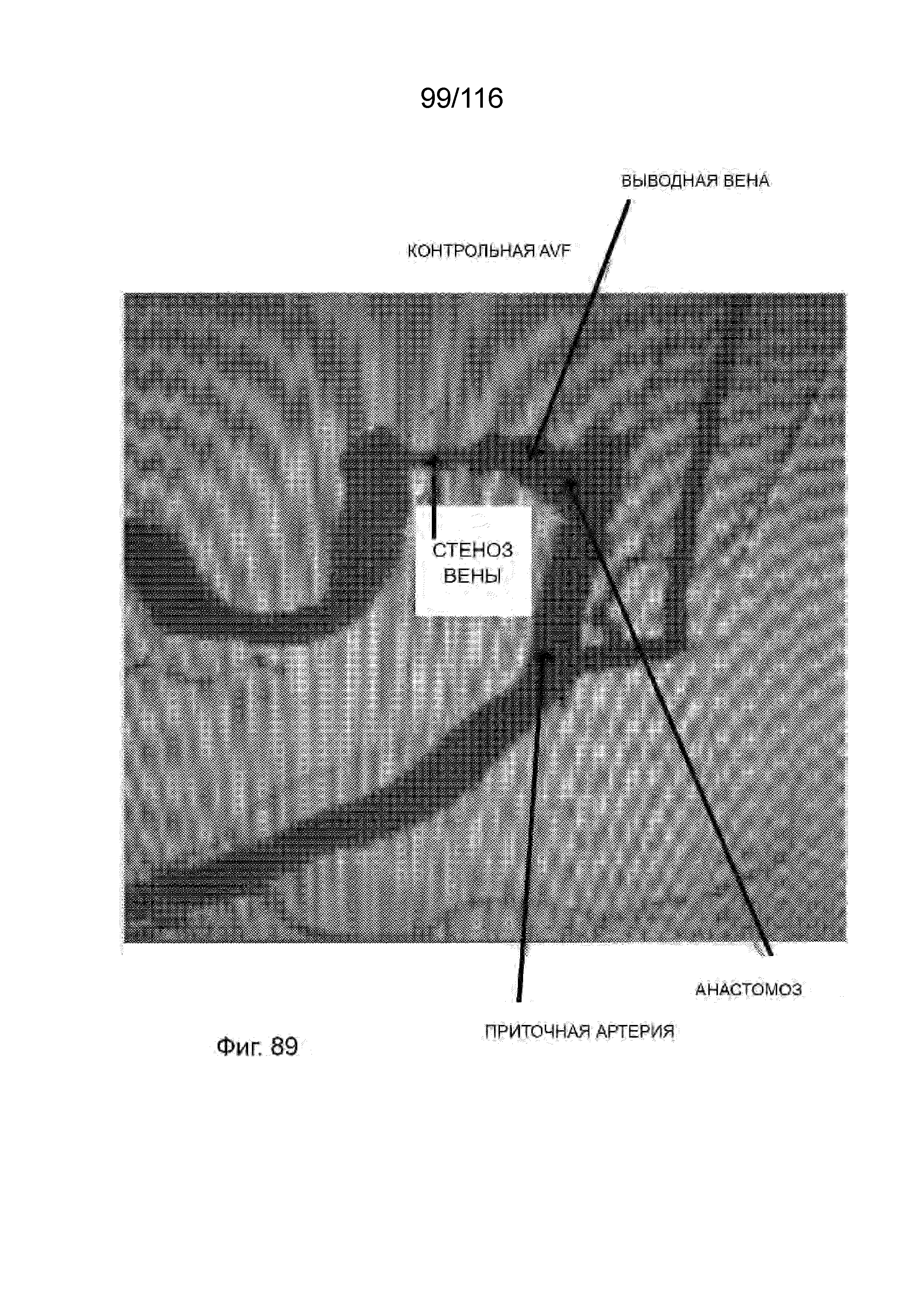
[174] На фиг. 88-89 приведены ангиограммы AVF, выполненные на овце, без предшествующего лечения с помощью системы AFE, изображающие стенозы выводящей вены с AVF.
[175] На фиг. 90 приведена ангиограмма AVF, выполненная на овце, с предшествующим лечением с помощью системы AFE, изображающая анастомоз крупной артерии с веной и выводящую вену AVF без стеноза.
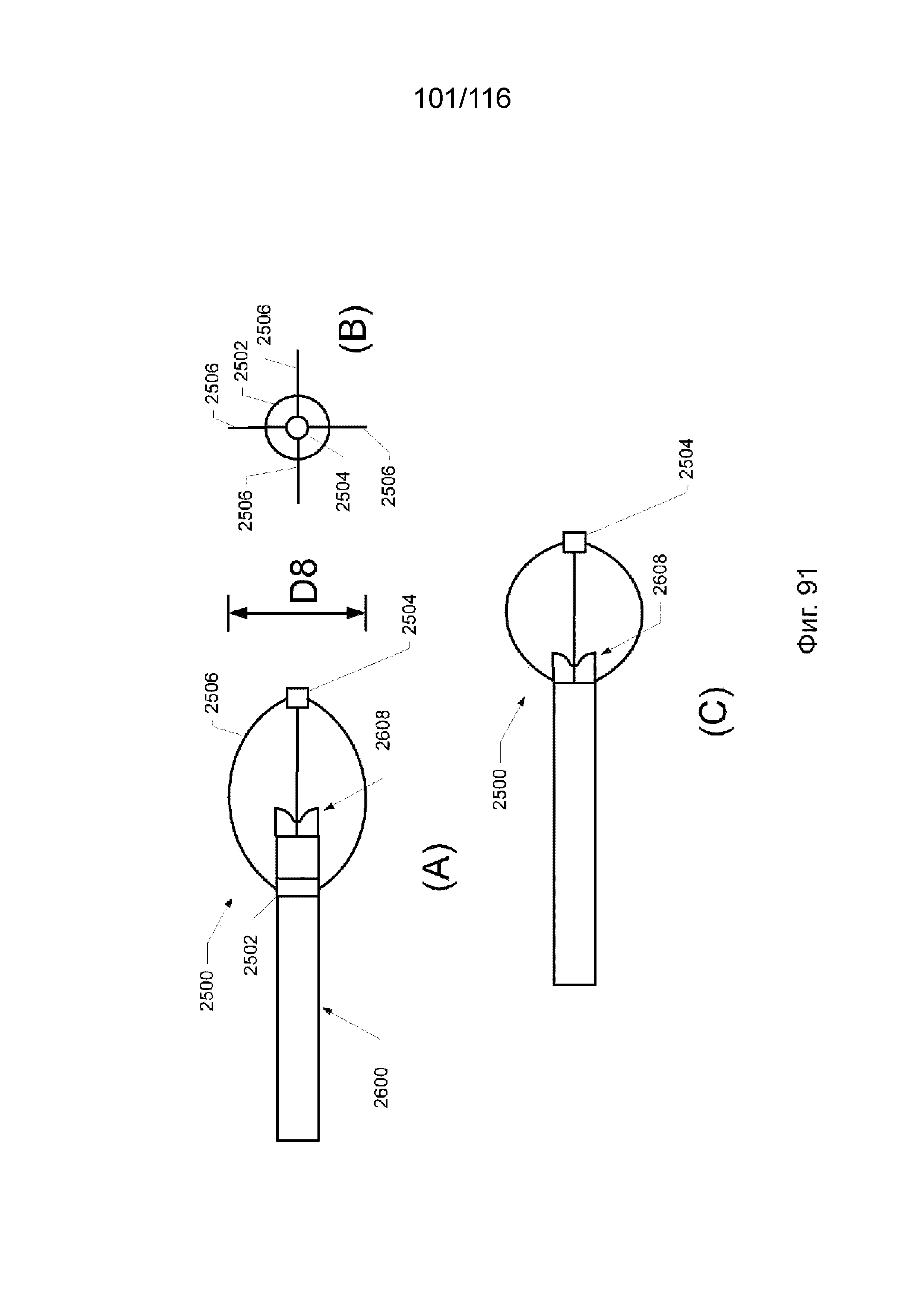
[176] На фиг. 91 представлен вид сверху и вид с торца приточного канала, содержащего наконечник приточного канала во взаимодействии с защитным каркасом наконечника, образующими узел наконечника приточного канала, согласно одному варианту реализации изобретения.
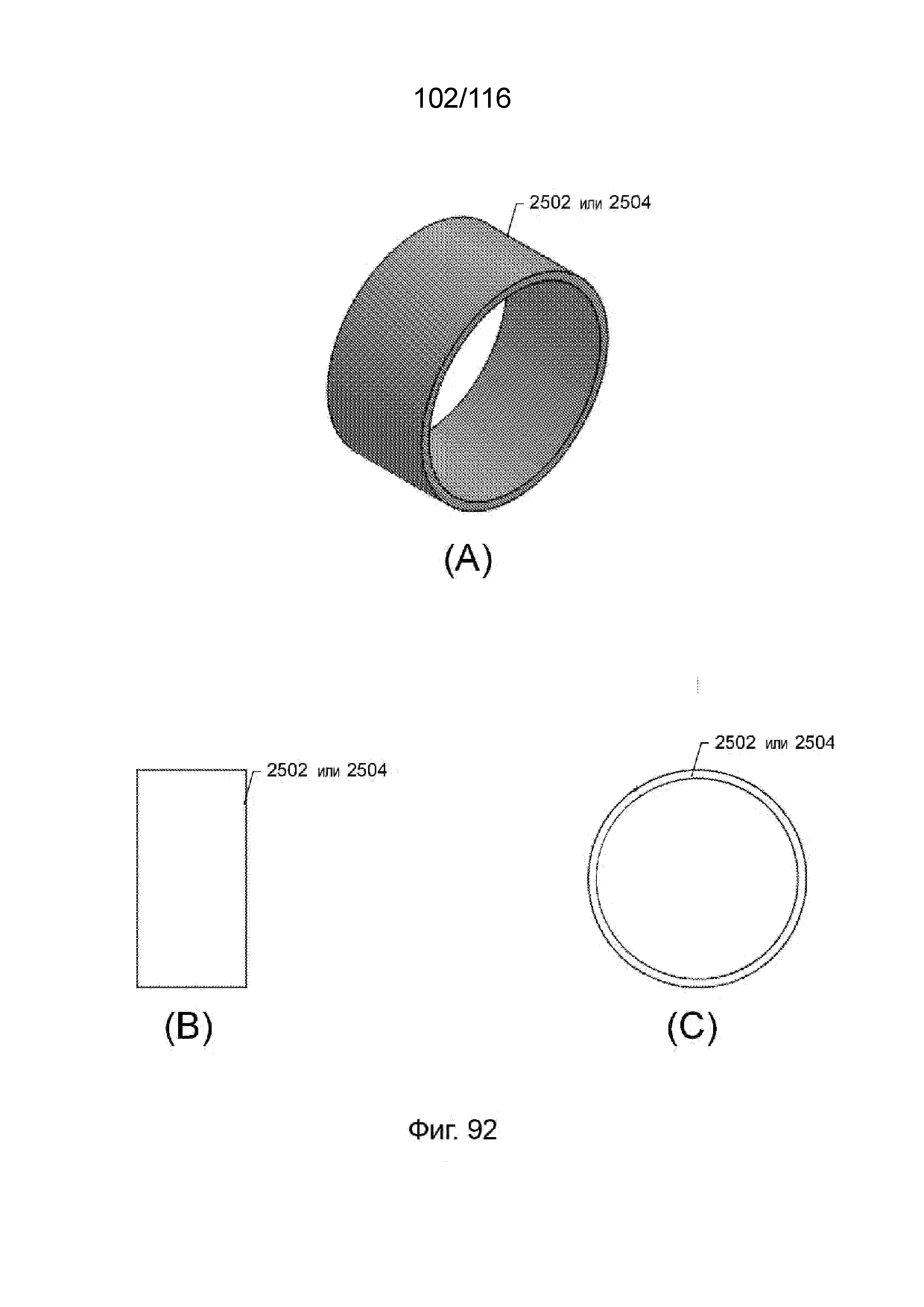
[177] На фиг. 92 А-С приведен вид в перспективе, сбоку и спереди кольцевого участка защитного каркаса наконечника согласно одному варианту реализации изобретения.
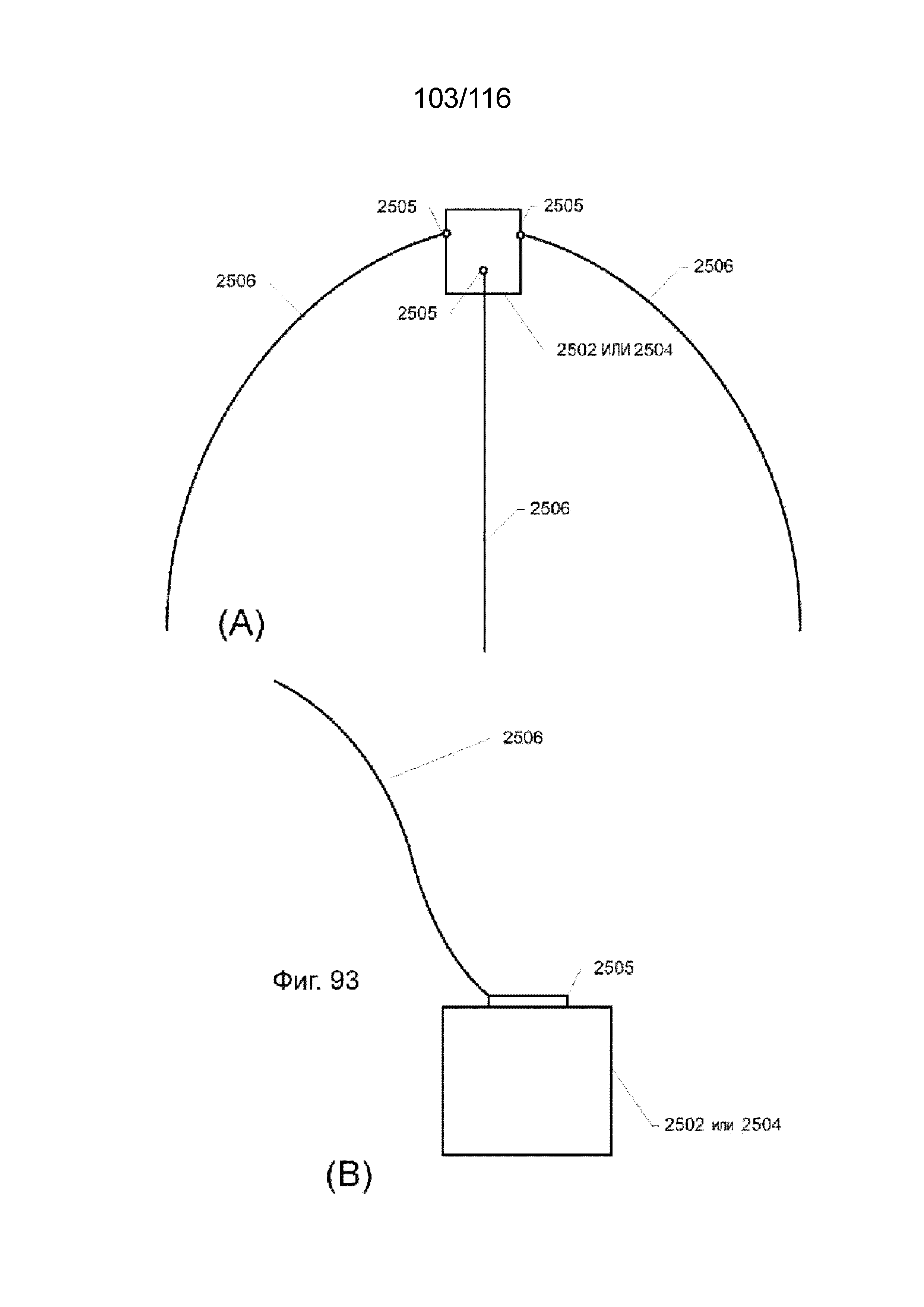
[178] На фиг. 93 А-В приведены в увеличенном масштабе виды точек крепления для участков ребристых участков защитного каркаса наконечника к кольцевым участкам защитного каркаса наконечника согласно одному варианту реализации изобретения.
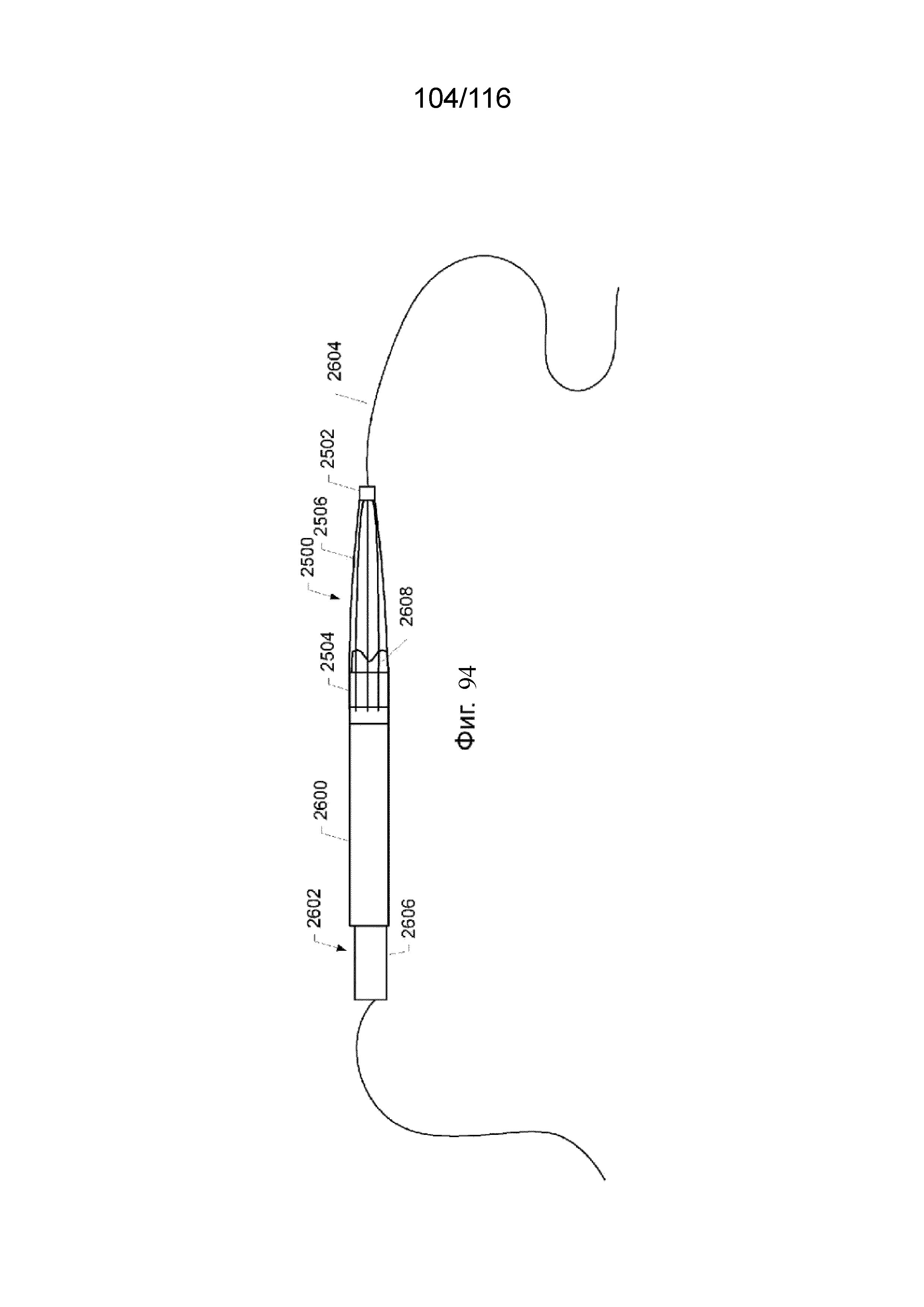
[179] На фиг. 94 приведен вид сверху приточного канала, изображающий наконечник приточного канала и защитный каркас наконечника, образующих узел наконечника приточного канала, и дополнительно изображающий уплотнитель вместо просвета приточного канала, который уменьшает профиль узла наконечника приточного канала, что облегчает введение приточного канала в сосуд благодаря изменению формы узла наконечника приточного канала до конфигурации подачи, согласно одному варианту реализации изобретения.
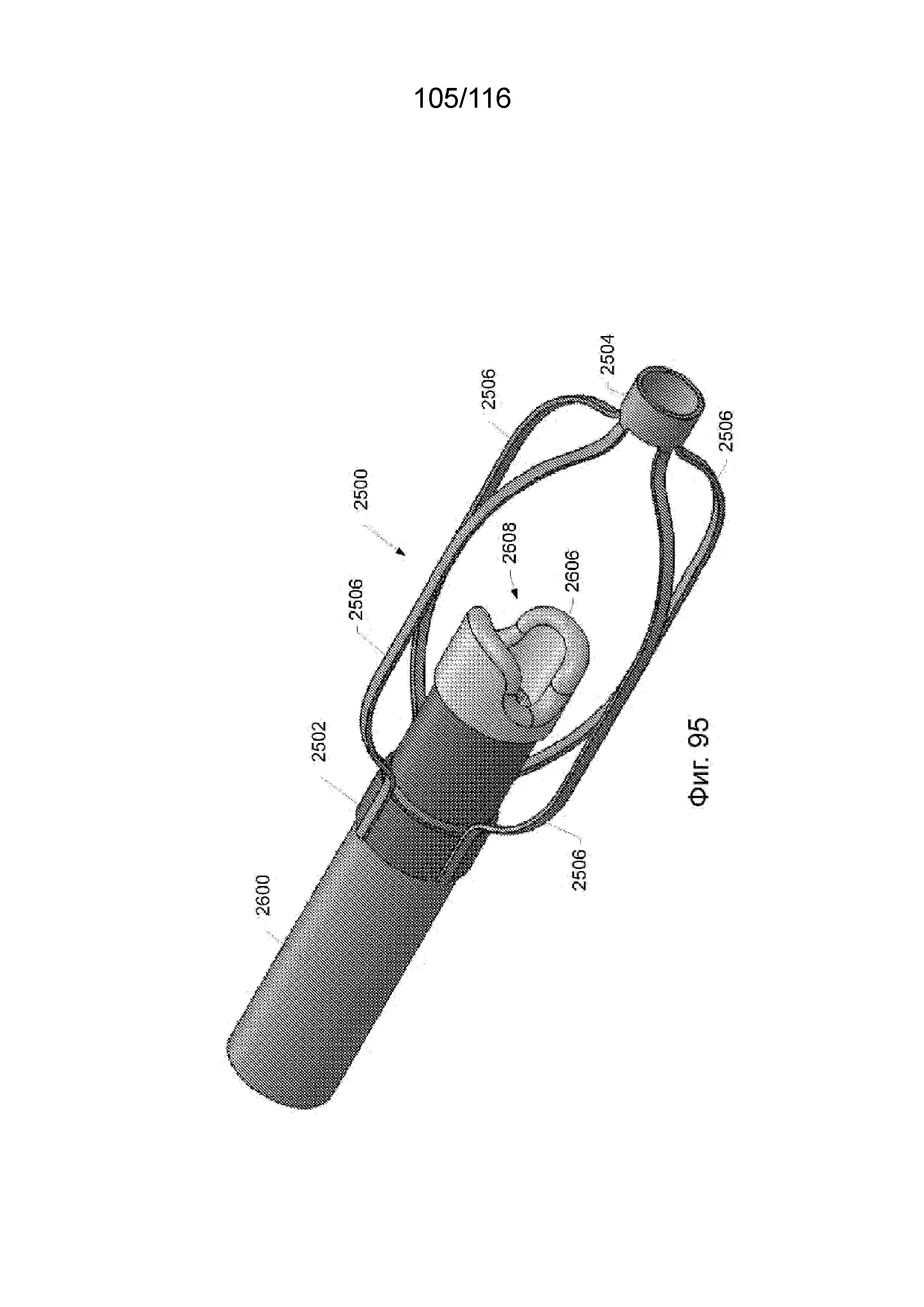
[180] На фиг. 95 приведен вид в перспективе узла наконечника приточного канала, изображающий наконечник приточного канала «утиный клюв» и защитный каркас наконечника во взаимодействии с каналом, согласно одному варианту реализации изобретения.
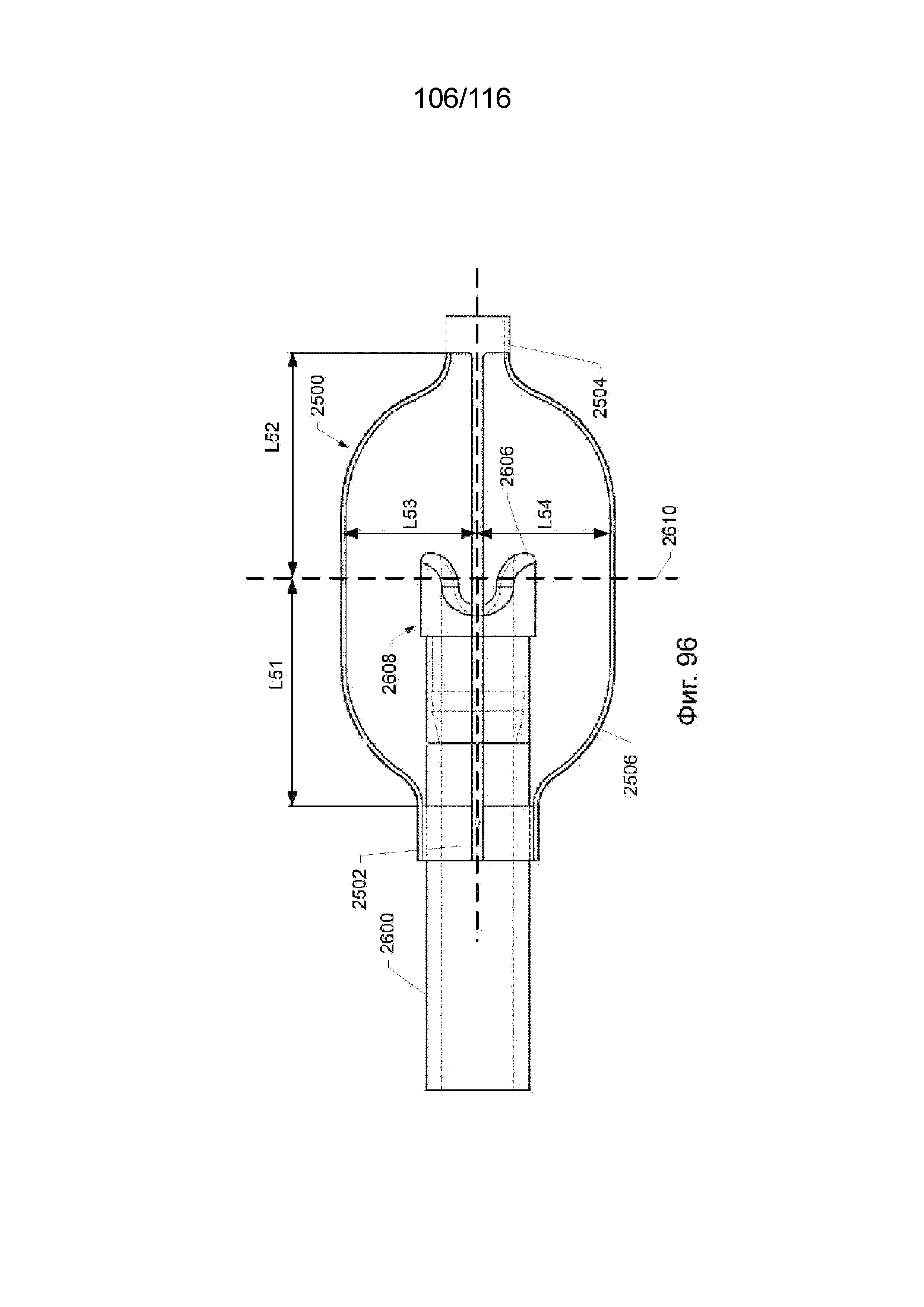
[181] На фиг. 96 приведен вид сверху узла наконечника приточного канала, показанного на фиг. 95.
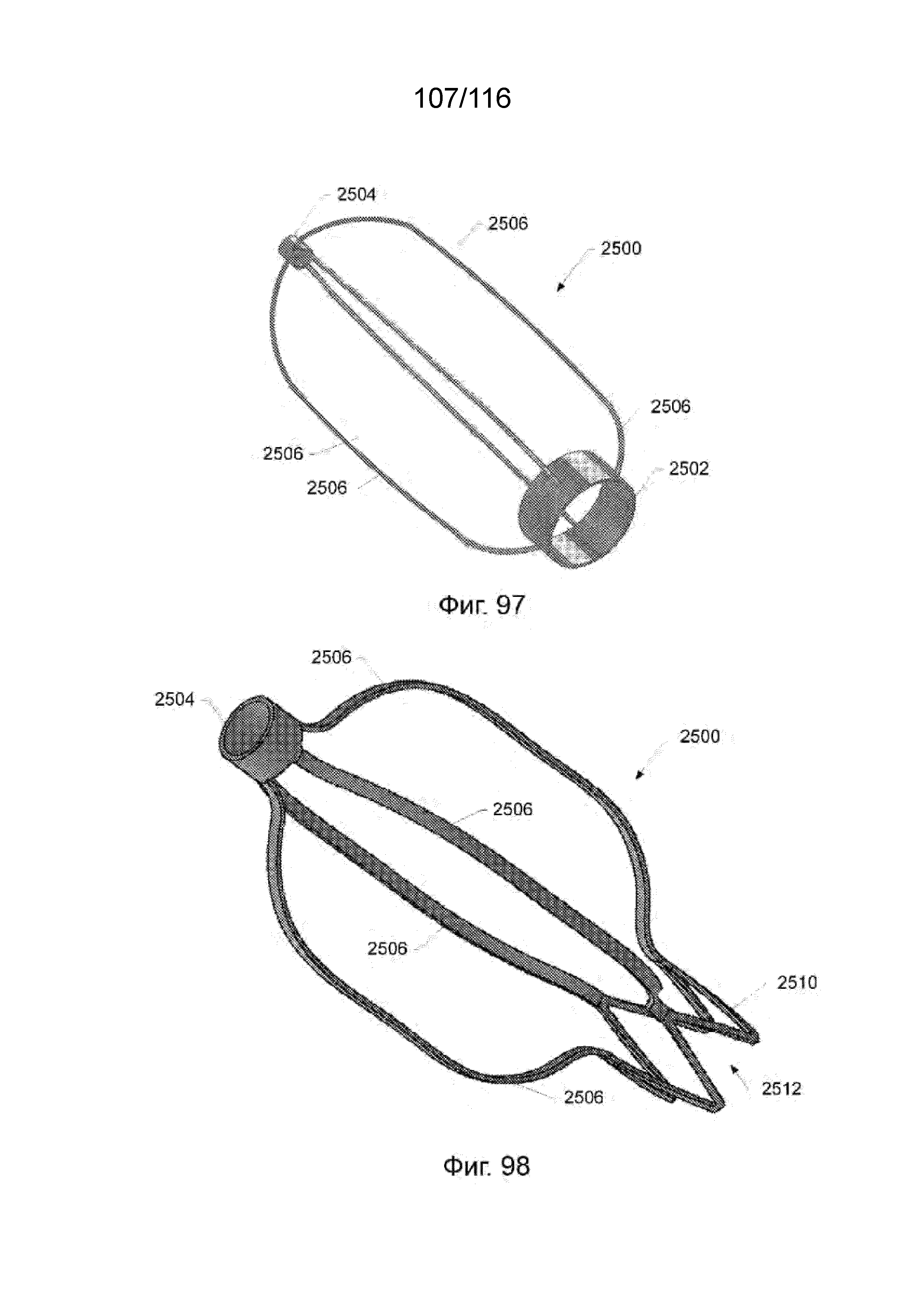
[182] На фиг. 97 приведен вид в перспективе защитного каркаса наконечника согласно одному варианту реализации изобретения.
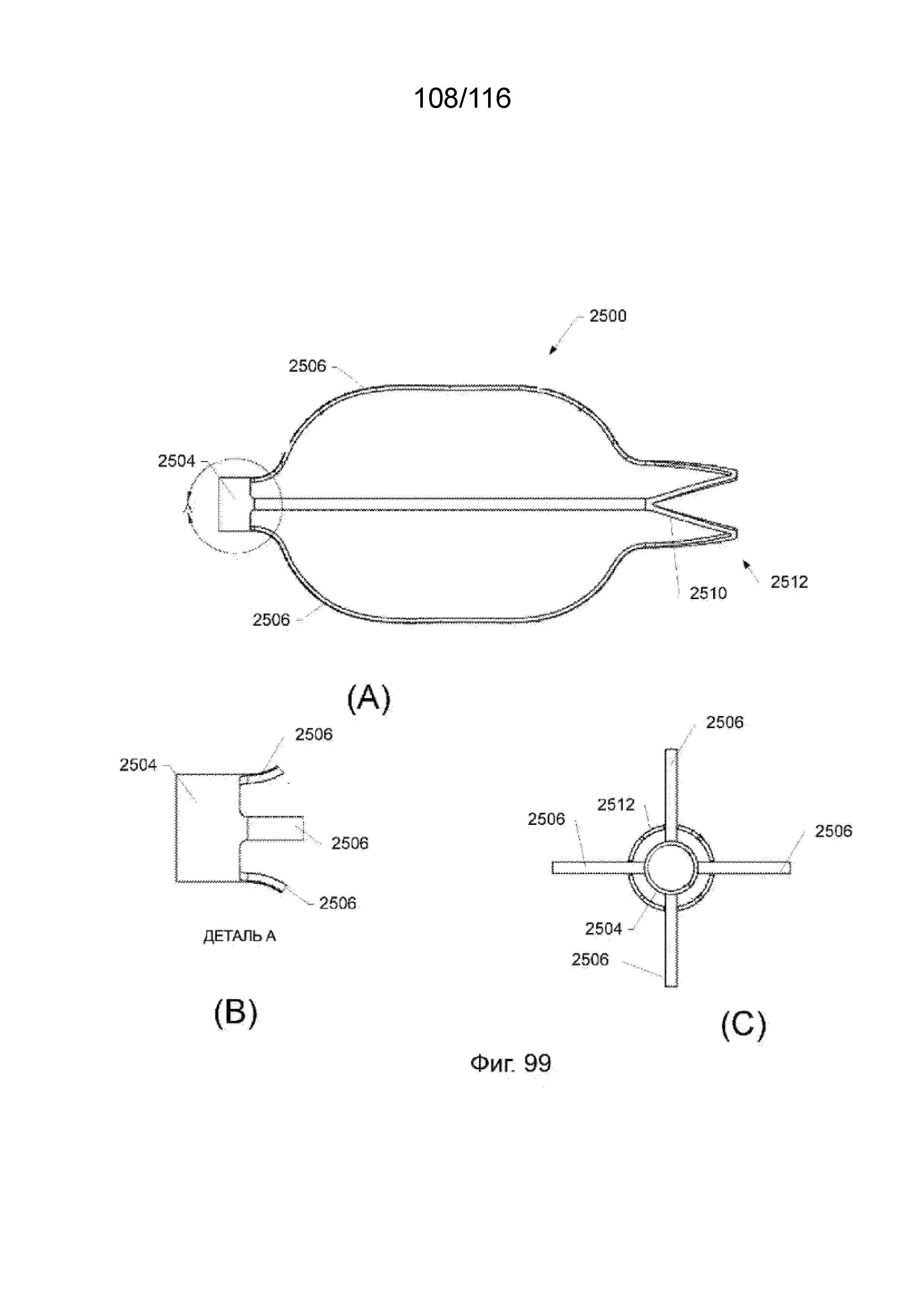
[183] На фиг. 98 приведен вид в перспективе защитного каркаса наконечника согласно другому варианту реализации изобретения.
[184] На фиг. 99 А-С приведен вид сверху, вид в увеличенном масштабе дальнего кольца и вид с торца защитного каркаса наконечника, показанного на фиг. 98.
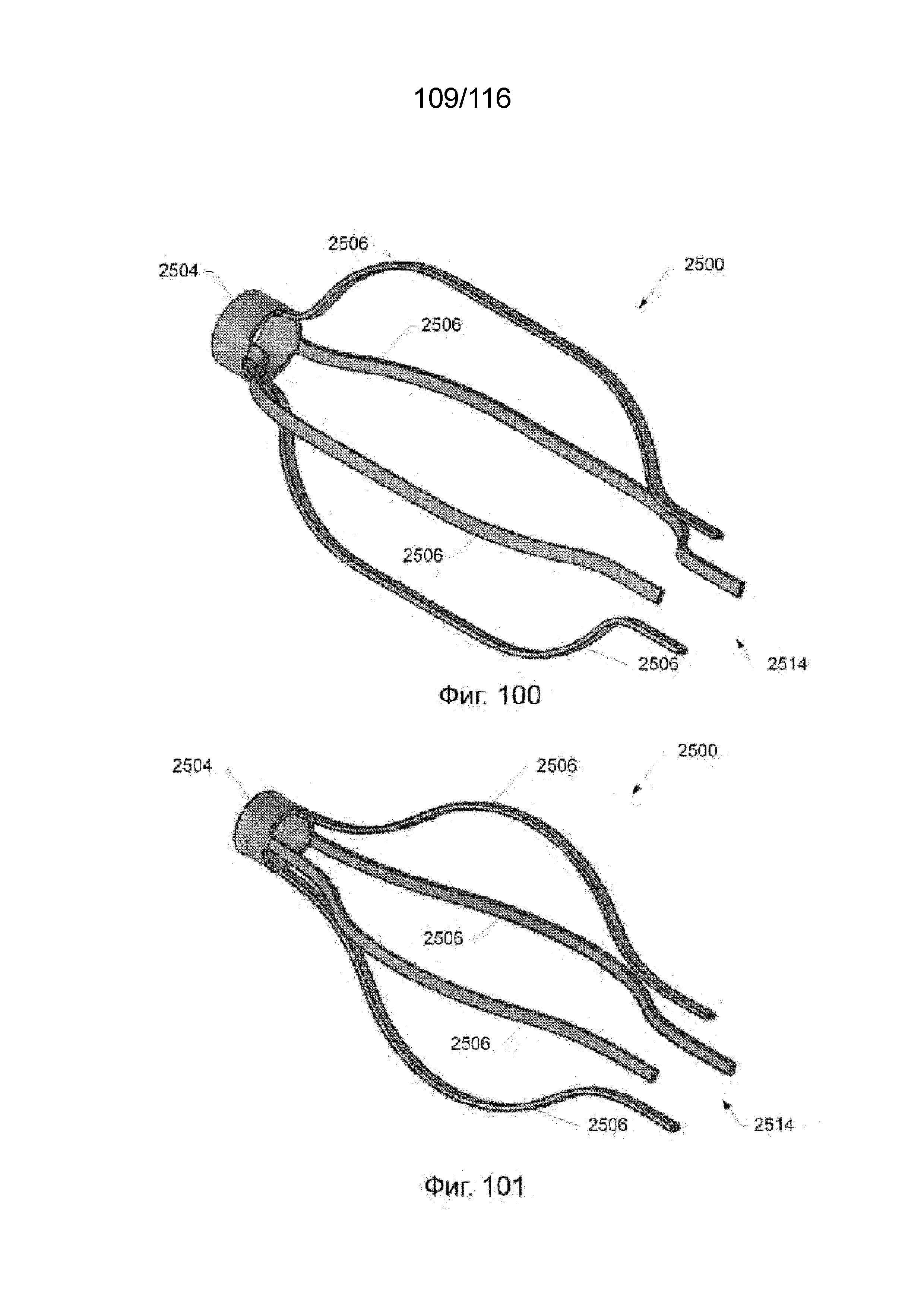
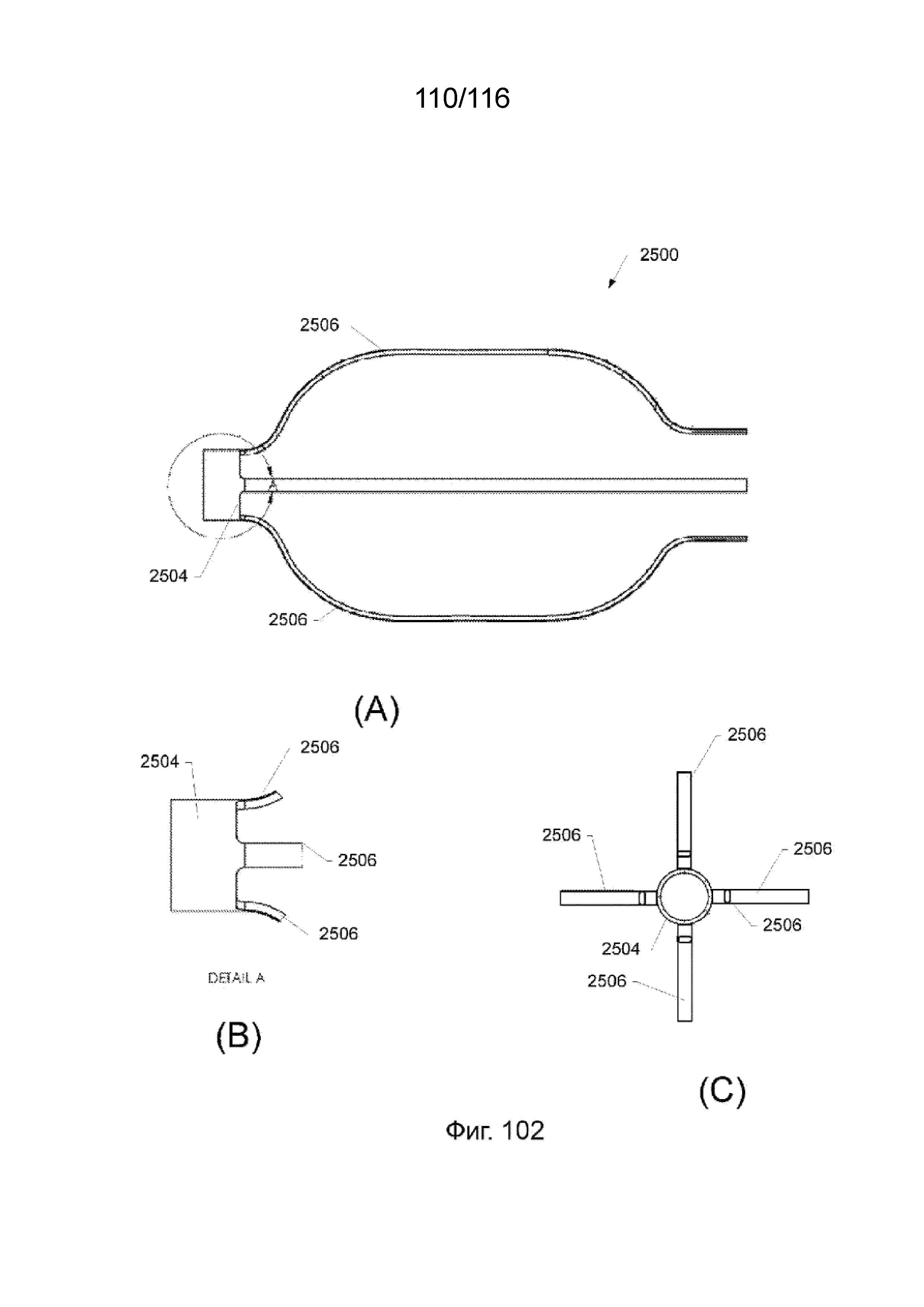
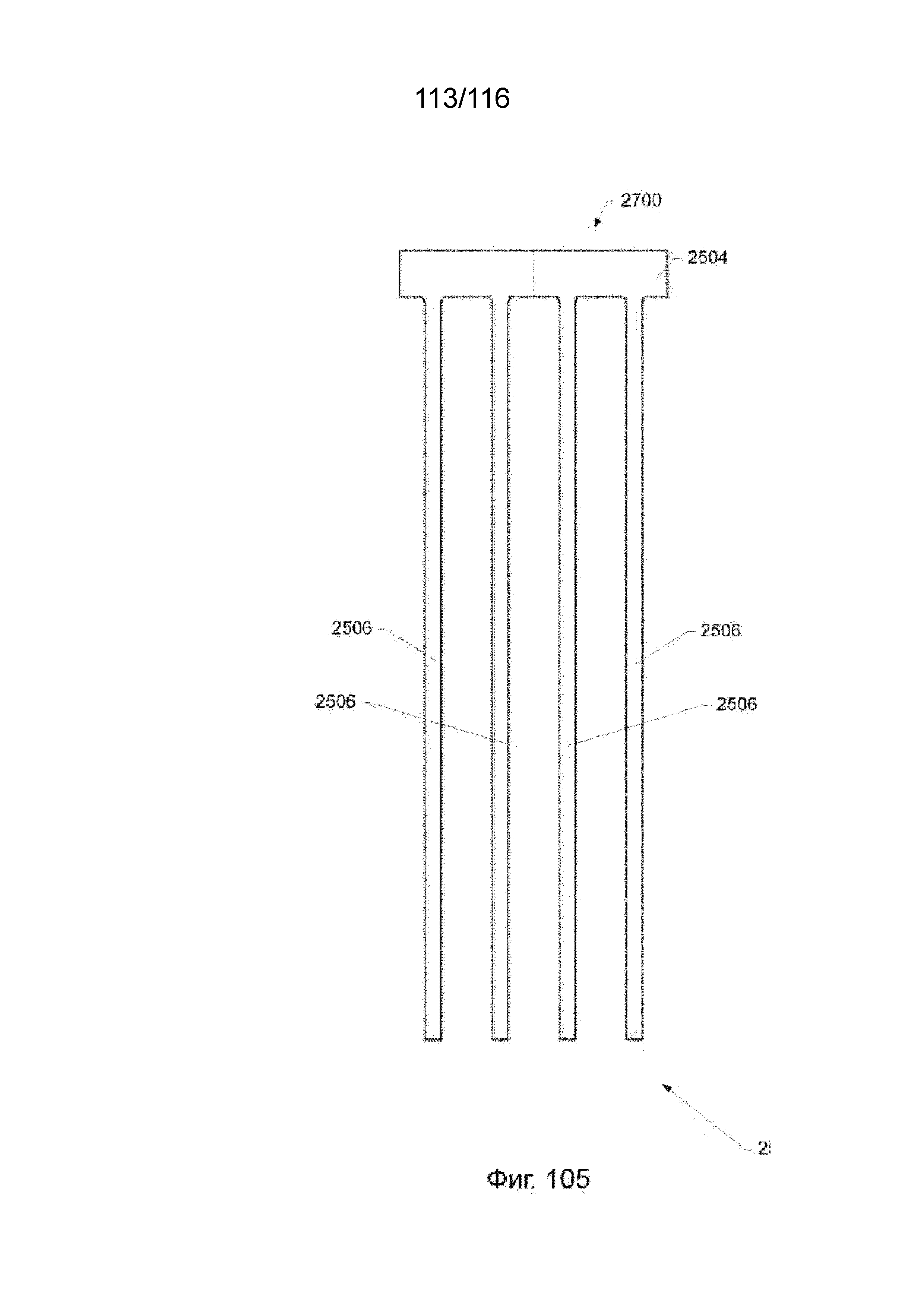
[185] На фиг. 100-101 приведены виды в перспективе дальнего кольца и компонентов ребер защитного каркаса наконечника согласно другим вариантам реализации изобретения.
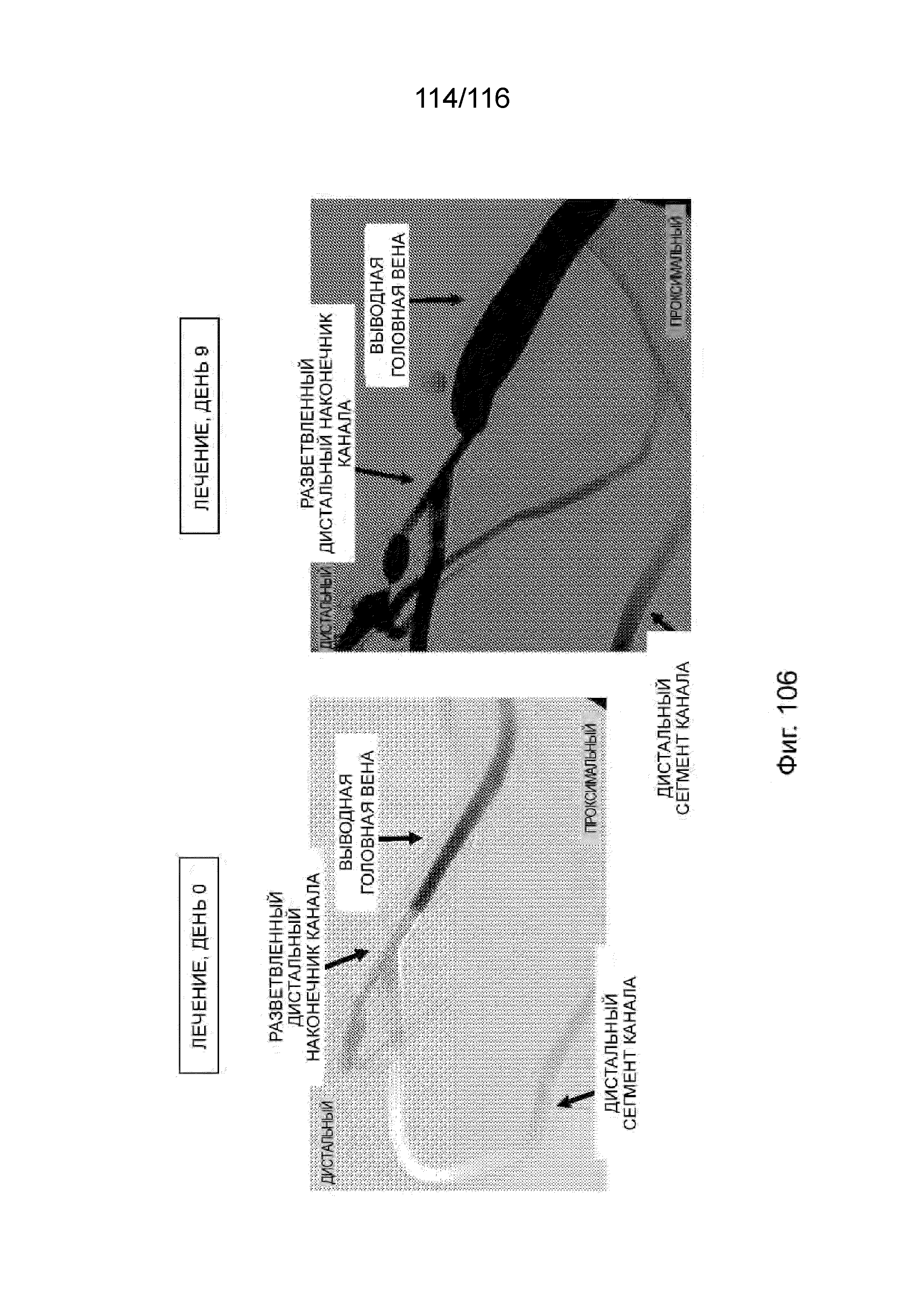
[186] На фиг. 102 А-С приведен вид сверху, вид в увеличенном масштабе и вид с торца дальнего кольца и ребристых участков защитного каркаса наконечника, показанного на фиг. 100.
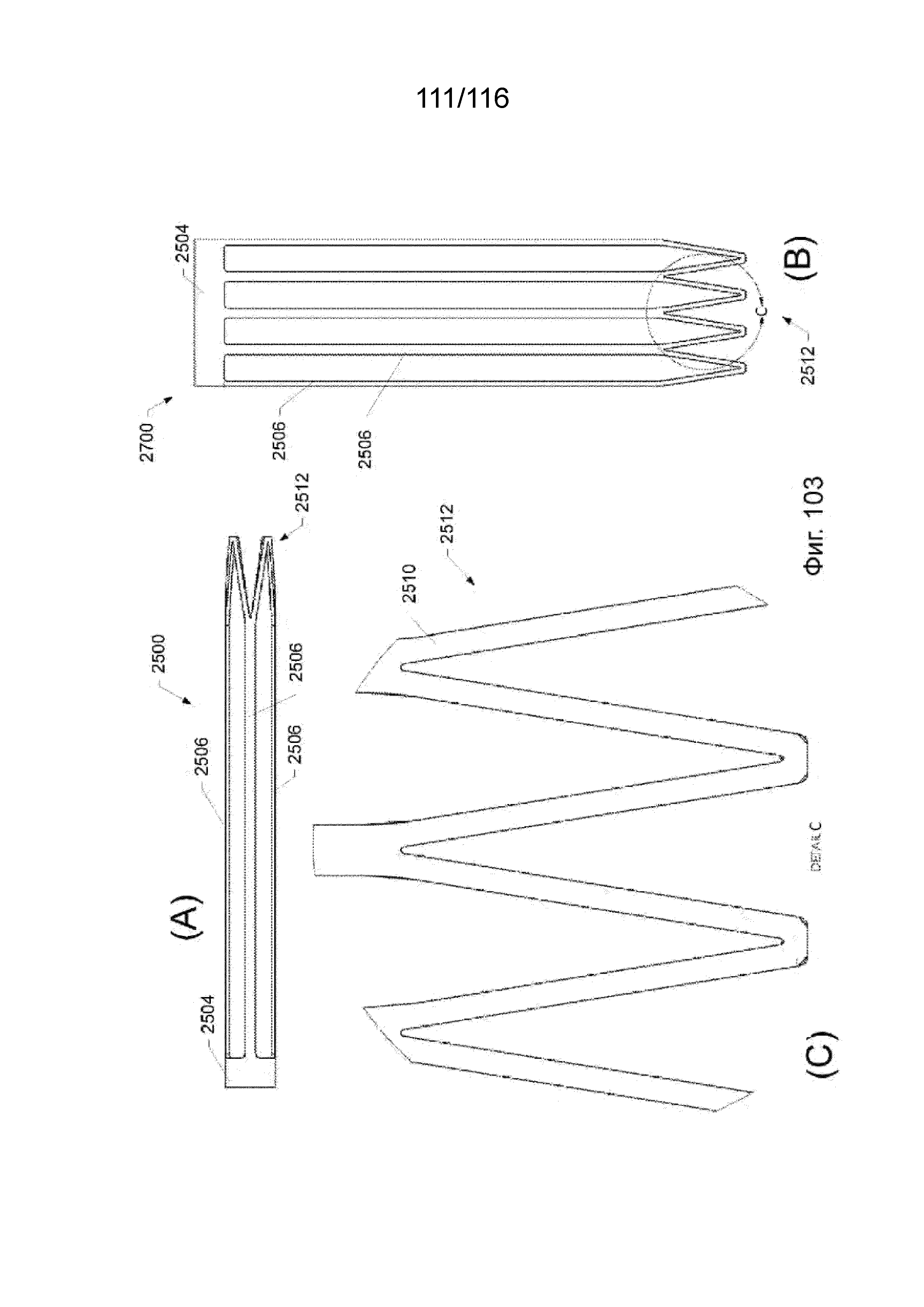
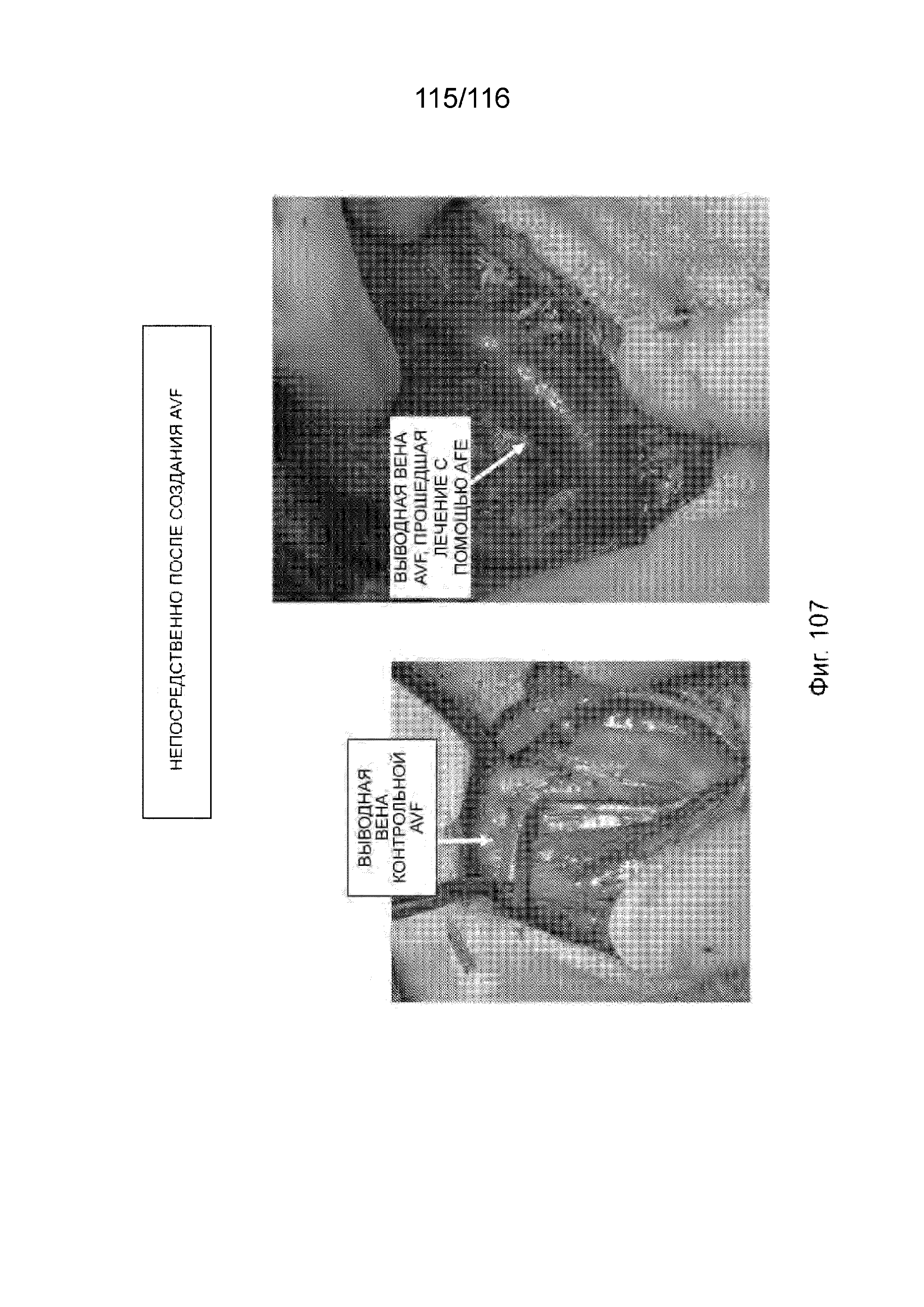
[187] На фиг. 103A приведен вид сбоку собранного защитного каркаса наконечника согласно одному варианту реализации изобретения.
[188] На фиг. 103B приведен вид сбоку разобранного защитного каркаса наконечника согласно одному варианту реализации изобретения.
[189] На фиг. 103C приведен вид сбоку ближнего участка защитного каркаса наконечника согласно одному варианту реализации изобретения.
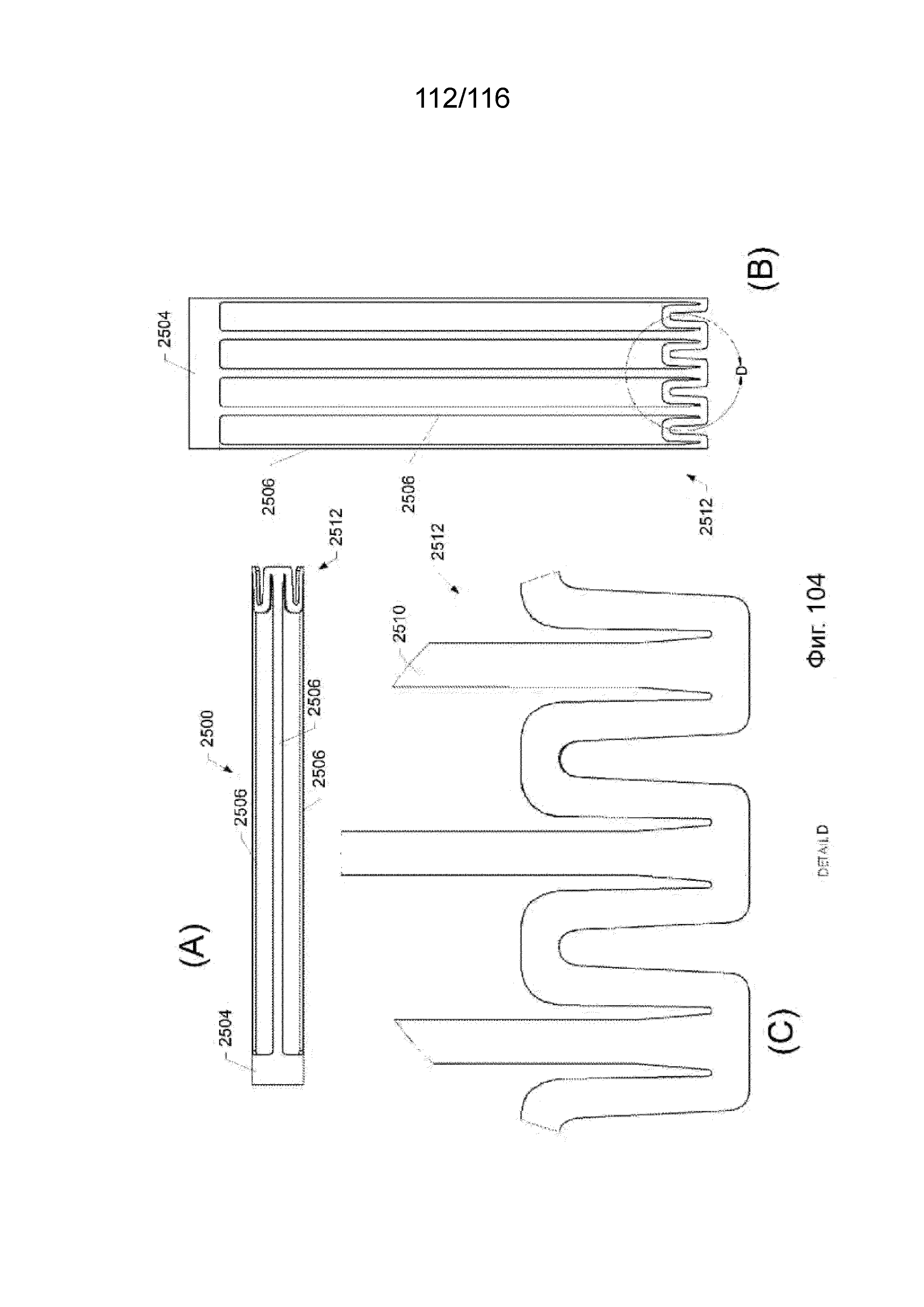
[190] На фиг. 104A приведен вид сбоку собранного защитного каркаса наконечника согласно одному варианту реализации изобретения.
[191] На фиг. 104B приведен вид сбоку разобранного защитного каркаса наконечника согласно одному варианту реализации изобретения.
[192] На фиг. 104C приведен вид сбоку ближнего участка защитного каркаса наконечника согласно одному варианту реализации изобретения.
[193] На фиг. 105 приведен вид сверху разобранного ребра и ближнего или дальнего кольцевых участков защитного каркаса наконечника согласно одному варианту реализации изобретения.
[194] На фиг. 106 приведены ангиограммы, изображающие в увеличенном масштабе вену с использованием системы, раскрытой в настоящем документе, с выводным каналом с Т-образным наконечником согласно одному варианту реализации изобретения.
[195] На фиг. 107 приведены интраоперационные фотографии, изображающие AVF, выполненные с предварительным лечением вены или без него, с использованием системы, раскрытой в настоящем документе, согласно одному варианту реализации изобретения, и изображающие результаты предварительного лечения в большей выводящей вене AVF по сравнению с веной, не прошедшей предварительного лечения.
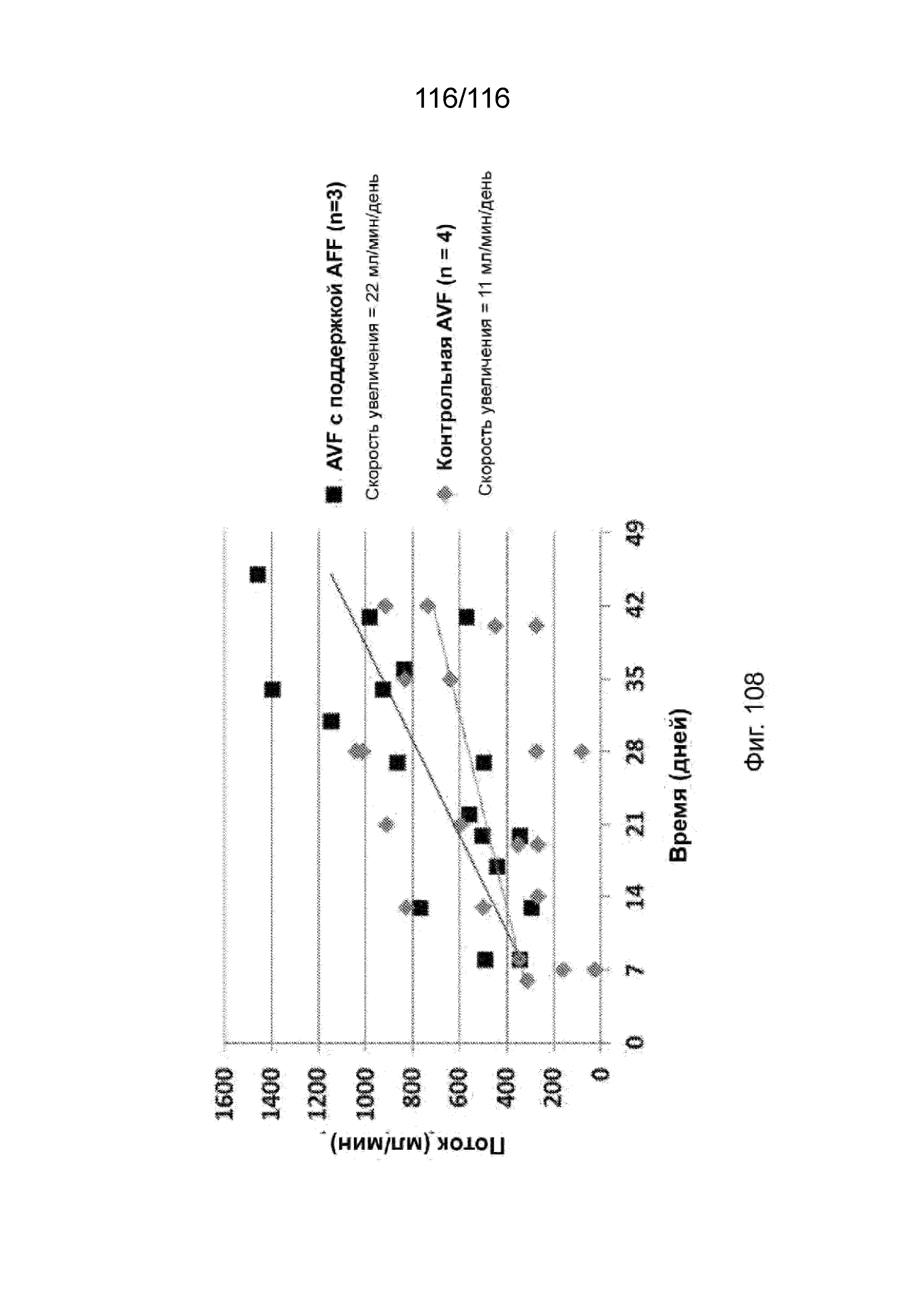
[196] На фиг. 108 приведен график, иллюстрирующий скорости потока в различные моменты времени через AVF, созданные с использованием одного варианта реализации устройств и способов, раскрытых в настоящем документе, и не прошедшие лечение AVF, изображающий, как правило, больший кровоток в AVF, прошедших предварительное лечение с помощью устройств и способов, раскрытых в настоящем документе, по сравнению с AVF, не прошедшими лечение.
[197] Какие-либо размеры, представленные на фигурах, приведены только в качестве примера, и необязательно ограничивают размер изображенных устройств.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
[198] Системы и компоненты согласно настоящей заявке относятся к перфузионной системе. В некоторых вариантах реализации изобретения настоящая заявка относится к перфузионному насосу, рассчитанному и выполненному с размерами, обеспечивающими выпуск крови в заданный сосуд или извлечение крови из заданного сосуда, таким образом и в течение такого периода времени, что диаметр заданного сосуда (т.е. вены или артерии) устойчиво увеличивается. Более конкретно, настоящая заявка относится к системе с ротационным перфузионным насосом, выполненной с возможностью устойчивого увеличения средней и/или максимальной скорости кровотока, а также среднего и/или максимального напряжения сдвига стенки (WSS) в выбранных сегментах вен или артерий в течение определенного периода времени, достаточного для устойчивого увеличения общего диаметра и диаметра просвета выбранных сегментов вен или артерий. Термин «устойчивое увеличение» или «устойчивое расширение» при использовании для описания расширения или увеличения общего диаметра и диаметра просвета артерии или вены используется в настоящем документе в том значении, что, даже если насос выключен, все еще может наблюдаться увеличение общего диаметра или диаметра просвета сосуда по сравнению с общим диаметром или диаметром просвета сосуда до периода перекачивания крови. То есть общий диаметр или диаметр просвета сосуда становится больше, независимо от давления, создаваемого насосом. Таким образом, перфузионная система может быть полезна для некоторых пациентов, включая пациентов с CKD, которым необходимо место сосудистого доступа для гемодиализа. Перфузионная система может содержать ротационный перфузионный насос, один или более каналов для переноса крови, систему управления и источник питания. Перфузионная система извлекает кровь из одного места в сосудистой системе и выводит кровь в другое место в сосудистой системе. Во время работы такая перфузионная система может устойчиво увеличивать среднюю и/или максимальную скорость кровотока, а также среднее и/или максимальное значение WSS в заданном кровеносном сосуде до уровня и в течение периода времени, достаточного для устойчивого увеличения диаметра и диаметра просвета заданного кровеносного сосуда. Система функционирует в конфигурациях, в которых кровь извлекается из заданного кровеносного сосуда или в конфигурациях, в которых кровь выводится в заданный кровеносный сосуд. Кроме того, система может быть использована одновременно для увеличения размера передающих и принимающих сосудов.
[199] В некоторых вариантах реализации изобретения настоящая заявка относится перфузионному насосу, рассчитанному и выполненному с размерами, обеспечивающими перенос венозной крови от нижней конечности к сердцу или к другому месту в венозной системе, из которого она может легче возвращаться к сердцу, уменьшение венозного кровяного давления в нижней конечности, а в некоторых случаях уменьшение опухания или увеличение скорости заживления сопутствующей кожной язвы. Более конкретно, настоящая заявка относится к системе с ротационным перфузионным насосом, выполненной с возможностью переноса венозной крови от нижней конечности к сердцу или к другому месту в венозной системе, из которого она может легче возвращаться к сердцу, для уменьшения венозного кровяного давления в нижней конечности, а в некоторых случаях для уменьшения опухания или увеличения скорости заживления сопутствующей кожной язвы. Таким образом, перфузионная система может быть полезна некоторым пациентам, в том числе с венозной гипертензией и/или венозным изъязвлением одной или обеих нижних конечностей, таким как пациенты с венозной непроходимостью нижних конечностей или пациенты с поврежденными или ослабленными венозными клапанами в одной или обеих нижних конечностях. Перфузионная система может содержать ротационный перфузионный насос, один или более каналов для переноса крови, систему управления и источник питания. Перфузионная система извлекает кровь из сегмента вены нижней конечности и выводит кровь в другое место в венозной системе. Места для возврата крови в венозном кровообращении включают яремную вену, подмышечную вену, подключичную вену, плечеголовную вену, полую верхнюю вену и правое предсердие.
[200] Необязательные каналы для переноса крови могут включать в себя приточный канал для переноса крови из места в сосудистой системе (например, передающая вена, передающая артерия или правое предсердие) в перфузионный насос и выводной канал для переноса крови из перфузионного насоса в определенное место в сосудистой системе (например, принимающая периферическая вена или артерия, или принимающее место, такое как правое предсердие). Перфузионная система также содержит систему управления. Предпочтительная система управления предназначена для сбора информации о рабочих параметрах и характеристиках перфузионной системы, и изменениях в сосудистой системе, таких как изменения диаметра передающей артерии, передающей вены, принимающей артерии или принимающей вены пациента. Перфузионная система в первую очередь выполнена с возможностью перекачивания достаточного количества крови, так что в сегменте кровеносного сосуда («заданный кровеносный сосуд» или «заданный сосуд») достигается необходимое среднее и/или максимальное значение WSS, и в течение достаточного периода времени, так что общий диаметр и диаметр просвета сегмента кровеносного сосуда постоянно или устойчиво увеличивается. Среднее значение WSS можно оценить с помощью вычислений с использованием измеренного, оцененного или предполагаемого диаметра сосуда и измеренной, оцененной или предполагаемой средней скорости кровотока через перфузионную систему.
[201] Диаметр кровеносных сосудов можно определить или оценить путем измерения диаметра пустоты в центре кровеносного сосуда. Для указанного применения это измерение или оценку называют «диаметр просвета». Диаметр кровеносных сосудов можно определить или оценить путем измерения диаметра таким образом, что включается пустота в центре кровеносного сосуда и стенка кровеносного сосуда. Для указанного применения это измерение или оценка называют «общий диаметр». Данное изобретение относится к одновременному и устойчивому увеличению общего диаметра и диаметра просвета периферической вены путем перемещения крови (предпочтительно с низкой пульсацией) в периферическую принимающую вену, тем самым увеличивая скорость кровотока в периферической принимающей вене и увеличивая WSS на эндотелии периферической принимающей вены. Предпочтительно насос активно выпускает кровь в периферическую принимающую вену, где перекачиваемая кровь уменьшает пульсацию, например, когда пульсовое давление ниже, чем давление крови в периферической артерии. Описаны системы и способы, в которых скорость кровотока в периферической принимающей вене и WSS на эндотелии периферической принимающей вены увеличивается при использовании насоса. Также описаны системы и способы, которые извлекают или «вытягивают» кровь, так что скорость кровотока и WSS увеличивается в передающем сосуде, либо в артерии, либо в вене.
[202] Перфузионные системы, описанные в настоящем документе, могут иметь характеристики, отличающиеся от других перфузионных систем. Например, описанная в настоящем документе перфузионная система может безопасно работать в широком рабочем диапазоне кровотока, например, от 50 мл/мин до 1500 мл/мин. В другом примере описанная в настоящем документе перфузионная система может быть изготовлена с низкой себестоимостью (COGS), например, в диапазоне от 1000 долларов США до 5000 долларов США. В еще одном примере описанная в настоящем документе перфузионная система предназначена для надежной работы вне стационара или клиники в течение промежуточного периода времени, например, от 1 часа до 7 дней, от 1 часа до 10 дней, от 1 часа до 14 дней, от 1 часа до 12 месяцев или от 7 дней до 12 месяцев. В некоторых примерах описанная в настоящем документе перфузионная система может иметь один, несколько или все эти факторы, поскольку одна или более перфузионных систем, описанных в настоящем документе, могут безопасно работать в широком рабочем диапазоне кровотока, включительно от 50 мл/мин до 1500 мл/мин, имеют низкую себестоимость от 1000 до 5000 долларов США, и могут надежно работать за пределами стационара или клиники в течение промежуточного периода времени, например, от 1 часа до 7 дней, от 1 часа до 10 дней, от 1 часа до 14 дней, от 1 часа до 12 месяцев или от 7 дней до 12 месяцев.
[203] Чтобы начать подробное описание перфузионного насоса 25 системы 10, ссылка сделана на фиг. 1, которая представляет вид в изометрии перфузионного насоса 25. В одном варианте реализации изобретения перфузионный насос 25 представляет собой миниатюрный центробежный насос, имеющий магнитный привод, в котором крыльчатка насоса приводится во вращение посредством вращающихся магнитных полей. Например, вращающиеся магнитные поля могут быть созданы путем возбуждения ряда электромагнитов в последовательности. В другом примере вращающиеся магнитные поля могут быть созданы за счет вращения ряда постоянных магнитов или возбуждаемых электромагнитов. В этом примере комбинация двигателя-ротора имеет вращающиеся магниты, которые функционально взаимодействуют и перемещают крыльчатку посредством магнитного взаимодействия. Насос может иметь диаметр, приблизительно равный диаметру монеты порядка, например, четверть доллара США, полдоллара США или большего диаметра, при необходимости. Например, насос 25 имеет диаметр в диапазоне примерно от 2,0 до 5,0 см в соответствии с некоторыми вариантами реализации изобретения. Как показано на фиг. 1, перфузионный насос 25 содержит корпус 105, впуск 110, выпуск 115 и кабель 120 питания. Кабель 120 питания соединяет перфузионный насос 25 с устройством 21 управления системы 14 управления и источником питания. Источник питания может быть частью устройства 21 управления или отдельным блоком. Кабель питания обеспечивает связь между устройством 21 управления и двигателем перфузионного насоса 25. Кабель также может быть использован для передачи энергии от источника питания к двигателю или насосу. Более конкретно, кабель 120 питания соединяет электрические компоненты магнитного привода внутри корпуса 105 с источником электрической энергии (например, аккумуляторной батареей).
[204] Впуск 110 выполнен с возможностью сообщения по текучей среде с приточным каналом 20 посредством соединителя (например, конца с кольцевыми зубцами, фланца и фиксирующего кольца). Впуск 110 обеспечивает канал текучей среды в зоне впуска (т. е. центре) крыльчатки насоса. Зона впуска крыльчатки может иметь разнообразные конструкции, при условии, что кровь на выпуске принимается со скоростью, большей, чем на впуске. Выпуск 115 выполнен с возможностью сообщения по текучей среде с приточным каналом 30 посредством соединителя, аналогичного впускному (например, конца с кольцевыми зубцами, фланца и фиксирующего кольца). Выпуск 115 обеспечивает канал текучей среды в зоне выпуска (т. е. периферии) крыльчатки насоса.
[205] Как показано на фиг. 2, на которой представлен вид в изометрии перфузионного насоса 25, показывающий его компоненты, заключенные в корпусе 105, указанном на фиг. 1, перфузионный насос 25 содержит впускную крышку 125, верхний опорный штифт 130, верхний корпус 135 крыльчатки, крыльчатку 140, ось 145 крыльчатки, узел 150 магнитов, корпус 155 магнитов, нижний опорный штифт 160, нижний корпус 165 крыльчатки, узел 170 электрических катушек и крышку 175 корпуса узла катушек. Каждый из элементов, впускная крышка 125 и верхний корпус 135 крыльчатки, содержит примерно половину впуска 110.
[206] Как показано на фиг. 3A и 3B которые представляют, соответственно, виды сбоку с частичным и полным разрезом перфузионного насоса 25 по линии 3-3 на фиг. 1, компоненты, упомянутые со ссылкой на фиг. 2, в основном, наложены друг на друга, образуя насос. Например, как можно понять из фиг. 2-3A, впускная крышка 125 и верхний корпус 135 крыльчатки, соответственно, содержат верхнюю, проходящую горизонтально, впускную часть 110A и нижнюю, проходящую горизонтально, впускную часть 110B. Как правило, впуск и выпуск противоположны друг другу и расположены в разных плоскостях. Когда впускная крышка 125 и верхний корпус 135 крыльчатки наложены друг на друга, они образуют впускной канал 180 текучей среды, проходящий через впуск 110 к впускному отверстию 185 крыльчатки. Впускная крышка 125 и верхний корпус 135 крыльчатки, соответственно, образуют приблизительно верхнюю половину и нижнюю половину канала 180. Канавка 190 под уплотнение выполнена в верхнем корпусе 135 крыльчатки, рядом с границей канала 180, и выполнена с возможностью установки упругого уплотнения по текучей среде для создания герметичного, непроницаемого для текучей среды уплотнения между впускной крышкой 125 и верхним корпусом 135 крыльчатки.
[207] На фиг. 4A и 4B приведены, соответственно, виды сбоку с частичным и полным разрезом перфузионного насоса 25 по линии 4-4 на фиг. 1. Как можно понять из фиг. 2, 4А и 4В, верхний корпус 135 крыльчатки и нижний корпус 165 крыльчатки, соответственно, содержат верхнюю, проходящую горизонтально, выпускную часть 115А и нижнюю, проходящую горизонтально, выпускную часть 115В. Когда верхний корпус 135 крыльчатки и нижний корпус 165 крыльчатки соединены друг с другом, они образуют выпускной канал 200 для текучей среды (то есть спиральный), ведущий из камеры 205 крыльчатки к выпуску 115. Верхний корпус 135 крыльчатки и нижний корпус 165 крыльчатки, соответственно, образуют приблизительно верхнюю половину и нижнюю половину канала 200. Канавка 211 под уплотнение выполнена в нижнем корпусе 165 крыльчатки, рядом с границей канала 200 и камерой 205 крыльчатки, и выполнена с возможностью установки упругого уплотнения по текучей среде для создания герметичного, непроницаемого для текучей среды уплотнения между верхним корпусом 135 крыльчатки и нижним корпусом 165 крыльчатки.
[208] Как показано на фиг. 2-4B, узел 150 магнитов крыльчатки представляет собой множество магнитов в виде кольца или диска. Магниты 150 расположены в объеме корпуса 155 магнитов и объеме крыльчатки 140. Корпус 155 магнитов установлен в крыльчатке 140. Корпус 155 магнитов и крыльчатка 140, соответственно, образуют верхнюю и нижнюю часть объема, в котором расположены магниты 150. Корпус 155 магнитов, магниты 150 и крыльчатка 140 соединены друг с другом в виде скрепленного цельного узла, который вращается как блок внутри камеры 205 крыльчатки. Могут быть использованы альтернативные конструкции, которые вызывают вращение крыльчатки.
[209] Как показано на фиг. 2-4B, узел 170 электрических катушек представляет собой множество электрических катушек 210, размещенных по круговой схеме на нижнем корпусе крыльчатки, и необязательно закрытых опорным диском 215. Узел 170 электрических катушек закреплен в камере 220 катушек, образованной в нижнем корпусе 165 крыльчатки, и закрыт крышкой 175 корпуса катушек. Внутренняя нижняя конструкция 225 отделяет камеру 205 крыльчатки от камеры 220 катушек. В одном варианте реализации изобретения камера 220 катушек также содержит одну или более пустот или промежутков, распорки 282 и ферромагнитную опорную пластину 284, как показано на фиг. 4C. Между магнитом 150 крыльчатки и опорной пластиной 284 создается сила магнитного притяжения, которая противодействует направленному вверх усилию, прилагаемому повышенным давлением крови, проходящей в зазоре 542 между нижней поверхностью крыльчатки 140 и нижним корпусом 165 крыльчатки, как показано на фиг. 4E, и понижает давление у впускного отверстия 185 камеры крыльчатки над крыльчаткой. Результирующий эффект заключается в разгрузке верхнего опорного штифта 130. В зависимости от положения опорной пластины 284 и скорости работы насоса 25, осевая нагрузка может быть разделена между верхним и нижним опорными штифтами 130 и 160, или может выдерживаться исключительно верхним опорным штифтом или нижним опорным штифтом. Например, усилие на верхнем опорном штифте 130 может быть меньше чем примерно 3 Н при рабочих скоростях примерно до 6000 об/мин. Аналогично, усилие на нижнем опорном штифте 160 может быть меньше, чем примерно 4 Н при рабочих скоростях примерно до 6000 об/мин. Напротив, в состоянии покоя (то есть 0 об/мин), осевое усилие, испытываемое при нижнем усилии, составляет по меньшей мере 0,1 Н и может составлять до 10 Н или больше.
[210] Был проведен ряд исследований для измерения нагрузки на верхнем и нижнем опорных штифтах 130 и 160 при различных скоростях насоса и ориентациях опорной пластины 284. Скорость, при которой нагрузка переносится с нижнего опорного штифта 160 на верхний опорный штифт 130, может быть настроена путем изменения расстояния между крыльчаткой 140 и опорной пластиной 284, например, посредством одной или более распорок 282. Аналогичным образом, нагрузка на верхний и нижний опорные штифты 130 и 160 при определенной скорости крыльчатки может быть настроена путем изменения расстояния между крыльчаткой 140 и опорной пластиной 284. Ферромагнитная опорная пластина 284 также работает для увеличения производительности двигателя и крутящего момента двигателя, поскольку опорная пластина вызывает магнитный поток для более глубокого проникновения в катушки 210, тем самым обеспечивая более высокую плотность осевого потока.
[211] Один вариант реализации опорной пластины 284 показан на фиг. 4D. Как показано, опорная пластина 284 обычно имеет форму диска и выполнена из ферромагнитного металла или сплава. В одном варианте реализации изобретения опорная пластина 284 выполнена из магнитомягкого железо-кобальт-ванадиевого сплава, такого как Hiperco® 50, производства Carpenter Technology. Опорная пластина 284 имеет толщину в диапазоне примерно от 0,04 мм до 0,07 мм и наружный диаметр в диапазоне примерно от 20 мм до 40 мм. В предпочтительном варианте реализации изобретения опорная пластина 284 представляет собой сплошной диск, имеющий толщину примерно 0,53 мм и наружный диаметр примерно 31 мм. Опорная панель 284 может содержать центральное отверстие 288 для размещения конструктивных элементов насоса 25; однако в других вариантах реализации изобретения может быть использован сплошной диск без отверстия 288. На фиг.4Е показан вариант реализации насоса 25. Как показано, в одном варианте реализации изобретения опорная пластина 284 расположена на расстоянии «D» от магнита 150. В одном варианте реализации изобретения расстояние «D» находится в диапазоне примерно от 4 до 8 мм. В предпочтительном варианте реализации изобретения расстояние «D» равно примерно 6 мм. В других вариантах реализации изобретения опорная пластина 284 может быть расположена ближе или дальше от магнитов 150 для достижения требуемого зазора 540 между верхней поверхностью крыльчатки 140 и верхним корпусом 135 крыльчатки и зазора 542 между нижней частью крыльчатки и нижним корпусом 165 крыльчатки.
[212] На фиг.4F показана крыльчатка 140 и опорная пластина 284, и график, изображающий экспериментальные результаты нагрузки, измеренной как на верхней оси, так и на нижней оси, в зависимости от положения опорной пластины 284 относительно магнитов 150. Эффективное положение опорной пластины 284 настраивается на основе различных вариантов размещения распорок 282 и толщины опорной пластины 284. Как показано, предпочтительный вариант реализации изобретения включает одиночную опорную пластину 284, расположенную на расстоянии примерно 6 мм от двигателей с использованием распорки 282 на 1,5 мм. В зависимости от требуемой или допустимой нагрузки на верхнюю и нижнюю опоры, могут использоваться другие комбинации опорной пластины и распорки. Аналогично, на фиг. 4H приведен график, изображающий осевую нагрузку на верхней опоре в зависимости от верхнего зазора 540 между крыльчаткой 140 и верхним корпусом 135, при насосе 25, работающем с частотой вращения примерно 4000 об/мин.
[213] Электрический кабель 120 (см. фиг. 1) проходит через канал 230 в нижнем корпусе 165 крыльчатки в камеру 220 катушек и к катушкам 210. Электрическая мощность, подаваемая на катушки 210 через электрический кабель 120, генерирует вращающиеся магнитные поля, которые воздействуют на магниты 150, чтобы вызвать вращение магнитов и крыльчатки 140, соединенной с магнитами. Вращение крыльчатки вызывает воздействие лопастей 235 крыльчатки на текучую среду (например, кровь), имеющуюся в камере крыльчатки, в результате чего импульс переносится в текучую среду, которая извлекается по мере увеличения давления в выпускном канале 200 для текучей среды. Таким образом, текучая среда втягивается во впуск 110 под низким давлением и выпускается из выпуска 115 под более высоким давлением.
[214] Как показано на фиг. 3A-4B, осью вращения для крыльчатки 140, магнитов 150 и корпуса 155 служит ось 145 крыльчатки. Как показано на фиг. 5A-B, ось 145 крыльчатки опирается с возможностью поворота (т.е. сдерживается по всем степеням свободы, за исключением вращения вокруг одной оси) посредством верхнего опорного штифта 130 и нижнего опорного штифта 160. Верхний опорный штифт 130 установлен и закреплен в цилиндрическом углублении 240 во впускной крышке 125, тогда как нижний опорный штифт 160 установлен и закреплен в цилиндрическом углублении 245 в нижнем корпусе 165 крыльчатки. Ось 145 крыльчатки проходит через центральное цилиндрическое отверстие 250 в крыльчатке 140 и закреплена в нем.
[215] В одном варианте реализации узла крыльчатки ось 145 крыльчатки, верхний опорный штифт 130 и нижний опорный штифт 160 выполнены из окиси алюминия (Al2O3) высокой чистоты, такой как CoorsTek® AD-998. В другом варианте реализации узла крыльчатки ось 145 крыльчатки, верхний опорный штифт 130 и нижний опорный штифт 160 выполнены из окиси алюминия, упрочненной нитевидными кристаллами карбида кремния, например Greenleaf® WG-300. В еще одном варианте реализации изобретения ось 145 крыльчатки, верхний опорный штифт 130 и нижний опорный штифт 160 выполнены из окиси алюминия, упрочненной двуокисью циркония (alumina toughened zirconia, ATZ), что может обеспечить опору, более устойчивую к износу, чем опоры, выполненные из окиси алюминия. Выполнение опорных компонентов из ATZ может также давать более гладкую поверхность, чем опорные компоненты, выполненные из окиси алюминия. Во всех трех вариантах реализации изобретения размеры оси 145 крыльчатки, верхний опорный штифт 130 и нижний опорный штифт 160 предназначены для ограничения контактных напряжений до допустимых уровней для окиси алюминия высокой чистоты, окиси алюминия, упрочненной карбидом кремния, или ATZ, соответственно, с учетом максимальных нагрузок, создаваемых гидростатическими силами и ударными нагрузками. В другом варианте реализации изобретения узла крыльчатки ось 145 крыльчатки выполнена из окиси алюминия, упрочненной нитевидными кристаллами карбида кремния, например Greenleaf® WG-300 или из окиси алюминия высокой чистоты, например CoorsTek® AD-998, тогда как верхний опорный штифт 130 и нижний опорный штифт 160 или оба из них выполнены из полиэтилена сверхвысокой молекулярной массы. В некоторых вариантах реализации изобретения частично или полностью верхний опорный штифт 130 и нижний опорный штифт 160 могут быть выполнены из полиэтилена. Кроме того, геометрия каждого компонента узла крыльчатки была выбрана таким образом, чтобы ограничивать усталость и износ, чтобы удовлетворить требованиям безопасности и долговечности системы 10. Был проведен ряд исследований, чтобы проиллюстрировать превосходную износостойкость ATZ в течение экспериментального срока службы насоса 25, что приводит к уменьшению изменений общей высоты пакета опоры по сравнению с опорными системами, выполненными из окиси алюминия и полиэтилена.
[216] Как показано на фиг. 6А-7В, ось крыльчатки содержит верхнюю полусферическую выпуклую опорную поверхность 255 и нижнюю полусферическую выпуклую опорную поверхность 260. Как показано на фиг. 6А, 6В и 8А, один вариант реализации оси крыльчатки имеет общую длину L1 примерно 10,15 мм плюс-минус 0,05 мм и диаметр D1 оси примерно 2 мм, плюс-минус примерно 0,01 мм. Верхняя опорная поверхность 255 имеет радиус R1 примерно 0,61 мм, плюс-минус 0,02 мм и продолжается до длины L2 за соседнюю кромку 265 примерно на 0,55 мм плюс-минус 0,02 мм. Нижняя опорная поверхность 260 имеет радиус R2 примерно 0,31 мм, плюс-минус 0,02 мм и продолжается до длины L21 за соседнюю кромку 265 примерно на 0,55 мм плюс-минус 0,02 мм. Аналогично, альтернативный вариант реализации оси 145 крыльчатки, как показано на фиг 7A, 7B и 8B, имеет общую длину L1 примерно 10,15 мм плюс-минус 0,05 мм и диаметр D1 оси примерно 2 мм, плюс-минус примерно 0,01 мм. Верхняя опорная поверхность 255 имеет радиус R1 примерно 0,31 мм, плюс-минус 0,02 мм и продолжается до длины L2 за соседнюю кромку 265 примерно на 0,55 мм плюс-минус 0,02 мм. Нижняя опорная поверхность 260 имеет радиус R2 примерно 0,31 мм, плюс-минус 0,02 мм и продолжается до длины L21 за соседнюю кромку 265 примерно на 0,55 мм плюс-минус 0,02 мм. В зависимости от требований к размеру и производительности насоса, могут быть использованы другие размеры и величины. Размеры таковы, что полученный насос может быть использован в пациенте для увеличения диаметра сосуда.
[217] Аналогично, альтернативный вариант реализации оси 145 крыльчатки, как показано на фиг 7A, 7B и 8B, имеет общую длину L1 примерно 10,15 мм плюс-минус 0,05 мм и диаметр D1 оси примерно 2 мм, плюс-минус примерно 0,01 мм. Верхняя опорная поверхность 255 имеет радиус R1 примерно 0,31 мм, плюс-минус 0,02 мм и продолжается до длины L2 за соседнюю кромку 265 примерно на 0,55 мм плюс-минус 0,02 мм. Нижняя опорная поверхность 260 имеет радиус R2 примерно 0,31 мм, плюс-минус 0,02 мм и продолжается до длины L21 за соседнюю кромку 265 примерно на 0,55 мм плюс-минус 0,02 мм.
[218] Как можно понять по фиг. 8C-8G, еще один вариант реализации оси 145 крыльчатки содержит верхнюю полусферическую выпуклую опорную поверхность 255 и нижнюю полусферическую выпуклую опорную поверхность 260. На фиг. 8D и 8Е изображены виды сверху верхней полусферической выпуклой опорной поверхности 255 и нижней полусферической выпуклой опорной поверхности 260, соответственно, если смотреть вдоль продольной оси, являющейся осью вращения крыльчатки140. На фиг. 8F и 8G приведены виды в увеличенном масштабе нижней полусферической выпуклой опорной поверхности 260 и верхней полусферической выпуклой опорной поверхности 255, соответственно. Как показано на фиг. 8C, один вариант реализации оси крыльчатки имеет общую длину L1 примерно 10,45 мм плюс-минус 0,05 мм и диаметр D1 оси примерно 1,5 мм, плюс-минус примерно 0,005 мм. Верхняя опорная поверхность 255 имеет радиус R1 примерно 0,6 мм, плюс-минус 0,02 мм и продолжается до длины L2 за соседнюю точку 266 перехода в конус примерно на 1,4 мм плюс-минус 0,10 мм. Точка 266 перехода в конус имеет радиус R3 примерно 0,20 мм плюс-минус 0,02 мм, при этом поверхность 267 оси крыльчатки сужается внутрь вдоль длины L2 под углом СА1 конуса примерно 20 градусов. Нижняя опорная поверхность 260 имеет радиус R2 примерно 0,60 мм, плюс-минус 0,02 мм и продолжается до длины L21 за соседнюю кромку 268 примерно на 0,5 мм плюс-минус 0,10 мм. Точка 268 перехода в конус имеет радиус R4 примерно 0,05 мм, при этом поверхность 267 оси крыльчатки сужается внутрь вдоль длины L21 под углом СА2 конуса примерно 90 градусов.
[219] Как можно понять по фиг. 5А и 5В, верхний опорный штифт 130 и нижний опорный штифт 160 обычно имеют одинаковую конфигурацию, но имеют противоположную ориентацию. Как показано на фиг. 9A-B, верхний опорный штифт 130 и нижний опорный штифт 160 имеют на одном конце чашку или полусферическую вогнутую опорную поверхность 270, и в основном плоскую поверхность 275 на противоположном конце. Аналогично на фиг. 10 изображен конкретный вариант реализации верхнего опорного штифта 130, который имеет чашку или полусферическую вогнутую опорную поверхность 270 на одном конце и в основном плоскую поверхность 275 на противоположном конце. В этом варианте реализации полусферическая вогнутая поверхность 270 верхнего опорного штифта 130 имеет больший радиус, чем вогнутая опорная поверхность на нижнем опорном штифте 160.
[220] Как показано на фиг. 11A, в одном варианте реализации опорный штифт 130, 160 имеет общую длину L3 примерно 7,5 мм, плюс-минус 0,1 мм, минимальный диаметр оси D2 примерно 2 мм, плюс-минус 0,01 мм, и радиус примерно 0,6 мм на краю вблизи опорной поверхности 270. Вблизи неопорного конца 275 опорного штифта 130, 160, по окружности вокруг штифта проходит канавка 280, чтобы обеспечить механическую блокировку для крепления опорного штифта на месте внутри перфузионного насоса 25. Аналогично, как показано на фиг. 11B, в альтернативном варианте реализации опорные штифты 130, 160 имеют общую длину L3 примерно 7,5 мм, плюс-минус 0,1 мм, минимальный диаметр оси D2 примерно 3 мм, плюс-минус 0,01 мм, и радиус примерно 0,2 мм на краю вблизи плоского конца 275. Вблизи неопорного конца опорного штифта 130, 160, по окружности вокруг его оси вращения проходит канавка 280, чтобы обеспечить механическую блокировку для крепления опорного штифта на месте. В зависимости от размера насоса, материалов опорного штифта, и сил, действующих на опорный штифт, могут быть использованы другие размеры и величины.
[221] Как можно понять по фиг. 3B, 4B и 5A-11B, выпуклая верхняя опорная поверхность 255 оси 145 крыльчатки вращательно установлена относительно вогнутой опорной поверхности 270 верхнего опорного штифта 130, а выпуклая нижняя опорная поверхность 260 оси 145 крыльчатки вращательно установлена относительно вогнутой опорной поверхности 270 нижнего опорного штифта 160. Таким образом, выпуклыеопорные концы 255, 260 оси 145 крыльчатки поддерживаются с возможностью поворота сопряженными вогнутыми опорными поверхностями 270 верхнего и нижнего опорных штифтов 130 и 160, соответственно. Соответственно, узел крыльчатки может свободно вращаться в камере 205 крыльчатки на оси 145 крыльчатки, которая поддерживается торцом к торцу опорными штифтами 130 и 160, в конфигурации, обычно называемой «опорами на два штифта».
[222] Как можно понять по фиг. 11C-11F, еще один вариант реализации опорного штифта 130, 160 имеет общую длину L3 примерно 7,5 мм, плюс-минус 0,1 мм и минимальный диаметр D2 оси примерно 2,0 мм плюс-минус 0,01 мм. Опорный конец 271 имеет радиус R5 примерно 0,3 мм на краю вблизи опорной поверхности 270. Вблизи неопорного конца 275 опорного штифта 130, 160, по окружности вокруг штифта проходит ряд канавок 281, чтобы обеспечить механическую блокировку для крепления опорного штифта на месте внутри перфузионного насоса 25. Ряд канавок 281 может быть образован одним или более углублений 283, имеющих радиус R6 примерно 0,20 мм и плоских участков 285, имеющих радиус кромки R7 примерно 0,03 мм. Расстояние V1 по каждому углублению составляет примерно 0,5 мм, тогда как расстояние P1 по плоскому участку 285 составляет примерно 0,3 мм. Опорные штифты 130 и 160 могут также содержать углубление 286, имеющее диаметр D3 примерно 0,8 мм плюс-минус 0,01 мм, и длину L4 примерно 2,0 мм, как показано на поперечном разрезе по фиг. 11E. На фиг. 11D показан вид опорной поверхности 270, если смотреть вдоль продольной оси опорного штифта 130, 160. Опорная поверхность 270 может иметь радиус R8 примерно 0,65 мм плюс-минус 0,01 мм и глубину L5, примерно 0,3 мм, как показано в разрезе на фиг. 11F.
[223] В еще одном варианте реализации узла крыльчатки узел крыльчатки представляет собой сочетание вала 145 крыльчатки, верхнего опорного штифта 130, и нижнего опорного штифта 160. Составная схема является полезной с точки зрения простоты, допусков, и стоимости обрабатываемых опорных компонентов. Указанные конструкции предназначены для того, чтобы обеспечить бесперебойную работу двигателя в непрерывном режиме в течение от одного дня до 1-12 недель или дольше.
[224] Как показано на фиг.12, вал 145 крыльчатки содержит корпус 146 оси крыльчатки и две вставки 147 оси крыльчатки. Корпус 146 оси крыльчатки содержит обрабатываемый металл, такой как нержавеющая сталь, а вставки 147 оси крыльчатки содержат окись алюминия высокой чистоты (Al2O3), например CoorsTek AD-998, окись алюминия, упрочненную нитевидными кристаллами карбида кремния, например Greenleaf WG-300, или окись алюминия, упрочненную двуокисью циркония (ATZ). Вставки 147 оси крыльчатки прикреплены к корпусу 146 оси крыльчатки с помощью клея и/или посадки с натягом. Глубина введения вставок 147 оси крыльчатки в корпус 146 оси крыльчатки ограничена заплечиками 149, выполненными на дальних концах вставок 147 оси крыльчатки. Необязательно, камера 146А может быть заполнена клейким веществом или другим герметизирующим материалом, который сопротивляется сжатию. Вышеупомянутая составная схема и материалы могут быть применены к вариантам реализации как верхнего опорного штифта 130, так и нижнего опорного штифта 160, причем вставки 148 штифтов взаимодействуют со вставками 147 оси крыльчатки. Необязательно, камеры 148A для каждого опорного штифта 130 и 160, могут быть заполнены с помощью клейкого вещества или другого герметизирующего материала, в том числе материала, который сопротивляется сжатию.
[225] Впускная крышка 125 и ее впускной канал 180 могут иметь множество конфигураций, в зависимости от варианта реализации перфузионного насоса 25. Например, впускная крышка 125, изображенная на фиг. 2, показана как в основном совмещенная с верхним корпусом 135 крыльчатки. В других вариантах реализации изобретения впускная крышка 125 может быть существенно меньше, чем верхний корпус 135 крыльчатки, а не одинаковой протяженности с ним, как показано на фиг. 13-15, которые представляют виды впускной крышки и корпуса крыльчатки.
[226] Как показано на фиг. 14-16, которые представляют, соответственно, поперечные разрезы по линиям сечения 14-14, 15-15, и 16-16 на фиг. 13, впуск 110 представляет собой состоящую из двух частей конструкцию, имеющую части 110A и 110B, каждая из которых образует примерно половину впуска 110, и представляет собой, соответственно, часть впускной крышки 125 и верхнего корпуса 135 крыльчатки. Каждая часть 110A и 110B имеет выполненную в ней примерно половину впускного канала 180. Как показано на фиг. 14, впускной канал 180 первоначально имеет диаметр D5 окружности примерно 4 мм. Как показано на фиг. 15, впускной канал 180 переходит от круглого поперечного сечения, в основном, в прямоугольное поперечное сечение, имеющее ширину W5 примерно 8,4 мм и высоту H5 примерно 1,5 мм. Кроме того, по мере изменения размеров так же будут перечислены измерения.
[227] Как показано на фиг. 16, впускной канал 180 окружает впускное отверстие 185 камеры крыльчатки, которое проходит вокруг верхней опоры 145, установленной во впускной крышке 125 и прикрепленной к ней. Как показано на фиг. 17, на которой представлено частичное поперечное сечение в изометрии впускного отверстия 185 камеры крыльчатки, впускное отверстие 185 камеры крыльчатки ведет к камере 205 крыльчатки вблизи зоны 300 впуска крыльчатки 140. Верхний опорный конец оси крыльчатки 145 расширяется внутри отверстия 185, чтобы сопрягаться с возможностью вращения с верхним опорным штифтом 130, удерживаемым во впускной крышке 125. Лопасти 235 крыльчатки проходят радиально наружу от зоны 300 впуска крыльчатки 140.
[228] Как показано на фиг. 18А и 18В, которые представляют, соответственно, вид сверху части 110А впускной крышки, образующей впускной канал 180, и ее вид с торца, при этом в одном варианте реализации изобретения впускной канал 180 может иметь эллиптическую конфигурацию. В частности, цилиндрический участок 180А канала переходит в участок 18°C в эллиптическом участке 180В канала. Цилиндрический изолированный участок или оправка 305, поддерживающая верхний опорный штифт 130, может быть, в основном, центрирована в эллиптической части 180В канала и содержит цилиндрическое отверстие 240, в котором установлен верхний опорный штифт 130, аналогично показанному на фиг. 17. В одном варианте реализации изобретения цилиндрический участок 180А канала имеет диаметр D6 примерно 4 мм. Эллиптический участок 180B канала имеет ширину W6 примерно 12,4 мм. Дальнее расстояние W7 между стенкой оправки 305 и дальним концом стенки, образующей эллиптический участок 180B канала, составляет примерно 1,5 мм. В других вариантах реализации изобретения цилиндрический участок 180А канала имеет диаметр D6 примерно 5 или 6 мм.
[229] Как показано на фиг. 19А и 19В, которые представляют те же соответствующие виды, что и на фиг. 18А и 18В, за исключением того, что это другой вариант реализации изобретения, впускной канал 180 может иметь круговую конфигурацию. В частности, цилиндрический участок 180А канала переходит в участок 18°C в круговом участке 180В канала. Цилиндрический изолированный участок или оправка 305, поддерживающая верхний опорный штифт 130, может быть, в основном, центрирована в круговом участке 180В канала и содержит цилиндрическое отверстие 240, в котором установлен верхний опорный штифт 130, аналогично показанному на фиг. 17. В одном варианте реализации изобретения цилиндрический участок 180А канала имеет диаметр D9 примерно от 3,5 до 4,5 мм, предпочтительно, 4 мм. Круговой участок 180B канала имеет ширину W9 примерно от 11,5 до 13 мм, предпочтительно, 12,4 мм. Дальнее расстояние W10 между стенкой оправки 305 и дальним концом стенки, образующей круговой участок 180B канала, составляет примерно от 3,5 до 4,5 мм, предпочтительно, 4,2 мм. В других вариантах реализации изобретения цилиндрический участок 180А канала имеет диаметр D6 примерно 5 или 6 мм.
[230] Как показано на фиг. 20А и 20В, которые представляют те же соответствующие виды, что и на фиг. 18А и 18В, за исключением того, что это другой вариант реализации изобретения, впускной канал 180 может иметь сложную дугообразную конфигурацию. В частности, цилиндрический участок 180А канала переходит в участок 18°C на сложном дугообразном участке 180В канала. Цилиндрический изолированный участок или оправка 305, поддерживающая верхний опорный штифт 130, в основном, центрирована в сложной дугообразной части 180В канала и содержит цилиндрическое отверстие 240, в котором установлен верхний опорный штифт 130, аналогично показанному на фиг. 17. В одном варианте реализации изобретения цилиндрический участок 180А канала имеет диаметр D12 примерно 4 мм. Сложный дугообразный участок 180B канала имеет ширину W13 примерно 8,4 мм. Дальнее расстояние W14 между стенкой оправки 305 и дальним концевым колпаком 307 стенки, образующей сложный дугообразный участок 180B канала, составляет примерно 1,75 мм. Дальнее расстояние W15 между стенкой оправки 305 и дальним торцевым углублением 310 стенки, образующей сложный дугообразный участок 180B канала, составляет примерно от 0,5 мм до 1,5 мм, предпочтительно, 1 мм. В других вариантах реализации изобретения цилиндрический участок 180А канала имеет диаметр D6 примерно 5 или 6 мм.
[231] Как показано на фиг. 21-23, которые представляют те же виды, что и на фиг. 18А, за исключением трех других вариантов реализации изобретения, впускной канал 180, как можно сказать, имеет каплевидную конфигурацию. В частности, цилиндрический участок 180А канала переходит в каплевидный участок 180B канала. Цилиндрический изолированный участок или оправка 305, поддерживающая верхний опорный штифт 130, в основном, центрирована в каплевидном участке 180В канала и содержит цилиндрическое отверстие 240, в котором установлен верхний опорный штифт 130, аналогично показанному на фиг. 17. В одном варианте реализации изобретения цилиндрический участок 180А канала имеет диаметр D15 примерно 4 мм. Каплевидный участок 180B канала имеет ширину W20 примерно 8 мм. Оправка 305 имеет диаметр D16 около 4 мм. Переходная зона 18°C канала 180 между каплевидным участком 180B и цилиндрическим участком 180A имеет стенки, расходящиеся друг от друга под углом AN1 примерно 8 градусов. В других вариантах реализации изобретения цилиндрический участок 180А канала имеет диаметр D6 примерно 5 или 6 мм.
[232] Для варианта реализации изобретения по фиг. 21 дальнее расстояние W21 между стенкой оправки 305 и дальним концом стенки, образующей каплевидный участок 180B канала, составляет примерно 2 мм. Для варианта реализации изобретения по фиг. 22 дальнее расстояние W21 между стенкой оправки 305 и дальним концом стенки, образующей каплевидный участок 180B канала, составляет примерно 1 мм. Для варианта реализации изобретения по фиг. 23, дальнее расстояние W21 между стенкой оправки 305 и дальним концом стенки, образующей каплевидный участок 180B канала, составляет примерно 0 мм, поскольку оправка пересекает дальний конец стенки, образующей каплевидный участок канала.
[233] Как показано на фиг. 24А и 24В, которые представляют соответственно, вид сверху и сбоку другого варианта реализации впускной крышки 110 и впускного канала 180, аналогичного показанному на фиг. 21, дугообразный клиновидный участок 320 может проходить между дальней стенкой каплевидного участка 180B канала до дальней стороны оправки 305. В указанном варианте реализации изобретения цилиндрический изолированный участок или оправка 305, в основном, центрирована в каплевидном участке 180В канала и содержит цилиндрическое отверстие 240, в котором установлен верхний опорный штифт 130, аналогично показанному на фиг. 17. В одном варианте реализации изобретения пространственная конфигурация варианта реализации изобретения, изображенного на фиг. 24А и 24В, по существу, такая же, как описано со ссылкой на фиг. 21, при этом существенное отличие заключается в наличии дугообразного клиновидного участка 320. Как можно понять по фиг. 24А и 24В, клиновидный участок 320 имеет стенки дугообразной формы, плавно переходящие от верхней стенки и соседней стенки каплевидного участка 180В канала к вертикальному продолжению оправки 305. Указанный клиновидный участок 320 можно видеть в варианте реализации изобретения, изображенном на фиг. 3А, 3В и 17, и он может уменьшать зоны застоя потока впускного канала и облегчать тангенциальный приток текучей среды через впускное отверстие 185 камеры крыльчатки.
[234] Как показано на фиг. 25, представляющей вид в изометрии перфузионного насоса 25 с удаленным верхним корпусом крыльчатки, чтобы открыть крыльчатку 140, занимающую рабочую камеру 205, выпускной канал 200 текучей среды выходит из камеры крыльчатки, по существу, по касательной к наружной периферийной кромке крыльчатки. Как показано на фиг. 3B, 4B, 17 и 25, множество отверстий 350 (т.е. промывных отверстий) распределены по окружности вокруг отверстия 250 центрирующего ось крыльчатки, и отверстия 350, как правило, параллельны центральному отверстию 250 и проходят по полной толщине крыльчатки, как на верхней, так и на нижней границах крыльчатки. Нижние отверстия каналов 350 расположены вблизи границы нижней опоры между нижней опорой 165 и нижней опорной поверхностью 260 оси крыльчатки (см. фиг. 8). В результате текучая среда (например, кровь) может проходить или течь через каналы 350 для промывки поверхности нижней опоры. Например, текучая среда (такая как кровь) может проходить или течь через впускное отверстие 185 камеры крыльчатки, радиально наружу по лопастям 235 крыльчатки, через зазор 542 под крыльчаткой, а затем обратно в зону впускного отверстия 185 камеры крыльчатки. Этот поток (который может содержать кровь) служит для промывки нижней стороны крыльчатки, нижней поверхности опоры, верхней поверхности опоры, и зоны позади оправки 305.
[235] Как можно понять по фиг. 3B, 5, 17 и 25, в одном варианте реализации изобретения крыльчатка 140 поддерживается с возможностью вращения в камере 205 крыльчатки на валу 145, проходящем через центр крыльчатки. Вал имеет верхний опорный конец и нижний опорный конец, при этом каждый конец связан с корпусом насоса. Крыльчатка имеет верхнюю поверхность, нижнюю поверхность и множество каналов 350, проходящих через крыльчатку от верхней поверхности до нижней поверхности. Множество отверстий, как правило, равномерно распределено радиально вокруг центра крыльчатки. Кроме того, множество отверстий 350 проходит через крыльчатку, в основном, параллельно друг другу и валу. Впускной канал 180 ведет к впускному отверстию 185 камеры крыльчатки. Впускной канал открыт к камере крыльчатки, в основном, перпендикулярной впускному каналу. Впускное отверстие проходит по меньшей мере вдоль части наружной периферической поверхности вала вблизи верхнего конца опоры. Впускное отверстие и отверстия открыты в направлениях, которые, в основном, параллельны друг другу. Во время работы насоса по меньшей мере часть крови, прокачанной через камеру крыльчатки, циркулирует по верхней и нижней поверхностям крыльчатки через каналы. Таким образом, каналы крыльчатки уменьшают глухие концы потока вокруг крыльчатки, обычно удерживающие кровь, проходящую вдоль всех контактирующих с кровью поверхностей крыльчатки. Соответственно, каналы помогают предотвратить накопление крови вблизи линии пересечения вала/крыльчатки, а также по боковой и нижней поверхности крыльчатки.
[236] В некоторых вариантах реализации изобретения зазор между верхней поверхностью крыльчатки 140 и верхним корпусом 135 крыльчатки находится в диапазоне между 0,05 и 0,3 мм, с предпочтительными вариантами реализации между 0,075 и 0,125 мм. Хотя это противоречит преобладающим мыслям и мнениям, предпочтительным может быть зазор между верхней поверхностью крыльчатки 140 и верхним корпусом 135 крыльчатки, который, как правило, меньше, чем в большинстве перфузионных насосов, поскольку это приводит к гидродинамическому режиму потока крови, проходящей по крыльчатке, который снижает осевую нагрузку, прилагаемую к верхней опоре, что в некоторых случаях может действовать как вид гидродинамической опоры и может либо заменять верхнюю опору, либо дополнять верхнюю опору. Гидродинамическая опора, фактически образованная верхней поверхностью лопастей 235 крыльчатки, с меньшим зазором между верхней поверхностью крыльчатки 140 и верхним кожухом 135 крыльчатки, уменьшает нагрузку и, следовательно, износ верхнего опорного штифта. В результате насос 25 может работать дольше, прежде чем потребуется замена насоса или опоры. В качестве примера, как показано на фиг. 4G, общая площадь поверхности верхней части лопастей 235 крыльчатки, обозначенная в целом как 237, обеспечивает гидродинамическую опору, имеющую площадь в диапазоне примерно от 70 мм2до 120 мм2. В одном варианте реализации изобретения общая площадь поверхности лопастей 235 крыльчатки, которая способствует гидродинамической опоре, составляет примерно 96 мм2. В этом варианте реализации изобретения примерная площадь верхней поверхности ротора, за исключением центральных и промывных отверстий, при удаленных лопастях составляет примерно 700 мм2. Поэтому, если площадь верхних поверхностей лопастей составляет примерно 100 мм2, то для формирования гидродинамической опоры используется примерно 14% площади поверхности. В других вариантах реализации изобретения для образования гидродинамической опоры также можно использовать большее отношение, такое как 20% или более, или меньшее отношение, такое как 10% или менее от площади поверхности крыльчатки.
[237] В некоторых вариантах реализации изобретения зазор 542 между верхней поверхностью крыльчатки и верхним корпусом 165 крыльчатки находится в диапазоне между 0,1 мм и 0,5 мм, с предпочтительными вариантами реализации зазора примерно от 0,2 до 0,35 мм. Предпочтительным является больший зазор 542 между нижней поверхностью крыльчатки 140 и нижним корпусом 165 крыльчатки (по сравнению с зазором между верхней поверхностью крыльчатки и верхним корпусом крыльчатки), поскольку это улучшает промывку нижней опоры и снижает напряжение сдвига на крови в нижнем зазоре.
[238] В некоторых вариантах реализации изобретения соблюден баланс между низким потоком в расчетной точке и широким диапазоном рабочего потока перфузионной системы. Указанные диапазоны верхнего и нижнего зазоров корпуса ротора обеспечивают одновременное достижение системой требований к гидравлическим характеристикам, затратам на производство, повреждению крови и сроку службы. Это было проверено в ряде исследований с использованием рабочих прототипов с помощью стендовых испытаний на долговечность in vitro, демонстрирующих незначительный износ опоры в течение 6 недель, и исследований, свидетельствующих о быстром и существенном расширении вены в течение 7-11 дней лечения без наблюдаемого клинически существенного гемолиза.
[239] Корпус и крыльчатка перфузионного насоса 25, включая контактирующие с кровью поверхности, изготовлены из множества жестких биосовместимых материалов. Предпочтительные варианты включают пластмассы для литья под давлением, такие как поликарбонат и полиэфирэфиркетон (polyetheretherketone, PEEK). В некоторых вариантах реализации изобретения контактирующие с кровью поверхности перфузионного насоса 25 могут содержать Ti6Al4V, Ti6Al7Nb или другие технически чистые титановые сплавы. В одном варианте реализации изобретения поверхности компонентов насоса, подвергаемые воздействию крови пациента, могут иметь антитромботические покрытия. Например, на поверхности просвета может быть нанесено покрытие Astute®, антитромботическое покрытие на основе гепарина компании BioInteractions Ltd., или Applause™, гепариновое покрытие компании SurModics, Inc. В другом варианте реализации изобретения поверхности приточного или выводного каналов, подвергаемые воздействию крови пациента, могут иметь антитромботические покрытия. Например, на поверхности просвета может быть нанесено покрытие Astute®, антитромботическое покрытие на основе гепарина компании BioInteractions Ltd., или Applause™, гепариновое покрытие компании SurModics, Inc. В другом варианте реализации изобретения поверхности боковых каналов, подвергаемые воздействию крови пациента, могут иметь антитромботические покрытия. Например, на поверхности просвета может быть нанесено покрытие Astute®, антитромботическое покрытие на основе гепарина компании BioInteractions Ltd., или Applause™, гепариновое покрытие компании SurModics, Inc.
[240] В других вариантах реализации изобретения поверхности компонентов перфузионной системы, находящиеся в контакте с тканью пациента, могут иметь противомикробные покрытия. Например, наружные поверхности синтетических каналов 16 и 18 или наружные поверхности насоса или шнура 120 питания (также называемого «проводник») могут быть покрыты Avert®, поверхностно-активным противомикробным покрытием компании BioInteractions Ltd.
[241] В некоторых вариантах реализации изобретения перфузионный насос 25 может быть имплантирован в пациента. Напротив, в других вариантах реализации изобретения перфузионный насос 25 может оставаться внешним по отношению к пациенту. Например, при расположении снаружи пациента, перфузионный насос 25 может быть прикреплен к пациенту с использованием ленты, швов или других подходящих средств для прикрепления насоса к пациенту. Система 10 может питаться от носимых электронных устройств, имеющих перезаряжаемые аккумуляторы 28, как показано на фиг. 34.
[242] Насос для насосной системы 10, описанный в настоящем документе, может представлять собой ротационный насос, в том числе, например, центробежный насос, осевой насос, радиально-осевой насос или диагонально-центробежный насос. Как показано на фиг. 1-15, в одном варианте реализации изобретения насос представляет собой центробежный насос. Без учета конкретных ограничений, перфузионный насос 25 может быть выполнен с возможностью регулярного прокачивания, например, примерно от 0,05 до 1,5 л/мин, от 0,1 до 1,5 л или от 0,5 до 3,0 л/мин.
[243] Хотя конфигурация насоса, описанная выше со ссылкой на фиг. 1-25 является предпочтительной, с системами и способами перекачивания, описанными в настоящем документе, могут быть использованы другие конфигурации насосов. Соответственно, описанные в настоящем документе системы и способы не должны ограничиваться конфигурацией насоса, описанной выше со ссылкой на фиг. 1-25, но должны включать все типы насосов, применимых для систем и способов, описанных в настоящем документе.
[244] Предпочтительный вариант реализации изобретения насосной системы 10, описанной в настоящем документе со ссылкой на фиг. 1-25, удовлетворяет нескольким уникальным потребностям, которые не могут быть удовлетворены с помощью каких-либо перфузионных систем, известных в данной области. В частности, насосная система приемлемости артериовенозной фистулы (Arteiovenous Fistula Eligibility, «AFE») («система AFE») может быть выполнена в виде системы с центробежным ротационным насосом для низкой скорости потока и широкого рабочего диапазона (например, от 50 до 1500 мл/мин) и среднего диапазона давлений (например, от 25 до 350 мм рт. ст.), который подходит для использования по назначению в течение срока до 12 недель.
[245] Схема управления, используемая с насосной системой AFE, может быть оптимизирована для поддержания устойчивого и повышенного среднего WSS от 0,76 до 23 Па или более предпочтительно от 2,5 Па до 10 Па в заданных венах, непосредственно сообщающихся по текучей среде с перфузионным насосом или каналом перфузионной системы, или заданных венах, сообщающихся по текучей среде с веной, которая непосредственно сообщается по текучей среде с перфузионным насосом или каналом перфузионной системы. С помощью этой схемы управления система AFE выполнена с возможностью работы в течение определенного периода времени, так что общий диаметр и диаметр просвета заданной вены будут устойчиво увеличиваться на 25%, 50%, 100%, 200%, 300% или более, используя измерение рабочих параметров и периодическую регулировку скорости. Схема управления, используемая с насосной системой системы AFE, может быть оптимизирована для поддержания устойчивого давления в сегменте выводного канала рядом с заданной веной в диапазоне от 10 мм рт. ст. до 350 мм рт. ст., предпочтительно от 25 мм рт. ст. до 100 мм рт. ст. С помощью этой схемы управления система AFE выполнена с возможностью работы в течение определенного периода времени, так что общий диаметр и диаметр просвета заданной вены будут устойчиво увеличиваться на 25%, 50%, 100%, 200%, 300% или более, используя измерение рабочих параметров и периодическую регулировку скорости.
[246] В некоторых вариантах реализации изобретения приточный канал может быть размещен посредством хирургического или чрескожного доступа, причем участок приточного канала находится во внутрисосудистом положении, а выводной канал может быть размещен посредством хирургического или чрескожного доступа, адаптируемого к начальному диаметру вены от 1 до 6 мм.
[247] В некоторых вариантах реализации изобретения выводной канал может быть размещен посредством хирургического или чрескожного доступа, причем участок выводного канала находится во внутрисосудистом положении, а приточный канал может быть размещен посредством хирургического или чрескожного доступа, адаптируемого к начальным диаметрам вены или артерии между 1 и 6 мм.
[248] В некоторых вариантах реализации изобретения повышенное среднее значение WSS в заданном кровеносном сосуде является результатом выпуска крови из системы AFE в заданный кровеносный сосуд. Кроме того, в некоторых вариантах реализации изобретения повышенное среднее значение WSS в заданном кровеносном сосуде является результатом удаления крови из заданного кровеносного сосуда в систему AFE. В определенных условиях значение WSS может быть увеличено, как в кровеносном сосуде, из которого удаляется кровь, так и в кровеносном сосуде, в который выпускается кровь, что делает оба кровеносных сосуда заданными кровеносными сосудами.
[249] Насосная система 10 обеспечивает как легкость введения/удаления, так и устойчивость к инфекции. Насосная система 10 представляет собой мобильную систему с насосом, которая выполнена с возможностью имплантации или экстракорпорального размещения. В некоторых вариантах реализации изобретения насосная система 10 питается от носимых электронных устройств с перезаряжаемым аккумулятором. Насосная система 10 содержит приточный канал 20 и выводной канал 30, как показано на фиг. 26. Приточный канал 20 размещен с сообщением по текучей среде с одним местом в сосудистой системе, извлекает кровь из этого места и переносит его в перфузионный насос 25. В некоторых вариантах реализации изобретения приточный канал 20 выполнен с возможностью размещения по меньшей мере части приточного канала в просвете сосудистой системы. В других вариантах реализации изобретения приточный канал 20 соединен с кровеносным сосудом посредством хирургического анастомоза Выводной канал 30 выполнен с возможностью осуществления сообщения по текучей среде с другим местом в сосудистой системе и направляет кровь от перфузионного насоса 25 в другое место в сосудистой системе. В некоторых вариантах реализации изобретения выводной канал 20 выполнен с возможностью размещения по меньшей мере части выводного канала в просвете сосудистой системы. В других вариантах реализации изобретения выводной канал 30 соединен с кровеносным сосудом посредством хирургического анастомоза.
[250] Каналы 20 и 30 могут иметь длину, которая находится в диапазоне между 2 и 110 см, и общую длину от 4 до 220 см. Длина каждого канала 20 и 30 может быть обрезана до требуемой длины, определяемой местонахождением перфузионного насоса 25 и местонахождением соединений между каналами и сосудистой системой. Каналы 20 и 30 также имеют устойчивые к сжатию и к изгибу стенки, которые имеют толщину от 0,5 до 4 мм и внутренние диаметры, составляющие от 2 до 10 мм. Предпочтительно внутренние диаметры основной части приточных и выводных каналов составляют от 3 до 6 мм. Предпочтительно внутренние диаметры для участка наконечника выводного канала, который размещен во внутрисосудистом положении, составляют от 1,5 до 4,0 мм. В одном варианте реализации изобретения поверхности приточного и выводного каналов, подвергаемые воздействию крови пациента, могут иметь антитромботические покрытия. Например, на поверхности просвета может быть нанесено покрытие Astute®, антитромботическое покрытие на основе гепарина компании BioInteractions Ltd., или Applause™, гепариновое покрытие компании SurModics, Inc.
[251] Приточный и выводной каналы 20 и 30 могут быть соединены с перфузионным насосом 25 с использованием любого подходящего соединителя, который является прочным, препятствует утечкам и не подвержен непреднамеренному разъединению. Как правило, передняя кромка соединителя является тонкой, чтобы минимизировать ступенчатое изменение в диаметре пути текучей среды между внутренним диаметром каналов 20 и 30 и внутренним диаметром соединителя. Предпочтительно, ступенчатое изменение в диаметре пути текучей среды должно быть меньше, чем 0,5 мм. В одном варианте реализации изобретения, как показано на фиг. 27A-27D, каналы 20 и 30 соединены с перфузионным насосом 25 с помощью фитингов 400A и 400B с кольцевыми зубцами и радиально сжимающих фиксаторов (т. е. фиксирующих колец) 402A и 402B. В качестве примера, а не ограничения, радиально сжимающие фиксаторы 402A и 402B могут быть фиксаторами BarbLock® производства компании Saint-Gobain Performance Plastics, подразделения Saint-Gobain S.A. со штаб-квартирой в Курбевуа (Courbevoie), Франция. В другом варианте реализации изобретения каналы 20 и 30 соединены с перфузионным насосом 25 с использованием стерильных соединителей Pure-Fit®, также производимых компанией Saint-Gobain Performance Plastics.
[252] Радиальные сжимающие фиксаторы 402А и 402В размещены над ближними концами 404 и 406 приточного и выводного каналов 20 и 30, соответственно. Каналы 20 и 30 затем размещают на фитингах 400А и 400В с кольцевыми зубцами для сообщения по текучей среде между каналами и перфузионным насосом 25. Цанги 408А и 408В радиальных сжимающих фиксаторов 402А и 402В размещены вдоль каналов 20 и 30 таким образом, что окружают каналы и фитинги 400A и 400B с кольцевыми зубцами. Наружные гильзы 410A и 410B радиальных сжимающих фиксаторов 402A и 402B затем перемещают по продольной оси фиксаторов для взаимодействия с возможностью сжатия с соответствующими цангами 408A и 408B, каналами 20 и 30 и фитингами 400A и 400B с кольцевыми зубцами. В одном варианте реализации изобретения наружные гильзы 410A и 410B перемещают с помощью сжимающего инструмента, выполненного с возможностью сцепления наружных гильз и несущих полок 412А и 412В фитингов 400A и 400B с кольцевыми зубцами, соответственно. Сжимающий инструмент также может быть выполнен с возможностью удаления радиальных сжимающих фиксаторов 402А и 402В.
[253] В других вариантах реализации изобретения могут быть использованы альтернативные соединители. Предпочтительно, альтернативные соединители являются прочными, препятствующими утечкам и не подверженными непреднамеренному смещению. Например, как показано на фиг. 28A-B, каналы 20 и 30 взаимодействуют с фитингами с кольцевыми зубцами, аналогичными фитингам 400A и 400B с кольцевыми зубцами, чтобы образовывать сообщение по текучей среде между каналами и перфузионным насосом 25. Каналы 20 и 30 прикреплены к фитингам с кольцевыми зубцами, с использованием круглых зажимов 414A и 414В, которые прилагают радиальное сжимающее усилие к участкам каналов на фитингах с кольцевыми зубцами посредством храпового механизма 416А-416В зажимов. Круглые зажимы 414A и 414B обеспечивают герметичное и прочное соединение, которое может быть удалено с помощью съемного инструмента (не показан), который освобождает храповые механизмы 416A-416B зажимов.
[254] В другом варианте реализации изобретения приточный канал может содержать по меньшей мере один боковой канал 417, как показано на фиг. 29A-B, 30A-B и 50, 51A-B и 52A-B, который обеспечивает контролируемый доступ к пути прохождения текучей среды. В другом варианте реализации изобретения выводной канал 30 может содержать по меньшей мере один боковой канал 417, как показано на фиг. 29A-B, 30A-B и 50, 51A-B и 52A-B, который обеспечивает контролируемый доступ к пути прохождения текучей среды. В другом варианте реализации изобретения как приточный канал 20, так и выводной канал 30 могут содержать по меньшей мере один боковой канал 417, как показано на фиг. 29A-B, 30A-B и 50, 51A-B и 52A-B, который обеспечивает контролируемый доступ к пути прохождения текучей среды. Боковые каналы 417 могут использоваться периодически, чтобы вводить контрастное вещество в путь прохождения текучей среды, чтобы обеспечить визуальное наблюдение частей системы AFE или частей сосудистой системы, сообщающихся по текучей среде с каналом (каналами) системы AFE с помощью рентгеноскопии. Боковые каналы 417 также могут быть использованы для удаления и возврата крови из сосудистой системы пациента во время гемодиализа, плазмафереза, афереза или других клинических показаний, в которых кровь быстро удаляется и возвращается пациенту. Боковые каналы 417 также могут быть использованы для получения образцов крови, для введения лекарств или для других клинически полезных целей. Подходит какая-либо конструкция бокового канала, которая обеспечивает периодический доступ к пути прохождения текучей среды и не протекает или не изменяет путь потока текучей среды, когда доступа нет. В одном варианте реализации изобретения поверхности боковых каналов, подвергаемые воздействию крови пациента, могут иметь антитромботические покрытия. Например, на поверхности просвета может быть нанесено покрытие Astute®, антитромботическое покрытие на основе гепарина компании BioInteractions Ltd., или Applause™, гепариновое покрытие компании SurModics, Inc. В качестве примера, а не ограничения, боковой канал 417 может быть «T-образным» фитингом, содержащим обратный клапан, который открывается при введении шприца и закрывается при удалении шприца. Как показано на фиг. 29А-В, узел 418 «Т-образного» канала со вспомогательной трубкой 420 сообщается по текучей среде с выпуском 115 насоса и выводным каналом 30.
[255] В другом варианте реализации изобретения боковой канал 417 для приточного канала 20, выводного канала 30 или их обоих использует канал 422 доступа в перегородке, имеющий перегородку 424, как показано на фиг. 30A-B, через которую для доступа можно ввести, а затем удалить, подходящую иглу для подкожных инъекций, после чего перегородка закрывается, предотвращая потерю текучей среды из канала. Подходящие материалы для перегородки 424 включают, но не ограничиваются ими, силиконовые, полиуретановые и другие эластомерные полимеры. Сегмент приточного и/или выводного канала 20 или 30, соответственно, который содержит перегородку 424, имеет подходящую толщину, чтобы закрывать отверстие для подкожного прокола при удалении иглы. На фиг. 30A-B показано отверстие 422 доступа в перегородке, при этом перегородка 424 составляет часть выводного канала 30. В качестве примера, а не ограничения, канал 422 доступа в перегородке может проходить примерно на один сантиметр по длине выводного канала 30. Перегородка 424 может быть прикреплена к выводному каналу 30 с помощью любого подходящего средства, включая, но не ограничиваясь ими, крепление с помощью клея, термическое соединение, и термическое соединение между внутренним и наружным слоями трубки канала.
[256] В некоторых вариантах реализации изобретения каналы 20 и 30 могут быть выполнены из материалов, обычно используемых для изготовления катетеров для гемодиализа, таких как полиуретан, поливинилхлорид, полиэтилен, силикон и политетрафторэтилен (polytetrafluoroethylene, PTFE), и в том числе Pellethane® или Carbothane®. В других вариантах реализации изобретения каналы могут быть выполнены из материалов, обычно используемых для изготовления имплантатов для гемодиализа или синтетических периферических шунтирующих трансплантатов, таких как вспененный политетрафторэтилен (ePTFE) или Dacron. В других вариантах реализации изобретения часть каналов может быть выполнена из металлов, таких как нержавеющая сталь, титан или нитинол. В других вариантах реализации изобретения каналы могут быть выполнены из комбинаций полиуретана, поливинилхлорида, полиэтилена, силикона, PTFE, Pellethane ®, Carbothane ®, Carbothane® PC-3575, ePTFE, Dacron, нержавеющей стали, титана или нитинола.
[257] Например, вся длина приточного канала 20 может быть выполнена из полиуретана. В другом варианте реализации изобретения, показанном на фиг. 31, сегмент 500 выводного канала 30, выполненный с возможностью сообщения по текучей среде с перфузионным насосом 25, выполнен из полиуретана, тогда как сегмент 502 выводного канала, выполненный с возможностью сообщения по текучей среде с сосудистой системой, выполнен из ePTFE, включая кольцевую несущую конструкцию из ePTFE.
[258] В качестве примера, а не ограничения, и, как показано на фиг. 41, на которой представлен продольный разрез соединения между ближним сегментом 500 и дальним сегментом 502, ближний сегмент 500 выводного канала 30 соединен с дальним сегментом 502 выводного канала в ходе процесса изготовления путем размещения одного или более слоев 502A из ePTFE дальнего сегмента между слоями 500A из полиуретана ближнего сегмента. Затем перекрывающиеся слои полиуретана и ePTFE подвергают термическому ламинированию для соединения ближнего сегмента 500 и дальних сегментов 502 друг с другом.
[259] В другом примере перед термическим ламинированием канала в перекрывающихся участках ePTFE сегмента 502 выполняют одно или более отверстий. Когда выводной канал 30 нагревают до температуры, достаточной для расплавления полиуретана без плавления ePTFE (например, от 93,3 до 260°C (от 200 до 500 °F)), расплавленный полиуретан заполняет отверстия, созданные в сегменте 502 ePTFE, а затем охлаждается внутри них. Внутренние и наружные полиуретановые слои сегмента 500 соединены в отверстиях для механического соединения двух сегментов 500 и 502 друг с другом, а также механического соединения внутреннего и наружного слоев полиуретана в перекрывающемся сегменте.
[260] Вариант реализации выводного канала 30, изготовленного таким образом, что слой 502А ePTFE, заключен между слоями 500A полиуретана, является предпочтительным, поскольку слой 502A ePTFE можно легко сшивать с кровеносными сосудами, используя стандартные способы. Это также имеет место для приточного канала 20, изготовленного, как описано выше со ссылкой на фиг. 41.
[261] Как показано на фиг. 42, представляющей вид сверху медицинского комплекта 920, перфузионный насос 25, выводной канал 20, приточный канал 30, устройство 21 управления и шнур 120 питания могут поставляться в стерильной упаковке 925 с инструкциями 930 о том, как собирать и имплантировать насосную систему пациенту. Медицинский комплект 920 может также включать фитинги 400A и 400B с кольцевыми зубцами и радиально сжимающие фиксаторы 402A и 402B. В одном варианте реализации изобретения один или оба канала 20, 30 изготовлены, как описано выше со ссылкой на фиг. 41, и заключены в стерильную упаковку 925 вместе с перфузионным насосом 25. Медицинский комплект 920, как минимум, содержит систему для выпуска или удаления крови и инструкции по ее применению и использованию.
[262] В одном варианте реализации изобретения работа перфузионного насоса 25 регулируется посредством блока 21 управления системы 14 управления насосом путем измерения венозного давления и регулировки скорости работы насоса, соответственно. Например, как показано на фиг. 43, представляющей принципиальную схему насосной системы 10, регулируемой в соответствии с венозным давлением, датчик 935 венозного давления может быть функционально связан с выходом 115 перфузионного насоса 25 или далее вниз по потоку, например, в каком-либо месте по длине выводного канала 30. Процессор 24 может сравнивать показания давления от датчика 935 венозного давления с диапазоном заданных значений венозного давления, сохраненных в памяти 27. Затем процессор будет регулировать скорость привода 170 насоса, соответственно, чтобы приводить показания давления от датчика 935 венозного давления в соответствие с диапазоном заданных значений венозного давления, хранящихся в памяти.
[263] В одном варианте реализации изобретения система 14 управления также содержит датчик 940 приточного давления, который может быть функционально связан с впуском 110 перфузионного насоса 25 или далее вверх по потоку, например, в каком-либо месте по длине приточного канала 20 или бокового канала. В одном варианте реализации изобретения система 14 управления также содержит датчик венозного давления, который может быть функционально связан с выпуском перфузионного насоса 25 или далее вниз по потоку, например, в каком-либо месте по длине выводного канала или бокового канала. В одном варианте реализации изобретения процессор 24 может считывать как показания давления от датчика 935 венозного давления, так и показания давления от датчика 940 приточного давления, и вычислять разность давлений. Указанная разность давлений затем может сравниваться с диапазоном заданных разностей давлений, сохраненных в памяти 1055. Затем процессор будет регулировать скорость привода 170 насоса, чтобы приводить вычисленную разность давлений в соответствие с диапазоном заданных разностей давлений, хранящихся в памяти. В одном варианте реализации изобретения процессор 24 может считывать показания давления от датчика 935 венозного давления. Указанное давление затем может сравниваться с диапазоном заданных давлений, сохраненных в памяти 1055. Затем процессор будет регулировать скорость привода 170 насоса, чтобы приводить измеренное давление в соответствие с диапазоном заданных разностей давлений, хранящихся в памяти.
[264] В других вариантах реализации изобретения приточные и выводные каналы 20 и 30 могут быть выполнены из каких-либо материалов или комбинации материалов, при условии, что каналы 20 и 30 обладают необходимыми характеристиками, такими как необходимая толщина стенки, гибкость, стерильность, устойчивость к изгибу и сжатию, и могут быть соединены с кровеносным сосудом посредством анастомоза или дальнего участка, введенного в просвет кровеносного сосуда, при необходимости. Кроме того, каналы 20 и 30 предпочтительно обладают характеристиками, необходимыми для подкожной туннелизации, при необходимости, например, содержащие смазочные покрытия наружной поверхности, такие как улучшенные смазочные покрытия Harmony™.
[265] В качестве другого примера приточные и выводные каналы 20 и 30 могут иметь наружный слой, выполненный из другого материала, чем внутренний слой. Наружные слои приточных и выводных каналов 20 и 30, полностью или частично, также могут быть покрыты смазочным агентом, таким как силиконовое или гидрофильное покрытие, для способствования подкожной туннелизации и удалению из организма, а также для смягчения возможных аллергических реакций на латекс. В некоторых вариантах реализации изобретения по меньшей мере часть поверхности наружного слоя приточных и выводных каналов 20 и 30 может иметь противомикробное покрытие. В других вариантах реализации изобретения по меньшей мере часть поверхности перфузионного насоса 25 или шнура 120 питания может иметь противомикробное покрытие. Например, может быть использовано поверхностно-активное противомикробное покрытие Avert TM. В некоторых вариантах реализации изобретения часть поверхности наружного слоя приточного и выводного каналов может включать материал, способный противостоять инфекции и стимулирующий инкорпорирование ткани, такой как Dacron, полиэфирный велюр или силикон. Одним из таких материалов является противомикробная манжета VitaCuff® компании Vitaphore Corp. Манжета VitaCuff содержит два концентрических слоя материала. Внутренний слой изготовлен из медицинского силикона. Наружный слой, взаимодействующий с тканью, содержит коллагеновую матрицу с противомикробной активностью, которая свойственна ионам серебра, связанным с коллагеном. В некоторых вариантах реализации изобретения указанный материал поглощает физиологические жидкости, быстро расширяется и помогает обеспечить физический барьер в месте выхода. Происходит врастание ткани, что дополнительно закрепляет канал на месте и уменьшает перемещение канала, чтобы уменьшить частоту инфицирования места выхода.
[266] Как можно понять по фиг. 48A-F, вариант реализации манжеты 800 служит для крепления приточного и выводного каналов 20 и 30 к пациенту на длительное время и уменьшения проникновения посторонних веществ, таких как бактерии, на месте введения в кожу или в тело вдоль пути каналов. Манжета 800 может содержать конструкцию из двух частей, имеющую съемную верхнюю часть 802 и съемную нижнюю часть 804, которые механически соединены друг с другом и каналами. Как показано на фиг. 48В и 48D, каждая из верхней и нижней частей 802 и 804 содержит один или более элементов 806 защелки и соответствующих гнезд 808 защелки. В одном варианте реализации изобретения каждая из верхних и нижних частей 802 и 804 содержит два элемента 806 защелки, которые входят в гнезда 808 защелки на противоположной части, для крепления двух частей друг с другом, как показано на фиг. 48А-В. Каждая часть 802 и 804 может также содержать направляющий элемент 810 для дополнительного выравнивания двух половинок, и соответствующее направляющее гнездо 812 для установки направляющего элемента на противоположной части. Каждая из верхней и нижней частей 802 и 804 образует канал 814 для установки канала 20 или 30. Канал 814 дополнительно образует ряд непрерывных по окружности или, альтернативно, прерывистых выступов 816, которые выступают в канал 814. Выступы 816 надежно сцепляют каналы 20 или 30, когда манжета 800 прикреплена к каналам, чтобы предотвратить перемещение или проскальзывание манжеты относительно канала. Выступы 816 также обеспечивают уплотнение вокруг наружной поверхности каналов 20 и 30. В некоторых вариантах реализации изобретения наружная часть манжеты может быть покрыта или облицована материалом 818, чтобы стимулировать инкорпорирование ткани или противостоять инфекции, таким как Dacron, полиэфирный велюр или силикон, как показано на фиг. 48E-F. Материал 818 может также содержать агенты с противомикробными свойствами. Материал 818 обеспечивает пористую наружную поверхность манжеты 800, чтобы стимулировать врастание ткани, локально увеличивать адгезию между пациентом и каналом 20 или 30, и уменьшать попадание посторонних веществ и бактерий в место разреза кожи, тело пациента или по пути канала.
[267] Врач может регулировать длину подкожного туннеля для канала 20 или 30, так что манжета 800 прикрепляется к каналу в месте, которое надлежащим образом расположено в туннеле. Когда манжета 800 выполнена с возможностью крепления и отсоединения к каналу 20 или 30, который может быть обрезан до соответствующей длины, манжета 800 может быть прикреплена к обрезанному каналу таким образом, что манжета надлежащим образом располагается внутри подкожного туннеля.
[268] В некоторых вариантах реализации изобретения по меньшей мере часть контактирующих с кровью поверхностей просвета приточных и выводных каналов 20 и 30 может быть покрыта антитромботическим средством или материалом. Аналогично, по меньшей мере часть контактирующих с кровью поверхностей перфузионного насоса 25 может быть покрыта антитромботическим средством или материалом. Например, поверхности могут быть покрыты покрытием Applause® компании SurModics, Inc. или покрытием Astute® компании BioInteractions Ltd., оба из которых представляют собой гидрофильные покрытия из сополимера, содержащие гепарин.
[269] В некоторых вариантах реализации изобретения по меньшей мере часть приточного канала 20 и выводного канала 30 предпочтительно упрочнена для обеспечения устойчивости к изгибу, сжатию, спадению и сближению. Например, каналы 20 и 30 могут быть упрочнены нитинолом или другим сплавом с памятью формы или саморасширяющимся, или радиально расширяющимся материалом. Предпочтительно слой плетеного или спирального нитинола обернут по меньшей мере вокруг части каждого из каналов 20 и 30 или встроен в стенки каналов. В одном варианте реализации изобретения приточный канал 20 упрочнен оплеткой из нитинола, встроенной в стенки канала. В другом варианте реализации изобретения приточный канал может быть упрочнен оплеткой из нержавеющей стали, которая встроена в стенку каналов 20 и 30. Альтернативно, спираль из нитинола или PTFE может быть обернута вокруг участков каналов 20 и 30 или встроена в них. Например, как показано на фиг. 31, дальний сегмент 502 выводного канала 30 имеет спираль 504 из PTFE, встроенную вокруг канала из ePTFE, образующего стенку 514 канала. В других вариантах реализации изобретения спираль из нитинола может быть обернута вокруг участков каналов 20 и 30 или встроена в них. Упрочняющая проволока (например, нитинол) может иметь круглое, кольцевое поперечное сечение, продолговатое поперечное сечение или, в основном, прямоугольное поперечное сечение.
[270] Плотность плетения для оплетки из нитинола, встроенной в приточный и выводной каналы 20 и 30, обычно измеряемая в пикселях на дюйм (pixels per inch, «PPI»), обычно составляет примерно от 10 до 200 и предпочтительно примерно от 20 до около 60. В некоторых вариантах реализации изобретения плотность оплетки может изменяться по длине приточного и выводного каналов 20 и 30. Например, плотность плетения может быть большей на участках каналов 20 и 30, примыкающих к перфузионному насосу 25, для повышения жесткости каналов и сведения к минимуму вероятности сжатия, перегибания, сближения или спадения наружного канала во время всасывания, при этом обеспечивая большую гибкость в других сегментах каналов.
[271] В одном варианте реализации изобретения, как показано на фиг. 32А-32В, внутрисосудистый участок 506 приточного канала 20 пронизан множеством боковых отверстий 508. Эти боковые отверстия усиливают приток крови и уменьшают риск всасывания вены или стенки правого предсердия торцевым отверстием в случае частичного засорения наконечника канала. Боковые отверстия 508 могут быть круглыми и иметь диаметр в диапазоне от 1,0 до 3,0 мм. Альтернативно, боковые отверстия 508 могут быть эллиптическими или иметь любую другую форму и размеры, подходящие для внутрисосудистой аспирации крови.
[272] Как показано на фиг. 31 и 32А-32В, дальний конец 506 приточного канала 20 и дальний конец 510 выводного канала 30 может быть разрезан или скошен под углом примерно между 10° и 80°. В некоторых вариантах реализации изобретения скос уменьшает риск всасывания вены или стенки правого предсердия торцевым отверстием в случае частичного засорения наконечника канала во время аспирации крови. В других вариантах реализации изобретения скос увеличивает площадь канала, когда он соединяется с сосудистой системой в анастомотическом соединении. В некоторых вариантах реализации изобретения дальние концы 506 и 510 скошены под углом 45°. Приточный и выводной каналы 20 и 30 выполнены с обеспечением удобства введения, подкожной туннелизации и удаления, а также обеспечивают устойчивость к инфицированию и тромбозу.
[273] В другом варианте реализации изобретения, как показано на фиг. 32C-32I, внутрисосудистый участок 506 приточного канала 20 и/или выводная канюля 30 имеет дальний наконечник 507, который оптимизирован для уменьшения застойного или рециркуляционного потока внутри канала. Дальний наконечник 507 выполнен коническим и не скошенным, с круглым торцевым отверстием 511, имеющим диаметр в диапазоне примерно от 1,0 мм до 6,0 мм, предпочтительно диаметр составляет примерно 2,0 мм. Дальний наконечник 507 пронизан множеством рядов боковых отверстий 513 и 515. Боковые отверстия 513 и 515 могут иметь различные размеры, формы и ориентации. Например, ряд из четырех боковых отверстий 513 симметрично расположен сразу за носиком наконечника. Каждое из боковых отверстий в ряде 513 имеет круглую форму и расположено под углом относительно центральной линии 517 просвета приточного канала. В одном аспекте боковые отверстия 513 имеют диаметр в диапазоне примерно от 0,8 до 2,5 мм и предпочтительно составляют примерно 1,7 мм в диаметре. Кроме того, боковые отверстия 513 ориентированы под углом относительно центральной линии 517 в диапазоне примерно от 30° до 60°; предпочтительно отверстия ориентированы примерно под углом 40°. Другой ряд из четырех боковых отверстий 515 симметрично расположен примерно на расстоянии 6,5 мм от носика наконечника 507. Боковые отверстия 515 обычно имеют эллиптическую форму с большой осью длиной в диапазоне примерно от 2,5 до 7,0 мм, предпочтительно большой осью длиной примерно 4,8 мм. Боковые отверстия 515 также имеют малую ось длиной в диапазоне примерно от 1,0 до 2,5 мм, предпочтительно малая ось имеет длину около 1,7 мм. В некоторых вариантах реализации изобретения кромки боковых отверстий 513 и 515 отверстий округлены или выполнены с радиусом скругления во избежание повреждения крови. Варианты реализации наконечника 507 канюли, описанного в настоящем документе, выполнены с возможностью уравновешивания необходимости в снижении максимальных уровней WSS на поверхностях наконечника канюли, уменьшая риск всасывания соседней стенки наконечником канюли, и в уменьшении гемолиза за счет увеличения диаметра или площади торцевого отверстия или одного или более боковых отверстий, или диаметра канюли; с необходимостью в увеличении потока крови и промывки поверхности наконечника канюли, и в уменьшении риска тромбоза наконечника за счет уменьшения диаметра или площади торцевого отверстия, или одного или более боковых отверстий или диаметра канюли. Считается, что увеличение или уменьшение WSS на поверхностях наконечника канюли зависит от разности диаметров отверстия (в квадрате), а также обусловлено общим уменьшением диаметра канюли.
[274] В некоторых вариантах реализации изобретения наконечник 507 канюли не имеет упрочнения спиралью или оплеткой приточного канала 20 или выводного канала 30. Как показано на фиг. 32D, оплетка 519 из нитинола, встроенная в приточные или выводные каналы 20 и 30, соответственно, не распространяется на наконечник 507 канюли. Вместо этого упрочняющая спираль 519 заканчивается возле или вблизи наконечника 507 канюли, как указано 521. Как показано на фиг. 32Е, наконечник 507 канюли может также содержать непроницаемый для рентгеновских лучей материал, такой как кольцо или полоска 523. Маркерная полоска 523 или более непроницаемая для рентгеновских лучей стенка канала способствует размещению приточных или выводных каналов 20 и 30 во время введения в кровеносный сосуд с использованием рентгеноскопии.
[275] В одном аспекте настоящее изобретение также относится к способу изготовления дальнего наконечника 507 канюли, как показано на фиг. 32C-32I. На фиг. 32J приведена схема последовательности операций, изображающая способ 900 изготовления наконечника 507 канюли. На этапе 902 жесткую оправку вводят через дальнее отверстие 511 наконечника неупрочненного дальнего конца приточной канюли 20. В этом примере наконечник 507 канюли имеет внутренний диаметр примерно 4,0 мм и наружный диаметр примерно 5,4 мм, тогда как оправка имеет диаметр в диапазоне примерно от 1,5 мм до 2,0 мм. В некоторых вариантах реализации изобретения оправка может быть выполнена из любого жесткого материала, включая металл, такой как нержавеющая сталь. На этапе 904 сегмент тонкой термоусадочной фторированной этиленпропиленовой трубки (fluorinated ethylene propylene, FEP) размещают поверх наконечника 507 и узла оправки. На этапе 906 примерно от 0,5 см до 2,5 см дальнего участка наконечника 507 нагревают примерно до 204,4°C (400 °F). В одном аспекте дальний участок располагают в среде нагретого воздуха, размягчающего наконечник 507 канюли, который может быть выполнен из полиуретана, а также принуждающего FEP сжиматься и сжимать наконечник канюли относительно оправки и уменьшать внутренний диаметр дальнего отверстия 511 наконечника примерно до 1,5 мм -2,0 мм. Кроме того, путем размещения дальнего участка наконечника 507 и узла оправки в нагретой среде, температурный градиент прилагают по трубке FEP, которая сжимается до разных величин, соответствующих разным температурам вдоль температурного градиента. В результате наконечник 507 полиуретановой канюли сжимается в виде конуса с наибольшей силой сжатия, прилагаемой к дальнему участку, на котором температура является наибольшей, и уменьшающейся силой сжатия в ближнем направлении.
[276] В некоторых вариантах реализации изобретения степень конусности, придаваемая дальнему концу 507, может изменяться в соответствии с конфигурацией, требуемой изготовителем или пользователем, а также вследствие изменений переменных процесса, включая, но не ограничиваясь этим, температуру нагрева окружающей среды, материал дальнего конца 507, длину и начальный диаметр трубки FEP. После формирования конической конфигурации на дальнем наконечнике 507, наконечнику канюли дают остыть, и на этапе 908 трубку FEP удаляют, в результате получается плавно сужающийся дальний наконечник 507.
[277] В одном варианте реализации изобретения на этапе 910 к наконечнику канюли приклеивают непроницаемую для рентгеновских лучей маркерную полоску 522 дальнего кольца. В одном аспекте маркерная полоска имеет диаметр, меньший, чем наружный диаметр дальнего конца приточной канюли 20, и на этапе 904-908 ее с усилием устанавливают поверх наконечника 507 канюли перед наложением трубки FEP и процессом сужения. Маркерная полоска предпочтительно прикреплена в том положении, в котором она будет помещена в нагретую среду. Когда трубка FEP сжимается относительно маркерной полоски, размягченный материал канюли (например, полиуретан) растекается вокруг полоски и над ней, тем самым внедряя полоску в стенку канюли.
[278] На этапе 912 в наконечнике 507 канюли формируют боковые отверстия 513 и 515. В одном аспекте боковые отверстия 513 и 515 выполняют путем прокалывания стенок наконечника 507 канюли с использованием длины жесткого канала, например, но не ограничиваясь этим, трубки из нержавеющей стали. Например, круглые боковые отверстия 513 могут быть образованы путем прокалывания боковых стенок наконечника 507 канюли трубкой из нержавеющей стали, имеющей толщину стенки примерно 0,5 мм. Один конец трубки заострен и выполнен с возможностью формирования передней внутренней кромки и конической поверхности между внутренней и наружной поверхностями трубки под углом примерно 45°. Для формирования более удлиненных боковых отверстий 515 используют заостренную трубку из нержавеющей стали, аналогичную той, которая используется для формирования боковых отверстий 513. Однако трубка, используемая для формирования боковых отверстий 515, обычно имеет больший диаметр и ее сжимают до тех пор, пока не будут достигнуты соответствующие размеры эллипсоида. Сжатая трубка, имеющая удлиненное овальное или эллиптическое поперечное сечение, используется для прокалывания боковых стенок наконечника 507 канюли.
[279] В еще одном аспекте на этапе 912 заостренный наконечник трубки из нержавеющей стали, используемой для изготовления боковых отверстий 513 и 515, перед прокалыванием может быть нагрет до температуры примерно от 121,1 до 204,4°C (250-400 °F) через поверхность наконечника 507 канюли. В одном аспекте нагретая трубка нагревает и по меньшей мере размягчает материал наконечника 517 канюли, заставляя его «течь», и образует гладкую, закругленную внутреннюю поверхность относительно боковых отверстий 513 и 515. Напротив, в других вариантах реализации изобретения, боковые отверстия 513 и 515 могут быть выполнены любым подходящим способом, включая, но не ограничиваясь этим, вырезание лазером или другим прецизионным режущим инструментом.
[280] В одном варианте реализации изобретения участок приточного канала 20 может быть введен в просвет кровеносного сосуда с использованием способа чрескожной инъекции или открытого хирургического доступа, и может быть продвинут в нужное положение с использованием рентгеноскопии для содействия в продвижении и установке устройства. Чтобы помочь в установке приточного и выводного каналов 20 и 30, каналы могут иметь непроницаемые для рентгеновских лучей маркерные полоски или другие непроницаемые для рентгеновских лучей материалы, встроенные в стенки 512 и 514 приточных и выводных каналов соответственно, которые видны при использовании рентгеноскопии. Например, участки приточного и выводного каналов 20 и 30 могут быть выполнены из полиуретана Carbothane® PC-3575, содержащего соли сульфата бария. В других вариантах реализации изобретения участки приточного и выводного каналов 20 и 30, которые выполнены с возможностью введения в просвет сосудистой системы, могут иметь саморасширяющиеся или радиально расширяющиеся стенки (такие, которые могут быть выполнены за счет внедрения нитинола), так что диаметр внутрисосудистой части приточного и выводного каналов 20 и 30 будет соответствовать диаметру сосудистой системы в этом месте, например, как показано, с саморасширяющимся сегментом гибридного сосудистого имплантата GORE®.
[281] В некоторых вариантах реализации изобретения, включая вариант реализации изобретения, показанный на фиг. 37, приточный и выводной каналы 20 и 30 могут быть прикреплены к кровеносным сосудам с использованием хирургического анастомоза, используя непрерывный или узловой шов, далее описываемый как «анастомотическое соединение». Анастомотическое соединение также может быть выполнено с помощью хирургических зажимов и других стандартных способов выполнения анастомоза. Например, может быть выполнено анастомотическое соединение между дальним сегментом 502 выводного канала из ePTFE или Dacron 30 и кровеносным сосудом.
[282] В некоторых вариантах реализации изобретения, в которых выполнено анастомотическое соединение, выводной канал 30 прикреплен к кровеносным сосудам, имеющим начальный диаметр от 1 мм до 20 мм, и предпочтительно сосудам, имеющим начальный диаметр от 1,5 мм до 6 мм.
[283] И наоборот, в других вариантах реализации изобретения, показанных на фиг. 32А-В и 37-40, участки приточного и выводного каналов 20 и 30 установлены в кровеносном сосуде или правом предсердии. Например, дальний конец 506 приточного канала 20 может быть расположен в правом предсердии или в верхней полой вене. Как показано на фиг. 32A-32B, боковые отверстия 508 способствуют аспирации или выпуску крови, когда дальний конец 506 размещен внутри кровеносного сосуда.
[284] В некоторых вариантах реализации изобретения по меньшей мере один из приточного и выводного каналов 20 и 30 может быть совместим для использования с установкой для гемодиализа или установками, используемыми для плазмафереза или афереза. Например, пациент, использующий перфузионную систему 10, может также нуждаться в лечении гемодиализом. В указанном примере кровь может быть удалена из перфузионной системы, пропущена через аппарат для гемодиализа, а затем выпущена обратно в перфузионную систему для доставки обратно в сосудистую систему, тем самым устраняя необходимость в создании дополнительного места сосудистого доступа в пациенте. Боковые каналы 417 на приточном и выводном каналах 20 и 30 могут облегчать удаление и возврат крови из системы AFE во время гемодиализа, плазмафереза, афереза или других процедур, при которых кровь удаляется и возвращается пациенту. В некоторых вариантах реализации изобретения боковые каналы 417 могут быть выполнены с возможностью обеспечения стерильного введения эндоваскулярных устройств, таких как проволочный направитель катетера, баллоны для ангиопластики, сосудистые стенты, сосудистые окклюзионные устройства, местные катетеры для доставки лекарств и катетеры для тромболизиса, и тромбэктомические устройства, такие как катетеры-баллоны Фогарти. В некоторых из этих конкретных вариантов реализации изобретения длинная ось бокового канала 417 может быть выполнена под углом к длинной оси канала, например, под углом 30 градусов, под углом 40 градусов или под углом 45 градусов, среди прочих. В некоторых из этих вариантов реализации изобретения боковой канал 417 или узел бокового канала может содержать гемостатический клапан для облегчения быстрого и простого введения и удаления эндоваскулярных устройств с минимальной потерей крови.
[285] Боковые каналы 417 могут быть прикреплены к приточному и выводному каналам 20 и 30, соответственно, любым подходящим способом. В одном варианте реализации изобретения клей наносят на поверхности бокового канала 417, которые будут установлены в каналах 20 и 30. Боковой канал 417 сцепляется с каналами, и клей обеспечивает образование непроницаемого для текучей среды уплотнения, как показано на фиг. 50. В одном аспекте клей представляет собой отверждаемый под воздействием ультрафиолетового излучения (ultraviolet, UV) медицинский клей.
[286] На фиг. 51А-В и 52А-В изображены варианты реализации изобретения узла 419 бокового канала, который является «готовым к доступу» или «способным к доступу», и выполнен с возможностью обеспечения извлечения текучей среды из каналов 20 или 30 и введения в каналы веществ и других материалов, включая, но не ограничиваясь только ими, лекарства, вливания, медицинские инструменты или медицинские устройства. В частности, на фиг. 51А и 52А изображены не собранные узлы 419, а на фиг. 51В и 52В изображены соответствующие собранные узлы боковых каналов. В некоторых вариантах реализации изобретения боковой канал 417 содержит колпачок для уплотнения бокового канала, при необходимости. В качестве примера, а не ограничения, колпачок может быть твердым или жестким торцевым колпачком 421 с резьбовым фитингом Люэра, который можно навинтить и отвинтить от бокового канала. В другом примере крышка может содержать инфузионный клапан 423, содержащий плунжер, который обычно закрыт до введения шприца в колпачок для инъекции, вливания или аспирации. Когда шприц удаляют, плунжер возвращается в закрытое положение для герметизации колпачка. В другом варианте реализации изобретения колпачок может содержать гемостатический клапан 425, похожий на клапан в стандартном ангиографическом интродьюсере. Гемостатический клапан 425 позволяет колпачку оставаться закрытым до тех пор, пока через клапан не будет введен проволочный направитель или катетер. Это позволяет оператору перемещать провода и катетеры внутрь и наружу из бокового канала 417 без открывания или закрывания колпачка вручную. В другом варианте реализации изобретения колпачок может содержать адаптер Туохи Борста с круглым участком, который может поворачиваться для открывания и закрывания клапана. Боковой канал 417 может также содержать 3-ходовое боковое ответвление 427, которое обеспечивает одновременно инъекцию, вливание или аспирацию. Как показано на фиг. 51B, собранный вариант реализации «готового к доступу» бокового канала 417 содержит различные комбинации колпачков, 3-ходового бокового ответвления 427, а также один или более зажимов 429. В других вариантах реализации изобретения также может быть использовано меньше или больше колпачков в различных других комбинациях. В каналах 20 или 30 перед их соединением с боковыми каналами 417 также могут быть установлены зажимы 429.
[287] Когда используется система кровеносных насосов с указанными «готовыми к доступу» боковыми каналами, на каналах и связанной с ними сосудистой системе могут быть легко выполнены эндоваскулярные процедуры, такие как тромбэктомия каналов, баллонная ангиопластика связанных сосудов, таких как выводящая вена системы AFE, эндоваскулярная окклюзия сосудистых боковых ветвей и местная доставка лекарств в каналы и связанные с ними сосуды, например, тромболизис, направляемый катетером. В одном варианте реализации изобретения использование системы AFE сочетается с использованием эндоваскулярных устройств для окклюзии. Например, во время лечения заданной вены с помощью системы AFE одна или несколько боковых ветвей заданной вены могут расширяться в ответ на повышенное значение WSS, тем самым уменьшая дозу WSS в сегменте ниже по потоку. В этой ситуации кровоток в указанные боковые ветви вен может быть заблокирован путем размещения эндоваскулярного устройства для окклюзии в боковые ветви вены. Устройства, которые могут быть использованы для этой цели, содержат стандартные спирали для окклюзии периферических сосудов, устройства Amplatzer® Vascular Plug (St. Jude Medical, Inc.) или Blockstent Microcatheters™ (Metactive Medical, Inc.). Эти устройства могут быть установлены через боковой канал на выводном канале 30 или через отдельный сосудистый доступ, такой как интродьюсер, установленный в периферической вене, например, бедренной вене или головной вене.
[288] Как показано на фиг. 35, один вариант реализации системы 14 управления содержит устройство 21 управления, имеющее по меньшей мере один процессор 24 и память 27 для подачи мощности к насосу и приема информации от перфузионного насоса 25, посредством чего информация используется для установки и регулирования скорости работы насоса и оценки скорости кровотока или текучей среды через насосную систему. Процессор 24 выполнен с возможностью считывания, обработки и выполнения систем, способов и команд, зашифрованных на машиночитаемом носителе. Затем система 14 управления оценивает WSS в заданном сосуде с использованием измеренного или вычисленного диаметра сосуда и измеренной или вычисленной средней скорости потока насосной системы. Устройство управления также содержит источник 26 питания, необязательно имеющий аккумулятор 28.
[289] В одном варианте реализации изобретения система 14 управления принимает сигнал обратной связи датчика от одного или более датчиков 122. Любой из множества подходящих датчиков может быть использован для обнаружения какого-либо из множества изменений физического количества крови, перфузионного насоса 15, перфузионной системы 10 или заданного сосуда. В некоторых вариантах реализации изобретения датчики могут использоваться для обнаружения положения тела или изменения положения тела. Датчики 122 создают сигнал, указывающий изменение, которое необходимо проанализировать и/или обработать. По существу, датчики 122 отслеживают различные свойства перфузионной системы 10, крови, протекающей через систему, и заданного кровеносного сосуда относительно изменений, которые могут быть обработаны и сравнены с необходимыми опорными значениями или заданными стандартными значениями. Необходимые опорные значения или установленные стандартные значения могут храниться в базе данных или на других подходящих носителях.
[290] В некоторых вариантах реализации изобретения один или более датчиков 122 могут сообщаться с перфузионным насосом 25, приточным каналом 20, выводным каналом 30, передающим сосудом или местом, или принимающим сосудом или местом. В некоторых вариантах реализации изобретения система 14 управления или ее части могут быть расположены внутри корпуса или кожуха перфузионного насоса 25. Например, один или более датчиков 122 могут быть расположены во впускном отверстии 110 или выпускном отверстии 115 перфузионного насоса 25. В другом примере датчик температуры может быть расположен в перфузионном насосе. В других вариантах реализации изобретения система 14 управления может быть внешней по отношению к насосу.
[291] WSS может использоваться как переменная для настройки работы насосной системы 10, чтобы обеспечить увеличение общего диаметра и диаметра просвета заданного сосуда или увеличение длины заданного сосуда, в том числе длины в распрямленном виде заданного сосуда.
[292] При условии потока крови Хагена-Пуазейля (то есть ламинарного потока с полностью установившимся параболическим профилем скорости) в просвете сосуда, имеющего круговое поперечное сечение, WSS можно определить, используя уравнение:
WSS (Па)=4Qμ/πR3, [Уравн. 1]
где:
Q=производительность (м3/с)
μ=вязкость крови (Па·с)
R=радиус сосуда (м)
Способ № 1 регулирования напряжения сдвига: вручную
[293] Среднее или максимальное значение WSS в заданном кровеносном сосуде можно изменять или поддерживать, регулируя скорость насоса, которая влияет на скорость кровотока через систему насоса-канала и, следовательно, кровотока через заданный сосуд. Как показано на фиг. 36А, способ 600 ручного регулирования может включать непосредственное измерение вязкости крови на этапе 602 (путем отбора пробы крови пациента и анализа ее в вискозиметре), скорости кровотока в перфузионной системе или скорости кровотока в заданном сосуде на этапе 604 (путем размещения ультразвукового датчика потока на приточном или выводном канале или с помощью способов ультразвуковой или термодилюции, соответственно) и радиуса сосуда на этапе 606 (с помощью различных способов визуализации, включая ангиографию, ультразвуковую, компьютерную томографию или магнитно-резонансную томографию). На этапе 608 определяют значение WSS, действующее на стенку сосуда, по сравнению с необходимым уровнем на этапах 610 или 612, а затем на этапах 614 или 616 производительность (Q) насоса регулируют посредством изменения скорости вращения крыльчатки насоса. Изменения в скорости насоса выполняют путем изменения рабочего цикла PWM входного напряжения двигателя.
Способ № 2 регулирования напряжения сдвига: автоматический с косвенными измерениями вязкости крови, прямого кровотока и диаметра заданного кровеносного сосуда.
[294] Автоматическая система управления WSS может включать непосредственное измерение скорости кровотока в насосной системе или заданном сосуде и непосредственное измерение диаметра заданного кровеносного сосуда. Как показано на фиг. 36В, указанный автоматический способ 620 управления WSS может включать косвенные измерения вязкости крови на этапе 622 (вычисляемой на основе известной связи с измеренным гематокритом и приблизительным средним значением WSS). Периодическая калибровка оценки вязкости на этапе 624 может быть выполнена с использованием непосредственных измерений вязкости, как описано выше. В клинической практике вязкость крови обычно незначительно изменяется в течение 1-2 недельного периода лечения.
Способ № 3 регулирования напряжения сдвига: автоматический с косвенными измерениями вязкости крови, кровотока, диаметра заданного кровеносного сосуда и непосредственными измерениями давления вены.
[295] Как показано на фиг. 36C, способ 630 автоматического регулирования WSS может включать косвенные измерения вязкости крови (вычисляемые на основе известной связи с измеренным гематокритом и приблизительным средним значением WSS) на этапе 622, скорости кровотока через перфузионную систему (вычисляемой на основе ее связи с переменными состояния двигателя) на этапе 632, измерения давления заданного кровеносного сосуда на этапе 634 и измерения радиуса сосуда (вычисляемого на основе сосудистого сопротивления) на этапе 638. Сосудистое сопротивление вычисляют на этапе 636 на основе вычисленной производительности насоса и измеренного кровяного давления в сосуде. Периодическая калибровка вязкости крови, потока насоса и оценочных значений радиуса заданного сосуда, соответственно, может выполняться с использованием непосредственных измерений на этапах 624, 640 и 642 соответственно, как описано выше.
Способ № 4 регулирования напряжения сдвига: автоматический с косвенными измерениями вязкости крови, кровотока, статического напора насоса и диаметра заданного кровеносного сосуда.
[296] Как показано на фиг. 36D, способ 650 автоматического регулирования WSS может включать косвенные измерения вязкости крови (вычисляемые на основе известной связи с измеренным гематокритом и приблизительным средним значением WSS) на этапе 622, скорости кровотока через перфузионную систему (вычисляемой на основе ее связи с переменными состояния двигателя) на этапе 632 и измерения радиуса сосуда (вычисляемого на основе сосудистого сопротивления) на этапе 638. На этапе 636 вычисляют сосудистое сопротивление, на основании производительности насоса, вычисленной на этапе 632, и статического напора насоса, при этом на этапе 652 также вычисляют статический напор насоса на основе его связи с переменными состояния двигателя. Периодическая калибровка вязкости крови, потока насоса и оценочных значений радиуса заданного сосуда может выполняться с использованием непосредственных измерений на этапах 624, 640 и 642 соответственно, как описано выше. Периодическая калибровка вычисленного значения статического напора насоса может быть выполнена на этапе 654 путем измерения давлений на впуске насоса и на выпуске насоса с помощью отдельных датчиков давления и вычисления разности их показаний, либо путем непосредственного измерения статического напора в насосе посредством датчика разности давлений.
Бессенсорное определение производительности и статического напора перфузионной системы
[297] Как показано на фиг. 35, процессор 24 выполнен с возможностью измерения и мониторинга электрического тока, возникающего в одной или нескольких электрических катушках узла 170 катушек насоса, посредством кабеля 120 питания, что в сочетании с мониторингом напряжения, подаваемого на узел катушек, позволяет процессору 24 выводить входную мощность (Pin), потребляемую перфузионным насосом 25, и фактическую скорость вращения крыльчатки 140 (ω). Процессор 24 может вычислять производительность (Q) насоса или изменения производительности (ΔQ) в зависимости от Pin и ω. Например, Q=f[Pin, ω]. В частности, используется следующее уравнение:
Q=a+b · ln(Pin)+c · ω0,5, [Уравн. 2]
где:
Q=производительность (л/мин)
Pin=Входная мощность двигателя (Вт)
ω=Скорость вращения насоса (об/мин)
Входная мощность двигателя выводится из измеренного тока и напряжения двигателя. Значения для a, b и c выводятся из кривой, соответствующей графику производительности насоса в зависимости от скорости двигателя и входной мощности.
[298] Процессор 24 может вычислять статический напор (Hp) насоса или изменения статического напора (ΔHp) насоса в зависимости от Pin и ω. Например, Hp=f[Pin,ω]. В частности, используется следующее уравнение:
Hp=d+e · ln(Pin)+f · ω2.5 [Уравн. 3]
Значение для d, e, и f выводят из аппроксимации кривой участка статического напора насоса в зависимости от скорости работы насоса и входной мощности двигателя, где Нр измеряют в приточном канале 20, насосе 25 и выводном канале 30.
Определение сосудистого сопротивления и вычисление радиуса сосуда
[299] Сосудистое сопротивление (Rv) представляет собой сопротивление потоку, которое должно преодолеваться для прохождения крови через систему кровообращения. Сопротивление равно вытесняющему давлению (Hv), разделенному на скорость потока. Когда перфузионная система подключена к заданному сосуду, который представляет собой вену, сосудистое сопротивление рассчитывают с использованием следующего уравнения:
Rv=(Pv- CVP)/Q [Уравн. 4]
где:
Hv=потеря статического напора в периферическом сосуде на пути возврата крови к сердцу (мм рт. ст.)
Pv=давление вены у анастомоза (мм рт. ст.)
CVP=венозное центральное давление (мм рт. ст.)
Rv=сосудистое сопротивление (мм рт. ст.·мин/л)
В большинстве случаев CVP находится в диапазоне от 2 до 8 мм рт. ст., и в приведенном выше уравнении им можно пренебречь, поскольку рабочие диапазоны Pv и Q пропорционально намного больше. Как показано на фиг. 36Е, сосудистое сопротивление может быть представлено графически как наклон различных кривых 660 Pv в сравнении с Q. Поскольку кривые 660 нелинейные, наклон является функцией Q. Как показано в следующем уравнении, сосудистое сопротивление может быть получено путем временного увеличения скорости вращения на несколько сотен об/мин (Δω), с измерением результирующего изменения давления в венах (ΔPv) и вычислением результирующего изменения производительности насоса (ΔQ):
Rv (Q)=ΔPv/ΔQ [Уравн. 5]
Следует заметить, что сосудистое сопротивление сильно зависит от диаметра или радиуса сосуда, то есть, при меньших венах сосудистое сопротивление велико. Сосудистое сопротивление можно количественно определить в разных единицах, например, единицы Вуда (мм рт. ст. ·мин/л) могут быть умножены на восемь для преобразования в единицы СИ (Па·с/м3).
[300] В качестве альтернативы, статический напор (Hp) насоса можно использовать в качестве основы для вычисления сосудистого сопротивления. Когда система насоса-канала выполнена с возможностью вывода крови из одного места в сосудистой системе для выпуска в периферическую артерию или вену, обосновано предположить, что статический напор, полученный во всей системе (Hp), в точности равен потере статического напора через периферический сосуд на пути возврата крови к сердцу (Hv):
Hv=Hp [Уравн. 6]
Радиус периферического сосуда обратно пропорционален его сосудистому сопротивлению (Rv), отношению Hv к Q. При условии кровотока Хагена-Пуазейля в сосуде с круглым поперечным сечением, сосудистое сопротивление может быть представлено с использованием уравнения:
Rv(Па·с/м3)=Pv/Q=8·μ·L/π·R4, [Уравн. 7]
где:
Pv выражено в единицах Па
Q выражено в единицах (м3/с)
μ=вязкость крови (Па·с)
R=радиус сосуда (м)
L=длина сосуда (м)
На практике уравнение 7 следовало бы уточнить на основе измерений in vivo перепада давления по конкретным венам известного диаметра. Это обеспечивает эмпирическую форму уравнения:
Rv(Па·с/м3)=K·μ/R4, [Уравн. 8]
где:
K - эмпирическая постоянная для заданной вены (м)
Определение напряжения сдвига стенки
[301] WSS в заданном сосуде можно определить на основе приведенных выше уравнений. Используя уравнение 4, производительность насоса может быть выражена в соответствии со следующим уравнением:
Q=Pv/Rv [Уравн. 9]
Используя уравнение 8, радиус сосуда может быть выражен в соответствии со следующим уравнением:
R

Используя уравнение 1, 9 и 10, значение WSS может быть выражено в соответствии со следующим уравнением:
WSS (Па)=((4·Pv)/(π·K0,75)) · (μ/Rv)0,25 [Уравн. 11]
[302] В некоторых вариантах реализации изобретения вычисляемые переменные, используемые системой управления, периодически калибруют. Например, вычисленную производительность и статический напор периодически калибруют с использованием фактических измеренных значений с интервалом от 1 минуты до 30 дней. Аналогично, вычисленный радиус артерии или вены периодически калибруют с использованием фактических измеренных значений с интервалом от 1 минуты до 30 дней.
Функции обеспечения безопасности и аварийные сигналы
[303] Система автоматического управления может также включать функции обеспечения безопасности, чтобы избежать опасностей, связанных с изменениями сердечнососудистой системы пациента или неисправностями насосной системы или системы управления насосом.Как показано на фиг. 36F, способ 670 регулирования скорости на этапе 672 может обнаруживать характерные изменения в форме сигнала тока двигателя, связанные с уменьшенной предварительной нагрузкой или увеличением постнагрузки (например, из-за тромбоза), всасыванием, ограничением потока и надвигающимся спадением сосуда возле наконечника 1000 приточного канала. На этапе 674 выполняют спектральный анализ формы сигнала тока двигателя с использованием преобразования Фурье. Когда амплитуда второго члена гармоники ряда Фурье на этапе 676 превышает заданное значение, происходит всасывание, и спадение считается надвигающимся. На этапе 616 скорость насоса немедленно уменьшается, и на этапе 678А в устройстве 21 управления срабатывает сигнал тревоги. Когда нормальная работа восстанавливается, на этапе 678В аварийный сигнал отменяется.
[304] Как показано на фиг. 36G, в способе 680 регулирования скорости можно обнаруживать условия низкого потока. Когда производительность насоса падает ниже безопасного порогового уровня, чтобы на этапе 682 избежать тромбоза системы 10 насоса-канала, на этапе 614 скорость работы насоса немедленно увеличивается, и на этапе 678А срабатывает сигнал тревоги в устройстве 21 управления. Когда нормальная работа восстанавливается, на этапе 678В аварийный сигнал отменяется.
[305] Как показано на фиг. 36H, способ 690 регулирования скорости может обнаруживать условия высокого WSS. Когда WSS возрастает выше безопасного порогового уровня, чтобы избежать повреждения стенки сосуда или эндотелия на этапе 692, на этапе 616 скорость насоса немедленно уменьшается, и на этапе 678А срабатывает сигнал тревоги в устройстве 21 управления. Когда нормальная работа восстанавливается, на этапе 678В аварийный сигнал отменяется.
[306] В еще одном варианте реализации изобретения, в котором приточный канал 20 соединен с артерией, а выводной канал 30 соединен с веной, система 14 управления отслеживает и изменяет пульсацию кровотока, который выпускается в принимающую вену. Например, система 14 управления может отслеживать электрокардиограмму или отслеживать циклические изменения пульсовой волны крови, поступающей в систему кровотока. Во время сокращения желудочков и распространения пульсовой волны система управления может уменьшать частоту вращения насоса. Во время систолы и после прохождения пульсовой волны система управления может увеличивать частоту вращения насоса. Таким образом, пульсация крови, поступающей в принимающую вену, может быть уменьшена. В качестве альтернативы, пульсация крови в принимающей вене может периодически проверяться вручную, что может быть выполнено с помощью ультразвука, и насос может регулироваться вручную, например, путем настройки характеристик пульсирующего выброса насоса, добавления податливого резервуара или эластичного резервуара (сегментное или диффузное изменение) к притоку или оттоку насоса, или модулирования скорости работы насоса. Также могут быть выполнены другие регулировки. В качестве альтернативы, податливый резервуар или эластичный резервуар могут быть добавлены к впускным или выводным каналам во время имплантации перфузионной системы.
[307] В некоторых вариантах реализации изобретения часть контроллера пациента системы 14 управления может содержать устройства для пациентов и медицинских работников для немедленного изменения скорости насоса в ответ на неотложные или возникающие события, такие как кровотечение или боль. Например, пациент или медицинский работник может остановить насос с помощью функции аварийного останова или изменить работу насоса в «безопасном режиме», в котором скорость насоса снижается, так что давление в канале и кровоток снижается, но кровоток через насосную систему остается на уровне, достаточном для работы без тромбоза. Эти средства могут дополнительно содержать систему для подачи команд пациентам или медицинским работникам, например, для немедленной медицинской помощи в ближайшей больнице или клинике.
[308] В некоторых вариантах реализации изобретения система 14 управления отслеживается и корректируется вручную или с помощью программно реализованной программы или приложения, зашифрованного на машиночитаемом носителе и исполняемого процессором 24 или другими автоматизированными системами. Машиночитаемый носитель может включать энергозависимые носители, энергонезависимые носители, съемные носители, несъемные носители и/или другой доступный носитель, к которому может обращаться система 14 управления. В качестве примера, а не ограничения, машиночитаемый носитель может включать компьютерные запоминающие устройства и средства связи. Компьютерные запоминающие устройства включают память, энергозависимые носители, энергонезависимые носители, съемные носители и/или несъемные носители, реализованные способом или методом для хранения информации, такие как машиночитаемые инструкции, структуры данных, программные модули или другие данные.
[309] Программно реализованная программа может включать выполняемые команды для автоматической регулировки скорости работы насоса для поддержания требуемого количества кровотока, средней скорости крови, максимальной скорости крови и среднего значения WSS или максимального значения WSS в сегменте сосуда, подлежащего лечению («заданного сосуда» или «заданного кровеносного сосуда», в котором требуется устойчивое увеличение общего диаметра и диаметра просвета, длины или длины в распрямленном виде, будь то передающая артерия, передающая вена, принимающая артерия или принимающая вена. В качестве альтернативы, общий диаметр, диаметр просвета, длина, длина в распрямленном виде и кровоток в заданном сосуде могут периодически проверяться вручную, что может быть выполнено с помощью ультразвука, и насос может регулироваться вручную, например, путем настройки напорных характеристик насоса или модулирования скорости насоса. Также могут быть выполнены другие регулировки.
[310] В одном варианте реализации изобретения среднюю скорость крови определяют путем вычисления среднего числа отдельных измерений скорости крови с помощью суммирования отдельных измерений и деления суммы на количество измерений. Средняя скорость крови может быть вычислена путем измерений в течение нескольких миллисекунд, секунд, 1 минуты, 5 минут, 15 минут, 30 минут, 1 часа или нескольких часов.
[311] В другом варианте реализации изобретения среднее значение WSS определяют путем проведения ряда отдельных измерений, выполнения множества отдельных подсчетов WSS (с использованием этих измерений), суммирования отдельных подсчетов WSS и деления общего числа на количество подсчетов. Среднее значение WSS крови может быть вычислено путем измерений и выполнения отдельных подсчетов WSS в течение секунд, 1 минуты, 5 минут, 15 минут, 30 минут, 1 часа или нескольких часов.
[312] В одном варианте реализации изобретения система 14 управления принимает информацию от датчика 22, сообщающегося с перфузионным насосом 25. В других вариантах реализации изобретения система 14 управления принимает информацию от датчика 22, сообщающегося с приточным каналом 20 или выводным каналом 30, или находящегося в сосуде, сообщающемся по текучей среде с приточным или выводным каналом. В некоторых вариантах реализации изобретения система 14 управления полностью или частично может быть расположена внутри корпуса 25 насоса, в то время как в других вариантах реализации изобретения система управления полностью или частично может быть расположена внутри каналов или внутри устройства 21 управления.
[313] Описанные в настоящем документе системы и способы повышают средний уровень WSS в периферических венах и артериях. Нормальное среднее значение WSS для вен колеблется между 0,076 и 0,76 Па. Описанные в настоящем документе системы выполнены с возможностью увеличения среднего уровня WSS в принимающей периферической вене до диапазона между 0,76 Па и 23 Па, предпочтительно до диапазона между 2,5 Па и 10 Па. Нормальное среднее значение WSS для артерий колеблется между 0,3 Па и 1,5 Па. Для расширения артерии системы и способы, описанные в настоящем документе, увеличивают средний уровень WSS до диапазона от 1,5 Па до 23 Па, предпочтительно до диапазона от 2,5 Па до 10 Па. Устойчивое среднее WSS, превышающее 23 Па в артериях или венах, может вызвать или продлить денудацию (потерю) эндотелия кровеносных сосудов или повреждение эндотелия, что, как известно, замедляет расширение кровеносных сосудов в ответ на увеличение средней скорости крови и среднего значения WSS. Перекачивание крови способом, который увеличивает среднее значение WSS до требуемого диапазона, предпочтительно от 1 дня до 84 дней, и более предпочтительно, примерно между 7 и 42 днями, например, вызывает устойчивое увеличение общего диаметра и диаметра просвета в принимающей вене, передающей вене или передающей артерии или принимающей артерии, так что вены и артерии, которые изначально были непригодными или неоптимальными для использования в качестве участков доступа для гемодиализа или шунтирующих трансплантатов из-за малого диаметра вены или артерии, становятся пригодными или более оптимальными. Процесс перекачивания крови может отслеживаться и периодически корректироваться. Например, насос может регулироваться в течение минут, часов, 1 дня, 3 дней, 1 недели или нескольких недель для учета изменений периферической вены или артерии (таких как постоянное увеличение общего диаметра и диаметра просвета) до достижения требуемого уровня устойчивого расширения.
[314] Как показано на фиг. 37-40, система 10 для увеличения общего диаметра и диаметра просвета вен и артерий показана на примере пациента. На фиг. 37 система 10 извлекает венозную кровь, в том числе бедную кислородом кровь, из венозной системы пациента и выводит эту кровь в принимающий периферийный сосуд 700. Система 10 также увеличивает среднюю скорость крови в принимающем периферическом сосуде 700 и увеличивает среднее значение WSS на эндотелии принимающего периферийного сосуда 700, для увеличения общего диаметра и диаметра просвета принимающего периферийного сосуда 700, расположенного, например, в руке или ноге. Диаметр кровеносных сосудов, таких как периферические вены, можно определить, путем измерения диаметра просвета, представляющего собой пространство в центре кровеносного сосуда, в котором протекает кровь, или путем измерения диаметра всего сосуда, который включает открытое пространство и стенки кровеносного сосуда.
[315] Изобретение также относится к одновременному и постоянному увеличению диаметра и диаметра просвета периферической вены или артерии путем направления крови в периферическую вену или артерию, или из нее, тем самым увеличивая среднюю скорость крови в периферической вене или артерии и увеличения средней WSS на эндотелии периферической вены или артерии. Описаны системы, в которых средняя скорость крови в периферической вене или артерии и среднее значение WSS на эндотелии периферической вены или артерии увеличивается с использованием перфузионной системы. Предпочтительно насос направляет кровь в периферическую вену, где перекачиваемая кровь уменьшает пульсацию, например, когда пульсовое давление ниже, чем давление кровь в периферической артерии.
[316] Система 10 подходит для поддержания скорости потока предпочтительно между 50 и 2500 мл/мин и, необязательно, от 50 до 1500 мл/мин или от 100 до 1000 мл/мин, при этом поддерживая диапазон давления в выпускном канале от 10 до 350 мм рт. ст., предпочтительно от 25 до 100 мм рт. ст. Как описано выше, система 14 управления может быть оптимизирована для поддержания устойчивого среднего значения WSS между 0,76 и 23 Па, предпочтительно между 2,5 и 10 Па или между 2,5 и 7,5 Па, в периферических венах, так что общий диаметр и диаметр просвета периферических вен устойчиво увеличивается от более чем 5% до более чем 500%.
[317] Описанные в настоящем документе системы также увеличивают среднюю скорость крови в периферических венах. В состоянии покоя средняя скорость крови в головной вене человека (при среднем диаметре просвета 2,4 ± 0,5 мм) обычно составляет от 5 до 9 см/с (0,05-0,09 м/с). Для описанных в настоящем документе систем средняя скорость крови в периферической вене увеличивается до диапазона между 9 и 235 см/с (0,09 и 2,35 м/с), предпочтительно до диапазона между 15 и 100 см/с (0,15 и 1,0 м/с), в зависимости от исходного общего диаметра или диаметра просвета периферической принимающей вены и требуемого конечного общего диаметра или диаметра просвета. Описанные в настоящем документе системы также увеличивают среднюю скорость крови в периферических артериях. В состоянии покоя средняя скорость крови в плечевой артерии человека (при среднем диаметре просвета 3,7 ± 0,7 мм) обычно составляет от 10 до 15 см/с (0,1-0,15 м/с). Для описанных в настоящем документе систем средняя скорость крови в периферической артерии увеличивается до диапазона между 15 и 360 см/с (0,1 и 3,6 м/с), предпочтительно до диапазона между 25 и 160 см/с (0,25 и 1,6 м/с), в зависимости от исходного общего диаметра или диаметра просвета периферической артерии и требуемого конечного общего диаметра или диаметра просвета.
[318] Предпочтительно средняя скорость крови увеличивается в течение от 1 дня до 84 дней или предпочтительно между 7 и 42 днями, чтобы создать устойчивое увеличение общего диаметра и диаметра просвета в периферической принимающей вене, периферической принимающей артерии, периферической передающей вене или периферической передающей артерии, так что вены и артерии, которые были первоначально не пригодными или неоптимальными для использования в качестве места доступа для гемодиализа или шунтирующего трансплантата из-за малого диаметра вены или артерии, становятся пригодными или более оптимальными. Это также может быть достигнуто путем периодического увеличения средней скорости крови в течение периода лечения с промежуточными периодами нормальной средней скорости крови.
[319] Исследования показали, что базовые гемодинамические силы и изменения в гемодинамических силах внутри вен и артерий играют жизненно важную роль в определении общего диаметра и диаметра просвета, а также длины этих вен и артерий. Например, постоянное увеличение средней скорости крови и среднего значения WSS может привести к постоянному увеличению диаметра просвета и общего диаметра, длины и длины в распрямленном виде вен и артерий. Повышенная средняя скорость крови и среднее значение WSS ощущаются эндотелиальными клетками, которые запускают механизмы сигнализации, приводящие к стимуляции клеток гладких мышц сосудов, привлечению моноцитов и макрофагов, а также синтезу и высвобождению протеаз, способных разрушать компоненты внеклеточного матрикса, такие как коллаген и эластин. Таким образом, настоящее изобретение относится к увеличению средней скорости крови и среднего значения WSS в течение периода времени, достаточного для ремоделирования вены и артерии, увеличения общего диаметра и диаметра просвета, длины и длины в распрямленном виде вен и артерий.
[320] Описанные в настоящем документе системы увеличивают средний уровень WSS в периферической вене или артерии. Нормальное среднее значение WSS для вен колеблется между 0,076 и 0,76 Па. Описанные в настоящем документе системы увеличивают средний уровень WSS в венах до диапазона между 0,76 и 23 Па, предпочтительно до диапазона от 2,5 до 10 Па или от 2,5 до 7,5 Па. Нормальное среднее значение WSS для артерий колеблется между 0,3 Па и 1,5 Па. Для устойчивого увеличения общего диаметра и диаметра просвета артерий описанные в настоящем документе системы и способы увеличивают средний уровень WSS до диапазона от 1,5 до 23 Па, предпочтительно до диапазона от 2,5 до 10 Па или от 2,5 до 7,5 Па. Предпочтительно среднее значение WSS увеличивается в течение от 1 дня до 84 дней или предпочтительно между 7 и 42 днями, чтобы создать устойчивое увеличение общего диаметра и диаметра просвета в периферической принимающей вене, периферической принимающей артерии, периферической передающей вене или периферической передающей артерии, так что вены и артерии, которые были первоначально непригодными или неоптимальными для использования в качестве места доступа для гемодиализа или шунтирующего трансплантата из-за малого диаметра вены или артерии, становятся пригодными или более оптимальными. Это также может быть достигнуто путем периодического увеличения среднего значения WSS в течение периода лечения с промежуточными периодами нормального среднего значения WSS.
[321] Устойчивые средние уровни WSS в периферических венах и артериях, большие, чем примерно 23 Па, могут вызывать или продлевать денудацию (потерю) эндотелия вен или повреждение эндотелия или стенки вен. Известно, что денудация эндотелия или повреждение эндотелия или стенки кровеносных сосудов уменьшает увеличение общего диаметра и диаметра просвета кровеносных сосудов при увеличении средней скорости крови и увеличении среднего значения WSS. Увеличенное среднее значение WSS вызывает достаточное устойчивое увеличение общего диаметра и диаметра просвета, длины или длины в распрямленном виде в венах и артериях, так что те из них, которые первоначально были непригодными или неоптимальными для использования в качестве места доступа для гемодиализа или шунтирующего трансплантата из-за малого диаметра вены или артерии, становятся пригодными или более оптимальными. Диаметр периферической принимающей вены, периферической принимающей артерии, периферической передающей вены или периферической передающей артерии может определяться периодически, например, каждый 1 день, 3 дня, 1 неделю или несколько недель, например, чтобы обеспечить регулировку скорости работы насоса до оптимальной скорости, и степень устойчивого увеличения общего диаметра и диаметра просвета вены и артерии в течение периода лечения.
[322] Описанные в настоящем документе системы также увеличивают среднюю скорость крови в периферических венах. В состоянии покоя средняя скорость крови в головной вене человека (при среднем диаметре просвета 2,4 ± 0,5 мм) обычно составляет от 5 до 9 см/с (0,05-0,09 м/с). Для описанных в настоящем документе систем средняя скорость крови в периферической вене увеличивается до диапазона от 9 до 235 см/с (0,09-2,35 м/с), предпочтительно до диапазона от 15 до 100 см/с (0,15-1,0 м/с), в зависимости от исходного общего диаметра или диаметра просвета периферической принимающей вены и требуемого конечного общего диаметра и диаметра просвета периферической принимающей вены. Описанные в настоящем документе системы также увеличивают среднюю скорость крови в периферических артериях. В состоянии покоя средняя скорость крови в плечевой артерии человека (при среднем диаметре просвета 3,7 ± 0,7 мм) обычно составляет 10-15 см/с (0,1-0,15 м/с). Для описанных в настоящем документе систем и способов средняя скорость крови в периферической артерии увеличивается до диапазона от 15 до 360 см/с (0,1- 3,6 м/с), предпочтительно до диапазона от 25 до 160 см/с (0,25-1,6 м/с), в зависимости от исходного общего диаметра или диаметра просвета периферической артерии и требуемого конечного общего диаметра или диаметра просвета периферической артерии. Предпочтительно средняя скорость крови увеличивается в течение от 1 дня до 84 дней или предпочтительно между 7 и 42 днями, чтобы создать устойчивое увеличение общего диаметра и диаметра просвета или длины в периферической принимающей вене, периферической принимающей артерии, периферической передающей вене или периферической передающей артерии, так что вены и артерии, которые были первоначально не пригодными или неоптимальными для использования в качестве места доступа для гемодиализа или шунтирующего трансплантата из-за малого диаметра вены или артерии или неподходящей длины, становятся пригодными. Средние уровни скорости крови в периферической принимающей или передающей вене, большие, чем 160-235 см/с (0,16-2,35 м/с) или средние уровни скорости крови в периферической принимающей или передающей артерии, большие, чем 250-360 см/с (0,25-0,36 м/с), могут вызвать или продлить денудацию (потерю) эндотелия вен или повреждение эндотелия вен. Известно, что денудация или повреждение эндотелия или стенки кровеносных сосудов уменьшает увеличение общего диаметра и диаметра просвета кровеносных сосудов, наблюдаемого при установлении увеличенной средней скорости крови. Увеличенная средняя скорость крови в требуемом диапазоне и в течение достаточного периода времени вызывает достаточное устойчивое увеличение общего диаметра и диаметра просвета, или длины в венах и артериях, так что те из них, которые первоначально были непригодными или неоптимальными для использования в качестве места доступа для гемодиализа или шунтирующего трансплантата из-за малого диаметра или неподходящей длины вены или артерии, становятся пригодными или более оптимальными. Общий диаметр или диаметр просвета периферической принимающей вены, периферической принимающей артерии, периферической передающей вены или периферической передающей артерии может определяться периодически, например, каждую минуту (минуты), час (часы), 1 день, 3 дня, 1 неделю или несколько недель, например, чтобы обеспечить регулировку скорости работы насоса до оптимальной скорости, и степень устойчивого увеличения общего диаметра и диаметра просвета заданной вены и артерии в течение периода лечения.
[323] В одном варианте реализации изобретения, показанном на фиг. 34, система 10 содержит перфузионный насос 25, пару каналов 12 и устройство 21 управления для перемещения венозной крови из передающей вены или места в венозной системе пациента в периферическую принимающую вену. В некоторых вариантах реализации изобретения периферическая принимающая вена может представлять собой головную вену, лучевую вену, серединную вену предплечья, локтевую вену, боковую подкожную вену руки, головную серединную вену, промежуточную медианную вену, медиальную подкожную вену руки, плечевую вену, малую подкожную вену ноги, большую подкожную вену ноги, бедренную вену, или другие вены. Могут быть использованы другие вены, которые могут быть полезны при создании мета доступа для гемодиализа или шунтирующего трансплантата, или другие вены, пригодные для других процедур сосудистой хирургии, требующих использования вен. Каналы 12 перемещают кровь в периферическую принимающую вену. Устойчиво повышенная средняя скорость крови и повышенное среднее значение WSS в периферическом сосуде вызывает устойчивое и прогрессирующее увеличение общего диаметра и диаметра просвета периферической принимающей вены. Таким образом, система 10 согласно настоящему изобретению преимущественно увеличивает диаметр, длину или длину в распрямленном виде периферической вены 4, так что ее можно использовать, например, для создания места доступа для гемодиализа (например, AVF или AVG), шунтирующего трансплантата, или использовать в других клинических условиях, в которых необходима вена определенного диаметра или длины, как определяет специалист в данной области.
[324] В контексте настоящего документа, бедная кислородом кровь представляет собой кровь, прошедшую через капиллярную систему, из которой кислород удален окружающими тканями, а затем переходящую в венозную систему. Периферическая вена в контексте настоящего документа означает любую вену с участком, находящимся вне грудной клетки, брюшной полости или таза. В варианте реализации изобретения, показанном на фиг. 37А, периферийная принимающая вена 712 представляет собой головную вену. Однако в других вариантах реализации изобретения периферическая принимающая вена может представлять собой лучевую вену, серединную вену предплечья, локтевую вену, боковую подкожную вену руки, головную серединную вену, промежуточную медианную вену, медиальную подкожную вену руки, плечевую вену, малую подкожную вену ноги, большую подкожную вену ноги, бедренную вену, или другие вены. В дополнение к периферической вене могут быть использованы другие вены, которые могут быть полезны при создании места доступа для гемодиализа или шунтирующего трансплантата, или в качестве принимающих вен также могут быть использованы другие вены, пригодные для других процедур сосудистой хирургии, требующих использования вен, например, находящиеся в грудной клетке, брюшной полости или тазе.
[325] На фиг. 37B показан другой вариант реализации изобретения для использования системы 10 для увеличения общего диаметра и диаметра просвета кровеносного сосуда. В этом варианте реализации изобретения система 10 выполнена с возможностью удаления крови из передающей вены 700, включая бедную кислородом кровь, и перемещения крови в верхнюю полую вену или правое предсердие 702 сердца 704. Как показано, приточный канал 706 соединен с сообщением по текучей среде с передающей веной 700, в этом случае головной веной. В одном варианте реализации изобретения соединение может быть выполнено с использованием короткого сегмента из ePTFE приточного канала 706, который используется для крепления приточного канала 706 к передающей вене 700, в то время как остальная часть сегмента приточного канала выполнена с использованием полиуретана. В других вариантах реализации изобретения по меньшей мере часть приточного канала или выводного канала дополнительно содержит нитинол для обеспечения устойчивости к изгибу и сжатию. Как показано, один конец выводного канала 710 соединен с перфузионным насосом 25, в то время как другой конец выводного канала сообщается по текучей среде с верхней полой веной и правым предсердием 702 посредством внутрисосудистого участка. В других вариантах реализации изобретения один или оба сегмента выводного канала 706 дополнительно содержат нитинол, для обеспечения устойчивости к изгибу и сжатию. Для варианта реализации изобретения по фиг. 37 использован перфузионный насос, увеличивающий скорость, с которой кровь перемещается от передающей вены 700 к верхней полой вене и правому предсердию 702 сердца 704 для достижения требуемого повышенного уровня средней скорости крови и повышенного уровня среднего значения WSS в передающей вене 700. Насос работает со скоростью и в течение времени, достаточного для достижения требуемого устойчивого увеличения общего диаметра и диаметра просвета передающей вены, например, увеличения на 10%, увеличения на 25%, увеличения на 50% увеличения на 100%, увеличения на 200%, увеличения на 300% или увеличения на 300% от первоначального диаметра. В другом варианте реализации изобретения один или более венозных клапанов между соединением приточного канала 706 и передающей вены 700 и правым предсердием 702 могут оказаться неработоспособными или менее работоспособными (с использованием любого из способов, доступных специалисту в данной области) для обеспечения прохождения крови в ретроградном режиме в передающую вену 700, а затем в приточный канал 706.
[326] На фиг. 38 показан другой вариант реализации изобретения для использования системы 10 для увеличения общего диаметра и диаметра просвета кровеносного сосуда. В этом варианте реализации изобретения система 10 выполнена с возможностью удаления крови из передающей артерии 712, включая насыщенную кислородом кровь (в данном случае плечевой артерии), и перемещения крови в верхнюю полую вену или правое предсердие 702 сердца 704. Как показано, приточный канал 706 соединен с сообщением по текучей среде с передающей артерией 712. В одном варианте реализации изобретения соединение может быть выполнено с использованием короткого сегмента из ePTFE приточного канала 706, который используется для крепления приточного канала к передающей артерии 712, в то время как остальной сегмент приточного канала выполнен с использованием полиуретана. В других вариантах реализации изобретения один или оба сегмента приточного канала 706 дополнительно содержат нитинол, например, для обеспечения устойчивости к изгибу и сжатию. Как показано, один конец выводного канала 710 соединен с перфузионным насосом 25, в то время как другой конец выводного канала сообщается по текучей среде с верхней полой веной и правым предсердием 702 посредством внутрисосудистого участка. В других вариантах реализации изобретения один или оба сегмента выводного канала 706 дополнительно содержат нитинол, для обеспечения устойчивости к изгибу и сжатию. Для варианта реализации изобретения по фиг. 38 использован перфузионный насос, увеличивающий скорость, с которой кровь перемещается от передающей артерии 712 к правому предсердию 702 сердца 704 для достижения требуемого повышенного уровня средней скорости крови и повышенного среднего уровня WSS в передающей артерии 712. Насос работает со скоростью и в течение времени, достаточного для достижения требуемого устойчивого увеличения общего диаметра и диаметра просвета передающей артерии, например, увеличения на 10%, увеличения на 25%, увеличения на 50%, увеличения на 100%, увеличения на 200%, увеличения на 300% или увеличения на 300% от первоначального диаметра.
[327] В других вариантах реализации изобретения артериальная кровь, включая насыщенную кислородом кровь, может перемещаться из передающей артерии в место приема. Передающие артерии могут включать в себя, но не ограничиваются ими, лучевую артерию, локтевую артерию, межкостную артерию, плечевую артерию, переднюю большеберцовую артерию, заднюю большеберцовую артерию, малоберцовую артерию, подколенную артерию, глубокую артерию, поверхностную бедренную артерию или бедренную артерию.
[328] На фиг. 39 показан другой вариант реализации изобретения для использования системы 10 для увеличения общего диаметра и диаметра просвета кровеносного сосуда. В этом варианте реализации изобретения система 10 выполнена с возможностью удаления крови из передающей артерии 712, включая насыщенную кислородом кровь (в данном случае плечевой артерии), и перемещения крови в верхнюю полую вену или правое предсердие 702 сердца 704. Как показано, канал 716 соединен с сообщением по текучей среде с передающей артерией 712. В одном варианте реализации изобретения соединение может быть выполнено с использованием короткого сегмента из ePTFE канала 716, который используется для крепления приточного канала к передающей артерии 712, в то время как остальная часть сегмента приточного канала выполнена с использованием полиуретана. В других вариантах реализации изобретения один или оба сегмента канала 716 дополнительно содержат нитинол, например, для обеспечения устойчивости к изгибу и сжатию. Для варианта реализации изобретения по фиг. 39 насос отсутствует, и кровь пассивно перемещается из передающей артерии 712 с более высоким давлением в верхнюю полость вены и правое предсердие 702 с более низким давлением, а канал 716 выполнен с такой длиной и диаметром просвета, чтобы достигать требуемого повышенного уровня средней скорости крови и среднего значения WSS в передающей артерии 712. Канал 716 остается на месте в течение времени, достаточного для достижения требуемого устойчивого увеличения общего диаметра и диаметра просвета передающей артерии 712, например, увеличения на 10%, увеличения на 25%, увеличения на 50% или увеличения на 100% или более от первоначального диаметра.
[329] На фиг. 40 показан другой вариант реализации изобретения для использования системы 10 для увеличения общего диаметра и диаметра просвета периферической артерии. В этом варианте реализации изобретения система 10 выполнена с возможностью удаления крови из заданной артерии 718, включая насыщенную кислородом кровь, например, из лучевой артерии, и перемещения крови в принимающую артерию 720, такую как плечевая артерия. Как показано, приточный канал 706 соединен с сообщением по текучей среде с заданной артерией 718. В одном варианте реализации изобретения соединение между приточным каналом 706 и артерией или отводным каналом 710 и артерией может быть выполнено с использованием короткого сегмента из ePTFE соответствующего канала, который используется для сообщения по текучей среде приточного канала с заданной артерией 718 или отводным каналом 710, который сообщается по текучей среде с принимающей артерией 720, в то время как остальные сегменты приточных и отводных каналов могут быть изготовлены с использованием полиуретана. В других вариантах реализации изобретения один или оба сегмента приточного канала 706 или выводного канала 710 дополнительно содержат нитинол, например, для обеспечения устойчивости к изгибу и сжатию.
[330] Как показано, один конец выводного канала 710 соединен с перфузионным насосом 25, в то время как другой конец выводного канала сообщается по текучей среде с принимающей артерией 720. Для варианта реализации изобретения по фиг. 40 использован перфузионный насос 25 крови, увеличивающий скорость, с которой кровь выводится из заданной артерии 718, для достижения требуемого повышенного уровня средней скорости крови и повышенного среднего уровня WSS в заданной артерии. Насос работает со скоростью и в течение времени, достаточного для достижения требуемого устойчивого увеличения общего диаметра и диаметра просвета заданной артерии 718, например, увеличения на 10%, увеличения на 25%, увеличения на 50% или увеличения на 100% или более от первоначального диаметра.
[331] Как показано на фиг. 44A-D, насосная система 10 также может быть использована для увеличения возврата венозной крови из нижней конечности к сердцу, уменьшения венозной гипертензии нижних конечностей и заживления венозных язв путем перекачивания венозной крови из нижней конечности, такой как нога, в другое место в венозном кровообращении, в данном случае, верхнюю полую вену и правое предсердие.
[332] В одном варианте реализации изобретения, как показано на фиг. 45А, приточный канал 20 содержит несущую конструкцию из нитинола, гидрофильное покрытие и связанный сегмент 503 из ePTFE, который выполнен с возможностью формирования анастомоза 290 в бедренной вене 292. Спадение и окклюзия на наконечнике 1000 приточного канала могут быть предотвращены с использованием алгоритма обнаружения всасывания, как показано на фиг. 36F, чтобы регулировать скорость насоса и/или упрочненную спиралью секцию трансплантата из ePTFE, как показано на фиг. 31, чтобы препятствовать спадению при давлениях ниже атмосферного. Выводной канал 30 также содержит несущую конструкцию из нитинола, гидрофильное покрытие и не упрочненный сегмент 509 с боковыми выпускными отверстиями, выполненными с возможностью введения в полую верхнюю вену и правое предсердие, как показано на фиг. 45В.
[333] Могут быть использованы различные конфигурации устройства 21 управления. Например, насосная система 10 может регулироваться посредством небольшого переносного устройства 21 управления, оптимизированным для использования амбулаторными пациентами, как показано на фиг. 46А, которое пациент может носить на поясе, в кармане или носить в переносном футляре во время лечения. Переносное устройство 21 управления может содержать перезаряжаемые аккумуляторы для обеспечения питания насоса 25 через проводник 120. Устройство 21 управления может также представлять данные о состоянии системы пациенту и регулировать скорость работы насоса и другие параметры системы на основе положения тела пациента (например, стоя или лежа и т. п.) или кровяное давление в приточном канале 20, выводном канале 30, в сегменте вены, примыкающем к приточному каналу или выводному каналу. В другом варианте реализации изобретения устройство 21 управления может быть более крупным базовым блоком, оптимизированным для использования амбулаторными пациентами в больницах или клиниках, или для ночного использования дома амбулаторными пациентами, как показано на фиг. 46B, и может быть выполнено с возможностью размещения на столе при питании от сети переменного тока или на тележке при питании от аккумуляторных батарей.
[334] В одном аспекте насосная система 10 может транспортировать венозную кровь из нижней конечности в другое место в венозной системе для снижения венозного давления нижней конечности и способствовать заживлению изъязвления примерно через три месяца использования, как показано на фиг. 44С. Насосная система 10 может быть удалена после полного заживления язвы, как показано на фиг. 44D.
[335] В некоторых вариантах реализации устройства 21 управления, как показано на фиг. 46A-B, процессор 24 для управления насосом 25 может быть расположен внутри насоса. Размещение процессора 24 внутри насоса 25 уменьшает проводку, расположенную внутри шнура питания 120. Это уменьшение улучшает возможность определения времени коммутации посредством обратной EMF, которая поступает из невозбужденной ветви при трехфазной конфигурации обмотки двигателя.
[336] Один вариант реализации устройства 21 управления, как показано на фиг. 46B, который включает базовый блок, питаемый от сети переменного тока и оптимизированный для использования в больницах или клиниках не амбулаторными пациентами, связан к перфузионным насосом 25 с помощью кабеля 120, как показано на фиг. 47А. В указанном варианте реализации изобретения процессор 24 и источник питания 26 расположены внутри устройства 21 управления. Поскольку длинный кабель 120 может выступать в качестве антенны, любые сигналы коммутации двигателя, создаваемые перфузионным насосом 25, которые должны приниматься в устройстве 21 управления, а также любые импульсы переменного тока переменного тока двигателя, создаваемые в устройстве управления, которые должны поступать к перфузионному насосу, очень восприимчивы к радиочастотным (radio frequency, RF) помехам. Поэтому для обеспечения надежной работы необходимо уделять внимание экранированию радиочастот и заземлению компонентов.
[337] В вариантах реализации устройства 21 управления и насоса 25, в которых процессор 24 находится в непосредственной близости от насоса, независимо от того, находится ли он внутри корпуса 105 перфузионного насоса, как показано на фиг. 47B, или по меньшей мере подключен в линии между кабелем 120 и перфузионным насосом, влияние радиочастотных помех уменьшается. В этих вариантах реализации изобретения постоянный ток, подаваемый по кабелю 120, в меньшей степени зависит от радиочастотных помех.
[338] В других вариантах реализации устройства 21 управления, как показано на фиг. 46A, которое содержит переносной блок с батарейным питанием, оптимизированный для использования амбулаторными пациентами, используется более короткий кабель 120, который менее восприимчив к радиочастотным помехам. Таким образом, процессор 24 может находиться либо в устройстве 21 управления, либо в насосе 25.
Приточные каналы
[339] Настоящее изобретение относится к проектированию, изготовлению и использованию каналов для транспортировки крови. Когда канал для транспортировки крови принимает кровь из артерии, вены, камеры сердца или другой структуры, содержащей кровь, и передает кровь в насос, тогда в настоящем документе канал может называться «приточным каналом», «дренажным каналом», «дренажной канюлей» или «каналом».
[340] Настоящее изобретение также относится к проектированию, изготовлению и использованию ближнего и дальнего сегментов приточных каналов. Такие приточные каналы (или каналы) могут содержать i) ближний сегмент канала, который может быть гибким, упругим и устойчивым к сжатию и изгибу; ii) дальний сегмент канала, который может быть гибким, упругим и устойчивым к сжатию и изгибу; iii) дальний наконечник канала, который может быть гибким, упругим и устойчивым к сжатию и изгибу, или может быть жестким, или может иметь гибкие и упругие зоны и жесткие зоны; и iv) один или более боковых каналов, которые могут быть гибкими, упругими и устойчивыми к сжатию и изгибу, или могут быть жесткими, или могут иметь гибкие и упругие зоны и жесткие зоны.
[341] Дальний наконечник канала можно использовать с разнообразными сегментами канала. Каналы могут быть полностью собранными перед имплантацией, частично собранными перед имплантацией, или могут быть собраны во время процедуры имплантации или операции. Ближний конец дальнего наконечника канала может быть выполнен с возможностью крепления или может быть прикреплен к ближнему сегменту канала, дальнему сегменту канала, или к боковому каналу. В некоторых вариантах реализации изобретения боковой канал, ближний сегмент канала, дальний сегмент канала и дальний наконечник канала соединены друг с другом до операции или процедуры имплантации. В других вариантах реализации изобретения боковой канал, ближний сегмент канала, дальний сегмент канала и дальний наконечник канала выполнены с возможностью соединения, и соединяются друг с другом во время операции или процедуры имплантации при настройке перфузионной системы для использования. В некоторых вариантах реализации изобретения ближний сегмент канала, дальний сегмент канала и дальний наконечник канала соединены друг с другом до операции или процедуры имплантации. В других вариантах реализации изобретения ближний сегмент канала, дальний сегмент канала и дальний наконечник канала выполнены с возможностью соединения, и соединяются друг с другом во время операции или процедуры имплантации при настройке перфузионной системы для использования. В некоторых вариантах реализации изобретения ближний сегмент канала и дальний наконечник канала соединены друг с другом до операции или процедуры имплантации. В других вариантах реализации изобретения ближний сегмент канала и дальний наконечник канала выполнены с возможностью соединения, и соединяются друг с другом во время операции или процедуры имплантации при настройке перфузионной системы для использования.
[342] В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) боковой канал, ближний сегмент канала, дальний сегмент канала и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, боковой канал, дальний сегмент канала и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, дальний сегмент канала, боковой канал и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, дальний сегмент канала и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, боковой канал и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) боковой канал, ближний сегмент канала и дальний сегмент канала, при этом дальний наконечник канала объединен с дальним концом дальнего сегмента канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, боковой канал и дальний сегмент канала, при этом дальний наконечник канала объединен с дальним концом дальнего сегмента канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала и дальний сегмент канала, при этом дальний наконечник канала объединен с дальним концом дальнего сегмента канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, при этом дальний наконечник канала объединен с дальним концом ближнего сегмента канала.
[343] Настоящее изобретение относится к конфигурациям и способам соединения отдельных компонентов приточных каналов. Отдельные компоненты приточных каналов могут быть выполнены с возможностью соединения или могут быть соединены различными способами. Различные конфигурации и способы могут включать в себя фрикционную посадку; фитинг с кольцевыми зубцами; радиально сжимающий фиксатор или фиксирующее кольцо, встроенный в линию соединитель с одним или более фитингами с кольцевыми зубцами и радиально сжимающими фиксаторами или фиксирующими кольцами, или клеем.
[344] В некоторых вариантах реализации изобретения ближний или дальний сегменты канала могут быть выполнены, выполнены в основном или выполнены по существу из гибких или упругих полимеров. Такие гибкие или упругие полимеры включают полиуретаны, полиуретаны Pellethane®, полиуретаны Carbothane®, Carbothane® PC-3575A с твердостью по Шору 70A, ароматические полиуретановые эластомерные сплавы, ароматические полиуретановые эластомерные сплавы Polyblend 1100, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 45A, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 55A, поливинилхлориды, полиэтилены, силиконовые эластомеры, политетрафторэтилены, вспененный политетрафторэтилен, полиэтилентерефталаты, эластомеры из термопластичного кремнийорганического поликарбоната, полиэфирблокамиды и их комбинации с твердостью по Шору в диапазоне от 20A до 80A, от 20A до 30A, от 30A до 40A, от 40A до 50A, от 50A до 60A, от 60A до 70A, от 70A до 80, или с твердостью по Шору 20A, 25A, 30A, 35A, 40A, 45A, 50A, 55A, 60A, 65A, 70A, 75A, или 80A. Сегменты канала могут содержать проволочную или сетчатую несущую конструкцию. Проволочная или сетчатая несущая конструкция может быть выполнена в виде оплетки или спирали. Проволочная или сетчатая несущая конструкция может содержать упругие металлы или полимеры, или металлы или полимеры с памятью формы. Проволочная или сетчатая несущая конструкция может быть выполнена, выполнена в основном или выполнена по существу из нитинола или нержавеющей стали, PTFE или их комбинаций. Проволочная или сетчатая несущая конструкция может быть расположена на внутренней (просветной) поверхности или наружной поверхности каналов или сегментов каналов, или может быть встроена в стенку каналов или сегментов каналов. Проволочная или сетчатая несущая конструкция может обеспечивать гибкость, устойчивость к сжатию или устойчивость к изгибу гибких сегментов ближнего или дальнего сегментов канала. В некоторых вариантах реализации изобретения ближний или дальний сегменты канала могут иметь длину от 2 до 110 см и могут быть отрезаны до требуемой длины хирургом или другим врачом, в том числе при имплантации канала, ближнего или дальнего сегмента канала, или дальнего наконечника канала.
[345] Ближний конец ближнего сегмента канала может быть выполнен с возможностью крепления или может быть прикреплен к сегменту бокового канала или к перфузионному насосу. Дальний конец ближнего сегмента канала может быть выполнен с возможностью крепления или может быть прикреплен к дальнему сегменту канала, боковому каналу, дальнему наконечнику канала, или может быть выполнен с возможностью введения в артерию, вену, камеру сердца, или другую структуру, содержащую кровь. Ближний конец дальнего сегмента канала может быть выполнен с возможностью крепления или может быть прикреплен к ближнему сегменту канала, или к боковому каналу. Дальний конец дальнего сегмента канала может быть выполнен с возможностью крепления или может быть прикреплен к боковому каналу, дальнему наконечнику канала, или может быть выполнен с возможностью введения в артерию, вену, камеру сердца, или другую структуру, содержащую кровь. Полностью или частично, поверхность просвета ближнего и дальнего приточных сегментов канала могут содержать антитромботическое покрытие. Антитромботическое покрытие может содержать гепарин. Антитромботическое покрытие может содержать гепарин. Антитромботическое покрытие может представлять собой покрытие Astute® или Applause™.
[346] Настоящее изобретение относится к конструкции, изготовлению и использованию различных конфигураций дальнего конца каналов для транспортировки крови, включая дальние наконечники канала. Дальние наконечники каналов для каналов для транспортировки крови, в которых канал принимает кровь из артерии, вены, камеры сердца или другой структуры, содержащей кровь, и доставляет или передает кровь в насос, в настоящем документе могут упоминаться как «дренажный наконечник», «узел дренажного наконечника», «наконечник приточного канала» или «дальний наконечник канала». Участок дальнего наконечника канала, выполненный с возможностью размещения в просвете кровеносного сосуда, вены, артерии, камеры сердца или другой структуры, содержащей кровь, может упоминаться в настоящем документе как «внутрисосудистый участок», «внутрисосудистый сегмент» или «дальний сегмент» дальнего наконечника канала.
[347] Дальний конец дальнего наконечника канала может быть выполнен с возможностью установления соединения по текучей среде с артерией, веной, камерой сердца или другой структурой, содержащей кровь. Дальний конец дальнего наконечника канала может быть выполнен с возможностью установления соединения по текучей среде с артерией, веной, камерой сердца или другой структурой, содержащей кровь, посредством анастомоза. Дальний конец дальнего наконечника канала, выполненный с возможностью установления сообщения по текучей среде с артерией, веной, камерой сердца или другой структурой, содержащей кровь, посредством анастомоза, может содержать вспененный политетрафторэтилен (ePTFE) или Dacron. Дальний конец дальнего наконечника канала может быть выполнен с возможностью установления сообщения по текучей среде с артерией, веной, камерой сердца или другой кровеносной структурой путем введения, полностью или частично, дальнего наконечника канала в артерию, вену, камеру сердца или другую структуру, содержащую кровь.
[348] В некоторых вариантах реализации изобретения дальний наконечник канала выполнен, выполнен в основном или выполнен по существу из металла или металлического сплава, включая, но не ограничиваясь ими, нержавеющую сталь, нитинол, титан, золото, платину, их сплавы, и их комбинации. В некоторых вариантах реализации изобретения дальний наконечник канала выполнен, выполнен в основном или выполнен по существу из нержавеющей стали. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. Также может быть использована нержавеющая сталь марки 400. В некоторых вариантах реализации изобретения дальний наконечник канала выполнен из одной заготовки, трубки или другого материала из нержавеющей стали. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. Также может быть использована нержавеющая сталь марки 400. В некоторых вариантах реализации изобретения дальний наконечник канала может быть выполнен из одной или более заготовок сплошного металла или металлического сплава, включая, но не ограничиваясь ими, нержавеющую сталь, нитинол, титан, золото, платину, их сплавы, и их комбинации. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. Также может быть использована нержавеющая сталь марки 400.
[349] В некоторых вариантах реализации изобретения дальний наконечник канала выполнен, выполнен в основном или выполнен по существу из жесткого полимера, включая, но не ограничиваясь ими, поликарбонат или полиэфирэфиркетон или их комбинации. В некоторых вариантах реализации изобретения дальний наконечник канала выполнен, выполнен в основном или выполнен по существу из полностью или частично металлизированного полимера для обеспечения требуемых характеристик, таких как желаемая форма, материал поверхности или текстура поверхности. В некоторых вариантах реализации изобретения дальний наконечник канала выполнен из одной заготовки, трубки или другого материала из поликарбоната или полиэфирэфиркетона. Также могут быть использованы другие жесткие полимеры.
[350] В некоторых вариантах реализации изобретения дальний наконечник канала может быть выполнен, выполнен в основном или выполнен по существу из гибких или упругих полимеров. Такие гибкие или упругие полимеры включают полиуретаны, полиуретаны Pellethane®, полиуретаны Carbothane®, Carbothane® PC-3575A с твердостью по Шору 70A, ароматические полиуретановые эластомерные сплавы, ароматические полиуретановые эластомерные сплавы Polyblend 1100, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 45A, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 55A, поливинилхлориды, полиэтилены, силиконовые эластомеры, политетрафторэтилены, вспененный политетрафторэтилен, полиэтилентерефталаты, эластомеры из термопластичного кремнийорганического поликарбоната, полиэфирблокамиды и их комбинации с твердостью по Шору в диапазоне от 20A до 80A, от 20A до 30A, от 30A до 40A, от 40A до 50A, от 50A до 60A, от 60A до 70A, от 70A до 80, или с твердостью по Шору 20A, 25A, 30A, 35A, 40A, 45A, 50A, 55A, 60A, 65A, 70A, 75A, или 80A. Гибкие сегменты дальнего наконечника канала могут содержать проволочную или сетчатую несущую конструкцию. Проволочная или сетчатая несущая конструкция может быть выполнена в виде оплетки, спирали, обмотки или сетки. Проволочная или сетчатая несущая конструкция может содержать упругую проволоку или полимеры, или проволоку или полимеры с памятью формы. Проволочная или сетчатая несущая конструкция может быть выполнена, выполнена в основном или выполнена по существу из нитинола или нержавеющей стали, PTFE или их комбинаций. Проволочная или сетчатая несущая конструкция может быть расположена на внутренней (просветной) поверхности или наружной поверхности гибких сегментов дальнего наконечника канала, или может быть встроена в стенку гибких сегментов дальнего наконечника канала. Проволочная или сетчатая несущая конструкция может обеспечивать гибкость, устойчивость к сжатию или устойчивость к изгибу гибких сегментов дальнего наконечника канала.
[351] Дальний наконечник канала может быть выполнен из различных материалов, включая комбинацию металлов, комбинацию полимеров, комбинацию металлов и полимеров и комбинацию различных металлов и различных полимеров. Ближний наконечник, корпус, и дальний конец дальнего наконечника канала может быть выполнен из различных материалов, включая комбинацию металлов, комбинацию полимеров, комбинацию металлов и полимеров и комбинацию различных металлов и различных полимеров. В некоторых вариантах реализации изобретения, полностью или частично, дальний наконечник канала образован путем литья под давлением, механической обработки, стереоскопической печати или их комбинаций.
[352] На фиг. 62 показан вид в перспективе одного варианта реализации дальнего наконечника 1000 канала. Наконечник канала содержит, как правило, трубчатый корпус 1100, имеющий ближний конец 1200 для соединения с ближним или дальним сегментом канала и дальним концом 1300, принимающим или выпускающим текучую среду. Трубчатый корпус 1100 дополнительно образует продолговатый просвет 1102 (показанный на фиг.66), обеспечивающий сообщение по текучей среде между дальним концом 1300 и ближним концом 1200, с ближним или дальним сегментом канала, который может быть сцеплен с ближним концом. В некоторых вариантах реализации изобретения наконечник 1000 канала может иметь внутренний диаметр D20 примерно между 2 мм и 20 мм. В других вариантах реализации изобретения внутренний диаметр может быть увеличен или уменьшен, чтобы обеспечить больший или меньший внутренний диаметр для любого предполагаемого использования.
[353] Как показано на фиг. 63, каждый из трубчатого корпуса 1100 и ближнего конца 1200 имеет наружный диаметр D17 и D18, который меньше, чем диаметр D19 дальнего конца 1300. В одном варианте реализации изобретения участок наконечника 1000 канала, на котором дальний конец 1300 переходит в корпус 1100, образует кольцевой фланец 1104, как показано на фиг. 65, 66 и 68.
[354] В одном аспекте кольцевой фланец 1104 имеет ширину W22, показанную на фиг. 66 и 69, примерно равную толщине 1402 деформированной стенки требуемого канала 1400, который соединяют с наконечником 1000, как показано на фиг. 71. Толщину 1402 стенки деформированного канала определяют на основании расчета деформации растяжения и сдвига канала, когда он соединен с ближним концом 1200. В качестве примера, а не ограничения, радиальную деформацию и/или сжатие канала можно вычислить путем измерения первоначальной толщины стенки канала, определения величины деформации стенки, необходимой для растяжения канала на кольцевых зубцах, а затем вычисления величины утончения или деформации стенки, требуемой для соединения канала с соединителем с кольцевыми зубцами. Поскольку ширина W22 фланца 1104 примерно равна толщине 1402 стенки канала соединяемого канала 1400, наружный диаметр D19 дальнего конца 1300 примерно равен наружному диаметру 1404 канала. Это обеспечивает плавный переход 1406 наружной поверхности наконечника канала к остальной части канала. Это предпочтительная конфигурация, поскольку она минимизирует выступы или рельефы по длине канала, которые могут отрицательно влиять на кровоток, что приводит к тромбу или гемолизу.
[355] В соответствии с одним вариантом реализации изобретения надежное крепление между приточным наконечником 1000 и ближним или дальним сегментом 1400 канала обеспечивается одним или несколькими кольцевыми зубцами 1202 и 1204, выполненными в ближнем конце 1200. Как показано на фиг. 63-65, один вариант реализации изобретения приточного наконечника 1000 содержит два или более кольцевых зубцов на ближнем конце 1200. В этом варианте реализации изобретения первый кольцевой зубец 1202 или кольцевой выступ, самый близкий к ближнему краю 1206, сформирован под углом α1 относительно продольной оси 1020 приточного наконечника 1000. Второй кольцевой зубец 1204, расположенный дистально относительно первого кольцевого зубца 1202, сформирован под углом α2 относительно продольной оси 1020. В этом варианте реализации изобретения угол α1 больше, чем угол α2. Аналогично, для вариантов реализации изобретения, имеющих более двух выступов, угол проецирования относительно продольной оси 1020 каждого выступа кольцевого зубца меньше, чем угол наклона для каждого последующего выступа, перемещаясь проксимально вдоль приточного наконечника 1000. В других вариантах реализации изобретения наконечник приточного канала может не иметь кольцевых зубцов, и соединен с каналом посредством клея или соединения с фрикционной посадкой. В качестве альтернативы, приточный наконечник может быть соединен с каналом посредством других подходящих механизмов, включая, но не ограничиваясь этим, сварку или упругую втулку. В некоторых вариантах реализации изобретения дальний наконечник канала вводят в дальний конец ближнего или дальнего сегмента канала.
[356] Наконечник 1000 приточного канала может иметь общую длину в диапазоне от 5 до 50 мм. Кроме того, длина ближнего конца 1200 может изменяться в пропорциональном отношении к общей длине. Например, в одном варианте реализации изобретения ближний конец 1200 может составлять примерно 60% общей длины (имея длину в диапазоне примерно от 3 до 30 мм). В других вариантах реализации изобретения ближний конец может составлять примерно 20 до 80% общей длины приточного наконечника 1000. Например, ближний конец 1200 может иметь длину от 2 до 40 мм, в зависимости от необходимого применения и конфигурации наконечника 1000 приточного канала.
[357] Как показано на фиг. 66 и 71, в соответствии с одним вариантом реализации изобретения, толщина стенки ближнего конца 1200 наконечника 1000 приточного канала, включая первый кольцевой зубец 1202, сужается или уменьшается до минимума примерно 0,1 мм (0,004 дюйма). В одном аспекте сужающаяся толщина ближней стенки 1208 обеспечивает минимальное изменение высоты стенки на внутреннем диаметре узла наконечника канюли, создавая плавный переход поверхности между металлическим наконечником и корпусом канюли для текучих сред, поступающих в ближний конец приточного наконечника из канала, что, возможно, уменьшает вероятность образования кольцевого тромба при переходе. При использовании для извлечения или подачи крови сужающаяся конфигурация минимизирует риск образования тромбов в застойном кровотоке, который контактирует с приточным наконечником 1000 вблизи внутренней стенки канала, одновременно уменьшая риск активации тромбоцитов или гемолиза крови, которая контактирует с приточным наконечником вблизи внутренней стенки канала.
[358] Далее, как показано на фиг. 62, 63, 66 и 67, в одном варианте реализации изобретения дальний конец наконечника 1000 приточного канала имеет толщину стенки Т1 примерно от 0,5 до 8 мм и образует дальнее отверстие 1302. Дальнее отверстие 1302 дополнительно образовано рядами дугообразных выступов и углублений на дальней торцевой поверхности 1304 приточного наконечника. В одном варианте реализации изобретения ряд выступов и углублений на дальней торцевой поверхности 1304 образует, как правило, синусоидальную кривую. В качестве примера, а не ограничения, один вариант реализации приточного наконечника 1000 имеет волнистую дальнюю торцевую поверхность 1304, образованную выступающими участками или зонами 1308, которые примерно в 2,5 раза шире, чем углубленные участки или зоны 1306. В одном конкретном варианте реализации изобретения, выступающие участки выступают наружу от поперечной оси 1030, которая расположена вдоль центральной линии между выступающими и углубленными участками по длине дуги, составляющей примерно 256 градусов. Напротив, углубленные участки 1306 простираются от оси 1030, напротив выступающих участков 1308 по длине дуги, составляющей примерно 104 градуса. Каждый выступающий участок 1308 или углубленный участок 1306 имеет полукруглый контур.
[359] В некоторых вариантах реализации изобретения отношение углубленной зоны к выступающей зоне общей длины дуги может находиться в диапазоне примерно 10% или 36 градусов для углубленного участка до 90% или 324 градусов дальнего наконечника, оформленного в виде углубленных участков, в зависимости от предполагаемого применения. Аналогично, разница в высоте между нижней точкой углубленного участка 1306 (то есть точкой, наиболее удаленной от поперечной оси 1030) и самой дальней точкой выступающего участка 1308 (то есть точками, наиболее удаленными от поперечной оси 30) может быть изменена для достижения большей эффективной глубины углублений, за счет увеличения протяженности длин выступов от таковых для чисто синусоидальной волны до таковых для растянутой синусоидальной волны, причем переход между углублением и выступом лежит вдоль вытянутой по существу плоской поверхности стенки. В одном примере коэффициент удлинения может, как правило, соответствовать, но без ограничения, величине, составляющей от доли площади поперечного сечения канала до величины, равной одной или более площадей поперечного сечения канала.
[360] В одном аспекте, как показано на фиг. 63, углубленная зона 1306 может быть образована радиусом кривизны R9, измеренным от поперечной оси 1030, которая перпендикулярна продольной оси 1020 и проходит через дальнюю торцевую поверхность 1304. Радиус R9 кривизны углубленной зоны может быть аналогичен радиусу кривизны R10 по меньшей мере части выступающей зоны 1308, показанной на фиг. 65. Как показано на фиг. 65 и 71, выступающая зона 1308 может иметь, как правило, полуэллиптическую конфигурацию, так что выступающая зона имеет ширину 1310, перпендикулярную продольной оси, большую, чем ширина 1312 углубленного сегмента, измеренная вдоль поперечной оси 1030. Таким образом, наконечник 1000 канала обычно может иметь форму или ориентацию «утиного клюва».
[361] Согласно некоторым вариантам реализации изобретения дальняя торцевая поверхность 1304 имеет полный радиус и является полностью дугообразной, от наружной поверхности 1050 приточного наконечника 1000 до внутренней поверхности 1040, как показано на фиг. 71. В некоторых вариантах реализации изобретения дальняя торцевая поверхность 1304 образована дугообразной поверхностью, имеющей полный радиус скругления, равный половине толщины стенки приточного наконечника. В качестве примера радиус дальней торцевой поверхности 1304 может находиться в диапазоне примерно от 0,5 до 0,65 мм. Полный радиус дальней торцевой поверхности 1304 выполнен, возможно, посредством полностью металлической конструкции наконечника 1000 приточного канала. Кроме того, полный радиус дальней торцевой поверхности обеспечивает много преимуществ по сравнению с менее дугообразными поверхностями. Как показано на фиг. 66-67, конфигурация канала 1000 с полным радиусом «утиного клюва» обеспечивает улучшенную промывку в отверстии 1302 по сравнению с другими конфигурациями наконечника канала, такими как конструкция корончатого наконечника с 3 или более выступами и 3 или более углублениями. Свойства улучшенного промывания конфигурации «утиный клюв» минимизируют случаи тромбоза из-за застойного кровотока. Одновременно конфигурация «утиного клюва» с полным радиусом также уменьшает случаи чрезмерного WSS в кровотоке, проходящем через приточный наконечник 1000 и соединенный с ним канал 1400. Как показано, уменьшенные случаи чрезмерного WSS дополнительно минимизируют активацию тромбоцитов и гемолиз по сравнению с другими конфигурациями дальнего наконечника канала.
[362] В некоторых вариантах реализации изобретения по меньшей мере часть контактирующей с кровью наружной и внутренней поверхностей дальнего наконечника канала, включая дальний конец и дальнюю торцевую поверхность, дополнительно образованы полированной поверхностью. В некоторых вариантах реализации изобретения по меньшей мере часть контактирующей с кровью наружной и внутренней поверхностей дальнего наконечника канала имеет шероховатость поверхности в диапазоне от 2 до 16 мкм Ra или в диапазоне от 4 до 8 мкм Ra. В некоторых вариантах реализации изобретения по меньшей мере часть поверхностей, не контактирующих с кровью, или внутренних поверхностей, включая выступы 1202 и 1204 кольцевых зубцов, при их наличии, остаются неполированными для усиления связи с дальним концом ближнего или дальнего сегментов 1400 канала, соединенных с дальним наконечником 1000 канала.
[363] Полностью или частично, поверхность просвета дальнего наконечника канала может содержать антитромботическое покрытие. Антитромботическое покрытие может содержать гепарин. Антитромботическое покрытие может представлять собой покрытие Astute® или Applause™.
[364] Настоящее изобретение также относится к конструкции, изготовлению и использованию «узлов дальних наконечников канала» для i) ближнего или дальнего сегмента канала; ii) дальнего наконечника канала; и iii) гибкой или упругой конструкции защитного каркаса дальнего наконечника канала. Настоящее изобретение также относится к конструкции, изготовлению и использованию «узлов дальних наконечников канала» для i) дальнего наконечника канала; и ii) гибкой или упругой конструкции защитного каркаса дальнего наконечника канала. При использовании in vivo, такие узлы дальних наконечников канала могут уменьшить риск контакта между дальним наконечником канала и стенкой артерии, вены, камеры сердца или другой структуры, содержащей кровь. При использовании in vivo, такие узлы дальних наконечников канала могут уменьшить риск повреждения стенок артерий, вен, камер сердца или других структур, содержащих кровь, рядом с узлом дальнего канала. При использовании in vivo, такие узлы дальних наконечников канала могут также действовать, чтобы уменьшить риск спадения стенок артерий, вен, камер сердца или других структур, содержащих кровь, рядом с узлом дальнего канала.
[365] Конструкция защитного каркаса дальнего наконечника канала в настоящем документе также может быть названа «внутрисосудистый каркас», «защитный каркас дальнего наконечника», «защитный каркас дальнего наконечника канала» или «каркас». Как показано на фиг. 91-93, в некоторых вариантах реализации изобретения защитный каркас 2500 дальнего наконечника канала содержит одно или несколько ребер 2506. В некоторых вариантах реализации изобретения может иметься одно, два, три, четыре, пять или шесть ребер. В некоторых вариантах реализации изобретения конструкция защитного каркаса дальнего наконечника канала окружает частично или полностью дальний наконечник 1000 канала (или дренажный наконечник).
[366] В некоторых вариантах реализации изобретения по меньшей мере одно ребро 2506 может представлять собой продолговатую, упругую или пружинистую конструкцию. В некоторых вариантах реализации изобретения по меньшей мере одно из ребер 2506 может представлять собой провод, стержень или пруток. В некоторых вариантах реализации изобретения форма поперечного сечения по меньшей мере одного ребра растягиваемой конструкции защитного каркаса дальнего наконечника канала является круглой, квадратной, прямоугольной или эллипсоидной. В некоторых вариантах реализации изобретения по меньшей мере одно ребро имеет диаметр или ширину в диапазоне от 0,3 до 2,0 мм или в диапазоне от 0,6 до 1,0 мм. В некоторых вариантах реализации изобретения по меньшей мере одно из ребер 2506 может быть выполнено, выполнено в основном или выполнено по существу из нитинола, нержавеющей стали или полимера, или их комбинаций.
[367] В некоторых вариантах реализации изобретения конструкция защитного каркаса дальнего наконечника канала, соединена или сцеплена с ближним или дальним сегментом 2600 канала (или сегментом) и окружает частично или полностью дальний наконечник 1000 канала (или дренажный наконечник). В некоторых вариантах реализации изобретения конструкция защитного каркаса дальнего наконечника канала, соединена или сцеплена с дальним наконечником канала и окружает частично или полностью дальний наконечник 1000 канала (или дренажный наконечник). В некоторых вариантах реализации изобретения защитный каркас дальнего наконечника канала может быть соединен с возможностью отсоединения с ближним или дальним сегментом канала, в том числе способом, при котором может быть преодолено трение фрикционной посадки между защитным каркасом дальнего наконечника канала и ближним или дальним сегментом канала, чтобы удалить защитный каркас дальнего наконечника канала. В некоторых вариантах реализации изобретения защитный каркас дальнего наконечника канала может быть жестко связан с ближним или дальним сегментом канала с использованием клея, фрикционной посадки или клея и фрикционной посадки, для соединения одного или более удлиненных и упругих ребер защитного каркаса дальнего наконечника канала с дальним концом ближнего или дальнего сегмента канала. В некоторых вариантах реализации изобретения защитный каркас дальнего наконечника канала может быть неподвижно связан с ближним или дальним сегментом канала, путем частичного внедрения одного или более ребер в стенку ближнего или дальнего сегмента канала.
[368] В некоторых вариантах реализации изобретения дальний конец ребер 2506 может перемещаться радиально при изменении из сжатой конфигурации до растянутой конфигурации. В некоторых вариантах реализации изобретения дальний конец ребер 2506 может перемещаться в осевом направлении при изменении из сжатой конфигурации до растянутой конфигурации. Вариант реализации растягиваемого защитного каркаса 2500 дальнего наконечника канала показан на фиг. 91 A-C. Вариант реализации сжатого защитного каркаса 2500 дальнего наконечника канала показан на фиг. 94.
[369] В некоторых вариантах реализации изобретения диаметр каркаса 2500 при растяжении может составлять от 6 до 30 мм. В некоторых вариантах реализации изобретения диаметр каркаса 2500 при растяжении может составлять на 10%-25%, на 25%-50%, на 50%-75%, на 75%-100%, на 100%-200% или на 200%-400% больше, чем диаметр дальнего наконечника канала. В некоторых вариантах реализации изобретения длина ребер каркаса 2500 при растяжении может составлять от 10 до 60 мм. В некоторых вариантах реализации изобретения длина ребер каркаса 2500 при растяжении может составлять от 10 до 60 мм. В некоторых вариантах реализации изобретения длина ребер каркаса 2500 при растяжении может быть такой же длины, как длина дальнего наконечника канала. В некоторых вариантах реализации изобретения длина ребер каркаса 2500 при растяжении может составлять на 10%-25%, на 25%-50%, на 50%-75%, на 75%-100%, на 100%-200% или на 200%-400% больше, чем длина дальнего наконечника канала. В некоторых вариантах реализации изобретения, когда защитный каркас дальнего наконечника канала находится в растянутом состоянии, одно, более одного или все ребра 2506 могут соприкасаться со стенкой сосуда. В некоторых вариантах реализации изобретения, когда защитный каркас дальнего наконечника канала находится в растянутом состоянии, одно, более одного или все ребра 2506 могут не соприкасаться со стенкой сосуда.
[370] В некоторых вариантах реализации изобретения защитный каркас 2500 дальнего наконечника канала содержит ближнее кольцо 2502. Как показано на фиг. 91-93, в некоторых вариантах реализации изобретения защитный каркас 2500 дальнего наконечника канала содержит ближнее кольцо 2502 и дальнее кольцо 2504, которые сцеплены с противоположными концами одного или более ребер 2506. В некоторых вариантах реализации изобретения ближний конец ребер 2506 соединен с ближним кольцом, но дальний конец ребер 2506 не соединен с дальним кольцом. В некоторых вариантах реализации изобретения дальний конец ребер 2506 соединен без дальнего кольца, тогда как в других вариантах реализации изобретения ребра 2506 не соединены друг с другом.
[371] Ребра 2506 соединены с кольцами 2502 и 2504 с использованием любого подходящего способа. В качестве примера, когда и ребра 2506, и кольца 2502 и 2504 выполнены из металла, ребра могут быть соединены с кольцами сварными швами или клейкими веществами 2505, как показано на фиг. 93. В некоторых вариантах реализации изобретения одно или более ребер 2506 могут быть выполнены с необходимой формой до или после соединения с одним или обоими кольцами 2502 и 2504.
[372] В некоторых вариантах реализации изобретения ближнее кольцо 2502 конструкции защитного каркаса дальнего наконечника канала соединено или сцеплено с ближним или дальним сегментом 2600 канала (или сегментом) и окружает частично или полностью дальний наконечник 1000 канала (или дренажный наконечник). В некоторых вариантах реализации изобретения ближнее кольцо 2502 конструкции защитного каркаса дальнего наконечника канала соединено или сцеплено с дальним наконечником канала и окружает частично или полностью дальний наконечник 1000 канала (или дренажный наконечник). В некоторых вариантах реализации изобретения ближнее кольцо 2502 защитного каркаса дальнего наконечника канала может быть соединено с возможностью отсоединения с ближним или дальним сегментом канала, в том числе способом, при котором может быть преодолено трение фрикционной посадки между ближним кольцом 2502 защитного каркаса дальнего наконечника канала и ближним или дальним сегментом канала, чтобы удалить защитный каркас дальнего наконечника канала. В некоторых вариантах реализации изобретения ближнее кольцо 2502 защитного каркаса дальнего наконечника канала может быть жестко связано с ближним или дальним сегментом канала с использованием клея, фрикционной посадки или клея и фрикционной посадки, для соединения ближнего кольца защитного каркаса дальнего наконечника канала с дальним концом ближнего или дальнего сегмента канала. В некоторых вариантах реализации изобретения ближнее кольцо защитного кожуха дальнего наконечника канала может быть связано или соединено с наружной поверхностью дальнего конца ближнего или дальнего сегмента канала. В некоторых вариантах реализации изобретения ближнее кольцо защитного каркаса дальнего наконечника канала может быть неподвижно связано с ближним или дальним сегментом канала, путем полного или частичного внедрения ближнего кольца 2502 в стенку ближнего или дальнего сегмента канала. Для вариантов реализации защитной оболочки дальнего наконечника канала с ближним и дальним кольцом, дальнее кольцо 2504 обычно имеет диаметр, равный диаметру ближнего кольца 2502 или меньший, чем он. Однако в некоторых вариантах реализации изобретения диаметр дальнего кольца 2504 может быть больше диаметра ближнего кольца 2502. В некоторых вариантах реализации изобретения кольца 2502 и 2504 могут быть выполнены, выполнены в основном или выполнены по существу, из нитинола, нержавеющей стали, золота, платины, какого-либо биосовметимого металла или полимера, или их комбинаций.
[373] Для вариантов реализации защитного каркаса дальнего наконечника канала с ближним и дальним кольцом во время растяжения диаметр D8 защитного каркаса дальнего наконечника канала увеличивается, когда дальнее кольцо 2504 перемещают проксимально к ближнему кольцу 2502. Для вариантов реализации защитного каркаса дальнего наконечника канала с ближним и дальним кольцом во время сжатия диаметр D8 защитного каркаса дальнего наконечника канала уменьшается, когда дальнее кольцо 2504 перемещают дистально от ближнего кольца 2502.
[374] Как показано на фиг. 94, сужающийся гибкий уплотнитель 2602 может быть дополнительно использован для изменения конфигурации защитного каркаса дальнего наконечника канала из растянутой конфигурации в конфигурацию доставки. Конический гибкий уплотнитель 2602 может содержать центральный просвет для проволочного направителя. Центральный просвет может иметь диаметр 1,016-1,27 мм (0,040-0,050 дюйма) и может быть совместим с проволочным направителем диаметром 0,9652 или 0,889 мм (0,038 или 0,035 дюйма). Диаметр конца конического гибкого уплотнителя 2602 может быть большим, равным или меньшим диаметра дальнего кольца 2504.
[375] Как показано на фиг. 94, конический уплотнитель 2602 может быть использован для продвижения канала 2600 и каркаса 2500 на место вдоль проволочного направителя 2604. Уплотнитель 2602 может содержать ручку 2606 или другое устройство для облегчения введения и удаления. После введения в вену, артерию, камеру сердца или другую структуру, содержащую кровь, и расположенную соответствующим образом, каркас 2500 может быть растянут. В некоторых вариантах реализации изобретения после растягивания каркаса дальний наконечник 2608 канала располагается вблизи средней линии (как указано, на плоскости, параллельной длинной оси ближнего или дальнего сегмента канала) 2610 каркаса, причем длины L51 и L52 примерно равны, как показано на фиг. 96. В альтернативных вариантах реализации изобретения дальний конец дальнего наконечника 2606 канала может быть более ближним (т. е. L51 < L52) или дальним (т. е. L51 > L52) относительно средней линии 2610. В некоторых вариантах реализации изобретения после растягивания каркаса дальний наконечник 2608 канала располагается вблизи средней линии (как указано, на плоскости, поперечной длинной оси ближнего или дальнего сегмента канала) 2611 каркаса, причем длины L53 и L54 примерно равны, как показано на фиг. 96. В альтернативных вариантах реализации изобретения дальний конец дальнего наконечника 2606 канала может быть более ближним (т. е. L53 < L54) или дальним (т. е. L53 > L54) относительно средней линии 2610.
[376] Дополнительные варианты реализации изобретения и конфигурации каркаса 2500 показаны на фиг. 97-105. Как показано, другие варианты реализации каркаса 2500 включают дальнее кольцо 2504, но с заменой ближнего кольца 2502 другой конструкцией. В этих вариантах реализации изобретения ближний участок каркаса может быть выполнен из трубчатого или плоского сегмента 2510 различных конфигураций, аналогично ребрам 2506. Как показано, ближние концы ребер 2506 соединены с ближней корончатой или похожей на стент конструкцией 2512. В одном аспекте корончатая или похожая на стент конструкция 2512 может представлять собой отдельную конструкцию, которая соединена с ребрами 2506 или корончатая или похожая на стент конструкция может составлять единое целое с ребрами 2506. В альтернативных вариантах реализации изобретения ближние концы ребер 2506 могут оставаться свободными в открытой конфигурации 2514, как показано на фиг. 100-102. В таких вариантах реализации изобретения ближний конец каркаса 2500 прикреплен к каналу 2600 путем пакетирования концов ребер 2506 в стенку канала 2600.
[377] В других вариантах реализации изобретения, показанных на фиг. 103-105, каркас 2500 может быть выполнен из трубки или плоского листового металла или полимера 2700, который был разрезан для образования дальнего кольца 2504, ребер 2506 и, необязательно, ближней корончатой или похожей на стент конструкции 2512. В одном аспекте плоский лист 2700 может быть прокатан для образования, как правило, цилиндрической каркасной конструкции 2500, содержащей либо корончатый, либо похожий на стент ближний участок 2512, соединяемый с ближним или дальним сегментом 2600 канала, или открытый ближний участок 2514, соединяемый со стенкой ближнего или дальнего сегмента 2600 канала, в том числе, путем соединения посредством клея, сварки, фрикционной посадки или пакетирования.
[378] В некоторых вариантах реализации изобретения по меньшей мере часть контактирующих с кровью наружных и внутренних поверхностей каркаса дополнительно образована полированной поверхностью. В некоторых вариантах реализации изобретения вся или по меньшей мере часть контактирующих с кровью поверхностей каркаса имеет шероховатость поверхности в диапазоне от 2 до 16 мкм Ra или в диапазоне от 4 до 8 мкм Ra. В некоторых вариантах реализации изобретения по меньшей мере часть поверхностей, не контактирующих с кровью, или внутренних поверхностей, включая ближнее кольцо, остаются неполированными для усиления связи с дальним концом ближнего или дальнего сегментов 1400 канала, соединенных с дальним наконечником 1000 канала.
[379] В некоторых вариантах реализации изобретения все поверхности каркаса могут содержать антитромботическое покрытие. В некоторых вариантах реализации изобретения часть контактирующих с кровью поверхностей и каркаса может содержать антитромботическое покрытие. Антитромботическое покрытие может содержать гепарин. Антитромботическое покрытие может представлять собой покрытие Astute® или Applause™.
[380] Каналы с различными элементами и характеристиками могут быть выполнены путем сборки различных сегментов и составных частей. В некоторых вариантах реализации изобретения более длинные каналы могут быть образованы путем включения как проксимальных сегментов канала, так и дальних сегментов канала. В некоторых вариантах реализации изобретения каналы могут быть собраны с ближними сегментами канала, которые являются высокоупругими, и дальними сегментами канала, которые являются очень гибкими и устойчивыми к сжатию или изгибу. В этих вариантах реализации изобретения ближний сегмент канала можно многократно зажимать и разжимать с меньшей деформацией, в то время как дальний сегмент канала может быть выполнен с крутыми изгибами для установления сообщения по текучей среде с веной, артерией, кровеносным сосудом, камерой сердца или другой структурой, содержащей кровь. В качестве примера, а не ограничения, (приточный) канал может быть собран с ближним сегментом канала, пригодным для повторного зажимания и разжимания, и сегментом дальнего канала для введения в яремную вену, подключичную вену или другую вену, и продвижения в извилистую венозную систему до тех пор, пока дальний наконечник канала или узел дальнего наконечника канала не будет находиться в верхней полой вене или в правом предсердии. В качестве примера, а не ограничения, в таком канале ближний сегмент канала может иметь проволочную несущую конструкцию из нитинола в виде оплетки, а дальний сегмент канала может иметь проволочную несущую конструкцию из нитинола в виде несущей спирали, предпочтительно в конфигурации с зазором между витками, который больше, чем ширина проволоки. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может иметь более толстую стенку, чем весь дальний сегмент канала или его часть. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из полимеров с более высокой твердостью, чем весь дальний сегмент канала или его часть. Например, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из полиуретана, а дальний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из ароматического полиуретанового эластомерного сплава. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из полиуретана Pellethane ® или Carbothane®. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из полиуретана с твердостью по Шору 70A. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен, выполнен в основном или выполнен по существу из полиуретана Pellethane ® или Carbothane® с твердостью по Шору 70A. В качестве примера, а не ограничения, в таком канале дальний сегмент канала полностью или частично может быть выполнен, выполнен, выполнен в основном или выполнен по существу из ароматического полиуретанового эластомерного сплава с твердостью по Шору 45A или 55A, или их комбинаций. В качестве примера, а не ограничения, в таком канале дальний сегмент канала полностью или частично может быть выполнен, выполнен, выполнен в основном или выполнен по существу из полимера Polyblend 1100 компании AdvanSource Biomaterials, Уилмингтон, штат Массачусетс, с твердостью по Шору 45A или 55A.
[381] В качестве примера, а не ограничения, в некоторых вариантах реализации изобретения могут быть собраны каналы, в которых дальний сегмент канала имеет меньший наружный диаметр, чем ближний канал для способствования введению в яремную, подключичную вену или другую вену и для уменьшения риска повреждения стенок вен или тромбоза вен. В некоторых вариантах реализации изобретения наружный диаметр дальнего сегмента канала уменьшен за счет уменьшения толщины стенки канала, за счет уменьшения внутреннего диаметра стенки канала, или их комбинаций. Кроме того, каналы, собранные по меньшей мере из двух гибких сегментов, включая варианты реализации изобретения с ближним и дальним сегментами канала, могут упростить процесс туннелирования участков канала под кожей пациента. В некоторых вариантах реализации изобретения приточный канал может быть использован для приема крови от насоса и доставки или передачи крови в артерию, вену, камеру сердца или другую структуру, содержащую кровь.
[382] Настоящее изобретение относится к проектированию, изготовлению и использованию каналов для транспортировки крови. Когда канал для транспортировки крови принимает кровь от насоса и передает кровь в артерию, вену, камеру сердца или другую структуру, содержащую кровь, тогда в настоящем документе канал может называться «выводным каналом», или «каналом».
[383] Настоящее изобретение также относится к проектированию, изготовлению и использованию сегментов ближнего и дальнего сегментов выводных каналов. Такие выводные каналы (или каналы) могут содержать i) ближний сегмент канала, который может быть гибким, упругим и устойчивым к сжатию и изгибу; ii) дальний сегмент канала, который может быть гибким, упругим и устойчивым к сжатию и изгибу; iii) дальний наконечник канала, который может быть гибким, упругим и устойчивым к сжатию и изгибу, или может быть жестким, или может иметь гибкие и упругие зоны и жесткие зоны; и iv) один или более боковых каналов, которые могут быть гибкими, упругими и устойчивыми к сжатию и изгибу, или могут быть жесткими, или могут иметь гибкие и упругие зоны и жесткие зоны.
[384] В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) боковой канал, ближний сегмент канала, дальний сегмент канала и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, боковой канал, дальний сегмент канала и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, дальний сегмент канала, боковой канал и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, дальний сегмент канала и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, боковой канал и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала и дальний наконечник канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) боковой канал, ближний сегмент канала и дальний сегмент канала, при этом дальний наконечник канала объединен с дальним концом дальнего сегмента канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, боковой канал и дальний сегмент канала, при этом дальний наконечник канала объединен с дальним концом дальнего сегмента канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала и дальний сегмент канала, при этом дальний наконечник канала объединен с дальним концом дальнего сегмента канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) боковой канал и ближний сегмент канала, при этом дальний наконечник канала объединен с дальним концом ближнего сегмента канала. В некоторых вариантах реализации изобретения канал может содержать (от ближнего до дальнего конца) ближний сегмент канала, при этом дальний наконечник канала объединен с дальним концом ближнего сегмента канала.
[385] Настоящее изобретение относится к конфигурациям и способам соединения отдельных компонентов выводных каналов. Отдельные компоненты выводных каналов могут быть выполнены с возможностью соединения или могут быть соединены различными способами. Различные конфигурации и способы могут включать в себя фрикционную посадку; фитинг с кольцевыми зубцами; радиально сжимающий фиксатор или фиксирующее кольцо, встроенный в линию соединитель с одним или более фитингами с кольцевыми зубцами и радиально сжимающими фиксаторами или фиксирующими кольцами, или клеем. Каналы могут быть полностью собранными перед имплантацией, частично собранными перед имплантацией, или могут быть собраны во время процедуры имплантации или операции.
[386] В некоторых вариантах реализации изобретения ближний или дальний сегменты канала могут быть выполнены, выполнены в основном или выполнены по существу из гибких или упругих полимеров. Такие гибкие или упругие полимеры включают полиуретаны, полиуретаны Pellethane®, полиуретаны Carbothane®, Carbothane® PC-3575A с твердостью по Шору 70A, ароматические полиуретановые эластомерные сплавы, ароматические полиуретановые эластомерные сплавы Polyblend 1100, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 45A, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 55A, поливинилхлориды, полиэтилены, силиконовые эластомеры, политетрафторэтилены, вспененный политетрафторэтилен, полиэтилентерефталаты, эластомеры из термопластичного кремнийорганического поликарбоната, полиэфирблокамиды и их комбинации с твердостью по Шору в диапазоне от 20A до 80A, от 20A до 30A, от 30A до 40A, от 40A до 50A, от 50A до 60A, от 60A до 70A, от 70A до 80, или с твердостью по Шору 20A, 25A, 30A, 35A, 40A, 45A, 50A, 55A, 60A, 65A, 70A, 75A, или 80A. Сегменты канала могут содержать проволочную или сетчатую несущую конструкцию. Проволочная или сетчатая несущая конструкция может быть выполнена в виде оплетки, спирали или сетки. Проволочная или сетчатая несущая конструкция может содержать упругую проволоку или полимеры, или проволоку или полимер с памятью формы. Проволочная или сетчатая несущая конструкция может быть выполнена, выполнена в основном или выполнена по существу из нитинола или нержавеющей стали, PTFE или их комбинаций. Проволочная или сетчатая несущая конструкция может быть расположена на внутренней (просветной) поверхности или наружной поверхности каналов или сегментов каналов, или может быть встроена в стенку каналов или сегментов каналов. В некоторых вариантах реализации изобретения ближний или дальний сегменты канала могут иметь длину от 2 до 110 см и могут быть отрезаны до требуемой длины хирургом или другим врачом, в том числе при имплантации канала, ближнего или дальнего сегмента канала, или дальнего наконечника канала.
[387] Ближний конец ближнего сегмента канала может быть выполнен с возможностью крепления или может быть прикреплен к сегменту бокового канала или к перфузионному насосу. Дальний конец ближнего сегмента канала может быть выполнен с возможностью крепления или может быть прикреплен к дальнему сегменту канала, боковому каналу, дальнему наконечнику канала, или может быть выполнен с возможностью введения в артерию, вену, камеру сердца, или другую структуру, содержащую кровь. Ближний конец дальнего сегмента канала может быть выполнен с возможностью крепления или может быть прикреплен к ближнему сегменту канала, или к боковому каналу. Дальний конец дальнего сегмента канала может быть выполнен с возможностью крепления или может быть прикреплен к боковому каналу, дальнему наконечнику канала, или может быть выполнен с возможностью введения в артерию, вену, камеру сердца, или другую структуру, содержащую кровь. Полностью или частично, поверхность просвета ближнего и дальнего выводных сегментов канала может содержать антитромботическое покрытие. Антитромботическое покрытие может содержать гепарин. Антитромботическое покрытие может представлять собой покрытие Astute® или Applause™.
[388] Настоящее изобретение относится к конструкции, изготовлению и использованию различных конфигураций дальнего конца каналов для транспортировки крови, включая дальние наконечники канала. Дальние наконечники каналов для каналов для транспортировки крови, в которых канал принимает кровь от насоса, и доставляет или передает кровь в артерию, вену, камеру сердца или другую структуру, содержащую кровь, в настоящем документе могут упоминаться как «наконечник выводного канала», «дальний наконечник канала», «Т-образный наконечник» или «дальний наконечник канала».
[389] В некоторых вариантах реализации изобретения дальний наконечник канала может содержать один сегмент с двумя концами, ближний конец, который может быть соединен или соединен с дальним концом ближнего или дальнего сегмента канала, и дальний конец, который может быть выполнен с возможностью установления сообщения по текучей среде с артерией, веной, камерой сердца или другой структурой, содержащей кровь. Дальний конец дальнего наконечника канала может быть выполнен с возможностью установления соединения по текучей среде с артерией, веной, камерой сердца или другой структурой, содержащей кровь, посредством анастомоза. Дальний конец дальнего наконечника канала, выполненный с возможностью установления сообщения по текучей среде с артерией, веной, камерой сердца или другой структурой, содержащей кровь, посредством анастомоза, может содержать вспененный политетрафторэтилен (ePTFE) или Dacron.
[390] Дальний конец дальнего наконечника канала может быть выполнен с возможностью установления сообщения по текучей среде с артерией, веной, камерой сердца или другой кровеносной структурой путем введения, полностью или частично, дальнего наконечника канала в артерию, вену, камеру сердца или другую структуру, содержащую кровь. Участок дальнего наконечника канала, выполненный с возможностью размещения в просвете кровеносного сосуда, например, периферической вены и артерии, может упоминаться в настоящем документе как «внутрисосудистый участок», «внутрисосудистый сегмент» или «дальний сегмент» дальнего наконечника канала.
[391] Ближний конец дальнего наконечника канала может быть выполнен с возможностью крепления или может быть прикреплен к ближнему сегменту канала, дальнему сегменту канала, или к боковому каналу. В некоторых вариантах реализации изобретения боковой канал, ближний сегмент канала, дальний сегмент канала и дальний наконечник канала соединены друг с другом до операции или процедуры имплантации. В других вариантах реализации изобретения боковой канал, ближний сегмент канала, дальний сегмент канала и дальний наконечник канала выполнены с возможностью соединения, и соединяются друг с другом во время операции или процедуры имплантации при настройке перфузионной системы для использования. В некоторых вариантах реализации изобретения ближний сегмент канала, дальний сегмент канала и дальний наконечник канала соединены друг с другом до операции или процедуры имплантации. В других вариантах реализации изобретения ближний сегмент канала, дальний сегмент канала и дальний наконечник канала выполнены с возможностью соединения, и соединяются друг с другом во время операции или процедуры имплантации при настройке перфузионной системы для использования. В некоторых вариантах реализации изобретения ближний сегмент канала и дальний наконечник канала соединены друг с другом до операции или процедуры имплантации. В других вариантах реализации изобретения ближний сегмент канала и дальний наконечник канала выполнены с возможностью соединения, и соединяются друг с другом во время операции или процедуры имплантации при настройке перфузионной системы для использования.
[392] В некоторых вариантах реализации изобретения дальний наконечник канала выполнен, выполнен в основном или выполнен по существу из металла или металлического сплава, включая, но не ограничиваясь ими, нержавеющую сталь, нитинол, титан, золото, платину, их сплавы, и их комбинации. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. Также может быть использована нержавеющая сталь марки 400. В некоторых вариантах реализации изобретения дальний наконечник канала выполнен, выполнен в основном или выполнен по существу из нержавеющей стали. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. Также может быть использована нержавеющая сталь марки 400. В некоторых вариантах реализации изобретения дальний наконечник канала выполнен из одной заготовки, трубки или другого материала из нержавеющей стали. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM.
[393] В некоторых вариантах реализации изобретения дальний наконечник канала выполнен, выполнен в основном или выполнен по существу из жесткого полимера, включая, но не ограничиваясь ими, поликарбонат или полиэфирэфиркетон или их комбинации. В некоторых вариантах реализации изобретения дальний наконечник канала выполнен, выполнен в основном или выполнен по существу из полностью или частично металлизированного полимера для обеспечения требуемых характеристик, таких как желаемая форма, материал поверхности или текстура поверхности. В некоторых вариантах реализации изобретения дальний наконечник канала выполнен из одной заготовки, трубки или другого материала из поликарбоната или полиэфирэфиркетона. В некоторых вариантах реализации изобретения дальний наконечник канала может быть выполнен из одной или нескольких заготовок из сплошного полимера, включая, но не ограничиваясь ими, поликарбонат или полиэфирэфиркетон и их комбинации.
[394] В некоторых вариантах реализации изобретения дальний наконечник канала может быть выполнен, выполнен в основном или выполнен по существу из гибких или упругих полимеров. Такие гибкие или упругие полимеры включают полиуретаны, полиуретаны Pellethane®, полиуретаны Carbothane®, Carbothane® PC-3575A с твердостью по Шору 70A, ароматические полиуретановые эластомерные сплавы, ароматические полиуретановые эластомерные сплавы Polyblend 1100, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 45A, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 55A, поливинилхлориды, полиэтилены, силиконовые эластомеры, политетрафторэтилены, вспененный политетрафторэтилен, полиэтилентерефталаты, эластомеры из термопластичного кремнийорганического поликарбоната, полиэфирблокамиды и их комбинации с твердостью по Шору в диапазоне от 20A до 80A, от 20A до 30A, от 30A до 40A, от 40A до 50A, от 50A до 60A, от 60A до 70A, от 70A до 80, или с твердостью по Шору 20A, 25A, 30A, 35A, 40A, 45A, 50A, 55A, 60A, 65A, 70A, 75A, или 80A. Гибкие сегменты дальнего наконечника канала могут содержать проволочную или сетчатую несущую конструкцию. Проволочная или сетчатая несущая конструкция может быть выполнена в виде оплетки, спирали или сетки. Проволочная или сетчатая несущая конструкция может содержать упругую проволоку или полимеры, или проволоку или полимеры с памятью формы. Проволочная или сетчатая несущая конструкция может быть выполнена, выполнена в основном или выполнена по существу из нитинола или нержавеющей стали, PTFE или их комбинаций. Проволочная или сетчатая несущая конструкция может быть расположена на внутренней (просветной) поверхности или наружной поверхности гибких сегментов дальнего наконечника канала, или может быть встроена в стенку гибких сегментов дальнего наконечника канала. Проволочная или сетчатая несущая конструкция может обеспечивать гибкость, устойчивость к сжатию или устойчивость к изгибу гибких сегментов дальнего наконечника канала.
[395] В некоторых вариантах реализации изобретения дальний наконечник канала может быть выполнен из различных материалов, включая комбинацию металлов, комбинацию полимеров, комбинацию металлов и полимеров и комбинацию различных металлов и различных полимеров. Ближний (или внутрисосудистый) участок и дальний (или внутрисосудистый) участок дальнего наконечника канала может быть выполнен из различных материалов, включая комбинацию металлов, комбинацию полимеров, комбинацию металлов и полимеров и комбинацию различных металлов и различных полимеров. В некоторых вариантах реализации изобретения, полностью или частично, дальний наконечник канала образован путем литья под давлением, механической обработки, стереоскопической печати или их комбинаций.
[396] Один вариант реализации (линейного) дальнего наконечника 2000 канала показан на фиг. 72А. Этот вариант реализации изобретения представляет собой удлиненную трубчатую структуру, имеющую ближний участок 2002, дальний участок 2004 и медиальный участок 2006, расположенный между ближним и дальним участками. Как показано, ближний участок 2002 имеет внутренний диаметр D21, который больше, чем внутренний диаметр D22 дальнего участка 2004. Внутренний диаметр медиального участка 2006 уменьшается по продольной оси 1 наконечника 2000 от первого диаметра, примерно равного D21, до второго диаметра, примерно равного D22. В качестве примера, а не ограничения, как показано, внутренний диаметр D21 ближнего участка 2002 находится в диапазоне примерно от 3 до 5 мм, тогда как внутренний диаметр D22 дальнего участка 2004 находится в диапазоне примерно от 1,0 до 3,5 мм. В качестве примера, а не ограничения, как показано, наружный диаметр D23 медиального участка сужается, что соответствует уменьшению его внутреннего диаметра. В некоторых вариантах реализации изобретения линейный дальний наконечник 2000 канала может иметь общую длину в диапазоне примерно от 1 до 20 см, 1 и 10 см, 1 и 5 см, 2 и 10 см и 2 и 5 см. В качестве примера, а не ограничения, как показано, дальний наконечник 2000 канала выполнен, выполнен по существу или содержит, главным образом, гибкий полимер. Как показано, и в качестве примера, а не ограничения, гибкий дальний наконечник 2000 канала может быть выполнен из полиуретанов, полиуретанов Pellethane®, полиуретанов Carbothane®, Carbothane® PC-3575A с твердостью по Шору 70A, ароматических полиуретановых эластомерных сплавов, ароматических полиуретановых эластомерных сплавов Polyblend 1100, ароматических полиуретановых эластомерных сплавов Polyblend 1100 с твердостью по Шору 45A, ароматических полиуретановых эластомерных сплавов Polyblend 1100 с твердостью по Шору 55A, поливинилхлоридов, полиэтиленов, силиконовых эластомеров, политетрафторэтиленов, вспененного политетрафторэтилена, полиэтилентерефталатов, эластомеров из термопластичного кремнийорганического поликарбоната, полиэфирблокамидов и их комбинации с твердостью по Шору в диапазоне от 20A до 80A, от 20A до 30A, от 30A до 40A, от 40A до 50A, от 50A до 60A, от 60A до 70A, от 70A до 80, или с твердостью по Шору 20A, 25A, 30A, 35A, 40A, 45A, 50A, 55A, 60A, 65A, 70A, 75A, или 80A. Гибкий дальний наконечник 2000 канала полностью или частично может быть упрочнен оплеточным, спиральным, навитым или сетчатым материалом с памятью формы, таким как нитинол или другой саморасширяющийся или радиально расширяющийся материал, такой как нержавеющая сталь или PTFE. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. В некоторых вариантах реализации изобретения слой оплеточного нитинола, нержавеющей стали или оплеточного PTFE может быть обернут полностью или частично вокруг наружной поверхности дальнего наконечника 2000 канала, или встроен полностью или частично в его стенку. В некоторых вариантах реализации изобретения спираль или навивка из нитинола, нержавеющей стали или PTFE может быть обернута полностью или частично вокруг наружной поверхности дальнего наконечника 2000 канала или встроена полностью или частично в его стенку. В некоторых вариантах реализации изобретения проволочная или сетчатая несущая конструкция может быть расположена на внутренней (просветной) поверхности или наружной поверхности гибких сегментов дальнего наконечника канала, или может быть встроена в стенку гибких сегментов дальнего наконечника канала. Проволочная или сетчатая несущая конструкция может обеспечивать гибкость, устойчивость к сжатию или устойчивость к изгибу гибких сегментов дальнего наконечника канала. Ближний конец дальнего наконечника 2000 канала может быть выполнен с одним или несколькими кольцевыми зубцами или может быть выполнен с возможностью соединения с фитингом с кольцевыми зубцами.
[397] Как показано на фиг. 72В другой (линейный) вариант реализации дальнего наконечника 2000 канала содержит ближний участок 2002 и дальний участок 2004. Ближний участок 2002 удлинен и сужен таким образом, что внутренний диаметр D21 уменьшается до D21' по продольной оси 1 наконечника 2000. Как показано, и в качестве примера, а не ограничения, ближний участок 2002 имеет длину от 1 до 30 см, на которой внутренний диаметр уменьшается от D21 в диапазоне от 3 до 5 мм до уменьшенного внутреннего диаметра D22, в диапазоне примерно от 1,0 до 3,5 мм, так что D22 меньше, чем D21. Дальний участок 2004 имеет длину от 1 до 30 см. Ближний конец дальнего наконечника 2000 канала может быть выполнен с одним или несколькими кольцевыми зубцами или может быть выполнен с возможностью соединения с фитингом с кольцевыми зубцами.
[398] Другой вариант реализации (линейного) дальнего наконечника 2000 канала показан на фиг. 73A-C. Как показано, и в качестве примера, а не ограничения, в данном варианте реализации изобретения дальний наконечник канала выполнен, выполнен по существу или содержит, главным образом, нержавеющую сталь. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. Дальний наконечник 316 канала из нержавеющей стали имеет ближний участок 2002 и дальний участок 2004. Ближний участок содержит фитинг 2110 с кольцевыми зубцами для введения в ближний или дальний сегмент 30 канала. Дальний участок может содержать фитинг с кольцевыми зубцами и закругленными краями для введения в кровеносный сосуд 2306 или может не содержать фитинг с кольцевыми зубцами. В качестве примера, а не ограничения, согласно одному варианту реализации изобретения, внутренний диаметр D21 ближнего участка 2002 находится в диапазоне примерно от 3 до 5 мм, тогда как внутренний диаметр D22 дальнего участка 2004 находится в диапазоне примерно от 1,0 до 3,5 мм. В качестве примера, а не ограничения, согласно одному варианту реализации изобретения, линейный дальний наконечник 2000 канала может иметь общую длину в диапазоне примерно от 1 до 30 см, а уменьшение внутреннего диаметра от D21 до D22 происходит в диапазоне примерно от 10 до 90% от этой длины или от 25 до 75% от этой длины. В одном варианте реализации изобретения, показанном на фиг. 73D, ближний конец (линейного) дальнего наконечника 2000 канала собран с дальним концом ближнего или дальнего сегмента 502 канала (выводного) канала 30. Ближний конец дальнего наконечника канала соединен с дальним концом ближнего или дальнего сегмента канала посредством фрикционной посадки, фитинга с кольцевыми зубцами, клеевого соединения, сварки или их комбинации.
[399] Как показано на фиг. 74 и фиг. 75, дальний (выводной) наконечник канала может быть выполнен в виде разветвленного дальнего наконечника канала с ближним сегментом (или ветвью 2102) и дальним сегментом (или ветвью) 2104. Разветвленный дальний наконечник канала в настоящем документе может называться «Т-образным наконечником» или «Т-образным соединителем». Ближний сегмент дальнего наконечника канала в настоящем документе может упоминаться как «приточный патрубок», «приточный участок патрубка», «приточный патрубок канала», «боковая ветвь» или «боковой участок ветви». Дальний сегмент дальнего наконечника канала может упоминаться в настоящем документе как «внутрисосудистый патрубок» или «внутрисосудистый сегмент». Ближний конец ближнего сегмента разветвленного дальнего наконечника канала выполнен с возможностью соединения или соединен с дальним концом ближнего сегмента канала или дальнего сегмента канала таким образом, что устанавливает или будет устанавливать сообщение по текучей среде с дальним концом ближнего сегмента канала или дальнего сегмента канала. Ближний конец ближнего сегмента разветвленного дальнего наконечника канала может содержать один или более кольцевых зубцов. Ближний конец ближнего сегмента разветвленного дальнего наконечника канала выполнен с возможностью соединения или соединен с дальним концом ближнего сегмента канала или дальнего сегмента канала посредством фрикционной посадки, фитинга с кольцевыми зубцами, клеевого соединения, сварки или их комбинаций. Дальний сегмент дальнего наконечника канала имеет два конца, а дальний конец ближнего сегмента разветвленного дальнего наконечника канала соединен с корпусом дальнего сегмента между двумя концами дальнего сегмента.
[400] В некоторых вариантах реализации изобретения трубчатый дальний наконечник канала может быть выполнен из двух разветвленных трубчатых сегментов, ближнего сегмента, соединенного и сообщающегося по текучей среде с дальним сегментом. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента разветвленного дальнего наконечника канала выполнен с возможностью соединения, может быть соединен, или соединен с дальним концом ближнего или дальнего сегмента канала. Дальний сегмент дальнего наконечника канала имеет два конца, а дальний конец разветвленного дальнего наконечника канала соединен и сообщается по текучей среде с корпусом дальнего сегмента разветвленного дальнего наконечника канала между двумя концами. В некоторых вариантах реализации изобретения оба конца дальнего сегмента дальнего наконечника канала могут быть выполнены с возможностью обеспечения сообщения по текучей среде с артерией, веной, камерой сердца или другой структурой, содержащей кровь. Разветвленный дальний наконечник канала в настоящем документе также может называться «Т-образным наконечником», «выводным каналом» или «Т-образным наконечником выводного канала». Ближний сегмент разветвленного дальнего наконечника канала в настоящем документе может также упоминаться как «приточный патрубок» или «впускной патрубок». Дальний сегмент разветвленного дальнего наконечника канала может упоминаться в настоящем документе как «внутрисосудистый патрубок».
[401] В некоторых вариантах реализации изобретения трубчатый ближний сегмент дальнего наконечника 2102 канала простирается от дальнего сегмента (внутрисосудистого патрубка) дальнего наконечника 2104 канала под углом 2106 в диапазоне от 15 до 75 градусов к продольной оси 2108 дальнего сегмента дальнего наконечника канала. В примерах вариантов реализации изобретения, показанных на фиг. 74-80D, угол отклонения составляет примерно 30 градусов. В некоторых вариантах реализации изобретения трубчатый ближний сегмент дальнего наконечника 2102 канала простирается от ретроградного (от сердца) участка дальнего сегмента (внутрисосудистого патрубка) дальнего наконечника 2104 канала под углом в диапазоне от 15 до 75 градусов, 30 градусов или 45 градусов.
[402] В некоторых вариантах реализации изобретения ближний сегмент дальнего наконечника 2102 канала может быть жестким, гибким или может иметь один или более сегментов, которые являются жесткими, и один или более сегментов, которые являются гибкими. В некоторых вариантах реализации изобретения, как показано на фиг. 74-80D, ближний конец ближнего сегмента дальнего наконечника 2102 канала может быть выполнен с возможностью сцепления или сцеплен с дальним концом ближнего или дальнего сегмента 502 канала.
[403] В некоторых вариантах реализации изобретения один или оба конца трубчатого дальнего сегмента дальнего наконечника 2104 канала (внутрисосудистый патрубок) выполнен с возможностью размещения внутри кровеносного сосуда, артерии, вены, камеры сердца или другой структуры, содержащей кровь. В некоторых вариантах реализации изобретения дальний сегмент дальнего наконечника 2104 канала может быть жестким, гибким или может иметь один или более сегментов, которые являются жесткими, и один или более сегментов, которые являются гибкими.
[404] В некоторых вариантах реализации изобретения диаметр, длина, форма и состав ближнего сегмента дальнего наконечника 2102 канала и дальнего сегмента дальнего наконечника канала могут изменяться, в зависимости от клинической ситуации. Например, как показано на фиг. 74, для некоторых вариантов реализации изобретения ближний сегмент дальнего наконечника 2102 канала больше, чем дальний сегмент дальнего наконечника 2104 канала, и как ближний, так и дальний сегменты дальнего наконечника канала выполнены из гибкого эластомерного материала, такого как, но не ограничиваясь ими, полиуретан, поливинилхлорид, полиэтилен, силиконовый эластомер, политетрафторэтилен (PTFE), вспененный политетрафторэтилен (ePTFE), полиэтилентерефталат (PET), эластомеры из термопластичного кремнийорганического поликарбоната или их комбинаций. Подобно прямолинейному дальнему наконечнику 2000 канала, показанному на фиг. 72-73, ближние 2102 или дальние сегменты дальнего наконечника 2104 канала полностью или частично могут быть упрочнены оплеткой, спиралью, навивкой или сеткой из материала с памятью формы, такого как нитинол или другой саморасширяющийся или радиально расширяющийся материал, такой как нержавеющая сталь или PTFE. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. В некоторых вариантах реализации изобретения слой оплеточного нитинола, нержавеющей стали или оплеточного PTFE может быть обернут полностью или частично вокруг наружной поверхности дальнего наконечника 2000 канала, или встроен полностью или частично в его стенку. В некоторых вариантах реализации изобретения спираль или навивка из нитинола, нержавеющей стали или PTFE может быть обернута полностью или частично вокруг наружной поверхности дальнего наконечника 2000 канала или встроена полностью или частично в его стенку. В некоторых вариантах реализации изобретения проволочная или сетчатая несущая конструкция может быть расположена на внутренней (просветной) поверхности или наружной поверхности гибких сегментов дальнего наконечника канала, или может быть встроена в стенку гибких сегментов дальнего наконечника канала. Проволочная или сетчатая несущая конструкция может обеспечивать гибкость, устойчивость к сжатию или устойчивость к изгибу гибких сегментов дальнего наконечника канала. В некоторых вариантах реализации изобретения ближний сегмент дальнего наконечника 2102 канала имеет длину, большую, чем длина дальнего сегмента дальнего наконечника 2104 канала, в то время как в других вариантах реализации изобретения ближний сегмент дальнего наконечника 2102 канала имеет длину, меньшую, чем длина дальнего сегмента дальнего наконечника 2104 канала. Длина ближнего сегмента дальнего наконечника 2102 канала находится в диапазоне от 0,5 до 110 см, от 1 до 20 см, предпочтительно в диапазоне от 1 до 5 см или от 1 до 10 см. В некоторых вариантах реализации изобретения ближний сегмент дальнего наконечника 2102 канала является жестким. В некоторых вариантах реализации изобретения ближний сегмент дальнего наконечника 2102 канала является гибким. В некоторых вариантах реализации изобретения ближний сегмент дальнего наконечника 2102 канала является достаточно гибким, чтобы выполнять поворот на 180° или больше, когда он находится на месте в пациенте. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента дальнего наконечника 2102 канала имеет внутренний диаметр D21 от 2 до 5 мм и наружный диаметр от 2,5 до 9 мм. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента дальнего наконечника 2102 канала выполнен с возможностью приема и удержания дальнего конца ближнего или дальнего сегмента канала посредством какого-либо соединения, включая конец с кольцевыми зубцами, фланец, сжимающий фиксатор, фрикционную посадку и клеевое соединение, сварку или пайку, или их комбинации.
[405] Как показано на фиг. 75, для некоторых вариантов реализации изобретения ближний сегмент дальнего наконечника 2102 канала короче, чем дальний сегмент дальнего наконечника 2104 канала. В этом примере ближний и дальний сегменты дальнего наконечника канала выполнены, выполнены в основном или выполнены по существу из нержавеющей стали. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. Также может быть использована нержавеющая сталь марки 400. В некоторых вариантах реализации изобретения длина ближнего сегмента дальнего наконечника 2102 канала находится в диапазоне от 0,5 до 10 см, предпочтительно в диапазоне от 1 до 5 см. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента дальнего наконечника 2102 канала имеет внутренний диаметр D21 от 2 до 5 мм и наружный диаметр от 2,5 до 9 мм. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента дальнего наконечника 2102 канала выполнен с возможностью приема и удержания дальнего конца ближнего или дальнего сегмента канала посредством какого-либо соединения, включая конец с кольцевыми зубцами, фланец, сжимающий фиксатор, фрикционную посадку и клеевое соединение, сварку или пайку, или их комбинации. Как показано на фиг. 75, внутренний диаметр D24 или площадь поперечного сечения канала текучей среды на дальнем конце дальнего сегмента дальнего наконечника 2100 канала являются такими же, как внутренний диаметр D25 или площадь поперечного сечения канала текучей среды на ближнем конце ближнего сегмента дальнего наконечника 2102 канала. В настоящем варианте реализации изобретения внутренний диаметр ближнего конца ближнего или дальнего сегмента канала может быть больше, чем внутренний диаметр ближнего конца и дальнего конца разветвленного дальнего наконечника канала. В настоящем варианте реализации изобретения внутренний диаметр проточного канала в ближнем конце ближнего или дальнего сегмента канала составляет от 3 до 6 мм, а внутренний диаметр проточного канала в дальнем конце ближнего или дальнего сегмента канала составляет от 1,0 до 3,0 мм. Когда указанный вариант реализации разветвленного дальнего наконечника канала используют с указанным ближним или дальним сегментом канала в качестве части перфузионной системы, скорость текучей среды, проходящей через дальний конец разветвленного дальнего наконечника 2100 канала, больше, чем скорость текучей среды, проходящей через ближний конец ближнего или дальнего сегмента канала.
[406] Как показано на фиг. 76-80, для некоторых вариантов реализации изобретения длина ближнего сегмента дальнего наконечника 2102 канала аналогична длине дальнего сегмента дальнего наконечника 2104 канала. В этом примере ближний и дальний сегменты дальнего наконечника канала выполнены, выполнены в основном или выполнены по существу из нержавеющей стали. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. Также может быть использована нержавеющая сталь марки 400. В некоторых вариантах реализации изобретения длина ближнего сегмента дальнего наконечника 2102 канала находится в диапазоне от 1 до 10 см, предпочтительно в диапазоне от 1 до 5 см. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента дальнего наконечника 2102 канала имеет внутренний диаметр D21 от 2 до 5 мм и наружный диаметр от 2,5 до 9 мм. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента дальнего наконечника 2102 канала выполнен с возможностью приема и удержания дальнего конца ближнего или дальнего сегмента канала посредством какого-либо соединения, включая конец с кольцевыми зубцами, фланец, сжимающий фиксатор, фрикционную посадку и клеевое соединение, сварку или пайку, или их комбинации. Как показано на фиг. 75, внутренний диаметр D24 или площадь поперечного сечения канала текучей среды на дальнем конце дальнего сегмента дальнего наконечника 2100 канала меньше, чем внутренний диаметр D25 или площадь поперечного сечения канала текучей среды на ближнем конце ближнего сегмента дальнего наконечника 2102 канала. В некоторых вариантах реализации изобретения длина ближнего сегмента дальнего наконечника 2102 канала составляет от 0,5 до 10 см, предпочтительно, между 1 и 5 см. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента дальнего наконечника 2102 канала имеет внутренний диаметр D25 от 2 до 5 мм и наружный диаметр от 2,5 до 9 мм. В некоторых вариантах реализации изобретения ближний конец ближнего сегмента дальнего наконечника 2102 канала выполнен с возможностью приема и удержания дальнего конца ближнего или дальнего сегмента канала посредством какого-либо соединения, включая конец с кольцевыми зубцами, фланец, сжимающий фиксатор, фрикционную посадку и клеевое соединение, сварку или пайку, или их комбинации. В этом варианте реализации изобретения внутренний диаметр или площадь поперечного сечения проточного канала в ближнем конце ближнего сегмента разветвленного дальнего канала D25 больше, чем внутренний диаметр или площадь поперечного сечения проточного канала в дальнем конце дальнего сегмента разветвленного дальнего наконечника D24 канала. В настоящем варианте реализации изобретения внутренний диаметр проточного канала в ближнем конце ближнего сегмента дальнего наконечника канала D25 составляет от 3 до 6 мм, а внутренний диаметр проточного канала в дальнем конце дальнего сегмента наконечника приточного канала D24 составляет от 1 до 4 мм. Когда указанный вариант реализации разветвленного дальнего наконечника канала используют в качестве части перфузионной системы, скорость текучей среды, проходящей через дальний сегмент разветвленного дальнего наконечника 2100 канала, больше, чем скорость текучей среды, проходящей через ближний конец ближнего сегмента дальнего наконечника канала.
[407] В некоторых вариантах реализации изобретения внутренние поверхности проточных каналов разветвленного дальнего наконечника канала, кроме того, образованы полированной поверхностью. В некоторых вариантах реализации изобретения внутренние поверхности проточных каналов разветвленного дальнего наконечника канала имеют шероховатость поверхности в диапазоне от 2 до 16 мкм Ra или от 4 до 8 мкм Ra. В некоторых вариантах реализации изобретения наружные поверхности разветвленного дальнего наконечника канала, кроме того, образованы полированной поверхностью. В некоторых вариантах реализации изобретения наружные поверхности разветвленного дальнего наконечника канала имеют шероховатость поверхности в диапазоне от 2 до 16 мкм Ra или от 4 до 8 мкм Ra. В некоторых вариантах реализации изобретения соединение 2112 между приточным ответвлением 2102 и внутрисосудистым ответвлением 2104 дополнительно образовано полированной и скругленной поверхностью. Когда разветвленный дальний наконечник канала вводят в кровеносный сосуд, артерию, вену, камеру сердца или другую структуру, содержащую кровь, полированные наружные поверхности уменьшают повреждение стенок кровеносных сосудов, артерий, вен, сердечных камер или других структур, содержащих кровь. Когда разветвленный дальний наконечник канала вводят в кровеносный сосуд, артерию, вену, камеру сердца или другую структуру, содержащую кровь, полированные наружные поверхности уменьшают повреждение крови и клеточных элементов крови, в том числе, снижают активацию тромбоцитов и гемолиз.
[408] В других вариантах реализации изобретения ближний и дальний концы разветвленного дальнего наконечника 2114 и 2116 канала имеют полный радиус и являются полностью дугообразными от наружной поверхности до внутренней поверхности, как показано на фиг. 76B. Полный радиус дальнего и ближнего концов рассчитан для уменьшения повреждения стенки сосуда во время размещения, уменьшения случаев тромбоза из-за застойного кровотока и уменьшения повреждения крови и клеточных элементов крови, включая снижение активации тромбоцитов и гемолиза крови, покидающей наконечник 2100.
[409] В некоторых вариантах реализации разветвленного (выводного) дальнего наконечника 2100 канала ближний сегмент 2102 имеет в основном эллипсоидное поперечное сечение с малой осью D26 и большой осью D27 на пересечении 2112 ближнего сегмента 2102 и дальнего сегмента 2104, как показано на фиг. 78В. Внутренний диаметр D26 ближнего сегмента дальнего наконечника 2102 канала уменьшается вдоль одной оси от ближнего конца ближнего канала до дальнего конца ближнего канала. В качестве примера, внутренний диаметр D26 ближнего сегмента дальнего наконечника 2102 канала уменьшается примерно от 4 до 3 мм от ближнего конца ближнего канала до дальнего конца ближнего канала. Внутренний диаметр D27 ближнего сегмента дальнего наконечника 2102 канала увеличивается вдоль второй оси, перпендикулярной продольной оси 2108, от ближнего конца ближнего канала до дальнего конца ближнего канала. В качестве примера, а не ограничения, диаметр D27 ближнего сегмента дальнего наконечника 2102 канала увеличивается примерно от 4 до 13 мм. Указанное уменьшение D26 и увеличение D27 также проиллюстрировано на фиг. 80A и 80B, причем коническая конфигурация ближнего сегмента дальнего наконечника 2102 канала может быть количественно определена углом α относительно длины наконечника 2100. В качестве примера, а не ограничения, угол α может находиться в диапазоне от 5 до 15 градусов.
[410] В одном варианте реализации изобретения, показанном на фиг. 75-80, ближний конец ближнего сегмента дальнего наконечника 2102 канала выполнен с фитингом 2110 с кольцевыми зубцами для приема дальнего конца гибкого сегмента канала, такого как ближний или дальний сегмент канала. В некоторых вариантах реализации изобретения ближний или дальний сегмент канала может иметь длину от 2 см до 110 см и может быть отрезан до требуемой длины хирургом или другим врачом, в том числе при имплантации канала, ближнего или дальнего сегмента канала, или дальнего наконечника 2000 или 2100 канала. В некоторых вариантах реализации изобретения ближний или дальний сегмент канала может быть выполнен, выполнен в основном или выполнен по существу из полиуретана (например, Pellethane ® или Carbothane®), поливинилхлорида, полиэтилена, силиконового эластомера, политетрафторэтилена (PTFE), вспененного политетрафторэтилена (ePTFE), полиэтилентерефталата (PET, например, сложный полиэфир Dacron), эластомеров из термопластичного кремнийорганического поликарбоната или их комбинаций. В некоторых вариантах реализации изобретения ближний наконечник 2102 канала или дальние сегменты дальнего наконечника 2104 канала, полностью или частично могут быть упрочнены оплеточным, спиральным, навитым или сетчатым материалом с памятью формы, таким как нитинол или другой саморасширяющийся или радиально расширяющийся материал, такой как нержавеющая сталь или PTFE. Могут быть использованы различные марки биосовместимой нержавеющей стали, в том числе нержавеющая сталь марки 300, и предпочтительно, нержавеющая сталь марок 304, 316, 316L, или 316LVM. В некоторых вариантах реализации изобретения слой оплеточного нитинола, нержавеющей стали или оплеточного PTFE может быть обернут полностью или частично вокруг наружной поверхности дальнего наконечника 2000 канала, или встроен полностью или частично в его стенку. В некоторых вариантах реализации изобретения спираль или навивка из нитинола, нержавеющей стали или PTFE может быть обернута полностью или частично вокруг наружной поверхности дальнего наконечника 2000 канала или встроена полностью или частично в его стенку. В некоторых вариантах реализации изобретения проволочная или сетчатая несущая конструкция может быть расположена на внутренней (просветной) поверхности или наружной поверхности гибких сегментов дальнего наконечника канала, или может быть встроена в стенку гибких сегментов дальнего наконечника канала. Проволочная или сетчатая несущая конструкция может обеспечивать гибкость, устойчивость к сжатию или устойчивость к изгибу гибких сегментов дальнего наконечника канала. В некоторых вариантах реализации изобретения внутренний диаметр проксимальных или дальних сегментов D31 или D41 канала, как показано на фиг. 81B и 82B, может быть постоянным. В других вариантах реализации изобретения внутренний диаметр ближнего или дальнего сегментов D31 или D41 канала может сужаться до меньшего внутреннего диаметра.
[411] Когда перфузионная система, описанная в настоящем документе, выполненная с возможностью устойчивого увеличения диаметра периферических вен или артерий, содержит ближний сегмент канала, дальний сегмент канала или дальний наконечник канала, сужающийся от ближнего конца к дальнему концу, используемый для перекачивания крови в вену или артерию определенного диаметра, и система перекачивает кровь в артерию или вену со скоростью, равной или большей определенного уровня, тогда в просвете сегмента вены или артерии, прилегающей к дальнему концу дальнего канала может быть создан эффект струи, при котором этот сегмент вен или артерии испытывает более высокое WSS, чем более ближние сегменты вены или артерии. Те сегменты вены или артерии, которые испытывают более высокое WSS, могут устойчиво расширяться, создавая сегмент вены или артерии с устойчиво большим общим диаметром сосуда или диаметром просвета сосуда, который может быть больше оптимизирован для различных целей, в том числе для создания AVF, AVG, шунтирующих трансплантатов или других операций или процедур, для которых требуется больший общий диаметр сосуда или диаметр просвета сосуда.
[412] В некоторых вариантах реализации изобретения канал может содержать единственный трубчатый элемент из гибкого материала, причем дальний наконечник канала объединен с каналом, и при этом дальний конец канала сообщается по текучей среде с кровеносным сосудом, артерией, веной, камерой сердца или другой структурой, содержащей кровь, путем введения дальнего участка канала в просвет кровеносного сосуда, артерии, вены, камеры сердца или другой структуры, содержащей кровь, или при этом дальний конец выводного канала соединен с кровеносным сосудом, артерией, веной, камерой сердца или другой структурой, содержащей кровь, посредством анастомоза или других устройств для сообщения по текучей среде выводного канала с кровеносным сосудом, артерией, веной, камерой сердца или другой структурой, содержащей кровь. В других вариантах реализации изобретения канал может содержать ближний сегмент канала, соединенный с дальним сегментом канала, причем дальний наконечник канала объединен с дальним сегментом канала, а дальний конец сегмента дальнего выводного канала сообщается по текучей среде с кровеносным сосудом, артерией, веной, камерой сердца или другой структурой, содержащей кровь, путем введения дальнего участка дальнего сегмента выводного канала в просвет кровеносного сосуда, артерии, вены, камеры сердца или другой структуры, содержащей кровь, или при этом дальний конец дальнего сегмента выводного канала соединен с кровеносным сосудом, артерией, веной, камерой сердца или другой структурой, содержащей кровь, посредством анастомоза или других устройств для сообщения по текучей среде дальнего конца дальнего сегмента выводного канала с кровеносным сосудом, артерией, веной, камерой сердца или другой структурой, содержащей кровь. В других вариантах реализации изобретения канал может содержать ближний сегмент выводного канала, соединенный с дальним сегментом выводного канала, который соединен с дальним наконечником канала, как показано на фиг. 83. В некоторых вариантах реализации изобретения дальний наконечник канала может быть выполнен, выполнен в основном или выполнен по существу из полимера, необязательно с металлической или полимерной несущей конструкцией в виде оплетки, спирали или сетки, включая несущую конструкцию из нитинола, нержавеющей стали и PTFE. В некоторых вариантах реализации изобретения наконечник дальнего канала может быть выполнен, выполнен в основном или выполнен по существу из металлов или металлических сплавов, таких как нержавеющая сталь, титан, нитинол, золото, платина или их комбинаций.
[413] В одном варианте реализации изобретения, показанном на фиг. 80D, дальний наконечник 2100 канала представляет собой разветвленный наконечник канала и выполнен с возможностью введения в вену, артерию или кровеносный сосуд и использования в качестве наконечника выводного канала. Дальний наконечник 2100 канала собран с дальним сегментом 502 канала для канала 30. Ближний конец ближнего сегмента разветвленного дальнего наконечника 2110 канала может содержать кольцевые зубцы, или не содержать их, и может быть соединен с дальним концом дальнего сегмента канала посредством фитинга с кольцевыми зубцами, фрикционной посадки, клеевого соединения, сварки или пайки, или их комбинаций. Ближний конец дальнего сегмента 502 канала может быть соединен с дальним концом ближнего сегмента 500 канала путем установки между ними трубчатого встроенного в линию соединителя 501. В некоторых вариантах реализации изобретения встроенный в линию соединитель может содержать фитинг с кольцевыми зубцами на одном или обоих концах, а ближний конец дальнего сегмента канала или дальний конец ближнего сегмента канала может быть соединен с встроенным в линию соединителем с использованием радиально сжимающих фиксаторов или фиксирующих колец. В некоторых вариантах реализации изобретения ближний и дальний сегменты канала могут быть соединены со встроенным в линию соединителем посредством фрикционной посадки или клеевого соединения или их комбинаций. В некоторых вариантах реализации изобретения диаметр просвета одного конца встроенного в линию соединителя может быть больше или меньше диаметра просвета другого конца встроенного в линию соединителя. Использование этих вариантов реализации изобретения обеспечивает способ соединения двух сегментов канала с различными диаметрами просвета, включая ближние сегменты канала, дальние сегменты канала, боковые каналы и ближние сегменты дальних наконечников канала.
[414] Другой вариант реализации изобретения канала 30 показан на фиг. 83, причем канал имеет ближний сегмент 500 канала и дальний сегмент 502 канала. Ближний конец ближнего сегмента 500 канала выполнен с возможностью крепления к перфузионному насосу или боковому каналу. Как показано на фиг. 83, встроенный в линию соединитель с фитингами с кольцевыми зубцами на обоих концах соединен с ближним концом ближнего сегмента канала с использованием радиально сжимающего фиксатора или фиксирующего кольца. Как показано на фиг. 83, дальний конец ближнего сегмента 500 канала соединен с ближним концом дальнего сегмента 502 канала посредством промежуточного соединения встроенного в линию соединителя с фитингами с кольцевыми зубцами на обоих концах с использованием радиально сжимающих фиксаторов или фиксирующих колец на обоих концах. Как показано на фиг. 83, ближний сегмент канала содержит проволочную несущую конструкцию в виде оплетки, а дальний сегмент канала содержит проволочную несущую конструкцию в виде спирали. Как показано на фиг. 83, дальний конец дальнего сегмента канала соединен с ближним концом (прямого) дальнего наконечника 2000 канала. Канал 30 может быть использован для соединения насосной системы 10 AFE с веной, артерией, кровеносным сосудом, камерой сердца, или другой структурой, содержащей кровь. Конфигурация наконечника 2000 выводного канала устраняет необходимость в создании хирургического анастомоза для достижения гемостатического сообщения по текучей среде между каналом и артерией, кровеносным сосудом, камерой сердца или другой структурой, содержащей кровь, что потенциально сокращает время, необходимое для имплантации системы AFE и начала лечения.
[415] Как показано на фиг. 81A и 81B, ближний сегмент 500 канала может иметь общую длину L31 примерно от 1 до 110 см, от 5до 100 см или от 2 до 20 см, внутренний диаметр D31 от 2 до 6 мм или от 3 до 5 мм, и наружный диаметр D32 от 2,5 до 9 мм или от 4 до 8 мм. В одном варианте реализации изобретения ближний сегмент 500 канала выполнен из четырех слоев. Внутренний слой 2702, средний слой 2706 и наружный слой 2708 представляют собой биосовместимые полимеры, такие как полиуретаны, полиуретаны Pellethane®, полиуретаны Carbothane®, Carbothane® PC-3575A, Carbothane® PC-3575A с твердостью по Шору 70A, ароматические полиуретановые эластомерные сплавы, ароматические полиуретановые эластомерные сплавы Polyblend 1100, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 45A, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 55A, поливинилхлориды, полиэтилены, силиконовые эластомеры, политетрафторэтилены, вспененные политетрафторэтилены, полиэтилентерефталаты, эластомеры из термопластичного кремнийорганического поликарбоната, полиэфирблокамиды и их комбинации с твердостью по Шору в диапазоне от 20A до 80A, от 20A до 30A, от 30A до 40A, от 40A до 50A, от 50A до 60A, от 60A до 70A, от 70A до 80, или с твердостью по Шору 20A, 25A, 30A, 35A, 40A, 45A, 50A, 55A, 60A, 65A, 70A, 75A, или 80A. Предпочтительно один или более слоев ближнего сегмента канала выполнен из полимера Carbothane® PC-3575A твердости по Шору 70A. Предпочтительно упрочнение ближнего сегмента канала представляет собой проволоку из нитинола диаметром 0,05-0,2 мм (0,002-0,008 дюйма), предпочтительно 0,1 мм (0,004 дюйма), в виде оплетки, показанной в виде слоя 2704 между внутренним слоем и наружным слоем. В некоторых вариантах реализации изобретения проволока из нитинола может применяться в виде одной жилы, в то время как в других вариантах реализации изобретения проволока из нитинола может применяться в виде двух жил. Предпочтительно, оплетка из проволоки из нитинола ближнего сегмента канала применяется в виде двух жил. В одном варианте реализации изобретения ближний сегмент 500 канала выполнен из трех слоев. Внутренний слой 2702, несущий слой 2704 и наружный слой 2708. В некоторых вариантах реализации изобретения внутренний слой выполнен, выполнен в основном или выполнен по существу из политетрафторэтилена (PTFE). В некоторых вариантах реализации изобретения ближний конец ближнего сегмента канала, дальний конец ближнего сегмента канала или оба конца могут быть оставлены без упрочнения по длине L43 от 5 до 25 мм.
[416] Как показано на фиг. 82A и 82B, дальний сегмент 502 канала может иметь общую длину L31 от 1 до 110 см, от 5до 100 см или от 2 до 20 см, внутренний диаметр D41 от 2 до 6 мм или от 3 до 5 мм, и наружный диаметр D42 от 2,5 до 9 мм или от 4 до 8 мм. В одном варианте реализации изобретения дальний сегмент 502 канала выполнен из трех слоев. Внутренний слой 2702 и наружный слой 2708 представляют собой биосовместимые полимеры, такие как полиуретаны, полиуретаны Pellethane®, полиуретаны Carbothane®, Carbothane® PC-3575A с твердостью по Шору 70A, ароматические полиуретановые эластомерные сплавы, ароматические полиуретановые эластомерные сплавы Polyblend 1100, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 45A, ароматические полиуретановые эластомерные сплавы Polyblend 1100 с твердостью по Шору 55A, поливинилхлориды, полиэтилены, силиконовые эластомеры, политетрафторэтилены, вспененные политетрафторэтилены, полиэтилентерефталаты, эластомеры из термопластичного кремнийорганического поликарбоната, полиэфирблокамиды и их комбинации с твердостью по Шору в диапазоне от 20A до 80A, от 20A до 30A, от 30A до 40A, от 40A до 50A, от 50A до 60A, от 60A до 70A, от 70A до 80, или с твердостью по Шору 20A, 25A, 30A, 35A, 40A, 45A, 50A, 55A, 60A, 65A, 70A, 75A, или 80A.
[417] Предпочтительно один или более слоев дальнего сегмента канала выполнен из ароматических полиуретановых эластомерных сплавов Polyblend 1100 с твердостью по Шору 45A или 55A или Carbothane® PC-3575A с твердостью по Шору 70A. Предпочтительно упрочнение дальнего сегмента канала представляет собой проволоку из нитинола диаметром 0,20-0,254 мм (0,008-0,010 дюйма), с шагом навивки 0,508-0,762 мм (0,02-0,03 дюйма) в виде спирали, показанной в виде слоя 2710 между внутренним слоем и наружным слоем. В некоторых вариантах реализации изобретения проволока из нитинола может применяться в виде одной жилы, в то время как в других вариантах реализации изобретения проволока из нитинола может применяться в виде двух жил. Предпочтительно, оплетка из проволоки из нитинола ближнего сегмента канала применяется в виде двух жил. В одном варианте реализации изобретения ближний сегмент 500 канала выполнен из трех слоев. Внутренний слой 2702, несущий слой 2704 и наружный слой 2708. В некоторых вариантах реализации изобретения внутренний слой выполнен, выполнен в основном или выполнен по существу из политетрафторэтилена (PTFE).
[418] В некоторых вариантах реализации изобретения ближний конец дальнего сегмента канала может быть оставлен без упрочнения по длине L43 от 5 до 25 мм. В некоторых вариантах реализации изобретения дополнительный слой 520 толщиной примерно от 0,5 до 2 мм может быть нанесен на ближний конец дальнего сегмента канала. В некоторых вариантах реализации изобретения указанный дополнительный слой может перекрывать неупрочненный сегмент с длиной L43, составляющей от 5 до 25 мм, и упрочненный сегмент с длиной L44, составляющей от 5 до 25 мм. В некоторых вариантах реализации изобретения дальний конец дальнего сегмента канала может быть оставлен без упрочнения по длине L46 от 5 до 25 мм. В некоторых вариантах реализации изобретения дополнительный слой 520 толщиной примерно от 0,5 до 2 мм может быть нанесен на ближний конец дальнего сегмента канала. В некоторых вариантах реализации изобретения указанный дополнительный слой может перекрывать неупрочненный сегмент с длиной L46, составляющей от 5 до 25 мм, и упрочненный сегмент с длиной L45, составляющей от 5 до 25 мм.
[419] Согласно одному варианту реализации изобретения, как показано на фиг. 83, канал 30 собран путем соединения ближнего сегмента 500 канала и дальнего сегмента 502 канала друг с другом с использованием встроенного в линию соединителя 501. В некоторых вариантах реализации изобретения манжета 800 прикреплена к ближнему сегменту 500 канала. В других вариантах реализации изобретения манжета 800 прикреплена к дальнему сегменту 502 канала. В некоторых вариантах реализации изобретения ближний сегмент соединен с боковым каналом 417, а дальний сегмент 502 соединен с дальним каналом (линейным) 2000 или дальним наконечником 2100 канала дальнего (разветвленного) канала.
[420] Некоторые варианты реализации изобретения каналов, в которых прием крови из насоса и доставка или передача крови в вену или артерию, содержащую дальний (выводной) наконечник 2000 и 2100 каналов, могут обеспечивать локализованные зоны повышенного WSS, благодаря по меньшей мере частично эффекту струи, вызванному увеличением скорости крови. На фиг. 84 показаны изображения 2300А и 2300В овечьей головной вены после лечения с использованием варианта реализации системы 10 AFE и способов, описанных в настоящем документе. В этом варианте реализации изобретения был использован канал для передачи крови из перфузионного насоса в головную вену овцы. Ближний сегмент канала выполнен из полимера Carbothane® PC-3575A с твердостью по Шору 70A с проволочной несущей конструкцией из нитинола в виде оплетки. Дальний сегмент канала выполнен из ePTFE. Дальний конец дальнего сегмента канала был соединен по текучей среде со стороной овечьей головной вены посредством анастомоза 2100. По истечении периода заживления кровь перекачивали в головную вену овцы. Во время периода заживления в стенке вены в антероградном сегменте вены (в направлении сердца) образовывалась рубцовая ткань, что приводило к стенозу. Неожиданно, рубцевание и стеноз усиливали лечебное действие системы AFE. Перекачивание крови через указанный стеноз создавало эффект струи в сегменте вены, антероградном относительно суженного сегмента. Через 9 дней сегмент вены, антероградный относительно суженной зоны, которая принимала струйную кровь 2302, расширялся до большей величины, чем сегменты, ближние и дальние относительно этой зоны, по-видимому, из-за увеличения WSS в указанном сегменте 2302. Указанный сегмент вены большего диаметра затем был рассечен и соединен, и связан по текучей среде с соседней артерией посредством анастомоза для образования AVF. Учитывая, что многие AVF не достигают созревания или теряют проходимость из-за образования стеноза в сегменте вены, прилегающем к анастомозу с артерией, эта зона вены с большим диаметром была особенно оптимальна для создания AVF.
[421] Как показано на фиг. 106, система AFE была собрана с (выводным) каналом для передачи крови из насоса в головную вену овцы. Канал состоял (от ближнего до дальнего) из бокового канала, встроенного в линию соединителя, ближнего сегмента канала, встроенного в линию соединителя, дальнего сегмента канала и разветвленного дальнего наконечника канала. В указанном варианте реализации изобретения площадь поперечного сечения пути текучей среды в ближнем сегменте канала, дальнем сегменте канала и ближнем сегменте разветвленного дальнего наконечника канала была одинаковой, а площадь поперечного сечения пути текучей среды на обоих концах дальнего сегмента пути дальнего канала была меньше площади поперечного сечения пути текучей среды на ближнем конце ближнего сегмента дальнего канала. Когда кровь закачивали в вену, эффект струи создавался по мере выхода крови из ближнего конца дальнего сегмента дальнего наконечника канала, создавая зону более высокого WSS, что приводило, через 9-11 дней лечения, к образованию зоны с увеличенным диаметром в сегменте вены, прилегающем к антероградному дальнему концу разветвленного дальнего наконечника канала. Указанный сегмент вены большего диаметра затем был рассечен и соединен, и связан по текучей среде с соседней артерией посредством анастомоза для образования AVF. Учитывая, что многие AVF не достигают созревания или теряют проходимость из-за образования стеноза в сегменте вены, прилегающем к анастомозу с артерией, эта зона вены с большим диаметром была особенно оптимальна для создания AVF. Примеры AVF, выполненных в овечьих головных венах, но без предварительного лечения с помощью системы AFE, показаны на фиг. 88 и 89, со стенозом вены, который развился, помеченным стрелками. На фиг. 88 и 89, также показано небольшое отверстие между артерией и веной, которое может ограничить поток AVF. На фиг. 90 показана AVF, выполненная в овечьей головной вене, предварительно прошедшая лечение с помощью системы AVF, которая демонстрирует большее отверстие между артерией и веной, и отличается большим сегментом вены, прилегающим к артерии, и отсутствием стеноза вены.
[422] Разветвленный дальний наконечник канала на фиг. 106 улучшен по сравнению с наконечником дальнего канала из ePTFE на фиг. 84, так как после лечения он создавал контролируемый и воспроизводимый стеноз в дальнем конце выводного канала для создания струйной крови и расширенного сегмента вены. Разветвленный дальний наконечник канала на фиг. 106 (называемый «Т-образным соединителем выходного канала») также поддерживает антероградный поток крови из места, дальнего относительно дальнего наконечника канала, через просвет дальнего сегмента дальнего наконечника канала, и в сегмент вены, ближний относительно дальнего наконечника канала, что уменьшает риск дальнего наконечника канала или тромбоза вены, когда система AFE выключена или работает при низкой скорости потока. Как показано на фиг. 85 и 106, дальний сегмент разветвленного дальнего наконечника 2104 канала также защищает стенку сосуда напротив впускной ветви 2102 от возможной травмы, вызванной быстрым потоком крови, выходящей из дальнего конца ближнего сегмента дальнего наконечника канала, который направлен к стенке сосуда. Как показано на изображении CFD на фиг.85, кровь, выходящая из дальнего наконечника канала, имеет увеличенную скорость. Дополнительные изображения, иллюстрирующие необходимое увеличение кровеносных сосудов с использованием некоторых вариантов реализации выводного наконечника 2000 или 2100, показаны на фиг.88-82B и 106-107.
[423] На фиг. 86-87 показаны способы введения и крепления разветвленного дальнего наконечника 2100 канала в кровеносном сосуде 2306. На 2400 в сосуде выполнен разрез 2308 или венотомия. На этапе 2402 ближний конец 2104 и дальний конец 2114 дальнего сегмента дальнего наконечника 2100 канала вводят в сосуд и размещают на ближнем конце венотомии 2308. Альтернативно, как показано на этапе 2404, дальний наконечник 2100 канала может быть расположен в центре венотомии 2308. После достижения желаемого положения наконечник 2100 закрепляют на месте, размещая один или более швов в сосуде 2306 для герметизации сосуда, как показано на этапе 2406. В одном варианте реализации изобретения, наконечник 2100 удерживают на месте, накладывая шов на сосуд 2306, чтобы создать плотную фрикционную посадку с наконечником. В другом варианте реализации изобретения разветвленный дальний наконечник 2100 канала может содержать подшиваемую манжету 2310, как показано на фиг. 77, которая жестко связана с дальним наконечником канала в зоне между ближним и дальним сегментами. Подшиваемая манжета может содержать прокалываемый, но прочный материал, включая, но не ограничиваясь этим, велюр из материала Dacron (полиэтилентерефталата), который можно использовать для крепления дальнего наконечника канала к сосуду 2306. Таким образом, различные конфигурации шва, включая, но не ограничиваясь ими, кисетные, непрерывные или узловые швы, могут быть использованы для закрепления дальнего наконечника канала путем наложения швов через сосуд 2306 и подшиваемую манжету 2310. Один пример крепления дальнего наконечника 2100 канала с использованием одного или более кисетных швов 2208 и линейных швов 2210 показан на фиг. 87. В этом примере клей 2212 (например, BioGlue®) также может быть использован для дополнительного крепления сосуда 2306 к дальнему наконечнику 2100 канала и уменьшения утечки крови из венотомии или шовных отверстий.
[424] В некоторых вариантах реализации изобретения некоторые или все внутренние поверхности, наружные поверхности или обе поверхности сегмента ближнего сегмента канала, дальнего сегмента канала или дальнего наконечника 2000 или 2100 канала могут быть покрыты для минимизации или уменьшения инфекции, осаждения белка или активации тромбоцитов. В качестве примера, а не ограничения, покрытие может содержать гепарин или противомикробное вещество. Может быть использовано гепаринизированное гидрофильное покрытие компании Astute® BioInteractions. Также может быть использовано любое другое биосовместимое антитромботическое или противомикробное покрытие.
[425] Каналы с различными элементами и характеристиками могут быть выполнены путем сборки различных сегментов и составных частей. В некоторых вариантах реализации изобретения более длинные каналы могут быть образованы путем включения как проксимальных сегментов канала, так и дальних сегментов канала. В некоторых вариантах реализации изобретения каналы могут быть собраны с ближними сегментами канала, которые являются высокоупругими, и дальними сегментами канала, которые являются очень гибкими и устойчивыми к сжатию или изгибу. В этих вариантах реализации изобретения ближний сегмент канала можно многократно зажимать и разжимать с меньшей деформацией, в то время как дальний сегмент канала может быть выполнен с крутыми изгибами для установления сообщения по текучей среде с веной, артерией, кровеносным сосудом, камерой сердца или другой структурой, содержащей кровь. В качестве примера, а не ограничения, в таком канале ближний сегмент канала может иметь проволочную несущую конструкцию из нитинола в виде оплетки, а дальний сегмент канала может иметь проволочную несущую конструкцию из нитинола в виде несущей спирали, предпочтительно в конфигурации с зазором между витками, который больше, чем ширина проволоки. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может иметь более толстую стенку, чем весь дальний сегмент канала или его часть. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из полимеров с более высокой твердостью, чем весь дальний сегмент канала или его часть. Например, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из полиуретана, а дальний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из ароматического полиуретанового эластомерного сплава. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из полиуретана Pellethane ® или Carbothane®. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен в основном или выполнен по существу из полиуретана с твердостью по Шору 70A. В качестве примера, а не ограничения, в таком канале ближний сегмент канала полностью или частично может быть выполнен, выполнен, выполнен в основном или выполнен по существу из полиуретана Pellethane ® или Carbothane® с твердостью по Шору 70A. В качестве примера, а не ограничения, в таком канале дальний сегмент канала полностью или частично может быть выполнен, выполнен, выполнен в основном или выполнен по существу из ароматического полиуретанового эластомерного сплава с твердостью по Шору 45A или 55A, или их комбинаций. В качестве примера, а не ограничения, в таком канале дальний сегмент канала полностью или частично может быть выполнен, выполнен, выполнен в основном или выполнен по существу из полимера Polyblend 1100 компании AdvanSource Biomaterials, Уилмингтон, штат Массачусетс, с твердостью по Шору 45A или 55A.
[426] В некоторых вариантах реализации изобретения могут быть собраны каналы, в которых дальний конец дальнего (выводного) наконечника канала или дальнего конца дальнего сегмента канала с встроенным дальним наконечником канала может иметь внутренний диаметр 1,5 мм для использования при лечении пациента с головной веной 2,0 мм, нуждающегося в месте сосудистого доступа AVF для гемодиализа, и который не подходит для создания AVF из-за малого диаметра вен. В некоторых вариантах реализации изобретения могут быть собраны каналы, в которых дальний конец дальнего (выводного) наконечника канала или дальнего конца дальнего сегмента канала с встроенным дальним наконечником канала может иметь внутренний диаметр 3 мм для использования при лечении пациента с головной веной 3,5 мм, нуждающегося в месте сосудистого доступа AVF для гемодиализа, который подходит для создания AVF, но существует риск не достижения созревания AVF после хирургического вмешательства. Кроме того, каналы, собранные по меньшей мере из двух гибких сегментов, включая варианты реализации изобретения с ближним и дальним сегментами канала, могут упростить процесс туннелирования участков канала под кожей пациента.
[427] В некоторых вариантах реализации изобретения выводной канал может быть использован для приема крови из артерии, вены, камеры сердца или другой структуры, содержащей кровь, и доставки или передачи крови в насос.
Примеры исследований и экспериментов
[428] В ряде исследований применимости in vivo варианты реализации системы AFE System имплантированы свиньям. В частности, система AFE была установлена с сообщением с левой яремной веной и боковой подкожной веной (saphenous vein, SV) левой задней конечности. В одном исследовании были измерены различные параметры гемодинамики, включая среднее давление правого предсердия (right atrial pressure, RAP), среднее давление легочной артерии (pulmonary artery pressure, PAP), насыщение кислородом (O2), артериальное давление (arterial blood pressure, ABP) и поток насоса, при исследовании непосредственных эффектов на свинье массой 21 кг. Во время исследования ближайших результатов потоки насоса 100-500 мл/мин не вызывали изменений в параметрах гемодинамики или сердечной функции по сравнению с исходными значениями.
[429] Другое исследование заключалось в исследовании отдаленных результатов антикоагулированной свиньи массой 28 кг, боковую подкожную вену лечили в течение 9 дней с дозой WSS около 4 Па. Во время исследования отдаленных результатов поток насоса возрастал от 270 мл/мин в начальный 0 день до 947 мл/мин на 9 день, и выводной сегмент подкожной вены расширился с 3,7 до 13,8 мм, как показано на фиг. 49A, без ангиографических признаков стеноза. Вскрытие, проведенное на 9 день, показало расширенную подкожную вену, которая была удлиненной и легко мобилизуемой. Гистологическое исследование продемонстрировало значительное дилатационное ремоделирование и предельно малую гиперплазию интимы, как показано на фиг. 49В.
[430] Для сравнения результатов использования системы AFE с текущим стандартом лечения артериовенозной фистулы (AVF) было проведено исследование, в котором боковая подкожная вена была мобилизована и соединена с бедренной артерией посредством анастомоза бок (артерии) в конец (вены) для создания AVF. Диаметр и кровоток из выводящей вены AVF определяли в течение 4 недель с помощью ультразвука и ангиографии. Все четыре из созданных AVF не смогли достичь созревания по критериям KDOQI (Kidney Disease Outcomes Quality Initiative, Инициатива качества лечения заболевания почек) (диаметр вен 6 мм и кровоток 600 мл/мин) из-за развития тяжелой гиперплазии интимы и стеноза в выводном сегменте вены, прилегающем к артерии. К 4-й неделе одна AVF была закрыта, а остальные три AVF были почти закрыты.
[431] Было проведено исследование отдаленных результатов на антикоагулированных свиньях массой 20-25 кг, у которых была выполнена артериовенозная фистула между бедренной артерией и мобилизованной боковой подкожной веной на 2 свиньях (n=4 артериовенозных фистулы).
[432] Результаты этих экспериментальных исследований продемонстрировали эффективность системы AFE для расширения и созревания периферических вен in vivo. В частности, исследования показали, что расширение вен примерно 10,1 мм, примерно равное 275% увеличению, было достигнуто после девятидневного курса лечения с поддержанием WSS 4 Па с небольшим образованием гиперплазии интимы в прошедшей лечение расширенной вене. Эти результаты от использования системы AFE резко отличаются от результатов от стандарта лечения AVF, когда расширение вен было слабым, а кровоток AVF был ограничен появлением выраженной гиперплазии интимы и стеноза в выводящей вене.
[433] В другом исследовании гемолитические свойства экстракорпоральных установок перфузионного насоса (extracorporeal blood pump, EBP), в том числе одного, аналогичного насосу 25, были оценены как до, так и после серии испытаний гидравлических характеристик. В качестве эталона были оценены гемолитические свойства испытуемых установок EBP. Для каждого насоса при испытаниях на гемолиз был создан замкнутый имитационный испытательный контур не пульсирующего кровообращения. Пример замкнутого имитационного контура, используемого во время исследования, показан на фиг. 54. Каждый контур содержит трубки из PVC внутренним диаметром (inner diameter, ID) 4 мм (заготовка из материала Tygon № AAC1S1518) для приточных и выводных каналов 5402 и 5404, резервуар 5406 и насос 5408. Приточные и выводные каналы выполнены с размером 0,5 м по длине. Бычью кровь, собранную посредством венопунктуры и хранящуюся в баллоне с антикоагулянтом CPDA-1 (Citrate Phosphate Dextrose Adenine, цитрат-фосфат-декстроза-аденин) (компании Lampire, CN № 7200805), использовали в течение 48 часов, в соответствии со стандартом ASTM F1830-97. Кровь переносили в другие баллоны для крови (1L, компании Sorin Group № 00-700-1001), которые использовали в качестве резервуаров, каждый из которых содержал три канала 5410, используемые в качестве впускных, выпускных и пробоотборных каналов. Прямолинейные соединители с кольцевыми зубцами были использованы для надежного соединения трубки с каналами резервуара. Водяную баню 5412 доводили до 37 °С. Раствор BBS (blood bank saline, солевой раствор консервированной крови) прокачивали через каждый насос и контур в течение 30 минут для промывки систем перед испытаниями. Перед испытаниями резервуары выдерживали над водяной баней с приточными и выводными каналами, подвешенными в ванне, для нагрева циркулирующей крови до 37 °С, как показано на фиг. 54.
[434] Насосы, испытанные при анализе гемолиза, представляли собой насос Medtronic BP-50, используемый для педиатрического кардиопульмонального шунтирования (pediatric cardiopulmonary bypass, CPB) и экстракорпоральной оксигенации (extracorporeal oxygenation, ECMO) и испытательные установки EBP. Скорости насоса выбиралась такими, чтобы поддерживать скорость потока 500 мл/мин. Скорость каждой установки EBP регулировалась посредством блока управления mPBU, а скорость BP-50 5414 поддерживалась с помощью консоли (Medtronic BioMedicus 540 Bioconsole). Поток в каждом цикле измеряли с использованием заказного ультразвукового датчика потока (модель Transonic Systems ME3PXL) крови при 37°C и расходомера (модель Transonic Systems TS410). Каждое испытание на гемолиз проводилось в течение 6 часов, с образцами 3-5 мл, отобранными из каждого насоса через 15-минутные интервалы. Для получения характеристик повреждения крови использовали колориметрический анализ с использованием ранее описанных способов. Результаты были построены в виде графика зависимости концентрации свободного гемоглобина в плазме (plasma free hemoglobin, PFH) от времени, а наклон линии наилучшего соответствия был использован для расчета скоростей гемолиза. Эти исследования проводились три раза на каждом насосе как до, так и после ресурсных испытаний. После каждого этапа исследования на гемолиз насосы промывали с помощью солевого раствора консервированной крови при комнатной температуре.
[435] Результаты гемолиза вычисляли как нормализованный по миллиграммам индекс гемолиза (мг N.I.H.) на основе ASTM F-1841, предпочтительное измерение для сравнения данных в литературе и единиц измерения BP-50. Единицы измерения BP-50 учитывают ежедневные изменения хрупкости крови от одного животного к другому путем нормализации скорости гемолиза EBP с использованием результатов испытаний BP-50, полученных в тот же день с использованием одного и того же источника крови. Вывод выполняют путем деления нормы мг N.I.H. EBP на норму мг N.I.H. BP-50. Величину мг N.I.H определяют по формуле:
мг N.I.H.=Δ несвязанный гемоглобин x V x (100-Ht)/100×100/(QxT);
где величина мг PFH, добавленных на 100 мл перекачиваемой крови, корректируется для объема плазмы и нормализуется по скорости потока и времени выполнения. По существу такие более высокие значения ожидаются при более высоких скоростях потока, если насосы имеют одинаковые гемолитические характеристики. Единицы измерения BP 50 нормализуют с использованием мг NIH BP-50 при одинаковой скорости потока, используя тот же источник крови.
[436] На фиг. 55 показаны непарные результаты для EBP по сравнению с BP-50 в зависимости от единиц мг N.I.H. На фиг. 56 показаны парные результаты предварительных ресурсных испытаний на гемолиз для установок EBP по сравнению с BP-50. На фиг. 57 приведен график, изображающий испытания на гемолиз насоса при различных скоростях потока, выраженных в единицах мг N.I.H., а на фиг. 58 - график, изображающий испытания на гемолиз насоса при различных скоростях потока, выраженных в единицах BP-50.
[437] Было проведено несколько исследований для определения оптимальных расстояний для зазоров 540 и 542 между крыльчаткой и корпусом крыльчатки. Эти зазоры предпочтительно оптимизированы для ограничения разрушения эритроцитов (red blood cells, RBCs) из-за воздействия напряжения сдвига в результате гемолиза. Кроме того, желательно добиться эффекта гидродинамической опоры в верхнем зазоре для противодействия гидростатической силе давления, действующей на нижнюю поверхность ротора, и уменьшить усилия на верхней опоре. Таким образом, верхние и нижние зазоры корпуса ротора были выбраны таким образом, чтобы обеспечить минимальный гемолиз и максимальный эффект гидродинамической опоры для EBP, для применения которых требуется скорость, поток и статический напор 3800 об/мин, 538 мл/мин и 125 мм рт. ст. и в идеале диапазон рабочего потока 50-1250 мл/мин.
[438] В сильно упрощенных моделях повреждения крови гемолиз является степенной функцией напряжения сдвига и времени воздействия. RBC могут выдерживать высокие напряжения сдвига (> 100 Па) в течение кратковременного воздействия (<1 с). В ламинарном потоке между вращающейся пластиной и параллельной неподвижной пластиной напряжение сдвига увеличивается прямо пропорционально скорости поверхности и обратно пропорционально ширине зазора. Небольшие зазоры, порядка диаметра RBC (10 мкм) не допускают эритроциты и ограничивают гемолиз. Большие зазоры, порядка 1 мм, связаны с рециркуляцией, которая может продлить время воздействия и способствовать гемолизу. С помощью компьютерного моделирования динамики текучей среды EBP были проверены верхние зазоры 50, 75 мкм и 125 мкм, а для оценки гемолиза был проверен нижний зазор 250 мкм. На практике эти зазоры имеют производственные допуски, а способы производства разрабатывают на ситуационной основе, чтобы ограничить допуски для этих расстояний в зазорах как можно более низкими, практичными или экономичными.
[439] Для первого исследования, описанного ниже, EBP были созданы с использованием заданных верхних зазоров 125 ± 50 мкм корпуса ротора и заданных нижних зазоров 250 ± 50 мкм корпуса ротора. Обработанные компоненты имели допуски ± 100 мкм. Сообщалось о среднем от 3 измерений общего (т.е. верхнего+нижнего) зазора на собранном насосе. Конический корпус или поверхности ротора были притерты, чтобы достичь заданного общего зазора. Верхний зазор опоры был установлен путем герметизации верхней опоры.
[440] Испытания на гемолиз in vitro прототипов EBP с верхним зазором 125 мкм и нижним зазором 250 мкм показали, что показатели гемолиза в среднем составляют 14-130 мг N.I.H. (или мг плазмы, не содержащей гемоглобина, добавленной на 100 л перекачиваемой крови) в рабочем диапазоне 100-1000 мл/мин потоков насоса (показано на фиг. 57). Это выгодно отличается от параллельных испытаний одобренного FDA (Food and Drug Administration, Администрация по контролю за продуктами питания и лекарствами) центробежного перфузионного насоса модели BP-50 Bio-Pump® компании Medtronic в одинаковом диапазоне потоков, при этом EBP демонстрирует нормализованные показатели гемолиза 1,1-2,4 единиц BP-50 (показано на фиг. 58).
[441] Испытания на гемолиз in vitro прототипов EBP с верхним зазором 50 мкм демонстрировали показатели гемолиза в среднем 3,0-4,2 мг N.I.H. (или мг плазмы, не содержащей гемоглобина, добавленной на 100 л перекачиваемой крови) при работе со скоростью потока 500 мл/мин (показано на фиг. 55). Это выгодно отличается от параллельных испытаний одобренного FDA центробежного перфузионного насоса модели BP-50 Bio-Pump® компании Medtronic при одинаковой скорости потока, при этом EBP демонстрирует нормализованные показатели гемолиза 0,8-2,0 единиц BP-50 (показано на фиг. 56).
[442] Испытания на гемолиз in vitro прототипов EBP с верхним зазором 100 мкм демонстрировали показатели гемолиза в среднем 0,2 мг N.I.H. (или мг плазмы, не содержащей гемоглобина, добавленной на 100 л перекачиваемой крови) при работе со скоростью потока 500 мл/мин (показано на фиг. 55). Это выгодно отличается от параллельных испытаний одобренного FDA центробежного перфузионного насоса модели BP-50 Bio-Pump® компании Medtronic при одинаковой скорости потока, при этом EBP демонстрирует нормализованные показатели гемолиза менее 0,1 единиц BP-50 (показано на фиг. 56).
[443] Эффекты гидродинамической опоры возникают, когда пленка текучей среды между движущейся и неподвижной поверхностью сходится в направлении скольжения. Текучая среда втягивается в пленку и через нее движущейся поверхностью. Давление внутри пленки текучей среды пропорционально скорости поверхности, умноженной на вязкость жидкости и обратно пропорционально квадрату толщины пленки. Усилия гидродинамической опоры между поверхностями пропорциональны площади, на которую действует это давление.
[444] Верхние поверхности 7 лопастей крыльчатки EBP имеют общую площадь 96,1 мм2 (со ссылкой на фиг. 4G). В исследованиях нагрузки на опору in vitro прототипов EBP без опорных пластин двигателя демонстрируется разгрузка верхней опоры при 4000 об/мин для верхних зазоров 0-175 мкм (показано на фиг. 4H).
[445] На основании описанных выше анализов и испытаний, верхний и нижний зазоры корпуса ротора в настоящем варианте реализации EBP находятся в диапазоне 25-225 мкм и 150-350 мкм, соответственно, или предпочтительно в диапазоне 75-175 мкм и 200-300 мкм соответственно или номинально 100 мкм и 250 мкм соответственно.
[446] Артериовенозную фистулу (AVF) создают, когда между артерией и веной выполняют прямое хирургическое соединение. При попытке выполнения AVF для использования в качестве сосудистого доступа для обычного гемодиализа, пациенту обычно требуется периферическая вена диаметром более 2,5-3,0 мм. После создания «приточную» артерию и «выводную» вену, которые содержат AVF, необходимо расширять, а кровоток в выводной вене AVF необходимо увеличить, для того чтобы AVF созрела и стала пригодной для гемодиализа. Согласно критериям, установленным Национальным почечным фондом (KDOQI) для того, чтобы AVF считалась созревшей, выводная вена должна расширяться как минимум до 6 мм, а кровоток выводной вены должен увеличиться по меньшей мере до 600 мл/мин.
[447] С использованием имитационного контура AVF, показанного на фиг. 59, был проведен стендовый эксперимент для оценки влияния диаметра выводной вены AVF на WSS выводной вены, когда начальный диаметр приточной артерии составлял 4 мм (ID). Для создания среднего артериального давления (mean arterial pressure, MAP)=120 мм рт. ст. в имитационном контуре кровообращения использовалось имплантируемое пневматическое устройство поддержки левого желудочка HeartMate 2000 IP LVAS (Implantable Pneumatic Left Ventricular Assist Device). Для имитации приточной лучевой артерии AVF использовали примерно 50 см трубки Tygon с внутренним диаметром 4 мм. Для имитации выводной головной вены AVF с внутренними диаметрами 2, 3, 4, 5 или 6 мм использовали примерно 80 см трубки Tygon. Для определения скоростей кровотока в отводной вене AVF использовали ультразвуковой датчик потока Transonic (TS410/ME3PXL). На впуске насоса, выпуске насоса и анастомозе вены и канала размещали датчики давления NETech (Digimano 200-2000IN). Для имитации крови использовали 35% раствор глицерина в водопроводной воде при температуре 22 °С. Как показано на фиг. 60, уровни WSS выводной вены AVF различаются в широких пределах в зависимости от диаметров выводной вены AVF, демонстрируя, что артериальное кровяное давление и диаметр сосуда определяют уровни WSS выводной вены AVF, то есть, факторы, которые невозможно эффективно регулировать во время создания и созревания AVF.
[448] Используя имитационный контур AVF, показанный на фиг. 53, был проведен стендовый эксперимент для оценки влияния скорости работы насоса системы AFE и диаметра выводной вены системы AFE на WSS выводной вены системы AFE. Испытательный контур содержит приточные и выводные каналы 5302 и 5304, имитационную выводную вену 5306 и имитационные коллатеральные сосуды 5308 и 5310. Для имитации венозной системы использовали резервуар емкостью 1 л. Для имитации приточных и выводных каналов системы AFE использовали примерно 45 см трубки Tygon внутренним диаметром 4 мм. Для имитации выводной вены с внутренними диаметрами 2, 3, 4, 5 или 6 мм использовали примерно 80 см трубки Tygon. Для определения скоростей кровотока в отводной вене AVF использовали ультразвуковой датчик потока Transonic (TS410/ME3PXL). На впуске насоса, выпуске насоса и анастомозе вены и канала размещали датчики давления NETech (Digimano 200-2000IN). Для имитации крови использовали 35% раствор глицерина в водопроводной воде при температуре 22 °С. Как показано на фиг. 61, последовательная доза WSS 4 Па может применяться на отводной вене системы AFE при диаметрах вены до 5 мм путем изменения скорости насоса.
[449] На первом этапе изучения применимости in vivo на овцах варианты реализации системы AFE были имплантированы трем овцам массой 50-60 кг. Была установлена система AFE, в которой приточный канал был введен в левую наружную яремную вену, и узел дальнего наконечника канала был продвинут в верхнюю полую вену, а ближний конец приточного канала был соединен с насосом с помощью фитинга с кольцевыми зубцами и сжимающего кольца, устанавливая сообщение по текучей среде между перфузионным насосом и верхней полой веной. Приточный канал дополнительно содержал:
• дальний наконечник канала из нержавеющей стали с конфигурацией «утиный клюв» и фитингом с кольцевыми зубцами на ближнем конце;
• защитный каркас дальнего наконечника канала с ближним кольцом, дальним кольцом и четырьмя ребрами;
• ближний сегмент канала с проволочной несущей конструкцией из нитинола в виде оплетки, расположенной между двумя слоями полимера Carbothane® PC-3575A с твердостью по Шору 70A с одним зажимом; и
• боковой канал с проволочной несущей конструкцией из нитинола в виде оплетки, двумя зажимами и жесткой крышкой; при этом:
• дальний конец ближнего сегмента канала был соединен с ближним концом дальнего наконечника канала посредством фитинга с кольцевыми зубцами и клея;
• ближнее кольцо каркасной конструкции было соединено с дальним концом ближнего сегмента канала с помощью клея; и
• контактирующие с кровью поверхности ближнего сегмента канала, дальнего наконечника канала и каркасной конструкции были покрыты гепариновым покрытием.
[450] Выводной канал был соединен по текучей среде с головной веной левого предплечья посредством анастомоза, а ближний конец выводного канала был соединен с насосом посредством фитинга с кольцевыми зубцами и сжимающего кольца, устанавливая сообщение по текучей среде между перфузионным насосом и головной веной левого предплечья. Приточный канал дополнительно содержал:
• ближний сегмент канала с проволочной несущей конструкцией из нитинола в виде оплетки, расположенной между двумя слоями полимера Carbothane® PC-3575A с твердостью по Шору 70A с одним зажимом; и
• боковой канал с проволочной несущей конструкцией из нитинола в виде оплетки, тремя зажимами и жесткой крышкой;
• дальний сегмент канала, выполненный из ePTFE, связанный с ближним сегментом канала, путем пакетирования; причем:
• контактирующие с кровью поверхности ближнего сегмента канала и дальнего наконечника канала были покрыты гепариновым покрытием.
[451] Система AFE применялась на головной вене левого предплечья в течение 6-11 дней с дозой WSS примерно 4 Па. Во время исследования поток системы AFE увеличивался примерно с 300 мл/мин в начальный (0) день примерно до 900 мл/мин в конце периода лечения, а выводной сегмент головной вены левого предплечья расширился примерно от 3,5-5,5 мм примерно до 8-13 мм, как показано на фиг. 84. Затем каждому животному вводили артериовенозную фистулу (AVF) с использованием прошедшей лечение головной вены левого предплечья и смежного объединенного ствола радиальной и медианной артерий, как показано на фиг. 90. Для сопоставления результатов с использованием системы AFE по сравнению с существующими стандартами лечения AVF, AVF, использующие одни и те же сосуды, также были созданы билатерально на двух контрольных животных с использованием не прошедших лечение головных вен предплечья, как показано на фиг. 88 и 89. Затем все семь AVF были оставлены для созревания в течение 6 недель с еженедельной оценкой с помощью сосудистого ультразвукового обследования и катетеризационной ангиографии. Как показано на фиг. 108, затем была вычислена скорость увеличения кровотока в головной вене левого предплечья с помощью ультразвука в течение периода созревания и показано, что она составляет 22 мл/мин/день для AVF, выполненных с использованием системы AFE, прошедших кардиоваскулярное (cardiovascular, CV) лечение, и 11 мл/мин/день для контрольных AVF, что указывает на улучшение созревания AVF для AVF, выполненных с использованием вен, предварительно прошедших лечение с помощью системы AFE. Результаты этих экспериментальных исследований подтвердили эффективность системы AFE для расширения вен на второй модели на животном и достижение высоких скоростей AVF через 6 недель созревания по сравнению с контрольными AVF, выполненными на не прошедших лечение венах.
[452] На втором этапе изучения применимости in vivo на овцах варианты реализации системы AFE были имплантированы двум овцам массой 50-60 кг. Была установлена система AFE, в которой приточный канал был введен в левую наружную яремную вену, и узел дальнего наконечника канала был продвинут в верхнюю полую вену, а ближний конец приточного канала был соединен с насосом с помощью фитинга с кольцевыми зубцами и сжимающего кольца, устанавливая сообщение по текучей среде между перфузионным насосом и верхней полой веной. Приточный канал дополнительно содержал:
• дальний наконечник канала из нержавеющей стали с конфигурацией «утиный клюв» и фитингом с кольцевыми зубцами на ближнем конце;
• защитный каркас дальнего наконечника канала с ближним кольцом, дальним кольцом и четырьмя ребрами;
• ближний сегмент канала с проволочной несущей конструкцией из нитинола в виде оплетки, расположенной между двумя слоями полимера Carbothane® PC-3575A с твердостью по Шору 70A с одним зажимом; и
• боковой канал с проволочной несущей конструкцией из нитинола в виде оплетки, двумя зажимами и жесткой крышкой; при этом:
• дальний конец ближнего сегмента канала был соединен с ближним концом дальнего наконечника канала посредством фитинга с кольцевыми зубцами и клея;
• ближнее кольцо каркасной конструкции было соединено с дальним концом ближнего сегмента канала с помощью клея; и
• контактирующие с кровью поверхности ближнего сегмента канала, дальнего наконечника канала и каркасной конструкции были покрыты гепариновым покрытием.
[453] Отводной канал был соединен по текучей среде с головной веной левого предплечья посредством введения дальнего сегмента из нержавеющей стали, разветвленного дальнего наконечника канала в просвет вены. Ближний конец выпускного канала затем соединяли с насосом посредством фитинга с кольцевыми зубцами и сжимающим кольцом, устанавливая сообщение по текучей среде между перфузионным насосом и головной веной левого предплечья. Приточный канал дополнительно содержал:
• ближний сегмент канала с проволочной несущей конструкцией из нитинола в виде оплетки, расположенной между двумя слоями полимера Carbothane® PC-3575A с твердостью по Шору 70A с одним зажимом; и
• боковой канал с проволочной несущей конструкцией из нитинола в виде оплетки, тремя зажимами и жесткой крышкой;
• дальний сегмент канала, выполненный из ePTFE, связанный с ближним сегментом канала путем пакетирования;
• дальний сегмент канала, при этом:
• контактирующие с кровью поверхности ближнего сегмента канала, дальнего сегмента канала и разветвленного дальнего наконечника канала были покрыты гепариновым покрытием.
[454] Система AFE применялась на головной вене левого предплечья в течение 10-11 дней с дозой WSS примерно 4 Па. Во время исследования поток системы AFE увеличивался примерно с 300 мл/мин в начальный (0) день примерно до 900 мл/мин в конце периода лечения, а выводной сегмент головной вены левого предплечья расширился примерно от 3,5-5,5 мм примерно до 8-11 мм, как показано на фиг. 106. Затем каждому животному вводили артериовенозную фистулу (AVF) с использованием прошедшей лечение головной вены левого предплечья и смежного объединенного ствола радиальной и медианной артерий. Затем обе AVF были оставлены для созревания в течение 6 недель с еженедельной оценкой с помощью сосудистого ультразвукового обследования и катетеризационной ангиографии.
Хотя изобретение было описано в связи с примерами аспектов и вариантов реализации изобретения, следует понимать, что его различные модификации будут очевидными для специалистов в данной области после прочтения описания. Поэтому должно быть понятно, что изобретение должно охватывать такие модификации, которые подпадают под объем действия прилагаемой формулы изобретения.
Реферат
Группа изобретений относится к медицинской технике. Канал для транспортирования крови из артерии, вены или камеры сердца в перфузионный насос содержит гибкий ближний сегмент канала, содержащий трубчатый корпус ближнего канала, имеющий ближний конец ближнего канала и дальний конец ближнего канала. Трубчатый корпус ближнего канала образует просвет ближнего канала между ближним концом ближнего канала и дальним концом ближнего канала. Дальний наконечник канала содержит трубчатый корпус наконечника, имеющий ближний конец наконечника и дальний конец наконечника. Трубчатый корпус наконечника образует просвет наконечника между ближним концом наконечника и дальним концом наконечника. Ближний конец наконечника дальнего наконечника канала соединен с дальним концом ближнего канала ближнего сегмента канала. Конструкция защитного каркаса дальнего наконечника канала содержит ближнее кольцо, соединенное с дальним концом ближнего канала ближнего сегмента канала, с дальним наконечником канала или с обоими из дальнего конца ближнего канала и дальним наконечником канала, и одно или более удлиненных ребер, проходящих дистально от ближнего кольца до зоны, дальней относительно торцевой поверхности дальнего наконечника канала. Раскрыты альтернативные варианты выполнения канала для транспортирования крови и перфузионная система, в которой использованы упомянутые каналы. Технический результат сводится к обеспечению расширения сосудов и снижению риска тромбоэмболии. 4 н. и 38 з.п. ф-лы, 108 ил.

Комментарии