Макромономеры, содержащие полиизобутеновые группы, и их гомо- и сополимеры - RU2745788C2
Код документа: RU2745788C2
Описание
Настоящее изобретение описывает новые макромономеры, содержащие полиизобутеновые группы, и их гомо- или сополимеры.
Содержащие полиизобутеновые группы макромономеры на основе, например, ангидрида полиизобутенил-янтарной кислоты (PIBSA) уже известны, например, из международной заявки WO 04/092227. Здесь, однако, при получении ангидридов полиизобутенилянтарной кислоты вместе с янтарным ангидридом могут присутствовать структуры с множественными функциональностями, которые в последующей реакции с производными (мет)акриловой кислоты приводят к мономерам, имеющим функциональность (мет)акриловой кислоты > 1, и, таким образом, ведут к содержанию в реакционной смеси сшивающих макромономерных структур. Кроме того, взаимодействие PIBSA со спиртами приводит к образованию свободной кислотной группы, которая дополнительно снижает гидрофобность макромономеров и может приводить к последующим побочным реакциям.
Полиизобутены, которые имеют концевые функциональные ОН-группы, являются ценными промежуточными соединениями при получении монофункциональных макромеров или соответственно макромономеров. Заслуга Кеннеди и Ивана состоит в том, что они первыми опубликовали синтетический путь к таким соединениям посредством реакции присоединения борана (Ivan, Kennedy, Chang; J. Polym. Sci. Polym. Chem. Ed. 18, 3177 (1980)). Использование боранов для получения технических полимеров является слишком трудоемким, см. также международную заявку WO 14/090672. Кроме того, использование полиизобутениловых спиртов, полученных с помощью гидроформилирования, не подходит для использования в производстве макромономеров из-за длительного времени реакции при высоких температурах в присутствии родиевых или кобальтовых катализаторов, а также сравнительно низкой степени функционализации спиртовыми функциональными группами, см. например европейскую заявку EP 277345.
Также макромономеры получают посредством преобразования полиизобутена, например, в полиизобутенамины (коммерчески доступные как Kerocom® PIBA фирмы BASF), а затем далее в (мет)акриламиды. Однако они содержат высококипящие растворители (до 35%) и поэтому непригодны для некоторых исключающих растворители применений.
Использование макромономерных структур на основе трех указанных здесь предшественников уже описано в европейской заявке ЕР 1899393 и еще раз иллюстрирует низкую степень функционализации (<80%) полученных из них макромономеров. Из публикации K. Maenz, D. Stadermann, Angewandte Makromolekulare Chemie, 242 (1996) 183-197 известно об этерификации метакрилоилхлоридом содержащих полиизобутеновые группы фенолов. Из публикации E.L. Malins, C. Waterson, CR. Becer, J. Polym. Sc, Part A: Polymer Chemistry 2016, 54, 634-643 известно об этерификации акрилоилхлоридом содержащих полиизобутеновые группы фенолов и об их гомо- или сополимеризации. Из международной заявки WO 14/90672 известно об этоксилировании содержащих полиизобутеновые группы фенолов, или их этерификации (мет)акриловой кислотой. Полученные продукты могут находить применение при получении клеящих веществ, сырья для клеящих веществ, топливных и смазочных добавок, в качестве эластомеров или в качестве основного компонента герметиков и уплотнительных масс. Недостатком полученных таким образом (мет)акрилатов является то, что для их получения требуется взаимодействие свободного фенола с ангидридом или хлорангидридом (мет)акриловой кислоты. Взаимодействие с хлорангидридом акриловой кислоты также подробно описано в одном из примеров международной заявки WO 14/90672. Раскрытая в общем виде в описании к международной заявке WO 14/90672 этерификация (мет)акриловой кислотой или переэтерификация сложными эфирами (мет)акриловой кислоты, приводит к продуктам с исключительно плохими выходами. Кроме того, получаемые таким образом (мет)акрилаты в полимеризационных условиях нестабильны в присутствии кислот, например, содержащих кислотные группы сомономеров, и приводят к ингибированию полимеризации в результате высвобождения фенола и к сильно окрашенным смесям продуктов. Из европейской заявки EP 2762506 A1 известны полиизобутенильные полимеры, имеющие (мет)акрилоильные концевые группы. Заявленная цель европейской заявки ЕР 2762506 А1 состоит в получении сшиваемых макромолекул, предпочтительно с функциональностью 2 или 3. Макромолекулы, подробно раскрытые в примерах, имеют функциональность 1,9 или выше. Это приводит к сшиванию в условиях полимеризации.
Кроме того, раскрытые там макромолекулы получают посредством катионной полимеризации соответствующим образом функционализированных стартовых молекул, и полученные таким образом полифункциональные полиизобутеновые полимеры, несущие атом хлора на каждом конце цепи, посредством алкилирования Фриделя-Крафтса соединяют с (мет)акрилоилзамещенным фенолом.
Данный способ получения обуславливает, что в продуктах из-за технологической необходимости присутствует заметное содержание хлора, которое в примерах указано как 79-85 ч.н.млн.
Из европейской заявки ЕР 832960 А1 известно алкоксилирование полиизобутенилзамещенных фенолов карбонатами или в качестве альтернативы алкиленоксидами.
В качестве продуктов описаны только моноалкоксилированные продукты, не приводится никаких данные о мультиалкоксилированных продуктах, и в частности, о распределение мультиалкоксилированных продуктов согласно данному способу. Задача настоящего изобретения состояла в предоставлении отдельных монофункциональных соединений, с помощью которых в полимеры может быть введена большая доля структурных звеньев фенолов, содержащих полиизобутеновые группы. Данные соединения должны быть более легкодоступными и стабильными в условиях полимеризации, чем указанные соединения предшествующего уровня техники, и иметь более низкое содержание галогена, чем раскрыто в примерах европейской заявки EP 2762506 A1.
Указанная задача была решена посредством соединений (А) формулы (I)
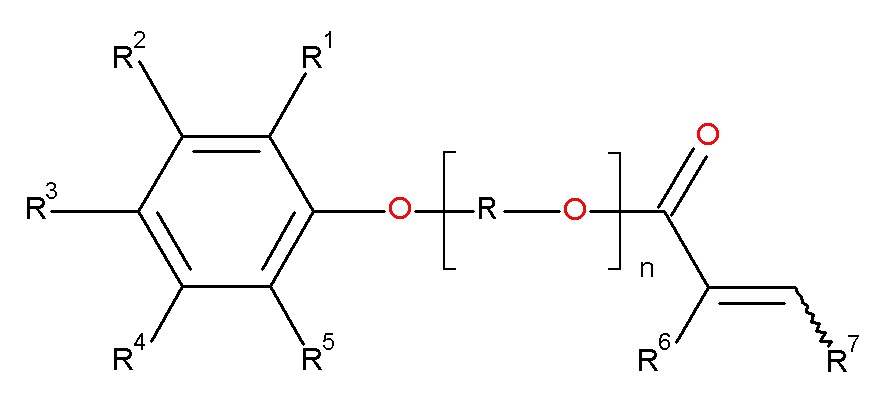
в которой
R1 - R5 в каждом случае независимо друг от друга выбраны из группы, состоящей из водорода, алкила с 1-20 атомами углерода, алкилокси с 1-20 атомами углерода и полиизобутила с 8-3500 атомами углерода и полиизобутенила с 8-3500 атомами углерода,
R означает алкиленовую группу, имеющую от 2 до 10, предпочтительно от 2 до 6 и особенно предпочтительно от 2 до 4 атомов углерода,
R6 означает водород или метил,
R7 означает водород, метил или COOR8 ,
R8 означает водород или алкил с 1-20 атомами углерода,
n означает целое положительное число от 1 до 50,
при условии,
что по меньшей мере один из остатков R1- R5 представляет собой полиизобутил с 8-3500 атомами углерода или полиизобутенил с 8-3500 атомами углерода.
Еще одним объектом изобретения являются полимеры, содержащие в заполимеризованной форме по меньшей мере одно соединение (А) формулы (I)

в которой
R1 - R5 в каждом случае независимо друг от друга выбраны из группы, состоящей из водорода, алкила с 1-20 атомами углерода, алкилокси с 1-20 атомами углерода и полиизобутила с 8-3500 атомами углерода и полиизобутенила с 8-3500 атомами углерода,
R означает алкиленовую группу, имеющую от 2 до 10, предпочтительно от 2 до 6 и особенно предпочтительно от 2 до 4 атомов углерода,
R6 означает водород или метил,
R7 означает водород, метил или COOR8 ,
R8 означает водород или алкил с 1-20 атомами углерода,
n означает целое положительное число от 1 до 50,
при условии,
что по меньшей мере один из остатков R1- R5 представляет собой полиизобутил с 8-3500 атомами углерода или полиизобутенил с 8-3500 атомами углерода
и при необходимости по меньшей мере один мономер (В), выбранный из группы, состоящей из
(B1) (мет)акрилатов, отличных от (A),
(B2) производных фумаровой и малеиновой кислот, отличных от (A),
(B3) простых алкилвиниловых эфиров,
(B4) стирола и α-метилстирола,
(B5) акрилонитрила,
(B6) винилалканоатов и
(B7) (мет)акриламидов.
В которых
алкил с 1-20 атомами углерода означает, например, метил, этил, изопропил, н-пропил, н-бутил, изобутил, втор-бутил и трет-бутил, н-пентил, 2-пентил, 3-пентил, 2-метилбутил, 3-метилбутил, 3-метилбут-2-ил, 2-метилбут-2-ил, 2,2-диметилпропил, н-гексил, 2-гексил, 3-гексил, 2-метилпентил, 2-метилпент-3-ил, 2-метилпент-2-ил, 2-метилпент-4-ил, 3-метилпент-2-ил, 3-метилпент-3-ил, 3-метилпентил, 2,2-диметилбутил, 2,2-диметилбут-3-ил, 2,3-диметилбут-2-ил, 2,3-диметилбутил, 2-этилгексил, н-октил, 2-пропилгептил, н-децил, н-додецил, н-тетрадецил, н-гексадецил, н-октадецил и эйкозил, предпочтительно метил, этил, н-бутил, изопропил, трет-бутил, 2-этилгексил и 2-пропилгептил и особо предпочтительно метил, этил, н-бутил, изопропил или трет-бутил, наиболее предпочтительно метил, этил или н-бутил, в частности метил или этил, особенно метил.
алкилокси с 1-20 атомами углерода означает, например кислородные остатки, замещенные алкильными группами с 1-20 атомами углерода, предпочтительно метокси, этокси, изопропокси, н-пропилокси, н-бутилокси, изобутокси, втор-бутилокси и трет-бутилокси, особо предпочтительно метокси, этокси, н-бутилокси, изопропилокси и трет-бутилокси и наиболее предпочтительно метокси.
Алкиленовая группа с 2-10 атомами углерода представляет собой 1,2-этилен, 1,2-пропилен, 1,3-пропилен, 1,2-бутилен, 1,3-бутилен, 1,4-бутилен, 1-фенил-1,2-этилен и 2-фенил-1,2-этилен, предпочтительно 1,2-этилен, 1,2-пропилен и 1,2-бутилен.
Полиизобутил с 8-3500 атомами углерода и полиизобутенил с 8-3500 атомами углерода означают остатки, получаемые путем присоединения к ароматическим соединениям полиизобутена, содержащего от 8 до 3500 атомов углерода.
При этом полиизобутильные остатки с 8-3500 атомами углерода и полиизобутенильные остатки с 8-3500 атомами углерода могут быть основаны в принципе на любом распространенном и коммерчески доступном полиизобутене, который подходящим образом вводят в синтез соединений формулы (I). Такой полиизобутен предпочтительно имеет среднечисловую молекулярную массу Mn по меньшей мере 200. Предпочтение отдается полиизобутенам, имеющим среднечисловую молекулярную массу Mn в диапазоне от по меньшей мере 500, особо предпочтительно от по меньшей мере 700 и наиболее предпочтительно от по меньшей мере 900 г/моль.
Можно использовать полиизобутены, имеющие среднечисловую молекулярную массу Mn в диапазоне до 50000, предпочтительно до 45000, особо предпочтительно до 40000 и наиболее предпочтительно до 35000 г/моль.
В предпочтительном варианте осуществления среднечисловая молекулярная масса Mn полиизобутенов может составлять до 30000, особо предпочтительно, до 20000, и, наиболее предпочтительно, до 10000 г/моль.
В еще одном предпочтительном варианте осуществления среднечисловая молекулярная масса Mn полиизобутенов может составлять от 700 до 2500 и особо предпочтительно от 900 до 1100 г/моль. С точки зрения настоящего изобретения термин «полиизобутен» также включает олигомерные изобутены, такие как димерные, тримерные, тетрамерные, пентамерные, гексамерные и гептамерные изобутены.
Предпочтительно полиизобутильные остатки с 8-3500 атомами углерода и полиизобутенильные остатки с 8-3500 атомами углерода, включенные в соединения формулы (I), получены из так называемого «высокореактивного» полиизобутена. «Высокореактивные» полиизобутены отличаются от других полиизобутенов содержанием концевых двойных связей. Таким образом, высокореактивные полиизобутены содержат по меньшей мере 50 мол.% концевых двойных связей, в пересчете на общее количество полиизобутеновых макромолекул. Особо предпочтительными являются полиизобутены, имеющие по меньшей мере 60 мол.%, и в частности по меньшей мере 80 мол.% концевых двойных связей, в пересчете на общее количество полиизобутеновых макромолекул. В случае концевых двойных связей речь может идти как о винильных двойных связях [-CH=C(CH3)2] (β-олефин), так и о винилиденовых двойных связях [-CH-C(=CH2)-CH3] (α-олефин), предпочтительно об α-олефинах. Кроме того, в основном гомополимерные полиизобутенильные остатки имеют однородные полимерные каркасы. В рамках настоящего изобретения под этим понимают такие полиизобутеновые системы, которые содержат по меньшей мере 85 мас.%, предпочтительно по меньшей мере 90 мас.%, и особо предпочтительно по меньшей мере 95 мас.% изобутеновых повторяющихся структурных единиц [-CH2C(CH3)2-].
В настоящем описании проводится различие между полиизобутильными и полиизобутенильными остатками, причем полиизобутильные остатки в основном не содержат двойных связей, а полиизобутенильные остатки как правило имеют по меньшей мере одну двойную связь на остаток.
Катализируемое кислотой Бренстедта или Льюиса присоединение полиизобутена к ароматическим соединениям обычно происходит в результате реакции по двойной связи и, следовательно, дает в основном несодержащий двойных связей полиизобутил. При этом термин «в основном несодержащий двойных связей» означает, что не более 25% всех остатков имеют двойную связь, предпочтительно не более 15%, особо предпочтительно не более 10% и наиболее предпочтительно не более 5%.
Полиизобутильные остатки являются предпочтительными в сравнении с полиизобутеновыми остатками.
Другой предпочтительный признак полиизобутенов, которые могут лежать в основе соединений формулы (I) согласно изобретению, состоит в том, что они содержат в качестве концевой группы по меньшей мере 15 мас.%, в частности по меньшей мере 50 мас.%, прежде всего по меньшей мере 80 мас.%. трет-бутильной группы [-СН2С(СН3)3].
Кроме того, полиизобутены, которые предпочтительно используют в качестве основы для соединений формулы (I) согласно изобретению, предпочтительно имеют индекс полидисперсности (PDI) от 1,05 до 10, предпочтительно от 1,05 до 3,0, в частности от 1,05 до 2,0. Под полидисперсностью понимают отношение средневесовой молекулярной массы Mw и среднечисловой молекулярной массы Mn (PDI = Mw/Mn).
В рамках настоящего изобретения под "полиизобутенами, которые предпочтительно используют в качестве основы для соединений формулы (I) согласно изобретению," также понимают все получаемые катионной полимеризацией полимеризаты, которые предпочтительно содержат по меньшей мере 60 мас.% изобутена, особо предпочтительно по меньшей мере 80 мас.%, прежде всего по меньшей мере 90 мас.%, и в частности по меньшей мере 95 мас.% изобутена в заполимеризованной форме. Кроме того, полиизобутены могут содержать в заполимеризованной форме дополнительные бутеновые изомеры, такие как 1- или 2-бутен, а также различные олефинненасыщенные мономеры, способные к сополимеризации с изобутеном в условиях катионной полимеризации. Подходящими изобутеновыми исходными материалами для получения полиизобутенов, которые могут быть использованы в качестве основы для соединений формулы (I) согласно изобретению, являются, соответственно, как сам изобутен, так и изобутен-содержащие потоки С4-углеводородов, например С4-рафинаты, С4-фракции из процесса дегидрирования изобутена, С4-фракции из процессов парового крекинга, FCC-крекинга (FCC: Fluid Catalyzed Cracking (каталитический крекинг текучих сред)), при условии, что они в основном избавлены от содержавшегося в них 1,3-бутадиена. Особо подходящие потоки С4-углеводородов обычно содержат менее 500 ч.н.млн, предпочтительно менее 200 ч.н.млн бутадиена. При использовании С4-фракций в качестве исходных материалов отличные от изобутена углеводороды играют роль инертного растворителя.
В качестве мономеров, способных к сополимеризации с изобутеном, пригодными являются винилароматические соединения, такие как стирол и α-метилстирол, алкилстиролы с 1-4 атомами углерода в алкиле, такие как 2-, 3- и 4-метилстирол, а также 4-трет-бутилстирол, изоолефины с 5-10 атомами углерода, такие как 2-метилбутен-1, 2-метилпентен-1, 2-метилгексен-1, 2-этилпентен-1, 2-этилгексен-1 и 2-пропилгептен-1.
Типичными полиизобутенами, которые служат основой для соединений формулы (I) согласно изобретению, являются, например, марки Glissopal® фирмы BASF SE, Людвигсхафен, например Glissopal 1000, Glissopal 1300 и Glissopal 2300, а также марки Oppanol® фирмы BASF SE, например, Oppanol® B10, B12 и B15.
В формуле (I) остатки имеют следующие значения:
R1 - R5 в каждом случае независимо друг от друга выбраны из группы, состоящей из водорода, алкила с 1-20 атомами углерода, алкилокси с 1-20 атомами углерода и полиизобутила с 8-3500 атомами углерода и полиизобутенила с 8-3500 атомами углерода,
Те из остатков R1-R5, которые представляют собой полиизобутильный или полиизобутенильный, предпочтительно полиизобутильный остаток, имеют по меньшей мере 8, предпочтительно по меньшей мере 12, особо предпочтительно по меньшей мере 16, наиболее предпочтительно по меньшей мере 20, и в частности по меньшей мере 35 атомов углерода.
В предпочтительном варианте осуществления они имеют по меньшей мере 50 и особо предпочтительно по меньшей мере 60 атомов углерода. Как правило, полиизобутильные или полиизобутенильные остатки имеют до 3500 атомов углерода, предпочтительно до 3200, особо предпочтительно до 2200, наиболее предпочтительно до 1500, и в частности до 750.
В предпочтительном варианте осуществления они имеют до 200, особо предпочтительно до 100 и в частности до 80 атомов углерода.
При этом актуально условие, что по меньшей мере один из R1-R5 представляет собой один из указанных полиизобутилов или полиизобутенилов, предпочтительно один, два или три, особо предпочтительно один или два и наиболее предпочтительно только один. Те из остатков R1-R5, которые не являются одним из указанных полиизобутильных или полиизобутенильных остатков, предпочтительно выбраны из группы, состоящей из водорода, метила, изопропила, трет-бутила, метокси, трет-бутилокси, особо предпочтительно, выбраны из группы, состоящей из водорода, метила, трет-бутила, и наиболее предпочтительно в их случае речь идет о водороде.
В предпочтительном варианте осуществления по меньшей мере один из R1, R3 и R5 представляет собой полиизобутильный или полиизобутенильный остаток, а другие остатки не являются таковыми, более предпочтительно R3 представляет собой полиизобутильный или полиизобутенильный радикал, а другие остатки не являются таковыми.
В случае R речь идет об алкиленовой группе, имеющей от 2 до 10, предпочтительно от 2 до 6 и особо предпочтительно от 2 до 4 атомов углерода, предпочтительно о 1,2-этилене, 1,2-пропилене, 1,3-пропилене, 1,2-бутилене, 1,4-бутилене, 1-фенил-1,2-этилене или 2-фенил-1,2-этилене, особо предпочтительно о 1,2-этилене, 1,2-пропилене или 1,2-бутилене и наиболее предпочтительно о 1,2-этилене.
В случае числа n речь идет о целом положительном числе от 1 до 50, предпочтительно от 1 до 30, особо предпочтительно от 1 до 20, наиболее предпочтительно от 1 до 10, в частности от 1 до 5 и конкретно о 1.
R6 представляет собой водород или метил, предпочтительно метил.
R7 представляет собой водород, метил или COOR8, предпочтительно водород или COOR8 и особо предпочтительно водород.
R8 представляет собой водород или алкил с 1-20 атомами углерода, предпочтительно водород, метил, этил, н-бутил или 2-этилгексил, особо предпочтительно водород или метил и наиболее предпочтительно водород.
Следует отметить, что в случае соединений формулы (I) речь идет о реакционных смесях, имеющих распределение по составу продуктов в зависимости от условий реакции. Таким образом, длина цепи полиизобутильного или полиизобутенильного остатка подвергается распределению вокруг статистического среднего значения, как и замещенный образец с полиизобутильныи или полиизобутенильными остатками в ароматическом кольце, и при необходимости длина цепи -[-RO-]n-, которая также может иметь распределение вокруг статистического среднего значения n. Таким образом, значение n для каждого отдельного соединения формулы (I) предполагает положительные целые числа, а также может принимать нецелые значения для реакционной смеси в среднем статистическом значении. В предпочтительном варианте осуществления реакционная смесь имеет среднюю функциональность по α,β-ненасыщенными карбонильным функциональным группам, предпочтительно (мет)акрилатным группам, не более 1,2, особо предпочтительно не более 1,1, наиболее предпочтительно не более 1,05.
Средняя функциональность как правило составляет по меньшей мере 0,8, предпочтительно по меньшей мере 0,9 и наиболее предпочтительно по меньшей мере 0,95.
Степень функционализации можно определить с помощью количественной 1H-ЯМР-спектроскопии. Для этого интегрируют сигналы протонов на ароматическом соединении, которые обычно легко идентифицируются и распознаются, а также не перекрываются с другими сигналами, и сигналы протонов способной к полимеризации двойной связи, и определяют их соотношение друг с другом.
Получение соединений (А) может быть осуществлено, например, посредством взаимодействия свободных фенолов формулы

с алкиленоксидами или алкиленкарбонатами формулы

с последующим декарбоксилированием и дальнейшей этерификацией (мет)акриловой кислотой, кротоновой кислотой, фумаровой кислотой, малеиновой кислотой или ангидридом малеиновой кислоты или переэтерификацией с помощью сложных эфиров (мет)акриловой кислоты, сложных эфиров кротоновой кислоты, сложных эфиров фумаровой кислоты или сложных эфиров малеиновой кислоты.
Получение свободных фенолов известно из цитированного в начале уровня техники, например, из международной заявки WO 02/059237 или WO 14/90672, и из цитируемой там литературы.
Согласно европейской заявке EP 2762506 A1 катионную полимеризацию осуществляют, исходя из хлорированных стартовых молекул, что приводит к образованию несущих на каждом конце цепочки атом хлора полиизобутеновых полимеров, которые соединяют с фенолом, в предпочтительном варианте осуществления настоящего изобретения содержащий двойную связь полиизобутен в присутствии кислоты Льюиса присоединяют к фенолу посредством алкилирования по Фриделю-Крафту. Таким образом, соединения согласно EP 2762506 A1 имеют технологически обусловленное существенно более высокое содержание галогена, чем таковые из предпочтительной формы осуществления реакции содержащего двойную связь полиизобутена с фенолом в присутствии кислоты Льюиса.
Таким образом, предпочтительно получают реакционные смеси с содержанием галогена, предпочтительно фтора, не более 70 масс. ч.н.млн, особо предпочтительно не более 50 масс. ч.н.млн, наиболее предпочтительно не более 40 масс. ч.н.млн, в частности не более 30 масс. ч.н.млн и конкретно не более 20 масс. ч.н.млн. Можно даже получить реакционные смеси с содержанием галогена, предпочтительно фтора, не более 10 масс. ч.н.млн или даже не более 5 масс. ч.н.млн.
Получение алкоксилированных продуктов как правило осуществляют посредством взаимодействия свободных фенолов с соответствующим эпоксидом с желаемой стехиометрией в присутствии катализатора, например гидроксида-, оксида-, карбоната- или гидрокарбоната щелочного или щелочноземельного металла, предпочтительно гидроксида щелочного металла, особенно предпочтительно гидроксида калия. Возможные варианты реализации можно найти в Houben-Weyl, Methoden der Organischen Chemie, 4. Издание, 1979, Thieme Verlag Stuttgart, под ред. Heinz Kropf, Том 6/1 a, Часть 1, страницы 373 - 385. Предпочтительный вариант осуществления может быть найден в международной заявке WO 02/059237 A2, в частности, со страницы 9, строка 12 до страницы 10, строка 21, который тем самым включен посредством ссылки в настоящее описание.
Получение алкоксилированных продуктов может быть также осуществлено с помощью мультиметаллических цианидных соединений, часто также называемых DMC-катализаторами, которые давно известны и многократно описаны в литературе, например, в американских патентах US 3,278,457 и US 5,783,113.
DMC-Катализаторы обычно получают взаимодействием соли металла с цианометаллатным соединением. Для улучшения свойств DMC-катализаторов обычно во время и/или после взаимодействия добавляют органические лиганды. Описание получения DMC-катализаторов можно найти, например, в патенте США US-A 3,278,457.
Типичные DMC-катализаторы имеют следующую общую формулу:
M1a[M2(CN)b]d∙fM1jXk∙h(H2O) eL∙zP
в которой
M1 означает ион металла, выбранный из группы, содержащей Zn2+, Fe2+, Fe3+, Co2+, Co3+, Ni2+, Mn2+, Sn2+, Sn4+, Pb2+, Al3+, Sr2+, Cr3+, Cd2+, Cu2+, La3+, Ce3+, Ce4+, Eu3+, Mg2+, Ti4+, Ag+, Rh2+, Ru2+, Ru3+, Pd2+,
M2 означает ион металла, выбранный из группы, содержащей Fe2+, Fe3+, Co2+, Co3+, Mn2+, Mn3+, Ni2+, Cr2+, Cr3+, Rh3+, Ru2+, Ir3+,
и М1 и М2 являются одинаковыми или различными,
Х представляет собой анион, выбранный из группы, включающей галогенид, гидроксид, сульфат, гидросульфат, карбонат, гидрокарбонат, цианид, тиоцианат, изоцианат, цианат, карбоксилат, оксалат, нитрат или нитрит (NO2-) или смесь двух или более из вышеуказанных анионов или смесь одного или нескольких из вышеуказанных анионов с одним из незаряженных химических соединений, выбранных из CO, H2O и NO,
Y представляет собой отличный от X анион, выбранный из группы, включающей галогенид, сульфат, гидросульфат, дисульфат, сульфит, сульфонат (=RSO3- с R = алкил с 1-20 атомами углерода, арил с 6-12 атомами углерода, алкиларил с 1-20 атомами углерода), карбонат, гидрокарбонат, цианид, тиоцианат, изоцианат, изотиоцианат, цианат, карбоксилат, оксалат, нитрат, нитрит, фосфат, гидрофосфат, дигидрофосфат, дифосфат, борат, тетраборат, перхлорат, тетрафторборат, гексафторфосфат, тетрафенилборат,
L представляет собой смешивающийся с водой лиганд, выбранный из группы, включающей спирты, альдегиды, кетоны, простые эфиры, простые полиэфиры, сложные эфиры, сложные полиэфиры, поликарбонаты, карбамиды, амиды, нитрилы и сульфиды, или их смеси,
Р представляет собой органическую добавку, выбранную из группы, состоящей из простых полиэфиров, сложных полиэфиров, поликарбонатов, сложных полиалкиленгликольных эфиров сорбита, полиалкиленгликольглицидиловых простых эфиров, полиакриламида, сополимеров акриламида с акриловой кислотов, полиакриловой кислоты, сополимеров акриламида с малеиновой кислотой, полиакрилонитрила, полиалкилакрилатов, полиалкилметакрилатов, простого поливинилметилового эфира, простого поливинилэтилового эфира, поливинилацетата, поливинилового спирта, поли-N-винилпирролидона, сополимеров N-винилпирролидона с акриловой кислотой, поливинилметилкетона, поли-4-винилфенола, сополимеров акриловой кислоты со стиролом, оксазолиновых полимеров, полиалкилениминов, сополимеров малеиновой кислоты и малеинового ангидрида, гидроксиэтилцеллюлозы, полиацетатов, соединений с ионной поверхностью и поверхностно-активных соединений, желчных кислот или их солей, сложных эфиров или амидов, сложных эфиров карбоновых кислот с многоатомными спиртами и гликозидами,
а также
a, b, d, g, n, r, s, j, k и t являются целыми или дробными числами больше нуля,
e, f, h и z являются целыми или дробными числами, больше или равными нулю,
причем
a, b, d, g, n, j, k и r, а также s и t выбраны таким образом, чтобы обеспечить электронейтральность,
М3 представляет собой водород или щелочной или щелочноземельный металл, а также
М4 означает ионы щелочного металла или ион аммония (NH4+) или ион алкиламмония (R4N+, R3NH+, R2NH2+, RNH3+ с R = алкил с 1-20 атомами углерода).
В особо предпочтительном варианте осуществления изобретения M1 представляет собой Zn2+ и M2 - Co3+ или Co2+.
Металлы М1 и М2 являются в частности одинаковыми, если они представляют собой кобальт, марганец или железо. В предпочтительном варианте осуществления алкоксилирование проводят таким образом, что содержащий полиизобутеновые группы фенол взаимодействует с алкиленоксидом, предпочтительно выбранным из группы, состоящей из этиленоксида, пропиленоксида, бутиленоксида, оксида стирола и их смесей, в присутствии сильных оснований, предпочтительно солей щелочных и щелочноземельных металлов спиртов с 1-4 атомами углерода, гидроксидов щелочных и щелочноземельных металлов, кислот Бренстедта или кислот Льюиса, таких как AlCl3, BF3 и т.д. Предпочтение отдается солям щелочных и щелочноземельных металлов спиртов с 1-4 атомами углерода, гидроксидам щелочных и щелочноземельных металлов, особо предпочтительно, метилату натрия, метилату калия, трет-бутилату калия, гидроксиду натрия и гидроксиду калия, наиболее предпочтительно, трет-бутилату калия и гидроксиду калия. Количество используемых катализаторов обычно находится в диапазоне от около 0,01 до 1 мас.%, в частности от 0,05 до 0,5 мас.%, в пересчете на общее количество исходных реагентов.
Алкоксилирование предпочтительно проводят при температурах в диапазоне от около 70 до 200 °С, предпочтительно от около 100 до 160 °С. Давление предпочтительно находится в диапазоне между давлением окружающей среды и 150 бар, в частности в диапазоне от 3 до 30 бар. При желании алкиленоксид может содержать примесь инертного газа, например от около 5 до 60%.
Продукт взаимодействия может быть обработан обычными способами, известными специалисту в данной области, например, посредством дегазации летучих компонентов в вакууме или посредством отгонки вместе с инертным в данных условиях газом, и при необходимости посредством фильтрации.
Катализатор также может быть отделен обработкой продукта силикатами магния (например, Ambosol®) с последующей фильтрацией.
Остатки катализатора могут оставаться в полученном продукте или могут быть нейтрализованы кислотой, предпочтительно соляной кислотой, серной кислотой, фосфорной кислотой или уксусной кислотой, причем затем соли можно удалить предпочтительно с помощью, например, промывки или ионообменных материалов. При необходимости, может иметь место частичная нейтрализация, и продукт может быть использован далее без дополнительного отделения солей. Взаимодействие с алкиленкарбонатами, предпочтительно 1,2-этиленкарбонатом, 1,3-пропиленкарбонатом и 1,2-пропиленкарбонатом, проводят как правило при стехиометрии от 1 до 2 молей карбоната : 1 моль фенола, предпочтительно 1,05-1,8 : 1, особо предпочтительно 1,1-1,7 : 1, наиболее предпочтительно 1,2-1,5 : 1 моль/моль. В качестве катализаторов взаимодействия с алкиленкарбонатами могут быть использованы неорганические соли, третичные амины, трифенилфосфин, гидрид лития и органические станнаты. Неорганическая соль предпочтительно имеет по меньшей мере один анион, выбранный из группы, состоящей из карбоната (CO32-), оксида (O2-), гидроксида (OH-), гидрокарбоната (HCO3-), фосфата (PO43-) гидрофосфата (HPO42-) и дигидрофосфата (H2PO4-). Предпочтительными являются оксид, гидроксид и фосфат или их смеси, особо предпочтительным является фосфат. Неорганическая соль предпочтительно имеет по меньшей мере один катион, выбранный из группы, состоящей из щелочных металлов, щелочноземельных металлов, тетраалкиламмония, аммония, церия, железа, марганца, хрома, молибдена, кобальта, никеля или цинка. Предпочтительными являются щелочные и щелочноземельные металлы, и особо предпочтительны литий, натрий, калий или кальций. Особо предпочтительны неорганические соли, включая их гидраты, представляющие собой LiOH, Li3PO4, Na3PO4, K3PO4, Na2CO3, K2CO3 и CaO, наиболее предпочтительной является K3PO4.
Возможными, хотя и менее предпочтительными, являются галогениды тетраалкиламмония, предпочтительно галогениды тетра-C1-C20-алкиламмония, более предпочтительно галогениды тетра-C1-C4-алкиламмония, предпочтительными галогенидами являются хлориды, бромиды и йодиды, особо предпочтительны хлориды или бромиды и наиболее предпочтительны хлориды, и предпочтительно третичных аминов, таких как триэтиламин и 2-метилимидазол, наиболее предпочтительно 2-метилимидазола.
Может быть выгодно оставить катализатор в реакционной смеси после завершения реакции и использовать его в последующей реакции, см. ниже. Однако также возможно удалить катализатор из реакционной смеси, например, посредством водной экстракции реакционной смеси или посредством фильтрации. Промывку, например, можно проводить в резервуаре с мешалкой или другом стандартном устройстве, например в колонне или экстракционном аппарате типа смеситель-отстойник. С технологической точки зрения в способе согласно изобретению для промывки могут быть использованы все известные сами по себе методики и устройства для экстракции и промывки, например, те, которые описаны в Ullmann's Encyclopedia of Industrial Chemistry, 6-е изд., 1999 г., Электронное издание, Глава „Liquid - Liquid Extraction - Apparatus". Например, они могут представлять собой одностадийные или многостадийные, предпочтительно одностадийные экстракции, а также экстракции в прямоточном или противоточном режиме.
Отделение от гетерогенного катализатора как правило проводят фильтрацией, электрофильтрацией, абсорбцией, центрифугированием или декантацией, предпочтительно фильтрацией. Отделенный гетерогенный катализатор затем может быть использован для дальнейших реакций.
Фильтрация может быть проведена, например, при помощи нутч-фильтра, работающего под давлением. С технологической точки зрения в способе согласно изобретению для фильтрации могут быть использованы все известные сами по себе методики и устройства для фильтрации, например, те, которые описаны в Ullmann's Encyclopedia of Industrial Chemistry, 7-е изд., 2013 г., Электронное издание, Глава: Filtration, 1. Fundamentals und Filtration 2. Equipment. Например, это могут быть патронные фильтры, фильтр-прессы, дисковые нагнетательные фильтры, мешочные фильтры или барабанные фильтры. Предпочтительно используют патронные фильтры и дисковые нагнетательные фильтры.
Фильтрация может быть проведена с или без вспомогательного вещества для фильтрования. Подходящими вспомогательными веществами для фильтрования являются вспомогательные вещества для фильтрования на основе кизельгура, перлита и целлюлозы. Подходящие центрифуги и сепараторы известны специалисту в данной области. С технологической точки зрения в способе согласно изобретению для центрифугирования могут быть использованы все известные сами по себе методики и устройства для центрифугирования, например, те, которые описаны в Ullmann's Encyclopedia of Industrial Chemistry, 7-е изд., 2013 г., Электронное издание, Глава: Centrifuges, Filtering und Centrifuges, Sedimenting.
Взаимодействие как правило проводят при температуре от 70 до 200 °С, особенно от 100 до 190 и наиболее предпочтительно от 150 до 170 °С.
Также возможно повысить температуру процесса в ходе реакции, чтобы ускорить декарбоксилирование после осуществленного раскрытия цикла карбоната.
Взаимодействие как правило завершается в течение 24 часов, предпочтительно в течение от 1 до 20 часов, особо предпочтительно в течение от 2 до 16 часов, наиболее предпочтительно от 3 до 12 часов.
Взаимодействие может быть проведено без растворителя или в присутствии таковых, например, простых эфиров, кетонов или углеводородов, предпочтительно без растворителя.
Под углеводородами предпочтительно понимают ароматические растворители, имеющие диапазон кипения при конкретном давлении выше температуры реакции. Примерами таких являются те, которые содержат в основном ароматические углеводороды с 7-14 атомами углерода и могут иметь диапазон кипения от 110 до 300 °С, особо предпочтительными являются толуол, о-, м- или п-ксилол, изомеры триметилбензола, изомеры тетраметилбензола, этилбензол, кумол, тетрагидронафталин и их содержащие смеси.
Другими примерами являются марки Solvesso® фирмы ExxonMobil Chemical, в частности Solvesso® 100 (CAS № 64742-95-6, в основном ароматические соединения с 9 и 10 атомами углерода, интервал кипения около 154-178 °C), 150 (диапазон кипения около 182 - 207 °C) и 200 (CAS № 64742-94-5), а также марки Shellsol® фирмы Shell, Caromax® (например, Caromax® 18) фирмы Petrochem Carless и Hydrosol фирмы DHC (например, как Hydrosol® А 170). Углеводородные смеси парафинов, циклопарафинов и ароматических соединений также коммерчески доступны под названиями Kristallöl (например, Kristallöl 30, диапазон кипения около 158-198 °С или Kristallöl 60: CAS № 64742-82-1), Уайт-спирит (например, также CAS № 64742-82-1) или Нафта (легкая: диапазон кипения около 155-180 °С, тяжелая: диапазон кипения около 225-300 °С). Содержание ароматических соединений в таких углеводородных смесях как правило составляет более 90 мас.%, предпочтительно более 95, особо предпочтительно более 98 и наиболее предпочтительно более 99 мас.%. Может быть полезно использовать углеводородные смеси с особенно пониженным содержанием нафталина.
Предпочтительным вариантом осуществления настоящего изобретения является взаимодействие свободного фенола сначала с карбонатом, предпочтительно этиленкарбонатом, а затем взаимодействие получаемого таким образом, содержащего -R-O-H группу продукта реакции с алкиленоксидом или смесью алкиленоксидов до достижения желаемого числа n в структурной единице -[-RO-]n-.
Это приводит к преимуществу, заключающемуся в получении более узкого молекулярно-массового распределения.
Другое преимущество состоит в том, что доступны такие продукты, в которых в структурной единице -[-RO-]n- первая структурная единица -[-RO-]- может отличаться от второй и до n-ой структурной единицы -[-RO-]-.
Этерификацию (мет)акриловой кислотой, кротоновой кислотой, фумаровой кислотой, малеиновой кислотой или ангидридом малеиновой кислоты или переэтерификацию с помощью сложных эфиров (мет)акриловой кислоты, сложных эфиров кротоновой кислоты, сложных эфиров фумаровой кислоты или сложных эфиров малеиновой кислоты алкоксилированных фенолов формулы

осуществляют как правило следующим образом:
Для этого алкоксилированный фенол и (мет)акриловую кислоту, кротоновую кислоту, фумаровую кислоту, малеиновую кислоту или малеиновый ангидрид подвергают взаимодействию при молярном соотношении кислоты к фенолу как правило по меньшей мере 1 : 1, предпочтительно по меньшей мере 1,05 : 1, особо предпочтительно по меньшей мере 1,1 : 1, наиболее предпочтительно по меньшей мере 1,25 : 1, и в частности по меньшей мере 1,5 : 1. Как правило, необходимым является молярное соотношение не более 5 : 1, предпочтительно не более 4 : 1, особо предпочтительно не более 3 : 1 и наиболее предпочтительно не более 2 : 1.
Пригодными катализаторами этерификации являются серная кислота, арил- или алкилсульфокислоты или их смеси. Примерами арилсульфокислот являются бензолсульфокислота, паратолуолсульфокислота или додецилбензолсульфокислота, примерами алкилсульфокислот являются метансульфокислота, этансульфокислота или трифторметансульфокислота. Сильнокислотные ионообменные материалы или цеолиты также могут быть использованы в качестве катализаторов этерификации. Предпочтительными являются серная кислота и сульфокислоты, особо предпочтительны метансульфокислота и пара-толуолсульфокислота.
Их как правило используют в количестве от 0,1 до 5 мас.% в пересчете на этерификационную смесь, предпочтительно от 0,5 до 5, особо предпочтительно от 1 до 4 и наиболее предпочтительно от 2 до 4 мас.%.
В случае необходимости катализатор этерификации может быть удален из реакционной смеси с помощью ионообменного материала. Ионообменный материал при этом может быть добавлен непосредственно в реакционную смесь и затем отфильтрован, или реакционная смесь может быть пропущена через засыпку ионообменного материала.
Предпочтительно катализатор этерификации оставляют в реакционной смеси. Однако, если катализатор представляет собой ионообменный материал, его предпочтительно удаляют, например, посредством фильтрации.
Предпочтительно этерификацию или переэтерификацию проводят в присутствии известного как такового ингибитора полимеризации в общем количестве от 0,01 до 5 мас.%, в пересчете на смесь этерификации, предпочтительно от 0,02 до 3, особо предпочтительно от 0,05 до 2 мас.%, наиболее предпочтительно от 0,1 до 1, и в частности от 0,3 до 1 мас.%.
Примеры таких ингибиторов полимеризации приведены например в международной заявке WO 2005/082828 A1, в частности, со страницы 15, строка 27 до страницы 19, строка 18, которые тем самым включены посредством ссылки в настоящее описание.
Для эффективности ингибиторов полимеризации может быть выгодным пропускать кислородсодержащий газ, например воздух или обедненный воздух, над реакционной смесью или предпочтительно через нее. Реакционная вода, образующаяся в ходе реакции, может быть отделена дистилляцией во время или после этерификации, причем этому процессу может помочь растворитель, образующий с водой азеотроп.
В качестве растворителя для азеотропного удаления реакционной воды, в случае такой необходимости, подходящими являются помимо прочих алифатические, циклоалифатические и ароматические углеводороды или их смеси.
Предпочтение отдается использованию н-пентана, н-гексана, н-гептана, циклогексана, метилциклогексана, бензола, толуола или ксилола. Особенно предпочтительными являются циклогексан, метилциклогексан и толуол.
Предпочтительно этерификацию проводят в присутствии растворителя. Количество применяемого растворителя составляет от 10 до 200 мас.%, предпочтительно от 20 до 100 мас.%, особо предпочтительно от 30 до 100 мас.% в пересчете на сумму фенола и кислоты. В случае если вода, содержащаяся в реакционной смеси, не удаляется с помощью образующего азеотроп растворителя, ее можно удалить путем отгонки с инертным газом, предпочтительно кислородсодержащим газом, особо предпочтительно воздухом или обедненным воздухом.
Температура реакции этерификации обычно составляет 40-160 °С, предпочтительно 60-140 °С и особо предпочтительно 80-120 °С. Температура в ходе реакции может оставаться постоянной или возрастать, предпочтительно она повышается в ходе реакции. В этом случае конечная температура этерификации на 5-30 °С выше начальной температуры.
В случае если используется растворитель, то после завершения реакции он может быть удален из реакционной смеси дистилляцией.
Реакционную смесь при необходимости обрабатывают в промывочном аппарате водой или 5-30 %-ным по массе, предпочтительно 5-20 %-ным по массе, особо предпочтительно 5-15 %-ным по массе раствором хлорида натрия, хлорида калия, хлорида аммония, сульфата натрия или сульфата алюминия, предпочтительно раствором поваренной соли.
Количественное соотношение реакционная смесь : промывочная жидкость обычно составляет 1 : 0,1-1, предпочтительно 1 : 0,2-0,8, особенно предпочтительно 1 : 0,3-0,7. Промывку, например, можно проводить в резервуаре с мешалкой или другом стандартном устройстве, например в колонне или экстракционном аппарате типа смеситель-отстойник, с технологической точки зрения в способе согласно изобретению для промывки могут быть использованы все известные сами по себе методики и устройства для промывки, например, те, которые описаны в Ullmann's Encyclopedia of Industrial Chemistry, 6-е изд., 1999 г., Электронное издание, Глава: "Liquid - Liquid Extraction - Apparatus". Например, они могут представлять собой одностадийные или многостадийные, предпочтительно одностадийные экстракции, а также таковые в прямоточном или противоточном режиме.
Предпочтительно применяют предварительную промывку тогда, когда в качестве ингибиторов (дополнительно) используют соли металлов, предпочтительно медь или соли меди.
Органическую фазу предварительной промывки, которая все еще содержит небольшие количества катализатора и большую часть избытка (мет)акриловой кислоты, обрабатывают 5-25, предпочтительно 5-20, особо предпочтительно 5-15 %-ным по массе водным раствором основания, такого как, например, гидроксид натрия, гидроксид калия, гидрокарбонат натрия, карбонат натрия, гидрокарбонат калия, гидроксид кальция, нашатырный спирт или карбонат калия, к которым при необходимости может быть добавлено 5-15 мас.% хлорида натрия, хлорида калия, хлорида аммония или сульфата аммония, предпочтительно нейтрализуют раствором гидроксида натрия или раствором гидроксида натрия и поваренной соли. Добавление основания осуществляют таким образом, чтобы температура в аппарате не поднималась выше 35 °С, предпочтительно от 20 до 35 °С, а рН составлял 10-14. Отвод тепла нейтрализации при необходимости осуществляют посредством охлаждения резервуара с помощью внутренних охлаждающих змеевиков или с помощью охлаждения через двойные стенки.
Количественное соотношение реакционная смесь : нейтрализующая жидкость как правило составляет 1 : 0,1-1, предпочтительно 1 : 0,2-0,8, особенно предпочтительно 1 : 0,3-0,7.
Что касается устройства, то для него также действительно все ранее указанное.
При необходимости для удаления следов основания или соли из нейтрализованной реакционной смеси может быть предпочтительно проводить последующую промывку, которая может проводиться аналогично предварительной промывке.
Альтернативно, реакционную смесь можно обработать посредством добавления 20-50%-ного водного раствора гидроксида натрия, предпочтительно 25-35%, особо предпочтительно 30%, и последующего добавления минерального, водопоглощающего вещества и проведения фильтрации, в результате чего отделяют избыток кислоты и катализатор. Например, можно использовать содержащие монтмориллонит слоистые силикаты, такие как бентонит или алюмосиликаты (Ambosol®).
В другом варианте осуществления этерификацию можно проводить посредством взаимодействия спирта с ангидридом (мет)акриловой кислоты, предпочтительно в присутствии по меньшей мере одного основного катализатора.
Предпочтительными являются такие катализаторы, которые имеют значение pKB не более 11,0, предпочтительно не более 7,0 и особо предпочтительно не более 3,0.
В принципе, подходящими являются все основания, такие как гидроксиды щелочных и щелочноземельных металлов, а также неорганические соли. Гидроксиды щелочных и щелочноземельных металлов могут быть использованы как в твердом, так и растворенном виде, например, в форме водных растворов.
Неорганическая соль предпочтительно имеет по меньшей мере один анион, выбранный из группы, состоящей из карбоната (CO32-), оксида (O2-), гидроксида (OH-), гидрокарбоната (HCO3-), фосфата (PO43-) гидрофосфата (HPO42-) и дигидрофосфата (H2PO4-). Предпочтительными являются оксид, гидроксид и фосфат или их смеси, особо предпочтительным является фосфат. Неорганическая соль предпочтительно имеет по меньшей мере один катион, выбранный из группы, состоящей из щелочных металлов, щелочноземельных металлов, тетраалкиламмония, аммония, церия, железа, марганца, хрома, молибдена, кобальта, никеля или цинка. Предпочтительными являются щелочные и щелочноземельные металлы, и особо предпочтительны литий, натрий, калий или кальций. Особо предпочтительны неорганические соли, включая их гидраты, представляющие собой LiOH, NaOH, KOH, Li3PO4, Na3PO4, K3PO4, Na2CO3, K2CO3 и CaO, наиболее предпочтительными являются NaOH, K2CO3 и K3PO4. В альтернативном варианте осуществления получение соединения формулы (I) может также быть осуществлено переэтерификацией вместо этерификации. Для этого вместо свободной кислоты предпочтительно используют сложный C1-C4-алкиловый эфир кислоты, то есть метиловый, этиловый, н-пропиловый, изопропиловый, н-бутиловый, втор-бутиловый, изобутиловый или трет-бутиловый сложный эфир, предпочтительно метиловый, этиловый или н-бутиловый сложный эфир, особо предпочтительно метиловый или этиловый сложный эфир и наиболее предпочтительно метиловый сложный эфир.
В качестве катализаторов получения сложных эфиров (мет)акриловой кислоты посредством переэтерификации можно использовать, например, алкоголяты титана, алкильные группы которых представляют собой алкильные остатки с 1-4 атомами углерода, например, тетраметил-, тетраэтил-, тетраизопропил-, тетрапропил-, тетраизобутил- и тетрабутилтитанат (см., например, европейские заявки EP-B 298 867, EP-A2 960 877). Кроме того, в качестве катализаторов помимо прочих предлагаются феноляты титана (DE-OS 200 86 18), металлхелатные соединения, например, гафния, титана, циркония или кальция, алкоголяты щелочных металлов и магния, органические соединения олова, такие как оксид диметилолова, оксид дибутилолова или оксид дифенилолова, или неорганические соли.
Другими подходящими оловосодержащими катализаторами являются соединения, содержащие Sn (IV), например дихлорид диалкилолова, оксид диалкилолова, диацетат диалкилолова, оксид бис(триалкилолова), оксид бис(дибутилхлоролова), например дихлорид дибутилолова, дихлорид диметилолова и оксид дибутилолова. Хлоридсодержащие катализаторы можно использовать вместе с алкоголятами, например, с метилатом натрия.
Неорганическая соль предпочтительно имеет по меньшей мере один анион, выбранный из группы, состоящей из карбоната (CO32-), оксида (O2-), гидроксида (OH-), гидрокарбоната (HCO3-), фосфата (PO43-) гидрофосфата (HPO42-) и дигидрофосфата (H2PO4-). Предпочтительными являются оксид, гидроксид и фосфат или их смеси, особо предпочтительным является фосфат. Неорганическая соль предпочтительно имеет по меньшей мере один катион, выбранный из группы, состоящей из щелочных металлов, щелочноземельных металлов, тетраалкиламмония, аммония, церия, железа, марганца, хрома, молибдена, кобальта, никеля или цинка. Предпочтительными являются щелочные и щелочноземельные металлы, и особо предпочтительны литий, натрий, калий или кальций. Особо предпочтительны неорганические соли, включая их гидраты, представляющие собой LiOH, Li3PO4, Na3PO4, K3PO4, Na2CO3, K2CO3 и CaO, наиболее предпочтительной является K3PO4.
Особенно подходящими являются гетерогенные катализаторы или гомогенные катализаторы, которые могут быть переведены в гетерогенные осадки, как в способах переэтерификации, которые описаны, например в заявках DE 2 317 226 А1, DE 10 2004 036 930 А1 и WO 2009/080380. Катализаторы или осадки катализаторов как правило отделяют посредством фильтрации, электрофильтрации, абсорбции, центрифугирования или декантации.
Для получения соединений формулы (I) можно использовать все катализаторы переэтерификации, описанные в предшествующем уровне техники, предпочтительно неорганические соли, включая их гидраты: LiOH, Li3PO4, Na3PO4, K3PO4, Na2CO3, K2CO3 и CaO.
Реакцию переэтерификации обычно проводят при температуре от 60 до 140 °С, предпочтительно от 70 до 110 °С. При этом непрерывно отделяют дистилляцией азеотроп из выводящего вещества и спирта.
Подходящими выводящими веществами, которые образуют азеотропно кипящую смесь со спиртами, имеющими 1-4 атомов углерода, являются, прежде всего, сами соответствующие сложные алкиловые эфиры, имеющие 1-4 атомов углерода в алкиле. В качестве отдельных выводящих веществ подходящими являются помимо прочих циклогексан, метилциклогексан, бензол, толуол, гексаны и гептаны и их смеси. Предпочтительными являются метилакрилат, метилметакрилат, этилакрилат и этилметакрилат и их смеси с н-гептаном и циклогексаном. Термин «выводящее вещество» в данном контексте включает сам исходный реагент и, при необходимости, дополнительно используемый отдельный растворитель.
В предпочтительном варианте осуществления в качестве выводящего вещества не используют отдельный растворитель. В этом случае в качестве выводящего вещества выступает сам исходный реагент алкил(мет)акрилат.
Выводящее вещество затем может быть опять добавлено в реактор. Для этого азеотропную смесь спирта и выводящего вещества в предпочтительном варианте отделяют дистилляцией в подходящей колонне, перемешивают в смесительном сосуде с водой и затем переносят в фазовый сепаратор, при этом спирт, в основном метанол или этанол, растворяется в воде, а органическая фаза отделяется в виде верхнего слоя. Органическую фазу предпочтительно подают обратно в реакционную смесь через верх колонны и, таким образом, возвращают в цикл лишь с небольшими потерями. Однако также в качестве альтернативы возможно добавить свежее выводящее вещество и осуществить обработку смеси выводящего вещества со спиртом на отдельной стадии или исключить добавление выводящего вещества полностью или частично.
Как правило, алкил(мет)акрилат используют в стехиометрическом избытке. Предпочтительно избыток метил(мет)акрилата на каждую подлежащую этерификации гидроксильную группу составляет от 0,1 до 100 эквивалентов, особо предпочтительно от 3 до 50 эквивалентов, в частности от 10 до 40 эквивалентов.
Катализатор используют в концентрации от 2 до 20 мол.% в пересчете на количество спирта, предпочтительно в концентрации от 3 до 10 мол.%.
Переэтерификация может быть проведена при атмосферном давлении, но также при избыточном или пониженном давлении. В основном ее проводят при 300-1000 мбар, предпочтительно при 800-1000 мбар (атмосферное давление = 1000 мбар). Время реакции обычно составляет от 1 до 24 часов, предпочтительно от 3 до 18 часов, особо предпочтительно от 6 до 12 часов. Переэтерификация может быть проведена непрерывно, например, в каскаде резервуаров с мешалкой или периодически.
Реакцию можно проводить во всех реакторах, подходящих для такой реакции. Такие реакторы известны специалисту в данной области. Взаимодействие предпочтительно происходит в реакторе типа резервуара с мешалкой.
Для перемешивания исходных смесей можно использовать любые способы, такие как, например, перемешивающие устройства. Перемешивание также можно осуществлять посредством подачи газа, предпочтительно кислородсодержащего газа.
Удаление образовавшегося спирта, в основном метанола или этанола, происходит непрерывным или поэтапным методом, известным сам по себе, посредством азеотропной дистилляции в присутствии выводящего вещества. Кроме того, метанол также может быть удален посредством отгонки с выводящим газом.
В предпочтительном варианте осуществления из отделенного дистилляцией азеотропа из выводящего вещества и спирта спирт отделяют путем промывки водой, и выводящее вещество возвращают в реакционный сосуд.
После завершения реакции катализатор может быть удален из продукта с помощью уже описанных процессов разделения экстракции или фильтрации, а выводящее вещество может быть отделено дистилляцией.
В одном предпочтительном варианте осуществления настоящего изобретения между взаимодействием свободного фенола с карбонатом и/или алкиленоксидом и этерификацией или переэтерификацией, не проводят стадий обработки, таких как, например, экстракция или фильтрация.
В другом предпочтительном варианте осуществления настоящего изобретения для взаимодействия свободного фенола с карбонатом и/или алкиленоксидом и для этерификации или переэтерификации, особо предпочтительно для взаимодействия свободного фенола с карбонатом и последующей переэтерификации или взаимодействия с ангидридом (мет)акриловой кислоты, используют одинаковый катализатор.
Это выгодно в частности тогда, когда катализаторы, используемые для взаимодействия свободного фенола с карбонатом и/или алкиленоксидом, и катализаторы этерификации или переэтерификации негативно взаимодействуют друг с другом, например, кислоты и основания.
Целесообразно проводить взаимодействие свободного фенола с карбонатом при катализе галогенидом тетраалкиламмония, ЭДТА или третичного амина, такого как триэтиламин, 2-метилимидазол, и переэтерификацию, как это уже было подробно описано выше.
Целесообразно проводить взаимодействие свободного фенола с карбонатом при катализе галогенидом тетраалкиламмония или ЭДТА и переэтерификацию в присутствии кислоты, как это уже было подробно описано выше.
Целесообразно также проводить взаимодействие свободного фенола с карбонатом при катализе галогенидом тетраалкиламмония, ЭДТА или третичного амина, такого как триэтиламин, 2-метилимидазол, и этерификацию ангидридом (мет)акриловой кислоты, как это уже было подробно описано выше.
Особо целесообразно проводить, как взаимодействие свободного фенола с карбонатом, так и переэтерификацию или этерификацию ангидридом (мет)акриловой кислоты при катализе неорганической солью, как это уже было подробно описано выше.
Особое преимущество здесь заключается в простом отделении катализатора посредством фильтрации после проведения обоих стадий реакции.
В равной степени выгодно проводить как взаимодействие свободного фенола с карбонатом, так и переэтерификацию при катализе следующими катализаторами:
галогениды, гидроксиды, оксиды, карбонаты, гидрокарбонаты или фосфаты щелочных металлов, щелочноземельных металлов или тетраалкиламмония.
Преимущество данной процедуры проведения способа состоит в том, что в этом случае можно обойтись без удаления катализатора из алкоксилированного фенола, или это может иметь место только на стадии соединения формулы (I).
Еще одним объектом настоящего изобретения являются полимеры, содержащие в заполимеризованной форме по меньшей мере одно соединение (А) формулы (I). В предпочтительном варианте осуществления в случае данных полимеров речь идет о гомополимерах, содержащих исключительно соединения формулы (I) в заполимеризованной форме, или в другом столь же предпочтительном варианте осуществления о сополимерах, которые содержат не только по меньшей мере одно соединение формулы (I), но также по меньшей мере один другой мономер (В), выбранный из группы, состоящей из
(B1) (мет)акрилатов, отличных от (A),
(B2) производных фумаровой и малеиновой кислоты,
(B3) простых алкилвиниловых эфиров,
(B4) стирола и α-метилстирола,
(B5) акрилонитрила
(B6) винилалканоатов и
(B7) (мет)акриламидов.
Мономерами (B1) являются акриловая кислота, метакриловая кислота и отличные от (A) (мет)акрилаты, предпочтительно акриловая кислота, метакриловая кислота, циклоалкил(мет)акрилаты, алкил(мет)акрилаты и (мет)акрилаты моноэфиров полиалкиленгликоля.
Предпочтительными циклоалкил(мет)акрилатами являются циклоалкил(мет)акрилаты, циклоалкильный остаток которых образован из 3-12-ти членного кольца, предпочтительно из 5-12-ти членного кольца и особо предпочтительно из пяти- или шестичленного кольца.
В частности предпочтительными являются циклопентил(мет)акрилат, циклогексил(мет)акрилат, циклооктил(мет)акрилат и циклододецил(мет)акрилат, особо предпочтительны циклопентил(мет)акрилат, циклогексил(мет)акрилат и циклододецил(мет)акрилат, наиболее предпочтительны циклопентил(мет)акрилат и циклогексил(мет)акрилат, и в частности циклогексил(мет)акрилат, причем акрилаты в каждом случае предпочтительнее метакрилатов.
Примерами алкил(мет)акрилатов являются алкил(мет)акрилаты, алкильный остаток которых содержит от 1 до 20 атомов углерода, предпочтительно от 1 до 12 и особо предпочтительно от 1 до 8. В частности, предпочтительными являются метил(мет)акрилат, этил(мет)акрилат, изопропил(мет)акрилат, н-пропил(мет)акрилат, н-бутил(мет)акрилат, изобутил(мет)акрилат, втор-бутил(мет)акрилат, трет-бутил(мет)акрилат, н-гексил(мет)акрилат, н-гептил(мет)акрилат, н-октил(мет)акрилат, н-децил(мет)акрилат, н-додецил(мет)акрилат, н-тетрадецил(мет)акрилат, н-гексадецил(мет)акрилат, н-гептадецил(мет)акрилат, н-октадецил(мет)акрилат, н-эйкозил(мет)акрилат, 2-этилгексил(мет)акрилат и 2-пропилгептил(мет)акрилат, особо предпочтительными являются метил(мет)акрилат, этил(мет)акрилат, н-бутил(мет)акрилат, трет-бутил(мет)акрилат и 2-этилгексил(мет)акрилат, наиболее предпочтительными являются метилакрилат, метилметакрилат, этилакрилат, н-бутилакрилат, трет-бутилакрилат и 2-этилгексилакрилат и наиболее предпочтительны н-бутилакрилат и 2-этилгексилакрилат.
Примерами (мет)акрилатов моноэфиров олиго- и полиалкиленгликоля являются (мет)акрилаты моноалкиловых эфиров олиго- и полиэтиленгликоля, предпочтительно фениловые эфиры, метиловые эфиры или н-бутиловые эфиры, особо предпочтительны метиловые эфиры или н-бутиловые эфиры и наиболее предпочтительны метиловые эфиры.
В качестве производных фумаровой и малеиновой кислот (В2) упоминаются фумаровая и малеиновая кислоты и их сложные алкиловые эфиры с 1-4 атомами углерода в алкиле, а также в случае малеиновой кислоты малеиновый ангидрид. Предпочтительными являются фумаровая и малеиновая кислота, метиловые, этиловые, н-бутиловые и 2-этилгексиловые эфиры фумаровой и малеиновой кислот, а также малеиновый ангидрид, особо предпочтителен малеиновый ангидрид.
В случае простых алкилвиниловых эфиров (B3) предпочтительно речь может идти о простых алкилвиниловых эфирах, предпочтительно о простых алкилвиниловых эфирах, имеющих от 1 до 8 атомов углерода в алкиле, особо предпочтительно выбранных из группы, состоящей из простого метилвинилового эфира, простого этилвинилового эфира, простого н-пропилвинилового эфира, простого изопропилвинилового эфира, простого н-бутилвинилового эфира, простого втор-бутилвинилового эфира, простого изобутилвинилового эфира, простого трет-бутилвинилового эфира, простого гексилвинилового эфира и простого октилвинилового эфира и их смесей.
В качестве мономера (B4) необходимо упомянуть стирол и α-метилстирол, предпочтительно стирол.
В случае мономера (B5) речь идет об акрилонитриле.
В случае винилалканоатов (В6) предпочтительно речь идет о сложных виниловых эфирах карбоновых кислот, имеющих 2-13 атомов углерода, предпочтительными являются таковые, выбранные из группы, состоящей из винилацетата, винилпропионата, винилбутирата, винил-2-этилгексаноата, винилового эфира неопентановой кислоты, винилового эфира гексановой кислоты, винилового эфира неононановой кислоты и винилового эфира неодекановой кислоты, особо предпочтительно выбранные из группы, состоящей из винилацетата, винилпропионата, винилбутирата и винилового эфира неопентановой кислоты, наиболее предпочтительным является винилацетат.
В случае мономера (B7) речь предпочтительно идет о метакриламиде и акриламиде, особо предпочтительно об акриламиде.
Предпочтительными при этом являются мономеры (B1), (B3), (B4) и (B7), особо предпочтительны (B1) и (B3) и наиболее предпочтительны (B1).
Может оказаться достаточным, если доля мономера (А) в заполимеризованной форме в полимере составляет по меньшей мере 1 мас.%, предпочтительно по меньшей мере 2 мас.%, особо предпочтительно по меньшей мере 5 мас.% и наиболее предпочтительно по меньшей мере 8 мас.%. Предпочтительно доля мономера (А) в заполимеризованной форме в полимере должна составлять по меньшей мере 10 мас.%, предпочтительно по меньшей мере 20 мас.%, особо предпочтительно по меньшей мере 30 мас.% и наиболее предпочтительно по меньшей мере 50 мас.%.
Доля мономера (А) в заполимеризованной форме может составлять до 100 мас.% (гомополимер), предпочтительно до 95 мас.%, особо предпочтительно до 90 мас., наиболее предпочтительно до 85 мас.% и в частности до 70 мас.%.
В случае сополимеров можно использовать один или более мономеров, отличных от (А), предпочтительно один, два или три, особо предпочтительно один или два, и наиболее предпочтительно только один.
Мономерные компоненты (А) и, при необходимости, (В) можно полимеризовать, предпочтительно в виде индивидуального вещества, в суспензии или в растворе, особо предпочтительно в растворе или суспензии, наиболее предпочтительно в эмульсии. Для этой цели реакцию полимеризации как правило проводят при нормальном давлении и в атмосфере инертного газа, такого как азот, но можно работать также и при повышенных давлениях, например, в автоклаве. Температуры полимеризации как правило находятся в диапазоне от 50 до 250 °С, в частности от 90 до 210 °С, прежде всего от 120 до 180 °С, обычно от 140 до 160 °С. Подходящими полимеризационными реакторами в принципе являются все обычные устройства непрерывного или периодического действия, такие как, например, резервуар с мешалкой, каскад резервуаров с мешалкой, трубчатый реактор или реактор с внутренним контуром циркуляции.
В случае эмульсионной полимеризации полимеризацию предпочтительно проводят без приложения внешнего давления при температуре от 50 до 95 °С.
Обычно полимеризацию инициируют радикально разлагающимися инициаторами, подходящими для этой цели являются воздух или кислород или неорганические или органические пероксиды и/или гидропероксиды, а также органические азосоединения. В качестве органических пероксидов или соответственно гидропероксидов подходящими являются, например, гидропероксид диизопропилбензола, гидропероксид трет-бутила, гидропероксид кумола, пероксид метилизобутилкетона, ди-трет-бутилпероксид и трет-бутилперизононаноат. В качестве органического азосоединения пригодным является, например, азобисизобутиронитрил («AIBN»). Кроме того, помимо пероксида водорода следует упомянуть пероксодисульфаты, в частности пероксодисульфаты натрия.
Также допустимыми являются окислительно-восстановительные пары вышеуказанных пероксидов или гидропероксидов с дисульфитами, аддуктом из дисульфита и ацетона, предпочтительно ацетон-бисульфитом или Rongalit® C.
Кроме того, в полимеризации могут быть использованы подходящие регуляторы длины полимерной цепи, такие как алифатические альдегиды или кетоны или также водород.
Если в полимеризации используют растворители или суспендирующие агенты, то пригодными для этого являются обычные инертные жидкости, такие как ароматические углеводороды, например, толуол, ксилолы или соответствующие технические смеси углеводородов, такие как Solvesso® или Solvent Naphtha, и алифатические и циклоалифатические углеводороды и смеси углеводородов, такие как пентан, гексаны, гептаны, петролейный эфир, лигроин, циклогексан, метилциклогексан и декалин.
В предпочтительном варианте осуществления полимеризацию проводят посредством эмульсионной полимеризации, особо предпочтительно посредством миниэмульсионной полимеризации.
В предпочтительном варианте осуществления ее выполняют посредством эмульсионной полимеризации, как в международной заявке WO 2016/046195 A1, в частности, со страницы 15, строка 31 до страницы 27, строка 32, которая тем самым включена посредством ссылки в настоящее описание.
В этих способах на первой стадии как правило готовят смесь из мономеров, необходимого количества эмульгатора и/или защитного коллоида, при необходимости гидрофобной добавки и воды, и из нее получают эмульсию. Гидрофобные мономеры при этом предварительно эмульгируют при помощи вспомогательных веществ.
На первой стадии предпочтительно получают гомогенную органическую фазу, а на второй стадии данную органическую фазу добавляют к водной фазе или водную фазу добавляют к полученной таким образом органической фазе.
Затем посредством перемешивания получают макроэмульсию "масло-в-воде". Частицы макроэмульсии измельчают посредством ультразвука и/или гомогенизацией под высоким давлением до размера менее 1 мкм.
Предпочтительно средний размер частиц (среднее значение z), измеренный с помощью динамического рассеяния света, в приготовленной таким образом эмульсии в основном составляет <1000 нм, предпочтительно <500 нм и особо предпочтительно 20-500 нм. В обычном случае диаметр составляет 50-400 нм.
Полученные частицы отличаются по размеру в сравнении с классической эмульсионной полимеризацией. В то время как при классической эмульсионной полимеризации размер капель составляет более 1,5 мкм, особенно от 2 до 50 мкм, то размер капель при приготовлении миниэмульсии равен менее 1000 нм.
Мономеры, находящиеся в форме эмульгированных капель, затем полимеризуют при помощи инициатора.
Для получения эмульсии согласно изобретению требуется подвод энергии не более 108 Вт/м3.
Целесообразно осуществлять приготовление эмульсии так быстро, чтобы время эмульгирования было небольшим по сравнению со временем реакции мономеров друг с другом.
Предпочтительный вариант осуществления способа состоит в том, чтобы приготовить все количество эмульсии при охлаждении до температур ниже комнатной температуры. Предпочтительно приготовление эмульсии осуществляют менее чем за 10 минут. Посредством увеличения температуры эмульсии при перемешивании доводят преобразование до конца. Температуры реакции находятся в диапазоне между комнатной температурой и 120 °С, предпочтительно между 60 и 100 °С. В случае необходимости может быть приложено давление, чтобы сохранить легкокипящие компоненты в виде жидкости.
Как правило, при получении эмульсий в качестве поверхностно-активных соединений применяют ионные и/или неионные эмульгаторы и/или защитные коллоиды или соответственно стабилизаторы.
Подробное описание подходящих защитных коллоидов приведено в книге Houben-Weyl, Methoden der organischen Chemie, Band XIV/1, Makromolekulare Stoffe, Georg-Thieme-Verlag, Stuttgart, 1961, стр. 411 – 420. Подходящими эмульгаторами являются как анионные, катионные, так и неионные эмульгаторы. Предпочтительно в качестве сопутствующих поверхностно-активных веществ используют исключительно эмульгаторы, молекулярная масса которых, в отличие от защитных коллоидов, обычно составляет менее 2000 г/моль. Само собой разумеется, что в случае применения смесей поверхностно-активных веществ отдельные компоненты должны быть совместимы друг с другом, что в случае сомнений можно проверить в нескольких простых предварительных опытах. Предпочтительно в качестве поверхностно-активных веществ применяют анионные и неионные эмульгаторы. Обычными сопутствующими эмульгаторами являются, например, этоксилированные жирные спирты (степень этоксилирования: от 3 до 50, алкильный остаток: С8-С36), этоксилированные моно-, ди- и триалкилфенолы (степень этоксилирования: от 3 до 50, алкильный остаток: C4-C9), соли щелочных металлов диалкиловых эфиров сульфоянтарной кислоты, а также соли щелочных металлов и/или аммония алкилсульфатов (алкильный остаток: C8-C12), этоксилированных алканолов (степень этоксилирования: от 4 до 30, C9) алкилсульфоновых кислот (алкильный остаток: С12-С18) и алкиларсульфоновых кислот (алкильный остаток: C9-C18).
Подходящие эмульгаторы приведены также в книге Houben-Weyl, Methoden der organischen Chemie, Band XIV/1, Makromolekulare Stoffe, Georg-Thieme-Verlag, Stuttgart, 1961, стр. 192 – 208. Торговыми марками эмульгаторов являются, например, Dowfax® 2 A1 фирмы Dow, Emulan® NP 50, Emulan® OG, Disponil® FES 27, Disponil® FES 32, Disponil® FES 77, Lutensol® AT 11, Disponil® SDS, Lutensol® AT 18, Lutensol® TO 2, Lutensol® TO 3, Lutensol® TO 5, Lutensol® TO 8, Lutensol TO® 10, Nekanil® 904 S фирмы BASF, Lumiten® 1-RA и Lumiten E 3065 фирмы BASF, Dextrol® OC 50 фирмы AVEBE GmbH и др.
В зависимости от количества мономеров, содержащихся в водной эмульсии, количество эмульгаторов как правило находится в диапазоне от 0,1 до 10 мас.%. Как уже упоминалось, к эмульгаторам можно дополнительно добавлять защитные коллоиды, которые способны стабилизировать дисперсное распределение окончательно полученной водной дисперсии полимера. Независимо от количества используемого эмульгатора защитные коллоиды можно применять в количестве до 50 мас.%, например, в количестве от 1 до 30 мас.% в пересчете на мономеры.
В качестве со-стабилизаторов в виде гидрофобной добавки к мономерам можно добавлять вещества в количестве от 0,01 мас.% до 10 мас.%, предпочтительно от 0,1 до 1 мас.%, которые имеют растворимость в воде менее 5×10-5, предпочтительно 5х10-7 г/л. Примерами являются углеводороды, такие как гексадекан, галогенированные углеводороды, силаны, силоксаны, гидрофобные масла (оливковое масло), красители и т.д. Помимо них выполнять функцию гидрофобности также могут блокированные полиизоцианаты.
В предпочтительном варианте осуществления сначала готовят смесь из мономеров, эмульгаторов и/или защитных коллоидов, а также при необходимости гидрофобной добавки и воды. Затем получают эмульсию и нагревают ее при перемешивании. После достижения требуемой температуры реакции в водную фазу добавляют инициатор. Само собой разумеется однако, что инициатор также может быть добавлен сразу в масляную фазу эмульсии, т.е. в мономерную фазу, перед диспергированием, или может быть добавлен в водную фазу сразу после приготовления эмульсии. Затем нагревают при перемешивании и полимеризуют. Особо предпочтительно процесс получения дисперсии посредством миниэмульсионной полимеризацией может быть описан следующим образом:
i. Смешивание мономеров и возможное добавление со-растворителя
ii. Получение макроэмульсии посредством добавления гидрофобной фазы со стадии i. в предварительно смешанный раствор эмульгатора с водой
iii. Размельчение частиц посредством ультразвука и/или гомогенизации под высоким давлением до размера частиц менее 1000 нм, предпочтительно менее 500 нм и особо предпочтительно 20-500 нм
iv. Инициирование свободно-радикальной полимеризации миниэмульсии "масло-в-воде" со стадии iii.
Средневесовая молекулярная масса Mw получаемых таким образом полимеров обычно составляет 5000 г/моль или более, предпочтительно по меньшей мере 10000 г/моль, особо предпочтительно по меньшей мере 20 000 г/моль, наиболее предпочтительно по меньшей мере 30 000 г/моль, и в частности по меньшей мере 50 000 г/моль, и конкретно по меньшей мере 100000 г/моль.
Верхняя граница средневесовой молекулярной массы Mw получаемых таким образом полимеров как правило составляет до 1000000 г/моль, предпочтительно до 700000 и особо предпочтительно до 300000 г/моль.
Полидисперсность Mw/Mn как правило составляет не более 5, предпочтительно не более 4, особо предпочтительно не более 3, наиболее предпочтительно не более 2, и в частности не более 1,5.
Особое преимущество миниэмульсионной полимеризации состоит в том, что при этом по сравнению, например, с полимеризацией в растворе или в массе могут быть достигнуты более высокие молекулярные массы. Соединения (А), получаемые по настоящему изобретению, и полимеры, содержащие их в заполимеризованной форме, находят применение при получении клеящих веществ, сырья для клеящих веществ, топливных добавок, добавок к смазочным материалам, в качестве эластомеров или в качестве основного компонента герметиков и уплотнительных масс.
Примеры
Аналитические данные
Эксклюзионную хроматографию по размеру проводили в THF + 0,1% трифторуксусной кислоты при 35 °С и скорости потока 1 мл/мин с комбинацией колонок из при необходимости используемой предварительной колонки PLgel и двух колонок PLgel MIXED-B (внутренний диаметр 7,5 мм, длина 30 см, пределы исключения 500-10 000 000 г/моль). Калибровку проводили с использованием полистирольных стандартов с узким распределением.
Пример А
1775 г полиизобутена (Mn 1000 г/моль) растворяли в 360 г гексана. 345 г фенола помещали в 180 г толуола в 4 л емкости фирмы HWS с нижним выводом и охлаждали с помощью охлаждающего термостата до 16 °С. 32,7 г комплекса BF3-фенол добавляли к фенольному раствору. В течение 5 ч 30 мин при 16 °С добавляли раствор полиизобутена. Реакционную смесь перемешивали в течение ночи при комнатной температуре и затем гасили 1 л метанола. Обработку и отделение избытка фенола проводили путем разбавления гексаном и экстракции метанолом. Конверсию определяли с помощью 1H-ЯМР (400 МГц в CDCI3).
1H-NMR (400 МГц в CDCI3) δ (ppm) = 7,22 (м, 2H), 6,75 (м, 2H), 4,57 (с, 1 H), 1,79 (с, 2H), 1,65-0,90 (CH3и CH2, PIB), 0,81 (с, 6H).
Пример В
1380 г полиизобутена (Mn 2300 г/моль) растворяли в 400 г гексана. 113 г фенола помещали в 200 г толуола в 4 л емкости фирмы HWS с нижним выводом в атмосфере азота и охлаждали с помощью охлаждающего термостата до 19 °C. 15,4 г комплекса BF3-фенол добавляли по каплям к фенольному раствору. В течение 4 ч при 17-20 °С добавляли раствор полиизобутена. Реакционную смесь перемешивали в течение 48 ч при комнатной температуре и затем гасили смесью метанол/гексан (1 л/500 мл). Обработку и отделение избытка фенола проводили посредством экстракции метанолом. Конверсию определяли с помощью 1H-ЯМР (400 МГц в CD2CI2).
Пример 1
Переэтерификацию проводили с пропусканием обедненного воздуха в 4 л-реакторе с двойными стенками, снабженном якорной мешалкой, вводом для обедненного воздуха, разделительной колонной и распределителем жидкости. В этом аппарате 3383 г 30%-ного раствора моноэтоксилированного фенола, содержащего полиизобутеновый остаток, в соответствии с примером 9, помещали в метилметакрилат. Добавляли 0,3 г метилгидрохинона (MEHQ) и 14,9 г фосфата калия и реакционную смесь нагревали при пропускании обедненного воздуха (2 л/ч) при температуре бани, первоначально составляющей 110 °С. Устанавливали давление в 600 мбар (абс.) и непрерывно удаляли дистилляцией азеотроп из метанола и метилметакрилата, при этом устанавливали температуру в кубе от 84 до 87 °С. Коэффициент орошения (флегмовое число) варьировал от 10 : 1 до 20 : 1 (возврат флегмы : отвод). После завершения реакции продукт смешивали с 15 г Hyflo Super Cel® и 15 г Ambosol® MP 25, отфильтровывали через фильтр, работающий под давлением, при макс. 2 бар и реакционную смесь концентрировали в вакууме. Было получено 970 г продукта. Конверсию определяли как > 99% с помощью ЯМР после обработки трихлорацетил изоцианатом (TAI). Содержание стабилизатора составляло 130 ч.н.млн MEHQ (определено ВЭЖХ).
1H-NMR (400MHz в CD2CI2) δ (ppm) = 7,28 (м, 2H), 6,83 (м, 2H), 6.11 (м, 1 H), 5,58 (м, 1 H), 4,46 (м, 2H), 4,20 (м, 2H), 1,94 (с, 3H), 1,82 (с, 2H), 1,65-0,90 (CH3 и CH2, PIB), 0,81 (с, 6H).
Содержание фтора (определенное с помощью ионной хроматографии продуктов сгорания) составляло <1 ч.н.млн.
Пример 2 (Сравнительный)
Переэтерификацию проводили с пропусканием воздуха в 0,75 л-реакторе с двойными стенками, снабженном якорной мешалкой, вводом для воздуха, разделительной колонной и распределителем жидкости. В этот аппарат помещали 50 г содержащего полиизобутеновый остаток фенола, полученного аналогично примеру А, и 600 г метилметакрилата. Добавляли 0,24 г метилгидрохинона (MEHQ) и 0,75 г фосфата калия и реакционную смесь нагревали при пропускании воздуха (0,3 л/ч) при температуре бани, составляющей 115 °С. Устанавливали давление в 600 мбар (абс.) и непрерывно удаляли дистилляцией метилметакрилат с частью метанола, при этом устанавливали температуру в кубе от 85 до 86 °С. Через 6 ч реакционную смесь отфильтровывали через фильтр, работающий под давлением, при макс. 2 бар и концентрировали в вакууме. Конверсию определяли как 2,5 % с помощью 1Н-ЯМР.
Пример 3
Взаимодействие проводили в четырехгорлой круглодонной колбе объемом 500 мл с обогревом масляной баней, термометром, обратным холодильником, подводом воздуха и тефлоновой мешалкой типа "полумесяц". 145 г прогретого до 60 °С моноэтоксилированного фенола, содержащего полиизобутеновый остаток, (полученного с 2-метилимидазолом в качестве катализатора в соответствии с примером 9) и 33 мг трет-бутилгидрокситолуола смешивали при температуре бани 80 °С. При пропускании воздуха (около 0,3 л/ч) и температуре бани 95 °С добавляли 18,9 г ангидрида метакриловой кислоты (94%-ного, стабилизированного при помощи Topanol® А) и повышали температуру бани до 100 °С. Через 1,33 часа добавляли 80 мг NaOH. Через суммарно 6 часов определяли конверсию как > 90 % с помощью ЯМР после обработки трихлорацетил изоцианатом (TAI). Дополнительно дозировали 1,6 г ангидрида метакриловой кислоты и давали возможность реагировать еще 3 часа при температуре бани 100 °С. Конверсию определяли как > 95 % с помощью ЯМР после обработки трихлорацетил изоцианатом (TAI).
111 г продукта смешивали с 3 г н-бутанола при 60 °С и перемешивали в течение 1 часа. Фазу продукта трижды экстрагировали соответственно 30 мл метанола, метанольные фазы каждый раз отделяли и отбрасывали. Фазу продукта концентрировали в вакууме. Содержание метакриловой кислоты составляло 1 мас.%, ангидрид метакриловой кислоты больше не обнаруживался (определено с помощью 1H ЯМР).
Пример 4
Взаимодействие проводили в четырехгорлой круглодонной колбе объемом 500 мл с обогревом масляной баней, термометром, обратным холодильником, подводом воздуха и тефлоновой мешалкой типа "полумесяц". 145 г прогретого до 60 °С моноэтоксилированного фенола, содержащего полиизобутеновый остаток, (полученного с 2-метилимидазолом в качестве катализатора в соответствии с примером 9) и 33 мг трет-бутилгидрокситолуола смешали при температуре бани 80 °С. При пропускании воздуха (около 0,3 л/ч) и температуре бани 95 °С добавили 19,7 г ангидрида метакриловой кислоты (94%-ного, стабилизированного при помощи Topanol® А). Через 2,75 часа добавили 80 мг NaOH и повысили температуру бани до 100 °С. Через суммарно 5,5 часов останавливали реакцию и выгружали теплый (80°C) продукт.
Из продукта в вакууме до 2,2 мбар при 80 °С удаляли дистилляцией метакриловую кислоту. Образец все еще содержал 2,3 % мас. метакриловой кислоты (определено с помощью ЯМР). Был получен приблизительно 50%-ный раствор в толуоле. С помощью 32%-ного водного раствора NaOH рН раствора доводили до > 12 и перемешивали в течение 2 ч при комнатной температуре. Добавляли 10 г Bentonit® и 10 г Hyflo Super Cel®. Затем отфильтровывали через фильтр, работающий под давлением, при макс. 2 бар и продукт концентрировали в вакууме. Конверсию определяли как > 95 % с помощью ЯМР после обработки трихлорацетил изоцианатом (TAI). Содержание метакриловой кислоты составляло < 0,25 мас.%, ангидрид метакриловой кислоты больше не обнаруживался (определено с помощью ЯМР).
Пример 5
Взаимодействие с этиленкарбонатом проводили при пропускании азота (около 0,3 л/ч) в реакторе с двойными стенками объемом 750 мл, снабженном якорной мешалкой, вводом для газа, разделительной колонной и распределителем жидкости. В данном аппарате смешивали 230,2 г содержащего полиизобутеновый остаток с молекулярной массой 1000 фенола, полученного аналогично примеру А, 21,9 г этиленкарбоната, а также 4,1 г фосфата калия и нагревали при температуре бани 177-180 °С, при этом выделялся CO2. Внутренняя температура составляла 169-170 °С. Через 7,5 часов смесь охлаждали до 60 °С. Добавляли 500 г метилметакрилата и 0,1 г MEHQ. Реакционную смесь нагревали при пропускании воздуха (0,3 л/ч) и температуре бани, составляющей 115 °С. Устанавливали давление в 600 мбар (абс.) и непрерывно удаляли дистилляцией азеотроп из метанола и метилметакрилата, при этом устанавливали температуру в кубе от 84 до 87 °С. Дистилляты собирали и анализировали на содержание метанола. После окончания реакции продукт отфильтровывали через фильтр, работающий под давлением, при макс. 2 бар и реакционную смесь концентрировали в вакууме. Конверсию определяли как > 99 % с помощью ЯМР после обработки трихлорацетил изоцианатом (TAI).
Пример 6
Переэтерификацию проводили при пропускании воздуха в реакторе с двойными стенками объемом 750 мл, снабженном якорной мешалкой, вводом для воздуха, разделительной колонной и распределителем жидкости. В данном аппарате 990 г 29,3%-ного раствора моноэтоксилированного фенола, содержащего полиизобутеновый остаток, в соответствии с примером 9 (полученного с 2-метилимидазолом в качестве катализатора), помещали в метилметакрилат. Добавляли 0,495 г метилгидрохинона (MEHQ) и при пропускании воздуха, температуре бани 95 °С и вакууме при абс. 300 мбар отделяли дистилляцией 150 мл метилметакрилата.
Добавляли 150 мл метилметакрилата и реакционную смесь нагревали при пропускании воздуха (0,3 л/ч) и атмосферном давлении и при температуре бани 120 °С. Добавляли 2,3 г тетраизопропилтитаната и при температуре бани 125 °С и вакууме в абс. 700 мбар непрерывно удаляли дистилляцией азеотроп из метанола и метилметакрилата, при этом устанавливали температуру в кубе 98 °С.
После завершения реакции анализировали реакционную смесь. Конверсию определяли как 14 % с помощью ЯМР после обработки трихлорацетил изоцианатом (TAI).
Пример 7
Взаимодействие проводили в четырехгорлой круглодонной колбе объемом 500 мл с обогревом масляной баней, термометром, обратным холодильником, насадкой Дина-Старка, подводом воздуха и тефлоновой мешалкой типа "полумесяц". 145 г прогретого до 60 °С моноэтоксилированного фенола, содержащего полиизобутеновый остаток, в соответствии с примером 9 (полученного с 2-метилимидазолом в качестве катализатора), 100 г толуола, 10,3 г метакриловой кислоты (стабилизированной 200 ч.н.млн MEHQ), 0,76 г моногидрата п-толуолсульфоновой кислоты, а также 49 мг MEHQ смешивали при температуре бани 80 °C. Реакционную смесь нагревали. При температуре бани 127 °С смесь начала кипеть. В ходе реакции температуру бани повышали до 140 °С. Добавляли еще 1,17 г моногидрата п-толуолсульфоновой кислоты. После общего времени реакции 4,5 часа не образовывалось существенных количеств воды (около 0,2 мл воды). Реакционную смесь охлаждали и затем при температуре куба 95 °С добавляли 7,7 г метансульфоновой кислоты, а также дополнительные 5,1 г метакриловой кислоты. Температуру бани вновь устанавливали на 140 °С. В течение следующих 3 часов реакции из системы было удалено в общей сложности 72% ожидаемого количества воды, и в течение следующего часа (таким образом суммарное время реакции 8,5 часов) вода больше не образовывалась. Реакцию останавливали.
Пример 9
Содержащий полиизобутеновый остаток фенол, полученный аналогично примеру А (1 экв.) и этиленкарбонат (1,1 экв.) смешивали в атмосфере азота и нагревался до 100 °С. Добавляли 2-метилимидазол (0,6%мас.) и реакционную смесь медленно нагревали до 150 °С в течение 5 часов, до тех пор пока не прекращалось выделение газа. При 140 °С наблюдалось изменение окраски реакционной смеси от светло желтого до коричневого/черного. Конверсию определяли с помощью1H-ЯМР-спектроскопии.
Пример 11
Содержащий полиизобутеновый остаток фенол, полученный аналогично примеру А (1 экв.) и этиленкарбонат (1,3 экв.) смешивали в атмосфере азота и нагревали до 170 °С. Добавляли фосфат калия (1,46 мас.%) и реакционную смесь перемешивали в течение 6 часов, до тех пор пока не прекращалось выделение газа. Изменения окраски не наблюдалось. Конверсию определяли с помощью 1H-ЯМР-спектроскопии.
Пример 12
Содержащий полиизобутеновый остаток фенол, полученный аналогично примеру В (1 экв.) и этиленкарбонат (1,3 экв.) смешивали в атмосфере азота и нагревали до 110 °С. Добавляли фосфат калия (1,46 мас.%) и реакционную смесь перемешивали в течение 48 часов при 120-170 °C в условиях вакуума.
Конверсию определяли с помощью1H-ЯМР-спектроскопии.
Пример 13
Переэтерификацию проводили при пропускании обедненного воздуха в 4 л-реакторе с двойными стенками, снабженном многоступенчатой лопастной мешалкой, вводом для обедненного воздуха, разделительной колонной и распределителем жидкости. В данном аппарате раствор из 450 г моноэтоксилированного фенола, содержащего полиизобутеновый остаток, в соответствии с примером 12, помещали в 1500 г метилметакрилата. Добавляли 0,13 г метилгидрохинона (MEHQ) и 10,5 г фосфата калия и реакционную смесь нагревали при пропускании обедненного воздуха (0,5 л/ч) при температуре бани, первоначально составляющей 115 °С. Устанавливали давление в 600 мбар (абс.) и непрерывно удаляли дистилляцией азеотроп из метанола и метилметакрилата, при этом устанавливали температуру в кубе 84 °С. Коэффициент орошения (флегмовое число) составлял 20 : 1 (возврат флегмы : отвод). В ходе реакции температуру бани снижали до 110 °С. После окончания реакции реакционную смесь отфильтровывали через фильтр, работающий под давлением, при макс. 2 бар и концентрировали в вакууме при 75°C. Было получено 449 г продукта. Конверсию определяли как > 99% с помощью ЯМР после обработки трихлорацетил изоцианатом (TAI).
Гомополимеризации
Полимеризация в растворе:
Пример полимеризации 1:
Полимеризацию проводили под слабым потоком азота в сосуде объемом 4 л с двойными стенками и контуром нагрева, циркуляционным насосом, перемешивающим устройством марки Pilot, длинным высокоэффективным холодильником, якорной мешалкой и перемешивающим мотором. 98,17 г продукта из примера 3 помещали в 391,32 г орто-ксилола и нагревали до 80 °С. При внутренней температуре 79 °С в течение 3 часов добавляли 0,26 г трет-бутилперпивалата (75%-ный) в 19,63 г орто-ксилола. Затем смесь в течение 15 минут нагревали до 90 °С, и в течение 30 минут дозировали 0,18 г трет-бутилпероктоата в 19,63 г орто-ксилола. Конверсию определяли как 55% с помощью 1H-ЯМР. Mw 27 700 г/моль (PDI = 12,4) определяли с помощью гель-проникающей хроматографии с рефрактометрическим детектором (RI) и Mw 25000 г/моль с помощью гель-проникающей хроматографии с проточный многоугловым фотометром (MALLS).
Миниэмульсионная полимеризация:
Пример полимеризации 2:
21,5 г продукта из примера 3 сначала растворяли в 31,5 г гексана.
В сосуде объемом 250 мл предварительно смешали 70,88 г воды и 3,68 г Disponil® FES 27, и медленно добавили раствор макромономера. Полученную при этом предварительную эмульсию далее эмульгировали в течение 50 минут при интенсивном перемешивании. Затем предварительную эмульсию обрабатывали ультразвуком в течение 2 мин на самой высокой ступени ультразвуковым зондом при 400 Вт и 24 кГц. При этом эмульсию охлаждали. Миниэмульсию помещали в перемешивающее устройство объемом 250 мл и инертизировали потоком азота при 150 об/мин в течение 10 минут. Внутреннюю температуру доводили до 70 °С и добавляли 2,15 г 10%-ного раствора трет-бутилгидропероксида. Затем дозировали 17,2 г 2%-ного раствора ацетон-бисульфита натрия с временем подачи 3 часа. Молекулярную массу (Mw) полученной дисперсии определяли с помощью ГПХ (рефрактометрический детектор) как 293000 г/моль и ГПХ (УФ 275 нм) как 326000 г/моль. Молекулярную массу (Mn) полученной дисперсии определяли с помощью ГПХ (рефрактометрический детектор) как 5720 г/моль и ГПХ (УФ 275 нм) как 6590 г/моль. Низкие значения Mn обусловлены остаточными мономерами.
Сополимеры
Пример полимеризации 3:
30 г продукта из примера 3 и 30 г метилметакрилата помещали в 207 г толуола и нагревали до 80 °С. 5% раствора 4 г трет-бутилперпивалата (75%-ного) в 37,33 г толуола добавляли в течение одной минуты и перемешивали в течение 10 минут при 80 °C (150 об/мин) перед тем, как добавляли оставшиеся 95% раствора в течение 4,5 часов. После завершения дозирования перемешивали еще в течение 1,5 часов при 80 °С.
Пример полимеризации 4:
45 г продукта из примера 3 и 15 г метилметакрилата помещали в 207 г толуола и нагревали до 80 °С. 5% раствора 4 г трет-бутилперпивалата (75%-ного) в 37,33 г толуола добавляли в течение одной минуты и перемешивали в течение 10 минут при 80 °C (150 об/мин) перед тем, как добавляли оставшиеся 95% раствора в течение 4,5 часов. После завершения дозирования перемешивали еще в течение 1,5 часов при 80 °С.
Реферат
Изобретение относится к новым соединениям (А) формулы (I), а также к полимеру, содержащему в заполимеризованной форме по меньшей мере одно соединение (А) формулы (I). Технический результат: получены новые соединения, которые являются более легкодоступными и стабильными в условиях полимеризации и имеют более низкое содержание галогена. 4 н. и 9 з.п. ф-лы, 17 пр.формула (I)
Формула


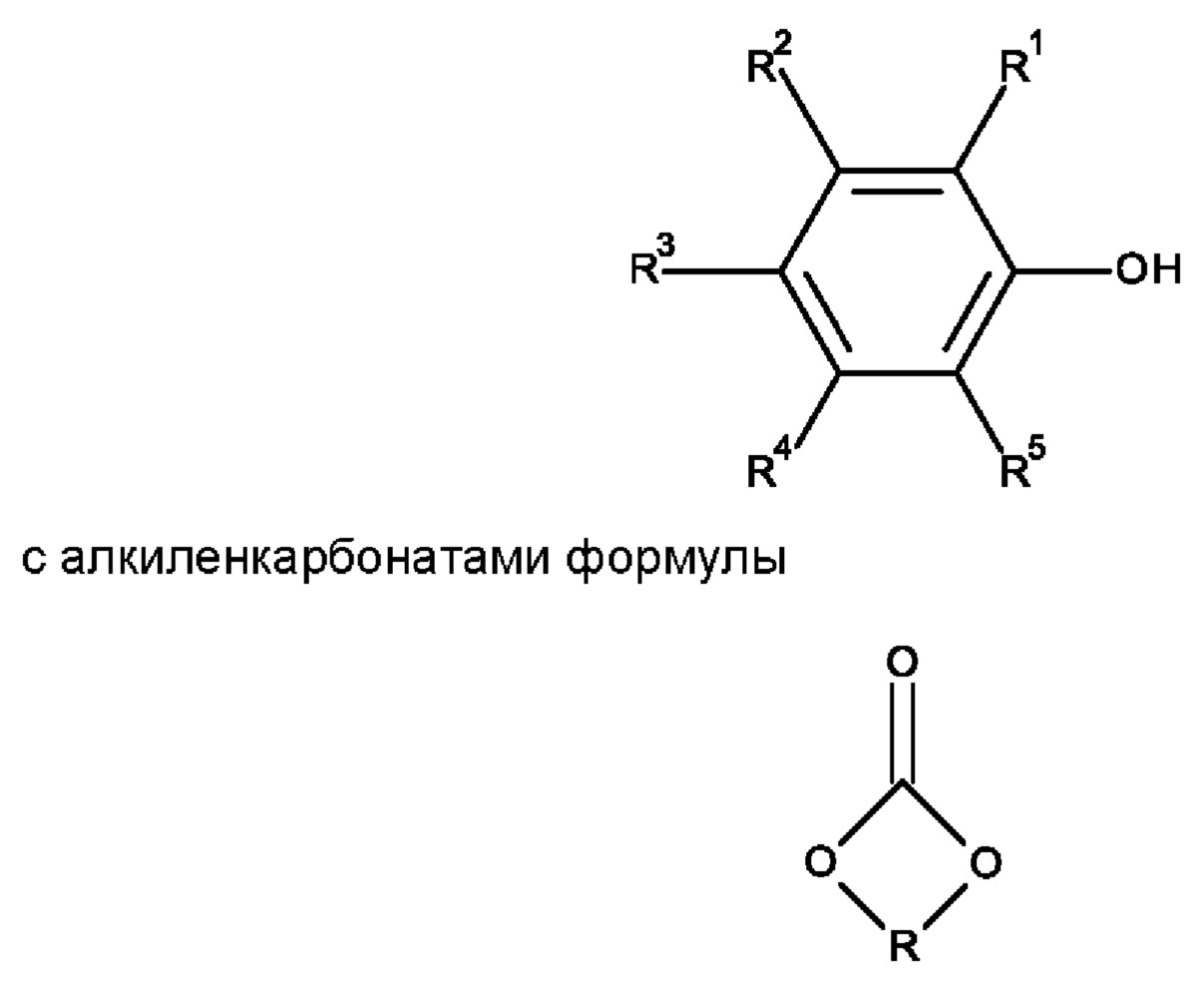
Документы, цитированные в отчёте о поиске
Полиалкил(мет)акрилат для улучшения свойств смазочного масла

Комментарии