Композиции, излучающие позитроны и содержащие неорганические частицы, и их применение в медицине, в частности для диагностических процедур - RU2461392C2
Код документа: RU2461392C2
Чертежи




Описание
Более чем из 50 известных источников излучения позитронов лишь немногие могут быть использованы в медицине. В настоящее время наиболее важными PET нуклидами (нуклидами для позитронно-эмиссионной томографии) являются [18]F, [11]C, [13]N и [15]O. Они отличаются чрезвычайно коротким периодом полураспада, который находится в пределах приблизительно от 110 минут для [18]F вплоть до 2 мин для [15]O.
Действительно, эти короткие периоды полураспада являются причиной огромных потребностей, касающихся обеспечения этих субстанций и оценки измерений, но все же приносят пациенту преимущество слабого воздействия излучения вследствие очень короткого времени экспозиции.
Дополнительным преимуществом этих PET нуклидов является то, что в принципе с их помощью можно радиоактивно пометить любую органическую молекулу. Каждая органическая молекула имеет один или более атомов углерода (как правило: [12]С), один из которых можно заменить на [11]С; более того, многие органические молекулы содержат атом кислорода или азота.
Несмотря на то, что фтор встречается относительно редко в природных и синтетических соединениях, тем не менее он может быть относительно легко включен в органические молекулы заменой атомов водорода или гидроксильных групп. Так как сравнительно длинный период полураспада [18]F облегчает получение и использование [18]F-меченых радиофармацевтических средств, он и является PET нуклидом, который используется наиболее часто.
Таким образом, все вышеупомянутые соединения, которые являются эндогенными относительно тела, такие как углеводороды, аминокислоты, ферменты, гормоны или нейромедиаторы, а также другие фармацевтические средства, могут быть помечены источниками излучения позитронов без существенного изменения их структуры и, таким образом, их биохимических и фармакологических свойств. Абсолютные количества введенных меченых субстанций являются такими низкими (в микромолярных пределах), что не влияют на физиологические концентрации.
Получение источников излучения позитронов
Так как все источники излучения позитронов, применимые с медицинской точки зрения, имеют чрезвычайно короткие периоды полураспада, их нельзя держать в запасе, а нужно приготавливать отдельно на месте. Поскольку для этого необходим ускоритель элементарных частиц (часто циклотрон), существует всего только несколько PET центров, обычно в наиболее крупных университетских клиниках.
Так называемая целевая реакция объясняется на примере получения ионов [18]F. При этом ускоренный протон в мишени сталкивается с [18]О атомом [18]O-обогащенной воды. Атом фтора [18]F образуется с эмиссией нейтрона:
18/8O+p→18/9F=n
Он заряжен отрицательно и выходит как водный [18]F-фторсодержащий раствор.
[18]Фтор без сомнения играет наибольшую роль в приготовлении PET радиофармацевтических средств. [18]F также является единственным источником излучения позитронов, который в известной мере можно транспортировать из PET центра с циклотроном до другого устройства, используемого в ядерной медицине.
В этом контексте радиофармацевтическое средство может быть доставлено как готовое для введения или также как радиационный продукт (как правило [18]-фторид), так что фактический радиохимический синтез затем проводят на месте.
Источники излучения позитронов [11]С, [13]N и [15]O могут быть изготовлены только для непосредственного применения в PET центрах вследствие короткого периода полураспада.
Радиохимический синтез
В небольшом количестве случаев радионуклид в такой форме, как он образуется в мишени циклотрона, уже является радиоактивным медикаментом. Следовательно, затем его можно включить в органохимическое соединение (структура из органической химии, в отличие от неорганической химии).
Тогда как изотоп технеция Тс-99m, используемый в сцинтиграфии (гамма-томографии), обычно связывается в виде комплекса на рецептор-специфической несущей субстанции, PET нуклиды объединены в радиофармацевтическое средство посредством ковалентной связи.
Для этого необходим химический синтез, который не отличается от обычных реакций препаративной химии, так как радиоактивные элементы и вещества имеют те же самые химические свойства, как их нерадиоактивные аналоги.
Однако, так как доза излучения, выпущенная исходными активностями, как правило, гораздо выше допустимых предельных значений, почти все обычным образом приготовленные PET радиофармацевтические средства готовят не вручную, а посредством отдаленного контроля с помощью модулей автоматического синтеза или с помощью роботов.
Фактически принцип работы всех модулей автоматического синтеза является всегда одинаковым. Модули синтеза дают возможность жидкостям перемещаться из одного сосуда в другой и позволяют помешивать их, нагревать, охлаждать, концентрировать, экстрагировать, (стерилизовать-) фильтровать и переносить в контейнеры.
Процедуры промывки и очистки, необходимые после синтеза, также должны происходить автоматически, где, возможно, и должны быть быстро и легко выполнимы, так что повторный (возобновленный) синтез может возобновляться в аппарате в течение короткого промежутка времени.
Наконец, часто является необходимой очистка продукта с помощью (также автоматической) препаративной ВЭЖХ (высокоэффективной жидкостной хроматографии). В конце концов, водный раствор радиофармацевтического средства приводят в состояние изотонического посредством добавления соответствующего количества хлорида натрия (раствор) и вводят в сосуд для доставки через стерильный фильтр.
Наиболее важные PET радиофармацевтические средства включают:
- [11]С-метионин, как важный маркер в метаболизме аминокислот,
- 1-[11]С-ацетат для диагностики болезней сердца,
- [15]O-меченая вода для диагностики нарушений кровообращения и
- [18]F-фтор-DOPA для ранней диагностики болезни Паркинсона и других допаминэргических расстройств,
- [18]F-2-фтор-2-дезоксиглюкоза (ФДГ) без сомнения является наиболее важным PET радиофармацевтическим средством, которое используют прежде всего в диагностике онкологических заболеваний, но также в других областях (см. ниже).
Более того, важной чертой всех радиофармацевтических средств, в частности PET радиофармацевтических средств, используемых в диагностике человека, является то, что все субстанции (вещества) имеют только одну метку в составе диагностически активного нуклида. Каждая молекула может соответственно излучать самое большее один диагностически пригодный сигнал.
Диагностика в ядерной медицине
Предварительным условием всех исследований в ядерной медицине является введение радиоактивной субстанции, радиофармацевтического средства, в тело человека. Обычно его вводят внутривенно, и сначала оно распределяется в крови более или менее однородно по всему организму.
По причине биологического функционирования радиофармацевтического средства или его специфического сродства к определенным субстанциям и рецепторам, происходит неоднородное перераспределение, которое может быть измерено с помощью внешних детекторов или томографов на основе радиоактивного излучения и обеспечит заключения о функциональном состоянии исследуемых органов и областей тела.
Диагностика опухолей с помощью ФДГ-РЕТ
Наиболее часто используемым PET радиофармацевтическим средством является [18]F-2-фтор-2-дезоксиглюкоза, обычно сокращенно ФДГ. Она представляет собой молекулу глюкозы, которая несет радиоактивный атом [18]F вместо ОН групп на С2. После внутривенного введения она больше всего накапливается в клетках с повышенной потребностью в глюкозе.
Организм фактически не различает "нормальную" глюкозу и [18]F-меченую фтордезоксиглюкозу. Так как в опухолевых клетках некоторых типов опухолей преобладает повышенный обмен веществ, они поглощают больше глюкозы или ФДГ, чем неперерожденные клетки, так что ФДГ-РЕТ может определить местонахождение опухолей.
Однако необычная концентрация радиоактивной глюкозы не всегда указывает на раковый процесс. Например, ФДГ крайне неспецифическим образом накапливается в мозге, что, с одной стороны, делает трудным исследование неврологических проблем, а также дает в результате значительное воздействие радиации на ткань мозга.
Кроме того, диагностика с помощью ФДГ-РЕТ является успешной только в случае опухолей с повышенным потреблением глюкозы, и следовательно, исключает определение местоположения медленно растущих опухолей.
Измерительная техника
Дальность полета излученного позитрона в ткани составляет самое большее всего несколько миллиметров до того, как он встретится с электроном и превратится в два γ-кванта, вылетающих в диаметрально противоположных направлениях. Полный процесс от излучения позитрона до превращения массы в два γ-кванта занимает около 10-10 секунд (0,1 нсек).
Для обнаружения γ-кванта при PET используют детектор совпадений или парный детектор. Если каждый из двух отдельных детекторов, помещенных под углом 180°, регистрирует γ-квант определенной энергии в течение очень короткого промежутка времени около 10 нсек, делается заключение, что распад позитрона происходит где-то в соединительной зоне между двумя детекторами.
В дополнение к ограничениям в области технической разработки детектора, действительный предел разрешения определяется средней длиной свободного пути позитрона в ближайшей среде (ткани, тканевой жидкости, крови и т.д.). Если электронная плотность в окрестности позитронного распада может быть увеличена, вероятность взаимодействия позитрона с электроном увеличивается. Следовательно, средняя длина свободного пути укорачивается, и предел разрешения может быть улучшен до более низких величин.
Суммируя, предшествующий уровень имеет в частности следующие преимущества и ограничения.
Предшествующий уровень техники описывает только диагностические средства из множества веществ органической химии. Для приготовления органических веществ необходим отнимающий много времени, часто многостадийный синтез и стадии очистки, а это значит, что по причине небольшого периода полураспада нуклидов относительный выход диагностически активного продукта становится более низким с увеличением времени приготовления. ФДГ, PET диагностическое средство, используемое в большинстве случаев, кроме того, накапливается крайне неспецифическим образом в мозге, что с одной стороны делает трудным исследование неврологических проблем, а также дает в результате значительное воздействие радиации на ткань мозга. Кроме того, PET диагностика с помощью ФДГ является успешной только в случае опухолей с повышенным потреблением глюкозы, и следовательно, жестко ограничивает определение местоположения медленно растущих опухолей. Так как радиофармацевтические средства, используемые согласно предшествующему уровню техники в диагностике человека, в частности PET радиофармацевтические средства, имеют только одну метку в составе диагностически активного нуклида, каждая молекула может соответственно излучать самое большее один диагностически пригодный сигнал. Более того, органические PET радиофармацевтические средства имеют сходную электронную плотность с окружающей тканью. Следовательно, пространственная разрешающая способность не может быть улучшена.
Следовательно, целью, на которой основано настоящее изобретение, было предоставление новых пригодных с медицинской точки зрения, в частности для диагностики, средств, которые лишены недостатков предшествующего уровня техники, описанных выше.
Следовательно, предметом настоящего изобретения является фармацевтическое средство, содержащее неорганический матрикс в виде частиц (твердый неорганический матрикс), который в дополнение к природному распределению изотопов структурных тип-образующих элементов анионов и катионов содержит долю (часть) позитрон-излучающих нуклидов, в которой число позитрон-излучающих нуклидов на неорганический матрикс в виде частиц предпочтительно составляет больше чем или равно 1.
Возможные структурные типы неорганического матрикса в виде частиц могут включать и кристаллические структуры и аморфные структуры или смеси из этих двух. Термин включает как коллоиды, соли, суспензии, наносуспензии, так и аморфные и кристаллические частицы.
Предпочтительно, число пригодных с медицинской точки зрения, в частности диагностически пригодных, позитрон-излучающих нуклидов на неорганический матрикс в виде частиц составляет от 1 до 10000000 и особенно предпочтительно от 5 до 1000000, и наиболее предпочтительно от 10 до 100000.
Частицы (в нижеследующем также в общем смысле неорганический матрикс в виде частиц) согласно изобретению состоят в основном (см. также определение структурных типов) из неорганических соединений, которые являются плохо растворимыми в воде и физиологических жидкостях, например, таких как топаз, (Al2F2)[SiO4], и хиолит, Na[Al3F4], предпочтительно вавеллит, Al3(PO4)2(ОН, F)2, карбонат кальция, СаСО3, маггемит, γ-Fe2O3, особенно предпочтительно цеолиты, общая формула Mn[(AlO2)x(SiO2)y] (М = металл, например, Na), магнетит, Fe3O4, и сульфат бария, BaSO4, и наиболее предпочтительно фосфат галлия, GaPO4, апатит или фторгидроапатит, Са5(PO4)3(ОН,F)=3Са3(PO4)2*Са(ОН, F)2, и флюорит CaF2.
Позитрон-излучающие нуклиды предпочтительно выбирают из группы, содержащей [15]O, [30]Р, [13]N, [65]Ga, [11]С, [131]Ва, [26]Al и [68]Ga и [18]F. Таким образом, пригодными с медицинской точки зрения, в частности диагностически пригодными нуклидами, для частиц согласно изобретению являются [15]O, [30]Р, [13]N, предпочтительно [65]Ga, [11]C, особенно предпочтительно [131]Ва, [26]Al и наиболее предпочтительно [68]Ga или [18]F. Более того, все пригодные с медицинской точки зрения изотопы, известные специалистам в данной области техники, можно использовать для приготовления частиц согласно изобретению. Выделение некоторых изотопов можно найти в таблице 1.
Диаметр частиц согласно изобретению может находиться в пределах от 0,1 нм до 100 мкм, предпочтительно от 1 нм до 10 мкм, особенно предпочтительно от 1 нм до 1 мкм.
В предпочтительном варианте осуществления фармацевтического средства согласно изобретению частицы согласно изобретению находятся в фармацевтической оболочке. Согласно изобретению оболочку выбирают из группы, содержащей: синтетический полимер или сополимер, крахмал или его производное, декстран или его производное, циклодекстран или его производное, жирную кислоту, полисахарид, лецитин или моно-, ди- или триглицерид или его производное, или их смеси.
Синтетический полимер или сополимер можно выбрать из группы, содержащей сложные эфиры полиоксиэтиленсорбитана, полиоксиэтилы и их производные, полиоксипропилы и их производные, неионные поверхностно-активные вещества, полиоксистеараты (35-80), поливиниловые спирты, полимеризованную сахарозу, полигидроксиалкилметакриламиды, сополимеры молочной кислоты и гликолевой кислоты, сложные полиортоэфиры, полиалкилцианоакрилаты, полиэтиленгликоль, полипропиленгликоль, полиглицерины, полигидроксилированные поливиниловые матриксы, полигидроксиэтиласпартамиды, полиаминокислоты, сополимеры стирола и малеиновой кислоты, поликапролактоны, карбоксиполисахариды и полиангидриды.
Производные крахмала можно выбрать из группы, состоящей из 2-гидроксиметилового эфира крахмала и гидроксиэтил-крахмала.
Декстран и его производные можно выбрать из группы, содержащей галактозилированный декстрап, лактозилированный декстран, аминированный декстран, декстран с группами SH, декстран с карбоксильными группами, декстран с альдегидными группами и биотинилированный декстран.
Циклодекстрин можно выбрать из группы, содержащей бета-циклодекстрин и гидроксипропилциклодекстрин.
Жирная кислота может быть выбрана из группы, содержащей лаурилсульфат натрия, стеарат натрия, стеариновую кислоту, сорбитмонолаурат, сорбитмоноолеаты, сорбитмонопальмитат и сорбитмоностеарат.
В другом предпочтительном варианте осуществления фармацевтического средства согласно изобретению неорганические частицы соединены с мишень-специфическими лигандами. Лиганд можно выбрать из группы, состоящей из протеинов, антител, фрагментов антител, пептидов, аптамеров, дарпинов и других молекул, которые имеют высокое сродство к болезнь-специфическим рецепторам. Подходящие молекулы с рецепторным сродством известны специалистам в данной области техники.
Три представленных схематически типа структур или вариантов осуществления частиц согласно изобретению описаны здесь (см. фигуры 1 и 2):
Описание фигур 1 и 2
Фигура 1, Тип 1 описывает частицы согласно изобретению из группы плохо растворимых неорганических соединений (С), описанных выше, которые не содержат стабилизатор и ингибируются коагуляцией. При этом молекулы адсорбированной воды или/и электрический заряд на поверхности частицы способствуют повышению стабилизации частиц (системы также названы sol).
Фигура 1, Тип 2 - частицы согласно изобретению, которые являются устойчивыми к агрегации с поверхностно-активными молекулами. В дополнение к обычным стабилизаторам, которые можно вводить внутривенно (вв.), таким как, например, полоксамеры, также можно использовать блоксополимеры со специально заданными свойствами. Это включает, например, так называемые двойные гидрофильные А-блок-В сополимеры, из которых блок А имеет координирующие/стабилизирующие способности, а второй блок В защищает частицы от агрегации и часто состоит из полиэтиленгликоля (PEG).
Более того, частицы согласно изобретению могут быть покрыты дополнительными материалами, например обычными материалами для покрытия, такими как углеводороды, полиэтиленгликоли, полиакриловые или метакриловые кислоты, жирные кислоты, двуокись кремния или/и силан и т.д.
Фигура 1, Тип 3 показывает дополнительный вариант осуществления частиц согласно изобретению с мишень-специфической структурой частиц, которые получают дополнительным соединением специфических лигандов. Эти лиганды могут быть например, антителами, их фрагментами, пептидами, аптамерами, дарпинами или другими небольшими молекулами, которые имеют высокое сродство к болезнь-специфическим рецепторам. Лиганды могут быть или соединены посредством химической модификации веществ, используемых для стабилизации, или закреплены непосредственно на частице согласно изобретению.
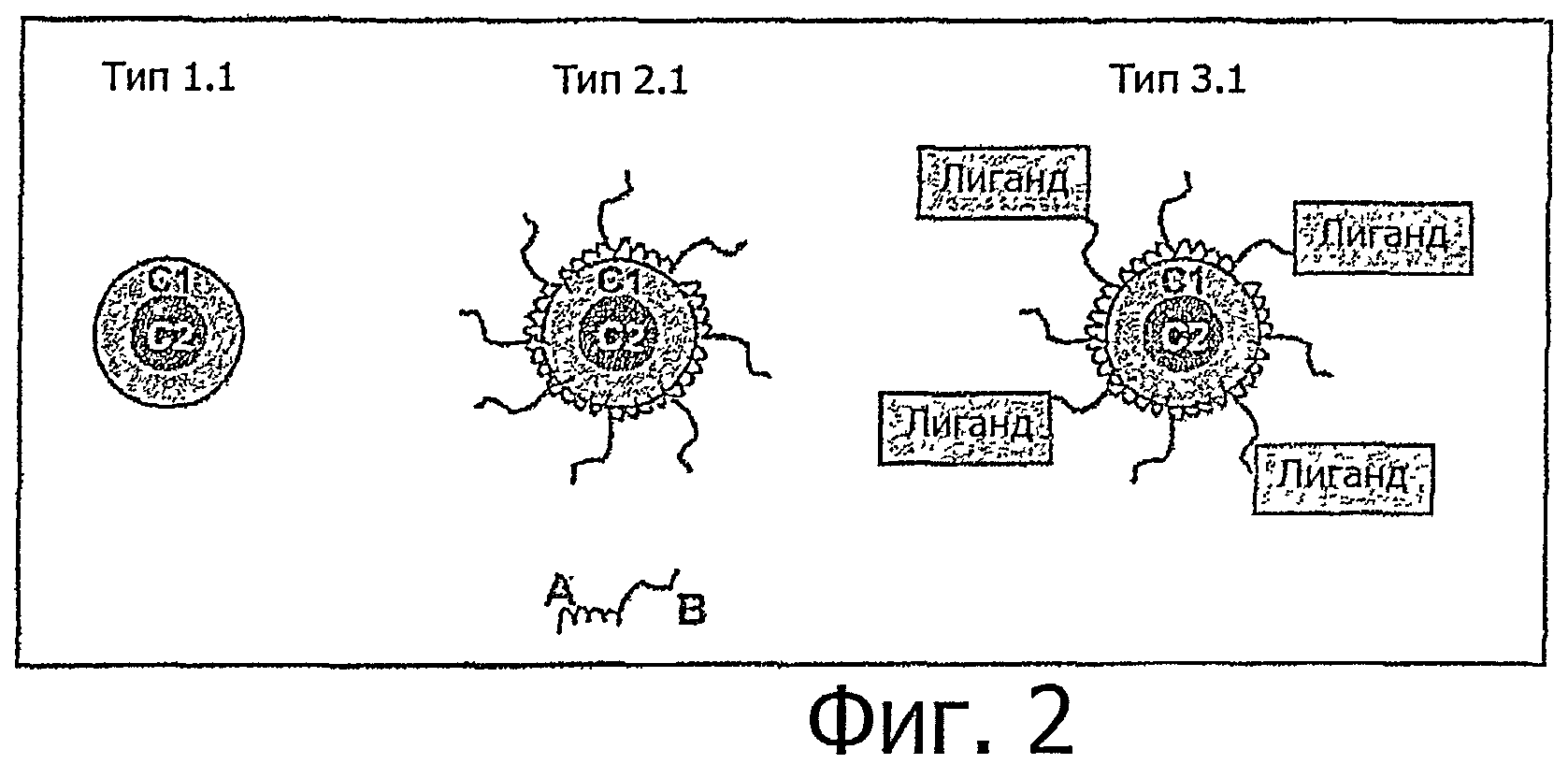
Кроме того, внутренняя часть (ядро, сердцевина) частиц согласно изобретению может состоять из двух различных материалов (структура ядро-оболочка; фигура 2, Тип 1.1, 2.1, 3.1). В этом контексте, в предпочтительном варианте осуществления внутренняя часть С2 (или внешняя С1) может состоять из дополнительного диагностически пригодного средства. Например, магнетиты (такие как Resovist или Supravist, Sobering AG Германия) можно использовать как зерна нуклеации, а плохо растворимые неорганические соединения, описанные выше, можно осадить на или нанести на них.
В дополнительном варианте осуществления оболочка частиц согласно изобретению типа 1.1, 2.1 и 3.1 может состоять из любой фармацевтически приемлемой оболочки.
Предметом настоящего изобретения также является фармацевтически приемлемая композиция, в которой по меньшей мере 0,001% частиц, содержащихся в композиции, являются частицами согласно изобретению. Иначе говоря, при определенных обстоятельствах низкое содержание частиц, содержащихся в фармацевтическом средстве согласно изобретению в фармацевтически пригодной композиции, уже является достаточным, чтобы сделать эту композицию диагностически или терапевтически годной к применению.
Если частицы согласно изобретению сравнить с ФДГ (известный уровень техники на рынке PET индикаторов), можно описать преимущества, получаемые непосредственно от твердого характера частиц согласно изобретению.
1. Простое получение: В противоположность ФДГ для приготовления неорганических наночастиц не требуется стадий органического синтеза и очистки. Неорганические PET индикаторы в виде частиц согласно изобретению формируются спонтанно при комнатной температуре. Например, это осуществляется добавлением изотопа, например, [18]F, к гидроксиапатиту и смешиванием продуктов, предварительно собранных в так называемый "холодный набор". Центр распределения или опытный практик в области ядерной медицины таким образом бережет ресурсы.
"Холодный набор" здесь означает, что первоначально неорганический матрикс в виде частиц является свободным от радиоактивных частиц. Затем непосредственно перед применением фармацевтического лекарственного средства вводят радиоактивные ионы путем добавления соответствующих радиоактивных нуклидов в ионной форме, причем радиоактивные ионы занимают пространственные решетки в неорганическом матриксе в реакции замещения без возбуждения структуры сверхрешетки неорганического матрикса.
2. Короткое время приготовления: Время приготовления композиции частиц согласно изобретению ниже, по меньшей мере, в 10 раз, чем время, необходимое для синтеза и очистки ФДГ одинаковой активности, т.е. более активный продукт доставляется заказчику в тот же срок. Время приготовления наночастиц определяется скоростью осаждения неорганического матрикса и составляет обычно меньше, чем 5 мин, предпочтительно меньше, чем 1 мин, более предпочтительно меньше, чем 10 сек. Например, частицы фторида кальция образуются спонтанно в течение одной секунды после смешивания водных растворов хлорида кальция и фторида натрия согласно уравнению реакции осаждения.
3. Более длительная пригодность к использованию: Период полураспада изотопов, например [18]F, является действительно природной константой (t1/2 приблизит. 110 мин), но частица согласно изобретению в диагностически пригодной композиции может содержать до нескольких сотен тысяч атомов [18]F, в зависимости от размера частиц, что регулируется с помощью процесса приготовления. Это означает, что каждая фармакологически активная частица также является активной при получении PET изображения в сотни тысяч раз дольше, чем отдельно [18]F-меченый индикатор. Это представляет коммерческий интерес, в частности, если используются коньюгаты 1:1 дорогостоящих биомолекул, таких, как антитела и PET изотопы. Клетки, меченые таким способом, также можно контролировать в организме в течение более длительного времени с помощью PET визуализации.
4. Пассивное нацеливание: Здоровые кровеносные сосуды имеют замкнутый эндотелий. Они являются непроницаемыми и задерживают большие молекулы, такие как, например, альбумин, или также наночастицы, от движения обратно в кровообращение. Эндотелий кровеносных сосудов в опухолях имеет отверстия, и через них небольшие частицы согласно изобретению легко могут диффундировать из кровообращения в ткань. Более того, так как транспортировка лимфы уменьшена в опухолевой ткани, частицы согласно изобретению накапливаются в опухоли, исключительно вследствие правильной наноразмерной величины.
5. Специфичность: Наночастицы пригодны для нацеливания, связанного с клетками, т.е. частицы главным образом поглощаются клетками ретикулоэндотелиальной системы (RES), в зависимости от их размера и структуры поверхности и заряда. В этом контексте макрофаги, циркулирующие в крови, могут быть помечены непосредственно частицами согласно изобретению после инъекции композиции. Это делает возможным визуализацию, например, воспалительных процессов, которые всегда сопровождаются повышенной активностью макрофагов.
6. Основание для молекулярной визуализации: В дополнение к возможностям пассивного и связанного с клетками нацеливания, частицы согласно изобретению предлагают дополнительную нацеленную адресацию неорганических частиц. Посредством соединения болезнь-специфических лигандов с поверхностью частиц согласно изобретению, становится возможным активное нацеливание на рецепторы, например, на клеточных поверхностях.
7. Низкое воздействие излучения на мозг: В противоположность ФДГ (предшествующий уровень техники) частицы согласно изобретению не накапливаются неспецифически в мозге. С одной стороны, это уменьшает экспозицию мозга к излучению, а с другой стороны, возможно изучение неврологических проблем.
8. Обнаружение очень маленьких очагов: Наряду с дополнительными факторами, пространственное разрешение PET визуализации зависит по существу от средней длины свободного пути позитронов в ткани (например, приблизительно 3 мм в случае позитронов от [18]F). Так как, например, изотоп [18]F ФДГ распадается свободно в ткани, разрешение не может быть ниже этого физического предела. В противоположность этому, изотопы частиц согласно изобретению плотно заключены в кристаллическую решетку. Это увеличивает вероятность взаимодействия позитронов с электронами и уменьшает среднюю продолжительность свободного пути. Может быть достигнуто улучшение в пространственной разрешающей способности PET. Следовательно, возможно разрешение, при котором можно обнаружить опухоли с диаметром меньше, чем 3 мм. В действительности этого разрешения нельзя достигнуть в каждом случае, так как оно зависит от использованного детектора, но оно достижимо при использовании подходящих детекторов.
9. Расширенный спектр применения: Частицы согласно изобретению имеют одинаковую или даже более высокую электронную плотность относительно скелета, т.е. накопление частиц может быть отображено в компьютерной томографии (СТ). Нерадиоактивная композиция частиц согласно изобретению (например, состоящая из CaF2, наиболее часто встречающегося природного изотопа фтора, [19]F, не является радиоактивной) является применимой для визуализации в F-MRI.
10. Многомодальная визуализация: Частицы согласно изобретению, в частности вариантов осуществления 1.1, 2.1 и 3.1 (см. фиг.2) являются пригодными для многомодальной визуализации, в связи с тем, что они содержат дополнительное диагностически пригодное вещество в дополнение к источнику излучения позитронов.
Возможные варианты получения
Более того, изобретение относится к способам приготовления фармацевтических средств, содержащих неорганический матрикс в виде частиц, который в дополнение к природному распределению изотопов структурных тип-образующих элементов анионов и катионов, содержит долю позитрон-излучающих нуклидов, в которой число позитрон-излучающих нуклидов на неорганический матрикс в виде частиц составляет предпочтительно больше чем или равно 1.
Предметом настоящего изобретения, таким образом, является также способ получения фармацевтического средства согласно изобретению, включающий, по меньшей мере, одну из следующих стадий:
(i) Смешивание, по меньшей мере, двух растворов растворимых солей согласно уравнению реакции осаждения, в которой, по меньшей мере, одна соль обогащена позитрон-излучающими нуклидами, и в которой катионы одной соли осаждаются (выпадают в осадок) с анионами другой соли, и в которой позитрон-излучающее содержимое является частью осажденного соединения, и образуется неорганический матрикс в виде частиц, который в дополнение к природному распределению изотопов структурных тип-образующих элементов анионов и катионов, содержит долю позитрон-излучающих нуклидов.
(ii) Образование суспензии в соответствии с уравнением реакции осаждения, содержащей неорганический матрикс в виде частиц, который в дополнение к природному распределению изотопов структурных тип-образующих элементов анионов и катионов, содержит долю позитрон-излучающих нуклидов.
(iii) Смешивание, по меньшей мере, двух растворов растворимых солей согласно уравнению реакции осаждения для образования неорганического матрикса и последующее добавление позитрон-излучающих нуклидов в анионной или катионной форме.
Более того, предметом настоящего изобретения, таким образом, является также способ получения фармацевтического средства согласно изобретению, включающий, по меньшей мере, одну из следующих стадий:
(iv) Смешивание по меньшей мере двух растворов растворимых солей согласно уравнению реакции осаждения, в которой по меньшей мере одна соль обогащена по меньшей мере одним из вышеупомянутых позитрон-излучающих нуклидов, и в котором катионы одной соли выпадают в осадок с анионами другой соли, и в котором позитрон-излучающее содержимое является частью осажденного соединения, и образуется неорганический матрикс в виде частиц, который в дополнение к природному распределению изотопов структурных тип-образующих элементов анионов и катионов, содержит долю, по меньшей мере, одного из вышеупомянутых позитрон-излучающих нуклидов.
(v) Образование суспензии согласно уравнению реакции осаждения, содержащей неорганический матрикс в виде частиц, который в дополнение к природному распределению изотопов структурных тип-образующих элементов анионов и катионов, содержит долю по меньшей мере одного из вышеупомянутых позитрон-излучающих нуклидов.
(vi) Смешивание по меньшей мере двух растворов растворимых солей согласно уравнению реакции осаждения для образования неорганического матрикса и последующее добавление, по меньшей мере, одного из вышеупомянутых позитрон-излучающих нуклидов в анионной и катионной форме.
В контексте настоящего изобретения могут быть добавлены стабилизаторы и/или лиганд-несущие стабилизаторы. В контексте настоящего изобретения дополнительно можно использовать нерадиоактивные изотопы. Дополнительно может быть осуществлено получение и использование предшественников в качестве зерен нуклеации для способа согласно изобретению. Способ согласно изобретению можно также осуществить с помощью обменных процессов, которые делают возможным, например, обмен ОН- ионов на [18]F- ионы в структуре частиц. В способе согласно изобретению размер частиц можно регулировать изменением концентрационных отношений исходных веществ. Способ согласно изобретению может сопровождаться стадиями модификации поверхностных свойств посредством выбора фармацевтической оболочки. Способ может сопровождаться стадиями соединения лигандов с помощью физических и химических, а также биохимических способов, известных специалистам в данной области техники. В способе согласно изобретению изотоничность композиции можно отрегулировать. В способе согласно изобретению необязательно можно проводить стерилизацию, автоклавирование или стерильную фильтрацию. В способе согласно изобретению в дополнительной стадии можно отобрать неорганические частицы заранее установленного общего диаметра.
Предпочтительные варианты осуществления способа согласно изобретению более подробно описаны в нижеследующем.
(а) Общее получение: Соединения, описанные выше, можно получить простым смешиванием двух водных растворов водорастворимых солей с природным распределением изотопов и необходимого количества позитрон-излучающих исходных веществ. Это можно выполнить, например, добавлением по каплям, при перемешивании или встряхивании, в специальных смесительных камерах, например в трехстороннем смесителе для жидкостей (в форме Y) с двумя подводящими трубопроводами, смесительной камерой и отводящим трубопроводом, или также с использованием микросмесителей, которые известны из технологии микросистем. Также можно использовать обычные модули для специального синтеза радио фармацевтических средств, так как они содержат в своей конструкции необходимые смешивающие и взбалтывающие элементы. Однако получение частиц, описанных здесь, является настолько простым, что обыкновенные смесительные системы, в которых объединены исходные продукты, смесительная камера и инжекторное устройство также могут быть разработаны. Суспензия в виде частиц образуется немедленно после смешивания растворов, а время приготовления находится в пределах секунд.
(b) Необязательное получение разных структурных типов: Смешивание может быть выполнено без добавления стабилизатора (структурный тип 1 и 1.1; фигура 1 и 2), со стабилизатором (структурный тип 2 и 2.1; фигура 1 и 2) или с лиганд-несущим стабилизатором (структурный тип 3 и 3.1; фигура 1 и 2). Также можно провести соосаждение с лигандами или модифицированными лигандами.
(c) Необязательное дополнительное применение нерадиоактивных изотопов: Частицы можно получить из растворимых соединений непосредственно с радиоактивными изотопами, например [18]F-, который получают в водном растворе с помощью ядерной реакции в циклотроне. Технологическую процедуру можно оптимизировать путем использования нерадиоактивных изотопов, таких как, например, [19]F-.
(d) Необязательное получение и использование предшественников: Дополнительный вариант получения относится к использованию предшественников, которые могут служить в качестве зерен нуклеации, так что образуется структура сердцевина-оболочка. Само целевое соединение - несмотря на природное распределение изотопов - или также второе контрастное вещество, такое как, например, частицы магнетита или магтемита, может быть использовано как зерно нуклеации.
(e) Необязательное получение с использованием обменных процессов: Нерадиоактивные нуклиды в неорганическом матриксе позже могут быть заменены на радиоактивные нуклиды в контексте настоящего изобретения, для того чтобы таким образом получить неорганический матрикс согласно изобретению. На примере гидроксиапатита окончательная композиция структурных типов согласно изобретению совсем просто может реагировать с водным раствором [18]F-. Ионы [18]F- заменяют ионы ОН- в структуре гидроапатита и образуется [18]F-фторгидроксиапатит в виде частиц, Са5(PO4)3(ОН,[18]F), без нарушения (возбуждения) структуры сверхрешетки.
(f) Необязательная регулировка размера частиц: Размер наночастиц можно регулировать с помощью концентраций исходных веществ.
В способе согласно настоящему изобретению ионы, используемые в реакции осаждения, которые составляют неорганический матрикс, предпочтительно добавляют в концентрации от 1*10-11 моль/л до 40 моль/л, более предпочтительно в концентрации от 1*10-7 моль/л до 10 моль/л, наиболее предпочтительно от 1*10-4 моль/л до 1 моль/л. Путем установления определенных концентраций ионов в реакции осаждения можно регулировать необходимый размер частиц согласно изобретению, как определено выше.
Особенно предпочтительно в способе согласно настоящему изобретению ионы, применяемые в реакции осаждения, которые составляют неорганический матрикс, добавляют в концентрации от 1,1*10-4 до 184 г/л в случае топаза (Al2F2)[SiO4] в качестве неорганического матрикса, в концентрации от 3,9*10-4 до 180 г/л в случае хиолита Na[Al3F4] в качестве неорганического матрикса, в концентрации от 2,1*10-4 до 343 г/л в случае вавеллита Al3(PO4)2(ОН,F)2 в качестве неорганического матрикса, в концентрации от 7,1*10-3 до 100 г/л в случае карбоната кальция (СаСО3) в качестве неорганического матрикса, в концентрации от 9,4*10-4 до 160 г/л в случае маггемита (γ-Fe2O3) в качестве неорганического матрикса, в концентрации от 1,3*10-4 до 230 г/л в случае цеолитов (общая формула Mn[(AlO2)x(SiO2)y] (М = металл, например Na)) в качестве неорганического матрикса, в концентрации от 9,4*10-4 до 230 г/л в случае магнетита (Fe3O4) в качестве неорганического матрикса, в концентрации от 9,1*10-3 до 233 г/л в случае сульфата бария (BaSO4) в качестве неорганического матрикса, в концентрации от 5,2*10-9 до 164 г/л в случае фосфата галлия (GaPO4) в качестве неорганического матрикса, в концентрации от 1,8*10-4 до 504 г/л в случае апатита или фторгидроксиапатита (Са5(PO4)3(ОН,F)=3Са3(PO4)2*Са(ОН,F)2) в качестве неорганического матрикса и в концентрации от 1,6*10-2 до 78 г/л в случае флюорита (CaF2) в качестве неорганического матрикса.
В способе согласно настоящему изобретению реакции осаждения предпочтительно осуществляют при температуре от 0°С до 100°С, более предпочтительно при температуре от 4°С до 60°С, наиболее предпочтительно при температуре от 10°С до 40°С.
(g) Необязательная модификация свойств поверхности: Использованием разных стабилизаторов можно регулировать свойства поверхности. Предпочтительными являются стабилизаторы, которые образуют фармацевтическую оболочку.
(h) Необязательное соединение лигандов: Добавление лигандов выполняют с помощью обычных физических и химических, а также биохимических способов. Подходящие методы связывания известны специалистам в данной области техники.
(i) Необязательное регулирование изотоничности: При применении растворимых соединений Cl или Na в виде частиц (или других традиционных веществ для регулирования изотоничности) можно непосредственно принять во внимание более позднюю изотоничность получающейся композиции. Изотонический раствор имеет то же самое осмотическое давление, как кровь человека (около 7,5 бар) и соответствует солевому раствору с концентрацией около 0,9%.
(j) Необязательная стерилизация/автоклавирование/стерилъная фильтрация: Композиции (предшественник или окончательный препарат) можно простерилизовать обычными способами. Подходящими способами, среди прочих, являются стерильная фильтрация при размере пор 0,2 мкм или стерилизация нагреванием в автоклаве при 121°С, 1 бар, от 15 до 30 мин.
Описанные варианты осуществления и способы получения демонстрируют, что частицы согласно изобретению могут быть предоставлены в различных композициях с учетом их свойств, таких как, например, состав, содержание изотопа, размер и поверхностные свойства, которые таким образом можно целенаправленно подобрать относительно фармакологических требований.
Применение частиц согласно изобретению
Фармацевтические средства согласно изобретению применяются in vitro и in vivo в медицине, предпочтительно в качестве диагностических средств. Особенно предпочтительным является применение в позитрон-эмиссионной томографии (PET) и также при диагностике с помощью РЕТ-СТ. Частицы согласно изобретению можно использовать и в фармакологических исследованиях, и в ветеринарии, и также в медицине для человека. Для использования в диагностике пациенту вводят активную дозу. Введение предпочтительно является внутривенным. Затем распределение частиц согласно изобретению в организме определяют с помощью PET или РЕТ-СТ или необязательно другими подходящими способами после заранее установленного времени. Подходящие способы известны специалисту в данной области техники. Фармацевтические средства согласно изобретению также используются в локо-региональной терапии.
Возможные указания и механизмы применения описаны далее в примерах.
Применение частиц согласно изобретению аналогично коллоидам для MRI, например, Resovist u Supravist (Sobering AG, Германия).
Применение частиц согласно изобретению возможно при всех показаниях для применения Resovist, например при исследовании печени, и показаниях для Supravist, например ангиографии.
Применение частиц согласно изобретению аналогично коллоидам для SPECT, например наноцис (CisBio, Франция).
В принципе возможно применение частиц согласно изобретению при всех показаниях для применения NanoCis/NanoColl, например, при обнаружении сигнальных лимфатических узлов. Типы структур сердцевина-оболочка с магнетитом в сердцевине также могут быть использованы для комбинированных методов визуализации в области определения сигнального лимфатического узла.
Применение частиц согласно изобретению для "пассивного нацеливания"
Контролирование размера и поверхностных свойств дает возможность специально подбирать наночастицы для пассивного нацеливания на опухолевую ткань. Механизм пассивного нацеливания схематически показан на Фигуре 3.
Описание фигуры 3
Здоровые кровеносные сосуды имеют замкнутый эндотелий. Они являются непроницаемыми и удерживают большие молекулы, такие как, например, альбумин или также наночастицы, от движения в обратном направлении в кровообращение. Эндотелий кровеносных сосудов в опухолях имеет отверстия, и через них небольшие частицы согласно изобретению легко могут диффундировать из кровообращения в ткань. Более того, так как транспортировка лимфы уменьшена в опухолевой ткани, частицы согласно изобретению накапливаются в опухоли исключительно вследствие правильной наноразмерной величины.
Более того, особая среда в опухолевой ткани может гарантировать, что частицы согласно изобретению приобретают здесь другие диагностически пригодные свойства.
Применение частиц согласно изобретению для нацеливания, связанного с клетками
Частицы согласно изобретению главным образом поглощаются клетками ретикулоэндотелиальной системы (RES) в зависимости от размера и структуры поверхности и заряда. В этом контексте макрофаги, циркулирующие в крови, могут быть помечены непосредственно частицами согласно изобретению после инъекции композиции. Это делает возможным визуализацию, например, воспалительных процессов, которые всегда сопровождаются повышенной активностью макрофагов.
Применение частиц согласно изобретению для "активного нацеливания"
С помощью специфических лигандов тканевые структуры можно распознавать целенаправленно. Например, анти-L-селектин является пригодным для демонстрирования лимфатических узлов. ICAM и VCAM являются специфическими маркерами воспаления, которые также играют большую роль в случае установления MS (рассеянного склероза). Более того, Е-селектин является пригодным для распознавания очагов воспаления, а также многих типов опухолей. EDB-фибронектин является ангиогенез-специфическим, а анти-CD105 (эндоглин) антитело можно использовать для демонстрации рака молочной железы. Дополнительные лиганды и рецепторы, которые можно использовать, известны специалистам в данной области техники.
Так как получение частиц согласно изобретению является несложным, и специфические лиганды могут быть изменены, в частности, с помощью стабилизаторов, частицы согласно изобретению служат в качестве гибкой технологической платформы.
Применение частиц согласно изобретению для визуализации стволовых клеток (прослеживание стволовых клеток)
С помощью частиц согласно изобретению возможно мечение стволовых клеток.
Применение частиц согласно изобретению для преодоления гематоэнцефалического барьера (ВВВ доставка)
С помощью стратегий доставки, известных из литературы (например, pathfinder (наведения) технологии), возможно преодоление гематоэнцефалического барьера.
Таким образом, предметом настоящего изобретения также является фармацевтическое средство согласно изобретению для диагностики посредством позитрон эмиссионной томографии болезней, выбранных из группы, состоящей из пролиферативных болезней, воспалительных болезней, аутоиммунных болезней, болезней пищеварительного тракта, артериосклероза, инсульта, инфаркта, патологических изменений в системе кровеносных сосудов, лимфатической системе, поджелудочной железе, печени, почке, мозге и мочевом пузыре, и болезней передачи электрического стимула и нейродегенеративных болезней. В этом контексте пролиферативная болезнь может быть выбрана из группы, состоящей из опухоли, предраковой стадии, дисплазии, эндометриоза и метаплазии. В этом контексте аутоиммунную болезнь можно выбрать из группы, состоящей из ревматоидного артрита, воспалительного кишечного заболевания, остеоартрита, невропатической боли, очаговой алопеции, псориаза, псориатического артрита, острого панкреатита, отторжения аллотрансплантата, аллергии, аллергических воспалений легких, рассеянного склероза, болезни Альцгеймера, болезни Крона и системной красной волчанки.
Таким образом, предметом настоящего изобретения также является фармацевтическое средство согласно изобретению для локо-региональной терапии болезни, выбранной из группы, состоящей из пролиферативных болезней, воспалительных болезней, аутоиммунных болезней, болезней пищеварительного тракта, артериосклероза, инсульта, инфаркта, патологических изменений в системе кровеносных сосудов, лимфатической системе, поджелудочной железе, печени, почке, мозге и мочевом пузыре, и болезней передачи электрического стимула и нейродегенеративных болезней. В этом контексте пролиферативную болезнь можно выбрать из группы, состоящей из опухоли, предраковой стадии, дисплазии, эндометриоза и метаплазии. В этом контексте аутоиммунную болезнь можно выбрать из группы, состоящей из ревматоидного артрита, воспалительного кишечного заболевания, остеоартрита, невропатической боли, очаговой алопеции, псориаза, псориатического артрита, острого панкреатита, отторжения аллотрансплантата, аллергии, аллергических воспалений легких, рассеянного склероза, болезни Альцгеймера, болезни Крона и системной красной волчанки.
Изобретение дополнительно объясняется с помощью следующих примеров:
Подробный пример 1. Фторид кальция в виде наночастиц, CaF2, в качестве PET диагностического средства
1.1 Общее описание
CaF2 осаждается как плохо растворимое соединение (растворимость флюорита: 17 мг/л при 20°С и 16 мг/л при 18°С) в виде осадка после смешивания водорастворимых соединений CaCl2 и NaF (успешное получение также можно осуществить с использованием KF, NH4F или HF) или также в коллоидно-дисперсной форме ("наночастицы") после смешивания подходящих низких концентраций.
Уравнение реакции осаждения:
CaCl2+2F→CaF2↓+2Cl-
В присутствии подходящих стабилизаторов, например полоксамера F68, наночастицы также формируются при смешивании гораздо более высоких концентраций. В частности для этого являются пригодными Calcophilic стабилизаторы, такие как сополимеры полиакриловой кислоты-блок-PEG, фосфат-функционализированные полимеры-блок-PEG и фосфонат-функционализированные полимеры-блок-PEG типа.
Это можно установить с помощью "низкомолекулярных" растворимых продуктов:
Са карбоксилат pKs (25°C)=8.1
Са фосфат pKs (25°С)=29.5
Са фосфонат pKs (25°С)=52
Химическое соединение стабилизаторов с мишень-специфическими лигандами, такими как антитела, их фрагменты, пептиды и т.д. типа лиганд-PEG-блок-calcophilic полимер дает наночастицы, которые могут связываться нацеленным образом с соответствующими мишенями у пациента.
[18]F- химически ведет себя подобно [19]F-. Что касается PET диагностического средства, [18]F-, например, в виде раствора H[18]F или Na[18]F необходимой радиоактивности, добавляют к раствору Na[19]F, компоненты смешивают и продукт используют для осаждения согласно реакции осаждения.
Нуклид [18]F имеет период полураспада приблизительно t1/2=110 мин. Его получают согласно следующей целевой реакции в циклотроне:
[18]F- получают как HF в водном растворе. Концентрация фторида здесь, как правило, составляет между 50 и 400 ГБк/мкмоль, в зависимости от течения процесса и модели циклотрона.
1.2. Методики
1.2.1. CaF2 наночастицы без поверхностно-активных веществ
Соответствующее количество раствора [18]F- смешивают с нерадиоактивным раствором фторида калия (KF), так что образуется 1 мл водного раствора KF с концентрацией 0,1 моль/л. 1 мл водного раствора KF (0,1 моль/л) смешивают, встряхивая в пузырьке, с 1 мл водного раствора CaCl2 с концентрацией 0,05 моль/л. Немедленно образуются наночастицы CaF2, которые можно видеть по небольшой опалесценции образованной дисперсии (Фигура 4).
Определение распределения частиц по размерам с помощью динамического рассеяния света (ДРС) дает средний размер частиц 71,5 нм (интенсивность-взвешенная).
Повторение эксперимента дает размер частиц 81,7 нм.
С помощью тонкослойной хроматографии (мобильная фаза: метанол или метилэтилкетон) и подходящего детектора можно продемонстрировать, что больше чем 90% использованной радиоактивности является связанной в частицах согласно изобретению и остается на базовой линии (Rf=0).
Во второй серии экспериментов вместо раствора KF смешивают раствор фторида натрия (NaF) (0,1 моль/л) с 1 мл водного раствора CaCl2 (0,05 моль/л). При этом также образуются наночастицы CaF2, и дисперсия выглядит опалесцентной. При этом определение размера частиц с помощью ДРС дает 75,9 нм. Здесь также больше чем 90% использованной радиоактивности является связанной в частицах согласно изобретению.
1.2.2. Наночастицы CaF2, стабилизированные поверхностно-активным веществом
1 мл водного раствора KF (0,1 моль/л) с необходимой радиоактивностью смешивают, встряхивая в пузырьке, с 1 мл водного раствора CaCl2 (0,05 моль/л), в котором был заблаговременно растворен 1 вес.% Плюроника F68 (также известный как полоксамер 188). Немедленно образуются наночастицы CaF2, которые можно видеть по небольшой опалесценции образованной дисперсии.
Свыше 90% использованной радиоактивности является связанной в частицах согласно изобретению.
Определение распределения частиц по размерам с помощью динамического рассеяния света дает средний размер частиц 64,5 нм (интенсивность-взвешенная). Пример распределения частиц по размерам показан на Фигуре 5.
Эксперимент повторяют семь раз и определяют размер частиц с помощью ДРС. Через 24 часа вновь измеряют распределение частиц по размерам. Результаты суммированы в таблице 2.
Серии экспериментов показывают очень хорошую воспроизводимость размера наночастиц (коэффициент вариации <7%). Средний размер частиц после времени выдерживания в течение 24 часов при комнатной температуре немного увеличивается от 60,3±4,0 нм (n=7) до 64,9±3,5 нм (n=6), но это увеличение еще находится в рамках простого среднеквадратичного отклонения в серии экспериментов и, следовательно, не является статистически значимым. Следовательно, наночастицы CaF2 являются стабильными в отношении распределения размера частиц в течение, по меньшей мере, 24 часов.
1.2.3. Контролирование размера наночастиц CaF2
Аналогично сериям экспериментов, описанным выше, CaF2 наночастицы получают из гораздо более концентрированного раствора KF и раствора CaCl2. Вместе с результатами исследования воспроизводимости (пример 1.2.2), размеры частиц в результате смешивания в каждом случае 1 мл 0,2 моль/л раствора KF с 0,1 моль/л раствором CaCl2 или 0,4 моль/л раствора KF с 0,2 моль/л раствором CaCl2 показаны на фигуре 6. Размер частиц увеличивается от около 60 нм примерно до 400 нм при увеличении концентрации.
Пример 2. Плохорастворимое неорганическое [11]С или [15]O карбонатное соединение в виде наночастиц и его применение в качестве PET диагностического средства
Пример: Карбонат кальция, CaCO3, в виде наночастиц в качестве PET диагностического средства
Нуклиды получают с помощью следующей целевой реакции в циклотроне:
C[11]t1/2=20,7 мин
O[15]t1/2=2 мин
Уравнение реакции осаждения:
CO2+H2O↔Н2СО3
Ca(ОН)2+Н2СО3→СаСО3↓+2H2O
Наночастицы образуются согласно реакции осаждения в присутствии растворимых стабилизаторов, например F68. В частности, являются пригодными Calcophilic стабилизаторы, такие как блок-сополимеры полиакриловой кислоты-блок-PEG, фосфат-функционализированные полимеры-блок-PEG и фосфонат-функционализированные полимеры-блок-PEG типа. Химическое соединение стабилизаторов с мишень-специфическими лигандами, такими как антитела, их фрагменты, пептиды и т.д., лиганд-PEG-блок-calcophilic полимерного типа дает наночастицы, которые могут связываться нацеленным образом с соответствующими мишенями у пациента.
Пример 3. Соединения [18]фторгидроксиапатита (Са5(PO4)3(ОН, [18]F) в виде наночастиц и их применение в качестве PET диагностического средства
3.1. Получение частиц гидроксиапатита
Лимонную кислоту добавляют к 0,1 молярному водному раствору CaCl2, так что он находится в концентрации 5 процентов по весу. Значение рН 9-11 устанавливают с помощью 0,1 молярного раствора NaOH. Затем приготавливают водный Na3PO4 таким способом, при котором в растворах получается отношение Са/Р 1,67. Раствор Na3PO4 добавляют по каплям к раствору CaCl2 при комнатной температуре при перемешивании с помощью магнитной мешалки. Образуется осадок гидроксиапатита.
3.2. Получение частиц [18]фторгидроксиапатита
Для получения частиц [18]фторгидроксиапатита дисперсию согласно примеру 3.1. смешивают с раствором, содержащим ионы [18]F- при необходимой интенсивности радиоактивности, то есть в соответствующей концентрации. При замене ионов гидроксила на ионы фторида образуются частицы [18]фторгидроксиапатита, пригодные для диагностической визуализации.
Описание фигур:
Фиг.1:
Фигура 1, Тип 1 описывает частицы согласно изобретению из группы плохо растворимых неорганических соединений (С), описанных выше, которые не содержат стабилизатор и ингибируются коагуляцией. При этом молекулы адсорбированной воды или/и электрический заряд на поверхности частицы способствуют повышению стабилизации частиц (системы также названы sol).
Фигура 1, Тип 2 - частицы согласно изобретению, которые являются устойчивыми к агрегации с поверхностно-активными молекулами. В дополнение к обычным стабилизаторам, которые можно вводить внутривенно (вв.), таким как, например, полоксамеры, также можно использовать блоксополимеры со специально заданными свойствами. Это включает, например, так называемые двойные гидрофильные А-блок-В сополимеры, из которых блок А имеет координирующие/стабилизирующие способности, а второй блок В защищает частицы от агрегации и часто состоит из полиэтиленгликоля (PEG).
Более того, частицы согласно изобретению могут быть покрыты дополнительными материалами, например обычными материалами для покрытия, такими как углеводороды, полиэтиленгликоли, полиакриловые или метакриловые кислоты, жирные кислоты, двуокись кремния или/и силан и т.д.
Фигура 1, Тип 3 показывает дополнительный вариант осуществления частиц согласно изобретению с мишень-специфической структурой частиц, которые получают дополнительным соединением специфических лигандов. Эти лиганды могут быть например, антителами, их фрагментами, пептидами, аптамерами, дарпинами или другими небольшими молекулами, которые имеют высокое сродство к болезнь-специфическим рецепторам. Лиганды могут быть или соединены посредством химической модификации веществ, используемых для стабилизации, или закреплены непосредственно на частице согласно изобретению.
Фиг.2: Кроме того, внутренняя часть (ядро, сердцевина) частиц согласно изобретению может состоять из двух различных материалов (структура ядро-оболочка; Фигура 2, Тип 1.1, 2.1, 3.1). В этом контексте, в предпочтительном варианте осуществления внутренняя часть С2 (или внешняя С1) может состоять из дополнительного диагностически пригодного средства. Например, магнетиты можно использовать как зерна нуклеации, а плохо растворимые неорганические соединения, описанные выше, можно осадить на них или нанести на них.
В дополнительном варианте осуществления оболочка частиц согласно изобретению типа 1.1, 2.1 и 3.1 может состоять из любой фармацевтически приемлемой оболочки.
Фиг.3: Иллюстрация механизма пассивного нацеливания
Здоровые кровеносные сосуды имеют замкнутый эндотелий. Они являются непроницаемыми и задерживают большие молекулы, такие как, например, альбумин или также наночастицы, от движения в обратном направлении в кровообращение. Эндотелий кровеносных сосудов в опухолях имеет отверстия, и через них небольшие частицы согласно изобретению легко могут диффундировать из кровообращения в ткань. Более того, так как транспортировка лимфы уменьшена в опухолевой ткани, частицы согласно изобретению накапливаются в опухоли исключительно вследствие правильной наноразмерной величины.
Фиг.4: Фотография дисперсии CaF2 в соответствии с примером 1.2.1, готовой для введения. Наночастицы CaF2 видны по небольшой опалесценции образованной дисперсии.
Фиг.5: Пример распределения размера наночастиц CaF2 согласно примеру 1.2.2, определенного с помощью динамического рассеяния света.
Фиг.6: Контролирование размера наночастиц CaF2 с помощью 11 независимых экспериментов аналогично инструкциям по получению, описанным в примере 1, в частности в примере 1.2.3. Средний диаметр распределения размера частиц можно таким образом установить от 60 нм до около 400 нм.
Реферат
Изобретение относится к фармацевтическому средству для использования в качестве диагностического агента, которое содержит неорганический матрикс в виде частиц из аморфных или смеси аморфных и кристаллических структур, который в дополнение к природному распределению изотопов структурных тип-образующих элементов анионов и катионов содержит долю позитрон-излучающих нуклидов. В качестве неорганического матрикса выбирается топаз (Аl2F2)[SiO4], хиолит Na[Al3F4], вавеллит Аl3(РО4)2(ОН, F)2, карбонат кальция СаСО3, маггемит γ-Fe2O3, цеолиты общей формулы Mn[(AlO2)x(SiO2)y] (М=металл), магнетит Fе3O4, сульфат бария BaSO4, фосфат галлия GаРО4, апатит или фторгидроксиапатит Са5(РO4)3(ОН, F)=3Са3(РO4)2*Са(ОН, F)2 и флюорит CaF2. Позитрон-излучающие нуклиды выбираются из [15]O, [30]Р, [13]N, [65]Ga, [11]C, [131]Ва, [26]Аl, [68]Ga и [18]F, и их число на неорганический матрикс составляет больше чем 1. Изобретение также относится к способу получения указанного фармацевтического средства, который включает смешивание двух растворов растворимых солей и их осаждение, где одна соль обогащена позитрон-излучающими нуклидами, а катионы одной соли осаждаются с катионами другой соли с образованием неорганического матрикса. Изобретение также относится к фармацевтической композиции для использования в диагностической визуализации, в которой более 0,001% частиц, содержащихся в композиции, представляют собой указанный неорганический матрикс. Изобретение обеспечивает упрощенное получение специфических частиц с более длительной пригодностью к использованию, которые пригодны для диагностической визуализации. 3 н. и 6 з.п. ф-лы, 6 ил., 2 табл., 3 пр.
Формула
в которой структурный тип неорганического матрикса содержит аморфные структуры или смесь аморфных и кристаллических структур,
в которой число позитронизлучающих нуклидов на неорганический матрикс в виде частиц предпочтительно составляет больше чем или равно 1,
в которой неорганический матрикс в виде частиц выбирают из группы, содержащей топаз (Al2F2)[SiO4], хиолит Na[Al3F4], вавеллит Аl3(РO4)2(ОН, F)2, карбонат кальция (СаСО3), маггемит (γ-Fе2O3), цеолиты (общая формула Mn[(AlO2)x(SiO2)y] (М=металл, например Na), магнетит (Fе3O4), сульфат бария (BaSO4), фосфат галлия (GaPO4), апатит или фторгидроксиапатит (Са5(РO4)3(ОН, F)=3Са3(РO4)2·Са(ОН, F)2) и флюорит (CaF2), и
в которой позитронизлучающие нуклиды выбирают из группы, содержащей [15]O, [30]Р, [13]N, [65]Ga, [11]C, [131]Ba, [26]Al и [68]Ga и [18]F.
(i) смешивание по меньшей мере двух растворов растворимых солей согласно уравнению реакции осаждения, в которой по меньшей мере одна соль обогащена позитронизлучающими нуклидами, и в которой катионы одной соли осаждаются с анионами другой соли, и в которой позитронизлучающее содержимое является частью осажденного соединения, причем образуется неорганический матрикс в виде частиц, который в дополнение к природному распределению изотопов структурных типобразующих элементов анионов и катионов содержит долю позитронизлучающих нуклидов;
(ii) образование суспензии в соответствии с уравнением реакции осаждения, содержащей неорганический матрикс в виде частиц, который в дополнение к природному распределению изотопов структурных типобразующих элементов анионов и катионов содержит долю позитронизлучающих нуклидов;
(iii) смешивание по меньшей мере двух растворов растворимых солей согласно уравнению реакции осаждения для образования неорганического матрикса и последующее добавление позитронизлучающих нуклидов в анионной или катионной форме.

Комментарии