Бандаж с дистанционным управлением для регулирования работы внутреннего органа или канала, а также способы его изготовления, имплантации и использования - RU2396925C2
Код документа: RU2396925C2
Чертежи

























Описание
Область техники
Настоящее изобретение относится к лапароскопическим имплантатам, предназначенным для имплантации в организм пациента вокруг биологического органа, имеющего карман или канал, с целью регулирования работы этого органа или канала. Говоря более конкретно, настоящее изобретение касается имплантируемого кольца с дистанционным электропитанием и управлением, предназначенного для использования в качестве желудочного бандажа при лечении ожирения или в качестве искусственного сфинктера.
Уровень техники
Об ожирении речь может идти тогда, когда вес тела превышает его нормальные конституционные и физические нормы. Одним из общепринятых параметров для классификации ожирения является не сам вес, а так называемый «индекс массы тела» (ИМТ), в котором учтен рост пациента: ИМТ рассчитывается путем деления веса на квадрат роста и измеряется в кг/м2.
Диагноз «ожирение» ставится обычно, если ИМТ составляет 30 кг/м2 и более, причем в зависимости от степени ожирения его делят на следующие степени: 1 степень (ИМТ 30-34,9 кг/м2), II степень (ИМТ 35-39,9 кг/м2), которую называют также как «тяжелое ожирение», и III степень (ИМТ 40 кг/м2 и более), называемая также «очень тяжелым ожирением». Ожирение называют «морбидным» (патологическим), если ИМТ превышает индекс 40 (очень тяжелое ожирение) или 35 (тяжелое ожирение) и при этом имеют место серьезные сопутствующие заболевания.
Ожирение повсеместно считается довольно серьезной проблемой для здоровья и ему обычно сопутствуют многочисленные осложнения - от легких, неопасных заболеваний до хронических болезней, представляющих угрозу для жизни. По данным Всемирной Организации Здравоохранения к числу неопасных, но негативно влияющих на здоровье проблем, связанных с ожирением, относятся нарушения работы дыхательных органов, хронические проблемы, связанные с опорно-двигательной системой, кожные заболевания и бесплодие. Что касается проблем, представляющих угрозу для жизни, то их можно разделить на четыре следующие основные категории: сердечно-сосудистые заболевания; заболевания, связанные с резистентностью к инсулину, типа диабета второго типа; некоторые виды рака, в частности, вызываемые гормональными нарушениями, и также рак толстой кишки; болезни желчного пузыря. Помимо указанных физиологических проблем ожирение имеет также психологические последствия, начиная с пониженной самооценки и заканчивая клинической депрессией.
Для лечения пациентов, страдающих морбидным ожирением, обычно используют хирургическое вмешательство. Такое вмешательство не только облегчает многочисленные проблемы, вызванные избыточным весом, но и способно уменьшить риск преждевременной смерти пациента. Если патологическое ожирение оставить без лечения, оно может привести к сокращению предполагаемой продолжительности жизни пациента на десять-пятнадцать лет.
Пациенты с морбидным ожирением в целом плохо поддаются лечению, при котором длительное постоянное снижение веса достигается посредством нехирургических методов типа строгих диет в сочетании с физическими нагрузками и изменениями поведенческого режима, несмотря на то, что такие методы признаны самыми безопасными. По этой причине существует постоянная потребность в эффективных способах непосредственного вмешательства, обеспечивающих эффективное долгосрочное лечение морбидного ожирения.
В настоящее время используют три следующих основных хирургических приема: шунтирование желудка по Ру (RYGB), вертикальная гастропластика с бандажированием (VBG) и регулируемое бандажирование желудка (AGB).
При проведении RYGB формируют небольшой желудочный карман и присоединяют к этому карману Y-образный участок тонкой кишки, в результате чего пища идет в обход нижнего желудка, двенадцатиперстной кишки и первого участка тонкой кишки. Рассматриваемая методика RYGB является как ограничивающей, поскольку небольшой размер кармана ограничивает объем потребляемой пищи, так и основанной на мальабсорбции, в том смысле, что шунтирование приводит к уменьшению количества получаемых организмом калорий и питательных элементов.
При проведении VBG используют нерегулируемый синтетический бандаж и скобы для формирования небольшого желудочного кармана. А при AGB применяют стягивающее синтетическое кольцо, которое помещают вокруг верхнего конца желудка с целью формирования внутри желудка искусственного сужения. Бандаж заполняют физиологическим раствором и присоединяют к небольшому резервуару - порту доступа, расположенному под кожей живота. Путем прокалывания порта доступа иглой и добавления или выведения из него физиологического раствора бандаж AGB может раздуваться, что позволяет уменьшать просвет сужения, или же сдуваться, увеличивая тем самым просвет сужения. Как VBG, так и AGB являются ограничивающими методиками и не связаны с эффектом мальабсорбции.
Пример использования методики AGB описан, в частности, в патенте U.S. 5074868, выданном на имя Kuzmak. Согласно описанному в этом патентном документе в зону вокруг желудка имплантируют гибкий бандаж из упругого полимерного материала, из которого формируют замкнутую петлю с фиксированным заданным диаметром. Основа этого гибкого бандажа содержит расширяющуюся камеру, которая посредством трубки связана с подкожным инъекционным портом. В этот инъекционный порт могут с помощью шприца вводить жидкость, что позволяет добавлять или выводить раствор из расширяющейся камеры и, таким образом, варьировать внутренний диаметр бандажа и диаметр просвета сужения. При этом благодаря расширению камеры в сочетании с поддержанием заданного и фиксированного диаметра бандажа удается регулировать диаметр просвета, а следовательно, и количество проглатываемой пищи.
Хотя система, описанная в патенте Kuzmak'a, и позволяет достичь удовлетворительных результатов, она все же имеет некоторые недостатки. Так, инъекционный порт является источником многочисленных проблем, с которыми приходится сталкиваться при использовании гидравлических желудочных бандажей, включая попадание инфекции, повреждение трубки вследствие неточного прокола иглой, неудобства, испытываемые пациентом из-за наличия порта, и трудности с определением местоположения этого порта (для определения его места и ориентации часто приходится пользоваться рентгеном).
Кроме того, несмотря на то, что с помощью инъекционного порта можно выполнять ограниченную регулировку диаметра кольца без кардинального хирургического вмешательства, установка данного бандажа может сопровождаться такими побочными явлениями, как рвота. Эти недостатки могут быть обусловлены многими причинами, и в том числе чрезмерным уменьшением диаметра просвета сужения, неэффективным действием бандажа вследствие слишком большого диаметра просвета, его закупоркой, инфицированием, местным или общим воспалением.
Таким образом, иногда возникает необходимость в повторной операции либо для облегчения состояния пациента, либо для подгонки или замены ранее имплантированного бандажа. В этих случаях ранее имплантированный бандаж должен быть разрезан, а затем либо снят, либо заменен, для чего необходима операция, которая является довольно сложной, дорогостоящей и плохо переносится пациентами.
В патенте U.S. 50938669, выданном на имя Klaiber и др., рассмотрены некоторые проблемы, возникающие при использовании инъекционного порта, и описан желудочный бандаж, который можно регулировать неинвазивным методом посредством дистанционного управления. Предложенная здесь система включает в себя блок управления, который имплантирован в тело пациента и соединен с желудочным бандажом. Этот блок управления снабжен электронасосом на батарейках и клапаном, которые установлены между расширяющейся камерой и резервуаром с жидкостью. Кроме того, блок содержит приемо-передающее радиоустройство и микропроцессор, предназначенные для связи с внешним пультом дистанционного управления, управляющим работой насоса, который, в свою очередь, выполняет введение или выведение жидкости из резервуара в расширяющуюся камеру, что позволяет варьировать диаметр просвета сужения. Указанным внешним пультом дистанционного управления управляет сам врач.
Хотя описанное выше в патенте Klaiber'a устройство и представляет собой довольно интересную и полезную для пациентов разработку, оно также несвободно от некоторых недостатков. Так, имплантация указанного резервуара с жидкостью в тело пациента является достаточно сложной процедурой, поскольку необходимо избежать прокола и обеспечить герметичность резервуара. Аналогичным образом, введение в тело пациента батареи приводит к тому, что система становится в высокой степени уязвимой. Так, например, для замены разрядившейся или имеющей утечки батареи бывает необходимо дополнительное хирургическое вмешательство.
Из уровня техники известны неоднократные попытки устранения недостатков, связанных с использованием желудочных бандажей с гидроприводом типа описанных в патентах Kuzmak'a и Klaiber'a. Так, в патенте U.S. 6547801, выданном на имя Dargent и др., описана хирургически имплантируемая гастропластическая система, в состав которой входит гибкий растягивающийся элемент, входящий в зацепление с зубчатым тянущим механизмом с электроприводом. Электропитание и управление двигателем осуществляется посредством индуктивной цепи, так что диаметр кольца можно изменять исключительно посредством внешнего пульта дистанционного управления.
Хотя описанная в патенте Dargent'a система и позволяет решить проблемы, связанные с инъекционными портами, используемыми в известных ранее бандажах, а также проблемы, обусловленные необходимостью использования имплантируемых батарей, представляется, что и она несвободна от некоторых недостатков. Так, например, хотя в этом патенте Dargent и упомянул, что зубчатого привода тянущего механизма вполне достаточно для предотвращения разматывания бандажа в периоды отсутствия электропитания, все-таки конфигурация этого тянущего механизма такова, что, если бандаж подвергается сжатию, то нельзя исключить его «скачка» или соскальзывания. Кроме того, как явствует из чертежей, приложенных к указанному патенту, при сжатии бандажа на его внутренней поверхности образуются складки, которые могут вызвать воспаление или механическое повреждение желудка.
Кроме сказанного, было обнаружено, что в течение нескольких недель после имплантации гастропластического бандажа волокнистая ткань имеет тенденцию разрастаться и обволакивать этот бандаж. Можно ожидать, что, как и в системе, описанной в патенте Dargent'a, в которой наружная часть диаметра бандажа сжимается под воздействием электропривода, такая волокнистая ткань будет оказывать неблагоприятное воздействие на функционирование устройства. И, наконец, хотя описанный в патенте Dargent'a бандаж является гибким, он неспособен к растягиванию, которое может понадобиться, например, для адаптации при конвульсивных движениях желудка, например, во время рвоты, что чревато возникновением у пациента явлений непереносимости.
Все перечисленные выше хирургические методы требуют кардинального оперативного вмешательства и могут послужить причиной серьезных осложнений. Последние разработки были направлены, в основном, на имплантацию желудочного кольца лапароскопическим методом, что позволяет свести к минимуму дискомфорт пациента и продолжительность восстановительного периода.
Так, например, в патенте U.S. 5226429, выданном на имя Kuzmak, описан желудочный бандаж с гидроприводом, конфигурация которого позволяет имплантировать его с использованием лапароскопических методов. Конструкция бандажа разработана с таким расчетом, чтобы его можно было вводить через лапароскопическую канюлю, при этом он содержит инъекционный порт для регулирования степени сжатия, создаваемого бандажом. Однако, как было отмечено выше, можно полагать, что такой бандаж будет иметь те же недостатки, что и используемые ранее гидравлические желудочные бандажи. Кроме того, в рассматриваемом патенте не приведено рекомендаций и предложений относительно того, какой вариант конструкции желудочных бандажей негидравлического типа обеспечил бы возможность их лапароскопической имплантации. Так, например, в патенте не раскрыто, каким образом следует практикующему специалисту адаптировать негидравлическое устройство, описанное в патенте Dargent'a, для лапароскопической имплантации.
Принимая во внимание указанное выше, существует потребность в создании устройства и способа регулирования работы внутреннего органа или канала, которые обеспечивали бы регулировку с высокой точностью действующего на орган или канал сжатия и были бы свободны от недостатков, связанных с использованием известных из уровня техники инъекционных портов.
Также существует потребность в создании устройства регулирования работы внутреннего органа или канала, которое обеспечивало бы поддержание необходимой степени сжатия в течение длительного периода посредством системы с механическим приводом, которую можно было бы имплантировать лапароскопическим методом, а также соответствующих способов.
Также существует потребность в создании устройства и способов регулирования работы внутреннего органа или канала, которые бы обеспечивали возможность адаптации к случайным конвульсивным движениям органа или канала.
Также существует потребность в создании устройства регулирования работы внутреннего органа или канала, которое бы имело дистанционное электропитание, что позволит избежать необходимости повторной операции для замены или восстановления неисправного или разрядившегося источника питания, а также соответствующих способов.
Кроме того, существует потребность в создании устройства и способов регулирования работы внутреннего органа или канала, при которых имело бы место дистанционное управление, обеспечивалась высокая степень безопасности и с высокой степенью надежности осуществлялся воспроизводимый уровень сжатия.
Дополнительно, также существует потребность в создании устройства и способов регулирования работы внутреннего органа или канала, которые обеспечивали бы поддержание постоянного наружного диаметра и не выходили бы из строя в результате врастания ткани или обволакивания волокнистой тканью.
Наконец, существует потребность в создании устройства регулирования работы внутреннего органа или канала, регулирование которого мог бы осуществлять сам врач неинвазивным, безопасным и несложным образом без необходимости использования рентгенографии, а также соответствующего способа.
Сущность изобретения
Принимая во внимание сказанное выше, одной из целей настоящего изобретения является создание устройства и способа регулирования работы внутреннего органа или канала, которые обеспечивали бы высокую точность регулировки действующего на орган или канал сжатия и были бы свободны от недостатков, связанных с использованием известных из уровня техники инъекционных портов.
Другая цель настоящего изобретения - создание устройства регулирования работы внутреннего органа или канала, которое обеспечивало бы поддержание необходимой степени сжатия в течение длительного периода посредством системы с механическим приводом, которую можно было бы имплантировать лапароскопическим методом, а также соответствующего способа.
Еще одна цель настоящего изобретения - создание устройства и способа регулирования работы внутреннего органа или канала, которые бы обеспечивали возможность адаптации к случайным конвульсивным движениям органа или канала.
Следующая цель настоящего изобретения - создание устройства регулирования работы внутреннего органа или канала, которое бы имело дистанционное электропитание, что позволит избежать необходимости повторной операции для замены или восстановления неисправного или разрядившегося источника питания, а также соответствующего способа.
Следующая цель настоящего изобретения - создание устройства регулирования работы внутреннего органа или канала, которое бы имело дистанционное управление, обеспечивало бы высокую степень безопасности и с высокой степенью надежности осуществляло воспроизводимый уровень сжатия, а также соответствующего способа.
Следующая цель изобретения - создание устройства регулирования работы внутреннего органа или канала, которое обеспечивало бы поддержание постоянного наружного диаметра и не выходило бы из строя в результате врастания ткани или обволакивания волокнистой тканью, а также соответствующего способа.
Наконец, еще одна цель изобретения - создание устройства регулирования работы внутреннего органа или канала, регулирование которого мог бы осуществлять сам врач неинвазивным, безопасным и несложным образом без необходимости использования рентгенографии, а также соответствующего способа.
Эти и другие цели настоящего изобретения достигают посредством создания устройств и способов, при которых в тело пациента лапароскопическим методом имплантируют негидравлическое кольцо и связанный с ним имплантируемый регулятор, в результате чего кольцо охватывает орган или канал и обеспечивает контролируемую степень их сжатия. Кольцо согласно изобретению имеет жесткий дорсальный периферийный участок, поддерживающий постоянным наружный диаметр, и пружинный участок, который позволяет облегчить лапароскопическую имплантацию устройства и обеспечивает такую степень податливости, при которой возможны конвульсивные движения этого органа или канала, что улучшает переносимость данного устройства.
В соответствии с принципами, положенными в основу настоящего изобретения, кольцо снабжено высокоточным и энергосберегающим механическим приводным механизмом, сохраняющим определенный диаметр кольца при отсутствии электропитания устройства в течение длительного периода. Имплантируемый регулятор имеет дистанционное электропитание и управление, что устраняет необходимость повторной операции для восстановления или замены неисправного или разрядившегося источника питания.
В соответствии с одним из предпочтительных вариантов реализации кольцо снабжено высокоточным двигателем, который осуществляет обратимое сжатие органа или канала при приведении в действие двигателя, причем степень сжатия может быть легко определена без необходимости проведения рентгенографического исследования. Кроме того, кольцо содержит гибкий элемент с заданным шагом винтовой резьбы, который обеспечивает высокую точность с сохранением при этом удовлетворительной гибкости. На свободном конце гибкого элемента предусмотрен специальный контакт, который соединен с электрическим выключателем, предназначенным для определения исходного положения кольца, соответствующего полностью открытому состоянию.
Дополнительно, кольцо содержит мягкую гибкую деталь из растянутого политетрафторэтилена (ePTFE), окруженную герметичной гибкой мембраной, обеспечивающую наличие гладкой контактной поверхности с органом или каналом, что дает кольцу возможность претерпевать значительное сужение диаметра без формирования при этом волнистых участков или пучков в лежащем под ним органе или канале.
Кольцо согласно изобретению снабжено неинвазивным и простым в использовании внешним блоком управления, который может быть использован самим врачом и регулировку посредством которого можно осуществлять в амбулаторном порядке без необходимости рентгенографического подтверждения. Кроме того, конфигурация кольца и имплантируемого регулятора выбрана с таким расчетом, чтобы их можно было легко вводить через имеющийся в продаже 18-миллиметровый троакар и имплантировать с применением традиционных лапароскопических методов.
Предлагаются также способы имплантации устройства согласно изобретению.
Краткое описание чертежей
Перечисленные выше и другие объекты изобретения будут более понятны из нижеследующего подробного описания в сочетании с приложенными графическими материалами, где одинаковые элементы обозначены одними и теми же цифровыми позициями, и на которых:
На фиг.1 представлено аксонометрическое изображение типовой кольцевой системы согласно изобретению, в состав которой входят внешний блок управления и имплантируемое кольцо;
На фиг.2А и 2В представлены соответственно схематическое изображение, частично в поперечном сечении, желудочного бандажа согласно фиг.1 и вид бандажа, представленного на фиг.2А, в разрезе по линии 2В-2В;
На фиг.3А и 3В - аксонометрические изображения, иллюстрирующие степень сжатия, оказываемого желудочным бандажом согласно изобретению, в диапазоне между полностью открытым и полностью закрытым положениями;
На фиг.4А и 4В - виды желудочного бандажа согласно изобретению в поперечном разрезе по линиям 4А-4А и 4В-4В, обозначенным соответственно на фиг.3А и 3В;
На фиг.5 - фрагментарное аксонометрическое изображение участка винтовой резьбы растягивающегося элемента согласно изобретению;
На фиг.6 - аксонометрическое изображение растягивающегося элемента целиком, предназначенного для использования в желудочном бандаже согласно изобретению;
На фиг.7 - аксонометрическое изображение растягивающегося элемента, представленного фиг.6, соединенного с жестким дорсальным периферийным участком и кожухом двигателя желудочного бандажа;
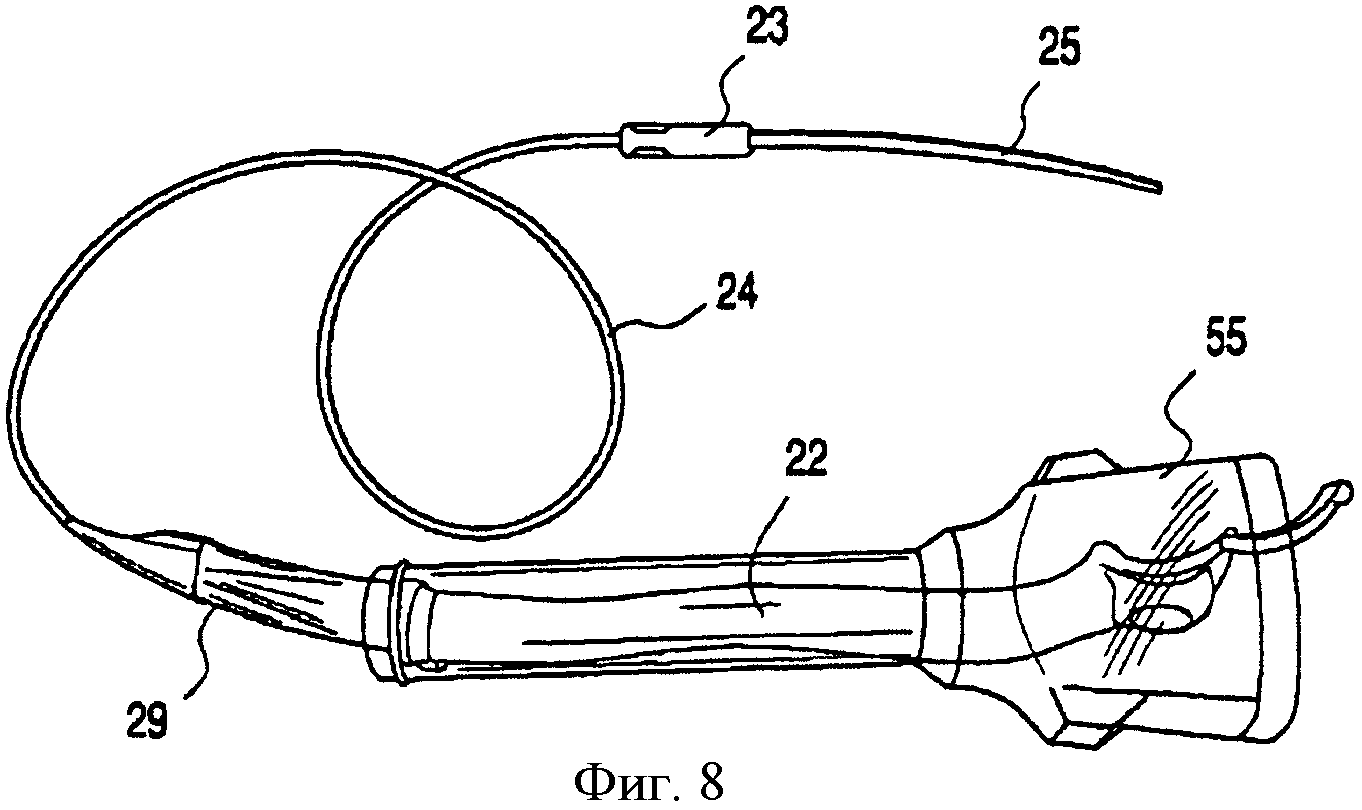
На фиг.8 - аксонометрическое изображение желудочного бандажа, представленного на фиг.1, который разогнут и вставлен внутрь стандартного 18-миллиметрового троакара;
На фиг.9 - вид в поперечном разрезе кожуха желудочного бандажа из эластичного полимера, иллюстрирующий расположение антенного провода и полости для растягивающегося элемента;
На фиг.10 - аксонометрическое изображение кожуха приводного механизма, растягивающегося элемента и самого приводного механизма согласно изобретению;
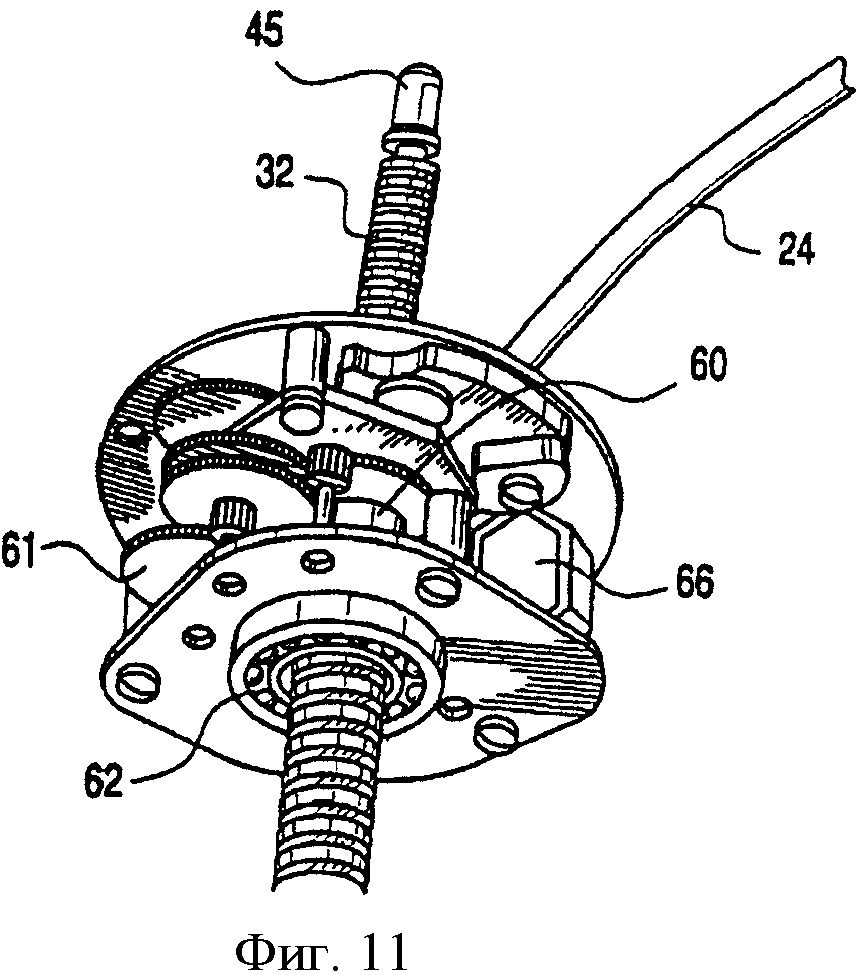
На фиг.11 - аксонометрическое изображение растягивающегося элемента, находящегося в зацеплении с приводным механизмом;
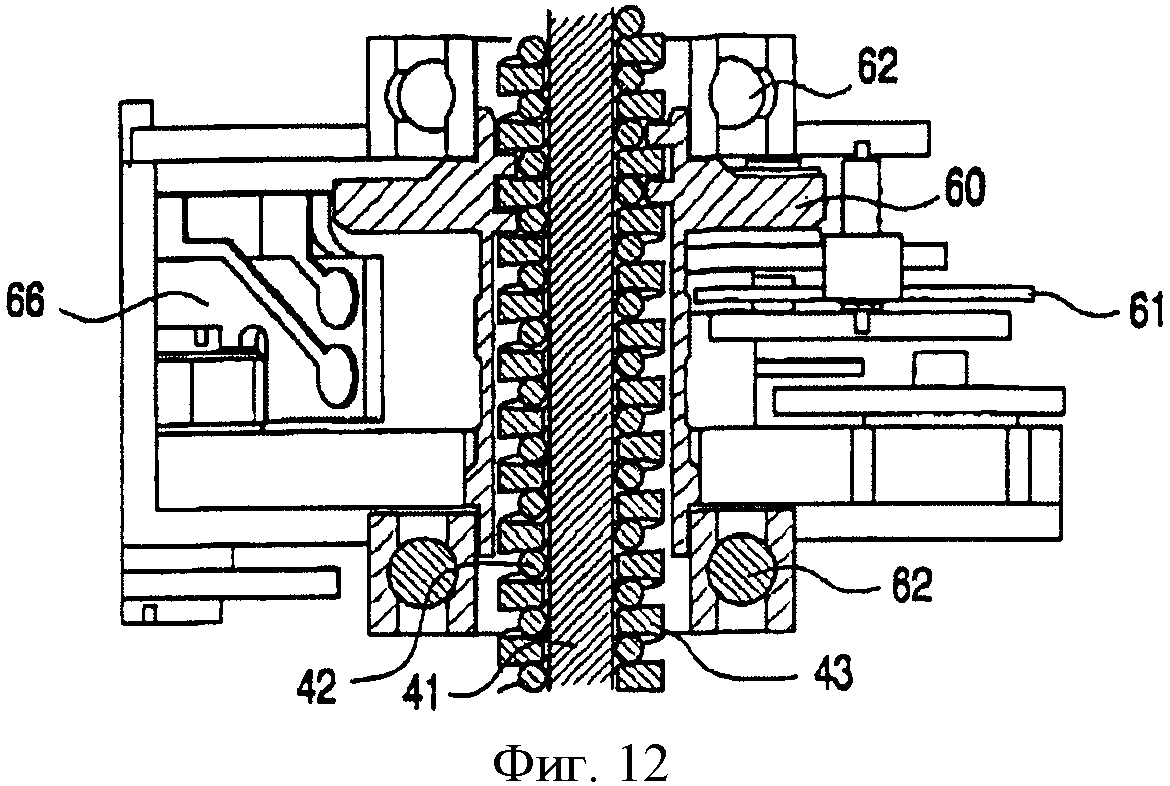
На фиг.12 - вид в поперечном разрезе, иллюстрирующий конструкцию приводного механизма согласно фиг.11;
На фиг.13 - вид в поперечном разрезе, иллюстрирующий конструкцию выключателя исходного положения;
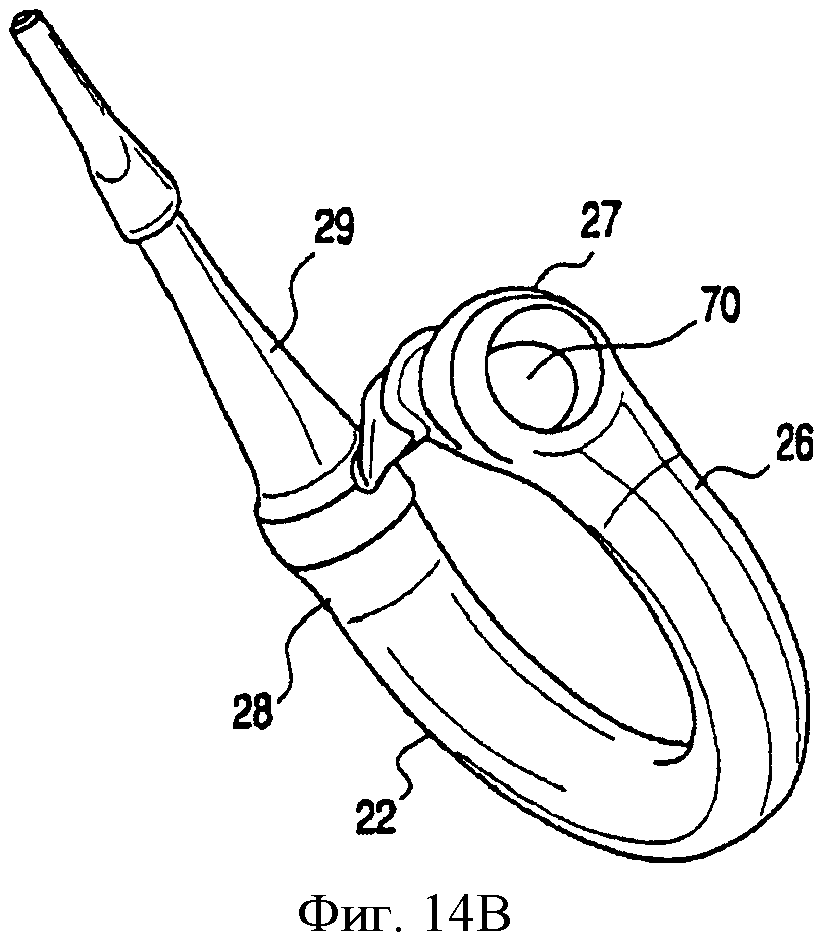
На фиг.14А и 14В - аксонометрические изображения, иллюстрирующие зажим, предназначенный для замыкания желудочного бандажа с формированием петли;
На фиг.15 - аксонометрическое изображение антенно-регуляторной капсулы согласно изобретению;
На фиг.16 - изображение в разрезе внутренней части имплантируемой антенно-регуляторной капсулы согласно фиг.15;
На фиг.17 - вид антенного кабеля, согласно фиг.15, в поперечном разрезе;
На фиг.18 - блок-схема блока дистанционного электропитания и управления согласно изобретению;
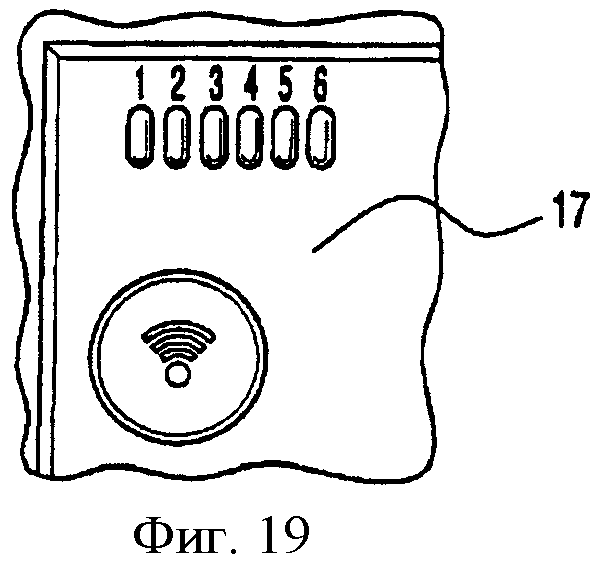
На фиг.19 - фрагментарное изображение участка индикатора уровня сигнала в блоке дистанционного управления, представленном на фиг.1А;
На фиг.20 - схематическое изображение, иллюстрирующее внедрение в тело пациента имплантируемой части устройства согласно изобретению;
На фиг.21А-21Н - изображения, иллюстрирующие способ лапароскопической имплантации в тело пациента желудочного бандажа согласно изобретению.
Предпочтительный(ые) вариант(ы) реализации изобретения
Согласно изображению, представленному на фиг.1, можно видеть, что предлагаемая система бандажирования содержит внешний пульт 10 управления и имплантируемый желудочный бандаж 21. В последующем тексте описания в качестве иллюстрации речь будет идти о желудочном бандаже, предназначенном для имплантации в зону вокруг желудка с целью избирательного регулирования диаметра просвета сужения и, соответственно, объема потребляемой пищи. Такое регулирование позволяет создать у пациента ощущения сытости после потребления относительно небольшого количества пищи, что обеспечивает эффективное лечение морбидного ожирения.
Однако следует иметь в виду, что настоящее изобретение не ограничивается одной лишь гастропластикой, - напротив, его можно с успехом применить и для регулировки функционирования других внутренних органов или каналов, как, например, в случае лечения гастроэзофагеального рефлюкса, недержания мочи или кала, при колостомии и илеостомии, или для регулирования кровотока при перфузии изолированных органов в ходе лечения рака. В случае лечения недержания мочи имплантируемый участок системы следует вживлять в зону вокруг мочевого пузыря или мочевых путей, тогда как при недержании кала кольцо можно имплантировать вокруг какого-либо отрезка желудочно-кишечного тракта, например анальных структур кишечника.
Краткое описание системы
Как видно на фиг.1, автономный внешний пульт 10 управления имеет кожух 11 с панелью управления 12 и экраном дисплея 13. Внешний пульт 10 управления включает в себя цифровой процессор обработки сигналов, и он может получать электропитание либо от батареи, либо от какого-либо внешнего источника (например, подключаться к стенной розетке). К пульту 10 дистанционного управления посредством кабеля 15 подключена внешняя антенна 14. Как описано более подробно при рассмотрении фиг.18, внешний пульт 10 управления содержит микропроцессор, который контролирует передачу высокочастотных сигналов на желудочный бандаж 10, предназначенных для управления его работой и обеспечения его электропитанием.
Во внешний пульт 10 управления может быть вставлена снабженная микрочипом карточка 16 пациента, которая соответствует конкретному желудочному бандажу, имплантированному в тело данного пациента, и обеспечивает хранение таких данных, как идентификационный номер имплантата, параметры регулирования (например, верхний и нижний пределы диапазона регулировки и т.д.) и информацию о последнем положении регулировки кольца. В состав внешнего пульта 10 управления входят индикатор 17 уровня связи, рассмотренный более детально далее применительно к фиг.19, кнопка 18 ВКЛ./ВЫКЛ., кнопка 19а ОТКР., кнопка 19b ЗАКР., кнопка 19с СВЯЗЬ и панель 20 с перечнем меню.
В процессе эксплуатации устройства врачу надо всего лишь включить внешний пульт 10 управления с помощью кнопки 18 ВКЛ., поместить внешнюю антенну 14 на грудь пациента над антенно-регуляторной капсулой 23, проверить связь нажатием кнопки 19с СВЯЗЬ и по достижении достаточного уровня связи отрегулировать степень сжатия с помощью кнопки 19а ОТКР. или кнопки 19b ЗАКР. Диаметр бандажа непрерывно отображается на экране дисплея 13 с точностью порядка 0,1 мм для всего диапазона диаметров кольца, например от 19 мм для полностью закрытого положения до 29 мм для полностью открытого положения.
Как изображено на той же фиг.1, желудочный бандаж 21 содержит кольцо 22, связанное с помощью кабеля 24 с имплантируемой антенно-регуляторной капсулой 23. Эта капсула 23 снабжена съемным наконечником 25, который может быть использован для установки кольца 22 лапароскопическим методом. Кольцо 21 имеет первый конец 26, снабженный зажимом 27, который надевается посредством скольжения и образует со вторым концом 28 кольца надежное зацепление.
Как будет подробно разъяснено далее, кольцо 22 выполнено с возможностью разгибания, что обеспечивает его проход через просвет обычного 18-миллиметрового троакара с целью внедрения его в брюшную полость пациента. Затем наконечник 25, капсулу 23 и кабель 24 пропускают через зажим 27 с формированием кольца в виде, по существу, круглой петли вокруг верхнего отдела желудка пациента, что обеспечивает уменьшение диаметра просвета желудка. Будучи в недеформированном состоянии, кольцо 22 приобретает форму дуги окружности, при которой облегчается установка кольца вокруг желудка и которая также направляет процесс его скрепления при помощи зажима.
Кольцо 22 согласно изобретению представляет собой гибкую трубчатую полоску с гладкой, гибкой и эластичной мембраной, благодаря которой обеспечивается нетравматичный контакт с желудочной тканью пациента, который довольно легко переносится. Находясь в зацеплении с дорсальным элементом 38, мембрана 39 претерпевает определенное растяжение (на 20-40%), в результате чего, когда кольцо 22 находится в полностью закрытом положении, на поверхности мембраны либо вообще не образуется морщин, либо образуются лишь очень небольшие морщины. Кольцо 22 имеет форму приблизительно тора вращения с, по существу, цилиндрическим поперечным сечением. В соответствии с другим вариантом, оно может иметь любое другое подходящее поперечное сечение, включая прямоугольное. Расположенный на втором конце 28 кожух 29, расположенный на первом конце 26 зажим 27 и дорсальный периферийный участок 30 кольца 22 (изображенный на фиг.1 в виде более темного участка кольца) предпочтительно содержат какой-либо биологически совместимый материал, например силикон. Внутренний участок 31 кольца 22 предпочтительно содержит вытянутый политетрафторэтилен (вПТФЭ (ePTFE)), обеспечивающий возможность продольного сжатия без образования пучков или волн, и это участок покрыт тонкой мембраной из защитного материала, например силикона или на основе силикона.
Предпочтительно участки кольца 22, изображенного на фиг.1, выполнены из полимерных компонентов разного цвета, что позволит облегчить лапароскопические манипуляции и процесс имплантации. В соответствии с одним из предпочтительных вариантов реализации, для внутреннего участка 31 кольца использованы материалы более светлой окраски, а зажим 27 и кожух 29 выполнены из материалов более темной окраски, благодаря чему врач может видеть, за какие участки кольца 22 можно осуществлять захват в процессе имплантации. В частности, может быть использован черный цвет, белый цвет и различные оттенки серого, которые можно создать посредством используемого в имплантации силикона.
Имплантируемое кольцо
Перейдем к рассмотрению фиг.2А и 2В, где проиллюстрировано внутреннее устройство кольца 22. В частности, как видно из фиг.2А, кольцо 22 содержит гибкий растягивающийся элемент 32, который имеет зафиксированный конец 33, закрепленный в первом конце 26 кольца, и свободный конец 34, который находится в зацеплении с приводом 35, приводимым в движение двигателем, и который заходит в полость, выполненную в кожухе 29. Растягивающийся элемент 32 помещен с возможностью скольжения в, по существу, цилиндрическую трубку из сжимающегося материала 36, например из вПТФЭ, которая представлена на фиг.2В, в результате чего, когда растягивающийся элемент протягивается через приводной механизм 35, сжимающийся материал 36 претерпевает сжатие и диаметр просвета 37 сокращается. Предпочтительно, чтобы сжимающийся материал 36 был окружен с дорсальной стороны гибким, но менее податливым эластичным полимерным материалом, например силиконовым элементом 38. Как сжимающийся материал 36, так и силиконовый элемент 38 предпочтительно окружены, как проиллюстрировано на фиг.2В, мембраной 39 из эластичного полимерного биологически совместимого материала, что предотвращает прорастание ткани между трубкой из вПТФЭ и силиконовым элементом 38. Мембрана 39 может быть прикреплена к дорсальному элементу 38 посредством биологически совместимого клея, что предотвратит протечку при случайном проколе дорсальной поверхности.
В соответствии с одним из аспектов настоящего изобретения кольцо 22 содержит также слой 40 относительно жесткого материала, расположенный на дорсальной периферии этого кольца. Слой 40, который может содержать пластик или металлический сплав, препятствует изменению наружного диаметра кольца 22 при уменьшении внутреннего диаметра 37 кольца в процессе регулировки растягивающегося элемента. Благодаря своей структурной жесткости слой 40 обеспечивает сохранение формы кольца 22 в виде дуги окружности. Позитивная роль слоя 40 состоит в том, что он обеспечивает возможность регулировки растягивающегося элемента при обволакивании после имплантации желудочного кольца волокнистой тканью, поскольку регулирование внутреннего диаметра 37 этого кольца не приводит к изменению его наружного диаметра.
Упомянутый выше признак проиллюстрирован на фиг.3 и 4. На фиг.3А и 3В кольцо 22 изображено соответственно в полностью открытом и полностью закрытом положениях. Как описано выше, слой 40 образует жесткий каркас, который позволяет изменять внутренний диаметр кольца с сохранением при этом постоянного наружного диаметра. Радиальное перемещение растягивающегося элемента 32 передается посредством сжимающегося материала 36 на мембрану 39. В качестве сжимающегося материала 36 особенно предпочтительно использовать вПТФЭ, так как этот материал способен претерпевать уменьшение длины в соотношении 3:1 без сколько-нибудь заметного увеличения поперечного сечения.
Соответственно, как изображено на фиг.4А и 4В, увеличение или уменьшение длины растягивающегося элемента 32 приводит к обратимому радиальному смещению внутренней периферии кольца, противоположной по отношению к дорсальной периферии. Это, в свою очередь, ведет к изменению внутреннего диаметра D кольца в диапазоне от диаметра, соответствующего полностью открытому положению, до диаметра, соответствующего полностью закрытому положению. Предпочтительно, чтобы «полностью открытый» диаметр составлял порядка 35 мм, а «полностью закрытый» - порядка 15 мм. Более предпочтительно, чтобы полностью отрытый диаметр составлял 29 мм, а полностью закрытый - 19 мм.
Обратимся теперь к фиг.5, где изображен растягивающийся элемент 32. Растягивающий элемент 32 предпочтительно должен иметь достаточную гибкость, которая позволит ему придать, по существу, круглую форму, соответствующую форме кольца, но одновременно он должен быть способным сообщать усилие, необходимое для регулирования диаметра кольца. Итак, растягивающийся элемент 32 содержит гибкий сердечник 41, предпочтительно в виде проволоки из металлического сплава с круглым поперечным сечением, на котором закреплена и намотана коаксиально, по меньшей мере, одна винтовая пружина с непримыкающими друг к другу витками, имеющая определенный шаг винтовой резьбы.
Как проиллюстрировано на фиг.5, растягивающийся элемент 32 предпочтительно содержит две винтовые пружины с непримыкающими витками, образующие шаг резьбы: первую пружину 42, намотанную по спирали вдоль гибкого сердечника 41, и вторую пружину 43 с бóльшим наружным диаметром. Вторая пружина 43 предпочтительно содержит витки 44 прямоугольного поперечного сечения, описывающие плоские наружные образующие поверхности. Первая пружина 42 помещена между витками 44 второй пружины 43, что позволяет задать и поддерживать практически постоянный прямоугольный шаг винтовой резьбы, даже когда растягивающийся элемент подвергают изгибу.
Благодаря описанной выше конструкции способность растягивающегося элемента 32 при его изгибе поддерживать шаг резьбы, по существу, постоянным позволяет достичь высокой точности регулировки кольца 22.
Особенно это важно, когда при протягивании растягивающегося элемента 32 через приводной механизм 35 оставшаяся часть этого растягивающегося элемента приобретает все возрастающую кривизну. Однако, учитывая, что описанная выше конструкция из винтовых пружин с непримыкающими друг к другу витками обеспечивает практически постоянный шаг винтовой резьбы, энергия, необходимая для приведения в движение приводного механизма 35, остается небольшой, а эффективность передачи энергии благодаря использованию прямоугольной винтовой резьбы сохраняется на высоком уровне. Кроме того, использование прямоугольной винтовой резьбы гарантирует стабильность отрегулированного положения даже в случае отсутствия электропитания приводного механизма.
Вторая пружина 43 предпочтительно изготовлена методом лазерной резки цилиндрической полой трубы, выполненной, например, из нержавеющей стали, или же посредством намотки проволоки прямоугольного, трапецеидального или иного поперечного сечения. При спиральном переплетении с первой пружиной 42 витки 44 второй пружины 43 естественным образом активируются благодаря внутренней силе упругого сжатия, действующей со стороны соседних витков первой пружины 42. Следует заметить, что один из концов первой пружины 42 неподвижно соединен с гибким сердечником 41. На другом конце, на небольшом расстоянии от концов пружин 42 и 43, находится гофрированный колпачок 45 (см. фиг.6), обеспечивающий возможность незначительного удлинения (для компенсации кривизны растягивающегося элемента 32), но, одновременно, и ограничивающий это удлинение с целью поддержания шага резьбы, по существу, постоянным.
Рассмотрим теперь растягивающий элемент 32 в целом, со ссылками на фиг.6. На его свободном конце 34 имеются гофрированный колпачок 45, вторая пружина 43 с витками прямоугольного поперечного сечения и первая пружина 42 (на чертеже ее не видно, но она вплетена между витками второй пружины 43). Через первую и вторую пружины 42 и 43 проходит гибкий сердечник 41, который заканчивается вблизи колпачка 45. В соответствии с одним из аспектов настоящего изобретения растягивающийся элемент 32 дополнительно содержит третью пружину 46, которая соединена с гибким сердечником 41 и первой и второй пружинами 42, 43 в точке 47 соединения. Третья пружина 46 имеет на конце, противоположном по отношению к точке 47 соединения, петлю 48, посредством которой растягивающийся элемент можно прикреплять к первому концу 26 кольца 22.
В соответствии с принципами, лежащими в основе настоящего изобретения, третья пружина 46 является относительно жесткой, но при этом обеспечивает растягивающему элементу необходимую степень податливости. Если известные ранее бандажи из эластичных полимеров обеспечивают невысокую степень податливости, то традиционные желудочные бандажи негидравлического типа - такие, как описаны в цитировавшемся выше патенте Dargent'a, - вообще не обладают податливостью. Таким образом, при рвоте, которая часто возникает как осложнение при использовании желудочных бандажей, традиционные бандажи препятствуют судорожным движениям желудка, что чревато очень большим дискомфортом для пациента. Напротив, в конструкции согласно настоящему изобретению третья пружина 46 дает возможность временного расширения желудочного бандажа при судорожных движениях, после чего его заданный внутренний диаметр восстанавливается. Можно ожидать, что указанный признак позволит значительно уменьшить дискомфорт для пациента и ослабить явления непереносимости.
На фиг.7 растягивающийся элемент 32 изображен внутри каркаса 50 желудочного кольца 22. Этот каркас 50 имеет слой 51, который образует дорсальную периферию (соответствует слою 40 на фиг.2 и 5), крючок 52, на который надевается петля 48 растягивающегося элемента 32, и кожух 53 приводного механизма. Каркас предпочтительно содержит высокопрочный формуемый пластик. Как проиллюстрировано также на фиг.7, каркас 50 простирается вдоль дуги окружности большей длины, чем растягивающийся элемент 32. В соответствии с другим аспектом настоящего изобретения третья пружина 46 обеспечивает возможность разгибания желудочного бандажа 21 с целью его введения через стандартный 18-миллиметровый троакар, несмотря на различное удлинение при этом каркаса и растягивающегося элемента. Этот признак проиллюстрирован на фиг.8, где кольцо 22 изображено введенным в 18-миллиметровый троакар 55, при этом указанное кольцо имеет практически прямую форму.
На фиг.9 представлен кожух 29 свободного конца кольца 22. Этот кожух содержит эластичный полимерный материал типа силикона с участком углубления 56, полостью 57 для растягивающегося элемента и внутренним каналом 58 для кабеля. Форма углубления 56 выбрана такой, чтобы в него мог входить входящий в состав каркаса 50 кожух 53 приводного механизма так, что когда растягивающийся элемент 32 протягивается через приводной механизм 35, он размещается в полости 57. Внутренний канал 58 для кабеля имеет в кожухе 29 такое расположение, при котором кабель 24 может быть соединен с приводным механизмом 35. Предпочтительно, кожух 29 выполнен с возможностью захвата за участок G посредством атравматических лапароскопических захватов при манипуляции устройством.
На фиг.10 представлен входящий в состав каркаса 50 кожух 53 приводного механизма с установленным в нем приводным механизмом 35 и проходящим через него растягивающимся элементом 32. К двигателю (не представлен), расположенному в кожухе 53, подсоединен антенный кабель 24. Растягивающийся элемент 32 находится в полностью открытом положении (максимальный диаметр), вследствие чего гофрированный колпачок 45 входит в контакт с печатной платой 59 выключателя исходного положения, описанного далее при рассмотрении фиг.13.
Приводной механизм
Как видно на фиг.11 и 12, приводной механизм 35 содержит двигатель 66, соединенный с антенным кабелем 24 и приводящий в действие через посредство шестерен 61 гайку 60. Гайка 60 поддерживается с помощью верхних и нижних подшипников 62, что обеспечивает сведение к минимуму потерь энергии, обусловленных трением. Эта гайка является самоцентрирующейся, самонаправляющейся и обеспечивает высокое передаточное отношение усилия вращения в осевое усилие. Кроме того, можно полагать, что гайка 60 будет являться более надежной, чем конструкции с тангенциальными винтами, применявшиеся в известных из уровня техники механических желудочных кольцах, и не будет соскакивать или соскальзывать. Дополнительно, гайка 60 выполнена самоконтрящейся, что означает, что гайка 60 не будет проворачиваться при воздействии на растягивающий элемент 32 толкающих или тянущих сил. Это может быть реализовано при том условии, когда отношение высоты (h) резьбы к длине (2πR) окружности винта будет меньше, чем арктангенс коэффициента (µ) трения:
h/(2πR) Шестерни 61 предпочтительно выбирают таким образом, чтобы обеспечить высокий механический КПД, предпочтительно с коэффициентом понижения более 1000. Кроме того, объем приводного механизма, изображенного на фиг.11 и 12, может быть довольно небольшим, так что общий объем будет менее 1 см3 и диаметр менее 12,5 мм, что позволит данному устройству легко проходить через стандартный троакар. В соответствии с одним из предпочтительных вариантов реализации шестерни 61 выбираются таким образом, чтобы обеспечить усилие, прикладываемое к винтовой резьбе растягивающегося элемента, более 2 кг, при потребляемой мощности всего лишь 50 мВт. Шестерни и прочие компоненты приводного механизма 35 предпочтительно выполняют из нержавеющей стали или с покрытием позолотой, что обеспечивает возможность работы в условиях высокой влажности, которые, как правило, имеют место в человеческом теле. Используемый в приводном механизме 35 двигатель 66 предпочтительно представляет собой высокоточный шаговый двигатель типа Lavet с плоской магнитной цепью, подобный используемым в часовых механизмах. Это может быть предпочтительно двухфазный (с двумя обмотками) двигатель, обеспечивающий вращение в обоих направлениях и имеющий высокий КПД, а его питание может представлять собой излучение в виде прямоугольных импульсов, поступающее непосредственно от цепи микроконтроллера, расположенной внутри антенно-регуляторной капсулы 35, что устраняет необходимость в наличии цепи сопряжения. Согласно другому варианту используемый в приводном механизме 35 двигатель может представлять собой бесщеточный двигатель постоянного тока. Кроме того, этот двигатель предпочтительно должен быть совместимым с системами магниторезонансной томографии, то есть оставаться в работоспособном состоянии при воздействии сильных магнитных полей, используемых в медицинских томографических устройствах. Переходим к описанию выключателя исходного положения согласно настоящему изобретению, представленного на фиг.13. Поскольку в приводном механизме согласно изобретению применена гайка 60, приводимая в действие от шагового двигателя, то для определения длины участка растягивающегося элемента 32, протянутого через приводной механизм, нет необходимости включать в состав системы сенсор или датчик положения. Вместо этого можно вычислить диаметр кольца 22 непосредственно как функцию, зависящую от шага винтовой резьбы и числа оборотов гайки 60. Однако для обеспечения точного расчета степени сжатия желудочного кольца желательно предусмотреть по меньшей мере одну точку исходного положения. Такая контрольная точка реализована в желудочном кольце согласно изобретению благодаря использованию специального выключателя исходного положения, который активируется, когда кольцо 22 перемещают в полностью открытое положение. Имеющийся на свободном конце растягивающегося элемента 32 гофрированный колпачок 45 реализует эту функцию посредством замыкания электрических контактов 63 на печатной плате 59 (кроме того, он ограничивает удлинение винтовой резьбы). Печатная плата 59 расположена сразу над подшипником 65, который является составной частью приводного механизма 35 (см. также фиг.10). В момент контакта гофрированного колпачка 45 с контактами 63 происходит замыкание выключателя, который подает на имплантируемый регулятор сигнал о том, что желудочное кольцо находится в полностью открытом положении. Система замыкания кольца На фиг.14А и 14В представлен предпочтительный вариант реализации зажима 27, предназначенного для закрепления желудочного бандажа в замкнутом положении. Находящийся на первом конце 26 желудочного кольца зажим 27 имеет отверстие 70, язычок 71 с шарниром 72 и прорезь 73. Размер отверстия 70 выбирают таким, чтобы через него мог проходить второй конец 28, а размер прорези 73 должен быть таким, чтобы в него мог входить расположенный на втором конце 28 выступ 74. Для замыкания кольца 22 зажим 27 берут за язычок 71 и наконечник 25 капсулы 23 (см. фиг.1) вводят в отверстие 70. Затем натягивают зажим 27 в направлении второго конца 28 таким образом, чтобы кожух 29 прошел через отверстие 70, при этом кожух 29 захватывают атравматическими щипцами; эта операция облегчается благодаря конической форме кожуха 29. К язычку 71 прикладывают усилие до тех пор, пока прорезь 73 не захватит выступ 74, в результате чего желудочное кольцо закрепляется в замкнутом положении. После этого врач может предпочесть, например, с целью изменения положения кольца, разъединить прорезь 73 и выступ 74, манипулируя язычком 71 с помощью атравматических щипцов. Однако преимущество данной конструкции состоит в том, что при случайном воздействии на язычок 71 в противоположном направлении этот язычок будет сгибаться в месте шарнира 72, что не приведет к выходу выступа 74 из прорези 73. Соответственно, предусмотренный в язычке 71 шарнир 72 предотвращает случайное размыкание зажима 70 в случае, когда на язычок 71 действуют силы, вызывающие ее загибание в направлении назад в сторону от кожуха 29, что может происходить, например, вследствие движения пациента, органа или проходящей через орган порции жидкости. Антенно-регуляторная капсула На фиг.15 и 16 представлена антенно-регуляторная капсула 23 согласно настоящему изобретению. Эта капсула, расположенная на дистальном конце кабеля 24, имеет съемный наконечник 25 и отверстия 75. Конструкция наконечника 25 приспособлена для его захвата, что облегчает манипуляции с капсулой и ее позиционирование в процессе имплантации; по завершении имплантации наконечник можно удалить, отрезав его ножницами. Кроме этого, в наконечнике 25 выполнено отверстие 25b, которое обеспечивает возможность использования хирургической нити при проведении антенно-регуляторной капсулы 23 позади желудка. Размер отверстий 75 должен также быть согласован со стандартными хирургическими иглами с размерами от 1-0 до 7-0, что обеспечит возможность пришивания капсулы 23 к грудине пациента, в этом положении капсула 23 будет доступна для внешней антенны и не сможет самостоятельно смещаться из зоны имплантации. Как видно на фиг.16, внутрь антенно-регуляторной капсулы 23 помещена печатная плата 76, на которую нанесены схемы антенны и микроконтроллера желудочного бандажа 22. Антенна получает электропитание и команды от внешнего пульта 10 управления (см. фиг.1) и передает эти сигналы на микроконтроллер, который, в свою очередь, обеспечивает питанием двигатель 66 приводного механизма 35. Схема антенно-регуляторной капсулы 23 использует энергию, поступающую с входным сигналом, для электропитания схемы, интерпретирует команды, получаемые из внешнего пульта 10 управления, и посылает соответствующие сигналы на двигатель приводного механизма 35. Кроме того, эта схема также извлекает информацию о функционировании двигателя приводного механизма 35 и передает эту информацию через антенну на внешний пульт 10 управления. Печатная плата предпочтительно покрыта специальным водостойким полимерным покрытием, например, из парилена, что позволяет использовать ее в условиях высокой влажности (до 100%), которые имеют место в теле пациента. Антенно-регуляторная капсула 23 содержит механическую замыкающую систему, которая усилена силиконовым клеем, благодаря чему капсула становится влагонепроницаемой. Этот силиконовый клей используют также для защиты припаянных проводов 79 от влаги. Капсула имеет небольшие размеры, например 16×33×4 мм, благодаря чему она может быть совместима со стандартным 18-миллиметровым троакаром и может быть помещена на грудине. Предпочтительно капсула имеет гладкую атравматическую форму во избежание повреждения тканей, достаточную механическую прочность для того, чтобы выдержать манипуляции с хирургическими захватами и предотвратить механическую деформацию печатной платы, а также высокую электромагнитную проницаемость, при которой возможна эффективная передача энергии через эту капсулу. Предпочтительно, чтобы антенно-регуляторная капсула 23 имела относительно тонкую плоскую конфигурацию, которая бы препятствовала ее поворотам при установке под кожей, и чтобы капсула была снабжена отверстиями для ее пришивания в нужном положении. На фиг.17 изображен в поперечном сечении антенный кабель 24. Кабель 24 предпочтительно представляет собой коаксиальный экранированный кабель, окруженный для обеспечения биологической совместимости силиконовой трубкой 77. Трубку 77 выбирают таким образом, чтобы обеспечить герметичную изоляцию с прочностью, достаточной для того, чтобы кабелем можно было манипулировать с помощью атравматических захватов. Экранирующая оплетка 78 кабеля предохраняет его от продольной деформации и охватывает пять спирально смотанных изолированных проводов 79. Четыре провода используются для подачи электропитания на микродвигатель приводного механизма 35, а оставшийся провод и экранирующую оплетку 78 - для передачи сигнала от выключателя исходного положения на регулятор. Как было описано ранее при рассмотрении фиг.1, желудочный бандаж согласно настоящему изобретению представляет собой интегрированную систему для регулирования проглатывания пищи в желудке пациента, при этом диаметр желудочного кольца можно регулировать без какого бы то ни было инвазивного хирургического вмешательства. Для этой цели приводной механизм 35 связан с подкожной антенно-регуляторной капсулой 23, обеспечивающей прием высокочастотного управляющего и питающего сигнала. В соответствии с предпочтительным вариантом реализации двигатель приводного механизма не имеет внутреннего источника энергии, а получает питание от приемной цепи антенны через посредство специального перезаряжаемого устройства хранения энергии, например конденсатора. В частности, приемная цепь преобразует высокочастотные колебания, поступающие через антенну из внешнего пульта 10 управления, в сигнал управления и питания двигателя. Согласно другому, правда, менее предпочтительному варианту приводной механизм может получать питание от специальной имплантируемой перезаряжаемой батареи. Цепи электропитания и управления Ниже описан, со ссылками на фиг.18, предпочтительный вариант реализации внешнего пульта 10 управления и желудочного бандажа 22 согласно настоящему изобретению, основанный на применении принципа пассивной телеметрии посредством ЧМ-АМ-модуляции поглощения. Внешний пульт 10 управления, изображенный в левой части схемы, содержит микропроцессор 80, соединенный с панелью 12 управления и дисплеем 13 (см. фиг.1). Внешний пульт 10 управления вырабатывает сигнал, состоящий из одного или более информационных байтов, который передается в имплантируемую антенно-регуляторную капсулу 23 и приводной механизм 35 (изображены в правой части схемы фиг.18). Внешний пульт 10 управления содержит модулятор 81, предназначенный для амплитудной модуляции ВЧ-излучения, поступающего от ВЧ-генератора 82, а далее эти сигналы излучаются внешней антенной 14. Эти колебания принимает антенна 83, предусмотренная в антенно-регуляторной капсуле 23, где AM-демодулятор 84 обеспечивает выделение информационных байтов из огибающей принятого ВЧ-сигнала. Далее производятся декодирование информационных байтов и их запись в ЭСППЗУ (электрически стираемое программируемое постоянное запоминающее устройство) микроконтроллера 85. При этом применяется специальный код, обеспечивающий беспрепятственное декодирование данных в микроконтроллере 85, а, кроме того, максимально надежную защиту от сбоев связи. Имеется внешний генератор 86, который является генератором, управляемым напряжением (VCO), который вырабатывает синхронизирующий сигнал, поступающий в микроконтроллер 85. Генератор 86 может представлять собой, например, генератор релаксационных колебаний, содержащий внешнюю резистивно-емкостную цепь, соединенную с разрядной логической схемой, которая уже встроена в микроконтроллер, или же кварцевый генератор, содержащий резонансный контур с пьезокристаллом, конденсаторы и логические схемы. Для первого из этих технических решений требуются только два дополнительных компонента, оно пригодно в тех случаях, когда стабильность частоты не имеет решающего значения, и это решение отличается невысокой потребляемой мощностью; что касается второго варианта, то он обеспечивает более высокую стабильность частоты, однако требует применения большего числа дополнительных компонентов и потребляет больше мощности. Генератор 86 предпочтительно содержит внешнюю RC-цепь, поскольку она является довольно простой. Микроконтроллер 86 интерпретирует принимаемые команды и вырабатывает выходной сигнал, приводящий в действие двигатель приводного механизма 35. Как говорилось выше, приводной механизм 35 содержит реверсивный шаговый двигатель, который приводит в действие гайку 60 через посредство ряда понижающих шестерен. Предпочтительно, чтобы две обмотки шагового двигателя приводного механизма 35 были соединены непосредственно с микроконтроллером 85, который принимает рабочие команды от демодулятора 84, интерпретирует их и вырабатывает последовательности напряжений, подаваемые на обмотки двигателя. Шестерни выполнены таким образом, что при прекращении подачи на шаговый двигатель импульсов напряжения они остаются неподвижными, даже если к гайке 60 со стороны растягивающегося элемента 32 приложен в противоположном направлении крутящий момент или усилие. Кроме этого, как описано выше, благодаря использованию в приводном механизме 35 шагового двигателя, становится возможным получение информации о положении гайки 60 и растягивающегося элемента 32 даже в отсутствие сенсоров или датчиков положения, поскольку перемещение растягивающегося элемента 32 пропорционально количеству импульсов, поступающих на обмотки шагового двигателя. Для достижения точного регулирования используют два сигнала - сигнал исходного положения SRP, вырабатываемый выключателем исходного положения, изображенным на фиг.13, и сигнал приводного механизма SA. В соответствии с одним из предпочтительных вариантов реализации сигнал SA представляет собой сигнал напряжения, принимаемый на одном из выходов микроконтроллера 85, соединенного с обмотками двигателя приводного механизма 35. Согласно другому варианту этот сигнал SA может быть производным от тока, подаваемого на обмотку двигателя, а не от напряжения, или может представлять собой напряжение, наведенное во вторичной обмотке, намотанной вокруг одной из обмоток двигателя приводного механизма 35. В любом случае сигнал SA будет являться импульсным сигналом, который содержит информацию о количестве совершенных ротором шагов и, кроме того, указание о том, имела ли место блокировка механизма. Если говорить более конкретно, то если ротор шагового двигателя не может вращаться, то происходит возмущение магнитопровода, который посредством индукции воздействует на сигнал SA, например, изменяя его форму. Это возмущение может быть зарегистрировано во внешнем пульте управления, как будет описано ниже. Сигналы SA и SRP преобразуются в частоты при помощи внешнего генератора 14, в результате чего уровень напряжения в сигнале SA, поступающем на внешний генератор 86, вызывает пропорциональное сигналу SA изменение частоты Fosc генератора. Таким образом, Fosc будет содержать всю информацию, которую несет сигнал SA. Когда гофрированный колпачок 45 и растягивающийся элемент 32 находятся в исходном положении (желудочное кольцо 22 полностью открыто), выключатель исходного положения вырабатывает сигнал исходного положения SRP. Сигнал SRP используется для индуцирования постоянного сдвига для частоты Fosc, причем это сдвиг будет легко отличим от изменений, обусловленных сигналом SA. Если в качестве генератора 86 используется генератор релаксационного типа, как описано выше, то сигналы SA и SRP изменяют зарядный ток внешней резистивно-емкостной цепи. В этом случае релаксационный генератор предпочтительно содержит внешнюю резистивно-емкостную цепь, подключенную к транзистору и логической схеме, реализованную в микроконтроллере 85. Назначение сигналов SA и SRP состоит в изменении зарядного тока конденсатора RC-цепи, что приводит к изменению частоты релаксационного генератора. Если зарядный ток невелик, то напряжение на конденсаторе будет медленно расти, а когда будет достигнут порог транзистора, произойдет разряд конденсатора через этот транзистор. Частота цикла заряда-разряда определяется величиной зарядного тока. Если же в качестве генератора 86 используется кварцевый генератор, то сигналы SA и SRP изменяют емкость резонансного контура. В этом случае схема кварцевого генератора предпочтительно содержит пьезоэлемент, подключенный параллельно конденсаторам, при этом пьезоэлемент и конденсаторы образуют резонансный контур, который генерирует сигналы на фиксированной частоте. Эту частоту можно регулировать путем изменения емкости. Если одной из этих емкостей является варикап (разновидность диода), то значение его емкости можно варьировать посредством изменения приложенного к нему обратного напряжения, а для изменения этого напряжения можно использовать сигналы SA и SRP. В любой из рассмотренных выше ситуаций сигналы SA и SRP используются для изменения по меньшей мере одного параметра резистивно-емкостной (RC) цепи, связанной с генератором 14, или по меньшей мере одного параметра кварцевого генератора, который входит в состав генератора 14. Как можно видеть из той же схемы на фиг.18, SA и SRP, получаемые от шагового двигателя или из выходного сигнала микроконтроллера 85, могут быть непосредственно использованы для реализации частотной модуляции в генераторе 86 без какого бы то ни было кодирования или влияния микроконтроллера 85. Благодаря использованию генератора 86 микроконтроллера 85 в качестве составной части управляемого напряжением генератора (VCO), генерирующего сигнал обратной связи, отпадает необходимость в каких-либо дополнительных компонентах, при этом изменение частоты генератора Fosc не воздействует неблагоприятным образом на микроконтроллер 85. Сигнал генератора Fosc приводит в действие работающий от напряжения выключатель 87, предназначенный для модуляции поглощения, вследствие чего осуществляется передача сигнала обратной связи посредством пассивной телеметрии с использованием ЧМ-АМ-модуляции поглощения. Если говорить более конкретно, сигнал Fosc приводит в действие выключатель 87 таким образом, что в положении ВКЛ. этого выключателя происходит повышенное поглощение энергии ВЧ-Пост.Ток преобразователем 88. Соответственно, уровень поглощения модулируется при этом с частотой Fosc, и, таким образом, частота амплитудной модуляции отраженного излучения, детектируемого во внешнем пульте 10 управления, содержит информацию о сигнале SA. Как будет описано далее, имеющийся во внешнем пульте 10 управления датчик 90 выделяет отраженное излучение, которое может быть декодировано посредством ЧМ-демодуляции в демодуляторе 90 с получением сигнала SA'. Таким образом, предложенный способ обеспечивает передачу различных сигналов на разных частотах и имеет то преимущество, что состояние ВКЛ. выключателя 87 может быть очень кратковременным, а поглощение чрезвычайно интенсивным, что при этом не вызовет увеличения среднего потребления. Благодаря этому передача сигнала обратной связи оказывается менее чувствительной к изменению качества связи между антеннами 83 и 14. Во внешнем пульте 10 управления сигнал обратной связи Fosc детектируется датчиком 89 и подается на ЧМ-демодулятор 90, который вырабатывает выходное напряжение VOUT, пропорциональное Fosc. Это напряжение VOUT подается в фильтр 91 и детектор 92 уровня для получения информации, соответствующей управляющему сигналу SA, который, в свою очередь, соответствует импульсам, подаваемым на обмотку шагового двигателя. Микропроцессор 80 отсчитывает эти импульсы и рассчитывает соответствующее перемещение растягивающегося элемента 32, которое пропорционально количеству импульсов. Сигнал VOUT пропускается также через аналого-цифровой преобразователь 93, цифровой выходной сигнал которого подается в микропроцессор 80, где осуществляется обработка сигнала с целью обнаружения искажений формы сигнала обратной связи, которые могли бы свидетельствовать о блокировке ротора шагового двигателя. Микропроцессор 80 прекращает отсчет любых детектированных импульсов двигателя, когда он обнаруживает, что приводной механизм заблокирован, и выдает указание этого состояния. Детектор 94 уровня вырабатывает выходной сигнал, когда он обнаруживает, что демодулированный сигнал VOUT указывает на наличие сигнала исходного положения SRP, вызванного активацией выключателя исходного положения. Этот выходной сигнал обеспечивает повторную установку положения растягивающегося элемента, вычисляемого микропроцессором 80 во внешнем пульте управления. Благодаря этому становится возможной коррекция небольших неточностей, например сдвигов. Как следует из приведенного выше описания, внешний пульт 10 управления передает в схему имплантируемого регулятора, находящуюся в антенно-регуляторной капсуле 23, как электропитание, так и команды. Кроме того, этот внешний пульт 10 управления принимает от имплантируемого регулятора информацию обратной связи, которая находится в зависимости от положения растягивающегося элемента и диаметра кольца. Как должно быть очевидно специалистам в данной области техники, внешний пульт 10 управления и имплантируемый регулятор образуют систему «ведущий-ведомый», где имплантируемый регулятор является полностью пассивным элементом, ожидающим команд и электропитания от внешнего пульта 10 управления. Режимы работы Перейдем теперь к рассмотрению фиг.19, которая иллюстрирует некоторые признаки системы согласно настоящему изобретению, относящиеся к его безопасности. Как описано выше применительно к схеме на фиг.18, из внешнего пульта 10 управления в имплантируемый регулятор поступают как электропитание, так и управляющие сигналы. Поскольку питание подается в имплантируемый регулятор посредством магнитной индукции, количество энергии, поступающей в этот регулятор, зависит от качества связи между внешней антенной 14 и антенной цепью, расположенной в антенно-регуляторной капсуле 23. Качество связи можно оценить путем анализа уровня сигнала обратной связи, принимаемого внешним пультом 10 управления, при этом возможна индикация показателей, соответствующих этому параметру, на индикаторе 17 уровня сигнала, который содержит 6 СИДов (соответствующих шести уровням связи). Если связь между антеннами недостаточна, двигатель приводного механизма 35 не сможет функционировать нормально, что может привести к неточностям при регулировке желудочного бандажа 21. Следовательно, при работе в стандартном режиме работы реализация регулировки возможна только лишь в том случае, если качество связи достаточно высокое, что можно видеть, если будет зажжен по меньшей мере СИД 5 или СИД 6, изображенные на фиг.19. Если же, напротив, имеет место слабая связь (например, зажжен один из первых четырех светодиодов), тогда все еще можно реализовать некоторую регулировку устройства, хотя такая регулировка может оказаться неточной. Кроме того, конструкция внешнего пульта 10 управления в сочетании с карточкой 16 пациента, снабженной микрочипом, (см. фиг.1) обеспечивает высокую степень эффективности и безопасности. Прежде всего, будучи разработанным для совместной работы с желудочным бандажом 21 согласно изобретению, внешний пульт 10 управления рассчитан, в первую очередь, на использование врачом в кабинете или в условиях стационара, а не пациентом в одиночку. Разумеется, некоторые альтернативные варианты реализации, относящиеся, например, к лечению недержания мочи или кала, могут предусматривать наличие такого внешнего пульта управления, которым мог бы управлять сам пациент. При использовании таких вариантов простота конструкции внешнего пульта управления и удобство пользования им позволят пациенту справиться с этой задачей безо всякого труда. Как уже было упомянуто при рассмотрении фиг.1, на снабженной микрочипом карточке 16 пациента хранятся, среди прочих данных, серийный номер, идентифицирующий соответствующий желудочный бандаж, и диаметр кольца, установленный по завершении предыдущей регулировки. Когда внешний пульт управления первый раз передает энергию в имплантируемый регулятор желудочного бандажа, этот бандаж идентифицирует себя для внешнего пульта управления. В стандартном режиме работы серийный номер, хранящийся на карточке пациента с микрочипом, должен соответствовать номеру, принимаемому от желудочного бандажа, так как в противном случае регулирование не будет разрешено. Однако для обеспечения надежности врач все-таки должен иметь возможность отрегулировать желудочный бандаж, даже если пациент утерял или неправильно поместил свою карточку с микрочипом. В этом случае внешний пульт управления может быть установлен в режим «без карточки». В этом режиме информация, отображаемая на экране дисплея 13 внешнего пульта управления, соответствует только относительному изменению желудочного бандажа в процессе данного сеанса регулировки, но уже не отражает абсолютный диаметр. Когда врач активизирует данный режим, в запоминающее устройство имплантируемого регулятора вводится аварийный бит с целью индикации режима «без карточки». В ходе последующих сеансов регулирования имплантируемый регулятор будет сигнализировать о том, что желудочный бандаж был отрегулирован в режиме «без карточки», и сообщения обо всех последующих регулировках будут иметь относительный характер. Если пациент снова установит карточку с микрочипом, аварийный бит можно будет сбросить путем полного открывания желудочного бандажа, что позволит достичь контакта исходного положения, который обеспечит повторную инициализацию отсчета положения. При этом последующие регулировки будут снова выполняться в стандартном рабочем режиме. В процессе регулирования желудочного кольца врач помещает внешнюю антенну 14 на кожу пациента точно напротив антенно-регуляторной капсулы 23 желудочного кольца таким образом, чтобы осуществлялся прием информации обратной связи, на основе которой может быть вычислен диаметр желудочного кольца в сжатом положении. В соответствии с принципами настоящего изобретения, имеется возможность изменять диаметр желудочного кольца без необходимости инвазивного хирургического вмешательства, причем такое изменение можно осуществлять произвольно по своему усмотрению, так как можно проводить многочисленные циклы регулирования с равномерными или неравномерными интервалами исключительно под контролем лечащего врача. Можно ожидать, что желудочный бандаж согласно настоящему изобретению будет исключительно надежным по сравнению с ранее известными гидравлическими бандажами, которые может регулировать сам пациент, поскольку, как правило, только врач будет иметь доступ к внешнему пульту управления, используемому для регулирования кольца. Таким образом, если говорить о варианте реализации кольца, предназначенном для лечения морбидного ожирения, пациент не будет иметь свободного доступа к каким бы то ни было средствам регулирования диаметра кольца. Кроме того, учитывая, что желудочный бандаж согласно изобретению позволяет добиться точной индикации текущего диаметра кольца в стандартном рабочем режиме, пациенту нет необходимости глотать рентгенографические вещества (например, бариевый краситель), необходимые для рентгенографической визуализации кольца с целью подтверждения отрегулированного размера. Соответственно, процесс регулирования бандажа можно проводить в кабинете врача, без необходимости затрат, связанных с рентгенографическим подтверждением таких регулировок. Кроме того, благодаря самоконтрящемуся исполнению растягивающегося элемента и гайки в сочетании с механической природой желудочного бандажа удается устранить проблемы, с которыми приходится сталкиваться при использовании существующих систем желудочных бандажей. Способы имплантации и извлечения Рассмотрим теперь фиг.20, где изображен желудочный бандаж 21 согласно настоящему изобретению, имплантированный в тело пациента. Кольцо 22 располагают таким образом, чтобы оно охватывало верхнюю часть S желудка пациента, тогда как антенно-регуляторную капсулу 23 помещают вблизи грудины ST. Капсулу 23 устанавливают в этой позиции под кожей SK пациента таким образом, чтобы к ней был возможен свободный доступ в зоне грудной клетки для обеспечения связи этой капсулы с внешней антенной 14 внешнего пульта 10 управления (см. фиг.1). Перейдем к рассмотрению фиг.21А-21Н, на которых проиллюстрирован способ имплантации желудочного бандажа согласно изобретению. Этот способ сходен с лапароскопическими процедурами, используемыми при имплантации известных из уровня техники желудочных бандажей. Доступ к брюшной полости обеспечивают посредством выполнения от 4 до 6 небольших отверстий, как правило, диаметром от 10 до 18 мм, в каждое из которых вводят по одному троакару, как изображено на фиг.21А. Через эти троакары хирург вводит камеру и лапароскопические инструменты и производит с ними необходимые манипуляции. Кроме того, для обеспечения свободного перемещения хирургических инструментов и камеры в брюшную полость вдувают газ СО2 до достижения избыточного давления порядка 0,15 бар. Как проиллюстрировано на фиг.21В-21Е, желудочный бандаж согласно изобретению разгибают (как изображено на фиг.8) и вводят, начиная с антенны, в брюшную полость через 18-миллиметровый троакар. В соответствии с другим вариантом, для выполнения рассечения могут использовать лапароскопическую канюлю, которая затем будет извлечена, и вводить устройство через полученное таким путем отверстие (для выполнения такой лапаротомии могут использовать и другие инструменты). Как видно на фиг.21В, наконечник 25 антенно-регуляторной капсулы 23 вводят в брюшную полость через троакар 100 с помощью атравматических захватов 110. На фиг.21С проиллюстрировано, как в брюшную полость через троакар 100 также с помощью атравматических захватов 110 втягивают кожух 29 желудочного кольца. На фиг.21D изображено введение в брюшную полость кольца 22 в вытянутом состоянии. На фиг.21Е изображено, как кольцу предоставлена возможность восстановления его предпочтительной круглой формы. Далее с целью закрепления желудочного кольца 22 в зоне вокруг верхней части желудка пациента с этим кольцом производят манипуляции с помощью атравматических захватов 100 (как описано выше при рассмотрении фиг.14А и 14В) до тех пор, пока прорезь 73 зажима 27 не войдет во взаимодействие с выступом 74, как изображено на фиг.21F. Затем складку желудочной ткани могут пришить вокруг желудочного кольца для предотвращения смещения желудочного бандажа, как это традиционно происходит при использовании бандажей с гидравлической системой. Наконец, как проиллюстрировано на фиг.21G, в брюшной стенке могут сформировать канал и через него ввести антенно-регуляторную капсулу 23. После этого от капсулы 23 отрезают наконечник 25 и пришивают ее в зоне над грудиной пациента, как изображено на фиг.21Н. Затем троакары вынимают, и теперь желудочный бандаж могут активировать для регулировки диаметра кольца по усмотрению врача. Процесс извлечения желудочного кольца согласно настоящему изобретению содержит, по существу, описанные выше шаги в обратной последовательности и может быть осуществлен неразрушающим способом. В частности, в брюшную полость вводят несколько канюль, после чего полость надувают для формирования пневмоперитонеума. Теперь, пользуясь лапароскопическими захватами, могут разжать зажим желудочного кольца и переместить удлиненный элемент с положения, в котором он охватывал желудок пациента. После этого могут распрямить желудочное кольцо и извлечь его из брюшной полости либо через одну из нескольких канюль, либо посредством лапаротомии. Другие признаки Желудочный бандаж согласно изобретению имеет в силу своих конструктивных особенностей несколько воздушных промежутков, при этом заявителями было замечено, что при его вживлении необходимо принять некоторые меры предосторожности. Так, в частности, имеющиеся внутри кольца 22 воздушные промежутки содержат, как правило, воздух, в состав которого входит примерно 80% N2, и значительная часть кольца заключена в тонкую герметичную силиконовую мембрану (см. фиг.2 и 4). Поскольку через эту мембрану газ CO2 может проникать в кольцо посредством диффузии приблизительно в 20 раз быстрее, чем из него может выходить находящийся внутри газ N2, при введении желудочного кольца в брюшную полость, раздутую газом CO2, возможно сильное раздувание мембраны. Когда устанавливается равновесие между давлениями газов N2 и CO2, указанное раздувание спадает, что занимает, как правило, около трех часов. Однако, когда мембрана расширена, существует опасность ее прокола, например, острыми иглами при пришивании складки желудочной ткани поверх кольца или при пришивании антенно-регуляторной капсулы в нужном положении. Поэтому заявители нашли четыре следующих решения для устранения этой проблемы: (1) предварительная обработка CO2; (2) упаковка с CO2; (3) применение клапанной системы; (4) использование менее растяжимой мембраны. Предварительная обработка СО2 подразумевает помещение желудочного бандажа перед проведением имплантации в наполненный газом CO2 контейнер на определенное время, например на 3 часа, что позволит до начала имплантации прийти в равновесие давлениям N2 и CO2. Перед такой предварительной обработкой желудочное кольцо может находиться в герметичной стерильной упаковке. Операция «упаковки с CO2» предполагает упаковку желудочного бандажа при его изготовлении в контейнер, наполненный CO2, с тем чтобы во время имплантации не происходило сколько-нибудь значительного раздувания. Применение клапанной системы предусматривает установку перекрывающего давление клапана на мембране кольца, который предотвратит накопление внутри устройства избыточного давления и одновременно предотвратит поступление в это устройство физиологических жидкостей. Наконец, во избежание раздувания могут быть выбраны мембраны из различного материала или различной толщины. Предполагается, что на этапе первоначального клинического тестирования устройства будет применен вариант предварительной обработки, хотя в промышленном производстве наиболее предпочтительным решением следует считать вариант упаковки с CO2. Для расширения брюшной полости могут быть использованы и другие газы, помимо углекислого, причем эти заранее выбранные альтернативные газы могут быть также использованы и для предварительной обработки желудочного кольца согласно изобретению. Как было упомянуто в первой части данной заявки, предлагаемая кольцевая система с дистанционным электропитанием и управлением, помимо желудочного бандажирования для лечения морбидного ожирения, может иметь самые разнообразные применения. Так, например, эту систему можно с успехом применять для лечения недержания кала, при илеостомии, колостомии, гастроэзофагеальной рефлюксной болезни, недержании мочи и при перфузии изолированных органов. Для лечения недержания кала можно использовать предложенное кольцо с очень незначительными изменениями или вовсе без изменений. Кроме того, поскольку пациенту придется выполнять процедуру регулировки кольца, по меньшей мере, с ежедневной периодичностью, он может применять удобный для пользователя переносный внешний пульт управления. Далее, учитывая, что кольцо будет регулярно переходить из закрытого в полностью открытое положение, нет необходимости в наличии карточки пациента с микрочипом. Вместо этого информация о полностью закрытом положении может храниться в памяти имплантируемого регулятора и при каждом очередном использовании ее считывают с помощью внешнего пульта управления (и эта информация может периодически меняться врачом). Аналогичное модифицированное устройство может быть использовано пациентами, перенесшими илеостомию или колостомию, либо помещено вокруг эзофагеального клапана при лечении гастроэзофагеальной рефлюксной болезни. При лечении недержания мочи кольцо может быть дополнительно модифицировано с целью минимизации его объема, охватывающего уретру, чего можно достичь путем помещения двигателя приводного механизма в какую-нибудь зону в нижнем отделе живота или таза и присоединения приводного механизма к двигателю с помощью передающего кабеля. Настоящее изобретение может быть также успешно использовано для выполнения перфузии изолированных органов. Лечение некоторые видов рака требует воздействия таких доз химиотерапевтических препаратов, которые слишком высоки для введения их в большой круг кровообращения. Было предложено одно из решений этой проблемы, при котором выполняют процедуру открытой хирургии, в ходе которой приостанавливают кровоток к пораженному раком органу и для нециркулирующей крови обеспечивают циркуляцию от какого-либо внешнего источника, содержащего необходимую дозу лекарства. Тогда для изоляции пораженного раком органа и обеспечения возможности перфузии органа большими дозами лекарства в качестве клапанов могут быть использованы отдельные кольца или несколько колец согласно настоящему изобретению. Такие процедуры можно производить неоднократно без оперативного вмешательства, благодаря чему снижаются травматизм и риск для пациента, и одновременно улучшается результат его лечения. Несмотря на то, что выше были подробно описаны некоторые конкретные варианты реализации изобретения, следует понимать, что данное описание было приведено лишь с иллюстративной целью. Специалистам в данной области техники очевидна возможность создания дополнительных вариантов, которые также будут входить в объем патентной защиты, определенный в прилагаемой формуле изобретения.
Реферат
Группа изобретений относится к медицине и может использоваться при лечении ожирения. Устройство для регулирования содержит удлиненный элемент, имеющий первый конец и вторые концы. Удлиненный элемент имеет сжимающуюся вентральную поверхность и жесткую дорсальную периферию. Зажим расположен на первом конце удлиненного элемента и выполнен с возможностью зацепления со вторым концом удлиненного элемента, в результате удлиненный элемент образует петлю вокруг органа или канала. Гибкий элемент установлен с возможностью скольжения внутри удлиненного элемента. Гибкий элемент имеет спиральную винтовую резьбу. Дистанционно управляемый приводной механизм расположен на втором конце удлиненного элемента. Приводной механизм входит в зацепление со спиральной винтовой резьбой. Гибкий элемент установлен с возможностью затягивания петли на органе или канале пациента под воздействием приводного механизма. Удлиненный элемент содержит эластичную мембрану, предотвращающую врастание ткани. Для уменьшения раздувания эластичной мембраны удлиненный элемент предварительно обработан в среде СО2. Раскрыто устройство для желудочного бандажирования. Технический результат заключается в повышении точности регулирования действующего на орган сжатия. 2 н. и 74 з.п. ф-лы, 32 ил.
Формула
удлиненный элемент, имеющий первый конец и вторые концы, причем этот удлиненный элемент имеет сжимающуюся вентральную поверхность и жесткую дорсальную периферию;
зажим, расположенный на первом конце удлиненного элемента, выполненный с возможностью зацепления со вторым концом удлиненного элемента, в результате которого удлиненный элемент образует петлю вокруг органа или канала;
гибкий элемент, установленный с возможностью скольжения внутри удлиненного элемента, причем этот гибкий элемент имеет спиральную винтовую резьбу; и
дистанционно управляемый приводной механизм, расположенный на втором конце удлиненного элемента, причем приводной механизм входит в зацепление со спиральной винтовой резьбой, и гибкий элемент установлен с возможностью затягивания петли на органе или канале пациента под воздействием этого приводного механизма,
причем удлиненный элемент дополнительно содержит эластичную мембрану, предотвращающую врастание ткани, при этом для уменьшения раздувания эластичной мембраны удлиненный элемент предварительно обработан в среде СО2.
проволочный сердечник, имеющий конец;
колпачок, прикрепленный к концу проволочного сердечника;
первую винтовую пружину, расположенную на проволочном сердечнике, причем винтовая пружина имеет квадратный поперечный профиль; и
вторую винтовую пружину, переплетенную с первой винтовой пружиной и задающую шаг первой винтовой пружины,
в котором вторая винтовая пружина имеет первый конец, прикрепленный к проволочному сердечнику, и второй конец, который может свободно растягиваться со скольжением вдоль проволочного сердечника на заданную длину, что обеспечивает возможность изгиба спиральной винтовой резьбы, причем колпачок ограничивает растяжение свободного второго конца, поддерживая тем самым шаг постоянным.
удлиненный элемент, имеющий первый конец и вторые концы, причем этот удлиненный элемент имеет сжимающуюся вентральную поверхность и, по существу, жесткую дорсальную периферию и выполнен с возможностью образования петли вокруг желудка пациента;
кожух, расположенный на втором конце удлиненного элемента;
электродвигатель, расположенный внутри кожуха;
приводной механизм, расположенный внутри кожуха и соединенный с электродвигателем;
гибкий элемент, расположенный с возможностью скольжения внутри удлиненного элемента, причем этот гибкий элемент имеет спиральную винтовую резьбу и, кроме того, этот гибкий элемент имеет неподвижный конец, связанный с первым концом удлиненного элемента, и свободный конец, который проходит через приводной механизм и находится в зацеплении с ним, в котором гибкий элемент выполнен с возможностью изменения диаметра петли под воздействием приводного механизма, причем удлиненный элемент дополнительно содержит эластичную мембрану, предотвращающую врастание ткани, при этом для уменьшения раздувания эластичной мембраны удлиненный элемент предварительно обработан в среде СО2.
проволочный сердечник;
первую винтовую пружину, расположенную на проволочном сердечнике, причем винтовая пружина имеет прямоугольный или трапецеидальный поперечный профиль; и
вторую винтовую пружину, переплетенную с первой винтовой пружиной и задающую шаг первой винтовой пружины, причем вторая винтовая пружина имеет первый и второй концы, функционально связанные с проволочным сердечником, что обеспечивает возможность изгиба спиральной винтовой резьбы с одновременным поддержанием шага, по существу, постоянным.

Комментарии