Применение цианиновых красителей для диагностики пролиферативных заболеваний - RU2007129919A
Код документа: RU2007129919A
Реферат
1. Применение соединения согласно формуле (I)
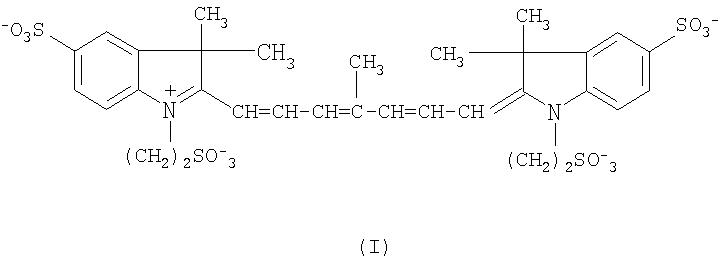
или его фармацевтически приемлемой соли, для приготовления диагностической композиции для выявления пролиферативного заболевания, в котором диагностическая композиция включает соединение в количестве менее 0,5 и более 0,001 мг/кг массы тела на диагностическую процедуру.
2. Применение по п.1, в котором соединение сопряжено с нацеленным на мишень соединением.
3. Применение по п.2, в котором нацеленное на мишень соединение выбирается из группы нацеленных на мишень соединений, состоящей из полипептида, нуклеиновой кислоты, маленькой молекулы или сахара.
4. Применение по п.3, в котором полипептид выбирается из группы, состоящей из лиганда рецептора, антитела, одноцепочечного антитела или связывающего фрагмента антитела или одноцепочечного антитела.
5. Применение по п.4, в котором пролиферативное заболевание выбирается из группы, состоящей из опухоли, предракового состояния, дисплазии, метаплазии, псориаза, псориатического артрита, ревматоидного артрита, эндометриоза и/или болезни глаз.
6. Применение по п.5, в котором опухоль является первичной опухолью или метестазом.
7. Применение по п.6, в котором опухоль представляет собой малигному желудочно-кишечного или колоректального тракта, печени, поджелудочной железы, почки, мочевого пузыря, щитовидной железы, предстательной железы, эндометрия, яичника, яичек, меланому, дисплазию слизистой оболочки ротовой полости, инвазивный рак ротовой полости, мелкоклеточный или не мелкоклеточный рак легкого; опухоль молочной железы, включая гормонозависимый рак молочной железы, гормононезависимые виды рака молочной железы; переходно-клеточные и плоскоклеточные виды рака; неврологические злокачественные новообразования, включая нейробластому, глиомы, астроцитомы, остеосаркому, менингиому; саркому мягких тканей; гемангиому и эндокринологическую опухоль, включая аденому гипофиза, феохромоцитому, параганглиому, гематологические злокачественные новообразования, включая лимфому и лейкемию или метастаз, развивающийся из одной из вышеупомянутых опухолей.
8. Применение по п.6, в котором диагностическое соединение вводится во время скрининга опухоли или до, в течение или после хирургического вмешательства.
9. Применение по п.5, в котором предраковое состояние выбирается из группы, состоящей из предракового состояния кожи, в особенности, актинического кератоза, кожного нароста, актинического хейлита, дегтярного кератоза, мышьякового кератоза, лучевого кератоза, чечевицеобразного дискоидного дискератоза, бовеноидного папулеза, злокачественного лентиго (lentigo maligna), склерозирующего лишая (lichen sclerosus) и красного лишая слизистой оболочки; предракового состояния пищеварительного тракта, в особенности, эритроплакии, лейкоплакии, пищевода Барретта, синдрома Пламмера-Винсона, бедренной язвы, гипертрофической гигантской гастропатии, пограничной карциномы, неопластического кишечного полипа, ректального полипа, «фарфорового» желчного пузыря; предракового состояния женских половых органов, в особенности, протокового рака in situ (CDIS), интраэпителиальной цервикальной неоплазии (CIN), лейкоплакии, гиперплазии эндометрия (стадия III), дистрофии вульвы, интраэпителиальной неоплазии вульвы (VIN), гидатидообразного родимого пятна; предракового состояния урогенитального тракта, в особенности, папилломатоза мочевого пузыря, эритроплазии Кейра, тестикулярной интраэпителиальной неоплазии (TIN), лейкоплакии; карциномы in situ (CIS); предракового состояния, вызванного хроническим воспалением, в особенности, пиодермии, остеомиелита, конглобатных угрей, люпозного туберкулеза кожи и фистулы.
10. Применение по п.5, в котором метаплазия выбирается из группы, состоящей из агногенной миелоидной метаплазии, апокринной метаплазии, атипичной метаплазии, аутопаренхиматозной метаплазии, метаплазии соединительных тканей, эпителиальной метаплазии, кишечной метаплазии, метапластической анемии, метапластического окостенения, метапластических полипов, миелоидной метаплазии, первичной миелоидной метаплазии, вторичной миелоидной метаплазии, плоскоклеточной метаплазии, плоскоклеточной метаплазии амниона, симптоматической миелоидной метаплазии и регенеративной метаплазии.
11. Применение по п.5, в котором дисплазия выбирается из группы, состоящей из изангидротической эктодермальной дисплазии, антеролицевой дисплазии, асфиктической дисплазии грудной клетки, атриодигитальной дисплазии, бронхопульмональной дисплазии, церебральной дисплазии, цервикальной дисплазии, хондроэктодермальной дисплазии, ключично-черепного дизостоза, врожденной эктодермальной дисплазии, черепно-диафизарной дисплазии, черепно-карпотарзальной дисплазии, черепно-метафизарной дисплазии, дентинной дисплазии, диафизарной дисплазии, эктодермальной дисплазии, несовершенного амелогенеза, энцефало-офтальмической дисплазии, пяточно-эпифизарной дисплазии, множественной эпифизарной дисплазии, эпифизарной точечной остеодисплазии, эпителиальной дисплазии, фациодигитогенитальной дисплазии, семейной фиброзной дисплазии челюстей, семейной белой складчатой дисплазии, фиброзно-мышечной дисплазии, фиброзной остеодисплазии, дисплазии красного костного мозга, наследственной почечно-ретинальной дисплазии, гидротической эктодермальной дисплазии, гипогидротической эктодермальной дисплазии, лимфопенической дисплазии тимуса, дисплазии молочной железы, челюстно-лицевой остеодисплазии, метафизарной дисплазии, дисплазии Мондини, моностотической фиброзной дисплазии, слизисто-эпителиальной дисплазии, множественной эпифизарной дисплазии, глазнично-ушно-вертебральной дисплазии, окулодентодигитальной дисплазии, окуловертебральной остеодисплазии, одонтодисплазии, офтальмо-челюстно-лицевой остеодисплазии, периапикальной цементной дисплазии, полиостотической фиброзной дисплазии, псевдоахондропластической спондилоэпифизарной дисплазии, дисплазии сетчатки, септо-оптической дисплазии, спондилоэпифизарной дисплазии и ветрикулорадиальной дисплазии.
12. Применение по п.5, в котором глазная болезнь выбирается из группы, состоящей из трахомы, ретролентальной фиброплазии, диабетической ретинопатии, неоваскулярной глаукомы и возрастной дистрофии желтого пятна.
13. Применение по п.12, в котором диагностическая композиция дополнительно включает фармацевтически приемлемую соль, носитель, вспомогательное вещество и/или буфер.
14. Применение по п.13, в котором соединение включается в диагностическую композицию в количестве 0,1 мг/кг массы тела или менее.
15. Диагностический комплект, включающий соединение формулы (I) по п.1 или его фармацевтически приемлемую соль в количестве для приготовления диагностической композиции для введения, составляющем меньше, чем 0,5 и больше, чем 0,001 мг/кг массы тела соединения на диагностическую процедуру, и необязательно фармацевтически приемлемую соль, носитель, вспомогательное вещество и/или буфер.

Комментарии