Модуляция активности гепаринсвязывающего эпидермального фактора роста для заживления барабанной перепонки - RU2676483C2
Код документа: RU2676483C2
Чертежи








Описание
УРОВЕНЬ ТЕХНИКИ
[001] Перфорация барабанной перепонки (БП) наиболее часто возникает в результате среднего отита или травмы. Наиболее частыми клиническими проявлениями перфорации БП являются кондуктивная тугоухость и хроническая инфекция. Наиболее распространенной причиной перфорации БП является инфекция. Перфорации, связанные с неосложненным острым средним отитом, обычно являются небольшими; подавляющее большинство заживает самопроизвольно после ослабления инфекции. Кроме того, большие перфорации могут возникнуть в результате инфицирования некротизирующими микроорганизмами. Другой основной причиной перфорации БП является травма уха. Обычно причинами травмы являются тупые и проникающие повреждения, быстрые изменения барометрического давления (баротравмы) и чрезмерное звуковое давление.
[002] Как известно, после травмы ткани проходят несколько стадий заживления. Несмотря на то, что заживление ран в барабанной перепонке включает сначала гемостатическую и противовоспалительную стадии, которые похожи на обычное заживление кожи, пролиферативная и миграционная фазы в барабанной перепонке существенно отличаются от этих фаз в других тканях. В большинства ситуаций заживления ран образуется основание грануляционной ткани, которое служит в качестве платформы, на которой происходит реэпителизация. При заживлении барабанной перепонки эти события происходят в обратном порядке. Слой плоского эпителия вначале образует мост через рану, и только потом следует переформирование волокнистого компонента. БП уникальна тем, что слой эпидермиса играет критическую роль в начальной миграции, причем этот процесс контролирует пролиферирующий базальный слой.
[003] Большинство перфораций барабанной перепонки заживает самопроизвольно; однако ряд факторов может задерживать или предотвращать закрытие, что приводит в результате к хронической перфорации. Постоянно существующие перфорации обычно возникают в условиях персистирующей инфекции, что ухудшает процесс восстановления. В этих ситуациях не происходит процесс регенеративного заживления мембраны, предотвращается хемотаксис и последующая миграция эпителиальных клеток в ране. Гистологически при хронических перфорациях плоский эпителий растет по краю перфорации до встречи с медиальным слоем слизистой оболочки БП.
[004] Целями лечения хронической перфорации БП являются лечение или предупреждение хронического среднего отита и восстановление слуха. Обычная терапия включает использование трансплантатов ткани, например, при использовании в тимпанопластике аутотрансплантатов, можно использовать в качестве аутотрансплантата височную фасцию. Можно использовать поверхностную височную фасцию, состоящую из фибробластов в коллагеновой матрице. Хотя тимпанопластика с использованием трансплантата из аутологичной соединительной ткани является весьма успешным способом восстановления постоянно существующих перфораций БП, было бы полезно разработать процедуру, которая не требует микрохирургических навыков, является менее затратной и может применяться в условиях поликлиники. Настоящее изобретение удовлетворяет эту потребность.
Публикации
[005] Santa Maria et al. (2010) J Mol Histol. 2010 Dec; 41 (6): 309-14. Santa Maria (2011) Thesis, University of Western Australia. Johnson and Wang (2013) J Control Release 166 (2): 124-9. Ishihara et al. (2003) J Biomed Mater Res A. 64 (3): 551-9. Tolino et al. (2011) Biochim Biophys Acta. 1810 (9): 875-8; Shirakata et al. (2005) J Cell Sci. 118 (Pt 11): 2363-70;

СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[006] Предлагаются композиции и способы лечения хронической перфорации барабанной перепонки. В способах по настоящему изобретению хронически перфорированная барабанная перепонка находится в местном контакте с эффективной дозой гепарин-связывающего эпидермального фактора роста, HB-EGF, или агента, обладающего активностью HB-EGF, в течение периода времени, достаточного для обеспечения улучшенного заживления перфорации мембраны. В некоторых вариантах реализации настоящего изобретения доза HB-EGF предлагается в композиции с замедленным высвобождением; в других вариантах реализации настоящего изобретения предлагается регулярное введение композиции без замедленного высвобождения. В некоторых вариантах реализации настоящего изобретения композиция замедленного высвобождения является биоразлагаемой. В других вариантах реализации настоящего изобретения замедленное высвобождение осуществляется устройством, например насосом или другим устройством для высвобождения.
[007] Подлежащая лечению БП контактирует с HB-EGF в течение периода времени, достаточного для улучшения заживления перфорации БП, т.е. чтобы получить в результате значительное закрытие перфорации, например до площади перфорации меньшей чем приблизительно 0,1 мм2. Закрытие можно контролировать визуально, в том числе микроскопически; функционально, например, по уменьшению тугоухости; и т.п. Период времени контактирования с HB-EGF может составлять по меньшей мере одни сутки, по меньшей мере 3 суток, по меньшей мере 5 суток, по меньшей мере 7 суток, по меньшей мере 10 суток, по меньшей мере 2 недели, по меньшей мере 3 недели; и может составлять вплоть до одних суток, вплоть до 3 суток, вплоть до 5 суток, вплоть до 7 суток, вплоть до 10 суток, вплоть до 2 недель, вплоть до 3 недель или более в соответствии с потребностями индивидуума.
[008] В некоторых специфических вариантах реализации настоящего изобретения эффективная доза HB-EGF предоставляется в не ототоксичной композиции замедленного высвобождения, например, в геле, пене, вставке и т.п., предпочтительно, в биоразлагаемой композиции. В одном таком варианте реализации настоящего изобретения эффективная доза HB-EGF введена в состав геля, содержащего хитозан, полимолочную кислоту и фибриноген.
[009] В одном варианте реализации настоящее изобретение включает способ, состоящий из (i) идентификации пациента, имеющего хроническую перфорацию БП; (ii) контактирования пораженной БП с эффективной дозой HB-EGF, например, предоставляемого в форме капель для введения через подходящие промежутки времени, в устройстве для замедленного высвобождения HB-EGF, в композиции замедленного высвобождения и т.д.; и (iii) мониторинг индивидуума для определения эффективного закрытия перфорации.
[0010] Другой аспект настоящего изобретения относится к применению агента с активностью HB-EGF при производстве лекарственного средства для лечения хронической перфорации БП, причем указанное лекарственное средство вводят пациенту с хронической перфорацией БП в течение периода времени и в дозе, достаточных, чтобы вызвать закрытие перфорации.
[0011] В еще одном аспекте настоящего изобретения предлагается набор для лечения хронической перфорации БП. Набор включает в себя композицию, которая обеспечивает эффективную дозу HB-EGF, например, в форме капель, устройств, композиций и т.п. Набор также может включать в себя устройство доставки, например, дозатор для ушных капель, шприц для доставки композиции, двуствольный шприц для доставки двухкомпонентной композиции и т.п. Набор может также содержать инструкции по применению.
[0012] В других вариантах реализации настоящего изобретения предлагаются способы временного открытия барабанной перепонки, например для введения трубок и т.п. В таких вариантах реализации настоящего изобретения БП контактирует с эффективной дозой ингибитора HB-EGF включая, без ограничения, ингибитор шеддинга лиганда EGFR, в течение периода времени, достаточного для создания небольшой перфорации в БП. В некоторых таких вариантах реализации настоящего изобретения небольшую перфорацию можно сделать механическим путем до контактирования с ингибитором.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0013] Фигура 1. Типичные изображения БП после перфораций, которые лечили OSU8-1 (ингибитор шеддинг лиганда EGFR) на (а) день 2 (b) день 14 (с) день 44 (d) день 90 (3 месяца). Перфорация обведена голубым цветом.
[0014] Фигура 2. Пограничные показатели теста-ответа слухового отдела ствола мозга (ABR) и отоакустических выделений продуктов искажения (DPOAE) определяли у 9 мышей через 60 дней после хирургической перфорации обеих барабанных перепонок. В одно ухо не вводили инъекцию (контроль), в то время как противоположное ухо заполнили полимерным средством доставки для доставки хитозана, фибриногена и полилактида.
[0015] Фигура 3. Евстахиева труба (ЕТ) перед (а) и после (b) окклюзии гуттаперчей. Процедуру у крыс адаптировали посредством открытия слуховой буллы с помощью устройства для иссечения с фрезой 0,5 мм. Открытие буллы латерально позволяет гуттаперче наполнять ЕТ вниз с меньшей ретракцией дыхательных путей. ЕТ исследовали посмертно, что подтверждало полную окклюзию.
[0016] Фигура 4. Лечение хронических перфораций с использованием GF в мышиной модели окклюзии ЕТ. В верхнем ряду представлены (а) репрезентативные изображения группы лечения, демонстрирующие заживление перфораций. В нижнем ряду представлены (b) репрезентативные изображения контрольной группы (введение только полимера), демонстрирующие сохраняющуюся перфорацию (обведена голубым цветом).
Примечание. Некоторые БП в верхнем ряду зажили с образованием тимпаносклеррза.
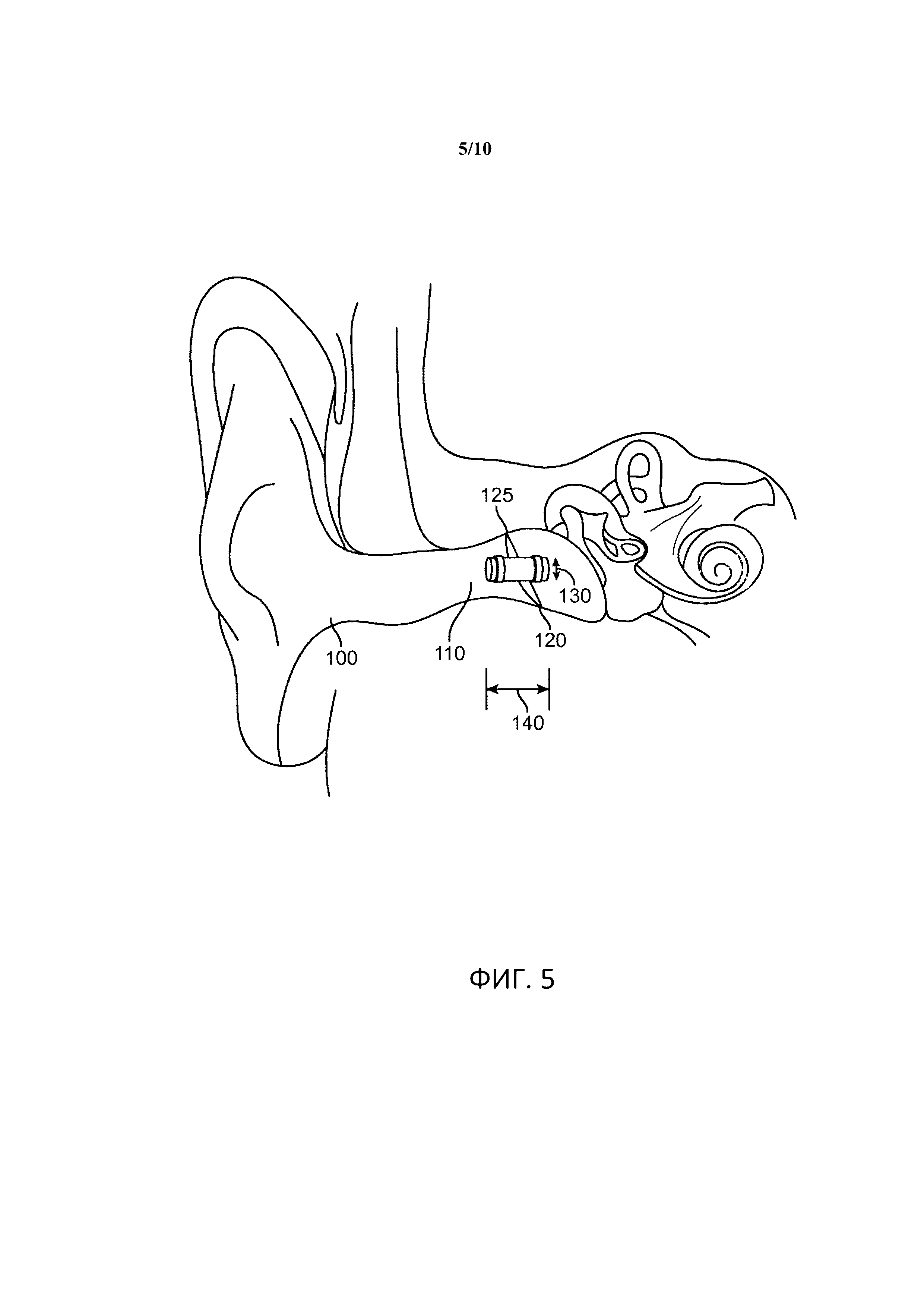
[0017] Фигура 5. Транстимпанальная доставка фактора роста.
[0018] Фигура 6. Транстимпанальная доставка фактора роста.
[0019] Фигура 7. Транстимпанальная доставка фактора роста.
[0020] Фигура 8. Интратимпанальная доставка фактора роста.
[0021] Фигура 9. Средство доставки лекарственного средства к области, прилегающей к барабанной перепонке.
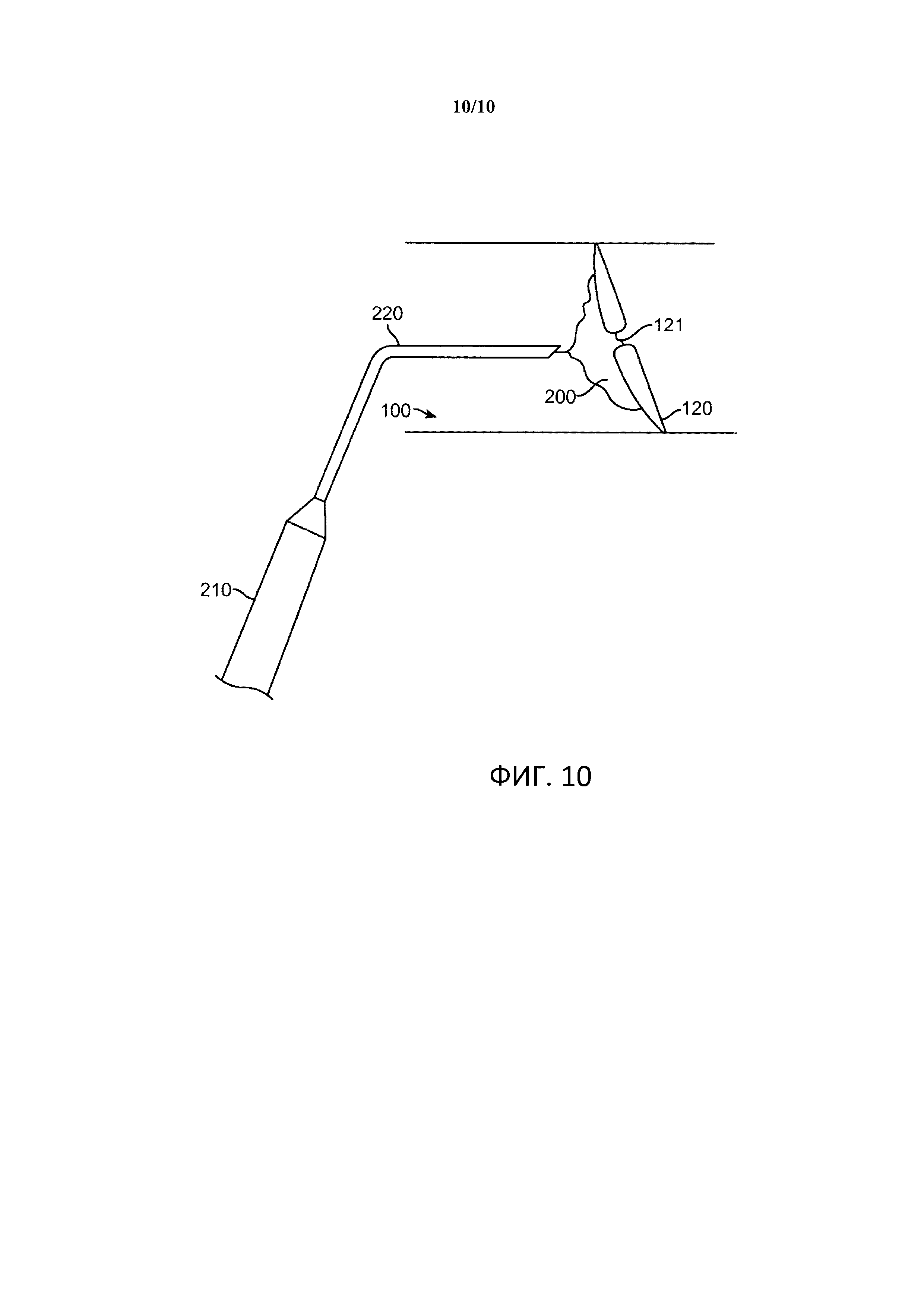
[0022] Фигура 10. Текучая композиция для доставки лекарственного средства.
[0023] Отличительные признаки и многие другие преимущества настоящего изобретения станут более понятными при обращении к нижеследующему подробному описанию, приведенному в сочетании с прилагаемыми чертежами.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0024] Перед дальнейшим описанием настоящего изобретения следует понять, что изобретение не ограничено конкретными вариантами реализации настоящего изобретения, описанными ниже, поскольку могут быть сделаны изменения конкретных вариантов реализации, которые все еще будут попадать в объем прилагаемой формулы изобретения. Кроме того, следует учитывать, что используемая терминология предназначена для описания конкретных вариантов реализации настоящего изобретения и не предназначена для ограничения. В настоящем описании и приложенной формуле изобретения единственное число включает ссылку на множественное число, если из контекста очевидно не следует обратное.
[0025] В случае если предлагается диапазон значений, следует понимать, что каждое промежуточное значение, до десятых долей единицы нижнего предела, если контекстом четко не указывается иное, между верхним и нижним пределом этого диапазона, а также любое другое указанное либо промежуточное значение в этом указанном диапазоне, включается в объем настоящего изобретения. Упомянутые верхний и нижний пределы этих меньших диапазонов могут независимо включаться в меньшие диапазоны и также входят в объем настоящего изобретения при соблюдении любого конкретно исключенного предела в указанном диапазоне. В том случае, если указанный диапазон включает один или оба предела, диапазоны, исключающие любой из или оба упомянутые включенные пределы, также включаются в настоящее изобретение.
[0026] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, что обычно понимается специалистом в той области техники, к которой относится настоящее изобретение. Несмотря на то, что при практическом осуществлении либо испытании настоящего изобретения могут использоваться любые способы, устройства и материалы, подобные либо эквивалентные описанным в настоящем документе, далее будет представлено описание иллюстративных способов устройств и материалов.
[0027] Все публикации, упомянутые в настоящем документе, включены в него посредством ссылки с целью описания и раскрытия компонентов по изобретению, которые описаны в указанных публикациях, тех компонентов, которые можно использовать в связи с описываемым изобретением.
[0028] Это изобретение описано в терминах конкретных вариантов реализации, установленных или предложенных авторами настоящего изобретения для охвата предпочтительных форм практического применения настоящего изобретения. Специалистам в данной области техники будет понятно, что в свете настоящего описания в конкретных проиллюстрированных вариантах реализации настоящего изобретения могут быть сделаны многочисленные модификации и изменения, не отступая от предполагаемого объема настоящего изобретения. Например, из соображений биологической функциональной эквивалентности в структуре белка могут быть сделаны изменения, не влияющие на вид или размер биологического действия. Все такие модификации предназначены для внесения в объем прилагаемой формулы изобретения.
Определения
[0029] Термины, используемые в данном описании, в рамках данного изобретения и в конкретном контексте, в котором используется каждый термин, как правило, имеют свои обычные принятые в данной области техники значения. Некоторые термины будут рассмотрены ниже или в других местах настоящего описания, чтобы обеспечить дополнительное руководство в описании композиций и способов настоящего изобретения, их получение и применение.
[0030] Субъект. Индивидуумы, подлежащие лечению способами по настоящему изобретению, могут принадлежать к любому виду млекопитающих или птиц, включая человека. Животные, не относящиеся к человеческому роду, включают, без ограничения, млекопитающих, экспериментальных животных, таких как мыши, крысы, кролики, хомяки, морские свинки, шиншиллы и т.д.; домашних животных, таких как собаки и кошки; и сельскохозяйственных животных, таких как овцы, козы, свиньи, лошади и коровы. Животные по настоящему изобретению, не относящиеся к человеческому роду, могут быть млекопитающими или не млекопитающими животными; позвоночными или беспозвоночными.
[0031] «Лечение» субъекта или «лечение» субъекта от заболевания или патологического состояния в данном описании означает снижение или ослабление клинических симптомов заболевания или патологического состояния, такого как хроническая перфорация БП.
[0032] «Стимулирование», «повышение» или «улучшение» заживления барабанной перепонки или раны обычно означает увеличение скорости, с которой рана или перфорация заживает, или уменьшение степени остаточного рубца или появления келоидной или некротической ткани во время или после заживления раны или перфорации.
[0033] «Рана» представляет собой разрушение или разрыв в структуре органа или ткани, включая эпителий, соединительную ткань и мышечную ткань. Примеры ран включают в себя, но не ограничиваются перечисленным, раны кожи, гематомы, язвы, пролежни, ссадины, трещины, порезы, проколы, псориатические раны, перфорации барабанной перепонки, царапины и разрывы роговицы и ожоги.
[0034] «Местное» применение относится к несистемному местному нанесению активного ингредиента на поверхность раны.
[0035] Барабанная перепонка. Барабанная перепонка представляет собой тонкую, конусообразную мембрану, которая у людей и других млекопитающих отделяет наружное ухо от среднего уха. Ее функция заключается в передаче звука из воздуха на косточки внутри среднего уха, а затем в овальное окно в заполненную жидкостью улитку. Следовательно, она, в конечном счете, усиливает и преобразует вибрацию в воздухе в вибрацию в жидкости. Косточка молоточек является мостиком в промежутке между барабанной перепонкой и другими косточками.
[0036] В барабанной перепонке различают две основные области: ненатянутую часть и натянутую часть. Ненатянутая часть состоит из двух слоез, является относительно хрупкой, и связана с дисфункцией евстахиевой трубы и холестеатомами. Большая по размеру область натянутой части состоит из трех слоев: кожи, волокнистой соединительной ткани и слизистой оболочки. Она сравнительно прочная и представляет собой область, которая наиболее часто связана с перфорациями.
[0037] Разрыв или перфорация БП может быть результатом различных травм, инфекции и т.п. Перфорации БП могут приводить к кондуктивной тугоухости (CHL), которая колеблется в диапазоне от незначительной до 50 дБ. Перфорации могут варьировать по площади и локализации, например передняя, задняя или та и другая; и по площади от приблизительно 0,1 до приблизительно 60 мм2, как правило, в диапазоне от приблизительно 2,5 до 10 мм2 (см. Mehta et al. (2006) Otol Neurotol. 27 (2): 136-143). Перфорация может быть острой или хронической. Острую перфорацию обычно не лечат, поскольку БП обычно заживает самопроизвольно. Однако у некоторых индивидуумов не происходит заживления БП, что приводит к хронической перфорации.
[0038] Хроническая перфорация барабанной перепонки. Перфорация, которая не заживает при отсутствии лечения или при лечении обычными способами, например, при лечении антибиотиками, может рассматриваться как хроническая перфорация. Специалистам в данной области техники будет понятно, что между индивидуумами могут быть различия в продолжительности времени, необходимого для заживления, но, как правило, перфорация, не зажившая после периода вплоть до приблизительно 3 месяцев, после периода вплоть до приблизительно 2 месяцев, после периода вплоть до приблизительно 1 месяца, может быть классифицирована как хроническое патологическое состояние.
[0039] Хронические или незаживающие раны представляют собой открытые раны, которые не эпителизировались и не закрылись за разумный срок. Эти раны являются клинически застойными без признаков дальнейшего закрытия. Хронические раны могут рассматриваться как раны с отсутствием соответствующих «стартовых» сигналов. (См., например, Lorenz and Longaker, in Wounds: Biology, Pathology, and Management, Chapter 7, pp 77-88).
[0040] «Гепарин-связывающий эпидермальный фактора роста» при использовании в настоящем документе относится к эндогенно встречающемуся у млекопитающих, например, к гепарин-связывающему эпидермальному фактору роста человека, аллельному гепарин-связывающему эпидермальному фактору роста, функциональным консервативным производным гепарин-связывающего эпидермального фактора роста, функционально активным фрагментам гепарин-связывающего фактора роста и гомологам гепарин-связывающего эпидермального фактора роста, таким как гепарин-связывающий фактор роста, подобный эпидермальному фактору роста. HB-EGF также относится к вариантам форм HB-EGF, например к тем, которые обеспечивают повышенную активность, повышенную стабильность, более высокий выход или лучшую растворимость. Композиции для использования в способах по изобретению могут содержать одну или смесь из видов активности HB-EGF, например, содержать множество различных молекул HB-EGF. Обычно активность HB-EGF, при использовании в настоящем документе, относится к связыванию с родственным рецептором, активации указанного рецептора, проявлениям видов биологической активности, которые являются результатом связывания рецептора и активации и т.п.
[0041] HB-EGF является преимущественным фактором роста процесса эпителизации, необходимым для заживления ран кожи. Митогенное и миграционное влияние HB-EGF на кератиноциты и фибробласты способствует восстановлению кожи и ангиогенезу, необходимым для заживления ран, и этот фактор является основным компонентом раневых жидкостей. Связывание HB-EGF клеточной поверхности с гепарансульфат-протеогликанами повышает возможности митогенного стимулирования, ускоряя заживление ран кожи, сокращая время, необходимое для приживления трансплантата кожи человека, и способствует быстрому заживлению язв, ожогов и эпидермальных ран расщепленного лоскута.
[0042] HB-EGF синтезируется в виде связанного с мембранной митогенного и хемотаксисного гликопротеина. HB-EGF является гликопротеином, состоящим из 87 аминокислот, который демонстрирует экспрессию гена с высокой точностью регулирования. Шеддинг эктодомена приводит к образованию растворимой зрелой формы HB-EGF, которая влияет на факторы митогенности и хемотаксиса гладкомышечных клеток и фибробластов. Трансмембранная форма HB-EGF является уникальным рецептором для дифтерийного токсина и функционирует при юкстакринной передаче сигнала в клетках. Обе формы HB-EGF участвуют в нормальных физиологических процессах и в патологических процессах, включая прогрессирование и метастазирование опухолей, гиперплазию органов и атеросклероз. Для целей настоящего изобретения, как правило, используется растворимая, зрелая форма белка. Белок или агент может быть по сути чистым, например, не содержать другие белки, не содержать клеточный материала и т.д., обычно он может быть по меньшей мере приблизительно на 50% чистым, по меньшей мере приблизительно на 75% чистым, по меньшей мере приблизительно на 80% чистым, по меньшей мере приблизительно на 90% чистым, по меньшей мере приблизительно на 95% чистым, по меньшей мере приблизительно на 99% чистым.
[0043] В предпочтительном варианте реализации настоящего изобретения используют по сути чистый препарат HB-EGF человека. HB-EGF можно приобрести в очищенной форме или получить путем очистки компонента от людей или других животных, или путем рекомбинантной продукции в клетках-хозяевах, включая прокариотические клетки-хозяева, такие как S. cerevisiae или Е. coli и, более предпочтительно, клетки-хозяева млекопитающих, такие как клетки СНО. HB-EGF может быть человеческим дикого типа, гомологом млекопитающих или модифицированным/мутировавшим. В частности, могут быть использованы фрагменты компонента, которые сохраняют по меньшей мере часть требуемой активности полноразмерного компонента.
[0044] В некоторых вариантах реализации настоящего изобретения HB-EGF представляет собой HB-EGF человека и содержит аминокислотную последовательность номера доступа GenBank: L17032.1 GI 348175 или номера доступа GenBank: L17033.1 GI 34817 или номера доступа GenBank: L17032.1 GI 348175, включая, в частности, растворимые зрелые формы белков, описанные в данном документе.
[0045] «Функционально консервативные варианты» представляют собой белки, в которых данный аминокислотный остаток заменен без изменения всей конформации и функции белка, включая, но не ограничиваясь перечисленным, замену аминокислоты другой аминокислотой, имеющей аналогичные свойства (такие как, например, кислотные, основные, гидрофобные и т.п.). Аминокислоты с аналогичными свойствами хорошо известны в данной области техники. Например, аргинин, гистидин и лизин являются гидрофильными основными аминокислотами и могут быть взаимозаменяемыми. Аналогично, изолейцин, гидрофобная аминокислота, может быть заменен лейцином, метиониом или валином. Аминокислоты, отличные от указанных как консервативные аминокислоты, могут отличаться в белке или ферменте таким образом, что процентное содержание белка или сходство аминокислотной последовательности между любыми двумя белками с аналогичной функцией, может варьироваться, и может составлять, например, от 70% до 99%, как определяется в соответствии со схемой выравнивания, например, с помощью кластерного метода, в котором сходство определяется на основе алгоритма MEGALIGN. «Функционально консервативный вариант» также включает в себя полипептид или фермент, имеющий по меньшей мере 60% аминокислотной идентичности при определении алгоритмами 20 BLAST или FASTA, предпочтительно по меньшей мере 75%, более предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, и еще более предпочтительно 95%, и который имеет такие же или по существу аналогичные свойства или функции, что и нативный или родительский белок или фермент, с которым его сравнивают.
[0046] При использовании в настоящем документе термин HB-EGF может включать в себя варианты, гомологи и ортологи предоставленных последовательностей. Вариант может быть по сути аналогичен нативной последовательности, т.е. отличаться по меньшей мере одной аминокислотой, и может отличаться по меньшей мере двумя, но обычно не более чем приблизительно десятью аминокислотами (количество различий зависит от размера нативной последовательности). Изменения последовательности могут представлять собой замены, инсерции или делеции. Сканирующие мутации, которые систематически вводят аланин или другие остатки, могут быть использованы для определения ключевых аминокислот для сохранения в вариантных последовательностях. Консервативные аминокислотные замены, которые могут быть использованы, чтобы обеспечить вариантную последовательность по изобретению, обычно включают замены в пределах следующих групп: (глицин, аланин); (валин, изолейцин, лейцин); (аспарагиновая кислота, глутаминовая кислота); (аспарагин, глутамин); (серии, треонин); (лизин, аргинин); и (фенилаланин, тирозин).
[0047] Аминокислотная последовательность встречающегося в природе белка может быть изменена различными известными в данной области техники способами для генерирации целевых изменений в последовательности и, таким образом, обеспечивать вариантные последовательности по изобретению. Такие варианты обычно будут представлять собой функционально-сохранившиеся варианты, которые отличаются, как правило последовательностью, от соответствующего нативного или родительского белка, но по-прежнему сохраняют желательную или демонстрируют повышенную биологическую активность и/или функцию. Различные способы, известные в данной области техники, можно использовать для генерации целевых изменений например, способ фагового дисплея в комбинации со случайными и целевыми мутациями, введение сканирующих мутаций и т.п., а также обеспечить вариантную последовательность по изобретению. В качестве примера в настоящее описание включено добавление меток His или эпитопных меток с целью облегчения очистки. Ферменты, модифицированные для обеспечения специфической характеристики, представляющей интерес, могут быть дополнительно модифицированы, например, посредством мутагенеза, «перемешивания» экзонов и т.д., как известно в данной области техники, с последующим скринингом или отбором, с оптимизацией или восстановлением активности фермента, например, до уровней дикого типа, и таким образом обеспечивать другие вариантные последовательности по изобретению.
[0048] Термин «НВ-EGF» также включает в себя биологически активные фрагменты. Фрагменты, представляющие интерес, включают фрагменты, состоящие по меньшей мере из приблизительно 20 смежных аминокислот, обычно по меньшей мере из приблизительно 50 смежных аминокислот, и могут содержать 100 или более аминокислот, вплоть до полноразмерного белка, и могут удлиняться дальше и содержать дополнительные последовательности.
[0049] Представляющие интерес модификации белка, не изменяющие первичную последовательность, но обеспечивающие другие вариантные белки по изобретению, включают химическую дериватизации белков, в том числе, например, ацилирование, например лаурильных, стеарильных, миристильных, децильных и т.п. групп, ПЭГилирование, этерификацию или амидирование. Такие модификации могут быть использованы для повышения устойчивости фермента к протеолизу, например посредством присоединения боковых цепей ПЭГ или лаурильных групп к поверхностным лизинам. Также включены модификации гликозилирования, например, выполненные посредством модификации паттернов гликозилирования белка в процессе его синтеза и обработки или в дальнейших этапах обработки; например, подвергая белок действию ферментов, которые влияют на гликозилирование, например, ферментов млекопитающих, которые вызывают гликозилирование или дегликозилирование. Также охвачены последовательности, имеющие фосфорилированные остатки аминокислот, например, фосфотирозин, фосфосерин или фосфотреонин.
[0050] Также подходят для использования на практике и предложена в настоящем изобретении белки, которые были модифицированы с помощью способов молекулярной биологии и/или химии для улучшения их УСТОЙЧИВОСТИ к протеолитической деградации, окислению и т.д., а также для оптимизации свойств растворимости или для того, чтобы сделать их более подходящими для применения в качестве терапевтического агента. Например, остов белка может быть подвергнут циклизации для повышения стабильности (см. Friedler et al. (2000) J. Biol. Ghent. 275: 23783-23789). Аналоги таких белков включают те, которые кроме природных L-аминокислот содержат и другие остатки, например, D-аминокислоты или не встречающиеся в природе синтетические аминокислоты.
[0051] Миметики HB-EGF. HB-EGF агенты, представляющие интерес, также включают в себя миметики, например малые молекулы, белки, аптамеры и т.п., обеспечивающие биологическую активность HB-EGF. Такие виды активности включают связывание HB-EGF с рецептором EGF и гепаринсульфат-протеогликангми на клеточной поверхности.
[0052] Про-HB-EGF синтезируется в виде одного трансмембранного белка-предшественника I типа, который затем подвергается значительной протеолитической обработке, называемой шеддингом эктодомена (см., например, Yan et al. J Cell Biol. 2002; 158 (2): 221-6; Asakuraet al. Nat Med. 2002; 8 (1): 35-40; Izumi et al. Embo J. 1998; 17 (24): 7260-72; Nakagawa et al. J Biol Chem. 1996; 271 (48): 30858-63). Это обеспечивает высвобождение растворимой зрелой формы HB-EGF. Металлопротеиназы (включая ADAM 9, 10, 12, 17), которые несут ответственность за шеддинг эктодомена про-HB-EGF, преимущественно регулируют связывание зрелого HB-EGF и регулируют активацию EGFR(cm. Cisse et al. J Biol Chem. 2005; 280 (49): 40624-31; Peschon al. Science. 1998; 282 (5392): 1281-4; Sahin and Blobel FEBS Lett. 2007; 581 (1): 41-4; Sahin et al. J Cell Biol. 2004; 164 (5): 769-79). Впоследствии НВ-ЕGF действует как через EGFR-зависимые, так и через EGFR-независимые механизмы. HB-EGF содержит EGF-подобный домен, который, как считается, необходим представителям семейства EGF для связывания и активации EGFR (Thompson et al. J Biol Chem. 1994; 269 (4): 2541-9).
[0053] Представители семейства EGF могут индуцировать юкстакринную, аутокринную, паракринную или эндокринную передачу сигналов в зависимости от окружающей среды клетки, потому что под действием металлопротеиназ они отщепляются от мембраны с образованием зрелого растворимого фактора роста (Singh and Harris, Cell Signal. 2005; 17 (10): 1183-93). Существует четыре идентифицированных представителя семейства EGFR (HER1, HER2, HER3 и HER4). Они являются структурно родственными тирозинкиназе с одним трансмембранным доменом и доменом в цитоплазме (Plowman, et al. Proc Natl Acad Sci USA. 1993; 90 (5): 1746-50; Taylor ft al. Semin Cell Dev Biol. 2014). Представители семейства EGF имеют отличающуюся от семейства EGFR активность связывания. В отличие от EGF, HB-EGF связывается как с HER1, так и с HER4, как это делают бетацеллюлин и нейрегулин 2. См. Higashiyama et al. Science. 1991; 251 (4996): 936-9; Chang et al. Nature. 1997; 387 (6632): 509-12; Carraway et al. Nature. 1997; 387 (6632): 512-6; Shing et al. Science. 1993; 259 (5101): 1604-7. HB-EGF также уменьшает количество эпителиальных маркеров, таких как кератины 1, 5; 10 и 14, при этом увеличивая количество генов клеточной подвижности, таких как SNA1, ZEB1, СОХ-2 и ММР1 (см. Stoll et al. J Invest Dermatol. 2012; 132 (9): 2148-57).
[0054] Термин «эффективное количество» или «терапевтически эффективное количество» HB-EGF или агента, обеспечивающего активность HB-EGF, представляет собой дозу, которая при применении в течение периода времени, улучшает заживление хронической перфорации БП.
[0055] Композиция, т.е. жидкие капли, гель с замедленным высвобождением и т.д. может содержать HB-EGF или агент с эквивалентной активностью, обеспечивающий активность HB-EGF, в концентрации, составляющей по меньшей мере приблизительно 1 нг/мл, по меньшей мере приблизительно 10 нг/мл, по меньшей мере приблизительно 100 нг/мл, по меньшей мере приблизительно 1 мкг/мл, по меньшей мере приблизительно 10 мкг/мл, по меньшей мере приблизительно 100 мкг/мл, по меньшей мере приблизительно 200 мкг/мл по меньшей мере приблизительно 500 мкг/мл, по меньшей мере приблизительно 750 мкг/мл, по меньшей мере приблизительно 1 мг/мл, по меньшей мере приблизительно 5 мг/мл, по меньшей мере приблизительно 10 мг/мл, по меньшей мере приблизительно 50 мг/мл, по меньшей мере приблизительно 100 мг/мл и вплоть до приблизительно 10 мг/мл, вплоть до приблизительно 25 мг/мл, вплоть до приблизительно 50 мг/мл, вплоть до приблизительно 100 мг/мл, вплоть до приблизительно 500 мг/мл. Композиция, предназначенная для замедленного высвобождения, может быть предоставлена с более высокой исходной концентрацией по сравнению с композицией для повторного введения.
[0056] Объем композиции, как правило, является таким, который необходим для обеспечения подходящего контакта с барабанной перепонкой, например, вплоть до приблизительно 5 мкл, вплоть до приблизительно 10 мкл, вплоть до приблизительно 25 мкл, вплоть до приблизительно 35 мкл, вплоть до приблизительно 50 мкл, вплоть до приблизительно 75 мкл, вплоть до приблизительно 100 мкл, вплоть до приблизительно 250 мкл, вплоть до приблизительно 375 мкл, вплоть до приблизительно 500 мкл. Альтернативно может быть предоставлена капельница, в которой доза составляет одну каплю, две капли, капли, три капли, причем, как известно в данной области техники, капля имеет объем около 50 мкл.
[0057] Терапевтически эффективное количество обеспечивает клинически значимый ответ у субъекта, проявляющийся в том, например, что происходит стимуляция заживления перфорации барабанной перепонки. Альтернативно, терапевтически эффективное количество является достаточным для улучшения клинически значимого состояния заживления раны у хозяина.
[0058] Могут быть разработаны композиции или устройство для замедленного или пролонгированного высвобождения, имеющие t½ высвобождения лекарственного средства, т.е. промежуток времени для высвобождения половины активного агента, подходящий для начальной дозы и желаемой локальной концентрации, например, t½ составляет приблизительно 24 часа, приблизительно 48 часов, приблизительно 3 суток, приблизительно 4 суток, приблизительно 5 суток, приблизительно 1 неделю, приблизительно 10 суток, приблизительно 2 недели, приблизительно 3 недели и т.д.
[0059] Композиция, не являющаяся композицией замедленного или пролонгированного высвобождения, например, жидкие ушные капли и т.д., может быть введена с интервалами, подходящими для поддержания эффективной дозы, например, приблизительно каждые 3 часа, приблизительно каждые 4 часа, приблизительно каждые 6 часов, приблизительно каждые 12 часов, приблизительно каждые 18 часов, приблизительно каждые 24 часа, приблизительно каждые 48 часов и т.д.
[0060] Альтернативно, эффективное количество HB-EGF или агента, обеспечивающего активность HB-EGF, представляет собой количество, которое приводит к более быстрому заживлению перфорации или раны по сравнению с заживлением при отсутствии такого агента. Эффективное количество может также означать количество или дозу, достаточную для увеличения локальных и/или системных уровней HB-EGF, например, приблизительно на 10 процентов, предпочтительно, приблизительно на 50 процентов, и более предпочтительно приблизительно на 100 процентов от уровня, обнаруженного до введения активного агента или лекарственного средства.
[0061] Период времени контактирования с HB-EGF может составлять вплоть до одних суток, вплоть до 2 суток, вплоть до 3 суток, вплоть до 5 суток, вплоть до 7 суток, вплоть до 10 суток, вплоть до 12 суток, вплоть до 2 недель, вплоть до 3 недель или более в соответствии с потребностями индивидуума.
[0062] «Контроль», «контрольное значение» или «эталонное значение» в анализе представляет собой значение, которое используется для обнаружения изменения, например, заживления перфорированной барабанной перепонки или раны кожи, или в каких-либо других анализах, описанных в настоящем документе. Например, при изучении заживления перфорации барабанной перепонки, ингибирующее/стимулирующее влияние агента может быть оценено путем сравнения заживления раны или перфорации с контрольным заживлением. Контроль или эталон может представлять собой, например, предварительно заданное эталонное значение или может быть определен экспериментально. Например, в таком анализе контроль или эталон может представлять собой заживление аналогичной раны или перфорации у животного, не подвергавшегося воздействию лекарственного средства или активного агента, или у животного, пролеченного этим же препаратом или активным агентом, но у которого способность заживления ран не нарушена.
[0063] Термин «ингибитор» включает природную или синтетическую композицию или вещество, которое предотвращает действие HB-EGF, которое снижает уровень HB-EGF или его рецептора, которое блокирует внутриклеточную передачу сигналов, когда HB-EGF приводит в действие свой родственный рецептор и т.д. Ингибиторы включают в себя нуклеиновые кислоты, например, антисмысловые, миРНК, рибозимы и т.д.; антитела, специфичные для HB-EGF или его родственного рецептора, ингибиторы малых молекул и т.д. В некоторых вариантах реализации настоящего изобретения ингибитор представляет собой OSU8-1/KB-R7785 (см. Tokomaru et al. (2000) JCB 151: 209-219, включен в данный документ путем ссылки). Антитела, специфичные для HB-EGF, и реагенты миРНК, мшРНК известны в данной области техники и коммерчески доступны (например, см. Santa Cruz Biotechnology или Bertram et al. (2009) Mech. Ageing Dev. 130: 657-669.
[0064] Альтернативно, моноклональные антитела могут быть получены с помощью обычных способов получения моноклональных антител, причем можно использовать любой способ, который обеспечивает антитела, вырабатываемые культурами стабильных клеточных линий. Примеры включают методику гибридомы (Kohler & Milstein, Nature, 256: 495-497 (1975)), методику триомы, методику В-клеточной гибридомы человека (Kozbor et al., Immunology Today 4: 72 (1983)) и методику EBV-гибридомы для получения моноклональных антител человека (Cole, et al., Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, Inc., pp. 77-96 (1985)). Методики, описанные для получения одноцепочечных антител (патент США №4946778) могут быть адаптированы для получения одноцепочечных антител к продуктам иммуногенного полипептида по настоящему изобретению. Кроме того, для экспрессии гуманизированных антител к продуктам иммуногенных полипептидов по настоящему изобретению, могут использоваться трансгенные мыши.
[0065] Термин «структура», в отношении доставки HB-EGF или ингибиторов HB-EGF, включает в себя, но не ограничивается перечисленным, любой каркас, полимер, конструкцию, сооружение, установку, поддержку, диск, блок, покрытие, слой, опору, подложку, устройство, пену. Он также включает использование собственной ткани пациента, остатков органических веществ в ране или трансплантат для действия в качестве способа доставки. Структура может применяться либо в сформированном состоянии или может быть нанесена в виде вязкой жидкости, которая впоследствии принимает твердое состояние или остается в жидкой форме.
[0066] Термин «средство доставки», когда речь идет о доставке HB-EGF или ингибиторов HB-EGF, включает, но не ограничивается перечисленным, любой полимер, агент, носитель, инструмент, процесс, среду, аппарат, прибор, приспособление, гаджет, инструмент, виджет, принадлежности или посуду. Термин «средство доставки» также относится к любому растворимому носителю или вспомогательному веществу, включая, но не ограничиваясь перечисленным, физиологический раствор, буферный физиологический раствор, декстрозу, воду, глицерин и их комбинации. Композиция должна соответствовать способу введения. Примеры подходящих композиций, известных в данной области техники, приведены в публикации Remington’s Pharmaceutical Sciences (последнее издание), Mack Publishing Company, and Easton, Pa.
[0067] При использовании в настоящем документе термины «около» или «приблизительно» означают в пределах 50 процентов, предпочтительно в пределах 20 процентов, более предпочтительно в пределах 5 процентов от заданного значения или диапазона.
[0068] Значение, которое «существенно отличается» от другого значения может означать, что существует статистически значимая разница между этими двумя значениями. Любой подходящий статистический способ, известный в данной области техники, может быть использован для оценки того, являются ли различия существенными или нет.
[0069] «Статистически значимое» различие означает значимость, определяемую в доверительном интервале, по меньшей мере при 90%, более предпочтительно при 95% доверительном интервале.
[0070] В соответствии с настоящим изобретением в нем могут быть использованы обычные способы молекулярной биологии, микробиологии и методики рекомбинантных ДНК в пределах квалификации в данной области техники. Такие методики подробно описаны в литературе. См, например., Sambrook et al (Molecular Cloning-A Laboratory Manual, Cold Spring Harbor Laboratory Press, 1989); Glover (DNA. Cloning: A Practical Approach, Volumes I and II, 1985); Hames and Higgins (Nucleic Acid Hybridization, 1985); Hames and Higgins (Transcription And Translation, 1984): Freshney (Animal Cell Culture, 1986); Perbal (A Practical Guide To Molecular Cloning, 1984); и Ausubel et al. (Current Protocols in Molecular Biology, John Wiley & Sons, Inc., 1994).
Фармацевтические композиции
[0071] Композиции, которые могут быть использованы для доставки HB-EGF и агента HB-EGF, или ингибитора HB-EGF, или другие композиции в соответствии с настоящим изобретением, включают, но не ограничиваются перечисленным, лекарственные формы для инъекций, инфузий, гель, пасты, бальзамы, воски, лосьоны, кремы для кожи, а также различные другие формы для местного применения, известные в данной области техники. Композиции также могут быть доставлены местно в форме порошка или раствора, распыляемого на рану. Альтернативно, композиции по изобретению могут быть представлены в виде раневых повязок, прокладок, пластырей, марли или других средств для нанесения на рану, из которых они переносятся в область раны. Такие устройства также включают в себя устройства замедленного высвобождения, которые непрерывно высвобождают HB-EGF, или ингибитор HB-EGF, или другие компоненты в течение пролонгированного периода времени. Что касается заживления барабанных перепонок, введение композиции с использованием геля, спрея или введение по каплям через наружный слуховой канал, является одним из предпочтительных вариантов реализации настоящего изобретения. Лекарственные формы для инъекций или инфузий содержат раствор HB-EGF или ингибитора EGF-HB в фармацевтически приемлемом жидкости, такой как, например, изотонический солевой раствор, стерильная вода или водные буферные системы. Средство доставки может также включать любую структуру, проходящую через рану. В случае барабанной перепонки оно включает, но не ограничивается перечисленным, ушные шунты или катетеры.
[0072] Фармацевтические композиции могут включать, в зависимости от желаемого состава, фармацевтически приемлемые нетоксичные носители или разбавители, которые определяются как средства доставки, обычно используемые для разработки фармацевтических композиций для введения животным или человеку. Разбавитель выбирают так, чтобы он не влиял на биологическую активность активного агента. Примерами таких разбавителей являются дистиллированная вода, забуференная вода, физиологический раствор, ФСБ, раствор Рингера, раствор декстрозы и раствор Хенкса. Кроме того, фармацевтическая композиция или состав может включать в себя другие носители, адъюванты или нетоксичные, нетерапевтические, неиммуногенные стабилизаторы, вспомогательное вещества и т.п. Композиции могут также содержать дополнительные вещества, чтобы приблизиться к физиологическим условиям, такие как регулирующие уровень рН и буферные агенты, агенты, регулирующие токйчность, смачивающие агенты и детергенты.
[0073] Композиция может также содержать любой из множества стабилизирующих агентов, таких как, например, антиоксидант. Если фармацевтическая композиция содержит полипептид, указанный полипептид может присутствовать в виде комплекса с различными хорошо известными соединениями, которые повышают стабильность полипептида in vivo, или иным образом усиливают его фармакологические свойства (например, увеличивают период полужизни полипептида, снижают его токсичность, повышают растворимость или поглощение). Примеры таких модификаций или комплексообразующих агентов включают сульфат, глюконат, цитрат и фосфат. Полипептиды композиции могут также образовывать комплексы с молекулами, которые улучшают их характеристики in vivo. Такие молекулы включают, например, углеводы, полиамины, аминокислоты, другие пептиды, ионы (например, натрий, калий, кальций, магний, марганец) и липиды.
[0074] Дальнейшие указания относительно композиций, подходящих для различных типов введения, можно найти в Remington’s Pharmaceutical Sciences, Mace Publishing Company, Philadelphia, Pa., 17th ed. (1985). См. краткий обзор способов доставки лекарственных средств в публикации Langer, Science 249: 1527-1533 (1990).
[0075] Фармацевтические композиции могут быть введены для терапевтических видов лечения. Токсичность и терапевтическая эффективность активного ингредиента может быть определена в соответствии со стандартными фармацевтическими процедурами в культурах клеток и/или с использованием экспериментальных животных, включая, например, определение LD50 (дозы, летальной для 50% популяции) и ED50 (дозы, терапевтически эффективной у 50% популяции). Соотношение доз между токсичным и терапевтическим эффектами представляет собой терапевтический индекс, который выражают как соотношение LD50/ED50. Предпочтительными являются соединения, демонстрирующие большие терапевтические индексы.
[0076] Данные, полученные из исследований в культурах клеток и/или с использованием животных, можно применять для определения диапазона доз для человека. Доза активного ингредиента обычно находится в пределах диапазона циркулирующих концентраций, которые включают ED50 с низкой токсичностью. Доза может изменяться в пределах этого диапазона в зависимости от используемой лекарственной формы и пути введения.
[0077] Фармацевтические композиции, описанные в настоящем документе, можно вводить, используя множество различных способов. Примеры включают введение композиции, содержащей фармацевтически приемлемый носитель посредством местных путей введения, например на поверхность БП, внутрь барабанной перепонки, через барабанную перепонку и т.д.
[0078] По
стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостатические и растворенные вещества, которые придают композиции изотоничность, и водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты, солюбилизаторы, загустители, стабилизаторы и консерванты.
[0079] Компоненты, используемые для разработки фармацевтических композиций являются предпочтительно компонентами высокой чистоты и по существу не содержат потенциально вредных примесей (например, по меньшей мере соответствуют категории чистоты согласно требованиям Национальной комиссии по продовольствию США (NF), как правило, по меньшей мере соответствуют аналитической категории, и более типично по меньшей мере фармацевтической категории). Кроме того, композиции, предназначенные для применения in vivo, как правило, являются стерильными. В случае если данное соединение необходимо синтезировать перед применением, полученный продукт, как правило, по сути не содержит каких-либо потенциально токсичных веществ, в частности любых эндотоксинов, которые могут присутствовать в процессе синтеза или очистки. Композиции для парентерального введения также являются стерильными, по сути изотоническими и произведенными в условиях GMP.
[0080] Эффективное количество терапевтической композиции для введения конкретному пациенту будет зависеть от множества факторов, некоторые из которых будут отличаться от пациента к пациенту. Компетентный врач сможет определить эффективное количество терапевтического агента для введения пациенту для стимуляции заживления хронической перфорации БП. Используя данные ED50, полученные у животных, и другую доступную информацию, врач может определить безопасную дозу для индивидуума, в зависимости от пути введения. Для поддержания терапевтической концентрации, композиции, которые быстро выводятся из организма, можно вводить в более высоких дозах или в повторных дозах. Используя обычную квалификацию, компетентный врач сможет оптимизировать дозу конкретной терапевтической или визуализирующей композиции в ходе обычных клинических испытаний. Обычно доза составляет от 0,001 до 100 мг агента на килограмм массы тела субъекта.
Композиция, т.е. жидкие капли, гель с замедленным высвобождением и т.д. может содержать HB-EGF или агент с эквивалентной активностью, обеспечивающий активность HB-EGF, в концентрации, составляющей по меньшей мере приблизительно 1 мкг/мл, по меньшей мере приблизительно 10 мкг/мл, по меньшей мере приблизительно 100 мкг/мл, по меньшей мере приблизительно 200 мкг/мл, по меньшей мере приблизительно 500 мкг/мл, по меньшей мере приблизительно 750 мкг/мл, по меньшей мере приблизительно 1 мг/мл, по меньшей мере приблизительно 5 мг/мл, по меньшей мере приблизительно 10 мг/мл, по меньшей мере приблизительно 50 мг/мл, по меньшей мере приблизительно 100 мг/мл и вплоть до приблизительно 10 мг/мл, вплоть до приблизительно 25 мг/мл, вплоть до приблизительно 50 мг/мл, вплоть до приблизительно 100 мг/мл, вплоть до приблизительно 500 мг/мл. Композиция, предназначенная для замедленного высвобождения, может быть предоставлена с более высокой исходной концентрацией по сравнению с композицией для повторного введения. Терапевтически активное количество может варьироваться в зависимости от таких факторов, как состояние заболевания, возраст, пол и масса тела индивидуума. Для обеспечения оптимального терапевтического ответа схема дозирования может быть скорректирована. Например, ежедневно можно вводить более одной отдельной дозы, или доза может быть пропорционально уменьшена в соответствии с показаниями и необходимостью терапевтической ситуации.
[0081] Может быть обеспечен объем от приблизительно 1 до 3 капель или, при введении в твердой или полутвердой форме, могут быть приготовлены композиции заданного объема, например, с объемом от вплоть до приблизительно 5 мкл до вплоть до приблизительно 500 мкл. Устройство может быть сформировано в любой форме или конформации, которая облегчит его применение в целевой области для стимуляции или ингибирования заживления. Геометрическая форма твердой или полутвердой лекарственной формы представляет собой любую подходящую для доставки к барабанной перепонке, например сфера, сплющенная сфера, пленка, пластырь, диск равномерной или неравномерной толщины и т.п.
[0082] Композицию можно вводить субъекту в виде серии из более чем одного введения. Для терапевтических композиций иногда необходимо регулярное периодическое введение (например, каждые 4 часа, каждые 6 часов, каждые 12 часов, каждые 24 часа и т.д.), например если композиция предоставлена в виде жидкости для местного применения.
[0083] Композиции, пригодные для местного, чрескожного и трансдермального введения, могут быть получены путем использования соответствующих суспендирующих агентов, солюбилизаторов, загустителей, стабилизаторов и консервантов. Композиции для местного применения могут быть использованы также со средствами для обеспечения непрерывного введения, например, включены в гранулы с медленным высвобождением или пластыри с контролируемым высвобождением.
[0084] Активный агент может также быть введен в состав композиции в виде биологически совместимого геля, причем этот гель можно наносить местно или имплантировать (например, для обеспечения замедленного высвобождения в месте лечения). Подходящие гели и способы составления рецептуры желаемого соединения для доставки с помощью геля хорошо известны в данной области (см., например, патенты США под номерами 5801033; 5827937; 5700848; и MATRIGEL™). Примером этого варианта реализации настоящего изобретения является доставка HB-EGF или ингибитора HB-EGF через слуховой канал посредством биосовместимой жидкости или устройства, которое отвердевает внутри слухового канала вблизи барабанной перепонки и доставляет HB-EGF или ингибитор HB-EGF по мере того, как средство доставки со временем растворяется. Средство доставки можно размещать в канале, в барабанной перепонке или внутри среднего уха.
[0085] Композиции могут быть предоставлены в единичной дозированной форме, причем термин «единичная дозированная форма» относится к физически дискретным единицам, подходящим в качестве единичных доз для субъектов-людей, где каждая единица содержит предварительно заданное количество протеазы, рассчитанное как достаточное количество для обеспечения заданного эффекта, в сочетании с фармацевтически приемлемым разбавителем, носителем или средством доставки. Характеристики единичных дозированных форм настоящего изобретения зависят от конкретного используемого комплекса и эффекта, который должен быть достигнут, а также от фармакодинамики, связанной с каждым комплексом, в организме хозяине.
[0086] Аспекты настоящего изобретения включают в себя гидрогелевые композиции на основе сшитых сополимеров, содержащие эффективную дозу абсорбированного HB-EGF, как описано выше. Гидрогелевые композиции на основе сшитых сополимеров по настоящему изобретению в соответствии с определенными вариантами реализации включают сополимер хитозана и сложного полиэфира и гидролизуемый сшивающий агент. В некоторых вариантах реализации настоящего изобретения сшитые гидрогели дополнительно содержат фибриноген. В некоторых таких вариантах реализации настоящего изобретения гидрогели на основе сшитых сополимеров включают сополимер хитозана и сложного полиэфира и гидролизуемый сшивающий агент, например, полилактид. Сшитые гидрогели хитозана и полилактида могут иметь соотношение хитозана к полилактиду в диапазоне от 1:1 до 10:1, например, от 1:1 до 8:1, причем в некоторых случаях, сшитые гидрогели хитозана и полилактида имеют соотношение хитозана к полилактиду 8:1. Массовый процент хитозана в гидрогелях на основе сшитого сополимера, представляющих интерес; может варьироваться в диапазоне от 1% до 99%, а массовый процент сложного полиэфира может варьироваться в диапазоне от 1% до 99%. В некоторых вариантах реализации настоящего изобретения гидрогели на основе сополимера содержат один или более сложноэфирных или амидных связей между хитозаном и компонентами сложного полиэфира. Гидрогели на основе сшитых сополимеров, представляющие интерес, также включают сшивающий агент. В некоторых вариантах реализации настоящего изобретения сшивающий агент предназначен для гидролиза в физиологических условиях. В некоторых вариантах реализации настоящего изобретения сшивающий агент может быть акрилатным сшивающим агентом, например, метакрилатным сшивающим агентом. Гидролизуемые сшивающий агент может присутствовать в гидрогеле на основе сшитого сополимера в количестве в диапазоне от 0,05% до 10% масс./масс. сшивающего агента, например от 0,1% до 9% масс./масс, например от 0,5% до 8% масс./масс, например от 0,75% до 7% масс./масс. и включительно от 1% до 5% масс./масс. В зависимости от протокола, используемого для сшивания обсуждаемых гидрогелей, плотность сшивки может варьироваться. В некоторых случаях гидрогель сшит химической сшивкой. Таким образом, плотность сшивки может варьироваться в зависимости от типа и концентрации используемого химического сшивающего агента. Альтернативно, гидрогель может подвергаться фотосшивке и плотность сшивки может варьироваться в зависимости от интенсивности электромагнитного излучения, контактировавшего с гидрогелевой композицией, а также от продолжительности облучения. В некоторых вариантах реализации настоящего изобретения плотность сшивки обсуждаемых гидрогелей на основе сшитых сополимеров может быть, например, в диапазоне от 1×10-15 моль/см3 до 1×10-3 моль/см3. Альтернативно, в зависимости от количества сшивающего агента, коэффициент набухания обсуждаемых гидрогелей может изменяться в пределах, например, от 1 до 35. Аналогичным образом, модуль сжатия гидрогелей может изменяться, например, в диапазоне от 1 кПа до 35 кПа: Смотри, например, находящуюся одновременно на рассмотрении международную патентную заявку PCT/US 2014/033512, включенную в настоящий документ путем ссылки.
[0087] Гидрогелевые композиции необязательно содержат фибриноген. Фибриноген может быть введен в гидрогелевую композицию перед или после сшивки гидрогеля. Например, в некоторых случаях фибриноген добавляют к предшественнику гидрогелевой композиции. Фибриноген может присутствовать в гидрогеле на основе сшитого сополимера в количестве в диапазоне от 0,05% до 50% масс./масс. фибриногена, например от 0,1% до 45% масс./масс., например от 0,5% до 40% масс./масс., например от 0,75% до 35% масс./масс., например от 1% до 30%, например от 2% до 20%, например от 5% до 15% и включая 10% масс./масс.
[0088] Гидрогели могут быть синтезированы для достижения определенного профиля высвобождения. В некоторых вариантах реализации настоящего изобретения гидрогели на основе сшитых сополимеров, предложенные в настоящем изобретении, предназначены для высвобождения HB-EGF или агента HB-EGF в физиологических условиях по сути со скоростью высвобождения нулевого порядка. В других вариантах реализации настоящего изобретения обсуждаемые гидрогели на основе сшитых сополимеров предназначены для высвобождения HB-EGF или агента HB-EGF, в физиологических условиях по сути со скоростью высвобождения первого порядка. В других вариантах реализации настоящего изобретения обсуждаемые гидрогели на основе сшитых сополимеров предназначены для высвобождения HB-EGF или агента HB-EGF в физиологических условиях по сути со скоростью высвобождения второго порядка. В некоторых вариантах реализации настоящего изобретения обсуждаемые гидрогели на основе сшитых сополимеров предназначены для профиля высвобождения, который включает: 1) первый период, во время которого HB-EGF или агент HB-EGF высвобождается из гидрогеля с первой предварительно заданной скоростью; и 2) второй период, во время которого HB-EGF или агент HB-EGF высвобождается из гидрогеля со второй предварительно заданной скоростью.
[0089] В некоторых вариантах реализации настоящего изобретения соотношение хитозана и сложного полиэфира в гидрогеле может варьировать, в некоторых вариантах реализации настоящего изобретения в диапазоне от 10:1 до 9,5:1; от 9,5:1 до 9:1; от 9:1 до 8,5:1; от 8,5:1 до 8:1; от 8:1 до 7,5:1; от 7,5:1 до 7:1; от 7:1 до 6,5:1; от 6,5:1 до 6:1; от 6:1 до 5,5:1; от 5,5:1 до 5:1; от 5:1 до 4,5:1; от 4,5:1 до 4:1; от 4:1 до 3,5:1; от 3,5:1 до 3:1; от 3:1 до 2,5:1; от 2,5:1 до 2:1; от 2:1 до 1,5:1; от 1,5:1 до 1:1. Например, массовое соотношение компонента хитозана и компонента сложного полиэфира может быть в диапазоне от 10:1 до 1:1, например от 8:1 до 1:1, например от 5:1 до 1:1, например от 4:1 до 1:1, включая от 2:1 до 1:1. В некоторых случаях соотношение хитозана и сложного полиэфира составляет 1:1. В других вариантах реализации настоящего изобретения соотношение хитозана и сложного полиэфира может варьироваться, в некоторых вариантах реализации настоящего изобретения в диапазоне от 1:1 до 1:1,5; от 1:1,5 до 1:2; от 1:2 до 1:2,5; от 1:2,5 до 1:3; от 1:3 до 1:3,5; от 1:3,5 до 1:4; от 1:4 до 1:4,5; от 1:4,5 до 1:5; от 1:5 до 1:5,5; от 1:5,5 до 1:6; от 1:6 до 1:6,5; от 1:6,5 до 1:7; от 1:7 до 1:7,5; от 1:7,5 до 1:8; от 1:8 до 1:8,5; от 1:8,5 до 1:9; от 1:9 до 1:9,5; от 1:9,5 до 1:10. Например, соотношение хитозана и сложного полиэфира может находиться в диапазоне от 1:1 до 1:10, например от 1:1 до 1:8, например от 1:1 до 1:5, например от 1:1 до 1:4, включая от 1:1 до 1:2.
[0090] Гидрогели на основе сшитых сополимеров могут иметь массу 1 кДа или больше, например 2 кДа или больше, например 3 кДа или больше, например 5 кДа или больше, например 10 кДа или больше, например 15 кДа или больше, например 20 кДа или больше, например 25 кДа или больше, например 30 кДа или больше, например 40 кДа или больше, например 50 кДа или больше, например 60 кДа или больше и включая 75 кДа или больше.
[0091] После приготовления фармацевтические композиции могут быть помещены в соответствующий контейнер и промаркированы для лечения указанного патологического состояния. Для введения композиции по настоящему изобретению, такая маркировка будет включать количество, частоту и способ введения.
Комбинированные композиции;
[0092] Составы по настоящему изобретению могут содержать эффективную дозу HB-EGF в комбинации со вторым активным агентом, в частности, другим антимикробным агентом. Например, другие агенты представляющие интерес, включают широкое разнообразие антибиотиков, как известно в данной области техники. Классы антибиотиков включают в себя пенициллины, например пенициллин G, пенициллин V, метициллин, оксациллин, карбенициллин, нафциллин, ампициллин и тд.; пенициллины в комбинации с β-ингибиторами лактамаз, цефалоспорины, например цефаклор, цефазолин, цефуроксим, моксалактам и тд.; карбапенемы; монобактамы; аминогликозиды; тетрациклины; макролиды; линкомицины; полимиксины; сульфаниламиды; хинолоны; хлорамфеникол; метронидазол; спектиномицин; триметоприм; ванкомицин; и т д. противовирусные агенты например ацикловир, ганцикловир и т.д. могут быть включены.
[0093] Цитокины и факторы роста также находят применение в комбинации с HB-EGF, например такие факторы роста, как трансформирующий фактор роста (TGF)-β, тромбоцитарный фактор роста (PDGF), фибробластный фактор роста (FGF) и эпидермальный фактор роста (EGF), VEGF, фактор некроза опухоли-α (TNF-α), эндотелин-1, кератиноцитарный фактор роста и т.п. См., например, Steed, D. et al., J. Am. Call. Surg. 183: 61-64 (1996); Richard, J. et al., Diabetes Care 18: 64-69 (1995); Steed, D., J. Vase. Surg. 21: 71-78 (1995); Kelley, S. et al., Proc. Soc. Exp. Biol. 194: 320-326 (1990).
Способы применения
[0094] В соответствии с настоящим изобретением заживление раны при хронической перфорации барабанной перепонки улучшается при предоставлении повышенных уровней HB-EGF. Это может быть достигнуто несколькими различными способами. Например, пациента можно пролечить эффективным количеством активного агента, такого как, например, лекарственное средство, гормон, цитокин, антитело или другого соединения, которое стимулирует экспрессию HB-EGF; уменьшает деградацию HB-EGF; или увеличивает местные или системные уровни HB-EGF или гомолога или производного HB-EGF. В терапевтических целях можно также вводить нуклеиновые кислоты, кодирующие HB-EGF.
[0095] Обычно композицию, содержащую белок HB-EGF, например растворимую форму HB-EGF человека, местно вводят индивидууму, страдающему хронической перфорацией БП, через наружный слуховой канал, в течение периода времени, по сути достаточного для закрытия перфорации. Субъект, являющийся человеком или не являющийся человеком, может страдать от патологического состояния, которое препятствует или замедляет заживление перфорации барабанной перепонки или не страдать от такого состояния.
[0096] В настоящем изобретении предложены композиции HB-EGF или ингибитора HB-EGF, которые при введении в эффективном количестве приводят к увеличению или снижению уровня HB-EGF в области раны субъекта. Например, для ускорения заживления барабанной перепонки, композиция, содержащая HB-EGF, может быть нанесена на область, окружающую перфорацию барабанной перепонки. Ингибитор HB-EGF можно также наносить для ингибирования нормального или чрезмерного заживления раны. В случае композиций HB-EGF для ускорения заживления барабанной перепонки, композиция может быть нанесена на область, прилегающую или соседствующую с перфорацией барабанной перепонки. Их можно наносить с помощью любого биоразлагаемого или бионеоразлагаемого источника или структуры.
[0097] В другом варианте реализации настоящего изобретения способ настоящего изобретения применяют для ингибирования заживления перфорированной барабанной перепонки у субъекта. Субъект, являющийся человеком или не являющийся человеком, может страдать от патологического состояния, которое препятствует или замедляет заживление перфорации барабанной перепонки или не страдать от такого состояния. Например, такие способы можно применять в качестве замены миринготомии и введения тимпаностомических трубок, которые обычно назначают при хроническом среднем отите, пороке развития барабанной перепонки уха или евстахиевой трубы, синдроме Дауна, расщеплении неба (волчья пасть) и баротравмах (травма среднего уха, вызванная снижением давления воздуха) и т.д. Обычно тимпаностомическую трубку вводят в БП и удерживают в течение продолжительного периода времени, например в течение периода вплоть до одного месяца, вплоть до 2 месяцев, вплоть до 3 месяцев, вплоть до 4 месяцев, вплоть до 6 месяцев или более.
[0098] Способы также находят применение в группе животных моделей, которая обеспечивает клинически значимую модель патологических состояний перфорированной барабанной перепонки человека. В таких моделях животное может быть любым удобным экспериментальным животным, например грызунами, зайцеобразными и т.д, и включая, но не ограничиваясь перечисленным, мышей, крыс, морских свинок, кроликов, котов, собак, приматов, не относящихся к человеческому роду и т.п.
[0099] В таких вариантах реализации настоящего изобретения для создания перфорации БП вводят эффективную дозу ингибитора шеддинга лиганда EGFR, обычно посредством местного контактирования с барабанной перепонкой. В некоторых таких вариантах реализации настоящего изобретения вначале можно выполнить небольшую перфорацию, например площадью от приблизительно 0,1 до 10 мм2, от приблизительно 0,1 до приблизительно 5 мм2, от приблизительно 0,1 до 2,5 мм2, от приблизительно 0,1 до приблизительно 1 мм2. После начальной перфорации рана контактирует с эффективной дозой ингибитора HB-EGF, находящейся в композиции, и в течение периода времени, как предложено в настоящем документе. Активная доза ингибитора может поддерживаться в течение периода времени, необходимого для наличия перфорации.
Наборы
[00100] В другом аспекте настоящего изобретения предлагается набор для лечения хронической перфорации БП. Набор включает в себя композицию, которая обеспечивает эффективную дозу HB-EGF, например, в форме капель, устройств, композиций и т.п. Набор также может включать в себя устройство доставки, например, дозатор для ушных капель, шприц для доставки композиции, двуствольный шприц для доставки двухкомпонентной композиции и т.п. Набор может также содержать инструкции по применению.
[00101] Альтернативно может быть предложен набор для создания хронической перфорации БП. Набор включает в себя композицию, которая обеспечивает эффективную дозу HB-EGF, например, в форме капель, устройств, композиций и т.п. Набор также может включать в себя устройство доставки, например, дозатор для ушных капель, шприц для доставки композиции, двуствольный шприц для доставки двухкомпонентной композиции и т.п. Набор может также содержать инструкции по применению. Набор может дополнительно содержать стерильную иглу или скальпель для создания начальной перфорации в БП.
Пример 1
Ингибирование HB-EGF
[00102] HB-EGF является критически важным для заживления раны в модели барабанной перепонки. Нормализованная интенсивность сигнала HB-EGF-подобного фактора роста после перфорации барабанной перепонки у крыс показывает 8,5-кратное стимулирование HB-EGF-подобного фактора роста. В настоящем описании показано, что экспериментальное ингибирование активности HB-EGF предотвращает заживление барабанной перепонки.
[00103] Для создания модели хронической перфорации барабанной перепонки можно ингибировать шеддинг лиганда EGFR. Промежуточные перфорации были созданы в натянутой части БП с использованием изогнутой иглы у 20 мышей. OSU8.1 (10 мМ), селективный ингибитор HB-EGF (см. Tokumaru et al. (2000) J. Cell Biol.), вводили инъекцией в гелевую пену (размещенную через перфорацию и на ней) в течение семи дней. Мышей умерщвляли в моменты времени (день 2, 7, 14, 30, 44, 60 и 90), чтобы наблюдать эффекты миграции кератиноцитов. Противоположное ухо использовали в качестве контроля, в него на гелевую пену помещали физиологический раствор. Все из этих перфораций закрывались в пределах 2 недель. Пять из семи (71%) перфораций в обработанных ушах были открытыми через три месяца. Репрезентативные изображения хронической перфорации БП показаны на Фигуре 5. Размер перфорации был стабильным в течение трех месяцев (с использованием программного обеспечения ImageJ для расчета площади перфорации в виде процента от площади натянутой части). У большей когорты, 87,9% (n=58), было наличие через 3 месяца хронических перфораций. В предварительном исследовании, проведенном авторами настоящего изобретения, была установлена воспроизводимая животная модель на основе применения фактора роста при хронической перфорации БП.
[00104] В таблице 1 показаны результаты применения ингибитора HB-EGF (OSU8-1) для создания острой перфорации барабанной перепонки у мышей. 100% перфораций, пролеченных ингибитором HB-EGF, присутствовали через два месяца по сравнению с 5% в контрольной группе, и 71% присутствовали через три месяца по сравнению с 5% в контрольной группе.

[00105] Создание животной модели хронического гнойного среднего отита. После создания модели хронической перфорации с окклюзией ЕТ, через существующие хронические перфорации в среднее ухо инокулировали два типа бактерий. Через 2 недели отбирали жидкость из уха и отправляли для проведения исследования на наличие бактерий с помощью полимеразной цепной реакции (ПЦР). Выбранные бактерии представляли собой две из наиболее часто вовлеченных при хроническом заболевании уха, Streptococcus pneumonia типа 3 (доза 6×106 колониеобразующих единиц на мл) и Pseudomonas aeruginosa (доза 6×109 колониеобразующих единиц на мл).
Пример 2
Лечение хронической перфорации барабанной перепонки
[00106] Была продемонстрирована эффективность лечения хронических перфораций БП с помощью HB-EGF.
[00107] Биосовместимый рассасывающийся полимер для инъекций для доставки фактора роста в ушной канал. Для лечения хронической перфорации БП желательно иметь жидкость, которую можно закапать в ухо, и которая затем отвердевает и медленно рассасывается в течение назначенного периода времени, с элюированием лекарственного средства. Скорость рассасывания полимера и скорость элюирования лекарственного средства легко регулируется в соответствии с целью, представляющей интерес.
[00108] Был разработан биоразлагаемый гидрогель на основе хитозана для доставки факторов роста, чтобы обеспечить биосовместимый, биорассасывающийся, инъекционный полимер, который может нести лекарственное средство выбора, а затем может быть инсталлирован в ушной канал. Гель имеет два жидких компонента и может отвердевает в течение нескольких минут после смешивания двух компонентов. Его можно легко вводить двуствольным шприцем. Альтернативно, растворы можно смешивать со сшивающим агентом перед доставкой и инсталлировать с помощью шприца с одним выпускным отверстием.
[00109] Недавно разработанный гидрогель на основе хитозана содержит гидрофильные молекулы остова хитозана и гидрофобные полилактидные боковые цепе. В сети сополимеров для улучшения аффинности связывания, повышения прикрепление клеток и обеспечения протеолитически разлагаемых сайтов может быть включен фибриноген. Высвобождение лекарственного средства из полимерного гидрогеля изменяется в соответствии с характеристиками, такими как гидрофильная аффинность, особенности набухания, рассасываемость и плотность сшивки полимера. Измеряли профили лекарственного высвобождения rhBMP-2 из гидрогелей на основе хитозака и особенности деградации полимерного гидрогеля в различных условиях.
[00110] Конкретное соотношение хитозана к полилактиду для геля, используемого в настоящих примерах, составляет 8:1. Кроме того, в полимерный раствор вводят 10% масс./масс. фибриногена. Композиция гидрогеля может отвердевает в течение нескольких минут после смешивания с катализатором химической сшивки. Его можно легко вводить двуствольным шприцем или шприцем с одним выпускным отверстием.
[00111] Гидрогели не ототоксичны. Гидрогели вводили в барабанные перепонки мышей после перфораций. Одно ухо заполняли полимером, в то время как в противоположное ухо инъекцию не вводили (контроль). Пороговые значения теста-ответа слухового отдела ствола мозга (ABR) и отоакустических выделений продуктов искажения (DPOAE) определяли у 9 мышей через 60 дней после хирургической перфорации обеих барабанных перепонок. Ко времени самопроизвольного заживления барабанных перепонок не было никаких различий порогов слышимости между двумя сторонами (Фигура 2). Эти данные демонстрируют, что гидрогели не ототоксичны.
[00112] HB-EGF заживляет хронические перфорации барабанной перепонки. При лечении когорты мышей с хроническими перфорациями в ушах с помощью 40 мкл геля, содержащего рекомбинантный HB-EGF в концентрации 5 мкг/мл (замедленное высвобождение дозы через биоразлагаемый полимер на основе хитозана), заживление происходило у 92% (22 из 24) по сравнению с 38% (10 из 26) контрольных животных (только полимер) за 4 недели (р<0,01). Возможность преодолеть этот критический этап хронического заживления раны БП с помощью GF, чтобы активировать шеддинг лиганда эктодомена GFR, демонстрирует пригодность для вмешательства с использованием биотерапевтических средств. Это исследование является первым исследованием лечения фактором роста в животной модели хронической перфорации, которое показало значительное преимущество по сравнению с контролем.
[00113] HB-EGF заживляет хронические перфорации барабанной перепонки с окклюзией евстахиевой трубы. Была создана животная модель хронической перфорации БП и окклюзиии ЕТ, как показано на Фигуре 3. Существующую крысиную модель окклюзии ЕТ (см. Herda et al. (2002) Laryngoscope 112: 1657-62) адаптировали для мышей, и с тех пор успешно реализовали у 80 живых мышей. Окклюзию ЕТ выполняли в модели хронической перфорации, описанной выше. Это за 3 месяца создало влажную стерильную перфорацию с отделяемым. Эта модель имитирует патологическое состояние хронической перфорации в сочетании с дисфункцией ЕТ у человека.
[00114] При лечении когорты мышей в этой модели (хронические перфорации и окклюзия ЕТ) рекомбинантным HB-EGF, в объеме 40 мкл с концентрацией 5 мкг/мл (замедленное высвобождение дозы через биоразлагаемый полимер на основе хитозана), заживление происходило у 94% (18 из 19) по сравнению с 9% (2 из 23) контрольных животных (только полимер) за 6 недель (р<0,01). Репрезентативные изображения заживших и не заживших хронических перфораций БП показаны на Фигуре 4. Гистологически перфорации закрываются толстым слоем кератиноцитов, по сравнению с контрольными животными с отсутствием слоя кератиноцитов даже в тех немногих случаях, когда произошло закрытие. Возможность преодолеть этот критический этап хронического заживления раны БП с помощью HB-EGF, чтобы активировать шеддинг лиганда эктодомена EGFR при наличии выделений из среднего уха и окклюзии ЕТ, полезна при лечении пациентов с хронической перфорацией барабанной перепонки.
[00115] Исследования в животной модели хронического гнойного среднего отита. После создания модели хронической перфорации с окклюзией ЕТ, проводили инокуляцию в среднее ухо Pseudomonas aeruginosa (доза 6×109 колониеобразующих единиц на мл) через существующие хронические перфорации. Через 2 недели отбирали жидкость из уха и отправляли для проведения исследования для подтверждения наличия бактерий с помощью полимеразной цепной реакции (ПЦР). Этот положительный результат ПЦР подтверждал модель CSOM.
[00116] Затем мышей разделяли на две когорты. Одна получала только полимер. Другая получала HB-EGF в дозе 5 мкг/мл (та же доза, что и в описанных выше моделях). Заживление в группе HB-EGF составляло 100% (16 из 16) по сравнению с 41% (7/17) в контрольной группе (р<0,01). В контрольной группе при наличии заживления оно также имело отличия. Часто БП была очень тонкой и полупрозрачной по сравнению с почти непрозрачной нормальной БП. Заживление в группе HB-EGF оказалось нормальным. Возможность все еще преодолеть этот критический этап хронического заживления раны БП с помощью HB-EGF, чтобы активировать лиганд эктодомена EGFR в ближайшей модели CSOM подтверждает этот способ лечения.
Пример 3
[00117] Транстимпанальный способ доставки (Фигуры 5, 6 и 7). Средство доставки для доставки HB-EGF или HB-EGF размещают вплотную к барабанной перепонке или вводят через канал или через евстахиеву трубу. Через некоторый период времени его можно удалить или оно подвергнется биоразложению. Средство доставки может иметь конфигурацию для удержания его внутри барабанной перепонки. Оно может представлять собой кольцо, манжету, иметь выступы, канавки или любое изменение по ширине или высоте. Средство доставки может иметь более чем один из вышеперечисленных элементов для удержания его на месте. Средство доставки может быть перфорировано или иметь просвет любого подходящего размера. В нем может быть любое количество выступов любой ширины и размеров, которые считаются достаточными или избыточными по сравнению с необходимым средством, чтобы удерживаться в барабанной перепонке.
[00118] На Фигуре 5 изображен ушной канал 100; наружное ухо 110; и барабанная перепонка 120. Также изображено устройство 125 для трансмембранной доставки лекарственного средства, имеющее ширину 130 и длину 140.
[00119] На Фигуре 6 изображен альтернативный вариант реализации устройства 126 для трансмембранной доставки. Устройство имеет ширину 131 и длину 141. Устройство 126 содержит один или оба из внешнего ограничителя 150 и внутреннего ограничителя 155, причем ограничитель имеет ширину 160.
[00120] На Фигурах 7А-7В изображен альтернативный вариант реализации устройства 127 для трансмембранной доставки. На Фигуре 7А представлен вид сверху, демонстрирующий ушной канал 100 и барабанную перепонку 120. Устройство 127 для доставки имеет ширину 132 и длину 142. Устройство содержит множество выступов 170, расположенных в продольном направлении вдоль устройства, причем эти выступы имеют длину 171 и ширину 172. На Фигуре 7В изображено устройство в поперечном сечении.
Пример 4
Устройство для интратимпанальной доставки
[00121] Устройство для доставки фактора роста может быть помещено между слоями барабанной перепонки. Ели средство доставки является цельным, его можно размещать, поднимая один или более слоев как лоскут, а затем заменить лоскут после размещения. Если средство является жидким, его можно ввести посредством инъекции.
[00122] На Фигуре 8 представлено устройство 128 для доставки внутри барабанной перепонки. Устройство введено в барабанную перепонку 120. Устройство имеет ширину 133 и длину 143.
Пример 5
[00123] Размещение средства доставки в виде цельного объекта смежно с барабанной перепонкой (Фигура 9). Средство доставки можно размещать вплотную к барабанной перепонке и обеспечивать местный источник HB-EGF или ингибитора HB-EGF. Средство доставки можно размещать медиально или латерально, частично или полностью через барабанную перепонку. Часть, проходящая через барабанную перепонку, может быть меньше, больше или соответствовать по размеру перфорации, при ее наличии.
[00124] На фигуре 9 изображено устройство 128 для доставки фактора роста, размещенное смежно с барабанной перепонкой 120. Устройство имеет ширину 134 и длину 144.
Пример 6
[00125] Способ применения фактора роста с использованием инъекции показан на Фигуре 10. Композицию, содержащую фактор роста 200, можно доставить в ушной канал 100 для создания контакта с барабанной перепонкой 120 на ее латеральной и/или медиальной поверхности, и она может дальше протекать в область перфорации 121 барабанной перепонки. Композицию можно распределять из шприца 210 через трубку 220 для доставки. Композиция может быть предоставлена в виде одного раствора или в виде двух растворов, которые смешиваются в момент доставки.
[00126] Двукамерные шприцы известны в данной области техники и легко доступны, например, смотри среди прочего: Lyo-Ject® дву-камерный шприц; или любой из описаных в патенте США №5971953; заявке на патент США US 20030040701; US 20140012196; US 20130060232; международной заявке WO 1999017820 A1; и т.д.
[00127] Такие композиции включают композиции, которые, при смешивании изменяют состояние на более вязкое или твердое. Агенты, увеличивающие вязкость, включают, не ограничиваясь перечисленным, геллан, N-изопропилакриламид с акрилатом натрия и н-N-алкилакриламидом, полиакриловую кислоту с полиэтиленгликолем, полиметакриловую кислоту с полиэтиленгликолем, CARBOPOL® с гидроксипропилметилцеллюлозой, латекс из ацетата гидрофталата целлюлозы, альгинат натрия или обратный термоотверждаемый гель, такой как полоксамер или полоксамин.
[00128] Такие композиции могут быть доставлены к внешней, эпидермальной поверхности барабанной перепонки в состоянии, подобном жидкому т.е. в текучей форме. Однако после введения композиция принимает твердое состояние, так что композиция остается в контакте с барабанной перепонкой. В результате композиция остается локализованной вплотную к барабанной перепонке, и фармакологический агент может передаваться на барабанную перепонку. Вязкая или твердая композиция может быть биоразлагаемой или бионеразлагаемой.
Реферат
Группа изобретений относится к медицине и может быть использована для улучшения заживления хронической перфорации барабанной перепонки у индивидуума. Для этого обеспечивают контактирование места хронической перфорации барабанной перепонки с композицией, содержащей эффективную дозу агента, обеспечивающего активность гепаринсвязывающего эпидермального фактора роста (HB-EGF), который представляет собой HB-EGF человека. При этом контактирование композиции происходит в течение периода времени, достаточного для существенного закрытия перфорации. Также предложены фармацевтическая композиция и применение композиции при производстве лекарственного средства для лечения хронической перфорации барабанной перепонки. Группа изобретений обеспечивает эффективное лечения хронической перфорации барабанной перепонки без проведения тимпанопластики. 3 н. и 14 з.п. ф-лы, 10 ил., 1 табл., 6 пр.

Комментарии