Применение по меньшей мере одного пептида в косметической композиции или для получения лекарственного средства - RU2180590C2
Код документа: RU2180590C2
Чертежи

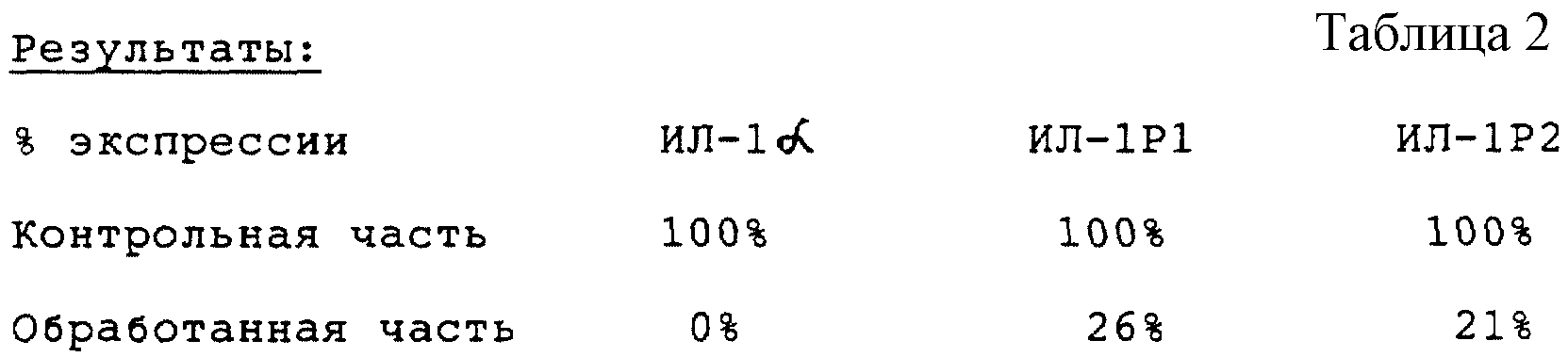

Описание
Настоящее изобретение относится к применению в качестве активного агента, в физиологически приемлемой среде, в косметической композиции или для получения лекарственного средства, эффективного количества по меньшей мере одного пептида, содержащего трипептид Лиз-Про-Вал, или его любого функционального биологического эквивалента, в котором остаток пролина присутствует в форме своего правовращающего оптического изомера, предназначенного для лечения воспаления.
Воспаление представляет собой совокупность биологических реакций, которые встречаются во всем животном мире. У человека два заболевания из трех имеют признаки воспаления. Воспаление может быть локализовано.
Оно может проявляться как первичный ответ на любое локальное воздействие рядом неспецифических пусковых реакций независимо, чем оно вызвано, и развивается в три периода: сосудистый, клеточно-сосудистый и тканевого фиброза.
Припухлость, боль, краснота, жжение являются проявлениями локализованного воспаления. Обычно они возникают вследствие инфильтрации поврежденных тканей, отека и/или расширения капиллярных сосудов.
Симптомы воспаления могут доходить до жара, общего недомогания и/или увеличения концентрации некоторых протеинов в плазме крови.
Это явление, которое среди прочего вовлекает ряд местных клеточных реакций и выделение цитокинов и других метиаторов, таких как вещество Р, простагландины, гистамин или альтернативно серотонин.
Оно проявляется как изменение тока крови с увеличением, на уровне очага воспаления, сосудистой проницаемости, приводящей к просачиванию плазматических протеинов и клеток во внеклеточную жидкость, а также к экстравазации лейкоцитов, главным образом, нейтрофильных лейкоцитов и макрофагов к очагу воспаления.
На самом деле эти явления являются результатом действия медиаторов воспаления.
Среди факторов, вовлекаемых в эти воспалительные явления, можно назвать цитокины, в особенности интерлейкин-1-α, интер-лейкин-1-β, интерлейкин 6, факторы некроза опухоли α и β (TNF-α и -β), хемокины, как, например, интерлейкин 8 или хемотаксический и активирующий фактор моноцитов (MCAF), или еще другие хемотаксические факторы, ответственные за пополнение лимфоцитарных клеток, моноцитарных клеток, клеток Лангерганса или базофилов в месте воспаления или еще другие факторы, вовлекаемые в воспалительный каскад, такие как арахидоновая кислота, или простагландины, в особенности простагландины Е2.
Воспаление связано с многочисленными патологиями. В качестве примера можно назвать солнечную эритему, зуд, узловатую эритему, крапивницу, системный мастоцитоз, псориаз, укусы насекомых, другие дерматологические заболевания, такие как атрофирующий полихондрит, эритермия, липоидный некробиоз. Можно также назвать диссеминированную эритематозную волчанку, спондилоартропатии или суставные заболевания типа хронических энтеропатий.
В течение многих лет в фармацевтической промышленности ищут вещества, позволяющие лечить воспаления.
В этом отношении недавно было предложено использовать достаточное количество производного меланоцитстимулирующего гормона α типа (α-MSH), или Меланотропина, и в особенности пептида, содержащего трипептид Лиз-Про-Вал (американские патенты 5028592 и 5157023).
Однако было показано, что оптическая форма изомеров, использованных в композиции трипептида, имеет большое значение. Так, было показано, что когда остаток пролина присутствует в трипептиде в форме своего правовращающего оптического изомера (D-Про), трипептид или пептид, содержащий трипептид, полностью теряет эффективность в лечении воспаления (Hiltz et al. Peptides, vol. 12, pp. 767-771, 1991).
Однако после проведенных исследований в этом направлении было обнаружено, что пептид, содержащий трипептид Лиз-Про-Вал, в котором остаток пролина присутствует в трипептиде в форме своего правовращающего оптического изомера (D-Про) или его любого функционального биологического эквивалента, активен в лечении воспаления.
Под функциональным биологическим эквивалентом подразумевают пептид, функционально эквивалентный в смысле биологической функции, в котором по меньшей мере один из аминокислотных остатков может быть заменен аминокислотным остатком, имеющим аналогичный гидропатический индекс.
Таким образом, изобретение относится к применению в косметической композиции и/или в получении лекарственного средства, предназначенного для лечения воспаления, по меньшей мере одного пептида, содержащего трипептид Лиз-Про-Вал, в котором остаток Пролина присутствует в форме своего правовращающего оптического изомера (D-Про) или его любого функционального биологического эквивалента.
В области аминокислот геометрия молекул такова, что теоретически они могут находиться в форме различных оптических изомеров. В самом деле, существует молекулярная конфигурация аминокислоты(аа), которая отклоняет плоскость поляризации света вправо (правовращающая конфигурация или D-aa) и молекулярная конфигурация аминокислоты (аа), которая отклоняет плоскость поляризации света влево (левовращающая конфигурация или L-aa).
Аминокислоты, встречающиеся в природе, имеют только левовращающую конфигурацию. Соответственно, пептид природного происхождения будет состоять только из аминокислот типа L-aa.
Лабораторный химический синтез позволяет получить аминокислоты, имеющие две возможные конфигурации. Из этого исходного продукта во время синтеза пептидов можно ввести аминокислоты в виде их как левовращающих, так и правовращающих оптических изомеров.
Таким образом, при синтезе пептидов, помимо остатка D-пролина (D-Про) можно ввести аминокислотные остатки Лизин или Валин, независимо от их вида D-лизин (D-Лиз), L-лизин (L-Лиз), D-валин (D-Вал) или L-валин (L-Вал).
Таким образом, изобретение относится, более конкретно, к применению эффективного количества указанного выше пептида, в котором остатки Лизина или Валина трипептида Лиз-(D)-Про-Вал, могут находиться в виде как правовращающих, так и левовращающих оптических изомеров.
Ниже приведены пептиды, содержащие, по меньшей мере, один из следующих трипептидов:
D-Лиз-D-Про-D-Вал
D-Лиз-D-Про-L-Вал
L-Лиз-D-Про-D-Вал
L-Лиз-D-Про-L-Вал
Предпочтительно, чтобы трипептид находился на С-конце пептида.
Предпочтительно, когда пептид настоящего изобретения представляет собой трипептид Лиз-Про-Вал, в котором остаток Пролина присутствует в форме своего правовращающего оптического изомера (D-Про).
Также предпочтительным является пептид, содержащий трипептид Лиз-Про-Вал, в котором остатки Лизина, Пролина и Валина находятся в форме правовращающих оптических изомеров (D-Лиз-D-Про-D-Вал).
Согласно изобретению может быть использовано более одного пептида. В этом случае смесь пептидов может представлять собой одну из возможных комбинаций пептидов, описанных выше.
В описании используются следующие термины. Под пролином понимают остаток пролина в форме его правовращающего изомера (D-Про), и термин "пептид" обозначает как "пептид, содержащий трипептид Лизин-Пролин-Валин или его любой функциональный биологический эквивалент", так и изолированный "трипептид Лизин-Пролин-Валин", в которых остаток Пролина находится в форме своего правовращающего оптического изомера (D-Про).
Возможно, что для придания пептиду устойчивости к разложению согласно изобретению необходимо использовать его защищенную форму. Очевидно, что защита должна быть с ним биологически совместимой. Могут быть рассмотрены многочисленные формы биологически совместимых защит, как, например, ацилирование или ацетилирование аминного конца или амидирование карбоксильного конца.
Итак, изобретение раскрывает применение пептида, в котором пептид находится в зищищенной или незащищенной форме.
Предпочтительно, согласно изобретению, используют защиту либо ацилированием или ацетилированием аминного конца, либо амидированием карбоксильного конца, либо с помощью обеих реакций.
Эффективное количество активного агента соответствует количеству, необходимому для получения желаемого результата.
Более конкретно, в косметической композиции пептид присутствует в таком количестве, что концентрация трипептида Лиз-Про-Вал составляет от 10-12 М до 10-3 М и предпочтительно от 10-9 М до 10-4 М.
Более конкретно, при получении лекарственного средства пептид присутствует в таком количестве, что трипептид Лиз-Про-Вал может быть использован в концентрации от 10-12 М до 1М и предпочтительно от 10-6 М до 10-1 М.
Количество продукта варьируется в зависимости от того, используется ли пептид, содержащий трипептид Лиз-Про-Вал, или любой его функциональный биологический эквивалент, или трипептид Лиз-Про-Вал.
Композиция согласно изобретению может быть введена парентерально, энтерально или локально. Предпочтительно композицию наносят локально.
Физиологически приемлемая среда, в которой используют пептид, согласно изобретению может быть безводной или водной. Под безводной средой понимают среду растворителя, содержащую менее 1% воды. Эта среда может состоять из растворителя или смеси растворителей, выбранных в особенности из низших спиртов, содержащих 2-4 атома углерода, например, этилового спирта, алкиленгликолей, например пропиленгликоля, и простых алкиловых эфиров алкиленгликолей или диалкиленгликолей, в которых алкильные или алкиленовые радикалы содержат 1-4 атома углерода. Под водной средой понимают среду, состоящую из воды или смеси воды и другого физиологически приемлемого растворителя, выбранного особенно среди органических растворителей, указанных выше. В последнем случае эти другие растворители, когда они присутствуют, составляют приблизительно 5-95% от массы композиции.
Возможно, что физиологически приемлемая среда может содержать другие адъюванты, обычно используемые в косметической или фармацевтической области, такие как поверхностно-активные вещества, загустители или гелеобразующие агенты, косметические добавки, консерванты, подщелачивающие или подкисляющие агенты, хорошо известные в технике, в количествах, достаточных для получения желаемого вида, особенно более или менее густого лосьона, геля, эмульсии или крема.
При необходимости средство может применяться в виде аэрозоля, находящегося под давлением, или в форме паров из флакона с насосом.
Возможно также использование в сочетании с пептидом описанных выше соединений как обладающих противовоспалительной активностью.
Можно более конкретно назвать глюкокортикоиды, витамин D и его производные и нестероидные противовоспалительные соединения.
Пептид настоящего изобретения может применяться путем наружного нанесения косметической композиции, содержащей эффективное количество по меньшей мере одного пептида, содержащего трипептид Лиз-Про-Вал, в котором остаток Пролина находится в форме своего правовращающего оптического изомера (D-Про), на участок тела, имеющий симптомы воспаления.
Итак, предметом настоящего изобретения равным образом является способ косметического лечения, в котором на кожу, волосяной покров и/или слизистые оболочки кожных зон, имеющие симптомы воспаления, наносят косметическую композицию, содержащую эффективное количество, по меньшей мере, одного пептида, содержащего трипептид Лиз-Про-Вал, в котором остаток пролина присутствует в форме своего правовращающего оптического изомера (D-Про).
Способ косметического лечения согласно изобретению может быть осуществлен, предпочтительно, нанесением косметических композиций, описанных выше, в соответствии с обычным способом использования этих композиций. Например: нанесение кремов, гелей, сывороток, лосьонов, молочка для снятия макияжа или солнцезащитных композиций на кожу или на волосяной покров, шампуней или еще нанесение зубной пасты на десны.
Далее приведены примеры, которые иллюстрируют данное изобретение, не ограничивая его объем. Содержания компонентов в композициях указаны в массовых процентах по отношению к общей массе композиции.
Пример 1: активность доза-ответ трипептида Ac-LPV-NH2* в отношении к
продуцированию интерлейкина-1α в супернатанте удаленных волос, взятых при воспалительном облысении:
Волосы удаляют у добровольцев из области макушки голов в месте воспалительного
облысения. Их помещают в среду выживания Вильямса Е (поставляемую фирмой Жибко БРЛ), содержащую пенициллин G (100 единиц/мл), стрептомицин-S (100 мкг/мл), амфотерицин (250 нг/мл), в присутствии или в
отсутствие (контроль) трипептида Ac-LPV-NH2*, синтезированного по заказу фирмы Неосистем С.А. (Страсбург) в указанных дозах. После 20 ч инкубации надосадочные слои культуры собирают в
пробирку и центрифугируют в течение 5 минут при 14000 оборотов/минут (центрифуга Eppendorf, модель 5415С). Затем супернатант переносят в чистую пробирку и хранят при температуре 4oС.
Концентрацию интерлейкина-1-α затем определяют в 100 мкл супернатанта при помощи набора ELISA Biotrak, выпущенного в продажу фирмой Амерсхам, в соответствии с инструкциями поставщика (см. табл.1).
Пример 2: Ингибирование экспрессии матричной РНК про-воспалительных и воспалительных цитокинов в ответ на трипептид Ac-LPV-NH2*.
Десять удаленных волос берут у добровольцев из области макушки головы в месте воспалительного облысения. Их помещают в среду выживания Вильямса Е (продаваемую фирмой Жибко БРЛ), содержащую пенициллин G (100 единиц/мл), стрептомицин-s (100 мкг/мл), амфотерицин (250 нг/мл), в присутствии (обработанная часть) или в отсутствие (контрольная часть) трипептида Ac-LPV-NH2*, синтезированного по заказу фирмой Неосистем С.А. (Страсбург).
После 3 часов 30 минут инкубации матричные РНК, соответствующие этим двум частям, очищают при помощи набора "quick prep mRNA purification Kit" (набор для очистки мРНК быстрого приготовления), поставляемого в продажу фирмой Фармасиа. ДНК, комплементарные этим мРНК, получают затем при помощи набора для обратной транскрипции, поставляемого в продажу фирмой Фармасиа, следуя инструкциям поставщика, после чего подвергают их полимеразной цепной реакции (ПЦР) с использованием праймеров, специфических для мРНК глицеральдегид-3-фосфатдегидрогеназы (ГАФДГ), ИЛ-1α, рецептора ИЛ-1 типа 1 и рецептора ИЛ-1 типа 2. Количество амплифицированной ДНК оценивают затем путем электрофореза в 1.5% агарозном геле в присутствии этидий-бромида. Интенсивность полос определяют при облучении ультрафиолетовым светом при помощи видеокамеры и аналитического программного обеспечения (Bioprofil TM), поставляемых в продажу фирмой Вильберт-Лурмат. Интенсивность полос, полученных с праймерами ИЛ-1α, ИЛ-1Р1, ИЛ-1Р2, делят на интенсивность полос, полученных с праймерами, амплифицирующими внутренний стандарт ГАФДГ (см. табл.2).
Пример 3: Ингибирующее действие Ac-LPV-NH2* на экспрессию мРНК ИЛ-1α, вычисленное через отношение ИЛ-1α/ГАФДГ
У двух разных доноров удаляют по 5 волос и
затем инкубируют их в течение 20 часов при 37oС (5% СО2) в среде Е Вильямса, в которую добавлены антибиотики и глютамин, в присутствии Ac-LPV-NH2* в указанных
концентрациях. Осуществляют контроль, при котором добавленный пептид отсутствует. Результаты выражены в % по отношению к контролю (см. табл.3).
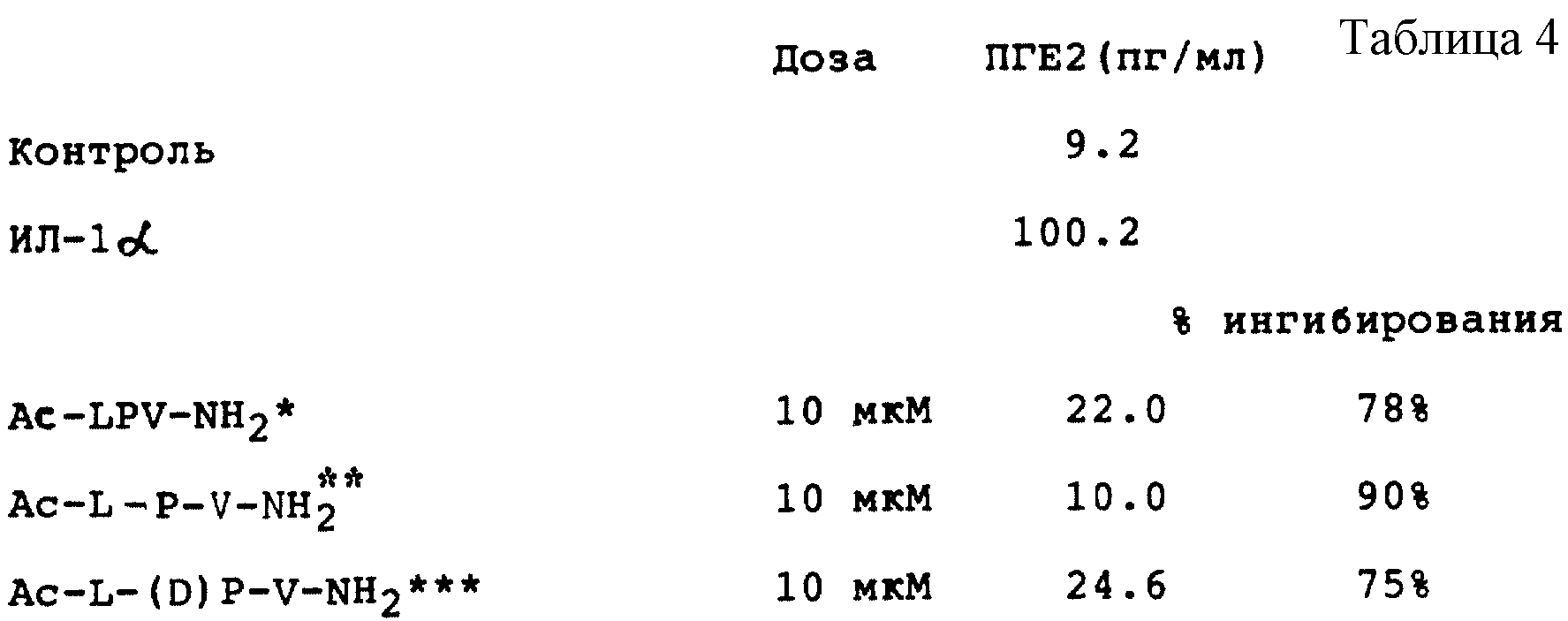
Пример 4: Измерение ингибирования
продуцирования ПГЕ2 (простагландина Е2) папиллярными катагенными клетками, культивируемыми in vitro:
Клетки (1000 на лунку) на 24 пересеве инкубируют в среде 199, поставляемой в продажу
фирмой ЖИБКО в присутствии околоплодной телячьей сыворотки и антибиотиков. 20 часов спустя среду заменяют идентичной средой, содержащей трипептиды, которые определяют в конечной концентрации 10 мкМ.
Через пять часов добавляют интерлейкин-1α в конечной концентрации 10 нг/мл. Спустя 20 часов уровни содержания ПГЕ2, продуцированных культивируемыми папиллярными клетками, оценивают при помощи
набора Biotrak, поставляемого в продажу фирмой Амерсхам, следуя инструкциям поставщика. Этот метод позволяет таким образом оценить ингибирующий эффект этих трипептидов на продуцирование ПГЕ2,
индуцированное про-воспалительным цитокином: интерлейкином-1α (см. табл.4).
Из этих результатов видно, что трипептиды, содержащие либо форму (D)-Пpo, либо форму (L)-Pro, встречающегося в природе, обладают сравнительной противовоспалительной активностью.
Пример 5: Примеры композиций, содержащих трипептид Ac-LPV-NH2*.
Эти композиции получены известными способами, в частности, простым смешиванием ингредиентов.
Композиция 1: Аэрозоль, 2:
Ac-LPV-NH2* - 5•10-6
Миноксидил - 0,5 г
Этанол 95o - 55,1
Пропиленгликоль - 22,8
Отдушка - достаточное количество.
Вода деминерализованная - достаточное количество до 100.
Композиция 2: Лосьон для ежедневного употребления, г:
Ac-LPV-NH2* - 12,5-10-6
2,4-диаминопиримидин-3-оксид - 0,75
Этанол 95o - 30
Отдушка - достаточное количество.
Красители - достаточное количество.
Вода деминерализованная - достаточное количество до 100
Композиция
3: Липосомный гель, г:
Natipide II(либо 2 г фосфолипидов) - 10
Ac-LPV-NH2* - 5•10-5
Карбомер - 0,25
Триэтаноламин - достаточное
количество рН 7.
Консерванты - достаточное количество.
Вода деминерализованная - достаточное количество до 100.
(Natipide II - Смесь вода/спирт/лецитин
фирмы Наттерманн)
Композиция 4: Ниосомный гель, г:
Chimexane NS - 1,8
Стеароилглютамат мононатрия - 0,2
Ac-LPV-NH2* - 7,5-10-4
Карбомер - 0,2
Триэтаноламин - достаточное количество рН=7.
Консерванты - достаточное количество.
Отдушки - достаточное количество.
Вода деминерализованная - достаточное количество до 100.
(Chimexane NS - Неионное поверхностно-активное вещество, поставляемое фирмой Шимекс)
Композиция 5: Ниосомный лосьон, г:
Chimexane NL - 0,475
Холестерин - 0,475
Стеароилглютамат мононатрия - 0,05
Ac-LPV-NH2* - 10-3
Консерванты - достаточное количество.
Красители - достаточное количество.
Отдушка - достаточное количество.
Вода деминерализованная - достаточное количество до 100.
(Chimexane
NL - Неионное поверхностно-активное вещество, поставляемое фирмой Шимекс)
Композиция 6: Крем для ухода: эмульсия М/В, г:
Цетилстеариловый спирт/оксиэтиленированный цетилстеариловый
спирт, содержащий 33 моля окиси этилена (80/20) - 5
Моностеарат глицерина - 1,5
Цетиловый спирт - 0,75
Вазелиновое масло - 10
Полидиметилсилоксан - 0,75
Глицерин - 4
Консерванты - Достаточное количество.
Ac-LPV-NH2* - 5•10-3
Вода деминерализованная - достаточное количеcтво до 100.
Композиция 7: Раствор для подкожной инъекции:
Ac-LPV-NH2* - 0,7 мг
Физиологический раствор (NaCl 9г/Н2О достаточное количество до 100 мл)- достаточное
количество до 1 мл.
*: Ацетил-(D)Лиз-(D)Про-(D)Baл-NH2
**: Ацетил-(L)Лиз-(L)Про-(D)Baл-NH2
***: Ацетил-(L)Лиз-(D)Про-(L)Вал-NН2:
Реферат
Изобретение относится к медицине и к применению по меньшей мере одного пептида, содержащего на С-конце трипептид Лизин-Пролин-Валин, в котором остаток Пролина находится в форме правовращающего оптического изомера для местного лечения воспаления. Изобретение позволяет повысить эффективность лечения воспаления. 2 с. и 6 з.п. ф-лы, 4 табл.

Комментарии