Эндопротез ортотопического искусственного мочевого пузыря - RU2667196C1
Код документа: RU2667196C1
Чертежи

Описание
Задача настоящего изобретения заключается в создании эндопротеза ортотопического искусственного мочевого пузыря.
Применение настоящего изобретения связано с заменой мочевого пузыря пациента, если последний страдает серьезными неизлечимыми заболеваниями, нарушающими нормальное функционирование мочевого пузыря.
Известные эндопротезы мочевого пузыря содержат баллонную оболочку, выполненную из многослойной силиконовой мембраны.
Такой баллон является достаточно жестким, чтобы устойчиво сохранять свою форму, и гибким, чтобы его можно было сжать вручную для обеспечения опорожнения.
Оболочка имеет соединительный элемент, расположенный на нижнем участке оболочки, для соединения с уретрой пациента. Аналогичным образом два соединительных тела расположены сверху, чтобы обеспечить соединение с мочеточниками.
Такие соединения достигаются путем сшивания или просто взаимным сцеплением.
Некоторые примеры можно найти в документах WO 2007/095193, WO 2011/064110 и WO 2011/018300.
К сожалению, известные эндопротезы мочевого пузыря имеют ряд недостатков.
В действительности эндопротезы известного типа имеют форму, которая не вполне естественна, что часто приводит к проблемам с потоком мочи, поступающей в них и/или выходящей из них.
Реальность такова, что в процессе изгнания мочи на фазе мочеиспускания часть ее может поступать обратно в мочеточники, а оттуда в направлении почек.
Разумеется, данное явление вовсе нежелательно, поскольку может привести к повреждению или инфицированию почек.
В этой связи техническая задача, лежащая в основе настоящего изобретения, заключается в том, чтобы предложить эндопротез ортотопического искусственного мочевого пузыря, преодолевающий недостатки вышеуказанного предшествующего уровня техники.
В частности, задача настоящего изобретения заключается в создании эндопротеза ортотопического искусственного мочевого пузыря, обеспечивающего его более естественное функционирование, а значит, предотвращающего возможное повреждение и/или инфицирование почек.
Указанная задача по существу решается посредством эндопротеза ортотопического искусственного мочевого пузыря, имеющего технические характеристики, изложенные в одном или нескольких пунктах приложенной формулы изобретения.
Дополнительные характеристики и преимущества настоящего изобретения станут более понятными из неограничивающего приведенного в качестве примера описания предпочтительного, но не эксклюзивного варианта осуществления эндопротеза ортотопического искусственного мочевого пузыря, представленного на сопроводительных чертежах:
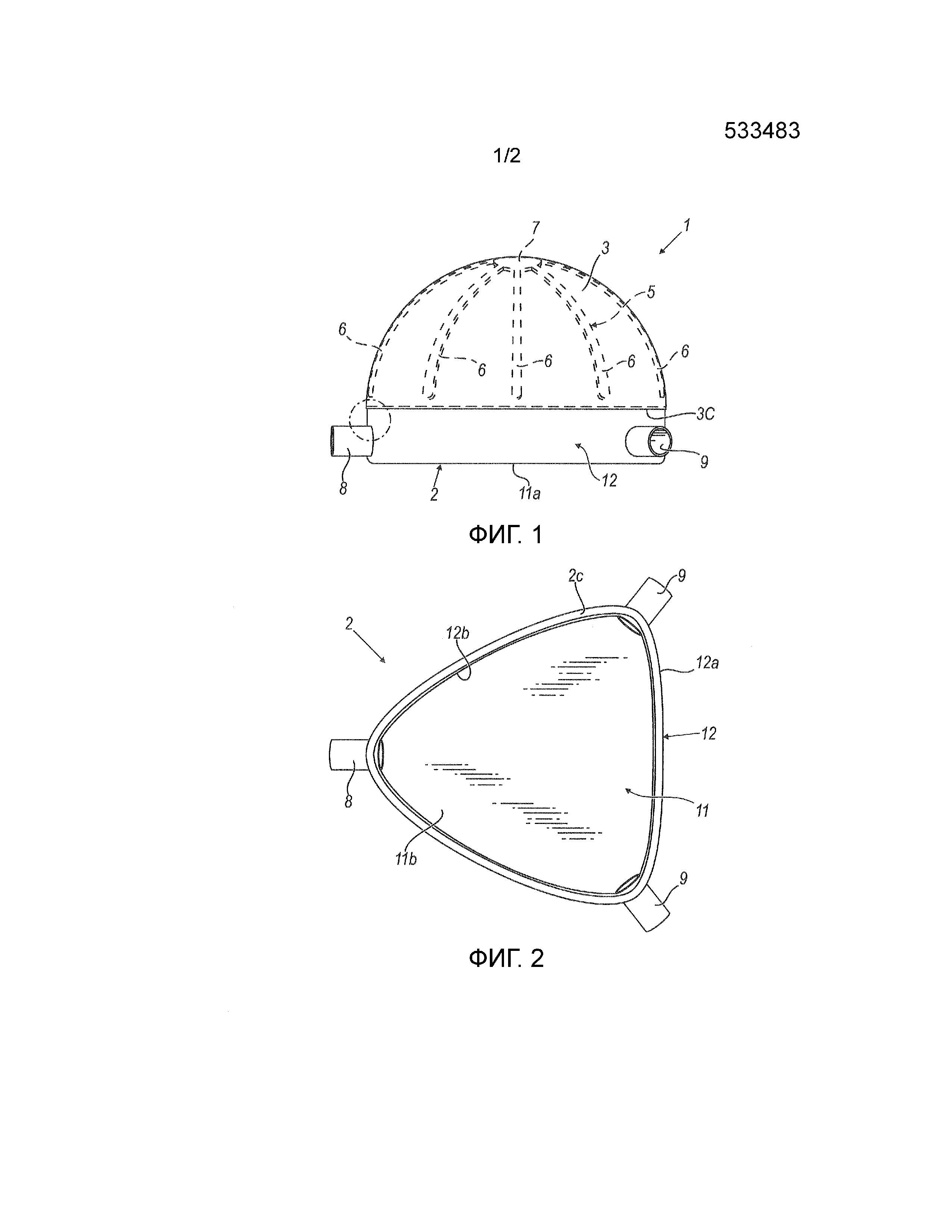
- Фигура 1 – вид сбоку, частично в разрезе, эндопротеза ортотопического искусственного мочевого пузыря согласно настоящему изобретению;
- Фигура 2 – вид сверху компонента эндопротеза, представленного на Фигуре 1;
- Фигура 3 – вид в перспективе компонента, проиллюстрированного на Фигуре 2;
- Фигура 4 – увеличенный вид в разрезе увеличенной детали, представленной на Фигуре 1.
На сопроводительных Фигурах ссылочная позиция 1 в целом обозначает эндопротез ортотопического искусственного мочевого пузыря согласно настоящему изобретению.
Эндопротез 1 содержит вогнутое основание 2 и вогнутый колпак 3, соединенные вместе вдоль соответствующих краев 2c, 3c. В частности, основание 2 и колпак 3 расположены так, что соответствующие впадины обращены друг к другу. Таким образом, между основанием 2 и колпаком 3 образовано замкнутое пространство 4 для содержания мочи пациента. Замкнутое пространство имеет объем по существу от 100 см3 до 900 см3, предпочтительно 400 см3.
Основание 2 содержит плоскую панель 11 и стенку 12, продолжающуюся от внешней границы плоской панели 11 ортогонально ей.
Основание 2 имеет наружную поверхность и внутреннюю поверхность и создано с помощью многослойной силиконовой мембраны.
Наружная и внутренняя поверхности основания 2 соответственно образованы наружной поверхностью 11a и внутренней поверхностью 11b плоской панели 11, а также наружной поверхностью 12a и внутренней поверхностью 12b стенки 12.
Мембрана основания 2 имеет толщину от 500 мкм до 700 мкм; предпочтительно толщина мембраны составляет по существу 600 мкм.
В предпочтительном варианте осуществления мембрана содержит по существу 20 слоев, при этом толщина каждого составляет около 30 мкм.
Таким образом, основание 2 имеет достаточную жесткость для сохранения своей формы, при этом одновременно оно является достаточно гибким, так что оно может сдавливаться снаружи, чтобы способствовать изгнанию мочи.
Мембрана изготавливается посредством способа, проиллюстрированного в патентной заявке WO 2007/039159, включенной в настоящее описание в качестве ссылочного материала.
В качестве примера используемый силикон может быть образован сополимерами диметил- и метилвинилсилоксана, армированными оксидом кремния.
Предпочтительно к силикону могут быть подмешены рентгеноконтрастные вещества, такие как сульфат бария, диоксид титана и т.п., так чтобы эндопротез 1 можно было распознать с использованием технологий рентгенодиагностики.
Как на наружной поверхности, так и на внутренней поверхности основания 2 наложены соответствующие слои, выполненные из защитного материала, обладающего высокой биосовместимостью. В качестве примера такой материал представляет собой пиролитический турбостратный углерод толщиной от 0,2 мкм до 0,3 мкм.
Наложение углеродного слоя на наружную поверхность основания 2 позволяет исключить риск того, что образующаяся фиброзная капсула может прилипнуть к основанию 2. Наложение углеродного слоя на внутреннюю поверхность основания 2 позволяет защитить основание 2 от коррозии, вызванной мочой.
Колпак 3 имеет наружную поверхность 3a и внутреннюю поверхность 3b и выполнен из полотна, полученного с применением сверхлегкого филамента или нити, извлеченной из PGA волокон (полигликолида или полигликольной кислоты), предпочтительно гомополимера. PGA представляет собой обладающий высокой биосовместимостью рассасывающийся полимер, устойчивый к действию мочи. Если говорить конкретнее, время рассасывания PGA составляет приблизительно один месяц.
Предпочтительно использование PGA волокон при получении полотна позволяет сформировать мышечно-фиброзную ткань за пределами эндопротеза 1. Внутри в процессе рассасывание образуется слой переходного эпителия, который также именуется уротелием. Предпочтительно слой уротелия обладает непроницаемостью, что является важнейшим условием для обеспечения надлежащего функционирования протеза и образующегося артифициального мочевого пузыря.
Полотно может быть получено переплетением PGA нити различными способами, приводя к созданию вязаного полотна, тканого полотна или нетканого полотна.
Предпочтительно полотно представляет собой вязаное полотно, еще более предпочтительно – полотно основовязаного типа.
В данном случае полотно имеет более грубую поверхность, способную принять форму сетки, имеющей достаточно малые ячейки.
Если говорить подробнее, его уточные нити таковы, что промежуточное пространство в них составляет менее 200 мкм, предпочтительно около 160 мкм, что соответствует средней площади отверстий, равной приблизительно 0,02 мм2. Это обеспечивает непроницаемость для мочи, не допуская протечек.
Кроме того, полотно предпочтительно текстурировано так, чтобы сделать его поверхность еще более грубой, а также придать более высокую жесткость и непроницаемость. Повышенная шероховатость полотна ограничивает риск прилипания фиброзной капсулы.
Предпочтительно эндопротез дополнительно содержит каркас 5, наложенный на колпак 3, чтобы придать ему необходимые механические и конструкционные характеристики. Точнее говоря, каркас 5 установлен на внутренней поверхности 3b колпака 3.
Каркас 5 содержит множество ветвей 6, расположенных в виде звезды и образующих куполообразный профиль. Если говорить подробнее, все ветви 6 имеют криволинейную форму и жестко скреплены между собой на соединительном участке 7, расположенном в верхней части колпака 3. Предпочтительно каркас 5 крепится к полотну колпака 3 посредством рассасывающихся шовных материалов.
Обычно толщина каркаса 5 или ветвей 6 и соединительного участка 7 составляет от 0,1 мм до 10 мм, предпочтительно от 0,5 мм до 2 мм. В предпочтительном варианте осуществления эта толщина составляет по существу 1 мм.
Каркас 5 получают путем инжектирования сополимера молочной кислоты и гликолевой кислоты, обозначаемых PGA/PLA (поли(молочная-ко-гликолевая) кислота), куполообразная форма которой придается в горячем состоянии посредством термоформования.
Поскольку молекулы молочной кислоты обладают свойством хиральности, существуют различные типы полимеров, PDLA, PLLA, PDLLA, где D и L представляют два стереоизомера. PLLA обладает упорядоченностью структуры 37%, переходной температурой стеклования от 50°C до 80°C и температурой плавления от 173°C до 178°C, в то время как полимер, полученный путем полимеризации рацемической смеси, PDLLA, является аморфным.
Термин «поли(молочная) кислота» в настоящем описании обозначает все вышеуказанные типы PLA.
PGA/PLA сополимер, из которого выполнен каркас 9, образован PGA в количестве от 20% до 30% и PLA соответственно в количестве от 70% до 80%.
В особенности предпочтительным PGA/PLA (поли(молочная-ко-гликолевая) кислота) сополимером является сополимер (поли(L-молочной-ко-гликолевой) кислоты) (PLLA/PGA), в котором молярный процент L-молочной кислоты составляет 82-88%, а молярный процент гликолевой кислоты составляет 18-12%. Данный сополимер известен под фирменным наименованием Resomer® LG855S.
Следует отметить, что колпак 3, полученный из вышеописанного PGТ-полотна, в частности текстурированного, в сочетании с PGA/PLA каркасом 5 демонстрирует высокое постоянство механических свойств и достаточную жесткость даже в присутствии мочи, а значит, способен обеспечивать надлежащее деформирование мочевого пузыря в процессе его опорожнения и/или заполнения, одновременно демонстрируя высокое сопротивление утечке мочи.
Кроме того, колпак 3 и каркас 5 доказали свою нейтральность, пребывая в контакте с растущей «артифициальной тканью». Это предполагает быстрое заполнение устройства клетками окружающей растущей ткани. В то же время подтверждено, что адгезия носит ограниченный характер вследствие ограниченного взаимодействия между полимерами, входящими в состав колпака 3 и каркаса 5, и биологическими молекулами, что обеспечивает слияние с внутренними тканями организма пациента.
Следовательно, основание 2 является постоянным во времени, в то время как колпак 3 рассасывается.
Согласно настоящему изобретению, основание 2 имеет по существу треугольную форму на виде сверху.
Если говорить конкретнее, форма основания 2 в плане представляет собой равносторонний треугольник. Вершины предпочтительно закруглены.
В частности, плоская панель 11 основания 2 имеет форму равностороннего треугольника.
В качестве примера сторона плоской панели 11 имеет длину от 3 см до 6 см, предпочтительно от 4 см до 5 см.
Кроме того, основание 2 может соединяться как с уретрой, так и с мочеточниками пациента.
Для этой цели основание 2 содержит, по меньшей мере, один первый соединитель 8 для соединения основания 2 с уретрой, чтобы позволить выводить мочу из накопительного замкнутого пространства 4.
В частности, первый соединитель 8 неподвижно закреплен на стенке 12 основания 2.
Аналогичным образом основание 2 содержит, по меньшей мере, два вторых соединителя 9 для соединения основания 2 с мочеточниками, чтобы позволить поступать моче в накопительное замкнутое пространство 4.
В частности, вторые соединители 9 неподвижно закреплены на стенке 12 основания 2.
Лишь в качестве примера первый соединитель 8 и/или вторые соединители 9 могут содержать соответствующие рукава, закрепленные на стенке 12 основания 2 в соответствующих отверстиях.
В качестве примера рукава первого соединителя 8 и/или вторых соединителей 9 могут быть получены с помощью многослойной силиконовой мембраны с покрытием из пиролитического турбостратного углерода.
Предпочтительно вторые соединители 9 эквидистантны относительно первого соединителя 8.
Предпочтительно расстояние между первым соединителем 8 и вторыми соединителями 9 равно расстоянию между вторыми соединителями 9.
В качестве примера такое расстояние составляет от 3 см до 6 см, предпочтительно от 4 см до 5 см.
Как указано выше, основание 2 и колпак 3 соединены на соответствующих своих краях 2c, 3c.
Для этой цели основание 2 содержит ленту 10, встроенную в стенку 12 вблизи края 2c самого основания 2.
В частности, лента 10 продолжается вдоль всего края 2c основания 2. Если говорить конкретнее, лента 10 продолжается вдоль всей стенки 12 основания 2.
Лента 10 выполнена из биосовместимого и предпочтительно нерассасывающегося материала.
Лента 10 крепится к колпаку 3 на краю 3c. В частности, лента 10 крепится вдоль всего края 3c колпака 3.
Предпочтительно лента 10 крепится к колпаку 3 посредством сшивания с использованием рассасывающейся нити. В качестве примера такая нить может быть образована из PGA.
В предпочтительном варианте осуществления лента 10 образована полотном, выполненным из полиэтилентерефталата (с использованием, например, изделия, известного под фирменным наименованием Dacron®) и/или волокон Goretex®, либо полотном, образованным политетрафторэтиленовыми мембранами. Согласно иллюстрации (на Фигуре 4) лента 10 “встроена” в мембрану, образующую основание 2. Иными словами, лента 10 содержится между двумя смежными силиконовыми слоями мембраны. В частности, лента 10 установлена между двумя слоями, расположенными вблизи наружной поверхности основания 2.
Высота ленты 10 по существу равна 0,5 см.
Описанное изобретение решает поставленную задачу.
Разумеется, форма основания и тот факт, что оно соединено как с уретрой, так и с мочеточниками пациента, придают эндопротезу более естественную конфигурацию, близкую к конфигурации мочевого пузыря человека.
Это позволяет создать более физиологичные потоки мочи и, в частности, не допускает нарушений поступления и выведения мочи из самого эндопротеза.
Следовательно, возврат мочи к почкам не допускается, что ограничивает или полностью исключает причинение возможных сопутствующих повреждений.
Реферат
Изобретение относится к медицинской технике, а именно к эндопротезам мочевого пузыря. Эндопротез ортотопического искусственного мочевого пузыря содержит основание и рассасывающийся колпак. Основание имеет многослойную силиконовую мембрану, имеющую наружную поверхность и внутреннюю поверхность, каждая из которых имеет покрытие из пиролитического турбостратного углерода. Рассасывающийся колпак имеет PGA волокнистое полотно. Основание и колпак соединены между собой вдоль соответствующих краев с образованием закрытого пространства. Основание может соединяться с уретрой и мочеточниками пациента. Основание имеет по существу треугольную форму. Изобретение позволяет избежать прилипания фиброзной капсулы к протезу и внутренней коррозии протеза, а также обеспечивает более естественное функционирование протеза, а значит, предотвращает возможное повреждение и/или инфицирование почек. 9 з.п. ф-лы, 4 ил.
Формула
Документы, цитированные в отчёте о поиске
Ортотопический искусственный протез мочевого пузыря

Комментарии