Вирусные векторы и их применение в генной терапии - RU2233333C2
Код документа: RU2233333C2
Чертежи

Описание
Настоящее изобретение относится к новым вирусным векторам, их получению и их применению в генной терапии. Оно также относится к фармацевтическим композициям, содержащим вышеуказанные вирусные векторы. Более предпочтительно, настоящее изобретение относится к применению рекомбинантных аденовирусов животного происхождения как векторов для генной терапии.
Генная терапия заключается в исправлении дефекта или анормальности (мутация, ошибочная экспрессия и т.д.) путем введения генетической информации в клетку или пораженный орган. Эта генетическая информация может быть введена либо ин витро в извлеченную из органа клетку, причем модифицированную клетку затем снова возвращают в организм, либо прямо ин виво в соответствующую ткань. В этом втором случае существуют различные способы, среди которых различные способы трансфекции, где принимают участие комплексы ДНК (дезоксирибонуклеиновой кислоты) и диэтиламиноэтилдекстрана (Раgаnро и др., Ф.Virol I (1967), 891), ДНК и ядерных протеинов (белков) [Kaned а и до., Scienсе, 243 (1989) 375/, ДНК и липидов (РеIgner и др., PNAS 84 (1987) 7413); применение липосов (Frai eу и др. J.Biol Chem, 255 (1980) 10431) и т.д. Совсем недавно появилось использование вирусов как векторов для переноса генов как многообещающая альтернатива этим физическим способам трансфекции. В этом отношении были испытаны различные вирусы на их способность инфицировать некоторые клеточные популяции. В частности, ретровирусы (RSV, HMS, MMS и т.д.), вирус герпеса человека, адено-ассоциированные вирусы и аденовирусы.
Среди этих вирусов аденовирусы обладают некоторыми представляющими интерес свойствами для применения а генной терапии. Особенно они имеют довольно широкий спектр хозяев, способны инфицировать находящиеся в покое ("спокойные") клетки и не включаются в геном инфицированной клетки. На этих основаниях аденовирусы уже используют для переноса генов ин виво. С этой целью приготовляют различные векторные производные аденовирусов, включающие различные гены (β-gal, OTC, α-IАТ, цитоксины и т.д.). Все векторные производные аденовирусов, описываемые в уровне техники с целью их использования в генной терапии человека, до настоящего времени получают из аденовирусов человеческого происхождения. В самом деле, они представляются наиболее соответствующими для такого использования. Для ограничения опасностей размножения и образования инфекционных частиц ин виво используемые аденовирусы обычно модифицируют, чтобы сделать их неспособными к репликации в инфицированной клетке. Так, конструкции, описанные в уровне техники, представляют собой аденовирусы, подвергнутые делеции на участках Е 1 (E 1 а и/или Е 1 в) и в случае необходимости Е 3, на уровне которых вставлены представляющие интерес последовательности (Levrero и др. Gene, 101 (1991) 195; Gos h-Choudhury и др. Gene, 50 (1986) 161). Однако кроме этой необходимой стадии модификации описанные в уровне техники векторы имеют другие недостатки, которые ограничивают их использование в генной терапии, и особенно опасности рекомбинации с дикими аденовирусами. Настоящее изобретение относится к предпочтительному решению этой проблемы.
Настоящее изобретение на деле заключается в использовании рекомбинантных аденовирусов животного происхождения для генной терапии человека. Настоящее изобретение демонстрирует, что аденовирусы животного происхождения способы с большой эффективностью инфицировать человеческие клетки. Изобретение также базируется на выявлении того, что аденовирусы животного происхождения неспособны размножаться в человеческих клетках, в которых они подвергаются испытанию. Наконец, изобретение базируется на открытии, что аденовирусы животного происхождения не транскомплементны к аденовирусам человеческого происхождения, что исключает всякую опасность рекомбинации и размножения ин виво в присутствии человеческого аденовируса, которая может приводить к образованию инфекционной частицы. Векторы изобретения, следовательно, особенно предпочтительны, поскольку опасности, присущие использованию вирусов как векторов в генной терапии, такие как патогенность, трансмиссия, репликация, рекомбинация, и т.д., сильно уменьшены, даже ликвидированы.
Настоящее изобретение таким образом относится к вирусным векторам, особенно адаптированным для переноса и/или экспрессии человеку желательных ДНК-последовательностей.
Первый предмет настоящего изобретения, следовательно, относится к использованию рекомбинантного аденовируса животного происхождения, содержащего гетерологическую ДНК-последовательность, для приготовления фармацевтической композиции, предназначенной для терапии и/или хирургической обработки человеческого организма.
Аденовирусы животного происхождения, используемые в рамках настоящего изобретения, могут быть разных происхождений, за исключением человеческих аденовирусов. Человеческие аденовирусы представляют собой естественно инфекционные для человека вирусы, обычно обозначаемые термином Ha d или A d.
В особенности аденовирусы животного происхождения, используемые в рамках настоящего изобретения, могут быть собачьего, бычьего, мышиного, (например, Mа v I Beard и др.,Virology, 75 (1990) 81), овечьего, свиного, птичьего или еще обезьяньего (пример: SAV) происхождения.
Более предпочтительно, из птичьих аденовирусов можно назвать серотипы 1-10, имеющиеся в распоряжении в ATCС (Американская коллекция типовых культур), как, например, штаммы PheI рs (АТСС VR - 432), Fоntes (АТСС VR - 280), Р 7-А (АТСС VR - 827), IBH - 2А (АТСС VR - 828), J2 - A (АТСС VR - 829), T8-A (АТСС VR - 830), K-II (АТСС VR - 921), или еще штаммы, обозначаемые АТСС VR – 831-835.
Из бычьих аденовирусов можно использовать различные известные серотипы, и особенно таковые, имеющиеся в распоряжении в АТСС (типы 1-8) под обoзначениями ATCС VR - 313, 314, 639-642, 768 и 769. Также можно назвать мышиные аденовирусы FL (АТСС VR - 550) и Е20308 (АТСС VR - 528); овечий аденовирус типа 5 (АТСС VR - 1343) или типа 6 (АТСС VR - 1340); свиной аденовирус 5359 или обезьяньи аденовирусы, такие, как особенно аденовирусы, обозначаемые в АТСС под номерами V R - 591-594, 941-945, 195-203 и т.д.
Предпочтительно в рамках изобретения используют аденовирусы собачьего происхождения, и особенно любые штаммы аденовирусов CAV-2 [например, штамм Manhattan или А 26/61 (АТСС VR-800)]. Собачьи аденовирусы составляют предмет многочисленных структурных исследований. Так, полные карты рестрикции аденовирусов САV-1 и CAV-2 описаны в уровне техники (Spibеу и др., J.Gen. Virol 70 (1989) 165), и гены EIa, Е3 также, как последовательности ITR, клонированы и секвенированы (см. особенно Spibeу и др., Virus Res. 14, (1989) 241; Linnе Virus Res. 23 (1992) 119; BOИC 81/11525). Кроме того, собачьи аденовирусы уже используют для приготовления вакцин, предназначенных для иммунизации собак от бешенства, парвовирусов и т.д. (ВОИС 91/11525). Однако вплоть до настоящего времени в уровне техники никогда не шло речи о возможности использования этих аденовирусов для генной терапии в случае человека. Более того, никогда не проявляли интереса к такому использованию.
Аденовирусы, используемые в рамках изобретения, предпочтительно должны быть дефектными, т.е. неспособными размножаться автономно в организме, в котором они находятся. Как указано выше, заявитель показал, что аденовирусы животного происхождения способны инфицировать человеческие клетки, но не размножаться в них. В этом смысле, следовательно, они естественно дефектны в случае человека и в противоположность использованию человеческих аденовирусов не требуют в этом отношении генетической модификации. Тем не менее, дефектный характер этих аденовирусов может быть усилен за счет генетических модификации генома, и особенно за счет модификации последовательностей, необходимых для репликации вышеуказанного вируса в клетках. Эти участки могут быть либо удалены (полностью или частично), либо сделаны нефункциональными, либо модифицированы путем вставки других последовательностей, и особенно гетерологичной ДРН последовательности.
В зависимости от происхождения аденовируса, необходимые для репликации последовательности могут немного изменяться. Однако они обычно локализованы около концов генома. Так, в случае САV-2 участок ЕIа идентифицирован, клонирован и секвенирован (Spibey и др. Virnes. Res. 14 (1989) 241). Он находится на фрагменте длиной 2 кб (килобаз) у левого конца генома аденовируса.
Кроме того, в случае этих аденовирусов могут быть осуществлены другие генетические модификации, особенно для того, чтобы избежать продуцирования нежелательных вирусных протеинов у человека, для того чтобы можно было осуществить вставку гетерологичных ДНК последовательностей значительной величины; и/или для вставки определенных участков генома другого животного или человеческого аденовируса (пример: ген Е 3).
В смысле настоящего изобретения термин "гетерологичная ДНК-последовательность" обозначает любую последовательность ДНК, вводимую в вирус, к переносу и/или экспрессии которой человеку стремятся.
В особенности гетерологичная ДНК-последовательность может включать один или несколько терапевтических генов и/или один или несколько генов, кодирующих антигенные пептиды.
В особом варианте осуществления изобретение, следовательно, более предпочтительно относится к использованию аденовирусов животного происхождения для приготовления фармацевтических композиций, предназначенных для переноса терапевтических генов человеку. Терапевтические гены, которые таким образом могут быть перенесены, представляют собой любой ген, транскрипцию, и в случае необходимости перевод которого в целевую клетку генерирует продукты, обладающие терапевтическим эффектом.
В особенности речь может идти о генах, кодирующих протеиновые продукты, которые обладают терапевтическим эффектом. Таким образом, кодированный протеиновый продукт может представлять собой протеин, пептид, аминокислоту и т.д. Этот протеиновый продукт может быть гомологичен по отношению к целевой клетке (т.е. продукт, который нормально проявляется в целевой клетке, когда она не имеет никакой патологии). В этом случае экспрессия протеина позволяет, например, улучшать (исправлять) недостаточную экспрессию в клетке, или экспрессию неактивного протеина, или слабо активного протеина вследствие модификации, или еще сверхпроявлять вышеуказанный протеин. Терапевтический ген также может кодировать мутант клеточного протеина, обладающий повышенной стабильностью, модифицированной активностью и т.д. Протеиновый продукт также может быть гетерологичен по отношению к целевой клетке. В этом случае экспрессированный протеин, например, может дополнять или вносить дефицитную активность в клетку, позволяющую ей бороться против патологии.
Из терапевтических продуктов в смысле настоящего изобретения можно преимущественно назвать ферменты, относящиеся к крови производные, гормоны, лимфокины: интерлейкины, интерфероны и т.д. (патент Франции 9203120); факторы роста, нейропередатчики и их предшественники или ферменты синтеза; трофические факторы; BDNF, CNTF, NGF, IGF, GMF, aFGF, BFGF, NT3, NТ5, и т.д.; аполипопротеины: ApoAI, АроАIV, АроЕ и т.д. (патент Франции 93 05125); дистрофин или мини-дистрофин (патент Франции 9111947); суппрессорные гены опухолей: р 53, Rb, R ар IA. ДСС - к rev и т.д. (патент Франции 9304745), гены, кодирующие участвующие в коагуляции факторы: факторы VII, VIII, IX и т.д.
Терапевтический ген также может представлять собой антисмысловой ген или антисмысловую последовательность, экспрессия которого в целевой клетке позволяет контролировать экспрессию генов или транскрипцию клеточных АR Nm. Такими последовательностями могут, например, быть транскрипты в целевой клетке в виде AR Nm, комплементарных к клеточным AR Nm, таким образом блокирующие их перевод в протеин согласно способу, описанному в европейском патента 140308.
Как указано выше, гетерологическая ДНК-последовательность также может включать один или несколько генов, кодирующих антигенный пептид, способный генерировать у человека иммунный ответ. В этом особом варианте осуществления, следовательно, изобретение позволяет осуществлять получение вакцин, позволяющих иммунизировать человека особенно против микроорганизмов или вирусов. Речь может также идти особенно о специфических антигенных пептидах вируса Эпштейн-Барра, вируса гепатита Б (европейский патент 185573), вируса псевдобешенства или еще специфических для опухолей вирусах (европейский патент 259212).
Обычно гетерологическая ДНК-последовательность включает также последовательности, позволяющие осуществлять экспрессию терапевтического гена и/или гена, кодирующего антигенный пептид в инфицированной клетке. Речь может идти о последовательностях, которые естественно ответственны за экспрессию рассматриваемого гена, когда эти последовательности способны функционировать в инфицированной клетке. Речь может также идти о последовательностях различного происхождения (ответственных за экспрессию других протеинов или даже синтетических протеинов). Особенно речь может идти о промоторных последовательностях эукариотных или вирусных генов. Например, речь может идти о промоторных последовательностях, происходящих от генома клетки, которую хотят инфицировать. Также речь может идти о промоторных последовательностях, происходящих от генома вируса, включая используемый аденовирус. В этом отношении можно назвать, например, промоторы генов EIA, ML P, СMV, RSV и т.д. Кроме того, эти последовательности экспрессии могут быть модифицированы за счет добавления последовательностей активации, регуляции и т.д. Кроме того, когда вставленный ген не содержит последовательностей экспрессии, он может быть вставлен в геном дефективного вируса ниже такой последовательности.
Кроме того, гетерологическая ДНК-последовательность также может включать в особенности вышетерапевтического гена сигнальную последовательность, направляющую синтезированный терапевтический продукт в пути секреции целевой клетки. Эта сигнальная последовательность может представлять собой природную сигнальную последовательность терапевтического продукта, но речь может идти также о любой другой функциональной сигнальной последовательности или об искусственной сигнальной последовательности.
Дефективные аденовирусы согласно изобретению могут быть получены любым известным специалисту способом. В особенности они могут быть получены согласно описанной в заявке ВОИС 91/11525 методике (протоколу). Классический способ получения базируется на гомологической рекомбинации между животным аденовирусом и плазмидой, несущей гетерологичную ДНК-последовательность, которую хотят вставить. Гомологическая рекомбинация осуществляется после котрансфекции вышеуказанных аденовирусов и плазмиды в соответствующую линию клеток. Используемая линия клеток предпочтительно должна быть трансформируема вышеуказанными элементами и в случае, где используют модифицированный аденовирус животного, это происходит, если необходимо. Линия клеток может включать последовательность, способную комплементировать часть генома дефективного аденовируса, предпочтительно в интегрированной форме, чтобы избежать опасностей рекомбинации. В качестве примера линии можно указать линию почечных клеток борзой (lеvrier) GHK (Flow laboratories) или линию клеток МДСК. Условия культивирования клеток и получение вируса или вирусной ДНК также описаны в литературе [cм. особенно Масаtnеу и др., Science, 44 (1988) 9; Fowleks и др., J.МоI, BioI. 132 (1979) 163].
Затем векторы, которые размножились, рекуперируют и очищают классическими способами молекулярной биологии.
Другой предмет настоящего изобретения составляет рекомбинантный аденовируc животного происхождения, содержащий гетерологичную ДНК-последовательность, включающую по крайней мере один терапевтический ген, такой как указанный выше.
Предметом изобретения также является любая фармацевтическая композиция, содержащая рекомбинантный аденовирус животного происхождения, такой как описанный выше. Фармацевтические композиции изобретения могут быть сформулированы для введения топическим, оральным, парентеральным, интраназальным, внутривенным, внутримышечным, подкожным, внутриглазным и т.д. путем.
Предпочтительно фармацевтическая композиция содержит фармацевтические приемлемые наполнители, пригодные для инъекции лекарственного средства. Речь может идти в особенности о стерильных, изотонических солевых растворах (мононатрий-фосфат; динатрийфосфат; хлорид натрия, калия, кальция или магния и т.д., или смеси таких солей) или о сухих, особенно лиофилизированных, композициях, которые за счет добавления, в зависимости от случая, стерилизованной воды или физиологической сыворотки позволяют получать пригодные для инъекции растворы.
Используемые для инъекции дозы вирусов могут быть адаптированы в зависимости от различных параметров и особенно в зависимости от применяемого способа введения, имеющейся патологии, экспрессируемого гена или еще от продолжительности лечения, к которому стремятся. Вообще рекомбинантные аденовирусы согласно изобретению формулируют и вводят в виде доз 104-1014 рfu/мл, и предпочтительно 106-1010 рfu/мл. Термин "рfu" ("образующая бляшку единица") соответствует инфекционной способности раствора вируса и определяется путем инфекции соответствующей клеточной культуры и подсчета, обычно спустя 5 дней, числа бляшек инфицированных клеток. Способы определения титра "pu" вирусного раствора хорошо подтверждены документальными данными в литературе.
В зависимости от вставленной гетерологической ДНК-последовательности аденовирусы изобретения могут быть использованы для лечения или профилактики многочисленных патологий, включающих генетические заболевания (дистрофия, относящийся к желчному или мочевому пузырю фиброз и т.д.), нейродегенеративные заболевания (болезнь Альтцгеймера, болезнь Паркинсона, ALS и т.д.), раковые заболевания, патологии, связанные с нарушениями коагуляции или дислипопротеинемиями, патологии, связанные с вирусными инфекциями (гепатиты, SIД А и т.д.) и т.д.
Настоящее изобретение более полно описывается с помощью нижеследующих примеров, которые нужно рассматривать в качестве иллюстративных и не ограничивающих объема охраны изобретения.
Подписи под чертежами
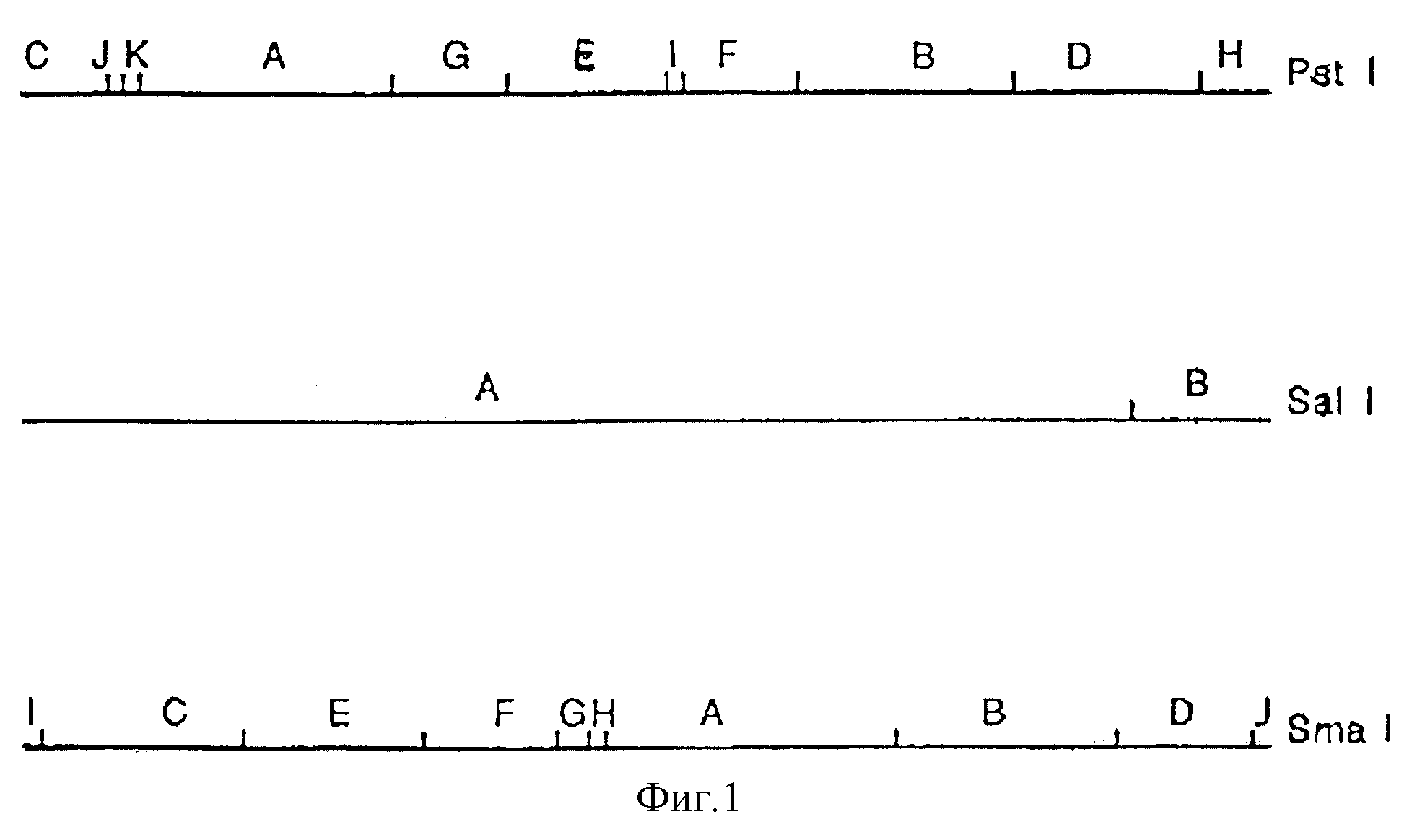
Фиг.1 - карта рестрикции аденовируса CAV-2 штамма Manhattan (согласно Spibey и др., цитировано выше);
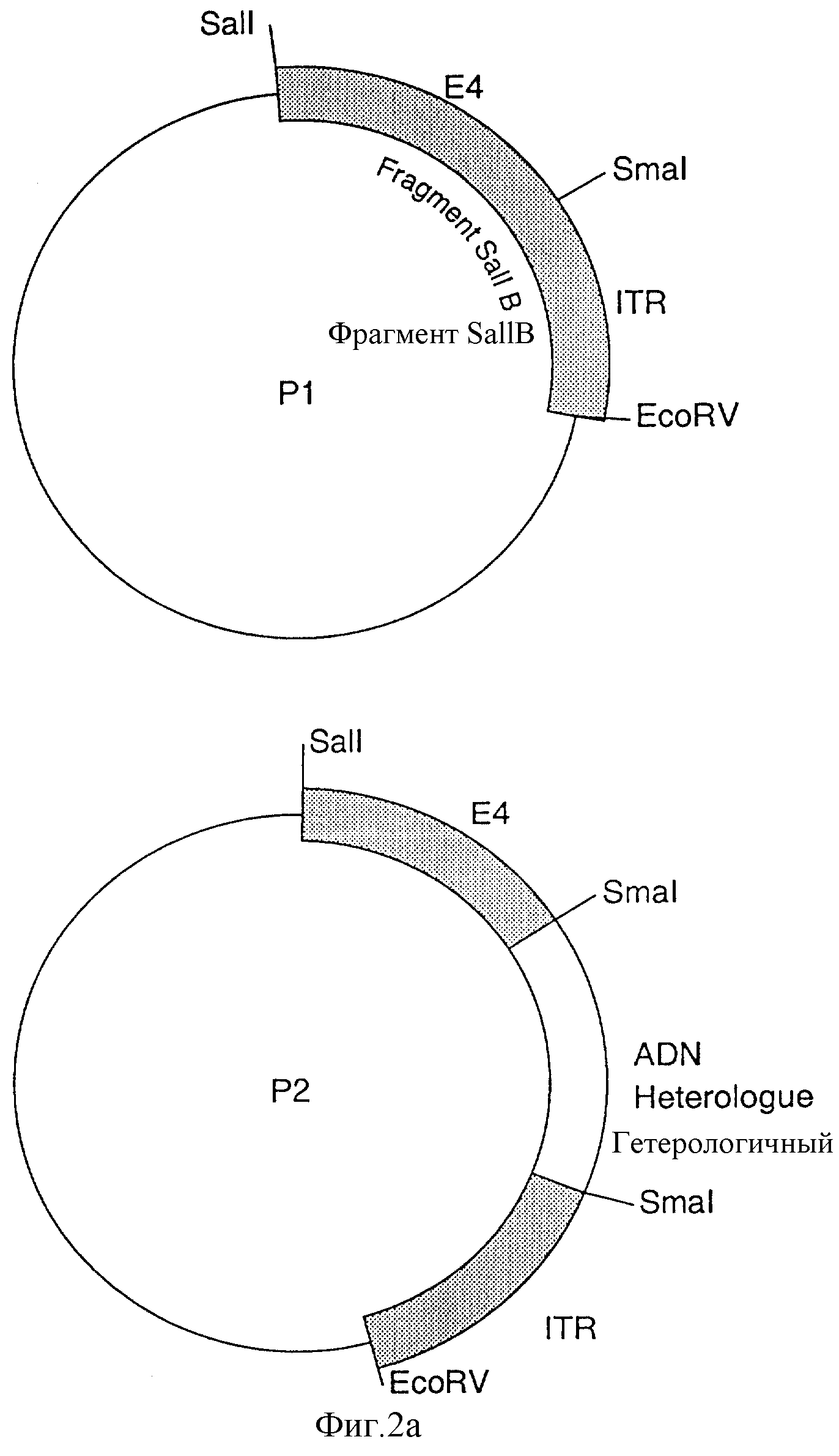
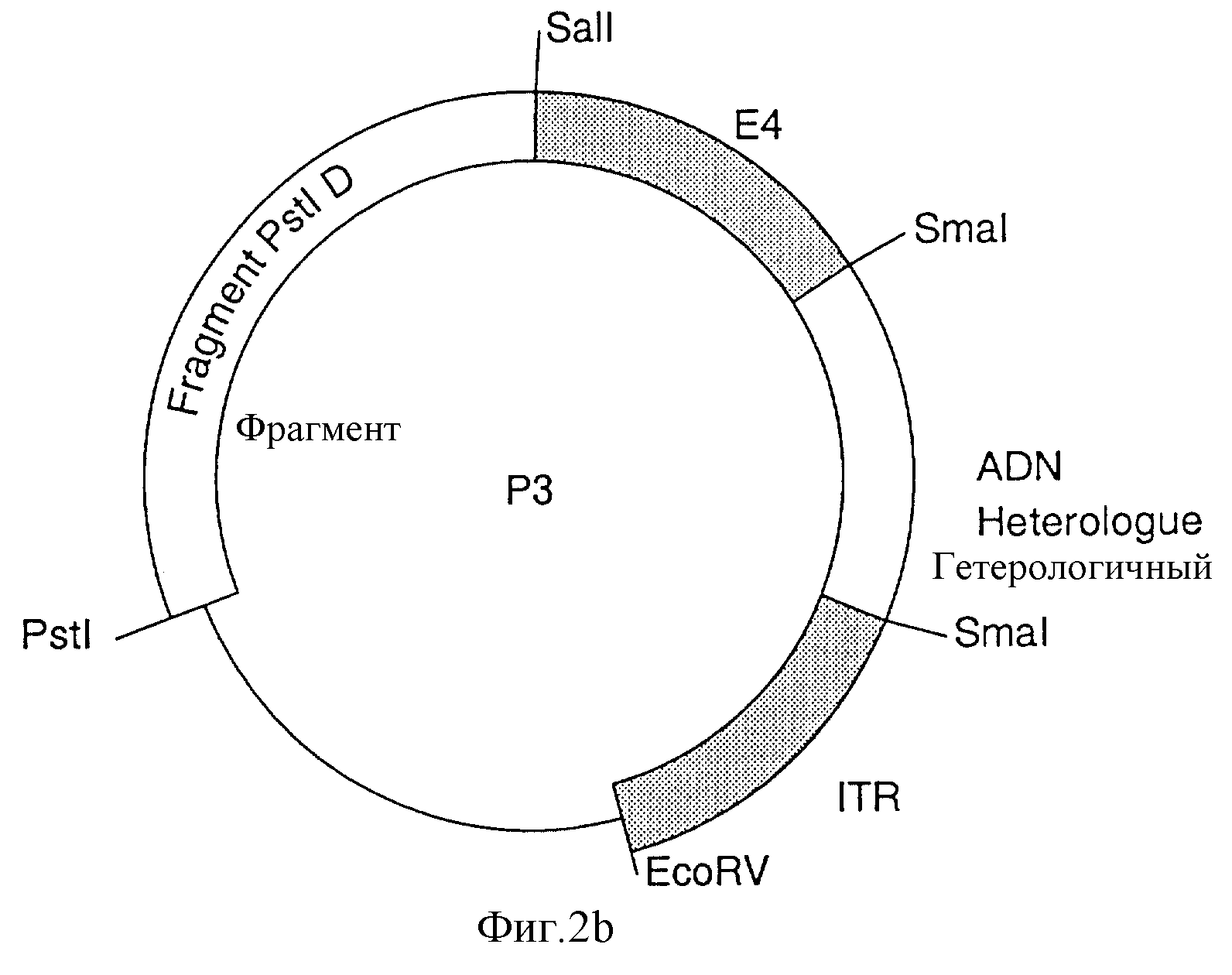
Фиг.2 - карта плазмид “p1”, “р2” (фиг.2а) и “р3” (фиг.2б);
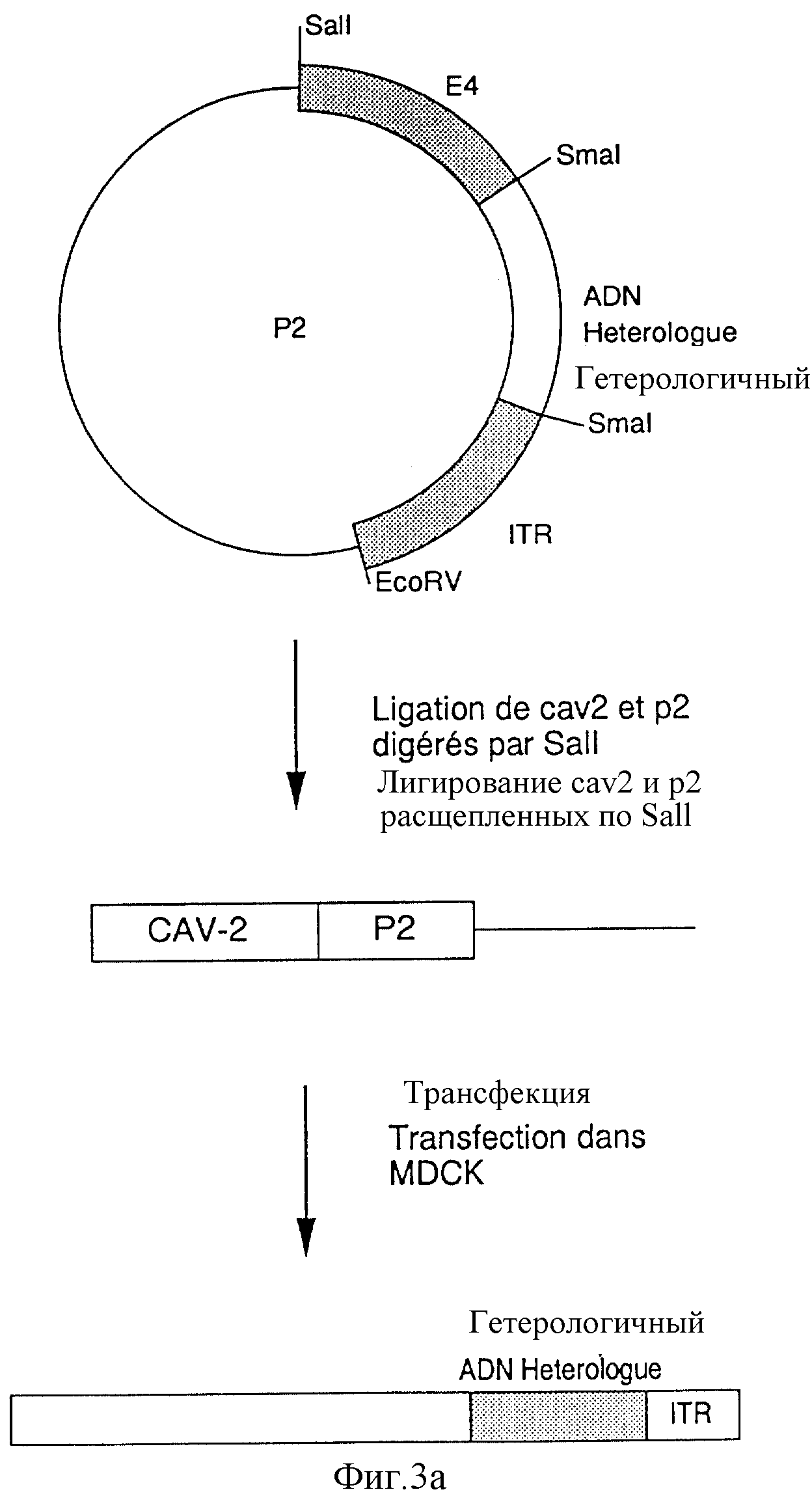
фиг.3 - стратегия конструкции рекомбинантного собачьего аденовируса, содержащего гетерологичную ДНК-последовательность.
Общие способы молекулярной биологии
Классически используемые в молекулярной биологии методы, такие как препаративные экстракции плазмидной ДНК, центрифугирование плазмидной ДНК в виде градиента хлорида цезия, электрофорез на агарозогелях или акриламиде, очистка фрагментов ДНК путем электроэлюирования, экстракция протеинов фенолом или смесью фенола с хлороформом, преципитация (осаждение) ДНК в солевой среде с помощью этанола или изопропанола, трансформация в Еscherichia coli, и т.д., хорошо известны специалисту и в большом количестве описаны в литературе [Маniats Т. и др., "МоIеcuI ar Сiоnig, a Loboratory Man и аI", Cold Spring Harbor, N.Y., 1982; Ausubel F.M и др. (изд.), “Current Protocols in Molecular Biologie” John Wiley and sons, New York, 1987].
Плазмиды типа рВR 322, рuС и фаги серии MI3 имеются в продаже (Веthesda Research Laboratories).
Для лигатур фрагменты ДНК можно разделять по их величине путем электрофореза в агарозогелях или акриламиде, экстрагировать фенолом или смесью фенола с хлороформом, осаждать в этаноле, затем инкубировать в присутствии ДНК-лигазы фага Т4 (BioIabs) согласно рекомендациям изготовителя.
Дополнение выступающих 5'-концов можно осуществлять с помощью фрагмента Кленова ДНК полимеразы I Е. соIi. (BioIabs) согласно инструкциям изготовителя. Деструкцию выступающих 3'- концов осуществляют в присутствии ДНК полимеразы фага Т4 (Вiolabs), используемого согласно рекомендациям изготовителя. Деструкцию выступающих 5’-концов осуществляют путем осторожной обработки нуклеазой SI.
Мутагенез, направляемый ин витро с помощью синтетических олигодезоксинуклеотидов, можно осуществлять по методу, разработанному TayIor и др. [Nucleic Acids Res. I3 (1985) 8749-8764], используя набор, выпускаемый фирмой Аmersham.
Ферментативную амплификацию фрагментов ДНК по так называемому методу PCR/РоIymerase-catalyzed Chain Reaction, Saiki R.K. и др., Scienсе 230 (1985) 1350-1354; MuIIis К.В. и Faloona F.A., Meth. Enzym 155 (1987) 335-350 осуществляют путем использования "DNA thermal cycler" (Perkin Elmer Cetus), согласно инструкциям изготовителя.
Проверку нуклеотидных последовательностей можно осуществлять методом, разработанным Sаngеr и др. [Proс. Natl. Acad. Sci. USA. 74, (1977) 5463-5467], используя набор, выпускаемый фирмой Amersham.
Примеры
Пример I: Инфекция человеческих клеток аденовирусами собачьего происхождения
Этот пример демонстрирует способность аденовирусов животного (собачьего) происхождения инфицировать человеческие клетки.
I.I. Используемые линии клеток
В этом примере используют следующие линии клеток:
- линия почки эмбриона человека 293 /Craham и др., J.Gen. Virol. 36 (1977) 59/. Эта линия особенно содержит интегрированную в свой геном левую часть генома человеческого аденовируса Аd 5 (12%);
- линия человеческих клеток KB: происходит от эпидермальной человеческой карциномы; эта линия имеется в ATCC (обозначение: CCI, 17) также, как условия, позволяющие ее культивировать;
- линия человеческих клеток HeIa: происходит от карциномы человеческого эпителия; эта линия имеется в АТСС (обозначение: CCL 2 ) также, как условия, позволяющие ее культивировать;
- линия собачьих клеток МДСК: условия культивирования клеток МДСК описаны особенно Масаthеу и др., Science, 44 (1988), 9.
1.2.Инфекция
Клетки вышеуказанных линий инфицируют с помощью вируса CAV-2 (штамм Маnhattan). Для этого клетки (примерно 107 на чашку) инкубируют в течение 1 часа при 37°С в присутствии 10 pfu/клетка вируса. Затем добавляют 5 мл культуральной среды и культивирование продолжают при 37°С в течение примерно 48 часов. В этот момент ДНК, находящуюся в эписомной форде в инфицированных клетках, анализируют: полученные результаты показывают, что все эти линии клеток содержат ДНК САV-2 в своих ядрах, что демонстрирует наличие собачьих аденовирусов.
Пример 2
Отсутствие размножения аденовирусов собачьего происхождения в человеческих клетках
Этот пример демонстрирует, что собачьи аденовирусы хотя и способны инфицировать человеческие клетки, не размножаются в них.
После инфекции клеток согласно примеру I количество ДНК CAV-2 определяют количественно с течением времени согласно следующей методике: эписомную ДНК, находящуюся в клетках, рекуперируют по способу, описанному Нirt и др. /J.Virol, 45 (1983) 91/, и количество ДНК определяют путем сравнения с эталонным рядом. Полученные результаты показывают, что количество вирусной ДНК не увеличивается в клетках КВ и 293, что свидетельствует о полном отсутствии репликации CAV-2 в этих клетках. В клетках МДСК и HeIa наблюдают незначительное повышение количества вирусной ДНК САV-2. Однако количественный анализ в отношении образования вирусных частиц показывает, что никакого размножения CAV-2 в человеческих клетках 293, KB и HeIa не происходит, а происходит только в линии собачьих клеток МДСК. Размножение определяют путем собирания инфицированных клеток, высвобождения возможных вирусов за счет замораживания/размораживания и инфекции клеток МДСК с помощью таким образом полученном надосадочной жидкости в вышеописанных условиях. После культивирования в течение 48 часов отсутствие вирусной ДНК в таким образом инфицированных клетках МДСК показывает, что нет никакого размножения вируса в человеческих клетках.
Эти результаты ясно показывают, что собачьи аденовирусы неспособны размножаться в человеческих клетках,
Пример 3
Демонстрирование отсутствия транскомплементарности собачьих аденовирусов к человеческим аденовирусам
Этот пример показывает, что отсутствие размножения собачьих аденовирусов в человеческих клетках не транскомплементарно к присутствию человеческих аденовирусов.
Клетки человеческих линий 293, KB и HeIa и собачьей линии МДСК коинфицируют за счет аденовируса СAV-2 и человеческого аденовируса Аd 5. Присутствие вирусной ДНК (собачьей и человеческой) в клетках обнаруживают, как в примере I, и количество ДНК определяют путем количественного анализа в течение времени также, как и размножение. Полученные результаты показывают, что количество ДНК САV-2 с течением времени не увеличивается в клетках KB и 293, что свидетельствует о том, что наличие человеческого аденовируса Ad-5 не индуцирует за счет транскомплементарности репликацию САV-2 в этих клетках. Отсутствие вирусной ДНК в клетках ДМCK, инфицированных возможными вирусами, происходящими из клеток KB, 293 и HeIa, показывает, таким же образом, что не происходит никакого размножения аденовируса CAV-2 в человеческих линиях клеток даже в присутствии человеческого аденовируса.
Пример 4
Конструкция банка геномной ДНК CAV-2.
Банк плазмид получают из фрагментов рестрикции генома аденовируса СAV-2. Этот банк получают путем переваривания САV-2 ферментами SmaI и РstI и клонирования фрагментов SmaI: А, В, С, D, Е, Р, I и J и фрагментов РstI: А, В, С, D, Е, F, G, Н (фиг.1) в вектор pGem 3Zf# (Рromega). Плазмиду, несущую фрагмент SmaI С, затем котрансфицируют в клетки МДСК с плазмидой р и C4KIXX (Рharmacia), содержащей ген резистентности к неомицину, для введения линии МДСК, конститутивно экспрессирующий гены EIA и EIB CAV-2. Эта линия позволяет осуществлять конструкцию рекомбинантных вирусов, подвергнутых делеции в этих сайтах (см. пример 5.2).
Пример 5
Конструкция рекомбинантных собачьих аденовирусов, несущих ген интерлейкина-2 под контролем промотора М PL Аd2
Разработаны две стратегии в отношении конструкции рекомбинантных собачьих аденовирусов, содержащих ген интерлейкина-2, под контролем человеческого промотора MPL Ad2.
5.1
Первая стратегия состоит во вставке желательной гетерологичной ДНК-последовательности (промотор ML Р - ген интерлейкина - 2) между сайтом Е4 и правой ITR целого генома СAV-2 на уровне сайта рестрикции Smal. Конструкцию такого рекомбинанта осуществляют либо путем лигирования, либо путем рекомбинации ин виво между несущей желательную гетерологичную ДНК-последовательность плазмидой и геномом САV-2.
Плазмиды, используемые для получения рекомбинантных аденовирусов, которые несут ген интерлейкина-2 под контролем промотора ML Р, конструируют следующим образом (фиг.2):
- первую плазмиду, обозначаемую р1, получают путем клонирования фрагмента SaIIB САV-2: (фиг.1), содержащего особенно правую IТR, сайт SmaI и ген Е4, в плазмиде р Gеm 3 Zf + (Promega), причем сайт SmaI является единственным в р1;
- гетерологичную ДНК-последовательность (промотор M LP-ген интерлейкина-2) вводят на уровне сайта SmaI плазмиды р1 для образования плазмиды p2;
- фрагмент PStI - SaII, содержащиеся во фрагменте Pste. Д геномного банка и несущий часть гена Е3, затем клонируют в соответствующий сайт в р2 для образования плазмиды р3 (фиг.2).
Таким образом, полученные плазмиды используют для получения рекомбинатных аденовирусов согласно двум следующим методикам (см. фиг.3):
а) лигирование ин витро плазмиды р2, переваренной с помощью SаII, с фрагментом SaII A CAV-2 и трансфекция продукта лигирования в клетки МДСК (фиг.3а);
б) рекомбинация между плазмидой р3 и фрагментом SaII A САV-2 после котрансфекции в клетки МДСК (фиг.3б).
Полученные рекомбинанты аденовирусы затем выделяют и амплифицируют известными специалисту методами.
Эти манипуляции позволяют осуществлять конструкцию рекомбинантных собачьих аденовирусов, несущих ген интерлейкина-2, которые используются для переноса этого терапевтического гена человеку (фиг.3).
5.2.
Вторая стратегия в отношении переваривания базируется на использовании линии клеток МДСК, конститутивно экспрессирующей гены ЕIА и ЕI В САV-2 (см. пример 4). Эта линия, на самом деле, позволяет транскомплементировать собачьи аденовирусы, подвергнутые делеции в этих сайтах, и таким образом получать конструкцию рекомбинатных вирусов, в которых гетерологичная ДНК-последовательность заменена в сайте ЕI. Для этого конструируют плазмиду, включающую левый конец (ITR-последовательность и последовательность инкапсуляции) генома CAV-2 и гетерологичную ДНК-последовательность. Эту плазмиду контрафицируют в клетки МДСК, описанные выше, и в присутствии генома аденовируcа CAV-2, подвергнутого делеции на своем собственном левом конце. Продуцированные рекомбинантные собачьи аденовирусы рекуперируют, в случае необходимости амплифицируют и хранят (консервируют) для их использования для человека.
Реферат
Изобретение относится к области биотехнологии. Предложены способ получения рекомбинантного аденовируса животных и рекомбинантный аденовирус животных. Способ получения рекомбинантного аденовируса заключается в том, что встраивают в аденовирус гетерологичную последовательность ДНК, включающую по меньшей мере один терапевтический ген, а в качестве аденовируса используют аденовирус животных. Рекомбинантный аденовирус животных содержит гетерологичную последовательность ДНК, включающую по меньшей мере один терапевтический ген, которая встроена в геном аденовируса, выбранного из группы штаммов Manhattan или А 26/61 (АТСС VR-800) аденовируса CAV-2 и штаммов АТСС VR-1343 и АТСС VR-1340 овечьего аденовируса. Полученный рекомбинантный аденовирус используют для генной терапии человека. 2 с. и 8 з.п. ф-лы, 3 ил.

Комментарии