Новый вирус репродуктивно-респираторного синдрома свиней (вррсс) корейского типа - RU2630306C2
Код документа: RU2630306C2
Чертежи
Описание
Область техники
Настоящее изобретение относится к новому вирусу репродуктивно-респираторного синдрома свиней (ВРРСС) корейского типа, композиции вакцины, полученной с его применением, и способу предотвращения репродуктивно-респираторного синдрома свиней.
Уровень техники
В 1987 году в сельскохозяйственных регионах США стали появляться сообщения о новом заболевании свиней неизвестной этиологии. Число случаев данного заболевания, которое выражалось комплексом репродуктивных расстройств и респираторных инфекций, мгновенно возросло летом 1988 и 1989 годов. Первоначально это заболевание, которое появилось неожиданно и оказало значительный ущерб свиноводству США, назвали загадочной болезнью свиней, и после того, как был выделен вирус-возбудитель и достигнуты успехи в исследованиях по изучению клинических симптомов, патогенности и т.д., к настоящему времени, это заболевание получило международное название РРСС (репродуктивно-респираторный синдром свиней) в соответствии с характеристиками клинических симптомов, которые проявляются в виде репродуктивных расстройств и респираторных инфекций.
В Корее, несмотря на отсутствие сообщений о распространенности симптомов, сходных с данной болезнью, с 1992 года начаты исследования данного заболевания по установлению способов его диагностики, проведены эпидемиологические исследования на корейских свинофермах, и в результате было подтверждено, что данное заболевание также имеет место в Корее, а вирус-возбудитель был выделен на зараженных корейских фермах. В Азии, в Японии и на Тайване, зарегистрированы случаи распространения и выделения вируса-возбудителя, отличающегося от корейского.
Даже после сообщения о появлении данного вируса точная причина установлена, не была, поэтому свиная промышленность оказалась в большом замешательстве. В июне 1991 года д-р Вензвут (Wensvoort) в Центральной ветеринарной лаборатории королевства Нидерланды впервые выделил вирус-возбудитель с помощью альвеолярных макрофагов свиней. Данный вирус был назван вирусом Лелистад (Lelystad) по названию места, где находится Центральная ветеринарная лаборатория королевства Нидерланды, и вскоре после этого вирус возбудителя был выделен во многих странах, включая США В результате исследований его свойств, патогенности и т.д., было обнаружено, что новое заболевание свиней, которое до этого в США и Европе приводило к комплексным нарушениям репродуктивного здоровья и респираторным инфекциям, вызвано данным вирусом.
Вирус РРСС, который в Европе часто называют вирусом Lelystad, а в США вирусом SIRS, имеет наружную мембрану, и указанный вирус представляет собой небольшой глобулярный вирус диаметром 45-80 мм с небольшими отростками на его поверхности. На участке, где расположены гены, находится одноцепочечная молекула РНК, имеющая диаметр 25-35 нм. Поскольку данный вирус не очень устойчив к внешней среде, при уровне кислотности менее 5 или более 7, инфекционный титр данного вируса снижается на 90% и более; а после инкубации от 10 до 24 часов при 37°C или в течение 6 дней при 20°C инфекционный титр снижается более чем в 10 раз. При заражении свиней исследуемым вирусом заболевание протекает по-разному, включая как случаи отсутствия клинических симптомов и экономического ущерба, когда инфекцию можно обнаружить только с помощью сывороточного теста, так и серьезные случаи, когда ущерб продукции на фермах достигает 20%.
Как следует из названия заболевания, репродуктивные расстройства и заболевания органов дыхания проявляются комплексно. Признаками репродуктивных расстройств, вызванных инфекционным вирусом РРСС являются выкидыш на поздней стадии беременности или преждевременный опорос между 107 и 113 днями беременности, появление мертворожденных и мумифицированных свиней, внезапное увеличение смертности до отъема поросят, увеличение смертности после отъема, задержка эструса и т.д. Данные симптомы интенсивно проявляются у инфицированных свиноматок и поросят, рожденных от них. Известно, что восстановление после репродуктивных расстройств, вызванных вирусной инфекцией РРСС, к доинфицированному состоянию происходит примерно через 6 месяцев после ранней стадии инфицирования. Респираторные заболевания, вызванные вирусом РРСС, могут проявиться в любом возрасте, и, в частности, указанные заболевания наиболее часто появляются у молочных поросят и поросят-отъемышей. В этом случае наблюдаются учащенное брюшное дыхание, а также отек глаз, конъюнктивит, чихание, диарея и другие признаки; имеют место случаи, когда возникает повышение температуры тела на короткий период времени, в редких случаях появляются признаки и симптомы неврологических нарушений. Респираторные заболевания в основном вызваны вторичными инфекциями или комплексной инфекцией, вызванной бациллами, патогенными вирусами, отличными от отдельного вируса РРСС, но в таком случае патогенность оказывается существенно выше. Кроме ранее перечисленного, зарегистрированы случаи появления синевы в области уха, живота, наружных женских половых органов и т.п., поэтому в Великобритании данное заболевание также называют болезнью «синего уха».
Указанные клинические симптомы могут предположительно иметь место при остром течении заболевания, а различные и характерные клинические симптомы наблюдаются реже при субклинической или хронической формах течения болезни. Хронические инфекции в основном распространены у поросят-отъемышей и поросят на стадии откармливания, а расстройство органов дыхания является следствием поражения вирусом РРСС в зародышевом состоянии, а также вирусом, вызывающим ринит и пневмонию. Как следствие, снижается среднесуточный привес, растет расход корма, смертность после отъема увеличивается в два раза в сравнении со средним показателем смертности до заражения вирусом РРСС. Болезнь легких от респираторной инфекции, вызванной вирусом РРСС, выражается характерной патологической эпилептической пневмонией.
Вирусы РРСС, в настоящее время это вирус Lelystad (Wensvoort и др., 1991), который был впервые выделен в Европе, и вирус VR-2332 [0004] (Benfield и др.; 1992), который был выделен в Северной Америке, классифицируются как прототипы европейских и североамериканских штаммов, соответственно, гомология нуклеотидных последовательностей которых составляет от 50 до 70%, что является очень низким показателем (Gagnon and Dea, 1998; Kwang et al., 1994; Murtaugh et al., 1995). В настоящее время, вирус РРСС, наряду с вирусом лошадиного артрита (EAV), вирусом, повышающим активность лактатдегидрогеназы (LDV), и вирусом геморрагической лихорадки обезьян (SHFV), относится к отряду Nidovirales и семейству Arteriviridae (Cavanagh, 1997). Вирус РРСС, будучи очень небольшим оболочечным вирусом, содержащим фосфатиды, имеет геном, представленный одноцепочечной РНК положительной полярности размером 15 тысяч нуклеотидных пар, заключенной в нуклеокапсид, имеющий форму правильного многогранника (Collins et al., 1992). Гены, кодирующие репликазы, которые не являются структурными белками и состоят из ферментов, необходимых для авторепликации вируса, занимают примерно 80% от 5'-конца геномной РНК, и они образованы генами ORF1a и ORF1b с зоной перекрытия экспрессируемой геномной РНК. Из них ORF1b, как сообщалось, экспрессируется механизмом рибосомного сдвига рамки считывания (Brierley et al., 1989). Структурные белки вируса занимают примерно 20% от 3'-конца геномной РНК, и они экспрессируются 7 генами: ORF2a, ORF2b до ORF7. Гены ORF2, ORF3 и ORF4 кодируют гликозилированные мембранные белки, которые представляют собой GP2, GP3 и GP4, соответственно. Ген ORF5 кодирует гликопротеин GP5, белок оболочки, который играет важнейшую роль в нейтрализующей активности вируса РРСС. Ген ORF6 кодирует белок М (матричный белок), и ген ORF7 кодирует белок N (нуклеокапсид) (Meulenberg et al., 1995; Bastos et al., 2004). Они экспрессируются на 5-конце моноцистронной субгеномной мРНК в инфицированных клетках (Meulenberg et al., 1993; Synder et al., 1999). Результаты исследований функций и молекулярно-биологических характеристик большинства белков, включая неструктурные белки, а также белков, образующих структуру вируса РРСС, все еще недостаточны. При инфицировании свиней вирусом РРСС, серьезные нарушения репродуктивной и дыхательных функций проявляются как клинические симптомы. Несмотря на невозможность доказательства существенного различия симптомов болезни вызванных европейскими либо североамериканскими штаммами вируса РРСС, они отличаются по антигенному составу или генотипу (Allende et al., 1999; Halbur et al., 1995; Wootton et al., 1998). Более того, у североамериканских и европейских штаммов имеются различия между изолятами. Например сообщалось, что различия последовательностей оснований между несколькими изолятами, принадлежащих к североамериканским штаммам могут быть вызваны существенной погрешностью РНК-полимеразы или рекомбинацией РНК, а его генетическая изменчивость может привести к существенной разнице патогенных свойств вируса (Андреев и др., 1997; Halbur et al., 1996; Ward et al., 1988).
Тем не менее, на рынке все еще отсутствуют вакцины, подходящие для корейских вариантов РРСС, полученные путем выделения ВРРСС корейского типа, а также способы получения ВРРСС корейского типа с использованием его выделения. Таким образом, необходимы исследования в отношении вакцин, подходящих для вируса РРСС корейского типа.
Краткое описание изобретения
Авторы настоящего изобретения провели исследования по выделению вируса репродуктивно-респираторного синдрома свиней (далее ВРРСС) от корейских свиней и обнаружили, что выделенный вирус является новым ВРРСС корейского типа, а затем создали настоящее изобретение.
Задача настоящего изобретения состоит в том, чтобы предложить новый ВРРСС корейского типа, композицию вакцины с его применением и способ предотвращения репродуктивно-респираторного синдрома свиней.
Для осуществления указанной выше задачи в настоящем изобретении предложен вирус репродуктивно-респираторного синдрома свиней корейского типа (далее ВРРСС) (номер доступа в КСТС 12096 ВР).
В настоящем изобретении также предложена композиция вакцины, содержащая вирус репродуктивно-респираторного синдрома свиней корейского типа (номер доступа в КСТС 12096 ВР) в качестве эффективного ингредиента.
В настоящем изобретении также предложен способ предотвращения репродуктивно-респираторного синдрома свиней, включающий введение свинье вирусной композиции вакцины.
В настоящем изобретении также предложен набор для диагностики вируса репродуктивно-респираторного синдрома свиней корейского типа, содержащий вирус репродуктивно-респираторного синдрома свиней корейского типа (номер доступа в КСТС 12096 ВР) или его антиген.
В настоящем изобретении также предложен способ обнаружения вируса репродуктивно-респираторного синдрома свиней корейского типа путем обнаружения репродуктивно-респираторного синдрома свиней корейского типа (номер доступа в КСТС 12096 ВР) в клетках для заражения или зараженных клетках с помощью реакции антиген-антитело с применением вируса репродуктивно-респираторного синдрома свиней корейского типа (номер доступа в КСТС 12096 ВР) или его антигена.
Вирус репродуктивно-респираторного синдрома свиней корейского типа с номером доступа в КСТС 12096 ВР в соответствии с настоящим изобретением является вирусом репродуктивно-респираторного синдрома свиней корейского типа, отличающимся от европейских и североамериканских штаммов, и может быть получена композиция вакцины, специфичная к вирусу репродуктивно-респираторного синдрома свиней корейского типа, способная предотвратить репродуктивно-респираторный синдром свиней корейского типа или обеспечить специфичную диагностику инфицирования вирусом репродуктивно-респираторного синдрома свиней корейского типа.
Краткое описание чертежей
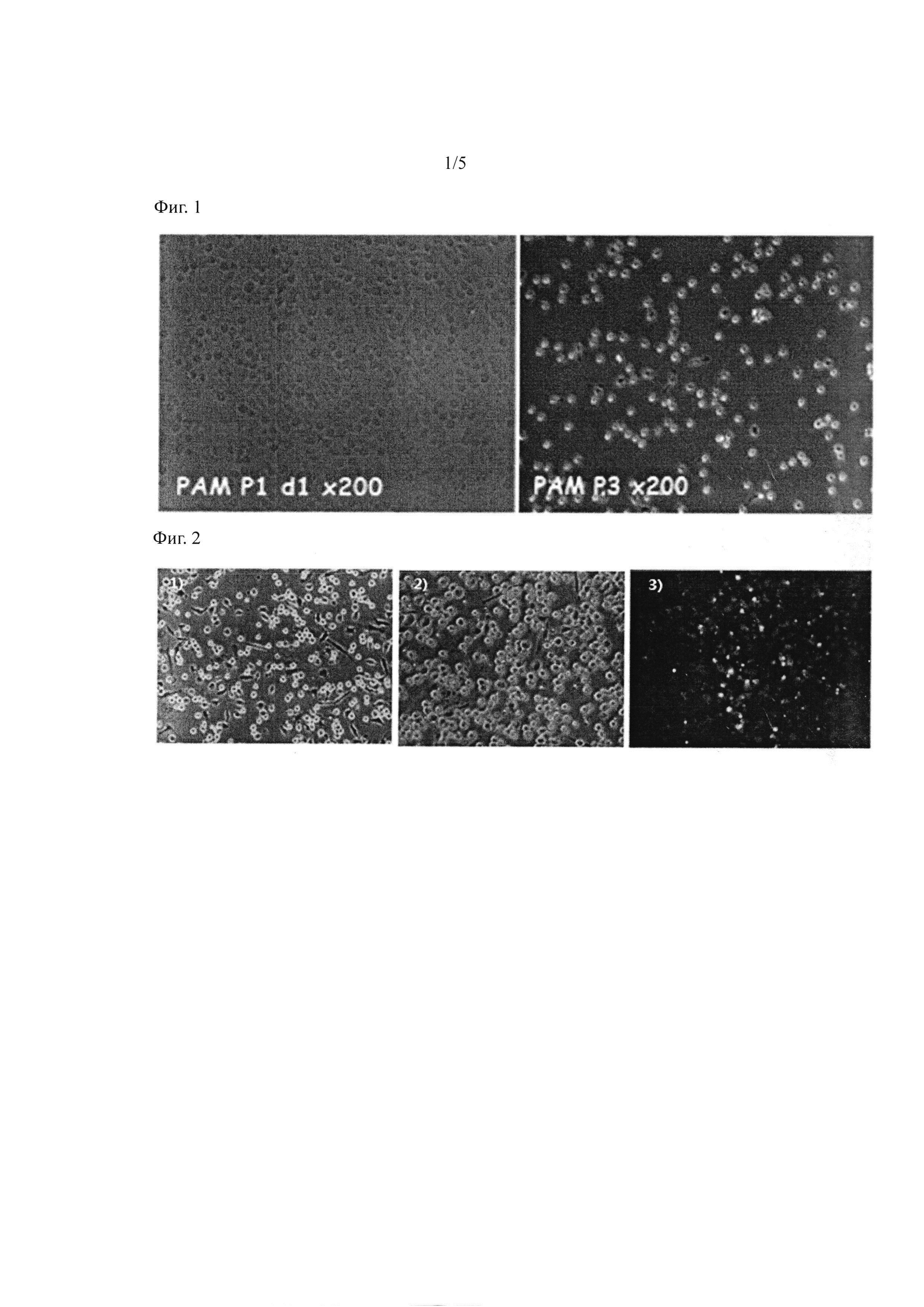
Фиг. 1. Изображение, на котором представлены альвеолярные макрофаги свиньи, выделенные из стерильных свиней (2×108 клеток/мл).
Фиг. 2. Изображение, на котором представлены результаты непрямой иммунофлуоресценции альвеолярных макрофагов свиньи, зараженных вирусом репродуктивно-респираторного синдрома свиней (далее ВРРСС).
Фиг. 3. Филогенетическое древо, построенное на основе анализа последовательности гена ORF5 ВРРСС корейского типа (JW-BPPCC).
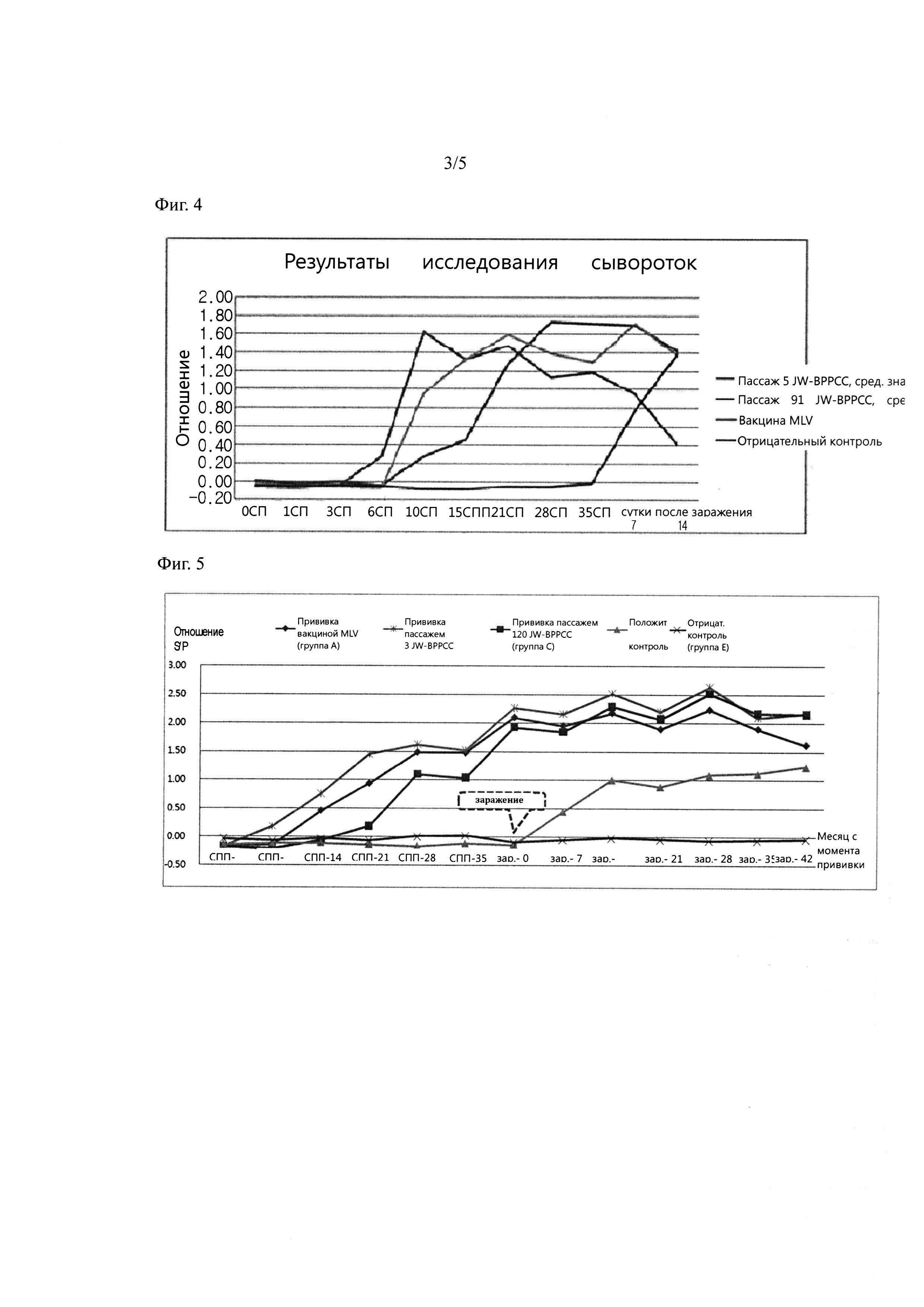
Фиг. 4. Диаграмма, на которой представлены результаты измерения титра антител после введения изолята РРССВ корейского типа (JW-PPCC) (пассаж 5, пассаж 91).
Фиг. 5. Диаграмма, на которой представлены результаты измерения титра антител в крови после введения ВРРСС корейского типа (JW-BPPCC) (пассаж 3, пассаж 120).
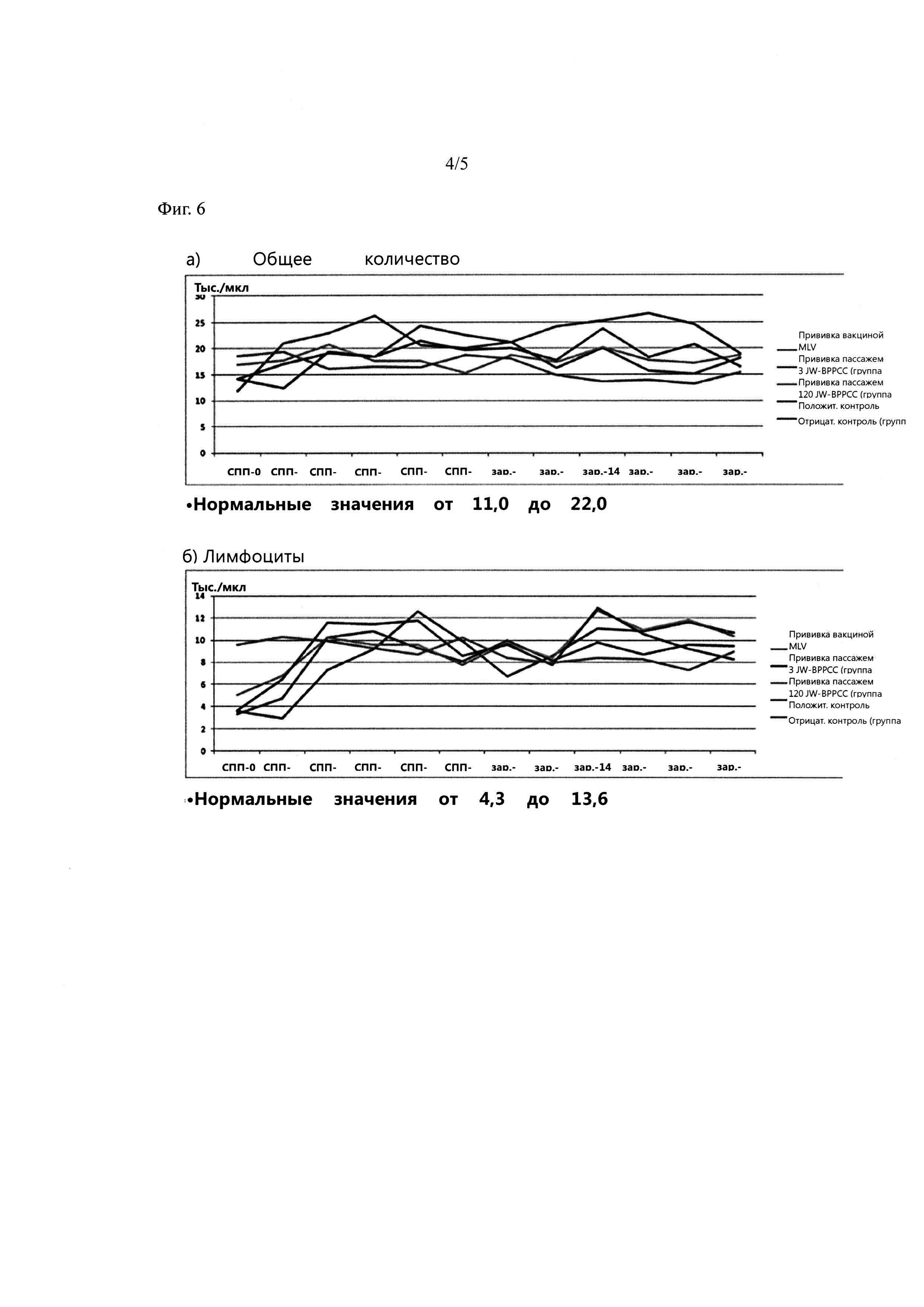
Фиг. 6. Диаграмма, на которой представлены результаты измерения количества лейкоцитов и лимфоцитов в крови животных, привитых ВРРСС корейского типа (JW-РРСС) (пассаж 3, пассаж 120).
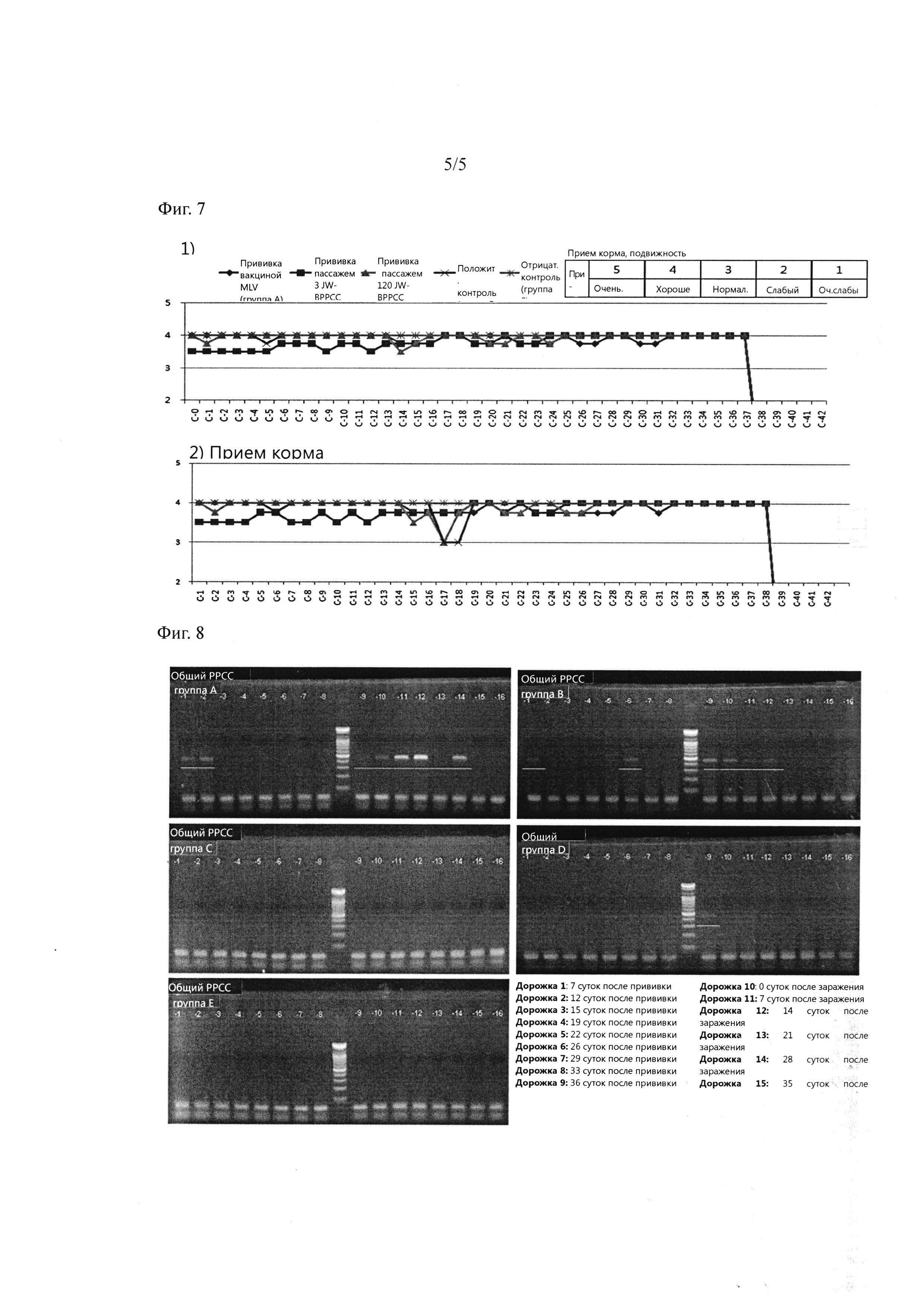
Фиг. 7. Диаграмма, на которой представлены результаты анализа клинических симптомов у животных после введения ВРРСС корейского типа (JW-BPPCC) (пассаж 3, пассаж 120).
Фиг. 8. Диаграмма, на которой представлены результаты, подтверждающие наличие вируса методом ПЦР после введения РРССВ корейского типа (JW-PPCC) (пассаж 3, пассаж 120). (группа А: группу прививали коммерческой вакциной MLV, группа В: группу прививали 3 пассажем JW-BPPCCB, группа С: группу прививали 120 пассажем JW-PPCCB, группа D: положительный контроль, группа Е: отрицательный контроль).
Наилучший вариант осуществления изобретения
В настоящем изобретении предложен вирус репродуктивно-респираторного синдрома свиней корейского типа (далее ВРРСС) (номер доступа в КСТС 12096 ВР).
Указанный вирус репродуктивно-респираторного синдрома свиней корейского типа (далее JW-BPPCC) (номер доступа в КСТС 12096 ВР) выделен в хозяйствах со свободным выгулом, способен к размножению в культурах клеток почки обезьяны MARC-145, альвеолярных макрофагов свиньи (АМС), которые непосредственно выделены от свиней и культивированы, также этот вирус способен к размножению в любой другой чувствительной клеточной культуре или среде, не ограниченной предыдущими примерами.
Кроме того, в настоящем изобретении предложена композиция вакцины, содержащая JW-BPPCC (номер доступа в КСТС 12096 ВР) в качестве эффективного ингредиента.
Указанная композиция вакцины может содержать JW-BPPCC, полученный путем культивирования JW-BPPCC в течение от 3 до 120 пассажей. Количество пассажей не ограничено, если активность указанного вируса не меняется, но композиция вакцины в качестве эффективного ингредиента может состоять из вируса JW-BPPCC, полученного путем культивирования в течение 3, 5, 91 или 120 пассажей.
Вирус репродуктивно-респираторного синдрома свиней корейского типа (JW-BPPCC) согласно настоящему изобретению может стимулировать противовирусную защиту, эквивалентную коммерческой вакцине MLV, что доказано по формированию титра антител и по результатам анализа клинических симптомов. Поэтому данный вирус фактически может быть компонентом нового кандидата на роль вакцины против репродуктивно-респираторного синдрома свиней. Более того, вирус репродуктивно-респираторного синдрома свиней корейского типа (JW-BPPCC) согласно настоящему изобретению не вызывает индивидуальных воспалительных реакций при прививании, безопасность проявляется в отсутствии каких-либо побочных эффектов, таких как нагноение на месте инъекции, некроз, лихорадка и т.д. Также" может быть решена проблема существующих вакцин ВРРСС, поскольку время выделения вируса уменьшается в сравнении с существующими вакцинами против ВРРССВ. Таким образом, указанный вирус может применяться в качестве композиции вакцины против нового свиного вируса репродуктивно-респираторного синдрома свиней корейского типа.
«Вакцина» представляет собой ветеринарную вакцину, включающую антигенную субстанцию. Такая вакцина является специфичной к репродуктивно-респираторному синдрому свиней, и ее вводят с целью стимулирования активного или пассивного иммунитета.
Композиция вакцины может включать в себя в дополнение к эффективному ингредиенту JW-BPPCC (номер доступа в КСТС 12096 ВР) один или более подходящих адъювантов, вспомогательных веществ или носителей.
Дополнительные ингредиенты, которые усиливают иммунную реакцию часто называют адъювантами, например, вспомогательные молекулы, например, но не ограничиваясь ими, интерферон, интерлейкин или фактор роста, которые добавляют, например, в гидроксид алюминия, минеральное или другое масло, или вакцину, или образуются в организме после индукции таким дополнительным ингредиентом.
Адъюванты, используемые в настоящем изобретении, включают вещества, которые усиливают иммунную реакцию у привитого животного. В данной области известно множество различных адъювантов. Примеры адъювантов, используемых в настоящем изобретении, могут включать полный и неполный адъюванты Фрейнда, витамин Е, неионные блокирующие полимеры, мурамилдипептид, Quil А, минеральные и неминеральные масла и карбопол. В качестве предпочтительного примера, вакцина согласно настоящему изобретению может включать в свой состав адъювант в виде эмульсии типа «вода в масле».
Подходящие носители для вакцины хорошо известны специалистам в данной области техники и включают, но не ограничиваются ими, белки, сахара и т.д. Такие носители могут представлять собой водные или неводные растворы, эмульсии и суспензии. Примерами неводных носителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и пригодные для инъекций органические сложные эфиры, такие как этилолеат. Водные носители представляют собой воду, спиртовые/водные растворы, эмульсии или суспензии, в том числе солевые и буферные среды. Носители для парентерального введения представляют собой раствор хлорида натрия, декстрозу Рингера, декстрозу и хлорид натрия, лактат Рингера или нелетучие масла. Носители для внутривенного введения представляют собой текучие и пищевые наполнители, электролитные наполнители, такие как наполнители на основе декстрозы Рингера, и тому подобное. Также могут присутствовать консерванты и другие добавки, такие как, например, противомикробные агенты, антиоксиданты, хелатирующие агенты, инертные газы и тому подобное. Предпочтительными консервантами являются формалин, тимеросалнеомицин, полимиксин В и амфотерицин В.
Кроме того, вакцина согласно настоящему изобретению может включать один или более подходящих эмульгаторов, таких как Спан или Твин.
Кроме того, композиция вакцины согласно настоящему изобретению может содержать защитные агенты, и без ограничений могут применяться любые защитные агенты, известные в данной области техники. Защитные агенты предпочтительно могут представлять собой лактозу (LPGG) или трегалозу (TPGG), но более предпочтительно трегалозу.
Более того, настоящее изобретение относится к способу предотвращения репродуктивно-респираторного синдрома свиней с применением JW-BPPCC, включающему введение свинье композиции вакцины на основе JW-BPPCC.4
Способ введения композиции вакцины свинье может быть реализован путем обычных способов введения вакцины, и указанное введение может быть осуществлено энтеральным или парентеральным способом, пероральным, интраназальным, внутривенным, внутримышечным, подкожным, внутрикожным или другими подходящими способами, перечень которых не ограничен указанными способами. Предпочтительно композицию можно инокулировать внутримышечно или интраназально.
Композиция вакцины предпочтительно включает от 2×105 до 2×107 бляшкоообразующих единиц (БОЕ)/мл вируса репродуктивно-респираторного синдрома корейского типа.
Кроме того, в настоящем изобретении предложен набор для диагностики вируса репродуктивно-респираторного синдрома корейского типа, содержащий вирус репродуктивно-респираторного синдрома корейского типа (номер доступа в КСТС 12096 ВР) или его антиген.
Указанный диагностический набор может быть получен в соответствии со способами, обычно используемыми в данной области.
Диагностический набор содержит инструменты, реагенты и т.д., обычно используемые в данной области техники для иммунологического анализа, а также вирус репродуктивно-респираторного синдрома корейского типа (номер доступа в КСТС 12096 ВР). Эти инструменты/реагенты включают, но не ограничиваются ими, подходящие носители, маркеры, способные вызывать сигналы обнаружения, растворители, моющие средства, буферы, стабилизаторы и тому подобное. Если маркер является ферментом, он может включать в себя субстрат и стоп-агент для остановки реакции, подходящие для измерения активности фермента. Подходящие носители включают, но не ограничены ими, растворимые носители, такие как физиологически приемлемые буферы, известные в данной области техники, такие как фосфатно-солевой буферный раствор; нерастворимые носители, такие как полистирол, полиэтилен, полипропилен, полиакрилонитрил, фторидную смолу, поперечно сшитый декстран, полисахариды; полимер, такие как магнитные частицы, в которых металл нанесен на латекс, бумагу, стекло, металл, агарозу, и их комбинации.
Кроме того, в настоящем изобретении предложен способ обнаружения вируса репродуктивно-респираторного синдрома свиней корейского типа, характеризующийся обнаружением вируса репродуктивно-респираторного синдрома корейского типа (номер доступа в КСТС 12096 ВР) в предназначенных для заражения либо зараженных клетках посредством реакции антиген-антитело с применением вируса репродуктивно-респираторного синдрома свиней корейского типа (номер доступа в КСТС 12096 ВР) или его антигена.
Реакция антиген-антитело может быть проанализирована с помощью иммуногистологических методов, радиоиммуноанализа (РИА), иммуноферментного анализа (ИФА), вестерн-блоттинга, иммунопреципитации, иммунодиффузии, реакции связывания комплемента, проточной цитометрии и белкового чипа, не ограничивась ими.
Далее настоящее изобретение будет описано более подробно с помощью примеров. Однако следующие примеры являются только примерами настоящего изобретения, и содержание настоящего изобретения не ограничивается данными примерами.
Пример 1. Выделение вируса репродуктивно-респираторного синдрома корейского типа
1.1 Выделение альвеолярных макрофагов свиньи (далее АМС)
Для выделения клеток АМС, применяемых для размножения и выделения вируса, использовали стерильных свиней возрастом от 4 до 8 недель (Optifarm-Medipig), которых данная компания разводила в условиях, свободных от специфических патогенов. После обезболивания свиньи, всю ткань легких, включая легочные бронхи, осторожно отделяли таким образом, чтобы ткань не была повреждена. Пробирку для инъекции присоединяли к внутренней стороне бронха легкого, приготовленный раствор фосфатного буфера (рН 7,2) вводили в легочную ткань через бронхи. После расширения легочной ткани, фосфатный буферный раствор в легочной ткани собирали посредством наклона вставленной пробирки. Собранный фосфатный буферный раствор центрифугировали для осаждения клеток и суспендировали в среде, в которую добавляли фетальную бычью сыворотку в концентрации 10%, заменимые аминокислоты и пенициллин/стрептомицин. Суспензию клеток помещали в посуду для культивирования, и проводили культивирование при 37°C и 5% концентрации СО2. Первичную культуру выделенных альвеолярных макрофагов свиньи в концентрации 2×108 клеток/мл хранили при -80°C. Форма культуры альвеолярных макрофагов свиньи показана на фиг. 1.
1.2 Выделение вируса РРСС и подтверждение инфицирования АМС вирусом РРСС
Для вируса, применяемого в этом эксперименте, использовали вирус репродуктивно-респираторного синдрома свиней (далее РРСС), выделенный от инфицированных свиней с проявлением признаков заболевания среди свиней фермы JW. Ткани крови, легкого, лимфы и миндалины, полученные от свиней с подозрением на инфекцию, измельчали и суспендировали в растворе фосфатного буфера, и проводили эксперимент по выделению вируса из образцов, которые были определены как вирус-положительные методом ПЦР.
Культуру АМС, полученную в примере 1.1, разделяли по флаконам Т-25 по 2×106 клеток/мл, и после подтверждения клеточной адгезии образцы, такие как образцы крови, легкого, лимфы, миндалины и т.д., в которых было методом ПЦР обнаружено присутствие вируса, инокулировали посредством от 10 до 100 мкл вируса, соответственно. Далее после проявления цитопатического действия (ЦПД), образцы собирали и хранили при -80°C. Во флаконы Т25, в которых находились клетки АМС, добавляли 100 мкл собранного вируса, подтверждали присутствие вируса методом непрямой иммунофлюоресценции (ИФ), и непрерывно проводили слепое пассирование культуры. Более конкретно, клетки, в которых подтверждено инфицирование ВРРСС, фиксировали в течение 5 минут раствором 4% параформальдегида, а затем трехкратно промывали буферным раствором в течение 10 минут. После клетки обрабатывали 2% раствором БСА в течение 1 часа для блокирования неспецифических сайтов связывания антител, а затем трехкратно отмывали в течение 5 минут. В качестве первичного антитела использовали мышиные моноклональные антитела анти-ВРРСС Mab 4А5 (JBT, номер в каталоге 9041), а в качестве вторичного антитела использовали меченые ФИТЦ козьи антитела против мышиного иммуноглобулиа (Santacruz).
Результат показан на фигуре 2.
Как показано на фиг. 2, флуоресценция может быть обнаружена в клетках АМС через 96 часов после внесения вируса в выделенные АМС.Исходя из этого, было подтверждено, что клетки АМС эффективно инфицированы ВРРСС.
1.3 Выделение клона вируса методом отделения бляшек
Клетки АМС вносили в шестилуночный планшет в концентрации 3×105 клеток на лунку. После 12 часов культивирования, выделенный ВРРСС разбавляли из одной инфекционной дозы в 10 раз, ВРСС вносили в каждую лунку. После культивирования в течение 1 часа среду удаляли, а слой клеток, инфицированных вирусом, покрывали средой DMEM, в которой содержалось 0,5% агарозы и 10% фетальной бычьей сыворотки, и культивировали при 37°C, 5% СО2. Примерно после 72 часов культивирования, становились видны невооруженным глазом сформированные бляшки. Каждую бляшку независимо отделяли и очищали для выделения клона ВРРСС.
Пример 2. Выделение JW-BPPCC (КСТС 12096 ВР) методом генетического анализа вируса РРСС
2.1 Амплификация гена ВРРСС
Филогенетический анализ для классификации вируса проводили по генетической информации участка гена ORF5 изолята ВРРСС. Геномную РНК ВРРСС выделяли из 150 мкл культуральной среды с ВРРСС с применением набора для выделения вирусной РНК (Интрон. Корея) в соответствии инструкциям производителя. ПЦР с обратной транскрипцией проводили с целью синтеза вирусной кДНК, комплементарной соответствующим генным сегментам. 2 мкл с 10 пкмолями обратного праймера гена ORF5 добавляли к 10 мкл выделенной РНК, нагревали при 80°C в течение 3 минут, а затем охлаждали, и затем вносили 1 мкл ингибитора РНК (Promega, США), пятикратный буферный раствор для ОТ (50 ммоль Tris-HCl (рН 8,3), 75 ммоль KCl, 3 ммоль MgCl2, 10 мМ ДТТ), 2 мкл 10 мМ дНТФ (Promega, США), и 1 мкмоль M-MLV обратной транскриптазы (Promega, США), амплифицировали при 37°C в течение 1 час и 30 минут. ПЦР проводили с использованием синтезированной кДНК в качестве матрицы. ПЦР повторяли 34 раза с циклом серии реакций, состоящих из выдерживания смеси 16 мкл стерильной дистиллированной воды, 2 мкл кДНК и 1 мкл праймера в пробирке (Интрон) при 94°C в течение 5 минут, денатурации при 94°C в течение 20 секунд, отжига при 60°C в течение 30 секунд, и элонгации при 72°C в течение 45 секунд, и, наконец, культивирования при 72°C в течение 5 минут. В данном эксперименте использовали праймер гена VR2332 (штамм США, номер доступа в Генбанке U87383), последовательность оснований которого представлена для анализа нуклеотидной последовательности гена ORF5 в качестве образца сравнения, и использовали прямой (ОСО ТТС TGT TGG САА ТТТ GA) и обратный праймеры (САС СТТ TAG GGC ATA TAT CAT).
2.2 Филогенетический анализ выделенного ВРРСС
Продукты ПЦР подвергали электрофорезу в 1% агарозном геле, а затем очищали с использованием набора для выделения из геля (Macherey-Nagel, Германия). Полученные продукты ПЦР присоединяли к сайту мультиклонирования гена lacZ в плазмидном векторе pGEM-T. Каждый ген клонировали с применением компетентных клеток E.coli штамма DH5α в качестве клетки-хозяина. Более конкретно, штамм Е. coli DH5α, хранившийся при -70°C, размораживали на льду, а затем в количестве 50-70 мкл добавляли в пробирку с плазмидной ДНК. Содержимое пробирки, после инкубации на льду в течение 20 минут, подвергали тепловому шоку при 42°C в течение 90 секунд, а затем снова оставляли на льду в течение 3 минут. В пробирку вносили 1 мл среды LB (Luria-Bertani) и культивировали в культуральной среде при 37°C в течение 1 часа, а затем равномерно разносили на агаровую среду LB, содержащую ампициллин (300 мг/мл), X-Gal, ИПТГ и т.д., и культивировали при 37°C в течение одной ночи. После культивирования отбирали белые колонии для извлечения плазмидной ДНК и последующего анализа нуклеотидной последовательности. Каждую отобранную белую колонию помещали на 5 мл полоску LB агара, содержащую ампициллин, и культивировали в культуральной среде при 37°C в течение одной ночи, а затем центрифугировали в течение 10 минут при 3000 об/мин. После центрифугирования плазмидную ДНК выделяли с использованием набора QIAprep Spin Miniprep (Qiagen, USA). Генетическую информацию очищенной плазмидной ДНК исследовали с помощью программного обеспечения Workbench версии 4 (CLC Bio, Arthus, Дания), затем составляли филогенетическое древо и анализировали генетическую изменчивость путем сравнения нуклеотидных последовательностей оригинальных видов вирусов и вирусов, прошедших культуральное пассирование.
Результат показан на фигуре 3.
Как показано на фигуре 3, было установлено, что выделенный ВРРСС является новым ВРРСС корейского типа, который отличается от ВРРСС североамериканского типа на 18% нуклеотидов. Новый ВРРСС корейского типа был назван JW-BPPCC и депонирован под номером КСТС 12096 ВР 2 декабря 2011 года.
Пример 3. Подтверждение иммуногенности вакцины, разработанной с использованием ВРРСС корейского типа (далее JW-BPPCC) (пассажи 5 и 91)
3.1 Клинические измерения после введения JW-BPPCC
С целью разработки вакцины на основе недавно выделенного JW-BPPCC, свиньям был введен JW-BPPCC 5 и 91 пассажей, а затем проведены наблюдения. Более точно, для потверждения иммуногенности, двенадцать свиней, молозивной фазы питания, оказавшихся отрицательными к ВРРСС и свободными от специфичного патогена, в общей сложности разделены на четыре группы: вакцинированных пассажем 5 JW-BPPCC, вакцинированных пассажем 91 JW-BPPCC, вакцинированных вакциной MLV (коммерческой вакциной) и группу отрицательного контроля (таблица 1).
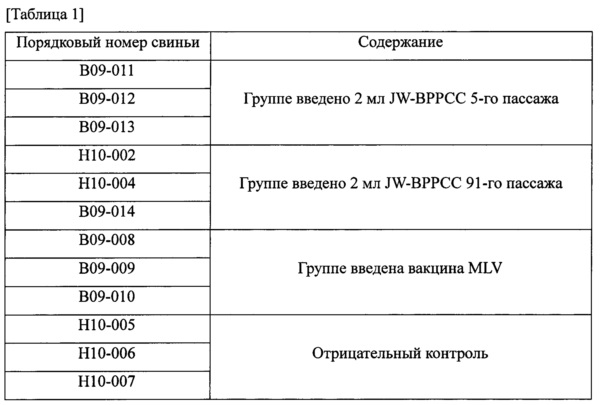
Каждой группе вводили 2 мл вируса в концентрации 1×105 БОЕ/мл, наблюдения за клиническими симптомами, такими как температура тела, подвижность, аппетит проводили на 1 сутки, 3 сутки, 6 сутки, 10 сутки, 15 сутки, 21 сутки, 28 сутки и 35 сутки после прививки. Через 37 суток после прививки, свиней заражали настоящим вирулентным исходным вирусом JW в дозе 1×104 БОЕ/мл и наблюдали за теми же показателями. Более точно, температуру тела и подвижность измеряли дважды за сутки в одно и то же время в течение всего экспериментального периода, а подвижность после наблюдения за объектом исследования оценивали в баллах, от 0 до 4 баллов с интервалом в 0,5 балла (0 баллов: подвижность отсутствует, 1 балл: слабая подвижность, 2 балла: нормальная подвижность, 3 балла: хорошая подвижность, 4 балла: очень хорошая подвижность). Далее, во время кормления подачу корма ограничивали в соответствии с весом. В случае употребления всего количества в течение 10 минут, аппетит определяли как очень хороший (4 балла), и в соответствии со временем, необходимым для приема всего количества корма, оценивали от 0 до 4 баллов с интервалом в 0,5 балла. Подвижность и аппетит оценивали по сумме оценок, полученных ранее.
Результат показан в таблице 2.
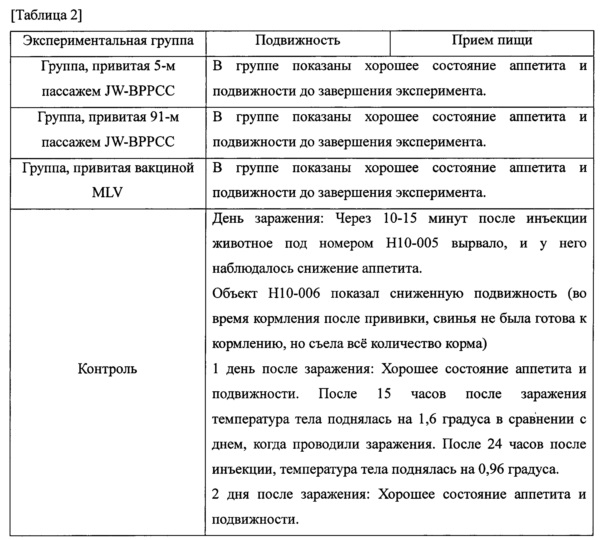
Как показано в таблице 2, в результате интерпретации баллов, группы, привитые пассажем 5 JW-BPPCC, пассажем 91 JW-BPPCC и вакциной MLV показали хорошее состояние аппетита и подвижности до завершения эксперимента. Таким образом, было подтверждено, что 5-й и 91-й пассажи JW-BPPCC, приводили к защите от вирусов эквивалентно коммерческой вакцине MLV.
3.2 Измерение титра антител после введения ВРРСС корейского типа (JW-BPPCC)
Для того чтобы оценить влияние вакцины из JW-BPPCC, вирус вводили при тех же условиях, что и в примере 3.1, а затем измеряли титр антител. Через 37 дней после прививки, свиней заражали настоящим вирулентным исходным штаммом вируса JW в концентрации 1×104 БОЕ/мл и наблюдали за теми же показателями, что и в примере 3.1. Через 14 дней после заражения проводили вскрытие всех животных, и осуществляли количественную ПЦР образцов легких, лимфы, миндалин, селезенки, печени, головного мозге и почек. Для того чтобы вакцинный вирус обеспечивал защиту от исходного вируса, в первую очередь, в сывороточном тесте должны быть определены положительные антитела, и вирус должен быть способным к нейтрализации. Изменение титра антител у привитых животных на положительный устанавливали методом ИФА (HerdChek: РРСС 2XR набор для ИФА (IDEXX Laboratories, Вестбрук, штат Мэн, США)). Наличие либо отсутствие антител к ВРРСС выражено отношением S/P, результат оценивали как положительный в том случае, когда отношение S/P было равно или превышало 0,4.
Результат показан в таблицах 3 и 4.
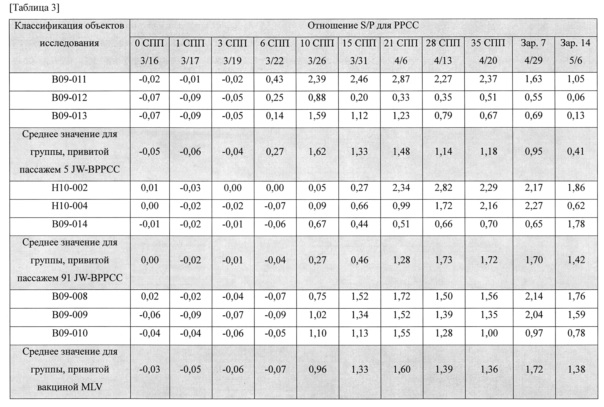
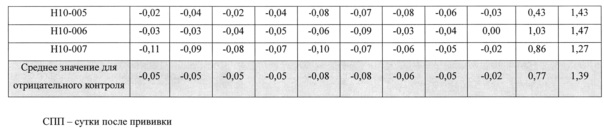
Как показано в таблицах 3 и 4, может быть подтверждено, что через 10 суток после прививки вируса животным опытных групп, привитых пассажем 5 JW-BPPCC, пассажем 91 JW-BPPCC и вакциной MLV, кроме контрольной группы, было установлено значительное увеличение титра антител, а через 35 суток после прививки, во всех опытных группах, титр антител становился положительным.
3.3 Измерение титров вируса JW-BPPCC
Для того чтобы оценить эффект вакцины, приготовленной из JW-BPPCC, группы животных прививали вирусом при тех же условиях, как и в примере 3.1, затем после вскрытия измеряли титр вируса ВРРСС в крови и тканях после вскрытия. Через 37 суток после прививки, свиней заражали настоящим вирулентным исходным штаммом вируса JW в концентрации 1×104 БОЕ/мл и наблюдали за теми же показателями, что и в примере 3.1.
Результаты представлены в таблице 4.
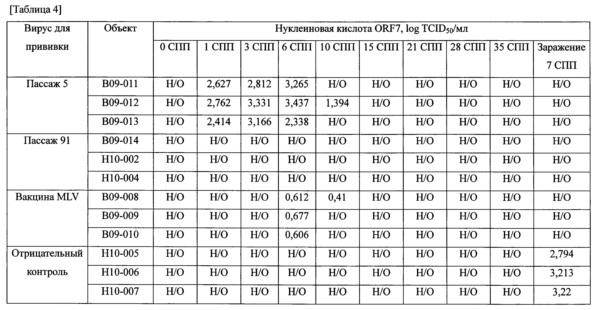
Как показано в таблице 4, в группе привитых пассажем 5 JW-BPPCC были животные, в крови которых вирус выявлен в течение 10 суток с момента прививки, в группе привитых пассажем 91 JW-PPCC, вирус не был обнаружен в крови до и после прививки. В группе животных, привитых коммерческой живой вакциной MLV, некоторое количество вируса обнаружено на шестые сутки после прививки, но после заражения вирус не выявлялся. В отрицательном контроле вирус был выявлен в крови в значительном количестве через 7 суток после заражения.
Пример 4 Подтверждение безопасности и иммуногенности вакцины, разработанной с применением ВРРСС корейского типа (JW-BPPCC)
20 свиней, находящихся в молозивной фазе питания, оказавшихся отрицательными к ВРРСС и свободными от специфичного патогена, были разделены на пять групп: привитые MLV вакциной (коммерческой вакциной; группа А.), привитые пассажем 3 JW-BPPCC (Группа В), привитые пассажем 120 JW-BPPCC (группа С), первый отрицательный контроль (отрицательный контроль заражения; группа D), второй отрицательный контроль (отрицательный контроль всего эксперимента; группа Е). В каждой группе вводили по 2 мл вируса в дозе 1×105 БОЕ /мл, а через 7, 14, 21, 28 и 35 суток после прививки наблюдали за клиническими симптомами, такими как температура тела/подвижность/аппетит и т.д., и, проведя сбор крови, определяли титр вируса и титр антител в крови, выполняли анализы клеток крови и клинических симптомов. Далее, через 42 суток после прививки, свиней заражали настоящим вирулентным исходным штаммом вируса JW в дозе 1×104 БОЕ /мл и осуществляли наблюдение за теми же показателями. Для того чтобы противовирусная вакцина оказывала защитное действие от исходного вируса, в первую очередь, должны быть определены положительные антитела в сывороточном тесте, и вирус должен быть способен к нейтрализации. Изменение титра антител у привитых животных на положительный устанавливали методом ИФА (HerdChek: набор для ИФА РРСС 2XR (IDEXX Laboratories, Вестбрук, штат Мэн, США)), появление вируснейтрализующих антител, определяли методом нейтрализации вируса (ВН).
4.1 Измерение титра вируса методом ОТ-ПЦР (ПЦР с обратной транскрипцией)
Для определения количества ВРРСС, праймер (ген ORF 7) был изготовлен с применением гена VR2332 (штамм США, номер доступа в Генбанке U87382) в качестве образца, последовательности оснований которого уже установлены (прямой праймер, ATG ATG RGC TGG CAT TACT, обратный праймер АСА CGG TCG ССС ТАА TTG). Геном РНК ВРРСС выделяли из 150 мкл культуральной среды ВРРСС с использованием набора для экстракции вирусной РНК вируса (Intron. Корея) в соответствии инструкциям производителя набора, ОТ-ПЦР проводили с целью синтеза вирусной кДНК, соответствующей комплементарному участку гена. 2 мкл обратного праймера ORF5 в концентрации 10 пмоль добавляли к 10 мкл выделенной РНК, нагревали при температуре 0°C в течение 3 минут, а затем охлаждали. Затем добавляли 1 мкл ингибитора РНК (Promega, США), пятикратный буфер для ОТ (50 ммоль/л Tris-HCl (рН 8,3), 75 ммоль/л KCl, 3 ммоль/л MgCl2, 10 ммоль/л ДТТ), 2 мкл 10 ммоль/л дНТФ (Promega, США), и 1 мкл M-MLV обратной транскриптазы (Promega, США) и амплифицировали при 37°C в течение 1 часа 30 минут. ПЦР проводили в течение 40 циклов, циклом одной серии реакций состоял из этапов смешивания 2 мкл синтезированной кДНК, 10 мкл красителя SYBR Green (Bio-Rad Корея), 6 мкл стерильной дистиллированной воды, 1 мкл праймеров при 95°C в течение 3 минут, денатурации при 95°C в течение 20 секунд, отжига при 60°C в течение 20 секунд, и элонгации при 72°C в течение 30 секунд, реакцию повторяли 71 раз при 55°C в течение 1 минуты и 60°C в течение 10 секунд повторяли 71 раз, а затем завершали. Поскольку в условиях ОТ-ПЦР проводят реакцию ПЦР с ДНК, с известным количеством разведения в течение всего процесса, в основном, в области, где амплификация проходит в геометрической прогрессии, калибровочную кривую получали с использованием порогового цикла (значение Ct), которое может обозначать постоянное количество амплифицированного продукта по горизонтальной оси и начальное количество ДНК по вертикальной оси, а неизвестную концентрацию образцов, реакция которых проходила в одинаковых условиях, вычисляли значением Ct измерением количества ДНК-мишени.
Результат показан в таблице 5.
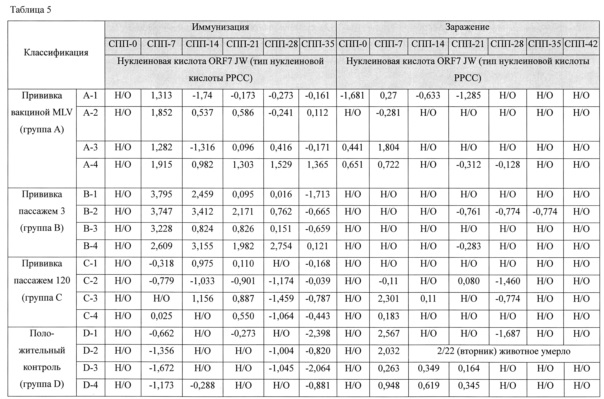
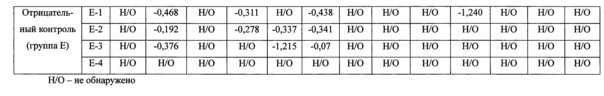
Как показано в таблице 5, в группе животных, привитых вакциной MLV (группа А), вирус был обнаружен у всех животных через 7 суток после прививки. Животных, у которых вирус не был обнаружен до 35 суток, не выявлено. В группе привитых пассажем 5 JW-BPPCC (группа В), вирус в высоких титрах выявляли у всех животных через 7 суток после прививки, однако не было определено постоянного присутствия вируса до 28 суток, не зарегистрировано животных, у которых вирус не был выявлен до 35 суток. В группе привитых пассажем 120 JW-BPPCC (группа С) вирус выявлен у двух животных через 14 суток после прививки, и оставался до 21 суток после прививки, и вирус не выявлялся через 28 суток. Согласно полученным данном, можно утверждать, что эта вакцина показала титр вируса в 6 раз ниже, чем коммерческая вакцины MLV (GA) и короткое время циркуляции в крови. Кроме того, в группе привитых вакциной MLV (группа А) у всех животных был выявлен вирус, однако в группе привитых пассажем 120 JW-BPPCC (группа С) вирус обнаружен только у двух животных. Через 42 суток после заражения, в группе привитых MLV вакциной (группа А), через 7 суток после прививки вирус обнаружен в крови трех животных, а в группе привитых пассажем 5 JW-BPPCC (группа В) вирус не выявлялся у всех четверых животных. Это считается гомологичной защитой от заражения (Доклад: Коллоквиум по перспективам развития эффективны вакцин против вируса РРСС, 13 августа 2007 года - D.L. Rock, PhD, университет штата Иллинойс). В группе привитых пассажем 120 JW-BPPCC (группа С), через 7 суток после заражения, вирус был обнаружен у двух животных. В группе отрицательного контроля (группа D) у двух животных вирус был обнаружен в значительном количестве через 7 суток после заражения, из которых одно животное умерло через 14 суток после заражения. Провели вскрытие указанного животного и определили количество вируса в легких, лимфе, миндалинах, бронхах, печени и т.д.
Результаты представлены в таблице 6.
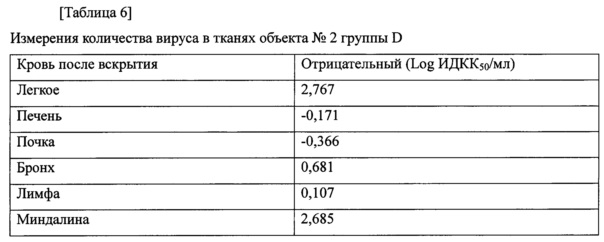
Как показано в таблице 6, может быть подтверждено, что в легком и миндалине умершего животного из группы отрицательного контроля обнаружено значительное количество вируса.
4.2 Результат измерения титра антител в крови
Образцы крови, полученные от каждой вакцинированной группы животных, для измерения титра антител в крови против РРСС, были исследованы в ИФА (HerdChek: комплект РРСС 2XR ELISA (HerdChek: набор ИФА для РРСС 2XR (IDEXX laboratories, Вестбрук, штат Мэн, США). Наличие или отсутствие антител против РРСС выражено отношением S/P, за положительный результат принято отношение S/P равное или больше 0,4.
Результат показан в таблице 7 и на фигуре 5.
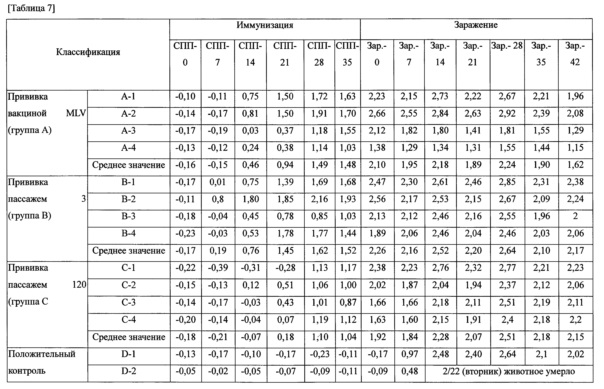
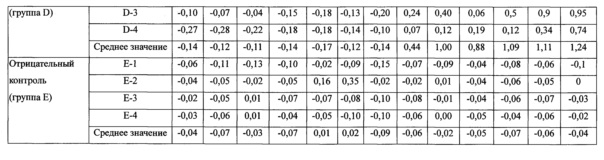
Как показано в таблице 7 и на фигуре 5, в группе животных, привитых коммерческой MLV вакциной (группа А), через 14 суток после прививки у двух животных содержание вируса оценивали как положительное, и через 25 суток, у четырех животных содержание вируса оценивали как положительное. В группе привитых пятым пассажем JW-BPPCC (группа В) через 7 суток после прививки у одного животного содержание вируса оценивали как положительное, и после 14 суток у четырех животных вирус оценивали как положительное. В группе привитых 120 пассажем JW-PPCC (группа С) через 21 сутки после прививки, у двух животных содержание вируса оценивали как положительное, и после 14 суток, у четырех животных, содержание вируса оценивали как положительное. Исходя из вышеизложенного, установлено, что прививка пассажем 120 JW-PPCC (группа С), который является кандидатом в вакцины, способна вызывать образование антител в достаточном количестве, будучи безопасной.
4.3 Результат анализа клеток крови
Количество различных клеток крови измеряли с помощью аутоцитометрии в образцах крови, взятых от каждой из групп привитых животных. Результат показан на фигуре 6.
Как показано на фиг. 6, может быть подтверждено, что в группе привитых пассажем 3 JW-PPCC (группа В), содержание лейкоцитов несколько завышено, однако в других группах, изменение количества лейкоцитов не было столь значительно до прекращения эксперимента (а). Более того, в результате измерения лимфоцитов в крови, даже после введения группе кандидата в вакцины, показаны нормальные значения лимфоцитов от 4,3 до 13600 клеток/мкл (b). Этот результат показывает, что субстанция, являющаяся кандидатом в вакцины, согласно настоящему изобретению представляет собой безопасное вещество, которое не вызывает воспаления у объекта исследования.
4.4 Результат клинического анализа
После заражения вакцинированных животных, наблюдали клинические симптомы, появляющиеся у свиней. В течение всего экспериментального периода измеряли температуру тела и подвижность в одно и то же время два раза в день, подвижность оценивали в баллах от 0 до 4 баллов с интервалом в 0,5 балла методом индивидуального обследования (0 баллов: подвижность отсутствует, 1 балл: слабая подвижность, 2 балла: нормальная подвижность, 3 балла: хорошая подвижность, 4 балла: очень хорошая подвижность). Для оценки аппетита подачу корма ограничивали в соответствии с весом, если было съедено все количество корма в течение 10 минут, аппетит оценивали как очень хороший (4 балла), и в соответствии с временем, необходимым для приема всего количества корма, оценивали от 0 до 4 баллов с интервалом 0,5 балла. Результаты показаны в таблице 8 и на фигуре 7.
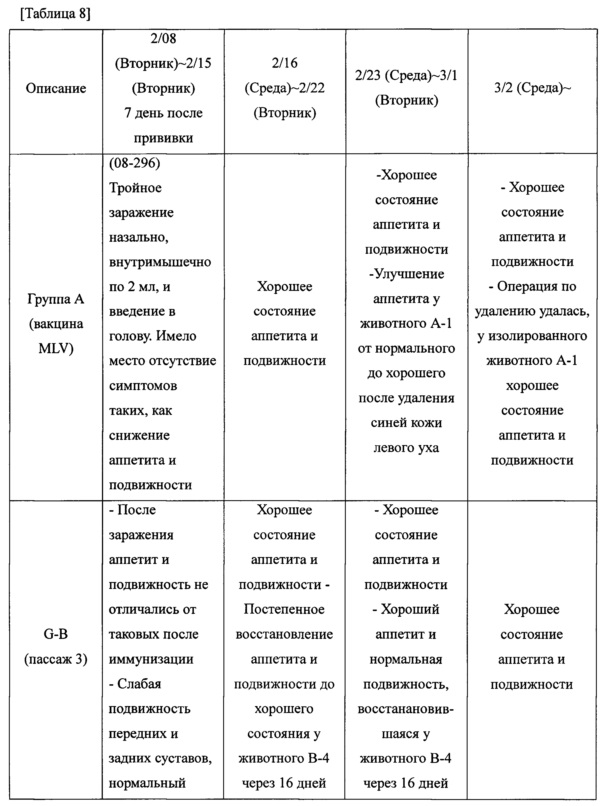


Как показано в таблице 8 и на фигуре 7, было сделано наблюдение, что группа, привитая пассажем 3 JW-BPPCC (группа В) демонстрировала слабую подвижность и плохой аппетит, но в целом имело место хорошее состояние аппетита и подвижности.
Пример 5. Получение вакцины JW-BPPCC
5.1 Способ пассирования и условия хранения
В культуру клеток MARC-145 вносили настоящий вирулентный вирус РРСС (пассаж 120) в дозе более 1040TCID50/мл, что было подтверждено в исследованиях по идентификации и иммуногенности, и культивировали при 37°C в течение 4-5 дней, полученный вирус замораживали или лиофилизировали и хранили температуре -80°C. Вирулентный ВРРСС был получен таким же образом, как и настоящий вирулентный вирус PRRS, а затем замораживали и лиофилизировали и хранили при -80°C. Настоящий вирулентный вирус не культивировали более 3 пассажей, значение титра вируса не превышало 1040TCID50/мл.
5.2 Масштабирование получения и исследования на содержание вируса
Клетки MARC-145 или АМС культивировали в роллерных бутылях с площадью поверхности 850 см2 в среде для выращивания клеток, пассирование клеток осуществляли с интервалом от 3 до 5 суток. В момент формирования клеточного монослоя на роллерной бутыли с площадью поверхности 850 см2, культуральную среду удаляли и вносили вируссодержащую жидкость в таком количестве, что она покрывала клетки, адсорбцию вируса осуществляли при 37°C в течение 1 часа. Внесенную вируссодержащую жидкость удаляли и добавляли среду для роста клеток, культивирование во вращающихся сосудах осуществляли при 37°C в течение 4-5 дней. Вируссодержащую культуральную жидкость центрифугировали, разбавляли в десять раз и вносили в 96-луночный планшет, содержащий клетки MARC-145 или АМС, и культивировали при 37°C в течение 7 дней, наблюдая за цитопатическим действием вируса (ЦПД). При достижении ЦПД на уровне 80-90% СРЕ после культивирования вируса, последний собирали в асептических условиях и замораживали, хранили при -80°C.
5.3 Получение экспериментальной вакцины
*Экспериментальную вакцину, в состав которой входил выделенный вирус в качестве антигена, получали посредством добавления защитного агента. Получено три вида экспериментальных вакцин с применением стерильного фосфатного буферного раствора фосфата и использованием морозильной камеры и сушилки (номера серий: 60 РРСС 01, 60 РРСС 02, 60 РРСС 03). Содержание полученных экспериментальных вакцин соответствует таблицам 9, 10 и 11.



В качестве защитного агента применяли трегалозу (TPGG), а не традиционно используемую лактозу (LPGG), контаминация, которая могла возникнуть при получении живой вакцины благодаря существующим защитным агентам может быть сведена к минимуму, а безопасность вакцины повышена. Сравнительные данные для субстацнии, содержащей вирус и защитные агенты, приведены в таблице 12.

5.4 Оценка безопасности экспериментальной вакцины
Для оценки безопасности экспериментальной вакцины, полученной в примере 5.3, исследовали показатели: внешний вид, уровень вакуума, концентрацию водородных ионов, влажность, контроль стерильности, содержание микоплазм, изменения вируса, содержание и титр. Исследования проводили на момент получения вакцины, а также через три и шесть месяцев после получения.
Результаты оценки безопасности показаны в таблице 13.
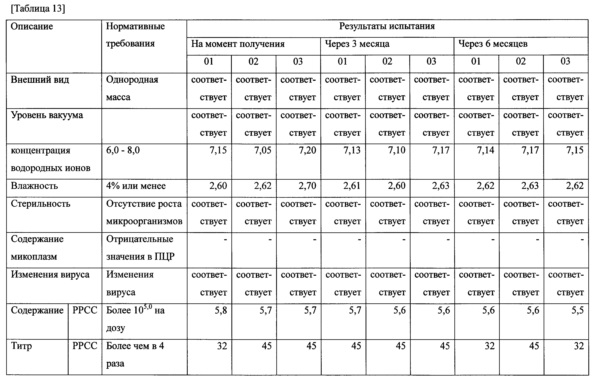
Как показано в таблице 13, было подтверждено, что готовые экспериментальные вакцины 60 РРСС 01, 60 РРСС 02 и 60 РРСС 03 соответствуют параметрам безопасности на момент получения, а также через три и шесть месяцев после получения. Таким образом, понятно, что вакцина с использованием JW-BPPCC, являющегося новым ВРРСС корейского типа согласно настоящему изобретению, соответствует требованиям безопасности.
Пример 6. Подтверждение безопасности экспериментальной вакцины
Для подтверждения важнейшего показателя безопасности живой вакцины, подопытным животным: мышам, морским свинкам и целевым животным, свиньям, вводили испытуемые вакцины и оценивали показатель выживаемости в течение 7 или 21 суток. Для введения животным использовали вакцины 60 РРСС 01, 60 РРСС 02 и 60 РРСС 03, полученные в примере 5.3, экспериментальные вакцины вводили подопытным и целевым животным в момент изготовления, через три и шесть месяцев после изготовления, затем наблюдали за показателями выживаемости.
6.1 Подтверждение безопасности испытуемой вакцины на мышах
8 мышей массой 15-20 г
Результаты показаны в таблице 14.
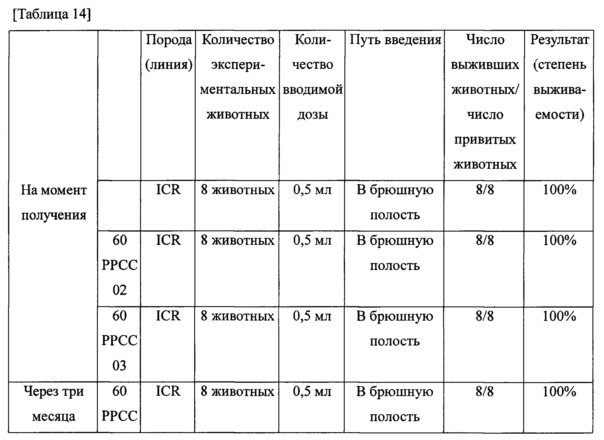
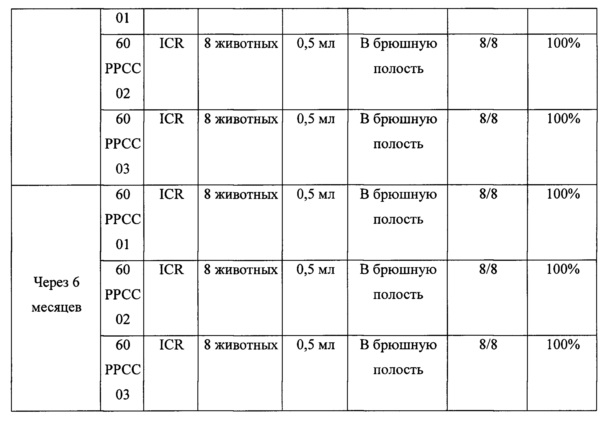
Как показано в таблице 14, все особи, которых прививали экспериментальной вакциной, выжили, таким образом подтверждено, что предложенная вакцина может быть безопасным кандидатом в вакцины.
6.2 Подтверждение безопасности экспериментальной вакцины на морских свинках
Использовали четырех морских свинок массой 300-350 г, двум морским свинкам вводили по 2 дозы экспериментальных вакцин внутримышечно или подкожно, а другим морским свинкам вводили по 2 дозы экспериментальных вакцин в брюшную полость (на момент получения, через три месяца, через шесть месяцев с момента получения), наблюдение осуществляли в течение 7 дней. Результаты показаны в таблице 15.
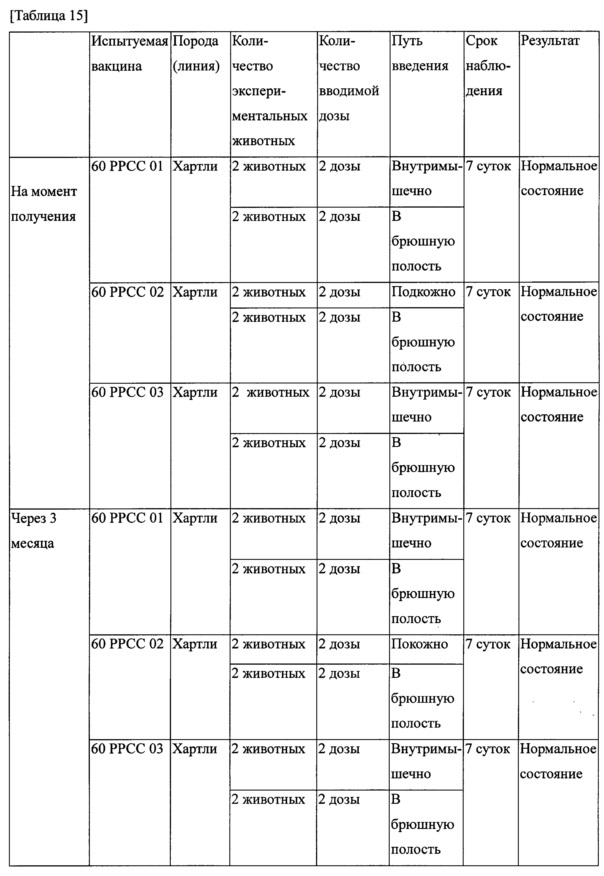
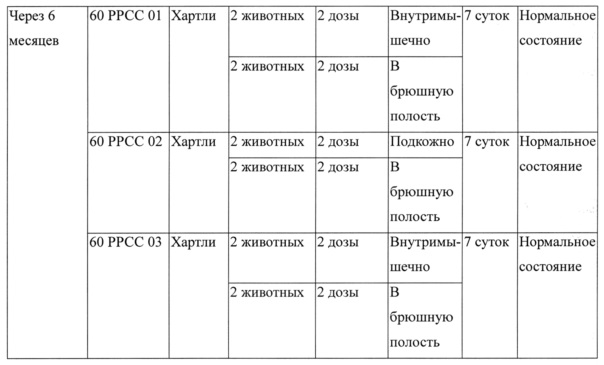
Как показано в таблице 15, группы животных, которым вводили экспериментальные вакцины, остались живыми без проявления отклонений от нормального состояния в течение 7 дней, и, таким образом подтверждена безопасность кандидата в вакцины.
6.3 Подтверждение безопасности экспериментальной вакцины на поросятах
Безопасность экспериментальной вакцины (на момент изготовления, после трех и шести месяцев после изготовления подтверждена на целевых животных, поросятах. 10 доз вводили 18 здоровым свиньям, показавшими отрицательный результат на наличие антител к ВРРСС, имеющих вес 8-10 кг (возраст 4-6 недель), наблюдение осуществляли течение 21 суток.
Результаты показаны в таблице 16.
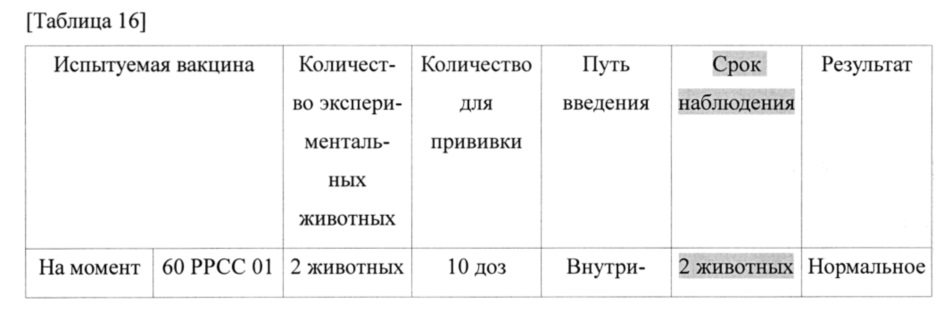
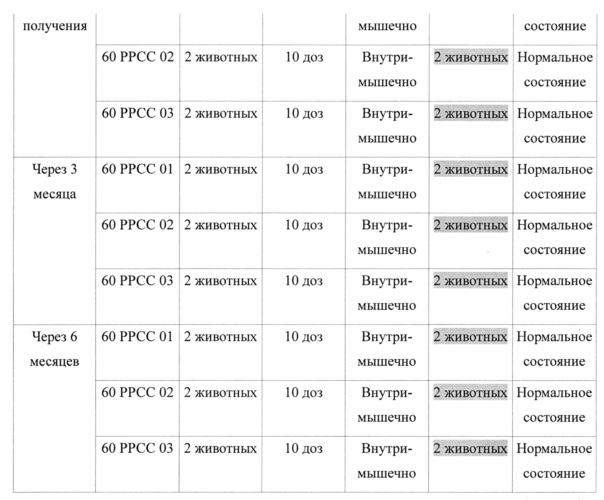
Как показано в таблице 16, у поросят не выявлено реакции гиперчувствительности в течение 1-2 часов после прививки, и подтверждено, что во время наблюдения в течение 21 суток, все поросята остались живыми без проявлений побочных эффектов, таких как нагноение в месте прививки, некроз, лихорадка и диарея. Таким образом, понятно, что экспериментальная вакцина согласно настоящему изобретению является безопасной и пригодна для вакцинации свиней против РРСС.
Пример 7. Подтверждение безопасности экспериментальной вакцины на поросятах, свободных от специфической инфекции
После введения целевым животным экспериментальной вакцины, полученной в примере 5, в высокой концентрации, установлено наличие инфицирующего вируса в крови и тканях, при введении последовательных пассажей вируса целевым животным факт реверсии вируса к исходному типу или восстановления патогенности не установлен. Начиная с первичной прививки двум свиньям, являющимся специфически свободными от вируса, внутримышечно вводили по 2 мл аттенуированного JW-BPPCC 120-го пассажа в концентрации 2×106 БОЕ/мл, затем подтверждали наличие инфицирующего вируса в крови, легких (после вскрытия животного), миндалинах и лимфе через 1, 3 и 7 суток. Возраст, масса, история пассирования вирусов и график исследования привитых животных приведены в таблице 17, результаты инфицирования вирусом, соответствующие графику исследования, показаны в в таблице 18.
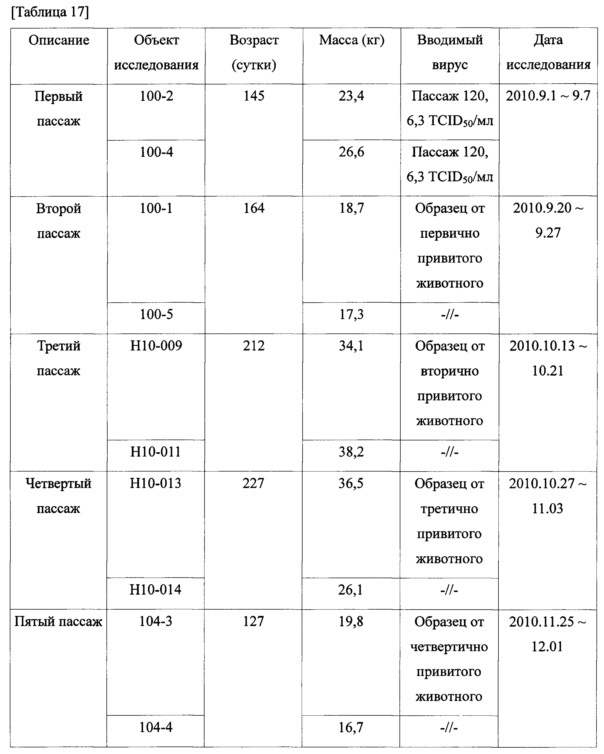
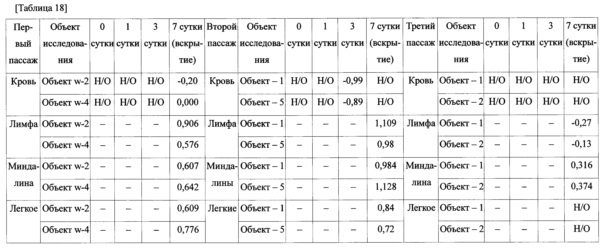
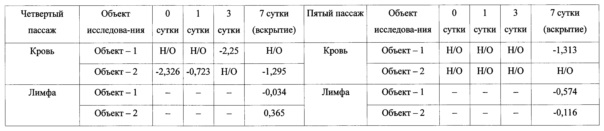
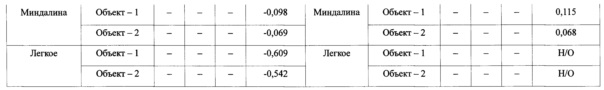
Как показано в таблице 18, с первого по пятое пассирование на целевых животных, согласно результатам измерения титра вируса в крови и тканях, после пассирования в культуре и до пятой прививки, в крови вирус не обнаружен.
В тканях наличие вируса показано в низких титрах, и в течение 5 пассажей отсутствовали увеличение количества, передача вируса и клинические симптомы (*Н/О, не обнаружено). Более того, в результате наблюдения от введения вируса до вскрытия, было подтверждено, что все животные оставались живыми без проявления побочных эффектов, таких как нагноение в месте введения, некроз, лихорадка и диарея.
Пример 8. Подтверждение выделения вируса
Как правило, при первой прививке живой вакциной, выделение вируса противовирусной вакцины наблюдается от 3 до 5 недель. Так как противовирусная вакцина не приводит к симптомам, выражающих отклонение от нормального состояния, проблематичным могут оказаться побочные проявления живого вирулентного вируса, выделяемого вакциной. Время выделения вируса кандидата в вакцины, относящегося к настоящему изобретению, исследовали и сравнивали относительно существующей коммерческой вакцины. Экспериментальные группы были разделены на группу, привитых MLV вакциной (А), группу, привитых 5-м пассажем JW-BPPCC (В), и группу, привитых 120-м пассажем JW-BPPCC (С); через 7, 12, 15, 19, 22, 26, 29, 33 и 36 суток после прививки и через 0, 7, 14, 21, 29, 35 и 42 суток после заражения отбирали образцы из носа животных, и исследовали выделение вируса в каждой группе методом ПЦР с использованием специфичных к вирусу праймеров. В качестве праймеров использовали последовательность, представленную в таблице 19. ПЦР проводили стандартным способом с определением результата в 1% агарозном геле.

Результат показан на фигуре 8.
Как показано на фиг. 8, было установлено, что в группе привитых вакциной MLV (GA), выделение вируса обнаружено до 12 суток с момента введения вакцины, и выделение вируса обнаружено до 28 суток с момента заражения. Напротив, в группе животных, привитых 120 пассажем JW-BPPCC (Группа С), выделения вируса не обнаружено в течение этапа вакцинации и после инфицирования исходным вирусом. Данный факт означает, что разработанная противовирусная вакцина демонстрирует быстрое выделение вируса по сравнению с существующей коммерческой вакциной против РРСС. При длительном выделении вируса происходит несколько процессов воспроизводства, и токсичность вируса восстанавливается при рекомбинации, поэтому появляется новый вирус, который может возвратиться к патогенному штамму. Таким образом, вакцина согласно настоящему изобретению, как ожидается, решит проблему существующей вакцины против вируса РРСС благодаря быстрому выделению вируса.
Реферат
Предложены композиция вакцины для предотвращения репродуктивно-респираторного синдрома свиней корейского типа, содержащая вирус репродуктивно-респираторного синдрома свиней (РРСС) корейского типа (номер доступа в КСТС 12096 ВР) в количестве от 2×10до 2×10БОЕ/мл в качестве эффективного ингредиента, способ предотвращения РРСС корейского типа, использующий такую вакцину, набор для диагностики вируса РРСС корейского типа и способ обнаружения вируса РРСС корейского типа. Вирус РРСС корейского типа JW-BPPCC (КСТС 12096 ВР) выделен в Корее и отличается от североамериканских и европейских штаммов. Изобретения позволяют предотвращать РРСС корейского типа, а также обеспечивают специфичную диагностику инфицирования вирусом РРСС корейского типа. 4 н. и 4 з.п. ф-лы, 8 ил., 19 табл., 8 пр.

Комментарии