Днк-вакцины против опухолевого роста и способы ихприменения - RU2343195C2
Код документа: RU2343195C2
Чертежи
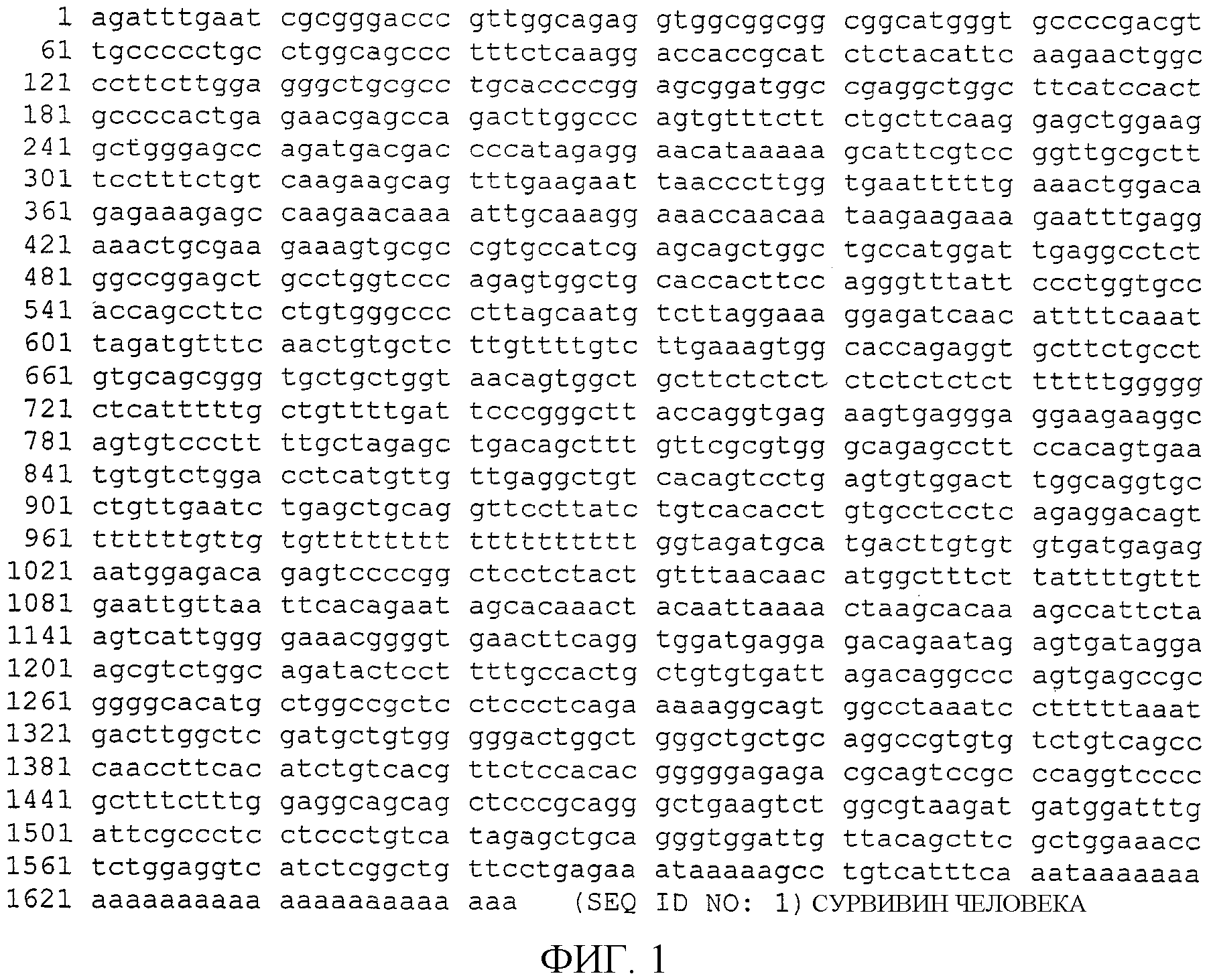






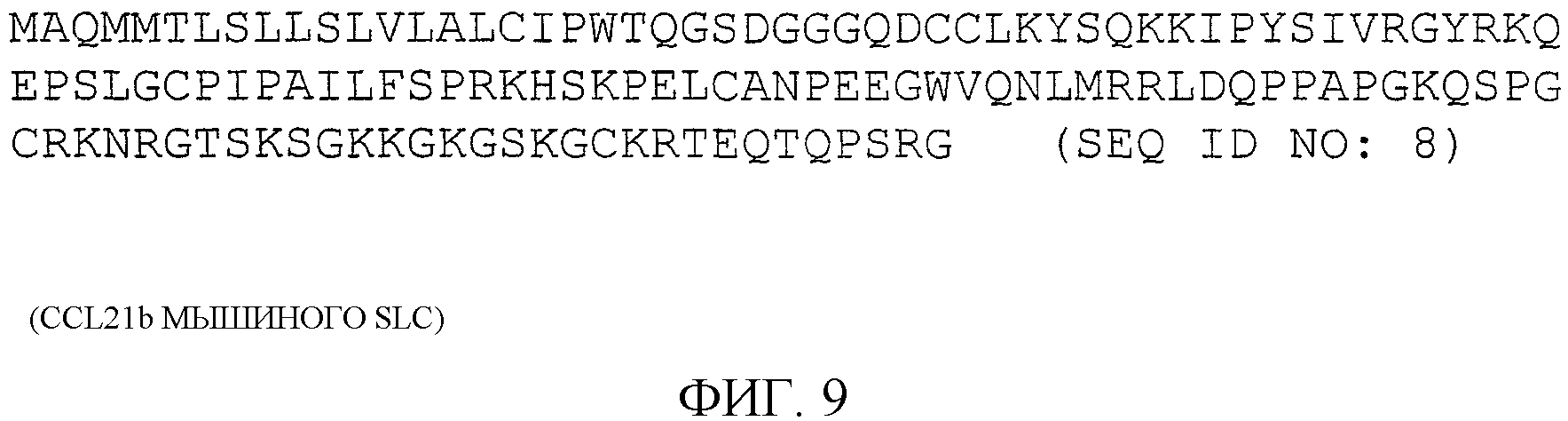























Описание
Перекрестная ссылка на родственные патентные заявки
Патентная заявка испрашивает приоритет предварительной заявки на патент США № 60/457009, поданной 24 марта 2003 года, описание которой приведено здесь в качестве ссылки.
Права правительства
Изобретение было сделано при поддержке Правительства, гранты № 1R01CA83856-01 и CA83856 National Institutes of Health, грант № 9RТ00-17 Tobacco Related Disease Research Program и гранты № DAMD17-02-1-0137 и DAMD17-02-1-0562 Department of Defense. Правительство имеет определенные права на изобретение.
Область техники, к которой относится изобретение
Изобретение относится к вакцинам дезоксирибонуклеиновой кислоты (ДНК), кодирующей молекулы, эффективные для активации иммунного ответа против опухолевых клеток. Более подробно, изобретение относится к ДНК-вакцинам, кодирующим белок семейства ингибиторов апоптоза (IAP), связанный с опухолеобразованием, и иммуноактивный генный продукт. Изобретение также относится к способам применения ДНК-вакцин для ингибирования роста опухоли.
Уровень техники изобретения
Вакцины использовали для долговременной защиты при множестве болезненных состояний путем весьма ограниченного введения профилактического средства, которое стимулирует иммунную систему организма и, таким образом, обезвреживает болезнетворные патогены до того, как они смогут начать пролиферацию и вызвать патологический эффект. Различные подходы к вакцинам и вакцинациям описаны Bernard R. Glick и Jack J. Pasternak, Molecular Biotechnology, Principles and Applications of Recombinant DNA, Second Edition, ASM Press pp. 253-276 (1998).
Вакцинация является способом стимуляции иммунной системы организма, направленным на обнаружение и уничтожение инфицирующего агента до того, как он вызовет патологический ответ. Как правило, вакцины являются либо живыми, но аттенуированными, инфекционными агентами (вирус или бактерии), либо мертвой формой агента. Вакцина, состоящая из живых бактерий или вируса, должна быть непатогенной. Как правило, бактериальная или вирусная культура аттенуирована (ослаблена) физической или химической обработкой. Хотя агент не является вирулентным, он все же может вызвать иммунный ответ у пациента, которому проводят вакцинацию.
Иммунный ответ вызывается антигенами, которые могут быть либо специфическими макромолекулами, либо инфекционными агентами. Эти антигены, как правило, представляют собой либо белки, полисахариды, липиды или гликолипиды, которые распознаются лимфоцитами, известными как B-клетки и T-клетки, как "чужеродные". Действие обоих типов лимфоцитов на антиген вызывает быстрое клеточное деление и дифференцировку, что приводит к образованию клонов коммитированных лимфоцитов. Из В-клеток образуются плазматические клетки, которые, в свою очередь, продуцируют белки, названные антителами (Ат), которые селективно связываются с антигенами инфекционного агента, таким образом, нейтрализуя или инактивируя патоген (гуморальный иммунитет). В некоторых случаях для B-клеточного ответа необходима помощь CD4 хелперных Т-клеток.
Специализированный T-клеточный клон, который формируется в ответ на антиген, представляет собой цитотоксические T-лимфоциты (CTL), которые способны связываться с патогенами и удалять патогены и ткани, в которых присутствует антиген (клеточный иммунитет). В некоторых случаях антигенпрезентирующая клетка (APC), такая как дендритная клетка, поглощает патоген или другую чужеродную клетку посредством эндоцитоза. APC затем процессируют антигены клеток и презентируют их в виде комплекса молекула гистосовместимости:пептид для Т-клеточного рецептора или CTL, таким образом, стимулируя иммунный ответ.
Гуморальный иммунитет, характеризующийся образованием специфических антител, в основном, наиболее эффективен против острых бактериальных инфекций и повторных вирусных инфекций, тогда как клеточно-опосредованный иммунитет наиболее эффективен против вирусной инфекции, хронической внутриклеточной бактериальной инфекции и грибковой инфекции. Также известно, что клеточный иммунитет оказывает противоопухолевую защиту и отвечает за отторжение трансплантатов органов.
Антитела к антигенам предшествующих инфекций определяются в крови в течение очень длительного периода времени, таким образом, позволяя определить, подвергался ли организм воздействию патогена ранее. После повторного воздействия того же патогена иммунная система эффективно предотвращает развитие повторной инфекции, устраняя патогенный агент до начала его пролиферации и возникновения патогенной реакции.
Такой же иммунный ответ, который может быть вызван патогеном, может также иногда вызывать непатогенный агент, который презентирует тот же антиген, что и патоген. Таким образом, индивидуума можно защитить от следующего воздействия патогена без предварительно перенесенной инфекции.
Тем не менее, не все инфекционные агенты могут быть легко культивированы и инактивированы, как это необходимо при получении вакцины. Современные методики рекомбинантной ДНК позволили разработать новые вакцины, с целью преодоления этих ограничений. Можно создать инфекционные агенты без патогенных генов, что, таким образом, позволяет использовать в качестве вакцины живую, невирулентную форму организма. Также возможно сконструировать относительно непатогенный организм, такой как E.coli, чтобы презентировать на поверхности клеток антигены патогенного носителя. Иммунную систему индивидуума, вакцинированного таким трансформированным носителем, «обманывают», и она образует антитела к патогену. Антигенные белки патогенного агента могут быть сконструированы и экспрессированы в непатогенных видах, и антигенные белки могут быть выделены и очищены с получением «субъединичной вакцины». Преимуществом субъединичной вакцины является ее стабильность, безопасность и возможность определения химически; однако ее производство может быть дорогостоящим.
В последние годы появился новый подход к вакцинам, названный генетической иммунизацией. В этом подходе ген, кодирующий антиген патогенного агента, операбельно встраивают в клетки индивидуума, который должен быть иммунизирован. Обработанные клетки, предпочтительно антиген-презентирующие клетки (APC), такие как дендритные, трансформируются и продуцируют антигенные белки патогена. Такие получаемые in vivo антигены затем вызывают необходимый иммунный ответ в организме хозяина. Генетическим материалом, используемым в таких генетических вакцинах, может быть конструкция либо РНК, либо ДНК. Часто полинуклеотид, кодирующий антиген, вводят в сочетании с другими промоторными полинуклеотидными последовательностями, чтобы усилить встраивание, репликацию или экспрессию гена.
ДНК-вакцины, кодирующие гены антигенов, можно вводить в клетки-хозяева с помощью различных систем доставки. Эти системы доставки включают в себя прокариотические и вирусные системы доставки. Например, один из подходов состоит в использовании вирусного вектора, такого как вирус коровьей оспы, с введенным новым генетическим материалом, для инокуляции клеток-хозяев. Альтернативно, генетический материал может быть встроен в плазмидный вектор или может быть доставлен непосредственно в клетки-хозяева как «голый» полинуклеотид, то есть просто как очищенная ДНК. Кроме того, ДНК может быть стабильно трансфецирована в аттенуированные бактерии, такие как Salmonella typhimurium. Когда пациент перорально принимает вакцину с трансформированными Salmonella, бактерии транспортируются к пейеровым бляшкам в кишечнике (то есть вторичным лимфоидным тканям), которые затем стимулируют иммунный ответ.
С помощью ДНК-вакцин можно проводить иммунизацию против болезненных состояний, которые вызваны нетипичными патогенами, например против генетических заболеваний и рака. Как правило, генетическая вакцина против рака встраивается в ген APC, который кодирует антиген, и, таким образом, трансформированные APC продуцируют антигены к определенному типу опухолевых клеток. С помощью эффективной универсальной вакцины против большого количества типов рака, таким образом, можно создать большое количество индивидуальных вакцин для каждого типа раковой клетки, против которой необходима иммунизация.
Белки-ингибиторы апоптоза (то есть белки семейства IAP) представляют собой класс природных антигенов, экпрессирующихся в большом количестве различных опухолевых клетках. Как следует из названия, эти белки, в их природной форме, ингибируют апоптоз (то есть запрограммированную гибель клетки), что, в свою очередь, может привести к устойчивости раковых клеток к апоптозу, вызванному химиотерапевтическими агентами, такими как этопозид. Примеры белков семейства IAP включают в себя сцепленный с X-хромосомой IAP (XIAP), NAIP, cIAP1 (также известный как BIRC2), cIAP2 (также известный как BIRC3), Bruce (также известный как BIRC6), сурвивин (также известный как BIRC5) и ливин (также известный как BIRC7, KIAP и ML-IAP). Белки семейства IAP млекопитающих включают в себя белки с тремя доменами BIR (например, XIAP, cIAP1, cIAP и NAIP), а также белки с одним доменом BIR (например, сурвивин и ливин).
В публикации Tamm et al. Cancer Res. 1998; 58 (23):5315-20 сообщалось об экспрессии сурвивина человека в 60 опухолевых клеточных линиях человека. Tamm с соавторами также сообщали, что как сурвивин, так и XIAP эффективны при ингибировании запрограммированной клеточной гибели (апоптоза), вызванной обработкой опухолевых клеток вызывающими апоптоз агентами, такими как Bax или Fas (CD95). Сурвивин и другие белки семейства IAP, по имеющимся данным, ингибируют апоптоз, связываясь с протеазами клеточной гибели эффекторных клеток, например с каспазой-3 и каспазой-7. Мутации белков семейства IAP могут привести к снижению ингибирующей апоптоз активности или даже к вызывающей апоптоз активности по сравнению с активностью белка семейства IAP дикого типа. Противоапоптотическая активность белков семейства IAP, как полагают, связана с доменом BIR.
Сообщалось, что сурвивин присутствует в раковых клетках наиболее распространенных онкологических заболеваний человека, включая рак легкого, простаты, молочной железы и поджелудочной железы. Сурвивин также был обнаружен в клетках неходжкинской лимфомы высокой степени злокачественности, но не был обнаружен в неходжкинских лимфомах низкой степени злокачественности. Сообщалось, что сурвивин присутствует в нормальных клетках во время эмбрионального развития, но, в отличие от большинства других белков семейства IAP, сурвивин фактически не определяется в нормальных тканях взрослого человека. См. Ambrosini et al. Nat. Med. 1997; 3(8): 917-21.
Ливин был обнаружен в некоторых тканях взрослого человека и в эмбриональных тканях. Сообщалось, что уровни экспрессии ливина повышаются в меланомах, раковых клетках толстой кишки, раковых клетках мочевого пузыря и раковых клетках легкого. Также сообщалось о двух сплайсированных вариантах ливина, которые оба содержат один домен BIR. Полноразмерный вариант альфа состоит из 298 аминокислотных остатков, а вариант бета состоит из 280 аминокислотных остатков.
Белки семейства IAP также были идентифицированы в большом количестве видов организмов помимо людей, включая млекопитающих, таких как мыши, амфибий, таких как виды Xenopus (африканские шпорцевые лягушки), насекомых, таких как виды Drosophila, и бакуловирусы.
Повсеместная и высокоселективная природа экспрессии сурвивина в раковых клетках делает его потенциально применимым диагностическим маркером рака. Например, Rohayem et al. Cancer Res. 2000; 60: 1815-17 было сообщено об идентифицировании аутоантитела к сурвивину у больных раком легкого человека и колоректальным раком.
Сурвивин также был идентифицирован как мишень для терапии рака. Ингибирующий эффект сурвивина на каспазу-3 и каспазу-7 связан с резистентностью раковых клеток к различным стимулирующим апоптоз химиотерапевтическим методикам лечения. Антисмысловой олигонуклеотид, который предназначен для воздействия на экспрессию сурвивина, как сообщалось, регулирует снижение экспрессии сурвивина в клеточной линии аденокарциномы и сенсибилизирует раковые клетки к химиотерапевтическому агенту этопозиду. Смотри Olie et al. Cancer Res. 2000; 60: 2805-9 и Mesri et al.J. Clinical Res., 2001; 108: 981-990.
Цитокины представляют собой белки и полипептиды, продуцируемые клетками, которые могут влиять на поведение других клеток, такое как клеточная пролиферация, клеточная дифференцировка, регуляция иммунных реакций, кроветворение и воспалительные реакции. Цитокины классифицированы на множество семейств, включая хемокины, гемопоэтины, иммуноглобулины, факторы некроза опухоли и множество не относящихся какому-либо семейству молекул. Смотри, главным образом, Oxford Dictionary of Biochemistry and Molecular Biology, Revised Edition, Oxford University Press, 2000 и C. A. Janeway, P. Travers, M. Walport and M. Schlomchik, Immunobiology, Fifth Edition, Garland Publishing, 2001 (здесь и далее обозначаемая как Janeway и Travers). Краткая классификация цитокинов представлена в Janeway и Travers, в приложении III, страницы 677-679, соответствующие описания которых приведены здесь в качестве ссылки.
Гемопоэтины включают в себя, например, эритропоэтин, интерлейкин 2 (IL-2, белок из 133 аминокислот, продуцируемый T-клеткой и вовлеченный в T-клеточную пролиферацию), IL-3, IL-4, IL-5, IL-6, IL-7, IL-9, IL-11, IL-13, IL-15 (белок, подобный IL-2, состоящий из 114 аминокислот, который стимулирует рост кишечного эпителия, T-клеток и NK-клеток), гранулоцитарный колониестимулирующий фактор (G-CSF), гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), онкостатин М (OSM) и фактор, ингибирующий лейкемию (LIF).
Интерфероны включают в себя, например, IFN-α, IFN-β и IFN-γ (гомодимерный белок из 143 аминокислот, продуцируемый T-клетками и NK-клетками, который вовлечен в активацию макрофагов, усиливает экспрессию молекул MHC и антиген-процессирующих компонентов, переключение класса IG и супрессию TH2).
Иммуноглобулины включают в себя, например, B7.1 (CD80) и B7.2 (CD86), каждый из которых совместно стимулирует T-клеточные ответы.
Семейство факторов некроза опухоли (TNF) включает в себя, например, TNF-α, TNF-β (лимфотоксин), лимфотоксин-β (LT- β), лиганд CD40, лиганд Fas, лиганд CD27, лиганд CD30, лиганд 4-1BB, Trail и лиганд OPG.
Различные цитокины, которые не относятся к какомк-либо семейству, включают в себя, например, фактор роста опухоли β (TGF-β), IL-1α, IL-1β, IL-1 RA, IL-10, IL-12 (фактор, стимулирующий природные клетки-киллеры; гетеродимер, содержащий цепь из 197 аминокислот и цепь из 306 аминокислот, который вовлечен в активацию NK-клеток и индукцию дифференцировки T-клеток в TH1-подобные клетки), фактор, ингибирующий миграцию макрофагов (MIF), IL-16, IL-17 (фактор, индуцирующий продукцию цитокина, который вызывает продукцию цитокина в эпителии, эндотелии и фибробластах) и IL-18.
Хемокины представляют собой семейство цитокинов, которые являются относительно небольшими хемоаттрактантными белками и полипептидами, которые стимулируют миграцию и активацию различных клеток, такую как миграция лейкоцитов (например, фагоцитов и лимфоцитов). Хемокины играют важную роль при воспалении и других иммунных ответах. Хемокины разделены на множество семейств, включая хемокины C, хемокины CC, хемокины CXC и хемокины CX3C. В названии указано количество остатков цистеина и расстояние между ними в молекулах; хемокины C содержат один цистеин, хемокины CC содержат два следующих друг за другом цистеина, CXC содержат два цистеина, отделенных друг от друга одним аминокислотным остатком, и хемокины CX3C содержат два цистеина, отделенных друг от друга тремя аминокислотными остатками. Хемокины взаимодействуют с большим количеством хемокиновых рецепторов, присутствующих на поверхности клеток. Смотри Janeway и Travers, приложение IV, страницу 680, соответствующие описания которых приведены здесь в качестве ссылки.
Кроме того, хемокины могут обладать иммуномодулирующей активностью и быть вовлечены в иммунные ответы при раке. Например, сообщалось, что мышиный 6Ckine/SLC, мышиный аналог хемокина вторичной лимфоидной ткани человека (SLC), в настоящее время называемый CCL21, вызывает противоопухолевый ответ в опухолевой клеточной линии карциномы толстой кишки C-26. Смотри Vicari, et al. J. Immunol. 2000; 165 (4): 1992-2000. CCL21 человека и его мышиный аналог, 6Ckine/SLC, относятся к хемокинам СС, которые взаимодействуют с хемокиновым рецептором CCR7. Vicari et al. также сообщалось, что мышиный 6Ckine/SLC (muCCL21) представляет собой лиганд хемокинового рецептора CXCR3. CCL21 человека, muCCL21 мыши и множество других хемокинов вовлечены в регуляцию различных клеток иммунной системы, таких как дендритные клетки, T-клетки и природные клетки-киллеры (NK).
Mig и IP-10 относятся к хемокинам CXC, которые взаимодействуют с рецептором CXCR3, ассоциированным с активированными T-клетками. Лимфотактин представляет собой хемокин C, который взаимодействует с рецептором XCR1, ассоциированным с T-клетками и NK-клетками. Фракталкин представляет собой хемокин CX3C, который взаимодействует с рецептором CX3CR1, ассоциированным с T-клетками, моноцитами и нейтрофилами.
NK-клетки представляют собой большие гранулярные лимфоциты, которые распознают и уничтожают клетки, зараженные вирусом. Регуляция NK-клеток может осуществляться посредством взаимодействия иммуномодулирующих полипептидных лигандов с рецепторами на поверхности NK-клетки. Например, лиганды рецептора NKG2D, которые могут регулировать активность NK-клетки, включают в себя хемокины, такие как muCCL21, и стресс-индуцируемые полипептидные лиганды, такие как антигены, связанные с цепью MHC I класса, и белки, связывающие UL16. Сообщалось, что мышиный антигенный пептид минорного комплекса гистосовместимости H60 также связывается с рецептором NKG2D. Смотри, например, Robertson et al. Cell Immunol. 2000; 199(1): 8-14; Choi et al. Immunity 2002, 17(5): 593-603 и Farag et al., Blood, 2002; 100(6): 1935-1947.
Настоящее изобретение удовлетворяет имеющуюся потребность в вакцинах, которые могут стимулировать общий иммунный ответ против раковых клеток, предлагая ДНК-вакцину, кодирующую связанный с опухолеобразованием белок семейства IAP и иммунноактивный генный продукт в общем векторе.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ДНК-вакцина, которая эффективно вызывает иммунный ответ против раковых клеток, содержит конструкцию ДНК, операбельно кодирующую белок семейства IAP, связанный с опухолеобразованием, и иммуноактивный генный продукт в фармацевтически приемлемом носителе. Предпочтительно конструкция ДНК операбельно встроена в вектор, такой как аттенуированная бактерия (например, аттенуированный вектор Salmonella typhimurium). ДНК-вакцина включает в себя полинуклеотид, который кодирует по крайней мере один белок семейства IAP, связанный с опухолеобразованием, вместе с полинуклеотидом, который кодирует иммуноактивный генный продукт. Предпочтительно конструкция ДНК кодирует белок семейства IAP, связанный с опухолеобразованием, который, по существу, отсутствует в дефинитивных тканях, но уровень которого повышен в раковых тканях, такой как белок сурвивин (например, сурвивин человека, мышиный сурвивин и тому подобное) или белок ливин. Предпочтительно иммунореактивный генный продукт, кодируемый конструкцией ДНК, представляет собой цитокин, лиганд рецептора на поверхности природной клетки-киллера или подобную иммунореактивную молекулу.
В одном из вариантов осуществления ДНК-вакцина предпочтительно включает в себя ДНК, которая операбельно кодирует белок сурвивин, выбранный из группы, включающей (a) сурвивин человека дикого типа с аминокислотной последовательностью SEQ ID NO: 2, (b) иммуногенный гомолог сурвивина человека дикого типа, который по крайней мере на 80% идентичен аминокислотной последовательности SEQ ID NO: 2, (c) сплайсированный вариант сурвивина человека с аминокислотной последовательностью SEQ ID NO: 23, (d) сплайсированный вариант сурвивина человека с аминокислотной последовательностью SEQ ID NO: 24 и (e) фрагмент белка сурвивина, который связывается с молекулой MHC I класса и распознается цитотоксическими T-клетками.
В еще одном варианте осуществления ДНК-вакцина предпочтительно включает в себя конструкцию ДНК, которая операбельно кодирует белок ливин, выбранный из группы, включающей (a) полноразмерный сплайсированный вариант альфа ливина человека дикого типа с аминокислотной последовательностью SEQ ID NO: 27, (b) сплайсированный вариант бета ливина человека с аминокислотной последовательностью SEQ ID NO: 29, (c) иммуногенный гомолог полноразмерного ливина человека дикого типа, который по крайней мере на 80% идентичен аминокислотной последовательности SEQ ID NO: 27, (d) иммуногенный гомолог сплайсированного варианта бета ливина человека дикого типа, который по крайней мере на 80% идентичен аминокислотной последовательности SEQ ID NO: 29 и (е) фрагмент белка ливина, который связывается с молекулой MHC I класса и распознается цитотоксическими T-клетками.
Предпочтительные цитокины включают в себя хемокины, такие как CCL21 человека, CCL21 мыши, лимфотактин, фракталкин, IP-10 и тому подобные, гемопоэтины, такие как IL-2, IL-15 и тому подобные; интерфероны, такие как IFN-γ и тому подобные; а также другие цитокины, связанные с миграцией или пролиферацией Т-клеток и NK-клеток, такие как IL-12, IL-17 и тому подобные.
Предпочтительные лиганды поверхностных рецепторов природных клеток-киллеров представляют собой стресс-индуцируемые белки, такие как MICA человека, MICB человека, ULBP1 человека, ULBP2 человека, ULBP3 человека и тому подобные лиганды, которые связываются с рецептором NKG2D на поверхности клеток. Особенно предпочтительными лигандами NKG2D являются MICA и MICB.
В вакцинах также могут присутствовать общепринятые адъюванты, такие как квасцы, эмульсии типа «масло в воде», консерванты и тому подобные. ДНК-вакцины по настоящему изобретению стимулируют иммунный ответ против клеток опухоли, включая стимуляцию апоптоза опухолевых клеток, таким образом, ингибируя рост опухоли и распространение метастазов.
В одном из аспектов способа по настоящему изобретению ДНК-вакцину используют для долговременного ингибирования роста опухоли у вакцинированного пациента. ДНК-вакцину, содержащую конструкцию из полинуклеотида, операбельно кодирующего белок семейства IAP и иммуноактивный генный продукт, вместе с фармацевтически приемлемым носителем вводят (предпочтительно перорально) пациенту при необходимости ингибирования роста опухоли в количестве, которое является достаточным для активации иммунного ответа против опухолевых клеток.
Вакцины по настоящему изобретению могут использоваться для лечения различных типов раков. Например, иммунизация вакцинами по настоящему изобретению может быть эффективна у пациента, страдающего раком легких, колоректальным раком, меланомой и тому подобное.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 показана последовательность нуклеиновой кислоты, кодирующая сурвивин человека, SEQ ID NO: 1.
На фиг.2 показана аминокислотная последовательность сурвивина человека, SEQ ID NO: 2.
На фиг.3 показана последовательность нуклеиновой кислоты, кодирующая TIAP мыши, SEQ ID NO: 3.
На фиг.4 показана аминокислотная последовательность TIAP мыши, SEQ ID NO: 4.
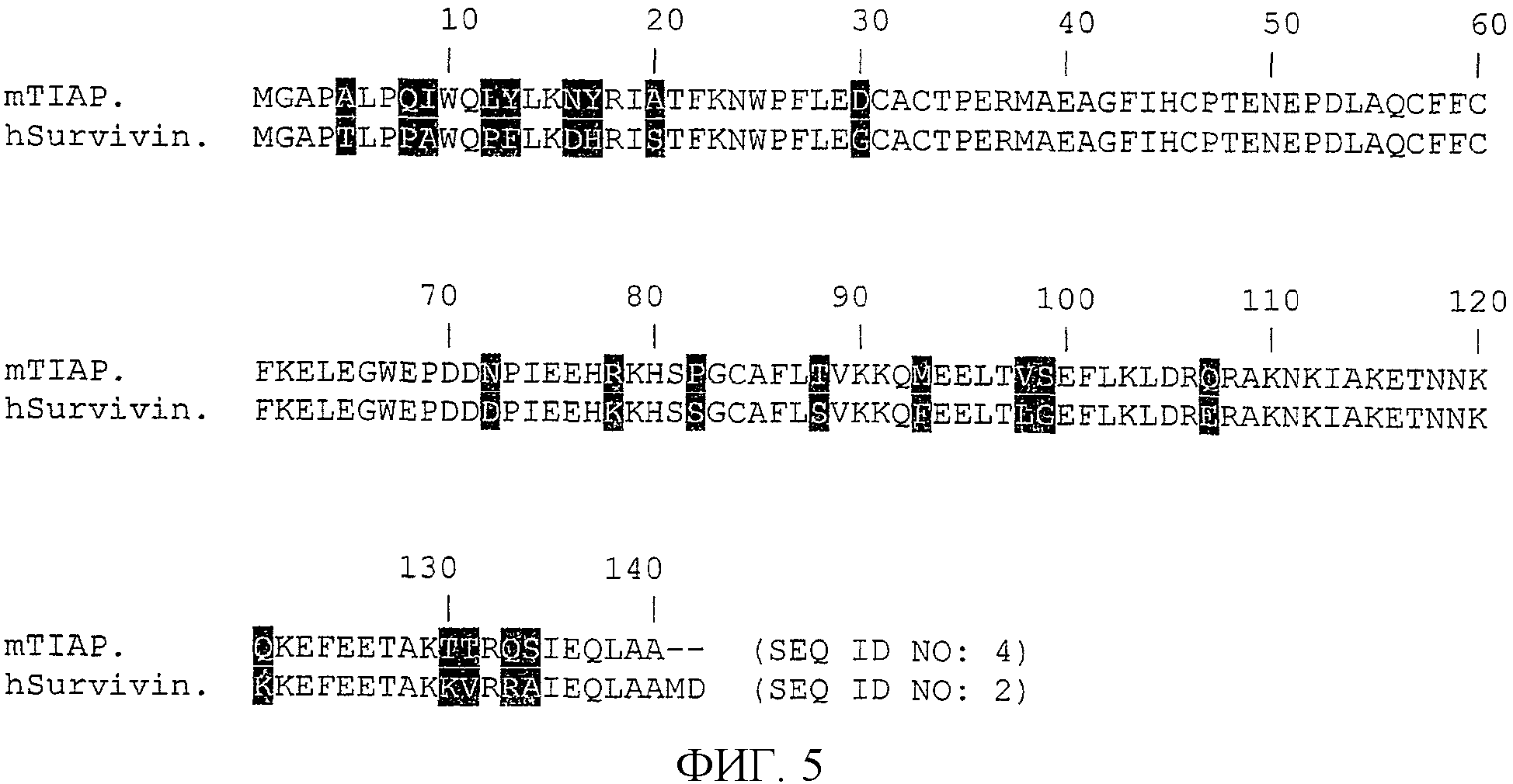
На фиг.5 показана гомология белков сурвивина человека и TIAP мыши.
На фиг.6 показана последовательность нуклеиновой кислоты, кодирующая SLC человека (CCL21), SEQ ID NO: 5.
На фиг.7 показана аминокислотная последовательность SLC человека (CCL21), SEQ ID NO: 6.
На фиг.8 показана последовательность нуклеиновой кислоты, кодирующая 6Ckine/SLC мыши (muCCL21), SEQ ID NO: 7.
На фиг.9 показана аминокислотная последовательность 6Ckine/SLC мыши (muCCL21), SEQ ID NO: 8.
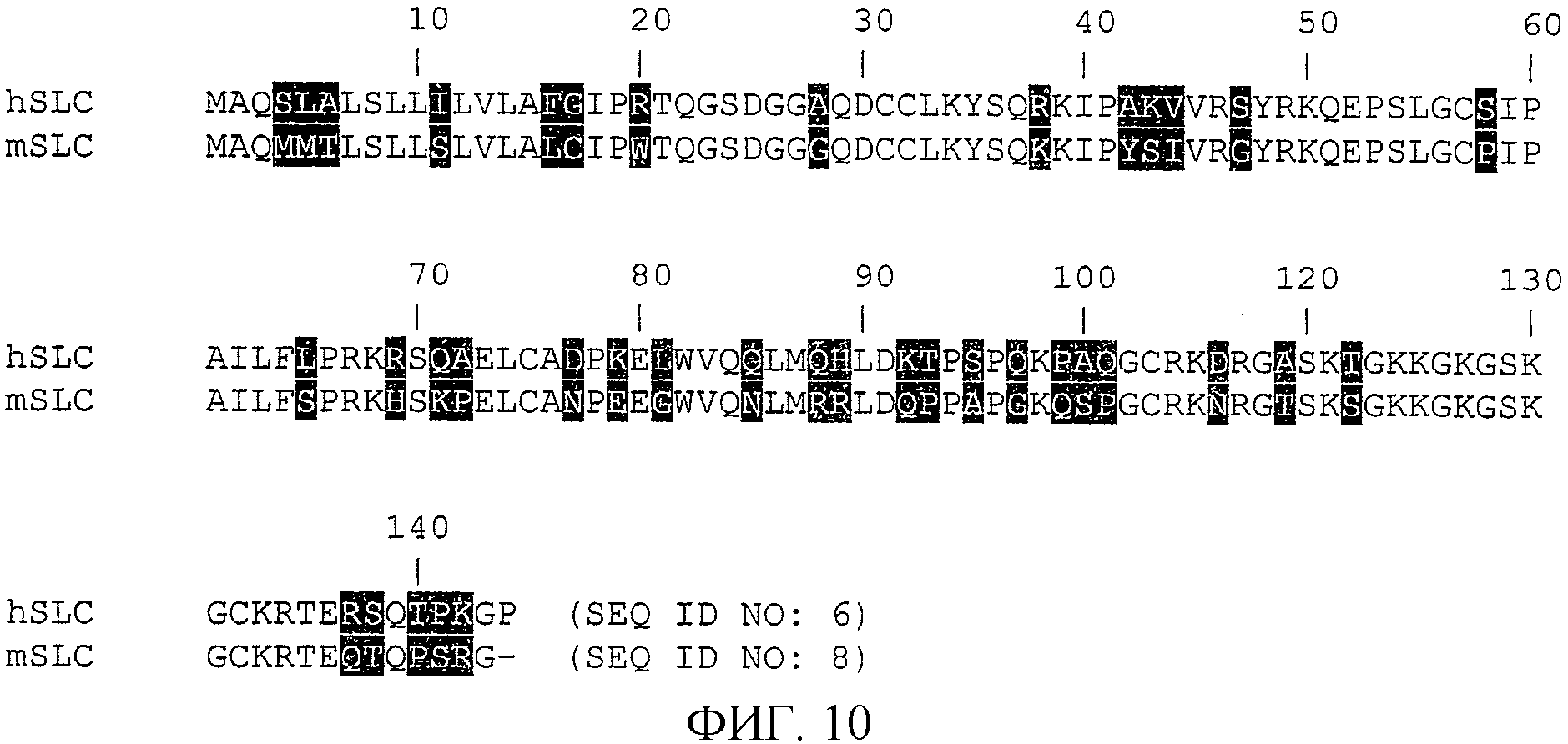
На фиг.10 показана гомология белков SLC человека (CCL21) и 6Ckine/SLC мыши (muCCL21).
На фиг.11 показана неполная последовательность нуклеиновой кислоты мышиного антигенного пептида Н60 минорного комплекса гистосовместимости, SEQ ID NO: 9.
На фиг.12 показана неполная аминокислотная последовательность мышиного антигенного пептида Н60 минорного комплекса гистосовместимости, SEQ ID NO: 10.
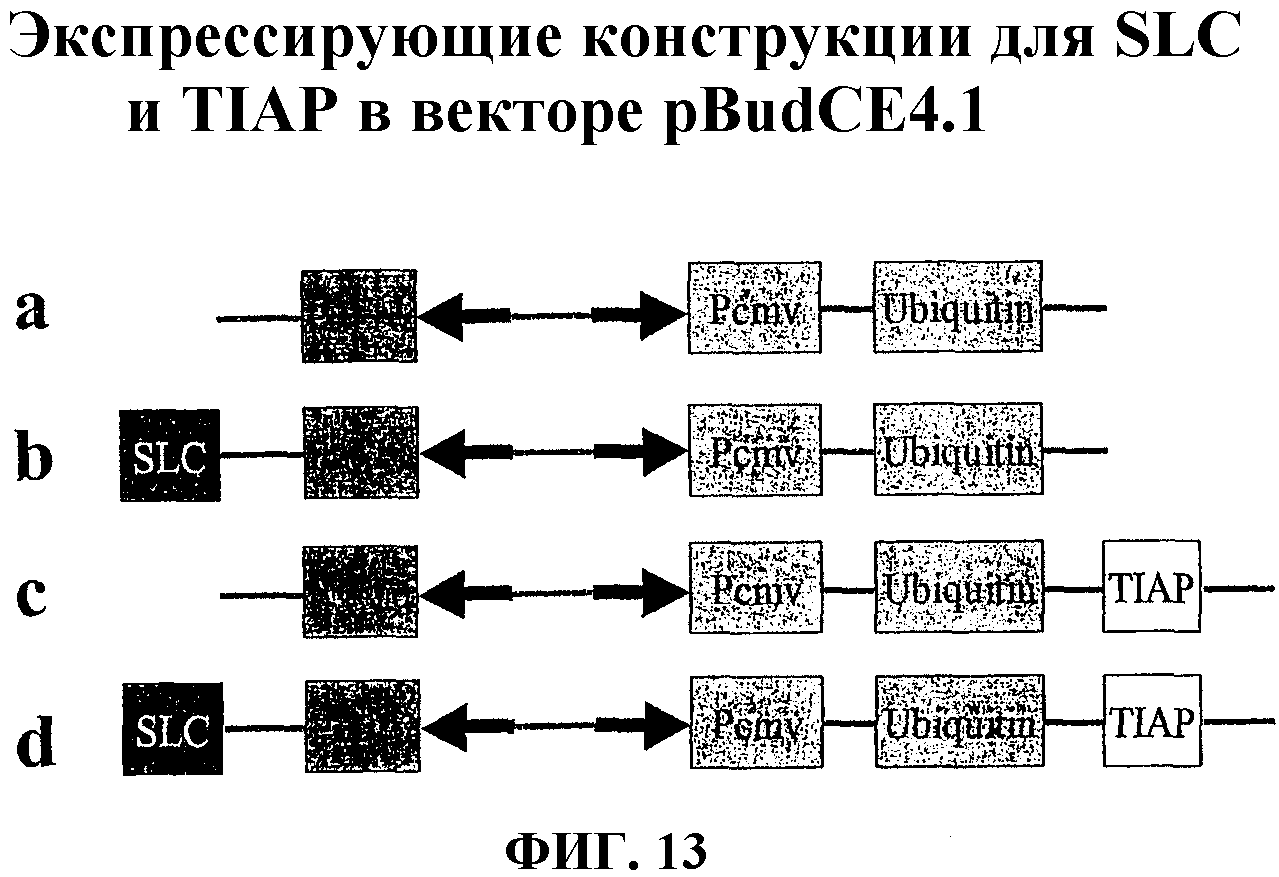
На фиг.13 представлено схематическое изображение конструкции ДНК, кодирующей белок сурвивин (сурвивин мыши, также известный как TIAP) и иммуномодулирующий хемокин (CCL21, также известный как SLC), в векторе pBudCE4.1.
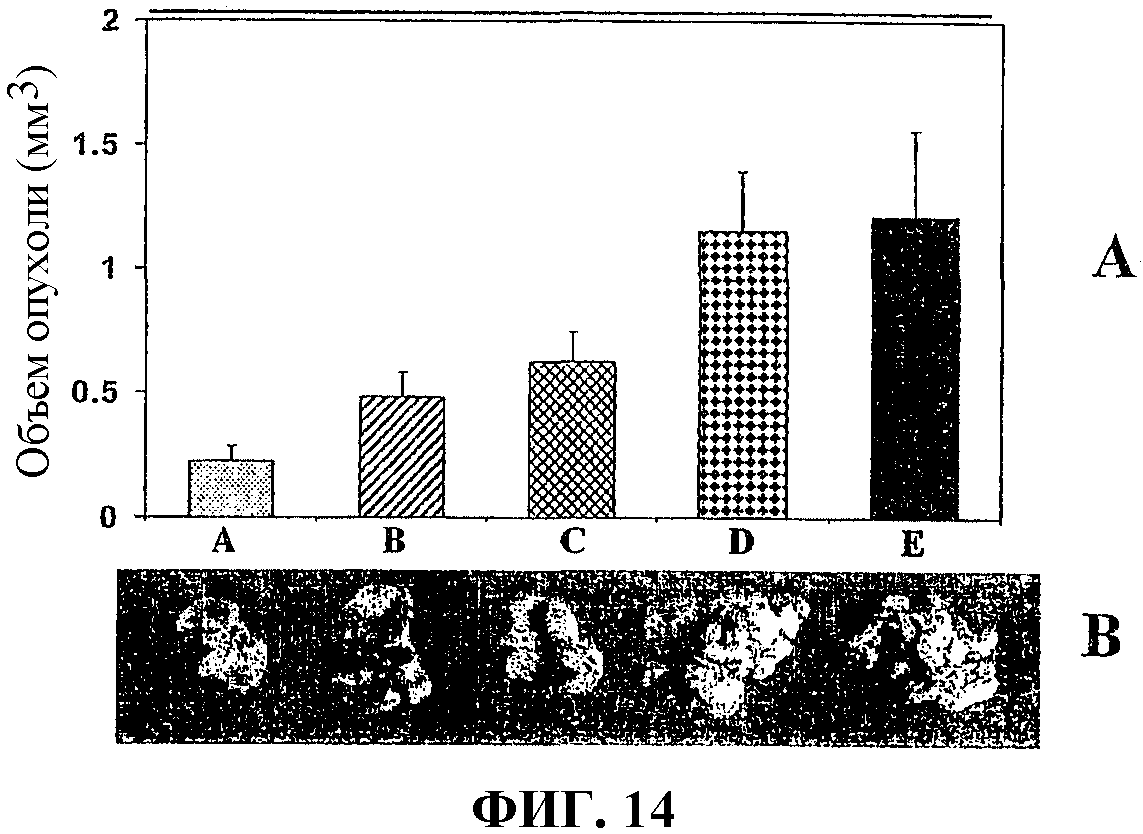
На фиг.14А графически показан средний объем легочных метастазов при карциноме легкого Льюиса у мышей, получавших контрольный буфер (Е), контрольную вакцину, содержащую пустой вектор (D), ДНК-вакцину, содержащую хемокин (С), вакцину, содержащую белок сурвивин (В), и вакцину по изобретению (А).
На фиг.14В представлено изображение типичных метастазов опухоли легкого, удаленных у мышей, вакцинированных, как описано для фиг.14А.
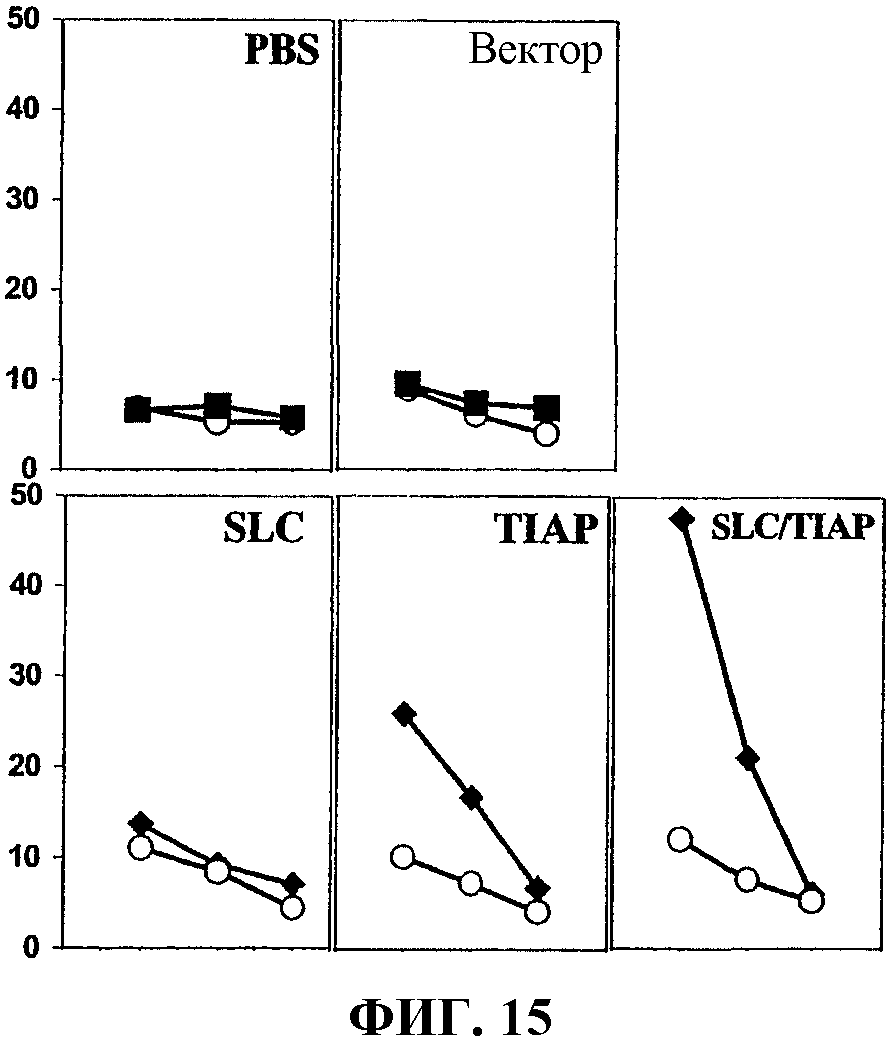
На фиг.15 показана опосредованная Т-клеткой цитотоксичность, вызванная ДНК-вакцинами, как описано для фиг.14А, против клеток рака легкого D121; процент лизиса (Y-ось) нанесен для трех различных соотношений эффекторных клеток и клеток-мишеней (E/T) для каждой вакцинации (то есть 100:1 - первая точка на графике; 50:1 - вторая точка на графике и 25:1 - третья точка на графике).
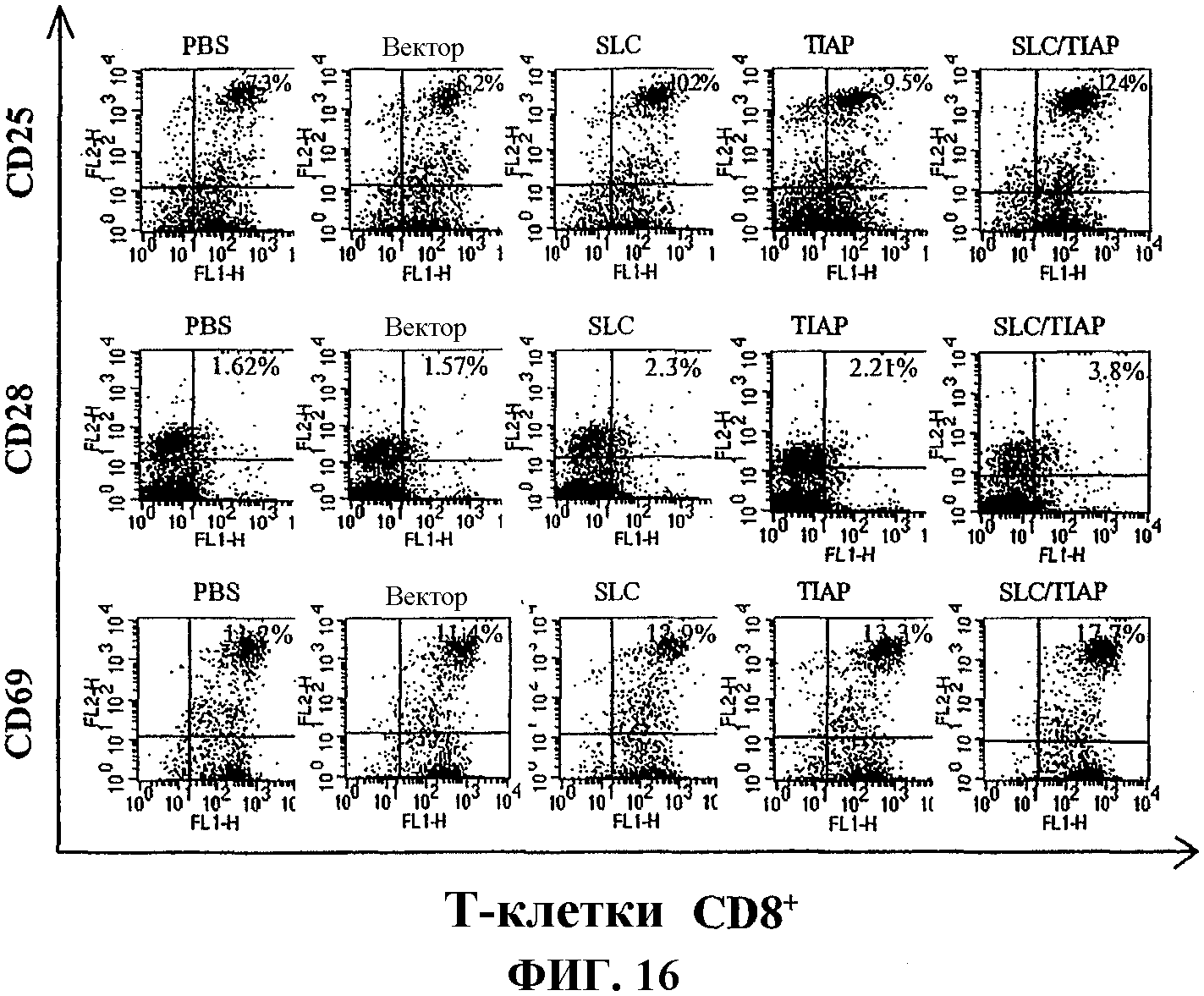
На фиг.16 графически показана повышенная экспрессия молекул активации T-клеток у мышей, вакцинированных вакциной по изобретению, определенная с помощью проточной цитометрии.
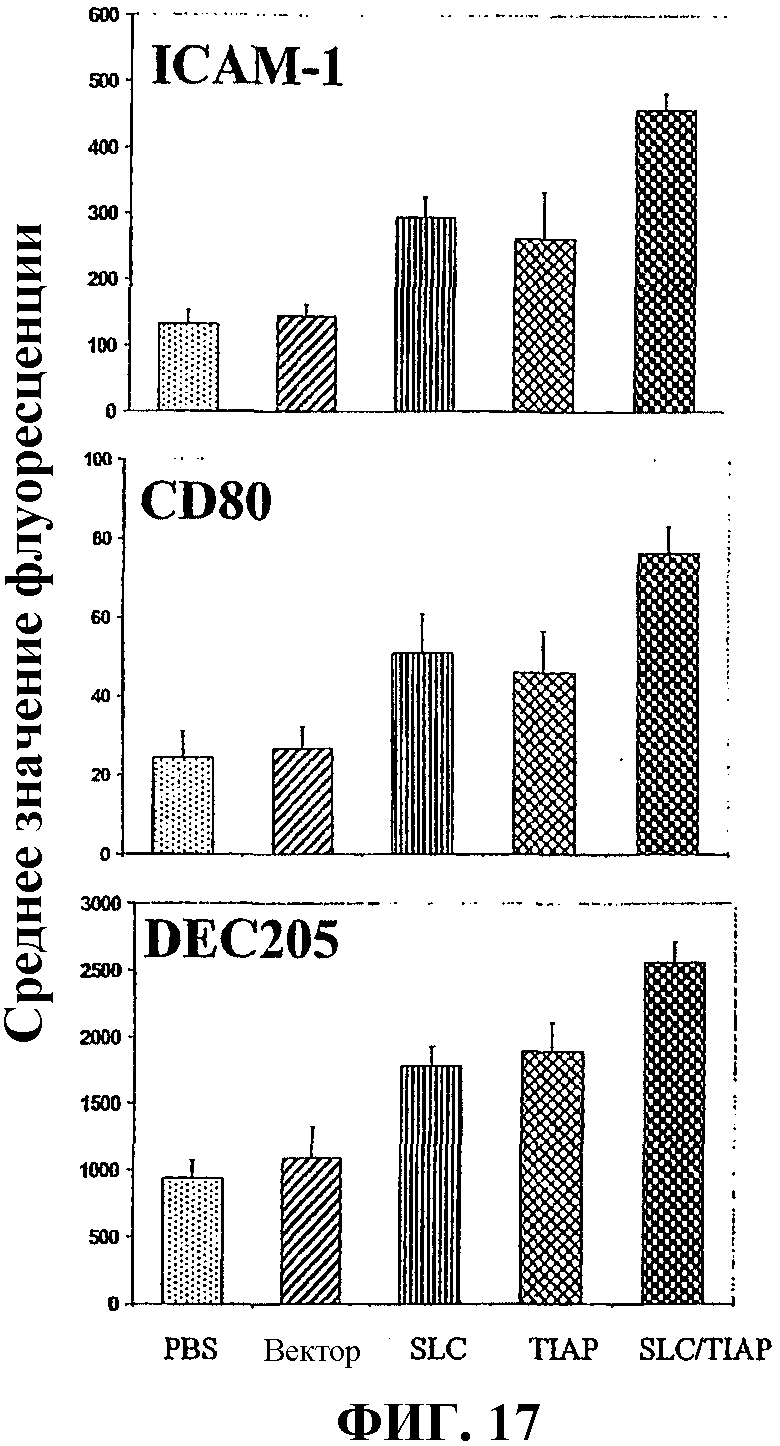
На фиг.17 графически показана повышенная экспрессия совместно стимулирующихся молекул дендритными клетками после вакцинации мышей вакциной по изобретению и различными контрольными вакцинами.
На фиг.18 показана индукция высвобождения внутриклеточных цитокинов после вакцинации мышей вакциной по изобретению и различными контрольными вакцинами, определенная с помощью проточной цитометрии.
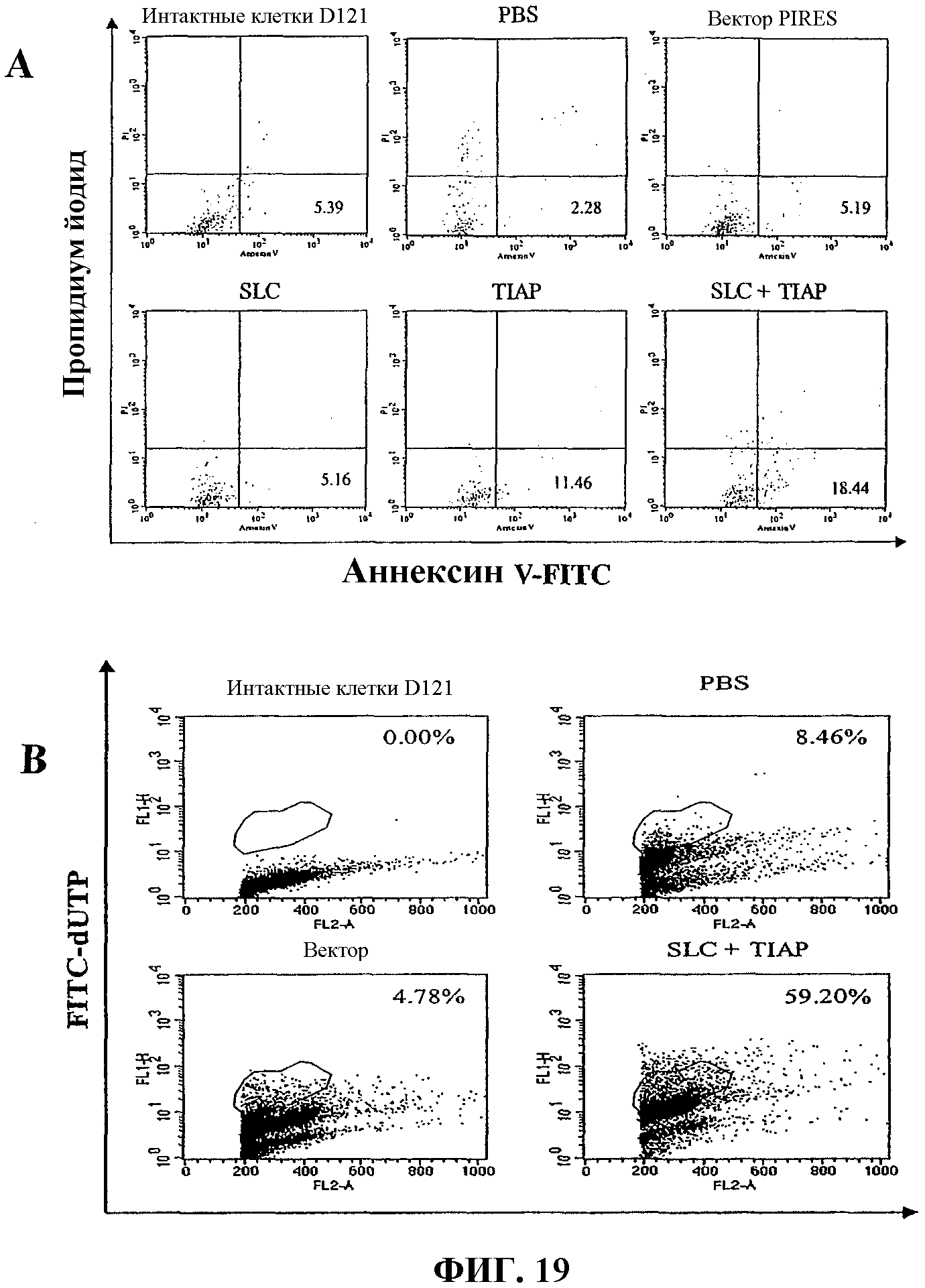
На фиг.19 показаны графики FACS, демонстрирующие увеличение апоптоза клеток опухоли легкого D121 после вакцинации мышей вакциной по изобретению и различными контрольными вакцинами (A) через 3 часа после вакцинации и (B) через 24 часа после вакцинации.
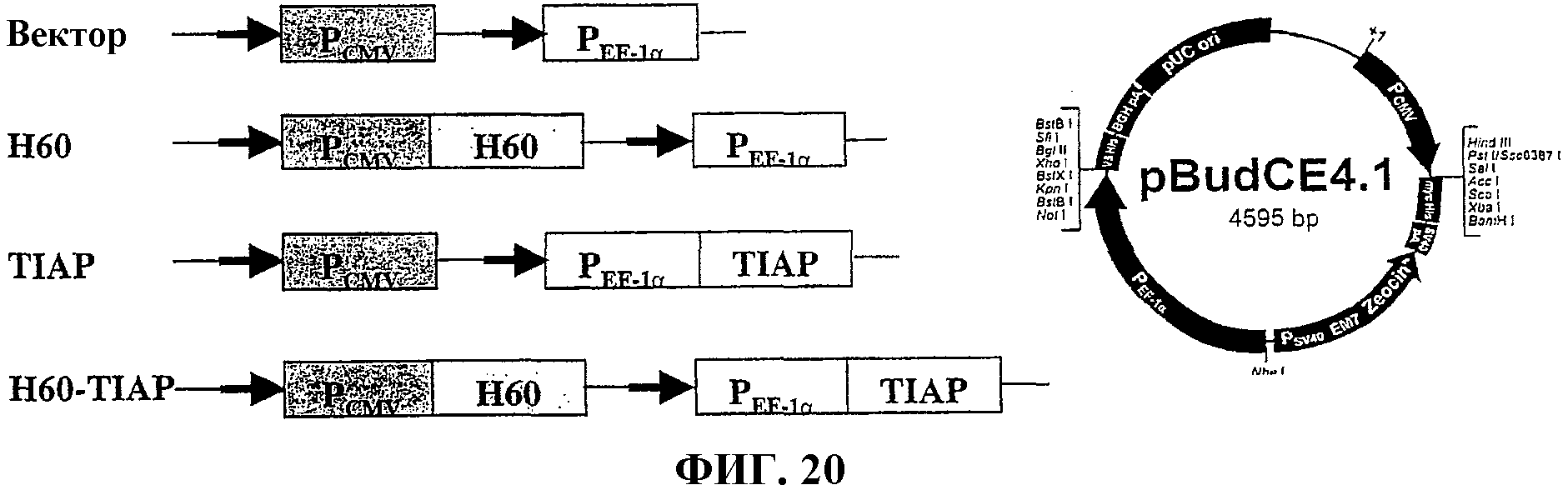
На фиг.20 показано схематическое изображение экспрессии конструкции, содержащей TIAP и антигенный пептид Н60 минорного комплекса гистосовместимости.
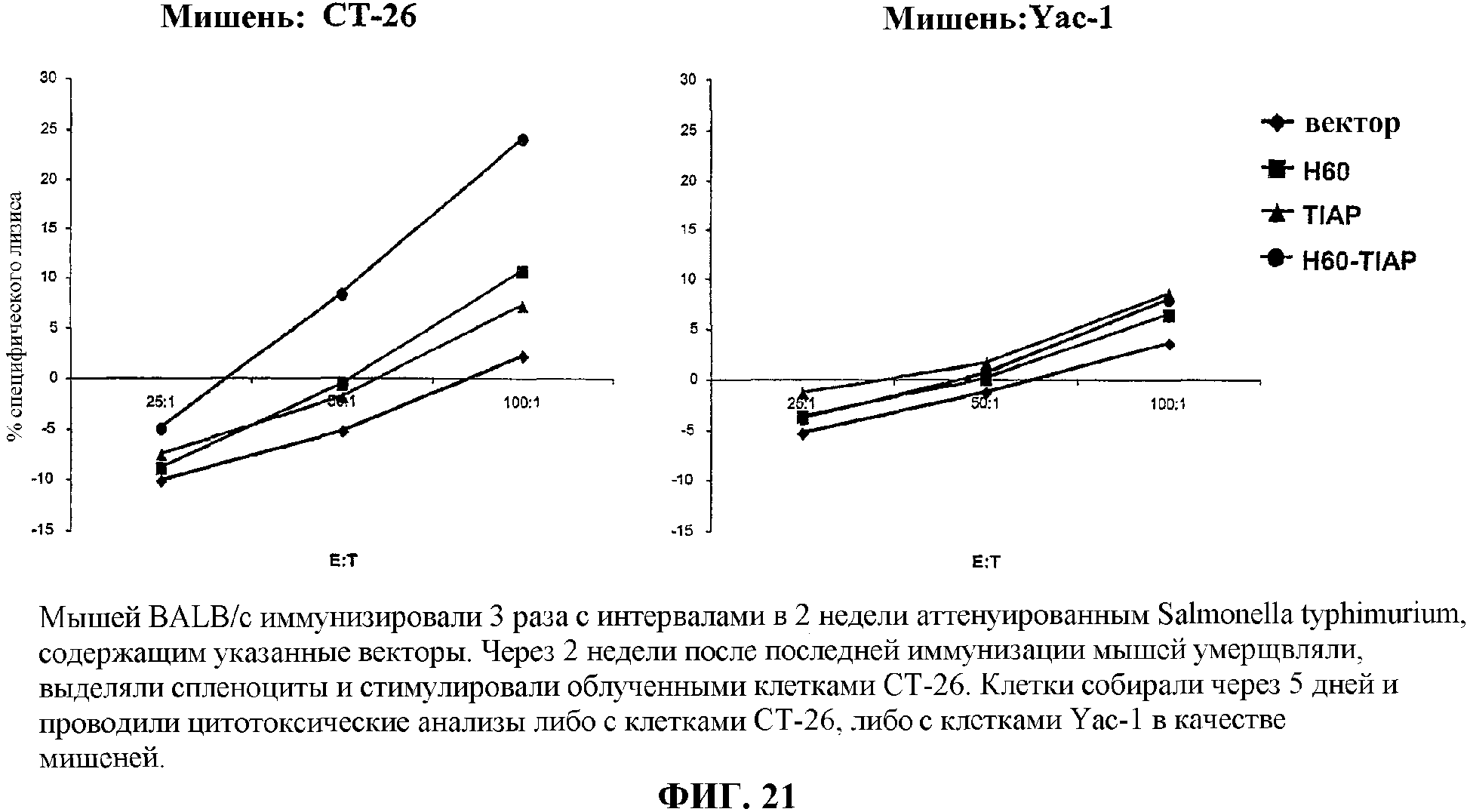
На фиг.21 графически представлены данные анализа цитотоксичности спленоцитов, выделенных у мышей, вакцинированных вакциной по изобретению.
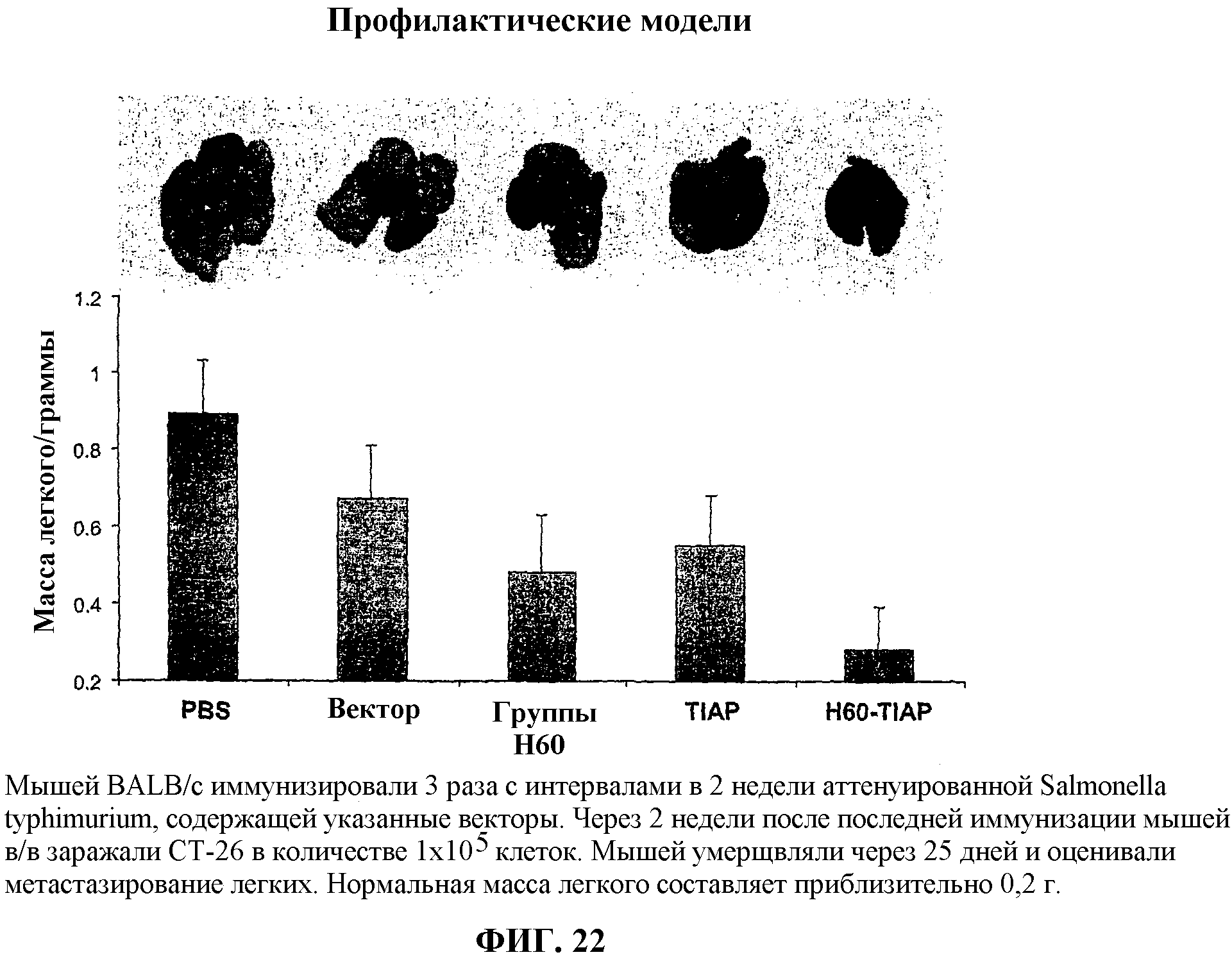
На фиг.22 показаны легкие, удаленные у мышей, вакцинированных, как описано в примере 10 (сверху), и гистограмма (снизу) средней массы легкого мышей исследованных групп.
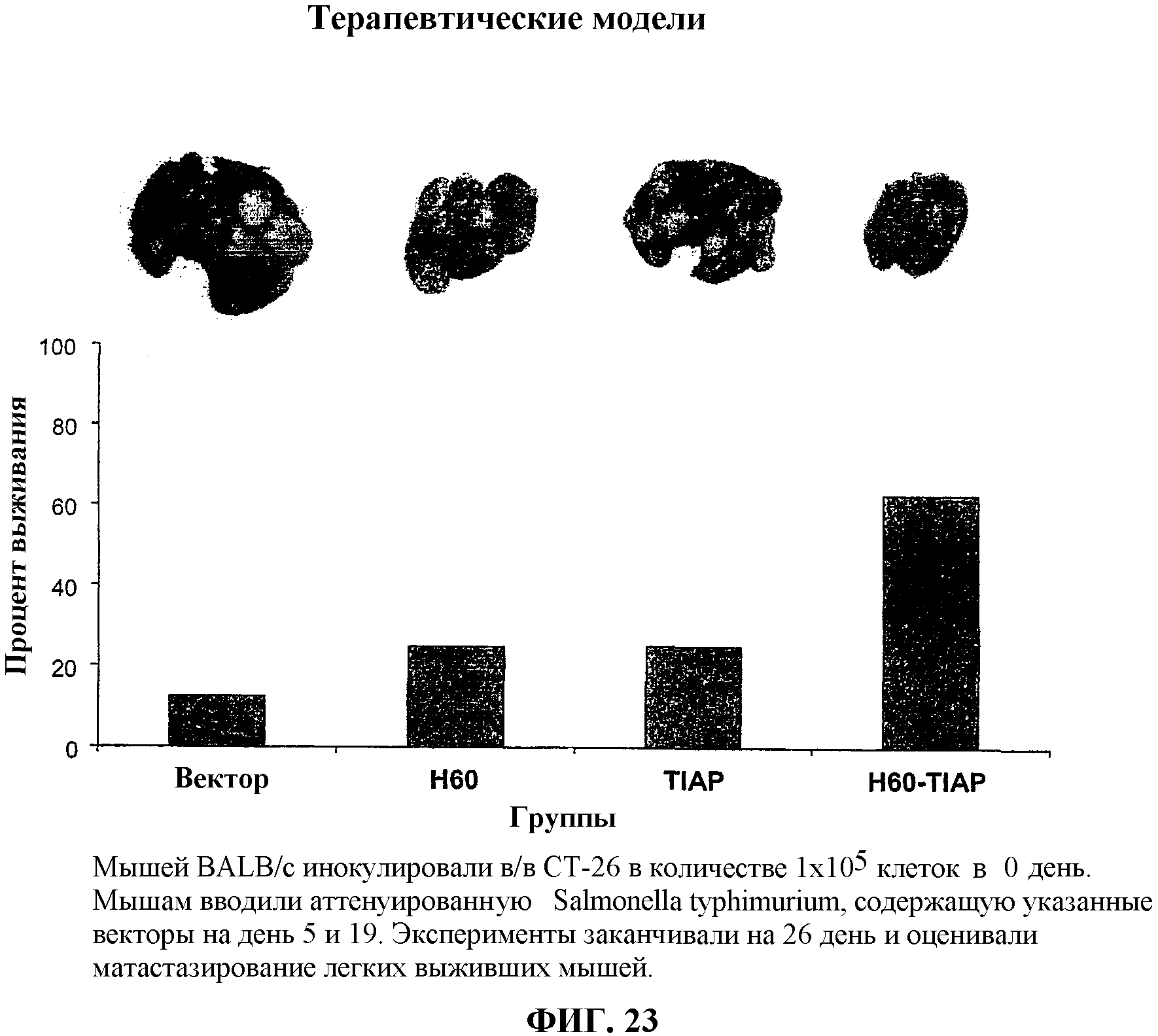
На фиг.23 представлено графическое изображение процента выживания мышей, вакцинированных и зараженных клетками опухоли СТ-26.
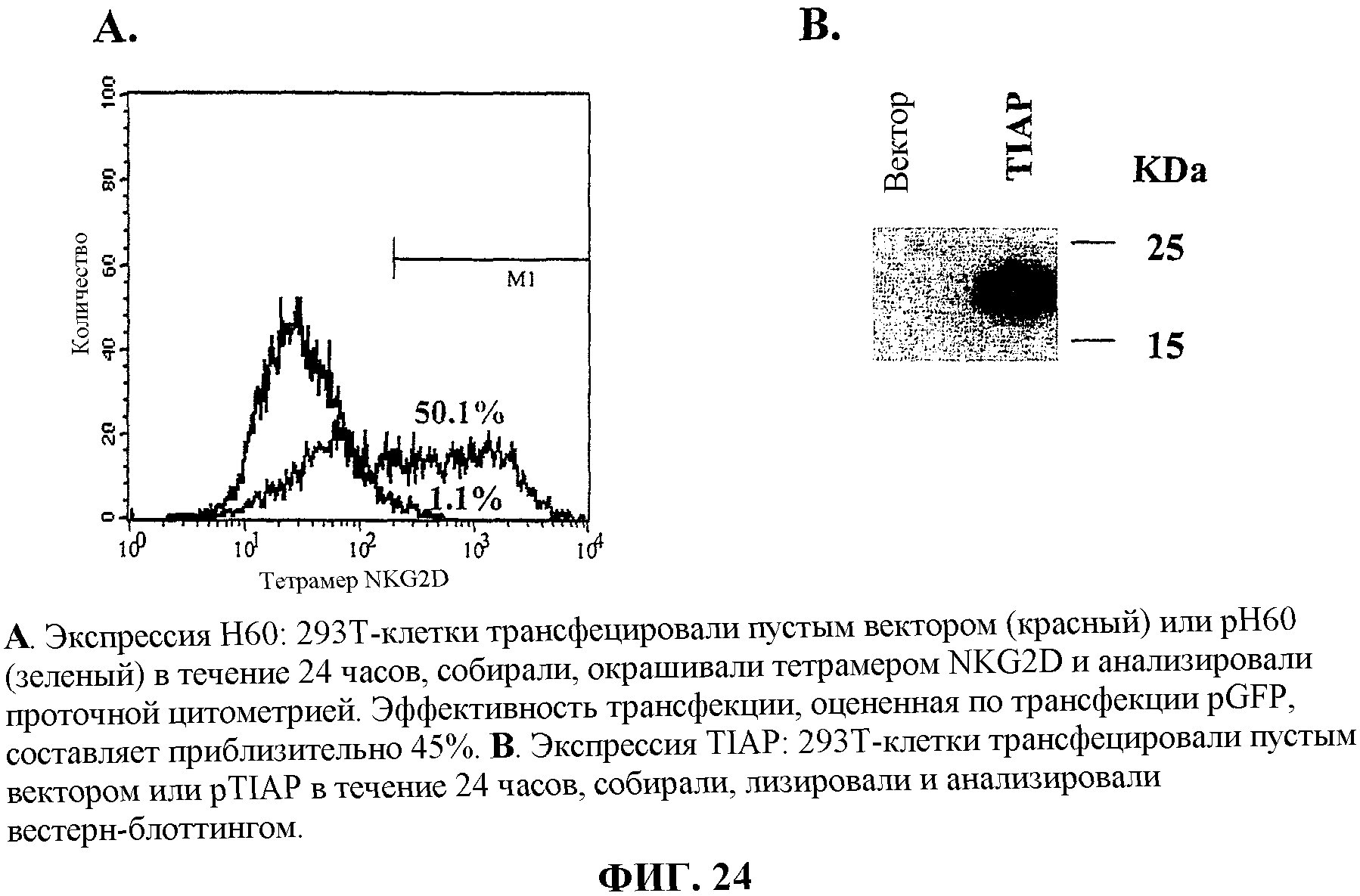
На фиг.24 показана экспрессия пептида H60 (A) и muSurvivin (B).
На фиг.25 показана последовательность нуклеиновой кислоты, кодирующая вариант CCL21a 6CKine/SLC, SEQ ID NO: 11.
На фиг.26 показана аминокислотная последовательность варианта CCL21a 6CKine/SLC, SEQ ID NO: 12.
На фиг.27 показана последовательность нуклеиновой кислоты, кодирующая MICA человека, SEQ ID NO: 13.
На фиг.28 показана аминокислотная последовательность MICA человека, SEQ ID NO: 14.
На фиг.29 показана последовательность нуклеиновой кислоты, кодирующая MICB человека, SEQ ID NO: 15.
На фиг.30 показана аминокислотная последовательность MICB человека, SEQ ID NO: 16.
На фиг.31 показана последовательность нуклеиновой кислоты, кодирующая ULBP1 человека, SEQ ID NO: 17.
На фиг.32 показана аминокислотная последовательность ULBP1 человека, SEQ ID NO: 18.
На фиг.33 показана последовательность нуклеиновой кислоты, кодирующая ULBP2 человека, SEQ ID NO: 19.
На фиг.34 показана аминокислотная последовательность ULBP2 человека, SEQ ID NO: 20.
На фиг.35 показана последовательность нуклеиновой кислоты, кодирующая ULBP3 человека, SEQ ID NO: 21.
На фиг.36 показана аминокислотная последовательность ULBP3 человека, SEQ ID NO: 22.
На фиг.37 показана аминокислотная последовательность сплайсированного варианта сурвивин-2В сурвивина человека (SEQ ID NO: 23) и сплайсированного варианта сурвивин-ΔEx3 (SEQ ID NO: 24).
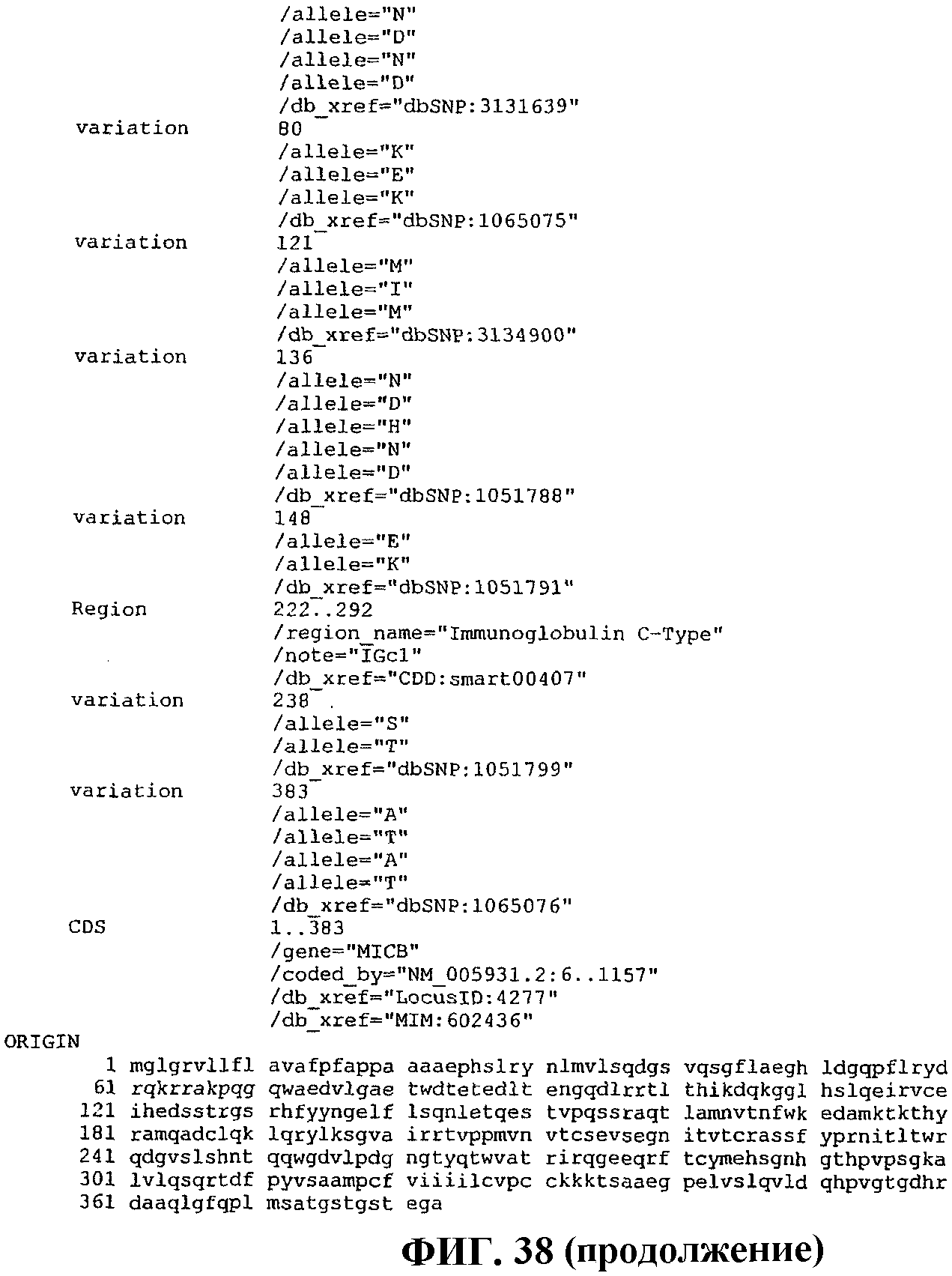
На фиг.38 представлено воспроизведение записи в GENBANK с номером доступа NP 005922, описывающей аллельные варианты MICB.
На фиг.39 показана последовательность нуклеиновой кислоты, кодирующая полноразмерный сплайсированный вариант альфа ливина человека, SEQ ID NO: 26.
На фиг.40 показана аминокислотная последовательность сплайсированного варианта альфа ливина человека, SEQ ID NO: 27.
На фиг.41 показана последовательность нуклеиновой кислоты, кодирующая сплайсированный вариант бета ливина человека, SEQ ID NO: 28.
На фиг.42 показана аминокислотная последовательность сплайсированного варианта бета ливина человека, SEQ ID NO: 29.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО ВАРИАНТА ОСУЩЕСТВЛЕНИЯ
ДНК-вакцина, эффективная для активации иммунного ответа против опухолевых клеток, содержит конструкцию ДНК, которая операбельно кодирует белок семейства IAP и иммуноактивный генный продукт. Используемый здесь и в прилагаемых пунктах формулы изобретения термин «конструкция ДНК» обозначает структуру синтетической ДНК, которую можно транскрибировать в клетках-мишенях. Конструкция может содержать линейную нуклеиновую кислоту, такую как очищенная ДНК, ДНК, встроенная в плазмидный вектор, или ДНК, встроенная в любой другой вектор, подходящий для введения ДНК в клетку хозяина. Предпочтительно ДНК встраивают в вирусный или бактериальный вектор, более предпочтительно в аттенуированный вирусный или бактериальный вектор, который является непатогенным, наиболее предпочтительно в аттенуированный бактериальный вектор.
Используемый здесь термин «иммунитет» обозначает долговременную защиту против вирулентных форм инфекционного агента или опухолевого антигена. Термин «иммунизация» обозначает профилактическое воздействие антигена патогенного агента, полученного из невирулентного источника, которое приводит к возникновению иммунитета к патогену у иммунизированного индивидуума.
Используемый здесь термин «антитело» обозначает молекулу, которая представляет собой гликозилированный белок, иммуноглобулин, который специфически связывается с антигеном.
Используемый здесь термин «антиген» обозначает нечто, что при введении иммунокомпетентному животному стимулирует продукцию определенного антитела или антител, которые могут связываться с антигеном. Используемый здесь термин «иммуноген» обозначает нечто, что не способно само по себе стимулировать продукцию антитела, но может осуществить такую стимуляцию, если объединить его с носителем.
Используемый здесь термин «консервативная замена» означает замену одного аминокислотного остатка на другой, биологически подобный остаток. Примеры консервативных замен включают в себя замену одного гидрофобного остатка, такого как изолейцин, валин, лейцин или метионин, на другой или замену одного гидрофильного остатка, такого как аргинин, на лизин и наоборот, глутаминовой кислоты на аспарагиновую кислоту и наоборот или глутамина на аспарагин и наоборот и тому подобное.
Используемый здесь термин «по существу соответствует» в его различных грамматических формах, относящийся к пептидным последовательностям, обозначает пептидную последовательность, как описано, плюс или минус три аминокислотных остатка на либо одном, либо двух из N- и С-концов и содержащую только консервативные замены в полипептидной последовательности.
Используемый здесь и в прилагаемых пунктах формулы изобретения термин «иммуноактивный генный продукт» и его грамматические формы включает в себя белки и полипепиды, обладающие иммуномодулирующей активностью, такие как белки и полипептиды, которые взаимодействуют с Т-клетками и NK-клетками и модулируют их активность.
Используемый здесь и в прилагаемых пунктах формулы изобретения термин «белок семейства IAP» включает в себя любой класс природных антигенов, экспрессируемых в опухолевых клетках, которые ингибируют апоптоз в их природной форме. Белки семейства IAP включают в себя, например, сурвивин человека, сцепленный с Х-хромосомой IAP (XIAP), TIAP мыши (аналог сурвивина у мыши), ливин человека, c-IAP-1 человека, c-IAP-2 человека, NAIP человека, любой другой белок, который включает в себя по крайней мере один домен повтора бакуловирусного ингибитора апоптоза (BIR) или его гомолога. Домен BIR присутствует во всех белках семейства IAP дикого типа. Он включает в себя четыре относительно коротких альфа-спирали и область трех расположенных антипараллельно бета-складчатых структур. Домен связывает Zn, используя три остатка цистеина и остаток гистидина, которые являются консервативными среди белков семейства IAP. Используемый здесь и в прилагаемых пунктах формулы изобретения термин «белок семейства IAP» также включает в себя варианты белков IAP дикого типа, такие как сплайсированные варианты, и тому подобное, а также фрагменты их иммуногенных гомологов, которые связываются с молекулой главного комплекса гистосовместимости (MHC) I класса и распознаются цитотоксическими T-клетками (то есть эпитопы белка сурвивина).
Используемый здесь и в прилагаемых пунктах формулы изобретения термин «связанный с опухолеобразованием» в отношении белков семейства IAP обозначает белок семейства IAP, который экспрессируется на повышенном уровне в раковых клетках, по сравнению с нормальными, нераковыми клетках. Примеры связанных с опухолеобразованием белков семейства IAP включают в себя, но ими не ограничиваясь, сурвивин человека и ливин человека.
Используемый здесь и в прилагаемых пунктах формулы изобретения термин «белок сурвивин» включает в себя полноразмерную молекулу сурвивина человека (SEQ ID NO: 2), полноразмерный мышиный аналог (то есть TIAP, как описано здесь), варианты сурвивина человека или сурвивина мыши, такие как сплайсированные варианты и варианты замен, а также фрагменты (например, эпитопы) сурвивина человека и иммуногенные гомологи сурвивина человека, которые связываются с молекулой главного комплекса гистосовместимости (MHC) I класса и распознаются цитотоксическими T-клетками. Известные варианты замен в сурвивине человека включают в себя белки, имеющие замену T34A в аминокислотной последовательности SEQ ID NO: 2, белки, имеющие замену D53A в аминокислотной последовательности SEQ ID NO: 2, и белки, имеющие замену C84A в аминокислотной последовательности SEQ ID NO: 2 (смотри Song et al., Mol. Biol. Cell, 2004; 15 (3): 1287-1296, электронная публикация от 29 декабря 2003 года). Каждый из этих известных вариантов обладает апоптотической активностью, в отличие от сурвивина дикого типа, который обладает противоапоптотической активностью.
В предпочтительном варианте осуществления ДНК-вакцина по настоящему изобретению содержит конструкцию ДНК, которая операбельно кодирует белок сурвивин, такой как сурвивин человека дикого типа с аминокислотной последовательностью SEQ ID NO: 2, иммуногенный гомолог сурвивина человека дикого типа с аминокислотной последовательностью, которая по крайней мере на 80% идентична SEQ ID NO: 2, сплайсированный вариант сурвивина человека с аминокислотной последовательностью SEQ ID NO: 23, сплайсированный вариант сурвивина человека с аминокислотной последовательностью SEQ ID NO: 24 и фрагмент белка сурвивина, который связывается с молекулой MHC I класса и распознается цитотоксическими T-клетками.
Используемый здесь и в прилагаемых пунктах формулы изобретения термин «белок ливин» включает в себя полноразмерный сплайсированный вариант альфа ливина человека (SEQ ID NO: 27), сплайсированный вариант бета ливина человека (SEQ ID NO: 29), варианты замен сплайсированных вариантов альфа и бета ливина человека, а также их фрагменты и иммуногенные гомологи, которые связываются с молекулой MHC I класса и распознаются цитотоксическими T-клетками.
В другом предпочтительном варианте осуществления ДНК вакцина по настоящему изобретению содержит конструкцию ДНК, которая операбельно кодирует белок ливин, такой как полноразмерный сплайсированный вариант альфа ливина человека дикого типа с аминокислотной последовательностью SEQ ID NO: 27, сплайсированный вариант бета ливина человека, с аминокислотной последовательностью SEQ ID NO: 29, иммуногенный гомолог полноразмерного ливина человека дикого типа с аминокислотной последовательностью, которая по крайней мере на 80% идентична SEQ ID NO: 27, иммуногенный гомолог сплайсированного варианта бета ливина человека дикого типа с аминокислотной последовательностью, которая по крайней мере на 80% идентична SEQ ID NO: 29, и фрагмент белка ливина, который связывается с молекулой MHC I класса и распознается цитотоксическими T-клетками.
Используемый здесь и в прилагаемых пунктах формулы изобретения термин «иммуногенный гомолог» и его грамматические формы, если используются в отношении белков семейства IAP, связанных с опухолеобразованием, таких как сурвивин и ливин, обозначает белок с высокой степенью гомологии с семейством IAP, связанным с опухолеобразованием, дикого типа, который может связываться с молекулой MHC I класса и может распознаваться цитотоксическими T-клетками, которые активны против соответствующего белка семейства IAP дикого типа. Предпочтительно иммуногенные гомологи имеют аминокислотную последовательность, которая по крайней мере приблизительно на 80% идентична аминокислотной последовательности белка семейства IAP, связанного с опухолеобразованием, дикого типа, более предпочтительно идентична по крайней мере приблизительно на 90%, наиболее предпочтительно идентична по крайней мере приблизительно на 95%.
Не привязываясь к какой-либо теории, предполагают, что вакцинация пациента, такого как больной человек, вакциной по изобретению приводит к селективному презентированию антигенов, полученных из связанных с опухолеобразованием белков семейства IAP, на поверхность иммунных клеток и, кроме того, к селективной экспрессии иммуноактивного генного продукта в данных клетках. Повышенное презентирование связанного с опухолеобразованием белка семейства IAP, такого как белок сурвивин или белок ливин, на клеточной поверхности антигенпрезентирующей клетки в сочетании с экспрессией иммуноактивного генного продукта, такого как цитокин или лиганд рецептора на поверхности NK-клетки, приводит к усиленному иммунному ответу против раковых клеток, которые экспрессируют связанные с опухолеобразованием белки семейства IAP, такие как белок сурвивин или белок ливин. У взрослых людей сурвивин экспрессируется практически почти в раковых клетках. Аналогично сообщалось, что экспрессия ливина увеличивается в некоторых раковых клеточных линиях, особенно в клеточных линиях меланомы.
В предпочтительном варианте осуществления ДНК-вакцина содержит полинуклеотидную последовательность, которая операбельно кодирует белок сурвивин и цитокин. Предпочтительно белок сурвивин представляет собой сурвивин человека, сурвивин мыши или его эпитоп. Предпочтительно цитокин модулирует активность T-клетки или NK-клетки. Предпочтительные цитокины включают в себя хемокины, гемопоэтины и интерфероны. Другие предпочтительные цитокины включают в себя цитокины, активирующие NK-клетку, такие как IL-12, и факторы, стимулирующие продукцию цитокинов, такие как IL-17.
В другом предпочтительном варианте осуществления ДНК-вакцина содержит полинуклеотидную последовательность, которая операбельно кодирует белок ливин и цитокин. Предпочтительно белок ливин представляет собой ливин человека дикого типа или его эпитоп. Предпочтительно цитокин модулирует активность T-клетки или NK-клетки. Предпочтительные цитокины включают в себя хемокины, гемопоэтины и интерфероны. Другие предпочтительные цитокины включают в себя цитокины, активирующие NK-клетку, такие как IL-12, и факторы, стимулирующие продукцию цитокинов, такие как IL-17.
Предпочтительные хемокины включают в себя хемокины CC, особенно те, которые представляют собой лиганды хемокинового рецептора CCR7, такие как CCL21 (SLC) и тому подобные; хемокины C, которые представляют собой лиганды рецептора CR1, такие как лимфотактин и ему подобные; хемокины CX3C, которые представляют собой лиганды рецептора CX3CR1, такие как фракталкин и ему подобные; хемокины CXC, особенно хемокины, которые представляют собой лиганды рецептора CXCR3, такие как IP-10 и ему подобные. Наиболее предпочтительно хемокин представляет собой CCL21 человека или его мышиный аналог (CCL21 мыши).
Предпочтительные гемопоэтины включают в себя факторы роста T-клетки, такие как IL-2, IL-15 и тому подобные. Предпочтительные интерфероны включают в себя интерфероны, продуцируемые T-клетками и NK-клетками, такие как IFN-γ и ему подобные. Другие предпочтительные цитокины включают в себя цитокины, активирующие NK-клетку, такие как IL-12 и ему подобные, и цитокины, которые индуцируют продукцию цитокинов в клетках, таких как эпителий, эндотелий и фибробласты, включая сюда IL-17 и ему подобные.
В другом предпочтительном варианте осуществления ДНК-вакцина содержит полинуклеотидную последовательность, которая операбельно кодирует белок сурвивин и лиганд рецептора на поверхности природной клетки-киллера. Предпочтительно белок сурвивин представляет собой сурвивин человека, сурвивин мыши или эпитоп сурвивина человека. Предпочтительно лиганд рецептора на поверхности природной клетки-киллера представляет собой лиганд рецептора NKG2D на поверхности клетки. Предпочтительно лиганд рецептора NKG2D на поверхности клетки представляет собой антиген, связанный с цепью MHC I класса (MIC), такой как MICA и MICB, белок, связывающий UL16 (ULBP), такой как ULBP1, ULBP2 и ULBP3 и тому подобный. Лиганды NKG2D мыши включают в себя, например, Rael или антигенный пептид Н60 минорного комплекса гистосовместимости. Наиболее предпочтительно лиганд рецептора NKG2D на поверхности клетки представляет собой MICA или MICB.
В еще одном предпочтительном варианте осуществления ДНК-вакцина содержит полинуклеотидную последовательность, которая операбельно кодирует белок ливин и лиганд рецептора на поверхности природной клетки-киллера. Белок ливин может представлять собой белок ливин дикого типа человека, или эпитоп ливина человека, или вариант ливина.
Предпочтительно конструкция ДНК по настоящему изобретению, которая операбельно кодирует связанный с опухолеобразованием белок семейства IAP и иммуноактивный генный продукт, также операбельно связана с регуляторными элементами, необходимыми для экспрессии генов, которые хорошо известны в данной области.
Предпочтительно конструкция ДНК операбельно встроена в экспрессирующий вектор, такой как экспрессирующий вектор BUDCE4.1, доступный от фирмы Invitrogen, Inc., Carlsbad, CA. Другие подходящие экспрессирующие векторы коммерчески доступны, например, от BD Biosciences Clonetech, Palo Alto, CA. После встраивания в экспрессирующий вектор конструкция ДНК может быть введена в вектор хозяина, такой как живой аттенуированный бактериальный вектор, посредством трансфекции клетки хозяина экспрессирующим вектором для получения вакцины по настоящему изобретению.
Конструкции ДНК предпочтительно включают в себя регуляторные элементы, необходимые для экспрессии нуклеотидов. Такие эелементы включают в себя, например, промотор, инициирующий кодон, стоп-кодон и сигнал полиаденилирования. Кроме того, часто необходимы энхансеры для экспрессии последовательности, которая кодирует иммуногенный белок-мишень. Как известно в данной области, такие элементы предпочтительно операбельно связаны с последовательностью, которая кодирует необходимый белок. Регуляторные элементы предпочтительно выбираны из элементов, которые совместимы с видами организмов, в которые их будут вводить.
Инициирующие кодоны и стоп-кодоны предпочтительно встраивают в качестве части нуклеотидной последовательности, которая кодирует белок сурвивин и иммуномодулирующий полипептид в генетической вакцине по настоящему изобретению. Инициирующие и терминирующие кодоны должны, конечно же, быть внутри рамки считывания кодирующей последовательности белка сурвивина и иммуномодулирующего полипептида.
Промотеры и сигналы полиаденилирования, включенные в состав вакцины по настоящему изобретению, предпочтительно выбирают так, чтобы они были функциональны внутри клеток индивидуума, которого необходимо иммунизировать.
Примеры промоторов, применимых в вакцинах по настоящему изобретению, особенно при получении генетической вакцины для людей, включают в себя в качестве неограничивающих примеров, промоторы обезьяньего вируса (SV40), промотор вируса опухоли молочной железы мышей (MMTV), промотор вируса иммунодефицита человека (HIV), такой как промотор длинного концевого повтора (LTR) HIV, промотор вируса Молони, цитомегаловируса (CMV), такой как предранний промотор CMV, вируса Эпштейна-Барра (EBV), вируса саркомы Рауса (RSV), а также промоторы генов человека, таких как актин человека, миозин человека, гемоглобин человека, мышечный креатин человека и металлотионеин человека.
Примеры сигналов полиаденилирования, применимых в вакцинах по настоящему изобретению, особенно при получении генетической вакцины для людей, включают в себя, в качестве неограничивающих примеров, сигналы полиаденилирования SV40 и сигналы полиаденилирования LTR.
В дополнение к регуляторным элементам, необходимым для экспрессии ДНК, можно также включать в состав молекулы ДНК другие элементы. Такие дополнительные элементы включают в себя энхансеры. Энхансером может быть, например, актин человека, миозин человека, гемоглобин человека, мышечный креатин человека и вирусные энхансеры, такие как энхансеры из CMV, RSV и EBV.
Регуляторные последовательности и кодоны, главным образом, зависят от вида организма. Для того чтобы сделать продукцию белка максимальной, регуляторные последовательности и кодоны выбирают так, чтобы они были эффективны в видах организмов, которые необходимо иммунизировать. Обычный специалист в данной области может легко получить конструкцию ДНК, которая является операбельной в данном виде индивидуума.
Конструкция ДНК по настоящему изобретению может представлять собой «голую» ДНК, как описано в публикации Restifo et al. Gene Therapy 2000; 7: 89-92, соответствующее описание которой приведено здесь в качестве ссылки. Предпочтительно ДНК операбельно встроена в вектор. Применимые векторы доставки включают в себя биодеградируемые микрокапсулы, иммуностимулирующие комплексы (ISCOM) или липосомы и генно-инженерные аттенуированные живые векторы, такие как вирусы или бактерии.
Примеры подходящих живых векторов включают в себя Salmonella typhimurium, Salmonella typhi, род Shigella, род Bacillus, род Lactobacillus, Bacille Calmette-Guerin (BCG), Escherichia coli, Vibrio cholerae, род Campylobacter, род Listeria или любой другой подходящий бактериальный вектор, хорошо известный в данной области. Предпочтительно вектор представляет собой аттенуированный живой вектор Salmonella typhimurium. Предпочтительная аттенуированная живая Salmonella typhimurium включает в себя штаммы AroA-, такие как SL7207, или дважды аттенуированные штаммы AroA-, dam-, такие как RE88. Дважды аттенуированная Salmonella typhimurium AroA-, dam- является особенно предпочтительным вектором.
Способы трансформации живых бактериальных векторов экзогенной конструкцией ДНК хорошо описаны в данной области. Смотри, например, Joseph Sambrook and David W. Russell, Molecular Cloning, A Laboratory Manual, 3rd Ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York (2001) (Sambrook и Russell).
Предпочтительные вирусные векторы включают в себя бактериофаги, вирус герпеса, аденовирус, вирус полиомиелита, вирус коровьей оспы и вирус птичьей оспы. Способы трансформации вирусного вектора экзогенной конструкцией ДНК хорошо известны в данной области. Смотри вышеуказанную публикацию Sambrook и Russell.
Липосомные векторы, которые можно использовать, представляют собой монослойные или многослойные везикулы, содержащие мембранную часть, состоящую из липофильного вещества, и внутреннюю водную часть. Водная часть, как ее используют в настоящем изобретении, содержит полинуклеотидный материал, который необходимо доставить к клетке-мишени. В общем случае предпочтительно, чтобы составляющее липосому вещество содержало катионную группу, такую как группу четвертичного аммония, и одну или более липофильных групп, таких как насыщенные или ненасыщенные алкильные группы, содержащие приблизительно от 6 до приблизительно 30 атомов углерода. Одна группа подходящих веществ описана в публикации европейского патента №0187702 и дополнительно обсуждается в патенте США №6228844 Wolff et al., соответствующие описания которых включены сюда в качестве ссылки. Множество других подходящих образующих липосому катионных липидных соединений описано в литературе. Смотри, например, L. Stamatatos, et al., Biochemistry 1988; 27:3917-3925 и H. Eibl, et al., Biophysical Chemistry 1979; 10: 261-271. Альтернативно, можно использовать такие микросферы, как полилактидкогликолидные биодеградируемые микросферы. Конструкция нуклеиновой кислоты инкапсулируют или иным образом связывают в комплекс с липосомой или микросферой для доставки нуклеиновой кислоты в ткань, как хорошо известно в данной области.
Другие применимые векторы включают в себя полимерные микросферы, содержащие биодеградируемые сложнополиортоэфирные вещества, как описано Wang et al., Nat. Mater., 2004; 3 (3): 190-6. Электронная публикация от 15 февраля 2004 г., соответствующее описание которой включено здесь в качестве ссылки.
Аспект способа по настоящему изобретению охватывает введение ДНК-вакцины, операбельно кодирующей связанный с опухолеобразованием белок семейства IAP и иммунореактивный генный продукт, в ткани млекопитающего, такого как человек. В некоторых предпочтительных вариантах осуществления ДНК-вакцины вводят перорально, внутримышечно, интраназально, внутрибрюшинно, подкожно, внутрикожно или местно. Предпочтительно ДНК-вакцину вводят перорально.
В предпочтительном способе ДНК-вакцину по настоящему изобретению можно использовать для долговременного ингибирования роста опухоли у пациентов, получающих вакцину. ДНК-вакцина содержит полинуклеотидную конструкцию ДНК, операбельно кодирующую связанный с опухолеобразованием белок семейства IAP, такой как сурвивин, и иммуноактивный генный продукт, такой как цитокин или лиганд рецептора на поверхности NK-клетки, и их фармацевтически приемлемый носитель. Вакцину вводят млекопитающим при необходимости ингибирования роста опухоли в количестве, которое достаточно, чтобы вызвать иммунный ответ против опухолевых клеток.
Предпочтительно млекопитающее, получающее вакцину по изобретению, является человеком. Иммунизация вакцинами по настоящему изобретению может быть эффективна у пациента, больного раком, таким как карцинома легкого или толстой кишки, опухоли молочной железы или опухоли простаты или подобным.
Вакцины по настоящему изобретению предпочтительно получают вместе с фармацевтически приемлемыми носителями или наполнителями, такими как вода, физиологический раствор, декстроза, глицерин и тому подобное, а также их сочетаниями. Вакцины также могут содержать вспомогательные вещества, такие как увлажняющие средства, эмульгирующие вещества, буферы, консерванты, адъюванты и тому подобное.
Вакцины по настоящему изобретению предпочтительно перорально вводят млекопитающим, например человеку, в виде раствора или суспензии в фармацевтически приемлемом носителе с концентрациями ДНК в пределах от приблизительно 1 до приблизительно 10 микрограмм на милилитр. Подходящая дозировка будет зависеть от индивидуума, получающего вакцину, и частично от решения лечащего врача, осуществляющего введение или назначение вакцины.
Вакцины по настоящему изобретению могут быть упакованы в подходящие стерильные емкости, такие как ампулы, флаконы или пузырьки, в виде либо многократной, либо однократной лекарственной формы. После заполнения препаратом вакцины емкости предпочтительно герметизируют. Предпочтительно вакцины упаковывают в емкости с прикрепленной к ним этикеткой, которая маркирует вакцину и на которой представлена запись в форме, предписанной правительственным учреждением, таким как Управление по контролю за качеством пищевых продуктов и медикаментов Соединенных Штатов, отражающая одобрение вакцины согласно соответствующим законам, информацию о дозировке и тому подобное. Этикетка предпочтительно содержит информацию о вакцине, которая может использоваться для введения вакцины пациенту медицинским работником. Упаковка также предпочтительно содержит напечатанные информационные материалы, касающиеся введения вакцины, инструкции, указания и любые обязательно необходимые предупреждения.
Последовательность ДНК сурвивина человека и ее соответствующая белковая последовательность опубликованы Strausberg в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, номер доступа ДНК BC034148, описания которой включены сюда в качестве ссылки. Последовательность ДНК и соответствующая белковая последовательность TIAP мыши опубликованы в Kobayashi et al., Proc. Natl. Acad. Sci. 1999; 96: 1457-62; номер доступа ДНК AB01389 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описания которой приведены здесь в качестве ссылки.
Последовательность нуклеиновой кислоты, кодирующая сурвивин человека, представлена на фиг.1 (SEQ ID NO: 1), и ее соответствующая аминокислотная последовательность (SEQ ID NO: 2) показана на фиг.2. Последовательность нуклеиновой кислоты, кодирующая сурвивин мыши (то есть TIAP), представлена на фиг.3 (SEQ ID NO: 3), и ее соответствующая аминокислотная последовательность (SEQ ID NO: 4) показана на фиг.4.
Гомология белков сурвивина человека и его аналога у мыши, TIAP, показана на фиг.5. Идентичность аминокислотной последовательности между сурвивином человека (SEQ ID NO: 2) и TIAP мыши (SEQ ID NO: 4) составляет приблизительно 83%, как показано на фиг.5.
Mahotka et al. идентифицировали два сплайсированных варианта сурвивина человека, обозначенных сурвивин-ΔEx3 и сурвивин-2B, которые также могут использоваться в настоящем изобретении. Mahotka et al., Cancer Res., 1999; 59: 6097-6102, соответствующее описание которой приведено здесь в качестве ссылки. Аминокислотные последовательности сурвивина-2B (SEQ ID NO: 23) и сурвивина-ΔEx3 (SEQ ID NO: 24) показаны на фиг.37. Hirohashi с соавторами идентифицировали активный T-клеточный эпитоп сурвивина-2B с аминокислотной последовательностью AYACNTSTL (SEQ ID NO: 25), обозначаемый сурвивин-2B80-88, который вызывает ответ цитотоксических T-лимфоцитов против сурвивина-2B. Hirohashi et al., Clinical Cancer Res., 2002; 8: 1731-39, соответствующее описание которой приведено здесь в качестве ссылки. Этот эпитоп представляет собой фрагмент сурвивина, который способен связываться с молекулой MHC I класса и распознается цитотоксическими Т-клетками и подходит для применения в качестве компонента белка семейства IAP в вакцине по настоящему изобретению.
Другой сплайсированный вариант сурвивина человека представляет собой вариант сурвивин-3B, описанный Badran et al., Biochem. Biophys. Res. Commun., 2004; 314 (3): 902-907. Полинуклеотидная последовательность, кодирующая сурвивин-3B, и ее соответствующая аминокислотная последовательность опубликованы в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, номер доступа ДНК AB154416, описание которой приведено здесь в качестве ссылки.
Полноразмерный ливин человека (известный как вариант альфа) представляет собой белок семейства IAP, имеющий один домен BIR и состоящий из 298 аминокислотных остатков. Последовательность ДНК и соответствующая белковая последовательность варианта альфа ливина человека опубликована Clark с соавторами в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, номер доступа ДНК NM139317, описание которой приведено здесь в качестве ссылки. Последовательность ДНК и соответствующая белковая последовательность варианта бета ливина человека опубликована под номером доступа ДНК NM022161 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описание которой приведено здесь в качестве ссылки.
Последовательность нуклеиновой кислоты, кодирующая полноразмерный ливин человека (альфа вариант), представлена на фиг.39 (SEQ ID NO: 26), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 27) показана на фиг.40. Последовательность нуклеиновой кислоты, кодирующая вариант бета ливина человека, представлена на фиг.41 (SEQ ID NO: 28), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 29) показана на фиг.42. В варианте бета ливина человека отсутствуют остатки с 216 по 233 полноразмерного сплайсированного варианта альфа ливина человека (SEQ ID NO: 27). Вариант бета идентичен варианту альфа ливина человека во всех прочих отношениях. Домен BIR как альфа, так и бета вариантов ливина человека находится в области от аминокислотного остатка R90 до аминокислотного остатка L155 в SEQ ID NO: 27 и SEQ ID NO: 29.
В предпочтительном варианте осуществления вакцины по настоящему изобретению содержат конструкцию ДНК, которая кодирует один или несколько белков сурвивина, таких как сурвивин человека, TIAP (сурвивин мыши) и их иммуногенные гомологи. Аминокислотная последовательность иммуногенных гомологов предпочтительно по крайней мере приблизительно на 80% идентична аминокислотной последовательности белка сурвивина человека, более предпочтительно по крайней мере приблизительно на 90% идентична аминокислотной последовательности, наиболее предпочтительно по крайней мере приблизительно на 95% идентична аминокислотной последовательности SEQ ID NO: 2. Альтернативно вакцина может содержать конструкцию ДНК, которая кодирует один или несколько T-клеточных эпитопов белка сурвивина человека.
В другом предпочтительном варианте осуществления вакцины по настоящему изобретению содержат конструкцию ДНК, которая кодирует один или несколько белков ливинов, таких как сплайсированные варианты альфа и бета ливина человека (SEQ ID NO: 27 и 29 соответственно), их иммуногенные гомологи. Аминокислотная последовательность иммуногенных гомологов предпочтительно по крайней мере приблизительно на 80% идентична аминокислотной последовательности сплайсированного варианта альфа или бета ливина человека, более предпочтительно по крайней мере приблизительно на 90% идентична аминокислотной последовательности, наиболее предпочтительно по крайней мере приблизительно на 95% идентична аминокислотной последовательности SEQ ID NO: 27 или SEQ ID NO: 29. Альтернативно вакцина может содержать конструкцию ДНК, которая кодирует один или несколько T-клеточных эпитопов белка ливина человека.
Вследствие генетически детерминированной вырожденности генетического кода, последовательности ДНК, которые кодируют, по существу, ту же самую функционально равнозначную нативной (то есть встречающейся в природе) аминокислотную последовательность связанных с опухолеобразованием белков семейства IAP, таких как сурвивин человека, сурвивин мыши и сплайсированные варианты ливина человека, можно использовать в вакцинах по изобретению. Такие последовательности ДНК включают в себя последовательности, которые способны гибридизоваться с последовательностями ДНК нативных сурвивина или ливина, а также и аллельных вариантов и тому подобного. Предпочтительно нуклеотидная последовательность ДНК функционально равнозначных гомологов по крайней мере приблизительно на 70% идентична ДНК, кодирующей вышеупомянутые нативные белки сурвивин или ливин, более предпочтительно по крайней мере приблизительно на 80%.
Иммуноактивные генные продукты, кодируемые конструкциями ДНК в вакцинах по настоящему изобретению, предпочтительно представляют собой цитокины или лиганды рецепторов на поверхности природных клеток-киллеров. Особенно предпочтительными цитокинами являются хемокины СС. Особенно применимыми хемокинами CC являются лиганды хемокинового рецептора CCR7. Селективные лиганды CCR7 включают в себя CCL19 (также известный как exodus-3, ELC, MIP-3β и CKβ11) и CCL21 (также известный как exodus-2, SLC, 6Ckine, TCA4 и CKβ9). Особенно предпочтительные хемокины представляют собой CCL21 человека и его мышиный аналог 6Ckine/SLC (muCCL21) и хемокины, по существу, им соответсвующие.
Последовательности ДНК и белка SLC человека были опубликованы Nishimura с соавторами в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, номер доступа ДНК AB002409, описания которых приведены здесь в качестве ссылки. Последовательности ДНК и белка мышиного варианта CCL21a 6Ckine/SLC опубликованы Hromas et al. J Immunol. 1997; 159 (6): 2554-2558, номер доступа ДНК NM011335 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описания которых приведены здесь в качестве ссылки. Последовательности ДНК и белка мышиного варианта CCL21b 6Ckine/SLC опубликованы Hedrick et al., J. Immunol. 1997; 159 (4): 1589-1593, номер доступа ДНК NM011124 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описание которых приведено здесь в качестве ссылки.
Последовательность нуклеиновой кислоты, кодирующая CCL21 человека (SLC), представлена на фиг.6 (SEQ ID NO: 5), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 6) показана на фиг.7. Последовательность нуклеиновой кислоты, кодирующая CCL21 мыши (вариант CCL21b), представлена на фиг.8 (SEQ ID NO: 7), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 8) показана на фиг.9.
Гомология белков CCL21 человека (SLC) и его мышиного аналога (6Ckine/SLC мыши, CCL21b) показана на фиг.10. Аминокислотная последовательность приблизительно на 73% идентична аминокислотной последовательности CCL21 человека (SEQ ID NO: 6) и CCL21 мыши (SEQ ID NO: 8), как показано на фиг.10.
Последовательность нуклеиновой кислоты, кодирующая вариант CCL21а мышиного SLC, представлена на фиг.25 (SEQ ID NO: 11), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 12) показана на фиг.26.
Предпочтительные лиганды рецепторов на поверхности природных клеток-киллеров представляют собой лиганды поверхностного рецептора NKG2D мыши. Предпочтительные лиганды поверхностного рецептора NKG2D представляют собой MICA, MICB, ULBP1, ULBP2 и ULBP3 и тому подобные. Наиболее предпочтительными являются MICA и MICB. Другие известные лиганды поверхностных рецепторов NKG2D включают в себя мышиный Rea-lβ и мышиный антигенный пептид Н60 минорного комплекса гистосовместимости.
Последовательности ДНК и белка мышиного антигенного пептида Н60 минорного комплекса гистосовместимости были опубликованы Malarkannan et al., J. Immunol. 1998; 161 (7): 3501-3509, номер доступа ДНК AF084643 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описания которых приведены здесь в качестве ссылки. Неполная последовательность нуклеиновых кислот, кодирующая мышиный антигенный пептид Н60 минорного комплекса гистосовместимости, представлена на фиг.11 (SEQ ID NO: 9), и соответствующая ей неполная аминокислотная последовательность (SEQ ID NO: 10) показана на фиг.12.
Последовательности ДНК и белка MICA человека была опубликована Zwirner et al., номер доступа ДНК AY204547 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описания которых приведены здесь в качестве ссылки. Последовательность нуклеиновой кислоты, кодирующая MICA человека, представлена на фиг.27 (SEQ ID NO: 13), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 14) показана на фиг.28.
Последовательности ДНК и белка MICB человека были опубликованы Bahram et al., Immunogenetics 1996; 45 (2): 161-162, номер доступа ДНК U65416 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описания которых приведены здесь в качестве ссылки. Последовательность нуклеиновой кислоты, кодирующая MICB человека, представлена на фиг.29 (SEQ ID NO: 15), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 16) показана на фиг.30. Аллельные варианты MICB описаны в GENBANK под номером доступа NP 005922, приведенного здесь в качестве ссылки. Фиг.38 является представлением записи в GENBANK для номера доступа NP 005922.
Последовательности ДНК и белка ULBP1 человека были опубликованы Cosman et al., Immunity 2001; 14 (2): 123-133, номер доступа ДНК AF304377 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описания которых приведены здесь в качестве ссылки. Последовательность нуклеиновой кислоты, кодирующая ULBP1 человека, представлена на фиг.31 (SEQ ID NO: 17), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 18) показана на фиг.32.
Последовательности ДНК и белка ULBP2 человека были опубликованы Cosman et al., Immunity 2001; 14 (2): 123-133, номер доступа ДНК AF304378 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описания которых приведены здесь в качестве ссылки. Последовательность нуклеиновой кислоты, кодирующая ULBP2 человека, представлена на фиг.33 (SEQ ID NO: 19), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 20) показана на фиг.34.
Последовательности ДНК и белка ULBP3 человека были опубликованы Cosman et al., Immunity 2001; 14 (2): 123-133, номер доступа ДНК AF304379 в базе данных EMBL European Bioinformatics Institute, Wellcome Trust Genome Campus, Hinxton, Cambridge CB10 1SD, UK, описания которых приведены здесь в качестве ссылки. Последовательность нуклеиновой кислоты, кодирующая ULBP3 человека, представлена на фиг.35 (SEQ ID NO: 21), и соответствующая ей аминокислотная последовательность (SEQ ID NO: 22) показана на фиг.36.
Особенно предпочтительные лиганды рецепторов на поверхности природных клеток-киллеров включают в себя лиганды рецептора NKG2D, такие как MICA, MICB, ULBP1, ULBP2, ULBP3 и их функциональные эквиваленты. Аминокислотная последовательность функциональных эквивалентов предпочтительно на по крайней мере приблизительно 80% идентична аминокислотной последовательности вышеупомянутых иммуномодулирующих полипептидов, более предпочтительно на по крайней мере приблизительно 90% идентична аминокислотной последовательности, наиболее предпочтительно на по крайней мере приблизительно 95% идентична аминокислотной последовательности.
Вследствие генетически детерминированной вырожденности генетического кода последовательности ДНК, которые кодируют, по существу, ту же самую или операбельно равнозначную аминокислотную последовательность применимым нативным иммуноактивным генным продуктам, таким как CCL21 человека, CCL21 мыши, MICA, MICB, ULBP1, ULBP2, ULBP3 и тому подобные вещества, по существу им соответствующие, можно использовать в вакцинах по изобретению. Такие последовательности ДНК включают в себя последовательности, которые способны гибридизоваться с последовательностями ДНК иммуномодулирующих полипептидов, а также аллельными вариантами и тому подобным. Предпочтительно нуклеотидная последовательность ДНК операбельно равнозначных гомологов по крайней мере приблизительно на 70% идентична ДНК, кодирующей вышеупомянутые иммуномодулирующие полипептиды.
Измененные последовательности ДНК, которые можно использовать в соответствии с настоящим изобретением, включают в себя делеции, вставки или замены различных нуклеотидных остатков в нативной полинуклеотидной последовательности, кодирующей связанный с опухолеобразованием белок семейства IAP дикого типа, приводящие к появлению последовательности, которая кодирует белок дикого типа либо его иммуногенный гомолог. Измененные последовательности ДНК, которые можно использовать в соответствии с настоящим изобретением, могут также включать в себя делеции, вставки или замены различных нуклеотидных остатков в нативной полинуклеотидной последовательности, кодирующей иммуногенный генный продукт, приводящие к появлению последовательности, которая кодирует иммуноактивный генный продукт или его функциональный эквивалент. Функциональный эквивалент иммуноактивного генного продукта может содержать делеции, вставки или замены аминокислотных остатков в цитокине дикого типа или лиганде рецептора на поверхности NK-клетки, которые приводят к «молчащим» изменениям, таким образом, получая операбельно равнозначную молекулу. Такие аминокислотные замены (например, консервативные замены) можно осуществить, основываясь на подобии полярности, заряда, растворимости, гидрофобности, гидрофильности и/или амфипатической природы интересующих остатков. Например, отрицательно заряженные аминокислоты включают в себя аспарагиновую кислоту и глутаминовую кислоту; положительно заряженные аминокислоты включают в себя лизин и аргинин; аминокислоты с незаряженными полярными концевыми группами, имеющие подобные величины гидрофильности, включают в себя следующие аминокислоты: лейцин, изодейцин, валин; глицин, аланин; аспарагин, глутамин; серин, треонин; фенилаланин, тирозин.
Используемый здесь функционально равнозначный иммуноактивный генный продукт, такой как цитокин или лиганд рецептора на поверхности NK-клетки, обозначает полипептид, обладающий, по существу, той же самой иммуномодулирующей активностью, что и его аналог, встречающийся в природе иммуноактивный генный продукт.
Можно сконструировать последовательности ДНК, операбельно кодирующие белок семейства IAP и иммуноактивные генные продукты, применимые в вакцинах по изобретению, для того чтобы изменить кодирующие последовательности для различных целей, включая, но не ограничиваясь этим, изменения, которые модифицируют процессинг и экспрессию генного продукта. Например, можно провести мутации с использованием методик, которые хорошо известны в данной области, например сайт-направленный мутагенез, чтобы встроить новые участки рестрикции, чтобы изменить паттерны гликозилирования, фосфорилирования и тому подобное.
Другим аспектом настоящего изобретения является способ вакцинации млекопитающих против рака. Способ охватывает введение млекопитающим вакцины по настоящему изобретению, как описано здесь, в количестве, достаточном, чтобы вызвать иммунный ответ против раковых клеток. Предпочтительно млекопитающее является человеком.
В другом аспекте настоящее изобретение также охватывает трансформированные клетки хозяина, которые были трансформированы вектором, содержащим конструкцию ДНК, операбельно кодирующую описанные здесь белок семейства ингибиторов апоптоза и иммуноактивный генный продукт. Клетка хозяина может представлять собой прокариотическую клетку или эукариотическую клетку.
Настоящее изобретение также относится к выделенным плазмидным векторам, содержащим конструкцию ДНК, операбельно кодирующую белок семейства ингибиторов апоптоза и иммуноактивный генный продукт. Векторы могут использоваться для трансфекции клеток хозяина, таких как аттенуированные бактериальные клетки, для получения вакцин по изобретению.
Следующие примеры предназначены для дополнительной иллюстрации характерных особенностей и осуществлений настоящего изобретения и не предназначены для его ограничения.
Материалы, способы и примеры
Материалы. Мышей C57/BL/6J и Balb/C получали от Scripps Research Institute breeding facility. ДНК, кодирующую TIAP (мышиную форму сурвивина), клонировали посредством ПЦР из кДНК MC3P. ДНК, кодирующую мышиный 6Ckine (мышиный CCL21), клонировали из клеток селезёнки. ДНК, кодирующая антигенный пептид H60 минорного комплекса гистосовместимости (мышиная форма MICA и MICB), любезно предоставлена Dr. David H. Ranlet из University of California (Berkley). ДНК для вакцины, кодирующую мышиный CCL21 (muCCL21, также известный как 6Ckine/SLC) и мышиный сурвивин (muSurvivin, также известный как TIAP), клонировали в эукариотические экспрессирующие векторы pBudCE4.1 из Invitrogen, Inc., используя участки рестрикции HindIII и BamHI для MuCCL21 и используя XhoI для обоих концов muSurvivin. ДНК для вакцины, кодирующую H60 и TIAP, клонировали в эукариотические экспрессирующие векторы pBudCE4.1 из Invitrogen, Inc., используя участки рестрикции HindIII и XbaI для H60, и для muSurvivin, используя участки рестрикции KpnI и XhoI. Аттенуированный штамм AroA- Salmonella typhimurium (SL2707) и дважды аттенуированный штамм AroA-, dam- Salmonella typhimurium (RE88) получали от Remedyne, Santa Barbara, CA. Антитела получали от BD Biosciences, Bedford, MA. Флуоресцеинизотиоцианат (FITC) и R-фикоэритрин (PE) получали от Molecular Probes, Eugene, OR. Меченные FITC и PE антитела приготавливали согласно протоколам, рекомендуемым производителем.
Часть А. Вакцины из трансформированной аттенуированной Salmonella typhimurium AroA-
ПРИМЕР 1. Получение ДНК-вакцины, кодирующей muSurvivin и muCCL21
Вектор pBudCE4.1, содержащий ДНК muSurvivin и muCCL21 (приблизительно 1-10 мкг пДНК), электропорировали в свежеприготовленную аттенуированную Salmonella typhimurium (SL2707), используя Bio-Rad Pulser, при 2,5 кВ, 25 мкF и 200 Ом согласно процедурам, рекомендуемым производителем. Salmonella, содержащую вектор, отбирали на планшете, содержащем зеоцин. Колонии собирали несколько дней и культивировали в течение ночи в бульоне LB (EM Science, Gibbstown, NJ) с добавленным зеоцином. Бактерии выделяли и отмывали фосфатно-буферным солевым раствором (PBS). Затем отмытые бактерии суспендировали в среде PBS в концентрации приблизительно 1×109 рекомбинантных Salmonella на милилитр PBS, чтобы образовался раствор вакцины для дальнейшего использования.
Контрольные вакцины, состоящие из Salmonella, трансформированных только одним вектором, вектором, содержащим только ДНК muSurvivin, и вектором, содержащим только ДНК muCCL21, также получали согласно той же процедуре. На фиг.13 показано схематическое изображение экспрессирующих конструкций.
Вакцины хранили в закрытых ампулах до дальнейшего использования. ДНК плазмиды хранили при приблизительно -80°C до трансформации Salmonella.
ПРИМЕР 2. Вакцинация мышей ДНК-вакцинами примера 1
Мышей Balb/C (приблизительно по 8 мышей в исследуемой группе) вакцинировали ДНК-вакцинами примера 1 (приблизительно 1×108 рекомбинантных Salmonella в приблизительно 100 мкл PBS) посредством перорального принудительного питания 3 раза с интервалами в 2 недели.
ПРИМЕР 3. Оценка устойчивости к опухоли вакцинированных мышей
Приблизительно через 1 неделю после последней вакцинации мышей Balb/C из примера 2 (приблизительно по 8 мышей на исследуемую группу) подвергали заражению клетками карциномы легкого Льюиса D121 (подкожно) в количестве приблизительно 1×105. Подкожные опухоли легкого Льюиса удаляли хирургическим путем через приблизительно 2 недели роста, чтобы осуществлялось самопроизвольное распространение по легкому. Рост подкожной опухоли через день измеряли в двух направлениях и вычисляли объем опухоли согласно формуле:
объем = (ширина2)(длина2)
для каждой опухоли. Количество самопроизвольных метастазов D121 в легких оценивали через от приблизительно 24 до приблизительно 28 дней после удаления первичной подкожной опухоли. Мышей умерщвляли и проводили вскрытие и опухолевые массы в легких оценивали как процент поверхности легкого, которая была покрыта опухолью, и оценивали как "0" при отсутствии опухоли, "1" в случае менее чем приблизительно 20% области распространения опухоли, "2" в случае от приблизительно 20 до приблизительно 30% области распространения опухоли и "3" - более чем приблизительно 50% распространения опухоли.
Оценки опухолевых масс для мышей, вакцинированных вакцинами примера 1, показаны в таблице 1. На фиг.14 представлено изображение легких мышей, вакцинированных вакцинами примера 1. Объемы опухолей приведены в таблице 1 и на фиг.14. На фиг.14 в столбце А представлен средний объем опухоли легкого (в кубических миллиметрах) у мышей, вакцинированных вакциной по изобретению muSurvivin/muCCL21; в столбце B приведен средний объем опухоли легкого у мышей, вакцинированных вакциной, в которую встроена только ДНК muSurvivin; в столбце C представлен средний объем опухоли легкого у мышей, вакцинированных вакциной, в которую встроена только ДНК muCCL21; в столбце D представлен средний объем опухоли легкого у мышей, вакцинированных вакциной, в которую встроен только пустой вектор, и в столбце E представлен средний объем опухоли легкого у мышей, вакцинированных буфером PBS. На фиг.14 также приведены изображения репрезентативных удаленных легких в каждой исследуемой группе, каждое из которых показано под соответствующим столбцом на фиг.14.
Результаты, показанные в таблице 1 и на фиг.14 (диаграммы А и В), демонстрируют, что с помощью ДНК-вакцины, содержащей конструкцию ДНК, кодирующую белок семейства IAP (то есть muSurvivin) и иммуноактивный генный продукт (то есть muCCL21), можно эффективно иммунизировать мышей против метастазов опухоли легкого и ингибировать рост опухолей легкого.
ПРИМЕР 4. Опосредованная T-клеткой цитотоксичность против клеток рака легкого D121, индуцированная ДНК-вакциной по изобретению
Мышей C5/7BL/6J (приблизительно по 8 мышей на исследуемую группу) вакцинировали ДНК-вакцинами примера 1, как описано в примере 2. Спленоциты выделяли приблизительно через 4 дня после вакцинации и анализировали их литическую активность с помощью 4-часового анализа высвобождения51Cr, как описано в Current Protocols in Immunology 3.11.4, Coligan, et al. Eds., John Wiley & Sons, Inc. (1994). Клетки D121 использовали в качестве клеток-мишеней для спленоцитов.
На фиг.15 графически проиллюстрирована опосредованная T-клеткой цитотоксичность против клеток рака легкого D121, индуцированная ДНК-вакциной по изобретению. Точки на графике, показанные белым кружком, представляют данные анализа ингибирования, где клетки обрабатывали антителами к антигенам MHC I класса H-2Kb/H-2Db в количестве 50 мкг/мл (клон SF1-1.1; 34-2-12 IgG2a, κ), а сплошные черные квадраты представляют данные при отсутствии ингибирующих антител. Процент лизиса опухолевых клеток (ось Y) показан для трех различных соотношений эффекторной клетки и клетки-мишени (E/T) для каждой группы вакцинации (то есть E/T 100:1 для первой точки на графике; 50:1 для второй точки на графике и 25:1 для третьей точки на графике). Результаты демонстрируют, что вакцина по изобретению muSurvivin/muCCL21 (обозначенная как SLC/TIAP) вызывала почти 5-кратное увеличение лизиса при соотношении E/T 100:1 по сравнению с контрольными вакцинами, содержащими PBS, пустой вектор и ДНК muCCL21, и приблизительно 2-кратное увеличение по сравнению с контрольной вакциной, содержащей только ДНК muSurvivin.
ПРИМЕР 5. Повышающая регуляция маркеров активации CD25, CD69 и CD28 в спленоцитах (T-клетки CD8+) вакцинированных мышей
Мышей C5/7BL/6J (приблизительно по 4 мыши на исследуемую группу) вакцинировали ДНК-вакцинами примера 1, как описано в примере 2. Через приблизительно 1 неделю после последней вакцинации выделяли спленоциты из иммунизированных мышей и контрольной группы мышей. Затем клетки окрашивали конъюгированным с FITC антителом к CD8+ и конъюгированными с PE антителами к CD25, CD69 и CD28. Суспензии клеток анализировали методом проточной цитометрии с использованием двухцветовой маркировки, сканируя FAC Becton Dickenson, чтобы определить процент CD8+ Т-клеток, положительных для CD25, CD28 и CD69 для каждого спленоцита. Результаты представлены на фиг.16. Численное значение в верхнем правом углу на каждом графике FACS указывает процент клеток, которые презентируют как антиген CD8+, так и CD25, CD28 или CD69, в зависимости от обстоятельств. Численные результаты приведены в таблице 2. Данные результаты демонстрируют увеличение экспрессии T-клеточных маркеров в случае применения вакцины по настоящему изобретению, указывающее на повышенную активацию Т-клетки.
Данные в таблице 2 и на фиг.16 демонстрируют, что вакцина по изобретению примера 1, содержащая конструкцию ДНК, кодирующую muSurvivin и muCCL21, приводит к повышающей регуляции экспрессии молекул активации T-клетки.
ПРИМЕР 6. Увеличенная экспрессия совместно стимулирующихся молекул в дендритных клетках вакцинированных мышей
Мышей C5/7BL/6J (приблизительно по 4 мыши на исследуемую группу) вакцинировали ДНК-вакцинами примера 1, как описано в примере 2. Спленоциты выделяли из иммунизированных мышей и контрольной группы мышей через приблизительно 1 неделю после последней вакцинации. Затем клетки окрашивали конъюгированными с FITC антителом к CD11c в комбинации с конъюгированными с PE антителами к совместно стимулирующимся молекулам B7 (CD80), ICAM-1 и DEC205. Суспензии клеток анализировали методом проточной цитометрии с использованием двухцветовой маркировки, сканируя FAC Becton Dickenson. На фиг.17 графически представлены средние величины флуоресценции для клеток, показывающих увеличенную экспрессию ICAM-1 (сверху), CD80 (по середине) и DEC205 (снизу), в случае спленоцитов, выделенных из мышей, вакцинированных вакциной по изобретению muSurvivin/muCCL21, относительно контрольных вакцин.
ПРИМЕР 7. Индукция высвобождения внутриклеточных цитокинов
Мышей, которым проводили иммунизацию, как в примере 2 (по 8 мышей на группу), подвергали заражению клетками рака легкого D121, как в примере 3. ОТ каждой мыши собирали спленоциты через приблизительно одну неделю после заражения опухолевой клеткой. Спленоциты окрашивали конъюгированным с FITC антителом против CD3 и затем фиксировали, нарушали проницаемость мембраны и далее окрашивали конъюгированным с РЕ антителом против IFN-γ. Окрашенные двухцветными маркерами клетки анализировали методом проточной цитометрии FACS. Результаты показаны на фиг.18. Клетки фиксировали, используя начальный набор для внутриклеточного окрашивания из BD Pharmingen, La Jolla, CA.
Результаты, показанные на фиг.18, демонстрируют, что процент клеток, высвобождающих IFN-γ, увеличивался до приблизительно 3,17% для спленоцитов, выделенных у мышей, вакцинированных вакциной по изобретению, по сравнению с только 0,41% для мышей, получающих контрольную вакцину с PBS, приблизительно 0,38% для мышей, получающих контрольную вакцину с пустым вектором, приблизительно 0,96% для мышей, получающих контрольную вакцину с SLC, и приблизительно 1,53% для мышей, получающих контрольную вакцину с muSurvivin.
ПРИМЕР 8. Увеличение апоптоза клеток рака легких у вакцинированных мышей
Мышей, иммунизированных, как в примере 2 (по 8 мышей на группу), подвергали заражению клетками рака легкого D121, как в примере 3. Спленоциты собирали от каждой мыши приблизительно через одну неделю после заражения опухолевыми клетками. Спленоциты инкубировали с опухолевыми клетками D121 при температуре приблизительно 37°C в течение приблизительно 3 часов. Затем опухолевые клетки выделяли и анализировали посредством FACS. Аннексин V-FITC использовали для количественного анализа процента клеток в популяции, которые активно подвергались апоптозу. Пропидиум иодид (PI) использовали для того, чтобы отличить жизнеспособные клетки от нежизнеспособных, используя Apoptosis Detection Kit, доступный от BDPharmingen, La Jolla, CA.
На фиг.19 графически представлены результаты анализа FACS, полученные приблизительно через 3 часа (верхний ряд графиков) и через приблизительно 24 часа (нижний ряд графиков). Число в нижнем правом углу каждого графика представляет процент клеток, подвергающихся апоптозу для каждой исследуемой группы. Через 3 часа приблизительно 5,39% интактных клеток D121 (то есть не имевших контактов со спленоцитами) подверглось апоптозу. Приблизительно 2,28% клеток D121, инкубированных со спленоцитами, вакцинированных контрольной вакциной, содержащей только буфер PBS, мышей подверглось апоптозу. Только приблизительно 5,19% клеток D121, инкубированных со спленоцитами мышей, вакцинированных содержащей ДНК пустого вектора контрольной вакциной, подверглось апоптозу. Точно так же приблизительно 5,15% клеток D121 подверглись апоптозу в случае, когда их инкубировали со спленоцитами мышей, вакцинированных контрольной вакциной, содержащей только ДНК muCCL21; тогда как приблизительно 11,46% клеток D121 подверглись апоптозу, если их инкубировали со спленоцитами мышей, вакцинированных контрольной вакциной, содержащей только ДНК muSurvivin. Поразительно, что через 3 часа приблизительно 18,44% клеток D121 подверглись апоптозу в случае, когда их инкубировали со спленоцитами мышей, вакцинированных вакциной по изобретению, содержащей как ДНК muCCL21, так и ДНК muSurvivin.
Подобным образом через 24 с помощью анализа FACS (проводимого для клеток, подвергшихся апоптозу) было обнаружено, что ни одна из интактных клеток D121 (то есть не имевших контактов со спленоцитами) не подверглась апоптозу. Приблизительно 8,46% клеток D121, инкубированных со спленоцитами мышей, вакцинированных контрольной вакциной, содержащей только буфер PBS, подверглось апоптозу. Только приблизительно 4,78% клеток D121, инкубированных со спленоцитами мышей, вакцинированных содержащей ДНК пустого вектора контрольной вакциной, подверглось апоптозу. Поразительно, что через 24 часа приблизительно 59,2% клеток D121 подверглись апоптозу, если их инкубировали со спленоцитами мышей, вакцинированных вакциной по изобретению, содержащей как ДНК muCCL21, так и ДНК muSurvivin.
ПРИМЕР 9. Получение ДНК-вакцины, кодирующей TIAP и мышиный антигенный пептид минорного комплекса гистосовместимости H60
Вектор pBudCE4.1, содержащий ДНК TIAP и мышиного антиген-минорного комплекса гистосовместимости H60 (приблизительно 1 мкг пДНК) электропорировали в свежеприготовленную аттенуированную Salmonella typhimurium (SL2707), используя Bio-Rad Pulser при 2,0 кВ, 25 мкF и 200 Ом согласно процедурам, рекомендуемым производителем. На фиг.20 показана схематическая диаграмма экспрессирующих векторов для Н60 и muSurvivin, встроенного в вектор.
Salmonella, содержащую вектор, отбирали на планшетах, содержащих зеоцин. Колонии собирали несколько дней и культивировали в течение ночи в бульоне LB (EM Science, Gibbstown, NJ) с добавленным зеоцином. Бактерии выделяли и отмывали фосфатно-буферным солевым раствором (PBS). Затем отмытые бактерии суспендировали в среде PBS при концентрации приблизительно 5×109 рекомбинантных Salmonella на миллилитр PBS, чтобы образовался раствор вакцины для дальнейшего использования.
Контрольные вакцины, состоящие из Salmonella, трансформированных только одним вектором - вектором, содержащим только ДНК muSurvivin, и вектором, содержащим только ДНК антигена минорного комплекса гистосовместимости Н60, также получали согласно той же процедуре.
Вакцины хранили в закрытых ампулах до дальнейшего использования. ДНК-плазмиды хранили при приблизительно -20°C до трансформации Salmonella.
ПРИМЕР 10. Вакцинация мышей ДНК-вакцинами примера 9
Мышей Balb/C (приблизительно по 8 мышей в исследуемой группе) вакцинировали ДНК-вакцинами примера 9 (приблизительно 5×108 рекомбинантных Salmonella в приблизительно 100 мкл PBS) посредством перорального принудительного питания три раза с интервалами в две недели.
ПРИМЕР 11. Анализ цитотоксичности спленоцитов, выделенных из мышей, вакцинированных ДНК-вакцинами примера 10
Спленоциты выделяли из мышей, вакцинированных в примере 10, и стимулировали облученными клетками CT-26. Через 5 дней спленоциты собирали и проводили анализ цитотоксичности против клеток CT-26 и клеток Yac-1 (NK-чувствительные T-клетки) в качестве мишеней. Степень специфического лизиса клеток определяли при соотношении E/T 25:1, 50:1 и 100:1 посредством 4-часового анализа высвобождения51Cr, как описано в Current Protocols in Immunology 3.11.4, Coligan, et al. Eds., John Wiley & Sons, Inc. (1994). Результаты графически представлены на фиг.21.
Результаты указывают на то, что спленоциты мышей, вакцинированных вакциной по настоящему изобретению, содержащей ДНК muSurvivin и H60, проявляют двухкратное или более увеличение лизиса клеток колоректального рака CT-26 по сравнению со спленоцитами, выделенными из мышей, вакцинированных пустым вектором, контрольными вакцинами с H60 и muSurvivin, при соотношении E/T 100:1. Очень слабый лизис Yac-1 наблюдали для всех вакцин при всех соотношениях E/T, указывая на то, что наблюдаемый лизис, вероятно, опосредован T-клетками.
ПРИМЕР 12. Оценка устойчивости к опухоли вакцинированных мышей
Приблизительно через 2 недели после третьей вакцинации мышей Balb/С примера 10 (приблизительно по 8 мышей на исследуемую группу) подвергали заражению мышиными клетками колоректального рака CT-26 в количестве приблизительно 1×105 (внутривенно; в/в).
Количество самопроизвольных метастазов клеток CT-26 в легкие оценивали приблизительно через 25 дней после в/в заражения клетками CT-26. Мышей умерщвляли и проводили вскрытие и опухолевые массы в легких оценивали, определяя среднюю массу легких из каждой группы. Нормальная масса легкого составляет приблизительно 0,2 грамма. На фиг.22 показаны типичные легкие (сверху), удаленные у вакцинированных зараженных CT-26 мышей. На фиг.22 также представлена диаграмма (снизу) средней массы легкого для каждой исследуемой группы. Значительное снижение опухолевой массы наблюдали у мышей, вакцинированных вакциной по изобретению с H60/muSurvivin, по сравнению с контрольными вакцинами.
На фиг.23 представлена диаграмма процентного соотношения мышей, выживших через 26 дней, для каждой исследуемой группы. Значительное увеличение выживаемости наблюдали у мышей, вакцинированных вакциной по изобретению с H60/muSurvivin, по сравнению с контрольными вакцинами.
ПРИМЕР 13. Оценка экспрессии H60 и muSurvivin в 293T-клетках
На фиг.24A проиллюстрирована экспрессия H60. 293T-клетки трансфецировали либо пустым вектором (V), либо pH60 (H) в течение 24 часов, собирали и окрашивали тетрамером NKG2D и анализировали посредством проточной цитометрии. Эффективность трансфекции составляла приблизительно 45%, как было определено с помощью трансфекции pGFP (зеленого флуоресцирующего белка). На фиг.24В проиллюстрирована экспрессия muSurvivin. 293T-клетки трансфецировали либо пустым вектором, либо pmuSurvivin в течение 24 часов, собирали, лизировали и анализировали вестерн-блоттингом. С помощью вестерн-блоттинга было обнаружено, что в трансфецированных клетках muSurvivin определяется, в отличие от нативных клеток, в которых он не определяется.
Часть B. Вакцины из дважды аттенуированных Salmonella typhimuriumAroA-, dam-
ПРИМЕР 14. Получение ДНК-вакцины, кодирующей muSurvivin и muCCL21
Полноразмерные кодирующие области мышиного сурвивина (muSurvivin) и мышиного CCL21 (muCCL21) амплифицировали посредством полимеразной цепной реакции с использованием обратной транскрипции суммарной РНК в количестве 1 мкг, экстрагированной из клеток карциномы легкого Льюиса D121 и активированных спленоцитов мышей соответственно. Суммарную РНК экстрагировали при помощи набора RNEASY® Mini (Qiagen, Valencia, CA) и OT-ПЦР проводили с помощью platinum quantitative RT-PCR thermoscript one-step system (Gibco/BRL) согласно инструкциям производителя. На основе вектора pBudCE4.1 (Invitrogen) было получено несколько конструкций с использованием продуктов ПЦР, созданных для независимой экспрессии двух генов из одной плазмиды, в экспрессирующих векторах млекопитающих. Первую конструкцию muSurvivn/muCCL21, содержащую полноразмерный мышиный сурвивин и мышиный CCL21, встраивали в участок мультиклонирования А между участками рестрикции HindIII и BamHI. Хемокин muCCL21 получали, встраивая ген в участок мультиклонирования В между участками рестрикции XhoI и NotI соответственно. Другие векторы, используемые для ДНК-вакцинации, были основаны скорее на первой конструкции, а не на отсутствии либо muCCL21, либо muSurvivin. В качестве контроля создали пустой вектор.
Экспрессию белка muSurvivin и muCCL21 обнаруживали с помощью вестерн-блоттинга клеточных лизатов после трансфекции плазмид в клетки COS-7 с использованием Ат против сурвивина и против CCL21 соответственно. Выраженность активности EGFP в пейеровых бляшках мышей C57BL/6J определяли у мышей после перорального введения трансформированной pEGFP Salmonella typhimurium (штамм AroA-, dam-RE88) в количестве 108. Мышей умерщвляли в моменты времени 8, 16 и 36 часов и свежие образцы тонкой кишки удаляли для анализа после тщательной отмывки PBS. Выраженность флуоресценции EGFP определяли при помощи конфокальной микроскопии.
Возможные токсические эффекты, вызываемые у хозяина аттенуированными бактериями, оценивали, сравнивая дважды аттенуированный штамм AroA-, dam-RE88 с однократно аттенуированным штаммом AroA-SL2707. Использование штамма RE88 привело к выживанию всех 16 мышей без каких-либо очевидных токсических побочных эффектов, тогда как 2 из 16 мышей, иммунизированных штаммом SL2707, умерли из-за токсичности и инфекции. Таким образом, мутация dam- в штамме RE88, которая контролирует бактериальную вирулентность, очевидно приводит к тому, что этот штамм является наиболее подходящим для использования в качестве носителя ДНК-вакцины.
ПРИМЕР 15. Заражение опухолью и пероральная вакцинация мышей вакциной примера 14
Мышей C57BL/6J разделяли на пять групп и 3 раза с интервалами в 2 недели проводили иммунизацию с помощью принудительного питания PBS в количестве приблизительно 100 мкл, содержащим приблизительно 1×108 дважды аттенуированных S.typhimurium (RE88), несущих любое из нижеследующего: пустой вектор pBUd; индивидуальные экспрессирующие векторы либо pBud-muSurvivn/muCCL21, либо pBud-muSurvivin, либо pBud-muCCL21 наряду с группами, получавшими PBS. Всех мышей в профилактических исследованиях заражали посредством в/в инъекций клетками карциномы легкого Льюиса D121 в количестве приблизительно 1×105 через приблизительно 1 неделю после последней иммунизации. В терапевтических исследованиях мышам сперва вводили в/в приблизительно 1×105 мышиных клеток карциномы легкого Льюиса D121, а через 1 неделю подвергали 3 вакцинациям трансформированными S.typhimurium. Мышей осматривали ежедневно, умерщвляли и проверяли метастазы в легких через приблизительно 28 дней после заражения опухолевыми клетками в профилактических исследованиях или через 63 дня после первоначальной инокуляции опухолевых клеток в терапевтической модели.
Оценки метастазирования опухолей после иммунизации либо PBS, либо пустым вектором, либо CCL21, либо сурвивином, либо вакциной CCL21/сурвивин, соответственно, вакцинами в профилактических целях показаны в таблице 3. Результаты в таблице 3 представлены в виде оценки метастазов, выраженной как % поверхности легкого, покрытого объединенными метастатическими очагами: 0 = отсутствие метастазов; 1 = менее чем 5%; 2 = от 5 до 50% и 3 ≥50%. Различия в оценках метастазирования между группами мышей, получавших вакцину CCL21/сурвивин и всеми контрольными группами являются статистически значимыми (P≤0,001). Ингибирование опухолевого роста также наблюдали в случае терапевтической модели.
В случае профилактического исследования авторы изобретения наблюдали несомненное подавление распространенных легочных метастазов мышиной карциномы легкого Льюиса D121 у мышей, которым проводили вакцинацию 3 раза с интервалами в 2 недели и затем заражали через 1 неделю посредством в/в инъекции опухолевых клеток. Действительно, 6 из 8 мышей полностью отторгали все легочные метастазы опухоли, в то время как оставшиеся животные показали заметно увеличенное подавление опухолевых метастазов (смотри таблицу 3). В отличие от этого, основанная на сурвивине ДНК-вакцина, в которой отсутствует muCCL21, вызывала полное подавление метастазов только у одного из 8 животных, у двух животных проявился менее чем 5% метастатический рост опухоли, в то время как у всех оставшихся мышей проявился обширный метастатический рост опухоли. В случае дополнительных животных, которым давали только контрольные вакцины либо с PBS, либо с пустым вектором, вообще не наблюдали никакой противоопухолевой защиты, и они умерли в течение 4 недель после заражения опухолевыми клетками вследствие обширного метастазирования. Хотя иммунизация дважды аттенуированными Salmonella, несущими только секреторную плазмиду, заметно не подавляла опухолевое метастазирование, она все же приводила к статистически значимым задержкам метастазирования по сравнению с контролями.
Важно, что основанная на muSurvivin/muCCL21 ДНК-вакцина также эффективно подавляля рост уже хорошо развитого легочного метастаза у всех экспериментальных животных в терапевтическом исследовании. В отличие от этого, у всех мышей, получающих только основанные на muSurvivin или muCCL21 вакцины per se или контроли с пустым вектором и PBS, выявили значительное распространение легочных метастаз немелкоклеточной карциномы легкого D121 в этом экспериментальном исследовании. Массы легких для различных экспериментальных групп в терапевтической модели представлены в таблице 4. Нормальная масса легкого составляла приблизительно 0,3 г.
ПРИМЕР 16. Определение антиангиогенных эффектов у вакцинированных мышей примера 15
Через две недели после последней вакцинации мышам подкожно (п/к) вводили в грудинные области приблизительно 500 мл Matrigel, фактора, снижающего рост (BD Biosciences), содержащего приблизительно 400 нг/мл мышиного FGF-2 (PeproTech, Rocky Hill, NJ), и опухолевые клетки D121 (1×104/мл), которые были облучены при 1000 Гр. У всех мышей, за исключением 2 контрольных животных, эндотелиальные ткани окрашивали спустя 6 дней посредством введения в латеральную хвостовую вену 200 мл флуоресцентного лектина I Bandeiraea simplicifolia, изолектина B4 (Vector Laboratories, Burlingame, CA.) в концентрации 0,1 мг/мл; приблизительно через 30 минут мышей умерщвляли и вырезали матригелевые пробки и оценивали их макроскопически. Лектин-FITC затем экстрагировали из 100 мл каждой пробки в 500 мл буфера для лизиса RIPA и количественно определяли при помощи флуорометрии при 490 нм. В каждом случае вычитали фоновую флуоресценцию, обнаруженную у двух контрольных мышей, которым ничего не вводили.
Основанная на muSurvivin/muCCL21 вакцина несомненно подавляла ангиогенез в сосудистой сети опухоли. Наблюдали значительное уменьшение образования новых сосудов в опухоли, как было показано с помощью анализа с применением матригеля и определения относительной флуоресценции, измеренной после окрашивания in vivo эндотелия мышей конъюгированным с FITC лектином. Невооруженным взглядом были видны различия в васкуляризации опухоли между группами, получавшими вакцину muSurvivin/muCCL212, и контрольными группами мышей после исследования репрезентативных матригелевых пробок, удаленных через 6 дней после п/к инъекции конъюгированного с FITC лектина. У мышей, вакцинированные вакциной по изобретению, наблюдали значительно меньшую васкуляризацию опухоли по сравнению с контрольными группами.
ПРИМЕР 17. Анализ цитотоксичности
Спленоциты выделяли у успешно вакцинированных мышей через 5 дней после заражения опухолевыми клетками. Цитотоксичность анализировали при помощи стандартного анализа высвобождения51Cr против либо клеток-мишеней опухоли D121, либо мышиных эндотелиальных клеток-мишеней с повышенной экспрессией сурвивина. Для того чтобы определить специфическую ограниченную по MHC I класса цитотоксичность, оценку ингибирования проводили с использованием Ат против H-2Kb/Db MHC I класса мыши (PharMingen, San Diego, CA) в концентрации 10 мкг/мл.
С помощью анализа высвобождения51Cr была обнаружена заметная цитотоксичность, вызванная специфическими CD8+ T-клетками, полученными у мышей после вакцинации и последующего заражения клетками карциномы легкого Льюиса D121. CD8+ T-клетки, выделенные из спленоцитов мышей, иммунизированных либо вакциной muSurvivin/muCCL21, либо вакциной muSurvivin per se, эффективно лизировали 50% и 30% клеток опухоли D121 соответственно. В отличие от этого, CD8+ T-клетки, выделенные из контрольных животных, были неэффективны в индукции какого-либо заметного уничтожения опухолевых клеток, поскольку для них наблюдали только фоновую цитотоксическую активность. Характерно, что наблюдаемая опосредованная CD8+ T-клетками цитотоксичность была ограничена по антигенам MHC I класса, поскольку цитотоксичность была полностью устранима при добавлении Ат против H2Kb/H2Db.
ПРИМЕР 18. Анализ с помощью проточной цитометрии и анализ высвобождения цитокинов
Маркеры активации T-клеток и экспрессии совместно стимулирующихся молекул на CD11c и DC, положительных по Ат MHC II класса, определяли с помощью проточной цитометрии с 2- или 3-цветовой маркировкой, используя BD Biosciences FACScan. Активацию T-клетки определяли, окрашивая свежевыделенные спленоциты успешно вакцинированных мышей меченным FITC Ат против CD3e в сочетании с конъюгированными с PE Ат против CD25, CD28 или CD69. Активацию совместно стимулирующихся молекул на APC измеряли с использованием меченного FITC Ат против CD11c и биотинилированного Ат против IAb, сопровождаемое стрептавидин-аллофикоцианином, и в сочетании с конъюгированными с PE Ат против ICAM-1, CD80 или DEC205. Все эксперименты проточной цитометрии проводили в присутствии 0,1 мкг/мл пропидиум иодида, чтобы исключить гибель клеток. Все реагенты для этих анализов получены от BDPharmingen (La Jolla, CA).
Проточную цитометрию использовали для определения внутриклеточных цитокинов. Для этого спленоциты выделяли из мышей B57BL/6J приблизительно через 2 недели после заражения клетками опухоли D121 и культивировали в течение приблизительно 24 часов в полной культуральной Т-клеточной среде вместе с облученными клетками D121, как описано ранее. Предварительно инкубированные клетки суспендировали с приблизительно 1 мг очищенного Ат 2.4G2 (BD Pharmingen), чтобы блокировать неспецифическое окрашивание. Клетки отмывали и затем окрашивали 0,5 мг конъюгированного с FITC Ат против CD3+. После 2-разового отмывания клетки фиксировали и окрашивали конъюгированными с PE Ат либо против IL2, либо против IFN-g в концентрации 1 мг/мл для анализа с помощью проточной цитометрии. Все Ат были получены от BD Pharmingen (La Jolla, CA.).
Оказалось, что только вакцина muSurvivin/muCCL21 per se была оптимально эффективна в заметной повышающей регуляции экспрессии T-клеточных маркеров активации CD25, CD28 и CD69. Повышающая регуляция CD28 является особенно важной, поскольку его взаимодействие с совместно стимулирующимися молекулами B7 на DC, как известно, необходимо для осуществления важных и множественных взаимодействий между нативными Т-клетками и антигенпрезентирующими DC. В отличие от этого, ДНК-вакцины, кодирующие только muSurvivin или muCCL21, per se способствовали увеличению экспрессии T-клеточных маркеров активации только 1-кратно. Вакцина muSurvivin/muCCL21 также обеспечивала активацию как CD4+, так и CD8+ T-клеток, на что указывало несомненное увеличение внутриклеточных провоспалительных цитокинов IFN-g и IL-2 в них. При сравнении с контролями с PBS и пустым вектором, а также с ДНК-вакцинами, кодирующими только muSurvivin или muCCL21, было обнаружено, что они значительно менее эффективны в индукции данных цитокинов.
Повышающая регуляция экспрессии ICAM-1, CD80 и DEC205 на DC, которая вызывается основанной на muSurvivin/muCCL21 ДНК-вакциной, особенна важна, поскольку хорошо известно, что активация T-клеток чрезвычайно сильно зависит от сильных межклеточных взаимодействий с данными совместно стимулирующимися молекулами, экспрессированными DC, для того чтобы достичь оптимального связывания с Т-клеточными рецепторами. Более того, иммунизация дважды аттенуированными Salmonella typhimurium, несущими эукариотические плазмиды, кодирующие muSurvivin/muCCL21, вызывала самую эффективную повышенную регуляцию данных маркеров активации, которая была в 2-3 раза выше, чем в контролях.
ПРИМЕР 19. Анализ апоптоза опухолевых клеток.
Апоптоз в клетках опухоли D121, вызванный вакцинацией, измеряли через приблизительно 3 часа и через приблизительно 24 часа после вакцинации соответственно. Как контрольных, так и экспериментальных животных заражали в/в клетками D121 в количестве приблизительно 1×105 клеток через 1 неделю после последней из 3 иммунизаций. Собирали спленоциты из каждой индивидуальной мыши через 1 неделю после заражения опухолевыми клетками и после этого приблизительно 2,5×107 спленоцитов культивировали в течение 4 часов совместно с клетками D121 в количестве приблизительно 5×105 в 6-луночных планшетах. Набор для определения апоптоза ANNEXIN®V-FITC apoptosis detection kit II (BD Biosciences Pharmingen, San Diego, CA) использовали для подтверждения апоптоза на ранней стадии. Для того чтобы подтвердить апоптоз клеток опухоли на поздней стадии, приблизительно 5×105 клеток D121 и приблизительно 2,5×107 спленоцитов совместно культивировали в течение 24 часов и затем анализировали при помощи FACS для апоптоза посредством анализа TUNEL с использованием набора APO-DIRECT™ (BD Biosciences Phramingen, San Diego, CA) согласно инструкциям производителя.
Апоптоз наблюдали уже через 3 часа, со значительным дальнейшим увеличением через 24 часа, что было показано в результате анализа данных, полученных с помощью проточной цитометрии с применением либо Annexin V, либо TUNEL. Таким образом, апоптоз на ранней стадии был от 3 до 4 раз выше в группах мышей, иммунизированных вакциной muSurvivin/muCCL21, чем в контролях, после того, как собранные из таких мышей спленоциты были совместно инкубированны с опухолевыми клетками. Вакцина, кодирующая один muSurvivin, вызывала некоторый апоптоз, но только в один раз выше, чем в контролях. Однако заметное увеличение апоптоза на 85% наблюдали через 24 часа только у мышей, иммунизированных вакциной muSurvivin/muCCL21, что позволяет предположить, что причиной данного явления был вызванный CTL устойчивый иммунитет опухолевых клеток.
ПРИМЕР 20. Получение ДНК-вакцины, кодирующей muSurvivin и H60
Плазмида, содержащая полноразмерный мышиный лиганд для NKG2D H60, была любезно предоставлена доктором A. Diefenbach и D. H. Raulet (University of California, Berkeley, CA). Экспрессирующие векторы конструировали на основе pBudCE4.1 (Invitrogen), как описано выше.
Дважды аттенуированные S.typhimurium (AroA-, dam-) трансформировали плазмидами ДНК-вакцин посредством электропорации, как описано ранее.
Кратко, свежеприготовленные бактерии (приблизительно 1×108), в середине логарифмической фазы роста, смешивали с ДНК плазмиды (1-2 мкг) на льду в 0,1-см кювете и электропорировали при приблизительно 2,0 кВ, 25 мкФ и 100 Ω. Устойчивые колонии, несущие векторы ДНК-вакцины, культивировали и хранили при -80°C после подтверждения кодирующих последовательностей.
ПРИМЕР 21. Заражение опухолью и пероральная вакцинация мышей вакциной примера 20
Группы мышей BALB/c A2Kb (n = 4-12) иммунизировали дважды с интервалами в 2 недели при помощи принудительного питания PBS в количестве приблизительно 100 мкл, содержащим приблизительно 5×108 дважды аттенуированных S.typhimurium, несущих экспрессирующие векторы. Мышей BALB/c заражали в/в клетками CT-26 в количестве 1×105 через 2 недели после последней вакцинации в профилактических моделях и за 5 дней до первой вакцинации - в терапевтических исследованиях. Мышей умерщвляли через 25 или 28 дней после заражения опухолью и определяли метастазирование легких и массы опухолей соответственно и сравнивали с контролями. Для определения статистической значимости разницы результатов между экспериментальными группами и контролями использовали t-критерий Стьюдента. Результаты считались значимыми, если двустороннее значение P составляло <0,05.
Эксперссию H60 и muSurvivin подтверждали путем трансфекции 293T-клетки и проверяя при помощи проточной цитометрии или вестерн-блоттинга. Эксперссию H60 подтверждали положительным окрашиванием тетрамера NKG2D. Тестирование клеток подтвердило их трансфекцию сурвивином, на что указывала единственная полоса в области ожидаемой молекулярной массы приблизительно 16,5 кДа. При сравнении с положительным контролем, клетками Yak-1, оказалось, что уровень экспрессированного СТ-26 лиганда NKG2D относительно низок. Как ранее сообщалось, опухолевые клетки с низкими уровнями экспрессии лиганда NKG2D не вызывают отторжение опухоли. В профилактическом исследовании массу легких и оценки метастазирования (как описано выше) определяли после умерщвления мышей через 25 дней после заражения опухолью. Результаты показаны в таблице 5 и таблице 6. Как видно из результатов, вакцины с H60 и muSurvivin по отдельности защищали мышей до некоторой степени, тогда как сочетание H60 и muSurvivin (вакцина muSurvivin/H60) значительно усиливало противоопухолевую защиту, как продемонстрировано значительно более низкими оценками метастазирования и сниженными массами опухоли в легких. Полученные данные являлись статистически значимыми, когда их сравнивали с контрольными группами с PBS, pBud, pH60 и pmuSurvivin (p<0,0001, 0,002, 0,01 и 0,005 соответственно).
В терапевтических иследованиях, то есть на фоне развившихся метастазов карциномы толстой кишки, опухолевую массу легкого оценивали после умерщвления на 28 день. Существенно, что 8 из 12 мышей, получавших вакцину H60/muSurvivin, выжили и, что еще более важно, у 2 из выживших животных полностью отсутствовали метастазы, в то время как у 2 других менее чем 5% поверхности легкого было покрыто объединенными опухолевыми метастазами. В контрольной группе, получавшей пустой вектор pBud, выжило только 2 мыши и более чем 50% поверхности легких всех выживших мышей было покрыто объединенными опухолевыми метастазами. В случае вакцинирования вакциной только с muSurvivin не наблюдали какой-либо значительной защиты в терапевтической модели, а лечение вакциной только с H60 имело минимальный терапевтический эффект. Последнее предположение было сделано исходя из того, что слегка увеличивалась степень выживания и что у одной из выживших мышей только <5% поверхности легких покрывали объединенные опухолевые метастазы.
ПРИМЕР 22. Анализ цитотоксичности
Цитотоксичность определяли посредством стандартного анализа высвобождения51Cr, как описано выше. Вкратце, спленоциты собирали через 2 недели после последней вакцинации и стимулировали их in vitro облученными (1000 Гр) клетками CT-26 при 37°C в течение 5 дней в RPMI 1640, дополненной 10% FBS, L-глутамином, 15 мМ HEPES, заменимыми аминокислотами, пируватом натрия, 2-ME и рекомбинантным IL-2 в количестве 20 ед./мл (PeproTech, Rocky Hill, NJ). Спленоциты собирали и разделяли с использоваем среды для отделения клеток Lympholyte-M (Cedarlane Laboratories Limited, Hornby, Ontario, Canada). Клетки-мишени метили51Cr в течение приблизительно 1,5 часов при комнатной температуре и инкубировали с эффекторными клетками при различных соотношениях эффекторных клеток и клеток-мишеней при приблизительно 37°C в течение 4 часов. Процент специфического лизиса клеток-мишеней вычисляли по формуле [(E-S)/(T-S)]×100, где E представляет собой среднюю величину экспериментального высвобождения, S представляет собой среднюю величину самопроизвольного высвобождения и T представляет собой среднюю величину полного высвобождения.
Было обнаружено значительное повышение уровня активности NK у мышей, иммунизированных вакциной H60, и даже более высокий уровень лизиса NK-клетками наблюдали у мышей, иммунизированных вакциной muSurvivin/H60. Спленоциты мышей, иммунизированных вакциной muSurvivin/H60, проявляли самую высокую цитотоксичность против клеток-мишеней CT-26. В отличие от этого, спленоциты, выделенные у контрольной группы, иммунизированной pBud, проявляли минимальную цитотоксичность, тогда как данные спленоциты из мышей, вакцинированных вакциной H60 или muSurvivin, per se показали более высокую цитотоксичность. Оказалось, что через 5 дней клеточного культивирования NK-клетки не играли основной роли в проявлении цитотоксичности, поскольку не наблюдали значительного отличия в случае использования Yac-1 в качестве клеток-мишеней NK, на основании чего предположили, что обнаруженная цитотоксичность, главным образом, опосредована CTL.
Многочисленные изменения и модификации описанных выше осуществлений изобретения можно произвести, не отступая от сущности и объема изобретения. Никоим образом не предполагается и не должно подразумеваться ограничение изобретения приведенными здесь иллюстративными вариантами его осуществления.
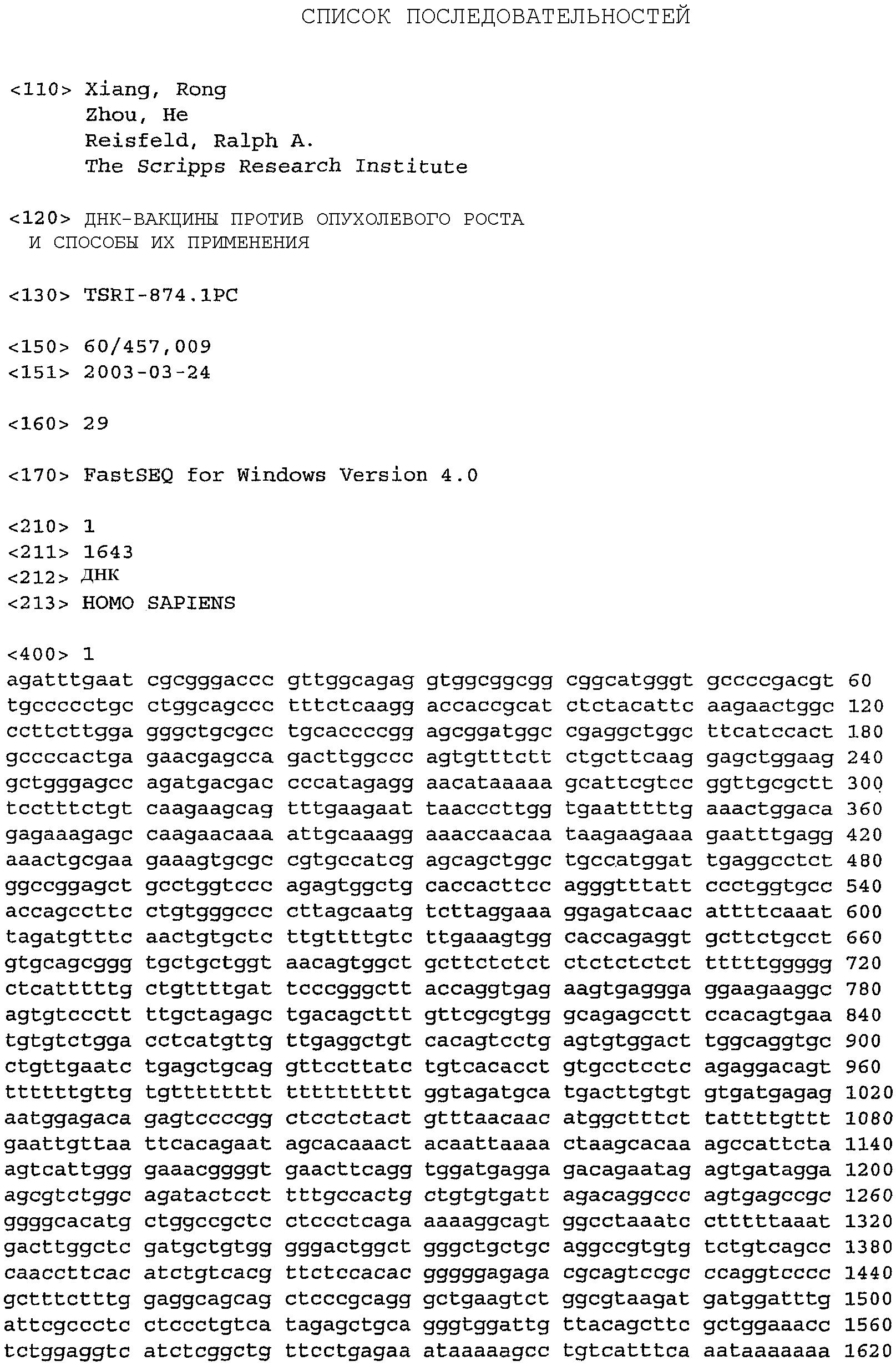





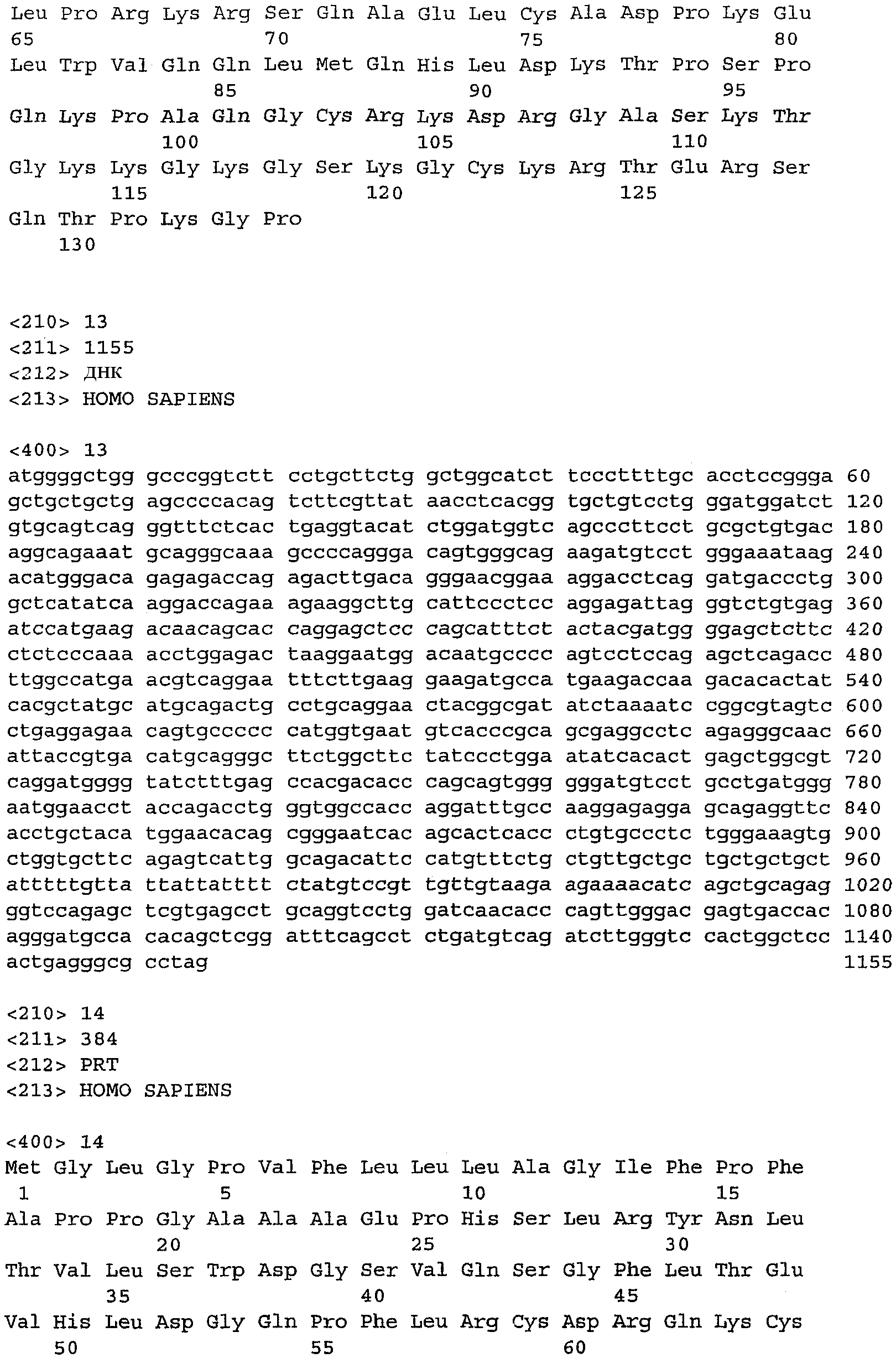






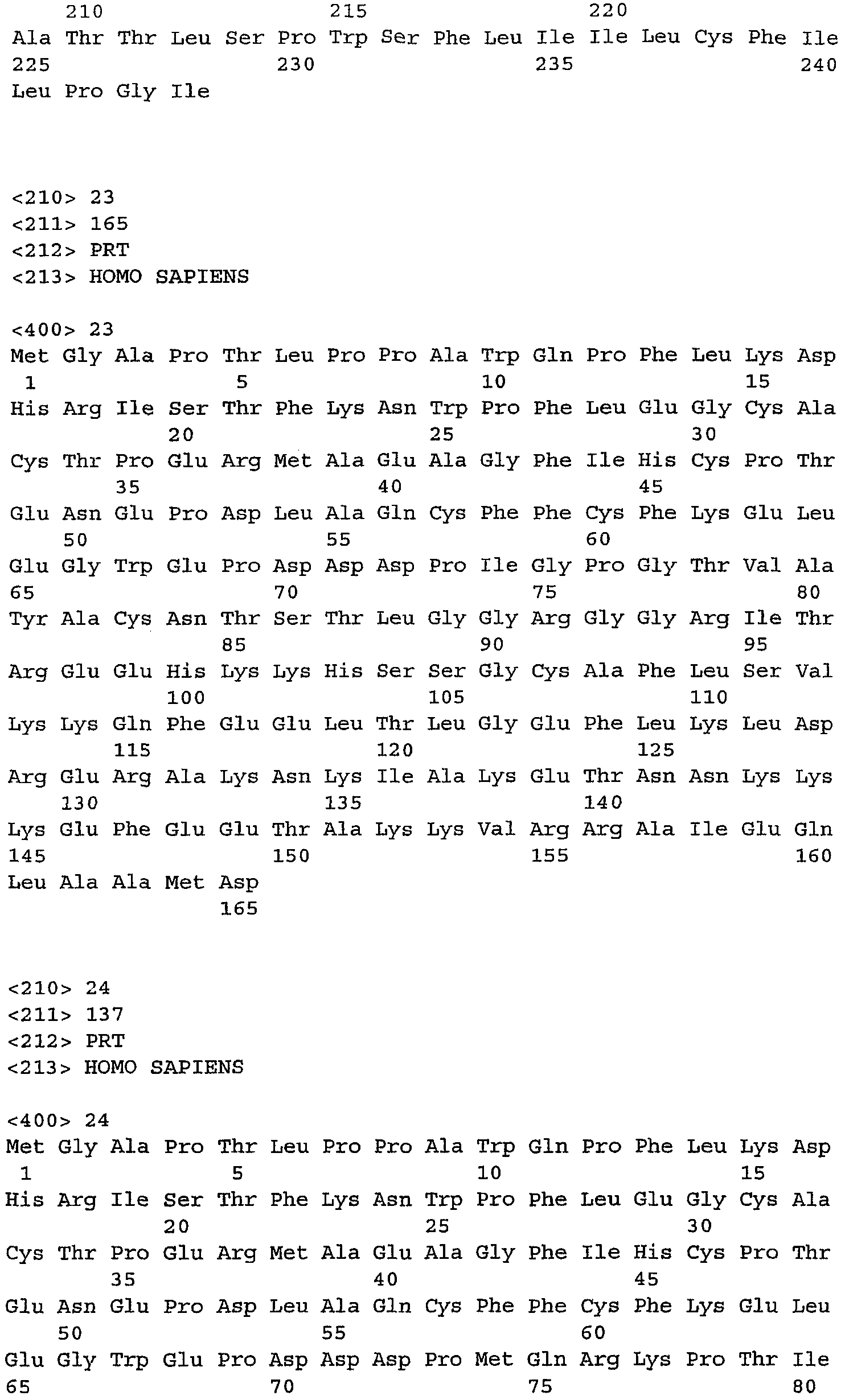





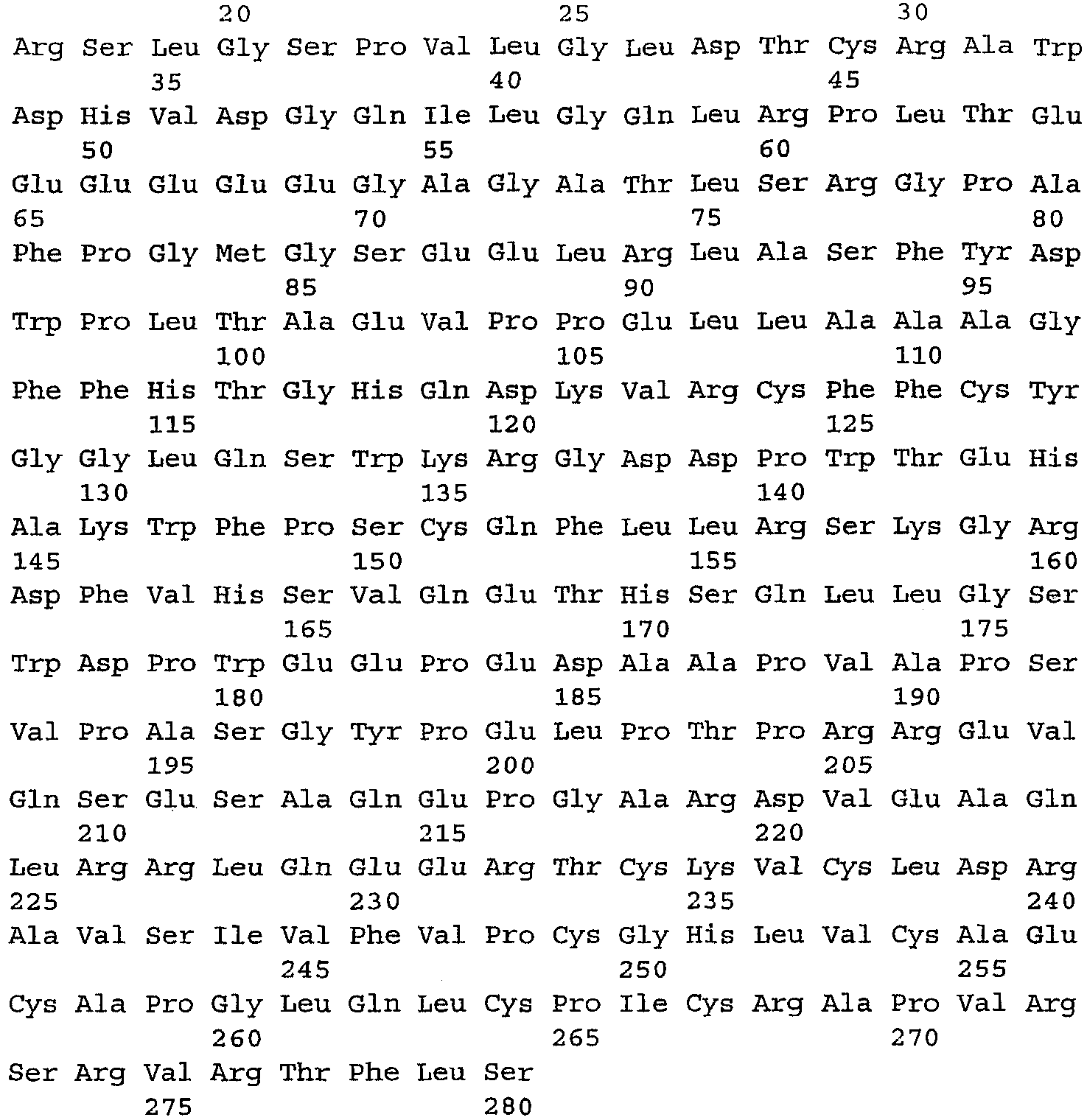
Реферат
Изобретение относится к биотехнологии. Описана ДНК-вакцина, предназначенная для активации иммунного ответа против раковых клеток, содержащая конструкцию ДНК, операбельно кодирующую белок сурвивин и цитокин CCL21, встроенные в аттенуированный вектор Salmonella typhimurium. Раскрыт способ ингибирования роста опухоли путем введения вакцины по изобретению млекопитающему. Представлено изделие, содержащее описанную вакцину. Предложен способ вакцинации млекопитающего против рака, где способ включает стадию введения млекопитающему эффективного количества описанной ДНК-вакцины, вызывающей иммунный ответ. Изобретение расширяет ассортимент ДНК-вакцин, вызывающих иммунный ответ, и обладает неожиданно высоким уровнем цитотоксичности против опухолевых клеток. 4 н. и 17 з.п. ф-лы, 42 ил., 6 табл.

Комментарии