Вирус козьего артрита-энцефалита, обеспечивающий иммунную защиту от инфекции вич-1 - RU2194529C2
Код документа: RU2194529C2
Чертежи















Описание
Изобретение относится в широком смысле к области иммунологии и медицины и, более конкретно, к способам обеспечения иммунной защиты от инфекции ВИЧ-1.
Число заболеваний синдромом приобретенного иммунодефицита (СПИД) достигло уровня эпидемии, особенно в странах третьего мира - в Африке, Азии и Карибском бассейне. Несмотря на миллиарды долларов, расходуемые на исследования с целью найти средство для лечения этого заболевания, достигнут лишь небольшой прогресс в области лекарств, которые могут замедлить развитие заболевания.
Возбудителем СПИД'а является вирус иммунодефицита человека (ВИЧ-1). ВИЧ-1 инфицирует особый тип клеток иммунной системы, Т-клетки. Попадая в Т-клетку, геномная ДНК ВИЧ-1 встраивается в геном Т-клетки, где она направляет синтез вирусных белков. Из инфицированной Т-клетки секретируются новые копии, которые далее инфицируют новые Т-клетки. В конечном счете инфицированные Т-клетки умирают и иммунная система инфицированного ВИЧ-1 человека ослабляется и не может противостоять последующим инфекциям. В результате жертвы СПИД'а, как правило, умирают от инфекций, которые обычно у здорового индивидуума вызвали бы, в худшем случае, легкое недомогание.
Первоначально лечение СПИД'а сводилось к способам лечения инфекций, возникавших в результате ослабления иммунного ответа. Позднее было найдено, что такие лекарственные препараты, как AZT (азидотимидин) и ddI, которые известны как аналоги нуклеозидов, могут препятствовать репликации ДНК ВИЧ-1. Эти препараты, особенно в комбинации, могут продлевать жизнь больных СПИД'ом. Еще позднее сообщалось, что класс лекарственных препаратов, называемых ингибиторами протеаз, является более эффективным для ингибирования репликации ВИЧ-1. Предполагали, что ингибиторы протеаз, возможно, в сочетании с нуклеозидными аналогами, сделают жизнь больного СПИД'ом еще более продолжительной и даже вылечат его.
Так как применение препаратов, как описано выше, приводит к уничтожению вируса у инфицированных ВИЧ-1, такие лекарства применимы только тогда, когда человек уже инфицирован; они не оказывают действия на активацию иммунной системы. Ясно, что более предпочтительным подходом к прекращению эпидемии СПИД'а прежде всего было бы предотвращение ВИЧ-1 инфекции. Логическим выбором в качестве средства для предотвращения ВИЧ-1 инфекции являются вакцины, которые стимулируют иммунный ответ человека на действующее вещество вакцины. Например, применялись вакцины для предотвращения или уменьшения тяжести различных вирусных заболеваний, включая полиомелит, корь, оспу и грипп. Кроме того, вакцина может стимулировать иммунную систему человека, уже инфицированного вирусом.
Применялись многочисленные способы усовершенствования вакцины, которая повысила бы сопротивляемость инфицированию вирусом СПИД'а. Однако, хотя были созданы и испытаны в клинических условиях различные ВИЧ-1 вакцины, каждая из них имеет серьезные ограничения. Например, вакцины подгруппы, созданной из частей белка ВИЧ-1, дают только временную или малоэффективную защиту. Одним из препятствий, мешающих улучшению вакцины является то, что ВИЧ-1 при репродукции претерпевает быструю мутацию. В результате стимулированный иммунный ответ на конкретный белок ВИЧ-1 или штамм ВИЧ-1 является малоэффективным по отношению к измененной форме вируса. Более того, антитела к участку поверхности ВИЧ-1, которые должны быть самыми активными в вакцине, на самом деле стимулируют ВИЧ-1-инфекцию.
Также предлагались ослабленные вакцины, которые содержат живые, но дефектные по репродукции вирусы. Однако введение такого вируса ВИЧ-1 человеку, особенно здоровому в других отношениях, должно быть оправданным. Таким образом, существует необходимость в вакцине, которая обеспечивает универсальный иммунный ответ на ВИЧ-1, но без сопутствующего риска и ограничений, связанных с применением ВИЧ-1 в качестве реагента для вакцинации. Данное изобретение удовлетворяет этому требованию и дает дополнительные преимущества.
Вирус козьего артрита-энцефалита (CAEV) представляет собой ретровирус, который сходен с вирусом иммунодефицита человека (ВИЧ-1), который вызывает СПИД у людей. Известно, что CAEV поражает коз, вызывает у них различные патологии, включая артрит и энцефалит. Инфекция CAEV встречается во всем мире и может привести к дорогостоящим потерям в животноводстве, связанном с разведением коз.
Во многих частях земного шара обычно потребляют козье молоко и, особенно в малоразвитых странах, оно представляет собой важный источник пищи. Однако в этих странах козье молоко редко пастеризуют перед потреблением его человеком. Также потребление сырого козьего молока увеличивается в Соединенных Штатах вследствие спроса на здоровую пищу.
В соответствии с настоящим изобретением в настоящее время признано, что CAEV-подобные вирусные формы могут инфицировать людей (h-CAEV), особенно тех, кто по роду своей работы контактирует с козами, или тех, кто потребляет сырое козье молоко. Хотя еще не доказано, вызывает ли CAEV патологические состояния у людей, близость CAEV и ВИЧ-1 предполагает, что лучше всего было бы свести к минимуму присутствие CAEV-инфекции у людей.
Хотя в молочном скотоводстве делались попытки предотвратить распространение CAEV у коз, заражение людей формами, адаптированными к человеку, до сих пор не было известно. Следовательно, необходим способ (метод) диагностики человека. Такой метод диагностирования CAEV-инфицированных индивидуумов был бы полезен для идентификации запасов крови, зараженной CAEV. В частности, важно иметь способ обнаружения CAEV-инфекции в запасах крови, так как энцефалит, связанный с CAEV-инфекцией, может встречаться только у детей раннего возраста, получающих инфицированную кровь при внутривенном вливании. К сожалению, ни один удобный метод не пригоден для идентификации наличия CAEV-инфекции у людей. Таким образом, необходим простой и недорогой способ диагностирования наличия CAEV-инфекции. Настоящее изобретение удовлетворяет этому требованию и дает дополнительные преимущества.
Данное изобретение предлагает вакцину, содержащую иммуноген вируса козьего артрита-энцефалита (CAEV), предпочтительно CAEV человека, и фармацевтически приемлемый носитель. Вакцина по данному изобретению применима, например, для стимуляции иммунозащитной реакции на CAEV-перекрестную защитную иммунную реакцию на вирус-1 иммунодефицита человека (ВИЧ-1) у индивидуума и для вакцинации человека или другого млекопитающего (кроме коз) от инфекции CAEV.
Данное изобретение также предлагает способ стимулирования иммунной реакции у индивидуума на CAEV или ВИЧ-1 введением ему CAEV-иммуногена. Такой способ применим, например, для повышения сопротивляемости заражению (инфекции) ВИЧ-1 или CAEV у человека, ранее не зараженного ВИЧ-1 или CAEV соответственно, или облегчить состояние, вызванное ВИЧ-1 у больного, инфицированного ВИЧ-1, или CAEV у больного, инфицированного CAEV. Далее, данное изобретение предлагает способ стимуляции иммунной реакции in vitro путем контакта лимфоцита с CAEV-иммуногеном.
Данное изобретение также предлагает способы диагностирования заражения вирусом козьего артрита-энцефалита (CAEV) у субъектов, подозреваемых в том, что они инфицированы CAEV. Например, данное изобретение предлагает способ твердофазного иммуносорбентного анализа (ELISA), отличающийся тем, что gp135 CAEV прикреплен к твердой подложке (носителю), и тем, что при контакте gp135 CAEV с образцом, например с образцом иммунной сыворотки, взятой у индивидуума, предпочтительно зараженного CAEV, определение (обнаружение) в сыворотке антитела, которое связывается с gp135 CAEV, и представляет собой то, что лежит в основе диагностики инфекции CAEV у этого индивидуума. Другие способы включают тесты на основе PCR. Данное изобретение также предлагает набор для осуществления такого диагностического подхода, как ELISA или теста на основе нуклеиновой кислоты.
На фиг. 1 изображено диагностическое древо, сравнивающее gag-последовательности CAEV с gag-последовательностями других лентивирусов. PCR (полимеразную цепную реакцию) и RT-PCR (полимеразную цепную реакцию с обратной транскрипцией) и клонирование и секвенирование продуктов PCR осуществляли, как описано в Примере I.D. Различные последовательности анализировали, и их порядковые номера такие, как описано в Примере I.D. Все относящиеся к CAEV последовательности заключены в рамку на фиг. 1. Все другие последовательности являются лентивирусными за исключением JSR (ретровирус овцы Яагзикте (Jaagsiekte)), который служит в качестве анцестральной (родовой) распознаваемой последовательности на фиг. 1. Для анализа 173 упорядоченных (выравненных) gag-сайтов, из которых 157 изменялись на фиг. 1, а 65 изменялись на фиг. 2, применяли оптимизированный (parsimony) алгоритм PAUL 3.1.1. Две из применявшихся опций представляли собой рандомизацию входа последовательности и MULPARS. Оптимизацию (parsimony) с обратным множителем применяли на фиг. 1, как описано в Примере I.D., получая длины ветвей, непропорциональные изменениям одиночного нуклеотида, но обеспечивающие наибольшие относительные расстояния для включенных последовательностей с высокой дивергенцией. Одно древо с наивысшей оптимизацией (most parsimonious) было обнаружено на фиг. 1 и порядок его разветвления был в дальнейшем подтвержден анализом "ближайших соседей" и анализом древа с использованием фрагментов гена полимеразы.
На фиг. 2 дан анализ филогенетического древа, сравнивающий gag-последовательности CAEV с gag-последовательностями друг с другом, как описано в Примере I. D. Обычная оптимизация показана на фиг. 2 (так как все эти последовательности тесно связаны) и, соответственно, длины ветвей выражены в единицах минимальных нуклеотидных изменений. Последовательность является распознаваемой (опозновательной) анцестральной (родовой) последовательностью. На фиг. 2 были получены два равно оптимизированных (parsimonious) древа, которые по существу не отличались.
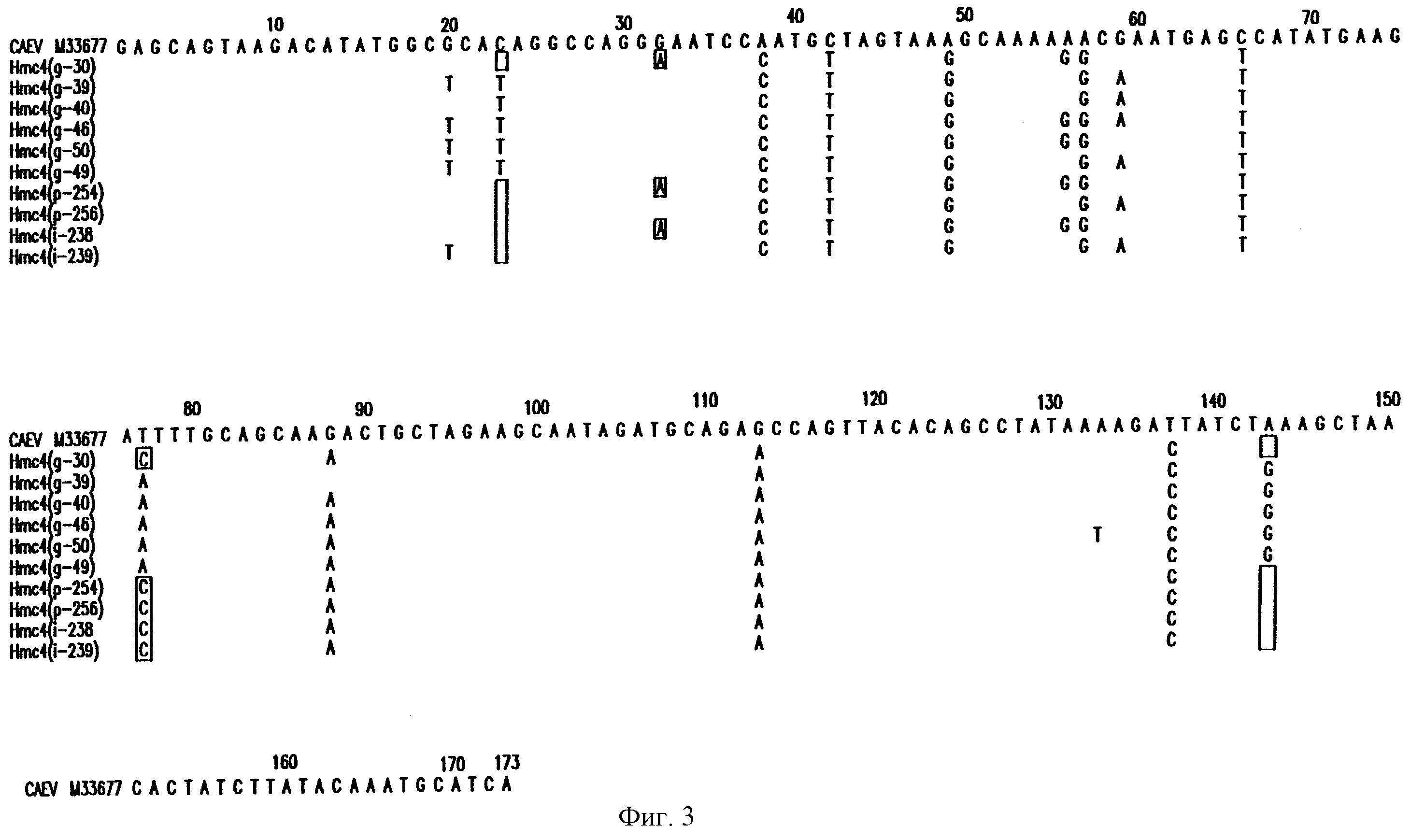
На фиг. 3 сравнивается нуклеотидная последовательность PCR-амплифицированных образованных из Hmc4 клонов gag CAEV человека с соответствующей областью инфицирующего CAEV козы, как описано в Примере I.I. Анализируемые клоны представляли собой геномные клоны Hmc4 g-30, g-39, g-40, g-46 и g-50; плазматические клоны Hmc4 p-254 и р-256; клоны из эксперимента по заражению (инфицированию) i-238 и i-239. "i"-клоны были получены из цитоплазмы инфицированных культур. Клоны "р" были получены из плазмы инфицированных пациентов.
На фиг. 4 сравнивается нуклеотидная последовательность PCR-амплифицированных полученных из клонов полимеразы Hmc4 CAEV человека с соответствующей областью с двумя CAEV инфицированных коз, как описано в Примере I.I.
На фиг. 5 непосредственно сравнивается последовательность полученных из коз штаммов CAEV CAEV-CO и gWa19 (т.е. CAEV-79-63) и h-CAEV штаммов человека Hmc1 и Hmc4.
Данное изобретение предлагает вакцину, содержащую иммуноген вируса козьего артрита-энцефалита (CAEV), предпочтительно адаптированного к человеку штамма CAEV, и фармацевтически приемлемый носитель. Как раскрывается ниже, вакцина по данному изобретению применима для стимуляции иммунозащитной реакции на ВИЧ-1 у человека. Кроме того, вакцина по данному изобретению применима для вакцинации человека или другого млекопитающего (кроме коз) от заражения CAEV.
Употребляемый ниже термин "иммуноген CAEV", означает CAEV-вирусную частицу, которая может быть живым, ослабленным или убитым CAEV, или иммуногенный участок CAEV-вирусной частицы, или пептидный фрагмент CAEV-белка, например пептидный фрагмент гликопротеина gp135 оболочки (см. Таблица 1; env). CAEV-иммуноген характеризуется тем, что он может стимулировать иммунную реакцию как in vivo, так и ex vivo. В частности, CAEV-иммуноген может стимулировать иммунную реакцию на CAEV при введении индивидууму и может стимулировать перекрестно-реактивный иммунный ответ на ВИЧ-1. Перекрестно-реактивный иммунный ответ на ВИЧ-1, который вызывается инфекцией CAEV, напоминает перекрестно-реактивный иммунный ответ на вирус оспы, который вызывается инфекцией коровьей оспы.
Пептидный фрагмент белка 70К, присутствующий в комплексе рибонуклеопротеида U1, который гомологичен аминокислотной последовательности ВИЧ-1, может вести себя как суррогатный иммуноген, который стимулирует иммунную реакцию, перекрестную с ВИЧ-1 (Douvas and Takehana. AIDS Res. Hum. Retrovir. 10: 253-262 (1994). Как раскрывается ниже, различные пептидные фрагменты белков CAEV гомологичны последовательностям 70К и ВИЧ-1 и, следовательно, могут применяться в качестве CAEV-иммуногенов для стимулирования иммунной реакции, перекрестной с ВИЧ-1, у человека.
Примеры пептидных фрагментов CAEV, гомологичные аминокислотным последовательностям 70К и ВИЧ-1, даны в Таблице 1. Другие примеры пептидных фрагментов CAEV, рассматриваемые ниже с соответствующими структурными особенностями в ВИЧ-1 (ВИЧ-1 --> CAEV), включают, например: 220-FAILKS--> 200-FAILKS (шарнир); 99-DMVEQM-->415-DMVEHM (α-спираль 1); 129-LKCTDL-->203-LKCTKW (консервативный поворот); 300-NNNTRT-->480-NNNTIT (консервативный поворот) и т. п. Другие такие петиды CAEV могут быть идентифицированы с помощью исследования ДНК- или аминокислотной последовательности CAEV с целью идентификации CAEV-пептидов, гомологичных иммунологически гомологичным последовательностям 70К и ВИЧ-1 (Douvas and Takehana, supra, 1994). Далее, ниже раскрываются способы обнаружения того, какие CAEV-пептиды, гомологичные пептидам 70К и ВИЧ-1, применимы в качестве CAEV-иммуногенов, включая такие способы, как ELISA или вестерн-блоттинг или реакция нейтрализации вируса (Пример I), или другие, известные в технике (см, например, Harlow and Lane, Antibodies: A laboratory manual (Cold Spring Harbor Laboratory Press 1988).
Употребляемый ниже термин "вакцина" означает композицию, содержащую иммуноген, который при введении индивидууму, представляющему собой обычно млекопитающее (кроме козы), например человеку и т. п., стимулирует в индивидууме иммунную реакцию (иммунный ответ). В частности, вакцина по данному изобретению содержит CAEV-иммуноген, который можно вводить, например, человеку. отличающийся тем, что он стимулирует иммунный ответ на CAEV, перекрестно-реактивный с ВИЧ-1. Таким образом, CAEV-иммуноген применим в качестве суррогатного иммуногена для стимулирования иммунного ответа на ВИЧ-1. Особенно предпочтительной вакциной является ослабленная ч-CAEV, например, такая, как таковые, представленные на фиг. 3 и 4.
Хотя ниже рассматривается с целью применения любой инфекционный CAEV, наиболее предпочтительными CAEV для применения ниже являются новые адаптированные к человеку штаммы CAEV, называемые ниже "CAEV человека, ч-CAEV", например, штаммы больных Hmc1 и Hmc4, описанные в Примере II, частичная геномная последовательность которых представлена на фиг. 3 и 4. Было найдено, что CAEV человека отличаются от CAEV, способных инфицировать коз. Например, в геномной области, соответствующей нуклеотидному фрагменту 173, амплифицированному праймерами, изображенными SEQ ID No 16 и 17, было найдено, что эта конкретная область вируса CAEV человека содержит, по меньшей мере, две мутации, присущие исключительно человеку (встречающиеся лишь у человека). Эти мутации соответствуют гуанину в положении 56 и цитозину в положении 77 внутри продукта амплификации gag-области 173.
Таким образом, в соответствии с другим вариантом данного изобретения, предложены новые изолированные CAEV человека. CAEV человека по данному изобретению можно выделить методами, описанными в Примере III, или используя методы, хорошо известные в технике.
Признано, что вакцину по данному изобретению можно вводить индивидууму, который не инфицирован ВИЧ-1, в этом случае вакцина стимулирует иммунный ответ, который может защитить индивидуума от инфекции вследствие контакта с ВИЧ-1, или можно вводить ВИЧ-1-инфицированному человеку, и в этом случае вакцина может стимулировать иммунный ответ так, чтобы противостоять иммунопатологии ВИЧ-1 (см. , например, Cease and Berzofsky, Ann. Rev. Immunol. 12:923-989 (1994)). Таким образом вакцину по данному изобретению можно применять для повышения сопротивляемости человека ВИЧ-1-инфекции или для облегчения тяжести патологии, вызванной ВИЧ-1 у ВИЧ-1-инфицированного индивидуума.
До данного открытия не было известно, что CAEV может инфицировать людей. Как обнаружено ниже, однако, CAEV-инфекция у людей распространена, особенно в популяциях, у которых потребление сырого козьего молока является общепринятым или где представители населения каким-либо другим образом контактируют с козами (см. Пример I.C.). Хотя еще не установлено, вызывает ли инфекция CAEV патологию, например, артрит или энцефалит у человека, как это происходит у коз, если такая, вызванная CAEV, патология существует, тогда важно вакцинировать людей, работающих в животноводстве и связанных с козами, от заражения CAEV. Вакцина по данному изобретению может применяться для этой цели. Кроме того, метод диагностики ELISA, как ниже показано, может применяться для обнаружения зараженных CAEV и может быть особенно полезен, например, для скрининга (исследования) системы кровоснабжения с целью идентификации крови, зараженной CAEV, что, таким образом, предотвращает распространение инфекции CAEV при введении крови, содержащей CAEV.
Так как сейчас найдено, что CAEV инфицирует людей, признается вероятность того, что CAEV также может инфицировать других млекопитающих (не коз), включая, например, нечеловекообразных приматов (например, обезьян и тому подобное), коров, лошадей, овец, собак, кошек и других млекопитающих. Таким образом ELISA по данному изобретению может применяться для диагностирования инфекции CAEV у любого такого млекопитающего ("не козы"). Далее, если найдено, что CAEV инфицирует других таких млекопитающих, вакцину по данному изобретению можно применять для предотвращения или ограничения распространения инфекции CAEV у этих млекопитающих ("не коз").
Как раскрывается ниже, контакт индивидуума с CAEV также может стимулировать иммунный ответ на CAEV, перекрестно-реактивный с ВИЧ-1 (Пример I.E.). CAEV представляет собой ретровирус, подтип лентивирусов, который близок вирусу-1 иммунодефицита человека (ВИЧ-1). CAEV инфицирует коз и вызывает артрит и отклонения (ненормальности) в иммунной системе инфицированных животных (см. , например, Banks et al., Arthrit. Rheum. 30:1046-1053 (1987); Crawford et al., Science 207:997-999 (1980)).
Вирус висны/мэди (VMV) представляет собой другой лентивирус, который тесно связан с CAEV и ВИЧ-1 и вызывает у овец заболевание, близкое к таковому, вызываемому CAEV у коз. Таким образом, ниже рассматривается то, что VMV или иммуногенный фрагмент VMV может быть заменен на CAEV или, если нужно, может применяться в сочетании с CAEV-иммуногеном в вакцине по данному изобретению. Вакцина, содержащая иммуноген VMV, применяется для стимуляции иммунного ответа у человека, который перекрестно реагирует на ВИЧ-1.
CAEV вызывает устойчивую инфекцию у коз и ассоциируется с тремя болезненными синдромами, включая артрит, который возникает у 20-30% инфицированных животных; лейкоэнцефалит, поражающий молодых животных; и единичные неврологические заболевания взрослых коз. Как обнаружено, инфекция CAEV широко распространена в мире и выявлена как причина артрита и энцефалита коз в 1980 г. В 1985 и 1986 г.г. описано сходство между нуклеотидными и аминокислотными последовательностями CAEV и ВИЧ-1 (затем названный HTLV-III). CAEV и ВИЧ-1 очень сходны филогенетически и имеют высокую степень гомологии, включая, например, между их РНК-зависимыми полимеразами ДНК (роl) и между gp120/41 в ВИЧ-1 и gp135/38 в CAEV (см., например, Gonda et al., Proc. Natl. Acad. Sci. . USA 83:4007-4111 (1986); Gonda et al., Retroviridae 3:83-109 (1994); Garry et al., Retroviridae 4:491-603 (1995).
CAEV передается среди коз через зараженное молоко, особенно через молозиво, и инфекция распространяется благодаря практике в сельском хозяйстве объединять запасы молозива для кормления молодых животных. CAEV размножается в клетках моноцитарно/макрофагальной линии и в клеточной линии фибробластов, но не инфицирует Т-клетки. Макрофаги, экспрессирующие CAEV, распределяются в синовии, легких, центральной нервной системе, лимфатических узлах, селезенке, желудочно-кишечном тракте и молочных железах инфицированных коз.
До настоящего открытия не было известно, что CAEV инфицирует человека. Однако обнаружение сероконверсии с помощью ELISA и вестерн-блоттинга на образцах крови человека (Пример I.C.), и провирусной ДНК, соответствующей gag и pol генам CAEV, анализом геномной ДНК больного MCTD с помощью полимеразной цепной реакции (PCR) (Пример I.D.) дает наглядное доказательство того, что CAEV инфицирует людей. Внедрение последовательностей вирусной ДНК в ДНК клетки-хозяина есть признак заражения лентивирусами, включая CAEV и ВИЧ-1.
Исходя из представленных ниже результатов CAEV, по-видимому, заражена половина населения Мексики и Центральной Америки, в особенности те, кто потребляет сырое козье молоко, что распространено в этих местах, или как-либо иначе соприкасаются с козами (см. Пример I.C.). Хотя нет доказательства, что CAEV вызывает патологическое состояние у человека, важно, тем не менее, определить размер распространения CAEV-инфекции в человеческой популяции, чтобы идентифицировать, коррелируется ли патология неизвестной этиологии с инфекцией CAEV. Анализ ELISA, приведенный ниже, позволяет проводить рутинный скрининг CAEV-инфекции у людей и дает дополнительное преимущество, так как применим для скрининга других млекопитающих, кроме козы, с целью определения CAEV-инфекции.
Также проводился анализ PCR геномной ДНК, полученной от трех групп коз из разных географических районов и от инфицированных CAEV индивидуумов (см. Пример I. D. ). PCR-анализ геномной ДНК человека и козы идентифицировал, по меньшей мере, два потенциальных штамма CAEV, которые отличаются от последовательности ДНК эталонного штамма CAEV (последовательность ДНК эталонного CAEV имеет в каталоге GenBank (Генбанка) N М33677). Следует заметить, что иммунные ответы, вызванные в двух или трех группах коз, инфицированных CAEV, и у нескольких инфицированных CAEV индивидуумов, были перекрестно-реактивными в отношении ВИЧ-1, что указывает, что любой из этих штаммов может быть использован в качестве источника иммунного CAEV для вакцины по данному изобретению.
Инфицированные CAEV козы использовали в качестве животных моделей для ревматоидного артрита человека, который является наиболее известным и широко распространенным синдромом в группе артритных/аутоиммунных расстройств, системных ревматических расстройств. Системные ревматические расстройства у женщин встречаются примерно в три раза чаще, чем у мужчин.
Смешанная соединительнотканная болезнь (MCTD) представляет собой еще одно системное ревматическое заболевание. Для MCTD характерны аутоантитела к комплексу сплайсинга U1 snRNP. Считают, что MCTD является общим синдромом, который охватывает клинические и серологические особенности, общие для трех других системных ревматических расстройств системного волчьего эритематоза (SLE), склеродермы и полимиозита. Клинический профиль MCTD включает артрит, лимфаденопатию, васкулит, миозит, синдром Шегрена (лимфоцитарная инфильтрация слюнных и слезных желез) и нарушение регуляции иммунной системы.
Клинический профиль, очевидный в MCTD-индивидуумах, также проявляется у индивидуумов, инфицированных ВИЧ-1. Однако эти клинические проявления имеют более тяжелое течение и менее поддаются лечению у ВИЧ-1-инфицированных индивидуумов. Например, синдром Шегрена у MCTD-индивидуумов характеризуется локализованной лимфоцитарной инфильтрацией, тогда как обширная гландулярная инфильтрация, называемая синдромом диффузного инфильтрационного лимфоцитоза, встречается при соответствующем ВИЧ-1-ассоциированном синдроме.
Тяжелый, вызывающий некроз васкулит, сопровождаемый невропатией, воспалительной полимиопатией, не связанной с лекарственной терапией, и другие формы сосудистого и нервно-мышечного заболевания, ассоциированного с ревматическими нарушениями (расстройствами), также возникают у ВИЧ-1-инфицированных индивидуумов. Вызывающая некроз лимфаденопатия, приводящая к серьезнейшему разрушению структуры лимфатического узла, происходит при заражении MCTD, SLE и ВИЧ-1. Два классических ревматических расстройства, псориатический артрит и синдром Рейтера, являются самыми ранними проявлениями заражения ВИЧ-1 и наименее поддающимися действию химиотерапевтических агентов, когда они связаны (ассоциированы) с ВИЧ-1-инфекцией.
Клиническое сходство инфекции ВИЧ-1 и системных ревматических расстройств, например MCTD, подтверждает, что ВИЧ-1 может вызывать ревматические патологии или что филогенетически родственный (близкий) более клинически неопасный лентивирус представляет собой этиологический фактор при ревматических нарушениях (расстройствах). Серологически MCTD характеризуется наличием антител RNP (рибонуклеопротеид), специфических к частице U1 snRNP, которая располагается на 5'-конце интронов во время сплайсинга ядерной РНК. Антитела против RNP также присутствуют у некоторых больных SLE и склеродермией. Частицы U1 snRNP состоят из центральной части U1 РНК и кластера РНК-связывающих белков, включая более 70К, А и С. Антитела против RNP ингибируют сплайсинг РНК, связывая U1 snRNP.
Хотя реакция гуморально анти-RNP-аутоантитела является патогномоничной в MCTD, белок 70К, например, содержит эпитопы как Т-клеток, так и В-клеток и гуморальные и клеточные аутоиммунные манифестации зависят друг от друга. Были выделены клоны Т-клеток, отвечающие на эпитопы 70К, и они включают CD8+ Т-клетки, обладающие цитотоксической Т-лимфоцитарной активностью, и CD4+ Т-клетки, проявляющие активность Т-хелперов. Некоторые из эпитопов Т-клеток 70К гомологичны эпитопам Т-клеток ВИЧ-1 (см. Douvas and Takehana, supra, 1994). Как раскрывается ниже, белки CAEV, включая CAEV gp135, также содержат эпитопы, которые гомологичны эпитопам Т-клеток 70К и ВИЧ-1 (см. Таблица 1). Таким образом, иммуноген CAEV, содержащий такой эпитоп, может вызывать универсальный перекрестно-реактивный иммунный ответ на ВИЧ-1.
Ввиду клинического сходства ВИЧ-1-инфекции и MCTD и идентификации CAEV-инфекции у индивидуумов с MCTD или в других отношениях здоровых индивидуумов, важно было выяснить, развивается ли у индивидуумов, инфицированных CAEV, иммунный ответ, перекрестно-реактивный с ВИЧ-1. Степень иммунитета по отношению к белку ВИЧ-1, gp120, в крови, взятой у инфицированных CAEV индивидуумов, изучали анализом ELISA и вестерн-блоттингом (см. Пример I.E.). Кроме исследования сходства между CAEV-инфекцией и роста иммунной реакции на ВИЧ-1, исследовали сходство между CAEV-инфекцией и MCTD. Так как некоторые больные MCTD из Мексики или Центральной Америки имеют антитела, которые реагируют на gp120 ВИЧ-1 и ингибируют инвазионную способность in vitro, остается установить, появляется ли также у CAEV-инфицированных индивидуумов, не имеющих MCTD, иммунитет против ВИЧ-1.
Как раскрывается в данном описании, инфекция CAEV у людей, страдающих ли MCTD, или в других отношениях здоровых, стимулировала гуморальную иммунную реакцию, перекрестно-реактивную в отношении вирусного антигена gp120 или р24 ВИЧ-1 (см. Пример I.E.). Следует заметить, что ни один из исследованных индивидуумов не был ВИЧ-1-инфицирован, что определяли, применяя официальные клинические анализы. Эти результаты показывают, что иммунизация индивидуума иммуногеном CAEV может вызвать перекрестно-реактивный иммунитет против ВИЧ-1-инфекции, таким образом повышая сопротивляемость ВИЧ-1-инфекции у неинфицированных индивидуумов или облегчая тяжесть патологии вследствие ВИЧ-1 у ВИЧ-1-инфицированных индивидуумов. Далее, наличие общего (системного) ревматического расстройства, например MCTD, у CAEV-инфицированного больного значительно повышало степень ВИЧ-1 перекрестной реактивной способности (Пример. I.E.). Таким образом, введение иммуногена CAEV, предпочтительно, в сочетании с аутоантигеном, связанным с MCTD, например, иммуногена 70К, который вызывает перекрестно-реактивный иммунный ответ на ВИЧ-1 (Douvas and Takehana, supra, 1994), может быть особенно эффективным для стимулирования иммунного ответа перекрестно реагирующего на ВИЧ-1 у человека.
Иммуноген CAEV может быть иммуногенным сам по себе или может быть соединен с молекулой носителя, например с альбумином телячьей сыворотки, или инертным носителем, так чтобы комплекс иммуноген-носитель мог стимулировать иммунный ответ (см., например, Harlow and Lane, supra, 1988). Например, если вакцина содержит целый вирус CAEV, вирус является иммуногенным и может стимулировать иммунную реакцию у вакцинированного. CAEV легко доступен в Американской Коллекции Культур Клеток (ФТСС VR-905).
Вакцина по данному изобретению также может содержать участок пептида белка CAEV, например, gp135 (см. Таблица 1, supra). Выяснено, что каждый из пептидов, приведенных в Таблице 1 или иначе примененных в данном изобретении, может сам по себе не быть иммуногенным. Однако хорошо известно, что такие гаптены могут соединяться с молекулой носителя так, что становятся иммуногенными (см. , например, Harlow and Lane, supra, 1988). Иммунная реакция может стимулироваться in vivo и ex vivo. Например, иммунные клетки, включая Т-клетки и В-клетки, можно взять у субъекта и поместить в культуральную среду ткани. Затем клетки могут контактировать с иммуногеном CAEV, который может стимулировать иммунные клетки и индуцировать иммунную реакцию Т-хелпера и цитоксической Т-клетки.
Вакцина по данному изобретению содержит, помимо иммуногена CAEV, фармацевтически приемлемый носитель. Фармацевтически приемлемые носители хорошо известны в технике и включают водные растворы, например физиологически забуференный солевой раствор, или другие растворители или носители, такие как гликоли (диолы), глицерин, масла, например оливкое масло, или пригодные для инъекций сложные органические эфиры. Адъюванты, например, квасцы и полный или неполный адъювант Фрейнда или другие подходящие адъюванты известны в технике и промышленно доступны (Ribi Immunochem Research, Inc.; Hamilton MT). Добавление адъюванта обычно снижает количество иммуногена CAEV, требуемого для стимуляции иммунной реакции.
Фармацевтически приемлемый носитель также может содержать физиологически подходящее соединение, которое реагирует, например, стабилизируя иммуноген CAEV или повышая его адсорбцию. Физиологически подходящее соединение включает, например, углеводы, такие как глюкоза, сахароза или декстрины; антиоксиданты, такие как аскорбиновая кислота или глутатион; хелатирующие агенты; низкомолекулярные белки; или другие стабилизаторы или наполнители. Специалист в данной области знает, что выбор фармацевтически приемлемого носителя, включая физиологически подходящее соединение, зависит, например, от способа введения вакцины и, в особенности, от физико-химических характеристик иммуногена CAEV. В технике известны различные способы введения вакцины для стимуляции иммунной реакции; они включают, например, внутривенную, внутрикожную и подкожную инъекции, оральное и трансдермальное введение.
Если необходимо, вакцина по данному изобретению может также содержать иммуноген 70К или его пептидный фрагмент, который является суррогатным иммуногеном (иммуногеном-заместителем), стимулирующим иммунный ответ, перекрестно-реактивный в отношении ВИЧ-1 (Douvas and Takehana, supra, 1994). Полезно добавлять в вакцину иммуноген 70К, так как он является аутоиммунным белком, который обогащен последовательностями, которые могут стимулировать ранние общие клоны, представляющие собой латентные Т-клетки и В-клетки анти-70К, которые могут легко активироваться для реакции с ВИЧ-1 или могут продуцировать антитела, перекрестно реагирующие на gp120/41, нейтрализующие ВИЧ-1. Добавление иммуногена 70К полезно также потому, что он способствует коамплификации или синергетической амплификации общих клонов с gp120/41. Кроме того, можно отобрать иммуногенные фрагменты 70К, не содержащие аминокислотных последовательностей, которые стимулируют антитела, опосредующие (разрушительное) вредное воздействие, ассоциированное с ВИЧ-1-инфекцией (Douvas and Takehana, supra, 1994).
Иммуноген CAEV может быть получен различными способами, включая, например, технику рекомбинантной ДНК или с помощью методов органического синтеза. Например, если нужен белок CAEV или его пептидный фрагмент, белок или его пептидный фрагмент можно получить клонированием кодирующей последовательности соответствующего CAEV в экспрессирующий вектор, например вектор бакуловируса, и белок или пептид могут экспрессироваться соответствующей клеткой-хозяином и изолироваться от нее. Последовательность нуклеиновой кислоты CAEV можно получить в GenBank, No. M33677 (см. также Saltarelli et al., Virology 179:347-364 (1990); Knowles et al., J. Virol. 65:5744-5750 (1991). Кроме того, желательно (получить) продуцировать рекомбинантный белок или пептид в клетке млекопитающего, которая может осуществить заданную пост-трансляционную модификацию. Соответствующие векторы экспрессии и клетки-хозяева хорошо известны в технике и промышленно доступны, и специалисты в данной области знают, как выбрать соответствующую систему вектор/клетка-хозяин, исходя из конкретных нужд.
Если выбранный иммуноген CAEV является пептидным иммуногеном, как например, иммуногены CAEV, представленные в Таблице 1, пептид можно синтезировать, используя хорошо известный способ химического синтеза, включая, например, автоматизированные твердофазные методы. Химический синтез иммуногена CAEV может быть особено желателен, так как он дает возможность вводить аминокислотные аналоги в пептид. Например, нужно синтезировть иммуноген CAEV, содержащий одну или несколько замен (D)-аминокислот вместо соответствующих природных (L)-аминокислот. Внедрение (D)-аминокислоты может придать иммуногену CAEV желательные свойства, включая, например, повышенную устойчивость пептида, что может быть особенно полезным для приготовления вакцины, которая распространяется в регионах мира, где охлаждение (рефрижирация) не всегда доступно или надежно. Кроме того, пептид CAEV может быть синтезирован и, если нужно, может содержать дополнительный цистеиновый остаток, который может облегчить специфическое соединение пептида с матрицей или молекулой носителя, например, как "ключ-замок" гемоцианина блюдечка, применяя соответствующие условия окисления.
Данное изобретение также предлагает способ стимулирования иммунного ответа индивидуума на CAEV или стимулирование перекрестно-реактивного иммунного ответа на ВИЧ-1 введением терапевтически эффективного количества иммуногена CAEV субъекту. Если требуется, иммуноген CAEV можно заменить на ВМВ (VMV) или иммуногенный фрагмент ВМВ. Далее, может оказаться полезным вводить индивидууму иммуноген 70К, или в сочетании с иммуногеном CAEV или VMV, или самостоятельно.
Хотя ниже говорится о введении иммуногена CAEV индивидууму или применении для вакцинации индивидуума, обнаружено, что иммунный ответ на ВИЧ-1 можно стимулировать in vivo или ex vivo. Каждый из этих способов (охватывается) входит в объем данного изобретения. Например, может оказаться нужным стимулировать иммунный ответ на ВИЧ-1 ех vivo, если индивидуум, подлежащий лечению, болен СПИД'ом. В этом случае у индивидуума должны быть взяты лимфоциты и иммунизированы в культуре. В то же самое время популяция лимфоцитов может быть увеличена. Стимулированные, подращенные иммунные клетки затем снова вливают индивидууму, таким образом обеспечивая индивидууму лечебный эффект. Далее, если даже способ по данному изобретению, например, иммунизация и реинфузия (повторное, обратное вливание) ех vivo, не оказывает лечебного воздействия, такая терапия может быть паллиативной и, следовательно, может улучшить (качество) жизнь индивидуума, страдающего СПИД'ом.
Как показано ниже, вакцинация индивидуума иммуногеном CAEV стимулирует перекрестно-реактивный иммунный ответ на ВИЧ-1. Вакцинация против ВИЧ-1 иммуногеном CAEV, либо одним, либо в сочетании с иммуногеном 70К дает значительные преимущества, например, перед убитой или ослабленной формой ВИЧ-1 или антигеном белка ВИЧ-1 в качестве вакцины, о CAEV которой неизвестно, чтобы он был патогенным по отношению к человеку, и он не инфицирует Т-клетки. Кроме того, инфекция CAEV, особенно у индивидуумов, страдающих MCTD, обеспечивает универсальную иммунологическую (сопротивляемость) устойчивость к ВИЧ-1, включая реакцию В-клеток и реакцию Т-клеток на различные штаммы ВИЧ-1. Например, из изученных в Примере I индивидуумов испанского происхождения более 60% были инфицированы CAEV (см. Пример I.D.). Кроме того, 22% инфицированных CAEV, но в других отношениях здоровых индивидуумов перекрестно реагировали на ВИЧ-1 и 55% инфицированных CAEV больных MCTD перекрестно реагировали на ВИЧ-1 (Пример I.E.). Контролируемые способы иммунизации иммуногеном CAEV, одним или в сочетании с иммуногеном 70К, могут увеличить число индивидуумов, проявляющих перекрестно-реактивный иммунитет в отношении ВИЧ-1 (см. Пример II).
Чтобы стимулировать иммунную реакцию на ВИЧ-1, индивидууму вводят терапевтически эффективное количество иммуногена CAEV. Употребляемый ниже термин "терапевтически эффективное количество" означает количество иммуногена, требуемое для стимуляции иммунной реакции. Количество иммуногена, например иммуногена CAEV, которое соответствует терапевтически эффективному количеству, меняется в зависимости, например, от того, происходит ли стимуляция иммунного ответа in vivo или ex vivo, от того, является ли этот прием (введение) первичным или бустерным; от того, вводится ли адъювант с иммуногеном; и, если вводится (принимается) in vivo, то от способа введения. Вообще терапевтически эффективное количество иммуногена CAEV составляет от примерно 50 мкг до примерно 50 мг, предпочтительно составляет от примерно 500 мкг до примерно 5 мг. Например, если вводится вирус CAEV, терапевтически эффективное количество иммуногена CAEV в виде частиц может быть от примерно 100 мкг до примерно 2 мг, тогда как при введении растворимого иммуногена CAEV терапевтически эффективное количество может составлять от примерно 1 мг до примерно 5 мг. Способы определения терапевтически эффективного количества иммуногена рутинны и хорошо известны в технике (см. Пример II; см. также Powell and Newman, Vaccine Design: The subunit and adjuvant approach (Plenum Publ. Corp.; 1994).
Способы вакцинации индивидуума с целью стимуляции иммунного ответа также хорошо известны (Harlow and Lane, supra, 1988). Например, иммуноген можно вводить внутрикожно, внутримышечно или внутривенно. Кроме того, может быть лучше сделать одну или более бустерных иммунизаций. Необходимость проведения бустерной иммунизации и время такой бустерной иммунизации можно определить экспериментально, определяя (измеряя) антитела анти-ВИЧ-1 в сыворотке вакцинированного индивидуума, используя способы, раскрытые ниже.
Способ по данному изобретению можно применять для повышения сопротивляемости ВИЧ-1-инфекции индивидуума, ранее не подвергавшегося воздействию ВИЧ-1. Аналогично, способ по данному изобретению может применяться для повышения устойчивости к инфекции CAEV человека или другого подверженного заболеванию млекопитающего (кроме коз), ранее не подвергавшегося воздействию CAEV. Употребляемый ниже термин "повышение (увеличение) сопротивляемости (устойчивости)" в применении к инфекции ВИЧ-1 или CAEV означает, что вероятность инфекции, вызванной вирусом, уменьшается вследствие стимуляции иммунного ответа на вирус и последующего размножения запоминающих иммунных клеток, которые быстро могут быть мобилизованы против и могут изолировать последующую вирусную инфекцию. В случае CAEV устойчивость повышается вследствие вакцинации иммуногеном CAEV или ВМВ (VMV) соответственно, тогда как в случае ВИЧ-1 устойчивость повышается вследствие вакцинации иммуногеном CAEV или ВМВ, который стимулирует перекрестно-реактивный ответ на ВИЧ-1.
Далее способ по данному изобретению можно применять в случае индивидуумов, включая человека и млекопитающего (не коз), которые в настоящее время инфицированы вирусом и страдают от патологии вследствие инфекции. В частности способ введения иммуногена CAEV человеку с целью стимулировать иммунный ответ у ВИЧ-1-инфицированного индивидуума, перекрестно реагирующего на ВИЧ-1, может применяться для снижения иммунопатологии ВИЧ-1. Конкретно, стимулирование такого ответа у ВИЧ-1-инфицированного индивидуума может предотвратить дальнейшее распространение ВИЧ-1-инфекции у индивидуума, таким образом, истощение Т-клеток у индивидуума. Так как многие из патологий, наблюдаемые у ВИЧ-1-инфицированных индивидуумов, возникают вследствие истощения иммунной системы, терапия, которая снижает истощение иммунной системы, может быть полезной (дать эффект).
Исходя из раскрытых ниже исследований видно, что значительная часть населения, особенно в Мексике и Центральной Америке, по-видимому, инфицирована CAEV. Таким образом, важно, чтобы был доступен простой и недорогой способ, лежащий в основе диагностики индивидуума, инфицированного CAEV.
В соответствии с этим данное изобретение далее предлагает способы диагностики инфекции CAEV у млекопитающих (не коз), предпочтительно у человека, предпочтительно инфицированного CAEV. Примеры способов, лежащих в основе диагностирования инфекции CAEV, включают тесты ELISA, PCR-амплификацию, анализы с помощью нуклеотидного зонда и тому подобное.
В одном варианте изобретения, например, предлагается твердофазный иммуноферментный анализ (ферментный иммуносорбентный тест ELISA), применимый для определения (диагностики) наличия инфекции CAEV у индивидуума, предположительно инфицированного CAEV, путем взятия образца, например, крови у индивидуума, контактированием образца с антигеном CAEV и обнаружением связывания антитела против CAEV, находящегося в образце, с антигеном CAEV; такое обнаружение (определение) и представляет собой то, что лежит в основе диагностики инфекции CAEV. Таким образом, способы и реагенты для осуществления методов диагностики по данному изобретению раскрываются ниже или они известны в технике (см. , например, Litt, Патент США 4,092,408, выданный 30 мая 1978, вводимый в данное описание в виде ссылки).
Примером способа по данному изобретению является ELISA (Пример I.C.), в котором в качестве антигенга CAEV применяли gp135 CAEV. Однако антиген CAEV, применимый в способе по данному изобретению, можно выбрать практически из любого антигенного фрагмента CAEV или им может быть частица полного вируса CAEV. При описании способа по данному изобретению полагают, что термин "антиген CAEV" является синонимом термина "иммуноген CAEV", определяемого выше.
Конкурентный тест ELISA может быть особенно полезен как способ диагностики инфекции CAEV в образце, взятом у индивидуума. Конкурентный тест ELISA осуществляют аналогично стандартному ELISA за исключением того, что в реакцию в качестве конкурента с антителом анти-CAEV, имеющимся в образце, вводят одно или более моноклональных антител, каждое из которых является специфическим по отношению к эпитопу CAEV; примеры таких эпитопов, определяемых иммуногенами CAEV, даны в Таблице 1. Применение конкурентного теста ELISA может вызвать повышеную чувствительность при обнаружении антитела анти-CAEV в образце. Способы проведения конкурентного теста ELISA, такие как метод рецептора порогового лиганда Бюхлера (Buechler et al. ) (Патент США 5,089,391, выдан 18 февраля 1992 г.
Моноклональные антитела, специфичные к конкретным эпитопам CAEV, можно получить, применяя хорошо известные методы (см., например, Harlow and Lane, supra, 1988). Например, можно иммунизировать мышь иммуногеном CAEV (см., например, Таблицу 1); затем берут клетки селезенки мыши с высоким титром антител к конкретному иммуногену CAEV. Способы идентификации антитела иммуногена анти-CAEV с соответствующими специфичностью и сродством (аффинностью) и, следовательно, применимого по данному изобретению, раскрываются ниже, либо они известны в технике и включают, например, твердофазные иммуноферментные анализы, радиоиммунные анализы и анализы с помощью преципитина (см. Пример I; см. также Harlow and Lane, supra, 1988, chap. 14). Клетки селезенки мыши можно слить с соответствующей клеточной линией миеломы, например, клетки миеломы SP/02 или P3Ч653.Ag8, для получения клеток гибридомы. Клонированные клеточные линии гибридомы можно подвергнуть скринингу, применяя меченый иммуноген CAEV для определения клонов, секретирующих моноклональные антитела, специфичные к иммуногену CAEV. Гибридомы, экспрессирующие антитела с заданными специфичностью и аффинностью можно выделить и использовать в качестве непрерывного (длительного) источника моноклональных антител для конкурентного теста ELISA.
Применяемый в данном описании термин "образец" в отношении метода диагностики по данному изобретению, означает пробу ткани или пробу жидкости, например крови, которая может представлять собой цельную кровь, плазму или сыворотку, или пробу мочи, взятой у индивидуума, например человека или другого млекопитающего, кроме козы, с целью определения инфекции CAEV. Способы получения такого образца, включая образец соответствующей ткани, хорошо известны в технике и являются стандартными.
Способ по данному изобретению позволяет диагностировать инфекцию CAEV у индивидуума частично вследствие присутствия антител против CAEV в образце, взятом у индивидуума. Образец, взятый у индивидуума, предпочтительно инфицированного CAEV, контактирует с антигеном CAEV в соответствующих условиях, которые позволяют антигену CAEV связываться в образце с антителом против CAEV, если оно присутствует. Таким образом, способом по данному изобретению может являться ELISA, приведенный в описании в качестве примера, им (способом) может быть радиоиммунный метод анализа, вестерн-блоттинг или другой такой способ, в основе которого лежит обнаружение специфического взаимодействия антитело-антиген (см. , например, Harlow and Lane, supra, 1988; см. также Gribnau et al., Патент США 4,373,932, выданный 15 февраля 1983 г, введеный в данное описание ссылкой).
Способы обнаружения (определения) взаимодействия антиген-антитело, например, взаимодействия антигена CAEV с антителом против CAEV, присутствующим в образце, хорошо известны в технике и включают, например, применение антигена, меченого в поддающейся обнаружению степени или меченого в такой же степени вторичного антитела, которое представляет собой антитело, специфично связывающее антитело конкретного класса, например, IgG, IgA, IgM, IgA, IgD или IgE конкретных видов млекопитающих (см., например, Greene and David, Патент США 4, 376,110, выданный в августе 1983 г.). Например, если образец представляет собой образец сыворотки крови или образец плазмы крови человека, вторичный образец может быть козий античеловеческий IgG (см. Пример I. C.). Такие вторичные антитела можно получать хорошо известными способами или приобрести готовые, выпускаемые промышленностью. Способы получения антигена и антитела CAEV, меченого в степени, поддающейся обнаружению, также хорошо известны в технике и являются стандартными.
gp135 CAEV был выбран в качестве антигена в приводимом примере ELISA, потому что наличие антител против gp135 в иммунной сыворотке индивидуума помимо того, что указывает на наличие инфекции CAEV у индивидуума, также показывает, что индивидуум может иметь антитела, перекрестно реагирующие с ВИЧ-1. В действительности у 22% индивидуумов, определяемых как инфицированные CAEV методом ELISA CAEV, также были антитела перекрестно-реактивные с ВИЧ-1, что определено тестом ELISA ВИЧ-1 и вестерн-блоттингом (см. Пример I. E. ). Кроме того, 55% индивидуумов с MCTD, инфицированных, как показал тест ELISA CAEV, CAEV также содержал антитела перекрестно-реактивные с ВИЧ-1. ELISA по данному изобретению также можно применять для скрининга, помимо человека, других млекопитающих (не коз), включая, например, других млекопитающих, чувствительных к инфекции CAEV с целью обнаружения инфицированных CAEV особей.
Способ по данному изобретению, например ELISA, особенно удобен, если он доступен в виде набора. Такой набор ELISA, например, может содержать антиген CAEV, например, gp135, прикрепленный к твердой подложке, такой как пластиковая подложка. Например, набор может содержать микропланшет, такой как 96-луночный планшет с антигеном CAEV, прикрепленным к нескольким или ко всем лункам. Известны в технике другие твердые подложки, применимые в анализе ELISA. Применение, например, 96-луночного микропланшета в тесте ELISA обеспечивает дополнительные преимущества, так как если выбирается соответствующая распознаваемая метка, такая как радиоактивная, флуоресцентная или люминесцентная метка, анализ может быть автоматизирован, что дает возможность быстро и легко обработать большое количество образцов, включая, если нужно, соответствующие стандартные или контрольные образцы.
Набор (комплект), такой как комплект ELISA, может также содержать, если нужно, стандартный реагент, например, предварительно определенное количество антител против gp135. Такие реагенты дают возможность легко определить, содержит ли образец, например образец крови или образец сыворотки, взятых у индивидуума, какое-то количество антител против CAEV в кровотоке. Исходя из этого, комплект (набор) по данному изобретению может содержать, например, соответствующий буфер, который создает подходящие условия для связывания антитела против CAEV, присутствующего в образце, с антигеном CAEV, прикрепленным к твердой подложке. Если в наборе имеются такие реагенты, тест ELISA можно сделать стандартизованным, так что различные тесты, проведенные в различных местах в разное время, можно сравнивать друг с другом. Выяснено, что в случае отобранного антигена CAEV должна быть проанализирована группа образцов сыворотки, взятой у неинфицированных индивидуумов (контроль), с целью определения нулевой (базовой) линии уровня (реактивности) реакционной способности для конкретного антигена CAEV.
Способ по данному изобретению, такой, который приведен в качестве примера ELISA CAEV, может применяться для обнаружения антител против CAEV в кровотоке или для того, чтобы наблюдать за изменением (ростом, развитием) иммунного ответа. Например, индивидуум может быть вакцинирован с помощью вакцины по данному изобретению и рост иммунного ответа можно наблюдать с помощью ELISA по данному изобретению. Такой способ можно применять для того, чтобы выяснить, требуется ли бустерная (усиливающая) иммунизация и, если необходимо, выяснить оптимальное время введения усилителя. Кроме того, анализ CAEV, такой как приведенный в качестве примера ELISA, можно применять для скрининга образца крови донора, чтобы определить и удалить кровь, содержащую CAEV, из банка крови.
В соответствии с другим вариантом по данному изобретению предлагаются способы на основе нуклеиновых кислот для диагностики инфекции CAEV у
млекопитающих - не коз -, преимущественно у человека. Один такой способ заключается:
в определении в указанном субъекте последовательности, геномная или транскрибированная мРНК,
соответствующей нуклеиновой кислоте.
В одном варианте изобретения определяемая последовательность нуклеиновой кислоты CAEV включает последовательности, присущие исключительно изолятам CAEV человека (т. е. ч-CAEV). Например, внутри геномного участка, соответствующего нуклеотидному фрагменту 173, амплифицированному праймерами, представленными SEQ ID NN: 16 и 17, было найдено, что вирус CAEV человека имеет, по меньшей мере, две мутации, присущие исключительно человеку. Эти мутации соответствуют гуанину в положении 56 и цитозину в положении 77 в gag-области 173 продукта амплификации. Помимо вышеописанных мутаций исключительно человеческого происхождения, коли дополнительная последовательность ч-CAEV обнаружена, специалисты в данной области могут легко найти области уникальных нуклеиновых кислот, имеющиеся в изолятах CAEV человека. Таким образом, ниже рассматривается с целью применения ряд областей нуклеиновых кислот исключительно человеческого происхождения в геноме CAEV человека.
Еще в одной форме воплощения данного изобретения предлагается способ, лежащий в основе диагностики инфекции CAEV у субъекта, предпочтительно у человека; указанный
способ заключается:
a) в контакте нуклеиновой кислоты, взятой у субъекта, предпочтительно инфицированного CAEV, с праймерами, которые амплифицируют фрагмент геномной нуклеиновой кислоты CAEV,
в условиях, пригодных для образования опознаваемого продукта амплификации; и
b) в обнаружении продукта амплификации, содержащего геномную нуклеиновую кислоту CAEV; при этом таковое
обнаружение указывает, что данный субъект был инфицирован CAEV.
Соответствующие праймеры для применения по данному изобретению в основанном на PCR диагностическом методе включает, по
меньшей мере, одну пару праймеров, способных амплифицировать нуклеиновую кислоту CAEV. Предпочтительно выбранные праймеры амплифицируют нуклеиновую кислоту, специфичную к CAEV, и не амплифицируют
последовательности ВИЧ-1. Смотрите, например, гнездовой набор PCR-праймеров, включающий SEQ ID NN: 16 и 17, которые амплифицируют область 173 нуклеотида gag-гена CAEV человека,
или гнездовой
набор PCR-праймеров, включающий SEQ ID NN: 20 и 21, которые амплифицируют область 146 нуклеотида pol-гена CAEV человека.
Хотя для применения ниже рассматривалась одиночная пара праймеров, в конкретном варианте данного изобретения для каждого анализируемого субъекта применяют панель наборов праймеров (например, пар праймеров или гнездовых наборов праймеров), которые амплифицируют определенные нуклеотидные области нуклеиновой кислоты CAEV человека. Так как известно, что ретровирусы мутируют с высокой скоростью для диагностики по данному изобретению применяют предпочтительно панель (множественных) наборов праймеров с целью повысить вероятность того, что в действительности определяется инфекция CAEV у инфицированного индивидуума. Ряд пар праймеров специалисты в данной области могут легко выбрать так, чтобы гарантировать, что обнаруживается, по меньшей мере, 99% CAEV-инфицированных субъектов. Например, для применения по данному изобретению рассматривается от 1 до примерно 100 или более пар праймеров. В одном варианте изобретения применяют панель, по меньшей мере, от примерно 10 до 70 пар праймеров или гнездовых наборов праймеров. В другом варианте изобретения применяют, по меньшей мере, примерно от 20 до 50 пар праймеров.
В соответствии с другой формой воплощения данного изобретения предлагаются диагностические системы, предпочтительно в форме набора, содержащие, по меньшей мере, одну нуклеиновую кислоту для проведения диагностики, предпочтительно полученную из нуклеиновой кислоты CAEV человека, в соответствующем упаковочном материале, комплекте (упаковке).
Системы диагностики (диагностические системы) по данному изобретению применяются для (анализа) теста на наличие или отсутствие инфекции CAEV. Соответствующие диагностические системы включают, по меньшей мере, одну нуклеиновую кислоту по данному изобретению, предпочтительно две или более нуклеиновых кислот по изобретению, в виде отдельно упакованного(-ых) химического(-их) реагента(-ов) в количестве, достаточном для проведения, по меньшей мере, одного анализа. Обычно также содержатся инструкции по применению комплектного реагента. Специалисты в данной области легко объединят нуклеотидные зонды и/или праймеры по данному изобретению в виде набора (комплекта) в сочетании с соответствующими буферами и растворами для применения способами по данному изобретению, как описано ниже.
Употребляемая в тексте фраза "упаковочный материал" относится к одной или более физических структур, применяемых для того, чтобы поместить содержимое набора (комплекта), таких как зонды или праймеры по данному изобретению и тому подобное. Упаковочный материал (материал для комплектации), упаковка делается хорошо известными способами, предпочтительно, чтобы обеспечить стерильную среду, без примесей (загрязнений). На упаковке имеется ярлык, который указывает, что нуклеиновую кислоту по данному изобретению можно применять для обнаружения нуклеиновой кислоты геномной или транскрибированной мРНК, что лежит в основе диагностики инфекции CAEV. Кроме того, упаковка содержит инструкции, указывающие, как материал, входящий в комплект, применять как для обнаружения конкретной последовательности, так и обнаружения инфекции CAEV.
Упаковочные материалы, применяемые ниже в связи с диагностическими системами, представляют собой таковые, которые применяются в системах диагностики на основе нуклеиновых кислот. Употребляемый в тексте термин "упаковка, комплект" относится к твердому носителю или материалу, например стеклу, полимеру, бумаге, фольге и тому подобное, способные (удерживать) содержать в определенном (фиксированном) объеме выделенную нуклеиновую кислоту, олигонуклеотид или праймер по данному изобретению. Таким образом, например, упаковка может представлять собой стеклянную ампулу (сосуд) для хранения миллиграммовых количеств исследуемой нуклеиновой кислоты, олигонуклеотида или праймера, или это может быть лунка микропланшета, с которой функционально связаны (прикреплены) микрограммовые количества зонда изучаемой нуклеиновой кислоты.
"Инструкции по применению" обычно содержат выраженное доступным языком описание концентрации реагента или, по меньшей мере, один параметр способа анализа, например относительные количества смешиваемых реагента и образца, время выдерживания вместе реагента/образца, температуру, состав буфера и тому подобное.
Следующие примеры призваны проиллюстрировать, но не ограничить данное изобретение.
ПРИМЕР I
Характеристика перекрестной реактивности ВИЧ-1 у индивидуумов, инфицированных CAEV
Этот пример описывает способы, применяемые для
демонстрации того, что CAEV-инфицированные индивидуумы вырабатывают перекрестно-реактивный иммунный ответ на gp120 ВИЧ-1.
А. Индивидуумы (люди) объекты исследования.
В
описываемом ниже исследовании приняло участие более 50 человек (индивидуумов). Участники эксперимента были поделены на группы (категории) в зависимости от наличия или отсутствия заболевания (MCTD или
нормальное состояние) и места, откуда они родом (Мексика/Центральная Америка или Соединенные Штаты); они были разбиты на группы следующим образом:
Группа A. MCTD - Женщины испанского
происхождения с клиническим диагнозом MCTD.
Группа В. MCTD - Женщины, черные, уроженки США или кавказского происхождения, клинический диагноз MCTD.
Группа С. MCTD - Женщины, жительницы Гвадалахары, клинический диагноз MCTD.
Группа D. - Нормальная (не-MCTD) Женщины испанского происхождения.
Группа Е. - Нормальная - Женщины и мужчины не испанского происхождения, включая двух работников ветеринарной службы, обслуживающие инфицированных коз.
Группа F. - Нормальная - 4 женщины и 4 мужчин, жителей деревни, расположенной в 30 км от Гвадалахары, включая владельца стада из 150 коз и 5 членов его семейства.
Группа G. - Больные склеродермой, у всех имеются антитела против Scl-70/тип 1.
В. Образцы крови и реагенты.
Отбирают образцы крови человека и коз (см. Раздел I.F., ниже), и сыворотку используют для иммунологического исследования. Антигены, применяемые в тестах ELISA и вестерн-блоттинге для измерения антител в сыворотке, включают gp135 неочищенной CAEV и очищенный методом аффинности gp135 и gp120 рекомбинантного ВИЧ-1 и р24 ВИЧ-1. gp120 рекомбинантного ВИЧ-1 и р24 получены от Intracel (Shepreth UK).
Неочищенный CAEV получают так, как описано у Klevjer-Anderson et al., (Virology 110:113-119 (1981), вводится в данное описание в качестве ссылки). Существенным является то, что CAEV выращивают в первичных клетках синовиальной мембраны (SM) зародыша козы, культивируемых в DMEM с буфером бикарбонат-HEPES, с добавленной средой 2 mM глутамина, 100 мг/мл стрептомицина и 100 единиц/мл пенициллина и содержащей 10% FBS. Среду SM культур, инфицированных CAEV, собирают и осветляют центрифугированием при 600 х g.
Аликвоты сырого (неочищенного) препарата CAEV можно хранить в замороженном состоянии при -70oС. Сырой препарат CAEV можно использовать для выделения очищенного CAEV или для получения очищенных белков CAEV. Очищенные белки CAEV, такие как очищенный gp135, можно также получить клонированием молекулы нуклеиновой кислоты, кодирующей gp135 (Номер по каталогу в GenBank М33677; см. также Saltarelli et al., supra, 1990; Knowles et al., supra, 1991) в вектор экспрессии, используя стандартные методы техники рекомбинантной ДНК и очищая gp135, как описано ниже.
gp135 CAEV аффинно (за счет сродства) очищают от сырого (неочищенного) препарата CAEV, используя антитело против gp135, связанное с хроматографической матрицей (подложкой, носителем). Существенно то, что неочищенный препарат CAEV доводят до 0,1% SDS для того, чтобы лизировать вирусные частицы CAEV, затем переносят на хроматографическую колонку с антителом против gp135 для аффинной хроматографии или на колонку для аффинной хроматографии переносят gp135, полученный техникой рекомбинантной ДНК.
Антитело против gp135 выделяют из сыворотки инфицированных CAEV коз или из сыворотки, полученной от коз, иммунизированных пептидным фрагментом gp135 CAEV. Если в качестве источника сыворотки используют инфицированных CAEV коз, то сыворотку берут у козы с высоким титром антител против gp135. Такую сыворотку можно определить вестерн-блоттингом нескольких разных коз. Антитела против gp135 выделяют из сыворотки осаждением сульфатом аммония с последующей хроматографией на колонке, при этом получают фракцию IgG. Антитела против gp135 прикрепляют к (наносят на) носителю для хроматографии, например, SepharoseTM, активированный цианогенбромидом. Способы выделения антител IgG и нанесения таких антител на носитель хорошо известны и являются в технике стандартными (см., например, Harlow and Lane, supra, 1988).
Неочищенный препарат CAEV или gp135, полученный техникой рекомбинантной ДНК, в PBS наносят на колонку с антителом против gp135 для аффинной хроматографии и gp135 связывается с антителами в течение ночи при 4oС. Вслед за связыванием колонку промывают PBS, затем связанный gp135 вымывают раствором 10 mM HCl, 0.15 М NaCl. Чистоту антигена gp135 определяют с помощью SDS-PAGE и окрашиванием серебром.
С. Способы анализа CAEV ELISA и вестерн-блоттинг.
Для тестирования с помощью ELISA неочищенный CAEV или аффинно очищенный антиген gp135 разбавляют 1:20 физиологическим раствором с фосфатным буфером (PBS; конечная концентрация gp135 примерно 1 мкг/мл) и в каждую лунку 96-луночного планшета (Corning) вносят по 50 мкл. Планшет закрывают и термостатируют в течение ночи при 4oС, затем антиген удаляют и каждую лунку отмывают 3 Ч 1 мин по 90 мкл промывного раствора (1 мг BSA/мл PBS). В каждую лунку добавляют 100 мкл блокирующего раствора (10 мг BSA/мл PBS) и планшеты (плашки) термостатируют 60 мин при комнатной температуре (РТ), затем блокирующий раствор удаляют и лунки отмывают промывающим раствором 3 Ч 1 мин каждую.
Пятьдесят мкл образца разведенной сыворотки (1:100 в промывающем растворе) вносят в каждую лунку и планшеты термостатируют 60 мин при РТ. В слепых (контрольных) лунках помещают один промывной раствор. Вслед за термостатированием лунки отмывают, как описано выше, затем вносят 50 мкл разведенного раствора вторичного антитела и термостатируют, см. выше. Если образец анализируемой сыворотки взят у человека (индивидуума), вторичное антитело представляет собой козье антитело против IgG человека, конъюгированное с пероксидазой хрена (HRP; Zymed Laboratories, Inc., South San Francisco CA; cat. N 62-8420), разведенное 1:1000 в PBS. Если анализируемый образец сыворотки получен от коз, вторичное антитело представляет собой кроличий антикозий IgG-HRP. (Jackson ImmunoResearch Labs, Inc.; West Grove PA; cat. # 305035003. lot # 28671), разведенное 1:3000 в PBS. После термостатирования лунки промывают 2 Ч промывным раствором, затем 2 Ч PBS.
Семьдесят пять мкл раствора для проявления окраски (10 мг О-фенилендиамина (Sigma) в 25 мл буфера ELISA; 50 мкл свежеприготовленного 30% Н2О2; буфер ELISA, представляющий собой раствор 500 мл 0,1 М лимонной кислоты, 500 мл 0.2 М Na2HPO4, доведенный до рН 5.0), добавляют в каждую лунку и термостатируют 10 мин при РТ в темноте. Проявление прекращают добавлением 25 мкл 6 N Н2SO4, затем измеряют оптическую плотность при ОD490.
Для вестерн-блоттинга CAEV аликвоты 0.1-0.5 мкг gp135 в SDS буфере для нанесения образца (Laemmli,

Образцы сыворотки разбавляют 1: 100 (20 мкл сыворотки/2 мл промывного буфера, 40 мкл/2 мл, если используется плазма), затем помещают в планшет для термостатирования с нитроцеллюлозным фильтром, и встряхивают 60 мин при RT. После термостатирования полоски (ленты) отмывают 3 Ч промывным буфером, затем добавляют 2 мл вторичного антитела (как описано выше, но разбавленное буфером для отмывания) и термостатирование продолжают 60 мин при RT. Полоски отмывают 3 Ч буфером для отмывания и инициируют ферментативную реакцию, добавляя 2 мл цветного проявителя (10 мг 3,3-диаминобензидинтетрагидрохлорида (Sigma Chemical Co.; St. Louis МО; cat. # D 5905), 1 мл 0.05 M Tris, pH 7.5, 39 мл WBS. 80 мкл свежеприготовленного Н2О2). Термостатируют в течение 10 мин при RT и осторожном встряхивании, затем проявление прекращают, перенося мембрану в дистиллированную воду.
Высокая реактивность по отношению к вытяжке CAEV и очищенному gp135 наблюдается в 62% образцов сыворотки у больных MCTD испанского происхождения (Таблица 2), включая таковых из LAC/USC (группа Ф) и таковых из Гвадалахары, Мексика (группа С). Образцы сыворотки контрольных больных (группа G) и здоровых индивидуумов неиспанского происхождения, за исключением двух ветеринаров, слабо реагируют или не реагируют. Образцы сыворотки человека, реагирующие на CAEV при вестерн-блоттинге, содержат антитела с тем же полипептидом, что и таковые, реагирующие с образцами, полученными от коз, инфицированных CAEV.
Реактивность (реакционная способность) по отношению к CAEV образцов сыворотки нормальных индивидуумов коррелируется с питьем сырого козьего молока или другим контактом с козами. Самую высокую реактивность проявил владелец стада коз из Гвадалахары и один из ветеринаров, который помимо обслуживания инфицированных CAEV коз, также, как сообщают, регулярно принимал сырое козье молоко. Второй ветеринар, также обслуживающий инфицированных CAEV коз, также давал положительную реакцию.
В целом 22 из 39 больных MCTD и 11 из 23 не-MCTD индивидуумов дают положительную реакцию на инфекцию CAEV, включая 20 из 33 MCTD-больных испанского происхождения (61%) и 9 из 14 не-MCTD индивидуумов испанского происхождения (6%; см. Таблицу 2). Эти результаты показывают, что более 60% изученных в данном исследовании индивидуумов испанского происхождения были инфицированы CAEV. У CAEV-реактивных индивидуумов реактивность сыворотки, взятой у MCTD-больных испанского происхождения выше, чем у не-MCTD индивидуумов испанского происхождения.
D. Анализ методом PCR.
PCR-анализ с целью идентификации генов gag и pol CAEV проводят, используя геномную ДНК, выделенную из мононуклеарных клеток периферической крови (РВМС). РВМС получали по Ficoll центрифугированием с градиентом плотности цельной цитратной крови или крови с добавкой гепарина, взятой у отобранных индивидуумов (людей) и у коз WA, UC Davis и Gua (см. ниже).
CAEV-специфичные последовательности геномной ДНК, кодирующие участки белка gag, амплифицируют в две стадии. На первой стадии получают продукты амплификации, представляющие собой нуклеотиды CAEV от 1057 до 1553. Праймерами являются 5'-GCAGTTGGCATATTATGCTACTAC-3' (SEQ ID NO: 14; нуклеотиды CAEV 1057-1080) и 5'-CTTGTTGTACTCTTTGTCCTAGTG-3' (SEQ ID NO: 15; нуклеотиды 1530-1553). На второй стадии получают продукты амплификации внутри продукта первой амплификации от нуклеотида 1329 до 1501. Праймерами на второй стадии являются 5'-GAGCAGTAAGACATATGGCGCAC-3' (SEQ ID NO: 16; нуклеотиды 1329-1351) и 5'-TGATGCATTTGTATAAGATAGTGTTAGCTTT-3' (SEQ ID NO: 17; нуклеотиды 1471-1501).
ДНК, кодирующая pol CAEV, также исследовалась методом PCR. Праймерами на первой стадии амплификации являются 5'-GGATTTGAACTACACCCGCAG-3' (SEQ ID NO: 18; нуклеотиды CAEV 2845-2865) и 5'-CCTGTTGATACTATGAACCCTAGAC-3' (SEQ ID NO: 19; нуклеотиды 3494-3518); Праймерами на второй стадии являются 5'-AAGAACCTAAGCATCCCGCAAC-3' (SEQ ID NO: 20; нуклеотиды 3223-3244) и 5'-GTGATGTTCCCTAATTGCAATTCTAGTC-3' (SEQ ID NO: 21; нуклеотиды 3341-3368).
Амплификацию осуществляют, применяя при гибридизации температуру 52oС, а для элонгации 72oС в течение 38 циклов. Полимеразу Tag или полимеразу flu Tag (Promega Corp. ; Madison WI) используют согласно рекомендациям изготовителя. Один мкл реакционной смеси, взятой на первой стадии амплификации, используют для второй стадии амплификации, которую проводят в тех же условиях. Продукты второй стадии амплификации разделяют электрофорезом на агарозе и собирают элюированием соответствующей (полосы) зоны. Образцы амплифицированной ДНК клонируют в вектор ТА3 pCRTM (Invitrogen; La Jolla CA) и секвенируют, применяя комплект для секвенирования ДНК SequenaseTM Version 2.0 (U. S. Biochemical Corp.; Cleveland ОН), как рекомендуется производителем. Последовательности клонированной ДНК сравнивают со стандартной (эталонной) последовательностью ДНК CAEV (GenBank, No. в каталоге М33677).
Анализ методом PCR показал, что провирусная ДНК CAEV присутствует в геномной ДНК индивидуумов, CAEV-позитивных (положительных), как определено методом ELISA или вестерн-блоттингом. Конкретно, ДНК, кодирующую gag и pol-последовательности CAEV, амплифицируют из геномной ДНК больного MCTD (группа А) и из CAEV-инфицированной козы US Davis (Дэвиса). Сравнение с эталонной gag-последовательностью CAEV показывает, что дивергенция (отклонение) gag-последовательности больного MCTD от эталонной последовательности составляет 8.2%, а таковая козы US Дэвиса (Davis) составляет 8.8%. Кроме того, сравнение с эталонной pol-последовательностью CAEV показывает, что дивергенция pol-последовательности CAEV у больного MCTD составляет 7.6% и у козы US Дэвиса (Davis) составляет 7.6%.
Сравнительно высокая степень сходства между последовательностями CAEV, наблюдаемая в образце геномной ДНК человека и эталонной последовательности CAEV коз, является четким доказательством наличия инфекции CAEV у людей. Среднее отклонение (дивергенция) около 8% между двумя последовательностями указывает, что CAEV-инфекция человека может быть вызвана особым адаптированным к человеку штаммом CAEV. Дополнительное секвенирование ДНК может выяснить, является ли адаптированный к человеку штамм CAEV ответственным за инфекцию CAEV.
Чтобы получить дополнительное непосредственное доказательство наличия CAEV в РВМС человека, последовательности вирусных gag- и pol-генов амплифицируют с помощью внутригенной PCR из ДНК gp135(+) 8 человек. gag CAEV также амплифицируют из свободной от клеток плазмы индивидуума Hmc4 с помощью RT-PCR. Попытки амплифицировать последовательности gag и pol CAEV из ДНК РВМС одиннадцати индивидуумов с gp135(-) были негативными. Все образцы ДНК, используемые для PCR gag и pol CAEV, также подвергают PCR, используя gag- и pol-праймеры ВИЧ-1, и все они были отрицательными, за исключением ВИЧ(+)-контрольной группы, gag-последовательности CAEV также амплифицируют из ДНК РВМС 4 коз с gp135(+). Две козы (gD1 и gWA19) с gp135(+) CAEV были из US животноводческих стад; gT38 и gT42 были мексиканскими (Mexican) gp135(+)-козами. Двадцать два клона gag РВМС человека, 3 клона gag плазмы НМС4 и 11 клонов gag РВМС коз секвенировали и сравнивали с опубликованной последовательностью gag CAEV-CO (M. Saltarelli, et al., Virology. 179:347 (1990).
Филогенетический анализ 8 последовательностей gag человека, амплифицированных из 7 индивидуумов, показан на фиг. 1. Также включены gag последовательности 4 коз. Клоны и соответствующие номера по каталогу в Банке Генов (GenBank) для gag-последовательностей CAEV, Висны (Visna) и OMVVSA, анализируемых на фиг. 1 и 2, следующие: Hmc4-c30(U69922), -c39(U69923), -c40(U69924), -c46(U69925). -c49(U69932), -c50(U69926), -fp-c254(U69933), -fp-c256(U69934), -fp-c261(U69935), gD1-c12(U69927), -c13(U69928), -c52(U69929), -c53(U69930); Tn8-c144(U69931), -c147(U69909), -c151(U69910), -c155(U69911); gWa19-c74(U69918), -c75(U69919), -c77(U69920), -c80(U69921); gT42-c84(U69916), -c90(U69917), gT38-c93(U69915); En1-c108(U69900), -c110(U69901); Oc1-c120(U69905), -c136(U69906), -c139(U69907); Oc2-c167(U69908); Umc5-c184(U69912), -c185(U69913), -c190(U69914); Hmc1-c209(U69902), -c212(U69903), -c213(U69904); CAEV-CO (M33677); Visna (M18039); OMVVSA (M31646). Все другие последовательности на фиг. 1 являются лентивирусными последовательностями, за исключением JSR из ретровируса овцы Яагзикте (Jaagsiekte). Далее, клоны pol CAEV и номера по каталогу, соответствующие последовательностям pol, обсуждаемые в тексте, следующие: Hmc4-c10(U69948), -c12(U69949), -c19(U69950), -c20(U69951), -c28(U69952); gD1-c1(U69944), -c2(U69945), -c3(U69946), -c30(U69947); gWa19-c51(U69953), -c52(U69954), -c53(U69955), -c60(U69956); En1-c43(U69940), -c46(U69941), -c47(U69942), -c48(U69943); Gmc15-c37(U69936), -c38(U69937), -c41(U69938), -c42(U69939).
Относительные расстояния последовательностей между gag CAEV человека и последовательностями gag CAEV-CO и некоторых других лентивирусов делают очевидным использование оптимизации с обратным множителем (обратную оптимизацию) (D.M. Hillis et al., Science. 264:671 (1994). B.T.M. Korber et al., J. Virol. . 68: 6730 (1994)). Обычную (простую) оптимизацию осуществляют, применяя PAUP 3.1.1 (D.L. Swofford, Illinois Natural History Survey, Urbana). Двенадцать четких замен из первичного PAUP-анализа затем были подтверждены с применением Macclade (W.P. Maddison and D.R. Maddison, "Macclade: Analysis of phylogeny and character evolution", Sinauer Associates, Inc., Sunderland, (1992)). Из этой матрицы частот замен была получена схема с обратным множителем, введенная затем в последующий оптимизированный (parsimony) анализ. Полученные в результате величины длин ветвей представляют собой количества соединения, полученного из матрицы с обратным множителем замен. Все последовательности вирусных gag, полученных у субъектов опыта, и последовательности gag коз образовывали кластеры с gag CAEV-CO.
Простые измерения расстояний в нуклеотидах, то-есть расстояний Хэмминга (Hamming), определяют, используя функцию подобия (SIMILARITY) MASE (D.V. Faulkner and J. Jurka, Trends Biochem. Sci.. 13:321 (1988)). Были определены только единичные расстояния в нуклеотидах, пробелы в этом ряду данных не отмечались. По данным измерения расстояний Хэмминга дивергенция последовательностей 8 клонов gag человека от gag CAEV-CO находится в интервале 5.3-9.4% по сравнению с дивергенцией 23.4-28% от опубликованной последовательности gag мэди/висны овцы (Р. Sonigo et al., Cell. 42:369 (1985)).
Для дополнительной оценки inter- и intra-индивидуального изменения в последовательностях gag человека и козы, методом простой оптимизации (parsimony) был осуществлен анализ 33 клонов (фиг. 2). Как и на фиг.1, все последовательности индивидуума (человека) образуют кластеры с CAEV-CO. Средняя дивергенция последовательностей всех 22 gag-клонов индивидуумов от CAEV-CO составляет (8.4±1.5)%.
Вирусные последовательности 3 человек (Hmc4, Gmc15 и En1) и 2 коз (gD1 и gWA19) также амплифицируют из ДНК РВМС, используя праймеры внутригенного pol CAEV. Последовательности pol на 4.8-8.2% отклонялись (имели дивергенцию) от опубликованной последовательности pol CAEV-CO (M. Saltarelli et al., Virology 179:347 (1990)) и на 22.6-26.0% от pol висны/мэди овцы (Р. Sonigo et al., Cell. 42: 369 (1985)). Оптимизированный анализ этих последовательностей pol дает представление о топологии, согласующуюся с таковой gag (фиг. 1). Примерно 40% gag и 17% pol нуклеотидных изменений приводит к изменениям аминокислот. Все pol изменения и 80% gag изменений являются консервативными (преимущественно I<-->V, К<-->R и D<-->Е). Таким образом, анализ последовательностей gag и pol указывает, что у 8 человек с gp135(+) CAEV, изученных в данном исследовании, имеется лентивирус жвачных, очень сходный с CAEV. Доказательство репликации in vivo этого агента, как описано ниже в Примере II, получено RT-PCR-амплификацией последовательностей gag CAEV из свободной от клеток плазмы объекта Hmc4 (фиг. 2).
Е. Анализ ВИЧ-1 методом ELISA и вестерн-блоттингом.
Используются сертифицированные (стандартные) диагностические наборы для ELISA и вестерн-блоттинга ВИЧ-1 фирмы Organon Teknika (Cambridge UK), анализы проводят в соответствии с рекомендациями поставщика. На основании клинического исследования с использованием стандартных методов ВИЧ-1 анализа с помощью ELISA и вестерн-блоттинга, все образцы сыворотки человека являются ВИЧ-1-отрицательными, за исключением известных ВИЧ-1-положительных образцов сыворотки и антител, взятых в качестве контрольных положительных.
ELISA и вестерн-блоттинг осуществляют, используя рекомбинантные антигены ВИЧ-1 индивидуумов, gp120 и р24 и HRP-конъюгированные кроличьи вторичные антикозьи антитела и таковые козьи античеловеческие (Zymed Laboratories Inc. ), как ранее описано (Douvas and Takehana, supra, 1994; Crow et al., Cell. Immunol. 121:99-112 (1989). Набор сывороток, которые реагируют с gp135 CAEV, реагируют с gp120 ВИЧ-1, включая и все 12 MCTD-сывороток, которые реагируют с gp120 ВИЧ-1 (см. Таблица 2, supra).
Как обсуждается в Разделе I.C., выше, 22 из 39 больных MCTD и 11 из 23 нe-MCTD-индивидуумов дают положительную реакцию на CAEV-инфекцию, включая 20 из 33 больных MCTD испанского происхождения (61%) и 9 из 14 "испанцев", не больных MCTD (не-MCTD) (64%; Таблица 2). Результаты анализов на ВИЧ-1 дополнительно показывают, что 12 из 24 CAEV-положительных больных MCTD "испанцев" (55%) и 2 из 9 CAEV-положительных нe-MCTD-индивидуумов испанского происхождения (22%) также дают положительную реакцию на gp120 ВИЧ-1 (см. Таблицу 2). Напротив, ни один из индивидуумов испанского происхождения с отрицательной реакцией на CAEV, больных и не больных MCTD, не был положительным в отношении gp120 ВИЧ-1.
Эти результаты указывают, что инфицирование CAEV индивидуумов, здоровых в других отношениях, не сопровождается сопутствующим развитием клинического заболевания, включая развитие симптомов MCTD. Однако контакт с CAEV приводит к появлению иммунной реакции на CAEV, которая распространяется на ВИЧ-1 в субпопуляции инфицированных индивидуумов. Кроме того, у CAEV-положительных больных MCTD реактивность по отношению к CAEV примерно в 1.6 раз сильнее, чем у CAEV-положительных не-MCTD-индивидуумов, и частота перекрестной реакции на gp120 ВИЧ-1 выше. Эти результаты показывают, что перекрестная реакция на ВИЧ-1 появляется в результате инфицирования CAEV и что перекрестно-реактивный иммунный ответ усиливается у индивидуумов с аутоиммунным заболеванием.
F. Козы, инфицированные CAEV.
Изучались три следующие группы коз:
Группа I. WA-неинфицированные козы
и козы, инфицированные в ходе опыта (CAEV), содержащиеся в Университете штата Вашингтон, Pullman WA.
Группа II. UC Davis (Дэвис) - естественным путем инфицированная (CAEV) коза, содержащаяся в Университете Калифорнии, Davis СА.
Группа III. Gua - 20 инфицированных естественным путем (CAEV) коз, принадлежащих владельцу стада в Гвадалахаре, Мексика (Группа F, см. выше).
Изучались образцы сыворотки различных CAEV-инфицированных и неинфицированных коз. У коз Gua (Группа III) отсутствовала реакция на gp135 CAEV, но около 50% их реагируют на gp38 и gag CAEV. Кроме того, козы Gua, но не козы WA проявляют высокую реакционную способность в отношении gp120 и р24 ВИЧ-1. Коза UC Davis реагирует как на gp135, gp120, так и на р24.
Эти результаты показывают, что существует различие между иммунологической реакцией коз WA и Gua на антигены CAEV и ВИЧ-1. Эти различия могут возникать вследствие разных штаммов вирусов или вследствие различных путей проникновения инфекции. Например, козы WA инфицировали внутривенно, тогда как козы Gua и коза UC Davis инфицированы естественным путем через инфицированное молоко.
G. Анализ с помощью реакции нейтрализации вируса ВИЧ-1.
Тесты на нейтрализацию вируса осуществляют в 48-луночных планшетах с культурами тканей, используя в качестве мишени (цели) для инфицирования РВМС нормального донора, активированные РНА, выдержанные в среде для выращивания, с концетрацией 1 Ч 106 клеток/мл. HIVIGTM, термостатированные MCTD-вытяжки или очищенный IgG в разном разведении термостатируют с 10 или 50 ТСID50 (инфицирующая доза культуры ткани - 50) вируса в течение 30 минут при 37oС.
Отрицательные (негативные) контрольные образцы сыворотки MCTD и HIVIGTM включают термостатированную сыворотку индивидуумов, не ВИЧ-1-инфицированных и не имеющих систематического расстройства ревматического характера, и IVIGTM соответственно. HIVIGTM, представляющий собой препарат, нейтрализующий IgG, из объединенных вытяжек 9 сероположительных доноров на ранних стадиях ВИЧ-1-инфекции, и IVIGTM, который представляет собой IgG нормальных доноров, получены от North American Biologicals Inc. (Miami FL). TCID50 определяют, применяя стандартные способы титрования вирусов.
Вслед за термостатированием сыворотки или IgG и вируса, смеси сыворотка/IgG-вирус вносят в клетки-мишени в три ячейки планшета. После термостатирования в течение ночи при 37oС плашки центрифугируют при 1000 об/мин в течение 5 минут и среду полностью заменяют. Эту стадию отмывания повторяют 3 Ч, чтобы быть полностью уверенными, что инокулят сыворотка/IgG-вирус полностью удален. На 4-й день выращивания культуры среду заменяют и на 7-й день надосадочную жидкость собирают для количественного определения бычьего антигена р24. Процент подавления определяют, сравнивая среднюю концентрацию бычьего антигена р24 в каждой лунке с обработанной сыворотка/IgG культурой ткани с таковой специфичного отрицательного контрольного образца.
Параллельно готовится контрольный образец с целью измерить любое неспецифичное уменьшение количества измеряемого бычьего антигена р24 вследствие того, что сыворотка или HIVIGTM не полностью удалены на стадии отмывания. В то время, когда смеси сыворотка/IgG-вирус добавляют к клеткам-мишеням, сыворотку, IVIGTM или HIVIGTM также добавляют к клеткам-мишеням без предварительного термостатирования с вирусом. Эти лунки обрабатывают параллельно экспериментальным культурам. После 7 дней культивирования надосадочную жидкость их каждой лунки смешивают с таковой отрицательного контрольного образца и количественно определяют концентрацию антигена р24. Величины (измерения), составляющие менее 50% значения отрицательного контроля, рассматриваются как неспецифичное ингибирование антигена р24, возможно, вследствие наличия остаточных антител р24.
Результаты этого эксперимента приведены в Таблице 3. Таблица 3 показывает, что сыворотки против RNP больных MCTD способны нейтрализовать инфицирование штаммами ВИЧ-1: MN, JR-FL и СО. Образец N 1 в Таблице 3 соответствует Hmc1 больного CAEV(+). Больной, соответствующий образцу N 4 в Таблице 3, как определено, тоже является CAEV(+). Больные, соответствующие образцам 2, 3, 5 и 7, не могли быть оценены с точки зрения наличия CAEV-инфекции. Следовательно, так как образцы 1, 4 и 6 соответствуют анти-CAEV сыворотке индивидуумов, по-видимому, анти-CAEV сыворотка человека нейтрализует ВИЧ-1-инфекцию.
ПРИМЕР II
In vitro
инфицирование РВМС человека с помощью PCR(+) плазмы человека
Этот пример показывет способность ч-CAEV инфицировать клетки РВМС человека. Будет представлено сравнение специально перенесенных
(внесенных) gag последовательностей CAEV.
Культуры 0.8 миллиона РВМС человека, взятых у донора с отрицательной реакцией на инфекцию CAEV, как определено с помощью PCR (т.е. PCR-), инокулируют со 100 мкл плазмы больного Hmc4, который, как было показано, дает CAEV-положительную реакцию (РСR+), общий объем составляет 1 мл. Через 4 дня экстрагируют геномную ДНК, клеточную РНК и РНК надосадочной культуральной жидкости и анализируют с помощью PCR и RT-PCR, используя праймеры gag CAEV, так как имеется 100 мкл первоначальной плазмы, разбавленной до 1 мл. Агарозные гели, на которые наносят продукты PCR-реакций, показывают сигналы gag CAEV в геномной ДНК, РНК и надосадочных культуральных жидкостей, тогда как уровни CAEV в инокулирующей плазме больного Hmc4 ниже уровня, поддающегося обнаружению. Это показывает, что CAEV продуктивно инфицирует клетки РВМС человека. Подобное инфицирование РВМС человека с помощью плазмы (PCR+) человека с установленным Hmc4 было осуществлено и дало сходные результаты.
Вирус CAEV в вышеописанном примере был искусственно перенесен из культур инфицированных клеток. Последовательности, искусственно перенесенные в эксперименте с Hmc4, сравнивают с таковыми геномной ДНК и РНК плазмы того же субъекта. Последовательности gag CAEV клонируют из выбранных инфицированных совпадающих РМВС из концентрированной плазмы больного Hmc4, как показано на фиг. 3. Ни фиг. 3 сравниваются следующие относящиеся к Hmc4 клоны gag CAEV, полученные с помощью PCR или RT-PCR: геномные клоны Hmc4 g-30, g-39, g-40, g-46 и g-50; плазменные клоны Hmc4 р-254 и р-256; клоны из эксперимента по инфицированию i-238 и i-239. Клоны "i" получены из цитоплазмы инфицированных культур. Прямоугольные рамки показывают, что есть определенное сходство между всеми "р" и "i" клонами и геномным клоном g-30 из Hmc4, и это наводит на мысль о том, что это есть субпопуляция особенно жизнеспособных форм у этого больного.
Из данных, представленных на фиг. 3, легко видно, что подтип CAEV, который инфицирует человека, отличается от известного, инфицирующего коз, CAEV M33677 (также называемого в данном описании "CAEV-CO"). Например, внутри относительно малой геномной области, соответствующей 173 нуклеотидному фрагменту, амплифицированному праймерами, представленными SEQ ID NN: 16 и 17, было найдено, что вирус ч-CAEV имеет, по меньшей мере, две мутации, по своему происхождению относящиеся исключительно к человеку. Эти мутации соответствуют гуанину в положении 56 и цитозину в положении 77 внутри продукта амплификации gag-участка 173 в клоне Hmc4.
На фиг. 4 дано сравнение последовательностей PCR-амплифицированного участка гена POL нуклеотида 146, который (участок) соответствует нуклеотидам 3223-3358 козьего вируса CAEV, штамм 79-63. Известный штамм CAEV-CO взят из мозга козы. Мозг является иммунологически неприкосновенным местом. Следовательно, эволюция вируса отличается от вируса, выделенного из синовиальной жидкости коз, страдающих артритом. gWa19 инфицируют вирусом из синовиальной жидкости, штамм его известен как 79-63. Эволюция форм, относящихся к человеку, по-видимому, более всего сходна с CAEV-63. На фиг. 4 дается сравнение вирусов: известного козьего CAEV-CO, ч-CAEV, выделенного из Hmc4 и CAEV-63 козы gWa19. Различия между последовательностями вируса, инфицирующего козу, и вируса CAEV, инфицирующего человека, легко видны на фиг. 4. Таким образом, в данном описании рассматриваются новые лентивирусы ч-CAEV, способные инфицировать человека.
На фиг. 5 непосредственно сравниваются последовательности козьего CAEV, штаммы CAEV-CO и gWa19 (т.е. CAEV-79-63), и ч-CAEV человека, штаммы Hmc1 и Нmс4, на одном и том же участке нуклеотида 173, представленного (участка) на фиг. 3. Процент дивергенции (отклонения) между вирусами CAEV, выделенными из человека (CAEV человека) и коз, представлен на Таблице 4. Hmc1 и Hmc4 соответствуют CAEV человека, тогда как gWa19, СО и g147 соответствуют козьему CAEV.
ПРИМЕР III
Применение вакцины САЕV для вакцинации индивидуума
В
этом примере описывается способ введения вакцины CAEV индивидууму для стимуляции иммунной реакции на CAEV.
Вирус CAEV человека получают инокуляцией клеток РВМС (см. Пример II) или клеток моноцитов. Надосадочную жидкость клеток собирают и вирионы высаживают центрифугированием 1500,00 х g при 4oС с целью получить стерильную суспензию примерно 2 Ч 108 бое/мл, содержащую 50% глицирина в качестве (растворителя) разбавителя (см. Graham et al., T. Infect. Dis. 166:244-252 (1992). Реципиентов живых вирусов вакцинируют интрадермально, используя стерильные раздвоенные иглы, 50ю-мкл суспензии CAEV в одно место на коже. Вакцинацию также можно осуществлять, используя препарат убитого или ослабленного CAEV или другого иммуногена, например, gp135 CAEV (см. также выше, Таблица 1). Место вакцинации покрывают стерильной прозрачной повязкой, которую удаляют после образования корки.
Образцы крови отбирают примерно через 14, 28 и 54 дня после введения иммуногена CAEV и используют для определения титра антител (гуморальный ответ, реакция) или иммунная реакция (ответ) Т-хелперов или цитотоксичных Т-клеток (клеточная реакция). Способы исследования (изучения) гуморальной и клеточной реакции раскрываются в Примере I или они хорошо известны в технике из других источников (см. , например, Egan et al., T. Infect. Dis. 171: 1623-1627 (1995); см. также Harlow and Lane, supra, 1988). Если надо, проводится вторичная (усилительная, бустерная) иммунизация примерно на 56 день после первичной вакцинации. Дополнительные определения гуморальной и клеточной реакции (ответа) делают примерно на 70, 90, 160, 180, 270 и 355 дни после первичной вакцинации. Если надо, примерно на 365 день проводят третичную (бустерную) иммунизацию.
Для введения иммуногена CAEV, которым является гаптеновый пептид, примерно 1 мг пептида соединяют (конъюгируют) с "ключ-замок" гемоцианином и вводят, с адъювантом, интрадермально, см. выше, в количестве примерно 0.1 мл по объему. Определение гуморальной и клеточной реакции осуществляют, как описано выше, и, если надо, проводят вторичную и третичную иммунизацию.
Хотя данное изобретение описано со ссылками на приведенные выше примеры, следует понимать, что могут быть сделаны различные модификации без отхода от сущности изобретения. Соответственно этому данное изобретение ограничивается только следующей формулой.
Реферат
Изобретение относится к медицине и предлагает вакцину, содержащую иммуноген вируса козьего артрита-энцефалита (CAEV) и фармацевтически приемлемый носитель. Изобретение также предлагает способ стимулирования у индивидуума иммунной реакции на инфекцию вируса иммунодефицита человека-1 или на инфекцию CAEV введением терапевтически эффективного количества иммуногена CAEV индивидууму. Изобретение далее предлагает способ стимулирования иммунной реакции in vitro контактированием лимфоцита с терапевтически эффективным количеством иммуногена CAEV, а также включает способы, лежащие в основе диагностики инфекции CAEV у человека, и выделенный CAEV человека, имеющий нуклеотидную последовательность с дивергенцией от эталонного CAEV-Со. Преимущество изобретения заключается в создании вакцины, содержащей иммуноген CAEV, стимулирующий иммуную реакцию на инфекцию ВИЧ-1 человека. 8 с. и 16 з. п. ф-лы, 4 табл., 5 ил.


Комментарии