Источник рентгеновского излучения с сформированной радиационной картиной - RU2155413C2
Код документа: RU2155413C2
Чертежи




















Описание
Настоящее изобретение относится к малогабаритному, программируемому источнику рентгеновского излучения малой мощности для использования при получении в значительной мере постоянного или импульсного рентгеновского излучения с низким уровнем мощности в специальной области.
Традиционные медицинские источники рентгеновского излучения представляют собой стационарно расположенные агрегаты больших размеров. Обычно головка рентгеновской трубки размещается в одной комнате, а консоль управления - в соседней. Комнаты разделяются защитной стеной, в которой имеется окно для наблюдения. Типичные размеры рентгеновской трубки составляют примерно от 20 до 35 сантиметров (см) в длину и около 15 см в диаметре. Источник питания высокого напряжения размещается внутри стойки, которая располагается в углу комнаты, содержащей рентгеновскую трубку. Пациентов направляют на рентген для диагностического, терапевтического или паллиативного лечения.
Диагностические рентгеновские аппараты обычно работают на напряжениях ниже 150 киловольт (кВ), и при токах приблизительно от 25 до 1200 миллиампер (мА). Для сравнения, токи в терапевтических аппаратах обычно не превышают 20. мА при напряжениях, которые могут находиться в пределах выше 150 кВ. При работе рентгеновского аппарата на номинальных значениях напряжений от 10 до 140 кВ проникновение рентгеновского излучения в организм человека ограничивается тканью и поэтому его можно использовать при лечении повреждений кожи. При более высоких напряжениях (порядка 250 кВ) достигается глубокое проникновение рентгеновского излучения, которое используется при лечении опухолей. Рентгеновские аппараты сверхвысокого напряжения, работающие в диапазоне напряжений от 4 до 8 мегавольт (MB), используются для удаления или разрушения всех типов тканей, кроме поверхностных повреждений кожи.
Традиционная рентгеновская трубка включает в себя анод, сетку и катодный узел. Катодный узел вырабатывает электронный пучок, который направляется на мишень электрическим полем, образующимся между анодом и сеткой. Падающий на мишень электронный пучок, в свою очередь, вырабатывает рентгеновское излучение. Излучение, поглощаемое пациентом, в основном является излучением, которое передается от мишени в рентгеновскую трубку через окно в трубке, приводя к потерям при передаче. Это окно обычно выполняют в виде тонкой пластинки берилия или другого подходящего материала. В традиционном рентгеновском аппарате, катодный узел состоит из торированной вольфрамовой спирали диаметром около 2 мм и длиной от 1 до 2 см, которая нагревается при прохождении тока, равного 4 Амперам (А) или выше, путем термоэлектрической эмиссии электронов. Эта спираль окружена металлической фокусирующей чашкой, которая фокусирует пучок электронов в пятно малых размеров на противоположно расположенный анод, который работает также как мишень. В моделях, имеющих сетку, именно сетка управляет траекторией пучка электронов и фокусировкой его.
Прохождение электронного луча от катода к аноду влияет на объемный электронный заряд, который становится заметным в традиционных рентгеновских аппаратах при токах больше 1 А. В таких традиционных аппаратах луч фокусируется на аноде в пятно диаметром в пределах от 0,3 до 2,5 миллиметров (мм). Во многих приложениях большая часть энергии электронного луча преобразуется в тепло на аноде. Для отвода такого тепла в медицинских источниках рентгеновского излучения высокой мощности часто используется охлаждающая жидкость и вращающийся с высокой скоростью анод. Таким образом, устанавливается повышенный эффективный размер области мишени и обеспечивается малый размер Фокального пятна при минимизации эффектов локального разогрева. Для достижения хорошей теплопроводности и эффективного рассеяния тепла анод обычно изготавливают из меди. Кроме того, область анода, на которую падает электронный луч, необходимо выполнять из материала с высоким атомным номером для обеспечения эффективной генерации рентгеновского излучения. Для выполнения требований по теплопроводности, эффективному рассеиванию тепла и эффективной генерации рентгеновского излучения в вольфрамовый сплав обычно добавляют мель.
В рабочем режиме общее время экспозиции рентгеновского источника прямо пропорционально интегралу по времени от интенсивности электронного луча. В течение относительно большого времени экспозиции (т.е. в пределах от 1 до 3 секунд) температура анода может значительно повышаться, приводя его к яркому свечению, связанному с локальными поверхностными проплавлениями и точечной коррозией, которые снижают мощность выходного излучения. Однако тепловое испарение спирального прямоканального катода трубки наиболее часто приводит к неисправности традиционных трубок.
Эффективность рентгеновского излучения зависит не только от тока электронного пучка, но и от ускоряющего напряжения. Ниже уровня напряжения 60 кВ только несколько десятых процента кинетической энергии электрона преобразуется в рентгеновское излучение, тогда как при напряжении 20 MB эффективность преобразования увеличивается до 70%. В спектре рентгеновского излучения содержится ряд дискретных энергетических переходов между граничными электронными энергетическими уровнями элемента мишени. В спектре также присутствует энергетический континуум рентгеновского излучения, известный как тормозное излучение, которое вызывается ускорением потока электронов при их проходе вблизи от ядер мишени. Максимальная энергия рентгеновского излучения не может превышать максимального значения энергии электрона в пучке. Кроме того, максимум кривой эмиссии тормозного излучения приходится примерно на одну третью часть от энергии электрона.
Увеличение тока электронов приводит к прямо пропорциональному увеличению эмиссии рентгеновского излучения при всех энергиях. Тем не менее, изменение ускоряющего напряжения приводит к общему изменению интенсивности выходного рентгеновского излучения, приблизительно равной квадрату напряжения с соответствующим сдвигом в максимуме энергии фотонов рентгеновского излучения. Эффективность образования тормозного излучения повышается с увеличением атомного номера элемента мишени. Пик выходной интенсивности в кривой тормозного излучения и характерные спектральные линии сдвигаются в область более высоких энергий по мере того, как увеличивается атомный номер мишени. Хотя вольфрам (z=74) представляет собой наиболее часто используемый материал мишени в современных трубках, золото (z=79) и молибден (z=42) используется в некоторых трубках специального назначения.
Рентгеновское взаимодействие происходит различными способами. Для биологических образцов наиболее важны следующие два типа взаимодействия: комптоновское рассеяние рентгеновского излучения с ослаблением энергии внешних электронных оболочек; и фотоионизационное взаимодействие с внутренней оболочкой электронов. В этих процессах вероятность атомной ионизации уменьшается с увеличением энергии фотона как в мягкой ткани, так и в кости. Для фотоэлектрического эффекта это соотношение следует из закона 1/3 для электрона.
Недостатком современных рентгеновских устройств, используемых для терапии, является высокое напряжение, которое требуется при облучении мягкой ткани внутри или под костью. Примером может служить облучение рентгеновским излучением областей мозга человека, закрытых костью. Для проникновения излучения в кость требуется высокая энергия рентгеновского пучка, при которой часто повреждается кожа и ткани мозга. Другим примером в радиационной терапии может служить облучение рентгеновским излучением мягкой ткани, расположенной внутри полости тела, которое находится в другой мягкой ткани или во внутренней структуре, содержащей кальций. Настоящие высоковольтные аппараты ограничены по своей способности в таких областях.
Другой недостаток современных рентгеновских источников с высоковольтным выходным напряжением заключается в повреждении, вызываемом в кожном покрове, при воздействии на орган или ткань человека. Поэтому высоковольтные устройства современных систем часто вызывают значительные повреждения не только в области мишени, но также во всех окружающих участках ткани и кожном покрове, особенно при использовании для лечения опухоли человека. Однако, поскольку в настоящих устройствах используется рентгеновское излучение в областях мишени, расположенных внутри пациента, от источника, расположенного во внешней области мишени, такое случайное повреждение ткани практически невозможно.
Лечение опухолей мозга требует точных технических приемов для осуществления специфического разрушения ткани, особенно как в ткани мозга, в которой отсутствует какая-либо реальная способность к регенерации. При использовании традиционных рентгеновских устройств при лечении опухоли мозга часто отсутствует прецизионное объемное облучение, что приводит к повреждению не раковой ткани мозга и связанных железистых структур.
Альтернативная форма лечения опухолей, называемая брахитерапией, включает имплантацию заключенных в капсулы радиоизотопов в опухоль, которую необходимо лечить, или рядом с ней. Хотя такое использование радиоизотопов может быть эффективным при лечении определенных типов опухолей, введение изотопов требует процедуры вторжения в организм, которая имеет возможные побочные эффекты, в виде возможной инфекции. Более того, в некоторых применениях может образоваться опухоль мозга вследствие неуправляемого облучения изотопами. Кроме того, в этом случае нельзя обеспечить требуемое управление временем облучения или необходимое значение интенсивности излучения. Обслуживание и размещение таких радиоизотопов имеет определенный риск как для обслуживающего персонала, так и для окружающей среды.
Методика вторжения в мозг человека требует точного контроля дозы облучения посредством выбора к концентрации используемых изотопов. Внутричерепное облучение приводит к значительному риску, также известному в технике.
С точки зрения выше указанных требований и ограничений для использования современных аппаратов рентгеновского излучения в терапевтических, диагностических, паллиативных или анализируемых средах существует необходимость в создании относительно небольшого, простого в обращении, управляемого, маломощного, рентгеновского устройства, в котором источник рентгеновского излучения можно устанавливать в непосредственной близости от среды, которая будет облучаться.
Такое устройство, работающее при малых энергиях и мощностях, будет пригодным для различных применений, описанных здесь.
Таким образом, задача настоящего изобретения - обеспечить простое в обращении и маломощное рентгеновское устройство.
Другая задача изобретения - обеспечить относительно небольшое, маломощное рентгеновское устройство, имеющее управляемый или программируемый источник питания.
Другая задача изобретения - обеспечить относительно небольшое, маломощное рентгеновское устройство, которое имплантируется в пациента для прямого облучения требуемой области ткани рентгеновским излучением.
Другая задача изобретения - обеспечить маломощное рентгеновское устройство для облучения объема с мишенью для установления профиля поглощения, определяемого посредством заданного контура изодозы для того, чтобы уменьшить повреждение ткани, расположенной снаружи требуемой области облучения.
Еще одна задача изобретения - обеспечить относительно небольшое, устанавливаемое на поверхности, маломощное рентгеновское устройство для воздействия на требуемую область поверхности рентгеновским излучением.
Еще одна задача изобретения - обеспечить относительно небольшое, маломощное рентгеновское устройство, которое вводится в пациента для непосредственного облучения специальных областей рентгеновским излучением.
Еще одна задача изобретения - обеспечить относительно небольшое, маломощное рентгеновское устройство для использования с соответствующим узлом Фрейма для управляемого позиционирования рентгеновского источника, расположенного рядом с опухолью пациента или внутри него для того, чтобы облучить и, следовательно, лечить эту опухоль.
Еще одна задача изобретения - обеспечить небольшое, маломощное рентгеновское устройство, которое может проходить через существующие, принимающие неправильные формы проходы.
Еще одна задача изобретения - обеспечить небольшое, маломощное рентгеновское устройство, которое включает улучшенный механизм для транспортировки электронного луча на элемент мишени.
Краткое содержание изобретения
Вкратце, изобретение представляет собой простое в
обращении устройство, имеющее малую мощность, электронный луч (e-луч), возбуждаемый источником рентгеновского излучения, с предварительно заданными или регулируемыми длительностью излучения,
действующей энергией и интенсивностью. Для использования в медицине устройство (или зонд) может быть целиком или с перемещением введен, имплантирован в требуемый участок тела пациента или установлен
на его поверхности для облучения области тела рентгеновским излучением. Кроме того, устройство можно собрать вместе с изменяемым по толщине рентгеновским экраном для вывода излучения и
последовательного поглащения в нем предварительно выбранным уровнем мощности, который определяется путем установления контуров изодозы, так чтобы уменьшить эффекты рентгеновского излучения вне
требуемой области облучения. Устройство можно собрать в комбинации с соответствующим кадром, например, стереотактическим кадром, и подсоединить и устройству связи, которое используется при лечении
опухолей мозга. Устройство также пригодно для облучения других опухолей типа тех, которые можно обнаружить в груди или печени или в других местах; также устройство можно использовать для лечения
раковых клеток на поверхности полостей тела типа мочевого пузыря.
Устройство работает при относительно низком напряжении, например, в диапазоне приблизительно от 10 кВ до 90 кВ, и при малом токе, например, в диапазоне приблизительно от 1 нА до 100 мкА. Для того, чтобы получить требуемую диаграмму направленности излучения над требуемой областью, при минимальном облучении других областей рентгеновское излучение выходит из условного или действующего "точечного" источника, размещенного внутри или рядом с требуемой областью, которая будет облучаться. Предпочтительно, точечный источник используется вместе с маской или экраном для управления конфигурацией излученного рентгеновского пучка. В некоторых применениях какую-либо часть требуемой области облучают с низкой скоростью дозы рентгеновского излучения, или постоянно, или периодически сверх нормированных периодов времени. При использовании с соответствующим кадром для лечения опухоли мозга обычно предпочтительна высокая скорость дозы для одной дозы облучения. При использовании "повторяющегося локализатора" единственную дозу можно перемещать, если требуется, посредством циклов с высокой скоростью доз, т.е. фракционированное лечение.
Устройство включает контролируемый или программируемый источник питания, размещенный снаружи требуемой области, которая будет облучаться для предоставления возможных изменений напряжения, тока и временного интервала электронного луча. Электронный луч управляется, проходя вдоль требуемой оси луча и будет падать на мишень, которая предпочтительно размещена в теле пациента, хотя для облучения поверхности тела, оси луча и мишень находятся вне тела. Ось может быть прямой или кривой. Состав и/или геометрия мишени или рентгеновское излучение, материал выбираются для обеспечения требуемой картины рентгеновского излучения. Экранирование на мишени или вокруг мишени, кроме того, дает возможность управления энергией или пространственным профилем рентгеновского излучения в строгом соответствии с требуемым распределением излучения через требуемую область. Источник рентгеновского излучения со стабильными и воспроизводимыми характеристиками можно создать при помощи электронного пятна большего или меньшего, чем мишень, хотя устройство формирования приводит к неэффективному использованию энергии электронов и в конечном счете может потерять сферическую изотропность вынужденного излучения.
Настоящее изобретение в дальнейшем обеспечивает способ облучения злокачественных клеток, типа обнаруженных в опухолях, in vivo, используя устройство, описанное выше. В общем, способ включает идентификацию и обнаружение злокачественных клеток устройством в общем пригодным в технике, таким как компьютерное томографическое (CT) сканирование или магниторезонансное изображение (MRI). Биопсию игольчатого типа опухолей можно представить для подтверждения диагноза. Затем выбирается область лечения и определяется доза излучения. Такое планирование лечения излучением включает определение размеров и конфигурации опухоли, определение точного их расположения в теле и идентификацию критической чувствительности к излучению биологических структур, окружающих опухоль, выбор правильности решения по распределению дозы излучения в опухоли и окружающей ткани и внутренней траектории в опухоли, имплантированных частях устройства. Для сферических опухолей планирование лечения можно представить вручную при использовании CT или MRI информации. Однако для более сложной геометрии близко расположенных критических структур или процедур с повышенной точностью предпочтительным является трехмерное компьютерное изображение. В этом случае опухоли и критические структуры, например, вручную или полуавтоматически сигментируются на последовательности цифрового CT сканирования, и предоставляется трехмерное изображение, которое позволяет просматривать опухоль в любом направлении. Для радиохирургических процедур разработаны различные системы программного обеспечения, наподобие тех, которые используют линак (Linac) или гамма-скальпель, и некоторые пригодны для коммерческого применения. Например, фирма Radionics Software Applications из Арлингтона, штат Массачусетс, предлагает для продажи программное обеспечение, которое позволяет получать изображение CRW и BRW-стереотактические кадры, совместно с графическим транспарантом черепа. Профили изодоз перекрываются на опухоли и другой ткани мозга. Подобное программное обеспечение можно использовать вместе с изобретением, описанным в патенте США N 955494, в котором получается изображение в соответствии со стереотактическим кадром, которое используется совместно с мишенью электронного луча, создающего рентгеновское излучение, которое введено в опухоль. Контуры изодозы вокруг мишени накладываются на опухоль и соседнюю ткань. Абсолютная дозировка излучения, получаемая вдоль каждого контура, определяется путем экспериментальной дозиметрии, представленной для калибровки зонда. В этих испытаниях доза измеряется на многократных участках вокруг мишени, погруженной в резервуар с водой. Мягкие ткани адекватно копируются водой. Доза измеряется посредством ионизационной камеры такой, как производится фирмой PTW из Фрейбурга, Германия, в которой ионы, генерирующие рентгеновское излучение, создают небольшой ток, который детектируется электрометром, таким как предлагает коммерчески пригодный вариант фирма Keithley Radiation Mesuvement из Кливленда, штат Огайо. С другой стороны, мишень можно погружать в моделирующий биологическую ткань иммитатор. Такие пластмассовые, из "твердой воды" иммитаторы находят коммерческое применение (фирма RMI, Мидлтон, WI) и моделируют различные ткани тела, мягкую ткань мозга. Термолюминесцентные детекторы (TLD), либо откалиброванную рентгеновскую чувствительную пленку (т. е. гафхромовую пленку фирмы Far West Technologies, Goleta, CA) можно установить в "твердой воде" для измерения непосредственно дозы облучения. Используя изображение и результаты дозиметрии из радиационного планирования лечением, источник электронного луча малой мощности и мишень, генерирующая рентгеновское излучение с выбираемой формой картины, и узел экрана, устанавливаются внутри или рядом с областью, содержащей клетки, которые будут облучаться, в общем опухолевые клетки, например, совместно со стереотактическим набором кадров, типа описанного в патенте США N 955494. Можно использовать и другие установленные наборы или способы.
В соответствии с настоящим изобретением геометрия узла мишени или экрана и материалы формируются и выбираются в соответствии с характеристиками требуемой области, которая будет облучаться. Предлагается программируемый источник питания, который можно использовать для изменения напряжения, тока и длительности излучения источника электронного луча для установления в соответствии с дозиметрической информацией требуемого электронного луча, который направляется на цель. В результате, рентгеновское излучение, испускаемое мишенью, как модифицированное узлом экрана, распространяется через требуемую область, которая будет облучаться для разрушения клеток в этой области. Используя способ сигнала с обратной отрицательной связью, в котором рентгеновское излучение, выходимое из мишени в обратном направлении вдоль траектории электронного луча, контролируется детектором, установленным позади электронного излучателя. Регулирование отклонения электронного луча можно производить в автоматическом режиме управления и при оптимальном положении области падения электронного луча или пятна на мишень.
В частности, лечение опухоли мозга можно осуществить при использовании устройства настоящего изобретения, содержащего сочетание рентгеновского источника малой мощности для генерации управляемой картины излучения с устройством для точного позиционирования источника рентгеновского излучения в мозге.
Источник рентгеновского излучения можно таким образом точно разместить в опухоли или рядом. Источник рентгеновского излучения вместе с мишенью и узлом экрана настоящего изобретения можно использовать в различных участках тела для выработки общепринятого типа полей облучения при лечении различных типов опухолей. Также, поля облучения можно создавать для каждой проходящей лечение опухоли. Однако геометрическое сходство для многих опухолей позволит проводить это лечение со стандартной установкой экранов.
Согласно дальнейшему воплощению изобретения зонд может быть в действительности гибким так, чтобы позволить ему проходить через существующие проходы или обходить препятствия. Согласно одному такому воплощению фотоэмиссионный элемент (т. е. фотокатод) размещен вдоль мишени элемента, в узле мишени. Кроме того, гибкий волоконно-оптический кабель, по которому проходит свет от источника лазерного излучения к фотокатоду, позволят сформировать основу для гибкого зонда.
Один вывод высоковольтного источника питания подсоединяется к фотокатоду через электрический провод, введенный в оптический волоконный кабель. Другой вывод источника питания подсоединяется к элементу мишени, через электрический провод, гибкий, снаружи оболочки, сформированной вокруг оптического волоконного кабеля. В этом случае устанавливается электрическое поле, которое действует для ускорения электронов, испускаемых из фотокатода вперед по направлению к элементу мишени. Как в предыдущих обсужденных вариантах воплощения, элемент мишени вырабатывает рентгеновское излучение в ответ на падающие электроны из фотокатода.
Краткое описание рисунков
В дальнейшем изобретение поясняется конкретным вариантом его воплощения со
ссылками на сопровождающие чертежи, на которых:
фиг. 1 - общий вид источника рентгеновского излучения малой мощности, воплощающий настоящее изобретение;
фиг. 2 - схема оболочки,
приспособленной для использования с устройством, изображенным на фиг. 1;
фиг. 3А и фиг. 3В - общий вид и вид в разрезе, соответственно, установленного на поверхности устройства, воплощающего
настоящее изобретение;
фиг. 4 - блок-схема воплощения, изображенного на фиг. 1;
фиг. 5А и фиг. 5В - графическое представление спектра рентгеновского излучения вольфрамовой и
молибденовой мишеней, соответственно;
фиг. 6 - детальная блок-схема источника питания воплощения, изображенного на фиг. 1;
фиг. 7 - детальная схема источника питания, изображенного
на фиг. 6;
фиг. 8 - общий вид узла управления лучом, воплощающего настоящее изобретение;
фиг. 8А - вид в разрезе узла фиг. 8, показанного вдоль линии 8А;
фиг. 9 - общий вид
системы лечения опухоли мозга рентгеновским излучением, содержащего стереотактический кадр для позиционирования источника рентгеновского излучения;
фиг. 10 - общий вид источника
рентгеновского излучения и соединительный узел системы фиг. 9;
фиг. 11 - схема источника питания высокого напряжения источника рентгеновского излучения, изображенного на фиг. 10;
фиг. 12 - вид в поперечном сечении конца зонда, имеющего альтернативный узел мишени, который включает экран рентгеновского излучения и мишень рентгеновского излучения для получения стабильного и
воспроизводимого источника рентгеновского излучения;
фиг. 13 - вид фрагментов поперечного сечения одной геометрической формы рентгеновской мишени;
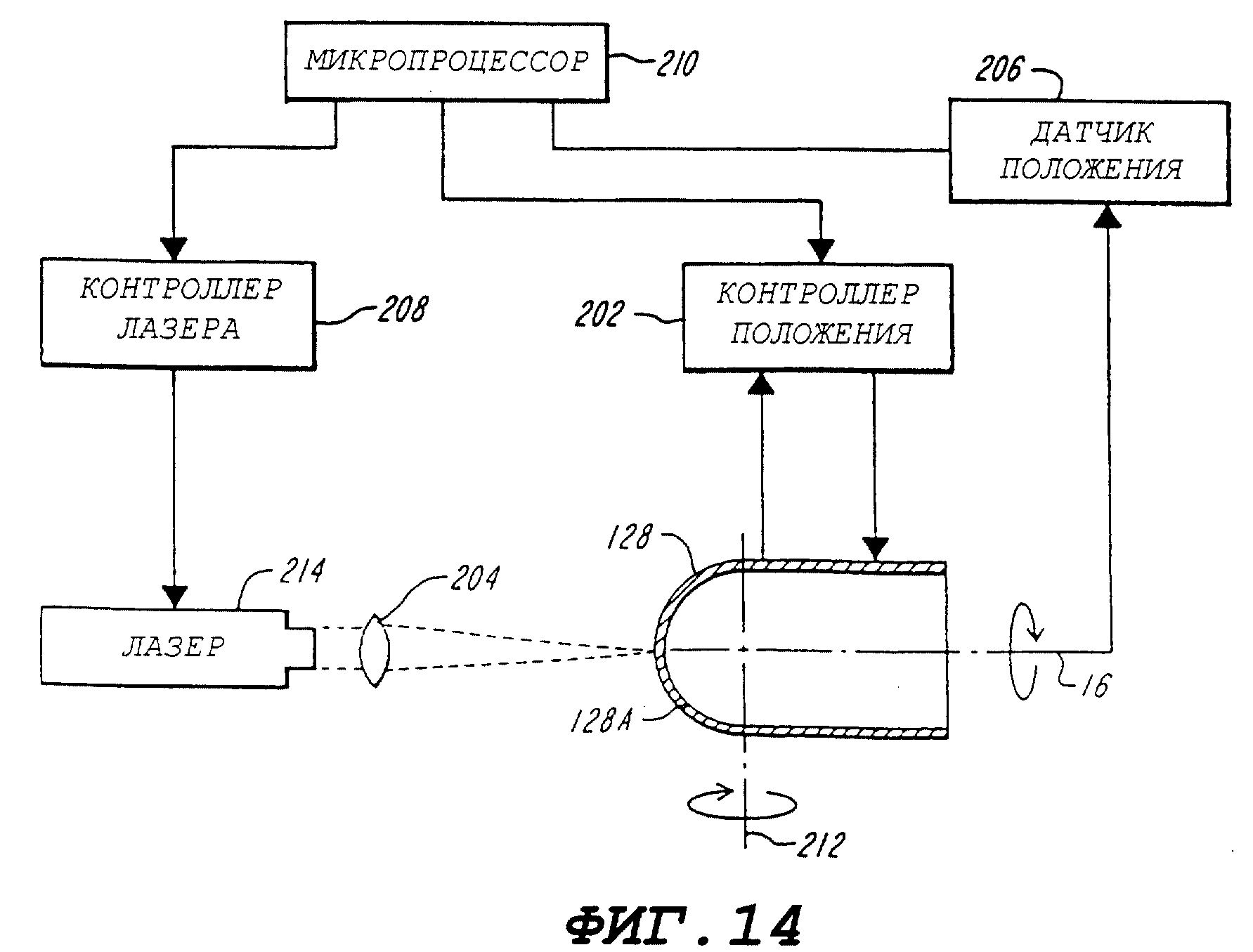
фиг. 14 - блок-схема лазерной
системы фрезерования для производства рентгеновских экранов с переменной толщиной;
фиг. 15А и фиг. 15В - общие виды зонда и узла мишени для точной угловой регулировки рентгеновского экрана;
фиг. 16 - вид в поперечном сечении источника рентгеновского излучения малой мощности, имеющего внутренний узел управления лучом, который включает контур обратной связи для установки
электронного луча;
фиг. 17 - вид в поперечном сечении источника рентгеновского излучения малой мощности, имеющего внешний узел управления лучом, который включает контур обратной связи для
установки электронного луча;
фиг. 18 - вид в поперечном сечении узла, изображенного на фиг. 17, показанного вдоль линий 16с;
фиг. 19 - вид в поперечном сечении устройства
механической установки зонда для облучения широкой области;
фиг. 20A и 20B - виды в поперечном сечении гибкого зонда, который состоит из фотоэмиттера, размещенного внутри узла мишени;
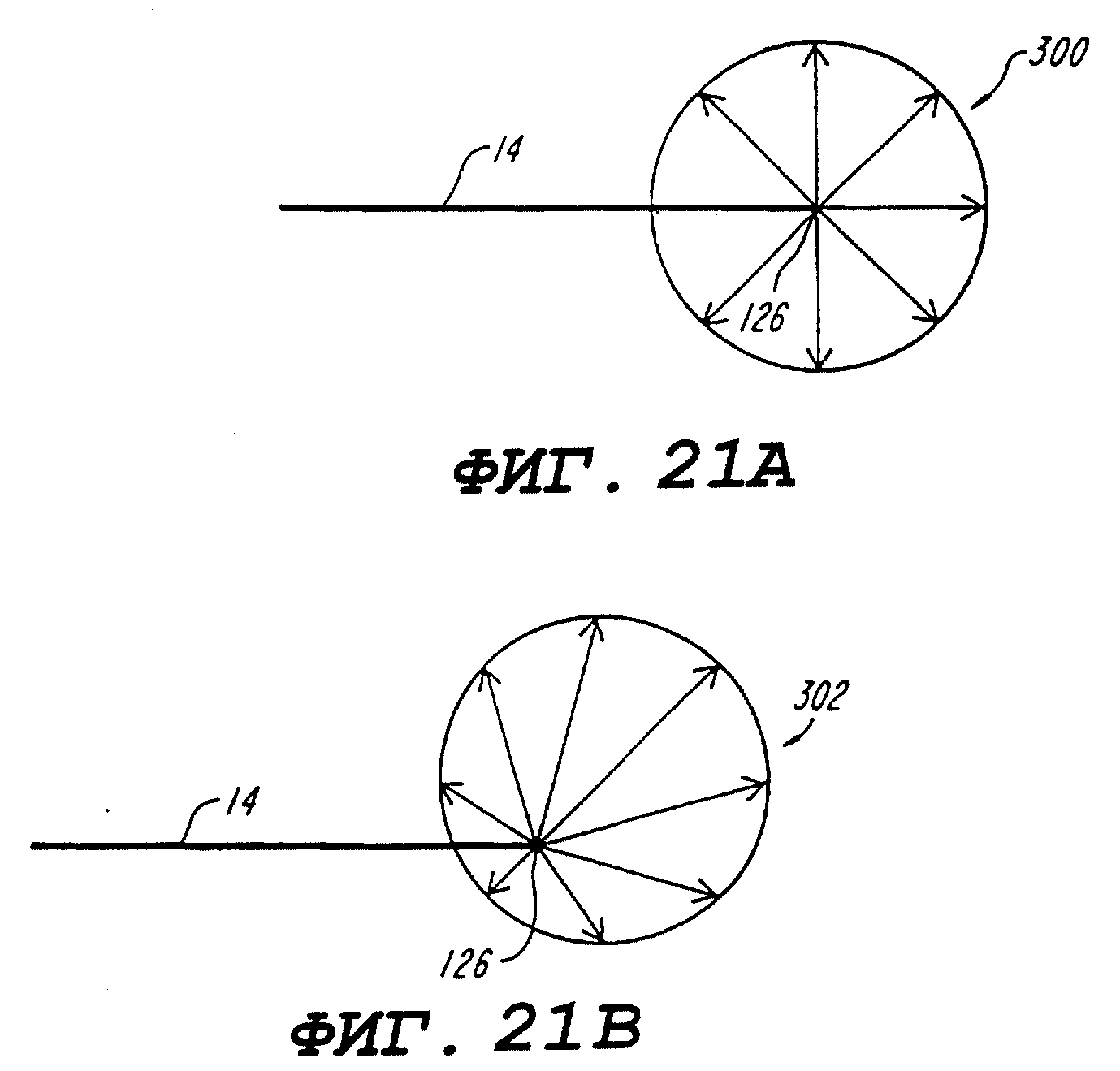
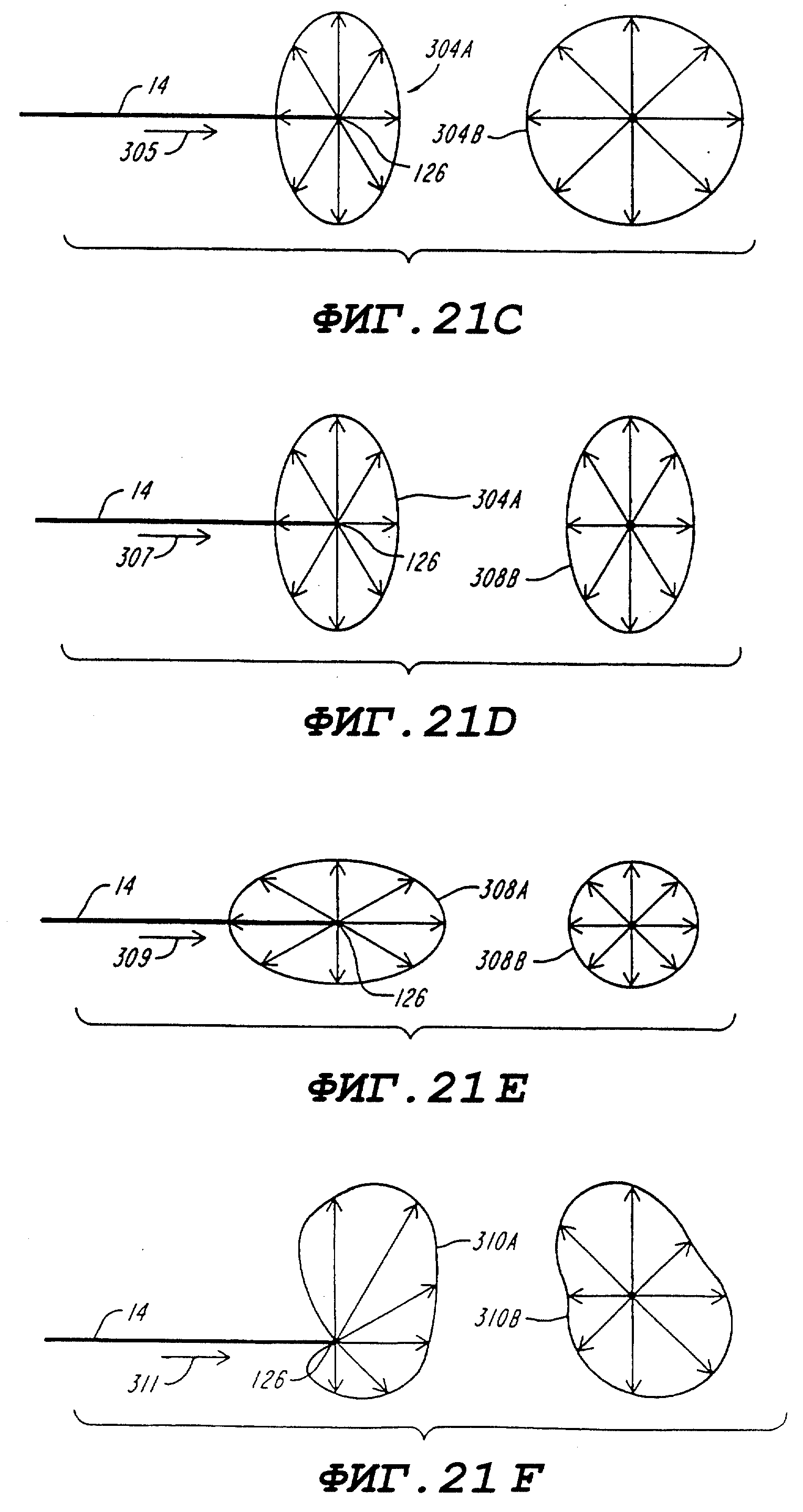
фиг. 21A-21F - изображают образцы различных контуров изодозы, которые можно получить при помощи изобретения;
фиг. 22 - схематически изображает в разрезе наконечник зонда, имеющего экран,
который установлен рядом с фотокатодом источника, изображенного на фиг. 20А.
Подобные перечисленные элементы на каждой фигуре представляют аналогичные или сходные элементы.
Описание предпочтительных вариантов
Настоящее изобретение представляет собой относительно небольшое, возбуждаемое электронным лучом, рентгеновское устройство малой мощности.
Устройство можно использовать для медицинских целей, например, при терапевтическом или паллиативном лечении облучением опухолей или для других целей.
В отношении медицинского использования устройство можно полностью имплантировать или частично вводить в заранее выбранную внутреннюю область пациента для проведения рентгеновского облучения рентгеновским излучением при выбираемых временах экспозиции. С другой стороны, устройство можно установить на поверхности пациента, внешней к области, которая будет облучаться. Также описан способ для лечения опухолей пациентов при использовании устройства изобретения.
В общем, устройство настоящего изобретения включает электронный луч (e-луч), возбуждаемый источником рентгеновского излучения, который работает при относительно малых напряжениях, т.е. в диапазоне приблизительно от 10 кВ до 90 кВ, и относительно малых токах электронного луча, т.е. в диапазоне приблизительно от 1 нА до 100 мкА. При этих рабочих напряжениях и токах, выходное рентгеновское излучение относительно мало, и устройство можно сделать относительно небольшим и приспособленным для имплантации в медицинских терапевтических применениях. С точки зрения низкого уровня выходного рентгеновского излучения адекватное проникновение в ткань и разрушительную дозу облучения можно достигнуть посредством размещения рентгеновского источника рядом с областью, которая будет облучаться, или внутри ее. Таким образом, рентгеновское излучение генерируется из хорошо определенного, маленького источника, размещенного внутри или рядом с областью, которая будет облучаться. В одном варианте воплощения малую дозу интенсивности рентгеновского излучения можно использовать для любой части опухоли, либо постоянно, либо периодически сверх установленных периодов времени, т.е. вплоть до одного месяца. При использовании стереотактического кадра для лечения опухолей мозга более высокую дозу интенсивности можно использовать для опухоли за более короткие периоды времени (т.е. порядка от 5 мин до 3 ч).
Настоящее изобретение обеспечивает промежуточную радиотерапию, подобную той, которая достигается посредством имплантированных капсул, иголок, трубок и нитей, содержащих натуральные радиоактивные изотопы, известные как брахитерапия. Однако программируемый источник питания можно включать в рентгеновский источник настоящего устройства для изменения энергии, интенсивности и длительности излучения. Это отличается от брахитерапии тем, что интенсивность и глубину проникновения рентгеновского излучения можно изменять без хирургического или без вторжения в организм перемещающихся изотопов. Более того, настоящее изобретение не ограничивается периодом полураспада характерных изотопов и отсутствует риск излучения при выключении.
Фиг. 1 показывает рентгеновское устройство 10, воплощающее настоящее изобретение. Устройство 10 включает корпус 12 и цилиндрический зонд 14, который проходит от кожуха 12 вдоль соответствующей оси 16. Кожух 12 закрывает источник 12А (источник питания высокого напряжения изображен в виде электрической схемы на фиг. 6 и 7). Зонд 14 представляет собой полую трубку, имеющую генератор электронного луча (катод) 22 рядом с источником 12А питания высокого напряжения. Катод 22 расположен в непосредственной близости с круглым фокусирующим электродом 23 обычно под одним потенциалом, как и катод 22. Круглый анод 24 установлен на расстоянии приблизительно 0,5 см или больше от круглого фокусирующего электрода 23. Полый трубчатый зонд 14 расположен вдоль такой же оси как катод, сетка и щель в аноде. Зонд 14 представляет собой одно целое с кожухом 12 и вытянут вперед по направлению к узлу 26 мишени. В различных вариантах воплощений часть зонда 14 можно выборочно экранировать для управления пространственным распределением рентгеновского излучения. Кроме того, зонд 14 можно снабдить магнитным экраном для предотвращения воздействия от внешних магнитных полей, вызывающих отклонения луча в сторону от мишени.
Генератор 22 электронного луча может включать термоэмиттер (управляемый ненагруженным источником питания низкого напряжения) или фотокатод (облучаемый светодиодом или лазером). Источник питания высокого напряжения устанавливает ускоряющую разность потенциалов между катодом и генератором 22 и заземленным анодом 24 так, что электронный луч устанавливается вдоль контрольной оси 16, через центральное отверстие анода и до узла 26 мишени, с областью между анодом 24 и узлом 26 мишени являясь в сущности свободным полем. Элементы генерации и ускорения луча приспособлены для установки тонкого (т. е. диаметром 1 мм или меньше) электронного луча внутри зонда 14 вдоль условной прямолинейной оси 16.
В предпочтительном варианте воплощения зонд 14 является полым цилиндром с откаченным воздухом, сделанным из берилиевой (Be) насадки и молибден-рениевого (Mo-Re), молибденового (Mo) или мю-мераллического корпуса и с удлиненным концом из нержавеющей стали. Цилиндр имеет длину 16 см с внутренним диаметром 2 мм и внешним диаметром 3 мм. Узел 26 мишени включает излучающий элемент, состоящий из небольшого берилиевого (Be) элемента 26A мишени, покрытого тонкой пленкой или слоем 26В из элемента с высоким Z, таким как вольфрам (W), уран (U) или золото (Au) на подвергаемой воздействию падающего электронного луча стороне. Например, с электронами, ускоренными до 30 кэВ, двухмикронная вольфрамовая пленка толщиной 2,2 микрона поглощает все падающие электроны, при передаче приблизительно 95%, от 30 кэВ, 88% от 20 кэВ, и 83% от 10 кэВ рентгеновского излучения, генерируемого в этом слое. В предпочтительном варианте воплощения берилиевый элемент 26А мишени имеет толщину 0,5 мм с результатом, что 95% этого рентгеновского излучения, генерируемого в перпендикулярном и прямом направлении к подложке, и прошедшего через вольфрамовую мишень, проходит далее через берилиевую подложку и наружу на отдаленный конец зонда 14. Хотя элемент 26A мишени, показанный на фиг. 3B, сделан в форме диска, можно использовать элементы с другими формами, такими, которые имеют полусферические или конические внешние поверхности.
В некоторые формы мишени, элемента 26A окна можно включить многослойную пленку (или сплав) 26B, в которой различные слои могут иметь разные характеристики эмиссии. Например, первый слой может иметь пик эмиссии (энергии) на относительно низкой энергии, и второй (основной) слой может иметь пик эмиссии (энергии) на относительно высокой энергии. С этой формой изобретения может использоваться низкая энергия электронного луча для генерации рентгеновского излучения для достижения первой характеристики излучения. В качестве примера электронный луч шириной 0,5 мм излучается на катоде и ускоряется до 30 кэВ анодом, с поперечными энергиями электронов 0,1 эВ, и попадает на узел 26 мишени, расположенный от анода на расстоянии шестнадцати сантиметров, с диаметром луча меньше 1 мм на элементе 26A мишени. Рентгеновское излучение генерируется в узле 26 мишени в соответствии с предварительно выбранным напряжением луча, током и составом элемента 26A мишени. Вырабатываемое таким образом рентгеновское излучение проходит через элемент 26A берилиевый мишени в зонде с минимальной потерей энергии. В качестве альтернативного варианта для берилия элемент 26A мишени можно сделать из углерода или другого подходящего материала, который позволяет рентгеновскому излучению проходить с минимальной потерей энергии. Оптимальным материалом для элемента 26A мишени является углерод в форме алмаза, так как этот материал обладает отличной теплопроводностью. Используя эти параметры, полученное в результате рентгеновское излучение имеет достаточную энергию для проникновения в мягкие ткани на глубину от сантиметра и более, точная глубина зависит от распределения энергии рентгеновского излучения.
Устройство, изображенное на фиг. 1, частично адаптировано для полной имплантации в пациента, где кожух 12 имеет биосовместимую внешнюю поверхность и закрывает как схему 12A источника питания высокого напряжения, предназначенного для установления управляющего напряжения для генератора 22 луча, так и объединенную батарею 12B для управления этой цепью 12A. В этом случае объединенный контроллер 12C управляет выходным напряжением в схеме 12A высоковольтного источника, способом, описанным ниже.
Устройство, изображенное на фиг. 1, можно также использовать в виде, где только зонд 14 вводится в пациента, хотя кожух остается вне пациента, т.е. транскатная форма. В последнем случае можно поочередно дистанционно перемещать некоторые или все различные элементы, показанные внутри кожуха 12.
В транскатной форме устройство 10 можно использовать с удлиненным закрытым концом (или в форме чашки) оболочки 34, как изображено на фиг. 2, имеющей биосовместимую биоповерхность, например, изготовленную из медицинского качественного алифатического полиуретана, который изготавливается под маркой фирмы "Tecoflex by Thermediсs, Inc., Woburn, Massachusetts. С этой конфигурацией зонд 14 первым вставляется в оболочку 34. Оболочка 34 и зонд 14 вводятся затем в пациента через кожу. С другой стороны, можно вводить порт через кожу и присоединяться к нему, как например, в порте Dermaport изготовленного фирмой Thermediсs Inc. , Woburn, Massachusetts. Зонд 14 далее вводится в порт.
Внутреннее покрытие оболочки или порта можно представить в виде рентгеновского экрана посредством введения сульфата бария или трехокиси висмута или других материалов, экранирующих рентгеновское излучение, в оболочке. Если необходимо, зонд 14 и кожух 12 можно поместить в теле пациента для предотвращения какого-либо относительного перемещения в течение всего времени лечения. Экземпляр оболочки 34 изображен на фиг. 2.
В одном варианте воплощения устройства в качестве изображенного на фиг. 1 основной корпус зонда 14 можно сделать из магнитного экранного материала, такого как мю-металл. С другой стороны, зонд 14 можно изготовить из немагнитного металла, имеющего предпочтительно высокое значение модуля Янга и ограничения по эластичности. Образцы такого материала включают молибден, рений или сплавы этих материалов. Внутреннюю и внешнюю поверхности зонда 14 можно в дальнейшем покрыть сплавом, обладающим высокой магнитной проницаемостью типа пермалоя (приблизительно 80% никеля и 20% железа) для того, чтобы обеспечить магнитное экранирование. С другой стороны, тонкую втулку из мю-металла можно подобрать над или внутри зонда 14. Рентгеновское устройство 10 можно в дальнейшем использовать в среде, в которой присутствуют постоянные и переменные магнитные поля, связанные с электрической энергией, магнитное поле Земли или другие магнитные тела, способные отражать электронный луч от оси зонда.
В имплантированной конфигурации источник 12A питания и узел 26 мишени предпочтительно закрыты металлической капсулой для защиты прохождения тока от источника рентгеновского излучения до пациента. Закрытый кожух 12 и зонд 14 помещены в капсулу с постоянной внешней оболочкой соответствующего экранирующего материала типа тех, которые указаны ранее.
Высоковольтный источник 12A питания в каждом из изображенных вариантов воплощения предпочтительно удовлетворяет трем критериям: 1) малые размеры; 2) высокая эффективность, позволяющая использовать мощность батареи; и 3) независимо изменяемые напряжение и ток рентгеновской трубки, которые позволяют программировать устройство для специальных применений. Мощный высокочастотный импульсный конвертер используется для выполнения этих требований. Наиболее подходящей схемой для генерации малой мощности и высокого напряжения является обратноходовый преобразователь напряжения, работающий совместно с высоковольтным умножителем, выпускаемым фирмой Cocknft-Walton. Малая мощность потерь, управление режимом переключения источника питания на основе интегральных схем (ИС) пригодны в настоящее время для управления такой схемы, имеющей несколько элементов. Для того, чтобы обеспечить действительное управление рентгеновским излучением, предпочтительный вариант воплощения настоящего изобретения устанавливает независимый контроль напряжения и тока катода без использования сеточного электрода. В этой форме изобретения нагревание осуществляется высокочастотным током в термокатоде 22, предпочтительно при использовании подсоединенного к источнику питания нити накала трансформатора с напряжением 0,6 В и изменяющимся током 0-300 мА на катоде с потенциалом 40 кВ.
Фиг. 3A и 3B показывают альтернативный вариант воплощения 10' изобретения, приспособленного для использования на поверхности, которое предназначено для прямого размещения на коже пациента. Эта форма изобретения особо используется для лечения рентгеновским излучением кожных повреждений или опухолей или для других дерматологических применений. На фиг. 3A и 3B элементы, которые соответствуют элементам в варианте воплощения, изображенного на фиг. 1, показаны со ссылками на аналогичные обозначения. Устройство 10' генерирует электронный луч в канале 40, закрытом кожухом 12, в котором канал 40 соответствует зонду 14. В настоящем варианте воплощения, изображенном на фиг. 3A и 3B, узел 26 мишени (элемент 26A или 26B) работает как анод также, как рентгеновский излучатель. С другой стороны, устройство 10' подобно устройству 10. При помощи конфигурации фиг. 3A и 3B рентгеновское излучение малой мощности можно направлять на требуемую область пациента.
Во всех выше описанных вариантах воплощения элемент эмиссии рентгеновского излучения узла мишени приспособлен для того, чтобы находиться рядом или внутри области, которая будет облучаться. Близкое расположение излучающего элемента к области мишени, т.е. к опухоли, устраняет необходимость использования современных высоковольтных аппаратов для достижения достаточного проникновения рентгеновского излучения через поверхность тела в расположение опухоли. В устройствах с низким напряжением также можно фокусировать излучение в намеченную опухоль и ограничивать разрушение в окружающей ткани и на поверхности кожи в точке проникновения. Например, получение дозы 4000 рад, которая необходима после мастектомии при напряжении электронного пучка 40 кВ и токе 20 мкА, может потребовать приблизительно от 1 до 3 часов облучения. Однако после того как источник рентгеновского излучения в этом предпочтительном варианте воплощения, устанавливается рядом или внутри области, которая будет облучаться, значительно уменьшается риск попадающей дозы радиации в другие части тела пациента.
Кроме того, специфику лечения опухолей можно достигнуть путем подбора геометрии мишени и экрана и материала в месте облучения. Этот подбор облегчает управление энергией и пространственным профилем рентгеновского излучения, гарантируя более однородное распределение излучения, которое проходит через намеченную опухоль.
Фиг. 4 схематически изображает устройство 10 источника рентгеновского излучения, показанного на фиг. 1. В этой предпочтительной конфигурации кожух 12 разделен на первую часть 12' и вторую часть 12''. Закрытая изнутри первая часть 12' кожуха имеет перезаряжаемую батарею 12B, разрядную цепь 12B, которая приспособлена для использования с внешним разрядником 50, и телеметрическую цепь 12E, приспособленную для того, чтобы отображать состояние внешнего телеметрического устройства 52, работа которого описана ниже. Часть 12' подсоединена кабелем к второй части 12'' кожуха. Вторая часть 12'' кожуха включает источник 12A питания высокого напряжения, контроллер 12C и зонд 14, а также элемент 22, генерирующий электронный луч. В одном варианте воплощения генератор электронного луча включает термоэмиттер 22, который в свою очередь генерирует электроны, которые затем ускоряются в направлении анода 24. Анод 24 не только притягивает электроны, но и пропускает их через свое центральное отверстие в направлении узла 26 мишени. Контроллер 12C управляет источником 12A питания для динамического управления напряжением катода, током электронного луча, временными параметрами или обеспечивает предварительную установку напряжения, тока луча и временных характеристик.
Также показано, что существует альтернативный генератор электронного луча, который включает в себя фотоэмиттер 22, облучаемый источником 56 света, таким как лазерный диод или светодиод, запитанный посредством устройства управления 55. Свет фокусируется на фотоэмиттер 22 посредством фокусирующей линзы 58.
В изображенном варианте воплощения устройство 52 и цепь 12E действуют совместно, позволяя внешнему управлению (динамическому или заданному) управлять источником 12A питания и временными характеристиками. В вариантах, где кожух 12'' не вводится, но где проходит в тело пациента только зонд 14, контроллер 12A может непосредственно использоваться для управления работы; в этом случае отсутствует необходимость в цепи 12E.
В важном аспекте изобретения узел 26 мишени можно сформировать так, чтобы получать рентгеновское излучение с требуемой картиной облучения в заданной спектральной области, и имеющего заданное пространственное распределение. Частично выполнить мишень с заданным спектром можно посредством выбора материалов мишени с известными характеристиками. Например, как показано на фиг. 5A и 5B, спектр излучения для вольфрамовых мишеней (фиг. 5A) и молибденовых мишеней (фиг. 5B) отличается. Фиг. 5A изображает спектр рентгеновского излучения от трубки с вольфрамовой мишенью, работающей при напряжениях 30 и 50 кВ. Необходимо отметить, что преобладает спектр тормозного излучения и что генерация рентгеновского излучения происходит в широком диапазоне энергии. Фиг. 5B показывает спектр излучения от трубки с молибденовой мишенью, также работающий при напряжениях 30 и 50 кВ. Следует отметить отсутствие рядом тормозного рентгеновского излучения. Необходимо отметить, что изменение потенциала напряжения в трубке от 30 до 50 кВ приводит к незначительному изменению спектра излучения рентгеновской трубки, использующей молибденовую мишень. Таким образом, спектр рентгеновского излучения от узла 26 мишени можно эффективно сформировать путем выбора материала мишени для обеспечения требуемого радиационного проникновения в ткань, например, опухоль.
Пространственное распределение рентгеновского излучения можно также сформировать путем изменения геометрической конфигурации элемента 26A мишени. Например, элемент 26 мишени можно сформировать так, что электроны, направляемые из анода, будут отклоняться на заданный угол, или можно выборочно направить в различные зоны области, из которой будет происходить эмиссия. Например, элемент 26A мишени можно изготовить так, чтобы он был достаточно тонким и непрозрачным для электронов, но достаточно тонким, чтобы выполнить роль транспаранта рентгеновского излучения. Особенно важно, если используется элемент сферической золотой мишени, имеющей толщину около 0,5 мкм, и при напряжении электронного луча 40 кВ, то в значительной степени все электроны останавливаются элементом мишени и в значительной степени может выводиться все рентгеновское излучение, генерируемое в элементе мишени.
Пространственное распределение рентгеновского излучения можно также сформировать посредством использования экрана передачи рентгеновского излучения, имеющего профиль с изменяемой толщиной, в узле 26 мишени. Фиг. 12 изображает зонд 14, имеющий альтернативный узел 126 мишени, для использования с рентгеновским устройством 10, показанным на фиг. 1, который содержит такой экран. В изображенном варианте воплощения зонд 14 в значительной степени подобен зонду 14, показанному на фиг. 1, за исключением узла 126 мишени. Узел 126 мишени включает верхнюю часть 126 зонда из материала (например, Be), который является транспарантом для рентгеновского излучения, мишень 126B рентгеновского излучения для генерации рентгеновского излучения после облучения электронным лучом, прикрепленную к зонду 14 вдоль оси 16 зонда на конечной части, отдаленному к катоду 22 и аноду 24 (показано на фиг. 1). В предпочтительном виде внешняя поверхность верхней части 236B зонда выпуклая и предпочтительно полусферическая, как в изображенном варианте воплощения, хотя можно использовать и другие выпуклые поверхности. Узел 126 мишени изготовлен таким образом, что внешний диаметр верхней части 126A зонда меньше внешнего диаметра зонда 14. Изменяемая толщина рентгеновского экрана (или теневой маски) 128, и лежащий под экраном носитель 128A расположены на верхней части 126A зонда узла 126 мишени. В месте соединения узла 126 мишени и зонда 14 внешний диаметр узла 126 мишени в значительной степени соответствует диаметру зонда 14.
Экран 128 рентгеновского излучения изготовлен из материала, который имеет высокую степень поглощения, и поддерживается посредством носителя 128A экрана. Поток рентгеновского излучения из любой точки узла 126 мишени частично зависит от толщины экрана 128 рентгеновского излучения вдоль оси, проходящей от мишени 126B и проходящей через эту точку. Таким образом, в соответствии с изобретением используется выборочное ограничение по толщине экрана рентгеновского излучения для генерации изменяемого в пространстве распределения дозы рентгеновского излучения.
В предпочтительном варианте зонд 14 имеет внешний диаметр 3 мм и внутренний диаметр 2 мм и имеет типичную длину от 10 до 16 см. Носитель 126 мишени изготовлен из берилия и имеет толщину 0,5 мм. Носитель 128A экрана изготавливается из легких элементов, таких как берилий, магний, алюминий или углерод, и имеет толщину 0,2 мм, и экран 128 имеет толщину в диапазоне от 0 до 0,1 мм, если сделан из золота.
Мишень 126B рентгеновского излучения представляет собой небольшой диск (например, с диаметром 0,1 мм), изготовленный из материала, обладающего эмиссией рентгеновского излучения (например, металл с высоким атомным номером типа золота), расположенного в центре носителя 126C мишени. Как будет подробно рассмотрено ниже, размер мишени 126B рентгеновского излучения может быть небольшим по отношению к диаметру электронного луча, устанавливаемого вдоль оси 16 зонда, так что источник рентгеновского излучения определяется посредством положения небольшой мишени, но не положением или размером электронного луча. Эта особенность позволяет освещать экран 128 рентгеновского излучения воспроизводимым и стабильным источником рентгеновского излучения. Однако для электронного луча, чье пятно на мишени 126B больше, чем мишень 126B, снижается за счет потерь эффективность генерации рентгеновского излучения. Такие потери можно избежать посредством фокусировки луча в небольшое пятно, сравнимое с размером мишени 126B, и контролируя ее положение на мишени 126B подходящими средствами.
Пространственное разрешение предварительно выбранного уровня дозы облучения, которое можно получить посредством использования экрана 128, ограничивается несколькими факторами, включая полутень вследствие конечного размера источника рентгеновского излучения; нестабильность размера и положения источника рентгеновского излучения, вследствие характерной нестабильности электронного пятна, возникающей при генерации рентгеновского излучения; рассеяние рентгеновского излучения, дающее вклад энергии в уровень дозы облучения; и воспроизводимость параметров источника рентгеновского излучения от зонда к зонду и его положение относительно экрана 128.
Полутень определяется отношением размера источника рентгеновского излучения к ее расстоянию от экрана 128. Для однородного источника предпочтительный диапазон для этого отношения составляет порядка от 1/20 до 1/3, который зависит от характера рассеяния. Стабильность размеров источника рентгеновского излучения и его положение является предпочтительным для небольшой доли оптимального источника в соотношении расстояний.
Один способ установления приемлемой полутени и регистрации экранированного источника рентгеновского излучения заключается в управлении положением и размером источника рентгеновского излучения посредством управления фокусным расстоянием и отклонением падающего электронного луча вдоль оси 16. Например, электронный луч можно сфокусировать в пятно на выходной поверхности рентгеновского излучения мишени 126B, таким образом диаметр фокального пятна определяет размеры источника рентгеновского излучения. Этот способ требует не только, чтобы размеры пятна были правильными, но и чтобы положение пятна относительно экрана 128 рентгеновского излучения было точно известным и поддерживаемым.
В этом варианте воплощения мишень может быть теоретически большой, как и при изготовлении с учетом традиционных требований. Однако в предпочтительном варианте воплощения мишень 126B рентгеновского излучения имеет размеры такие же или немного больше, чем у электронного луча.
Для того, чтобы гарантировать, что положение электронного пятна относительно экрана является как стабильным во времени для любой данной малогабаритной рентгеновской системы, так и пространственно воспроизводимым во всех других системах, что имеет место при эксплуатации, можно использовать точно размещенные отправные отметки вместе с дефлекторами электронного луча для определения положения электронного пятна относительно экрана. Такие отправные отметки состоят из угла, определяющего границу между двумя областями, которые сильно отличаются характером электронного пучка. Например, в данном случае граница между материалом 126B мишени таким, как Au, и материалом 126C носителя мишени таким, как Be, может служить в качестве отправного угла. Имеющееся различие в свойствах заключается в том, что Au имеет значительно большую эффективность в качестве источника рентгеновского излучения, чем Be, при воздействии электронного луча с высокой энергией. Так как луч проходит поперек отправной отметки, детектор рентгеновского излучения может регистрировать отличие в интенсивности рентгеновского излучения и генерировать соответствующий сигнал управления для использования в устройствах отклонения луча.
Детектор рентгеновского излучения может вводиться в контур управления обратной связи для того, чтобы управлять перемещением луча относительно мишени и предпочтительно в центре мишени, которая находится в поле зрения электронного источника. В одной такой конфигурации, где положение мишени в общем известно по отношению к траектории луча, но желательно сцентрировать траекторию луча на мишени, луч можно будет первым разворачивать поперек мишени в первом (по оси x) направлении, которое ортогонально траектории луча. Так как луч проходит отправные углы мишени (например, когда луч встречается с мишенью во время развертки, и затем когда луч покидает мишень), контроллер идентифицирует положение отправных углов и определяет составляющую по оси x сигнала управления, фиксирует среднюю точку между двумя отправными углами в развертке по направлению оси x. Затем луч устанавливается в положение в соответствии с элементом сигнала управления (т.е. середина пути между обнаруженными отправными углами развертки по оси x), и развернутые во втором (по оси y) направлении ортогональном направлению по оси x и траектории луча. В течение развертки в направлении по оси у, детектируются отправные углы и определяется сигнал управления составляющей по оси y, который показывает среднюю точку между двумя отправными углами, определяемыми в течение развертки в направлении по оси y. Составляющие по оси x и y затем используются для управления луча посредством центровки на мишени.
В случае, где положение мишени первоначально не известно относительно траектории луча, можно быстро установить относительное положение посредством сканирующим растром луча до тех пор, пока мишень не встретится при развертке в направлении по оси x или сканировании. Затем после обнаружения отправных углов в этой развертке определяется средняя точка и луч устанавливается в положении средней точки и затем осуществляется развертка в направлении по оси y, т.е. вдоль биссектрисы, перпендикулярной к линии, соединяющей отправные углы идентифицированной развертки. В ответ на обнаружение отправных углов при этой развертке по оси y, определяется средняя точка в направлении по оси y и используются сигналы, отображающие средние точки в направлениях по оси x и по оси y для центровки луча на мишени. Несмотря на описанное выше определение центра мишени, можно определить и другие требуемые контрольные точки на мишени, и отклоненный луч попадет в эти точки.
Другим путем установить правильное положение источника и, следовательно, гарантировать пространственное разрешение экранируемого поля излучения для всех систем, можно при использовании небольшой мишени 126B рентгеновского излучения, которая имеет размер требуемого источника рентгеновского излучения. Тем не менее, в принципе можно использовать любой размер электронного пятна, который требуется для создания пятна с такими же размерами или меньшими, чем у мишени 126B для того, чтобы получить максимальный коэффициент преобразования энергии электронов в рентгеновское излучение и, следовательно, уменьшить время для лечения пациентов или для решения любой другой требуемой задачи, использующей экранированный источник рентгеновского излучения. В этом контексте, если размер пятна определяется так, что 90% электронов в пятне содержится в определяемом таким образом размере пятна, то затем создание такого пятна с небольшим размером мишени будет оптимальным в том смысле, что пятно с более меньшими размерами не приведет к значительному улучшению эффективности системы. В любом случае использование небольшой мишени гарантирует, что все рентгеновские зонды, использующие экран для определения области облучения будет иметь в сущности такое же пространственное разрешение и положение относительно наконечника зонда.
Как изображено на фиг. 12 носитель мишени 126C удобно расположен в конечной части наконечника 126A зонда. В изображенном варианте воплощения, мишень 126B рентгеновского излучения расположена на носителе 126C мишени, перед этим вставленным в наконечник 126A зонда. В примерах, где наконечник 126A зонда прикреплен к основанию зонда 14 раньше до размещения мишени 126B рентгеновского излучения и носителя 126C мишени, носитель 126C мишени можно изготовить так, что внутренний диаметр зонда 14 немного больше внешнего диаметра носителя 126C мишени для того, чтобы сделать проще введение снизу основания зонда 14.
В общем желательно, чтобы носитель 126C мишени точно подходил наконечнику 126A зонда для того, чтобы гарантировать механическую целостность структуры. Это можно достигнуть, например, изготовлением частей с "натягом" или при использовании теплового расширения для фиксации одновременно двух частей. В последнем случае холодный носитель 126C мишени (например, охлажденный жидким азотом) вводится в относительно горячий (например, с комнатной температурой) наконечник 126A зонда. Когда части достигают теплового баланса, то они жестко фиксируются вместе.
В альтернативном варианте воплощения наконечник 126A зонда можно изготавливать включая цельный носитель мишени. Наконечник 126A зонда прикрепляется к зонду 14 последовательно с размещением мишени 126B рентгеновского излучения.
Мишень 126B рентгеновского излучения следует располагать на носителе 126C мишени перпендикулярно к оси 16 зонда, и в центре концентрических полусферических поверхностей, которые определяют конечную часть наконечника 126A зонда. Эта концентричность размещения цели рентгеновского излучения во многом упрощает расчеты, требуемые для конструкции с изменяемой реконструкцией экрана 128 рентгеновского излучения с переменной толщиной для того, чтобы обеспечить требуемые контуры изодозы рентгеновского излучения. Используемый здесь термин контур изодозы относится к поверхности трехмерного объема, на которой каждая точка одинаково поглощает рентгеновское излучение в единице массы ткани.
После того, как мишень 126B рентгеновского излучения можно расположить на носителе 126C мишени перед введением зонда 14, можно использовать любой из нескольких способов для формирования мишени 126B рентгеновского излучения в центре носителя 126C мишени. Один способ получения такой мишени 126B рентгеновского излучения заключается в напылении металла с высоким атомным номером через экран, который вводится в полость в носителе мишени. Экран может состоять из диска с центральным отверстием, соответствующим мишени 126B рентгеновского излучения, и, через который металл напыляется на носитель 126C мишени.
В добавлении к сказанному, также необходимо знать размер источника рентгеновского излучения и положение экрана 128 рентгеновского излучения для расчета поглощения рентгеновского излучения в самой мишени 126B рентгеновского излучения в направлении по касательной к плоскости мишени 126B рентгеновского излучения. Такое поглощение можно уменьшить, используя мишень 126B рентгеновского излучения с кривой поверхностью, вместо плоской поверхности. Например фиг. 13 изображает полусферическое углубление носителя 126C мишени, которое служит для определения формы мишени 126B рентгеновского излучения. Кривизна мишени 126B рентгеновского излучения служит как для уменьшения поглощения рентгеновского излучения в мишени, так и для коррекции любого "остатка" угловой зависимости рентгеновского излучения, испускаемого из мишени 126B рентгеновского излучения. Суммарный результат может быть намного больше изотропной эмиссии рентгеновского излучения из мишени 126B рентгеновского излучения, которое излучает экран 128 рентгеновского излучения, размещенный на носителе 128A экрана. Кривая форма мишени, показанная на фиг. 13 является только одним из вариантов воплощения; могут также использоваться и другие эффективные формы такие, как полусферическое или сферическое сечение в комбинации с усеченным конусом.
Когда мишень 126B наносится в углубление, ее можно изготавливать с носителем 126 мишени внутри наконечника 126A зонда или как целую часть наконечника 126A зонда. Напыленное осаждение может накрыть углубление и окружающие поверхности 126D. Металл с высоким атомным номером, напиленный на поверхности 126D, можно в определенной мере удалить с поверхности плоским скреппером, который не контактирует с углублением.
Существуют применения для рентгеновского зонда настоящего изобретения, в которых требуются источники с ограниченной областью точечного источника рентгеновского излучения. Например, удаление небольшой опухоли груди может переместить ткань на много сантиметров, окружая при этом фокальную точку опухоли. Может потребоваться последующее ее удаление с облучением "опухолевой гряды" для того, чтобы уничтожить любые остатки опухолевых клеток по периферии удаления. В предпочтительном варианте для того, чтобы уменьшить разрушение ткани, отдаленной от требуемого объема облучения, осуществляется облучение широкой области рентгеновским устройством, использующим экран 128 рентгеновского излучения в значительной степени подобной тому, который показан на фиг. 12. Широкую область излучения можно легко получить посредством размещения узла 126 мишени зонда 14 на определенном расстоянии от поверхности, которая будет облучаться. Фиксированным углом излучения, выходящего из узла 126 мишени, можно управлять посредством экрана 128 рентгеновского излучения. Толщина экрана 128 на каждой точке определяется так, чтобы в значительной степени получить одинаковую картину излучения. Узел 26 мишени можно использовать аналогичным образом.
Фиг. 19 изображает механический позиционер 300, который используется с рентгеновским устройством изобретения для достижения требуемой точности между узлом 26 или 126 мишени и облучаемой поверхностью (тканью). Механический позиционер 300 содержит плоскую пластину раздела 302, которая находится в контакте с тканью, и сделана из такого материала, который является прозрачным для рентгеновского излучения типа Be, С или пластмассы. Пластина раздела 302 прикрепляется к зонду 14 посредством непрозрачной для рентгеновского излучения задней пластины 304. В дальнейшей картине специфической области излучения, поверхность нормально расположенную к прозрачной для рентгеновского излучения пластине раздела 302 можно выполнить частично не прозрачной для рентгеновского излучения посредством рентгеновского экрана в виде, подобном рентгеновскому экрану 128, описанному выше.
Другим применением такого источника рентгеновского излучения с широкой зоной является внутриполостное облучение внутри тела, например, внутри мочевого пузыря. В таком случае пластина раздела 302 между тканью и источником рентгеновского излучения широкой зоны может быть надувным шаром, вытягивая низ пробника 14 так, что узел 126 мишени находится в центре шара. В этом случае задняя пластина 304 будет непрозрачной.
Фиг. 21A-21F изображает примеры различных контуров изодоз, которые можно обеспечить настоящим изобретением. Фиг. 21A изображает с особенностями зонд 14, приспособленный для получения контуров изодозы, которые формируют сферу излучения 300, сцентрированную у наконечника 126 зонда. Фиг. 21B изображает зонд 14, приспособленный для получения сферы излучения 302, в котором наконечник 126 зонда смещен от центра сферы 302. Фиг. 21C изображает зонд 14, имеющий наконечник 126, приспособленный для приема области излучения в виде сжатого у полюсов эллипсоида (т.е., в виде "блина"), как показано в перспективе на 304A и расположенного вдоль оси 305 на 304B. Фиг. 21 изображает зонд 14, имеющий наконечник 126, приспособленный для получения поля излучения в виде вытянутого эллипсоида (т.е., в виде "сигары"), как показано в перспективе на 306A и вдоль оси 307 на 306B. Как показано на фиг. 21D) зонд 14 входит в эллипсоид 306A вдоль ее минимальной оси. Фиг. 21E показывает наконечник 126, также приспособленный для получения поля излучения в виде вытянутого эллипсоида. Эллипсоид показан в перспективе 308 и вдоль оси 309 на 308B. Как видно, зонд 14 входит в эллипсоид 308A вдоль своей главной оси. Фиг. 21F изображает наконечник 126 зонда, приспособленного для получения асимметричного поля излучения, показанного в перспективе на 310A и вдоль оси 311 на 310B.
Конструирование рентгеновского экрана 128 с изменяемой толщиной для генерации рентгеновского излучения принципиально внутри заданных контуров изодозы будет в общем начинаться с цифровой информации, описывающей размеры и форму требуемого объема облучения (типа опухоли), которая получается посредством определенного способа изображения, типа сканирования CT или магнитного резонансного изображения. Из такой информации и знания свойств поглощения рентгеновского излучения в используемых материалах зонда и экрана, можно точно рассчитать профиль толщины зонда. В общем, контуры изодозы могут принимать различные формы и размеры и могут быть необязательно симметричными.
Можно использовать различные способы для претворения конструкторской информации в физический экран. Например, полусферический носитель 128A экрана покрывают слоем металла с высоким атомным номером (например, Au) около 100 мкм толщиной. Толщина экранирующих материалов, осажденных на носитель 128 экрана хорошо контролируется для того, чтобы знать сколько вещества устранить в последующем процессе фрезерования. Один способ достижения высокой степени контроля толщины заключается в напылении материалов, поглощающих рентгеновское излучение, гальваническим способом.
Фиг. 14 показывает систему 200 лазерного фрезерования для выработки соответствующей переменной толщины рентгеновского экрана 128 для получения заданных контуров изодозы рентгеновского излучения. Хорошо известно, что мощными лазерными импульсами можно устранять поверхностные слои металла. Система 200 лазерного фрезерования, изображенной на фиг. 14 содержит механическое устройство позиционирования, показанное в общем как контроллер 202 положения, который систематически представляет все поверхностные точки носителя 128A экрана лазерному лучу 204. Например, рентгеновский экран 128 и носитель 128A экрана можно вращать около оси 16 зонда или оси 212, которая перпендикулярно расположена к оси 16 зонда. В предпочтительном варианте, микропроцессор 210 имеет прямой контроль за перемещениями контроллера 202 положения, и информация о текущем положении поверхности рентгеновского экрана 128 передается обратно в микропроцессор 210 для подтверждения особого положения.
Параметры рентгеновского экрана, т.е. толщина профиля, рассчитываются перед фрезерованием и на основе этих данных процессор 210 выдает команды контроллеру 208 лазера, например, какая мощность излучения требуется для устранения требуемого количества экранирующего материала в каждой отдельной точке облучаемой поверхности на рентгеновском экране 128.
Если экранирующий материал полностью металлический, то может потребоваться мощный и дорогостоящий лазер для того, чтобы завершить процесс фрезерования за приемлемый промежуток времени. Предпочтительным лазером в этом случае является эксимерный лазер. Однако, когда экранирующий материал состоит из взвешенных частичек металла в органическом материале типа полиамида, то может использоваться лазер с гораздо меньшей мощностью, например, азотный лазер.
В другом варианте воплощения, можно обеспечить переменную толщину рентгеновского экрана 128 посредством управляемого напыления из экранирующего материала. Эта методика также поддается автоматизации и картина напыления может управляться микропроцессорной приводной системой.
В другом варианте воплощения, экранированный материал является первым покрытием в носителе с требуемой максимальной толщиной около 100 мкм для золота, и затем механически обрабатывается на станке CNC с высокой точностью. Этот вариант воплощения имеет преимущество использования простых механических процессоров и устраняет необходимость для включенной калибровочной системы, какая требуется для лазерного фрезерования.
Фиг. 15A и 15B изображают один вариант воплощения конструкции зонда, который позволяет проводить точную угловую регулировку носителя 128A экрана и таким образом, рентгеновского экрана 128 с зондом 14. Механический ключ, изображенный в виде петельки 140 в зонде 14 и соответствующий паз 142 в узле 126 цели можно обеспечить между двумя для гарантии точности позиционирования рентгеновского экрана 128 и зонда 14 для того, чтобы сориентировать картину рентгеновского излучения с геометрией требуемого объема облучения. Устройство фиг. 15A и 15B можно также использовать в комбинации с узлом 26 мишени, изображенном на фиг. 1.
В качестве дальнейшей особенности изобретения, можно использовать управление для направления выходного электронного луча в выборочной поверхности на эмиссионном элементе, например, в котором мишень имеет различные характеристики эмиссии в различных пространственных областях. Управление электронным лучом можно обеспечить под телеметрическим контролем или посредством предварительного программирования источника питания перед введением всего устройства 10 или его частей.
Фиг. 8 изображает образцовый узел 29 электростатического управления лучом. В изображенном варианте воплощения катод 22 вырабатывает электроны способом, согласующимся с выше описанными вариантами воплощения. Электроны ускоряются через фокусирующий электрод 23 по направлению к аноду 24 и проходят через апертуру 24A по направлению к узлу 26 мишени. По пути к узлу 26 мишени, электроны проходят через узел 30 электростатического отклонения, изображенного в поперечном сечении на фиг. 6A. Узел включает четыре дефлектора 32. Изменяя напряжение, прикладываемое к противоположным парам дефлекторов 32, электроны луча, входящие в узел, вдоль оси 16A отклоняются, или "управляются", так как они проходят вперед по направлению к узлу 26 мишени вдоль оси 16B. Таким образом можно контролировать ось луча, делая его прямым или искривленным по требованию. Как описано ниже, можно альтернативно использовать электромагнитные методы для управления лучом. В последнем случае, электростатические отражающие пластины 32 можно перемещать магнитными спиралями дефлектора, которые управляются посредством токов, которые устанавливают магнитные поля, необходимые для достижения характерного отклонения луча.
В другом виде варианта воплощения управления лучом, электронный луч проходит через устройство катушек, генерирующих магнитное поле, что предпочтительнее, чем прохождение электронного луча через узел 30 с электростатическим отклонением. Катушки можно привести к конфигурации подобной пластинам электростатического отклонения узла 30. При изменении тока через катушки создается магнитное поле с заданными характеристиками, которое влияет на траекторию электронного луча.
В таком виде, можно управлять электронным лучом, направляя электронный луч в определенные физические места на конусообразном узле мишени (фиг. 8) или мишени любой другой особой геометрической конфигурации. Например, в изображенном варианте воплощения, электронный луч, бомбардируя угловую сторону узла 26 мишени, приведет к генерации рентгеновского излучения с той стороны, с малым или не случайным излучением, переданным к противоположной стороне от узла мишени.
В другом виде варианта воплощения управления лучом, можно управлять характеристиками выходного рентгеновского излучения посредством пространственного изменения параметров эмиссии (такие как пик излучения в зависимости от энергии) в различных точках узла 26 мишени, например, с пространственной картиной типа "сигнальный фонарь", лучом можно управлять относительно высокой энергией рентгеновского излучения или в областях относительно низкой энергией рентгеновского излучения. Таким образом, луч можно выборочно направлять в области узла мишени для достижения требуемых характеристик и направленности рентгеновского излучения.
Узел 29 управления луча, изображенный на фиг. 8, можно также использовать в комбинации с узлом 126 мишени, изображенном на фиг. 12.
Фиг. 16, 17 и 18 изображают альтернативный узел 29 управления лучом, который включает систему 31 с контуром обратной связи для точной установки положения электронного луча на рентгеновской мишени 126B. В изображенном варианте воплощения узел 30 отклонения в значительной степени подобен тому, который показан на фиг. 8, (кроме того, что система магнитного отклонения размещена вне зонда) и установлен детектор 142 рентгеновского излучения для контроля рентгеновского излучения, выходящего из рентгеновской мишени 126B. Детектор 142 рентгеновского излучения можно установить вне оси электронного луча, как показано, или разместить по оси позади катода 22.
Изменения в траектории электронного луча можно измерять, когда существует изменение в рентгеновском излучении из мишени 126B. Контроллер 144 отклонения, который предпочтительно управляется микропроцессором может использовать данные детектора 142 рентгеновского излучения и, посредством управления напряжений, прикладываемых к дефлекторам 32 узла 30 отклонения, можно точно фиксировать электронный луч.
Например, систему 31 с контуром обратной связи можно использовать в центре электронного луча на небольшой цели 126B рентгеновского излучения. Однако, когда изменение в контрольном сигнале показывает, что центр луча перемещается от центра мишени, существует информация, в которой направление перемещения имеет место. Следовательно, может возникнуть необходимость для периодического отклонения луча в известном направлении и наблюдения отклонения контрольного сигнала для того, чтобы отцентрировать луч.
Контрольный сигнал, требуемый для сохранения луча, который устанавливается на мишени 126B рентгеновского излучения, можно получить посредством перемещения детектора 142 рентгеновского излучения позади электронной оптики 138 для контроля рентгеновского излучения, который излучается обратно вдоль оси 16 зонда 14. На фиг. 16 и 17 показано контрольное рентгеновское излучение 140, которое проходит в одну сторону от электронной оптики 138. Однако, если катод является достаточно тонким для того, чтобы пропускать рентгеновское излучение, то можно сконструировать систему так, что рентгеновское излучение 140 проходит через электронную оптику 138 и катод 22. Детектор 142 можно разместить либо внутри либо снаружи кожуха 12, как показано на фиг. 16 и 17, соответственно. Как изображено на фиг. 17, в случае если детектор 142 размещен снаружи кожуха 12, то выходное рентгеновское окно 148 будет размещено в стенке кожуха для обеспечения оптической связи детектора 142 с мишенью 126B рентгеновского излучения.
Затем луч точно центрируется на мишени 126B. Систему обратной связи, изображенную на фиг. 16 и 17, можно использовать для оптимизации фокусного расстояния электронного луча для получения максимального выходного рентгеновского излучения. Например, это можно сделать посредством максимизации сигнала, контролируемого системой обратной связи при использовании контроллера 144 отклонения для регулировки напряжения на фокусирующих элементах (такого, как фокусирующий электрод 23) электронной оптики 138.
Систему обратной связи, изображенную на фиг. 16 и 17, можно также использовать с узлом 26 мишени, показанным на фиг. 1 или 8. Например, можно использовать систему обратной связи для позиционирования луча, который будет падать на каждую отдельную точку эмиссионного элемента, имеющего области различных характеристик эмиссии (типа пространственной картины "сигнального фонаря", описанной выше). Кроме того, систему обратной связи можно использовать для управления ускоряющим напряжением электронной оптики.
Как показано в вышеописанных вариантах воплощения, устройство 10, изображенное на фиг. 1, включает источник питания 12A. Фиг. 6 представляет собой блок-схему источника 12A. На фиг. 7 показана более подробная схема источника, изображенного на фиг. 6. Как показано на фиг. 6 и 7, вариант воплощения включает обратноходовый импульсный преобразователь (конвертор) и стабилизатор 280, трансформатор 282 напряжения с коэффициентом трансформации 30, подсоединенный к выводу 282A напряжения управления (или высоковольтного входа умножителя) и 10-кратный умножитель 284 напряжения, подсоединенный к высоковольтному выводу 282, и приспособленного для возбуждения нити накала термоэмиттера 22. Возбудитель высокочастотной мощности нити накала и преобразователь 290 напряжение-частота (U/f) и действующий совместно высокочастотный возбудитель 292 нити накала подсоединены через вывод 292A тока управления и емкость Co посредством схемы 286 возбуждения нити накала к. нити накала эмиттера 22.
Дифференциальный усилитель 294 устанавливает токовую петлю обратной связи посредством управления возбудителем высокочастотной энергии и преобразователя 290 и U/f в ответ на выявленное рассогласование между токовым сигналом обратной связи на линии 295 и приложенным сигналом управления эмиссией на линии 296. Последний сигнал можно выборочно контролировать для установления требуемого временного изменения тока катода рентгеновской трубки в нити накала эмиттера (термокатод) 22. Высоковольтная амплитуда контура обратной связи устанавливается посредством импульсного преобразователя и стабилизатора 280 в ответ на обнаруженные различия между напряжением сигнала обратной связи на линии 297 и приложенным высоковольтным сигналом управления на линии 298. Последний сигнал можно выборочно контролировать, устанавливая требуемое изменение амплитуды потенциала на нити накала эмиттера (термокатода) 22.
Более подробное описание источника питания, изображенного на фиг. 7 даны в заявке США N 5153900 и также в первоначальной заявке США N 955494.
Фиг. 9 изображает образцовую систему 300, предназначенную для лечения рентгеновским излучением опухоли мозга. Система 300 включает стереотактический кадр 302 в комбинации с маломощным рентгеновским устройством 10A, подсоединенным к ней. В такой конфигурации, рентгеновское устройство 10A обычно подобно рентгеновскому устройству 10, изображенному на фиг. 1, но имеет цилиндрическую геометрию. Соответствующие элементы двух рентгеновских устройств 10 и 10A имеют аналогичные подобные стандартные обозначения. В общем стереотактические кадры обеспечивают фиксированную эталонную структуру относительно черепа пациента. Несмотря на то, что предпочтительный вариант воплощения, описанный выше, более приспособлен для стереотактического кадра, другие варианты воплощения изобретения можно подобным образом приспособить для использования с этими или другими кадрами, или с основным контрольными кадрами, например, кадр, устанавливающий работающую неподвижно установленную арматуру, рекомендуемой части тела, другой, чем голова. В изображенном варианте воплощения фиг. 9 стереотактический кадр 302 в значительной степени подобен системе Cosman-Roberts-Wells, изготовленной фирмой Radioniсs Inc., Birlington, Masscachusetts.
В изображенном варианте воплощения кадр 302 устанавливает эталонную систему отсчета в координатах x, y, z, расположенную относительно требуемой начальной точки отсчета 0. Кадр 302 включает в общем U-образный элемент 304 поддержки, определяющий контрольную плоскость. Четыре ручки 306A, 306B, 306C и 306D (не показано) выходят из поддержки кадра 304. Каждая ручка имеет установленный в определенном месте штырь 308. Штыри 308 выходят в общем навстречу друг к другу из соответствующих отдаленных наконечников ручек 306A, 306B, 306C и 306D. При использовании четырех штырей 308, расположенных напротив черепа пациента для установки фиксированного положения между кадром 302 и черепом пациента. Таким образом, кадр 302 определяет контрольную систему координат x, y, z по отношению к черепу пациента.
Рентгеновское устройство поддерживает деталь 310, подсоединенную к элементу поддержки 304 посредством пары подсоединяющих узлов 312 сцепления и пары линейных узлов 314 сцепления. Деталь 310 рентгеновского устройства поддерживает изогнутое звено 310 поддержки. Рентгеновское устройство 10 подсоединяется к звену 310A поддержки посредством подсоединения узла 316. Узел 316 подсоединения обеспечивает управляемое передвижение рентгеновского устройства 10 по круговой траектории вдоль звена 310A и между внутренней конечной точной и внешней конечной точкой вдоль оси (например, оси 316'), расположенных радиально направленных из круглой траектории изогнутого звена 310A по направлению к точке начала отсчета 0.
Кроме того, вращение вокруг втулок вращающихся узлов 312 подсоединения позволяет рентгеновскому устройству поддерживать деталь 310, которая будет вращаясь передвигаться вокруг оси x. Деталь 310 поддержки рентгеновского устройства перемещается в направлении перпендикулярном к плоскости, определяемом осями x и y (плоскость x-y), посредством передвижения вдоль треков 314A, линейных узлов 314 подсоединения. В изображенном варианте воплощения, Т-образный паз 314A соединяется с шипом блока 314B, который прикрепляется к узлу 304, обеспечивая линейное движение по направлению перпендикулярном к плоскости x-y. Установкой винтов 332 в блоке 314B можно регулировать закрытие узла 310 поддержки рентгеновского устройства на установленную высоту относительно кадра 304 поддержки.
Деталь 310 рентгеновской поддержки можно перемещать в направлении оси z посредством передвижения шипов, установленных от детали 310 в треках 304A элемента 304 поддержки. Управляемое положение детали 310 вдоль треков 304A можно установить, используя закрывающие винты 334.
Кроме того, элементом 304 поддержки можно регулировать положение в направлении оси x посредством скольжения детали 304 относительно своей детали 305 поддержки, и можно регулировать положение с тремя степенями свободы, устанавливая требуемое положение в начале точки отсчета 0 внутри черепа пациента.
Узел 316 подсоединения изображен вместе с рентгеновским устройством 310A в разобранном виде, изображенном на фиг. 10. Как показано узел 316 подсоединения включает приемный блок 316A, вставляемый в втулку элемент 316B, вместе с дополнительной сформированной частью рентгеновского устройства 10A. Как показано, центральная ось 16 зонда 14 рентгеновского устройства 10A коаксиально оси 316'. Электронный луч зонда 14 является условно коаксиальным к оси 316', но можно изменяться регулировкой, которая описана выше в соответствии с фиг. 8, 8A, 16, 17 и 18 и ниже в соответствии с фиг. 10.
Цилиндрический, вставляемый в втулку элемент 316B устанавливается частично внутри и коаксиально приемного блока 316A. Вставляемый в втулку элемент 316B скользит (в направлении радиальной оси 316') и может избирательно закрываться в месте, относительном блока 316A, используя установочные винты 318A. Вставляемый в втулку элемент 316A включает центральное отверстие (диаметром D), проходящий вдоль его центральной оси.
Как отмечено выше рентгеновское устройство 10A аналогично рентгеновскому устройству 10, изображенному на фиг. 1, но имеет обычно цилиндрической формы кожух 12; пробник 14 включает цилиндрическую часть 14A плеча (имеющую диаметр не много меньшей D) непосредственно рядом с кожухом 12, с основной частью маленького диаметра (3,0 мм в предпочтительном варианте воплощения). В этой конфигурации, рентгеновское устройство 10A можно устанавливать с его осью 16 коаксиально оси 316' и часть 14A плеча устанавливать со скольжением внутри отверстия, вставляемого в втулку элемента 316B. Относительное положение рентгеновского устройства 10A можно фиксировать вдоль оси 316', используя установочные винты 320 элемента 316B.
Рентгеновское устройство 310A может включать магнитную подсистему отклонения для своего электронного луча. Подсистема отклонения включает магнитные катушки 32 отклонения, как показано на фиг. 18, установленные по оси 16 внутри части 14A плеча. Эти катушки возбуждаются для регулируемого управления положения оси луча так, что луч падает на мишень узла 126 (изображенного, например, на фиг. 16 и на фиг. 17) требуемым способом. В предпочтительном виде излучение, вырабатываемое устройством 10A, контролируется (например, посредством детектора 142 рентгеновского излучения, изображенного на фиг. 16 и фиг. 17, и/или детектора рентгеновского излучения, установленного вне пациента), а катушки дефлектора возбуждаются соответственно посредством управляющих токов по отклоняющим X1, X2, Y1 и Y2 линиям, прикладываемых к катушкам отклонения, изображенных на фиг. 11. Как показано на фиг. 9, контроллер на основе микропроцессора может не располагаться внутри кожуха 12, но размешаться вне кожуха 12 в блоке управления 342. Блок 342 управления подсоединен к рентгеновскому устройству 10A посредством кабеля 342'. Удлиненный зонд 14 и рентгеновское устройство 10 имеют такую конфигурацию, которая позволяет зонду 14 проходить через трек слева посредством биопсийной иголки, посредством разрешения легкого введения зонда 14 в мозг пациента. Для опухолей, состоящих из твердых тканей, и в которых используется биопсийная иголка меньше по ширине зонда 14 надлежащее проникновение в опухоль может потребовать первый расширяющий трек слева от биопсийной иголки с промежуточным размером иголок.
В этой конфигурации наконечник пробника 14 содержит мишень, обладающую эмиссией рентгеновского излучения, и может передвигаться в и из относительно черепного места введения посредством передвижения вдоль оси 16'. Рентгеновское устройство 10A можно укрепить в данном положении вдоль установочных винтов 318A и 320. Длина зонда 14 рентгеновского устройства 10A выбирается так, чтобы центр кривизны наконечника пробника зонда 14 при полностью введенной вниз по направлению меньшему нижнему ограничительному положению вдоль оси 316 и с 316A, устанавливался точно на основной точке отсчета 0; когда рентгеновское устройство 10 полностью отходит в верхнюю ограничительную точку вдоль оси 316', отдаленный от центра наконечник зонда 14 намеревается быть вне черепа пациента. Координаты выгнутой поддержки трека 310A можно установить так, чтобы точка начала отсчета 0 размещалась на требуемом изоцентре облучения. Таким образом, посредством вращения рентгеновского устройства 10A деталь 310 поддержки и позиционирование рентгеновского устройства 10A вдоль окружности трека точной поддержки трека 310A и вдоль оси 316' пользователь может выбрать соответствующую траекторию (предпочтительно наименьшее разрушение) для введения зонда 14 в мозг пациента, наконечник зонда 14 всегда находящейся в начале системы отсчета 0 после полного введения зонда 14 в нижнюю ограничительную точку.
Фиг. 11 изображает схему предпочтительного высоковольтного источника питания 12A для использования с рентгеновским устройством 10A, показанного на фиг. 9 и фиг. 10. В этом источнике питания высоковольтный сигнал управления является сигналом управления с напряжением от 0 до 9 Вольт. Этот сигнал управляет полевым транзистором (FET) Q1 обратноходового импульсного преобразователя, который, в свою очередь, управляет высоковольтным обратноходовым трансформатором. Напряжение высоковольтного обратноходового трансформатора изменяется от +12 Вольт до нескольких тысяч вольт. Высоковольтный умножитель D1-D28, в свою очередь, повышает напряжение до требуемого выходного напряжения от 15 до 40 кВ. Цепь обратной связи по напряжению выдает информацию обратной связи для контроллера 12C так, чтобы выходное напряжение высоковольтного умножителя можно было бы поддерживать на постоянном уровне.
Положительные и отрицательные цепи нити накала обеспечивают соответственно 9 В и 250 кГц импульс управления прямоугольной формы для полевых транзисторов 02 и 03. Эти полевые транзисторы преобразовывают изменяемое постоянное напряжение нити накала в переменное напряжение, и управляют трансформатором Т2, изолированным по высокому напряжению от нити накала. Использование сигнала с высокой частотой для управления этим трансформатором позволяет единственному вторичному витку управлять нитью напала рентгеновской трубки. Это, в свою очередь, позволяет обеспечить малые габариты трансформатора при сохранении необходимой изоляции по высокому напряжению. Ток в цепи FB позволяет контроллеру 12C регистрировать ток луча, и затем контроллер устанавливает постоянное напряжение нити накала для требуемого тока луча, обеспечивая соответствующее нагревание при прохождении тока в термоэмиттере 22. Цепи отклонения X1, X2, Y1, Y2 вырабатывают токовые сигналы управления для магнитных катушек отклонения луча.
Как обсуждалось выше со ссылкой на фиг. 1, устройство 10 включает генерацию луча и ускоряющие элементы для генерации и ускорения электронов прежде, чем эти электроны попадут в зонд 14. Генерируемый электронный луч затем проходит через зонд 14, бомбардирует мишень 26B, и таким образом производит рентгеновское излучение. При отсутствии магнитных полей электроны проходят через зонд 14, следуя по прямолинейной траектории. Поэтому зонд 14 обычно жесткий без каких-либо изгибов.
Однако в определенных медицинских применениях полезно использовать гибкий зонд. Одно такое применение включает проходящий насквозь рентгеновский источник вниз по существующей траектории, такой как трахея. Другое такое применение включает рентгеновский источник, маневрирующий вблизи критических структур, таких как нервы или кровяные сосуды.
Фиг. 20A изображает схему устройства 200, включающую гибкий зонд. Устройство 200 включает высоковольтную схему 218, лазерный источник 220, узел 214 пробника и узел 226 мишени. Согласно первому аспекту изобретения устройство 200 обеспечивает требуемую гибкость без использования мощных магнитных полей, посредством перемещения элементов, генерирующих и ускоряющих электроны в узле мишени 226. Узел мишени 214 объединяет как лазерный источник 220, так и высоковольтную схему 218 в узле 226 мишени. Узел зонда включает гибкий волоконно-оптический кабель 202, закрытый в гибкой металлической трубке 204 небольшого диаметра. Узел 226 мишени, которая может быть, например, длиной от 1 до 2 см, проходит от конца узла 214 зонда и включает оболочку, которая закрывает мишень 228. Согласно одному варианту воплощения узел 226 мишени является жестким и обычно цилиндрической формы. В этом варианте воплощения цилиндрическую оболочку, закрывающую узел мишени, можно рассматривать для обеспечения кожуха для источника электронного луча, также как трубчатый зонд, протянувшийся от кожуха вдоль траектории электронного луча. Внутренняя поверхность 226A узла 226 находится вдоль линии с электрическим изолятором, хотя внешняя поверхность 226B узла 226 электрически проводящая. Согласно предпочтительному варианту узел мишени герметически запаян на конце узла 214 зонда и из него откачен воздух. Согласно другому варианту воплощения воздух внутри узла 214 откачивается.
Конечный вывод 202A волоконно-оптического кабеля 202 предпочтительно покрыт, по крайней мере на части своей поверхности, полупрозрачным фотоэмиссионным веществом таким, как Ag-O-Cs, таким образом формируя фотокатод 216. Высоковольтный проводник 208, введенный в волоконно-оптический кабель 202, подводит электроны к катоду 216 из высоковольтной схемы 218. Подобным образом, гибкая трубка 204 соединяет землю, поворачивая от мишени 228 до высоковольтной схемы 218, посредством установления высоковольтной области между катодом 216 и мишенью 228. Волоконно-оптический кабель 202 действует как изолирующий диэлектрик между высоковольтным проводником 208 и заземленной гибкой трубкой 204.
В одном варианте воплощения, для устранения поглощения и рассеяния света из волоконно-оптического кабеля 202 посредством высоковольтной проволоки 208, волоконно-оптический кабель может иметь круглую конфигурацию, как показано на поперечном сечении фиг. 208. Световой луч лазера 220 направляется вниз в круглое отверстие 250 волоконно-оптического кабеля 202. Оболочка 260 на каждой стороне отверстия 250 имеет коэффициент преломления такой величины, чтобы происходило преломление луча, падающего на границу раздела, обратно в отверстие 250. Заземленная гибкая металлическая трубка 204 окружает внешнюю оболочку 260.
Как и в предыдущих описанных вариантах воплощения, мишень 228 может быть, например, берилиевая (Be), покрытая на одной стороне тонкой пленкой или слоем 228A, содержащим элемент с высоким атомным номером, таким как вольфрам (W) или золото (Au).
В процессе работы небольшой полупроводниковый лазер 220, который светит на волоконно-оптический кабель 202, воздействует на пропускание фотокатода 216, который генерирует свободные электроны 222. Высоковольтная область между катодом 216 и мишенью 228 ускоряет эти электроны посредством их фокусировки для бомбардирования поверхности 228A мишени 228 и выработки рентгеновского излучения. Для того, чтобы генерировать, например, ток величиной 20 мкА из Ag-O-Cs фотокатода 216 при помощи лазера 220, излучающего свет на длине волны 0,8 мкм с квантовым выходом, равным 0,4% этого фотокатода 216 для этой длины волны, необходимо, чтобы лазер 220 излучал оптическую мощность, равную 7,5 мВт. Такой диодный лазер уже коммерчески используется. Согласно изобретению фотоэмиссионная поверхность, которая Формирует катод 216, может в действительности быть совсем маленькой. Например, для плотности тока на катоде 216 1 А/см2 необходимо иметь диаметр фотоэмиттера около 50 мкм.
Ускорение свободных электронов 222 в поле высокого напряжения от 30 до 50 кВ может вызвать положительные ионы, которые будут генерировать при столкновении в пленке 228A мишени 228. Эти ионы будут ускоряться вперед по направлению к фотокатоду 216, бомбардируя и возможно разрушая ее поверхность. Как изображено схематически на фиг. 22, в одном варианте воплощения для минимизации ионной бомбардировки фотокатода 216 экран 217 с высоким электрическим сопротивлением (тороидальная оболочка) устанавливается в непосредственной близости и электрически подсоединен вдоль своего внешнего угла к фотокатоду. Небольшая щель 217A в этом экране 217 фокусирует свободные электроны 222 и рассеивает их на цель 228. Возвращающиеся электроны ударяются об экран 217 вместо фотокатода 216.
Один трудный аспект изготовления в этом изобретении заключается в изготовлении фотокатода 216, который для реальных веществ с умеренным квантовым выходом выше 10-3, следовало бы содержать в вакууме. Эту процедуру можно осуществить при помощи волоконно-оптического кабеля 202, установленного в куполообразный сосуд, где, например, фотоповерхность из Ag-O-Сs изготовлена традиционным способом. Впоследствии без облучения в воздухе оптический кабель 202 можно ввести в трубку 204 и фотокатод 216 разместить в непосредственном контакте с экраном 217. Конец. 202B можно припаять в вакууме с гибкой трубкой 204.
В выше приведенных вариантах воплощения зонд 14 или 214 вдоль своего объединенного узла 26, 126 или 226 мишени можно покрыть двух составом внешним слоем таким, как нитрид титана на подслое никеля. Для дополнительной защиты оболочки, например, на зонд можно нанести полиуретан, такой как изображен на фиг. 2.
Изобретение можно воплотить и в другие особые формы без нарушения духа и сущности представленных в нем характеристик. Настоящий вариант воплощения поэтому должен рассматриваться во всех отношениях, как иллюстрирующий и не ограничивающий масштаб изобретения, представленного посредством дополненной формулы изобретения в большей степени, чем предшествующим описанием и все изменения, которые выявлены в значении и области равноценности формулы изобретения, поэтому включены здесь.
Реферат
Использование: для получения постоянного или импульсного рентгеновского излучения малой мощности. Источник рентгеновского излучения содержит кожух (12), источник питания, удлиненный трубчатый зонд (14), узел (26) мишени и узел (29') управления лучом. Кожух закрывает источник (22) электронного луча и имеет элементы для генерации электронного луча вдоль траектории луча. Источник питания является программированным для управления напряжением, током и временем генерации электронного луча. Узел (26) мишени включает элемент мишени, расположенный вдоль траектории луча и приспособленный для испускания рентгеновского излучения в заданной спектральной области в ответ на падающие электроны. Узел (29') управления лучом включает элемент (30) отклонения, контур (31) обратной связи и контроллер (144) отклонения. Элемент (30) отклонения отклоняет луч от условной оси, выбранной поверхностной области на элементе (26) мишени в ответ на сигнал управления отклонением. Контур (31) обратной связи включает элементы регистрации отклонения для регистрации отклонения луча и элементы для выработки характерного в этом случае сигнала обратной связи. Технический результат заключается в создании маломощного рентгеновского устройства. 5 с. и 79 з.п.ф-лы, 22 ил.


Комментарии