Спейсер для лобной пазухи - RU2494768C2
Код документа: RU2494768C2
Чертежи


























































Описание
Область техники
В целом, настоящее изобретение относится к медицинским устройствам и способам, более конкретно - к имплантатам, осуществляющим доставку вещества, и способам лечения широкого спектра заболеваний, включая, помимо прочего, синусит и другие заболевания уха, горла и носа.
Предпосылки создания изобретения
Для предотвращения развития хронической микробной инфекции в полости околоносовой пазухи необходима адекватная вентиляция околоносовых пазух. В норме для вентиляции пазух используются небольшие естественные отверстия, или устья, через которые полости пазух сообщаются с полостью носа. Помимо вентиляции устья выполняют функцию дренажных каналов, поскольку реснитчатые клетки, которыми выстлана изнутри полость пазухи, постоянно направляют поток слизи к устьям. Таким образом, при сужении или блокаде естественного отверстия нарушается вентиляция и отток слизи из полости пазухи. Развивающаяся вследствие этого гипоксия, изменение кислотности и застой слизи в полости пазухи формируют среду, благоприятную для размножения некоторых видов микробов. Такая микробная инфекция также может вызвать воспаление слизистой и последующее сужение или блокаду естественного отверстия пазухи.
Способы улучшения вентиляции и дренажа околоносовых пазух
Функциональная эндоскопическая хирургия околоносовых пазух (ФЭХОП) является наиболее распространенным видом хирургического вмешательства, в ходе которого эндоскоп вводят в полость носа, и хирург под визуальным контролем с помощью эндоскопа удаляет пораженную или гипертрофическую ткань или кость и может хирургическим путем увеличить устья околоносовых пазух с целью восстановления нормальной вентиляции и дренажа околоносовых пазух.
В качестве альтернативы инцизионной хирургии для некоторых пациентов применяется катетеризация, в ходе которой в суженное устье околоносовой пазухи вводится баллонный катетер, который используется для расширения устья, устраняя необходимость рассечения или удаления ткани, окружающей устье (технология баллонной синуспластики Balloon SinuplastyTM компании Acclarent, Inc., Менло Парк, Калифорния). Примеры баллонной дилатации описаны в заявках на патент США №№2006/0004286, 2006/0063973, 2006/0210605, 2007/0129751, 2007/0135789, 2007/0167682, 2007/0208252, 2007/0208301 и 2007/0293727, содержание каждой из которых полностью включено в настоящий документ путем ссылки.
Имплантация стентов и объемных материалов для предотвращения реокклюзии после хирургического вмешательства
В случае хирургического удаления или рассечения ткани, прилегающей к устью, образующаяся после операции рубцовая ткань, фиброз, полипоз или врастание ткани могут привести к реокклюзии устья пазухи. Для предотвращения реокклюзии лобных и клиновидных пазух после хирургического вмешательства в измененное хирургическим путем устье пазухи или выводной проток помещают небольшие трубчатые стенты, оставляя их на некоторый период времени после операции.
Примерами стентов для лобной пазухи могут являться доступные в продаже стенты FreemanTM (производитель InHealth Technologies, Inc., Карпинтерия, Калифорния). Стент FreemanTM выполнен в виде силиконовой трубки, каждый конец которой снабжен фланцем для удержания стента в выводном протоке лобной пазухи в течение необходимого периода времени после операции. Среди других доступных в продаже стентов для лобных пазух следует отметить стенты Jasin (производитель Medtronic Xomed, Inc., Джексонвилль, Флорида) и стенты Salman FES (производитель Boston Medical Products, Уэстборо, Массачусетс).
Стент для клиновидной пазухи описан в патенте США №7235099 (Duncavage, et al.). Такой стент представляет собой мягкую пластиковую трубку, один конец которой выполнен в виде преимущественно полукруглого полого купола. Диаметр купола превышает заданный диаметр пластиковой трубки. Стент также включает кольцеобразный фланец, расположенный на заданном расстоянии от полукруглого купола. Устройство вводят через расширенное хирургическим путем устье клиновидной пазухи так, чтобы купол находился в полости пазухи, а фланец упирался в костную стенку, окружающую устье. Такой стент предназначен для сохранения проходимости измененного хирургическим путем устья пазухи в течение послеоперационного периода и позволяет выполнять орошение (аспирацию) полости пазухи через просвет стента. Стент для клиновидной пазухи доступен в продаже под маркой SP-82020 (производитель Micromedics, Inc., Сент-Пол, Миннесота).
Вышеописанные стенты для лобных и клиновидных пазух не предусматривают доставку терапевтических веществ. Таким образом, они, как правило, используются одновременно с лекарственными препаратами для перорального введения (например, кортикостероидами) и(или) назальными спреями местного действия.
В некоторых случаях вместо стента хирурги помещают гелеобразные материалы в измененное хирургическим путем устье или выводной проток для предотвращения врастания рубцовой ткани в послеоперационный период. Одним из примеров такого материала является рассасывающаяся назальная повязка и стент для пазухи MeroPack™ (производитель Medtronic ENT, Inc., Джексонвилль, Флорида). Материал MeroPack™ на 80% состоит из этерифицированной гиалуроновой кислоты и на 20% - из коллагена. Материал вводится в сухом состоянии, а после контакта с жидкостью приблизительно в течение шести секунд набухает до 1,0 см в диаметре. Во влажном состоянии материал представляет собой рассасывающийся мукоадгезивный гель.
Локальная доставка лекарственных препаратов при лечении заболеваний околоносовых пазух
Известны различные имплантаты для доставки лекарственных препаратов, устанавливаемые в полости околоносовых пазух или в непосредственной близости от них, предназначенные для лечения синусита и(или) для предотвращения реокклюзии измененных хирургическим путем выводных протоков или устьев после операции.
Например, в заявке на патент США №20050043706 (Eaton et а1.) описаны рассасывающиеся имплантаты для лечения синусита. Такие имплантаты имеют соответствующие размеры, форму, плотность, вязкость и(или) мукоадгезивность, которые не позволяют реснитчатой эпителиальной выстилке пазух изгнать их из полости пазухи в период лечения. Такие рассасывающиеся имплантаты доставляют терапевтические агенты, например, антибиотики или стероиды либо и антибиотики, и стероиды одновременно. Такие рассасывающиеся имплантаты могут быть выполнены в виде палочек, пилюль, гранул, пластинок или микрочастиц, а для их доставки в полость пазух могут применяться различные фармацевтически приемлемые носители.
Кроме того, в заявке на патент США №20070005094 (Eaton et а1.) описаны имплантируемые устройства, используемые для лечения заболеваний околоносовых пазух. Устройства включают полостные элементы, которые имеют первую (сложенную) конфигурацию, позволяющую ввести устройство через устье пазухи, и вторую (растянутую) конфигурацию, в которую переходят после размещения в полости пазухи. Помимо полостного элемента устройства могут включать часть для размещения в полости носа и элемент для размещения в устье околоносовой пазухи. Полостной элемент прикреплен к дистальному концу элемента, размещаемого в устье пазухи. Часть для размещения в полости носа прикреплена к проксимальному концу элемента, размещаемого в устье, и располагается в полости носового отверстия. Активный агент может быть введен во все части устройства или только в растяжимый полостной элемент, в элемент, размещаемый в устье, или в часть для размещения в полости носа.
Некоторые исследователи предлагают рассмотреть возможность обеспечения доставки лекарственных препаратов в стентах для лобных пазух для доставки контролируемого количества лекарственного препарата в измененный хирургическим путем выводной проток после осуществления хирургического вмешательства на лобных пазухах. Например, в заявке на патент США №2004/0116958А1 (Gopferich et al.) описана трубчатая оболочка, или «спейсер», изготовленный из рассасывающегося или нерассасывающегося полимера, в который перед вводом в выводной проток помещается определенное количество активного препарата, такого как кортикостероид или антипролиферативный агент. После хирургического вмешательства с целью восстановления сообщения с лобной пазухой трубчатую оболочку, в которую предварительно было помещено активное вещество, вводят в созданное хирургическим путем отверстие, где она a) препятствует смыканию созданного хирургическим путем отверстия, b) выступает в качестве канала, облегчающего отток из полости пазухи, c) осуществляет доставку активного вещества. В некоторых вариантах осуществления изобретения трубчатая оболочка состоит из нескольких слоев полимерного материала, один или несколько из которых содержат активное вещество, а один или несколько из которых не содержат активного вещества. В других вариантах осуществления изобретения трубчатая оболочка имеет «полое тело», образующее систему резервуаров, в которых содержится активное вещество, и мембрану, контролирующую высвобождение активного вещества из резервуара. В некоторых вариантах осуществления изобретения предусмотрена фиксация трубчатой оболочки, когда ее конец, заходящий в полость пазухи, набухает или увеличивается иным способом. Кроме того, в заявке на патент США №2005/0245906 (Makower et al.) описано рассасывающееся полимерное устройство, которое представляет собой спейсер, устанавливаемый в устье пазухи. Спейсер имеет множество поперечных элементов, выделяющих активное вещество. Устройство может быть имплантировано таким образом, что поперечные элементы располагаются по существу параллельно потоку слизи, направляемому реснитчатым эпителием, вдоль стенок полости пазухи, благодаря чему нормальный транспорт слизи реснитчатым эпителием не нарушается.
Кроме того, известны другие типы имплантируемых устройств для доставки лекарственных препаратов для использования в полости носа и(или) околоносовых пазух. Например, в патенте США №3948254 (Zaffaroni) описаны имплантируемые резервуары с микропористыми стенками для доставки лекарственных препаратов. Резервуары могут быть выполнены из твердого носителя, проницаемого для лекарственных препаратов. Скорость прохождения лекарственного препарата через микропористую стенку может быть ниже скорости проникновения лекарственного препарата через твердый носитель, образующий резервуар. Zaffaroni также описывает ряд возможных вариантов применения имплантируемых устройств для доставки лекарственных препаратов, включая размещение устройства в полости носового отверстия. В частности, Zaffaroni патентует назальное устройство доставки для распределения лекарственного препарата в носовом отверстии с контролируемой скоростью, при этом назальное устройство включает (a) стенку, образующую устройство для введения и размещения в полости носового отверстия лекарственного препарата; стенка выполнена из приемлемого для использования в полости носа микропористого материала, (b) резервуара, окруженного стенкой и выполненного из твердого носителя, проницаемого для лекарственного препарата и содержащего лекарственный препарат в количестве, достаточном для непрерывного дозирования и высвобождения из устройства с контролируемой скоростью в течение продолжительного периода времени, (c) жидкую среду, пропускающую лекарственный препарат, высвобождающийся из микропор, (d) при этом устройство высвобождает лекарственный препарат в среду носовой полости. Лекарственный препарат высвобождается из носителя и проходит через жидкость к наружной стенке устройства для обеспечения терапевтического эффекта. Содержание патента США №3948254 (Zaffaroni) полностью включено в настоящий документ путем ссылки.
В других публикациях также сообщается об эффективности доставки лекарственного препарата непосредственно в околоносовые пазухи при лечении синусита. Например, в публикации Tarasov, D.I., et al.. Application of Drugs Based on Polymers in the Treatment of Acute and Chronic Maxillary Sinusitis, Vestn Otorinolaringol. Vol.6, с.45-47 (1978), а также в публикации R. Deutschmann, et al., A Contribution to the Topical Treatment of [Maxillary] Sinusitis Preliminary Communication, Stomat. DDR 26 (1976), с.585-592, описан процесс размещения рассасывающегося депо для доставки лекарственных препаратов в полость гайморовой пазухи для высвобождения лекарственного препарата, более конкретно - хлорамфеникола. В данной группе пациентов во время лечения в качестве носителя был использован водорастворимый желатин, перед применением и введением в полость пазухи смешанный с лекарственным препаратом. Поскольку вещество обладает низкой механической целостностью и растворяется в течение относительно небольшого периода времени, для достижения терапевтического эффекта автор предлагает вводить препарат малыми дозами каждые 2-3 дня. Альтернативой желатину может являться губка, содержащая терапевтическое вещество, как предлагается в патенте США №6398758 (Jacobsen, et al.). Согласно патенту, в котором описан способ доставки устройства с замедленным высвобождением к стенке кровеносного сосуда, в полую цилиндрическую губку вводят лекарственный препарат, после чего губка прижимается к стенке сосуда. Это обеспечивает контакт лекарственного препарата со стенкой сосуда, не препятствуя кровотоку по центру сосуда. Также предусмотрена защитная оболочка, направляющая лекарственный препарат в стенки кровеносного сосуда и препятствующая попаданию лекарственного препарата в просвет сосуда. Несмотря на то, что губки, в которые в процессе использования вводят лекарственный препарат, обеспечивают в некоторой степени замедленное высвобождение, время, необходимое для введения лекарственного препарата в губку, также зависит от времени, в течение которого губка высвобождает лекарственное вещество. Таким образом, если необходима доставка в течение длительного периода времени, требуются дополнительные механизмы регулирования высвобождения лекарственного препарата.
В патентной литературе также представлены примеры, в которых предлагается использовать различные механизмы замедленного высвобождения совместно с системами, в которых лекарственные препараты предварительно введены в матрицы или полимеры. Указанные примеры представлены в патентах США №3948254 (Zaffaroni), 2003/0185872A2 (Kochinke), международной заявке №WO 92/15286 (Shikani) и в патенте №5512055 (Domb, et al.). Как правило, в указанной литературе рассматриваются различные материалы и структуры, которые могут использоваться для изготовления приспособлений для длительной доставки лекарственных препаратов и позволяют контролировать состояние длительной доставки лекарственного препарата. Несмотря на то, что в источниках описываются материалы и схемы создания систем замедленного высвобождения лекарственных препаратов, в них не описываются конкретные способы, средства или структуры, которые позволяют адаптировать их для целевого использования, рассматриваемого в настоящем документе.
Примеры других имплантируемых устройств для доставки лекарственных препаратов представлены в патентах США №№3993073, 4217898, 5304123, 6042561, 6183461, 6780168 и 6783522, содержание которых полностью включено в настоящий документ путем ссылки.
Способы лечения заболевания решетчатой кости
В настоящее время использование стентов и спейсеров в хирургии носа и околоносовых пазух ограничивается их размещением в выводном протоке лобной пазухи или устье клиновидной пазухи после операции с иссечением или удалением участка ткани или кости. Однако по мере изобретения новых устройств и способов лечения других типов заболеваний полости носа и околоносовых пазух, вероятно, возникнет необходимость в интраназальных спейсерах и стентах или спейсерах и стентах для околоносовых пазух (с возможностью высвобождения лекарственных препаратов или без нее), пригодных для размещения в различных полостях, а не только в выводном протоке лобной пазухи.
Предшествующий уровень техники предполагал лечение пораженных ячеек решетчатой кости путем так называемой этмоидэктомии, во время которой между внутренними частями ячеек решетчатой кости и полостью носа формируется искусственный проход. По меньшей мере в некоторых случаях требуется стентирование и(или) доставка лекарственных препаратов или иных терапевтических веществ в этот искусственный проход, созданный в процессе этмоидэктомии. Для доставки лекарственных препаратов в искусственное отверстие помещают, а впоследствии извлекают из него, узкие лоскуты марли, пропитанные лекарственным препаратом. Кроме того, в связи с этим в патенте США №6543452 (Lavigne) описано устройство для интубации носовой полости, которое представляет собой гибкую трубку, имеющую дистальный наконечник с фланцем в виде стрелки. Дистальный наконечник устройства может пенетрировать ткань (например, решетчатую буллу), проникая в соответствующее место (например, в ячейки решетчатой кости). В дистальной части интубационного устройства есть отверстия, поэтому лекарственный препарат (например, типичный стероид), вводимый по гибкой трубке/ на выходе из трубки вступает в контакт с прилежащей областью (например, с пораженными ячейками решетчатой кости). В некоторых случаях сначала вводят канюлю-троакар, а затем назальное интубационное устройство проталкивают через канюлю-троакар. Кроме того, в публикации европейского патента №ЕР0624349 (Milewski) описан катетер-баллон, снабженный автоматически раскрывающимся баллоном, который вводится в полость тела через отверстие, выполненное хирургическим путем (например, в лобную пазуху или ячейку решетчатой кости) и раскрывается, принимая анатомическую форму полости и создавая таким образом тампонаду этой полости.
Способы лечения лобной пазухи
Описанные выше проблемы также характерны для лечения лобных пазух. Кроме того, вследствие особенностей анатомического строения лобных пазух могут возникать другие проблемы. Так, например, для получения доступа к лобным пазухам необходим специальный инструментарий. Кроме того, было установлено, что традиционные операции ФЭХОП на лобных пазухах вызывают повышенный риск образования рубцов. Образование рубцов влечет за собой вероятность повторного нарушения оттока из полости пазухи и ее вентилирования.
Хотя, как было установлено, применение кортикостероидов эффективно снижает риск реактивного образования рубцов в полости лобных пазух, остается актуальным ряд серьезных ограничений. Как правило, назальные спреи и мази не достигают критически важных областей вокруг выводного протока лобной пазухи. Также сложно обеспечить глубокое введение хирургических инструментов в полость лобной пазухи. Кроме того, возникают проблемы с удержанием хирургических инструментов в выводном протоке лобной пазухи.
Следовательно, сохраняется необходимость в разработке новых устройств и способов доставки лекарственных препаратов и других терапевтических или диагностических веществ в течение продолжительного периода времени в полость околоносовых пазух, евстахиевых труб, среднего уха и(или) в другие полости тела для лечения синусита, отита или иных заболеваний и расстройств. В частности, существует необходимость в разработке способа удобного и эффективного доступа и лечения околоносовых пазух, таких как лобная пазуха.
Настоящее изобретение удовлетворяет эти и другие потребности.
Краткое описание
Настоящее изобретение относится к спейсерному устройству и способу доставки вещества, включающему растяжимые резервуары, имплантируемые в полость околоносовых пазух и иные полости, отверстия и проходы тела для сохранения их проходимости и(или) обеспечения длительной местной доставки терапевтического или диагностического препарата. Также в патенте описываются устройства, системы и способы пенетрирования пазух для создания этмоидотомических отверстий или иных отверстий в стенках околоносовых пазух или других анатомических структур.
В одном конкретном аспекте изобретения разработана система и способ лечения лобных пазух.
Спейсерная система для доставки вещества в полость пазухи, в частности, лобной околоносовой пазухи, согласно изобретенияю содержит изогнутую направляющую доставки, выполненную с возможностью прохождения через носовое отверстие таким образом, что ее дистальный конец размещен в устье лобной околоносовой пазухи или рядом с ним, а проксимальный конец направляющей размещен снаружи носового отверстия; удлиненный катетер для доставки вещества, имеющий проксимальный конец и дистальный конец; и спейсерное устройство для носовой пазухи для доставки вещества, проходящее от дистального конца катетера доставки и сообщающееся по текучей среде с ним, при этом спейсерное устройство включает: удлиненный трубчатый ствол с атравматическим наконечником; растяжимый резервуар, прикрепленный к стволу, в который может быть помещен лекарственный препарат; и по меньшей мере два складных удерживающих элемента, выполненных с возможностью прилегания к резервуару и размещения внахлест поверх него.
Система может дополнительно содержать оболочку, съемно размещенную поверх спейсерного устройства для носовой пазухи для фиксирования удерживающих элементов в сложенном состоянии, при этом оболочка содержит ограничитель, расположенный на ее проксимальном конце или рядом с ним и предназначенный для ограничения продвижения оболочки по направляющей доставки. При этом катетер для доставки вещества содержит маркер, размещенный вдоль части длины катетера так, что когда катетер для доставки вещества и оболочка введены в направляющую, а дистальный конец маркера достигает проксимального конца оболочки, атравматический наконечник спейсера для носовой пазухи размещен на дистальном конце направляющей, и когда проксимальный конец маркера достигает проксимального конца оболочки, складные удерживающие элементы размещены снаружи дистального конца направляющей.
Изогнутая направляющая доставки включает жесткую проксимальную часть и гибкую изогнутую дистальную часть, и может также включать рентгеноконтрастный дистальный наконечник.
Предпочтительно катетер для доставки вещества выполнен непрозрачным, а спейсерное устройство для носовой пазухи является полупрозрачным.
Система модет дополнительно включать шовную петлю, соединенную со спейсерным устройством для носовой пазухи и предназначенную для присоединения спейсера к ткани внутри носовой полости или выводного протока лобной пазухи. Причем катетер дополнительно может включать люэровский соединительный элемент, соединенный с его проксимальным концом для соединения катетера с источником вещества.
Предпочтительно система, содержащая некоторое количество вещества, дополнительно включает рукоятку, подвижно подсоединяемую к проксимальному концу направляющей, при этом указанное вещество содержит стероид, где стероид представляет собой триамцинолона ацетонид.
Резервуар спейсерного устройства для носовой пазухи имеет по существу цилиндрическую боковую стенку и конические концы, при этом боковая стенка и конические концы имеют отверстия; таким образом, терапевтическое вещество, помещенное в резервуар, будет высвобождаься из резервуара через эти отверстия. Причем диаметр каждого отверстия составляет от приблизительно 20 до приблизительно 40 микрон.
Предпочтительно удерживающие элементы спейсерного устройства для носовой пазухи содержат крылья, выполненные в виде петель. Размах крыльев удерживающих элементов в растянутом состоянии составляет от приблизительно 13 до приблизительно 16 мм. При этом удерживающие элементы могут быть расположены на стволе диаметрально противоположно относительно друг друга, или расположены в шахматном порядке вдоль продольной оси устройства, или прикреплены вдоль одной стороны ствола.
Как указано выше система может включать трубку удлиненной формы, способную принимать необходимую анатомическую форму, или оболочку, выполненную с возможностью прохождения по анатомическим структурам тела пациента и образующую структуру для доступа к лобным пазухам. Также были разработаны различные подходы к осуществлению спейсеров для доставки вещества с удерживающей структурой. Таким образом, компенсируется вариабельность анатомии пациента. Также в одном из аспектов спейсерное устройство может иметь дополнительный атравматический наконечник, выполненный, например, из мягкого полимера.
Один из вариантов осуществления спейсера для доставки вещества, предназначенного для лечения лобной пазухи, включает ствол и растяжимый резервуар, присоединенный к дистальной части ствола. Резервуар в сложенном состоянии вводят в полость тела пациента, устанавливают в полости лобной пазухи, а затем растягивают. Для растяжения резервуара в него может быть введено вещество, такое как лекарственный препарат или иное терапевтическое вещество. Кроме того, резервуар может иметь отверстия, через которые лекарственный препарат или терапевтическое вещество может высвобождаться для лечения лобных пазух. Также может быть предусмотрена возможность отрезания ствола по заданной длине, оставляя при этом спейсер на месте хирургического вмешательства. Спейсер может включать удерживающую структуру, облегчающую фиксацию спейсера на лобных пазухах или внутри них. Для этого предусмотрено одно или несколько крыльев, проходящих вдоль различных частей резервуара. Крылья могут находиться в сложенном состоянии, необходимом для доставки устройства к месту хирургического вмешательства, и в развернутом состоянии, позволяющем зафиксировать спейсер внутри анатомической структуры.
Один из вариантов осуществления устройства и способа лечения заболевания пазух решетчатой кости включает пенетрирующее устройство, которое имеет дистальный наконечник и ограничительную отметку или элемент, расположенный на определенном расстоянии в проксимальном направлении от дистального наконечника. Расстояние между ограничительной отметкой или элементом и дистальным наконечником меньше расстояния между решетчатой буллой и расположенной на той же стороне клиновидной пазухой. Этмоидотомический канал формируется путем перемещения пенетратора через решетчатую буллу не перпендикулярно основанию черепа и преимущественно в направлении расположенной на той же стороне клиновидной пазухи. Перемещение пенетратора прекращается в тот момент, когда ограничительная отметка или элемент оказываются практически на одном уровне с решетчатой буллой. После этого пенетратор извлекают. Затем в этмоидотомический канал на определенный период времени может быть помещен стент, спейсер или спейсерное устройство для доставки вещества с целью сохранения проходимости и(или) эффективной локальной доставки терапевтического вещества.
В соответствии с одним из вариантов осуществления настоящего изобретения пенетрирующее устройство и способ пенетрации пазухи могут использоваться для формирования этмоидотомического канала или иного отверстия в стенке околоносовой пазухи или другой анатомической структуры. Такое устройство состоит из пенетрирующего элемента удлиненной формы и рукоятки, соединенной с пенетрирующим элементом на проксимальном конце или рядом с ним. Вдоль рукоятки или элемента удлиненной формы размещается прицельное приспособление, так чтобы он был виден из точки наблюдения, расположенной за пределами тела, когда дистальный конец элемента удлиненной формы вводят в полость тела пациента. Такое прицельное приспособление используется пользователем устройства для ориентации дистального конца пенетратора в необходимом направлении в полости тела пациента. В некоторых вариантах осуществления настоящего изобретения прицельное приспособление может быть выполнено в виде гребня. Прицельное приспособление может располагаться в плоскости, по существу параллельной плоскости, в которой расположен удлиненный элемент пенетратора, проходящий от рукоятки, и может необязательно включать другой элемент (например, поперечный элемент), размещенный по существу под прямым углом к плоскости, в которой расположен удлиненный пенетратор, проходящий от рукоятки. В некоторых вариантах осуществления настоящего изобретения удлиненный пенетратор может иметь изгиб, и по меньшей мере часть прицельного приспособления может проходить параллельно части удлиненного пенетратора, расположенной дистальнее изгиба, тем самым показывая направление или траекторию, по которой перемещается дистальная часть удлиненного пенетратора.
Также настоящее изобретение охватывает спейсерное устройство и способ доставки вещества. В одном из вариантов осуществления настоящего изобретения спейсерное устройство для доставки вещества включает ствол и растяжимый резервуар, размещенный на стволе. Резервуар в сложенном состоянии вводят в полость тела или отверстие (например, в полость околоносовой пазухи, этмоидотомический канал, выводной проток лобной пазухи или в любую другую полость тела, отверстие или проход). Затем в резервуар вводят терапевтическое вещество, заставляя резервуар растягиваться in situ. В соответствующем месте ствол можно отделить или отрезать, а после добавления лекарственного препарата в резервуар проксимальную часть ствола можно удалить. Резервуар выполнен таким образом, что вещество высвобождается из резервуара в течение определенного периода времени. Резервуар может иметь боковую стенку и конические концы, где боковая стенка и конические концы имеют отверстия. Таким образом, терапевтическое вещество, помещенное в резервуар, высвобождается из резервуара через такие отверстия. В некоторых вариантах осуществления настоящего изобретения устройство может включать приспособление (например, удерживающие крылья, выступы, шовные петли и т.д.) для удерживания резервуара в заданном положении в полости тела.
Кроме того, настоящее изобретение охватывает способ и систему, в которой спейсерное устройство для доставки вещества вышеописанной конструкции используется совместно с пенетратором околоносовых пазух (например, с устройством для этмоидотомии, описанным выше, или любым другим пенетратором) и оболочкой. Сначала на пенетратор околоносовых пазух надевают оболочку, после чего пенетратор вместе с оболочкой проталкивают через стенку околоносовой пазухи или воздухоносной ячейки. Затем пенетратор извлекают, а оболочка остается на месте. Спейсерное устройство для доставки вещества вводят в оболочку. Затем оболочку извлекают, оставляя спейсерное устройство для доставки вещества на месте в полости пазухи или воздухоносной ячейки. После этого в резервуар вводят терапевтическое вещество таким образом, чтобы впоследствии это вещество высвобождалось из резервуара в полость околоносовой пазухи или воздухоносной ячейки.
Кроме того, настоящее изобретение охватывает вариант осуществления изобретения и способ лечения синусита, в котором имплантируемое устройство с резервуаром, выделяющим вещество, помещают в полость околоносовой пазухи или в устье, или выводной проток околоносовой пазухи. После этого в резервуар, выделяющий вещество, вводят стероид. Таким образом, стероид высвобождается из резервуара в количестве, необходимом для лечения синусита.
Другие аспекты и подробности настоящего изобретения станут понятны после изучения подробного описания и примеров, изложенных ниже.
Краткое описание чертежей
На фиг.1 представлено спейсерное устройство, составляющее предмет настоящего изобретения, используемое совместно с эндоскопом для лечения человека.
На фиг.2 представлен вид сбоку варианта осуществления спейсерного устройства, составляющего предмет настоящего изобретения.
На фиг.2A представлен увеличенный вид в продольном сечении дистальной части устройства, изображенного на фиг.2.
На фиг.2B представлен увеличенный вид в продольном сечении дистальной части устройства, изображенного на фиг.2, в процессе добавления вещества в резервуар устройства.
На фиг.2C представлен вид в продольном сечении проксимальной втулки устройства, изображенного на фиг.2.
На фиг.2D представлен вид сбоку устройства, изображенного на фиг.2, с наложенной ограничивающей оболочкой во втянутом положении.
На фиг.2E представлен вид сбоку устройства, изображенного на фиг.2, с наложенной ограничивающей оболочкой в выдвинутом положении.
На фиг.2F схематически изображен растяжимый резервуар устройства, изображенного на фиг.2.
На фиг.2G представлен увеличенный вид участка 2G, показанного на фиг.2F.
На фиг.2H представлен вид проксимального конца растяжимого резервуара, изображенного на фиг.2F.
На фиг.3 представлен вид сбоку дистальной части другого варианта осуществления спейсерного устройства, составляющего предмет настоящего изобретения, включающей альтернативную систему удержания.
На фиг.4 представлен вид сбоку одного из вариантов осуществления оболочки, используемой совместно с иглой для этмоидотомии в соответствии с принципами настоящего изобретения.
На фиг.5 представлен вид сбоку одного из вариантов осуществления иглы для этмоидотомии, составляющей предмет настоящего изобретения.
На фиг.5A представлен вид в продольном разрезе дистальной части ручки иглы для этмоидотомии, изображенной на фиг.5.
На фиг.5B представлен вид дистального конца иглы для этмоидотомии, изображенной на фиг.5.
На фиг.5C представлен вид сбоку дистального наконечника иглы для этмоидотомии, изображенной на фиг.5.
На фиг.5D представлен вид сбоку другого варианта осуществления устройства для этмоидотомии, составляющего предмет настоящего изобретения и включающего вращающийся дробильный наконечник.
На фиг.5E представлен увеличенный вид сбоку вращающегося дробильного наконечника устройства для этмоидотомии, изображенного на фиг.50.
На фиг.6 представлен вид сбоку иглы для этмоидотомии, показанной на фиг.5, с надетой на нее оболочкой, изображенной на фиг.4.
На фиг.7A-7K поэтапно показан способ выполнения этмоидотомии и имплантации спейсерного устройства для доставки вещества в этмоидотомический канал в соответствии с принципами настоящего изобретения.
На фиг.8A-8G поэтапно показан способ использования катетера-направляющей для имплантации спейсерного устройства для доставки вещества, изображенного на фиг.2, в выводной проток лобной пазухи человека в соответствии с принципами настоящего изобретения.
На фиг.9A-9D поэтапно показан способ использования оболочки, изображенной на фиг.4, и дополнительного дилататора для имплантации спейсерного устройства для доставки вещества, изображенного на фиг.2, в выводной проток лобной пазухи человека в соответствии с принципами настоящего изобретения.
На фиг.10A показана система доставки вещества в полость лобной околоносовой пазухи, выполненная в соответствии с одним из вариантов осуществления настоящего изобретения.
На фиг.10B-10E представлены различные виды и детали устройства доставки вещества в полость лобной околоносовой пазухи и ограничивающей оболочки для устройства в соответствии с одним из вариантов осуществления настоящего изобретения.
На фиг.11A-D показаны различные альтернативные варианты осуществления спейсерных устройств для лобных пазух.
На фиг.12A показано направляющее устройство для направления устройства доставки вещества в полость лобной околоносовой пазухи в соответствии с одним из вариантов осуществления настоящего изобретения.
На фиг.12B-12E представлены различные виды и варианты осуществления дистального конца направляющих устройств, аналогичных устройству, изображенному на фиг.12A.
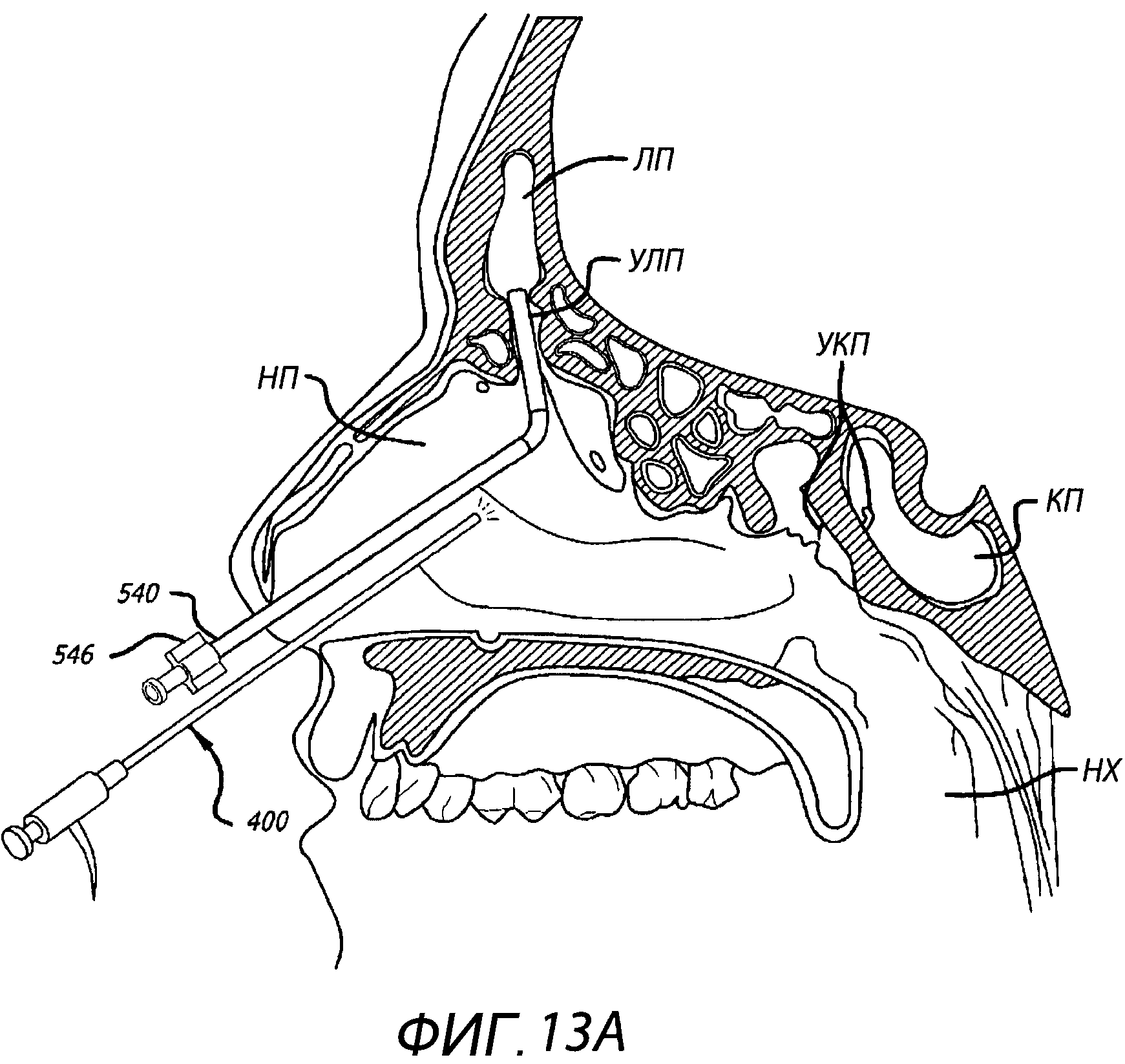
На фиг.13A-13H поэтапно показан способ лечения лобной пазухи.
На фиг.14A-D показана имплантация других различных спейсерных устройств в полость лобной пазухи.
На фиг.15 представлен график оценок по шкале Ланда-Маккея для 14 пациентов, указанных ниже.
На фиг.16 представлена столбчатая диаграмма, отображающая средние значения теста оценки исхода заболеваний носа и околоносовых пазух (SNOT-20) в различные моменты времени для пациентов, указанных ниже.
На фиг.17 представлен вид в перспективе винта для доставки вещества (пенетрации кости), являющегося предметом настоящего изобретения.
На фиг.17A схематически изображен винт для доставки вещества (пенетрации кости), изображенный на фиг.17, имплантированный в костную структуру полости носа, покрытую слизистой оболочкой.
На фиг.18 показана голова человека в частичном саггитальном сечении (слева/справа), в котором видна игла для этмоидотомии с контролирующим глубину проникновения ограничителем, введенная через ноздрю и продвинутая в полость пазух решетчатой кости так, что ограничитель упирается в нос пациента, препятствуя, таким образом, дальнейшему продвижению иглы.
На фиг.19A-D представлены различные виды другого варианта осуществления спейсерного устройства для доставки вещества, составляющего предмет настоящего изобретения и включающего многослойный растяжимый резервуар.
Подробное описание изобретения
Подробное описание, приведенное ниже, и сопроводительные чертежи предназначены для описания некоторых, но необязательно всех вариантов осуществления изобретения. Содержание подробного описания не ограничивает объем настоящего изобретения.
На фиг.1-2G представлен вариант осуществления имплантируемого устройства для доставки вещества и(или) спейсера 10, составляющего предмет настоящего изобретения. Настоящее устройство 10 включает удлиненный гибкий ствол катетера 12, имеющий проксимальную часть 12а и дистальную часть 12b, отделенные друг от друга разделительной меткой 15. Проксимальная часть ствола 12a и дистальная часть ствола 12b могут быть выполнены из одного или из разных материалов и могут иметь одинаковые размеры (например, диаметр, толщину стенки и т.п.). Например, в некоторых вариантах осуществления, предназначенных для имплантации в полости околоносовых пазух или в других областях в полости уха, носа или горла, Проксимальная часть ствола 12а может быть выполнена из подходящего биосовместимого материала, обладающего достаточной прочностью на сжатие (т.е. упругостью), что позволяет пользователю вводить и продвигать устройство для доставки вещества 10 в околоносовые анатомические структуры. Одним из таких материалов является полиамид. В некоторых вариантах осуществления дистальная часть ствола 12b может быть выполнена из более гибкого биосовместимого материала, такого как нейлон или полиэтилентерефталат (ПЭТ). Просвет 13 непрерывно проходит насквозь ствола 12. Дистальная часть ствола 12a может постепенно сужаться или постепенно уменьшаться в диаметре по сравнению с проксимальной частью ствола, что облегчает введение устройства, как описано ниже. На дистальном конце просвета 13 установлена заглушка 23. Заглушка 23 может содержать любой подходящий закрывающий элемент, например, стенку закрытого конца трубки, колпачок, массу, заполняющую конец просвета 13, или любой другой элемент, способный блокировать поток жидкости. В конкретном примере, представленном на чертежах, заглушка 23 представляет собой биосовместимый полимерный адгезив, заполняющий дистальный конец просвета 13. В некоторых вариантах осуществления заглушка 23 может включать мягкий атравматический (например, в форме луковицы или тупой) наконечник, выступающий за пределы дистального конца дистальной части ствола 12b.
Растяжимый резервуар 14 установлен в сложенном состоянии на дистальной части ствола 12b рядом с дистальным концом и растягивается по мере наполнения. Более детально конструкция одного варианта осуществления такого резервуара 14 видна на фиг.2A и 2B, а также на фиг.2F, 2G и 2H. В данном варианте осуществления изобретения резервуар 14 выполнен в виде баллона с цилиндрической боковой стенкой, в которой предусмотрены отверстия 31. Резервуар 14 может быть изготовлен из любого подходящего биосовместимого материала, а в некоторых вариантах осуществления может быть выполнен в виде баллона, изготовленного из неподатливого или полуподатливого материала, такого как нейлон 12. По меньшей мере в некоторых вариантах осуществления изобретения материал и толщина стенки резервуара предпочтительно должны обеспечивать достаточную гибкость резервуара, чтобы a) избежать серьезных травм при извлечении и удалении устройства из полости тела, b) предотвратить единовременное высвобождение всего содержимого резервуара и c) поддерживать постоянный размер отверстий 31 при раскрытии резервуара. Количество резервуаров 14 (например, два или несколько), размер резервуара (резервуаров), а также количество и размер отверстий 31 могут варьироваться в зависимости от предполагаемого места имплантации и (или) от содержания действующих веществ, вязкости, размера частиц (для суспензий) и(или) свойств доставляемого вещества. Например, в варианте осуществления устройства 10 для прохождения через этмоидотомический канал и размещения в полости воздухоносной ячейки решетчатой кости для лечения этмоидального синусита длина резервуара 14 может составлять от приблизительно 0,5 см до приблизительно 3,5 см, как правило, приблизительно 2 см; диаметр резервуара в растянутой конфигурации составляет от приблизительно 0,1 см до приблизительно 0,5 см, как правило, приблизительно 0,3 см. Кроме того, в зависимости от применяемого вещества и необходимой скорости высвобождения может быть предусмотрено соответствующее количество отверстий 31. Как правило, количество отверстий 31 диаметром от приблизительно 5 микрон до приблизительно 80 микрон колеблется в пределах от приблизительно 50 до приблизительно 5000.
Как сказано ниже, резервуар 14 в этом варианте осуществления вводят в сложенном состоянии в отверстие, проход или полость тела (например, выводной проток лобной пазухи, устье околоносовой пазухи, антротомическое отверстие, этмоидотомическое отверстие или другая полость уха, горла или носа пациента), затем резервуар заполняют нужным веществом, что заставляет резервуар растягиваться. Например, в случае лечения воспаления околоносовой пазухи с использованием конкретного резервуара 14, описанного выше, с отверстиями, размер и схема расположения которых показаны на фиг.2F-2H, резервуар 14 заполняют приблизительно 0,10 мл водной суспензии, содержащей 40 мг/мл суспензии триамцинолона ацетонида для инъекций (Фармакопея США) (Кеналог®-40 производства Bristol-Myers Squibb, Сомервилль, Нью-Джерси). Таким образом, из резервуара ежедневно будет выделяться приблизительно 100 мкг триамцинолона ацетонида в течение 14 дней. Для лечения грибкового синусита или других грибковых инфекций резервуар 14 также может служить для доставки противогрибкового препарата, такого как липосомный или нелипосомный амфотерицин В в концентрации 0,3-1,5 мг/кг (производства Pfizer под маркой Амфоцин® противогрибковый). Систематически вводимый амфотерицин, как правило, характеризуется ограниченной способностью к распределению и переходу из кровотока в слизистые оболочки и наоборот. При помощи устройства для доставки вещества 10 осуществляется локальное высвобождение амфотерицина в слизистую оболочку, где присутствуют болезнетворные грибковые организмы, и терапевтическая концентрация лекарственного препарата может достигаться в слизистой, распределяясь в полости пазух благодаря реснитчатому эпителию. Однако, как правило, не происходит всасывания значительного количества амфотерицина слизистой оболочкой пазух. Таким образом, вероятность развития системного побочного эффекта амфотерицина, такого как нефротоксичность, исключается. Кроме того, с помощью резервуара 14 может осуществляться доставка растворов и суспензий к окружающим анатомическим структурам. Указанный способ в особенности подходит для доставки стероидов, так как большинство стероидов применяются в форме суспензий.
Кроме того, резервуар 14 необязательно должен использоваться только для доставки терапевтического вещества. На практике он может использоваться в качестве объемного устройства (например, вместо стента для околоносовой пазухи). В таких случаях резервуар 14 in situ может быть заполнен физиологическим раствором или другой инертной жидкостью, вследствие чего резервуар 14 растягивается и плотно прилегает к анатомической структуре (анатомическим структурам) и удерживается силой трения в месте имплантации. Для этих целей резервуар 14 также может иметь утолщения на поверхности резервуара. Если предполагается функционирование резервуара 14
Резервуар 14 в сложенном состоянии может иметь относительно небольшой диаметр, что существенно облегчает его введение и извлечение. В тех вариантах осуществления настоящего изобретения, в которых резервуар 14 выполнен из неподатливого или полуподатливого материала, резервуар 14 не подвергается значительной упругой деформации в процессе заполнения. Таким образом, он не оказывает давления на содержимое с целью изгнания вещества через отверстия 31. Вещество, введенное в резервуар 14, вытесняется через отверстия 31 скорее под действием силы тяжести или путем взаимодействия со слизью или кровью, постоянно перемещаемыми реснитчатым эпителием в полости околоносовых пазух. Такой способ доставки, не предполагающий использования избыточного давления, позволяет добиться медленного выделения нужного вещества в течение нескольких дней. В других вариантах осуществления настоящего изобретения резервуар 14 может быть выполнен из деформируемого или эластичного материала с небольшими отверстиями 31, так что материал, из которого выполнен баллон 14, сжимается по мере высвобождения вещества через отверстия 31, тем самым поддерживая давление внутри баллона. В тех случаях, когда предполагается введение резервуара 14 в устье пазухи, выводной проток, антротомическое отверстие или этмоидэктомическое (этмоидотомическое) отверстие, и использование его для доставки водной суспензии, содержащей 40 мг/мл суспензии триамцинолона ацетонида для инъекций (Фармакопея США) (Кеналог®-40 производства Bristol-Myers Squibb, Сомервилль, Нью-Джерси), или другого вещества аналогичной консистенции, резервуар 14 может иметь приблизительно 2200 отверстий 31, вырезанных лазером в боковой стенке резервуара 14, диаметром приблизительно от 20 до 40 микрон. Как показано на фиг.2F-2H, отверстия 31 могут быть расположены продольными рядами, при этом отдельные отверстия 31 в соседних рядах располагаются в шахматном порядке относительно друг друга. В данном конкретном примере продольное расстояние D1 между отдельными отверстиями составляет 0,30+/-0,03 мм, а расстояние D2 между рядами составляет 0,68+/-0,1 мм. Кроме того, в данном примере резервуар имеет цилиндрическую боковую стенку 14a, которая определяет рабочую длину резервуара, дистальную сужающуюся часть 14b, переходящую от цилиндрической боковой стенки 14a к дистальному стволу 12b (дистально по отношению к резервуару), и проксимальную сужающуюся часть 14c, переходящую от цилиндрической боковой стенки 14a к дистальному стволу 12b (проксимально по отношению к резервуару), и отверстия 31, размещенные на проксимальной и дистальной сужающихся частях 14b и 14c, как показано на чертежах. Также в данном примере общая длина резервуара 14 составляет приблизительно 16 мм, а рабочая длина (т.е. длина цилиндрической боковой стенки 14c) составляет приблизительно 13 мм, при этом диаметр в полностью растянутом состоянии составляет 3,0-3,5 мм. В боковой стенке 14a резервуара 14 лазером вырезано приблизительно 768 отверстий 31. Диаметр каждого отверстия 31, вырезанного лазером, составляет 40 микрон. Данная конкретная конструкция резервуара, при условии что для заполнения резервуара используется от 0,31 до 0,35 мл суспензии триамцинолона ацетонида для инъекций 40 мг/мл (Фармакопея США) (Кеналог®-40 производства Bristol-Myers Squibb, Сомервилль, Нью-Джерси), обеспечивает доставку дозы, составляющей приблизительно 100 мкг триамцинолона ацетонида в день в течение 28 дней.
В данном конкретном примере дистальная часть ствола 12b может быть изготовлена из нейлона 12, ее внешний диаметр составляет 0,0711 см (0,028 дюймов), внутренний диаметр составляет 0,0508 см (0,020 дюймов), а длина равна 17 мм. Окно 28, как показано на фиг.2A-2B, предусмотрено в стволе катетера 12 для облегчения заполнения резервуара 14. Клапан 26 пропускает вещество (или компонент (компоненты) вещества) из просвета 13 ствола катетера 12 в резервуар 14 (см. фиг.1C), но препятствует значительному обратному оттоку из резервуара 14 в просвет 13 (см. фиг.1B). Клапан 26 может быть выполнен в виде одноходового клапана любого подходящего типа. В данном конкретном варианте осуществления изобретения клапан 28 представляет собой эластомерный золотниковый клапан, изготовленный из сегмента термопластичной эластомерной трубки C-flex® (производства Consolidated Polymer Technologies, Inc., Клируотер, Флорида).
При необходимости для облегчения позиционирования резервуара 14 в полости тела могут быть предусмотрены дистальная рентгеноконтрастная метка 24 и проксимальная рентгеноконтрастная метка 22. Каждая из этих меток 22 и 24 может быть выполнена в форме кольца из рентгеноконтрастного материала и установлена на стволе 12 на одной оси с обоими концами цилиндрической боковой стенки 14a резервуара. В данном конкретном примере каждая метка 22 и 24 выполнена в виде кольца из платиново-иридиевого сплава с внешним диаметром 0,0864 см (0,034 дюйма) и внутренним диаметром 0,0762 см (0,030 дюйма). Эти метки видны при использовании любого способа визуализации, включая рентгеноскопию и компьютерную томографию.
В представленном примере проксимальная часть ствола 12a может быть изготовлена из полиимидной трубки с внешним диаметром 0,157 см (0,0618 дюйма), внутренним диаметром 0,132 см (0,052 дюйма) и длиной 20 см. Втулка 16, включающая охватывающий люэровский соединительный элемент, изготовленный из прозрачного поликарбоната (№ партии 41519, производитель Qosina, Эджвуд, Нью-Йорк), присоединен к проксимальному концу ствола 12. Как показано на фиг.2C, втулка 16 имеет проксимальный канал 100, который, постепенно сужаясь, переходит в дистальный канал 102, тем самым позволяя осуществлять инфузию суспензий и вязких жидкостей. Дистальный канал 102 имеет приблизительно такой же диаметр и является продолжением просвета ствола 13.
Кроме того, в представленном примере устройство включает приспособления для фиксации положения двух типов, а именно шовную петлю 20, а также пару утолщений в виде фиксирующих крыльев 18. Фиксирующие крылья 18 расположены в диаметрально противоположных местах на стволе 12, проксимально относительно резервуара 14, и позволяют зафиксировать резервуар 14 в заданном положении в полости тела, как более подробно рассмотрено ниже. В настоящем примере каждое фиксирующее крыло 18 представляет собой предварительно сформированную петлю из никель-титановой (нитиноловой) проволоки диаметром 0,0218 см (0,0086 дюйма). Каждое фиксирующее крыло 18 может сгибаться или складываться в сложенном состоянии устройства, в котором оно по существу прижато к внешней поверхности ствола 12. Однако фиксирующие крылья 18 перемещаются в заранее сформированную конфигурацию так, что, при условии отсутствия любых ограничений, каждое фиксирующее крыло 18 упруго отскакивает наружу в вытянутое положение, в котором оно выступает под углом приблизительно от 65 до 90 градусов относительно продольной оси ствола 12. Такое предварительное формирование этих крыльев 18 выполняется путем термической обработки петли из нитиноловой проволоки при температуре 520°C в течение 20 минут для достижения температуры сварки аустенитной стали (Af) 20°C. Также могут использоваться различные альтернативные варианты осуществления фиксирующих крыльев 18. Например, на фиг.3 представлен альтернативный фиксирующий элемент 88, включающий проксимальный и дистальный упругие эластомерные фланцы 90 и 92, которые расположены на определенном расстоянии друг от друга, при этом они опираются и контактируют с противоположными сторонами анатомической стенки или структуры. На фиг.3 под анатомической стенкой или структурой подразумевается решетчатая булла или стенка пазухи, образованной костью В и покрытой слизистой оболочкой М. Дистальный фланец 88 обладает достаточной упругостью и гибкостью, что позволяет ему сжиматься при прохождении через небольшое отверстие в анатомической стенке и затем возвращаться в прежнее растянутое положение, как показано на фиг.3.
Шовная петля 20 (например, ушко или кольцо) может быть выполнена из податливого, гибкого, упругого, эластичного или суперэластичного материала, такого как шовная нить или проволока из сплава никеля и титана (нитинол). В представленном варианте осуществления настоящего изобретения шовная петля выполнена из черного одноволоконного нейлонового нерассасывающегося хирургического шовного материала диаметром 0,0190 см (0,0075 дюйма). Шовная петля 20 может быть прижата к внешней поверхности ствола 12. Шовная петля 20 может быть прикреплена к внешней поверхности ствола 12 путем обматывания проволоки или другого материала вокруг ствола и фиксации проволоки на поверхности ствола при помощи подходящего адгезива, такого как цианакриловый, эпоксидный или УФ-отверждаемый адгезив, и(или) путем установки полимерного рукава или термоусадочного элемента на части проволоки, которые обернуты вокруг ствола 12. В некоторых вариантах осуществления изобретения шовная петля может быть окрашена так, чтобы ее можно было визуально отличить от крови и розово-красной слизистой оболочки носовой полости. Например, шовная петля 20 может быть окрашена в черный, ярко-синий или зеленый цвет, чтобы хирург мог легко ее обнаружить. Шовная петля 20 может быть пришита к прилегающей ткани, чтобы зафиксировать на месте дистальную часть устройства 10.
Как показано на фиг.2D и 2E, на ствол 12 может быть надета трубчатая ограничивающая оболочка. В конкретном примере, представленном на чертеже, эта ограничивающая оболочка 30 представляет собой пластиковую трубку длиной 10 см с внешним диаметром 0,213 см (0,084 дюйма) и внутренним диаметром 0,191 см (0,075 дюйма). Ограничивающая оболочка 30 перемещается назад и вперед из втянутого положения (см. фиг.20) в вытянутое положение (см. фиг.2E), и наоборот. В вытянутом положении ограничивающая оболочка накрывает фиксирующие крылья 18, шовную петлю 20 и сложенный резервуар 14, таким образом удерживая фиксирующие крылья 18 в сложенном состоянии и образуя гладкое защитное покрытие на фиксирующих крыльях 18, шовной петле 20 и сложенном резервуаре 14. Кроме того, в вытянутом положении ограничивающая оболочка 30 усиливает прочность на сжатие всего устройства и препятствует сгибанию ствола 12 при проталкивании через относительно узкие и(или) извитые анатомические проходы. После введения и установки устройства 10 в необходимое положение ограничивающая оболочка 12 перемещается во втянутое положение, открывая таким образом доступ к шовной петле 20, позволяя фиксирующим крыльям 18 расправиться и перейти в вытянутое положение, а резервуару 14 раскрыться в процессе его заполнения веществом.
Несмотря на то, что в конкретных примерах осуществления спейсерного устройства 10, описанных выше, резервуар 14 представлен в виде однослойного баллона, в других вариантах осуществления изобретения резервуар может представлять собой многослойный баллон, в каждом слое которого предусмотрены отверстия разного размера. Кроме того, вещество можно избирательно вводить между конкретными слоями, что способствует доставке данного вещества с требуемой скоростью. В связи с этим в качестве примера на фиг.19-19D показан другой вариант осуществления спейсерного устройства для доставки вещества 610, имеющий ствол 612 и многослойный резервуар-баллон 614. Ствол 612 может иметь такую же конструкцию и оснащение, как и ствол 12 устройства 10, описанного выше. Однако в данном варианте осуществления изобретения в стволе 612 проходят три просвета 616, 618 и 620, а резервуар 614 представляет собой баллон, состоящий из трех слоев 614a, 614b и 614c. Внешний слой 614a имеет отверстия 631a первого размера. Средний слой 614b имеет отверстия 631b второго размера, который меньше размера отверстий 631a, выполненных во внешнем слое 614a. Внутренний слой 614c имеет отверстия 631c третьего размера, который меньше размера отверстий 631b, выполненных в среднем слое 614b. Первый просвет 616 открывается в пространство внутреннего слоя 614c. Второй просвет 618 открывается в пространство между внутренним слоем 614c и средним слоем 614b. Третий просвет 620 открывается в пространство между средним слоем 614b и внешним слоем 614a. Таким образом, оператор может выбирать пространство, в которое вводится конкретное вещество, с тем чтобы препарат проходил либо a) только через отверстия 631a во внешнем слое 614a, либо b) через отверстия 631b в среднем слое 614b так же, как и через отверстия 631a во внешнем слое 614a, либо c) через все отверстия 631a, 631b и 631c во всех трех слоях 614a, 614b и 614c. Таким образом, обеспечивается оптимизация скорости выделения вещества.
Как следует из изложенного ниже подробного описания, спейсерное устройство для доставки вещества 10 и 610 может быть имплантировано в любую часть или место организма человека или животного для выполнения разделительной функции (т.е. для предотвращения врастания ткани, образования рубцов, возникновения фиброза, адгезивных образований и т.д.) и(или) для доставки любого терапевтического вещества. Например, при использовании в полости уха, носа и горла устройство 10, 610 может быть имплантировано в естественное устье или искусственное отверстие в любой околоносовой пазухе или воздухоносной ячейке, либо в любое другое естественное, измененное или созданное хирургическим путем отверстие или проход, такой как выводной проток лобной пазухи, нижнее, верхнее или среднее носовое отверстие.
На фиг.4-5E показан пример системы для этмоидотомии, которая может использоваться как самостоятельно, так и в сочетании со спейсерным устройством для доставки вещества 10 и 610 описанного выше типа. Такая система для этмоидотомии состоит из оболочки 40 (см. фиг.5) и иглы для пункции пазухи 60 (см. фиг.6). Оболочка 40 и игла для пункции пазухи 60 могут использоваться по отдельности или вместе. Оболочка 40 и игла для пункции пазухи 60 в комплексе показаны на фиг.6.
Оболочка 40 может быть изготовлена из биосовместимого полимера, такого как ПЕБАКС, и включает проксимальный участок оболочки 42 первого диаметра, дистальный участок оболочки 44 второго диаметра (меньше первого диаметра) и суженный ступенчатый сегмент 54 между проксимальным участком оболочки 42 и дистальным участком оболочки 44. На проксимальном конце (ПК) оболочки 40 находится раструб 46. По желанию на проксимальном участке оболочки 42 рядом с проксимальным концом (ПК) может быть предусмотрена визуально различимая маркирующая полоса 50. Также по желанию на дистальной части ствола 44 на расстоянии приблизительно 17 мм от дистального конца (ДК) может быть предусмотрена вторая визуально различимая маркирующая полоса 48. Также по желанию на дистальном участке оболочки 44 на определенном расстоянии друг от друга могут быть предусмотрены рентгеноконтрастные метки 52 и 56. В конкретном примере, представленном на чертеже, дистальная рентгеноконтрастная метка 56 размещается на расстоянии приблизительно 1,5 мм от дистального конца, а проксимальная рентгеноконтрастная метка 52 размещается на расстоянии приблизительно 17 мм от дистального конца (ДК) под дистальной кромкой визуально различимого маркера 48. Кроме того, в некоторых вариантах осуществления дополнительные крылья 53 могут расходиться в стороны от дистального участка оболочки 44 в области визуально различимого маркера 48. Эти дополнительные крылья 53 могут иметь конструкцию, по существу аналогичную конструкции удерживающих крыльев 18 описанного выше спейсерного устройства для доставки вещества 10. В вытянутом положении длина каждого крыла 53 составляет приблизительно 2 см. Дополнительные крылья 53, упираясь в стенки прилегающей анатомической структуры, ограничивают расстояние, на которое оболочка 40 может быть продвинута через отверстие или канал в полости тела. Оболочка 40 облегчает введение описанного выше спейсерного устройства для доставки вещества 10. Кроме того, оболочка 40 может использоваться отдельно для улучшения оттока гноя или для доставки лекарственных или диагностических веществ.
В варианте осуществления настоящего изобретения, представленном на фиг.5, игла для пункции пазухи 60 включает удлиненное изогнутое тело иглы 62 с острым троакаром-наконечником 63. Твердый не вращающийся проксимальный конец тела иглы 62 закреплен на ручке 64. Как показано на фиг.5A, для этого проксимальный конец тела иглы 62 сгибают под углом 90 градусов и запрессовывают его в ручку 64, в результате чего образуется надежное соединение, препятствующее вращению тела иглы 62 относительно ручки 64. В варианте осуществления настоящего изобретения, показанном на чертежах, тело иглы 48 изготовлено из проволоки из нержавеющей стали с внешним диаметром приблизительно 0,178 см (0,07 дюйма). Тело иглы 62 имеет изгиб 65. Длина тела иглы 62 составляет приблизительно 102 мм, а центральная точка изгиба 65 находится на расстоянии приблизительно 31 мм от дистального наконечника 63 тела иглы 62. Изгиб 65 образует угол А2, равный приблизительно 33 градусам. Данный конкретный вариант осуществления иглы для пункции пазухи 60, в частности, подходит для иглы для этмоидотомии, подробно описанной ниже, а изгиб 52 позволяет ввести дистальную часть тела иглы 62 через решетчатую буллу в полость воздухоносной ячейки, обеспечивая снижение риска случайной пенетрации примыкающего основания черепа, который защищает мозг пациента. Кроме того, как показано в увеличенном виде на фиг.5B и 5C, в данном примере троакар-наконечник 63 имеет три скошенные кромки, расположенные симметрично вокруг центральной оси ствола иглы, при этом каждая скошенная кромка располагается под углом В, равным приблизительно 20 градусам, относительно продольной оси тела иглы 62. Такая конструкция позволяет использовать иглу для пункции пазухи 60 для проникновения через мягкую ткань (например, слизистую оболочку), а также через тонкую кость (например, решетчатую буллу и другие костные структуры, разделяющие воздухоносные ячейки).
Ручка 64 включает прицельный элемент, такой как гребень 66, верхний удлиненный элемент 70 и нижний удлиненный элемент 68, присоединенный к верхнему удлиненному элементу и по существу параллельный ему. Ручка также может включать дистальную захватную часть 72. Вся ручка или часть ручки 64 может иметь эластомерное покрытие и(или) выемки, бороздки или такую структуру поверхности, которая обеспечивает надежный захват ручки 64 оператором.
Прицельное приспособление 66 выходит из ручки в плоскости, параллельной плоскости изгиба иглы 65, благодаря чему оператор имеет возможность визуально определять латеральное направление, в котором продвигается дистальная часть тела иглы 62, даже если дистальный конец тела иглы 62 находится в полости тела пациента, то есть вне прямого поля зрения оператора. Кроме того, верхняя кромка 67 вертикального прицельного приспособления 66 проходит параллельно и по существу совпадает с дистальной частью тела иглы 62, благодаря чему оператор имеет возможность визуально контролировать вертикальный наклон или траекторию, по которой продвигается наконечник иглы 63, даже если дистальный конец тела иглы 62 находится в полости тела пациента, то есть вне прямого поля зрения оператора.
На фиг.6 представлена оболочка или направляющая иглы 40, размещенная поверх тела иглы для пункции пазухи 62. Как показано на чертеже, длина оболочки иглы 40 такова, что, когда оболочка 40 полностью закрывает тело иглы 62, раструб 46 на проксимальном конце (ПК) оболочки 40 упирается в дистальную поверхность ручки 64, а дистальный наконечник 63 тела иглы 62 выступает за пределы дистального конца (ДК) оболочки 40. Оболочка 40 является достаточно гибкой и повторяет форму изгиба 65 тела иглы для пункции пазухи 62, как показано на чертеже. При необходимости для некоторых целей к верхнему удлиненному элементу 70 ручки 64 может быть прикреплен оптический или электрический компонент системы визуального контроля 74 (например, датчик, отражатель, источник света и т.д.), как показано на фиг.6, что позволяет использовать оптическую или электромагнитную систему визуального контроля способами, хорошо известными в хирургии уха, горла и носа, для определения и(или) контроля позиционирования наконечника иглы 63 в полости тела человека или животного.
В патентах США №№5314417 «Безопасный троакар» и 5267965 «Безопасный троакар», содержание которых полностью включено в настоящий документ путем ссылки, описаны безопасные механизмы, которые дополнительно могут использоваться совместно с иглой для пункции пазухи 60 и оболочкой 40.
В качестве альтернативы телу иглы 63 с острым наконечником, таким как троакар-наконечник 63, игла для пункции пазухи может включать другие приспособления для пенетрации ткани, позволяющие осуществить пенетрацию соответствующей ткани (например, тканей решетчатой пазухи, слизистой оболочки и кости). Другие подходящие для пенетрации ткани приспособления включают, помимо прочего, вращающиеся сверла, боры, биполярные или монополярные радиочастотные или электрокаутерные электроды, лазерные электроды и т.п. На фиг.5D и 5E показан пример альтернативного пенетратора пазухи 60a, конструкция которого аналогична конструкции иглы для пункции пазухи 60, описанной выше, за исключением того, что вместо нижнего удлиненного элемента 68 ручка имеет корпус 68a с размещенным внутри него электрическим двигателем (не показан) и кнопкой включения и выключения. Кроме того, в данном устройстве тело иглы 62 заменяет вращающийся бор в сборе, включающий удлиненную изогнутую трубку 62a с гибким вращающимся приводным валом 84, проходящим внутри нее, и вращающимся бором-наконечником 82, присоединенным к дистальному концу приводного вала 84, как показано на фиг.5E. Благодаря тому, что приводной вал 84 имеет гибкую структуру, он может принимать форму изгиба 65а трубчатого корпуса 62a, сохраняя при этом способность вращаться. Вращающийся бор-наконечник представляет собой алмазный бор-наконечник диаметром 0,6, 0,7 или 0,8 мм. Двигатель, приводной вал 84 и бор-наконечник 82 могут по существу не отличаться от компонентов, используемых в устройстве UltraburTM Fixed Tip Drill (производства Invotec International, Inc., Джексонвилль, Флорида).
В других альтернативных вариантах осуществления настоящего изобретения, в которых вместо иглы 62 используется лазерный электрод, световод волоконно-оптического лазера может проходить через электрод, а подходящий тип лазерного излучения доставляется через световод и выходит из дистального конца электрода, проходя требуемую анатомическую структуру насквозь. Одним из подходящих для пенетрации решетчатой буллы или других мягких тканей или костных структур околоносовых пазух лазеров является гальмиевый лазер (holmium:YAG). См. публикацию Metson, Ralph; Holmium:YAG Laser Endoscopic Sinus Surgery: A Randomized, Controlled Study; Laryngoscope; 106(1) Supplement 77:1-18 (январь 1996 г.).
Лечение этмоидального синусита путем этмоидотомии и имплантации спейсерного устройства с возможностью доставки вещества для долговременной доставки кортикостероидов
На фиг.7A-7K представлен способ применения вышеописанной иглы для пункции пазухи 60, оболочки 40 и устройства доставки вещества 10 для этмоидотомии с целью эффективного стентирования этмоидотомического канала и доставки терапевтического вещества (например, кортикостероида) в пазухи решетчатой кости в течение определенного периода времени после оперативного вмешательства.
Сначала, как представлено на фиг.7A, оболочку иглы 40 надевают на тело иглы 62, как представлено на фиг.6. В данном варианте осуществления внутренний диаметр проксимальной части оболочки 42 имеет достаточный размер, чтобы вместить ограничивающую оболочку 30 устройства доставки вещества (фиг.20-2E), хотя внутренний диаметр дистальной части оболочки 44 имеет такой же или меньший размер, чем внешний диаметр подвижной оболочки 30, тем не менее, он имеет достаточно большой размер, позволяющий пропустить резервуар 14 и удерживающие крылья 18 в сложенном положении.
Пациенту вводят анестезирующие или подходящие анальгезирующие (седативные) средства. Как показано на фиг.7A, тело иглы 62 с надетой на него оболочкой 40 проводят через носовое отверстие пациента вместе с эндоскопом 400, таким как Storz HopkinsTM II, угол обзора 0 градусов, автоклавируемый, 4×18 мм, с ксеноновым источником света Storz Xenon 300TM или Xenon NovaTM (производитель Karl Storz GmbH & Co., Тутлинген, Германия). Кроме того, в настоящем примере также может использоваться рентгеноскопический аппарат с С-образной дугой для обеспечения рентгеноскопической визуализации на некоторых этапах операции. Примером рентгеноскопического аппарата с С-образной дугой, пригодного для использования в этих целях, может служить доступная в продаже мобильная система цифровой визуализации OEC 9800 PlusTM Digital Mobile Imaging System (производитель G.E. OEC Medical Systems, Inc., Солт-Лейк-Сити, Юта). Оператор может убедиться в том, что дистальная часть тела иглы 62 имеет соответствующий вертикальный наклон и боковое направление, визуально контролируя прицельное приспособление 66 и его ведущую кромку 67. Под эндоскопическим контролем наконечник иглы 50 проталкивают через решетчатую буллу (РБ) и вводят в полость одной или нескольких воздухоносных ячеек решетчатой кости (ВЯРК). В данном варианте осуществления тело иглы для пункции пазухи 62 образует угол 65, приблизительно равный тридцати трем градусам, что позволяет проталкивать дистальный наконечник 63 по траектории, по существу параллельной (или в некоторых случаях равно отклоненной от) примыкающему основанию черепа (ОЧ). В связи с этим при выполнении операции у взрослого пациента изгиб 65 тела иглы для этмоидотомии 62 может иметь радиус приблизительно 1,905 см (0,75 дюйма) и образовывать угол А, равный приблизительно 33 градусам. Дистальная часть тела иглы 62 (т.е. часть, отходящая от изгиба 62 к дистальному наконечнику 63) имеет длину приблизительно 24 мм, что обеспечивает простоту маневрирования иглы с оболочкой в сборе и позволяет вводить ее вдоль эндоскопа 400, при этом эндоскоп 400 может располагаться над иглой с оболочкой в сборе или под ней. Тело иглы для этмоидотомии 62 выполнено из проволоки из нержавеющей стали диаметром 304 (0,185 см, или 0,073 дюйма) с измеренным пределом прочности (ASTM A313-03) в пределах приблизительно от 253852 до 258665 psi. В тех случаях, когда компонент системы визуализации 74 прикреплен к ручке 64 иглы для пункции пазухи 60, оператор дополнительно может использовать известные способы и аппараты оптической или электромагнитной визуализации для контроля перемещения тела иглы для пункции пазухи 62 относительно основания черепа (ОЧ) и других анатомических структур. Кроме того, необходимо тщательно контролировать глубину пенетрации, чтобы полностью не пенетрировать стенку клиновидной пазухи и не проникнуть в полость клиновидной пазухи (КП). Для того чтобы не повредить стенку клиновидной пазухи, хирург может выбрать оболочку 40. Расстояние между дистальным концом (ДК) оболочки 40 и проксимальной кромкой визуально различимого маркера 48 меньше расстояния между передней поверхностью решетчатой буллы (РБ) и стенкой клиновидной пазухи (КП). Затем дистальный визуально различимый маркер 48 на оболочке 40 визуализируется при помощи эндоскопа с целью измерения глубины проникновения в полость воздухоносных ячеек решетчатой кости. Продвижение следует остановить, когда проксимальный конец визуально различимого маркера 48 сравняется с решетчатой буллой (РБ), тем самым обеспечивая целостность стенки клиновидной пазухи. Кроме того, если оболочка 40 оснащена дополнительными крыльями 53, устройство можно продвигать до тех пор, пока крылья 53 не упрутся в переднюю поверхность решетчатой буллы (РБ). Также, как показано на фиг.18, дополнительный наружный ограничительный элемент 600 может быть прикреплен с использованием любого подходящего способа или приспособления, такого как клипса 602, зажим, адгезив, сцепление силами трения или иные способы, к оболочке 40 в том месте, где ограничительный элемент 600 упирается в нос пациента, препятствуя, тем самым, продвижению иглы 62 и оболочки 40 за пределы безопасного расстояния в полость пазух решетчатой кости. Расстояние между проксимальной и дистальной рентгенографическими метками 52 и 56 по существу равно длине резервуара 14. Такие метки 44 хорошо визуализируются при рентгеноскопии. Хирург может прибегнуть к рентгеноскопической визуализации для позиционирования меток 52 и 56, чтобы по местоположению этих меток можно было определить местоположения проксимального и дистального концов резервуара 14.
Как показано на фиг.7B, после установки оболочки 40 в необходимое положение иглу 49 выводят из установленной на месте оболочки 40, при этом проксимальный конец оболочки 40 выступает из носового отверстия пациента.
Перед введением спейсерного устройства для доставки вещества 10 врач при необходимости может оттянуть ограничивающую оболочку 30, оголив шовную петлю 20, пропустить отрезок 2-O или 3-O шовного материала 17 с прямой или изогнутой иглой 19 через шовную петлю и согнуть ее пополам. Затем ограничивающая оболочка 30 перемещается в выдвинутое положение, при этом противоположные концы согнутой пополам петли 17 выступают наружу за пределы проксимального конца ограничивающей оболочки 30, как показано на фиг.7C. После этого устройство для доставки вещества 10 со сложенным резервуаром и выдвинутой оболочкой 30 (как показано на фиг.2E) вводят в проксимальный конец оболочки иглы 40, как показано на фиг.7C.
Затем, как показано на фиг.7D, устройство для доставки вещества 10 с выдвинутой оболочкой 30 проталкивают через оболочку 40 в положение, в котором чувствуется небольшое сопротивление дальнейшему продвижению вследствие того, что дистальный конец ограничивающей оболочки 30 упирается в сужающуюся стенку внутренней поверхности суженного сегмента 54.
Затем, как показано на фиг.7E, хирург, прилагая усилие для преодоления сопротивления, перемещает ограничивающую оболочку 30 проксимально во втянутое положение (см. фиг.20) по мере того, как дистальная часть спейсерного устройства для доставки вещества 10, включая резервуар 14 в сложенном состоянии, продвигается в дистальную часть оболочки 42. Затем положение резервуара 14 внутри дистальной части оболочки 42 проверяют рентгеноскопией путем визуализации положения рентгенографической метки 24 на устройстве 10 относительно положения рентгенографических меток 44 на дистальной части оболочки 42. Кроме того, при помощи этих меток можно проверить фактическое положение резервуара 14 относительно окружающих его анатомических структур.
После этого, как показано на фиг.7F, оболочка 40 с содержащейся в ней ограничивающей оболочкой 30 может извлекаться в проксимальном направлении. Это позволит удерживающим крыльям 18 раскрыться, отскочив наружу, и зацепиться за прилегающие септальные стенки между воздухоносными ячейками решетчатой кости (ВЯРК) или - в альтернативном варианте - за внутреннюю поверхность стенки решетчатой буллы (РБ). Контроль размещения и фиксации удерживающих крыльев 18 может осуществляться рентгеноскопическим путем. Кроме того, это позволит раскрыть шовную петлю 20 в носовую полость рядом с решетчатой буллой (РБ). Благодаря тому, что шовная петля отличается по цвету от крови и слизистой оболочки, раскрытие шовной петли также можно контролировать с помощью рентгеноскопии.
После этого, как показано на фиг.7C, к проксимальному люэровскому соединительному элементу 16 спейсерного устройства для доставки вещества 10 присоединяют шприц, содержащий от 0,31 до 0,35 см3 суспензии триамцинолона ацетонида для инъекций (Кеналог®-40 производства Bristoi-Myers Squibb, Сомервилль, Нью-Джерси). Суспензию триамцинолона ацетонида для инъекций впрыскивают, заставляя резервуар 14 раскрываться. В некоторых вариантах осуществления настоящего изобретения ствол 12 спейсерного устройства для доставки вещества 10 может быть прозрачным, благодаря чему доставку вещества по просвету 13 можно контролировать при помощи эндоскопа 400.
Затем, как показано на фиг.7H, ствол 12 обрезают рядом с проксимальным люэровским соединительным элементом 16, и вместе с ним удаляют люэровскую втулку 16. Это позволяет удалить оболочку иглы для пункции пазухи 42 вместе с содержащейся в ней ограничивающей оболочкой 30, тем самым освобождая шовный материал 17 и иглу 19 для наложения шва на анатомическую структуру рядом с шовной петлей 20. В качестве альтернативы в некоторых вариантах осуществления настоящего изобретения оболочка 40 может быть оснащена продольной перфорацией или линией отрыва, которые позволяют легко оторвать и извлечь оболочку.
Как показано на фиг.7I, оболочка иглы для пункции пазухи 40 с содержащейся в ней ограничивающей оболочкой и шовным материалом 17 используется для прикрепления шовной петли 20 к прилежащей ткани, такой как слизистая (C) носовой перегородки или слизистая, покрывающая назальную поверхность решетчатой буллы (РБ).
Затем, как показано на фиг.7J, ствол 12 обрезают по метке 15 или дистальнее нее, а проксимальную часть ствола 12a удаляют.
Как показано на фиг.7K, в результате этой процедуры образуется этмоидотомический канал или отверстие, ведущее в одну или несколько воздухоносных ячеек решетчатой кости (ВЯРК), при этом резервуар 14, выделяющий вещество, и дистальный ствол 12b остаются на месте в течение определенного периода времени (например, в пределах от 1 часа до 90 дней, предпочтительно - в пределах от 7 до 29 дней, более предпочтительно - приблизительно 14 дней, в некоторых случаях - приблизительно 7 дней) после выполнения этмоидотомии. Кроме того, небольшое количество вещества остается в дистальном стволе 12b дистальнее того места, в котором ствол обрезают. Такое оставшееся вещество медленно вытекает из обрезанного конца дистального ствола 12b, воздействуя на прилегающие спиралевидные или иные соседние анатомические структуры в полости носа.
В данном примере с пазухами решетчатой кости дистальная часть 44 оболочки иглы для пункции пазухи 40 изготовлена из нейлона, ее внешний диаметр составляет 0,221 см (0,087 дюйма), внутренний диаметр составляет 0,191 см (0,075 дюйма), а длина равна 25 мм. Переходный суженный сегмент 54 имеет длину приблизительно 5 мм и сужается, переходя от внешнего диаметра 0,264 см (0,104 дюйма) и внутреннего диаметра 0,224 см (0,088 дюйма) на проксимальном конце к внешнему диаметру 0,234 см (0,092 дюйма) и внутреннему диаметру 0,191 см (0,075 дюйма) на дистальном конце. Проксимальная часть ствола 42 изготовлена из нейлона 12, ее внешний диаметр составляет 0,259 см (0,102 дюйма), внутренний диаметр составляет 0,224 см (0,088 дюйма), а длина равна 8,89 см (3,5 дюйма). Дистальная и Проксимальная метки 44 выполнены в форме колец из платиноиридиевого сплава с внешним диаметром 0,221 см (0,087 дюйма) и внутренним диаметром 0,216 см (0,085 дюйма). Дистальная метка 44 располагается на расстоянии 1 мм от дистального конца (ДК) оболочки иглы 134. Проксимальная метка 148 располагается на расстоянии 18 мм от дистального конца оболочки иглы 40. Общая длина оболочки иглы 40 составляет 115 мм.
Несмотря на то, что варианты, представленные на фиг.7A-7K, предназначены для лечения этмоидита, система устройств, изображенных на фиг.3A-3L, также может использоваться для формирования пенетрационных каналов или отверстий (например, антростомических отверстий и т.д.) в различных околоносовых пазухах или иных анатомических структурах, а также для размещения спейсерного устройства для доставки вещества 10 внутри таких пенетрационных каналов или отверстий. Кроме того, спейсерное устройство для доставки вещества 10 может использоваться отдельно от иглы для пункции пазухи 60 в различных устьях, отверстиях, разрезах или проходах организма и функционировать исключительно в качестве спейсера и(или) устройства для доставки необходимо диагностического или терапевтического вещества. При лечении заболеваний околоносовых пазух доставка стероидов, таких как Кеналог®-40 (суспензия триамцинолона ацетонида для инъекций. Фармакопея США), в околоносовую область, а именно в полость пазух решетчатой кости, осуществляется при помощи устройства 10.
Имплантируемое устройство 10 предпочтительно используется для доставки жидкостей или суспензий с низким поверхностным натяжением. Жидкости с низким поверхностным натяжением легко рассеиваются по поверхности. Это особенно полезно для доставки веществ к поверхности большой площади, особенно в таких анатомических областях, как пазухи решетчатой кости, имеющие сложную трехмерную геометрию. В одном из вариантов осуществления настоящего изобретения жидкость с низким поверхностным натяжением представляет собой поверхностно-активное вещество. В одном из вариантов осуществления способа, составляющего предмет настоящего изобретения, оросительная жидкость с низким поверхностным натяжением, содержащая одно или несколько веществ, доставляется в полость пазух решетчатой кости. В некоторых вариантах осуществления настоящего изобретения по существу инертная жидкость, такая как физиологический раствор, доставляется для увлажнения окружающих тканей, а устройство может выполнять разделительную и(или) дренажную (вентилирующую) функцию. В других вариантах осуществления настоящего изобретения доставка активного вещества, такого как лекарственное или диагностическое вещество, может производиться наряду с выполнением разделительной и(или) дренажной (вентилирующей) функций имплантируемым устройством 10.
В некоторых случаях спейсерное устройство для доставки вещества 10 может быть имплантировано в отверстия (например, естественные устья, отверстия, измененные хирургическим путем, или иные искусственные отверстия) околоносовых пазух с целью лечения синусита или заболеваний, поражающих околоносовые пазухи. В таких случаях отверстие околоносовой пазухи может быть увеличено (например, расширено) перед размещением устройства 10 и 104, составляющих предмет настоящего изобретения, либо после размещения такого устройства. Одной из таких процедур по увеличению устья полости пазухи является баллонная дилатация. Во время такой процедуры катетер-направляющую, имеющую по существу неизменяемую форму, вводят через носовое отверстие и продвигают к местоположению, в котором дистальный конец катетера-напрвляющей располагается рядом с устьем околоносовой пазухи. Затем по направляющей (например, катетер-направляющей Relieve™ производства Acclarent, Inc., Менло-Парк, Калифорния) вводят проволочный направитель и продвигают в полость околоносовой пазухи. После этого по проволочному направителю вводят баллонный катетер (например, баллонный катетер Relieva™ производства Acclarent, Inc., Менло-Парк, Калифорния) для расширения устья околоносовой пазухи для улучшения оттока из полости околоносовой пазухи и(или) ее вентиляции. Примеры таких устройств и процедур баллонной дилатации устья околоносовой пазухи описаны в заявках на патент США №№10/829917 «Устройства, системы и способы диагностики и лечения синусита и других заболеваний уха, горла и носа», 10/944270 «Аппарат и способы дилатации и изменения отверстий околоносовых пазух и других внутриносовых и околоносовых структур», 11/116118 «Способы и устройства выполнения операций в полости уха, горла, носа и околоносовых пазух», 11/150847 «Устройства, системы и способы, используемые для лечения синусита» и 11/234395 «Устройства и способы доставки терапевтических веществ для лечения синусита и других заболеваний», содержание каждой из которых в явной форме включено в настоящий документ путем ссылки.
Лечение фронтального синусита путем баллонной дилатации выводных протоков лобных пазух и имплантации спейсерного устройства с возможностью продолжительной доставки кортикостероидов
На фиг.8A-8C представлен пример осуществления одного из способов размещения спейсерного устройства для доставки вещества 10 в выводном протоке лобной пазухи (ВПЛБ) с целью стентирования и доставки вещества после баллонной дилатации выводного протока лобной пазухи (ВПЛБ).
Во время операции осуществляется введение эндоскопа 400. При необходимости для рентгеноскопической визуализации может использоваться рентгеноскоп с С-образной дугой (не показан). Несмотря на то, что для ясности и простоты зрительного восприятия эндоскоп 400 показан только на фиг.8A-8B, такой эндоскоп 400 может оставаться на месте в течение всей операции или во время отдельного этапа операции и использоваться для визуализации перемещений и манипуляций, производимых с помощью устройств, в режиме реального времени, как описано в настоящем примере.
Под эндоскопическим визуальным контролем катетер-направляющую для лобной пазухи 500 (например, катетер-направляющую с наклоном 70 градусов Relieva® производства Acclarent, Inc., Менло-Парк, Калифорния) проводят через носовое отверстие таким образом, что ее дистальный конец размещен в устье лобной пазухи (УЛП) или рядом с ним. Позиционирование катетера-направляющую 500 можно контролировать путем эндоскопической визуализации и рентгеноскопии.
Затем проволочный направитель (ПН) (проволочный направитель для пазухи Relieva® производства Acclarent, Inc., Менло-Парк, Калифорния) продвигают по катетеру-направляющей 500 в полость лобной пазухи (ЛП), как показано на фиг.8A. Чтобы убедиться в том, что проволочный направитель (ПН) свернут в кольцо и находится в полости лобной пазухи (ЛП), можно использовать рентгеноскоп 404.
Затем, как показано на фиг.8B, по проволочному направителю (ПН) через катетер-направляющую (КП) 500 вводят дилатационный катетер 502 (например, баллонный катетер Relieva® или Relieva XL производства Acclarent, Inc., Менло-Парк, Калифорния) и размещают таким образом, чтобы дилатационный баллон 504 находился в устье лобной пазухи (УЛП). Чтобы убедиться в том, что проволочный направитель (ПН) свернут в кольцо и находится в полости лобной пазухи (ЛП), можно использовать рентгеноскоп 400. В таком положении дилататора 504 дилатационный баллон 504 растягивается, обеспечивая расширение устья лобной пазухи (УЛП) или другого выводного протока лобной пазухи. Процедура подробно описана в находящейся на одновременном рассмотрении заявке на патент США с серийным №11/355512, содержание которой полностью и в явной форме включено в настоящий документ. После дилатации баллон 504 сжимают и дилатационный катетер 502 извлекают, при этом проволочный направитель 504 остается на месте. Несмотря на то, что данный пример включает этап дилатации устья лобной пазухи (УЛП), этот этап является необязательным. У некоторых пациентов устье пазухи может быть уже расширено или изменено в результате предыдущих хирургических вмешательств или, по заключению врача, может отсутствовать необходимость в дилатации устья перед введением спейсерного устройства 10.
Затем спейсерное устройство для доставки вещества 10 подготавливают и вводят через катетер-направляющую 500 в полость лобной пазухи (ЛП). Перед введением устройства 10 в катетер-направляющую 500 можно снять ограничивающую трубку 42 и вручную провернуть вперед (т.е. в дистальном направлении) удерживающие крылья 18, слегка надавив на спейсерное устройство 10 во время его введения в проксимальный конец катетера-направляющей 500. Как только дистальный конец спейсерного устройства выдвинется за пределы дистального конца катетера-направляющей 500, удерживающие крылья 18 расправятся и закрепятся в устье лобной пазухи (УЛП), как показано на фиг.8C. Позиционирование резервуара 14 в полости лобной пазухи и раскрытие удерживающих крыльев 18 может контролироваться путем рентгеноскопии.
Затем, как показано на фиг.8D, к проксимальному люэровскому соединительному элементу спейсерного устройства для носовой пазухи 10 присоединяют шприц, содержащий от 0,31 до 0,35 см3суспензии триамцинолона ацетонида для инъекций (Кеналог®-40 производства Bristol-Myers Squibb, Сомервилль, Нью-Джерси). Суспензию триамцинолона ацетонида для инъекций впрыскивают, заставляя резервуар 14 раскрываться. Контроль раскрытия резервуара 14a может осуществляться с помощью компьютерной томографии.
Затем, как показано на фиг.8E и 8F, проксимальный конец спейсерного устройства для носовой пазухи 10 обрезают, катетер-направляющую втягивают в проксимальном направлении и извлекают из полости тела. Оператор может ухватить ствол 12 спейсерного устройства дистальнее дистального конца катетера-направляющей 500, чтобы при извлечении катетера-направляющей 500 стабилизировать спейсерное устройство 10 и избежать его нежелательного смещения из положения в полости лобной пазухи (ЛП).
Затем проксимальную часть ствола 12 спейсерного устройства 10 обрезают, при этом остается короткий участок ствола 12, размещенный в полости носа. Для прикрепления конца шовной петли 20 спейсерного устройства 10 к ткани в полости носа используется шовный материал 17 с прямой иглой 19, благодаря чему имплантированная часть спейсерного устройства 10 удерживается в необходимом положении в течение определенного периода времени после операции. Небольшое количество вещества сохраняется в оставшемся сегменте ствола 12 дистальнее среза и может попадать в носовую полость после операции, снабжая, таким образом, и другие структуры в носовой полости лекарственным препаратом.
Лечение фронтального синусита путем имплантации спейсерного устройства с возможностью продолжительной доставки кортикостероидов
В данном примере на фиг.9A-9D представлены этапы другого способа лечения фронтального синусита у взрослых пациентов. Устье лобной пазухи (УЛП) может оставаться неизменным или может быть изменено или расширено в результате предыдущих хирургических вмешательств, как описано выше. Под эндоскопическим визуальным контролем катетер-направляющую для лобной пазухи 500 (например, катетер-направляющую с наклоном 70 градусов Relieva® производства Acclarent, Inc., Менло-Парк, Калифорния) проводят через носовое отверстие таким образом, что его дистальный конец размещен в устье лобной пазухи (УЛП) или рядом с ним. Позиционирование катетера-напрвляющей 500 можно контролировать путем эндоскопической визуализации и рентгеноскопии.
Затем проволочный направитель (ПН) (проволочный направитель для пазухи Relieva® производства Acclarent, Inc., Менло-Парк, Калифорния) продвигают по катетеру-направляющей 500 в полость лобной пазухи (ЛП), как показано на фиг.9А. Чтобы удостовериться в том, что проволочный направитель (ПН) свернут в кольцо и находится в полости лобной пазухи (ЛП), можно использовать рентгеноскоп 404.
Как показано на фиг.9B, после введения проволочного направителя (ПН) в полость лобной пазухи катетер-направляющую для лобной пазухи 500 извлекают, а проволочный направитель (ПН) при этом остается на месте. Сосудистый дилататор 5 F 420 (например, сосудистый дилататор 5 F (внутренний диаметр равен 0,965 мм (0,038 дюйма)) производства Merritt Medical Systems, Inc., Саут-Джордан, Юта). Затем оболочку вместе с дилататором продвигают по проволочному направителю (ПН). Для контроля продвижения и установки оболочки с дилататором в положение, в котором проксимальная рентгенографическая метка 52 оболочки 40 располагается дистальнее лобного кармана (т.е. в полости лобной пазухи), может использоваться рентгеноскоп с С-образной дугой и(или) эндоскоп 400. После того как оболочка 40 достигает этого положения, находясь внутри просвета дилататора, дилататор 5F 420 и проволочный направитель (ПН) извлекают, при этом оболочка 40 остается на месте, как показано на фиг.9C.
Затем спейсерное устройство для доставки вещества 10 подготавливают соответствующим образом, как описано выше, ограничивающую трубку 30 устанавливают в выдвинутое положение, закрывая и удерживая шовную петлю 20, удерживающие крылья 18 и резервуар 14 в сложенном состоянии. Устройство 10 вставляют в предварительно введенную оболочку 40 и продвигают по существу таким же образом, как описано выше и показано на фиг.8C-8E.
После этого оболочку 40 и ограничивающую трубку 30 втягивают, и к проксимальному люэровскому соединительному элементу спейсерного устройства для доставки препарата для носовой пазухи 10 подсоединяют шприц, содержащий от 0,31 до 0,35 см3 суспензии триамцинолона ацетонида для инъекций (Кеналог®-40 производства Bristol-Myers Squibb, Сомервилль, Нью-Джерси). Суспензию триамцинолона ацетонида для инъекций впрыскивают, заставляя резервуар 14 растягиваться в полости лобной пазухи (ЛП), как было описано ранее. При необходимости контроль раскрытия резервуара 14a может осуществляться с помощью компьютерной томографии.
Затем проксимальный конец спейсерного устройства для носовой пазухи 10 обрезают, оболочку 40 и ограничивающую трубку 30 втягивают в проксимальном направлении и извлекают из полости тела, как описано выше и показано на фиг.8F-8C.
После этого проксимальную часть ствола 12 спейсерного устройства 10 обрезают, при этом остается короткий участок ствола 12, расположенный в полости носа. Для прикрепления кончика шовной петли 20 спейсерного устройства 10 к ткани в полости носа используется шовный материал 17 с прямой иглой 19, благодаря чему имплантированная часть спейсерного устройства 10 удерживается в необходимом положении в течение соответствующего периода времени после операции, как показано на фиг.9D. Как было описано выше, небольшое количество суспензии триамцинолона ацетонида сохраняется в оставшемся сегменте ствола 12 дистальнее среза и может попадать в носовую полость (НП) после операции, снабжая, таким образом, ткани этой области лекарственным препаратом.
Альтернативный подход к лечению фронтального синусита
На фиг.10A представлен вариант осуществления системы для доставки вещества 500, предназначенной для доставки веществ в лобные околоносовые пазухи. В одном из вариантов осуществления настоящего изобретения система 500 может включать устройство для доставки вещества 510, включающее спейсер для носовой пазухи 511, оболочку 530, покрывающую спейсер для носовой пазухи 530 перед началом процесса доставки и частично в течение процесса доставки, и направляющее устройство 540, по которому спейсер 511 направляется в полость лобной околоносовой пазухи. Каждое из перечисленных устройств будет подробно рассмотрено ниже. В некоторых вариантах осуществления настоящего изобретения система 500 также может включать шприц (не показан) или другое инъекционное устройство для введения вещества (жидкости), соединенное с проксимальным концом устройства для доставки вещества 510 для введения вещества (жидкости) через устройство 510 в спейсер 511. Некоторые варианты осуществления настоящего изобретения также могут содержать некоторое количество вещества, предварительно введенного в шприц, включая, помимо прочего, вещества, перечисленные в настоящем документе. При необходимости некоторые варианты осуществления настоящего изобретения также могут включать рукоятку (не показана), присоединяемую к направляющему устройству 540, которая облегчает манипулирование и введение устройства направляющей 540 в носовое отверстие пациента. В альтернативных вариантах осуществления настоящего изобретения могут использоваться любые подходящие рукоятки, например, в одном из вариантов осуществления изобретения может использоваться рукоятка для катетера-направляющей Relieva Sidekick™ (производства Acclarent, Inc., Менло-Парк, Калифорния).
На фиг.10B-10E детально показаны устройство для доставки вещества 510 и имплантируемый спейсер для носовой пазухи 511, представленный на фиг.10A. Устройство 510 включает удлиненный гибкий ствол катетера 512, имеющий проксимальную часть 512a и дистальную часть 512b, при этом дистальная часть 512b является неотъемлемой частью спейсера для носовой пазухи 511. Как и в ранее описанных вариантах осуществления настоящего изобретения, проксимальная и дистальная части 512a и 512b могут быть отделены друг от друга, например, путем разрезания в месте соединения 515 или рядом с ним. В представленном варианте осуществления изобретения проксимальная часть ствола 512a является непрозрачной, а дистальная часть ствола 512b является относительно светопроницаемой или прозрачной. Таким образом, во время операции место соединения 515 хорошо визуализируется при помощи эндоскопа. Кроме того, проксимальная часть ствола 512a и дистальная часть ствола 512b могут быть изготовлены из различных материалов и могут иметь одинаковые или разные размеры (диаметр, толщина стенки и т.д.). Например, одним из таких материалов является полиамид. В некоторых вариантах осуществления настоящего изобретения дистальная часть ствола 512b может быть изготовлена из более гибкого биосовместимого материала, такого как нейлон или полиэтилентерефталат (ПЭТ). По центру ствола 512 проходит просвет. Кроме того, дистальная часть ствола 512a может постепенно сужаться или постепенно уменьшаться в диаметре по сравнению с проксимальной частью ствола, что облегчает введение устройства. На дистальном конце просвета может быть установлена заглушка. Заглушка может быть выполнена в виде любого подходящего закрывающего элемента, например, в виде стенки закрытого конца трубки, колпачка, массы, заполняющей конец просвета или в виде любого другого элемента, способного блокировать поток жидкости.
Как правило, спейсер для носовой пазухи 511 включает дистальную часть ствола 512b, растяжимый резервуар 514, установленный на дистальной части ствола 512b рядом с ее дистальным концом, складные удерживающие элементы 518 для удержания спейсера 511 в полости пазухи и шовную петлю 517, позволяющую хирургу прикрепить спейсер 511 к слизистой оболочке для дополнительной фиксации спейсера 511 в необходимом положении. Как правило, спейсер для носовой пазухи 511 может иметь любые подходящие размеры, свойства, количество каналов (отверстий) в резервуаре, любое количество удерживающих элементов 518 любого размера и формы и т.д. Многие из таких свойств и компонентов уже были описаны выше. Некоторые различия между спейсером для лобной пазухи 511 и описанным выше спейсером для пазух решетчатой кости приведены ниже. Размах крыла удерживающих элементов 518, измеренный по длине размаха в растянутом состоянии, составляет приблизительно 13-16 мм у спейсера для лобной пазухи 511 и приблизительно 9-12 мм у спейсеров для пазух решетчатой кости. Каждый удерживающий элемент 518 в растянутом состоянии образует угол относительно ствола 512, равный приблизительно 70 градусам, а у спейсеров для пазух решетчатой кости этот угол равен 80 градусам. Кроме того, общая длина спейсера для лобной пазухи 511 (а именно, прозрачной дистальной части ствола 512b) составляет приблизительно 65+/-3 мм и приблизительно 50+/-3 мм у спейсеров для пазух решетчатой кости. Разумеется, эти особенности характерны для одного из вариантов осуществления спейсера для лобной пазухи 511; различные альтернативные варианты осуществления могут предусматривать другие размеры.
Резервуар 514 растягивается по мере наполнения. Резервуар 514 может быть изготовлен из любого подходящего биосовместимого материала, а в некоторых вариантах осуществления изобретения может быть выполнен в виде баллона, изготовленного из неподатливого или полуподатливого материала, такого как нейлон 12. Резервуар может иметь множество отверстий и конструкцию, как показано на фиг.2A и 2B. Более того, как было указано выше, материал и толщина стенки резервуара предпочтительно должны обеспечивать достаточную гибкость резервуара, чтобы a) избежать серьезных травм при извлечении и удалении устройства из полости тела, b) предотвратить единовременное высвобождение всего содержимого резервуара, c) поддерживать постоянный размер отверстий 531 при раскрытии резервуара.
Как описано ниже, резервуар 514 вводят в устье лобной пазухи или выводной проток в сложенном состоянии, затем резервуар заполняют необходимым веществом, что обеспечивает растяжение резервуара.
В некоторых вариантах осуществления настоящего изобретения резервуар 514 не используется для доставки терапевтического вещества. Он может использоваться в качестве объемного устройства. В таких случаях резервуар 514 in situ заполняют физиологическим раствором или другой инертной жидкостью, вследствие чего резервуар 514 растягивается и плотно прилегает к анатомической структуре (анатомическим структурам) и удерживается силой трения в месте имплантации. Для этих целей резервуар 514 также может иметь утолщения на поверхности резервуара.
Резервуар 514 в сложенном состоянии может иметь относительно небольшой диаметр, что существенно облегчает его введение и извлечение. В тех вариантах осуществления настоящего изобретения, в которых резервуар 514 выполнен из неподатливого или полуподатливого материала, резервуар 514 не подвергается существенной упругой деформации в процессе заполнения, таким образом, он не оказывает давления на содержимое с целью изгнания вещества через отверстия 531. Вещество, содержащееся в резервуаре 514, вытесняется через отверстия 531 под действием силы тяжести или путем взаимодействия со слизью или кровью, постоянно перемещаемыми реснитчатым эпителием в полости околоносовых пазух. Такой способ доставки, не предполагающий применения избыточного давления, позволяет добиться медленного выделения вещества в течение нескольких дней. В других вариантах осуществления настоящего изобретения резервуар 514 может быть выполнен из деформируемого или эластичного материала с небольшими отверстиями 531. Материал, из которого выполнен баллон 514, сжимается по мере высвобождения вещества через отверстия 531, тем самым поддерживая давление внутри баллона. Кроме того, в данном примере резервуар имеет цилиндрическую боковую стенку 514a, которая определяет рабочую длину резервуара, дистальную сужающуюся часть 514b, переходящую от цилиндрической боковой стенки 514a к дистальному стволу 512b (дистально по отношению к резервуару), и проксимальную сужающуюся часть 514c, переходящую от цилиндрической боковой стенки 514a к дистальному стволу 512b (проксимально по отношению к резервуару), и отверстия 531, размещенные на проксимальной и дистальной сужающихся частях 514b и 514c, как показано на чертежах. Резервуар 514 может иметь такие же размеры, отверстия и конструкцию, как описано выше применительно к другим вариантам осуществления настоящего изобретения.
В одном из вариантов осуществления настоящего изобретения дистальная часть ствола 512b может быть изготовлена из нейлона 12. Как было указано выше, в одном из вариантов осуществления настоящего изобретения общая длина спейсера для носовой пазухи 511 от дистального конца до проксимального конца дистальной части ствола 512b составляет приблизительно 65 мм+/-3 мм. В стволе катетера 512 предусмотрено отверстие для более удобного заполнения резервуара 514. Кроме того, может быть предусмотрен клапан для прохождения вещества (или компонента (компонентов) вещества) из просвета ствола катетера 12 в резервуар 514 и предотвращения по существу обратного тока из резервуара 514 в просвет 513. Клапан может быть выполнен в виде обратного клапана любого типа.
Также может быть предусмотрена дистальная рентгеноконтрастная метка 524 и проксимальная рентгеноконтрастная метка 522, которые облегчают позиционирование резервуара 514 в полости тела пациента. Каждая из этих меток 522 и 524 может быть выполнена в виде кольца из рентгеноконтрастного материала и установлена на стволе 512 на одной оси с обоими концами цилиндрической боковой стенки 514a резервуара. Например, каждая метка 522 и 524 может быть выполнена в виде кольца из платиноиридиевого сплава. Метки видны при использовании любого способа визуализации, включая рентгеноскопию и компьютерную томографию.
В одном из вариантов осуществления настоящего изобретения проксимальная часть ствола 512a может быть выполнена из полиимидной трубки. Втулка 516, включающая охватывающий люэровский соединительный элемент, изготовленный из прозрачного поликарбоната, присоединена к проксимальному концу ствола 512. Проксимальная часть ствола 512a и дистальная часть ствола 512b, как правило, могут быть любого размера, иметь любые свойства, быть изготовлены из любых материалов и т.д., характерных для подобных стволов катетеров, описанных выше применительно к другим вариантам осуществления настоящего изобретения. В одном из вариантов осуществления настоящего изобретения проксимальная часть ствола 512a может включать маркер ствола 513. Маркер ствола 513 может быть размещен вдоль ствола 512 так, что когда дистальный конец маркера ствола 513 достигает проксимального конца ограничителя 531 на оболочке 530 во время продвижения (подробно описано ниже), дистальный конец спейсера для носовой пазухи 511 приближается к дистальному концу устройства направляющей 540. Когда проксимальный конец маркера ствола 513 достигает проксимального конца ограничителя 531, спейсер для носовой пазухи 511 выдвигается за пределы дистального конца направляющей 540. Использование маркера ствола в процессе размещения спейсера для носовой пазухи подробно описано ниже со ссылкой на фиг.13A-13H.
Кроме того, имплантируемое устройство для доставки вещества или спейсер 510 может иметь пару удерживающих крыльев 518. Необходимо отметить, что в альтернативном варианте осуществления спейсер 510 может иметь три или четыре таких крыла. Удерживающие крылья 518 расположены в диаметрально противоположных точках ствола 512 и проходят дистально относительно резервуара 514. Каждое удерживающее крыло 518 представляет собой сформированную петлю из никель-титановой (нитиноловой) проволоки. Каждое удерживающее крыло 518 может сгибаться или складываться в сложенном состоянии устройства, в котором оно по существу прижато к внешней поверхности резервуара 514. Удерживающие крылья 518 перемещаются в заранее сформированную конфигурацию так, что при условии отсутствия ограничений каждое удерживающее крыло 518 упруго отскакивает наружу в вытянутое положение, в котором оно выступает под углом приблизительно от 20 до 90 градусов относительно продольной оси ствола 512, в более предпочтительном варианте этот угол равен 70 градусов. В различных вариантах осуществления настоящего изобретения крылья 518 образуют размах, равный от приблизительно 9 до приблизительно 20 мм или более, более предпочтительно - от приблизительно 13 до приблизительно 16 мм, а в одном из вариантов осуществления настоящего изобретения - приблизительно 15 мм. В одном из вариантов осуществления настоящего изобретения дистальный конец спейсерного устройства 511 может быть снабжен атравматическим наконечником, изготовленным из мягкого полимера. Кроме того, в некоторых вариантах осуществления настоящего изобретения геометрия и размещение крыльев 518 могут быть подобраны таким образом, что лекарственный препарат, помещенный в резервуар 514, выделяется через отверстия 531, расположенные проксимальнее и дистальнее крыльев 518. В альтернативном варианте осуществления настоящего изобретения крылья 518 могут располагаться вдоль ствола 512 так, что все отверстия 531 находятся дистально относительно крыльев 518.
Как показано на фиг.10D и 10E, трубчатая ограничивающая оболочка 530 может размещаться поверх ствола 512 имплантируемого устройства для доставки вещества 510. Например, в одном из вариантов осуществления настоящего изобретения такая ограничивающая оболочка 530 может быть выполнена в виде сегмента пластиковой трубки длиной приблизительно 75+/-2 мм (хотя в альтернативных вариантах осуществления настоящего изобретения могут использоваться сегменты другой длины). Ограничивающая оболочка 530 может перемещаться между втянутым положением (см. фиг.10D) и вытянутым положением (см. фиг.10E). В вытянутом положении ограничивающая оболочка накрывает удерживающие крылья 518 и сложенный резервуар 514, таким образом фиксируя удерживающие крылья 18 в сложенном состоянии и образуя гладкое защитное покрытие. В вытянутом положении ограничивающая оболочка 530 повышает прочность на сжатие всего устройства 510 и препятствует сгибанию ствола 512 при проталкивании через относительно узкие и(или) извитые анатомические проходы. После введения и установки устройства 510 в требуемом положении ограничивающая оболочка 512 перемещается во втянутое положение, позволяя, таким образом, удерживающим крыльям 518 вытягиваться, а резервуару 514 растягиваться в процессе его заполнения веществом.
В одном из вариантов осуществления настоящего изобретения оболочка 530 имеет проксимальный ограничитель 531. Ограничитель 531 упирается в проксимальный люэровский адаптер на устройстве направляющей 540 по мере продвижения оболочки 530 и устройства для доставки вещества 510 по направляющей 540. Таким образом, по мере продвижения оболочки 530 и устройства для доставки вещества 510 ограничитель 531 препятствует продвижению оболочки 530, в то время как устройство для доставки вещества 510 продолжает двигаться вперед. Таким образом, спейсер для носовой пазухи выходит из дистального конца направляющей 540. Иными словами, оболочка 530 с ограничителем 531 удерживают крылья 518 спейсера для носовой пазухи 511 перед введением устройства в полость тела пациента и в процессе введения до того момента, пока спейсер 511 не выходит из дистального конца направляющей 540.
Оболочка 530 также может иметь конусообразный или скошенный дистальный наконечник 532. Такая форма скошенного дистального наконечника 532 упрощает втягивание спейсера для носовой пазухи 511 назад в оболочку 530, если это необходимо в ходе операции. Наконечник 532 также облегчает продвижение оболочки 530 в направляющей 540.
Дополнительные альтернативные варианты осуществления имплантируемого устройства для доставки вещества представлены на фиг.11A-11D. В одном из вариантов осуществления, как показано на фиг.11A, имплантируемое устройство 510 может включать пару удерживающих крыльев 521 и 523 в виде петель, расположенных в шахматном порядке по корпусу устройства. Например, одно крыло 521 может быть прикреплено вдоль одной стороны устройства рядом с местом соединения резервуара 514 и ствола 512, а второе крыло 523 может быть прикреплено к стволу 512 проксимальнее первого крыла 518. При таком размещении крыльев нижнее крыло 523 упирается в стенку лобного кармана (прохода, ведущего в лобную пазуху и расположенного проксимальнее нее), тем самым поддерживая верхнее крыло 521 в требуемом положении в полости лобной пазухи. В другом варианте осуществления (см. фиг.11B) крылья 521 и 523 могут быть прикреплены в шахматном порядке вдоль одной стороны имплантируемого устройства для доставки вещества 510. В другом варианте осуществления изобретения (см. фиг.11C и 11D), помимо расположенных диаметрально противоположно крыльев 518, идущих вдоль периферии резервуара 514, имплантируемое устройство 510 может иметь нижнее крыло 525, которое может иметь различные конфигурации, например, L-образную (фиг.11D) или S-образную (фиг.11C). Кроме того, упругость и геометрия нижнего крыла 525 позволяет ему, опираясь на стенку лобного кармана, проталкивать ствол 512 устройства вбок. Боковые крылья обеспечивают улучшенную фиксацию устройства для доставки вещества 510 в полости лобного кармана (лобной пазухи).
На фиг.12A-D показаны различные варианты осуществления оболочки или направляющей 540. Направляющие 540 выполнены с возможностью введения имплантируемого устройства, например, описанного выше, в полость лобного кармана и (или) лобной околоносовой пазухи, как показано, например, на фиг.13A-13E. Как правило, направляющая 540 может включать проксимальную прямую часть 542, дистальную изогнутую часть 544 с рентгеноконтрастным дистальным наконечником 545 и проксимальный люэровский соединительный элемент 546. В одном из вариантов осуществления настоящего изобретения направляющая 540 может быть изготовлена из полимера и выполнена в виде трубки с изогнутой дистальной частью 544 и проксимальной частью 542, покрытой прямой гипотрубкой. В одном из вариантов осуществления настоящего изобретения изогнутая дистальная часть 544 может обладать относительной гибкостью, что позволяет вводить ее в носовую полость, не повреждая при этом стенки носовой полости и внутриносовых структур. Общая длина, угол изгиба и конфигурация направляющей 540 могут быть такими, что проксимальный люэровский соединительный элемент 546 остается снаружи, тогда как направляющая 540 проходит через носовое отверстие и носовую полость, а его дистальный конец 545 размещается рядом с устьем лобной околоносовой пазухи или внутри него.
В некоторых вариантах осуществления настоящего изобретения оболочка или направляющая 540 может иметь деформируемую (гибкую, податливую и тому подобное) дистальную часть или наконечник, легко адаптируемый к анатомической структуре пациента. Наконечник может иметь предварительно заданную форму с определенной кривизной, однако при необходимости форму наконечника может задавать пользователь. Материалом для наконечника может являться гибкая или податливая трубка, сохраняющая форму и пригодная для многократного формования (при необходимости). Например, в одном из вариантов осуществления настоящего изобретения в качестве подходящего материала может быть выбран пластик с проволочной оплеткой 527 (см. фиг.12B) или пружина 529 (см. фиг.12C). Кроме того, этот элемент конструкции может быть заключен в оболочку из пластика (см. фиг.12D-E), или элемент конструкции может обрамлять пластиковый элемент (см. фиг.12B-C). В качестве подходящего материала также может использоваться податливый металл. Таким образом, если невозможно использовать наконечник оболочки или направляющей с предварительно заданной формой, то пользователь может самостоятельно придать наконечнику необходимую форму, для того чтобы ввести его через лобный карман в полость лобной пазухи.
На фиг.13A-H представлен другой способ лечения фронтального синусита. Для ясности способ по данному варианту осуществления показан без использования рукоятки, соединенной с направляющей 540, однако в альтернативных вариантах осуществления настоящего изобретения рукоятка (как описано выше) может быть присоединена к направляющей 540 перед началом введения устройства.
В некоторых вариантах осуществления настоящего изобретения после соответствующей, как описано выше, подготовки устройства для доставки вещества 510 ограничивающая оболочка 530 переводится в выдвинутое положение, в котором она ограничивает и покрывает удерживающие крылья 518 и резервуар 514 в сложенном состоянии. В альтернативных вариантах осуществления настоящего изобретения оболочка 530 и устройство для доставки вещества 510 поставляются в готовом к использованию виде.
Как показано на фиг.13A, под эндоскопическим визуальным контролем катетер-направляющую 540 для лобной пазухи проводят через носовое отверстие таким образом, что его дистальный конец размещен проксимально, в устье лобной пазухи (УЛП) или рядом с ним. Позиционирование катетера-направляющей 540 можно контролировать путем эндоскопической визуализации при помощи эндоскопа 400 и(или) рентгеноскопии (например, путем визуализации положения рентгеноконтрастного дистального наконечника направляющей относительно устья лобной пазухи). Как было указано ранее, вследствие того что лобная пазуха имеет относительно длинный выводной проток (лобный карман), может понадобиться разместить спейсерное устройство 510 по меньшей мере частично в выводном протоке, однако для осуществления этого сначала необходимо разместить направляющую или оболочку 540.
Как показано на фиг.13B, следующим этапом является введение и продвижение устройства для доставки вещества 510 с ограничивающей оболочкой 530, размещенной поверх спейсера для носовой пазухи 511, по катетеру-направляющей 540. Затем, как показано на фиг.13C, устройство для доставки вещества 510 и оболочку 530 продвигают по направляющей 540 до тех пор, пока ограничитель 531, размещенный на оболочке, не упрется в люэровский соединительный элемент 546, размещенный на направляющей 540. Устройство для доставки вещества 510 продвигают далее по направляющей 540 и ограничивающей оболочке 530 до тех пор, пока дистальный конец маркера ствола 513 не достигнет проксимального конца ограничителя 531, показывая, таким образом, что дистальный конец спейсера для носовой пазухи 511 находится рядом с дистальным концом направляющего устройства 540. Как показано на фиг.13D, поскольку устройство для доставки вещества 510 продвигают далее по направляющей 540 и ограничивающей оболочке 530, когда проксимальный конец маркера ствола 513 достигает проксимального конца ограничителя 531, спейсер для носовой пазухи 511 выдвигается наружу из дистального конца направляющей 540, позволяя, таким образом, удерживающим крыльям 518 раскрываться в полости лобной пазухи.
Затем, как показано на фиг.13E, вещество по стволу катетера 512 вводят в растяжимый резервуар 514 спейсера для носовой пазухи 511, благодаря чему резервуар 514 растягивается, и вещество выделяется через отверстия в резервуаре 514. В одном из вариантов осуществления настоящего изобретения шприц, содержащий вещество, например, суспензию кортикостероида, такую как, например, триамцинолона ацетонид, антибиотик, противогрибковый, нестероидный противовоспалительный и(или) аналогичный препарат, присоединяют к проксимальному люэровскому соединительному элементу 516 устройства для доставки вещества 510. После этого вводят лекарственную композицию, заставляя резервуар 514 растягиваться. В некоторых вариантах осуществления настоящего изобретения вводимое вещество и(или) резервуар 514 могут быть рентгеноконтрастными для контроля обеспечения раскрытия резервуара 514a рентгеноскопическим или иными подходящими радиографическими способами.
Затем, как показано на фиг.13F, люэровский соединительный элемент 516 на проксимальном конце устройства для доставки вещества 510 обрезают или удаляют иным способом. После этого, как показано на фиг.13G, направляющую 540, которая располагается поверх устройства для доставки вещества 510, извлекают из носового отверстия. Затем, как показано на фиг.13H, спейсерное устройство для носовой пазухи 511 отделяют от проксимальной части ствола катетера 512a путем обрезания при помощи ножниц, вводимых в носовое отверстие. Разрез производят в месте соединения или рядом с местом соединения проксимальной части 512a и дистальной части 512b. Проксимальную часть ствола 512a извлекают из полости тела пациента, при этом спейсер для носовой пазухи 511 остается на месте в полости лобной пазухи, выступая в выводной проток лобной пазухи (лобный карман). В некоторых вариантах осуществления изобретения при необходимости производится дополнительная фиксация спейсера для носовой пазухи 511 путем прикрепления ушка шовной петли 517 к слизистой оболочке в носовой полости. Однако этот этап не является обязательным, и, как правило, спейсер для носовой пазухи 511 фиксируют в полости лобной пазухи при помощи удерживающих крыльев 518.
Спейсер для носовой пазухи 511 может содержать любое подходящее вещество или комбинацию веществ, включая, помимо прочего, вещества, перечисленные в настоящей заявке. Спейсер для носовой пазухи 511 может находиться в полости лобной пазухи в течение любого периода времени от одного дня до одного года, предпочтительно - в течение периода от приблизительно 7 дней до приблизительно 90 дней, еще более предпочтительно - в течение периода от приблизительно 14 дней до приблизительно одного месяца. В некоторых вариантах осуществления настоящего изобретения доставка вещества при помощи спейсера для лобной пазухи 511 осуществляется в полость лобной околоносовой пазухи. В альтернативном варианте осуществления вещество может доставляться в полость лобной пазухи и лобный карман или выводной проток, а в некоторых случаях и в более проксимальные области носовой полости. Часто доставляемое вещество подбирают таким образом, чтобы оказать положительное влияние не только на полость пазухи, но и на любую область в носовой полости, в которую оно может быть доставлено.
Как и в вариантах осуществления настоящего изобретения, описанных выше, настоящий способ может использоваться после расширения устья лобной пазухи и(или) выводного протока путем баллонной синуспластики (Balloon Sinuplasty™). В альтернативном варианте осуществления этот способ применяется для лечения «нативной», то есть неоперированной лобной околоносовой пазухи. Необходимость выполнения баллонной синуспластики (Balloon Sinuplasty™) зависит от размера устья лобной пазухи и(или) выводного протока лобной пазухи.
На фиг.14A-D представлены альтернативные варианты осуществления спейсерного устройства 510, имплантированного в полость лобной пазухи. В одном из альтернативных вариантов осуществления мембрана или резервуар 514 спейсера 510 имеет относительно длинный профиль, так что его часть проходит проксимально внутри лобного кармана. Кроме того, варианты осуществления спейсерного устройства 510 могут предусматривать удерживающие крылья 521 и 523, размещенные в шахматном порядке в различных областях, как показано на фиг.14B и 14C, при этом проксимальное крыло 523 располагается напротив лобного кармана, благодаря чему обеспечивается требуемая ориентация спейсерного устройства 510. Кроме того, спейсерное устройство 510, имеющее нижнее крыло 525, может быть имплантировано таким образом, что нижнее крыло 525 способствует фиксации и направляет спейсер во время оперативного вмешательства (см. фиг.14D).
Несмотря на то, что сопроводительные иллюстрации и описанные выше примеры демонстрируют способы имплантации спейсерного устройства для доставки вещества 510 в полость лобной пазухи, для имплантации устройства в полость других пазух могут применяться аналогичные способы. Разумеется, для выполнения такой процедуры могут применяться другие подходы и инструменты.
Стабильность триамцинолона ацетонида в спейсерном устройстве после имплантации
Было проведено исследование, направленное на подтверждения того факта, что суспензия триамцинолона ацетонида для инъекций (Кеналог®-40 производства Bristol-Myers Squibb, Принстон, Нью-Джерси), при помещении в резервуар 14 спейсерного устройства для доставки вещества 10, сохраняет интактность и фармакологическую активность по меньшей мере в течение 30 дней после имплантации устройства. В рамках данного исследования резервуар 14 одного устройства 10 был заполнен путем введения 0,31 см3 суспензии триамцинолона ацетонида для инъекций, как описано выше (далее по тексту «резервуар, заполненный триамцинолона ацетонидом»). Резервуар 14 второго устройства 10 был заполнен физиологическим раствором (далее по тексту «резервуар, заполненный плацебо»), а резервуар третьего устройства оставался пустым (далее по тексту «пустой резервуар»). Все три устройства содержались в стабильных условиях согласно Международной конференции по гармонизации (ICH) (40°C±2°C/75% RH (отн. влажности) ± 5% RH (отн. влажности)) в камере, устойчивой к воздействию окружающей среды. Высокоэффективная жидкостная хроматография (ВЭЖХ) была выполнена на аликвотах содержимого каждого резервуара на 0 и 30 день. Результаты исследования приведены ниже в таблице 1.

Только пики примесей ≥0,02% рассматриваются как значимое содержание примесей.
Активность образцов триамцинолона ацетонида, полученных из резервуара, заполненного триамцинолона ацетонидом на 0 и 30 день, соответственно, подтверждена ВЭЖХ. Исследование показало, что рост уровня содержания примесей находится в диапазоне допустимых значений, а активность триамцинолона ацетонида в резервуаре, заполненном триамцинолона ацетонидом, сохраняется в достаточной степени, чтобы оказывать предполагаемое местное противовоспалительное действие по меньшей мере в течение 30 дней.
Эффективность триамцинолона ацетонида, доставляемого при помощи спейсерного устройства для доставки вещества 10
Применение локальной кортикостероидной терапии для лечения хронического воспаления околоносовых пазух позволяет достичь более эффективных концентраций лекарственного препарата на локальных рецепторных участках слизистой оболочки полости носа с минимальным риском развития системного побочного действия. Триамцинолона ацетонид (ТА) - синтетический кортикостероид второго поколения. В настоящее время шесть соединений этого поколения одобрены для интраназального применения. Все шесть кортикостероидов обладают относительно аналогичной активностью и эффективностью. ТА был выбран для использования в спейсере для носовых пазух решетчатой кости как соединение с наиболее высоким индексом безопасности и благодаря его доступности в виде концентрированного раствора, пригодного для использования в устройстве. В частности, использование препарата Кеналог-40 обусловлено тем, что он является одним из одобренных препаратов триамцинолона ацетонида, представленных на рынке.
Было установлено, что дозы триамцинолона ацетонида для интраназального введения и(или) ингаляций не вызывают угнетения гипоталамо-гипофизарно-надпочечниковой системы (ГГНС), даже если доставка лекарственного препарата осуществляется в течение периода до трех лет. См. публикации Klossek JM et al., Local Safety Of Intranasal Triamcinolone Acetonide: Clinical And Histological Aspects Of Nasal Mucosa In The Long-Term Treatment Of Perennial Allergic Rhinitis, Rhinology, 39 (I):17-22 (2001); Lund, VJ., Maximal Medical Therapy for Chronic Rhinosinusitis, Otolaryngol Clin N Am 38, 1301-1310 (2005) and Laliberte F et al., Clinical And Pathologic Methods To Assess The Long-Term Safety Or Nasal Corticosteroids, Allergy 55(8): 718-722 (2000).
Вводимый местно ТА продемонстрировал способность обеспечивать снижение остроты аллергической реакции как на ранней, так и на поздней стадиях, снижение чувствительности рецепторов в полости носа, чувствительных к раздражению, снижение местного воспаления и вероятности развития вторичных риновирусных инфекций. Даже рассчитанная на продолжительный период доставка ТА в полость носа не наносит вреда слизистой оболочке полости носа.
Носителем в спейсерном устройстве для доставки вещества 10, использованном в данном исследовании, являлся резервуар 14 объемом 0,1 мл (при максимальном заполнении). При максимальном заполнении резервуара препаратом Кеналог-40 вмещается до 4 мг ТА. Такое количество ТА по степени активности приблизительно соответствует 35-40 мг кортизола, в норме ежедневно вырабатываемого надпочечниками человека. Таким образом, общее количество ТА массой 4 мг, даже при условии единовременного высвобождения, не вызовет неблагоприятного воздействия на кортикоидную активность надпочечников.
Как было указано выше, конструкция отверстий 31 в резервуаре 14 спейсерного устройства для доставки вещества 10 позволяет ограничить рассеивание ТА из резервуара так, что в течение двухнедельного курса ежедневно осуществляется доставка малых доз. Таким образом, доза, доставляемая местно в полость пазух решетчатой кости или других околоносовых пазух, может быть ниже рекомендованной дозы ТА, доставляемой при помощи представленных на рынке назальных ингаляторов (например, ингалятор Nasacort® производства Sanofi-Aventis, Бриджуотер, Нью-Джерси).
Тринадцать человек, страдающих этмоидальным синуситом, прошли лечение, включающее этмоидотомию с послеоперационной доставкой ТА путем имплантации спейсерного устройства для доставки вещества 10 по существу в соответствии со способом, описанным выше и показанном на фиг.7A-7K. Девять пациентов прошли лечение от двустороннего синусита, остальные четыре пациента - от одностороннего синусита. Таким образом, в общей сложности лечение проводили на двадцати двух пазухах решетчатой кости. Четырнадцатый пациент, страдающий фронтальным синуситом, прошел лечение, включающее баллонную дилатацию выводного протока лобной пазухи с послеоперационной доставкой ТА путем имплантации спейсерного устройства для доставки вещества 10 по существу в соответствии со способом, описанным выше и показанном на фиг.8A-8G.
Наблюдение после операции и сбор данных
Пациенты №1-10:
У пациентов 1-10 проводили контроль уровня ТА в крови перед введением анестезии и через 1, 2 и 4 часа после имплантации и заполнения спейсерного устройства для доставки вещества 10. Если конкретный пациент оставался в медицинском учреждении в течение суток, забор образцов крови проводили через 23 часа или непосредственно перед выпиской. Дополнительные образцы крови взяты у пациентов 1-10 на 3, 7, 10 и 14 день после операции и непосредственно перед извлечением спейсерного устройства для доставки вещества 10 из полости тела.
Помимо забора образцов крови, как было указано выше, пациенту было предложено ответить на вопросы теста оценки исхода заболеваний носа и околоносовых пазух (SNOT-20) (SNOT-20 Piccirillo, JF et al., Psychometric and clinimetric validity of the 20-Item Sino-Nasal Outcome Test (SNOT-20), Copyright © 1996 by Jay F. Piccirillo M.D., Washington University, St. Louis, Missouri) в исходном состоянии и через 1, 2 и 6 недель после извлечения спейсерного устройства для доставки вещества 10. Также пациенту было предложено ответить на вопросы, связанные с переносимостью спейсерного устройства для доставки вещества 10. Устройство было извлечено во время посещения врача на 14 день после имплантации. Дополнительную информацию относительно выделения триамцинолона ацетонида из спейсера для носовых пазух решетчатой кости во время имплантации устройства удалось получить путем количественной оценки остаточного содержания лекарственного препарата в устройстве.
Исследователи обеспечили соответствующий послеоперационный уход, за исключением предоставления стероидных назальных спреев и жидкостей для промывания полости носа. Послеоперационное лечение антибиотиками проводили в случае необходимости на усмотрение исследователя. Такие меры были призваны свести к минимуму влияние сопутствующих лекарственных препаратов на результаты исследования.
Через восемь недель был сделан контрольный срез КТ пазух решетчатой кости для оценки состояния пазух решетчатой кости и степени улучшения по сравнению с исходным состоянием.
Пациенты №11-13:
Пациентам №11-13 был обеспечен такой же послеоперационный уход и забор образцов крови, как и пациентам №1-10, за исключением следующего:
после забора образца крови в исходном состоянии перед введением анестезии был также произведен забор крови через 4 часа после имплантации в день проведения операции, а также в 1, (необязательно) 3, 7, 14, 21, 28 день и в день перед извлечением спейсерного устройства для доставки вещества 10.
В ходе исследования было запланировано 6 посещений на 3, 7, 14, 21 и 28 дни и заключительный визит через 10 недель после операции. Помимо забора образцов крови, как сказано выше, пациенту было предложено ответить на вопросы теста оценки исхода заболеваний носа и околоносовых пазух (SNOT-20) и вопросы относительно качества жизни (КЖ) в исходном состоянии и через 1, 2 и 6 недель после извлечения устройства. Также пациенту было предложено ответить на вопросы, связанные с переносимостью спейсера для носовых пазух решетчатой кости. Устройство было извлечено во время посещения врача на 28 день после имплантации.
Исследователи обеспечили соответствующий послеоперационный уход, за исключением предоставления стероидных назальных спреев и жидкостей для промывания полости носа. Послеоперационное лечение антибиотиками проводили при необходимости, на усмотрение исследователя. Такие меры были призваны свести к минимуму влияние сопутствующих лекарственных препаратов на результаты исследования.
Через восемь недель был сделан контрольный срез КТ пазух решетчатой кости для оценки состояния пазух решетчатой кости и степени улучшения по сравнению с исходным состоянием.
Пациент №14:
Пациент №14 был единственным пациентом, проходившим лечение по поводу фронтального, а не этмоидального, синусита. Для пациента №14 был обеспечен послеоперационный уход и сбор данных (т.е. забор образцов крови и анкетирование SNOT-20), по существу такой же, как и для пациентов №1-10.
Результаты КТ
Проведено КТ-исследование и выполнена оценка улучшения состояния пораженных пазух по шкале Ланда-Маккея. Оценки по шкале Ланда-Маккея отражены в графике на фиг.15. В исходном состоянии (до операции) средняя оценка по шкале Ланда-Маккея составляла 10,4. Средняя оценка по шкале Ланда-Маккея в послеоперационном периоде - 3,9. Таким образом, у 14 пациентов, принимавших участие в исследовании, отмечено снижение оценки по шкале Ланда-Маккея на 65,1%.
Результаты теста оценки исхода заболеваний носа и околоносовых пазух (SNOT-20) и анкетирования
На фиг.16 представлено среднее значение степени улучшения оценок SNOT-20, начиная с оценок в исходном состоянии и до оценок через 1, 2, 4 и 6 недель (Примечание. Один пациент отклонился от протокола, прервав 6-недельный период наблюдения на четвертой неделе.) Оценка 1,07 или ниже является показателем значительного снижения выраженности клинических симптомов синусита (т.е. снижение по меньшей мере на 0,8 по сравнению с оценкой, данной в исходном состоянии). Данные свидетельствуют о том, что наблюдается существенное снижение средних оценок SNOT-20 через 2, 4 и 6 недель после операции.
Облегчение симптомов также документально подтверждено путем анкетирования пациентов, проведенного через одну, две и шесть недель после операции. Все пациенты сообщали о значительном улучшении состояния или улучшении состояния спустя шесть недель после операции. Ни один из пациентов не сообщил об ухудшении состояния. Через шесть недель большинство пациентов были удовлетворены результатами и заявили, что если бы им предложили выбирать способ лечения, они бы вновь согласились на такую операцию.
Статистический анализ результатов
Результаты теста SNOT-20 фиксировали во время 5 контрольных посещений. На основе конечного показателя принимаются следующие нулевая и альтернативная гипотезы:
Но: µ (день 42 минус исходное значение) = 0
На: µ (день 42 минус исходное значение) ≠ 0
Результаты однофакторного анализа сопоставления динамики оценок теста SNOT-20, начиная с оценок, данных в исходном состоянии, проанализированы при помощи двухвыборочного t-теста. Результаты анализа показали существенное снижение оценок теста SNOT-20 в течение 7 дней после операции. Во время последующих контрольных посещений отмечалось стабильное снижение оценок. На момент окончания наблюдения 13 из 14 пациентов (92,9%) прошли контрольный осмотр на 42 день после операции. По сравнению с исходным значением через 42 дня после операции оценки снизились на 22,08 пункта по шкале оценок SNOT-20 с учетом стандартного отклонения 14,69 и значения вероятности <0,001. Величина эффекта согласно полученным результатам составляет 1,50, что отражает высокую эффективность лечения.
Оценки по шкале Ланда-Маккея (КТ)
КТ-исследование проводили в исходном состоянии и на 42 день после операции с целью определения оценки по шкале Ланда-Маккея (ЛМ). На основе конечного показателя принимаются следующие нулевая и альтернативная гипотезы:
Но: µ (день 42 минус исходное значение) = 0
На: µ (день 42 минус исходное значение) ≠ 0
Однофакторный анализ результатов на основе сопоставления динамики оценок по шкале ЛМ по сравнению с исходными данными проведен при помощи двухвыборочного t-теста. Результаты анализа показали существенное снижение оценок по шкале ЛМ на 42 день после операции. По сравнению с исходным значением, оценки снизились на 6, 50 пункта по шкале ЛМ с учетом стандартного отклонения 3,96 и значения вероятности <0,001. Величина эффекта согласно полученным результатам составляет 1,64, что отражает высокую эффективность лечения.
Для оценки динамики оценок по шкале ЛМ для пазух решетчатой кости был проведен подгрупповой анализ. Результаты этого анализа также позволили выявить существенное снижение оценок по шкале ЛМ через 42 дня после операции. По сравнению с исходным значением, оценки снизились на 2,21 пункта по шкале ЛМ с учетом стандартного отклонения 1,53 и значения вероятности <0,001. Величина эффекта согласно полученным результатам составляет 1,44, что отражает высокую эффективность лечения.
Оценка основных конечных показателей проведена способом статистики вывода. Учитывая успешность применения у 14 пациентов, участвовавших в исследовании, (100%), нижний 95% точный биноминальный доверительный интервал составил 76,84%.
Анализ плазмы крови
Для оценки второстепенных конечных показателей способности ТА к высвобождению из спейсерного устройства для доставки вещества 10 в течение времени, в плазме крови/ выделенной из каждого из собранных образцов крови, определяли уровень содержания ТА. Эти данные приведены ниже в таблице 2.
Низкий (т.е. системно активный), но обнаружимый уровень содержания ТА выявлен в плазме крови пациентов по прошествии 28 дней после имплантации и заполнения спейсерного устройства для доставки вещества 10.
Вывод
Доставку местных эффективных доз ТА осуществляли при помощи спейсерного устройства для доставки вещества 10 в течение 28 дней после операции. КТ показала значительное снижение воспаления в пазухе. У пациентов также отмечено существенное улучшение в отношении симптоматики синусита на основе результатов теста SNOT 20 и анкетирования.
Используемый в настоящем документе термин «вещество» следует толковать широко, включая все возможные лекарственные препараты, пролекарства, белки, препараты генной терапии, клеточные, диагностические, контрастные или радиофармацевтические препараты, биологические препараты и т.д. Такие препараты могут быть представлены в связанной или свободной форме, в жидкой, твердой или коллоидной форме или в форме суспензий, растворов или в газообразной, текучей или нетекучей форме. Например, в некоторых случаях, когда требуется лечение или предотвращение развития микробной инфекции, в качестве доставляемого вещества может использоваться фармацевтически приемлемая соль или лекарственная форма противомикробного препарата (например, антибиотик, противовирусное, противопаразитарное, противогрибковое средство и т.д.), кортикостероид или иное противовоспалительное средство (например, нестероидное противовоспалительное средство, или НПВС), противоотечный препарат (например, сосудосуживающее средство), разжижающий препарат (например, отхаркивающее или муколитическое средство), препарат, предотвращающий или модифицирующий аллергический ответ (например, антигистаминный препарат, ингибитор цитокина, ингибитор лейкотриена, ингибитор IgE, иммуномодулятор), анестетик с сосудосуживающими агентами или без них (например, ксилокаин с эпинефрином или без него), анальгетик, аллерген или иное вещество, вызывающее секрецию слизи тканями, гемостатические препараты для остановки кровотечения, антипролиферативные, цитотоксические препараты, например, спирт, биологические препараты, например, молекулы белка, стволовые клетки, генные препараты или препараты генной терапии, векторы, несущие вирусные белки, или нуклеиновые кислоты, такие как ДНК или мРНК, кодирующие важные терапевтические функции или вещества, средства для прижигания, например, нитрат серебра и т.д.
Неограничивающими примерами противомикробных препаратов, которые могут использоваться в рамках настоящего изобретения, являются ацикловир, амантадин, ремантадин, осельтамивир, занамивир, аминогликозиды (например, амикацин, гентамицин и тобрамицин), амоксициллин, амоксициллин/клавуланат, амфотерицин В, ампициллин, ампициллин/сульбактам, атоваквон, азитромицин, цефазолин, цефепим, цефотаксим, цефотетан, цефподоксим, цефтазидим, цефтизоксим, цефтриаксон, цефуроксим, цефуроксим аксетил, цефалексин, хлорамфеникол, клотримазол, ципрофлоксацин, кларитромицин, клиндамицин, дапсон, диклоксациллин, доксициклин, эритромицин, флуконазол, фоскарнет, ганцикловир, атифлоксацин, имипенем/циластатин, изониазид, итраконазол, кетоконазол, метронидазол, нафциллин, нафциллин, нистатин, пенициллины, включая пенициллин G, пентамидин, пиперациллин/тазобактам, рифампин, квинупристин/дальфопристин, тикарциллин/клавуланат, триметоприм/сульфаметоксазол, валацикловир, ванкомицин, мафенид, сульфадиазин серебра, мупироцин, нистатин, триамцинолон/нистатин, клотримазол/бетаметазон, клотримазол, кетоконазол, бутоконазол, миконазол, тиоконазол, дезинфицирующие химические средства, разрушающие или блокирующие микробы (например, ноноксинол-9, октоксинол-9, хлорид бензалкония, менфегол и N-докозанол); химические вещества, блокирующие присоединение микробов к клеткам-мишеням и(или) ингибирующие проникновение возбудителей инфекции (например, сульфатированные и сульфонированные полимеры, такие как PC-515 (каррагинан), Pro-2000 и декстрин 2 сульфат); антиретровирусные препараты (например, гель РМРА), предотвращающие репликацию ретровирусов в клетках, созданные методом генной инженерии или образованные естественным путем антитела, противодействующие возбудителям инфекции, такие как антивирусные антитела, созданные методами генной инженерии из растений, известные как растительные антитела, вещества, изменяющие состояние ткани таким образом, что она приобретает свойства среды, неблагоприятной для возбудителей инфекции (такие как вещества, изменяющие кислотность ткани (например, буферный гель и ацидформ)), непатогенные или «дружественные» микробы, стимулирующие выработку пероксида водорода или иных веществ, убивающих или ингибирующих рост патогенных микробов (например, молочнокислая бактерия), противомикробные белки или пептиды, например, описанные в патенте США №6716813 (Lin et al.), содержание которого в явной форме включено в настоящий документ путем ссылки, или металлы, обладающие противомикробными свойствами (например, коллоидное серебро).
Дополнительно или в качестве альтернативны в некоторых случаях, когда требуется лечение или предотвращение развития воспаления, в качестве доставляемых веществ в рамках настоящего изобретения могут использоваться различные стероиды или иные противовоспалительные (например, нестероидные противовоспалительные средства, или НПВС), болеутоляющие или жаропонижающие препараты. Например, могут использоваться кортикостероиды, ранее использовавшиеся для интраназального введения, среди них беклометазон (Ванценаз® или Беконаз®), флунизолид (Назалид®), флутиказон проприонат (Флоназ®), триамцинолон ацетонид (Назакорт®), будесонид (Ринокорт аква®), лотепреднол этабонат (Локорт) и мометазон (Назонекс®). Также могут использоваться и другие формы солей указанных выше кортикостероидов. Неограничивающими примерами стероидов, которые могут использоваться в рамках настоящего изобретения, также являются аклометазон, дезонид, гидрокортизон, бетаметазон, клокортолон, дезоксиметазон, флуоцинолон, флурандренолид, мометазон, предникарбат; амцинонид, дезоксиметазон, дифлоразон, флуоцинолон, флуоцинонид, галцинонид, клобетазол, усиленный бетаметазон, дифлоразон, галобетазол, преднизон, дексаметазон и метилпреднизолон. Среди прочих противовоспалительных, болеутоляющих или жаропонижающих препаратов, использование которых допускается в рамках настоящего изобретения, находятся следующие: неселективные ингибиторы циклооксигеназы (ЦОГ) (например, производные салициловой кислоты, аспирин, салицилат натрия, холина магния трисалицилат, салсалат, дифлунизал, сульфасалазин и олсалазин, производные пара-аминофенола, такие как ацетаминофен, индол- и инден-уксусные кислоты, такие как индометацин и сулиндак, гетероарил-уксусные кислоты, такие как толметин, диклофенак и кеторолак, арилпропионовые кислоты, такие как ибупрофен, напроксен, флурбипрофен, кетопрофен, фенопрофен и оксапрозин, антраниловые кислоты (фенаматы), такие как мефенамовая кислота и мелоксикам, эноловые кислоты, такие как оксикамы (пироксикам, мелоксикам) и алканоны, такие как набуметон) и селективные ингибиторы ЦОГ-2 (например, диарил-замещенные фураноны, такие как рофекоксиб; диарил-замещенные пиразолы, такие как целекоксиб, индол-уксусные кислоты, такие как этодолак, и сульфонанилиды, такие как нимесулид).
Дополнительно или в качестве альтернативы в некоторых случаях, когда требуется лечение или предотвращение аллергического или иммунного ответа и (или) клеточной пролиферации, в качестве доставляемых веществ в рамках настоящего изобретения могут использоваться a) различные ингибиторы цитокина, такие как гуманизированные анти-цитокиновые антитела, антитела рецепторов анти-цитокина, рекомбинантные (новая клетка, образование которой обусловлено генетической рекомбинацией) антагонисты или растворимые рецепторы, b) различные модификаторы лейкотриена, такие как зафирлукаст, монтелукаст и зилеутон, c) ингибиторы иммуноглобулина Е (IgE), такие как омализумаб (моноклональное анти-IgE антитело, ранее называвшееся rhu Mab-E25) и секреторный лейкоцитарный ингибитор протеазы.
Дополнительно или в качестве альтернативы в некоторых случаях, когда требуется сужение слизистой оболочки, снятие отека или воздействие на гемостаз, в качестве доставляемого вещества в рамках настоящего изобретения могут использоваться различные сосудосуживающие препараты для снятия отека и(или) остановки кровотечения, включая, помимо прочего, следующие препараты: псевдоэфедрин, ксилометазолин, оксиметазолин, фенилэфрин, эпинефрин и т.п.
Дополнительно или в качестве альтернативы в некоторых случаях, когда требуется улучшение оттока слизи, в качестве доставляемого вещества в рамках настоящего изобретения могут использоваться различные муколитические или иные препараты, изменяющие вязкость и консистенцию слизи или слизистых секретов, включая, помимо прочего, ацетилцистеин (МукомистТМ, МукозилТМ) и гвайфенезин.
Дополнительно или в качестве альтернативы в некоторых случаях, когда требуется предотвращение или ограничение выброса гистамина, в качестве доставляемых веществ в рамках настоящего изобретения могут использоваться различные стабилизаторы мастоцитов или лекарственные препараты, препятствующие выбросу гистамина, такие как кромолин (например, Назалкром®) и недокромил.
Дополнительно или в качестве альтернативы в некоторых случаях, когда требуется предотвращение или ингибирование воздействия гистамина, в качестве доставляемых веществ в рамках настоящего изобретения могут использоваться различные антигистаминные препараты, такие как азеластин (например, Астилин®), дифенгидрамин, лоратадин и т.п.
Дополнительно или в качестве альтернативны в некоторых случаях, когда требуется растворить, разрушить, иссечь, сломать или ремоделировать кость или хрящ, в качестве доставляемых веществ в рамках настоящего изобретения могут использоваться вещества, ослабляющие или модифицирующие кость и(или) хрящ, облегчая выполнение других процедур, составляющих предмет настоящего изобретения, в ходе которых выполняется ремоделирование, изменение формы, повреждение или удаление кости или хряща. Примером такого препарата может служить хелатор кальция, такой как этилендиаминтетрауксусная кислота (ЭДТА), которая впрыскивается или доставляется при помощи имплантата в область, расположенную рядом с участком кости, который требуется ремоделировать или модифицировать. В качестве другого примера препарата, состоящего из или содержащего клетки, вызывающие разложение костной ткани, можно указать остеокласты. Другие примеры включают различные энзимы материала, которые способны размягчать или разрушать компоненты кости или хряща, такие как коллагеназа (КГН), трипсин, трипсин/ЭДТА, гиалуронидаза и тозиллизилхлорметан (ТЛХМ).
Дополнительно или в качестве альтернативы в некоторых случаях в качестве доставляемых веществ в рамках настоящего изобретения могут использоваться иные классы веществ, которые используются для лечения ринита, полипоза, воспаления полости носа и других заболеваний уха, горла, носа, включая, помимо прочего, холинолитики, осушающие назальные секреты, такие как ипратропий (Атровент назал®), а также другие не указанные в настоящем документе препараты.
Дополнительно или в качестве альтернативы в некоторых случаях, в качестве доставляемых веществ в рамках настоящего изобретения могут использоваться диуретики местного или топического действия, такие как фуросемид, и(или) гиперосмолярные препараты, такие как гель, содержащий хлорид натрия, или иные солевые препараты, обезвоживающие ткань, или вещества, которые напрямую или опосредованно вызывают изменение осмолярного содержимого слизистой, в результате чего ткань теряет больше жидкости, а полипы уменьшаются в размерах.
Дополнительно или в качестве альтернативы в некоторых случаях, когда требуется лечение опухоли или злокачественного новообразования, в качестве доставляемых веществ в рамках настоящего изобретения могут использоваться противоопухолевые препарата (например, химиотерапевтические препараты, используемые для лечения онкологических заболеваний, модификаторы биологического ответа, ингибиторы васкуляризации, блокаторы рецепторов гормонов, криотерапевтические или иные препараты, разрушающие или ингибирующие неоплазию или онкогенез), такие как алкилирующие или иные препараты, непосредственно убивающие раковые клетки, атакуя их ДНК (например, циклофосфамид, изофосфамид), нитрозомочевина или иные препараты, убивающие раковые клетки, ингибируя изменения, необходимые для клеточной репарации ДНК (например, кармустин (БиКНУ) и ломустин (ССНУ)), антиметаболиты и иные препараты, блокирующие рост раковых клеток, нарушая определенные функции клеток, как правило, синтез ДНК (например, 6-меркаптопурин и 5-фторурацил (5FU), противоопухолевые антибиотики и иные лекарственные препараты, связывающие или включающиеся в ДНК и препятствующие синтезу РНК (например, доксорубицин, даунорубицин, эпирубицин, идарубицин, митомицин-С и блеомицин), алкалоиды растительного происхождения (барвинок) и иные противоопухолевые препараты растительного происхождения (например, винкристин и винбластин), стероидные гормоны, ингибиторы гормонов, антагонисты рецепторов гормонов и иные препараты, влияющие на развитие гормонально-зависимых опухолей (например, тамоксифен, герцептин, ингибиторы ароматазы, такие как аминоглутетимид и форместан, ингибиторы триазола, такие как летрозол и анастразол, стероидные ингибиторы, такие как экземестан), антиангиогенные белки, низкомолекулярные синтетические препараты, генная терапия и(или) иные препараты, ингибирующие ангиогенез или васкуляризацию опухолей (например, мет-1, мет-2, талидомид), бевацизумаб (авастин), скваламин, эндостатин, ангиостатин, ангиозим, АЕ-941 (неовастат), СС-5013 (ревимид), меди-522 (витаксин), 2-метоксиэстрадиол (2МЭ2, панзем), карбоксиамидотриазол (CAI), пролекарственная форма комбретастатина А4 (СА4Р), SU6668, SU11248, BMS-275291, COL-3, EMD 121974, IMC-1C11, IM862, TNP-470, целекоксиб (целебрекс), рофекоксиб (виокс), интерферон альфа, интерлейкин-12 (ИЛ-12) или любой из лекарственных препаратов, указанных в публикации Science Vol.289, Pages 1197-1201 (от 17 августа 2000 года), содержание которого в явной форме включено в настоящий документ путем ссылки, модификаторы биологического ответа (например, интерферон, бацилла Кальмета-Герена (БЦЖ), монокальные антитела, интерлюкен 2, гранулоцитарный колониестимулирующий фактор (ГКСФ) и т.д.), антагонисты рецептора тромбоцитарного фактора роста (ТФР), герцептин, аспарагиназа, бусульфан, карбоплатин, цисплатин, кармустин, хлорамбуцил, цитарабин, дакарбазин, этопозид, флукарбазин, фторурацил, гемцитабин, гидроксимочевина, ифосфамид, иринотекан, ломустин, мелфалан, меркаптопурин, метотрексат, тиогуанин, тиотепа, томудекс, топотекан, треосульфан, винбластин, винкристин, митоазитрон, оксалиплатин, прокарбазин, стрептоцин, таксол, таксотер, аналоги (родственные соединения) и производные этих лекарственных препаратов, а также противоопухолевые препараты, не указанные в настоящем документе.
Дополнительно или в качестве альтернативы в некоторых случаях, когда требуется стимуляция образования новых клеток или изменения существующих клеток, в качестве доставляемых препаратов в рамках настоящего изобретения могут использоваться клетки (слизистые клетки, фибропласты, стволовые клетки или клетки, полученные методами генной инженерии), а также гены и носители генов, например, плазмиды, аденовирусные векторы или оголенные ДНК, мРНК и т.д., вводимые вместе с генами, кодирующими противовоспалительные вещества и т.д., и, как было указано выше, остеокласты, изменяющие или размягчающие костную ткань, если это необходимо.
Любое из устройств и способов, описанных в настоящем документе, также может использоваться для доставки веществ к головному мозгу или влиять на работу системы обоняния. К примерам относятся питание энергией или депонирование устройств и(или) веществ и(или) имплантата (имплантатов) для доставки веществ с целью окклюзии или изменения ольфакторного восприятия, подавления аппетита или лечения ожирения, эпилепсии (например, барбитураты, такие как фенобарбитал или мефобарбитал, иминостильбены, такие как карбамазепин и окскарбазепин; сукцинимиды, такие как этилсуксимид, вальпроевая кислота, бензодиазепины, такие как клоназепам, клоразепат, диазепам и лоразепам, габапентин, ламотригин, ацетазоламид, фельбамат, леветирацетам, тиагабин, топирамат, зонисамид и т.д.), расстройств личности и психики (например, антидепрессанты, седативные препараты, нейролептики и т.д.), хронической боли, болезни Паркинсона (например, агонисты допаминового рецептора, такие как бромокриптин, перголид, ропинитрол и прамипексол, предшественники допамина, такие как леводопа, ингибиторы катехин-O-метилтрансферазы, такие как толкапон и энтакапон, селегилин, антагонисты мускариновых рецепторов, такие как тригексифенидил, бензотропин и дифенгидрамин) и болезни Альцгеймера, болезни Хантингтона и других деменций, нарушений сознания или хронических дегенеративных расстройств (например, такрин, донепезил, ривастигмин, галантамин, флуоксетин, карбамазепин, клозапин, клоназепам и белковая или генная терапия, ингибирующая образование бета-амилоидных бляшек) и т.д.
Устройства и способы, описанные в настоящем документе, могут использоваться для доставки двух или более веществ, указанных в настоящем документе, в нескольких комбинациях, к соответствующим анатомическим областям. В одном из вариантов осуществления настоящего изобретения устройства и способы, описанные в настоящем документе, применяются для доставки композиции, состоящей из противовоспалительного препарата (например, стероида или НПВС) и муколитического препарата.
Устройства и способы, описанные в настоящем документе, применяются для доставки гелей или вязких жидкостей, содержащих один или несколько лекарственных препаратов, в анатомические области, например, в околоносовые пазухи. Такие гели или вязкие жидкости могут покрывать и сцепляться со слизистой оболочкой для обеспечения долговременной доставки одного или нескольких лекарственных препаратов к слизистой оболочке. В одном из вариантов осуществления настоящего изобретения может осуществляться доставка пластифицированного углеводородного геля, содержащего желатин, пектин и натрий-карбоксиметилцеллюлозу, а также соответствующий лекарственный препарат, к слизистой оболочке, такой как слизистая оболочка околоносовой пазухи. Такие гели могут применяться для долговременной доставки соответствующего лекарственного препарата к слизистой оболочке.
Один или несколько резервуаров, описанных в настоящем документе, могут включать ячейки сложной формы, при этом каждая ячейка вмещает определенную лекарственную композицию. Ячейки со сложной формой предотвращают смешивание различных лекарственных композиций перед их доставкой в полость анатомической структуры.
Один или несколько резервуаров, имеющих отверстия или поры, заполняют соответствующим лекарственным препаратом под достаточно высоким давлением таким образом, чтобы часть лекарственного препарата выходила через отверстия или поры. Этот процесс используется для доставки начального болюса лекарственного препарата к прилегающим анатомическим структурам.
Один или несколько резервуаров, описанных в настоящем документе, заполняют соответствующим лекарственным препаратом после введения резервуара в полость анатомической структуры. В альтернативном варианте осуществления один или несколько резервуаров, описанных в настоящем документе, заполняют соответствующим лекарственным препаратом перед введением резервуара в полость анатомической структуры. В альтернативном варианте один или несколько резервуаров, описанных в настоящем документе, предварительно заполняют лекарственным препаратом в твердой, лиофилизированной или концентрированной форме. Лекарственный препарат в твердой, лиофилизированной или концентрированной форме переводят в активную форму путем введения растворителя в резервуар, содержащий лекарственный препарат. Растворитель вводят в резервуар непосредственно до или после введения резервуара в анатомическую область. В альтернативном варианте осуществления один или несколько резервуаров, описанных в настоящем документе, предварительно заполняют лекарственным препаратом в неактивной форме. Лекарственный препарат в неактивной форме преобразовывают в лекарственный препарат в активной форме путем введения активирующего агента в резервуар, содержащий лекарственный препарат. Активирующий агент вводят в резервуар непосредственно до или после введения резервуара в анатомическую область.
Необходимо также отметить, что, как было указано в настоящем документе, имплантируемая часть спейсерного устройства для доставки вещества 10 может иметь сквозной просвет, который может использоваться в качестве вентиляционного и(или) дренажного отверстия, когда имплантируемая часть устройства располагается в полости околоносовой пазухи, воздухоносной ячейки, евстахиевой трубы, отверстия в барабанной перепонке или в любой другой анатомической полости организма.
Устройства и способы, описанные в настоящем документе, могут применяться для разметки анатомической области при помощи соответствующего визуализируемого маркера. Например, устройства и способы, описанные в настоящем документе, могут применяться для доставки рентгеноконтрастной метки, например, в виде рентгеноконтрастного вещества, к устью околоносовой пазухи. Это позволяет пользователю визуализировать устье околоносовой пазухи с помощью рентгеновских лучей или рентгеноскопии.
Одно или несколько устройств для доставки вещества, описанных в настоящем документе, могут включать изогнутую, выгнутую или наклоненную под углом область, позволяющую продвигать устройство для доставки вещества через анатомические структуры.
Наиболее дистальные участки одного или нескольких устройств для доставки вещества, описанных в настоящем документе, могут быть снабжены атравматическим наконечником. Атравматический наконечник предназначен для предотвращения или снижения риска повреждения анатомических структур дистальными частями одного или нескольких устройств для доставки вещества.
Внешняя поверхность одного или нескольких устройств для доставки вещества, описанных в настоящем документе, может иметь покрытие, которое снижает или исключает риск налипания биологического материала на внешнюю поверхность. В одном из вариантов осуществления настоящего изобретения покрытие содержит материал, адсорбирующий воду и превращающий ее в гель. Примером такого материала является, помимо прочего, гиалуроновая кислота и т.д.
Одно или несколько устройств для доставки вещества, описанных в настоящем документе, могут иметь конструкцию, позволяющую легко извлекать устройство из анатомической полости по завершении лечения.
Одно или несколько устройств для доставки вещества, описанных в настоящем документе, могут быть повторно заполнены после осуществления доставки значительной части содержащегося в резервуаре лекарственного препарата в соответствующую анатомическую структуру.
Одно или несколько устройств для доставки вещества, описанных в настоящем документе, могут содержать один или несколько маркеров, позволяющих пользователю определить местоположение и(или) продвигать устройства для доставки вещества через анатомические структуры. Например, устройства для доставки вещества могут содержать визуально различимые маркеры, позволяющие пользователю определять глубину введения устройств для доставки вещества в анатомическую структуру. В другом примере устройства для доставки вещества могут содержать визуализируемые маркеры, позволяющие пользователю определить местоположение и(или) продвигать устройства для доставки вещества через анатомические структуры путем визуализации при помощи рентгеновских лучей, МРТ и т.д.
В рамках настоящего документа термин «отверстие околоносовой пазухи» относится к любому отверстию в околоносовой пазухе или воздухоносной ячейке, такое как естественные устья, хирургически измененные естественные устья, отверстия, созданные хирургическим путем, отверстия, созданные путем антростомии, отверстия, созданные путем остеотомии, трепанационные отверстия, просверленные отверстия, отверстия, созданные путем этмоидэктомии, и другие естественные и искусственные проходы и т.д.
В рамках настоящего документа термин «имплантируемый» относится к любому устройству, удерживаемому в полости организма человека или животного в период времени от 30 минут до 60 дней.
В каждом из описанных выше примеров, в котором используется эндоскоп 400, как показано на чертеже, его вводят отдельно от других устройств. Однако при любом применении или варианте осуществления настоящего изобретения, где это практически осуществимо, эндоскоп может быть присоединен или интегрирован с одним или несколькими другими устройствами, используемыми во время операции, как описано в заявке на патент с серийным №.
Необходимо отметить, что примеры 2 и 3, приведенные выше, иллюстрируют способы ввода спейсерного устройства 10 в полости лобных пазух, которые могли быть предварительно изменены хирургическим путем или путем баллонной дилатации или остались неизменными. В некоторых случаях, например, когда выводной проток лобной пазухи был предварительно расширен или изменен хирургическим путем, что относительно облегчает доступ к лобной пазухе (ЛП), оператор доставляет спейсерное устройство 10 через ограничивающую трубку 42 (или оболочку 40 и 40a) в полость лобной пазухи при помощи щипцов или других хирургических инструментов или без них, устраняя необходимость применения катетера-направляющей, проволочного направителя, дилататора или других направляющих устройств или устройств, облегчающих введение спейсерного устройства 10 в полость лобной пазухи, как описано в примерах 2 и 3.
Также необходимо отметить, что хотя в приведенных выше примерах 1, 2 и 3 в качестве лекарственного препарата, заполняющего резервуар и высвобождающегося из него, используется суспензия триамцинолона ацетонида для инъекций (Кеналог®-40 производства Bristol-Myers Squibb, Сомервилль, Нью-Джерси), помимо или в качестве альтернативы суспензии триамцинолона ацетонида для инъекций могут использоваться другие лекарственные препараты. В некоторых случаях, когда требуется применение имплантируемого спейсерного устройства 10a для доставки стероида, стероид может быть приготовлен в виде раствора, а не суспензии. В таких случаях стероид растворяют в соответствующем биологически совместимом растворителе. Например, в качестве подходящих растворителей для растворения по меньшей мере некоторых стероидов могут использоваться циклодекстрины. См. Khomutov, S.M., Dovbnya, D.V. and Donova, M.V., Dissolution of a Mixture of Steroids in Cyclodextrin Solutions: a Model Description; Pharmaceutical Chemistry Journal; Vol.35, No.1i, pp.627-629 (November, 2001).
В некоторых примерах устройства, составляющие предмет настоящего изобретения, могут применяться для доставки стероидов или иных веществ в составе лекарственных композиций, доступных в продаже в виде назальных капель или спреев или иным образом подходящих для интраназального введения (например, в виде назальных растворов). По меньшей мере в некоторых случаях такие назальные растворы близки по составу к носовым секретам, таким образом, они не препятствуют нормальной работе реснитчатого эпителия. Такие назальные растворы, как правило, являются изотоническими и слабо буферизированными (pH от 5,5 до 6,5). Кроме того, при необходимости в состав раствора могут быть включены противомикробные консерванты, подобные тем, которые используются в офтальмологических препаратах, и стабилизаторы лекарственных препаратов (при необходимости). Существуют различные назальные препараты, например, антибиотики, стероиды, антигистаминные, противоотечные препараты и ипратропия бромид.
Если это допустимо и приемлемо, любое из веществ, доставляемых при помощи устройств, составляющих предмет настоящего изобретения, может быть представлено в форме липосом или наночастиц (например, в форме нанокапсул). Процесс образования и использования липосом хорошо известен специалистам в данной области. Липосомы образуются из фосфолипидов, диспергированных в водной среде, где они спонтанно образуют мультиламеллярные концентрические бислойные везикулы, иначе называемые мультиламеллярные везикулы (МЛВ). МЛВ, как правило, имеют диаметр от 25 нм до 4 мкм. При диспергировании ультразвуком МЛВ образуют малые моноламеллярные везикулы (ММВ) диаметром приблизительно от 20 до 50 нм (200-500 ангстремов), ядро которых содержит водный раствор. В целом, при диспергировании в водной среде фосфолипиды могут образовывать различные структуры, отличные от липосом, в зависимости от молярной концентрации липидов в воде. При низкой концентрации липидов в воде образуются липосомы. Физические характеристики липосом зависят от pH, тоничности, а также от присутствия или отсутствия двухвалентных катионов. Липосомы могут взаимодействовать с клетками при помощи различных механизмов, включая 1) эндоцитоз (например, фагоцитоз липосом клетками, такими как макрофаги и нейтрофилы), поглощение поверхностью клеток, 2) взаимодействие с клеточными поверхностными компонентами, 3) встраивание в плазматическую мембрану путем внедрения липидного бислоя липосомы в плазматическую мембрану или 4) транспорт липосомных липидов в клеточные или внутриклеточные мембраны, и наоборот. Механизм(-ы) взаимодействия липосом с клетками полости околоносовой пазухи, слизистой оболочки и т.д. зависит(-ят) от состава липосомной композиции.
Нанокапсулой может являться любая наночастица, состоящая из оболочки и полости, в которую помещается соответствующий лекарственный препарат. Способы получения нанокапсул хорошо известны специалистам в данной области техники. Полимерные нанокапсулы могут иметь заданные размеры и форму. Нанокапсулы могут быть выполнены в виде монодисперсных частиц с точно заданными физическими и химическими свойствами и, таким образом, могут быть специально приспособлены для высвобождения лекарственного или диагностического препарата в ответ на срабатывание конкретного бимолекулярного механизма, такого как pH, отток слизи или иные условия в полости околоносовой пазухи или иной полости уха, носа, горла, где размещено имплантируемое устройство. Нанокапсулы могут применяться в рамках настоящего изобретения в качестве «умного лекарства», обладающего специфичными химическими рецепторами или сайгами связывания, которые связывают специфичные клетки-мишени (например, раковые клетки, ассоциированные с опухолями полости носа или околоносовых пазух, или клетки, ассоциированные с воспалительными процессами).
Необходимо понимать, что вышеизложенное описание настоящего изобретения опирается на конкретные примеры осуществления настоящего изобретения, однако эти примеры или варианты осуществления настоящего изобретения могут быть дополнены, упрощены, изменены или модифицированы без отклонения от предполагаемой сущности и объема изобретения. Например, любой элемент или свойство одного варианта осуществления или примера могут быть объединены или использованы совместно с другим вариантом осуществления или примером, если это не сделает вариант осуществления или пример непригодным для использования по назначению. Кроме того, если этапы способа или процесса описаны или перечислены в определенном порядке, порядок этих этапов может быть изменен, если не указано иное или если такой порядок действий не сделает способ или процесс непригодным для использования по назначению. Все приемлемые дополнения, варианты упрощения, модификации и изменения рассматриваются как аналоги описанных примеров или вариантов осуществления и охватываются прилагаемой формулой изобретения.
Реферат
Изобретение относится к медицине, а именно к оториноларингологии, и может быть использовано при лечении заболеваний околоносовых пазух. Для этого предлагается спейсерная система, содержащая изогнутую направляющую доставки, выполненную с возможностью прохождения через носовое отверстие таким образом, что ее дистальный конец размещен в устье лобной околоносовой пазухи или рядом с ним, а проксимальный конец направляющей размещен снаружи носового отверстия. Удлиненный катетер для доставки вещества, имеющий проксимальный и дистальный конец. Спейсерное устройство, проходящее от дистального конца катетера доставки и сообщающееся по текучей среде с ним. При этом спейсерное устройство включает удлиненный трубчатый ствол с атравматическим наконечником, растяжимый резервуар, в который помещен лекарственный препарат и по меньшей мере два складных удерживающих элемента, выполненных с возможностью прилегания к резервуару и размещения внахлест поверх него. Дополнительно система содержит оболочку, съемно размещенную поверх спейсерного устройства для фиксирования удерживающих элементов в сложенном состоянии. Изобретение обеспечивает эффективную и удобную доставку лекарственного вещества в околоносовые пазухи. 18 з.п. ф-лы, 2 табл., 19 ил., 3 пр.

Комментарии