Электрохимический реактор, содержащий отталкивающую жидкость пористую мембрану - RU2660125C2
Код документа: RU2660125C2
Чертежи













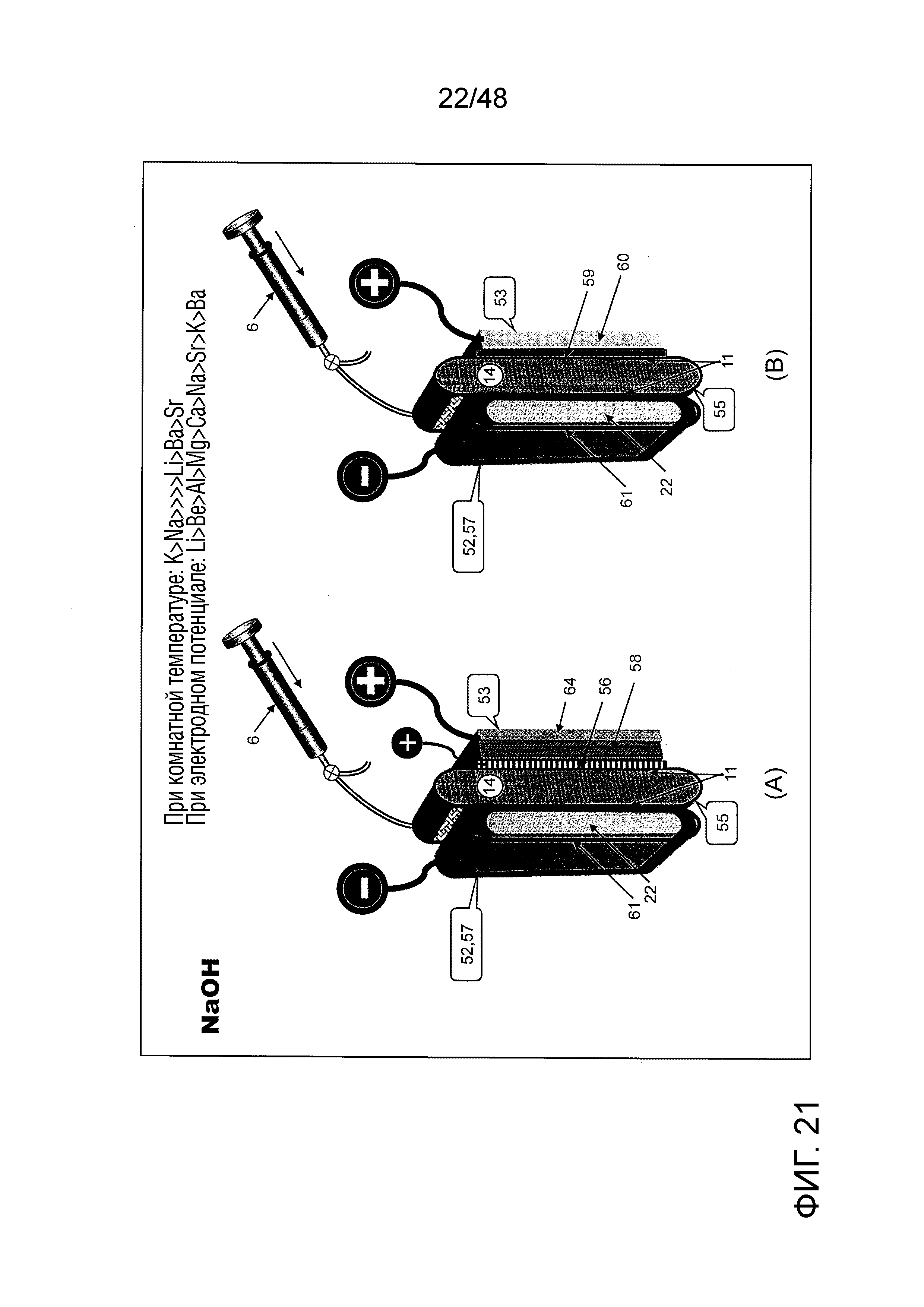


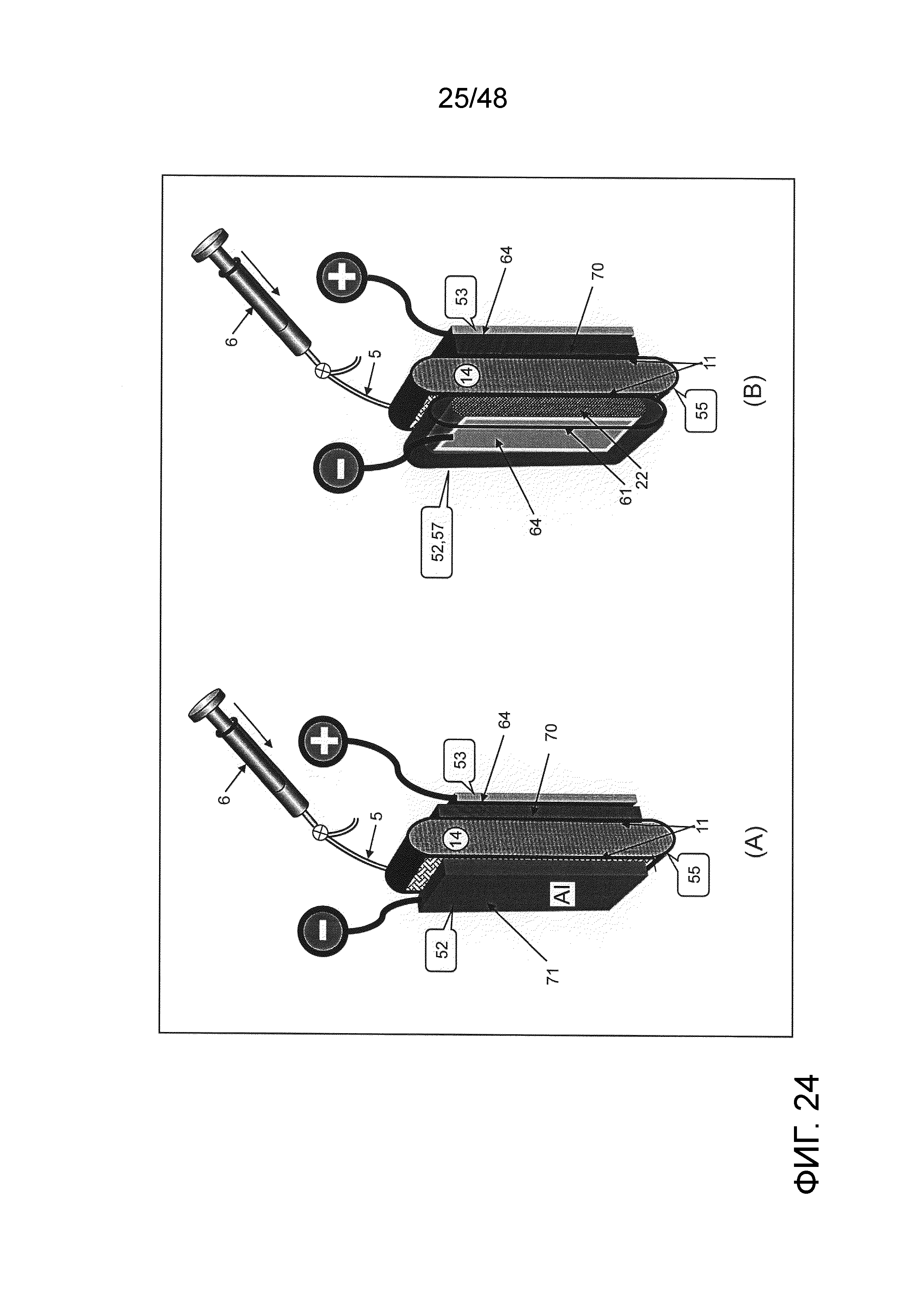

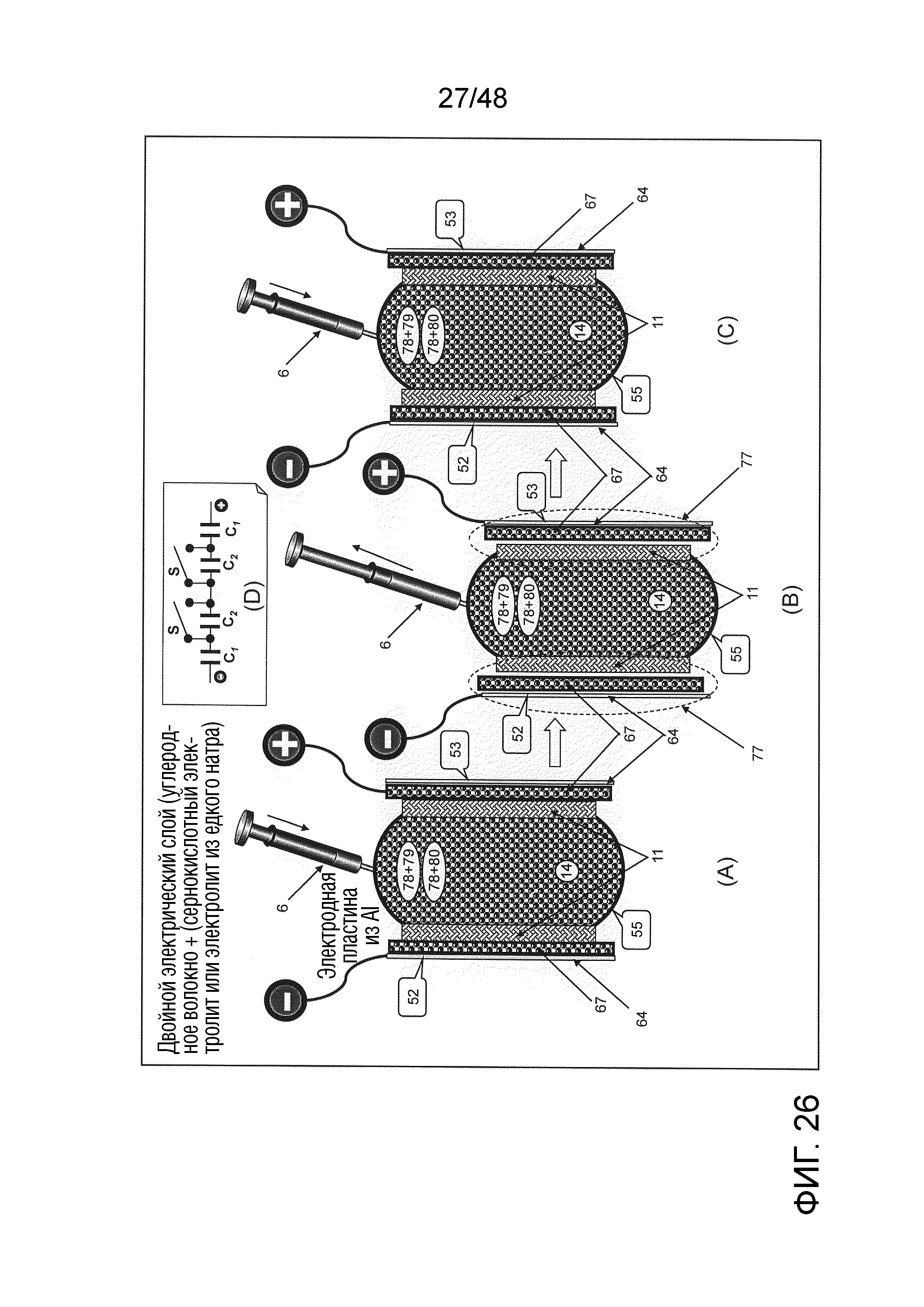
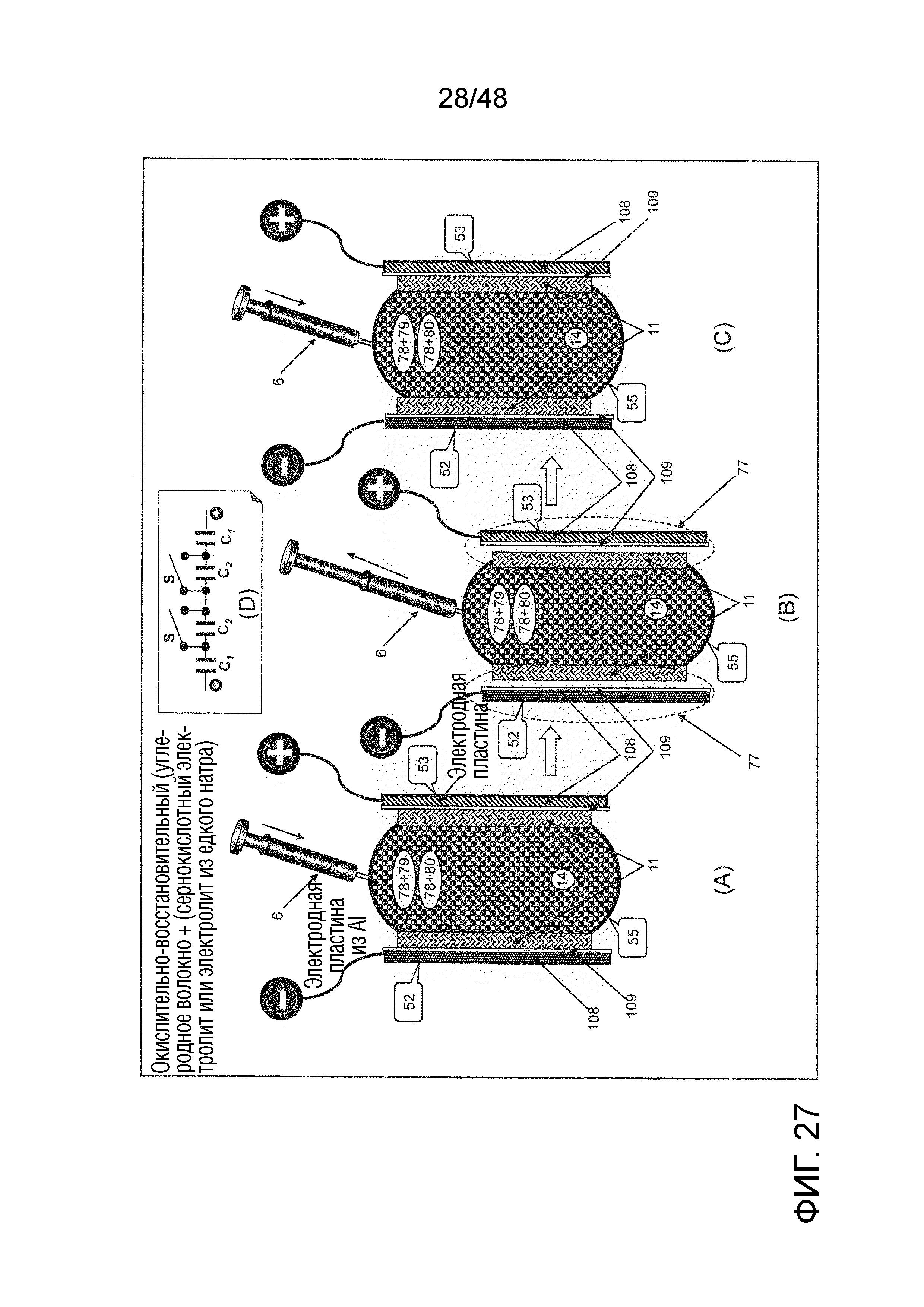













Описание
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
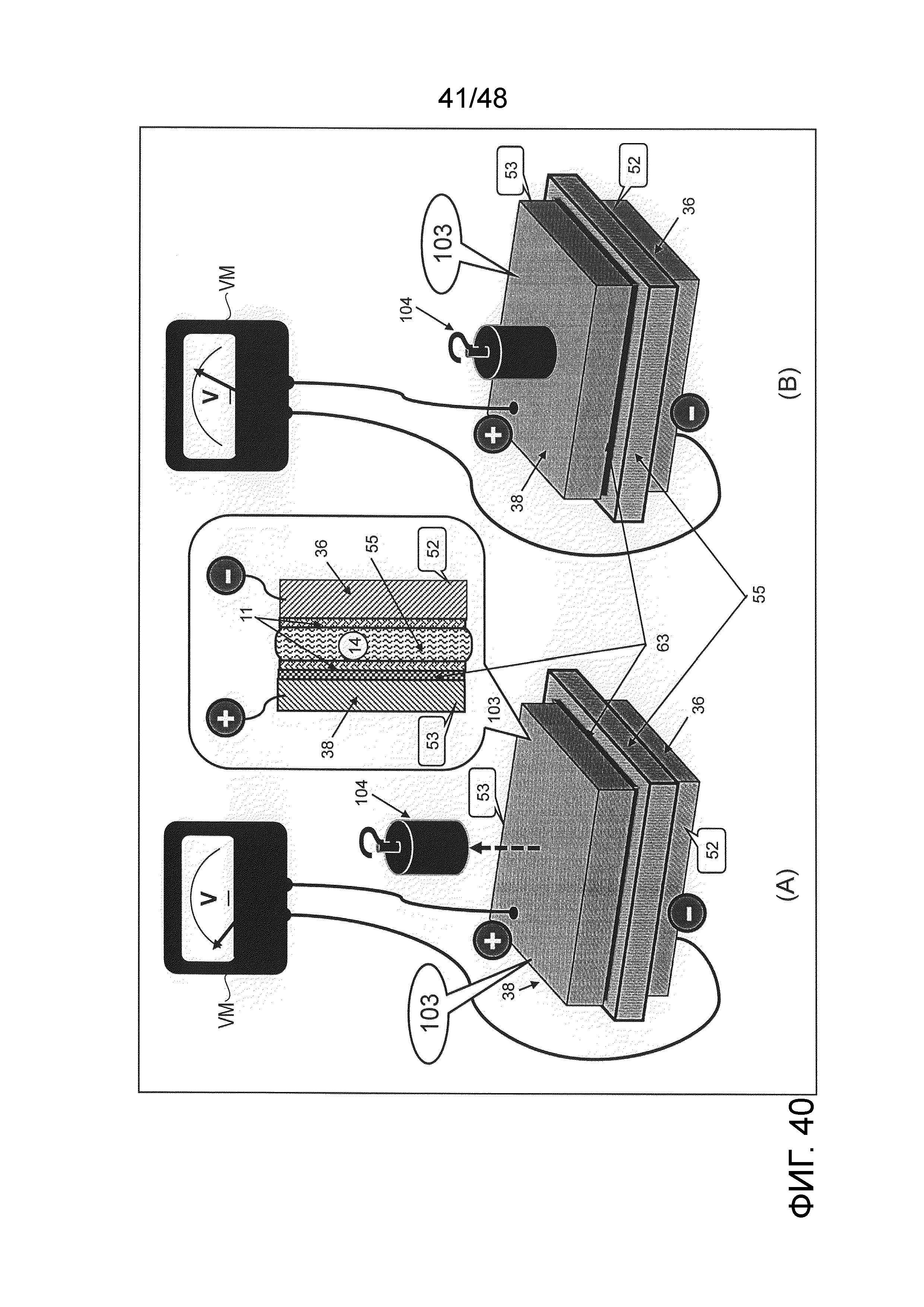
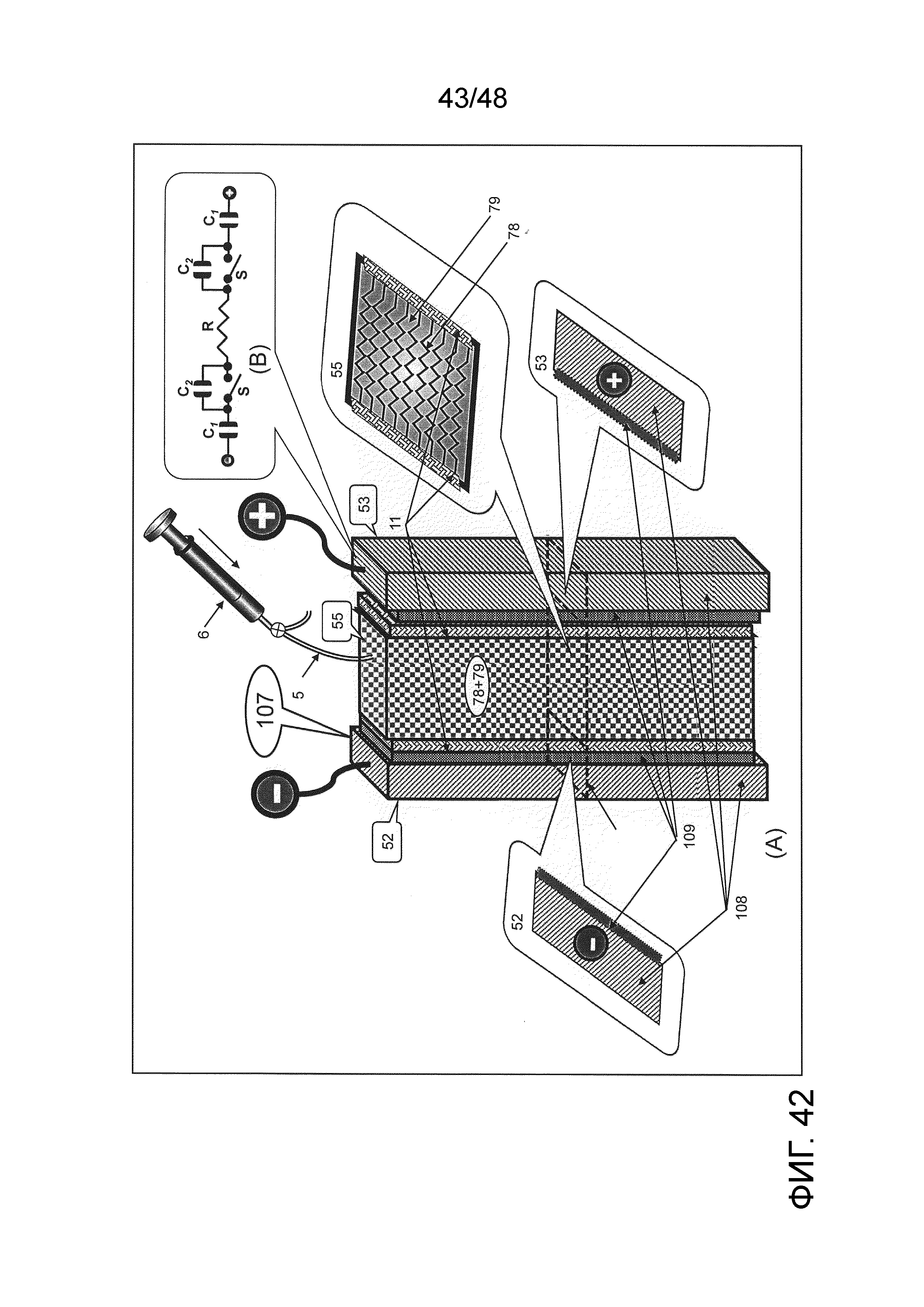
[0001] Настоящее изобретение относится к электрохимическому реактору, включающему в себя устройство электролитического рафинирования, практичную батарею и конденсатор, которые используют сопротивление давлению жидкости отталкивающей жидкость пористой мембраны.
УРОВЕНЬ ТЕХНИКИ
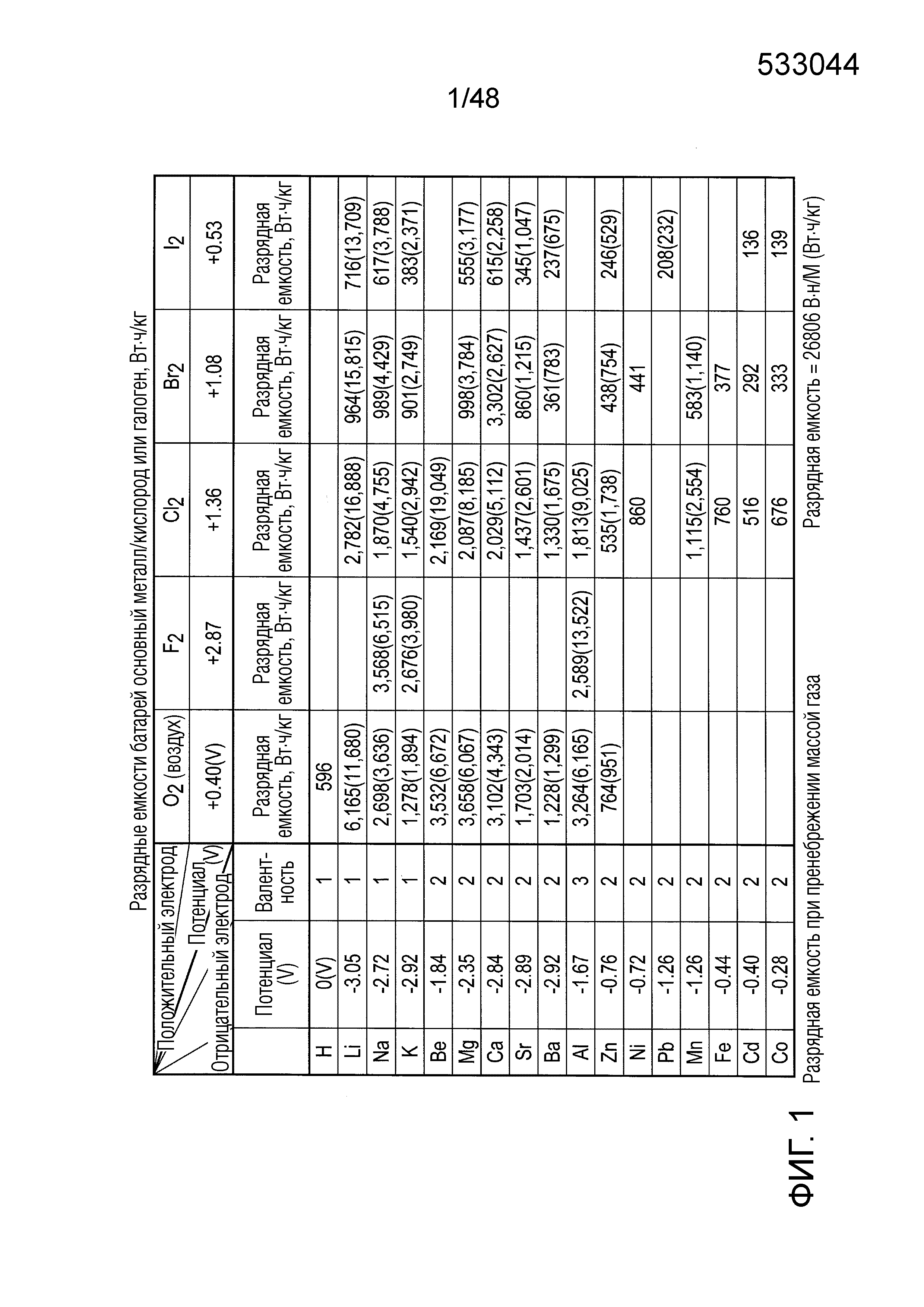
[0002] Элементы - основные металлы, принадлежащие к Группе 1, Группе 2 и Группе 13 Периодической таблицы, ионизируются при контакте с водой и немедленно саморазряжаются, производя водород. По этой причине этим элементам-металлам должно быть строго запрещено контактировать с водой. Таким образом, при электролитическом рафинировании для их осаждения нет никакого другого способа производства, кроме электролиза солевого расплава. Среди практичных батарей отсутствуют первичные или вторичные батареи, которые использовали бы раствор электролита с элементом Ca, Ba или Sr, который принадлежит к Группе 1 или 2 Периодической таблицы. Кроме того, существуют первичные батареи с элементами Be, Mg Группы 2 или алюминием, который является элементом Группы 13 Периодической таблицы, но нет вторичных батарей с этими элементами. В качестве вторичных батарей, которые включают литий-ионные и натрий-ионные вторичные батареи с элементами Группы 1, был разработан неводный раствор электролита (органический электролит) или твердый электролит. Кроме того, для батареи, использующей натрий - элемент из Группы 1, была разработана натрий-серная батарея (NS батарея), которая функционирует при высокой температуре в 300°C или выше и использует натрий в качестве расплавленного солевого электролита.
[0003] Для практичных батарей в настоящее время требуются более легкий материал электрода, более высокая электродвижущая сила и большая разрядная емкость. Следовательно, элементы Группы 1 Периодической таблицы являются идеальными материалами отрицательного электрода, но при этом трудно избежать саморазряда. Причина, по которой эти практичные батареи, устройство электролитического рафинирования и конденсатор испытывают саморазряд, заключается в том, что отрицательный электрод и положительный электрод присутствуют в одном и том же растворе электролита. При таких обстоятельствах существует потребность в срочных технических разработках для предотвращения саморазряда путем разделения электролита и электродов, а также для разъединения элемента основного металла Группы 1, 2 или 13 Периодической таблицы и воды друг от друга.
[0004] Для конденсаторов для хранения электроэнергии (конденсатора) желательны большая емкость и более быстрый заряд и разряд. В качестве конденсатора, который удовлетворяет этим требованиям, идеальным является электрохимический (электролитический) конденсатор, такой как конденсатор с двойным электрическим слоем (ДЭС), окислительно-восстановительный конденсатор или гибридный конденсатор. Недостатками этих конденсаторов являются высокий ток утечки и саморазряд. При таких обстоятельствах существует потребность в срочных технических разработках для подавления тока утечки.
[0005] Саморазряд - это явление, при котором металл отрицательного электрода растворяется и при этом образующиеся электроны и ионы водорода реагируют друг с другом, образуя водород, так что в итоге электроны не движутся к положительному электроду, и поэтому ток не течет. В качестве общего способа подавления саморазряда в водном растворе электролита патентный документ 1 раскрывает, что предусмотрено пористое тело на основе никеля на положительном электроде для щелочной аккумуляторной батареи, и это пористое тело заполнено частицами активного материала, который содержит никель и добавки, уменьшая тем самым саморазряд. Патентный документ 2 раскрывает способ подавления саморазряда путем задания такой формы электрода, которая не уменьшает реальную площадь реакции, даже если площадь противоположного электрода щелочной аккумуляторной батареи увеличивается. Патентный документ 3 раскрывает щелочную батарею с длительным сроком службы, содержащую в качестве сепаратора многослойный элемент из листа, содержащего волокна, содержащие волокна сульфированной полиолефиновой смолы в качестве главного компонента, и листа, подвергнутого гидрофилизирующей обработке, отличающейся от сульфирования, с меньшим саморазрядом и высокой сохранностью емкости. Патентный документ 4 раскрывает электрод для литиевых батарей, в котором тонкие пленки активного материала, которые адсорбируют/высвобождают литий, такие как тонкая пленка микрокристаллического кремния и тонкая пленка аморфного кремния, предусматриваются на коллекторе заряда через прослойку. Патентный документ 5 раскрывает, что в качестве активного электродного материала в литиевой батарее пористый титанат лития является превосходным по свойствам пропитывания неводным электролитом и улучшает циклические характеристики заряда/разряда. Патентный документ 6 раскрывает натриевую вторичную батарею, содержащую положительный электрод из активного материала положительного электрода на углеродной основе, который может адсорбировать и высвобождать анионы, и отрицательный электрод из материала отрицательного электрода, который может адсорбировать и высвобождать Na, которым является, например, Sn или Zn. Что касается натрий-серных батарей, в которых натрий является расплавленным, для формирования солевого расплава требуется температура атмосферы 300°C. Однако патентный документ 7 раскрывает работу батареи при температуре атмосферы в пределах диапазона от 60°C до 130°C, что может быть достигнуто путем использования составного солевого расплава, содержащего два или более типов расплавленных солей MFSI, содержащих бисфторсульфонилимид (FSI) в качестве анионов и щелочной металл М в качестве катионов.
[0006] Что касается изоляционной пленки между электролитом и электродом, то патентный документ 8 раскрывает, что полиолефиновая микропористая мембрана, имеющая диаметр пор 0,1 мкм или меньше, обладает термостойкостью, и поэтому она является подходящей в качестве сепаратора для батареи с высокой емкостью/высокой мощностью. Патентный документ 9 раскрывает, что предусмотрена ламеллярная неорганическая пористая мембрана из кремнезема, глинозема и т.п. на положительном электроде, отрицательном электроде или сепараторе, и поэтому эксплуатационные характеристики батареи могут быть сохранены без ухудшения ионной проводимости. Патентный документ 10 раскрывает, что изоляционная пленка, используемая для неводной вторичной батареи, представляет собой термостойкую пористую мембрану, содержащую хлор, или многослойную пленку из термостойкой смолы и пористого полиолефина, или многослойную пленку из слоя, включающего в себя термостойкую смолу и пористый полиолефин.
[0007] Что касается использования водоотталкивающей пористой мембраны, то патентный документ 11 раскрывает водоотталкивающую пористую мембрану на основе фтора, имеющую пористость от 60 до 90% и воздухопроницаемость 20 секунд или меньше, используемую в твердополимерном топливном элементе. Патентные документы 12, 13 и 14 каждый раскрывают способ производства водоотталкивающей пористой мембраны на основе фтора путем облучения водоотталкивающей пористой мембраны на основе фтора лучом эксимерного лазера в присутствии соединения, содержащего некоторый атом и гидрофильную группу и имеющего энергию связи между ними 128 или более ккал/моль. Кроме того, патентный документ 15 раскрывает способ производства трехмерного элемента в культурой клеток для пациентов, страдающих болезнью Паркинсона, болезнью Альцгеймера, диабетом, остеомаляцией и т.п., в котором внутренние поры водоотталкивающей пористой мембраны на основе фтора замещены гидрофильными группами с помощью фотохимической реакции, вызываемой ультрафиолетовым излучением, и производящими допамин клетками, фиброцитами, способствующими получению коллагена клетками, стволовыми клетками, клетками студенистого ядра, производящими инсулин клетками и т.д., культивируемыми внутри этих пор, которые проявляют гидрофильные свойства. Кроме того, Масатака Мурахара (Masataka Murahara) и др. сообщает в непатентном документе 1, что давление водостойкости водоотталкивающей пористой пленки полимера на основе фтора с диаметром пор 33 мкм составляет 1500 мм рт.ст., но внутренности пор фото-модифицированы так, чтобы быть гидрофильными, для понижения давления водостойкости до 20 мм рт.ст., и модифицированная таким образом пленка используется в клапане регулирования внутриглазной жидкости для пациентов с глаукомой.
СПИСОК ЦИТИРУЕМОЙ ЛИТЕРАТУРЫ
[0008] Патентная литература
Патентный документ 1: JP H9-180714 A
Патентный документ 2: JP 2009-181710 A
Патентный документ 3: JP 2002-63890 A
Патентный документ 4: WO 01/031724
Патентный документ 5: JP 2012-12261 A
Патентный документ 6: JP 2013-54987 A
Патентный документ 7: JP 2009-67644 A
Патентный документ 8: JP 2013-32535 A
Патентный документ 9: JP 2011-222129 A
Патентный документ 10: JP 2009-224097 A
Патентный документ 11: WO 2007/80763
Патентный документ 12: JP 2005-253305 A
Патентный документ 13: USP № 6167497
Патентный документ 14: EP № 0644227
Патентный документ 15: JP 2011-184260 A
Патентный документ 16: JP 2009-295789 A
Патентный документ 17: JP 2013-138050 A
Патентный документ 18: JP 2006-193612 A
Патентный документ 19: JP 2012-30637 A
Патентный документ 20: JP 2013-166406 A.
[0009] Непатентная литература
Непатентный документ 1: Proceeding of SPIE Vol. 4245, P. 221-227-(2001)
Непатентный документ 2: Electric Double Layer Capacitor and Power Storage System Nikkan Kogyo Shimbun (1999)
Непатентный документ 3: Consider Renewable Energy
Непатентный документ 4: «Wind Force» Save Corn From Ethanolization СУЩНОСТЬ ИЗОБРЕТЕНИЯ Технические проблемы [0010] Когда элемент - основный металл, принадлежащий к Группе 1, 2 и 13 Периодической таблицы, растворяется в воде, образующиеся из воды электроны и ионы водорода реагируют друг с другом, образуя газообразный водород. Газообразный водород поглощает электроны, образующиеся на основном металле (отрицательном электроде), и ток прекращает течь от отрицательного электрода к положительному электроду. Это явление называется саморазрядом. Задача настоящего изобретения состоит в том, чтобы предложить практичную батарею, которая подавляет саморазряд, и собирать элемент-основный металл непосредственно электролизом из водного раствора, в котором растворяется элемент-основный металл. [0011] В качестве электролита, используемого для электрохимических конденсаторов, таких как конденсатор с двойным слоем, окислительно-восстановительный конденсатор и гибридный конденсатор, используется сильная кислота или крепкий водный щелочной раствор, как раскрыто в непатентном документе 2. При этом патентный документ 16 раскрывает конденсатор с двойным слоем, включающий в себя первый электрод, второй электрод, первый сепаратор и второй сепаратор, намотанные вокруг сердечника в плоскую форму, в котором намоточный сердечник предусмотрен для того, чтобы увеличить поверхностное давление обоих электродов до определенного уровня или больше и подавить внутреннее сопротивление без увеличения толщины сепараторов, уменьшая таким образом ток утечки. Патентный документ 17 раскрывает, что внутреннее сопротивление уменьшается за счет замены материала электрода окислительно-восстановительного конденсатора с никеля или нержавеющей стали на алюминий или медь. Другая задача настоящего изобретения состоит в том, чтобы подавить внутреннее сопротивление электрохимических конденсаторов, уменьшая тем самым ток утечки. [0012] При электролитическом рафинировании металлов для осаждения только желаемого металла на отрицательном электроде в электролите те металлы, которые имеют меньшую энергию ионизации, чем у водорода, и легко реагируют с водой или кислотой, называются элементами - основными металлами, включая литий, калий, барий, кальций, натрий, магний, алюминий, титан, марганец, цинк, хром, железо, кадмий, кобальт, никель, олово и свинец. Те из них, которые перечислены первыми, более энергично реагируют с водой. Металлы, находящиеся ближе к концу этого списка, труднее реагируют с водой, но они реагируют с кислотой. Однако магний, алюминий, титан и т.п. легко образуют в атмосфере химически устойчивую поверхностную оксидную пленку, и как только такая пленка образуется, они начинают проявлять высокие антикоррозионные свойства даже в воде. В частности, литий, калий и натрий из Группы 1 Периодической таблицы, барий, кальций и магний из Группы 2 и алюминий из Группы 13 энергично реагируют с водой, и поэтому невозможно подвергать электролизу водные растворы солей этих металлов. Следовательно, эти металлы подвергаются электролитическому рафинированию с помощью процесса электролиза солевого расплава, в котором соль металла плавится при высокой температуре и через этот солевой расплав (электролит) пропускается электрический ток. Другая задача настоящего изобретения состоит в том, чтобы выяснить, как осуществлять электролиз солевого расплава в водном растворе электролита. [0013] Как правило батареи, которые нельзя заряжать, называют первичными батареями, а те батареи, которые можно и заряжать, и разряжать, называют вторичными батареями, или аккумуляторными батареями. Желательно, чтобы эти батареи были в состоянии поставлять большее количество электричества и более высокую электродвижущую силу с использованием менее активных материалов. Разность потенциалов между электродами изменяется в зависимости от материалов электродов и концентрации ионов в электролите. Если электродный потенциал иона водорода (H+) принят равным ±0 В, материалы отрицательного электрода имеют потенциалы: Li=-3,045 В>K=-2,925 В>Ba=-2,925 В>Ca=-2,840 В>Na=-2,714 В>Mg=-2,356 В>Be=-1,84 В>Al=-1,67 В>Pb=-1,26 В>Mn=-1,26 В>Zn=-0,76 В>Ni=-0,72 В>S=-0,55 В>Cr=-0,509 В>Fe=-0,44 В>Cd=-0,4 В>Sn=-0,14 В>Cd=-0,4 В>Co=-0,28 В, тогда как материалы положительного электрода имеют потенциалы: Cu=+0,337 В>O2=+0,401 В>Tc=+0,4 В>Ru=+0,46 В>I2=+0,5346 В>Rh=+0,758 В>Ag=+0,7991 В>Pd=+0,915 В>Br2=+1,0874 В>Ir=+1,16 В>Pt=+1,19 В>Cl2=+1,3583 В>Au=+1,68 В>F2=+2,87 В, которые выше, чем (H=±0 В). Для отрицательного электрода практичной батареи требуется легко ионизирующийся металл, тогда как для положительного электрода требуется металл, имеющий чрезвычайно низкую склонность к ионизации или окислитель (который может быть газообразным или жидким). Еще одна задача настоящего изобретения состоит в том, чтобы разработать практичную вторичную батарею, использующую водный раствор электролита с учетом этих электродных потенциалов. [0014] Для того, чтобы предотвратить смешивание продуктов отрицательного электрода и продуктов положительного электрода, таких как металлы, соединения металлов или газы, образующиеся при электролитическом рафинировании или электролизе электролита в практичной батарее, требуется изоляционная пленка (сепаратор). Среди требований к этой изоляционной пленке наиболее важным является то, чтобы эта пленка могла пропускать ионы, но не вещества или электролиты. Дополнительно требуется, чтобы изоляционная пленка имела высокое сопротивление изоляции, была устойчивой к кислотам или щелочам, теплу или вибрации, была механически прочной и имела длительный срок службы. Традиционно в качестве изоляционной пленки использовался материал бисквитного обжига, твердый электролит, фильтровальная бумага и т.д. Из них керамические твердые электролиты, включающие в себя глинозем, являются наиболее подходящими для разделения водного раствора электролита и продукта отрицательного электрода, но такие керамические твердые электролиты должны быть помещены в среду с высокой температурой для того, чтобы они могли функционировать в качестве электролитов. Из твердых материалов диафрагма бисквитного обжига может использоваться в водном растворе электролита, но водный раствор свободно проникает внутрь диафрагмы бисквитного обжига, и поэтому влага не может быть заблокирована. Это также справедливо и для фильтровальной бумаги. Следовательно, еще одна задача настоящего изобретения состоит в том, чтобы разработать пленку, которая могла бы блокировать электродную часть и водный раствор электролита друг от друга и дополнительно, при необходимости, могла бы управлять входом и выходом ионов. Средства решения проблем [0015] В решении обычных проблем настоящее изобретение отличается от обычного способа тем, что водоотталкивающая пористая пленка фторкаучука используется как изоляционная пленка в качестве переключателя давления. Традиционно при протекающей в водном растворе электрохимической реакции положительный и отрицательный электроды устанавливаются в водном растворе электролита. При такой конструкции во время электрохимической реакции трудно избежать явления изоляции, вызываемого газом, образующимся на границе раздела между водным раствором электролита и электродом. В соответствии с настоящим изобретением положительный электрод и отрицательный электрод, вставленные к водный раствор электролита, электрически изолируются и отделяются друг от друга водоотталкивающей пористой мембраной, и только когда происходит электрохимическая реакция, водный раствор электролита оказывается под повышенным давлением, которое вызывает заполнение мелких пор в водоотталкивающей пористой мембране водным раствором электролита, придавая ей таким образом роль переключателя электрической цепи для того, чтобы изоляционная пленка превращалась из изолятора в электрический проводник только во время повышения давления. В частности, в практичной батарее, водный раствор электролита герметизируется в мешке, выполненном из водоотталкивающей пористой мембраны, и батарея заряжается/разряжается при сжатии мешка из водоотталкивающий пористой мембраны, и давление снимается при накоплении электричества. При снятии давления электрод и электролит изолируются друг от друга, тем самым исключая увеличение саморазряда или внутреннего сопротивления. Кроме того, при электролизе (электролитическом рафинировании) электрод также не находится полностью в контакте с водным раствором электролита, что уменьшает шансы того, что продукты на каждом электроде снова растворятся в электролите, тем самым исключая явление изоляции, вызываемое между электродом и водным раствором электролита образующимся на электродах газом. Кроме того, когда сетчатый отрицательный электрод предусмотрен на границе раздела между водным раствором электролита и маслом, изолированным водоотталкивающей пористой мембраной, и водный раствор электролита подвергается электролизу при повышении давления водного раствора электролита, продукт отрицательного электрода осаждается в масле с обратной стороны сетчатого электрода. В этом случае при использовании водного раствора соли основного металла в качестве электролита элемент-основный металл, который является «не любящим воду» металлом (элементом Группы 1 или 2 Периодической таблицы, который энергично реагирует с водой), может быть осажден в масле, а, кроме того, может быть выполнено разделение в тяжелой жидкости (классификация под действием силы тяжести). [0016] Самым простым способом избежать контакта между соединением элемента-основного металла и водой является использование расплавленной соли элемента-основного металла. Безводная расплавленная соль является идеальной жидкостью-электролитом. Однако для того, чтобы получить расплавленную соль, необходимо поддерживать соль элемента-основного металла при температуре, большей или равной температуре плавления. Следовательно, количество потребляемого тепла не является незначительным. При этих обстоятельствах широко распространено приготовление смешанного солевого расплава путем смешивания с другой солью металла для того, чтобы понизить температуру плавления соли. Патентный документ 15 показывает на своей Фиг. 2 соотношение между смешанными солями и их температурами плавления соответственно. Находящимися в жидком состоянии при обычной температуре элементами, которые существуют в природе, являются только ртуть и бром, а другие элементы не могут быть превращены в жидкость при обычной температуре. При этом, если электролиз может быть осуществлен в то время, как основный металл и электролит в виде водного раствора соли основного металла изолированы друг от друга, могут быть реализованы электролитическое рафинирование и практичная вторичная батарея. Конечной задачей настоящего изобретения является разработка такой изоляционной пленки. Необходимые и достаточные условия для изоляционной пленки состоят в том, чтобы пленка имела превосходные свойства удержания жидкости для раствора электролита, а также низкое электрическое сопротивление. В настоящем изобретении для решения этой задачи используется пленка фторкаучука, которая демонстрирует водоотталкивающее свойство по отношению к водному раствору. При использовании пленки фторкаучука могут поддерживаться не только превосходные свойства удержания жидкости для электролита, но и нулевое электрическое сопротивление. Кроме того, пленка фторкаучука может использоваться в качестве пористой мембраны, и через нее могут проходить ионы. Таким образом, если давление водного раствора электролита повышается на величину, равную давлению водостойкости водоотталкивающей пористой пленки фторкаучука, может быть реализована ионопроницаемая пленка. Приложение давления водостойкости выполняет роль механического переключателя на нулевое электрическое сопротивление/проводимость. [0017] Как было описано, при электролитическом рафинировании или зарядке и разрядке практичной батареи или конденсатора водный раствор электролита подвергается воздействию давления, равного давлению водостойкости, а во время хранения заряда давление не прикладывается; следовательно, свойства удержания жидкости для электролита могут быть сохранены. Таким образом, во время хранения заряда активные материалы положительного и отрицательного электродов находятся в изолированном состоянии, и поскольку активные материалы не реагируют, нет никакого естественного разряда. Кроме того, материал изоляционной пленки является фторкаучуком, и поэтому он является превосходным по стойкости к щелочам, стойкости к кислотам и стойкости к воздействию химикатов даже при высокой температуре (примерно 80°C). Кроме того, эта пленка обладает превосходной механической прочностью, пластичностью и термостойкостью. Кроме того, во время зарядки и разрядки давление прикладывается со стороны водного раствора электролита, и поэтому пленка вступает во время работы в плотный контакт с электродом. Считается, что лучшим способом решения поставленной задачи является использование водоотталкивающей пористой пленки фторкаучука в качестве диафрагмы, как описано выше. [0018] В случае конденсатора, если диэлектрик является только изолятором, таким как масло, внутренним сопротивлением между положительным и отрицательным электродами можно пренебречь, но когда диэлектрики и электропроводящие материалы составляют эквивалентные схемы, электрически объединенные параллельно или последовательно, внутреннее сопротивление служит току утечки. В частности, в электрохимических конденсаторах, таких как конденсатор с двойным электрическим слоем, окислительно-восстановительный конденсатор и гибридный конденсатор, неизбежно увеличение внутреннего сопротивления электролитом внутри электрода или между электродами. В дополнение к этому, в случае водного электролита жидкость может также протекать. Таким образом, в настоящем изобретении для того, чтобы предотвратить утечку жидкости и электрическую утечку во время хранения заряда, водный раствор электролита, такой как сильная кислота или сильная щелочь, заключается в мешок, выполненный из водоотталкивающей пористой пленки фторкаучука, и этот мешок, выполненный из водоотталкивающей пористой пленки фторкаучука, располагается между парой электродов, состоящей из положительного электрода и отрицательного электрода. Во время зарядки и разрядки прикладывается давление водостойкости водоотталкивающей пористой мембраны, приводя поверхности обоих электродов и водного раствора электролита в контакт друг с другом. Кроме того, электропроводящий материал с пустотами, например, из металлических волокон или углеродных волокон, заключается вместе с электролитом в мешок из водоотталкивающей пористой пленки фторкаучука. При такой конструкции во время зарядки и разрядки, при которых водный раствор электролита сжимается, электрическое сопротивление между водными растворами электролита мало, тогда как во время аккумулирования электричества, при котором давление на водный раствор электролита снимается, водный раствор электролита, находящийся во внутренних порах водоотталкивающей пористой пленки фторкаучука, удаляется из внутренних пор. Таким образом, пленка начинает функционировать как слабый диэлектрик, и саморазряд подавляется. С другой стороны, во время зарядки и разрядки поры водоотталкивающей пористой пленки фторкаучука заполняются электролитом под действием давления водного раствора электролита, трансформируя ее в электропроводящую. Таким образом, конденсатору с двойным электрическим слоем или окислительно-восстановительному конденсатору придается высокий заряд. [0019] Непатентный документ 1 показывает на своей Фиг. 6 водоотталкивающую пористую пленку фторкаучука (вспененного политетрафторэтилена, вПТФЭ или ePTFE), имеющую диаметр пор 3 мкм и толщину 100 мкм, у которой разность давлений (перепад давления) между обеими сторонами пленки в то время, когда жидкость начинает проникать, принят(а) за давление водостойкости пленки. Этот документ указывает, что когда в качестве раствора используется физиологический раствор (сбалансированный солевой раствор, BSS), давление водостойкости составляет 300 мм рт.ст., выше которого поток физиологического раствора увеличивается. При этом, если водоотталкивающая пористая пленка фторкаучука рассматривается как электроизоляционная пленка, она функционирует в качестве изоляционной пленки тогда, когда перепад давления между обеими сторонами пленки является более низким, чем давление водостойкости, и жидкость начинает проникать через нее при достижении давления водостойкости, в результате чего эта пленка начинает функционировать в качестве проводящей пленки. Основной признак настоящего изобретения заключается в использовании давления водостойкости водоотталкивающей пористой мембраны в качестве переключателя давления для пропускания ионов. В частности, поскольку фторкаучуки проявляют водоотталкивающие свойства, водный раствор не входит в поры пористой пленки-мембраны, когда перепад давления между обеими сторонами мембраны меньше, чем давление водостойкости. Кроме того, давление водостойкости может меняться в зависимости от диаметра пор или концентрации соли электролита. Соотношение между концентрацией соли у пористой фторкаучуковой мембраны (имеющей диаметр пор 3 мкм) и осмотическим давлением между обеими сторонами мембраны является следующим. Давление водостойкости в воде (без солей; аналогично в дальнейшем) составляет 430 мм рт.ст.; при концентрации хлорида натрия 10%-330 мм рт.ст.; а при концентрации хлорида натрия 20%-280 мм рт.ст. Таким образом, чем выше концентрация электролита, тем более низким становится давление водостойкости. Соотношение между концентрацией соли у пористой фторкаучуковой мембраны (имеющей диаметр пор 10 мкм) и осмотическим давлением между обеими сторонами мембраны является таким, что давление водостойкости в воде составляет 130 мм рт.ст., 7 мм рт.ст., когда концентрация хлорида натрия составляет 1%, и 50 мм рт.ст., когда концентрация хлорида натрия составляет 2%; таким образом, давление водостойкости в этих случаях является низким. Таким образом, если используется двухпозиционная (ВКЛ/ВЫКЛ) работа давления водостойкости водоотталкивающей пористой мембраны, могут быть реализованы электролитическое рафинирование и практичная батарея в водном растворе электролита. [0020] Разности потенциалов материалов отрицательного электрода практичной батареи составляют: Li=Li+=-3,045 В, K=K+=-2,925 В, Ba=Ba2+=-2,925 В, Sr=Sr2+=-2,89 В, Ca=Ca2+=-2,840 В, Na=Na+=-2,714 В, Mg=Mg2+=-2,356 В и Al=Al3+=-1,67 В. Их плотности составляют Li: 0,54, K: 0,86, Na: 0,97, Ca: 1,55, Mg: 1,74, Sr: 2,54, Al: 2,6, Ba: 3,51, Fe: 7,87, Cu: 8,96 и Pb: 11,35 соответственно. С другой стороны, в терминах количества выдаваемого тока алюминий (Al) производит трехвалентные ионы, а магний (Mg), барий (Ba), кальций (Ca) и т.п. производят двухвалентные ионы. В практичной батарее желательно, чтобы был уменьшен саморазряд, при котором запасенное количество электричества постепенно уменьшается со временем, а также было уменьшено внутреннее сопротивление. Кроме того, во вторичной батарее желательно, чтобы во время зарядки не образовывался водород, а омическое сопротивление и поляризация во время зарядки должны быть низкими. Кроме того, на практике желательно, чтобы состояние регенерации после заряда и разряда было превосходным и обеспечивало возможность повторного использования. Однако на практике нет такого электродного материала, который мог бы удовлетворять всем этим условиям. Например, в случае материала отрицательного электрода литий, который имеет самую высокую электродвижущую силу, энергично реагирует в присутствии воды с образованием водорода, что вызывает саморазряд и блокирует поток электронов. [0021] В качестве решения этой проблемы настоящее изобретение предлагает следующее. Для удобства определим теоретическую эффективность выработки электроэнергии как VI/g, где V означает потенциал ионизации отрицательного электрода, I означает плотность тока=валентность, а g означает плотность (г/см3). Металлы будут перечислены в порядке убывания значения VI/g. Таким образом, Li=-3,045×1/0,54=-5,64; Ca=-2,84×2/1,55=-3,66; K=-2,925×1/0,86=-3,40; Na=-2,724×1/0,97=-2,81; Mg=-2,356×2/1,74=-2,71; Al=-1,67×3/2,6=-1,92; Ba=-2,925×2/3,51=-1,67; Sr=-2,89×2/2,54=-1,57; S (отрицательная двухвалентная)=-0,55×2/2,07=-0,53; Mn=-1,1×2/7,42=-0,3; Zn=-0,76×2/7,12=-0,27; Pb=-0,13×2/11,34=-0,23; Cr=-0,51×3/7,2=-0,21; Fe (двухвалентное)=-0,44×2/7,876=-0,11; Sn=-0,14×2/7,28=-0,04; и Fe (трехвалентное)=-0,04×3/7,86=-0,015. [0022] Для положительного электрода практичной батареи требуется металл, имеющий очень малую склонность к ионизации, или окислитель (который может быть газообразным или жидким). Их предпочтительными примерами являются: в качестве металла: Sb=Sb3+=+0,2 В, Bi=Bi3+=+0,28, Cu=Cu2+=+0,345, Hg=Hg2+=+0,793, Ag=Ag+=+0,808, Hg=Hg3+=+0,86; или в качестве окисляющего газа или жидкости: O2=ОН-=+0,4 В, Br2=Br-=+1,08 В, Cl2=Cl-=+1,36 В, F2=F-=+2,87, пермарганатная соль, хромовая кислота, азотная кислота, галоген, перекись, оксид, соль металла, кислород и серная кислота. Их плотности составляют: Sb: 6,69; Bi: 8,8; Cu: 8,93; Hg: 13,59; Ag: 10,5; O2: 1,429; Br2 (жидкий): 3,14; Cl2: 3,21; и F2: 1,696. Металлы будут перечислены в порядке убывания теоретической эффективности выработки электроэнергии VI/g, полученной из потенциала ионизации положительного электрода (V), плотности тока=валентности (I) и плотности g (г/см3). Таким образом, F2=+2,87×1/1,696=+1,692; Cl2=+1,36×1/3,21=+0,424; Br2=+1,08×1/3,14=+0,344; O2=+0,4×1/1,429=+0,28; Hg (трехвалентная)=+0,86×3/13,59=+0,19; Hg=+0,793×2/13,59=+0,117; Bi=+0,28×3/8,8=+0,095; Sb=+0,2×3/6,69=+0,09; Cu=+0,345×2/8,93=+0,077; и Ag=+0,808×1/10,5=+0,077. Следовательно, в качестве идеального сочетания электродов, которое обладает самой высокой электродвижущей силой, нужно использовать литий для отрицательного электрода и F2 для положительного электрода, и электродвижущая сила этой пары составляет 5,915 В (= +2,87-(-3,045)). Как описано, газообразный фтор (F2=-2,87 В) дает наибольшую электродвижущую силу на положительном электроде, но он является чрезвычайно токсичным и поэтому обычно используется газообразный кислород (O2=-0,4 В). При этом в батарее кислород(воздух)/основный металл положительным электродом является воздух, и поэтому емкость является бесконечной. Однако на поверхности отрицательного электрода батареи кислород/основный металл, магний (Mg), алюминий (Al), цинк (Zn) и т.д., используемые в качестве материалов отрицательного электрода, окисляются с образованием изоляционной пленки на поверхности электрода, блокирующей поток электронов. В данном случае, при использовании водоотталкивающей пористой пленки фторкаучука по настоящему изобретению, саморазряд может быть подавлен, и поэтому окисление поверхностей электрода может быть предотвращено. [0023] При электролитическом рафинировании количество электричества, требуемого для осаждения (разложения) эквивалентной 1 г массы (Eq) металла как продукта отрицательного электрода при электролизе электролита, составляет 1 Фарадей (Ф)=96500 кулон (Eq=молекулярная масса (M)/валентность (n) иона). Поскольку сила тока, получаемая, когда количество электричества в 1 кулон протекает за одну секунду, определяется как 1 A, количество электричества для тока в А ампер, протекающего в течение t секунд, (Q кулон) составляет: Q=At. Здесь количество (m) металла, осаждаемого в качестве продукта отрицательного электрода, получается из формулы: m=Eq×Q/96500=Eq×At/96500 (m:Q=Eq:96500). [0024] Количество энергии, накопленной в практичной батарее, эквивалентно количеству электроэнергии, требуемой для электролитического рафинирования, и поэтому ток (A), требуемый для осаждения m (г) за 1 секунду, получается из формулы: A=m x 96500/Eq×t. Следовательно, ток (А), требуемый для осаждения 1 кг за 1 час, получается из формулы: A=1000×96500/(Eq×3600)=26806/Eq. [0025] Разрядная емкость на единицу времени и единицу массы практичной батареи (массовая плотность энергии, накопленной в батарее (Вт × время (ч)/кг)=напряжение (В) × количество электричества (A×ч)/плотность электрода (кг)=ВAч/кг=Вт·ч/кг), определяется как 26806×V×n/М [Вт·ч/кг] (V: электродвижущая сила, М: массовое число реагента, n: валентность). Разрядные емкости (Вт·ч/кг) в зависимости от сочетаний различных типов материалов отрицательного электрода из основного металла и различных типов газовых материалов положительного электрода (кислород или галоген), получаемые, когда эта формула применяется к практичной батарее, представлены на Фиг. 1. Следует отметить, что разрядные емкости в случае, когда масса газа материала положительного электрода не учитывается (масса равна нулю), заключены в скобки в следующем списке. Батареи основный металл/галоген, в частности, показывают высокие привлекательные электродвижущие силы и поэтому являются предпочтительными. Например, могут быть получены следующие данные: Li/Cl2 (16,888)>Li/Br2 (15,815)>Li/I2 (13,709)>Al/F2 (13,522)>Al/Cl2 (9,025)>Mg/Cl2 (8,185)>Na/F2 (6,515)>CaBr2 (5,254)>Ca/Cl2 (5,112)>Na/Br2 (4,429)>K/F2 (3,980)>Na/I2 (3,788)>Mg/Br2 (3,784)>Mg/I2 (3,177). Однако в данном случае необходимо работать с газообразным галогеном, что сопровождается опасностью и требует осторожности в обращении. С другой стороны, в случае основного металла/кислорода, в качестве положительного электрода может использоваться воздух. Следовательно, возможно обеспечить безопасную и легкую батарею. Батареи, в которых кислород используется для положительного электрода, будут теперь перечислены в порядке убывания разрядной емкости: Li/O2 (11,680)>Be/O2 (6,672)>Al/O2 (6,165)>Mg/O2 (6,067)>Ca/O2 (4,343)>Na/O2 (3,636). [0026] Таким образом, во-первых, настоящее изобретение предлагает, в соответствии с первым аспектом, электрохимический реактор, содержащий положительный электрод с первой главной поверхностью и второй главной поверхностью на стороне, противоположной первой главной поверхности; отрицательный электрод с первой главной поверхностью и второй главной поверхностью на стороне, противоположной первой главной поверхности, причем положительный электрод и отрицательный электрод обращены друг к другу своими первыми главными поверхностями и расположены отстоящими друг от друга, образуя пространство между собой; электропроводящую жидкость и/или диэлектрическую жидкость, заполняющую это пространство; первый изоляционный элемент (средство изоляции) (раствора), предусмотренный(ое) на первой поверхности положительного электрода для изолирования положительного электрода от жидкости, причем первый изоляционный элемент содержит первую отталкивающую жидкость пористую мембрану, имеющую множество пор; второй изоляционный элемент (средство изоляции) (раствора), предусмотренный(ое) на первой поверхности отрицательного электрода для изолирования отрицательного электрода от жидкости, причем второй изоляционный элемент содержит вторую отталкивающую жидкость пористую мембрану, имеющую множество пор; и прикладывающий давление элемент, который сжимает жидкость, чтобы заполнить множество пор первой и второй отталкивающих жидкость пористых мембран этой жидкостью, тем самым вызывая электрохимическую реакцию с участием положительного электрода и отрицательного электрода. [0027] В одном варианте осуществления настоящего изобретения отталкивающая жидкость пористая мембрана может быть образована из фторкаучука, полипропиленовой смолы или полиэтиленовой смолы, а жидкость является водным раствором электролита, на который может оказываться давление, равное давлению жидкостойкости отталкивающей жидкость пористой мембраны. [0028] В другом варианте осуществления отталкивающая жидкость пористая мембрана образована из фторкаучука, а жидкость является маслом, на которое может оказываться давление, равное давлению жидкостойкости отталкивающей жидкость пористой мембраны. [0029] В еще одном варианте осуществления отталкивающая жидкость пористая мембрана выполнена из пористого углерода, а жидкость может быть электролитом из солевого расплава. [0030] Кроме того, в одном варианте осуществления настоящего изобретения первая отталкивающая жидкость пористая мембрана и вторая отталкивающая жидкость пористая мембрана объединяются вместе, составляя герметичный контейнер. Внутренность этого герметичного контейнера может соответствовать пространству между электродами. Кроме того, в другом варианте осуществления первая отталкивающая жидкость пористая мембрана и вторая отталкивающая жидкость пористая мембрана могут быть отдельными друг от друга пленками. Кроме того, положительный электрод и отрицательный электрод могут быть предусмотрены соответственно в камере положительного электрода и в камере отрицательного электрода, чьи отверстия, находящиеся напротив друг друга, закрыты соответствующими отталкивающими жидкость пористыми мембранами. [0031] Электрохимический реактор по настоящему изобретению может быть электролитическим устройством, первичной батареей, вторичной батареей или конденсатором. [0032] В электрохимическом реакторе, когда к проводящей или диэлектрической жидкости прикладывается заданное давление, эта жидкость входит в поры каждой водоотталкивающей пористой мембраны, приводя каждый электрод в контакт с жидкостью, тем самым вызывая желаемую электрохимическую реакцию (в которой участвуют положительный электрод и отрицательный электрод). Когда это давление снимается, контакт между каждым электродом и жидкостью исчезает. Таким образом, изоляционная пленка функционирует как двухпозиционный переключатель (ВКЛ/ВЫКЛ), чтобы активировать/дезактивировать электрохимическую реакцию путем приложения или неприложения заданного давления. [0033] Принцип действия двухпозиционного переключателя из водоотталкивающей пористой мембраны (изоляционной пленки) показан на Фиг. 2. Таким образом, герметичный контейнер 1, выполненный из водоотталкивающей пористой мембраны 11, располагается между камерой 3 отрицательного электрода, вмещающей в себя отрицательный электрод, и камерой 4 положительного электрода, вмещающей в себя положительный электрод, и водный раствор 14 электролита находится в герметичном контейнере 1. При этом, как показано на Фиг. 2(A), когда к водному раствору 14 электролита с помощью прикладывающего давление элемента 6 (например, цилиндрического груза) прикладывается давление меньшей величины, чем давление водостойкости водоотталкивающей пористой мембраны 11 (на фигуре - «без давления»), раствор электролита не входит в поры водоотталкивающей пористой мембраны 11, и поэтому вольтметр VM показывает состояние электроизоляции как ноль. С другой стороны, как показано на Фиг. 2(B), когда к водному раствору 14 электролита прикладывается давление с помощью прикладывающего давление элемента 6, водный раствор электролита входит в поры водоотталкивающей пористой мембраны 11, что заставляет вольтметр VM отклониться в положительную сторону, показывая электродвижущую силу. [0034] В ограниченной области электрических применений водоотталкивающая пористая мембрана может использоваться для электролитических устройств, практичных батарей или конденсаторов (см. Фиг. 3A и Фиг. 3B). В электрохимическом реакторе по настоящему изобретению (электролитическом устройстве, практичной батарее или конденсаторе) заряд/разряд осуществляется путем приложения к жидкости заданного давления (давления жидкостойкости) и останавливается при давлении меньшем, чем это заданное давление. Таким образом, отталкивающая жидкость пористая мембрана (изоляционная пленка) позволяет порам пропускать раствор и ионы при приложении к жидкости давления, равного давлению жидкостойкости, и поэтому функционирует в качестве переключателя для создания электропроводящего состояния, то есть в качестве электронного двухпозиционного переключателя. [0035] Здесь давление водо(жидко)стойкости отталкивающей воду (жидкость) пористой мембраны является разностью давлений между давлением на входной стороне (первичной стороне) отталкивающей воду (жидкость) пористой мембраны и давлением на выходной стороне (вторичной стороне) и представляет собой минимальный перепад давления, при котором жидкость может войти в поры пористой мембраны. Жидкость находится с одной стороны мембраны, а с другой стороны мембраны находится газ или жидкость. Жидкость может быть водным раствором электролита или неэлектролита, диэлектрической жидкостью, такой как масло или чистая вода, или раствором солевого расплава на основе основного металла. Газ может быть водородом, кислородом, газообразным хлором или т.п., образующимся на отрицательном электроде или положительном электроде при электролизе водного раствора, или водородом, нагнетаемым в солевой расплав. [0036] Жидкости могут быть классифицированы на электропроводящие материалы и диэлектрические материалы в соответствии с их электрическими свойствами. Проводящие жидкости включают водные растворы электролита и электролиты из солевого расплава, и водные растворы электролита используются для электролиза, батарей или электрохимических конденсаторов. В этом случае отталкивающая жидкость пористая мембрана может быть образована из фторкаучука, полипропиленовой смолы или полиэтиленовой смолы, и, как было описано выше, эта мембрана функционирует в качестве электронного переключателя. Когда раствор является электропроводящим материалом солевого расплава, используется пористая углеродная пленка, функционирующая и как изоляционная пленка, и как отрицательный электрод солевого расплава, и производится гидрид металла в процессе, в котором анионы газообразного водорода мигрируют от стороны отрицательного электрода к стороне положительного электрода в солевом расплаве. С другой стороны, диэлектрические жидкости включают в себя жидкости на основе масла и водные жидкости, и жидкости на основе масла могут использоваться для сбора продуктов отрицательного электрода, извлечения продуктов из элемента, функционирующего и как масляный конденсатор, и как отрицательный электрод, или для масляного конденсатора. В частности, при сборе продуктов отрицательного электрода элемент Группы 1 Периодической таблицы отделяется от воды и подвергается классификации под действием силы тяжести в масле, тогда как при сборе продуктов масляных конденсаторов и отрицательного электрода масляной стороне придается заряд, превращая границу раздела водного раствора электролита и масла в поверхность отрицательного электрода, на которой продукты отрицательного электрода подвергаются классификации под действием силы тяжести на масляной стороне. [0037] При применении только к конденсаторам, нитробензол и масло, которые имеют высокую диэлектрическую постоянную, используются в качестве масляных конденсаторов, тогда как чистая вода, муравьиная кислота и т.п. используются в качестве водных конденсаторов. Конденсатор имеет такую конструкцию, что положительная электродная пластина, водоотталкивающая пористая мембрана, диэлектрический раствор, водоотталкивающая пористая мембрана и отрицательная электродная пластина располагаются в указанном порядке. Для зарядки/разрядки диэлектрический раствор прижимается при давлении жидкостойкости к водоотталкивающей пористой мембране для того, чтобы заполнить внутренность водоотталкивающей пористой мембраны диэлектрическим раствором. При хранении заряда гидравлическое давление диэлектрического раствора снимается для того, чтобы освободить водоотталкивающую пористую мембрану от диэлектрического раствора, и сама водоотталкивающая пористая мембрана функционирует как конденсатор с низкой диэлектрической постоянной. Таким образом, при аккумулировании электричества берется конструкция из трех последовательных конденсаторов, в которой конденсатор с высокой диэлектрической постоянной располагается между двумя конденсаторами с низкой диэлектрической постоянной, тогда как при зарядке и разрядке берется конструкция из одного конденсатора. [0038] С другой стороны, когда изоляционная пленка является твердым диэлектриком, который проявляет маслоотталкивающие свойства, и, в частности, является фторкаучуком, масло должно быть примешано в водный раствор. Так как фторкаучук проявляет липофильные свойства, масло адсорбируется на поверхности фторкаучука. За счет использования этого свойства небольшое количество масла примешивается в водный диэлектрик, образуя ультратонкий слой масла на фторкаучуке со стороны диэлектрического раствора, и дополнительно электрод приводится в плотный контакт с противоположной стороной фторкаучука, образуя диэлектрик с высокой диэлектрической постоянной. Таким образом может быть обеспечен электрохимический реактор, использующий аналоговый переключатель для того, чтобы управлять переносом электронов между электродами. [0039] В электрохимическом реакторе по настоящему изобретению, когда водоотталкивающая пористая мембрана выполнена из полимерной смолы, гидрофильная группа или водоотталкивающая группа вводится в поверхность и пористую стенку существующей пористой мембраны, либо подходящий материал выбирается из материалов, которые имеют различные диаметры пор, либо изменяются концентрация соли или температура водного раствора электролита, либо прикладывается потенциал между этими водоотталкивающими пористыми мембранами с тем, чтобы изменить значение давления водостойкости пленки. Таким образом, может быть получен водный раствор электролита, который может проходить через водоотталкивающую пористую мембрану в соответствии с гидравлическим давлением водного раствора электролита, или можно управлять количеством ионов. [0040] Для того чтобы увеличить давление водостойкости, достаточно увеличить диаметр пор водоотталкивающей пористой мембраны. Однако, если диаметр пор увеличивается, ослабляется механическая прочность мембраны. При этом, если фторкаучук, который проявляет водоотталкивающие свойства и маслоотталкивающие свойства, преобразуется в гидрофильный, смачиваемость водой увеличивается, что понижает давление водостойкости. Однако, если обе поверхности пористой мембраны на основе фтора преобразуются в гидрофильные, пленка увеличивает свою смачиваемость относительно как водного раствора, так и электрода, нарушая сохранение электрической изоляции. Патентные документы 12, 13 и 14 раскрывают способ изготовления водоотталкивающей пористой мембраны на основе фтора путем облучения водоотталкивающей пористой мембраны на основе фтора лучом эксимерного лазера в присутствии соединения, содержащего атом с энергией связи 128 ккал/моль или больше и гидрофильную группу. Патентный документ 15 раскрывает способ придания смачиваемости внутренней стенке пор путем замещения внутренних отверстий водоотталкивающей пористой мембраны на основе фтора гидрофильной группой с помощью фотохимической реакции под воздействием ультрафиолетового излучения. Непатентный документ 1 раскрывает, что давление водостойкости водоотталкивающей пористой пленки фторкаучука, имеющей диаметр пор 33 мкм, составляет 1500 мм рт. ст., но давление водостойкости падает до 20 мм рт. ст. при фотопреобразовании внутренностей пор в гидрофильные. Кроме того, непатентный документ 1 указывает, что давление водостойкости понижается, если концентрация соли водного раствора электролита увеличивается. Патентный документ 18 раскрывает тот факт, что давление водостойкости понижается, если температура водного раствора электролита увеличивается, а также раскрывает электросмачивание, которое улучшает гидрофильные свойства за счет приложения электрического потенциала между этими водоотталкивающими пористыми мембранами. Таким образом, количеством ионов, которые могут проникать через водоотталкивающую пористую мембрану, можно управлять аналоговым образом в соответствии с гидравлическим давлением водного раствора. [0041] В электрохимическом реакторе по настоящему изобретению в соответствии с одним вариантом осуществления отталкивающая жидкость пористая мембрана (изоляционная пленка) помещается в открытый контейнер, такой как море, соленое озеро, горячий источник, бассейны минеральных источников, отстойники водных растворов отходов, ванна термовыдержки, резервуары, водопроводы, бассейны, открытые контейнеры, включая бак большого размера, герметичные контейнеры, такие как мешки, трубки и небольшие контейнеры или герметичные контейнеры, в которые вставляется герметичный контейнер меньшего размера. При этом водный раствор электролита проникает через водоотталкивающую пористую мембрану за счет оказания давления и происходит электрохимическая реакция водного раствора электролита между положительным электродом и отрицательным электродом. [0042] Путем приложения давления к водному раствору электролита в средствах изоляции с помощью прикладывающего давление элемента водный раствор электролита проникает через водоотталкивающую пористую мембрану, обеспечивая электрическую связь положительного электрода и отрицательного электрода, таким образом вызывая электрохимическую реакцию водного раствора электролита. Средства изоляции могут быть классифицированы на герметичный контейнер и открытый контейнер, как показано на Фиг. 4. [0043] Химический реактор (см. Фиг. 4(A)), использующий герметичный контейнер, относится к мешку, трубке, малому контейнеру и т.п., поверхность которого, контактирующая с парой положительного и отрицательного электродов, является водоотталкивающей пористой мембраной. Раствор электролита или диэлектрик герметизируется в этом герметичном контейнере, и непосредственно на произвольную наружную поверхность оказывается давление (см. Фиг. 5(A)) с помощью прикладывающего давление элемента 6, как показано на Фиг. 5. Либо на раствор в запечатанном контейнере оказывается давление с помощью цилиндра (шприца) 6, спринцовки, пипетки 7 и т.п., вручную или с помощью электрического устройства, или с помощью храпового механизма 8, или давление на раствор оказывается с помощью водяного бака 9, помещенного на таком высоком уровне, который может создать гидростатический напор, равный давлению водостойкости, и соединенного с контейнером соединительной трубой 6, и задания статического напора (h) 10 раствора электролита (см. Фиг. 5(B)). [0044] Как показано на Фиг. 4(B), открытый контейнер 11 относится к морю, соленому озеру, горячему источнику или минеральному источнику, заполненным огромным количеством раствора электролита, к отстойнику, хранящему отходы водного раствора или электролита, или к резервуару, такому как бак, ванна термовыдержки, пруд, техническая вода или бассейн. Обычно гидравлическое давление повышается примерно на 1 атм по мере того, как глубина от поверхности воды моря или озера увеличивается на 10 метров. Так как это эквивалентно давлению раствора на глубине, средство изоляции этой области может рассматриваться как открытый контейнер. Здесь камера сбора электродного продукта, в которой располагается пара из положительного электрода и отрицательного электрода с расположенной между ними водоотталкивающей пористой мембраной, погружается в огромное количество раствора электролита на определенную глубину, где может быть получено гидравлическое давление, равное давлению водостойкости водоотталкивающей пористой мембраны, при поддержании регулярного интервала, и водный раствор электролита подвергается непосредственно электролизу. [0045] Химический реактор, который использует герметичный контейнер в открытом контейнере, имеет, как показано на Фиг. 4(C), конструкцию, в которой герметичный контейнер 1 вставляется в открытый контейнер 2 так, чтобы герметичный контейнер 1 сжимался гидравлическим давлением внутри открытого контейнера 2 для осуществления электролиза между положительной и отрицательной электродными камерами, плотно присоединенными к герметичному контейнеру 1. Герметичный контейнер 1 снабжен по меньшей мере одной водоотталкивающей пористой мембраной в дополнение к двум водоотталкивающим пористым мембранам, присоединенным к паре электродов. Кроме того, в герметичный контейнер 1 помещается имеющий высокую проводимость водный раствор серной кислоты или едкого натра (гидроксида натрия) или т.п., и вода или водный раствор электролита, который прошел через водоотталкивающую пористую мембрану под действием гидравлического давления открытого контейнера, поступает для осуществления электролиза в герметичном контейнере 1. Вместо этого открытого контейнера может использоваться двухконтейнерная конструкция, в которой герметичный контейнер 1 вставляется в герметичный контейнер большого размера, в котором герметичный контейнер 1 сжимается гидравлическим давлением в герметичном контейнере большого размера для того, чтобы осуществлять электролиз между положительным и отрицательным электродами, плотно присоединенными к герметичному контейнеру 1. При использовании устройства получения водорода, имеющего двухконтейнерную конструкцию, водород может эффективно производиться из неэлектролитической воды, такой как морская вода, а также возможно производить водород путем помещения химического реактора в пресную воду озера или болота, или водный раствор электролита низкой концентрации, такой как соленая вода или минеральный источник, что является другой особенностью настоящего изобретения. Либо можно использовать электрохимический реактор, содержащий прикладывающий давление элемент для сжатия газа, заполняющего внутренность герметичного контейнера из отталкивающей жидкость пористой мембраны, с тем, чтобы сжимать газ для его проникновения в солевой расплав из пор отталкивающей жидкость пористой мембраны. [0046] Далее будет описан способ наливания водного раствора электролита в полый герметизирующийся мешок, выполненный из водоотталкивающей пористой мембраны. Материалом для водоотталкивающей пористой мембраны является, например, фторкаучук, полипропиленовая смола, полиэтиленовая смола и т.п., и из них фторкаучук имеет самую высокую химическую стойкость и самую высокую температуру теплостойкости. Как показано на Фиг. 6, примеры способа заполнения водным раствором 14 электролита внутренности полого герметичного мешка 1, выполненного из водоотталкивающей пористой мембраны 11, являются следующими. Водный раствор 14 электролита вводится непосредственно в полый мешок с помощью впрыскивающего жидкость цилиндра (шприца) 6 (см. Фиг. 6(A)). Либо при использовании водоотталкивающей пористой мембраны 11, которая не пропускает воду, но пропускает газ, полый герметичный мешок 1, в который заранее запечатано растворяемое вещество 15, такое как химикат, помещается в атмосферу водяного пара для того, чтобы вызвать гидролиз и реакцию растворения с растворяемым веществом и тем самым запасти воду внутри, либо полый герметичный контейнер, в который заранее запечатано растворяемое вещество, такое как химикат, вставляется в герметичный контейнер, в то время как внутренность полого герметичного мешка является открытой для атмосферы с помощью соединительной трубки, и вода, находящаяся в герметичном контейнере, сжимается гидравлическим давлением, равным давлению водостойкости, чтобы ввести воду в герметичный контейнер для гидролиза, производя тем самым водный раствор электролита (см. Фиг. 6(B)). Либо пока одна водоотталкивающая пористая мембрана 11 полого герметичного мешка отсасывается вакуумным насосом через всасывающее отверстие 94 под отрицательным давлением ниже давления водостойкости, водный раствор 14 электролита вводится в контейнер через водоотталкивающую пористую мембрану 11 с другой стороны для того, чтобы запасти водный раствор 14 электролита в герметичном контейнере 1, находящемся в герметичном контейнере (см. Фиг. 6(C)). Либо спирт 13 наносится на одну стенку полого герметичного контейнера, и растворителю или водному раствору 14 электролита позволяют войти через покрытую спиртом поверхность. После этого системе дают постоять или нагревают для того, чтобы испарить спирт, запасая таким образом водный раствор электролита в мешке (см. Фиг. 6(D)). Что касается способа нанесения спирта, непатентный документ 1 и патентный документ 12 раскрывают, что поверхностное натяжение воды, фторкаучука и метилового спирта составляют 72,3 дин/см, 28,5 дин/см и 22,3 дин/см соответственно. Эти документы также указывают, что в случае пористого фторкаучука вода, которая имеет более высокое поверхностное натяжение, чем у фторкаучука, не проникает в поры пористого материала, но метиловый спирт, который имеет более низкое поверхностное натяжение, чем у фторкаучука, проникает в поры. Кроме того, в этих документах также упоминается, что поскольку спирт имеет высокое сродство к воде, если вода помещается на пористый фторкаучук, в который проник спирт, вода проникает в поры этого материала только тогда, когда присутствует спирт. [0047] Как показано на Фиг. 7, в электрохимической реакции водного раствора электролита пара положительного электрода и отрицательного электрода образована из электродных пластин в случае батарей или конденсаторов, или из электродных камер, содержащих средства сбора электродных продуктов, в случае электролитических устройств. [0048] Для электродов, использующихся в батарее, если электродные пластины являются отрицательным электродом из амфотерного элемента, магния или металлического элемента, имеющего большую склонность к ионизации, чем у водорода, за исключением элементов Группы 1 или 2, а в качестве положительного электрода используется кислород, фторид графита или металлический элемент, имеющий меньшую склонность к ионизации, чем у водорода, оба электрода являются голыми электродами, подвергающимися воздействию внешнего воздуха. Либо, если отрицательный электрод состоит из элемента Группы 1 или 2, а положительный электрод состоит из галогена или галогенидного соединения, оба электрода могут быть помещены в электродные камеры, защищенные от внешнего воздуха. [0049] Для электродов, подвергающихся электролизу, электродная камера классифицируется на газопроницаемую электродную камеру, электродную камеру сбора основного металла, заполненную маслом, и электродную камеру сбора кислотного/основного водного раствора, заполненную водой. Когда электродный продукт является газом, внутренности обоих электродов образованы в виде пористого электрода, имеющего текстуру сетки, волокон, пористого материала или зерен металла или углерода, либо они помещаются в газопроницаемую электродную камеру, имеющую такую конструкцию, что задняя поверхность пористого электрода включает в себя зазор. Когда электродный продукт является элементом Группы 1, 2 или 13, отрицательный электрод в виде конструкции электродной камеры, заполненной маслом, или электродной камеры с пористым электродом, поры которого или зазор в задней поверхности которого заполнены маслом для того, чтобы подвергнуть продукты отрицательного электрода разделению в тяжелой жидкости, или электродной камеры, заполненной маслом (маслонаполненной электродной камеры), снабженной электродной пластиной позади масла и используемой в качестве диэлектрического конденсатора, а также среды хранения электроэнергии. Либо, когда электродный продукт превращается в кислотный водный раствор путем ионной реакции с водой, принимается такая конструкция, что передняя сторона положительной электродной пластины заполнена водой, к которой заранее добавлена разбавленная кислота. Когда электродный продукт является основным водным раствором, принимается такая конструкция электродной камеры (заполненной водой электродной камеры), в которой передняя часть отрицательной электродной пластины заполнена водой, к которой заранее добавлена разбавленная щелочь, а также принимается такая конструкция, что заполненные водой электродные камеры обоих электродов снабжены впуском для подачи воды и выпуском для подачи полученного кислотного или основного водного раствора, а также патрубком для сбора полученного газа в верхней части конструкции, либо вода циркулирует в порах выполненного из углерода пористого электрода или в зазоре на задней поверхности для сбора газообразного галогена, сульфита или азотистой кислоты путем абсорбции их водой. [0050] Когда электроды используются в конденсаторе, положительные/отрицательные электродные пластины являются голыми электродами однопластинчатого типа, между которыми находится масляный или водный диэлектрик, оба - через водоотталкивающие пористые мембраны, или электродами с двойным электрическим слоем, в которых органические молекулы адсорбируются на поверхности электрода из активированного угля, или электродами окислительно-восстановительного типа, например, из оксида металла, электропроводящего полимера или активированного угля, в которых окислительно-восстановительные электроды, изолированные друг от друга водоотталкивающей пористой мембраной, замыкаются накоротко электропроводящими волокнами, заполненными электролитом. При использовании окислительно-восстановительной конструкции высокий заряд может быть запасен в оксидных пленках как положительной, так и отрицательной электродных пластин. Кроме того, для сохранения кислотного или основного водного раствора электролита в герметичном контейнере (мешке), выполненном из водоотталкивающей пористой мембраны, в него включаются электропроводящие волокна, позволяя таким образом уменьшить внутреннее сопротивление. [0051] В одном варианте осуществления электрохимический реактор может быть представлен эквивалентной электрической схемой, показанной на Фиг. 8. Эта схема называется «схемой Мурахары». Как показано на эквивалентной схеме Фиг. 8, этот электрохимический реактор подвергает электролизу водный раствор электролита за счет использования границы раздела между водным раствором электролита и маслом в качестве отрицательного электрода для того, чтобы осадить катодные продукты в масляном слое и подвергнуть их разделению в тяжелой жидкости (классификации под действием силы тяжести). Этот реактор включает в себя виртуальный отрицательный электрод 19, чтобы подвергать электролизу водный раствор 14 электролита, имеющий электрическое сопротивление (R), с осаждением основного металла в маслонаполненной электродной камере 16. Виртуальный отрицательный электрод 19 практически является границей между масляной стороной и водной стороной, и эта граница раздела может быть установлена, когда масляная сторона и водная сторона перпендикулярны оси земли, в противном случае используется водоотталкивающая пористая мембрана. Эта водоотталкивающая пористая мембрана 11 принимается в качестве переключателя (S), и только когда к водоотталкивающей пористой мембране 11 прикладывается давление водного раствора электролита, равное давлению водостойкости, переключатель (S) замыкается накоротко для осуществления электролиза. Более подробно, граница раздела между маслом масляного слоя и водным раствором электролита, которые составляют маслонаполненную электродную камеру 16, предполагается в качестве отрицательного электрода 19. Таким образом, электрическая схема, включающая в себя масляный слой в качестве масляного конденсатора (C1+C2) и водный раствор 14 электролита в качестве водяного реостата (R), использует границу раздела между масляным слоем и водным раствором электролита в качестве отрицательного электрода 19 масляного конденсатора и содержит промежуточный электрод 18 между положительным электродом 17 и отрицательным электродом 19 масляного конденсатора, образуя диэлектрик 1 (C1) между положительным электродом 17 и промежуточным электродом 18 и диэлектрик 2 (C2) между промежуточным электродом 18 и отрицательными электродами 19. [0052] Одной из особенностей настоящего изобретения при этом является то, что граница раздела между масляным слоем и водным раствором электролита функционирует в качестве отрицательного электрода. Таким образом, только когда напряжение (E) 20 непрерывно прикладывается к диэлектрику 1 (C1) между положительным электродом 17 и промежуточным электродом 18, а также переключатель (S) водоотталкивающей пористой мембраны 11 замыкается накоротко в состоянии, в котором положительный электрод 17 масляного конденсатора используется в качестве положительного электрода водного раствора 14 электролита, образуется последовательная цепь для движения заряда, запасенного в масляных конденсаторах (C1+C2), к водному раствору 14 электролита, чтобы дать напряжение 20, большее или равное напряжению разложения, подвергая таким образом продукты отрицательного электрода разделению в тяжелой жидкости в масляном слое в диэлектрике 2 (C2). Здесь диэлектрик 1 (C1) может быть заменен конденсатором постоянной емкости для придания заряда диэлектрику 1 (C1), и одновременно водный раствор 14 электролита в качестве водяного реостата (R) может быть присоединен между отрицательным электродом 19 диэлектрика 2 (C2) и положительным электродом 16 диэлектрика 1 (C1), давая напряжение 20, большее или равное напряжению разложения, подвергая таким образом продукты отрицательного электрода разделению в тяжелой жидкости в масляном слое в диэлектрике 2 (C2). [0053] Фиг. 9 представляет собой концептуальную диаграмму, показывающую масляный конденсатор, который использует границу раздела масляной стороны и стороны водного раствора электролита в качестве отрицательного электрода. Фиг. 9(A) представляет собой диаграмму, показывающую конструкцию виртуального отрицательного электрода, использующего водоотталкивающую пористую мембрану. Здесь следует отметить, что граница раздела масла и водного раствора электролита не зависит от оси земли. Фиг. 9(B) представляет собой диаграмму, показывающую конструкцию такого случая, когда виртуальный отрицательный электрод имеет плоскость, вертикальную к оси земли, и удельный вес масла составляет менее единицы. Фиг. 9(С) представляет собой диаграмму, показывающую конструкцию такого случая, когда виртуальный отрицательный электрод имеет плоскость, вертикальную к оси земли, и удельный вес масла превышает единицу. [0054] Как показано на Фиг. 9(A), в случае, когда виртуальный отрицательный электрод (граница раздела между масляной стороной и стороной водного раствора электролита) 19 наклонен к оси земли под произвольным углом, виртуальный отрицательный электрод 19 образуется только тогда, когда водоотталкивающая пористая мембрана 11 вставляется между масляной стороной и стороной водного раствора электролита 19 для того, чтобы сжимать водный раствор 14 электролита. Если виртуальный отрицательный электрод 19 является плоскостью, вертикальной к оси земли, водоотталкивающая пористая мембрана 11 не требуется в обязательном порядке. Либо, если плотность (удельный вес) масла ниже, чем у водного раствора 14 электролита (т.е. удельный вес меньше единицы), масляный слой 23 образуется в верхней части водного раствора 14 электролита. Если плотность масла выше, чем у водного раствора 14 электролита (т.е. удельный вес больше единицы), масляный слой 24 образуется в нижней части водного раствора 14 электролита. В дополнение к вышеизложенному, заряд 20 придается диэлектрику 1 (C1 на Фиг. 8(A)), и одновременно водный раствор 14 электролита соединяется между отрицательным электродом 19 диэлектрика 2 (C2 на Фиг. 8(A)) и положительным электродом 17 диэлектрика 1, давая напряжение 20, большее или равное напряжению разложения, подвергая таким образом продукты отрицательного электрода разделению в тяжелой жидкости в масле в диэлектрике 2 (C2 на Фиг. 7(A)), для того, чтобы выгрузить их через патрубок 26 для сбора. [0055] В одном варианте осуществления пара газопроницаемых камер положительного и отрицательного электродов может быть погружена в море или соленое озеро, которое состоит из водного раствора электролита низкой концентрации, на уровне под морской поверхностью с требуемым напором, и таким образом можно производить водород и кислород или хлор непосредственно из морской воды (устройство получения водорода, см. Фиг. 10). Как правило, гидравлическое давление увеличивается примерно на одну атмосферу при погружении предмета от уровня моря или водной поверхности на каждые 10 м. Когда используется это естественное явление, и камеры воздухопроницаемых положительного и отрицательного электродов погружаются на глубину гидравлического давления, эквивалентного давлению водостойкости водоотталкивающей пористой мембраны, не будет никакой необходимости в искусственном приложении давления. Например, когда пара камер положительного и отрицательного электродов, электродные поверхности которых слегка отделены друг от друга, погружается на глубину под морской поверхностью, где получается давление водостойкости водоотталкивающей пористой мембраны, чтобы приложить электрический потенциал к обоим электродам, могут быть произведены водород, кислород или хлор. Следовательно, водный раствор 14 электролита низкой концентрации (водный раствор хлорида натрия) из открытого контейнера 2, такого как море или соленое озеро, вводится внутрь пары отрицательной электродной камеры 3 и положительной электродной камеры 4 через водоотталкивающую пористую мембрану 11, как показано на Фиг. 10(A). При использовании газопроницаемых электродных камер 3 и 4 соленая вода подвергается электролизу с получением водорода в отрицательной электродной камере 3 и кислорода или хлора в положительной электродной камере 4. Здесь каждый из положительного и отрицательного электродов выполнен в виде пористого электрода из металла или углерода, имеющего текстуру сетки, волокнистое строение или форму зерна, и самая верхняя часть каждой из газосборных электродных камер 3 и 4 содержит шланг 12 сбора полученного газа, составляя таким образом пару электродных камер 3 и 4, которые устанавливаются близко друг к другу в водном растворе 14 электролита (морской воде). Эта пара или группа соединенных пар положительных и отрицательных электродных камер устанавливаются под морской поверхностью, где получается гидравлическое давление, равное давлению водостойкости водоотталкивающей пористой мембраны, и электролиз осуществляется только путем приложения потенциала между обоими электродами с отдельным сбором водорода в отрицательной электродной камере и кислорода или хлора в положительной электродной камере. В настоящем изобретении электрод не вставлен непосредственно в водный раствор электролита, и поэтому электродным продуктом не создается состояние изолирования между электродом и электролитом. Кроме того, над водоотталкивающей пористой мембраной в качестве границы давление со стороны электролита является более высоким, чем давление со стороны электродного продукта. При такой конструкции эффективность сбора электродного продукта является высокой. Если герметичный контейнер 1 заменяется на открытый контейнер 2, он может быть также использован на суше, как показано на Фиг. 10(B). Водный раствор 14 электролита (соленая вода) из герметичного контейнера 1 сжимается с помощью прикладывающего давление элемента 6 или водяного бака 9, установленного в верхнем положении 10 и сообщающегося через соединительную трубу 5, морская вода, концентрированная морская вода или добавленный к воде электролит непосредственно подвергается электролизу, чтобы отдельно собирать газообразный водород в отрицательной электродной камере 3 и газообразный кислород или хлор в положительной электродной камере 4. [0056] В одном варианте осуществления пресная вода нагнетается в концентрированный водный раствор электролита, запечатанный в герметичном контейнере, через водоотталкивающую пористую мембрану (для проникания пресной воды) 27 из внешней стенки герметичного контейнера для осуществления электролиза, позволяя таким образом непосредственно производить водород и кислород или хлор с высокой эффективностью (см. Фиг. 11). [0057] Как показано на Фиг. 11(A), устройство 30 получения водорода, содержащее герметичный контейнер, образованный из водоотталкивающей пористой мембраны, заполненный водным раствором электролита с высокой растворимостью и высокой проводимостью (водным раствором электролита высокой концентрации), таким как разбавленная серная кислота или водный раствор едкого натра, погружается в открытый контейнер 2, такой как пресноводное озеро, водоем, морская вода или горячий источник, и таким образом пока водный раствор 14 электролита низкой концентрации, такой как пресная вода, морская вода, вода горячего источника или горячие сточные воды, нагнетается в герметичный контейнер 1 через водоотталкивающую пористую мембрану 27 для введения прилегающего к ней водного раствора, водный раствор подвергается электролизу с получением водорода. В состоянии, в котором водный раствор электролита высокой концентрации, такой как разбавленная серная кислота, водный раствор едкого натра и т.п., заключен в герметичном контейнере 1, водный раствор 14 электролита низкой концентрации непрерывно подается в герметичный контейнер через водоотталкивающую пористую мембрану (для проникания пресной воды) 27, прилегающей к внешней стенке герметичного контейнера 1, непрерывно производя тем самым водород. Следует отметить, что для того, чтобы заставить два вида водных растворов электролита с различными концентрациями между внутренней стороной и внешней стороной герметичного контейнера 1 проникать в поры водоотталкивающей пористой мембраны под тем же самым давлением водостойкости, должны быть выбраны различные типы водоотталкивающих пористых мембран а (11) и b (27), с большим размером пор у водоотталкивающей пористой мембраны b (27), чем у мембраны а (11), если они могут отличаться. Либо, если водоотталкивающие пористые мембраны а (11) и b (27) относятся к одному и тому же типу, стенки пор со стороны водоотталкивающей пористой мембраны b (27), приведенной в контакт с водным раствором электролита низкой концентрации, замещаются гидрофильной группой для способствования смачиваемости водой, тем самым позволяя как водному раствору электролита низкой концентрации, так и водному раствору электролита высокой концентрации проникать через водоотталкивающую пористую мембрану а (11) и водоотталкивающую пористую мембрану b (27) при том же самом гидравлическом давлении или значениях давления, близких друг к другу. Если водоотталкивающие пористые мембраны а (11) и b (27) относятся к одному и тому же типу, самый простой способ заключается в том, чтобы сделать гидравлическое давление со стороны водного раствора электролита низкой концентрации положительным (высоким), или сделать давление с выходной стороны водоотталкивающей пористой мембраны а, на которой содержится водный раствор электролита высокой концентрации, отрицательным (всасывание). Отрицательное давление означает всасывание газа, производимого газопроницаемыми электродными камерами, такими как отрицательная электродная камера 3 и положительная электродная камера 4, входящими в контакт с водоотталкивающей пористой мембраной а (11), перекачивающим газ вакуумным насосом в пределах такого диапазона, что разница давлений между гидравлическим давлением, прикладываемым к водному раствору электролита низкой концентрации, и давлением газа, образующегося в газопроницаемой электродной камере с выходной стороны водоотталкивающей пористой мембраны а (11), является более высоким или равным сумме давления водостойкости водоотталкивающей пористой мембраны b (27) и давления водостойкости водоотталкивающей пористой мембраны а (11). Во время электролиза образуется большое количество газа, и поэтому необходимо собирать образующийся газ и одновременно справляться с давлением газа в газопроницаемой электродной камере. Следовательно, желательно предусмотреть клапан 93 регулировки давления на стадии перед патрубком 12 сбора полученного газа из газопроницаемых электродных камер, а именно, электродной камеры 3 и положительной электродной камеры 4. [0058] Обычно давление водостойкости водоотталкивающей пористой мембраны будет становиться низким по мере того, как концентрация электролита становится высокой, как показано соотношением давления водостойкости и концентрации соли у пористой пленки фторкаучука, проиллюстрированным на Фиг. 28. [0059] В частности, в случае, когда водный раствор электролита, получаемый как водный раствор 14 электролита низкой концентрации, или пресная вода 88 и т.п. смешивается с водным раствором электролита высокой концентрации, таким как разбавленная серная кислота или разбавленная щелочь, в герметичном контейнере 1 через водоотталкивающую пористую мембрану b (27) и подвергается электролизу между отрицательной электродной камерой 3 и положительной электродной камерой 4, контактирующими с водоотталкивающей пористой мембраной а (11) для производства газа в газопроницаемых электродных камерах, и таким образом создается давление (Pg) благодаря газу в каждой газопроницаемой электродной камере, когда перепад давления между гидравлическим давлением Plb, прикладываемым к водоотталкивающей пористой мембране b (27) водным раствором 14 электролита низкой концентрации, и гидравлическим давлением Pla, прикладываемым к водоотталкивающей пористой мембране а (11) водным раствором электролита высокой концентрации, является давлением водостойкости Plba водоотталкивающей пористой мембраны а (11), а также перепад давления между гидравлическим давлением P3lag водного раствора электролита высокой концентрации и давлением (Pg) внутри газопроницаемой электродной камерой является давлением водостойкости водоотталкивающей пористой мембраны а (11), должны одновременно удовлетворяться соотношения: Plb-Pla≥Plba и Pla-Pg=Plag. Другими словами, чтобы удовлетворялось условие Plb-Pg≥Plba+Plag, гидравлическое давление Plb, прикладываемое к водному раствору 14 электролита низкой концентрации, должно быть высоким (положительным давлением), либо давление (Pg), поддерживаемое в газопроницаемой электродной камере, должно быть отрицательным за счет всасывания вакуумным насосом через клапан 93 регулировки давления. Таким образом, сумма давлений водостойкости всех водоотталкивающих пористых мембран задает гидравлическое давление Plb, прикладываемое к началу реакционной системы, и давление газа Pg, прикладываемое в ее конце, чтобы поддерживать электролиз, таким образом производя водород, кислород или хлор. На практике в качестве водоотталкивающих пористых мембран а (11) и b (27) используются одинаковые водоотталкивающие пористые мембраны, и гидравлическое давление Plb, прикладываемое к водному раствору 14 электролита низкой концентрации, делается положительным, либо давление Pg в газопроницаемой электродной камере делается отрицательным. При такой простой работе может осуществляться электролиз для производства водорода непосредственно из морской воды или озера. Более конкретно, герметичный контейнер 1, в котором заключен водный раствор электролита высокой концентрации, такой как разбавленная серная кислота или разбавленная щелочь, вставляется в открытый контейнер 2, который является морем или озером, где содержится водный раствор электролита низкой концентрации, и герметичный контейнер 1 погружается до положения такого гидростатического напора, при котором электролиз осуществляется непрерывно. [0060] Этот способ может использоваться на суше, как показано на Фиг. 11(B). Герметичный контейнер 1 вставляется в герметичный контейнер 29 большого размера, и гидравлическое давление водопроводной воды 28 во время ее подачи делается выше или равным давлениям водостойкости водоотталкивающей пористой мембраны 11 и водоотталкивающей пористой мембраны (для проникания пресной воды) 27, при этом с непрерывным получением водорода. Вместо водопроводной воды контейнер может заполняться пресной водой или морской водой или ванной термовыдержки горячего источника, и при повышении давления до величины, большей или равной давлению водостойкости водоотталкивающей пористой мембраны, вода может подаваться под давлением посредством механического сжатия или через соединительную трубу из положения напора. Здесь важно уравнять или сблизить давление водостойкости водоотталкивающей пористой пленки фторкаучука (электродной изоляционной пленки) 11 и давление водостойкости водоотталкивающей пористой мембраны (для проникания пресной воды) 88, вызываемое пресной водой. Пара или множество устройств 30 получения водорода, каждое из которых содержит пару газопроницаемых электродных камер 3 и 4, соединяются для того, чтобы подвергнуть электролизу водный раствор электролита под давлением, равным давлению водостойкости водоотталкивающей пористой мембраны, и при электрическом напряжении, большей или равном напряжению разложения воды, и таким образом газообразный водород может быть произведен в отрицательной электродной камере, а газообразный кислород или газообразный хлор может быть произведен в положительной электродной камере. [0061] В одном варианте осуществления едкий натр может быть произведен непосредственно в отрицательной электродной камере путем выполнения электролиза при приложении гидравлического давления к водоотталкивающей пористой мембране без использования диафрагмы или ионообменной мембраны, как в обычном способе. Как показано на Фиг. 12, едкий натр 31 производится следующим образом. Водный раствор 32 соли основного металла, например, хлорида натрия, натриевой селитры или сульфата натрия, сжимается с давлением водостойкости водоотталкивающей пористой мембраны 11 или гидравлическим давлением, большим или равным ему, для электролиза, и таким образом гидроксид основного металла (едкий натр) 31 производится в заполненной водой электродной камере 40, изолированной водоотталкивающей пористой мембраной 11. [0062] Как показано на Фиг. 12(A), гидравлическое давление, равное давлению водостойкости, прикладывается к водному раствору соли основного металла (водному раствору хлорида натрия) 32 в герметичном контейнере 1, и заполненная водой электродная камера 40 содержит внутри металл, такой как никель, или углеродный электрод. Кроме того, вода с температурой максимум 80°C подается через впуск 34 подачи воды. Здесь подаваемая вода может иметь комнатную температуру, но поскольку растворимость едкого натра является высокой при высокой температуре, то, следовательно, чтобы эффективно производить едкий натр, желательна температура около 80°C. В частности, в начале электролиза электрическое сопротивление воды в заполненной водой электродной камере 40 высоко, и поэтому необходимо заранее добавить разбавленный водный раствор едкого натра. Она содержит впуск 34 подачи воды для подачи воды в заполненную водой электродную камеру 40, патрубок 35 для сбора продукта отрицательного электрода для собирания производимых концентрированных гидроксидов 31 основного металла (концентрированного водного раствора едкого натра), а также трубу 12 сбора производимого газа (газообразного водорода) в верхней части. С другой стороны, положительный электрод образован газопроницаемой электродной камерой 41 и содержит положительный электрод 37 из, например, волокнистого углерода, гранулированного углерода или пористого углерода, плотно присоединенный к водоотталкивающей пористой мембране 11. Она также содержит трубу 12 сбора производимого газа для непосредственного собирания газов, образовавшихся на поверхности положительного электрода, таких как газообразный хлор, газообразная азотистая кислота и газообразная сернистая кислота. Однако, учитывая транспортировку продукта, водный раствор является более удобным, чем газ. Поэтому, как показано на Фиг. 12(B), в качестве положительного электрода принята конструкция заполненной водой электродной камеры 40, и для того, чтобы обеспечить реакцию отрицательного иона и воды, разбавленный водный раствор соляной кислоты заранее добавляется к воде комнатной температуры, подаваемой через впуск 34 подачи воды, а затем осуществляется электролиз между отрицательной электродной пластиной 36 и положительной электродной пластиной 38 через водоотталкивающую пористую мембрану 11, чтобы обеспечить ионную реакцию (2Cl-+2H2O→2HCl+O2). Образующаяся при этом кислота (соляная кислота) 33 собирается через выпуск 42 концентрированной кислоты (соляной кислоты), а кислород собирается через трубу 12 сбора производимого газа. [0063] В одном варианте осуществления водоотталкивающая пористая мембрана используется в качестве двухпозиционного переключателя для ионов с тем, чтобы осадить элемент-основный металл, который является наиболее гидрофобным, путем электролиза водного раствора (устройство сбора основного металла). Как показано на Фиг. 13(A) и (B), для того, чтобы получить основный металл на отрицательном электроде путем электролиза водного раствора хлорида основного металла в герметичном контейнере 1, сетчатый отрицательный электрод 43 из металла или углерода приводится в контакт со стороной отрицательного электрода герметичного контейнера 1 через изоляционную пленку из водоотталкивающей пористой мембраны 11, образуя маслонаполненную электродную камеру 16, чья задняя сторона заполнена маслом 23. С использованием этой конструкции основные металлы продукта отрицательного электрода, удельный вес которых меньше, чем у масла 23 (а именно, Li, K и Na), собираются через патрубок 35 для сбора продукта отрицательного электрода, предусмотренный в верхней части заполненной маслом электродной камеры 16, тогда как те основные металлы, удельный вес которых больше, чем у масла 23 (а именно Mg, Ca, Ba и Sr) собираются через патрубок 35 для сбора продукта отрицательного электрода, предусмотренный на дне заполненной маслом электродной камеры 16. Существует два способа сбора продуктов положительного электрода, а именно в виде газа и в виде жидкости. Для того, чтобы собрать продукт в виде газа, как показано на Фиг. 13(A), положительный электрод должен быть образован из газопроницаемой электродной камеры 41 и содержит положительный электрод 37 из, например, волокнистого углерода, гранулированного углерода или пористого углерода, плотно присоединенный к водоотталкивающей пористой мембране 11. Она также содержит трубу 12 сбора полученного газа для того, чтобы непосредственно собирать газы, производимые на поверхности положительного электрода (хлор). Однако, учитывая транспортировку продукта, водный раствор является более удобным, чем газ. Поэтому, как показано на Фиг. 13(B), в качестве положительного электрода принята конструкция заполненной водой электродной камеры 40, и для того, чтобы обеспечить реакцию отрицательного иона и воды, разбавленный водный раствор соляной кислоты заранее добавляется к воде комнатной температуры, подаваемой через впуск 34 подачи воды, а затем осуществляется электролиз между отрицательной электродной пластиной 43 и положительной электродной пластиной 38 через водоотталкивающую пористую мембрану 11, чтобы обеспечить ионную реакцию (2Cl-+2H2O→2HCl+O2). Образующаяся при этом кислота (соляная кислота) 33 собирается через выпуск 42 концентрированной кислоты (соляной кислоты), а кислород собирается через трубу 12 сбора производимого газа. [0064] В одном варианте осуществления граница раздела между водным раствором соли основного металла элемента Группы 1 или 2 Периодической таблицы и маслом может использоваться в качестве виртуального отрицательного электрода, и водный раствор соли основного металла может быть подвергнут электролизу, чтобы осадить продукт отрицательного электрода в масляном слое. Как показано на Фиг. 14(A) и (B), в заполненной маслом электродной камере 16, отделенной герметичным контейнером 1 и водоотталкивающей пористой мембраной 11, водный раствор 32 соли основного металла подвергается электролизу между поверхностью 19 виртуального отрицательного электрода границы раздела масла 23 и водного раствора 32 соли основного металла и положительным электродом 37 (когда используется газопроницаемая электродная камера) или положительной электродной пластиной 38 (когда используется заполненная водой электродная камера), чтобы осадить продукт отрицательного электрода в масле 23 в заполненной маслом электродной камере 16. Хотя Фиг. 13 показывает газособирающий электрод 41 как положительный электрод, также может использоваться заполненная водой электродная камера 40. Фиг. 14(A) показывает конструкцию заполненной маслом электродной камеры 16, в которой два конденсатора C1 и C2 располагаются последовательно, и она содержит положительную электродную пластину 17 со стороны, противоположной водоотталкивающей пористой мембране 11 заполненной маслом электродной камеры 16. Поскольку между водоотталкивающей пористой мембраной 11 и положительной электродной пластиной 17 вставлена промежуточная электродная пластина 18 для подачи напряжения (E) 20 к конденсатору C1, образованному между промежуточной электродной пластиной 18 в масляном баке и положительной электродной пластиной 17 в масляном баке. С другой стороны, водный раствор 32 соли основного металла сжимается в герметичном контейнере 1, и граница раздела между прошедшим через водоотталкивающую пористую мембрану 11 водным раствором 32 соли основного металла и маслом используется в качестве стороны 19 виртуального отрицательного электрода, таким образом замыкая накоротко положительную электродную пластину 17 в заполненной маслом электродной камере 16 и положительный электрод 37 в газособирающем электроде 41 или положительную электродную пластину в заполненной водой электродной камере 40. В результате, только если конденсатор C2 образован между промежуточной электродной пластиной 18 в заполненной маслом электродной камере и стороной 19 виртуального отрицательного электрода, и, кроме того, если гидравлическое давление водного раствора 32 соли основного металла повышается на величину, равную давлению водостойкости водоотталкивающей пористой мембраны, осуществляется электролиз для осаждения основных металлов в масле заполненной маслом электродной камеры 16. Фиг. 14(B) показывает случай, когда промежуточная электродная пластина 18 не предусмотрена в масляном баке заполненной маслом электродной камеры 16, но твердотельный конденсатор C1 предусмотрен вне системы заполненной маслом электродной камеры 16. При такой конструкции, когда положительная электродная пластина 17 в масляном баке и положительный электрод 37 в газособирающем электроде 41 или положительная электродная пластина в заполненной водой электродной камере 40 замыкаются накоротко, конденсатор C2 образуется между положительной электродной пластиной 17 в масляном баке и стороной 19 виртуального отрицательного электрода. При этом электролиз для осаждения основных металлов в масле заполненной маслом электродной камеры 16 осуществляется только в том случае, если гидравлическое давление водного раствора 32 соли основного металла, помещенного между положительным электродом 37 (газособирающим электродом 41) или положительной электродной пластиной 38 (заполненной водой электродной камеры 40) и стороной 19 виртуального отрицательного электрода, равно давлению водостойкости водоотталкивающей пористой мембраны. Таким образом, когда гидравлическое давление водного раствора соли основного металла 32 поддерживается равным давлению водостойкости водоотталкивающей пористой мембраны 11, желаемый основный металл может быть отобран с помощью разделения в тяжелой жидкости в масле заполненной маслом электродной камеры 16. Таким образом, когда положительный электрод является газопроницаемой электродной камерой, газ-продукт положительного электрода может извлекаться непрерывно, либо когда он является водной электролитической камерой, концентрированная неорганическая кислота, такая как концентрированная соляная кислота, или газ-продукт положительного электрода, такой как газообразный кислород, может извлекаться непрерывно. [0065] В одном варианте осуществления, когда пористая углеродная пленка используется как в качестве изоляционной пленки для солевого расплава, так и в качестве отрицательного электрода, гидрид металла может образовываться в процессе переноса анионов газа водорода со стороны отрицательного электрода к стороне положительного электрода солевого расплава. Как показано на Фиг. 15, солевой расплав 46 гидроксида основного металла (едкого натра) ионизируется нагревающим солевой расплав нагревателем 48 до состояния Na++ОН-. С другой стороны, электродная камера, которая составляет отрицательный электрод, является газопроницаемой электродной камерой 41, и газообразный водород подается под давлением в газопроницаемую электродную камеру 41 через патрубок 47 для нагнетания газообразного водорода и входит под давлением в солевой расплав 46 гидроксида основного металла (едкого натра) через элемент 44, функционирующий и как отрицательная электродная пластина из пористого углерода, и как изоляционная пленка. В этом состоянии, когда напряжение (E) 20, большее или равное напряжению разложения с образованием аниона водорода, прикладывается между элементом 44, функционирующим и как отрицательная электродная пластина из пористого углерода, и как изоляционная пленка, и положительной электродной пластиной 38, выделяется анион водорода (H-) 50, вызывая ионную реакцию с солевым расплавом 46 гидроксида основного металла (едким натром) в ионном состоянии Na++ОН-, а значит, образуется гидрид основного металла (Na++H-=NaH). При этом удельный вес солевого расплава едкого натра (NaOH) составляет 2,13, но поскольку удельный вес гидрида натрия (NaH) составляет всего 0,92, гидрид основного металла (гидрид натрия) 49, всплывающий на поверхность из солевого расплава 46 гидроксида основного металла (едкого натра) при кристаллизации и отвердевании в качестве верхнего остатка, собирается из патрубка 51 сбора гидрида основного металла. Образовавшийся таким образом гидрид основного металла энергично гидролизуется водой, давая вдвое больше водорода, чем простой элемент-основный металл. Кроме того, как показано на Фиг. 16, температуры плавления гидроксидов элементов Группы 1 (Li, K и Na), Группы 2 (Mg, Ca, Sr и Br) и Группы 13 (Al) являются заметно более низкими по сравнению с их оксидами. Температуры плавления гидридов этих элементов являются более высокими, чем температуры плавления их гидроксидов, за исключением Mg и Al. Кроме того, удельный вес гидрида ниже, чем у гидроксида. Следовательно, эти металлы, за исключением Mg и Al, могут образовывать расплавленные соли при относительно низких температурах, и при реагировании с анионом водорода полученные таким образом гидриды могут всплывать на поверхность как верхний остаток и подвергаться простому отделению под действием силы тяжести. В частности, применительно к элементам Группы 1 температура плавления является более высокой у гидрида, чем у самого элемента. Температура плавления Na составляет 98°C, температура плавления NaH составляет 800°C, а температура плавления K составляет 64°C, тогда как температура плавления KH равна 417°C. Хотя K и Na, которые имеют чрезвычайно низкую температуру плавления, требуют серьезных предосторожностей при обращении с ними, в гидрированном состоянии их температура плавления становится более высокой, плотность становится ниже, и, кроме того, при гидролизе может быть получено вдвое больше водорода. Следовательно, ожидается, что они могут выступать в качестве источника водорода для, например, выработки электроэнергии из водорода или водородного автомобиля. В соответствии с законом о пожарных службах Na является материалом третьего класса опасности, а также спонтанно воспламеняющимся и реагирующим с водой веществом; однако температура плавления NaH низка, особенно учитывая, что температура плавления Na составляет всего 98°C по вышеизложенной причине. При обращении с ним требуется осторожность, так как он может реагировать с влагой, находящейся в воздухе, вызывая взрыв. При сравнении металлического натрия (Na) и гидрида натрия (NaH) друг с другом по безопасности видно, что оба они являются опасными материалами третьего класса и энергично реагирующими с водой химическими веществами в соответствии с законом о пожарных службах. Однако по шкале опасных материалов гидрид натрия принадлежит Классу II, в отличие от металлического натрия, который принадлежит Классу I, и таким образом он является сравнительно безопасным и легким в обращении. Как правило, металлический натрий хранится в керосине, тогда как зерна гидрида натрия (NaH) просто покрываются листом парафина и с ними можно обращаться сравнительно безопасно. Кроме того, когда металлический натрий вступает в реакцию с водой, образуется 0,5 моль водорода (H): (Na+H2O→1/2H2+NaOH). Однако в случае гидрида натрия (NaH) образуется 1 моль водорода (в два раза больше): (NaH+H2O→H2+NaOH). Таким образом, гидрид натрия (NaH) является перспективным в качестве материала-источника водорода (H2). Таким образом, хотя натрий (Na) неустойчив, если он не хранится в масле, и существует опасность взрыва в зависимости от условий, при его преобразовании в гидрид натрия (NaH) с помощью гидрирования температура плавления повышается до 800°C, что обеспечивает безопасность и длительный срок хранения. Следовательно, он становится подходящим для использования в производстве водорода путем его реагирования с водой при необходимости. С другой стороны, в случае MgH2 или AlH3, которые имеют более низкую температуру плавления, чем их гидроксиды, используется способ сбора продуктов при охлаждении пара с помощью охлаждаемой стенки, предусмотренной в верхней части бака солевого расплава. При этом, поскольку на фторкаучук может оказываться воздействие при приведении в непосредственный контакт с металлическим натрием, при размещении водоотталкивающей пористой мембраны из фторкаучука и металлического натрия близко друг к другу должно быть добавлено масло, такое как газойль или нефть. [0066] В одном варианте осуществления предлагается первичная или вторичная батарея, имеющая конструкцию, в которой герметичный контейнер, образованный из водоотталкивающей пористой мембраны (оболочечного типа), заполненный водным раствором электролита, располагается между пластинами положительного электрода и отрицательного электрода. Эта батарея работает по такому механизму, что давление, равное давлению водостойкости водоотталкивающей пористой мембраны, прикладывается к водному раствору электролита с осуществлением электрохимической реакции между положительным и отрицательным электродами для зарядки и разрядки, и давление на водный раствор электролита снимается для того, чтобы избежать саморазряда между электродами при хранении заряда. Как показано на Фиг. 17, герметичный контейнер (оболочечного типа) 55, содержащий водный раствор 14 электролита, обе стороны которого выполнены из водоотталкивающих пористых мембран 11, располагается между отрицательной электродной камерой (для батареи) 52 и положительной электродной камерой (для батареи) 53. Затем давление, равное давлению водостойкости водоотталкивающих пористых мембран 11, прикладывается к водному раствору 14 электролита, находящемуся в герметичном контейнере (оболочечного типа) 55 с помощью прикладывающего давление элемента 6 для зарядки (см. Фиг. 17(A)), и при зарядке заряд подается к отрицательной электродной камере (для батареи) 52 и положительной электродной камере (для батареи) 53 через водный раствор 14 электролита, проходящий через водоотталкивающие пористые мембраны 11. После завершения зарядки давление на водный раствор 14 электролита в герметичном контейнере 55 (оболочечного типа) снимается, чтобы избежать саморазряда между обоими электродами, сохраняя таким образом заряд (см. Фиг. 17(B)). Для разрядки равное давлению водостойкости давление снова прикладывается к водному раствору 14 электролита в герметичном контейнере 55 (оболочечного типа) из водоотталкивающей пористой мембраны (см. Фиг. 17(C)). Для электродов батарей важными являются безопасность и длительная стабильность. Следовательно, следующие моменты должны быть учтены в конструкции электродных камер. В случае, когда отрицательная электродная пластина выполнена из амфотерного элемента (Zn, Al, Sn или Pb) или Mg, или из металлического элемента, за исключением элементов Группы 1 или Группы 2, у которых большая склонность к ионизации, чем у водорода (то есть, Ti, Mn, Cr, Ga, Fe, Cd, Co, Ni или Fe), окружение электродной пластины, плотно присоединенной к водоотталкивающей пористой мембране, не обязательно изолировано от внешней среды. С другой стороны, в случае, когда отрицательный электрод состоит из элемента Группы 1 или Группы 2 и представляет собой твердое тело, для хранения электродных продуктов отрицательного электрода из элемента Группы 1 или Группы 2 в полости внутри пористого электрода из углерода необходимо заключить электродную пластину в коробку, либо покрыть его покрытием, подвергнутой водоотталкивающей обработке мембраной или полимерной пленкой, чтобы изолировать ее от внешней среды. В случае положительного электрода, то есть если в положительной электродной пластине используется металл, имеющий меньшую склонность к ионизации, чем у водорода, оксид металла, воздух или кислород, не обязательно требуется изолировать присоединенную к водоотталкивающей пористой мембране электродную пластину от внешней среды. Либо, если положительный электрод состоит из газообразного галогена, за исключением фтора, или из галогенида металла, необходимо закрыть окружение электродной пластины, присоединенной к водоотталкивающей пористой мембране, коробкой, покрытием, подвергнутой водоотталкивающей обработке мембраной или полимерной пленкой, либо отлить под давлением всю батарею так, чтобы изолировать ее от внешней среды. Однако, если положительная электродная пластина состоит из водоотталкивающего материала или подвергнута водоотталкивающей обработке, водоотталкивающая пористая мембрана не требуется, и она может быть помещена непосредственно в водный раствор электролита. [0067] В первичной или вторичной батарее по настоящему изобретению высокая электродвижущая сила и разрядная емкость могут быть достигнуты за счет использования основного металла для отрицательного электрода и кислорода или галогена для положительного электрода (см. Фиг. 1). В этой батарее водный раствор электролита может быть выполнен из соединения элемента-основного металла и другого элемента - кислорода или галогена. В этом случае разрядная емкость становится более высокой, поскольку растворимость соединения в воде выше при комнатной температуре. Для выполнения высокоэффективной зарядки желательно, чтобы растворимость гидроксида основного металла (см. Фиг. 18) или галогенида основного металла (см. Фиг. 19) в воде была высокой при комнатной температуре при начале зарядки. При начале разрядки, для того, чтобы непрерывно отводить большую мощность в течение долгого времени, желательно, чтобы плотность растворения гидроксида основного металла или галогенида основного металла была небольшой. В конце разрядки желательно, чтобы плотность растворения была высокой, а также близкой к насыщению. При выполнении высокоскоростной зарядки или разрядки большой мощности желательно подогревать водный раствор электролита (с помощью, например, горячего источника, тепла промышленных отходов, охлаждающей двигатель жидкости). Растворимость соединения становится в некоторой степени более высокой, когда температура становится выше, за исключением NaCl, это свойство которого не зависит от повышения температуры. В частности, в случае Ba(ОН)2 растворимость составляет 5% при комнатной температуре, но резко повышается от 40°C и достигает растворимости 60% при 80°C. Растворимость каждого из соединений-кандидатов в воде при 60°C показана на Фиг. 20. На Фиг. 20 четверной кружок означает растворимость 80%; тройной кружок означает растворимость от 60 до 80%; двойной кружок означает растворимость от 30 до 60%; одиночный кружок означает растворимость от 10 до 30%; маленький кружок означает растворимость от 1 до 10%; × означает растворимость 1% или меньше; и треугольник (Δ) означает соединение, которое будет растворяться, если добавлена щелочь. Желательно использовать водные растворы электролита с высокой растворимостью, показанные на Фиг. 18, и водные растворы электролита с высокой разрядной емкостью, показанные на Фиг. 1. [0068] Батареи в соответствии с настоящим изобретением включают батарею кислород/основный металл. Для того, чтобы облегчить батареи, для отрицательного электрода применяется металл с низким удельным весом, а для положительного электрода - атмосферный воздух. Как показывает расчетное значение разрядной емкости батареи кислород/основный металл, показанное на Фиг. 1, при вычислении с учетом веса кислорода батарея Li/O имеет разрядную емкость 6165 Вт⋅ч/кг, но кислород может браться из атмосферы, и поэтому, пренебрегая весом кислорода, она может показать высокую разрядную емкость (такую как 11680 Вт⋅ч/кг). Аналогичным образом батарея Mg/O показывает разрядную емкость 3658 Вт⋅ч/кг, но, пренебрегая воздухом, она может дать 6067 Вт⋅ч/кг. Батарея Al/O показывает разрядную емкость 3264 Вт⋅ч/кг, но, пренебрегая воздухом, она может дать 6165 Вт⋅ч/кг. Однако в соответствии с соотношением между растворимостью гидроксида основного металла и температурой на Фиг. 18, Mg(OH)2 или Al(OH)3 почти не растворяется в воде, и в результате отрицательный электрод покрывается оксидной пленкой, блокируя поток электронов. Это также справедливо для Ca(ОН)2. Известно, что Al, который принадлежит к амфотерным элементам, растворяется, если к водному раствору электролита добавляется едкий натр (поскольку Al(OH)3+NaOH→Na[Al(OH)4]), но в настоящем изобретении рассматриваются только батареи Na/O, K/O, Ba/O, Li/O и Sr/O. Причиной этого является то, что в среде комнатной температуры порядок убывания эффективности этих батарей следующий: K/O>Na/O>Li/O>Ba/O>Sr/O (или Ba/O, когда температура является высокой, как, например, в горячем источнике), а порядок убывания разрядной емкости таков: Li/O>Be/O>Al/O>Mg/O>Ca/O>Na/O>Sr/O>K/O>Ba/O. Конструкция батареи, построенной с учетом этих результатов, показана на Фиг. 21. Здесь для положительной электродной камеры (для батареи) 53 используется кислород или воздух, тогда как для отрицательной электродной камеры (для батареи) 52 используется металл-элемент Группы 1, Группы 2 и/или Группы 13. Кроме того, в герметичном контейнере (оболочечного типа) 55, противоположные стенки которого выполнены из водоотталкивающей пористой мембраны 11, в качестве водного раствора 14 электролита используется основание, такое как едкий натр, едкий калий (гидроксид калия) или гидроксид бария, или кислота, такая как серная кислота, соляная кислота или азотная кислота. В частности, кислородный электрод положительной электродной камеры (для батареи) 53 адсорбирует воздух или кислород в выполненную из углерода пористую электродную пластину 58 (активированный уголь), образуя коллекторную электродную пластину 64 положительного электрода. Кроме того, предусмотрен вспомогательный положительный электрод 56 для зарядки (сетчатый электрод) между водоотталкивающей пористой мембраной 11 и выполненной из углерода пористой электродной пластиной 58 (активированного угля) для того, чтобы избежать выделения тепла в выполненной из углерода пористой электродной пластине 58 (активированного угля) (см. Фиг. 21(A)), или поверхность, контактирующая с водоотталкивающей пористой мембраной 11 положительного электрода, формируется в источник подачи кислорода в виде оксида металла (CuO или Al2O3) 59 металлической пластины 60 (см. Фиг. 21(B)). [0069] С другой стороны, отрицательная электродная камера (для батареи) 52 формируется в изолированный от внешнего воздуха отрицательный электрод 57, формируемый путем адсорбирования продуктов отрицательного электрода из элемента Группы 1 или Группы 2 и/или элемента Группы 13 в порах внутри или на поверхности твердотельного электрода из элемента Группы 1 или Группы 2 и/или элемента Группа 13, или выполненной из углерода электродной пластины, и окружение отрицательного электрода покрывается полимерной пленкой 61, или внутренность отрицательного электрода заполняется маслом 22 для того, чтобы изолировать его от внешней среды. [0070] В этой батарее (первичной или вторичной батарее) зарядка осуществляется в то время, как на водный раствор 14 электролита оказывается давление, а когда заряд закончен, давление, прикладываемое к водному раствору 14 электролита, снимается для того, чтобы сохранить заряд. Для разрядки водный раствор 14 электролита подвергается давлению, чтобы начать разрядку. [0071] Батареи по настоящему изобретению включают в себя батарею металл/хлор, конструкция электродов которой может быть сделана необслуживаемой. Вообще, газообразный галоген является ядовитым. Следовательно, в настоящем изобретении в качестве положительного электрода используется хлорид металла (твердый). Как показано на Фиг. 22, водный раствор хлорида металла запечатывается в качестве водного раствора 14 электролита в герметичном контейнере (оболочечного типа) 55, противоположные стенки которого образованы из водоотталкивающей пористой мембраны 11. Электродная камера 52, присоединенная к водоотталкивающей пористой мембране 11, содержит отрицательные электродные пластины (для батареи) 62 и 65, а положительная электродная камера 53 предусмотрена как металлическая пластина (для батареи) 64 посредством хлорида 63 металла. Хлорид 63 металла в качестве положительного электрода находится в непосредственном контакте с пористой мембраной 11. В этой батарее (первичной или вторичной батарее) зарядка осуществляется в то время, как на водный раствор 14 электролита оказывается давление с помощью оказывающего давление элемента 6. Затем положительные ионы металла, содержащиеся в водном растворе 14 электролита, осаждаются на отрицательной электродной пластине 62. Когда хлорид 63 металла образуется на поверхности металлической пластины 64 положительного электрода, завершая зарядку, давление на водный раствор 14 электролита снимается, чтобы сохранить заряд. Для разрядки давление прикладывается к водному раствору 14 электролита с помощью оказывающего давление элемента 6. Фиг. 22(A) представляет собой концептуальную диаграмму однослойной батареи, а Фиг. 22(B) представляет собой концептуальную диаграмму многослойной батареи. [0072] Многослойная батарея (см. Фиг. 22(B)) формируется путем последовательного соединения однослойных батарей (см. Фиг. 22(A)). Конструкция положительной электродной камеры 53 однослойной батареи включает в себя пленку 63 хлорида металла, которая является хлорированной частью одиночной металлической пластины, которая приведена в контакт с водоотталкивающей пористой мембраной 11, и коллекторную электродную пластину 64, которая представляет собой нехлорированную металлическую часть. Конфигурация электродов между первым слоем и вторым слоем многослойной батареи включает в себя положительный электрод (хлорид металла, используемый для отрицательного электрода) 66, приведенный в контакт с первым слоем, и коллекторную электродную пластину 64 однослойной батареи, используемую в качестве отрицательной электродной пластины 65 второго слоя, а также последующие слои, устроенные аналогично. В случае первичных батарей водный раствор 14 электролита может состоять из хлорида произвольного металла, включая хлорид натрия. При этом в однослойной батарее сочетанием отрицательного электрода и положительного электрода могут быть металлы, произвольно выбираемые из Zn, Mg, Al, Ni, Pb и т.д., или они могут быть из одного и того же металла, и положительный электрод может быть хлоридом произвольно выбираемого металла. В многослойной первичной батарее и отрицательный электрод, и положительный электрод состоят из одного и того же металла, и положительный электрод выполнен из хлорида этого металла, используемого для отрицательного электрода. В случае вторичных батарей водный раствор 14 электролита состоит из хлорида металла, используемого для отрицательного электрода, и в однослойной вторичной батарее сочетание отрицательного электрода и положительного электрода произвольно выбирается из Zn, Mg, Al, Ni, Pb и т.п., или они могут быть из одного и того же металла. Следует отметить, что желательно сделать грубой электродную поверхность положительного электрода, расположенного между противоположными поверхностями герметичного контейнера (оболочечного типа) 55 для того, чтобы увеличить площадь поверхности, а также предусмотреть покрытие для внешних стенок положительного электрода или всего устройства батареи, чтобы защитить хлорид металла от влаги. Что касается этой батареи металл/хлор, как показано на Фиг. 19, порядок следования хлоридов металлов по убыванию их растворимости при комнатной температуре является следующим: ZnCl2>CdCl2>LiCl>BeCl2>CaCl2>MnCl2>NiCl2>FeCl2>CoCl2>MgCl2>AlCl3> BaCl2>KCl>NaCl. С другой стороны, как показано на Фиг. 1, порядок по разрядной емкости является следующим: BeCl2>LiCl>AlCl3>MgCl2>CaCl2>NaCl>KCl>SrCl2>ZnCl2>BaCl2. Что касается настоящего изобретения, хотя Zn, Mg, Al, Ni и Pb рекомендуются в качестве отрицательной электродной пластины, используемой в атмосфере, но также могут использоваться и металлы Группы 1 и Группы 2. В этом случае отрицательный электрод является электродом, получаемым путем адсорбирования элементов Групп 1 и 2 в качестве продуктов отрицательного электрода на твердом электроде из элемента Группы 1 или 2 или порах в поверхности или внутри выполненной из углерода пористой электродной пластины, и, кроме того, необходимо покрыть окружение отрицательного электрода полимерной пленкой либо заполнить внутренность отрицательного электрода маслом для того, чтобы изолировать его от внешней среды. [0073] Батареи по настоящему изобретению дополнительно включают батареи металл/бром и металл/йод. Как правило, газообразный галоген является вредным газом, но при комнатной температуре бром (температура кипения 58,8°C) находится в жидком состоянии, а йод (температура кипения 113,6°C) находится в твердом состоянии. Кроме того, порядок бромидов металлов по убыванию растворимости при комнатной температуре выглядит следующим образом: ZnBr2>LiBr>CaBr2>MnBr2>NiBr2>FeBr2> CoBr2>SrBr2>CdBr2>NaBr>KBr. С другой стороны, как показано на Фиг. 1, порядок по разрядной емкости является следующим: CaBr2> MgBr2>NaBr>LiBr>KBr>SrBr2>MnBr2>NiBr2>FeBr2>BaBr2. Кроме того, порядок иодидов металлов по убыванию растворимости при комнатной температуре выглядит следующим образом: ZnI2>CaI2>BaI2>NaI>SrI2> LiI>KI>MgI2>CaI2>CoI2>PbI2. С другой стороны, как показано на Фиг. 1, порядок по разрядной емкости является следующим: LiI>NaI>CaI2 >MgI2>KI>SrI2>ZnI2>BaI2>PbI2>CoI2>CdI2. Основываясь на этом, в настоящем изобретении было рассмотрено использование положительной электродной камеры, которая хранит галоген в порах внутри твердого тела. В этом положительном электроде, как показано на Фиг. 22(A) и (B), зерна активированного угля или углеродные волокна 67 в изолированном от внешней среды контейнере смешаны с жидким бромом 68 или зернами йода 69, а положительная электродная камера 53 плотно присоединена к водоотталкивающей пористой мембране 11 герметичного контейнера (оболочечного типа) 55. Коллекторная электродная пластина 64 предусмотрена на задней поверхности. С другой стороны, в качестве отрицательного электрода может использоваться голая электродная пластина, выполненная из элемента-металла, имеющего большую склонность к ионизации, чем у водорода, за исключением амфотерных элементов, или магния, или элементов Группы 1 или 2, или может использоваться твердый электрод при применении элемента Группы 1 или 2. Либо, продукт отрицательного электрода из элемента Группы 1 или 2 должен быть осажден и сохранен в порах внутри выполненной из углерода пористой электродной пластины, а окружение отрицательного электрода должно быть покрыто полимерной пленкой или внутренность отрицательного электрода должна быть заполнена маслом, чтобы изолировать его от внешней среды. Для водного раствора 14 электролита этой батареи используется водный раствор бромида или йодида элемента-металла, используемого для отрицательного электрода, и температура атмосферы положительного электрода должна всегда поддерживаться ниже или равной температуре кипения. В отрицательном электроде, как показано на Фиг. 22(A), элемент-металл, имеющий большую склонность к ионизации, чем у водорода, за исключением амфотерных элементов (Zn, Al, Sn и Pb) и Mg, или элементов Группы 1 или 2, (то есть Ni, Pb, Ti, Mn, Cr, Ga, Fe, Cd, Co, Ni или Fe) используется в качестве отрицательной электродной пластины (голой электродной пластины) 62, которая не затрагивается при воздействии внешнего воздуха. Либо, как показано на Фиг. 22(B), при использовании металла Группы 1 или 2 отрицательная электродная камера (для батареи) 52 формируется в изолированный от внешнего воздуха отрицательный электрод 57, формируемый путем адсорбирования продуктов отрицательного электрода из элемента Группы 1 или Группы 2 в порах внутри или на поверхности твердотельного электрода из элемента Группы 1 или Группы 2 (Li, Na, K, Ca, Sr или Ba), либо выполненную из углерода пористую электродную пластину, и электроны отводятся из коллекторной электродной пластины 64. Кроме того, окружение отрицательного электрода покрывается полимерной пленкой 61, или внутренность отрицательного электрода заполняется маслом 22, чтобы изолировать его от внешней среды. В этой батарее (первичной или вторичной батарее) зарядка осуществляется в то время, как на водный раствор 14 электролита оказывается давление, а когда заряд закончен, давление на водный раствор 14 электролита снимается, чтобы сохранить заряд. Для разрядки водный раствор 14 электролита сжимается, чтобы начать разрядку. [0074] Батареи по настоящему изобретению дополнительно включают в себя батарею металл/фтор. Газообразный фтор является смертельно ядовитым и с ним вообще очень трудно обращаться. Однако, как показано на Фиг. 1, его электродный потенциал составляет +2,87 В, что в 7,175 раз выше по сравнению с +0,4 В кислорода. Разрядная емкость большая, поскольку NaF (3568 Вт⋅ч/кг)>KF (2676 Вт⋅ч/кг)>AlF3 (2589 Вт⋅ч/кг), но доступны несколько разновидностей. Кроме того, фториды обладают прочной связью, и большинство из них нерастворимо в воде с очень немногими исключениями типа KF, NaF и AlF3, имеющими растворимости 50%, 4% и 0,5% соответственно при комнатной температуре. Таким образом, перспективным материалом для отрицательного электрода является только калий (K), тогда как натрий (Na) и алюминий (Al) являются неэффективными. С другой стороны, если для положительного электрода используется фторированный графит, можно избежать смертельно ядовитого газообразного фтора при производстве батарей K/F, Na/F и Al/F. В качестве водного раствора 14 электролита этих батарей оптимальным является водный раствор фторида калия. Однако, поскольку фторид алюминия нерастворим, к водному раствору 14 электролита может быть добавлен гидроксид натрия и гидроксид калия. Таким образом может быть получена первичная батарея Al/F, имеющая электродвижущую силу 4,54 В. Первичная или вторичная батарея K/F имеет электродвижущую силу 5,79 В и обладает малым весом, и поэтому она является перспективной в качестве батареи с высокой разрядной емкостью. В положительном электроде, как показано на Фиг. 24(A, B), положительная электродная камера 53 выполнена из графита 70 и плотно присоединена к водоотталкивающей пористой мембране 11 герметичного контейнера (оболочечного типа) 55, и дополнительно содержит коллекторную электродную пластину 64 на задней поверхности. С другой стороны, в качестве отрицательного электрода алюминиевая отрицательная электродная пластина 71 плотно присоединена к водоотталкивающей пористой мембране 11 герметичного контейнера (оболочечного типа) 55, и едкий натр или едкий калий добавляются к фториду алюминия для того, чтобы приготовить водный раствор электролита, и таким образом готовится первичная батарея (см. Фиг. 24(A)). Как показано на Фиг. 24(B), при использовании калия или натрия для первичной или вторичной батареи отрицательная электродная камера (для батареи) 52 формируется в изолированный от внешнего воздуха отрицательный электрод 57, формируемый путем адсорбирования продуктов отрицательного электрода из элемента Группы 1 и/или Группы 2 в порах внутри или на поверхности твердотельного электрода из элемента Группы 1 и/или Группы 2 (Li, Na, K, Ca, Sr или Ba), либо выполненную из углерода пористую электродную пластину, и электроны отводятся из коллекторной электродной пластины 64. Кроме того, окружение отрицательного электрода покрывается полимерной пленкой 61, или внутренность отрицательного электрода заполняется маслом 22, чтобы изолировать его от внешней среды. При этом зарядка и разрядка осуществляются при водном растворе 14 электролита в герметичном контейнере (оболочечного типа) 55. [0075] Конденсаторы по настоящему изобретению включают в себя конденсатор такой конструкции, что положительная и отрицательная электродные пластины (обкладки) соответственно предусмотрены в контакте с противоположными поверхностями герметичного контейнера, выполненного из отталкивающей жидкость пористой мембраны (оболочечного типа), в котором запечатаны диэлектрическая жидкость или раствор электролита. В этом конденсаторе для зарядки и разрядки к этому раствору электролита прикладывается давление, равное давлению жидкостойкости отталкивающей жидкость пористой мембраны, чтобы осуществить электрохимическую реакцию между обоими электродами, а для хранения электричества давление на раствор электролита снимается. Как показано на Фиг. 25 (концептуальная диаграмма), этот конденсатор имеет такую конструкцию, в которой положительная электродная камера 53 и отрицательная электродная камера 52 предусматриваются на наружных поверхностях обеих противоположных боковых стенок герметичного контейнера 55, выполненного из водоотталкивающей пористой мембраны (оболочечного типа) и содержащего водную или образованную на основе масла диэлектрическую жидкость 72 или водный раствор 14 электролита. Электроды, которые составляют пару положительной и отрицательной электродных камер 52 и 53, расположенных на обеих противоположных боковых стенках герметичного контейнера (оболочечного типа) 55, выполненного из водоотталкивающей пористой мембраны, включают электрод 74 конденсатора с двойным электрическим слоем, в котором органические молекулы адсорбируются на поверхности электродной пластины 73 или угольного электрода, например, из активированного угля, графита или наноуглерода, либо электрод 75 окислительно-восстановительного конденсатора, выполненный с оксидной пленкой, образованной на поверхности электрического проводника, электропроводящего полимера, активированного угля и т.п., либо электрод 76 гибридного конденсатора из активированного угля, полифенола, графита титаната лития и т.п. В этом конденсаторе для зарядки к диэлектрической жидкости 72 или раствору 14 электролита прикладывается давление, равное давлению жидкостойкости отталкивающей жидкость пористой мембраны 11, чтобы пропустить заряд между обоими электродами (см. Фиг. 25(A)), приложение давления снимается для хранения заряда (см. Фиг. 25(B)), и давление, равное давлению жидкостойкости отталкивающей жидкость пористой мембраны 11, прикладывается для разряда. Замкнутая пунктирная линия 77, показанная на Фиг. 25(B), изображена для удобства, так как отталкивающая жидкость пористая мембрана 11 и электроды 73, 74, 75 и 76 электродных камер 52 и 53 разделены, но на практике они находятся в контакте. При этом, поскольку никакого давления не прикладывается, поры отталкивающей жидкость пористой мембраны 11 не содержат жидкости. По этой причине водоотталкивающая пористая мембрана 11 рассматривается как пленка с низкой диэлектрической постоянной. [0076] Следовательно, как показано на Фиг. 25(D), если диэлектрический раствор входит в поры, в виде электрической схемы он может быть изображен как конденсатор (C2) переменной емкости, который работает в соответствии с давлением, а если водный раствор электролита входит в поры, то он может быть изображен как реостат (R). Таким образом, при аккумулировании электричества, в порах отталкивающей жидкость пористой мембраны 11 нет жидкого диэлектрика, а только воздух, и поэтому считается, что конденсатор (C1), который хранит заряд, соединяется последовательно с конденсаторами с низкой диэлектрической постоянной (C2) на обоих своих концах. Если к нему прикладывается давление, то в случае диэлектрической жидкости получается C1=C2, тогда как в случае электролита значение R становится бесконечно близким к нулю для заряда или разряда. [0077] Конденсаторы по настоящему изобретению включают в себя конденсатор с двойным электрическим слоем и окислительно-восстановительный электрохимический конденсатор. В этом конденсаторном устройстве положительная и отрицательная электродные камеры являются конденсаторами с высокой диэлектрической постоянной, а внутренность герметичного контейнера (оболочечного типа) из водоотталкивающей пористой мембраны включает в себя электропроводящий материал и электролит. Кроме того, водоотталкивающая пористая мембрана является переключателем, который замыкает и размыкает цепь между положительной и отрицательной электродными камерами. Фиг. 26 представляет собой диаграмму, схематично показывающую конденсатор с двойным электрическим слоем, а Фиг. 27 представляет собой диаграмму, схематично показывающую окислительно-восстановительный конденсатор. Как показано на Фиг. 26 и Фиг. 27, пористый электропроводящий материал 78 из, например, металлического волокна, углеродного волокна или активированного угля, заполняющий герметичный контейнер (оболочечного типа) 55, выполненный из водоотталкивающей пористой мембраны, расположенной между парой положительной и отрицательной электродных камер 52 и 53, увлажняется водным раствором 14 электролита, таким как разбавленная серная кислота 79 или разбавленный едкий натр 80, и на водный раствор 14 электролита прикладывающий давление элемент 6 оказывает давление, равное давлению водостойкости отталкивающей жидкость пористой мембраны 11, чтобы заставить водный раствор электролита проходить поры отталкивающей жидкость пористой мембраны 11 (см. Фиг. 26(A), Фиг. 27(A)) для зарядки. Для хранения заряда давление на раствор электролита снимается (см. Фиг. 26(B), Фиг. 27(B)). Для разрядки равное давлению водостойкости давление снова прикладывается прикладывающим давление элементом 6. Замкнутая пунктирная линия 77, показанная на Фиг. 26(B) и Фиг. 27(B), изображена для удобства, так как отталкивающая жидкость пористая мембрана 11 и электродные камеры 52 и 53 разделены. Однако на практике они находятся в контакте. При этом давление не прикладывается, и поэтому в порах отталкивающей жидкость пористой мембраны 11 нет жидкости. В этом состоянии водоотталкивающая пористая мембрана 11 рассматривается как пленка с низкой диэлектрической постоянной. Следовательно, как показано на Фиг. 26(D) и Фиг. 27(D) вместе с эквивалентными электрическими схемами, в отсутствие давления водный раствор 14 электролита не входит в поры водоотталкивающей пористой мембраны 11, и таким образом формируется конденсатор (C2) с низкой диэлектрической постоянной. Под давлением водный раствор 14 электролита входит в поры водоотталкивающей пористой мембраны 11, включая переключатель (S) на электрической схеме, а значит, положительная электродная камера и отрицательная электродная камера замыкаются накоротко через герметичный контейнер (оболочечного типа) 55, выполненный из водоотталкивающей пористой мембраны, соединяя два последовательно включенных конденсатора (C1) с высокой диэлектрической постоянной для зарядки и разрядки. Если давление на водный раствор 14 электролита снимается, два конденсатора (C2) с низкой диэлектрической постоянной и два конденсатора (C1) с высокой диэлектрической постоянной соединяются последовательно для хранения заряда. С другой стороны, отрицательная электродная камера 52 и положительная электродная камера 53 имеют ту же самую конструкцию, но конденсатор с двойным электрическим слоем и окислительно-восстановительный конденсатор отличаются друг от друга. [0078] Что касается конструкции отрицательной электродной камеры 52 и положительной электродной камеры 53 конденсатора с двойным электрическим слоем, зерна 67 активированного угля плотно присоединяются к водоотталкивающей пористой мембране 11, а на противоположной поверхности предусмотрена коллекторная электродная пластина 64, изолируя таким образом положительную и отрицательную электродные камеры 52 и 53 от внешнего воздуха, как показано на Фиг. 26(A), (B) и (C). [0079] Конструкция отрицательной электродной камеры 52 и положительной электродной камеры 53 окислительно-восстановительного конденсатора содержит, как показано на Фиг. 27(A), (B) и (C), металлическую пластину (Al) 108 окислительно-восстановительного конденсатора и пленку 109 оксида металла (Al2O3) окислительно-восстановительного конденсатора в качестве диэлектрика, приготовленную путем электрического окисления той поверхности металлической пластины, которая обращена к водоотталкивающей пористой мембране 11. Каждая из металлических пластин, функционирующих как положительный и отрицательный электроды, плотно присоединяется к пористой мембране 11 через пленку 109 оксида металла. [0080] В настоящем изобретении элементы-основные металлы могут быть отдельно собраны из водного раствора, в котором смешаны соли основных металлов. Множество наборов вышеописанных устройств получения водорода и устройств сбора основного металла соединяются последовательно и в этих устройствах осуществляется электролитическое рафинирование, начиная с устройства получения водорода в порядке более низкого напряжения разложения металла, осаждаемого из водного раствора электролита, содержащего множество смешанных в нем солей основных металлов. Затем непрореагировавший водный раствор электролита переносится в последующее устройство сбора основного металла, где электролитическое рафинирование водного раствора электролита осуществляется под давлением. Здесь, поскольку устройства работают в порядке увеличения напряжения разложения, основные металлы собираются соответственно этому порядку. [0081] В соответствии с одним вариантом осуществления настоящего изобретения предложена находящаяся в море (морская) или на берегу (прибрежная) фабрика, которая производит водород или едкий натр на месте из морской воды в качестве сырья, используя естественные источники питания или энергии, получаемые в море, или, например, ночную электроэнергию от прибрежной теплоэлектростанции. В этом варианте осуществления на морской и/или прибрежной фабрике производится едкий натр или водород, как описано выше, и далее из полученного водорода и едкого натра производится гидрид натрия, как описано выше, в океане или на суше. Кроме того, на суше на гидрид натрия заливается вода для того, чтобы получить водород, а едкий натр, который производится в качестве побочного продукта, используется для воспроизводства гидрида натрия. Таким образом может быть реализован топливный цикл едкого натра. Кроме того, едкий натр, который является промежуточным продуктом, может также использоваться в качестве водного раствора электролита для вторичных батарей. [0082] Кроме того, в соответствии с настоящим изобретением заданное вещество помещается в контейнер, образованный из водоотталкивающей пористой мембраны, и этот контейнер помещается в жидкость из водного раствора или воды электролита или неэлектролита. Под давлением текучей среды, равным давлению водостойкости водоотталкивающей пористой мембраны, жидкость проникает через поры водоотталкивающей пористой мембраны для проведения ионной реакции, реакции гидролиза или реакции растворения между веществом внутри контейнера и этой жидкостью. [0083] Например, в соответствии с настоящим изобретением, в контейнере (реакционной камере) из водоотталкивающей пористой мембраны содержится вещество, которое дает газ при гидролизе или контакте с водой, вещество, которое дает тепло при гидролизе или контакте с водой, вещество, которое поглощает тепло при гидролизе или контакте с водой, или водорастворимое органическое соединение, или т.п., и реакционная камера помещается в жидкую воду или водный раствор неэлектролита, содержащийся в герметичном контейнере. Затем давление, которое делает разность между внешним и внутренним давлениями реакционной камеры большим или равным давлению водостойкости водоотталкивающей пористой мембраны, прикладывается к водоотталкивающей пористой мембране через жидкость, чтобы ввести эту жидкость в реакционную камеру. Здесь содержащееся в реакционной камере вещество реагирует с этой водой, вызывая реакции образования газа, теплообразования, поглощения тепла и растворения. Газ и водный раствор, получаемые здесь, могут использоваться для переноса химических или питательных веществ в живой организм или добавления органического соединения к водному раствору и т.д. [0084] Кроме того, в соответствии с настоящим изобретением трубка и т.п. для распыления химикатов, выполненная из водоотталкивающей пористой мембраны, предусмотрена для желаемого места, в котором подсоединяется шланг между подающим химикат входом трубки и источник подачи водного раствора химика, и к этому водному раствору химиката на подающем химикат входе может непрерывно или периодически по мере необходимости прикладываться давление, большее или равное давлению водостойкости водоотталкивающей пористой мембраны, позволяя тем самым подавать водный раствор химиката в желаемое место. Водный раствор химиката включает в себя, например, лекарственное вещество, питательное вещество и удобрение. [0085] Кроме того, в соответствии с настоящим изобретением предлагается капсула на конце эндоскопа, в которой запечатано экзотермическое гидролитическое средство, и к ней через водоотталкивающую пористую мембрану прикладывается гидравлическое давление, большее или равное давлению водостойкости, чтобы вызвать экзотермическую реакцию гидролиза, тем самым нагревая раковые клетки в органе выработанным таким образом теплом. Эффекты изобретения [0086] Как упомянуто выше, в соответствии с настоящим изобретением давление водостойкости или большее или равное ему гидравлическое давление прикладывается к пористой пленке фторкаучука, которая имеет высокие электроизоляционные свойства в водном растворе электролита, таком как морская вода и вода соленого озера, и водный раствор электролита и/или ионы проникают через поры пористой пленки фторкаучука. Исходя из этого, количеством водного раствора и ионов, которое может проходить через водоотталкивающую пористую мембрану, можно управлять аналоговым образом, и таким образом может быть реализована функция переключателя. Водоотталкивающая пористая мембрана используется в качестве изоляционной пленки между водным раствором электролита и положительной и отрицательной электродными камерами, и давление прикладывается к водному раствору электролита для того, чтобы вызвать электролиз водного раствора, который производит электродные продукты в каждой из положительной и отрицательной электродных камер. Произведенные таким образом продукты отделяются и собираются из водного раствора электролита. Таким образом, водород, едкий натр, элемент-основный металл и т.д. могут быть извлечены непосредственно из водных растворов электролита, таких как морская вода и вода соленого озера. Эта технология может быть применена не только к электролитическому рафинированию, но и к практичным батареям или крупногабаритным конденсаторам. Традиционно для этого существует только способ осуществления электролиза в солевом расплаве при высокой температуре с использованием большой мощности. Однако в соответствии с настоящим изобретением электролиз водных растворов может быть осуществлен при обычной температуре, создавая тем самым значительный экономический эффект. В частности, металлический натрий, получаемый из морской воды, может стать, как ожидается, альтернативой энергии нефти. Кроме того, он никогда не истощится как энергетический ресурс, который весьма неравномерно распределен по всему миру. Эта технология может способствовать созданию мира без войны за ресурсы. Кроме того, батарея основный металл/воздух и батарея основный металл/галоген, которые используют, например, литий, натрий или кальций в качестве сырья, для которых электролит может использоваться непосредственно в виде водного раствора, могут найти применение в качестве вторичной батареи для возобновляемых источников питания, которые, вероятно, будут зависеть от климата. Кроме того, она может использоваться в качестве легкой и высокоэффективной батареи, способствующей разработке электромобилей, что дополнительно способствует прогрессу водородного общества, которое не производит выбросов двуокиси углерода или излучения. КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ [0087] Фиг. 1 показывает сравнение между батареей основный металл/кислород и батареей основный металл/галоген по разрядной емкости. Фиг. 2 представляет собой диаграмму, объясняющую принцип работы переключателя давления из отталкивающей жидкость пористой мембраны (изоляционной пленки), где (A) показывает случай, в котором водный раствор электролита находится под давлением водостойкости или меньшим, тогда как (B) показывает случай, в котором водный раствор электролита находится под давлением водостойкости или большим. Фиг. 3A показывает сравнение между электрическими свойствами раствора и ролью отталкивающей жидкость пористой мембраны в электронном переключателе из отталкивающей жидкость пористой мембраны (изоляционной пленки). Фиг. 3B показывает другое сравнение между электрическими свойствами раствора и ролью отталкивающей жидкость пористой мембраны в электронном переключателе из отталкивающей жидкость пористой мембраны (изоляционной пленки). Фиг. 4 схематично показывает химический реактор, содержащий средство изоляции раствора электролита, предусмотренное между положительным и отрицательным электродами, где (A) показывает случай, в котором средство изоляции образует герметичный контейнер из отталкивающей жидкость пористой мембраны, (B) показывает случай, в котором химический реактор располагается в открытом контейнере, и (C) показывает случай, в котором средство изоляции образует герметичный контейнер из отталкивающей жидкость пористой мембраны, и этот герметичный контейнер располагается в открытом контейнере. Фиг. 5 схематично показывает прикладывающий давление элемент, где (A) показывает случай, в котором герметичный контейнер, образованный из отталкивающей жидкость пористой мембраны, сжимается непосредственно, (B) показывает случай, в котором используется ручное или электрическое повышение давления с использованием соединительной трубки или гидравлическое давление от гидростатического напора, и (C) показывает случай, в котором гидростатический напор применяется к герметичному контейнеру, находящемуся в открытом контейнере. Фиг. 6 представляет собой диаграмму, объясняющую способ заполнения внутренности полого герметичного контейнера (мешка) из водоотталкивающей пористой мембраны водным раствором электролита, где (A) показывает случай, в котором водный раствор электролита заливается непосредственно в полый герметичный контейнер (мешок), (B) показывает случай, в котором вода или пар подаются под давлением к растворяемому веществу, помещенному в полый герметичный контейнер (мешок), (C) показывает случай, в котором водный раствор электролита подается под давлением в полый герметичный контейнер (мешок) через водоотталкивающую пористую мембрану, и (D) показывает случай, в котором спирт наносится на водоотталкивающую пористую мембрану полого герметичного контейнера (мешка), чтобы запасти водный раствор электролита. Фиг. 7 показывает соотношение между конструкцией и использованием положительного и отрицательного электродов, изолированных водоотталкивающей пористой мембраной. Фиг. 8 показывает эквивалентную электрическую схему для электролиза водного раствора электролита с использованием границы раздела между стороной водного раствора электролита и стороной масла в качестве поверхности отрицательного электрода, где (A) показывает концептуальную диаграмму схемы Мурахары, а (B) показывает электрическую схему (формулу). Фиг. 9 представляет собой концептуальную диаграмму масляного конденсатора, который использует границу раздела между маслом и водным раствором электролита в качестве отрицательного электрода, где (A) представляет собой структурную диаграмму виртуального отрицательного электрода, использующего водоотталкивающую пористую мембрану, (B) представляет собой структурную диаграмму, показывающую случай, в котором виртуальный отрицательный электрод составляет вертикальную плоскость относительно оси земли, и удельный вес масла составляет меньше 1, и (C) представляет собой структурную диаграмму, показывающую случай, в котором виртуальный отрицательный электрод составляет вертикальную плоскость относительно оси земли, и удельный вес масла превышает 1. Фиг. 10 представляет собой диаграмму, схематично показывающую устройство для производства водорода путем погружения газопроницаемой электродной камеры под поверхность моря и непосредственного электролиза морской воды, где (A) показывает электролитическое устройство, использующее гидравлическое давление под морской поверхностью, и (B) показывает электролитическое устройство, которое сжимает соленую воду на суше. Фиг. 11 представляет собой диаграмму, схематично показывающую устройство получения водорода, которое подвергает электролизу воду в герметичном контейнере, вставленном в открытый контейнер или крупногабаритный герметичный контейнер, где (A) показывает электролитическое устройство, использующее гидравлическое давление под поверхностью воды пресноводного озера, а (B) показывают электролитическое устройство, сжимаемое водопроводной водой. Фиг. 12 представляет собой диаграмму, схематично показывающую устройство производства гидроксида основного металла (едкого натра), где (A) показывает устройство, которое производит гидроксид основного металла (едкий натр) на отрицательном электроде и газообразный продукт положительного электрода (хлор) на положительном электроде, а (B) показывает устройство, которое производит гидроксид основного металла (едкий натр) на отрицательном электроде и кислоту (соляную кислоту) на положительном электроде. Фиг. 13 представляет собой диаграмму, схематично показывающую устройство сбора основного металла, где (A) показывает устройство, которое производит основный металл в масляном баке заполненной маслом отрицательной электродной камеры и газообразный продукт положительного электрода (хлор) на положительном электроде, а (B) показывают устройство, которое производит основный металл в масляном баке заполненной маслом отрицательной электродной камеры и кислоту (соляную кислоту) на положительном электроде. Фиг. 14 представляет собой диаграмму, схематично показывающую устройство электролитического рафинирования, которое использует границу раздела между маслом и водным раствором электролита в качестве виртуального отрицательного электрода, где (A) показывает устройство электролитического рафинирования, включающее в себя промежуточную электродную пластину, вставленную в заполненную маслом электродную камеру, а (B) показывают устройство электролитического рафинирования, включающее в себя твердотельный конденсатор вне системы заполненной маслом электродной камеры. Фиг. 15 представляет собой диаграмму, схематично показывающую устройство производства гидрида основного металла с помощью ионной реакции между отрицательным ионом водорода и расплавленной солью. Фиг. 16 сравнивает и показывает температуру плавления и удельный вес гидрида основного металла и гидроксида основного металла. Фиг. 17 представляет собой диаграмму, схематично показывающую батарею, где (A) показывает батарею во время зарядки, (B) показывает батарею во время хранения заряда и (C) показывает батарею во время разрядки. Фиг. 18 показывает соотношение между растворимостью и температурой гидроксилированного основного металла. Фиг. 19 показывает соотношение между растворимостью и температурой галогенида (хлорида) основного металла. Фиг. 20 показывает растворимость в воде электролита, используемого для батареи основный металл/кислород или батареи основный металл/галоген. Фиг. 21 представляет собой диаграмму, схематично показывающую батарею основный металл/воздух, где (A) показывает батарею, включающую в себя вспомогательный электрод для зарядки и положительный электрод, выполненный из пористой углеродной пластины, а (B) показывает батарею, которая использует оксид металла в качестве положительного электрода. Фиг. 22 представляет собой диаграмму, схематично показывающую батарею основный металл/хлор, где (A) показывает однослойную батарею, а (B) показывает многослойную батарею. Фиг. 23 представляет собой диаграмму, схематично показывающую батарею основный металл/бром и батарею основный металл/йод, где (A) показывает батарею в том случае, когда отрицательный электрод состоит из металла, который не подвержен влиянию атмосферы, а (B) представляет собой концептуальную диаграмму батареи в том случае, когда отрицательный электрод состоит из металла Группы 1 или 2 Периодической таблицы, который подвергается влиянию атмосферы. Фиг. 24 представляет собой диаграмму, схематично показывающую батарею основный металл/фтор, где (A) показывает батарею типа Al/F, а (B) показывает батарею типа K/F или батарею типа Na/F. Фиг. 25 представляет собой диаграмму, схематично показывающую конденсатор, где (A) показывает конденсатор во время зарядки, (B) показывает конденсатор во время хранения заряда, (C) показывает конденсатор во время разрядки, а (D) представляет собой диаграмму, объясняющую работу схемы во время зарядки, хранения заряда и разрядки. Фиг. 26 представляет собой диаграмму, схематично показывающую конденсатор с двойным электрическим слоем, где (A) показывает конденсатор во время зарядки, (B) показывает конденсатор во время хранения заряда, (C) показывает конденсатор во время разрядки, а (D) представляет собой диаграмму, объясняющую работу схемы во время зарядки, хранения заряда и разрядки. Фиг. 27 представляет собой диаграмму, схематично показывающую окислительно-восстановительный конденсатор, где (A) показывает конденсатор во время зарядки, (B) показывает конденсатор во время хранения заряда, (C) показывает конденсатор во время разрядки, а (D) представляет собой диаграмму, объясняющую работу схемы во время зарядки, хранения заряда и разрядки. Фиг. 28 представляет собой график, показывающий зависимость между давлением водостойкости пористой пленки фторкаучука и концентрацией соли, где (A) показывает случай, в котором диаметр пор пористой пленки фторкаучука составляет 3 мкм, а (B) показывают случай, в котором диаметр пор пористой пленки фторкаучука составляет примерно 10 мкм. Фиг. 29 представляет собой диаграмму, схематично показывающую устройство получения водорода, используемое под морской поверхностью. Фиг. 30 представляет собой диаграмму, схематично показывающую устройство получения водорода многоступенчатого типа, используемое под морской поверхностью. Фиг. 31 представляет собой диаграмму, схематично показывающую устройство получения водорода, используемое под поверхностью озера. Фиг. 32 представляет собой диаграмму, схематично показывающую простое устройство получения водорода, использующее давление водопроводной воды. Фиг. 33 представляет собой диаграмму, схематично показывающую устройство, которое производит едкий натр и газообразный хлор непосредственно из водного раствора хлорида натрия. Фиг. 34 представляет собой диаграмму, схематично показывающую устройство, которое производит едкий натр и соляную кислоту непосредственно из водного раствора хлорида натрия. Фиг. 35 представляет собой диаграмму, схематично показывающую устройство, которое производит основный металл непосредственно из водного раствора хлорида основного металла. Фиг. 36 представляет собой диаграмму, схематично показывающую устройство, которое производит элемент-основный металл и соляную кислоту непосредственно из водного раствора хлорида основного металла. Фиг. 37 представляет собой диаграмму, схематично показывающую устройство получения основного металла, которое использует виртуальный отрицательный электрод, где (A) показывает устройство, а (B) показывает эквивалентную электрическую схему. Фиг. 38 представляет собой диаграмму, схематично показывающую устройство получения гидрида основного металла. Фиг. 39 представляет собой диаграмму, схематично показывающую резервуар водного раствора электролита, вставляемый в герметичный контейнер оболочечного типа, где (A) показывает устройство перед запасанием водного раствора электролита, а (B) показывает устройство после запасания водного раствора электролита. Фиг. 40 представляет собой диаграмму, схематично показывающую вторичную батарею со сжатием электролита, где (A) показывает случай, в котором на водный раствор электролита не оказывается давления, а (B) показывает случай, в котором на водный раствор электролита оказывается давление. Фиг. 41 представляет собой диаграмму, схематично показывающую вторичную батарею многослойного типа с едким натром, где (A) представляет собой вид в разрезе, а (B) представляет собой вид в перспективе. Фиг. 42 представляет собой диаграмму, схематично показывающую окислительно-восстановительный конденсатор, где (A) показывает вид в разрезе, а (B) показывает эквивалентную электрическую схему. Фиг. 43 представляет собой диаграмму, схематично показывающую устройство, которое извлекает основные металлы из водного раствора смеси солей основных металлов. Фиг. 44 представляет собой диаграмму, схематично показывающую топливный цикл едкого натра. Фиг. 45 представляет собой диаграмму, схематично показывающую реактор гидролиза. Фиг. 46 представляет собой диаграмму, схематично показывающую поставщика воды/удобрения для гидропонных систем. Фиг. 47 представляет собой диаграмму, объясняющую медицинское устройство типа эндоскопа, где (A) показывает сечение тела человека, (B) показывает питаемую через трубку капсулу с питательным веществом/химикатом, а (C) показывают капсулу для термотерапии рака. НАИЛУЧШИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ [0088] Эффективные варианты осуществления настоящего изобретения будут описаны подробно со ссылками на Фиг. 28 - Фиг. 47. [0089] Фиг. 28 представляет собой график, изображающий измеренные значения давления водостойкости водоотталкивающей пористой пленки фторкаучука, которая является основой настоящего изобретения, показывающий соотношение между концентрацией водного раствора электролита и минимальным давлением, требуемым для того, чтобы водный раствор электролита проходил через водоотталкивающую пористую пленку фторкаучука (минимальный перепад давления между обеими сторонами водоотталкивающей пористой пленки фторкаучука, требуемый для прохождения водного раствора электролита через водоотталкивающую пористую пленку фторкаучука, который иногда называют перепадом давления проникания). Давление водостойкости сформулировано в японском промышленном стандарте (JIS) L1092:2009. [0090] Фиг. 28(A) показывает результаты случая, в котором водные растворы хлорида натрия различных концентраций использовались в качестве водных растворов электролита для водоотталкивающей пористой мембраны из фторкаучука (пористой мембраны ПТФЭ NTF-1133 производства компании NITTO DENKO CORPORATION), имеющей диаметр пор 3 мкм. Обычно давление водостойкости является значением относительно чистой воды. Кроме того, соленость (концентрация хлорида натрия) морской воды составляет обычно примерно 3 мас.%, а концентрация насыщения хлорида натрия под водой составляет примерно 25 мас.%. Поэтому хлорид натрия в различных концентрациях от 0 мас.% до 25 мас.% был добавлен к воде и была измерена зависимость между концентрацией хлорида натрия и давлением водостойкости при комнатной температуре. Давление водостойкости выполненной из фторкаучука водоотталкивающей пористой мембраны составило 430 мм рт.ст. (0,57 атм) при концентрации хлорида натрия 0 мас.%, 320 мм рт.ст. (0,42 атм) при концентрации хлорида натрия 10 мас.%, 280 мм рт.ст. (0,37 атм) при концентрации хлорида натрия 20 мас.% и 270 мм рт.ст. (0,36 атм) при концентрации хлорида натрия 25 мас.%. Таким образом, по мере того, как концентрация хлорида натрия увеличивается, давление водостойкости уменьшается. Кроме того, давление водостойкости имеет тенденцию уменьшаться, если увеличивается температура водного раствора электролита. [0091] Фиг. 28(В) показывает результаты случая, в котором водные растворы хлорида натрия различных концентраций использовались в качестве водных растворов электролита для водоотталкивающей пористой мембраны из фторкаучука (F-3011-3 производства компании FLON INDUSTRY), имеющей диаметр пор 10 мкм. Давление водостойкости выполненной из фторкаучука водоотталкивающей пористой мембраны составляло 120 мм рт.ст. (0,16 атм) при концентрации хлорида натрия 0 мас.% и 50 мм рт.ст. (0,07 атм) при концентрации хлорида натрия 2 мас.%. [0092] Как можно заметить из результатов, показанных на Фиг. 28(A) и Фиг. 28(B), если диаметр пор пористой мембраны становится больше, давление водостойкости становится меньше. Кроме того, поскольку давление водостойкости уменьшается, если концентрация электролита увеличивается при том же самом давлении (гидравлическом давлении), электролиты различных концентраций, разделенные отталкивающей жидкость пористой мембраной, текут со стороны более высокой концентрации к стороне более низкой концентрации. Таким образом, когда водный раствор электролита с высокой концентрацией присутствует в герметичном контейнере, образованном из отталкивающей жидкость пористой мембраны, и водный раствор электролита с низкой концентрацией присутствует с внешней стороны герметичного контейнера, водный раствор электролита просачивается наружу герметичного контейнера. Для того чтобы избежать этого, необходимо понизить давление в электродной камере, плотно присоединенной к герметичному контейнеру, и управлять перепадом давления так, чтобы водный раствор электролита низкой концентрации с внешней стороны герметичного контейнера входил во внутренность герметичного контейнера через отталкивающую жидкость пористую мембрану и попадал в электродную камеру через другую отталкивающую жидкость пористую мембрану. [0093] Фиг. 29 представляет собой диаграмму, схематично показывающую устройство получения водорода, используемое под морской поверхностью. Отрицательная электродная камера 52 и положительная электродная камера 53, каждая из которых образована из газопроницаемой электродной камеры с пористым электродом, перечисленными на Фиг. 7, погружается под морскую поверхность, и морская вода непосредственно подвергается электролизу с получением водорода. [0094] В используемом под морской поверхностью устройстве 84 получения водорода по Фиг. 29 внешние стенки положительной и отрицательной электродных камер 52 и 53 образованы из трубы, выполненной из винилхлоридной смолы, продольно разрезанной пополам, и отверстие, полученное при разрезании в половинке, было закрыто пористой ПТФЭ мембраной (NTF-1133 производства компании NITTO DENKO CORPORATION) 11, имеющей диаметр пор 33 мкм. Как показано в разрезе отрицательной электродной камеры 52, волокно 81 из нержавеющей стали («Web» Naslon (зарегистрированный товарный знак) производства компании Nippon Seisen Inc.) было помещено в отрицательную электродную камеру 52, и, как показано на виде в разрезе положительной электродной камеры 53 с другой стороны, углеродная ткань (из углеродного волокна) 82 была помещена в положительную электродную камеру 53. Кроме того, шланг 12 сбора полученного газа был соединен с верхней частью каждой из электродных камер 52 и 53, и проводные линии положительного и отрицательного электродов были обеспечены внутри шлангов 12 сбора соответственно. [0095] Здесь водный раствор 14 электролита является морской водой, и средняя соленость морской воды составляет 3,5 мас.%. Кроме того, давление водостойкости пористой пленки фторкаучука с диаметром пор 3 мкм для водного раствора хлорида натрия, имеющего концентрацию 3,5 мас.%, как известно из соотношения между давлением водостойкости пористой мембраны и концентрацией соли, показанного на Фиг. 28(A), составляет 380 мм рт.ст. Поскольку гидравлическое давление в воде составляло 1 атм (760 мм рт.ст.) на глубине 10 м, глубина погружения (h) 10 была установлена равной примерно 5 м. Температура морской воды составляла 23°C, а удельная электропроводность составляла 0,03 См/см. При этом, когда межэлектродное расстояние d (83) было установлено равным 10 мм и между обоими электродами было подано напряжение 1,5 В, потребность в энергии на 1 м3 водорода и 0,5 м3 кислорода составила 18,3 кВт⋅ч. Когда напряжение между обоими электродами было 2,5 В или выше, на положительном электроде образовывался хлор. Следует отметить, что когда используемое здесь устройство 84 получения водорода было размещено на суше, и межэлектродное расстояние d (83) было установлено равным 10 мм и подано напряжение 1,5 В между обоими электродами с использованием водного раствора электролита (с удельной электропроводностью 0,18 См/см), в котором концентрация хлорида натрия была увеличена до 25 мас.%, потребность в энергии на 1 м3 водорода и 0,5 м3 кислорода составила примерно 10 кВт∙ч. [0096] Фиг. 30 представляет собой диаграмму, показывающую конструкцию используемого под морской поверхностью устройства получения водорода многоступенчатого типа, предназначенного для электролиза морской воды под поверхностью моря для производства водорода. Отрицательная электродная камера 52 и положительная электродная камера 53, каждая из которых выполнена из газопроницаемой электродной камеры с пористым электродом, перечисленными на Фиг. 7, погружены под морскую поверхность, и морская вода непосредственно подвергается электролизу с получением водорода. Средняя концентрация соли в морской воде, используемой в качестве водного раствора 14 электролита, составляет 3,5 мас.%. Давление водостойкости для водного раствора хлорида натрия, имеющего концентрацию 3,5%, как известно из соотношения между давлением водостойкости пористой пленки фторкаучука с диаметром пор 3 мкм и концентрацией соли, показанного на Фиг. 28(A), составляет 380 мм рт.ст. Таким образом, используемое под морской поверхностью устройство 84 получения водорода многоступенчатого типа опускали на глубину примерно 5 м (гидростатический напор (h) 10) для испытания. [0097] В устройстве 85 получения водорода многоступенчатого типа, проиллюстрированном на Фиг. 30, пористая ПТФЭ мембрана (NTF-1133 производства компании NITTO DENKO CORPORATION), имеющая диаметр пор 3 мкм, использовалась в качестве выполненной из фторкаучука водоотталкивающей пористой мембраны 11 для положительных и отрицательных электродных камер 52 и 53, а внешние стенки каждой из положительных и отрицательных электродных камер 52 и 53 были образованы из винилхлорида. Шланг 12 сбора продуктового газа был соединен с верхними частями электродных камер 52, и отрицательные электродные камеры 52 и положительные электродные камеры 53 были чередующимся образом расположены последовательно. Таким образом, газообразный водород, произведенный в каждой из отрицательных электродных камер 52, и кислород, произведенный в положительных электродных камерах 53, сразу собирали через трубу. В этом испытании используемое под морской поверхностью устройство 84 получения водорода многоступенчатого типа включает в себя три набора собирающих водород отрицательных электродных камер 52 и собирающих кислород положительных электродных камер 53, расположенных параллельно с расстоянием (83) между смежными электродами, установленным на 10 мм. Материалом электрода отрицательных электродных камер 52 было волокно 81 из нержавеющей стали («Web» Naslon (зарегистрированный товарный знак) производства компании Nippon Seisen Inc.), тогда как положительные электроды являлись электродными камерами той же самой конструкции, что и для отрицательных электродов, в которые была помещена углеродная ткань (углеродное волокно) 82. Так как устройство находится в морской воде, концентрация соли в электролите составляла 3,5 мас.%, температура морской воды составляла 23°C, а ее удельная электропроводность составляла 0,03 См/см. Когда напряжение 1,5 В было подано на оба электрода, потребность в энергии на 1 м3 водорода и 0,5 м3 кислорода составила примерно 17 кВт⋅ч. [0098] Фиг. 31 представляет собой диаграмму, показывающую конструкцию устройства получения водорода, используемого под водной поверхностью озера. Принцип, как показано на Фиг. 11, заключается в том, что пресная вода подается под давлением из внешней стенки герметичного контейнера в водный раствор электролита высокой концентрации, герметично запечатанный в герметичном контейнере из водоотталкивающей пористой мембраны, через водоотталкивающую пористую мембрану, для подачи водного раствора под давлением с целью непосредственного производства водорода и кислорода или хлора с высокой эффективностью. Герметичный контейнер из водоотталкивающей пористой мембраны, заполненный водным раствор электролита высокой концентрации (водным раствором электролита с высокой растворимостью и высокой проводимостью), погружается в открытый контейнер, такой как пресноводное озеро, пруд или море. Таким образом, в то время как пресная вода или водный раствор электролита низкой концентрации подается под давлением через водоотталкивающую пористую мембрану для подачи водного раствора под давлением, присоединенную к герметичному контейнеру, водный раствор подвергается электролизу с получением водорода. [0099] Фиг. 31 показывает устройство 86 получения водорода под поверхностью озера (или моря), содержащее герметичный контейнер 87 в форме четырехугольной призмы, расположенный между отрицательной электродной камерой 52 и положительной электродной камерой 53. Герметичный контейнер 87 в форме четырехугольной призмы включает в себя четыре боковых поверхности, две из которых (те, которые находятся в контакте с положительной и отрицательной электродными камерами 52 и 53) выполнены из водоотталкивающего пористого материала 11, а по меньшей мере одна из других поверхностей выполнена из водоотталкивающей пористой мембраны (для проникания пресной воды) 27. В герметичном контейнере 87 в форме четырехугольной призмы содержится серная кислота с нормальностью примерно 3 и водный раствор едкого натра с нормальностью 4 для усиления электролитической диссоциации. Пресная вода 88 или водный раствор электролита низкой концентрации, входящий снаружи в водоотталкивающую пористую мембрану 27 герметичного контейнера 87 пресноводного осмоса в форме четырехугольной призмы, подвергается электролизу положительной и отрицательной электродными камерами с получением водорода и кислорода. Используемые здесь кислота и щелочь называются катализаторами ионизации. Следует отметить, что в водном растворе хлорида натрия давление водостойкости водоотталкивающей пористой пленки фторкаучука (имеющей диаметр пор 33 мкм) по Фиг. 28(A) составляло 430 мм рт.ст. для воды и 330 мм рт.ст. для 10%-го водного раствора хлорида натрия, и таким образом перепад давления составлял 100 мм рт.ст. Здесь диаметр пор водоотталкивающей пористой пленки фторкаучука (электродной изоляционной пленки) 11 выбирается меньшим, чем у водоотталкивающей пористой мембраны (для проникания пресной воды) 27, или водоотталкивающая пористая пленка фторкаучука (электродная изоляционная пленка) 11 подвергается обработке для придания ей гидрофильных свойств с тем, чтобы уравнять или сблизить давление водостойкости водоотталкивающей пористой пленки фторкаучука (электродной изоляционной пленки) 11 вследствие концентрации соли с давлением водостойкости водоотталкивающей пористой мембраны (для проникания пресной воды) 27 вследствие пресной воды, что является особенностью настоящего изобретения. Следует отметить, что устройство 86 получения водорода применимо также к морям и воде горячего источника, отличающегося от озера. При использовании конструкции устройства по настоящему изобретению продуктовые газы из положительной и отрицательной электродных камер собираются на поверхности воды путем отсасывания газов на водной поверхности. Следовательно, если давления газов положительной и отрицательной электродных камер понижаются путем отсасывания вакуумным насосом, нет никакой необходимости опускать устройство 87 получения водорода на глубину гидростатического давления. Кроме того, поскольку давления газов положительной и отрицательной электродных камер 52 и 53 являются более низкими, чем гидравлическое давление пресной воды или слабого электролита, входящего в водоотталкивающую пористую мембрану (для проникания пресной воды) 27, серная кислота никогда не вытекает во внешнюю пресную воду из водоотталкивающей пористой мембраны (для проникания пресной воды) 88 герметичного контейнера. Кроме того, поскольку давлением газа в каждой из положительной и отрицательной электродных камер можно управлять путем отсасывания газа из положительной или отрицательной электродной камеры с помощью вакуумного насоса, водоотталкивающие пористые пленки фторкаучука (электродные изоляционные пленки) 11 и 27 могут состоять из одного и того же материала. Кроме того, требуется устанавливать высоким гидравлическое давление снаружи герметичного контейнера, прикладываемое к водоотталкивающей пористой мембране (для проникания пресной воды) 27, а давление газа со стороны электродной камеры - низким, создавая тем самым перепад давления. Кроме того, чтобы поддерживать давление на стороне образования газа на определенном уровне или ниже, самым легким является обеспечить клапан 93 регулирования давления перед выпуском для отвода продуктового газа для того, чтобы регулировать его за счет давления газа, производимого газопроницаемыми электродными камерами 52 и 53. При использовании под поверхностью озера устройства 86 получения водорода, имеющего вышеописанную конструкцию, в которой в герметичном контейнере 87 в форме четырехугольной призмы содержится серная кислота с нормальностью от 1 до 5 или едкий натр с нормальностью от 1 до 10, когда снаружи для электролиза подается пресная вода 88 в количестве, эквивалентном производимым количествам водорода и кислорода, возможно непрерывно производить водород и кислород. В настоящем изобретении эти серная кислота и едкий натр упоминаются как катализаторы ионизации. В этом испытании герметичный контейнер 87 в форме четырехугольной призмы с шириной от 10 до 100 мм был расположен между положительной и отрицательной электродными камерами, и в качестве электродного материала отрицательной электродной камеры 52 использовалось волокно 81 из нержавеющей стали («Web» Naslon (зарегистрированный товарный знак) производства компании Nippon Seisen Inc.), как показано на ее разрезе, тогда как в положительном электроде содержалась углеродная ткань (углеродное волокно) 82. Измерения были выполнены для двух отдельных случаев, в которых серная кислота с нормальностью 2,5 и едкий натр с нормальностью 2,5 были запечатаны в герметичном контейнере 87 в форме четырехугольной призмы. Устройство 86 получения водорода было погружено в бассейн глубиной 3 м, и при откачивании отрицательной электродной камеры 52 и положительной электродной камеры 53 через клапаны 93 регулировки давления в каждой из них давление соответственно поддерживалось равным от 200 до 400 мм рт.ст. Таким образом была измерена эффективность производства водорода. Удельная электропроводность серной кислоты, помещаемой в водный раствор 79 электролита высокой концентрации, составляла 0,8 См/см. Для сравнения, удельная электропроводность едкого натра с нормальностью 2,5 составляла 0,3 См/см. При этом, когда к обоим электродам устройства 86 получения водорода было подано напряжение 1,5 В, потребность в энергии на 1 м3 водорода и 0,5 м3 кислорода для случая, в котором водный раствор электролита высокой концентрации представлял собой серную кислоту, составила 5,2 кВт⋅ч, тогда как потребность в энергии на 1 м3 водорода и 0,5 м3 кислорода составила 2,3 кВт⋅ч для случая едкого натра. [0100] Фиг. 32 представляет собой диаграмму, показывающую конструкцию простого устройства получения водорода, использующего давление водопроводной воды. Фиг. 11(B) показывает его принцип, в котором герметичный контейнер, выполненный из водоотталкивающей пористой мембраны, вставляется в герметичный контейнер большого размера, и в него подается водопроводная вода, сжимая воду до давления, большего или равного давлению водостойкости водоотталкивающей пористой мембраны, таким образом непрерывно производя водород. [0101] В показанном на Фиг. 32 простом устройстве 89 получения водорода, использующем давление водопроводной воды, после того, как герметичный контейнер 1 из водоотталкивающей пористой мембраны был вставлен в герметичный контейнер 29 большого размера, гидравлическое давление водопроводной воды 28 дополнительно повышается до давления, большего или равного давлению водостойкости водоотталкивающей пористой мембраны (для проникания пресной воды) 27, и в то же самое время пресная вода (водопроводная вода) 88 подается под давлением через водоотталкивающую пористую мембрану (для проникания пресной воды) 27 для поддержания примерно 3-нормального (примерно 8%-го) водного раствора серной кислоты. Таким образом, электролиз выполняется в положительной и отрицательной электродных камерах 3 и 4 (газопроницаемых электродных камерах 52 и 53) одновременно, и водород собирается из шланга 12 сбора продуктового газа отрицательной электродной камеры 3, тогда как кислород собирается из шланга 12 сбора продуктового газа положительной электродной камеры 4. При сборе газа, чтобы регулировать давление пресной воды (водопроводной воды) 88 и поддерживать давление на производящую газ сторону на определенном уровне или меньше, перед выпуском для отвода продуктового газа предусмотрен клапан 93 регулирования давления в качестве механизма управления для регулирования давления газа, производимого каждой из газопроницаемых электродных камер 52 и 53. В частности, серная кислота, имеющая концентрацию от 2 до 5, имеет самую высокую удельную электропроводность, и поэтому для поддержания этой концентрации дополнительно предусмотрено устройство сжатия, чтобы регулировать давление впрыска пресной воды в вентиле для балансировки между производимыми водородом и кислородом посредством вакуумирования и компрессора. [0102] Фиг. 33 показывает устройство для получения едкого натра и хлора непосредственно из водного раствора хлорида натрия. Фиг. 12(A) и (B) показывают его принцип, по которому давление, равное давлению водостойкости водоотталкивающих пористых мембран, составляющих герметичный контейнер, присоединенных к положительной и отрицательной электродным камерам соответственно, прикладывается к водному раствору хлорида натрия во время электролиза, и таким образом едкий натр производится в отрицательной электродной камере. Давление, равное давлению водостойкости, прикладывается к водоотталкивающим пористым мембранам через водный раствор хлорида натрия. [0103] Как показано на Фиг. 33, устройство 90 для получения едкого натра и хлора непосредственно из водного раствора хлорида натрия содержит в своем центре герметичный контейнер 1, определяемый двумя водоотталкивающими пористыми мембранами 11, помещенными отстоящими друг от друга. Отрицательная электродная камера 3, предусмотренная с одной стороны герметичного контейнера 1, составляет электродную камеру 40, заполняемую водой, в которой также предусмотрена отрицательная электродная пластина 36 из углерода или никеля. Положительная электродная камера 4, предусмотренная с другой стороны герметичного контейнера 1, составляет газопроницаемую электродную камеру 41, в которой предусмотрен пористый электродный материал. Затем герметичный контейнер 1 заполняется водным раствором 32 хлорида натрия, имеющим концентрацию 26 мас.%. Растворимость хлорида натрия практически не зависит от температуры атмосферы, но растворимость производимого едкого натра зависит от температуры атмосферы. Как показано на Фиг. 18, растворимость едкого натра при температуре 40°C составляет 56%, а при температуре 80°C она составляет 74%, а значит, растворимость увеличивается при повышении температуры; следовательно, для того чтобы производить едкий натр 31 высокой концентрации, желательно залить горячую воду в электродную камеру 40 или нагревать электродную камеру 40 нагревателем. В этом эксперименте, в качестве простого способа, горячая вода с температурой 100°C или меньше заливалась через впуск 34 подачи воды отрицательной электродной камеры 3. Одна возможная идея, разработанная здесь, заключается в том, чтобы повышать электролитическую эффективность путем предварительного добавления разбавленного едкого натра 31 к воде в отрицательной электродной камере 3 при начале электролиза. При этом водоотталкивающая пористая мембрана 11 сжимается под давлением, равным давлению водостойкости, с помощью оказывающего давление элемента 6 при поддержании концентрации водного раствора 32 хлорида натрия постоянной на уровне 26 мас.%, чтобы произвести едкий натр 31 в отрицательной электродной камере 40 и собирать сконцентрированный едкий натр из патрубка 35 сбора продукта отрицательного электрода, а газообразный водород - с помощью шланга 12 сбора продуктового газа, присоединенного к верхней части. Кроме того, газообразный хлор собирается с помощью шланга 12 сбора продуктового газа, присоединенного к верхней части положительной электродной камеры 4. Для того чтобы поддерживать давление на сторону получения газообразного хлора на определенном уровне или ниже, перед выпуском продуктового газа предусмотрен клапан 93 регулирования давления, который регулирует давление газа в камере 31 производства едкого натра так, чтобы оно не стало равным 1 атм или выше. Когда, на оба электрода было подано напряжение 4 В и плотность тока была установлена равной 20 A, затраты энергии на производство едкого натра составили 3 кВт⋅ч на один килограмм. [0104] Фиг. 34 показывает устройство для получения едкого натра и соляной кислоты непосредственно из водного раствора хлорида натрия. Фиг. 12(B) показывает его принцип, по которому давление, равное давлению водостойкости водоотталкивающих пористых мембран, составляющих герметичный контейнер, присоединенных к положительной и отрицательной электродным камерам соответственно, прикладывается к водному раствору хлорида натрия во время электролиза, и таким образом едкий натр производится в отрицательной электродной камере. Давление, равное давлению водостойкости, прикладывается к водоотталкивающим пористым мембранам через водный раствор хлорида натрия. [0105] Показанное на Фиг. 34 устройство 91 для получения едкого натра и хлора непосредственно из водного раствора хлорида натрия содержит в своем центре герметичный контейнер 1, определяемый двумя водоотталкивающими пористыми мембранами 11, помещенными отстоящими друг от друга. Отрицательная электродная камера 3, предусмотренная с одной стороны герметичного контейнера 1, составляет электродную камеру 40, заполняемую водой, в которой также предусмотрена отрицательная электродная пластина 36 из углерода или никеля. Положительная электродная камера 4, предусмотренная с другой стороны герметичного контейнера 1, составляет также электродную камеру 40, заполняемую водой, в которой предусмотрена положительная электродная пластина из углерода. Затем герметичный контейнер 1 заполняется водным раствором 32 хлорида натрия, имеющим концентрацию 26 мас.%. Затем подается вода через впуск 34 подачи воды положительной электродной камеры 4, и горячая вода с температурой 100°C или меньше заливается через впуск 34 подачи воды отрицательной электродной камеры 3. Кроме того, в начале электролиза разбавленный едкий натр 31 заранее добавляется к воде в отрицательной электродной камере 3, и соляная кислота заранее добавляется к воде в положительной электродной камере 4, повышая таким образом электролитическую эффективность. При этом водоотталкивающая пористая мембрана 11 сжимается под давлением, равным давлению водостойкости, с помощью оказывающего давление элемента 6 при поддержании концентрации водного раствора хлорида натрия постоянной на уровне 26 мас.%, чтобы произвести едкий натр 31 в отрицательной электродной камере 40 и собирать сконцентрированный едкий натр из патрубка 35 сбора продукта отрицательного электрода, а газообразный водород - с помощью шланга 12 сбора продуктового газа, присоединенного к верхней части. Кроме того, концентрированная соляная кислота собирается из патрубка сбора продукта положительного электрода (выпуска концентрированной кислоты) 42 положительной электродной камеры 4, а газообразный кислород собирается с помощью шланга 12 сбора продуктового газа, присоединенного к ее верхней части. Едкий натр 31 производится в электродной камере 40 отрицательной электродной камеры 3, а соляная кислота 33 производится в электродной камере 41. Оба они имеют высокую электропроводность, и поэтому водный раствор 32 хлорида натрия, который является водным раствором 14 электролита в герметичном контейнере 1, изолированном водоотталкивающей пористой мембраной 11, эффективно подвергается электролизу при повышении давления водного раствора электролита до давления водостойкости. [0106] Фиг. 35 показывает устройство для получения элемента-основного металла непосредственно из водного раствора хлорида основного металла. Фиг. 13(A) показывает его принцип, по которому выполненный из углерода пористый электрод приводится в контакт со стороной отрицательного электрода герметичного контейнера через изоляционную пленку, выполненную из водоотталкивающей пористой мембраны, а его задняя поверхность заполняется маслом, собирая таким образом основные металлы с меньшим, чем у масла, удельным весом (а именно Li, K, Na) из верхней части, а основные металлы с большим, чем у масла 23, удельным весом (а именно Mg, Ca, Ba, Sr, Al) - из самой нижней части. [0107] Показанное на Фиг. 35 устройство 92 для получения элемента-основного металла принимает в качестве хлорида, соответствующего элементу-основному металлу, который желательно производить в герметичном контейнере 1, определяемом водоотталкивающей пористой мембраной 11, один вид, выбираемый из водных растворов, например, NaCl, KCl, LiCl, MgCl2, CaCl2, BaCl2, SrCl2 и AlCl3. Что касается хлоридов основных металлов, их растворимость имеет тенденцию увеличиваться при увеличении температуры раствора, за исключением NaCl, у которого нет температурной зависимости, как показано на Фиг. 19. Например, если температура водного раствора 32 хлорида основного металла в герметичном контейнере 1 повышается с помощью внутреннего нагревателя до 60°C, растворимости NaCl, KCl, LiCl, MgCl2, CaCl2, BaCl2, SrCl2 и AlCl3 будут составлять 27%, 31%, 50%, 38%, 58%, 32%, 47% и 32% соответственно. Из этих результатов можно понять, что давление должно быть поднято до давления водостойкости в то время, как температура водного раствора 32 хлорида основного металла повышается до 25-80°C, чтобы увеличить концентрацию до растворимости насыщения с тем, чтобы начать электролиз. Отрицательная электродная камера 3 устройства 92 для получения элемента-основного металла, показанного на Фиг. 35, составляет электродную камеру 16, заполненную маслом, в которой сетчатый отрицательный электрод 43 из углеродного волокна используется в качестве электрода, а газойль, удельный вес которого равен 0,8, используется в качестве масла 23. С другой стороны, положительная электродная камера 4 составляет газопроницаемую электродную камеру 41, в которой используется положительный электрод 37 из углеродного волокна, и газообразный хлор собирается из положительной электродной камеры 4 с помощью шланга 12 сбора продуктового газа. Когда LiCl используется в качестве водного раствора 32 хлорида основного металла, примерно 50% LiCl подвергается электролизу при 80°C, потому что его растворимость составляет 53% при 80°C, температура плавления Li составляет 179°C, а его удельный вес составляет 0,54 (см. Фиг. 16), и таким образом металлический Li всплывает в верхнюю часть газойля 23 в отрицательной электродной камере 3 и собирается через патрубок 35 сбора продукта отрицательного электрода, предусмотренный в верхней части отрицательной электродной камеры 3. С другой стороны, газообразный хлор собирается с помощью шланга 12 сбора продуктового газа в верхней части положительной электродной камеры. Для того, чтобы поддерживать давление на сторону производства газообразного хлора на определенном уровне или ниже, перед патрубком отвода продуктового газа предусмотрен клапан 93 регулирования давления. При предварительном испытании водный раствор хлорида натрия, сконцентрированный до 28%, был подвергнут обработке с одновременной подачей напряжения 4-5 В между положительным и отрицательным электродами при 25°C и плотности тока 10 A в течение 1 часа, и таким образом 8 г металлического натрия было осаждено в газойле, заполняющем электродную камеру 16. [0108] Фиг. 36 показывает устройство для получения элемента-основного металла и соляной кислоты непосредственно из водного раствора хлорида основного металла. Фиг. 13(A) и (B) показывают его принцип, по которому выполненный из углерода пористый электрод приводится в контакт со стороной отрицательного электрода герметичного контейнера через изоляционную пленку из водоотталкивающей пористой мембраны, а его задняя поверхность заполнена маслом, и таким образом основный металл, удельный вес которого меньше, чем у масла (а именно Li, K, Na), собирается в верхней части, тогда как основный металл, удельный вес которого больше, чем у масла 23 (а именно Mg, Ca, Ba, Sr, Al) собирается в самой нижней части. Способ получения продукта отрицательного электрода аналогичен описанному выше. С другой стороны, соляная кислота получается на положительном электроде следующим образом. Заполненная водой электродная камера 40 используется в качестве положительной электродной камеры 4 устройства 95 по Фиг. 36 для непосредственного получения элемента-основного металла и соляной кислоты, и разбавленный водный раствор соляной кислоты добавляется заранее к воде, подаваемой через впуск 34 подачи воды, чтобы вызвать реакцию между анионом и водой. Затем ионная реакция (2Cl-+2H2O→2HCl+O2) вызывается электролизом между сетчатой отрицательной электродной пластиной 43 и положительной электродной пластиной 38 через водоотталкивающую пористую мембрану 11. Таким образом, это устройство имеет такую конструкцию, что производимая в нем кислота (соляная кислота) 33 собирается через патрубок 42 отвода сильной кислоты (соляной кислоты), тогда как кислород собирается с помощью трубы 12 сбора продуктового газа. [0109] Фиг. 37 представляет собой диаграмму, показывающую конструкцию устройства для получения основного металла, которое использует виртуальный отрицательный электрод, из водного раствора хлорида основного металла. Фиг. 14(B) показывает его принцип, по которому граница раздела между поверхностью масла и водным раствором соли основного металла элемента Группы 1 или 2 Периодической таблицы используется в качестве поверхности виртуального отрицательного электрода, и водный раствор соли основного металла подвергается электролизу, чтобы собрать продукт отрицательного электрода в слое масла. Легко понять, что граница раздела между маслом и водным раствором электролита используется в качестве виртуального электрода. Однако, если этот виртуальный электрод не является отрицательным электродом, продукт отрицательного электрода не будет получен. Здесь то, как использовать виртуальный электрод в качестве отрицательного электрода, будет описано на основе устройства получения основного металла, которое использует эквивалентную электрическую «схему Мурахары» по Фиг. 37(B) и виртуальный отрицательный электрод по Фиг. 37(A). Таким образом, переключатель (S) эквивалентной электрической схемы по Фиг. 37(B) соответствует водоотталкивающей пористой мембране 11, которая устанавливается в положение ВКЛ/ВЫКЛ посредством водного раствора 14 электролита при давлении водостойкости с помощью прикладывающего давление элемента 6, а водный раствор 14 электролита обозначается как (R). Масло 23 в заполненной маслом электродной камере 16 обозначается как (C2), напряжение как (E), а установленный снаружи конденсатор большой емкости обозначается как (C1). Если давление, равное давлению водостойкости, прикладывается после того, как сначала к конденсатору большой емкости (C1) приложено напряжение (E), переключатели (S) обеих электродных камер включены. Поверхность 19 виртуального электрода функционирует как отрицательный электрод. При использовании заряда, запасенного в конденсаторе C1, через последовательные конденсаторы C1 и C2, потенциал прикладывается к сопротивлению R, и таким образом выполняется электролиз. Затем на стороне 19 виртуального отрицательного электрода основные металлы, удельные веса которых меньше, чем у масла (а именно Li, K, Na), собираются из верхней части, а те основные металлы, которые имеют большие удельные веса, чем у масла 23 (а именно Mg, Ca, Ba, Sr, Al), собираются из самой нижней части. В то же самое время газообразный хлор собирается с помощью шланга 12 сбора продуктового газа в верхней части газопроницаемой электродной камеры 41 положительной электродной камеры 4. Таким образом, устройство получения основного металла использует виртуальный отрицательный электрод, содержащий клапан 93 регулирования давления перед патрубком отвода продуктового газа для того, чтобы поддерживать давление на сторону, производящую газообразный хлор, на определенном уровне или ниже. [0110] Фиг. 38 показывает устройство получения гидрида основного металла. Обычно гидрид натрия производится путем объединения с водородом при высокой температуре металлического натрия, производимого электролизом едкого натра в солевом расплаве. Затраты при производстве металлического натрия высоки. Как описано в связи с Фиг. 15, температура плавления едкого натра является весьма низкой и равна 318°C. Следовательно, когда контейнер, содержащий едкий натр, нагревается до температуры 318°C или выше, получается ионизированный солевой расплав. Как показано на Фиг. 38, иллюстрирующей устройство 97 получения гидрида металла, если катион (H+) водорода и анион (H-) 50 водорода реагируют в солевом расплаве едкого натра (Na++ОН-), происходит следующая реакция: Na++OH-+H-+H+ → NaH+H2O. Тогда, чтобы получить анион (H-) 50 водорода в солевом расплаве 46 едкого натра, газообразный водород подается под давлением к пористой углеродной пленке 44 отрицательного электрода/изоляции, имеющей конструкцию газопроницаемой электродной камеры 41, через нагнетательный патрубок 47. Кроме того, солевой расплав 46 едкого натра помещается между отрицательным электродом 44, образованным из пористой углеродной пленки 44 отрицательного электрода-изоляции, и положительной электродной пластиной 38. При этом, если потенциал для получения аниона 50 водорода прикладывается к обоим электродам, он реагирует с ионом натрия (Na+) в солевом расплаве едкого натра, производя гидрид натрия (NaH) 49 только с помощью ионной реакции, а не тепловой реакции. Кроме того, удельный вес гидрида натрия (NaH) 49 меньше, чем у солевого расплава 46 едкого натра, а температура его плавления является значительно более высокой, чем у едкого натра 46; поэтому продукт всплывает как твердое вещество, и устройство позволяет его легко собирать. [0111] Фиг. 39 показывает устройство для запасания водного раствора электролита в герметичном контейнере оболочечного типа. Герметичный контейнер 55 оболочечного типа производится путем укладывания друг на друга двух листов водоотталкивающего пористого материала 11 и их термосварки с четырех сторон около 350°C. Герметичный контейнер 55 оболочечного типа имеет множество разнообразных применений в качестве контейнера для хранения водного раствора электролита батареи. Здесь устройство 98 удержания резервуара водного раствора электролита запасает водный раствор 14 или 102 электролита в герметичном контейнере 55 оболочечного типа. Как показано на Фиг. 39(A) и (B), обе поверхности герметичного контейнера 55 оболочечного типа содержат водоотталкивающую пористую фторкаучуковую пленку 100 и водоотталкивающую пористую фторкаучуковую пленку 101 соответственно. Давление водостойкости каждой из водоотталкивающих пористых фторкаучуковых пленок 100 и 101 меняется в зависимости от концентрации соли в водном растворе электролита, как показано на Фиг. 28. Здесь, как показано на Фиг. 39(B), если гидравлическое давление резервного водного раствора электролита 102, сжимаемого с помощью прикладывающего давление элемента 6, обозначается как (WP102), гидравлическое давление водного раствора электролита в герметичном контейнере 55 оболочечного типа обозначается как (WP55), давление водостойкости водоотталкивающей пористой фторкаучуковой пленки 100 на стороне водного раствора электролита 102 обозначается как (WP100), давление водостойкости водоотталкивающей пористой фторкаучуковой пленки 101 на стороне всасывающего отверстия 99 обозначается как (WP101), и давление воздуха во всасывающей части 99 обозначается как (P99), условие герметизации водного раствора электролита 102 внутри герметичного контейнера 55 оболочечного типа путем вынуждения его проходить сквозь поры водоотталкивающей пористой фторкаучуковой пленки 100 выглядит как WP102≥WP55+WP100, тогда как условие отрицательного давления для всасывания во всасывающем отверстии 99 для того, чтобы запасти водный раствор электролита в герметичном контейнере 55 оболочечного типа, выглядит как WP101≥P99≥-WP101. При этом, если водоотталкивающие пористые фторкаучуковые пленки 100 и 101, используемые для этих двух поверхностей, выполнены из одного и того же материала, это выражается как WP100=WP101. Таким образом, устройство 98 резервуара водного раствора электролита, проиллюстрированное на Фиг. 39(B), сначала начинает сжатие водного раствора электролита 102 с помощью прикладывающего давление элемента 6, поддерживая при этом отрицательное давление не меньшим, чем давление водостойкости (-WP101) водоотталкивающей пористой фторкаучуковой пленки 101 на стороне всасывающего отверстия 99, и одновременно изменяет давление во всасывающем отверстии 99 до величины (+WP101) для того, чтобы герметизировать водный раствор электролита 102 в герметичном контейнере 55 оболочечного типа. [0112] Фиг. 40 показывает вторичную батарею с водным раствором электролита сжимаемого типа. Фиг. 40(A) показывает конструкцию вторичной батареи 103 с электролитом сжимаемого типа, в которой водный раствор 14 электролита герметично запечатывается в герметичном контейнере 55 оболочечного типа, который использует водоотталкивающую пористую фторкаучуковую пленку 11 в качестве изоляционной пленки в отношении электрода, которая дополнительно вставляется между отрицательной электродной камерой 52 и положительной электродной камерой 53. При этом, когда груз 104 помещается для того, чтобы нагрузить устройство, будет появляться потенциал (V), как показано на Фиг. 40(A) и (B). Если груз 104 будет удален, то потенциал (V) станет равным 0 В. В этом варианте осуществления алюминиевая пластина использовалась в качестве отрицательной электродной пластины 36 отрицательной электродной камеры 52, и пленка 63 хлорида металла, такого как AlCl3, ZnCl2, MgCl2 и т.п., использовалась в качестве положительной электродной пластины 38 положительной электродной камеры 53. Сначала, в качестве предварительного испытания первичной батареи, обе поверхности герметичного контейнера 55 оболочечного типа, содержащего водный раствор хлорида натрия с концентрацией 10%, были помещены между отрицательным электродом, выполненным из магниевой пластины, и положительным электродом, выполненным из цинковой пластины, на поверхности которой сформирована хлоридная пленка, и если на водоотталкивающую пористую фторкаучуковую пленку 11 с диаметром пор 33 мкм оказывается давление грузом 104, эквивалентное давлению водостойкости и равное 330 мм рт.ст., показанное на Фиг. 28, получается электродвижущая сила, равная 3,5 В. Когда груз 104 удаляется, значение напряжения становится равным 0 В. Затем, в качестве предварительного испытания вторичной батареи, был подготовлен герметичный контейнер 55 оболочечного типа, содержащий водный раствор хлорида алюминия с концентрацией 25%, и обе его поверхности были помещены между алюминиевыми электродными пластинами. Здесь при нагрузке грузом 104, эквивалентной давлению водостойкости водоотталкивающей пористой фторкаучуковой пленки 11, батарея заряжалась постоянным током 10 A в течение 60 минут. Затем груз 104 был удален для того, чтобы завершить зарядку. Концентрация водного раствора хлорида алюминия в герметичном контейнере 55 оболочечного типа была равна 23%, что означает теоретическую зарядку до 10%. Затем батарея была оставлена без груза 104 на один месяц, а затем, когда вторичная батарея 103 с электролитом сжимаемого типа снова была сжата сверху грузом 104, была получена электродвижущая сила 3,5 В. Когда груз 104 был удален, значение напряжения стало равным 0 В. При повторении сжатия и снятия груза 104 не было отмечено никакого изменения в концентрации водного раствора хлорида алюминия, содержащегося в герметичном контейнере 55 оболочечного типа. Таким образом, было доказано, что саморазряд внутри батареи не происходит. [0113] Фиг. 41 показывает вторичную батарею пакетного типа с едким натром. Как показано на Фиг. 21, водный раствор едкого натра используется в качестве электролита, воздух используется в качестве положительного электрода, углеродное волокно используется в качестве отрицательного электрода, и при зарядке в порах углерода осаждается натрий. Фиг. 41(A) показывает поперечное сечение вторичной батареи 106 пакетного типа с едким натром, в которой герметичный контейнер 55 оболочечного типа располагается между отрицательной электродной камерой 52 и положительной электродной камерой 53. Герметичный контейнер 55 оболочечного типа представляет собой мешок, обе поверхности которого сделаны из водоотталкивающего пористого фторкаучука 11. Водный раствор 14 электролита, содержащийся внутри него, представляет собой едкий натр с нормальностью от 1 до 8, и отрицательные электродные камеры 52 и 57 представляют собой камеры, имеющие такую конструкцию, что натриевые электродные пластины или выполненные из углерода пористые электродные пластины, в которых Na адсорбируется в порах внутри или на поверхности, и отрицательные электроды заключены в полимерную пленку 61 или масло 22 абсорбируется внутри отрицательных электродов. С другой стороны, в кислородном электроде положительной электродной камеры 53 воздух адсорбируется на выполненной из углерода пористой электродной пластине (из активированного угля) 58, и между водоотталкивающей пористой мембраной 11 и выполненной из углерода пористой пластиной предусмотрен вспомогательный положительный электрод 56 для зарядки (сетчатый электрод) для того, чтобы избежать тепловыделения из выполненной из углерода пористой электродной пластины (из активированного угля) 58. Для мощности предусмотрена коллекторная электродная пластина 64 на задней поверхности выполненной из углерода пористой электродной пластины (из активированного угля) 58. Фиг. 41(B) представляет собой вид, схематично показывающий вторичную батарею, в которой вторичная батарея 106 пакетного типа с едким натром заключена в полимерную пленку 61 для ее изоляции от внешней среды и заряжается в то время, как водный раствор 14 электролита в герметичном контейнере 55 оболочечного типа сжимается с помощью груза 104. В то время, когда заряд завершен, давление на водный раствор 14 электролита снимается для поддержания состояния хранения заряда, а при разрядке водный раствор 14 электролита снова сжимается для того, чтобы начать разряд. Как показано на Фиг. 18, растворимость водного раствора едкого натра в воде является высокой и составляет 50% при комнатной температуре. Сначала 50%-ый водный раствор едкого натра запечатывается внутри герметичного контейнера 55 оболочечного типа из водоотталкивающей пористой фторкаучуковой пленки 11, и отрицательные электродные камеры 52 и 57 заключаются в полимерную пленку 61. Отрицательная электродная камера 57 выполнена из пористого углеродного электрода, пропитанного маслом с изоляцией от внешнего воздуха, тогда как положительный электрод является выполненной из углерода пористой электродной пластиной 58 из активированного угля, снабженной впуском 105 воздуха, через которое входит и выходит воздух, который заключен в полимерную пленку 61. Положительная электродная камера 53 содержит сетчатый вспомогательный положительный электрод 56 для зарядки между водоотталкивающей пористой мембраной 11 и выполненной из углерода пористой электродной пластиной 58 из активированного угля. Изолированная от внешнего воздуха отрицательная электродная камера 57 и положительная электродная камера 53 вставляются в герметичный контейнер 55 оболочечного типа, выполненный из водоотталкивающей пористой фторкаучуковой пленки 11. Здесь, в качестве предварительного испытания, сначала щелочная батарея 106 сжимается сверху с помощью груза 104, эквивалентного давлению водостойкости водоотталкивающей пористой фторкаучуковой пленки 11, и заряжается током 10 A в течение 60 минут в этом состоянии между вспомогательным положительным электродом 56 для зарядки и выполненной из углерода пористой электродной пластиной в изолированной от внешнего воздуха отрицательной электродной камере 57. После этого груз 104 удалялся и заряд завершался. В этот момент времени концентрация водного раствора едкого натра в герметичном контейнере 55 оболочечного типа составляла 43%, что означает теоретическую зарядку до 10%. При этом, когда между выполненной из углерода пористой электродной пластиной в изолированной от внешнего воздуха отрицательной электродной камере 57 и коллекторными электродными пластинами 64, выполненными из медных пластин, была подключена электрическая нагрузка, а груз 104 снова был помещен на батарею, начался разряд, и его электродвижущая сила была равна 3 В. Когда эта батарея была оставлена без груза 104 на один месяц, а затем снова была сжата с помощью груза 104, она показала электродвижущую силу 3 В. Когда груз 104 был удален, значение напряжения стало равным 0 В. При повторении сжатия и снятия груза 104 не было отмечено никакого изменения в концентрации водного раствора едкого натра, содержащегося внутри герметичного контейнера 55 оболочечного типа. Таким образом, было доказано, что саморазряд внутри батареи не происходит. [0114] Фиг. 42 показывает конструкцию окислительно-восстановительного конденсатора. Фиг. 27 показывает принцип его работы, в котором сегнетоэлектрические конденсаторы, в которых очень тонкая оксидная пленка сформирована на поверхности металлической пластины, располагаются как на положительном, так и на отрицательном электродах, и положительный электрод и отрицательный электрод конструктивно являются одинаковыми. Окислительно-восстановительный конденсатор 107 может быть описан в терминах электрической схемы следующим образом. Эквивалентная электрическая схема C1, показанная на Фиг. 42(B), является отрицательной электродной камерой 52, и, как показано на Фиг. 42(A) в ее поперечном сечении, очень тонкая оксидная пленка 109 для окислительно-восстановительного конденсатора формируется на поверхности металлической пластины 108 для окислительно-восстановительного конденсатора с тем, чтобы приготовить сегнетоэлектрический конденсатор. Следует отметить, что положительная электродная камера 53 и отрицательная электродная камера 52 также являются одинаковыми по материалу и конструкции. Герметичный контейнер 55 оболочечного типа располагается между парой положительной и отрицательной электродных камер 52 и 53 через водоотталкивающую пористую мембрану 11. Эквивалентными электрическими схемами водоотталкивающей пористой мембраны 11 являются конденсатор с низкой диэлектрической постоянной (C2) и переключатель (S), показанные на Фиг. 42(B). В частности, в настоящем изобретении внутренность герметичного контейнера 55 оболочечного типа заполняется пористым проводящим материалом 78 из углеродного волокна, металлического волокна и т.п., и поры пропитываются водным раствором электролита (разбавленной серной кислотой) 79 для электрохимических конденсаторов. При этом, если гидравлическое давление, равное давлению водостойкости, прикладывается с помощью прикладывающего давление элемента 6, разбавленная серная кислота 79 входит в поры водоотталкивающей пористой мембраны 11, включая переключатель (S) в электрической схеме. Положительная электродная камера и отрицательная электродная камера замыкаются накоротко пористым проводящим материалом 78, выполненным из углеродного волокна, металлического волокна и т.п., находящимся в герметичном контейнере 55 оболочечного типа. Таким образом, два конденсатора с высокой диэлектрической постоянной (C1) заряжаются и разряжаются последовательно. С другой стороны, если давление, оказываемое на водный раствор 14 электролита, снимается, два конденсатора (C2) с низкой диэлектрической постоянной и два конденсатора (C1) с высокой диэлектрической постоянной соединяются последовательно для хранения заряда. Когда водный раствор 14 электролита не сжимается, водный раствор 14 электролита не входит в поры водоотталкивающей пористой мембраны 11, и поэтому он функционирует как конденсатор с низкой диэлектрической постоянной (C2). Если на водный раствор 14 электролита оказывается давление, водный раствор электролита входит в поры водоотталкивающей пористой мембраны 11, включая переключатель (S) в терминах электрической схемы. Таким образом, положительная электродная камера и отрицательная электродная камера замыкаются накоротко через герметичный контейнер 55 (оболочечного типа), выполненный из водоотталкивающей пористой мембраны. Таким образом, два конденсатора с высокой диэлектрической постоянной (C1) заряжаются и разряжаются последовательно. Когда давление, оказываемое на водный раствор 14 электролита, снимается, два конденсатора (C2) с низкой диэлектрической постоянной и два конденсатора (C1) с высокой диэлектрической постоянной соединяются последовательно для хранения заряда. В устройстве окислительно-восстановительного конденсатора используется алюминий (Al) для металлической пластины 108 окислительно-восстановительного конденсатора и оксид алюминия (Al2O3) для пленки 109 оксида металла окислительно-восстановительного конденсатора. [0115] Фиг. 43 показывает способ выбора и сбора элементов-основных металлов, таких как Na, K и Li Группы 1, и Mg, Ca, Sr и Ba Группы 2, из смешанных водных солевых растворов, таких как морская вода, вода соленого озера, вода горячего источника и промышленные сточные воды. Следует отметить, что эффективность сбора увеличивается при увеличении концентрации соли. По этой причине первая выполняемая операция состоит в том, что сточная жидкость (концентрированная соленая вода) должна быть подвергнута электролизу после ее дегидратации с помощью тепла, или мембранного способа обратного осмоса, или после получения водорода путем электролиза морской воды. Однако, как показано на Фиг. 19, что касается хлоридов основных металлов, растворимость значительно отличается от одного элемента-металла к другому, и растворимость имеет тенденцию повышаться при повышении температуры раствора. Например, при 80°C значения растворимости ZnCl2, CaCl2, LiCl, KCl и NaCl составляют 84,4%, 60%, 53%, 34% и 28% соответственно. Желательно, чтобы элемент, подвергаемый осаждению, имел более высокую растворимость; однако на практике необходимо начинать с элемента с низким напряжением разложения растворенного вещества. Тогда для тех элементов, которые имеют потенциал 1,4 В или выше, что является электролитическим напряжением воды, подаваемое напряжение увеличивается в следующем порядке: MgSO4: 1,62 В, CaSO4: 1,904 В, MgCl2: 3,952 В, NaCl: 4,11 В и CaCl2: 4,23 В, и сточная жидкость после осаждения каждого соответствующего элемента передается к следующему устройству осаждения. В соответствии с этим способом каждый одиночный элемент отбирается и собирается из множества солей элементов-основных металлов. [0116] Фиг. 44 представляет собой схематичную диаграмму топливного цикла едкого натра. В соответствии с настоящим изобретением этот топливный цикл осуществляется на море. Что касается энергии и материалов, море является богатым хранилищем ресурсов. Как указывает автор настоящего изобретения в непатентных документах 3 и 4, 70,8% всей Земли занято океаном, 3,5% морской воды составляет соль, и 2,18 г NaCl содержится в каждом литре морской воды. Натрий (Na) рассматривается как источник энергии следующего поколения взамен ископаемого топлива и ядерного топлива. Водородное топливо, полученное с помощью натрия, является источником экологически чистой энергии, который не выделяет CO2 или радиоактивности. Кроме того, нет никакого риска его истощения, и его поставки не зависят от гегемонизма или политических условий в ресурсодобывающих странах, что может привести к мирному миру без войн за ресурсы. Более желательно, чтобы промышленность находилась рядом с местами нахождения сырья, а не в местах потребления. Кроме того, желательно, чтобы мощности по переработке сырья находились рядом с местами добычи сырья. Основываясь на этом, плавучая фабрика 110 размещается плавающей в океане для использования морской воды, находящейся прямо под ней, в качестве сырья. В качестве электроэнергии для обработки могут использоваться естественные источники энергии, такие как энергия морского ветра и солнечная энергия, или вырабатываемая за счет плавучести-гравитации энергия, которая может быть получена с использованием работающего за счет плавучести-гравитации энергогенератора 113, совершающего возвратно-поступательное движение между поверхностью моря и морским дном, создавая примерно в 1000 раз больше энергии, чем сила ветра, раскрытого автором настоящей заявки в патентных документах 19 и 20. Таким образом, с использованием устройства 86 получения водорода, показанного на Фиг. 31, водород производится за счет использования гидравлического давления под морской поверхностью. Затем с использованием устройств 90 или 91 получения едкого натра, показанных на Фиг. 33 или Фиг. 34, производятся едкий натр и соляная кислота или хлор. Помимо выработки электроэнергии из естественных источников, на плавучей фабрике 111 могут использоваться избыточная мощность или ночная мощность, например, прибрежной теплоэлектростанции и атомной электростанции для того, чтобы производить водород и едкий натр. При этом температура плавления едкого натра является достаточно низкой и составляет 318°C, как показано на Фиг. 16. Таким образом, едкий натр, расплавленный при нагреве нагревателем в устройстве 97 получения гидрида основного металла, снабжается положительным и отрицательным электродами, и обратное напряжение прикладывается к газообразному водороду для обеспечения реакции произведенных таким образом анионов водорода и катионов натрия с получением гидрида натрия 49. Кроме того, потребление энергии на производство гидрида натрия путем ионной реакции низко, и кроме того, как показано на Фиг. 16, удельный вес гидрида натрия составляет 0,92, ниже, чем удельный вес солевого расплава едкого натра в 2,13, а температура плавления гидрида натрия составляет 800°C, что выше температуры плавления едкого натра, составляющей 318°C. Следовательно, гидрид натрия может быть легко собран на поверхности как верхний остаток, который может быть легко подвергнут классификации под действием силы тяжести. Если произведенный здесь гидрид натрия 49 будет помещен в устройство 112 получения водорода и в него будет залита вода, будет получено вдвое больше водорода по сравнению с реакцией гидролиза металлического натрия. Полученный таким образом водород может подаваться на теплоэлектростанцию или водородную станцию через трубопровод. С другой стороны, едкий натр 31, который является отходом (побочным продуктом) устройства 112 получения водорода, используется в качестве сырья для устройства 97 получения гидрида основного металла, и таким образом снова производится гидрид натрия 49. Таким образом реализуется топливный цикл едкого натра, гораздо более безопасный, чем цикл ядерного топлива. Часть едкого натра, полученного в устройствах 90 и 91 получения едкого натра, используется для батареи пакетного типа с едким натром, показанной на Фиг. 41, в качестве батареи транспортного средства или аккумуляторной батареи для хранения электроэнергии. Кроме того, если гидрид натрия погружен в масло, и компактная версия устройства 112 получения водорода устанавливается на транспортном средстве, может быть создан работающий на водородном топливе автомобиль без водородных баллонов в самом транспортном средстве. Таким образом может быть реализована система с топливным циклом едкого натра для создания водородного общества, которое не зависело бы от ископаемого топлива. [0117] Фиг. 45 представляет собой схематическую диаграмму устройства управления реакцией гидролиза. Выполненный из водоотталкивающего пористого фторкаучука герметичный мешок 115, вмещающий в себя химикат 116, вставляется в устройство 114 управления реакцией гидролиза и снаружи в выполненный из водоотталкивающего пористого фторкаучука герметичный мешок 115 вводится вода 88. Таким образом, это устройство может использоваться для получения газа путем гидролиза, выработки или поглощения тепла, или реакций растворения. В настоящем изобретении самое замечательное явление может быть получено с Na, K и Li Группы 1, при котором водород получается, если химикат 116, такой как один из них, помещают в выполненный из водоотталкивающего пористого фторкаучука герметичный мешок 115 и воду вынуждают проникать в него путем создания перепада давления, большего или равного давлению водостойкости. Однако фторкаучук корродирует и разлагается при контакте с этими элементами Группы 1. Для того чтобы предотвратить это и иметь безопасную реакцию гидролиза, масло, такое как газойль, должно быть помещено вместе с элементом Группы 1 в выполненном из водоотталкивающего пористого фторкаучука герметичном мешке 115, поскольку фторкаучук обладает липофильными свойствами в воде и не входит в прямой контакт с Na, K, Li или т.п., находящимся внутри выполненного из водоотталкивающего пористого фторкаучука герметичного мешка 115, позволяя избежать его разложения. Например, если в него будут помещены бикарбонат натрия в качестве химиката 116 и лимонная кислота (1:1), получится двуокись углерода (CO2). При этом ее можно использовать в качестве источника газа для обеспечения плавучести работающего за счет плавучести-гравитации энергогенератора 113 (Фиг. 44), раскрытого автором настоящей заявки в патентных документах 19 и 20, для случая, когда глубина воды составляет 1300 м или мельче. Если в качестве химикатов 116 используются оксид кальция (CaO) и алюминий (Al), может быть получена следующая реакция: 2CaO+2Al+4H2O→2Ca(OH)2+2Al+2H2O+63,3 кДж/моль→2CaO+Al2O3+H2+390,1 кДж/моль, с одновременным получением высокой температуры и водорода. При этом масса этих химикатов используется в качестве груза, когда погружаемое транспортное средство опускается на дно глубокого океана, и морская вода на дне глубокого океана используется в качестве источника воды с получением водорода. Кроме того, одновременно вырабатываемое при этом тепло может использоваться для того, чтобы увеличить объем газа, который может быть использован в качестве газа, обеспечивающего плавучесть погружаемого транспортного средства. С помощью этого тепла сухой лед сублимируется на дне глубокого океана, на глубине глубже чем 1300 м, чтобы также использоваться в качестве средства обеспечения плавучести. Если в качестве химиката 116 в него помещается мочевина ((NH2)2CO), происходит реакция 2(NH2)CO+H2O→2NH3+CO2, дающая аммиак и двуокись углерода. Если в качестве химиката 116 используется карбид (CaC2), то происходит реакция: CaC2+2H2O→Ca(OH)2+C2H, дающая газообразный ацетилен. В качестве химиката 116 в него может быть помещен неэлектролит, такой как сахар, приправа, питательное вещество или лекарство, с тем, чтобы вызвать реакцию растворения с водой 88. [0118] Фиг. 46 представляет собой схематическую диаграмму устройства подачи питательного вещества или влаги в гидропонной системе. Устройство 121 подачи питательного вещества представляет собой устройство, которое периодически подает воду и питательное вещество под управлением гидравлического давления для растительности 119, такой как овощи и плодовые деревья на овощных фермах или в плодовых хозяйствах. С этим устройством посредством трубы (шланга) 118 подачи раствора соединяется химикатраспыляющий резервуар (мешок или трубка из водоотталкивающего пористого полимера) 120. Таким образом, вспомогательное питательное вещество 121, такое как удобрение, или влага подается в желаемое место непрерывно или периодически по мере необходимости с помощью прикладывающего давление элемента 6 из диспетчерской 122 плодового хозяйства для того, чтобы подавать влагу и питательное вещество (удобрение) эффективно к корневой системе растения, позволяя тем самым предотвратить гниение корней, вызванное чрезмерным поливом или избыточным питанием. [0119] Фиг. 47 представляет собой диаграмму, схематично показывающую медицинское устройство типа эндоскопа. Как показано на Фиг. 47(A), катетер 123 вставляется в орган, и внутренность вставленной в орган капсулы откачивается (до давления ниже атмосферного) или сжимается (до давления выше атмосферного) с помощью прикладывающего давление элемента 6 для того, чтобы доставить лекарство или водный питательный раствор в интересующее место или нагреть интересующее место. Для доставки лекарства или питательного вещества в интересующее место питательное вещество или лекарство 116 переносится в выполненный из водоотталкивающего пористого фторкаучука герметичный мешок 115 и раствор сжимается (до давления выше атмосферного) через катетер 123 путем приложения давления, большего или равного давлению водостойкости (дифференциальное давление) мульти-водоотталкивающей пористой пленки с помощью прикладывающего давление элемента 6, как показано на Фиг. 47(B). Так питательное вещество или лекарство могут быть эффективно доставлены в требуемое место. Таким образом, питательное вещество или лекарство может быть введено с высокой эффективностью в соответствии с биологическим ритмом субъекта без введения все время, как при существующем внутривенном вливании или зондовом кормлении. При лечении интересующего места лекарство может быть введено только в целевое интересующее место. Фиг. 47(C) представляет собой диаграмму, схематично показывающую капсулу 125 термотерапии для уничтожения раковых клеток. Раковые клетки самые слабые при температуре 39-43°C, что является сравнительно низкой температурой, подобной температуре ванны. Однако трудно нагревать непосредственно интересующее место при постоянной температуре в течение долгого времени. Здесь было виртуально проведено предварительное испытание. Сначала выполненный из водоотталкивающего пористого фторкаучука герметичный мешок 115, содержащий гидролитическое экзотермическое средство 124, вставили в капсулу 125, содержащую воду 88, и внутренность выполненного из водоотталкивающего пористого фторкаучука герметичного мешка 115 отсасывали (отрицательное давление) с создаваемым катетером 123 (затенен) перепадом давления, эквивалентным давлению водостойкости. Таким образом, вода 88 внутри капсулы 125 проникала в выполненный из водоотталкивающего пористого фторкаучука герметичный мешок 115 в количестве, эквивалентном отрицательному давлению, и вода реагировала с гидролитическим экзотермическим средством 124 с выделением тепла. Вода 88 внутри капсулы 126 нагревалась выделившимся таким образом теплом. Следовательно, при реальном клиническом тестировании интересующий часть тела, в которой живут раковые клетки, может быть нагрета напрямую. Отрицательное давление повторялось импульсами, и поэтому вода подавалась к гидролитическому экзотермическому средству 124 с помощью отрицательного давления. Таким образом, гидролитическое экзотермическое средство 124 и вода 88 реагировали друг с другом, поддерживая температуру 39-43°C в течение примерно 30 минут. Теплотворная способность гидролитического экзотермического средства 124, если используется CaO, составляет 65 кДж/моль; 18,1 кДж/моль для P2O3+ZnCl2+Ba(ОН)2; 12,6 кДж/моль для NaOH; 39,5 кДж/моль для KOH; 37 кДж/моль для серной кислоты; 97,4 кДж/моль для CaCl2; 126 кДж/моль для Al2O3; 27,5 кДж/моль для CuSO4; и 390,1 кДж/моль для CaO+Al. Таким образом, с учетом величины инъекции в капсулу, достигаемой температуры, продолжительности времени и т.п., можно полагать, что при клиническом применении CaO будет подходящим в качестве экзотермического средства. ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ [0120] Извлекаемые ресурсы нефти и угля ограничены, и эти материалы выделяют двуокись углерода. Ядерное топливо испускает радиоактивность. В отличие от этого, водород является неограниченным по извлекаемым ресурсам и не выделяет двуокиси углерода или радиации. Таким образом, водород представляет собой чистое топливо, также безвредное для окружающей среды. Сам водород является легким; однако его контейнеры (баллоны) для его хранения или сплавы, которые поглощают водород, слишком тяжелы для переноски. В качестве решения может быть использован водород из ресурса водорода (то есть натрия). Натрий повсеместно доступен и широко распространен в виде морской воды или каменной соли, и недостатка в нем не предвидится. Однако, чтобы собрать его, необходимо удалить воду. Традиционно не существовало никакого средства сбора, кроме электролиза солевого расплава. С использованием настоящего изобретения морская вода подвергается электролизу напрямую для сбора металлического натрия. Едкий натр также может быть произведен без использования ионообменной смолы. Кроме того, водород и кислород могут быть произведены просто путем приложения электрического потенциала между положительным и отрицательным электродами, погруженными под поверхность моря. Кроме того, могут быть изготовлены вторичные батареи типа основный металл/воздух, например, с литием, натрием, калием и кальцием, электролиты которых являются водными растворами, или вторичные батареи типа основный металл/галоген, у которых экономический эффект огромен. В частности, в качестве альтернативной нефти энергии, металлический натрий, получаемый из морской воды, может внести большой вклад в промышленность нашей страны как ресурс производства электроэнергии, без опасений насчет его исчерпания или неравномерного распределения, или как работающая с водным раствором основного металла вторичная батарея с высокой эффективностью выработки энергии. [0121] ОБЪЯСНЕНИЕ ССЫЛОЧНЫХ ПОЗИЦИЙ 1 - герметичный контейнер; 2 - открытый контейнер; 3 - отрицательная электродная камера; 4 - положительная электродная камера; 5 - соединительная трубка; 6 - прикладывающий давление элемент (цилиндр); 7 - резиновая пипетка; 8 - работающее с электроприводом устройство сжатия с храповым механизмом; 9 - водяной бак; 10 - гидростатический напор (h); 11 - отталкивающая жидкость (воду) пористая мембрана (изоляционная пленка); 12 - шланг сбора полученного газа; 13 - спирт; 14 - водный раствор электролита; 15 - растворяемое вещество (химикат); 16 - заполненная маслом электродная камера; 17 - положительная электродная пластина (внутри масляного бака); 18 - промежуточная электродная пластина (внутри масляного бака); 19 - поверхность виртуального отрицательного электрода (граница раздела между маслом и электролитом); 20 - заряд (напряжение); 21 - положительная электродная пластина в электролите; 22 - масло; 23 - масло (удельный вес 1 или менее); 24 - масло (удельный вес более 1); 25 - кислота (соляная кислота в случае хлорида); 26 - патрубок для сбора продукта отрицательного электрода; 27 - отталкивающая жидкость/воду пористая мембрана (для проникания пресной воды); 28 - водопроводная вода (использование давления воды); 29 - герметичный контейнер большого размера; 30 - устройство получения водорода; 31 - гидроксид основного металла (едкий натр); 32 - водный раствор хлорида основного металла (водный раствор хлорида натрия); 33 - концентрированная кислота (соляная кислота); 34 - впуск подачи воды; 35 - патрубок для сбора продукта отрицательного электрода; 36 - отрицательная электродная пластина; 37 - положительный электрод (углеродные волокна, углеродные частицы, пористый углерод); 38 - положительная электродная пластина; 39 - бак подачи водного раствора соли основного металла; 40 - заполненная водой электродная камера; 41 - газопроницаемая электродная камера; 42 - патрубок для сбора продукта положительного электрода (выпуск концентрированной кислоты); 43 - сетчатый отрицательный электрод (углеродные волокна, металлическая сетка); 44 - пористая углеродная отрицательная электродная пластина с изоляционной пленкой; 45 - газообразный водород; 46 - солевой расплав гидроксида основного металла (едкий натр); 47 - патрубок для нагнетания газообразного водорода; 48 - нагреватель для нагрева солевого расплава; 49 - гидрид основного металла (гидрид натрия); 50 - анион водорода; 51 - патрубок для сбора гидрида основного металла; 52 - отрицательная электродная камера (для батареи и для конденсатора); 53 - положительная электродная камера (для батареи и для конденсатора); 55 - герметичный контейнер оболочечного типа; 56 - вспомогательный положительный электрод для зарядки (сетчатый электрод); 57 - изолированный от внешнего воздуха отрицательный электрод; 58 - выполненная из углерода пористая электродная пластина (активированный уголь); 59 - пленка оксида металла (для положительного электрода батареи) (CuO, AlO3, ZnO2); 60 - металлическая пластина (для батареи) (Cu, Al); 61 - полимерная пленка; 62 - отрицательная электродная пластина (для батареи) (Al, Mg, Ca, Zn, Ni, Pb); 63 - пленка хлорида металла (для положительного электрода батареи) (ZnCl2); 64 - коллекторная электродная пластина (для батареи) (Cu, Al); 65 - отрицательная электродная пластина (Al, Mg, Zn); 66 - положительный электрод (хлорид металла, используемого для отрицательного электрода); 67 - частица активированного угля или углеродное волокно; 68 - жидкий бром; 69 - частица йода; 70 - графитовая пластина; 71 - алюминиевая (Al) отрицательная электродная пластина; 72 - диэлектрический раствор (на масляной основе, на водной основе); 73 - электродная пластина (конденсатор); 74 - электрод с двойным электрическим слоем (конденсатор); 75 - электрод окислительно-восстановительного конденсатора; 76 - электрод гибридного конденсатора; 77 - замкнутая пунктирная линия; 78 - электропроводящий материал с пустотами (металлическое волокно, углеродное волокно, активированный уголь); 79 - водный раствор электролита для электрохимического конденсатора (разбавленная серная кислота); 80 - разбавленный едкий натр (водный раствор электролита для электрохимического конденсатора); 81 - волокно из нержавеющей стали; 82 - углеродное волокно; 83 - межэлектродное расстояние (d); 84 - устройство получения водорода под морской поверхностью; 85 - устройство получения водорода многоступенчатого типа под морской поверхностью; 86 - устройство получения водорода под поверхностью озера (под морской поверхностью); 87 - герметичный контейнер в форме четырехугольной призмы; 88 - пресная вода (вода); 89 - простое устройство получения водорода, использующее давление водопроводной воды; 90 - устройство, напрямую производящее едкий натр и газообразный хлор из водного раствора хлорида натрия; 91 - устройство, напрямую производящее едкий натр и соляную кислоту из водного раствора хлорида натрия; 92 - устройство получения основного металла; 93 - первичный клапан регулирования давления (газопроницаемая электродная камера); 94 - всасывающее отверстие (до величины не более, чем давление водостойкости, с помощью вакуумного насоса); 95 - устройство, напрямую производящее элемент-основный металл и соляную кислоту; 96 - устройство получения основного металла, использующее виртуальный отрицательный электрод; 97 - устройство получения гидрида металла; 98 - устройство хранения водного раствора электролита; 99 - всасывающее отверстие (вакуумный насос); 100 - водоотталкивающая пористая мембрана (11a); 101 - водоотталкивающая пористая мембрана (11b); 102 - резервный водный раствор электролита; 103 - вторичная батарея с электролитом сжимаемого типа; 104 - груз; 105 - впуск воздуха; 106 - батарея пакетного типа с едким натром; 107 - окислительно-восстановительный конденсатор; 108 - металлическая пластина для окислительно-восстановительного конденсатора; 109 - пленка оксида металла для окислительно-восстановительного конденсатора; 110 - плавучая фабрика; 111 - прибрежная фабрика (прибрежная электростанция); 112 - устройство получения водорода; 113 - работающий за счет плавучести-гравитации энергогенератор; 114 - устройство управления реакцией гидролиза; 115 - выполненный из водоотталкивающего пористого фторкаучука герметичный мешок; 116 - химикат; 117 - газ; 118 - труба (шланг) подачи водного раствора; 119 - растение (овощ, плодовое дерево); 120 - химикатраспыляющий резервуар (мешок или трубка из водоотталкивающего пористого полимера); 121 - дополнительное питательное вещество (овощная ферма); 122 - диспетчерская; 123 - катетер (трубка); 124 - экзотермическое средство (CaO); 125 - капсула.
Реферат
Изобретение относится к электрохимическому реактору и способам осуществления химической реакции и топливного цикла едкого натра с использованием такого реактора. Электрохимический реактор включает в себя положительный электрод с первой главной поверхностью и второй главной поверхностью на стороне, противоположной первой главной поверхности, и отрицательный электрод с первой главной поверхностью и второй поверхностью на стороне, противоположной первой главной поверхности. Положительный электрод и отрицательный электрод обращены друг к другу своими первыми главными поверхностями и расположены отстоящими друг от друга, образуя пространство между ними. Это пространство заполняется электропроводящей жидкостью и/или диэлектрической жидкостью. Первый изоляционный элемент предусмотрен на первой поверхности положительного электрода для того, чтобы изолировать положительный электрод от жидкости, и второй изоляционный элемент предусмотрен на первой поверхности отрицательного электрода для того, чтобы изолировать отрицательный электрод от жидкости. Первый изоляционный элемент включает в себя первую отталкивающую жидкость пористую мембрану, имеющую множество пор, а второй изоляционный элемент включает в себя вторую отталкивающую жидкость пористую мембрану, имеющую множество пор. Реактор дополнительно включает в себя прикладывающий давление элемент, который сжимает жидкость для того, чтобы заполнить поры первой и второй отталкивающих жидкость пористых мембран жидкостью, вызывая тем самым электрохимическую реакцию с участием положительного электрода и отрицательного электрода. Изобретение обеспечивает высокоэффективный электрохимический реактор. 3 н. и 28 з.п. ф-лы, 47 ил.

Комментарии