Электрокатетер для побуждения стеноза сосуда, имеющий два множества расходящихся электродов - RU2207823C2
Код документа: RU2207823C2
Чертежи






























Описание
Изобретение в общем относится к способу и устройству для подачи энергии для сокращения полой анатомической структуры, например, фаллопиевой трубы или вены, но без ограничения поверхностными и сквозными венами, геморроидальными узлами и эзофагеальными варикозно-расширенными сосудами, а более конкретно к способу и устройству, использующему электродное приспособление, имеющее множество выводов для подачи высокочастотной энергии, сверхвысокочастотной энергии или тепловой энергии.
Венозная система нижних конечностей человека по существу состоит из поверхностной и внутренней венозных систем со сквозными венами, соединяющими эти две системы. Поверхностная венозная система содержит длинную и короткую вены, относящиеся к подкожной вене ноги. Внутренняя венозная система содержит переднюю и заднюю тибиальные вены, которые объединяются для образования подколенной вены, которая, в свою очередь, становится бедренной веной, при соединении посредством короткой вены, относящейся к подкожной вене ноги.
Венозная система содержит множество однопутевых клапанов для направления потока крови назад к сердцу. Венозными клапанами, как правило, являются левые предсердно-желудочковые двустворчатые клапаны, причем каждая створка клапана при катаболическом кровяном давлении образует мешок или емкость для крови, побуждает свободные поверхности створок клапана вместе препятствовать катаболическому потоку крови и позволяет только предшествующему потоку крови проходить к сердцу. Если на пути потока оказывается функционально неспособный клапан, то клапан неспособен закрыться, поскольку створки клапана не образуют должного уплотнения и катаболический поток крови не может быть остановлен. При недостаточности венозного клапана в нижних венозных секциях и соединительных тканях возникают повышенные деформация и давление, приводящие в некоторых случаях к дополнительной валвулярной недостаточности. Варикозно-расширенные вены и более симптоматичная хроническая венозная недостаточность часто являются результатом двух венозных состояний.
Состояние варикозно-расширенных вен включает в себя расширение и извитость поверхностных вен нижних конечностей, что приводит к уродливому изменению цвета, болям, опуханию и, возможно, к образованию язв. Варикозно-расширенные вены часто вызывают недостаточность одного или более венозных клапанов, которые позволяют рефлюкс крови в поверхностной системе. Это может также ухудшить рефлюкс внутренних и сквозных вен. Современные методы лечения венозной недостаточности предусматривают хирургические процедуры, например экстирпацию подкожной вены, лигирование и иногда трансплантацию участка вены.
Хроническая венозная недостаточность предполагает ухудшение состояния варикозно-расширенных вен, которое может быть вызвано дегенеративной слабостью в сегменте венозного клапана или гидродинамическими силами, действующими на ткани тела, например ног, лодыжек и стоп. При отказе клапанов в вене, на следующих венозных клапанах, расположенных ниже по течению, увеличивается гидростатическое давление, вызывая расширение этих вен. Когда это продолжается, в конечном счете откажет больше венозных клапанов. Когда они отказывают, эффективная высота столба крови выше стопы и лодыжек растет, а масса и гидростатическое давление, действующие на ткани, увеличиваются. Когда масса столба в результате отказов клапанов достигает критической точки, начинается образование язв, которые начинают углубляться и в конечном счете выходят на поверхность. Вследствие плохой циркуляции крови в венах из-за недостаточности клапана сердца во внутренней и других венозных системах такие язвы трудно поддаются лечению.
Другие состояния, родственные венозным, включают в себя расширенные геморроидальные узлы и эзофагеальные варикозно-расширенные сосуды. Давление и расширение геморроидальных венозных сплетений может побуждать внутренние геморроидальные узлы расширяться и/или выпадать и проталкиваться через анальное отверстие. Если геморроидальный узел остается выпавшим, то это может в результате привести к значительному дискомфорту, включая зуд и кровотечение. Венозный возврат из таких выпавших геморроидальных узлов оказывается блокированным анальными сфинктерами, что приводит к странгулированному геморрою. В результате, в выпавшей вене начинается свертываться кровь, что приводит к тромбообразованию. Крайне болезненное состояние могут вызвать отек и воспаление.
Варикозно-расширенные вены, называемые эзофагеальными варикозно-расширенными сосудами, могут образовываться в венозной системе вдоль подслизистой основы нижнего пищевода и приводить к кровотечению вздутых вен. Кровотечение или кровоизлияние из эзофагеальных расширенных сосудов, которые может быть трудно остановить, при отсутствии лечения могут развиться в состояние, угрожающее жизни. Такие варикозно-расширенные сосуды просто подвергаются эрозии и ведут к массивным желудочно-кишечным кровотечениям.
Лигирование фаллопиевой трубы (перевязка маточных труб) для стерилизации или других целей, как правило, осуществляют посредством лапароскопии. Врач разрезает фаллопиеву трубу или трубы и перевязывает концы. Может быть также использована внешняя каутеризация или пережимы. Должно быть использовано средство для общей или региональной анестезии. Все вышеуказанные операции выполняют снаружи фаллопиевой трубы.
Геморроидальные узлы и эзофагеальные варикозно-расширенные сосуды могут быть уменьшены посредством внутриполосного лигирования. Используемый в этой заявке термин "лигирование" или "внутриполостное лигирование" предусматривает окклюзию, спадение стенок или закрытие полости трубчатого органа или полой анатомической структуры посредством подачи энергии изнутри полости трубчатого органа или структуры. Используемый в этой заявке термин "лигирование" или "внутриполостное лигирование" включает в себя электролигирование. В случае лигирования фаллопиевой трубы было бы желательным выполнять лигирование изнутри фаллопиевой трубы для избежания травм, связанных с выполнением этой операции снаружи.
Лигирование предусматривает каутеризацию или коагуляцию полости трубчатого органа при использовании энергии, подаваемой, например, через электродное приспособление. Электродное приспособление вводят в полость трубчатого органа и позиционируют так, чтобы оно вступало в контактное взаимодействие со стенкой полости трубчатого органа. Как только электродное приспособление позиционировано должным образом, к стенке посредством электродного приспособления подают высокочастотную энергию, побуждая в соответствии с этим стенку полости трубчатого органа сокращаться, приводя к уменьшению диаметра поперечного сечения полости трубчатого органа. В случае вены уменьшение диаметра поперечного сечения вены, например, от 5 мм (0,2 дюйма) до 1 мм (0,04 дюйма) значительно уменьшает поток крови через полость трубчатого органа и в результате приводит к эффективной окклюзии. Хотя это и не требуется для эффективной окклюзии или лигирования, но можно вызвать полное спадение стенок вены, что приведет к полной обструкции полости трубчатого органа, которая блокирует прохождение потока крови через вену. Аналогичным образом, для осуществления стерилизации пациента может быть осуществлено достаточное спадение стенок фаллопиевой трубы.
Одно устройство для выполнения лигирования содержит трубчатый стержень, имеющий электродное приспособление, присоединенное на рабочем конце. Электрические выводы проходят через стержень от его дальнего конца к ближнему. На ближнем конце стержня выводы заканчиваются на электрическом соединителе, тогда как на дальнем конце стержня выводы соединены с электродным приспособлением. Электрический соединитель обеспечивает контактную поверхность между выводами и источником электропитания, как правило, высокочастотным генератором. Управление высокочастотным генератором осуществляется посредством управляющего устройства, как правило, микропроцессором.
Устройство для выполнения лигирования может работать в монополярной или биполярной конфигурации. В монополярной конфигурации электродное приспособление состоит из электрода, который заряжают положительно или отрицательно. Обратный путь тока, проходящего через электрод, предусмотрен вне тела пациента, например, путем размещения пациента в физическом контакте с большой подушкой, имеющей низкий импеданс. Ток проходит от устройства для выполнения лигирования к подушке, имеющей низкий импеданс. В биполярной конфигурации электродное приспособление состоит из двух противоположно заряженных электродов, разделенных диэлектрическим материалом. В соответствии с этим в биполярной конфигурации обратный путь тока предусмотрен самим электродным приспособлением. Ток проходит от одного электрода через ткань и возвращается через противоположно заряженный электрод.
Для предотвращения повреждения ткани, например от обугливания вследствие каутеризации в результате перегрева, к электродному приспособлению присоединен датчик температуры. Датчиком температуры может быть термопара, которая осуществляет текущий контроль температуры венозной ткани. Термопара через стержень соединена с высокочастотным генератором и контроллером и обеспечивает электрические сигналы к контроллеру, который осуществляет текущий контроль температуры и регулирует энергию, подаваемую к ткани, соответственно, через электродное приспособление.
Общая эффективность прибора для выполнения лигирования в большой степени зависит от электродного приспособления, содержащегося в устройстве. Монополярные и биполярные электродные приспособления, которые содержат твердотельные приборы, имеющие постоянные форму и размер, ограничивают эффективность устройства для выполнения лигирования по нескольким причинам. Во-первых, электродное приспособление постоянного размера, как правило, вступает в контактное взаимодействие со стенкой вены только в одной точке на окружности или на внутреннем диаметре стенки вены. В результате этого, подача высокочастотной энергии имеет высокую концентрацию в венозной ткани, находящейся с ним в контактном взаимодействии, тогда как поток высокочастотного тока через остальную венозную ткань непропорционально мал. В соответствии с этим, области стенки вены вблизи точки контактного взаимодействия спадают с более высокой скоростью, чем другие области стенки вены, приводя в результате к неравномерному сокращению полости вены, которое может в результате привести к недостаточности общей эффективности окклюзии и полость в конечном счете может снова открыться. Для предотвращения создания недостаточной окклюзии высокочастотная энергия должна быть подана в течение длительного периода времени так, чтобы ток проходил через ткань, генерируя тепловую энергию, включая участок ткани, не находящийся в контактном взаимодействии с электродом, чтобы побудить эту ткань сократиться также достаточно. При длительной подаче высокочастотной энергии имеется большая вероятность увеличения температуры крови до недопустимого уровня, что может в результате привести к образованию на электроде и в вене значительного количества коагулянта, которое не является желательным. Это может быть предотвращено посредством обескровливания вены перед обработкой и путем применения терморегулируемой подачи энергии.
Во-вторых, эффективность лигирующего устройства, имеющего электродное приспособление постоянного размера, ограничена для вен определенного размера. Попытка лигировать вену, имеющую диаметр, который существенно больше, чем электродное приспособление, может в результате привести не только к неравномерному нагреву стенки вены, как было только что описано, но также к недостаточному сокращению диаметра вены. Чем больше диаметр вены относительно диаметра электродного приспособления, тем меньше энергия, подаваемая к стенке вены в точках, отстоящих от точки контактного взаимодействия с электродом. В соответствии с этим стенка вены, вероятно, не полностью спадет прежде, чем венозная ткань подвергнется чрезмерной каутеризации в точке контактного взаимодействия с электродом. Хотя коагуляция в таком случае может вначале привести к окклюзии вены, такая окклюзия может быть только временной в том отношении, что коагулированная кровь может в конечном счете раствориться и вена частично откроется. Одним решением такой неадекватности является устройство, имеющее взаимозаменяемые электродные приспособления с различными диаметрами. Другим решением было бы наличие комплекта катетеров, имеющих разные размеры так, чтобы при необходимости под рукой был катетер соответствующего размера для диаметра интересующей вены. Однако такие решения экономически неэффективны и трудоемки при применении. Было бы желательно иметь один катетер, который был бы пригоден для применения в полостях трубчатых органов, имеющих широкий диапазон размеров.
Хотя указанные концепции описаны применительно к венам, эти концепции в общем применимы также для других полых анатомических структур в теле. Для избежания необязательного повторения описание, приведенное выше, было ограничено, как правило, обработкой вен.
Таким образом, квалифицированному в этой области техники специалисту становится очевидной потребность в поддающемся расширению электродном устройстве и способе его применения, которые были бы способны обеспечивать более равномерное распределение высокочастотной энергии вдоль кольцевой полосы стенки целевой анатомической структуры в том случае, когда диаметр стенки больше, чем электродное приспособление, и в соответствии с этим обеспечивать более предсказуемую и эффективную окклюзию анатомических структур при минимизации образования коагулянта, образуемого в результате повышения температуры. Такие устройство и способ должны быть применимы для лигирования всевозможных вен в теле, включая без ограничения поверхностные и сквозные вены, а также геморроидальные узлы и эзофагеальные варикозно-расширенные сосуды и фаллопиевы трубы. Настоящее изобретение обеспечивает удовлетворение этих и других потребностей.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ НАСТОЯЩЕГО
ИЗОБРЕТЕНИЯ
Настоящее изобретение обеспечивает получение устройства и способа для подачи энергии вдоль, как правило, кольцевой полосы стенки полой анатомической структуры, например, вены,
фаллопиевой трубы, геморроидального узла или эзофагеального варикозно-расширенного сосуда. Подача энергии с помощью таких устройства и способа приводит в результате к более равномерному и
предсказуемому сокращению структуры.
В первом аспекте настоящего изобретения устройство для подачи энергии к полой анатомической структуре содержит катетер, имеющий стержень с рабочим концом, которым энергия подается к структуре, первое множество поддающихся развертыванию электродных выводов, смонтированных на рабочем конце катетера, причем каждый вывод имеет электрод, второе множество поддающихся развертыванию электродных выводов, смонтированных на рабочем конце катетера, отдельное и отстоящее в продольном направлении от первого множества, причем каждый вывод имеет электрод, при этом каждый из электродов первого и второго множеств имеет развернутое положение, в котором электрод расположен в направлении наружу от стержня катетера, и сжатое положение, в котором электрод расположен ближе к стержню, и приспособление для развертывания, смонтированное на катетере, причем приспособление для развертывания имеет первое положение, в котором выбранные электроды находятся в сжатом положении, и второе положение, в котором электроды находятся в развернутом положении. В более детальном аспекте электродные выводы первого множества образованы так, чтобы они побуждались к движению в направлении наружу от стержня катетера, причем приспособление для развертывания содержит подвижный корпус, имеющий первое положение, в котором корпус окружает первое множество электродных выводов, по меньшей мере их часть, и ограничивает окруженные выводы сжатым положением, подвижный корпус имеет второе положение, в котором первому и второму множествам дается возможность развертываться в направлении наружу. Кроме того, электродные выводы второго множества образованы так, чтобы они побуждались к движению в направлении наружу от стержня катетера. Подвижный корпус в его первом положении также окружает второе множество электродных выводов, по меньшей мере их часть, и ограничивает окруженные выводы сжатым положением.
В других аспектах каждый из электродных выводов первого и второго множеств образован с изгибом в направлении наружу, который побуждает дальнюю часть каждого вывода развертываться в направлении наружу со вторым множеством электродных выводов, смонтированных на катетере вблизи от первого множества, подвижный корпус в его первом положении относительно электродных выводов удален от изгибов первого и второго множеств электродных выводов, удерживая благодаря этому первое и второе множества в сжатом состоянии. Подвижный корпус в его втором положении приближен к изгибам первого и второго множеств, позволяя благодаря этому первому и второму множествам развертываться в направлении наружу.
В других дополнительных аспектах электродные выводы смонтированы на рабочем конце, образуя консольную конструкцию. Каждый из электродных выводов первого и второго множеств расположен относительно рабочего конца так, чтобы в развернутом положении электроды выводов образовывали по существу симметричную конфигурацию по существу одинаково отстоящих друг от друга электродов. Каждый электродный вывод образован из электропроводного материала, изолированного вдоль его длины, и каждый электродный вывод имеет обращенную в направлении наружу часть, на которой отсутствует изоляция, образуя благодаря этому электрод. Электродные выводы образованы из материала, имеющего прочность, выбранную так, чтобы в том случае, когда корпус находится в его втором положении, выводы имели достаточно прочности, чтобы двигаться в контактном взаимодействии с полой анатомической структурой, и выводы имели достаточную прочность, чтобы позволять анатомической структуре сокращаться, но оставаться в контактном взаимодействии с сокращающейся структурой.
Первое множество электродных выводов смонтировано на первом электропроводном монтажном кольце, с которым электрически соединены электроды этих выводов. Второе множество электродных выводов смонтировано на втором электропроводном монтажном кольце, с которым электрически соединены электроды этих выводов. Предусмотрено также третье электропроводное монтажное кольцо, с которым соединены чередующиеся электродные выводы, выбранные из указанных множеств электродных выводов, благодаря этому приводя к тому, что смежные выводы выбранного множества соединены с разными монтажными кольцами. Источник питания соединен с электродами, а контроллер управляет источником питания. Переключатель соединен с контроллером, причем переключатель имеет первое положение, в котором контроллер обеспечивает получение на монтажных кольцах разных полярностей, и второе положение, в котором контроллер обеспечивает получение на монтажных кольцах одинаковых полярностей.
В еще одном аспекте источник питания соединен с электродами, контроллер управляет источником питания, а датчик температуры смонтирован на электродном выводе, причем датчик температуры формирует температурные сигналы к контроллеру, при этом контроллер управляет источником питания в ответ на температурные сигналы.
В дополнительных аспектах контроллер выполнен с возможностью переключения выбранной электрической полярности выводов, включая регулирование выходной мощности источника питания, подаваемой на электроды так, чтобы смежные электроды первого множества выводов имели противоположную полярность при сохранении полярности второго множества электродов таким образом, чтобы они были электрически нейтральными, переключение полярности электродов первого множества выводов так, чтобы все они имели одну полярность при спадении стенок полой анатомической структуры вокруг выводов первой полярности, и регулирование источника питания так, чтобы электроды выводов второй полярности имели противоположную полярность, чем у электродов первого множества выводов, при выполнении переключения полярности электродов. В более детальных аспектах контроллер дополнительно приспособлен управлять источником питания так, чтобы смежные электроды первой полярности были противоположной полярности, регулировать источник питания так, чтобы смежные электроды второй полярности были противоположной полярности, и регулировать источник питания так, чтобы полярности электродов второго множества были выбраны так, чтобы противоположные полярности в продольном направлении были выравнены с электродами первой полярности. В других дополнительных аспектах устройство дополнительно содержит спинную пластину, расположенную на поверхности пациента, причем контроллер дополнительно приспособлен регулировать энергию, подаваемую к одному из множеств электродных выводов так, чтобы электроды были первой полярности и регулировать энергию, подаваемую к спинной пластине так, чтобы она была второй полярности.
В другом аспекте приспособление для развертывания содержит подвижный корпус и выравнивающее устройство, позиционируемое внутри корпуса, причем выравнивающее устройство поддерживает разделение электродных выводов во время движения корпуса и контролирует развертывание или сжатие каждого электродного вывода.
Способ, соответствующий настоящему изобретению, предусматривает введение в полую анатомическую структуру катетера, имеющего стержень и рабочий конец с первым множеством электродных выводов, расположенных на рабочем конце, и вторым множеством электродных выводов, расположенных на рабочем конце и отстоящих в продольном направлении от электродных выводов первого множества, причем каждый вывод имеет электрод, соединенный с источником питания, развертывание выводов первого множества в направлении наружу от рабочего конца катетера, причем электроды первого множества движутся в направлении друг от друга в контактное взаимодействие с внутренней стенкой, и развертывание выводов второго множества в направлении наружу от рабочего конца катетера, при этом электроды второго множества движутся в направлении друг от друга и в контактное взаимодействие с внутренней стенкой в положениях, отстоящих в продольном направлении от точек контактного взаимодействия электродов первого множества на внутренней стенке. В другом аспекте способ дополнительно предусматривает подачу энергии к внутренней стенке от электродов электродных выводов для спадения стенки полой анатомической структуры для обеспечения эффективной окклюзии полой анатомической структуры.
В более детальном аспекте предусматривается перемещение корпуса и первого и второго множеств электродов относительно друг друга для избирательного развертывания электродных выводов в направлении наружу или для сжатия электродных выводов.
Способ дополнительно предусматривает перемещение катетера в полой анатомической структуре при продолжении подачи энергии посредством электродов к полой анатомической структуре. Кроме того, дополнительно предусматривается сжатие полой анатомической структуры до требуемого размера перед и/или в процессе подачи энергии. Дополнительно предусматривается сжатие полой анатомической структуры посредством жгута или эластичного бинта перед и/или в процессе подачи энергии и контроль полой анатомической структуры через ультразвуковое окно, образованное в жгуте или бинте. Более детальные аспекты способа предусматривают обескровливание полой анатомической структуры перед и/или в процессе подачи энергии путем подачи жидкости для вытеснения крови из анатомической структуры или путем сжатия полой анатомической структуры.
Кроме того, предусматриваются управление энергией, подаваемой к электродам первого множества выводов, так, чтобы они имели первую полярность, и управление энергией, подаваемой к электродам второго множества выводов, так, чтобы они имели вторую полярность, отличающуюся от первой полярности. В другом аспекте предусматриваются управление источником питания так, чтобы смежные электроды первого множества выводов имели противоположную полярность при поддержании полярности второго множества электродов такой, чтобы они были электрически нейтральными, переключение полярности электродов первой полярности выводов так, чтобы они все имели одну полярность при спадении стенки полой анатомической структуры вокруг первого множества выводов, и управление источником питания так, чтобы электроды второго множества выводов относительно электродов первого множества выводов имели противоположную полярность при осуществлении переключения полярности электродов.
Дополнительные аспекты предусматривают приложение спинной пластины к поверхности пациента, управление энергией, подаваемой к одному из множеств электродных выводов, так, чтобы электроды были первой полярности, и управление энергией, подаваемой к спинной пластине, так, чтобы она имела вторую полярность. В другом аспекте способ предусматривает управление источником питания так, чтобы смежные электроды первого множества выводов имели противоположную полярность, управление источником питания так, чтобы электроды второго множества выводов имели противоположную полярность, и управление источником питания так, чтобы полярности электродов второго множества выводов были выбраны так, чтобы противоположные полярности в продольном направлении были выравнены с полярностью электродов первого множества.
В других детальных аспектах способ предусматривает измерение температуры на электродном выводе и управление подачей мощности на электродные выводы в ответ на температуру, измеряемую на выводе. Кроме того, перед подачей энергии дополнительно предусматривается промывка полой анатомической структуры жидкостью. Дополнительные аспекты предусматривают введение катетера, имеющего первое и второе множества отстоящих в продольном направлении, поддающихся развертыванию электродных выводов, в вену, в фаллопиеву трубу, в геморроидальный узел или в эзофагеальный варикозно-расширенный сосуд.
Эти и другие аспекты настоящего изобретения станут очевидными из следующего более подробного описания, сделанного со ссылкой на сопроводительные чертежи, на которых иллюстрируются характерные примеры вариантов осуществления настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 - схематическое изображение системы подачи энергии (выполненное с частичным местным разрезом катетера), соответствующей предпочтительному варианту осуществления настоящего изобретения, на
котором показан рабочий конец, содержащий множество электродов, поддающихся развертыванию в направлении наружу, для подачи энергии к ткани, и соединительный конец, соединенный с источником питания,
управляемым посредством микропроцессорного контроллера для регулирования энергии, подаваемой на электроды рабочего конца.
Фиг. 2 - сечение рабочего конца катетера первого варианта осуществления, соответствующего настоящему изобретению, на котором показаны электроды в полностью развернутом положении.
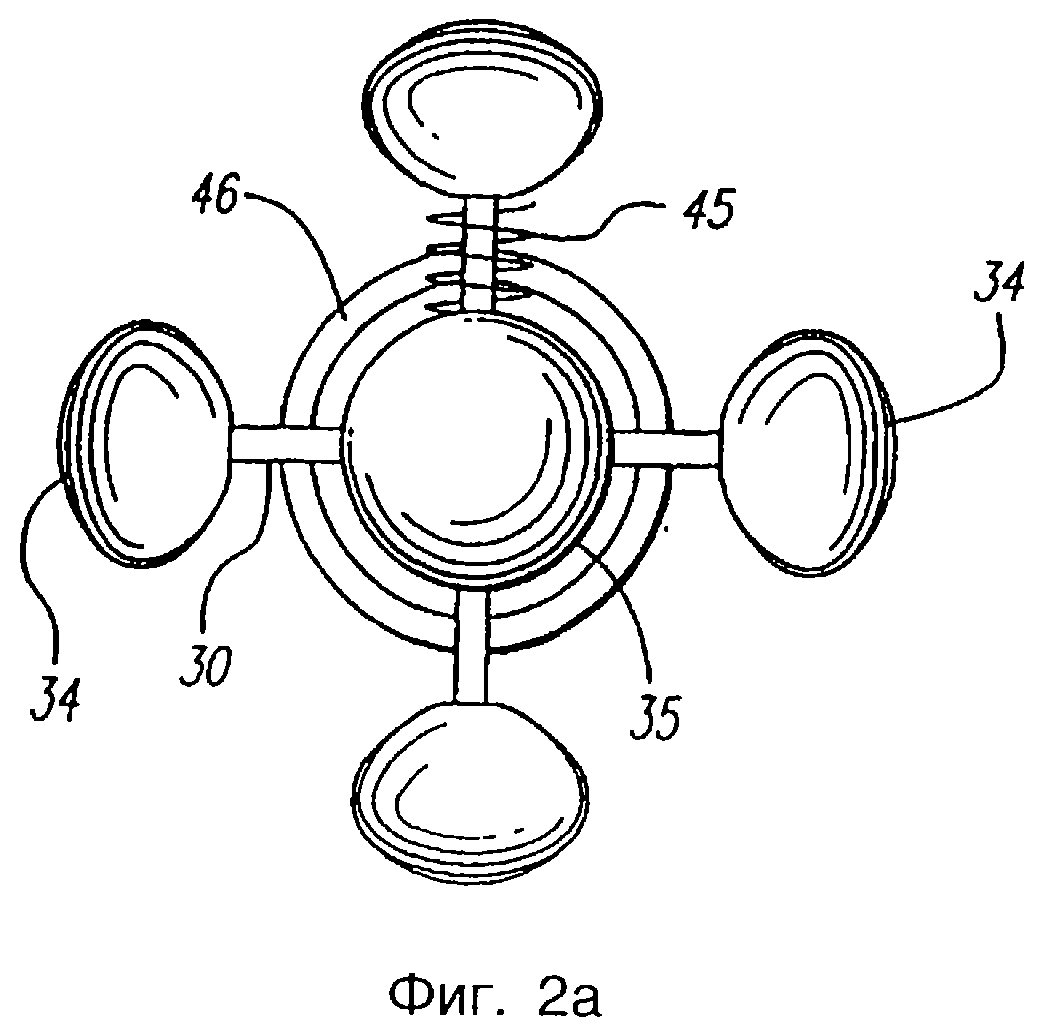
Фиг.2а - вид с торца (по линии 2а-2а, показанной на фиг.2) рабочего конца катетера первого варианта осуществления, соответствующего настоящему изобретению.
Фиг. 3 - сечение рабочего конца катетера первого варианта осуществления, соответствующего настоящему изобретению, на котором показаны электроды в полностью отведенном положении.
Фиг. 4 - сечение рабочего конца катетера второго варианта осуществления, соответствующего настоящему изобретению, на котором показаны электроды в полностью развернутом положении.
Фиг.4а - вид с торца (по линии 4а-4а, показанной на фиг.4) второго варианта осуществления, соответствующего настоящему изобретению.
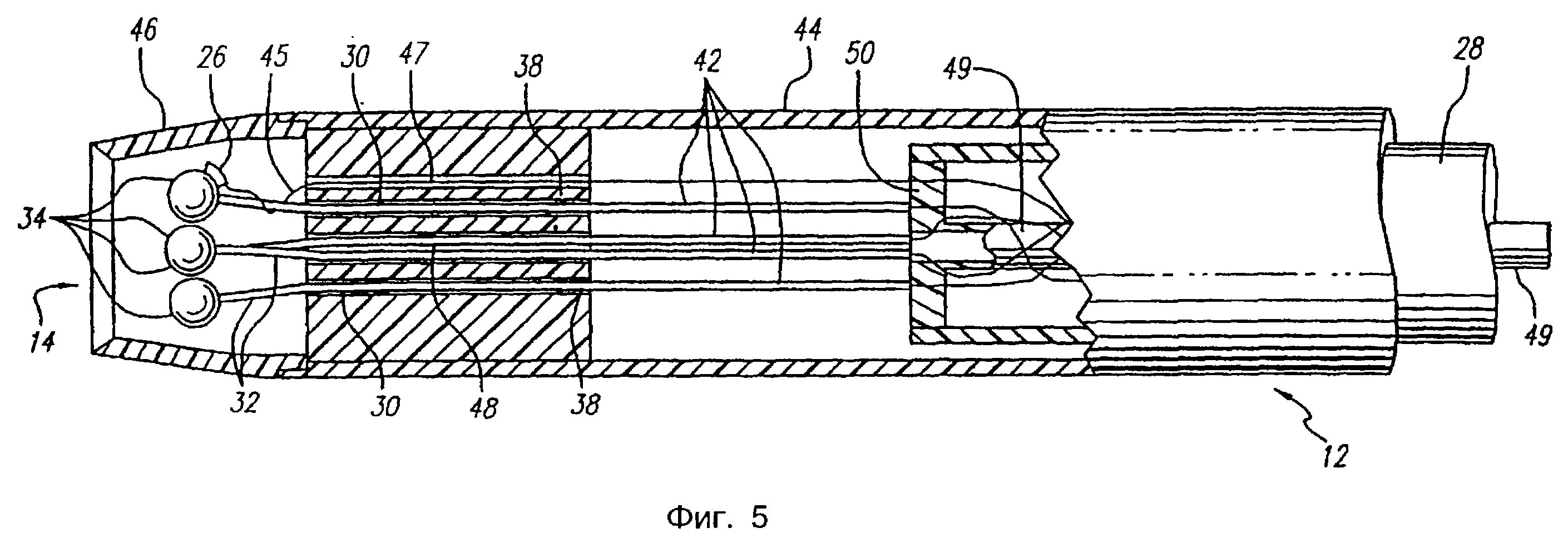
Фиг. 5 - сечение рабочего конца катетера второго варианта осуществления, показанного на фиг.4 и соответствующего настоящему изобретению, на котором показаны электроды в полностью отведенном назад положении.
Фиг. 6 - сечение анатомической структуры, содержащей катетер, показанный на фиг. 2, с электродами, находящимися в контактном взаимодействии с анатомической структурой.
Фиг.6а - вид с торца (по линии 6а-6а, показанной на фиг.6) анатомической структуры, содержащей катетер.
Фиг. 7а-7с - сечения анатомической структуры, содержащей катетер, соответствующий первому варианту осуществления настоящего изобретения, на которых показана анатомическая структура в разных стадиях лигирования.
Фиг. 8 - сечение анатомической структуры, содержащей катетер, показанный на фиг. 4, соответствующий второму варианту осуществления настоящего изобретения.
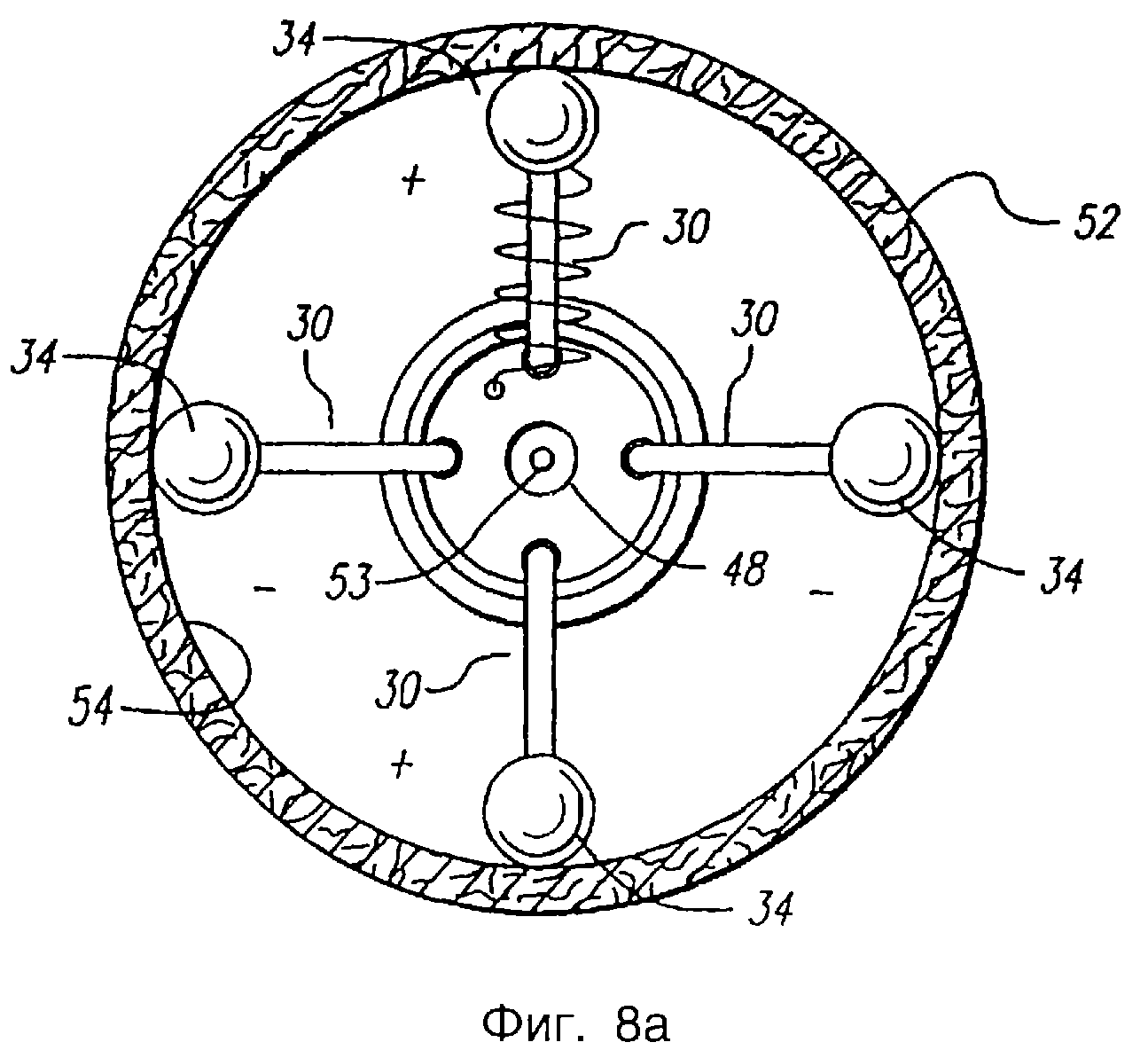
Фиг.8а - вид с торца (по линии 8а-8а, показанной на фиг.8) анатомической структуры, содержащей катетер.
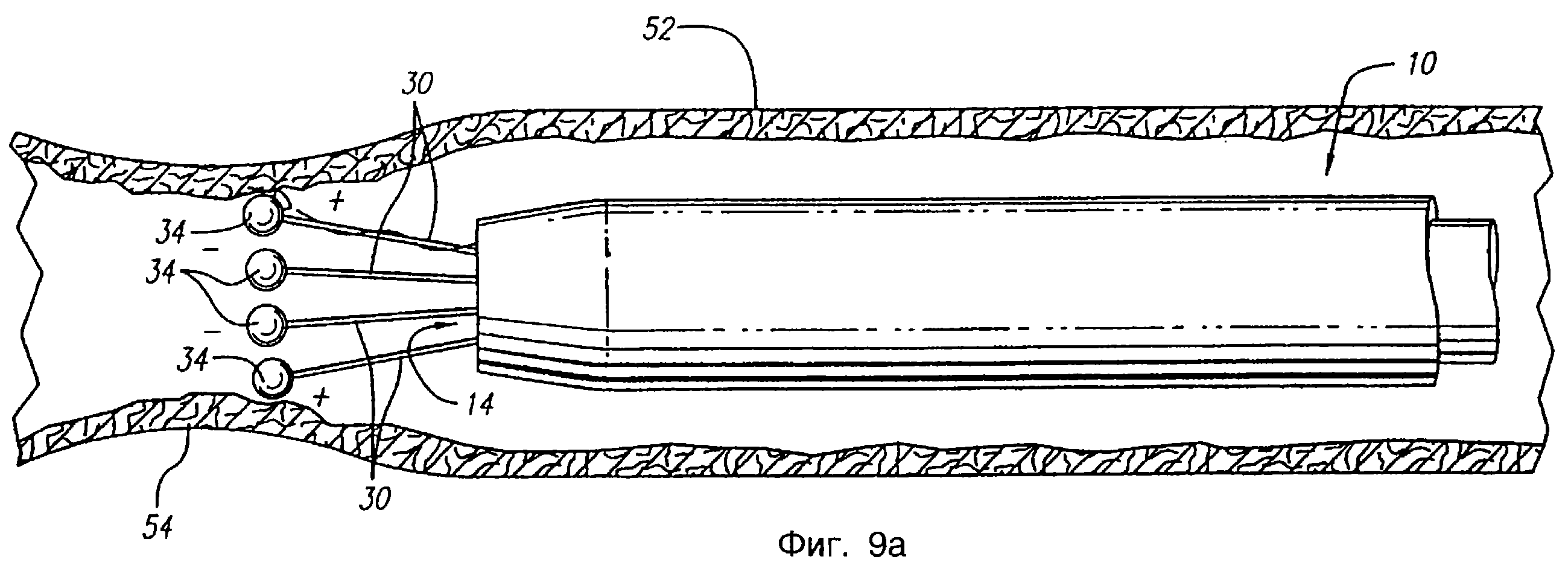
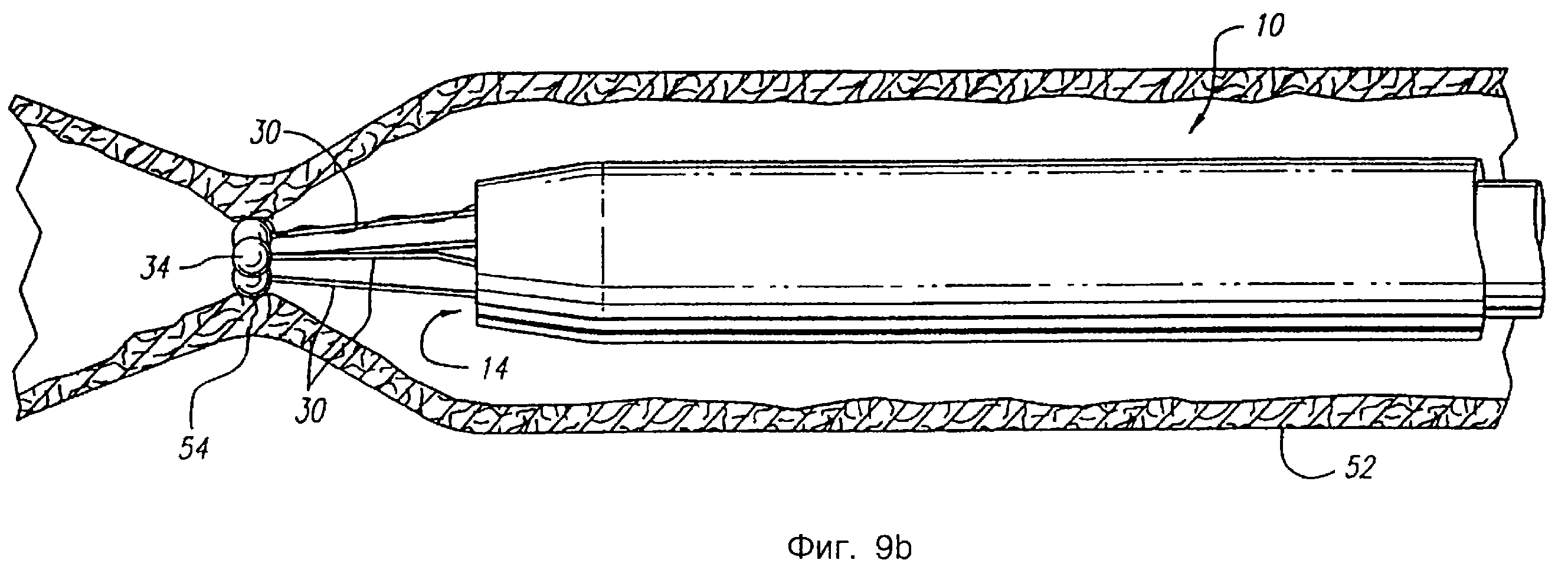
Фиг.9а и 9b - сечения анатомической структуры, содержащей катетер, соответствующий второму варианту осуществления настоящего изобретения, на которых показана анатомическая структура на разных стадиях лигирования.
Фиг. 10 - сечение рабочего конца катетера третьего варианта осуществления, соответствующего настоящему изобретению, на котором показаны электроды в полностью отведенном положении.
Фиг. 10а - вид с торца (по линии 10а-10а, показанной на фиг.10) рабочего конца катетера третьего варианта осуществления, соответствующего настоящему изобретению.
Фиг. 11 - сечение рабочего конца катетера третьего варианта осуществления, соответствующего настоящему изобретению, на котором показаны электроды в полностью развернутом положении.
Фиг. 11А - вид с торца (по линии 11а-11а, показанной на фиг.11) рабочего конца катетера третьего варианта осуществления изобретения с полностью развернутыми электродами.
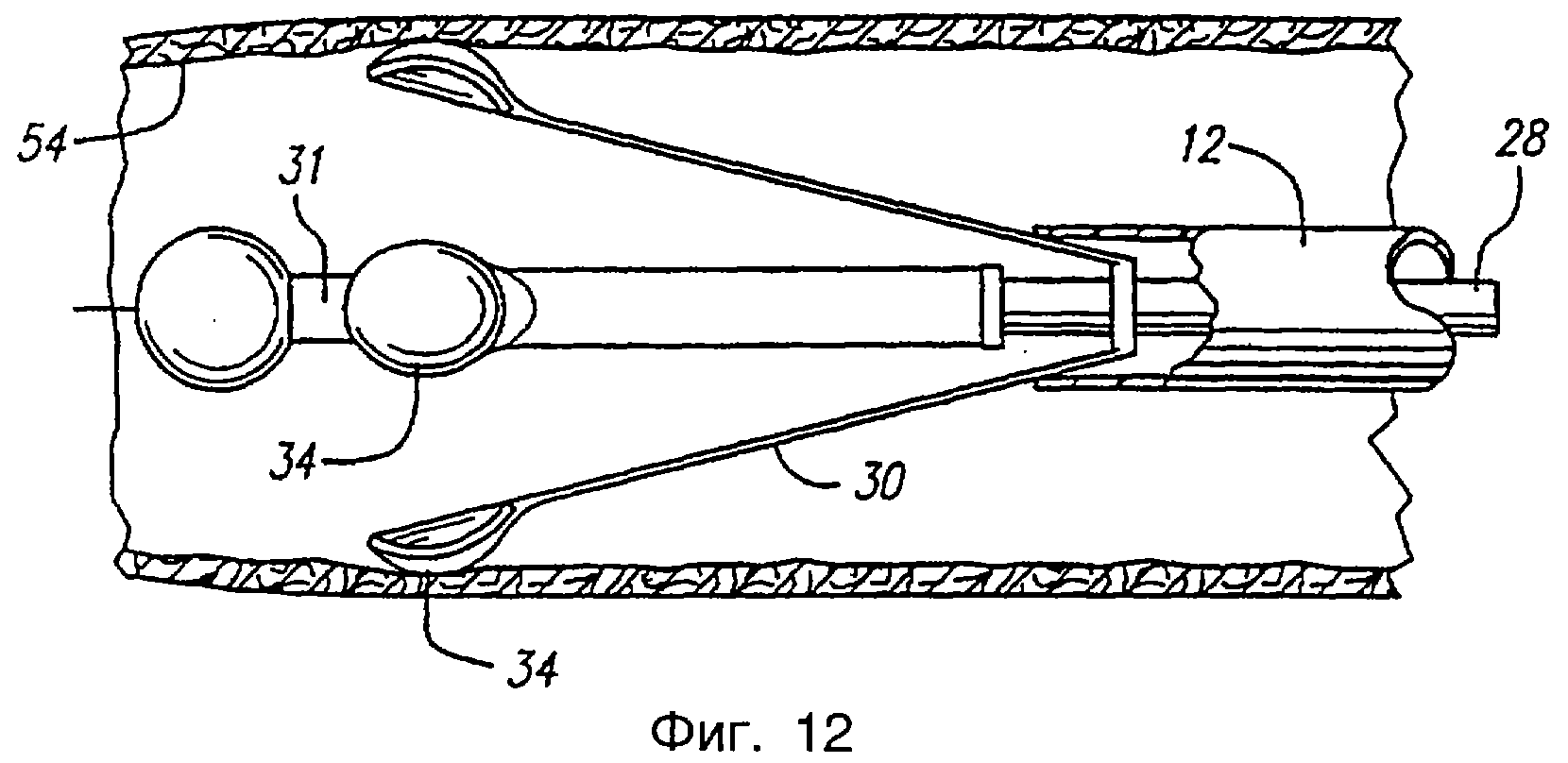
Фиг.12 - сечение анатомической структуры, содержащей катетер, показанный на фиг. 10, с электродами, находящимися в контактном взаимодействии с анатомической структурой.
Фиг.13 - сечение анатомической структуры, содержащей катетер, показанный на фиг.10, где анатомическую структуру лигируют путем подачи энергии от электродов.
Фиг.14 - сечение анатомической структуры, содержащей катетер, показанный на фиг. 10, с электродами, находящимися в контактном взаимодействии с анатомической структурой, где для уменьшения диаметра полой структуры для выполнения лигирования структуры перед подачей энергии от электродов осуществляют наружное сжатие.
Фиг.15 - вид сбоку другого варианта осуществления электродного катетера, имеющего баллон и коаксиальный жидкостной канал.
Фиг.16 - вид баллона и катетера, показанного на фиг.15, на котором показаны отверстия для надувания баллона, образованные в оболочке катетера, предназначенной для надувания, а также надувная полость, которая сообщается с отверстиями для надувания.
Фиг. 17 - сечение анатомической структуры, содержащей другой вариант осуществления катетера, соответствующего настоящему изобретению, имеющего баллон, расположенный вблизи поддающихся изгибу фиксирующих рычагов с электродами.
Фиг.18 - вид сбоку другого варианта осуществления электродного катетера, имеющего оболочку, перекрывающую развертываемые выводы электродов, выдвинутые из катетера.
Фиг.19 - вид сбоку другого варианта осуществления электродного катетера, имеющего баллон и коаксиальный жидкостной канал, расположенный вблизи выводов, поддающихся развертыванию, причем баллон имеет отверстия для приема крови для поддержания развертывания баллона.
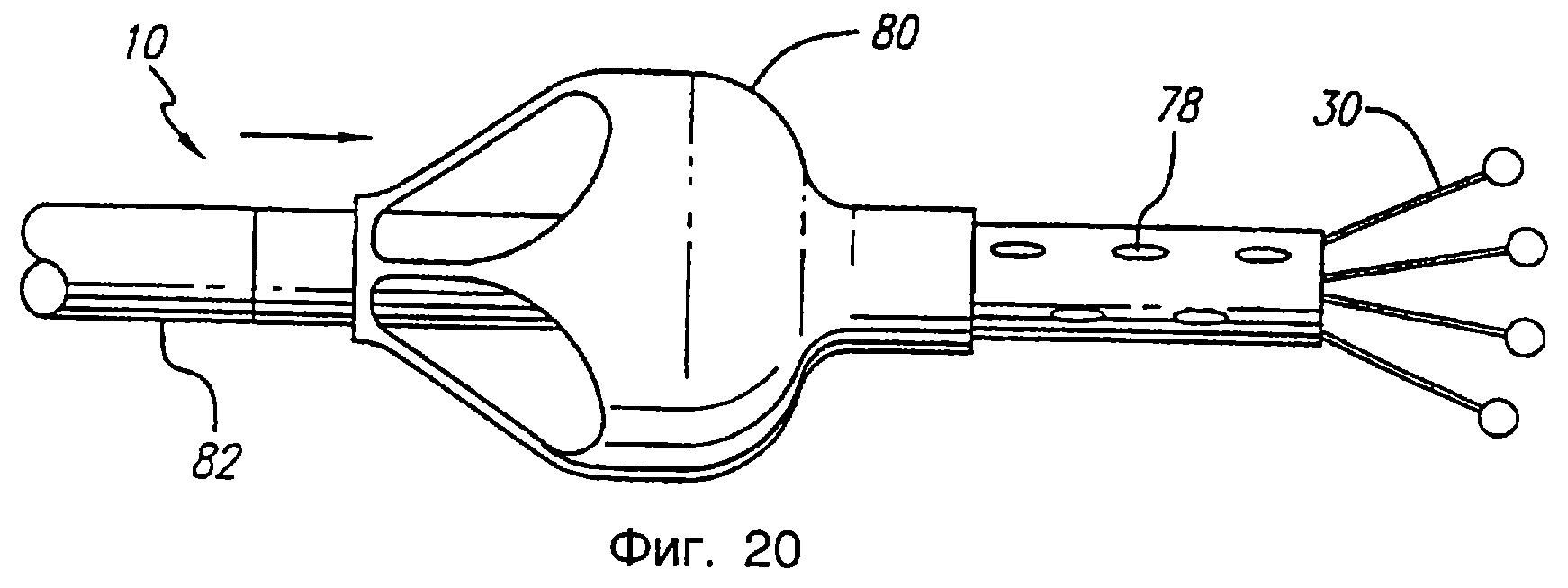
Фиг.20 - вид сбоку другого варианта осуществления электродного катетера, имеющего баллон и коаксиальный жидкостной канал, расположенный вблизи выводов, поддающихся развертыванию, причем баллон имеет отверстия для приема крови для поддержания развертывания баллона.
Фиг.21 - вид сбоку (с частичным разрезом) другого варианта осуществления электродного катетера, имеющего секцию, поддающуюся расширению.
Фиг. 22 - вид сбоку (с частичным разрезом) варианта осуществления электродного катетера, показанного на фиг.21, в расширенном состоянии.
Фиг. 23 - вид сбоку варианта осуществления электродного катетера, имеющего два множества отстоящих в продольном направлении друг от друга и поддающихся развертыванию электродов в отведенном состоянии.
Фиг. 24 - вид сбоку варианта осуществления электродного катетера, показанного на фиг.23, с обеими множествами электродов, находящимися в развернутом состоянии.
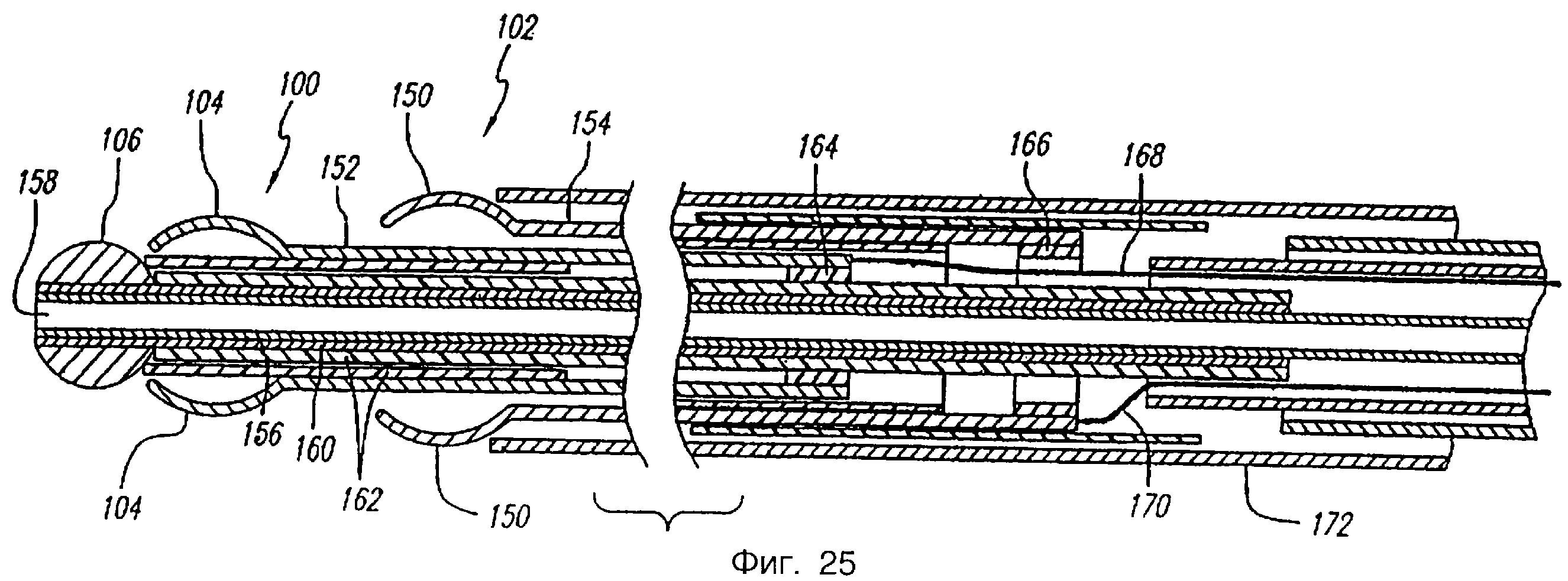
Фиг. 25 - частичный разрез варианта осуществления электродного катетера, показанного на фиг.23.
Фиг.26 - вид сбоку другого варианта осуществления электродного катетера, имеющего два множества отстоящих в продольном направлении друг от друга и поддающихся развертыванию электродов в отведенном состоянии.
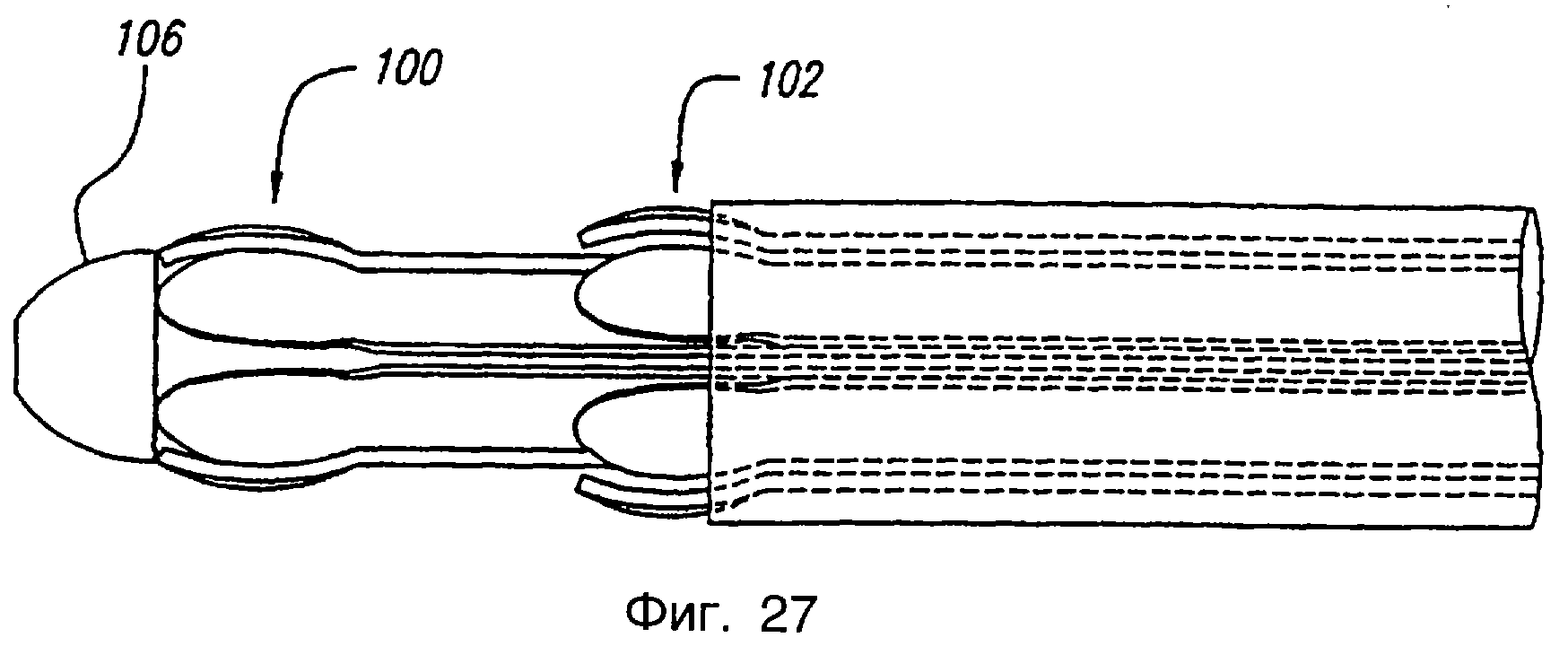
Фиг.27 - вид сбоку другого варианта осуществления электродного катетера, имеющего два множества отстоящих в продольном направлении друг от друга и поддающихся развертыванию электродов в отведенном состоянии.
Фиг.28 - вид сбоку другого варианта осуществления электродного катетера, имеющего два множества отстоящих в продольном направлении друг от друга и поддающихся развертыванию электродов в отведенном состоянии.
Фиг. 29 - вид катетера, применяемого в способе, соответствующем настоящему изобретению, для обработки геморроидального узла.
Фиг. 30 - вид катетера, применяемого в способе, соответствующем настоящему изобретению, для обработки эзофагеального варикозно-расширенного сосуда.
Фиг. 31 - вид катетера, применяемого в способе, соответствующем настоящему изобретению, для лигирования фаллопиевой трубы.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
На приведенных чертежах аналогичными ссылочными номерами указаны аналогичные или
соответствующие элементы. На фиг.1 показан катетер 10, предназначенный для подачи энергии к анатомической структуре, например к вене. Катетер 10 содержит внешний корпус 12, имеющий на своем рабочем
конце 15 дальнее отверстие 14. Соединительный конец 17 внешнего корпуса 12 прикреплен к рукоятке 16, которая содержит электрический соединитель 18, предназначенный для сопряжения с источником 22
питания, как правило, высокочастотным генератором, и микропроцессорным контроллером 23. Источник 22 питания и микропроцессор 23, как правило, смонтированы в одном блоке. Контроллер 23 регулирует
источник 22 питания в ответ на команды извне и данные, поступающие от датчика, например, термопары, расположенного в зоне внутриполостной обработки вены. В другом варианте осуществления пользователь
может выбрать постоянную выходную мощность так, чтобы не было автоматического регулирования температуры, а пользователь мог вручную регулировать выходную мощность, принимая во внимание значение
температуры, отображаемое на дисплее. Катетер 10 содержит поддающееся развертыванию электродное приспособление 24 (показанное частично), которое входит в и выходит из внешнего корпуса 12 через дальнее
отверстие 14. Электродное приспособление содержит множество электродов, которые могут быть развернуты путем перемещения электродов в стержне, или путем перемещения внешнего корпуса относительно
электродов. Хотя на фиг.1 иллюстрируется множество электродов, окружающих один центральный электрод, для такого катетера будут описаны другие электродные конфигурации.
Во внешнем корпусе 12 расположен внутренний корпус 28 или внутренний элемент. Жидкостной канал 21 сообщается с внутренней областью наружного корпуса 12. Катетер 10 может периодически промываться через канал 21 напором струи солевого раствора. Промывочный раствор может проходить между внешним и внутренним корпусами. Этот канал обеспечивает также возможность подачи лекарственных препаратов при лечении лекарственными средствами. Промывка катетера предотвращает накопление в катетере 10 биологической жидкости, например крови. Зона обработки полой анатомической структуры, например, вены, может быть промыта напором струи, например, солевого раствора или диэлектрической жидкости, для удаления крови из зоны обработки вены так, чтобы препятствовать образованию коагулянта или тромба. Применение диэлектрической жидкости может минимизировать непреднамеренный отвод тепла из зоны обработки. Диэлектрическая жидкость препятствует утечкам тока высокочастотной энергии из стенки вены.
Катетер 10, соответствующий одному варианту настоящего изобретения, содержит полость, которая начинается на дальнем конце внешнего корпуса 12, проходит по существу вдоль оси внешнего корпуса 12 и заканчивается у канала 20 проволочного направителя рукоятки 16. Проволочный направитель может быть введен через полость катетера 10 для использования при направлении катетера к требуемому участку обработки. Если катетер имеет небольшие размеры и предназначен для обработки небольших вен, то внешний диаметр катетера может не позволять промывку напором струи жидкости, подаваемой между внешним корпусом 12 и внутренним корпусом 28. Однако в таком варианте осуществления промывочная жидкость может быть введена через полость для проволочного направителя.
Как следует из чертежей, представленных на фиг. 2, 2а, 3, 4, 4а и 5, внешний корпус 12 содержит оболочку 44 и наконечник 46. Для обеспечения атравматического наконечника для катетера 10, когда им манипулируют в вене, наконечник 46 предпочтительно имеет сужение на дальнем конце или имеет форму "носового конуса". Однако наконечник 46 может иметь другие формы, которые облегчают продвижение катетера 10 по проволочному направителю и через изгибы в венозной васкулярной системе. Например, наконечник 46 в форме носового конуса может быть выполнен из полимера, имеющего невысокую твердость, составляющую, например, 70 единиц при измерении твердости по методике Шора. Оболочка 44 выполнена из биосовместимого материала, имеющего низкий коэффициент трения. В одной конфигурации, внешний корпус 12 имеет такие размеры, чтобы применяться в полости вены, соответствующие, например, размеру 5-9 френч, что соответствует диаметру, размеры которого соответствуют 1,7 мм (0,07 дюйма)-3,0 мм (1,2 дюйма), или другие соответствующие размеры.
Электродное приспособление 24 имеет некоторое количество выводов, включающих в себя изолированные первичные выводы 30 и в некоторых вариантах осуществления вторичный вывод 31. Предпочтительно, чтобы выводы были соединены с источником 22 питания, как показано на фиг.1, так, чтобы полярность выводов могла быть при желании изменена. В альтернативном варианте для изменения полярности, а также для регулирования мощности электродного приспособления может быть использован микропроцессорный контроллер. Таким образом, электродное приспособление может работать либо в биполярной, либо в монополярной конфигурации. Если смежные первичные выводы 30 имеют противоположную полярность, то электродное приспособление 24 работает как биполярное электродное приспособление. Если первичные выводы 30 имеют одну полярность, то электродное приспособление 24 может работать как монополярное электродное приспособление. Если первичные выводы 30 имеют общий заряд, а вторичный вывод 31 имеет противоположную полярность, то электродное приспособление 24 работает как биполярное электродное приспособление. Вариант осуществления, соответствующий настоящему изобретению, показанный на фиг.2 и 3, содержит электродное приспособление 24, имеющее четыре первичных вывода 30 и вторичный вывод 31, тогда как вариант осуществления, соответствующий настоящему изобретению, показанный на фиг.4 и 5, содержит электродное приспособление 24, имеющее только четыре первичных вывода. Устройство, соответствующее настоящему изобретению, не ограничено четырьмя первичными выводами 30, поскольку в любом варианте осуществления может быть использовано больше или меньше выводов. Число выводов может зависеть от размера или диаметра полой анатомической структуры, подлежащей обработке. Приложенные электроды должны поддерживаться на некотором расстоянии друг от друга. Сосуды большего размера могут потребовать больше первичных выводов для того, чтобы гарантировать должную плотность тока и должное распределение тепла.
Для обнажения проводящего провода на дальнем конце 32, 33 может быть удалена изоляция на каждом из выводов 30, 31. В первой конфигурации, показанной на фиг. 2, 2а и 3, каждый электрод 34 имеет форму полусферы. Во второй конфигурации электрод может иметь в общем сферическую форму или форму ложки. Как показано на фиг. 4, 4а и 5, электроды имеют форму ложки, которая при сведении электродов вместе может приводить к образованию сферы или другой формы так, чтобы минимизировать профиль при спадении стенок вены. Электроды 34 либо образованы интегрально на дальнем конце 32, припаяны мягким припоем, либо иначе получены на дальнем конце каждого первичного вывода 30. Должно быть очевидным, что, если дальний конец 32 должен работать как электрод, то это не ограничивает то, где на дальнем конце 32 интегрально образован электрод 34. Например, дальний конец может подавать энергию к окружающей ткани, где имеется электрод, интегрально образованный на дальнем конце, или где электрод отдельно припаян мягким припоем к дальнему концу, или где имеется другое устройство для подачи энергии, расположенное на дальнем конце. Как правило, электрод 34 имеет диаметр, который больше диаметра первичного вывода 30. Например, первичный вывод 30 может иметь диаметр в диапазоне от 0,18 мм (0,007 дюйма) до 0,28 мм (0,011 дюйма), тогда как электрод 34 имеет диаметр от 0,36 мм (0,014 дюйма) до 0,51 мм (0,020 дюйма). Первичные выводы 30 и электроды 34 предпочтительно выполнены из биологически совместимого материала, например из нержавеющей стали. Изоляция, окружающая первичные выводы 30, как правило, имеет толщину в диапазоне от 0,03 мм (0,001 дюйма) до 0,06 мм (0,0025 дюйма), приводя в результате к общему диаметру изолированного вывода, составляющему от 0,23 мм (0,009 дюйма) до 0,41 мм (0,016 дюйма). В альтернативной конфигурации, как показано на фиг.2 и 3, каждый первичный вывод 30 имеет форму полосы шириной от 0,76 мм (0,03 дюйма) до 1,0 мм (0,04 дюйма) и толщиной приблизительно 0,13 мм (0,005 дюйма), тогда как вторичный вывод 31 имеет, как правило, трубчатую форму. Необходимо отметить, что эти размеры указаны только с целью иллюстрации, а не для ограничения настоящего изобретения. Полусферический электрод 34 получают на дальнем конце, например, посредством пескоструйной очистки шестнадцатидюймовой сферы (диаметром 1, 6 мм), которую припаивают мягким припоем к дальнему концу 32 первичного вывода 30. Электроды требуемой формы или конфигурации могут быть получены штамповкой проводящего вывода. Электрод выполняют интегрально с выводом, а остальную часть вывода изолируют. Дальний конец 33 вторичного вывода 31 предпочтительно содержит электрод 35, как правило, сферической формы.
Выравнивающее устройство 36 располагает выводы 30, 31 так, чтобы они были соединены с катетером только ближними концами и так, чтобы между выводами поддерживалось разделение. При монтаже на выравнивающем устройстве выводы могут образовывать консоли. Предпочтительная конфигурация выравнивающего устройства 36 содержит множество смещенных от центра, проходящих в осевом направлении, полостей 38, которые по существу расположены симметрично относительно оси выравнивающего устройства 36. Выравнивающее устройство 36 получают, например, путем экструзии множества, проходящих в осевом направлении, полостей 38 в цельном цилиндре, выполненном из диэлектрического материала, например полиамида. Каждый вывод 30 проходит через отдельную, смещенную от центра, полость 38 и выходит из задней стороны выравнивающего устройства 36. Выравнивающее устройство 36 может дополнительно содержать центральную полость 48, которая может быть совмещена с осью. В некоторых вариантах осуществления настоящего изобретения центральную полость 48 используют для пропускания через нее проволочного направителя или для подачи или перфузии лекарственного препарата и охлаждающего раствора к зоне обработки в течение подачи высокочастотной энергии. В других вариантах осуществления центральная полость 48 может быть использована для вторичного вывода 31. Выравнивающее устройство 36 может также дополнительно содержать вспомогательную полость 47 для дополнительных выводов, например выводов термопары, используемой в качестве датчика температуры. Для предотвращения или минимизации образования каких-либо связей, которые могут возникнуть между выводами 30, 31 и с проволочным направителем, при его наличии, выравнивающее устройство 36 выполнено из диэлектрического материала. В одном варианте осуществления длина выравнивающего устройства составляет, например, от 12,5 мм (0,5 дюйма) до 19,0 мм (0,75 дюйма). Однако эти размеры приведены только для иллюстрации, а не для ограничения настоящего изобретения.
В варианте осуществления настоящего изобретения, показанном на фиг. 2, 2а и 3, внутренний корпус 28 прикреплен к выравнивающему устройству 36 и проходит за заднюю сторону 37 выравнивающего устройства. Предпочтительно, чтобы внутренний корпус 28 полностью окружал внешнюю стенку выравнивающего устройства 36 и был смонтирован на нем посредством адгезива или прессовой посадки или другим способом так, чтобы оно оставалось в неподвижном положении относительно внутреннего корпуса. Внутренний корпус 28 выполнен из биосовместимого материала с низким коэффициентом трения. Внутренний корпус 28 обеспечивает проход для межсоединения между выводами 30, 31 и электрическим соединителем 18 (фиг.1). Это межсоединение может быть осуществлено любым из нескольких способов. Выводы 30, 31 сами по себе могут быть непрерывными и проходить по всей длине внутреннего корпуса 28. В альтернативном (не показанном) варианте осуществления выводы 30, 31, на которые подается положительный потенциал, могут соединяться с общим проводом, несущим положительный потенциал, расположенным во внутреннем корпусе 28. Аналогичным образом, выводы 30, 31, на которые подается отрицательный потенциал, могут соединяться с общим проводом, несущим отрицательный потенциал. Предпочтительно, чтобы выводы 30, 31 были соединены с проводом, который позволяет изменять полярность выводов. Такой провод может содержать, например 36-жильный медный вывод с полиуретановым покрытием. Соединение может иметь место в любой точке во внутреннем корпусе 28. Для уменьшения величины провода, находящегося в катетере, предпочтительно соединять выводы 30, 31 в точке, в которой выводы выходят из задней стороны 37 выравнивающего устройства 36. Для дополнительного увеличения стабильности электродного приспособления 24 предпочтительно, чтобы связующий материал 40 окружал выводы 30, 31 на переднем конце выравнивающего устройства 36. В этом варианте осуществления настоящего изобретения выводы 30, 31 выходят через дальнее отверстие 14, когда внешний корпус 12 отведен назад поверх выравнивающего устройства 36. Сужающийся наконечник 46 препятствует движению отведения внешнего корпуса 12 для предотвращения обнажения выравнивающего устройства 36.
На фиг. 3 показаны выводы 30 и 31 в отведенном положении, в котором все выводы находятся в наконечнике 46, имеющем форму носового конуса, и во внешней оболочке. Выравнивающее устройство 36 смещено относительно внешней оболочки 44. Мягкий носовой конус обеспечивает получение атравматического наконечника, что необходимо для безопасного маневрирования катетера в извилистой венозной системе. Электрод на дальнем конце вторичного вывода 31 может иметь размер, который приблизительно равен размеру отверстия, образованного в носовом конусе 46. При отведении выравнивающего устройства во внешний корпус катетера, носовой конус вместе с электродом вторичного вывода образует закрытый атравматический наконечник. Такой наконечник может быть атравматическим даже в том случае, если носовой конус не изготовлен из мягкого материала.
Как следует из фиг.4 и 5, на которых показан другой вариант осуществления настоящего изобретения, выравнивающее устройство 36 соединено с внешним корпусом 12 и в соответствии с этим остается неподвижным относительно него. Внутренний корпус 28 смонтирован с возможностью перемещения сзади выравнивающего устройства 36 и в этом случае также обеспечивает проход для межсоединения между первичными выводами 30 и электрическим соединителем 18 (фиг.1). В некоторых вариантах осуществления внутренний корпус 28 содержит трубку 49 для проволочного направителя, которая проходит по всей длине внутреннего корпуса. Трубка 49 для проволочного направителя для обеспечения сообщения совмещена на одном конце с центральной полостью 48 выравнивающего устройства 36, а на другом конце - с каналом 20 проволочного направителя (фиг. 1). Первичные выводы 30 могут быть непрерывными и проходить по всей длине внутреннего корпуса 28 или они могут быть соединены с общими выводами, как было описано ранее. Первичные выводы 30 закреплены на переднем конце внутреннего корпуса 28, например, посредством герметика 50, так, чтобы перемещение внутреннего корпуса 28 приводило в результате к соответствующему перемещению первичных выводов 30 через полости 38 выравнивающего устройства 36. В этом варианте осуществления первичные выводы 30 не закреплены на выравнивающем устройстве 36 и по существу являются выводами, свободно плавающими в осевом направлении. Первичные выводы 30 перемещаются через выравнивающее устройство 36 и выходят через дальнее отверстие 14, когда передний конец внутреннего корпуса 28 перемещается к задней стороне 37 выравнивающего устройства 36.
В вышеописанных вариантах осуществления настоящего изобретения первичные выводы 30 образованы, например, дугообразными или изогнутыми, для их движения в направлении друг от друга и благодаря этому для предотвращения контактного взаимодействия между собой. "Дальней частью" первичных выводов 30 является часть вывода, которая проходит от переднего конца выравнивающего устройства 36, когда выводы полностью выдвинуты через дальнее отверстие 14. Предпочтительно, чтобы дальние части 42 были образованы так, чтобы они перемещались в радиальном направлении наружу друг от друга относительно оси выравнивающего устройства 36 и образовывали симметричную конструкцию. Это обеспечивается в обоих вариантах осуществления настоящего изобретения, показанных на фиг. 2а и 4а. Величина кривизны или изгиба первичных выводов 30 может быть любой, но которой достаточно для отклонения выводов в радиальном направлении, когда они выходят из внешнего корпуса 12 через дальнее отверстие 14. Существенно, чтобы величина кривизны или изгиба была достаточной, чтобы обеспечивать достаточное усилие для отклонения первичных выводов 30 через кровь и для приведения электродов 34 в контактное взаимодействие со стенкой вены. Чтобы гарантировать полный контакт предпочтительно, чтобы электроды частично внедрялись в стенку вены. Для достижения контактного взаимодействия всей поверхности так, чтобы для эффективного распределения тока, вся неизолированная площадь поверхности электрода приходила в контактное взаимодействие с венозной тканью, скругленная часть электрода внедряется в стенку вены. Предпочтительно, чтобы площадь поверхности электродов, находящихся в контактном взаимодействии с венозной тканью, была достаточна для предотвращения высокой плотности тока, которая может привести к местному перегреву венозной ткани. Предпочтительно, чтобы тепло от нагрева было равномерно распределено вдоль кольцевой полосы вены. Расположенные бок о бок электроды должны отстоять друг от друга не более, чем на 4 или 5 мм по длине окружности вены. Таким образом, расположение электродов должно соответствовать размеру или диаметру обрабатываемой вены. Другие свойства первичных выводов 30, например форма выводов и толщина изоляции, оказывают влияние на силу прижима вывода и величина кривизны или изгиба должна быть отрегулирована для компенсации этих факторов. Например, в одной конфигурации электродного приспособления 24 провод, имеющий диаметр от 0,18 мм (0,007 дюйма) до 0,28 мм (0,011 дюйма) при общей толщине изоляции от 0,05 мм (0,002 дюйма) до 0,13 мм (0,005 дюйма), изгибают на острый угол для обеспечения достаточного контактного взаимодействия с анатомической структурой. Очевидно, что эти размеры приведены только для иллюстрации, а не для ограничения настоящего изобретения.
Возможны другие технологии развертывания выводов в направлении наружу, как только они выходят из рабочего конца катетера. Например, выводы могут быть прямолинейными, но смонтированными в выравнивающем устройстве под углом так, чтобы они были нормально ориентированы в направлении наружу.
Для большей величины прикладываемых сил предпочтительно, чтобы первичные выводы 30 имели конфигурацию полосы прямоугольного поперечного сечения, имеющего, например, ширину от 0,76 мм (0,030 дюйма) до 1,0 мм (0,039 дюйма) и толщину приблизительно 0,13 мм (0,005 дюйма). Прямоугольное поперечное сечение обеспечивает повышенное сопротивление изгибу в направлении ширины и позволяет более свободно изгибаться выводу в направлении толщины. Такая полосообразная конфигурация первичных выводов 30 показана на фиг. 2, 2а и 3, которая обеспечивает повышенную стабильность в боковом направлении, позволяя в то же самое время изгиб в радиальном направлении. Как показано на фиг. 2, 2а и 3, каждый первичный вывод имеет прямоугольное поперечное сечение и смонтирован относительно катетера так, чтобы более тонкий элемент прямоугольного поперечного сечения совмещался с направлением развертывания вывода. Выводы менее вероятно изгибаются вбок, когда развертываются в направлении наружу, и между выводами гарантируется более равномерное расстояние. Равномерное расстояние обеспечивает равномерный нагрев вокруг венозной ткани, которая находится в контактном взаимодействии с электродами на дальних концах выводов.
Длина дальней части выводов 30 также оказывает влияние на конфигурацию электродного приспособления 24. На максимальное расстояние между двумя взаимно противоположными электродами 34, то есть эффективный диаметр электродного приспособления 24, оказывает влияние величина изгиба и длина дальней части 42. Чем больше длина дальней части 42, тем больше диаметр электродного приспособления 24. В соответствии с этим катетер 10 может быть использован для применения в анатомических структурах, имеющих разные размеры, путем изменения длины дальней части 42 и степени изгиба.
Катетеры могут иметь разное число выводов 30, 31. Число выводов 30, 31 ограничено диаметром выравнивающего устройства 36 и числом полостей 36, 38, 47, которые могут быть экструдированы через выравнивающее устройство. В случае биполярной конфигурации, для образования некоторого количества противоположно заряженных электродных пар предпочтительно четное число первичных выводов 30. Электроды, находящиеся в контактном взаимодействии с анатомической структурой, должны поддерживаться на некотором расстоянии друг от друга. В случае монополярной конфигурации может иметь место любое число одинаково заряженных выводов 30. В монополярной конфигурации распределение высокочастотной энергии в анатомической ткани получают созданием пути возврата для тока через ткань путем обеспечения устройства возврата в точке, находящейся вне ткани, например большой металлической подушки.
Как следует из фиг.1, исполнительный механизм 25 контролирует выдвижение электродного приспособления 24
через дальнее отверстие 14. Исполнительный механизм 25 может принимать форму переключателя, рычага, снабженной резьбой ручки управления или другого соответствующего пригодного механизма, и
предпочтительно может обеспечивать точное регулирование перемещения наружного корпуса 12 или внутреннего корпуса 28 в зависимости от особенностей используемой конструкции. В одном варианте
осуществления настоящего изобретения, исполнительный механизм 25 (фиг.1) сопряжен с внешним корпусом 12 (фиг.2, 2а и 3) для перемещения его назад и вперед
относительно внутреннего корпуса 28.
В другом варианте осуществления исполнительный механизм 25 (фиг.1) сопряжен с внутренним корпусом 28 (фиг. 4, 4а и 5) для перемещения его назад и вперед относительно внешнего корпуса 12. Таким образом
регулируется относительное положение внешнего и внутреннего корпусов, но могут быть использованы и другие способы регулирования.
Как следует из фиг. 2, 2а, 3, 4, 4а и 5, катетер 10 содержит датчик 26 температуры, например термопару. Датчик 26 температуры смонтирован на электроде 34 так, чтобы датчик 26 находился вблизи или по существу заподлицо с обнаженной поверхностью электрода 34. Датчик 26 показан на приведенных чертежах выступающим из электродов только для ясности иллюстрации. Датчик 26 измеряет температуру части анатомической ткани, которая находится в контактном взаимодействии с обнаженной поверхностью электрода. Контроль температуры анатомической ткани обеспечивает хорошее указание на то, готово ли начаться сокращение ткани. Датчик 26 температуры, расположенный на электроде, обращенном к анатомической ткани, обеспечивает показание того, когда сокращение имеет место (70oС или более) и когда на электродах может начаться образование значительного количества коагулянта. Следовательно, поддержание температуры выше 70oС дает терапевтическое сокращение анатомической структуры. Подачу высокочастотной энергии от электродов 34 поддерживают или уменьшают, если контролируемая температура достигает или превышает определенную температуру, которая была выбрана оператором, как правило, температуру, при которой начинается каутеризация анатомической ткани. Датчик 26 температуры сопряжен с контроллером 23 (фиг.1) через пару выводов 45 датчика, которые предпочтительно проходят через вспомогательную полость 47 и затем через внутренний корпус 28. Сигналы от датчика 26 температуры поступают в контроллер 23, который регулирует величину высокочастотной энергии, подаваемой на электроды 34 в соответствии с выбранными температурными критериями и контролируемой температурой. В автоматизированной системе, которая, если обнаружено достаточное сокращение вены или для предотвращения перегрева вены, отключает или регулирует подачу высокочастотной энергии электродами к участку вены, могут быть использованы другие технологии, например, текущий контроль импеданса или эхо-контроль ультразвуковых импульсов. Импеданс может быть использован для обнаружения начала образования коагулянта.
На фиг. 6, 6а и 7а-7с показано введение одного катетера 10 варианта осуществления, соответствующего настоящему изобретению, в полую анатомическую структуру, например в вену 52, в процессе работы. Этот катетер аналогичен варианту осуществления, описанному со ссылкой на фиг.2 и 3. Катетер 10 дополнительно содержит наружную оболочку 60, через которую к месту обработки может быть подана жидкость. В этом варианте осуществления жидкостной канал (не показан) сообщается с внутренней областью наружной оболочки 60 и внешнего корпуса 12. Наружная оболочка 60 окружает внешний корпус 12 для образования коаксиального канала, через который может впрыскиваться жидкость.
Для направления катетера в определенное место и подтверждения его положения в вене может быть использована технология получения изображения с помощью рентгеноскопии, ультразвука, капилляроскопа или другая технология. После этого для смещения внешнего корпуса относительно внутреннего (для обнажения выводов 30, 31 через дальнее отверстие 14), либо путем отведения внешнего корпуса 12 назад, либо путем перемещения внутреннего корпуса 28 вперед, управляют исполнительным механизмом (не показан). Когда выводы 30, 31 выходят из дальнего отверстия 14, первичные выводы развертываются в радиальном направлении наружу относительно оси выравнивающего устройства 36, тогда как вторичный вывод 31 остается по существу линейным. Первичные выводы 30 продолжают двигаться в направлении наружу до тех пор, пока не будет иметь место контактное взаимодействие со стенкой 54 стенки, и движение первичных выводов 30 в направлении наружу затормозится. Первичные выводы 30 вступают в контактное взаимодействие с веной вдоль, как правило, кольцевой полосы стенки 54 вены. Такое движение первичных выводов 30 в направлении наружу осуществляется по существу симметрично. В результате этого электроды 34 первичных выводов по существу равномерно отстоят друг от друга вдоль кольцевой полосы стенки 54 вены. Электрод 35 центрального вывода подвешен в вене 52 без контактного взаимодействия со стенкой вены.
При позиционировании электродов 34 в месте обработки вены для подачи соответствующей высокочастотной энергии приводят в действие источник 22 питания. Одной из приемлемых частот является частота 510 кГц. Одним критерием, используемым при выборе частоты подаваемой энергии, является требуемый контроль распространения, предусматривающий глубину теплового эффекта в венозной ткани. Другим критерием является совместимость с фильтрами, исключающими высокочастотные помехи из сигналов термопары.
При работе в биполярной конфигурации первичные выводы 30 первоначально заряжают так, чтобы смежные выводы были заряжены противоположно, тогда как вторичный вывод является электрически нейтральным. Эти множественные пары противоположно заряженных выводов 30 образуют активные электродные пары для формирования между ними высокочастотного поля. Таким образом, вдоль кольцевой полосы стенки 54 вены образуются дискретные высокочастотные поля. Эти дискретные поля образуют симметричную конфигурацию высокочастотного поля вдоль всей кольцевой полосы стенки 54 вены, когда смежные электроды 34 противоположной полярности формируют между собой высокочастотные поля. Вдоль стенки вены, подлежащей обработке, может быть достигнуто равномерное распределение температуры.
Высокочастотная энергия преобразуется в смежной венозной ткани в тепло и этот тепловой эффект побуждает венозную ткань сокращаться, уменьшая диаметр вены. Равномерное распределение температуры вдоль обрабатываемой стенки вены предотвращает образование участков местного перегрева в зоне обработки, способствуя в то же самое время контролируемому уменьшению диаметра вены. Тепловой эффект способствует структурному преобразования волокон коллагена в вене. В ответ на тепло от теплового эффекта волокна коллагена укорачиваются и утолщаются в поперечном сечении. Как показано на фиг.7а, подаваемая энергия побуждает стенку 54 вены спадать вокруг электродов 34 первичных выводов. Благодаря сокращению стенки 54 вены, электроды все более и более сближаются до тех пор, пока они не придут в соприкосновение и в этой точке ограничивается дополнительное спадение или лигирование стенки 54. При спадении стенки 54 вены вокруг электродов 34 первичных выводов полярность электродов первичных выводов изменяют так, чтобы электроды первичных выводов были одинаково заряжены. Не обязательно, чтобы изменение полярности выводов осуществлялось мгновенно. Подача высокочастотной энергии может быть прекращена, полярность изменена и после этого при измененной полярности снова подают высокочастотную энергию. После этого электрод 35 вторичного вывода заряжают так, чтобы его полярность была противоположна полярности электродов 34 первичных выводов. Между электродами 34 первичных выводов и электродом 35 вторичного вывода устанавливается высокочастотное поле.
Затем катетер 10 отводят назад, подавая в то же самое время энергию к электродному приспособлению. Как показано на фиг.7b, во время отведения катетера 10 назад электроды 34 первичных выводов остаются в контактном взаимодействии со стенкой 54 вены, тогда как электрод 35 вторичного вывода приходит в контакт с участком стенки вены, предварительно спавшей, благодаря воздействию посредством электродов 34 первичных выводов. В соответствии с этим, высокочастотная энергия проходит через стенку 54 вены между электродами 34 первичных выводов и электродом 35 вторичного вывода и стенка вены продолжает спадать вокруг электрода 35 вторичного вывода при отведении катетера 10. Как показано на фиг.7с, лигирование в соответствии с этим способом приводит в результате к окклюзии вдоль длины вены 52. Протяженная окклюзия в противоположность резкой окклюзии более сильна и менее чувствительна к восстановлению просвета вены.
Аналогичный результат получают, когда катетер 10, имеющий как первичные, так и вторичный выводы, работает в монополярной конфигурации. При работе в монополярной конфигурации электрод 35 вторичного вывода остается нейтральным, тогда как первичные выводы 30 заряжаются, как обычно, и действуют в связи с независимым электрическим устройством, например, большой возвратной подушкой (не показана), имеющей низкий импеданс, расположенной в наружном контакте с телом пациента для образования ряда дискретных высокочастотных полей. Эти высокочастотные поля по существу одинаково отстоят друг от друга по длине окружности вены и проходят вдоль аксиального участка стенки вены, побуждая стенку вены спадать вокруг электродов первичных выводов. При спадении стенки вены электрод вторичного вывода заряжают так, чтобы он имел ту же полярность, что и электроды первичных выводов. Электродное приспособление отводят и стенка вены спадает так, как описано при работе в биполярной конфигурации.
При работе как в биполярном, так и в монополярной конфигурации подача высокочастотной энергии по существу симметрично распределена по стенке вены независимо от диаметра вены 52. Такое симметричное распределение высокочастотной энергии увеличивает предсказуемость и равномерность сокращения и эффективность окклюзии. Кроме того, равномерное распределение энергии позволяет подавать высокочастотную энергию в течение короткого промежутка времени и в соответствии с этим уменьшает или предотвращает образование на электродах 34 коагулянта, вызываемое нагревом. Для дополнительного предотвращения нагрева окружающей крови выводы, включая невыпуклую внешнюю часть электрода, изолируют.
Жидкость может быть подана перед и в течение высокочастотного нагрева вены, подвергаемой обработке, через коаксиальный канал, образованный между наружной оболочкой 60 и внешним корпусом 12. Должно быть очевидно, что для подачи жидкости в место обработки в катетере может быть образована другая полость. Подаваемая жидкость вытесняет или выпускает кровь из вены так, чтобы избежать нагрева и коагуляции крови. Для предотвращения циркуляции крови назад к месту обработки жидкость может продолжать подаваться в течение высокочастотной обработки. Подача диэлектрической жидкости увеличивает окружающее полное электрическое сопротивление так, чтобы высокочастотная энергия направлялась в ткань стенки вены.
На фиг.8, 8а, 9а и 9b показана работа альтернативного варианта осуществления катетера 10, соответствующего настоящему изобретению, который может быть использован с проволочным направителем 53. Как и в предшествующем варианте осуществления, катетер 10 вводят в полую анатомическую структуру, например, в вену 52. Проволочный направитель 53 продвигают за зону, куда необходима подача энергии. После этого по проволочному направителю 53, проходящему через центральную полость 48 и трубку 49 для проволочного направителя, вводят катетер 10 и продвигают по проволочному направителю через вену к требуемой зоне. Перед подачей высокочастотной энергии к электродному приспособлению 24, проволочный направитель 53, как правило, отводят назад или удаляют.
После этого манипулируют исполнительным механизмом 25 (фиг.1) либо для отведения внешнего корпуса 12 назад, либо для продвижения внутреннего корпуса 28 вперед, для выдвижения выводов 30 через дальнее отверстие 14. Выводы 30 выходят из дальнего отверстия 14 и развертываются в радиальном направлении относительно оси выравнивающего устройства 36. Выводы 30 продолжают двигаться в направлении наружу до тех пор, пока не придут в контактное взаимодействие со стенкой 54 вены. Выводы 30 входят в контакт с веной вдоль, как правило, кольцевой полосы стенки 54 вены. Это движение выводов в направлении наружу осуществляется по существу в симметричной конфигурации. В результате такого движения электроды 34 по существу равномерно отстоят друг от друга вдоль кольцевой полосы стенки 54 вены. В альтернативном варианте осуществления электроды могут быть разнесены в шахматном порядке так, чтобы электроды не лежали вдоль одной плоскости. Например, смежные электроды могут выступать из катетера на другие расстояния так, чтобы при сведении электродов друг к другу достигался меньший профиль поперечного сечения.
При позиционировании электродов в зоне обработки вены, для обеспечения подачи соответствующей высокочастотной энергии к электродам 34 так, чтобы катетер 10 работал либо в биполярной, либо в монополярной конфигурации, как было описано выше, приводят в действие источник 22 питания. Как показано на фиг. 9а и 9b, подводимая энергия побуждает стенку 54 вены спадать вокруг электродов 34, заставляя выводы по существу выпрямляться, а электроды - собираться в группу. Стенка 54 продолжает спадать до тех пор, пока дальнейшее спадение не затормозится электродами 34 (фиг.9b). В этой точке подача энергии может прекратиться. Электроды могут иметь такую конфигурацию, чтобы при собирании вместе образовывать форму с уменьшенным профилем. Электроды могут быть также предназначены для образования формы уменьшенного профиля при их сближении друг с другом. Электроды могут быть также предназначены и быть изолированы для непрерывной подачи высокочастотной энергии после образования формы уменьшенного профиля, благодаря спадению стенки вены. Катетер 10 может отводиться назад для лигирования смежного венозного участка. При наличии датчика 26 температуры подача энергии может прекратиться до полного спадения стенки, если температура венозной ткани повышается выше допустимого уровня, ограничиваемого контроллером 23.
Если катетер содержит полость (не показана) для подачи жидкости, то жидкость может быть подана перед и в течение высокочастотного нагрева обрабатываемой вены. Для предотвращения коагуляции крови, жидкость может вытеснять кровь из зоны обработки в вену. Жидкость может быть диэлектрической средой. Жидкость может содержать коагулянт, например гепарин, который может химически препятствовать свертыванию крови в зоне обработки.
После завершения этой процедуры для выбранного участка вены исполнительный механизм побуждает первичные выводы возвращаться во внутреннюю область внешнего корпуса 12. Для изменения положения внешнего корпуса и внутреннего корпуса относительно друг друга, перемещают либо внешний корпус, либо внутренний корпус. Как только выводы 30 находятся во внешнем корпусе 12, катетер 10 может быть перемещен на другой участок вены, где повторяют операцию лигирования. При обработке всех участков вены катетер 10 удаляют из сосудистой сети. После этого зашивают место доступа к вене или прикладывают местное давление до тех пор, пока не будет контролироваться кровотечение.
На фиг.10 иллюстрируется другой вариант осуществления катетера, соответствующего настоящему изобретению. Внутренний элемент или внутренний корпус 28 содержится во внешнем корпусе 12. Внутренний корпус предпочтительно изготовлен из гибкого полимера, например полиимида, полиэтилена или нейлона, и может перемещаться по всей длине катетера. Для продвижения по извилистым каналам венозной системы, большая часть катетера должна быть гибкой. Поверх дальнего конца внутреннего корпуса 28 закреплена внутренняя трубка, имеющая расширяющийся дальний конец и круглую форму поперечного сечения. Внутренняя трубка имеет длину, составляющую предпочтительно не более приблизительно 20-30 мм. Внутренняя трубка действует как часть проводящего вторичного вывода 31. На внутреннюю трубку со стороны ее ближнего конца надет неизолированный проводящий сферический электрод 35. Расширяющийся дальний конец внутренней трубки препятствует сферическому электроду перемещаться за дальний конец внутренней трубки. Сферический электрод постоянно закреплен на внутренней трубке, например, посредством пайки мягким припоем, и не может перемещаться по трубке как вперед, так и назад. Большая часть или вся поверхность сферического электрода 35 остается неизолированной. Остальная часть внутренней трубки предпочтительно изолирована, так что сферический дальний конец может действовать как электрод. Например, внутренняя трубка может быть покрыта изоляционным материалом, в частности, париленом. Внутренняя полость внутренней трубки облицована внутренним корпусом 28, который прикреплен к расширяющемуся дальнему концу внутренней трубки посредством адгезива, например эпоксидной смолой.
Вторичный вывод 31 и сферический электрод 35 окружает множество первичных выводов 30, которые предпочтительно имеют форму плоских прямоугольных полос и могут действовать как рычаги. Как показано на фиг.11, множество первичных выводов предпочтительно соединено с общими проводящими кольцами 62. Такая конфигурация поддерживает положение множества первичных выводов, уменьшая в то же самое время число внутренних электрических соединений. Кольца 62 прикреплены к внутреннему корпусу 28. Положение колец и первичных выводов относительно внешнего корпуса следует положению внутреннего корпуса. Как было описано ранее, внутренняя трубка вторичного вывода 31 также прикреплена к внутреннему корпусу 28. Для того чтобы полярность разных первичных выводов могла контролироваться отдельно, могут быть использованы отдельные проводящие кольца. Например, смежные первичные выводы могут быть соединены одним из двух проводящих колец так, чтобы смежные выводы могли быть подключены таким образом, чтобы иметь противоположные полярности или одну полярность. Кольца предпочтительно отстоят друг от друга на небольшом расстоянии, но остаются электрически изолированными друг от друга вдоль внутреннего корпуса. Кольца и внутренняя трубка соединены с внутренним корпусом, а первичные выводы 30, которые соединены с кольцами, перемещаются вместе с ними и со вторичным выводом, оставаясь электрически изолированными друг от друга. Для крепления колец к внутреннему корпусу может быть использована эпоксидная смола или другой соответствующий адгезив. Первичные выводы от соответствующих колец чередуются между собой по длине окружности внутреннего корпуса. Короткому замыканию между кольцами препятствует изоляция вдоль нижней стороны выводов.
Кольцо и первичные выводы соединены вместе так, чтобы действовать как консольные балки, где кольцо образует основание, а прямоугольные первичные выводы работают как консольные части. Выводы 30 соединены с кольцом и образованы с кривизной или изгибом, так что выводы действуют как рычаги, которые склонны пружинить в направлении наружу от катетера по направлению к окружающей венозной ткани. Изоляция вдоль нижней стороны выводов и колец препятствует непреднамеренному электрическому соединению между выводами и противоположными кольцами. В альтернативном варианте осуществления выводы образованы прямолинейными и соединены с кольцом под углом, так что выводы склонны развертываться или пружинить в радиальном направлении наружу от кольца. Угол, под которым выводы прикреплены к кольцу, должен быть достаточным для воздействия на дальние концы первичных выводов и электроды 34 через кровь и в контактном взаимодействии со стенкой вены. Другие свойства первичных выводов 30, например, форма вывода и толщина изоляции, оказывающие влияние на силу нажима вывода и величину кривизны или изгиба, должны быть отрегулированы для компенсации этих факторов. Прямоугольное поперечное сечение выводов 30 может обеспечивать повышенную устойчивость в боковом направлении, обеспечивая в то же самое время возможность необходимого изгиба в радиальном направлении. Выводы 30 при их развертывании в направлении наружу должны с меньшей вероятностью изгибаться в боковом направлении и с большей гарантией одинакового расстояния между ними. Одинаковое расстояние между выводами 30 и дальними концами способствует равномерному нагреву электродами 34 вокруг вены.
Дальние концы первичных выводов 30 выполнены неизолированными для того, чтобы они действовали как электроды 34, имеющие форму ложки или полусферы. Для получения интегрального фасонного электрода на дальнем конце вывода, выводы могут быть подвергнуты обработке давлением. Неизолированная внешняя часть электрода 34 дальнего конца, которая должна входить в контактное взаимодействие со стенкой анатомической структуры, предпочтительно скруглена и выпукла. Плоская или невыпуклая внутренняя часть дальнего конца изолирована для минимизации какого-либо непреднамеренного теплового воздействия, например, на окружающую кровь в вене. Электроды 34 дальнего конца имеют такую конструкцию, чтобы при воздействии на дальние концы в направлении к внутреннему корпусу 28, как показано на фиг.10а, дальние концы вместе бы образовывали по существу сферическую форму, имеющую профиль, который меньше профиля сферического электрода 35 на дальнем конце вторичного вывода.
Внешний корпус 12 может скользить поверх и вокруг первичных и вторичного выводов 30, 31. Внешний корпус 12 имеет отверстие приблизительно такого же размера, что и сферический электрод 35 (на дальнем конце вторичного вывода), который функционирует как электрод. При этом достигается точная посадка электрода 35 на дальнем конце вторичного вывода на отверстие внешнего корпуса 12. Такая конфигурация обеспечивает получение атравматического наконечника катетера. Диаметр вторичного электрода 35 предпочтительно немного больше диаметра отверстия. Внутренний диаметр внешнего корпуса 12 приблизительно равен уменьшенному профилю сведенных вместе электродов 34 дальнего конца первичных выводов. Диаметр уменьшенного профиля сведенных вместе электродов 34 дальнего конца первичных выводов предпочтительно меньше внутреннего диаметра внешнего корпуса.
Жидкостной канал (не показан) может сообщаться с внутренней областью внешнего корпуса 12 так, чтобы жидкость могла быть впрыснута между внешним корпусом 12 и внутренним корпусом 28. В альтернативном варианте осуществления, жидкостной канал может сообщаться с центральной полостью 48 во внутренней трубке, через которую может также проходить проволочный направитель. Как было указано ранее, катетер 10 может периодически промываться солевым раствором, который может предотвращать накопление в катетере биологической жидкости, например крови. Проволочный направитель может быть введен через полость 48 для направления катетера в требуемую зону обработки. Как было описано ранее, через эту полость может также впрыскиваться или подаваться жидкость. Если центральной полости не требуется, то полость внутренней трубки может быть заполнена мягким припоем.
Предпочтительно, чтобы первичные выводы 30 и проводящие кольца были соединены с источником 22 питания так, чтобы при желании полярность выводов могла быть изменена. Это обеспечивает возможность электродному приспособлению 24 работать либо в биполярной, либо в монополярной конфигурации. Если смежные первичные выводы 30 имеют противоположную полярность, то становится возможной работа в биполярной конфигурации. Если первичные выводы 30 имеют одинаковую полярность, то в комбинации с большой подушкой возвратного электрода, помещенной в контакте с пациентом, становится возможной работа в монополярной конфигурации. Если первичные выводы 30 имеют одинаковую полярность, а вторичный вывод 31 имеет противоположную полярность, то становится возможной работа в биполярной конфигурации. Может быть использовано больше или меньше выводов. Число выводов может зависеть от размера или диаметра полой анатомической структуры, подлежащей обработке.
Хотя это и не показано, но должно быть очевидным, что катетер 10 может содержать датчик температуры, например термопару, смонтированный на дальнем конце или электроде 34 так, чтобы датчик был по существу заподлицо с обнаженной поверхностью электрода 34. Датчик измеряет температуру части анатомической ткани, которая находится в контактном взаимодействии с обнаженной поверхностью электрода. Подачу высокочастотной энергии от электродов 34 поддерживают или уменьшают, если контролируемая температура достигает или превышает определенную температуру, которая была задана оператором, например температуру, при которой начинается каутеризация анатомической ткани. В автоматизированной системе, которая, если обнаружено достаточное сокращение вены и для предотвращения перегрева вены, отключает или регулирует подачу высокочастотной энергии электродами к участку вены, при этом могут быть использованы другие технологии, например текущий контроль импеданса или эхо-контроль ультразвуковых импульсов.
На фиг. 12-14 показано введение катетера 10 одного варианта осуществления, соответствующего настоящему изобретению, в полую анатомическую структуру, например в вену. Для направления катетера в определенное место и для подтверждения его положения в вене может быть использована технология получения изображения с помощью рентгеноскопии, ультразвука, капилляроскопа или другая технология. После этого для смещения внешнего корпуса 12 для обнажения выводов 30, 31 управляют исполнительным механизмом. Когда внешний корпус больше не ограничивает выводы, первичные выводы перемещаются в направлении наружу относительно оси, ограниченной внешним корпусом, тогда как вторичный вывод 31 остается по существу линейным вдоль оси, ограниченной внешним корпусом. Первичные выводы 30 продолжают двигаться в направлении наружу до тех пор, пока электрод 34 дальнего конца первичных выводов не придет в контактное взаимодействие со стенкой 54 вены и не будет препятствия движению первичных выводов 30 в направлении наружу. Первичные выводы 30 входят в контакт с веной вдоль, как правило, кольцевой области стенки 54 вены. Такое движение первичных выводов 30 в направлении наружу осуществляется по существу симметрично, так что электроды 34 дальнего конца первичных выводов по существу одинаково отстоят друг от друга. Электрод 35 центрального вывода подвешен к вене, не имея контакта со стенкой 54 вены.
Когда электроды 34 позиционированы в зоне обработки вены, для обеспечения подачи соответствующей высокочастотной энергии приводят в действие источник 22 питания. В биполярной конфигурации первичные выводы 30 вначале заряжены так, чтобы смежные выводы были заряжены противоположно, тогда как вторичный вывод электрически нейтрален. Это множество пар противоположно заряженных выводов 30 образует активные электродные пары для получения между ними высокочастотного поля и для образования симметричной конфигурации высокочастотного поля вдоль кольцевой полосы стенки вены для достижения равномерного распределения температуры вдоль обрабатываемой стенки вены.
Высокочастотная энергия обеспечивает нагрев, который побуждает венозную ткань сокращаться, уменьшая диаметр вены. Как показано на фиг.13, эта энергия заставляет стенку 54 вены спадать до тех пор, пока дальнейшее спадение не затормозится электродами 34. Благодаря сокращению стенки вены, электроды сходятся ближе друг к другу. Электроды 34 сводят вместе для обеспечения уменьшенного профиля, который по существу так мал, чтобы вена лигировалась эффективно. После спадения стенки 54 вены вокруг электродов 34 первичных выводов полярность электродов первичных выводов изменяют так, чтобы все электроды первичных выводов были заряжены одинаково. После этого электрод 35 вторичного вывода заряжают так, чтобы его полярность была противоположна полярности электродов 34 первичных выводов. В том случае, если первичные электроды 34 и вторичный электрод 35 отстоят друг от друга достаточно близко при спадении стенки вены вокруг электродов первичных выводов, то электрод на дальнем конце вторичного вывода может прийти в контактное взаимодействие с частью стенки вены, так что между первичными электродами 34 и вторичным электродом 35 создается высокочастотное поле.
Для того чтобы гарантировать контактное взаимодействие между электродами на дальних концах выводов и стенкой вены, катетер 10 отводят назад. При отведении катетера 10 назад, электроды 34 первичных выводов остаются в контактном взаимодействии со стенкой 54 вены, тогда как электрод 35 вторичного вывода приходит в контактное взаимодействие с частью стенки вены, которая предварительно спала под действием электродов 34 первичных выводов. Высокочастотная энергия проходит через венозную ткань между электродами 34 первичных выводов и электродом 35 вторичного вывода. Лигирование при отведении катетера производит протяженную окклюзию, которая сильнее и менее чувствительна к восстановлению просвета вены, чем резкая точечная окклюзия.
В монополярной конфигурации электрод 35 вторичного вывода остается нейтральным, тогда как первичные выводы имеют общий заряд и действуют в связи с независимым электрическим устройством, например, большой возвратной подушкой (не показана), имеющей низкий импеданс, помещенной в наружный контакт с телом пациента для образования высокочастотных полей по существу равномерно разнесенных по длине окружности вены. Тепло, выделяемое этими высокочастотными полями вдоль аксиального участка стенки вены, побуждает стенку вены спадать вокруг электродов первичных выводов. После спадения стенки вены электрод вторичного вывода заряжают так, чтобы он имел ту же полярность, что и электроды первичных выводов. Электродное приспособление отводят как описано со ссылкой на биполярную конфигурацию.
При работе в биполярной или монополярной конфигурации подача высокочастотной энергии по существу симметрично распределена по толщине стенки вены. Как было описано ранее, электроды должны отстоять друг от друга по длине окружности вены не более чем на 4 или 5 мм, что ограничивает целевой диаметр вены для соответствующего электродного катетера. Там, где электроды по существу равномерно разнесены по существу в симметричной конфигурации и сохраняется расстояние между электродами, симметричное распределение высокочастотной энергии увеличивает предсказуемость и равномерность сокращения и эффективности окклюзии.
Как показано на фиг.14, после того, как электроды 34 пришли в контактное взаимодействие со стенкой вены (фиг.12), и прежде, чем для лигирования вены была подана энергия (фиг.13), наружный жгут, например эластичную сжимающую повязку или надувной пузырь с окном, прозрачным для ультразвука, используют для сжатия анатомии, например ноги, окружающей структуру, для уменьшения диаметра вены. Хотя сжимающее усилие, прикладываемое жгутом, может эффективно лигировать вену или иначе создавать окклюзию вены, благодаря уплощению вены, для некоторых вен такое сжимающее усилие не будет создавать полную окклюзию. В этом случае не будет эффективен электродный катетер, имеющий постоянный диаметр. В этой ситуации могут оказаться эффективными электроды 34, которые развертываются в направлении наружу под действием выводов 30.
Уменьшение диаметра вены помогает предварительно профилировать вену для ее подготовки к формованию в лигированном состоянии. Применение наружного жгута обескровливает вену и побуждает кровь покинуть зону обработки. С помощью такой процедуры может быть предотвращена коагуляция крови в процессе обработки. К обескровленной вене от электродов подают энергию и для достижения лигирования вену формуют до достаточно небольшого диаметра. Для облегчения заживления наружный жгут может оставаться на месте.
Для лигирования большого участка вены катетер может отводиться в процессе подачи высокочастотной энергии. Таким образом, вместо одной точки, в которой должен быть уменьшен диаметр вены, с помощью высокочастотной энергии катетером будет обработан большой участок вены. Отведение катетера таким образом позволяет получить протяженную окклюзию, которая менее чувствительна к восстановлению просвета вены. При комбинированном использовании первичных и вторичного электродов можно эффективно получать уменьшенный диаметр вдоль большого участка вены. Катетер можно перемещать, сжимая в то же самое время вену жгутом, после чего жгут снимают.
В том случае, если катетер содержит полость для подачи жидкости, жидкость может быть подана в вену перед подачей к вене высокочастотной энергии. Подаваемая жидкость вытесняет кровь из зоны обработки для того, чтобы гарантировать отсутствие крови в зоне обработки даже после сжатия вены жгутом.
В том случае, если жгут представляет собой надувной пузырь, имеющий окно, прозрачное для ультразвука, то для текущего контроля уплощения вены или уменьшения диаметра вены от сжимающего усилия, прикладываемого посредством надувного пузыря, используют ультразвуковой измерительный преобразователь. Окно может быть образовано из полиуретана или зазором между листами полиуретана, заполненным гелем. Гель может быть нанесен на окно для облегчения ультразвуковой визуализации вены с помощью измерительного преобразователя. Ультразвуковая визуализация через окно обеспечивает возможность оператору найти требуемую зону обработки вены и определить, эффективно ли была лигирована или закрыта вена. Ультразвуковая визуализация помогает при предварительном профилировании вены для ее подготовки к формованию в лигированном состоянии благодаря теплу, выделяемому в результате подачи от электродов высокочастотной энергии.
После завершения этой процедуры для выбранного участка вены исполнительный механизм побуждает выводы 30 вернуться во внутреннюю область внешнего корпуса 12. Как только выводы 30 оказались внутри внешнего корпуса 12, катетер может быть перемещен к другому участку вены, на котором повторяют процесс лигирования.
Как показано на фиг.15, на которой иллюстрируется другой вариант осуществления катетера, соответствующего настоящему изобретению, на катетере расположен надувной баллон 64, который для закрытия вены может быть надут через отверстия 66. Надутый баллон препятствует прохождению потока крови и облегчает вливание жидкости, имеющей высокий импеданс, в вену для того, чтобы уменьшить коагуляцию в результате направления энергии в стенку вены. Надувание баллона для обеспечения окклюзии вены перед подачей энергии может исключить применение жгута для обеспечения окклюзии вены. Кроме того, это также дает возможность обеспечения окклюзии даже глубоких вен в тех случаях, когда сжимающий жгут может оказаться неспособным сжать вену до окклюзии. Должно быть очевидным, что для увеличения диаметра катетера, чтобы создать непроницаемый барьер, который обеспечивает окклюзию вены, могут быть использованы другие механизмы.
Жидкость 61 может быть подана после надувания баллона 64 и перед высокочастотным нагревом вены, подлежащей обработке, через коаксиальный канал 62, образованный между наружной оболочкой 60 и внешним корпусом 12. Должно быть очевидным, что для подачи жидкости в зону обработки может быть образована другая полость. Например, для подачи жидкости может быть использована полость, через которую пропускают проволочный направитель. Подаваемая жидкость смещает или вытесняет из зоны обработки вены оставшуюся кровь для того, чтобы предотвратить нагрев и коагуляцию крови. Для предотвращения оттока крови назад в область обработки жидкость продолжают подавать в течение высокочастотной обработки. Подача диэлектрической жидкости, имеющей высокую диэлектрическую постоянную, увеличивает окружающий импеданс, так что высокочастотная энергия направляется в ткань стенки вены. При этом расходуется меньше энергии, поскольку она направляется в целевую область, то есть в стенку вены, а не рассеивается в крови. По этой причине стенка вены может более быстро достигать требуемой температуры, чем в том случае, когда энергии позволяют рассеиваться в крови, которая охлаждает стенку вены. Кроме того, при использовании этого способа предотвращают образование сгустков крови, поскольку для вытеснения крови и предотвращения образования ее сгустков кровь заменяют другой жидкостью, например деионизованной водой, смешанной с гепарином.
На фиг. 16 иллюстрируется частичное поперечное сечение этого варианта осуществления катетера, соответствующего настоящему изобретению, где надувная оболочка 70 окружает наружную оболочку 60 для получения коаксиальной надувной полости 72 для баллона 64. Надувная полость 72 для надувания сообщается с отверстиями 66 для подачи жидкости. Для надувания баллона может быть использован солевой раствор или любая другая соответствующая жидкость.
Как показано на фиг.17, в одном варианте осуществления катетера, соответствующего настоящему изобретению, баллон 64 может быть использован в комбинации с поддающимися изгибу элементами или рычагами 76, имеющими электроды, где в катетере между баллоном 64 и поддающимися отклонению рычагами 76 образованы отверстия 78 для перфузии. В этом варианте осуществления баллон 64 надувают через полость 72 для надувания баллона. Применение поддающихся изгибу рычагов для обработки вен описано в патентной заявке США 08/610911, которая включена в настоящую заявку в качестве ссылки. Рычаги, которые могут иметь конструкцию, обеспечивающую подпружинивание в направлении наружу от катетера, однако дают небольшое сопротивление движению назад в направлении к катетеру, когда диаметр вены уменьшается до окклюзии. Через отверстия 78 для перфузии в катетер могут быть введены антикоагулянт или солевой раствор или жидкость, имеющая высокий импеданс. Как описано ранее, жидкость, имеющая высокий импеданс, вытесняет кровь из зоны обработки вены и препятствует энергии рассеиваться в более проводящей среде, например в крови.
В другом варианте осуществления, иллюстрируемом на фиг.18, для предотвращения прохождения потока крови в вене, вокруг или внутри выводов 30 электродов 34 обернута гибкая оболочка 80. Оболочка 80 перекрывает область между скошенными выводами по длине окружности катетера, когда выводы выходят из отверстия, так, чтобы полотно оболочки блокировало прохождение потока крови в вене. Оболочка может быть реализована как зонтик или навес, защищающий от попадания крови на электроды. Когда электроды приходят в контактное взаимодействие со стенкой вены, то зазор (если он имеется) между электродами 34 и оболочкой 80 должен быть исключен или по меньшей мере минимизирован. Оболочка 80 должна быть непроницаемой для жидкости. Пригодные материалы для оболочки включают в себя полиэтилентерефталат или нейлон. Эластомерные материалы также пригодны в тех случаях, когда выводы необходимо перемещать близко отстоящими друг от друга при их движении назад, и сопротивление выводов движению предпочтительно минимизируется, когда благодаря подаче энергии диаметр вены уменьшается. Хотя этот вариант осуществления настоящего изобретения иллюстрируется только с первичными выводами, должно быть очевидным, что этот вариант осуществления не ограничен такой конфигурацией и что в катетере может иметься вторичный вывод, не мешающий применению оболочки.
Также, как в случае применения баллона, который был описан выше, оболочка обеспечивает окклюзию вены перед подачей энергии, так что для прекращения потока крови не требуется применения наружного сжимающего жгута. Кроме того, это также позволяет обеспечивать окклюзию даже глубоких вен, в том случае, когда сжимающий жгут может оказаться неспособным сжать вену до окклюзии. Перед подачей энергии жидкость, имеющая высокий импеданс, например деионизованная вода, или коагулянт, например гепарин или солевой раствор, или то и другое, или гепарин с деионизованной водой, может также вводиться или впрыскиваться через центральную полость (не показано) аналогично тому, как это показано на фиг.4, где для этого используется центральная полость 48, и как это показано на фиг.10 и 11. Для увеличения эффекта лигирования от подачи высокочастотной энергии, к зоне обработки вены может также подаваться жидкость, увеличивающая плотность ткани. Жидкость, увеличивающая плотность ткани, может вводиться помимо или вместо жидкостей, описанных ранее.
В варианте осуществления, иллюстрируемом на фиг.19, оболочка 80, имеющая форму парашюта, может быть ориентирована так, чтобы кровь захватывалась вогнутой частью оболочки и объем крови поддерживал развертывание оболочки. В этом случае оболочка представляет собой баллон, имеющий отверстия, которые позволяют крови собираться в баллоне и увеличивать баллон в объеме. Оболочка 80 может быть постоянно прикреплена к стержню катетера. Катетер может еще двигаться вдоль вены даже с баллоном, находящимся в надутом состоянии.
В варианте осуществления, иллюстрируемом на фиг.20, оболочка 80 соединена с внешней канюлей 82, окружающей стержень катетера и соединенной с исполнительным механизмом или рычагом. Внешняя канюля 82 может скользить вдоль продольной оси катетера, чтобы позволять одному концу оболочки 80 парашюта двигаться аксиально вдоль стержня катетера. В процессе введения катетера, подвижный конец оболочки оттянут от соединительного конца катетера для складывания оболочки против катетера. После подачи катетера в зону обработки вены канюля скользит по направлению к рабочему концу для развертывания оболочки, которая затем наполняется кровью, поступающей через отверстия, обеспечивая в соответствии с этим окклюзию вены. Оболочка развертывается при наполнении ее кровью и, когда оболочка приходит в контактное взаимодействие со стенкой вены, обеспечивается окклюзия вены. Также, как и в предшествующих вариантах осуществления, жидкость может быть введена через отверстия 78 для перфузии или через коаксиальный канал 48 (не показан).
В варианте осуществления катетера, разрез которого показан на фиг.21, катетер 10 содержит секцию, поддающуюся расширению, имеющую каркас 90, расположенный вдоль части рабочего конца катетера. Каркас 90 более гибок, чем окружающий стержень катетера, и может быть изготовлен из металлической или полимерной оплетки. Каркас 90 покрыт гибкой мембраной 92, причем концы мембраны прикреплены к стержню катетера смежно каркасу. Мембрана предпочтительно изготовлена из эластомерного материала. Как показано на фиг.22, когда край соединительного конца движется к рабочему концу катетера (или наоборот), каркас 90 деформируется и заставляет мембрану 92 входить в контактное взаимодействие со стенкой вены. Этот вариант осуществления не требует отдельной полости для жидкости, предназначенной для надувания баллона. Каркас 90 предпочтительно сделан таким упругим, чтобы возвращаться к своей первоначальной (исходной) форме, как только рабочий конец и соединительный конец больше не побуждаются двигаться по направлению друг к другу. Механизмы для перемещения соединительного конца по направлению к рабочему концу катетера с целью увеличения диаметра катетера также описаны в патентной заявке США 08/610911, которая включена в эту заявку в качестве ссылки. Хотя секция, поддающаяся расширению, может регулироваться отдельно от выдвижения электродов, эта секция, поддающаяся расширению, может регулироваться с помощью того же механизма, который выводит электроды из катетера.
На фиг.23 и 24 иллюстрируется другой вариант осуществления поддающегося развертыванию электродного катетера 98, который содержит два множества поддающихся развертыванию электродных выводов 100 и 102, хотя могут быть предусмотрены дополнительные множества электродных выводов. Электроды 104 этого варианта осуществления настоящего изобретения аналогичны электродам варианта осуществления, иллюстрируемого на фиг. 2, имеющего электроды с ложкообразной контактной областью. Для электрода могут быть использованы другие формы, например эллипсы, круги, овалы, формы гоночных треков и другие конфигурации. Хотя на фиг. 23 и 24 только один электрод указан ссылочным номером 104, это сделано только для ясности изображения. Предполагается, что все электроды указаны ссылочным номером 104. Хотя каждое множество электродных выводов может содержать только два электродных вывода, иллюстрируемый вариант осуществления содержит по шесть электродных выводов на множество, хотя также может быть использовано более шести электродных выводов.
В варианте осуществления, иллюстрируемом на фиг. 23 и 24, множества электродных выводов 100 и 102 отделены друг от друга в продольном направлении. Таким образом, электроды в каждом множестве электродных выводов отделены друг от друга в радиальном направлении, а каждый из этих электродов отделен от каждого электрода в другом множестве в продольном направлении вследствие разделения в продольном направлении. Следовательно, в устройстве, показанном на фиг.23 и 24, на рабочем конце катетера 98 существует разделение электродов как в радиальном, так и в продольном направлениях.
В конфигурации электродных выводов, иллюстрируемой на фиг.23 и 24, существует более высокая гибкость в формировании токовых потоков через ткань пациента. Как и в предшествующих вариантах осуществления, электроды развертываются в направлении наружу в контактное взаимодействие с тканью пациента. Если все электроды первого множества электродных выводов имеют одну полярность, то в множестве может быть нечетное или четное число электродов. Все электроды в множестве могут быть соединены с общим местом соединения, например, проводящим кольцом 62, показанным на фиг.11. Один провод, проходящий от соединительного конца катетера может обеспечивать электропитание для всех электродов множества посредством одного соединения с таким проводящим кольцом. Все электроды второго множества электродных выводов могут быть также обычным образом соединены в соответствующем проводящем кольце, но для обеспечения другого электрического потенциала, чем имеет первое множество. Поскольку на рабочем конце катетера существуют два разных электрических потенциала, энергия будет проходить через ткань пациента между этими множествами электродных выводов и будет образована биполярная конфигурация. Таким образом, энергию получит участок ткани (пациента), длина которого равна по меньшей мере расстоянию между первым и вторым множествами электродов.
При необходимости может быть образована монополярная конфигурация путем создания на всех электродах всех электродных выводов одинакового электрического потенциала и создания другого электрического потенциала вне пациента, например на "спинной пластине", находящейся в контакте с кожей пациента в выбранном месте. Энергия от рабочего конца катетера поступит через пациента для возврата, обеспечиваемого посредством спинной пластины.
В другом устройстве при поляризации или регулирования электрического потенциала на электродах, электроды в первом множестве электродных выводов могут контролироваться отдельно так, чтобы в одном множестве выводов были образованы электродные пары разных потенциалов. Если электроды второго множества выводов аналогичным образом соединены для получения у них разных потенциалов, то они также обеспечат получение биполярной конфигурации в своем собственном множестве и токи будут проходить через ткань пациента между электродами в каждом множестве электродных выводов. Если электроды, имеющие одну полярность в первом множестве, совмещены с электродами, имеющими другую полярность во втором множестве электродных выводов, то энергия будет проходить не только между биполярными электродами в множестве, но будет также проходить к электродам в другом множестве, приводя в результате к образованию двух биполярных устройств на одном рабочем конце катетера. Получит энергию участок ткани (пациента), длина которого по меньшей мере равна расстоянию между первым и вторым множествами электродных выводов, а также ткань пациента между электродами в каждом множестве выводов.
В дополнительном устройстве, соответствующем биполярной конфигурации, которая была только что описана, для обеспечения дополнительной возможности регулирования потока энергии через ткань пациента также будет использована спинная пластина при другом электрическом потенциале. В этом случае энергия будет поступать между электродами в каждом множестве выводов, между электродами в разных множествах выводов и между электродами и спинной пластиной.
В другом дополнительном варианте осуществления каждый из электродов может быть дополнительно соединен с источником питания (указанного на фиг.1 ссылочным номером 22) и на каждом электроде может отдельно регулироваться (посредством микропроцессорного контроллера, указанного на фиг.1 ссылочным номером 23) электрический потенциал. Такое устройство может обеспечивать даже более точный контроль плотностей тока, проходящего через ткань пациента. Например, если между определенными электродами множества выводов требуется пропустить меньший электрический ток, а между этими электродами и электродами второго множества выводов требуется пропустить больший электрический ток, то потенциал между электродами одного множества может быть уменьшен, а потенциал между этими электродами и электродами второго множества выводов может быть увеличен, приводя в результате к получению требуемых плотностей тока. В том случае, если также используется спинная пластина, то электроды могут регулироваться так, чтобы энергия проходила между такими электродами и спинной пластиной. Поскольку регулирование потенциала каждого электрода осуществляется отдельно, то поддается регулированию уровень энергии подаваемой к ткани.
Диаметр вены, подлежащей обработке, является фактором, который может повлиять на число электродов в множестве электродных выводов. Конструкция контактной площадки электронных выводов также может оказать влияние на требуемое число электродов для данной процедуры.
В этом варианте осуществления электродные выводы 100, 102 образованы для развертывания в направлении наружу в контактное взаимодействие с целевой тканью, однако при сокращении целевой ткани электроды поддерживаются в контакте с этой тканью и движутся под действием этой ткани внутрь. Вследствие такого устройства выводы компенсируют изменения диаметра вены. Следовательно, они способны поддерживать контактное взаимодействие с тканью в любом случае существует ли или не существует сжатие вены или анатомической структуры, например, посредством манжеты или жгута.
Наконечник 106 электродного катетера 98 должен иметь полусферическую или другую атравматическую форму. Наконечник 106 может быть электрически нейтральным и изготовлен из полимера или из нержавеющей стали. Поскольку наконечник 106 имеет скругленную форму и расположен в дальней крайней точке катетера, то он может выполнять функцию направителя при введении катетера в тело пациента.
Двойное множество поддающихся развертыванию электродов может быть использовано для лигирования вен или других полых анатомических структур так, как это было описано выше. Внешний корпус 108 может отводиться назад, чтобы давать возможность электродам развертываться в направлении наружу от катетера и в контактном взаимодействии со стенкой полости трубчатого органа, подлежащей обработке. Два множества электродов 100 и 102 подают энергию к полости трубчатого органа для побуждения ее сокращаться до меньшего диаметра. Катетер может перемещаться или отводиться назад при одновременной подаче энергии для обработки протяженной области полости трубчатого органа. Если требуемая область полости трубчатого органа или вены обработана (например, лигирована), то энергию больше не подают к электродам и внешний корпус 108 толкают вперед для побуждения развернутых электродов вернуться в неразвернутое положение. После этого катетер может быть извлечен из тела пациента или обработке может быть подвергнута другая секция вены.
Описание вышеуказанных компонентов устройства относится к катетеру, предназначенному для применения в вене, имеющей диаметр в диапазоне от 3 мм (0,12 дюйма) до 10 мм (0,39 дюйма). Должно быть очевидным, что эти размеры не ограничивают объем настоящего изобретения, а приведены только для его иллюстрации. Размеры компонентов могут быть изменены так, чтобы катетер 10 мог быть использован в венах других размеров или в других анатомических структурах.
На фиг.25 показано частичное сечение катетера, иллюстрируемого на фиг.23 и 24. Показаны два множества электродов 100 и 102, причем электроды первого множества 100 указаны ссылочным номером 104, а электроды второго множества 102 указаны ссылочным номером 150. Каждый электрод образован из электропроводного электродного вывода 152 и 154, соответственно, который электрически изолирован вдоль своей длины за исключением своего дальнего конца, на котором существует точка, не имеющая изоляции, образующая, таким образом, электрод. Каждый вывод имеет изгиб в направлении наружу (не показано). Внутренняя труба 156 имеет полость 158, через которую для промывки или для других целей может проходить поток жидкости или через которую может позиционироваться проволочный направитель. Гипотруба 160 позиционирована поверх внутренней трубы и поверх гипотрубы образованы слои изоляции 162. Первое множество 100 электродных выводов 152 проходит вблизи первого монтажного кольца 164, с которым они все соединены. Второе множество 102 электродных выводов 154 проходит вблизи второго монтажного кольца 166, с которым они все соединены. Кольца 164 и 166 смонтированы поверх изоляции гипотрубы так, чтобы между ними не было электрического замыкания. Проволочные проводники 168 и 170 проходят от ближнего конца катетера к каждому кольцу так, чтобы все соединенные электродные выводы были электрически соединены с соответствующим кольцом.
Возможны альтернативные устройства и в одном таком устройстве чередующиеся электроды конкретного множества соединены с двумя разными кольцами. Каждое кольцо отдельно соединено с источником питания и полярности этих колец могут быть, следовательно, сделаны разными для получения биполярной конфигурации в указанном множестве. Один электрод может быть сделан положительным, тогда как два смежных электрода могут быть сделаны отрицательными. Тогда в этом случае для всех электродов будет всего три кольца. В другом устройстве обе полярности будут иметь два кольца для соответствующих им электродов с чередующимися электродами, соединенными к разным кольцам так, чтобы в каждом множестве могла быть образована биполярная конфигурация. В этом случае для двух полярностей электродов будет задействовано всего четыре кольца.
Внешний подвижный корпус 172 при скольжении в направлении к дальней точке, как показано на фиг.25, будет побуждать электродные выводы сжиматься в показанное положение. При скольжении в ближнем направлении на достаточное расстояние корпус 172 действует как развертывающее приспособление в том отношении, что он будет двигаться за изгибом (не показано) каждого из электродных выводов второго множества 102, позволяя всем электродным выводам развертываться в направлении наружу, как показано на фиг.24.
В этом варианте осуществления электродные выводы образованы из нержавеющей стали и с тонким изоляционным слоем, а изгиб в направлении наружу имеет достаточную прочность, чтобы обеспечивать автоматическое движение в направлении наружу через поток крови (при применении в вене) и в контактном взаимодействии с внутренней стенкой целевой ткани. При сокращении внутренней стенки из-за нагрева, обеспечиваемого с помощью электродов, внутренняя стенка будет побуждать электродные выводы перемещаться в их сжатое положение, но электроды будут автоматически оставаться в контактном взаимодействии с внутренней стенкой в течение всего процесса лигирования из-за изгибов их выводов в направлении наружу и материала, из которого они образованы.
Другие варианты осуществления электродных катетеров, имеющих два множества отстоящих в продольном направлении поддающихся развертыванию электродов, иллюстрируются на фиг. 26-28. Эти варианты осуществления аналогичны вариантам осуществления электродного катетера, описанного со ссылкой на фиг. 23-25. Конфигурации наконечников 106 для вариантов осуществления электродных катетеров, иллюстрируемых на фиг. 26-28, отличаются. Электродный катетер, иллюстрируемый на фиг.26, содержит наконечник 106, имеющий радиус, который сопрягается с внутренним радиусом сложенных электродов 100 или меньше его. Электроды 100 складываются, образуя наконечник 106. Электродный катетер, иллюстрируемый на фиг.27, содержит наконечник 106, имеющий скругленную форму со срезом. Радиус скругленного и срезанного наконечника сопрягается с внутренним радиусом сложенных электродов 100 и электроды 100 складываются за срезом наконечника 106. Электродный катетер, иллюстрируемый на фиг.28, содержит наконечник 106, имеющий более полусферическую форму, чем наконечник, иллюстрируемый на фиг.27.
Со ссылкой на фиг.29 описывается обработка вен нижней области геморроидальных узлов при подготовке зоны доступа. В вену вводят проволочный направитель 120 и продвигают через
зону обработки вены. В альтернативном варианте осуществления катетер может быть введен в вену непосредственно и манипулирование им осуществляется без проволочного направителя. Проволочный направитель
может продвигаться к зоне обработки геморроидальных узлов в
обратном направлении. К зоне обработки геморроидальных узлов может быть проложено несколько маршрутов внутри вены и должно быть
очевидным, что для обработки внутренних или наружных геморроидальных узлов могут быть использованы другие зоны доступа.
На фиг. 29 приведено частичное сечение венозной системы, ведущей к области геморроидальных узлов. Геморроидальные узлы, как правило, определяют как внутренние, и наружные в зависимости от того, образованы ли они выше или ниже прямокишечно-заднепроходной линии DL, соответственно. Внутренние геморроидальные узлы IH, как правило, образуются при расширении меньших вен, дренирующих верхнюю геморроидальную вену SHV или среднюю геморроидальную вену MHV. Наружные геморроидальные узлы ЕН, как правило, образуются при расширении меньших вен, дренирующих нижнюю геморроидальную вену IHV.
Один способ доставки катетера 122 и проволочного направителя 120 заключается во введении проволочного направителя 120 в наружную подвздошную вену EI на стороне, которая противоположна расширенным венам геморроидального узла. Проволочный направитель продвигают через раздвоенную ветвь нижней полой вены IVC к нижней подвздошной вене II. После этого проволочный направитель продвигают в среднюю геморроидальную вену MHV для обработки внутреннего геморроидального узла. Проволочным направителем 120 маневрируют через венозную систему до тех пор, пока он не достигнет расширенных вен геморроидального узла. Затем катетер 122 по проволочному направителю 120 подают к зоне обработки вены, как показано на фиг.29. Рабочий конец 124 катетера 122 имеет множество выводов и электродов для подачи высокочастотной энергии при правильном позиционировании в зоне обработки вены для лигирования или обеспечения окклюзии вены. Катетер должен быть гибким для обеспечения возможности продвижения катетера по проволочному направителю и через изгибы в венозной васкулярной системе. Для определения направления движения катетера в определенное место и для подтверждения его положения в вене могут быть использованы рентгеноскопия, а также рентгенолучевая, ультразвуковая или другая технология визуализации.
Другой способ доставки катетера и проволочного направителя предусматривает введение проволочного направителя в верхнюю геморроидальную вену и направление проволочного направителя через верхнюю геморроидальную вену SHV к геморроидальной области. Проволочный направитель продвигают в заданное положение и затем по проволочному направителю продвигают катетер в зону обработки вены к внутреннему геморроидальному узлу. Зона обработки вены находится в полости расширенной вены и электродные выводы развертывают из корпуса катетера для приведения их в контактное взаимодействие со стенкой расширенной вены.
При позиционировании электродных выводов катетера 122 в зоне обработки вены, для побуждения нагрева окружающей венозной ткани приводят в действие высокочастотный генератор для обеспечения подачи соответствующей высокочастотной энергии. Энергия, выделяемая из электродов, преобразуется в венозной ткани в тепло. Как описано выше, подача энергии побуждает спадение стенок вены, обеспечивая получение требуемого уровня окклюзии или лигирования.
В другой анатомической области варикозно-расширенные вены, называемые эзофагеальными варикозно-расширенными сосудами, могут образовываться в венозной системе вдоль подслизистой основы нижнего пищевода и приводить к кровотечению вздутых вен. При обработке вен нижней эзофагеальной области подготавливают зону доступа и пропускают проволочный направитель 120 в вену, продвигая его к зоне обработки вены. Проволочным направителем можно манипулировать так, чтобы достичь зоны обработки для оказания благоприятного воздействия на эзофагеальные варикозно-расширенные сосуды. Зона обработки вены предпочтительно находится в полости расширенной вены. Проволочный направитель продвигают к зоне обработки вены, которая должна быть восстановлена. Предпочтительно, чтобы введению катетера в эзофагеальную зону обработки предшествовало введение проволочного направителя. В альтернативном варианте катетер может быть введен в вену непосредственно и продвинут в место назначения без проволочного направителя. Для определения направления движения катетера в определенное место и для подтверждения его положения в вене могут быть использованы рентгеноскопия, а также рентгенолучевая, ультразвуковая или другая технология визуализации. Катетер 122, имеющий соответствующие размеры, обеспечивает подачу электродных выводов в зону неправильного функционирования вены вдоль эзофагеального варикозно-расширенного сосуда. Электроды обеспечивают подачу высокочастотной энергии или другого вида энергии при соответствующих мощности или частоте для побуждения спадения стенок вены и обеспечения требуемого уровня окклюзии или лигирования.
Как иллюстрируется на фиг.30, где показано сечение венозной системы, ведущей к эзофагеальной области, катетер 122 продвигают по проволочному направителю 120 к расширенной секции вены. Один способ введения катетера и проволочного направителя предусматривает введение проволочного направителя через верхнюю мезентериальную вену SMV в воротную вену PV и коронарную вену CV, которая разветвляется и ведет к нижнему пищеводу Е для образования эзофагеальных вен EV. В альтернативном варианте проволочный направитель может быть введен в нижнюю мезентериальную вену и направлен через селезеночную вену SV, воротную вену PV и коронарную вену CV к эзофагеальному варикозно-расширенному сосуду, подлежащему обработке.
На фиг.31 иллюстрируется лигирование фаллопиевой трубы. Проволочный направитель 120 был расположен в фаллопиевой трубе F, причем катетер 122 также позиционировали в фаллопиевой трубе F через устье 126 фаллопиевой трубы. Стержень катетера вводили через матку U с помощью эндоскопа 128. Теперь на рабочий конец катетера могло быть подано соответствующее электропитание, как описано выше, для осуществления лигирования внутри фаллопиевой трубы. Аналогичным образом после этого может быть лигирована также вторая фаллопиева труба.
Перед подачей энергии к полой анатомической структуре последняя может быть сжата или ей могут приданы заданные размеры. Кроме того, полость трубчатого органа может быть обескровлена сжатием или с помощью промывки жидкостью. Одним способом сжатия полости фаллопиевой трубы посредством наружного средства является пневмоперитонеум. В другом способе полость трубчатого органа, в частности, полость фаллопиевой трубы, может быть сжата путем приложения отрицательного давления через катетер. Например, открытым концом катетера, например катетера, иллюстрируемого на фиг. 25, отрицательное давление может быть приложено к полости трубчатого органа у открытого конца. При необходимости, для того чтобы помочь приложению к полости трубчатого органа отрицательного давления, на стержне катетера, вблизи отверстия, через которое должно быть приложено отрицательное давление, может быть смонтирован надувной баллон. Могут быть использованы также и другие устройства, например, устройства, в которых в стенках катетера образованы каналы, через которые может быть приложено отрицательное давление.
Приводимые выше такие термины, как положительно заряженные, отрицательно заряженные или как положительный проводник или отрицательный проводник, используются только для пояснения. Эти термины, как правило, относятся к различным потенциалам электродов, а не к конкретному потенциалу, положительному или отрицательному. Кроме того, для создания теплового эффекта в полой анатомической структуре, предназначенной для обработки, могут быть использованы другие виды энергии, например световая энергия, подаваемая с помощью волоконной оптики, или сверхвысокочастотная энергия. Хотя полой анатомической структурой может быть вена (например, варикозно-расширенные вены, геморроидальные узлы, эзофагеальные варикозно-расширенные сосуды и так далее) или фаллопиева труба, должно быть очевидным, что с помощью системы, описанной в этой заявке, могут быть лигированы другие анатомические структуры.
Хотя были проиллюстрированы и описаны некоторые конкретные варианты осуществления настоящего изобретения, должно быть очевидным, что без отклонения от сущности и объема настоящего изобретения могут быть сделаны различные модификации. В соответствии с этим настоящее изобретение не ограничено вышеописанными вариантами осуществления, а только прилагаемой формулой изобретения.
Реферат
Изобретение относится к медицине, а именно к устройствам для сокращения полой анатомической структуры. Катетер содержит первое множество поддающихся развертыванию выводов и второе множество поддающихся развертыванию выводов, отдельное и отстоящее в продольном направлении от первого множества, для подачи энергии к полой анатомической структуре. Каждый из выводов имеет электрод, расположенный на дальнем конце соответствующего электродного вывода. Для получения требуемого распределения энергии может быть выбрана поляризация выводов. Каждый вывод имеет изгиб в направлении наружу, так что при движении подвижного корпуса из контактного взаимодействия с выводами, они развертываются в направлении наружу в контактное взаимодействие с внутренней стенкой структуры, подлежащей лигированию. Изобретение позволяет повысить эффективность хирургического вмешательства при операции лигирования. 4 с.и 46 з.п.ф-лы, 31 ил.


Комментарии