Способ получения порошков тантала - RU2582414C1
Код документа: RU2582414C1
Чертежи


Описание
Изобретение относится к области порошковой металлургии и может быть использовано для получения высокочистых порошков тантала гидридным методом.
Гидридный способ получения порошков переходных металлов, в том числе тантала, включает активацию компактного материала нагреванием, гидрирование (с целью перевода металла из пластичного в хрупкое состояние) путем охлаждения в атмосфере водорода, механическое дробление, измельчение и сепарацию (рассев, классификацию) синтезированного гидрида для получения порошков нужной степени дисперсности, а также дегидрирование с целью удаления водорода и снижения его остаточного содержания до требуемых потребителями значений.
Известен способ получения порошков тантала из компактных металлов, включающий следующие операции:
1) нагрев слитка в вакууме при температурах 800-1400°С, гидрирование при давлении водорода 300-400 мм рт. ст. (40-53 кПа), проводившееся при охлаждении как минимум в три стадии с выдержкой по несколько часов при температурах 600-1000, 200-500 и 60-120°С;
2) дробление охрупченного материала с получением крупного порошка, который при необходимости дополнительно измельчали до необходимой степени дисперсности (не более 150 мкм);
3) дегидрирование порошка в глубоком вакууме при температурах 600-1200°С (US Patent 3635693, МПК B22F 9/00, US Cl. 75/0.5 ВВ, publ. Jan. 18, 1972).
Основные недостатки такого способа - большой расход водорода на единицу выпускаемой продукции, обусловленный отсутствием утилизации откачиваемого вакуумными насосами газа и загрязнение металлического порошка примесями внедрения, попадающими в него с парами масла, выделяющимися при работе этих насосов.
К загрязнению получаемого порошка примесями внедрения может также привести недостаточная очистка используемого для гидрирования водорода. Зачастую она вызывает увеличение индукционного периода реакции и требует повышения температуры гидрирования (Гидриды металлов / под ред. В. Мюллера, Д. Блэкледжа, Дж. Либовица; пер. с англ.; под ред. Р.А. Андриевского, К.Г. Ткача. М.: Атомиздат, 1973, 432 с.). Кроме того, от чистоты водорода напрямую зависят скорости процессов гидрирования и дегидрирования, а также выход продукта. Среди известных способов получения высокочистого водорода наиболее эффективен, удобен и экономичен метод термического разложения гидридов (Препаративная химия гидридов / М.М. Антонова, Р.А. Морозова. Киев: Наук. думка, 1976, 99 с.).
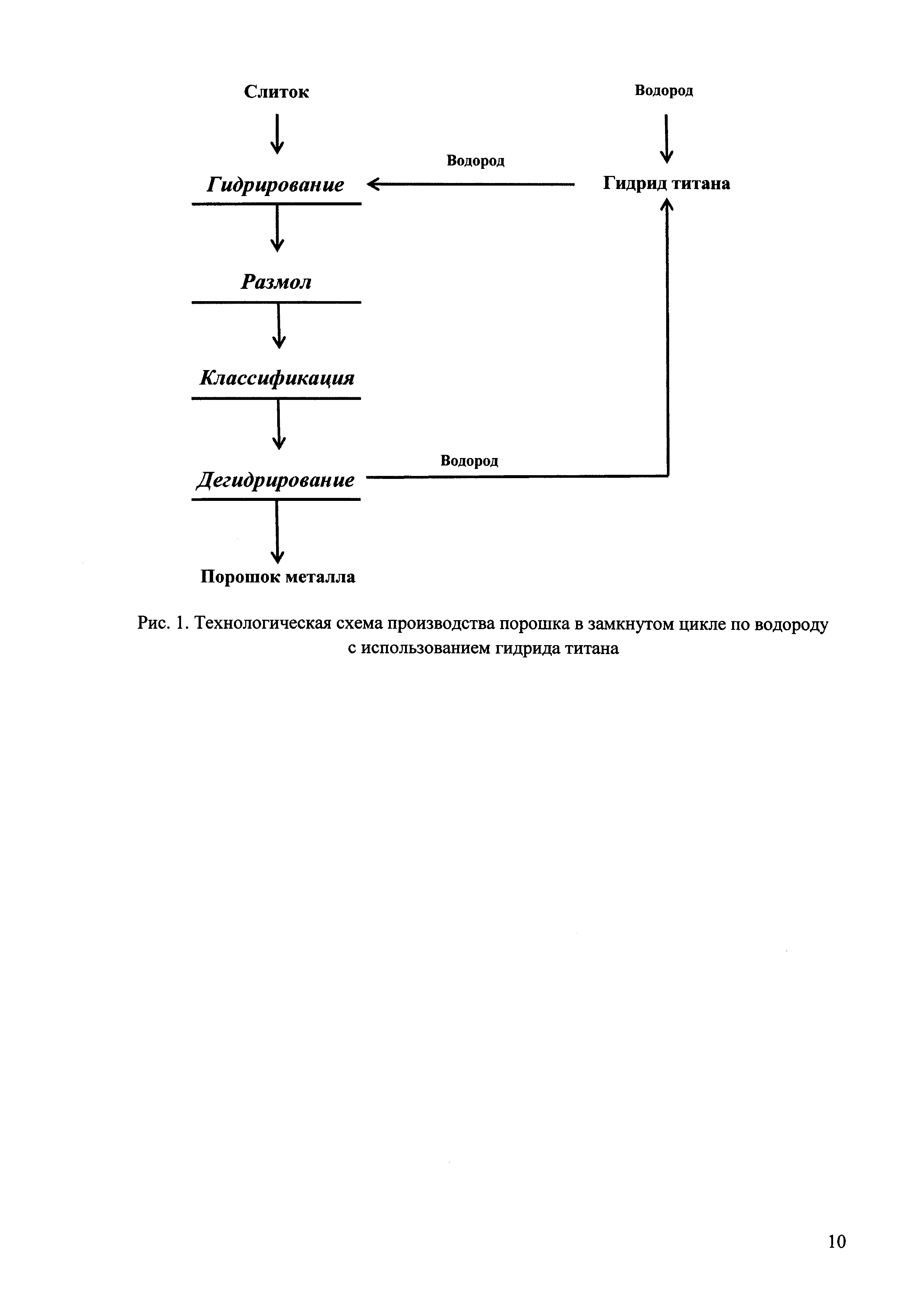
Процессы гидрирования-дегидрирования переходных металлов носят обратимый характер, что позволяет использовать систему Ме-Н не только как источник чистого водорода, но и в качестве поглотителя этого газа, осуществляя вышеописанный процесс получения порошков гидридным методом в замкнутом цикле по водороду. Для этой цели чаще всего применяют титановую губку, которая образует нестехиометрические гидриды TiHx в широком интервале концентраций (0 Известен способ получения порошка ванадия из компактного металла методом гидрирования-дегидрирования в замкнутом цикле по водороду. Согласно данному способу слитки активируют путем нагрева до 600-800°С, гидрируют посредством охлаждения с указанного температурного уровня до 50-200°С в атмосфере водорода, которую создают путем термического разложения гидрида титана с переводом его в ненасыщенное состояние. Затем синтезированный гидрид измельчают, подвергают классификации и дегидрируют путем нагрева до 650-800°С с удалением водорода и выдержкой при этой температуре до остаточного давления 0,05-0,50 мм рт. ст. При этом ненасыщенный гидрид титана используют для поглощения водорода, выделяющегося при дегидрировании порошка (Способ получения порошка ванадия: патент RU №2196024, МПК B22F 9/16, С22В 34/22, опубл. 10.01.2003). Известен также способ получения порошков редких металлов гидрированием-дегидрированием компактных материалов с использованием водорода в замкнутом цикле. Данный способ включает технологические операции гидрирования, размола, классификации и дегидрирования (технологическая схема представлена на рис. 1). При этом чистый водород поступает в систему из насыщенного гидрида титана, а удаление водорода, выделяющегося при дегидрировании порошка, обеспечивается за счет поглощения этого газа ненасыщенным TiHx (Исследования и разработки ИХТРЭМС КНЦ РАН в области материаловедения для решения задач специальной техники / В.Т. Калинников, А.Г. Касиков, В.М. Орлов, Н.Н. Гришин, Б.М. Фрейдин // Химическая технология. 2009. Т. 10, №3. С. 177-182). Способ принят за прототип. При использовании TiHx в производстве порошков редких металлов важные преимущества описанных выше технологий обеспечиваются во многом за счет высокого сродства к водороду и большой водородоемкости титана (в насыщенном гидриде TiH2 содержится около 4 мас. % водорода). Однако у этих способов получения порошков есть и существенные недостатки. Во-первых, из-за высоких температур образования (выше 400°С) и разложения (550-950°С) гидрида титана разогрев его до заданного температурного уровня требует много времени и больших затрат электроэнергии, что значительно удлиняет процессы гидрирования компактного металла, снижает их производительность и увеличивает стоимость продукта. Во-вторых, если в процессе участвует только один сорбент - TiHx, не исключены потенциально аварийные ситуации, которые могут возникнуть при его перегреве из-за инерционности печей и разницы в скоростях выделения водорода и поглощения его гидруемым металлом. Это может привести к резкому скачку давления (выше безопасного уровня). Техническим результатом заявленного изобретения является сокращение времени, необходимого для проведения операций гидрирования и дегидрирования, снижение энергетических затрат и повышение тем самым экономической эффективности технологического процесса, применяемого для получения высокочистых порошков тантала, а также повышение безопасности этого процесса и уменьшение потерь водорода за счет обеспечения возможности дополнительного поглощения излишнего количества выделяющегося газа. Технический результат достигается тем, что в способе получения порошков тантала, включающем активацию слитка тантала нагреванием до 700-900°С, гидрирование его с использованием насыщенного гидрида титана в качестве источника водорода, измельчение полученного гидрида тантала до заданной степени дисперсности и дегидрирование полученного порошка тантала с использованием ненасыщенного гидрида титана, согласно изобретению активацию слитка тантала нагреванием ведут в атмосфере водорода при избыточном давлении 0,01-0,3 МПа, которую создают путем десорбции водорода из насыщенного гидрида многокомпонентного интерметаллического соединения La1-yRyNi4Co, где R - редкоземельные металлы цериевой группы и/или мишметалл, (0 (Технологическая схема получения порошков представлена на рис. 2.) Сущность изобретения заключается в следующем. Активацию исходного слитка тантала осуществляют нагреванием его до температуры 700-900°С в атмосфере чистого водорода при избыточном давлении 0,01-0,3 МПа (0,1-3,0 кгс/см2), которую создают путем десорбции этого газа из насыщенного гидрида многокомпонентного интерметаллического соединения La1-yRyNi4Co (R - редкоземельные металлы цериевой группы, и или мишметалл, 0 Одновременно с активацией слитка тантала осуществляют нагрев насыщенного гидрида титана до достижения температуры его разложения (550-950°С), обеспечивающей необходимое давление и количество выделяющегося водорода. К моменту начала поглощения водорода слитком избыточное давление водорода, выделяющегося при разложении гидрида титана, достигает требуемых значений: 0,2-0,3 МПа (2-3 кгс/см2), и в дальнейшем для проведения процесса используют именно этот газ. Использование ИМС La1-yRyNi4Co на первом этапе процесса позволяет значительно сократить длительность гидрирования слитка тантала за счет исключения простоя оборудования в период разогрева гидрида титана до требуемой температуры, снизить энергетические затраты в результате того, что сорбция и десорбция водорода La1-yRyNi4Co осуществляются при температурах, близких к комнатной. Кроме того, присутствие второго сорбента позволяет избежать резких скачков давления в системе (благодаря обратимости процессов сорбции-десорбции водорода La1-yRyNi4Co при комнатной температуре, в случае повышения давления ИМС начнет поглощать газ) и, следовательно, повысить безопасность технологического процесса. Известно использование интерметаллического соединения LaNi4Co при гидрировании ниобия водородом, выделяющимся при разложении гидрида ИМС. Слитки ниобия помещали в реторту, которую затем герметизировали, вакуумировали, заполняли водородом, выделяющимся из насыщенного гидрида ИМС LaNi4Co, нагревали в электропечи до 750±50°С и делали выдержку при этой температуре в течение 4-5 час. Начавшийся процесс гидрирования продолжали путем ступенчатого снижения температуры: сначала до 450±50°С (с выдержкой на этом уровне около 5 час.), потом до 80-100°С (вместе с печью, на протяжении 20-30 час), а после извлечения реторты из печи - до комнатной температуры (Разработка оксидно-полупроводниковых конденсаторов на основе ниобия / А.В. Елютин, Ю.Б. Патрикеев, Н.С. Воробьева // ГИРЕДМЕТ - 70 лет в металлургии редких металлов и полупроводников: юбилейный сборник. М.: ЦИНАО, 2001. С. 291-306). К недостаткам данного способа относятся: 1) меньшая по сравнению с гидридом титана емкость ИМС LaNi4Co по водороду (при комнатной температуре в интервале 0,2-1,0 МПа она составляет 1,4-1,8 мас. %), что требует участия в процессах гидрирования-дегидрирования большего количества этого сорбента; 2) невысокое давление десорбции водорода из гидрида ИМС LaNi4Co при температурах, близких к комнатной, - ниже величин, необходимых для гидрирования тантала. Для создания и поддержания требуемого давления данный гидрид нужно подогревать до температур около 100°С, используя для этой цели электроэнергию или горячую воду, что усложняет аппаратурную схему процесса и увеличивает энергетические затраты; 3) меньшая сорбционная активность ИМС при абсолютном давлении ниже 0,1 МПа, что не позволяет полностью поглотить водород, выделяющийся из порошка при дегидрировании, и требует вакуумирования последнего для более полного удаления этой примеси внедрения. Таким образом, замкнутый цикл реализуется неполностью, поскольку часть водорода, которая теряется при откачивании газа насосами, больше, нежели при использовании гидрида титана. Примеры осуществления способа. Порошок тантала получали методом гидрирования-измельчения-дегидрирования. Исходным материалом служили слитки электронно-лучевой плавки массой около 150 кг. Порошки тантала получали известным методом (пример 1) и заявленным способом (пример 2). Активацию компактного металла осуществляли нагревом до 700-900°С. Причем в первом случае процесс вели сначала в вакууме (до 300-350°С), а затем в водороде, выделяющемся из насыщенного гидрида титана, разогретого до температуры 550-900°С (в зависимости от степени насыщенности титана водородом). Во втором случае атмосферу водорода создавали перед началом подъема температуры, используя для этой цели газ, образующийся при разложении гидрида ИМС La1-yRyNi4Co. Одновременно с гидрируемым металлом нагревали и насыщенный TiHx, а когда избыточное давление водорода, выделяющегося при его разложении, достигало 0,2-0,3 МПа, подавали этот газ в зону реакции. Для осуществления процессов гидрирования-дегидрирования использовали установку, принципиальная схема которой представлена на рис. 3. Слиток тантала загружали в стальную реторту 1, которую помещали в электропечь 2, герметизировали и вакуумировали с помощью форвакуумного (3) и диффузионного (4) насосов. Насыщенный гидрид ИМС находился в реторте 5, количество выделяющегося из него водорода измеряли счетчиком 6, показания которого соответствуют объему, занимаемому газом при нормальных условиях. Реторту 1 плавно нагревали до температуры, при которой начинался процесс гидрирования, о чем свидетельствовало снижение давления, регистрируемое мановакуумметром 7. Насыщенная водородом титановая губка (TiHx) находилась в третьей реторте (8), помещенной в электропечь 9, и нагревалась там до температуры, обеспечивающей необходимое для гидрирования тантала избыточное давление водорода, измеряемое мановакуумметром (10). После выдержки при высоких температурах, обеспечивающей диффузию водорода с поверхности в толщу слитка металла, температуру в реторте 1 постепенно снижали вплоть до полного остывания. Завершающая стадия процесса гидрирования тантала осуществлялась при температурах ниже 200°С. В этом диапазоне происходит интенсивное образование гидридных фаз в системе металл - водород и достигается концентрация этого элемента внедрения, необходимая для охрупчивания тантала, поэтому полученный гидрид легко измельчается. После измельчения до необходимой дисперсности частиц порошка гидрид тантала направляли на дегидрирование в реторту 11 (нагреваемую электропечью 12), оснащенную мановакуумметром 13, а выделяющийся водород пускали в реторту 14 (снабженную мановакуумметром 15 и нагреваемую электропечью 16) с ненасыщенной титановой губкой, чтобы поглотить его и в дальнейшем использовать для гидрирования очередного слитка тантала. Израсходованный в процессе активации водород из реторты 5 восполнялся за счет газа, поступающего из гидрида титана на начальной стадии процесса дегидрирования. Давление в этой реторте измеряли мановакуумметром 17. Потоки газа в системе регулировали с помощью вентилей 18. Технический водород, необходимый для первоначального гидрирования титановой губки и ИМС La1-yRyNi4Co, поступал из стандартного газового баллона 19 через редуктор 20. Для предотвращения загрязнения получаемого порошка парами масла, выделяющимися при работе вакуумного насоса, их вымораживали, используя ловушку 21, охлаждаемую с помощью жидкого азота. Получение порошка тантала Пример 1. Активацию слитка тантала проводили при нагреве сначала до 350°С в вакууме, а затем до 800°С в водороде, выделяющемся из насыщенного гидрида титана (реторта 8), при избыточном давлении 0,2-0,3 МПа до начала гидрирования. После этого температуру поддерживали в течение 3,5-4 ч, а затем отключали нагрев электропечи 2 и продолжали процесс гидрирования при постепенном охлаждении реторты 1 и непрекращающемся поступлении в нее водорода из насыщенного TiHx. Продолжительность активации до начала гидрирования составляла 9-10 ч, длительность всей высокотемпературной фазы процесса - 12,5-14 ч. Пример 2. Активацию слитка тантала начинали при избыточном давлении около 0,01-0,02 МПа. Этот газ подавали из реторты 5, заполненной гидридом ИМС La0,78Ce0,22Ni4Co. При этом танталовый слиток плавно нагревали от комнатной температуры до 750°С, за счет чего давление возрастало примерно до 0,25 МПа. Одновременно разогревали насыщенный TiHx (в реторте 8), создавая такое же избыточное давление водорода. Время активации до начала гидрирования не превышало 3,5-4 ч, выдержка при достигнутой температуре длилась примерно столько же, и общая продолжительность высокотемпературной фазы процесса составляла 7-8 ч. Далее в обоих случаях температуру в реторте 1 ступенчато снижали до комнатной в течение примерно 40 ч. После выгрузки из реторты синтезированный гидрид тантала измельчали в шаровой мельнице до порошка с размером частиц менее 250 мкм, подвергали классификации и затем дегидрировали в реторте 11 при температуре 850-900°С до остаточного давления (0,1±0,02) мм рт. ст. В результате получали порошок тантала, содержащий менее 0,01 масс. % водорода. В приведенной ниже таблице сопоставлены затраты времени на осуществление отдельных стадий и процесса гидрирования в целом для известного (1) и заявленного (2) способов получения порошков тантала.
Приведенные в таблице данные свидетельствуют о том, что использование ИМС на первом этапе гидрирования позволяет сократить продолжительность его высокотемпературной стадии в 1,5-2 раза, а длительность всего процесса на 9-17%.
Реферат
Изобретение относится к получению высокочистого порошка тантала гидридным методом. Способ включает активацию слитка тантала нагреванием до 700-900°С, гидрирование его с использованием насыщенного гидрида титана в качестве источника водорода, измельчение полученного гидрида тантала до заданной степени дисперсности и дегидрирование полученного порошка тантала с использованием ненасыщенного гидрида титана. Активацию слитка тантала нагреванием ведут в атмосфере водорода при избыточном давлении 0,01-0,3 МПа, которую создают путем десорбции водорода из насыщенного гидрида многокомпонентного интерметаллического соединения LaRNiCo, где R - редкоземельные металлы цериевой группы и/или мишметалл, 0

Комментарии