Упакованное медицинское устройство в антимикробной упаковке с длительным сроком хранения и способ его изготовления - RU2546289C2
Код документа: RU2546289C2
Чертежи









Описание
Настоящее изобретение относится к медицинскому устройству с антимикробными свойствами, к упакованному медицинскому устройству в антимикробной упаковке и к способам их изготовления.
Ежегодно в Соединенных Штатах Америки проводится огромное количество хирургических процедур. Согласно текущим данным, в год проводится более двадцати семи миллионов таких процедур. Приблизительно в двух-трех процентах случаев наблюдаются послеоперационные или хирургические раневые инфекции (РИ). Абсолютная численность таких случаев ежегодно оценивается в 675000.
Появление РИ часто обусловлено бактериями, колонии которых образуются на имплантируемых хирургических приспособлениях, используемых при операциях. Во время хирургической процедуры бактерии из окружающей атмосферы могут попадать на операционную рану и прикрепляться к медицинскому приспособлению. В частности, бактерии могут распространяться, попадая через имплантируемое устройство в окружающие ткани. Подобное заражение медицинского приспособления бактериями может привести к инфицированию и травмированию пациента. Следовательно, хирургические раневые инфекции могут значительно увеличивать затраты на лечение больных.
В отрасли описаны и реализованы имплантируемые медицинские устройства, содержащие нанесенные на поверхность или встроенные антимикробные агенты. Примеры подобных устройств приводятся в Заявке на Европейский патент № EP 0761243. Одними из реально производимых устройств, описанных в этой заявке, являются французские катетеры Percuflex. Данные катетеры были глубоко погружены в ванну для нанесения покрытий, содержащую 2,4,4'-трихлор-2-гидроксидифениловый эфир (Ciba Geigy Irgasan (DP300)) и другие добавки. Далее катетеры стерилизовали этиленоксидом и хранили в течение 30 суток. Катетеры, покрытые указанными растворами, демонстрировали антимикробные свойства, т.е. через 30 дней после нанесения покрытия при помещении в инкубационную среду и добавлении микроорганизмов они формировали зону ингибирования роста микроорганизмов. Из заявки не ясно, при какой температуре осуществляли хранение стерилизованных катетеров с нанесенным покрытием.
Большинство имплантируемых медицинских приспособлений производится, стерилизуется и хранится в упаковках до самого момента вскрытия и использования в ходе хирургической процедуры. Во время хирургической операции на вскрытую упаковку с медицинским устройством, на содержащиеся внутри упаковочные компоненты и на само медицинское устройство воздействует атмосфера операционной, в которую могут попадать бактерии. Придание антимикробных свойств упаковке и/или находящимся внутри компонентам позволяет по существу предотвратить образование колоний бактерий на упаковке и на содержащихся в ней компонентах после вскрытия упаковки. Антимикробная упаковка и/или упаковочные компоненты, а также придание антимикробных свойств самому медицинскому устройству позволяет по существу обеспечить антимикробную среду вокруг стерилизованного медицинского устройства.
Упакованные медицинские устройства, обладающие антимикробными свойствами, могут иметь ограниченный срок хранения. Следовательно, существует потребность в упакованном антимикробном медицинском устройстве, имеющем длительный срок хранения, а также в способах увеличения срока хранения упакованных антимикробных медицинских устройств.
В одном аспекте настоящего изобретения описывается способ изготовления упакованной антимикробной шовной нити, имеющей длительный срок хранения согласно которому:
создают внутреннюю упаковку, содержащую источник антимикробного агента;
создают адсорбирующий материал, который эффективно поглощает со временем часть антимикробного агента;
помещают шовную нить во внутреннюю упаковку, причем шовная нить имеет одну или более поверхностей;
закрывают внутреннюю упаковку внешней упаковкой, имеющей внутреннюю поверхность; и
воздействуют на шовную нить, внутреннюю упаковку и внутреннюю поверхность внешней упаковки такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к шовной нити и к внутренней упаковке, в результате чего по существу ингибируется образование колоний бактерий на шовной нити и внутренней упаковке,
причем упакованная антимикробная шовная нить проявляет свойства возможности хранения в течение длительного срока.
В одном варианте осуществления данного изобретения адсорбирующий материал формируется путем нанесения покрытия из адсорбирующего материала по меньшей мере на часть одной поверхности внутренней упаковки.
В другом варианте адсорбирующий материал формируется путем помещения адсорбирующего субстрата внутрь внешней упаковки.
В еще одном варианте адсорбирующий субстрат формируется путем нанесения адсорбирующего материала на основу.
В еще одном варианте адсорбирующий субстрат формируется из адсорбирующего материала.
В еще одном варианте антимикробный агент выбирают из группы, содержащей галогенированные гидроксильные простые эфиры, ацилоксидифениловые простые эфиры и их сочетания.
В еще одном варианте эффективное количество антимикробного агента, поступающего от источника антимикробного агента на шовную нить и внутреннюю упаковку, переносится в ходе процесса стерилизации этиленоксидом.
В другом варианте этап воздействия на шовную нить, внутреннюю упаковку и внутреннюю поверхность наружной упаковки условий, способствующих переносу паров эффективного количества антимикробного агента, включает помещение внешней упаковки, внутри которой находится внутренняя упаковка и шовная нить, в стерилизационное устройство, нагревание стерилизационного устройства до первой температуры, установку давления в стерилизационном устройстве в соответствии с первым значением давления, подачу пара в стерилизационное устройство с целью обработки водяным паром внутренней поверхности наружной упаковки, внутренней упаковки и нити в течение первого интервала времени, установку давления в стерилизационном устройстве в соответствии со вторым значением давления, введение химического стерилизующего реагента в стерилизационное устройство на второй интервал времени, чтобы сделать нежизнеспособным достаточное количество микроорганизмов, удаление остатков влаги и химического стерилизационного агента с шовной нити и высушивание упакованной антимикробной шовной нити до желательного уровня влажности.
В еще одном варианте внутренняя упаковка представляет собой универсальный конверт из картонной массы, по меньшей мере одна поверхность которого покрыта адсорбирующим материалом.
В еще одном варианте внутренняя упаковка представляет собой отделение с защитной оболочкой, имеющее внешний чехол, и по меньшей мере одна поверхность внешнего чехла покрыта адсорбирующим материалом.
В еще одном варианте адсорбирующий материал выбран из бентонита, активированного угля, активированного глинозема, силикагеля, цеолита, полимеров со сверхвысокой абсорбирующей способностью, гигроскопических веществ, полимерных покрытий, грунтовочных полимерных покрытий, продуктов природного происхождения, небумажных субстратов, а также глин, в том числе, каолина.
Настоящее изобретение также относится к способу увеличения срока хранения упакованного медицинского приспособления с антимикробными свойствами. Способ включает в себя создание внутренней упаковки, содержащей источник антимикробного агента, создание адсорбирующего материала, эффективно поглощающего со временем часть антимикробного агента, помещение медицинского устройства во внутреннюю упаковку, причем медицинское устройство имеет одну или несколько поверхностей, закрытие внутренней упаковки наружной упаковкой, имеющей внутреннюю поверхность, и воздействие на медицинское устройство, внутреннюю упаковку и внутреннюю поверхность наружной упаковки такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к медицинскому устройству и внутренней упаковке. При этом образование колоний бактерий на медицинском устройстве и внутренней упаковке по существу ингибируется, вследствие чего упакованное антимикробное медицинское устройство имеет длительный срок хранения.
Настоящее изобретение также относится к упакованной антимикробной шовной нити, имеющей длительный срок хранения. В комплект упакованной антимикробной шовной нити входит внутренняя упаковка, содержащая источник антимикробного агента и адсорбирующий материал, эффективно поглощающий со временем часть антимикробного агента, шовная нить, имеющая одну или несколько поверхностей, наружная упаковка, внутри которой находится внутренняя упаковка, причем на шовную нить, внутреннюю упаковку и внутреннюю поверхность наружной упаковки оказывается воздействие такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к шовной нити и внутренней упаковке. При этом образование колоний бактерий на шовной нити и внутренней упаковке по существу ингибируется.
В одном варианте осуществления изобретения упакованная антимикробная шовная нить характеризуется длительным сроком хранения.
Настоящее изобретение также относится к упакованному медицинскому устройству. В комплект упакованного антимикробного устройства входит внутренняя упаковка, содержащая источник антимикробного агента и адсорбирующий материал, эффективно поглощающий со временем часть антимикробного агента, медицинское устройство, имеющее одну или несколько поверхностей, наружная упаковка, внутри которой находится внутренняя упаковка, причем на медицинское устройство, внутреннюю упаковку и внутреннюю поверхность наружной упаковки оказывается воздействие такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к медицинскому устройству и внутренней упаковке. При этом образование колоний бактерий на медицинском устройстве и внутренней упаковке по существу ингибируется.
Дальнейшие разъяснения настоящего изобретения представлены в нижеследующем описании со ссылками на чертежи, которые иллюстрируют (но не ограничивают) различные варианты осуществления изобретения.
На фиг.1 представлен вид сверху на одну из форм упакованного антимикробного медицинского устройства в соответствии с настоящим изобретением, где медицинское устройство представляет собой одну иглу и шовную нить.
На фиг.2 представлен вид сверху на другую форму упакованного антимикробного медицинского устройства в соответствии с настоящим изобретением, где медицинское устройство представляет собой одну иглу и шовную нить.
На фиг.3 представлен вид сверху на упакованное антимикробное медицинское устройство, соответствующее фиг.2, где внешний чехол защитного отделения снят, чтобы полностью показать основную часть.
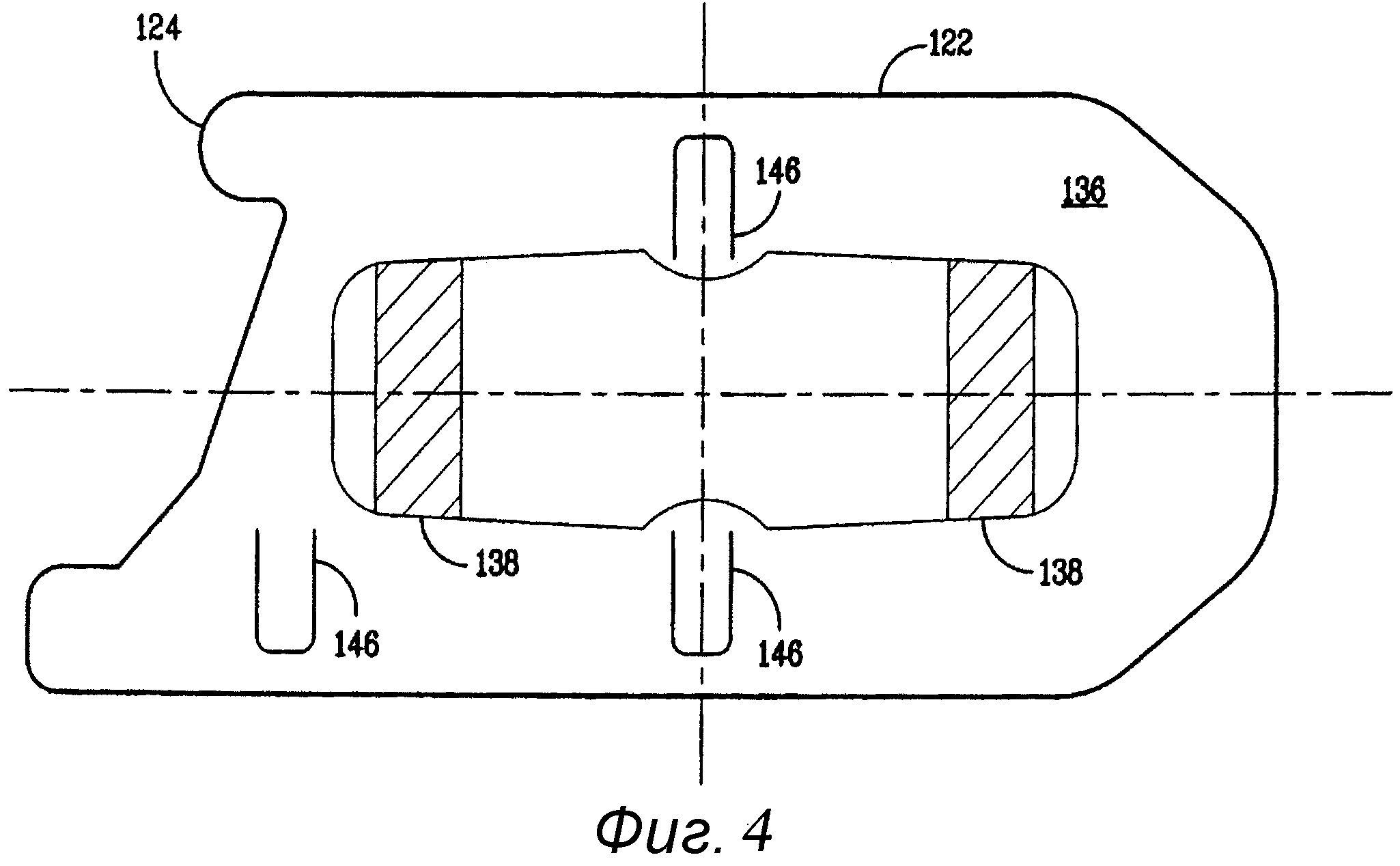
На фиг.4 представлен вид снизу на внешний чехол защитного отделения упакованного антимикробного медицинского устройства, соответствующего фиг.2.
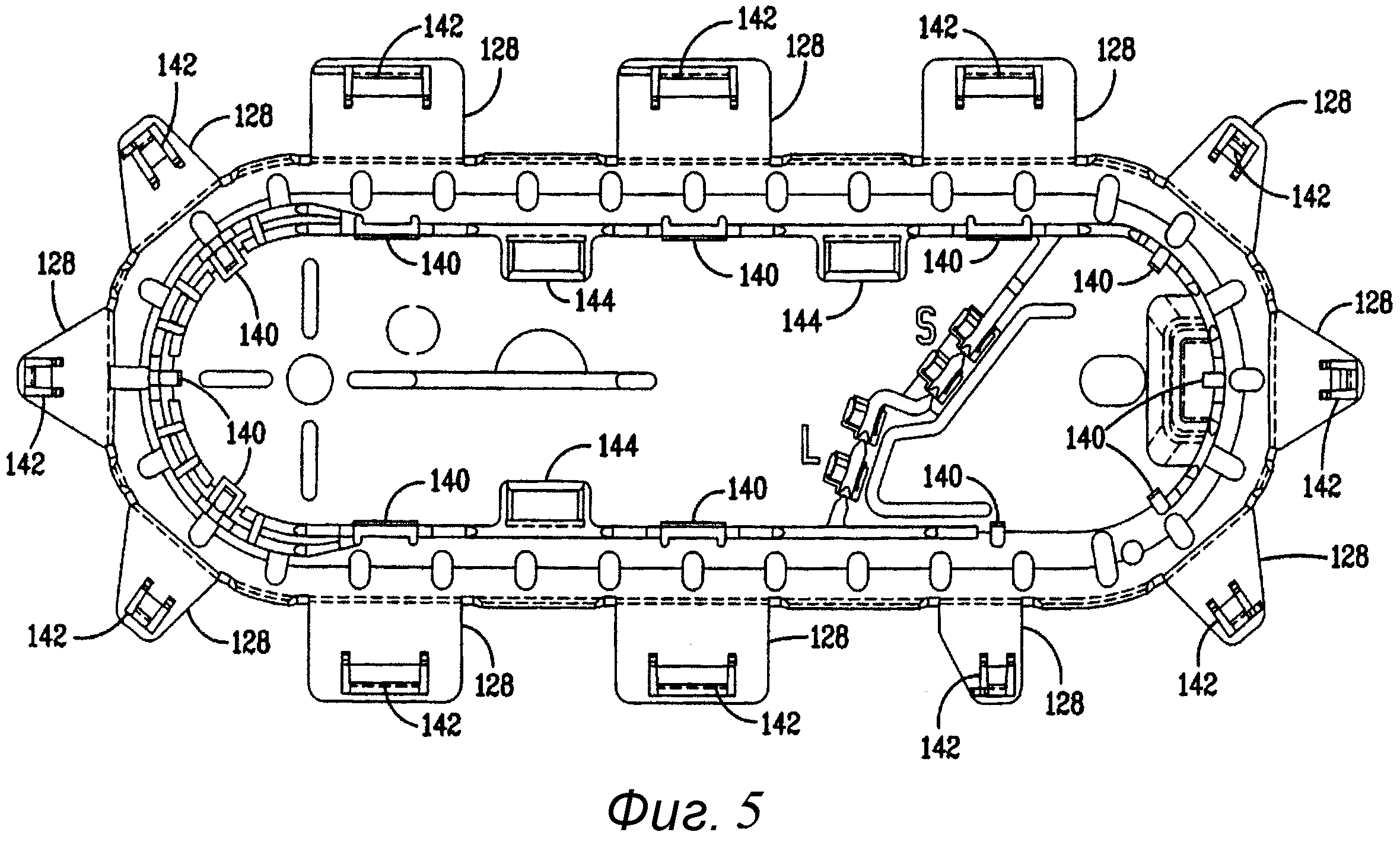
На фиг.5 представлен вид сверху на основную часть защитного отделения упакованного антимикробного медицинского устройства, соответствующего фиг.2.
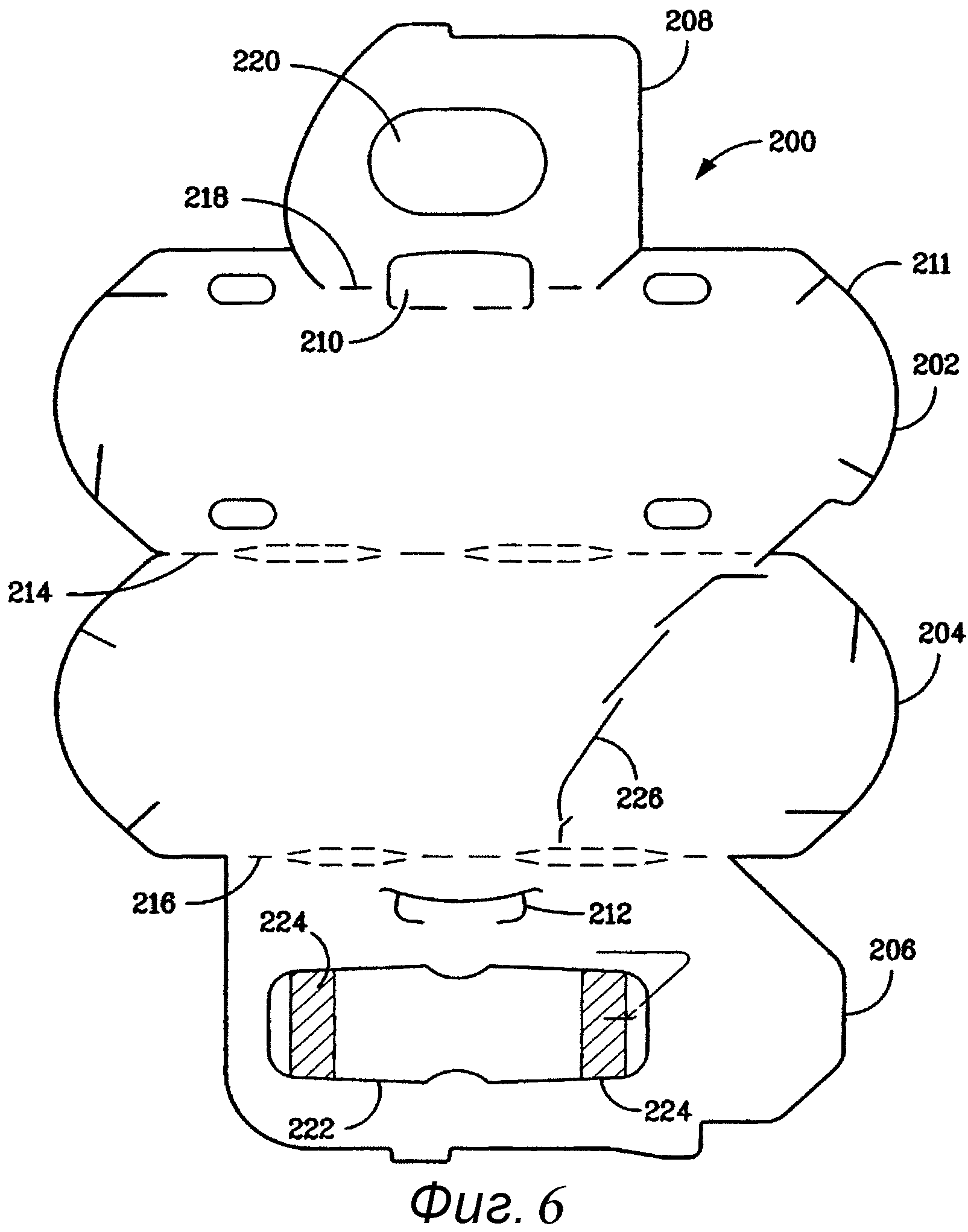
На фиг.6 представлен развернутый вид другого варианта внутренней упаковки, имеющего форму универсальной папки и соответствующего настоящему изобретению.
На фиг.7 показано процентное увеличение содержания триклозана в зависимости от времени хранения (при 25°C) в содержащей адсорбирующий материал упаковке шовной нити описанного в настоящем документе типа в сравнении с упаковкой шовной нити без адсорбента.
На фиг.8 показано процентное увеличение содержания триклозана в зависимости от времени хранения (при 25°C) в содержащей адсорбирующий материал упаковке шовной нити описанного в настоящем документе типа в сравнении с упаковкой шовной нити без адсорбента.
На фиг.9 показано процентное увеличение содержания триклозана в зависимости от времени хранения (при 50°C) в содержащей адсорбирующий материал упаковке шовной нити описанного в настоящем документе типа в сравнении с упаковкой шовной нити без адсорбента.
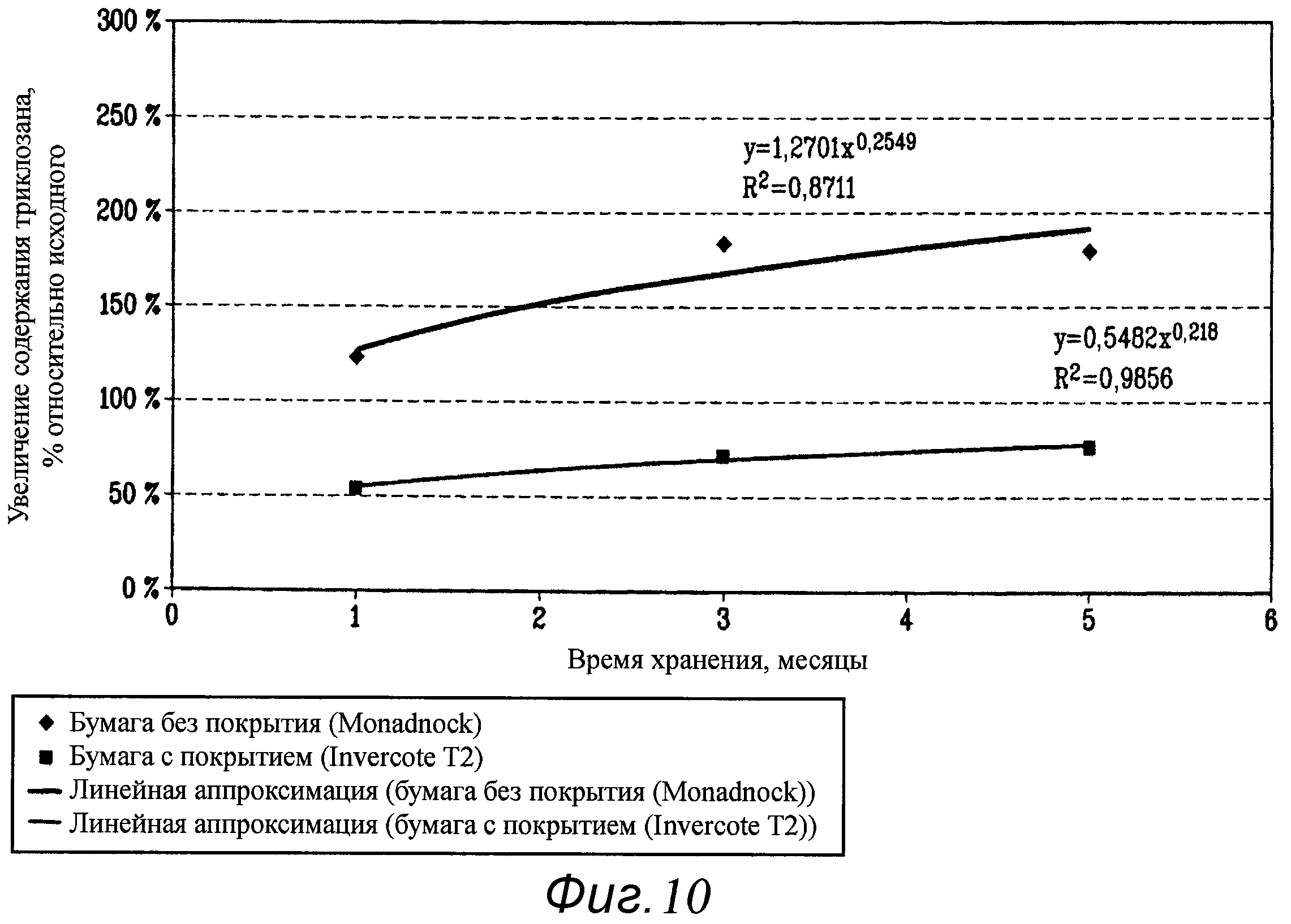
На фиг.10 показано процентное увеличение содержания триклозана в зависимости от времени хранения (при 50°C) в содержащей адсорбирующий материал упаковке шовной нити описанного в настоящем документе типа в сравнении с упаковкой шовной нити без адсорбента.
На фиг.11 показано процентное увеличение содержания триклозана в зависимости от времени хранения (при 25°C) в содержащей адсорбирующий материал упаковке шовной нити описанного в настоящем документе типа, в сравнении с упаковкой шовной нити без адсорбента.
На фиг.12 показано процентное увеличение содержания триклозана в зависимости от времени хранения (при 25°C) в содержащей адсорбирующий материал упаковке шовной нити описанного в настоящем документе типа в сравнении с упаковкой шовной нити без адсорбента.
На фиг.13 показано процентное увеличение содержания триклозана в зависимости от времени хранения (при 50°C) в содержащей адсорбирующий материал упаковке шовной нити описанного в настоящем документе типа в сравнении с упаковкой шовной нити без адсорбента.
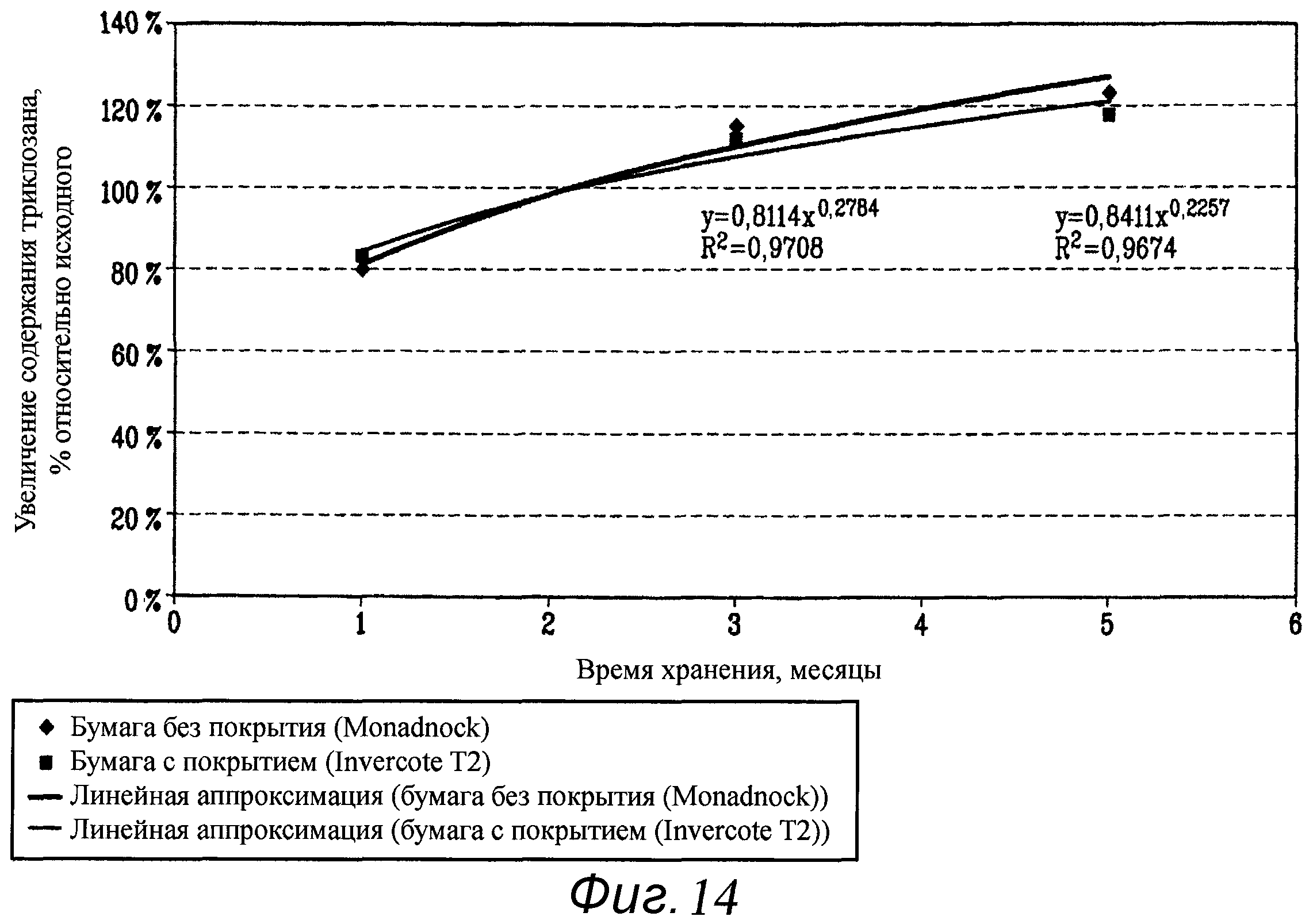
На фиг.14 показано процентное увеличение содержания триклозана в зависимости от времени хранения (при 50°C) в содержащей адсорбирующий материал упаковке шовной нити описанного в настоящем документе типа в сравнении с упаковкой шовной нити без адсорбента.
При ссылках на фиг.1-14 одинаковые номера обозначают одни и те же элементы на всех чертежах.
На фиг.1 показан один вариант осуществления упакованного антимикробного медицинского устройства 10. Упакованное антимикробное медицинское устройство 10 включает в себя внутреннюю упаковку 11, имеющую источник антимикробного агента. Медицинское устройство 14, которое может представлять собой иглу 16 и шовную нить 18, имеющее одну или несколько поверхностей 20, располагается внутри внутренней упаковки 11. В одном варианте внутренняя упаковка 11 содержит защитное отделение 12 и внешний чехол 22, причем внешний чехол 22 имеет одну поверхность 24, которая может быть покрыта адсорбирующим материалом. В одном варианте адсорбирующий материал эффективно поглощает со временем часть антимикробного агента. Наружная упаковка 50, имеющая внутреннюю поверхность 52, создана для герметичного запечатывания внутренней упаковки 11, помещенной внутрь наружной упаковки.
Защитное отделение 12 упакованного антимикробного медицинского устройства 10 имеет основную часть 26 и канальную покровную часть 28. Основная часть 26 имеет верхнюю сторону, нижнюю сторону и внешнюю периферическую зону 30. Как показано на чертеже, внешний чехол 22 может располагаться поверх канальной покровной части 28 и внутри внешней периферической зоны 30, закрывая по меньшей мере частично медицинское устройство 14. Основная часть 26 может представлять собой по существу плоскую деталь овальной формы, имеющую продольную ось. Хотя в случае с упаковкой шовной нити может быть желательным придать основной части 26 упакованного антимикробного медицинского устройства 10 овальную форму, могут использоваться и другие конфигурации, в том числе круглая, многоугольная, квадратная со скругленными углами и т.п., а также их сочетания и эквиваленты. Канальная покровная часть 28 имеет верхнюю сторону, нижнюю сторону, периферию 32 и продольную ось.
Сборка упакованного антимикробного медицинского устройства 10, составляющего предмет изобретения, может осуществляться следующим образом. Основная часть 26 совмещается с канальной покровной частью 28 так, чтобы заклепки, если они есть, совмещались с соответствующими отверстиями, а направляющие штифты, если они есть, совмещались с соответствующими отверстиями. Также штыри для намотки нити, если они есть, должны совмещаться с соответствующими отверстиями. Далее канальная покровная часть 28 устанавливается на основной части 26 таким образом, чтобы заклепки, если они есть, прошли в соответствующие отверстия, а направляющие штифты, если они есть, вошли в соответствующие отверстия. Концы заклепок, если таковые используются, могут быть расклепаны с использованием традиционных методов, таких как нагрев, ультразвуковое воздействие и т.п., так чтобы надежно закрепить канальную покровную часть 28 на основной части 26. В данном варианте, когда защитное отделение 12 сформировано таким образом, образуется канал 34, в котором может удобно размещаться шовная нить 18.
На фиг.2-5 представлен другой вариант осуществления упакованного антимикробного медицинского устройства 100. Упакованное антимикробное медицинское устройство 10 включает в себя внутреннюю упаковку 111, имеющую источник антимикробного агента. Медицинское устройство 114, которое может представлять собой иглу 116 и шовную нить 118, имеющее одну или несколько поверхностей 120, располагается внутри внутренней упаковки 111. В одном варианте внутренняя упаковка 111 содержит защитное отделение 112 и внешний чехол 122, и одна поверхность 124 внешнего чехла 122 может быть покрыта адсорбирующим материалом. Адсорбирующий материал эффективно поглощает со временем часть антимикробного агента. Наружная упаковка 150, имеющая внутреннюю поверхность 152, создана для герметичного запечатывания внутренней упаковки 111, помещенной внутрь наружной упаковки.
Защитное отделение 112 упакованного антимикробного медицинского устройства 100 имеет основную часть 126 и несколько покровных канальных клапанов 128. Основная часть 126 имеет верхнюю сторону, нижнюю сторону и внешнюю периферическую зону 130. В одном варианте внешний чехол 122 может располагаться поверх защитного отделения 112 и внутри внешней периферической зоны 130, закрывая по меньшей мере частично медицинское устройство 114.
Основная часть 126 может представлять собой по существу плоскую деталь овальной формы, имеющую продольную ось. Хотя в случае с упаковкой шовной нити может быть желательным придать основной части 126 упакованного антимикробного медицинского устройства 100 овальную форму, но могут использоваться и другие конфигурации, в том числе круглая, многоугольная, квадратная со скругленными углами и т.п., а также их сочетания и эквиваленты.
В частности, если обратиться к фиг.2-4, сборка упакованного антимикробного медицинского устройства 100, составляющего предмет настоящего изобретения, может осуществляться, как описано далее. Основная часть 126 может иметь несколько установочных штифтов 140. Покровные канальные клапаны 128 могут иметь несколько отверстий 142 под установочные штифты, куда при складывании покровных канальных клапанов 128 поверх установочных штифтов 140 должны входить установочные штифты 140. Далее покровные канальные клапаны 128 прикрепляются к установочным штифтам 140 основной части 126. Преимуществом является то обстоятельство, что можно избежать использования нагрева или ультразвукового воздействия для надежной фиксации канальных клапанов 128 к основной части 126. В данном варианте, когда защитное отделение 112 сформировано таким образом, образуется канал 134, в котором может удобно размещаться шовная нить 118.
В одном варианте, показанном на фиг.2-4, внешний чехол 122 может иметь несколько язычков 146, вставляемых в проушины 144, с целью закрепления внешнего чехла 122 к основной части 126 в пределах внешней периферической зоны 130 и по меньшей мере частичного закрытия медицинского устройства 114.
Прочая информация о конструкции и геометрии защитных отделений и упаковок, изготовленных с их использованием, более полно приводится в патентах США №№ 6047815, 6135272 и 6915623, содержание которых включено в настоящий документ посредством ссылки во всей полноте в отношении всего, что описано в этих патентах.
Защитные отделения 12 и 120 могут быть изготовлены из традиционных формуемых материалов. Особенно предпочтительным является использование полиолефиновых материалов, таких как полиэтилен и полипропилен, других термопластичных материалов и полиэстеров, таких как нейлон, и прочих подобных материалов. В одном варианте защитные отделения 12 и 120 настоящего изобретения могут формоваться методом литья под давлением, однако они также могут формоваться с использованием других принятых процессов и их эквивалентов, включая термоформование. При необходимости упаковки могут изготавливаться в виде отдельных узлов или компонентов, которые затем собираются воедино.
На фиг.6 представлен другой вариант реализации упакованного антимикробного медицинского устройства, имеющий внутреннюю упаковку 211, содержащую источник антимикробного агента. Специалисты в данной области могут оценить по достоинству то обстоятельство, что внутренняя упаковка 211 имеет форму универсальной папки и показана в развернутом плоском виде.
Видно, что внутренняя упаковка 211 включает первую главную внешнюю панель 202, вторую главную внешнюю панель 204, первую внутреннюю панель 206 и вторую внутреннюю панель 208. При складывании внутренней упаковки 211 в универсальный конверт первая внутренняя панель 206 загибается внутрь по линии сгиба 216, и вторая внутренняя панель 208 загибается внутрь по линии сгиба 218. Медицинское устройство (не показано), которое может представлять собой иглу и шовную нить и которое имеет одну или несколько поверхностей, помещается под вторую внутреннюю панель 208 внутренней упаковки 211 напротив внутренней поверхности второй главной внешней панели 204. Первая главная внешняя панель 202 может иметь язычок 210, соответствующий проушине 212, которая может находиться во второй внутренней панели 208, как показано на чертеже. В итоге внутренняя упаковка 211, первая главная внешняя панель 202 и вторая главная внешняя панель 204 складываются по линии сгиба 214, и язычок 210 вставляется в проушину 212. Как и в случае других вариантов реализации изобретения, описанных в данном документе, на одну поверхность может быть нанесен адсорбирующий материал, чтобы упакованное антимикробное медицинское устройство имело длительный срок хранения по сравнению с упакованным антимикробным медицинским устройством, не имеющим адсорбирующего материала.
Как и в случае других вариантов, описанных в данном документе, предлагается внешняя упаковка (не показана), которая имеет внутреннюю поверхность и герметично закрывает помещенную внутрь внутреннюю упаковку 211.
Медицинские устройства, описанные в настоящем документе, в основном представляют собой имплантируемые медицинские устройства и имплантаты, включая, помимо прочего, одноволоконные и многоволоконные шовные нити, хирургические сетки, например герниопластические сетки, герниопластические вставки, брахиотерапевтические прокладки, скобы и фиксаторы для соединения краев ран, противоадгезионные сетки и пленки, а также фиксаторы узлов шовной нити. Также сюда относятся рассасывающиеся и нерассасывающиеся имплантируемые медицинские устройства.
Под рассасывающимся полимером в настоящем документе понимается полимер, который, находясь под воздействием физиологических процессов, в течение некоторого периода времени разлагается и поглощается организмом. Рассасывающиеся медицинские устройства, как правило, создаются из общеизвестных традиционных рассасывающихся полимеров, включая, помимо прочего, гликолид, лактид, сополимеры гликолида, смеси полимеров, таких как полидиоксанон, поликапролактон, окисленная регенерированная целлюлоза и их эквиваленты. Предпочтительно такие полимеры включают полимерные материалы, выбираемые из группы, состоящей из гликолида со степенью полимеризации более 70%, лактида со степенью полимеризации более 70%, полимеризованного 1,4-диоксан-2-она, полипептида со степенью полимеризации более чем 70%, сополимеров гликолида и лактида, целлюлозных полимеров и производных целлюлозы со степенью полимеризации более 70%. Рассасывающиеся медицинские устройства предпочтительно изготавливают из полидиоксанона, полиглекапрона или гликолид-лактидного сополимера. К примерам рассасывающихся медицинских устройств относятся одноволоконные и многоволоконные шовные нити. К многоволоконным шовным нитям относятся шовные нити, где несколько волокон образуют плетеную нить. К примерам нерассасывающихся медицинских устройств относятся одноволоконные и многоволоконные шовные нити, хирургические сетки, такие как герниопластические сетки, герниопластические вставки и брахиотерапевтические прокладки, которые могут быть полимерными или неполимерными. Нерассасывающиеся медицинские устройства могут быть изготовлены полностью или частично из полимерных материалов, которые включают, помимо прочего, полиолефины, например полипропилен; полиамиды, например нейлон; хлорированные или фторированные углеводороды, такие как Тефлон (Teflon®); полиэстеры, такие как синтетические полиэстеры Дакрон (Dacron®); или из неполимерных материалов, к которым относятся, помимо прочего, шелк, коллаген, нержавеющая сталь, титан, кобальто-хромовый сплав, нитинол. Предпочтительно, чтобы нерассасывающиеся медицинские устройства изготавливались из нейлона или полипропилена.
В одном варианте к шовным нитям и иглам, которые могут быть упакованы в описанные в настоящем документе упаковки, относятся традиционные хирургические иглы и традиционные биорассасывающиеся или нерассасывающиеся хирургические шовные нити и их эквиваленты. Упаковки, составляющие предмет настоящего изобретения, могут использоваться для упаковывания шовных нитей малого диаметра. Ранее, при упаковке в лотки, это вызывало трудности, поскольку такую нить сложно было извлечь из упаковки и она застревала.
Подходящие антимикробные агенты могут быть выбраны из перечня, включающего, помимо прочего, галогенированные гидроксильные эфиры, ацилоксидифениловые эфиры или их сочетания. В частности, антимикробный агент может представлять собой галогенированный 2-гидроксидифениловый эфир и/или галогенированный 2-ацилоксидифениловый эфир, как описано в патенте США № 3629477 и как указано следующей формулой:
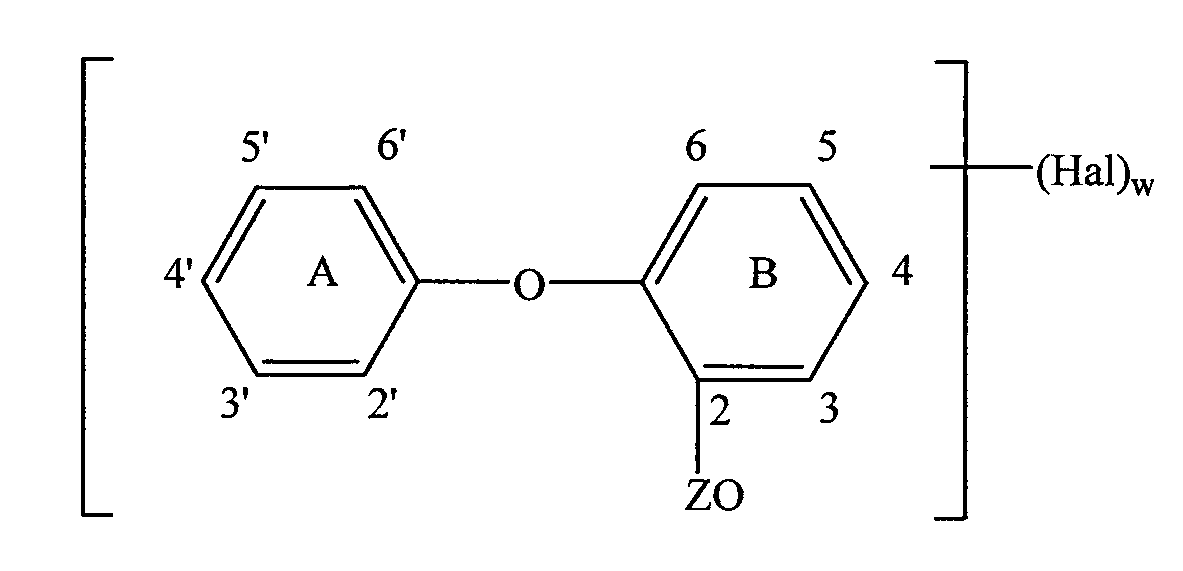
В вышеприведенной формуле каждый Hal обозначает разные или одинаковые атомы галогена, Z представляет собой атом водорода или ацильную группу, w представляет собой положительное целое число от 1 до 5, а каждое из бензольных колец, но предпочтительно кольцо А, также может содержать одну или несколько низших алкильных групп (которые могут быть галогенированными), низшую алкоксигруппу, аллильную группу, цианогруппу, аминогруппу или низшую алканоильную группу. Предпочтительно, в бензольных кольцах в качестве заместителей низших алкильных групп и низших алкоксигрупп могут использоваться, соответственно, метильные или метоксигруппы. Предпочтительной является галогенированная низшая алкильная группа, трифторметильная группа.
Антимикробная активность, сходная с активностью галоген-o-гидрокси-дифениловых эфиров с указанной выше формулой, также может быть получена с использованием их O-ацильных производных, которые частично или полностью гидролизуются в условиях, встречающихся на практике. Особенно подходящими являются сложные эфиры уксусной кислоты, хлоруксусной кислоты, метил- или диметилкарбаминовой кислоты, бензойной кислоты, хлорбензойной кислоты, метилсульфоновой кислоты и хлорметилсульфоновой кислоты.
Особо предпочтительным антимикробным агентом, соответствующим указанной выше формуле, является 2,4,4'-трихлор-2'-гидроксидифениловый эфир, обычно именуемый триклозаном (производится компанией Ciba Geigy под торговым наименованием Irgasan DP300 или Irgacare MP). Триклозан представляет собой белое порошкообразное твердое вещество с легким ароматическим/фенольным запахом. Как можно заметить, это хлорированное ароматическое соединение, имеющее функциональные группы, характерные как для простых эфиров, так и для фенолов.
Триклозан является антимикробным агентом широкого спектра действия, используемым в самых разных продуктах и являющимся эффективным в отношении множества микроорганизмов, часто связываемых с хирургическими раневыми инфекциями. К таким микроорганизмам относятся, не ограничиваясь этим перечнем, род Staphylococcus, Staphylococcus epidermidis, Staphylococcus aureus, устойчивый к метициллину Staphylococcus epidermidis, устойчивый к метициллину Staphylococcus aureus и их сочетания.
Наряду с антимикробными агентами, описанными выше, медицинское устройство может содержать бактерицидное, дезинфицирующее и/или антисептическое вещество. Их перечень включает, помимо прочего, спирты, например этанол и изопропанол; альдегиды, например глутаровый альдегид и формальдегид; анилиды, например трихлоркарбанилид; бигуаниды, например хлоргексидин; реагенты, выделяющие хлор, например гипохлорит натрия, двуокись хлора и кислый хлорит натрия; реагенты, выделяющие йод, например повидон-йод и полоксамер-йод; металлы, такие как нитрат серебра, сульфадиазин серебра и другие серебросодержащие агенты, медь-8-хинолат и тиолы висмута; пероксидные соединения, такие как пероксид водорода и перуксусная кислота; фенолы; соединения четвертичного аммония, такие как хлорид бензалкония, цетримид, и ионены - соединения поличетвертичного аммония. Медицинское устройство при необходимости может содержать антибиотики, включая, помимо прочего, пенициллины, такие как амоксициллин, оксациллин и пиперациллин; парентеральные цефалоспорины, такие как цефазолин, цефадроксил, цефокситин, цефпрозил, цефотаксим и цефдинир; монобактамы, такие как азтреонам; ингибиторы бета-лактамазы, такие как сульбактам клавулановой кислоты; гликопептид, такой как ванкомицин; полимиксин; хинолоны, такие как налидиксовая кислота, ципрофлоксацин и леваквин; метранидазол; новобиоцин; актиномицин; рифампин; аминогликозиды, такие как неомицин и гентамицин; тетрациклины, такие как доксициклин; хлорамфеникол; макролиды, такие как эритромицин; клиндамицин; сульфонамиды, например сульфадиазин; триметоприм; антибиотики местного применения; бацитрацин; грамицидин; мупироцин; и/или фусидовую кислоту. При необходимости медицинское устройство может содержать антимикробные пептиды, такие как дефензины, магаинин и низин; литический бактериофаг; поверхностно-активные вещества; блокаторы адгезии, например антитела, олигосахариды и гликолипиды; олигонуклеотиды, такие как антисмысловая РНК; ингибиторы откачивающих насосов; фоточувствительные красители, такие как порфирины; иммуномодуляторы, такие как ростовые факторы, интерлейкины, интерфероны и синтетические антигены; и/или хелатирующие агенты, такие как EDTA, гексаметафосфат натрия, лактоферрин и трансферрин.
Антимикробный агент может попадать в медицинское устройство из источника антимикробного агента, который располагается внутри или крепится к внутренней поверхности упаковки. В частности, антимикробный агент переносится из источника антимикробного агента на медицинское устройство, когда на источник антимикробного агента и на медицинское устройство оказывается воздействие такими температурой и давлением и в течение такого времени, как описано ниже. Например, источник антимикробного агента может представлять собой бумажный контейнер с антимикробным агентом, пористую подушку с антимикробным агентом, пластиковый контейнер с антимикробным агентом, губку или резервуар из пеноматериала с антимикробным агентом, пленку с антимикробным агентом (см. элемент) или таблетку с антимикробным агентом. Как вариант, источник антимикробного агента может быть частью самой упаковки, т.е. антимикробный агент встраивается в упаковку или наносится на нее, например (помимо прочего) наносится непосредственно на внутреннюю поверхность упаковки. Если источник антимикробного агента представляет собой бумажный или пластиковый резервуар, то такой резервуар может быть интегрирован в одну или несколько деталей упаковки.
Как уже отмечалось, в описанных в настоящем документе упакованных медицинских устройствах используется адсорбирующий материал с целью увеличения срока хранения по сравнению с упакованными антимикробными шовными нитями, где адсорбирующий материал не используется. Было показано, что срок хранения упакованного медицинского устройства, например шовной нити, содержащей триклозан, по-видимому, ограничивается концентрацией триклозана, которая увеличивается со временем при нормальных условиях хранения и условиях ускоренного старения. К удивлению, было обнаружено, что некоторые адсорбирующие материалы могут служить буферным средством, замедляющим скорость увеличения концентрации триклозана на медицинском устройстве.
Если вернуться к фиг.1, 2 и 6, в одном варианте реализации изобретения адсорбирующий материал создается путем нанесения покрытия из адсорбирующего материала по меньшей мере на часть одной поверхности внутренней упаковки 11, 111 или 211. В другом варианте адсорбирующий материал формируется путем помещения адсорбирующего субстрата (не показан) внутрь внешней упаковки. В другом варианте адсорбирующий субстрат формируется путем нанесения адсорбирующего материала на основу. В еще одном варианте адсорбирующий субстрат формируется из адсорбирующего материала. В еще одном варианте адсорбирующий материал, нанесенный по меньшей мере на часть одной поверхности внутренней упаковки, наносится по меньшей мере на одну поверхность внешнего чехла 22 или 122.
К адсорбирующим материалам, которые могут использоваться при практическом применении настоящего изобретения, относятся любые материалы, обладающие адсорбирующими свойствами, включая бентонит, активированный уголь, активированный глинозем, силикагель, цеолит, полимеры со сверхвысокой адсорбирующей способностью, гигроскопические вещества, полимерные покрытия, грунтовочные полимерные покрытия, продукты природного происхождения, небумажные субстраты, а также глины, в том числе каолин. Было доказано, что глины, в особенности каолин, являются особенно эффективными.
Если обратиться к фиг.6, внутренняя упаковка 211 представляет собой универсальный конверт из картонной массы, по меньшей мере одна поверхность которого покрыта адсорбирующим материалом. Подходящей картонной массой, которая может использоваться при практическом применении описанного в настоящем документе изобретения, является материал Invercote T2®, предлагаемый компанией Iggesund Paperboard of Edison, Нью-Джерси, США.
В дополнение к этому, на медицинское устройство при необходимости может быть нанесено покрытие и/или антимикробный агент может находиться на его одной или нескольких поверхностях еще до переноса антимикробного агента на медицинское устройство из источника антимикробного агента. Например, полезно нанести покрытие, в состав которого входит антимикробный агент, на поверхность медицинского устройства. Примеры медицинских устройств, а также покрытий, которые могут быть на них нанесены, можно найти в патентах США №№ 4201216, 4027676, 4105034, 4126221, 4185637, 3839297, 6260699, 5230424, 5555976, 5868244 и 5972008, каждый из которых полностью включен в настоящий документ. Как описано в патенте США № 4201216, покрытие может содержать пленкообразующий полимер и по существу нерастворимую в воде соль жирной кислоты с количеством углеродных атомов C6 или выше. В качестве другого примера, рассасывающееся покрытие, которое может использоваться в рассасывающемся медицинском устройстве, может содержать поли(алкилен оксалаты), где алкиленовые группы являются производными диолов C6 или смеси диолов от C4 до C12, которые наносятся на медицинское устройство из раствора, как описано в патенте США № 4105034. В состав покрытия может входить полимер или сополимер в качестве связующего агента, который может включать лактид и гликолид. В состав покрытия в качестве смазывающего вещества может входить стеарат кальция, а также антимикробный агент. Покрытие может наноситься на устройство с использованием способов нанесения из раствора, таких как нанесение погружением, нанесение напылением или нанесение каплевой взвесью, или любыми другими способами нанесения покрытий.
Рассасывающиеся медицинские устройства чувствительны к влажности, т.е. такие устройства будут разлагаться под действием влаги, содержащейся в атмосфере или в организме. Специалисту, имеющему среднюю степень подготовки в данной области техники, известно, что медицинские устройства, изготовленные из рассасывающихся полимеров, могут разрушаться и терять прочность, если они контактируют с водяными парами до использования в ходе хирургической операции. Например, желательные характеристики прочности шовной нити на растяжение внутри организма будут быстро утрачены, если до использования нить подвергалась воздействию влаги в течение сколько-нибудь значительного времени. Следовательно, для рассасывающихся медицинских устройств желательно использовать герметично закрытую упаковку. Под герметично закрытой упаковкой в настоящем документе понимается упаковка, изготовленная из материала, который служит барьером для поддержания стерильности и барьером против проникновения газов, т.е. предотвращает или по существу препятствует проникновению влаги и газа.
Если снова обратиться к фиг.1 и 2, к материалам, которые могут использоваться для изготовления наружной упаковки 50 и 150, и наружной упаковке, используемой в сочетании с универсальными конвертами, относятся, например, однослойные и многослойные материалы на основе обычной металлической фольги, часто называемые термосклеиваемой фольгой. Подобные продукты на основе фольги описаны в патенте США № 3815315, который полностью включен в настоящий документ в качестве ссылки. Другим пригодным к использованию типом продукта на основе фольги является фольгированный ламинат, который в отрасли называется отслаивающейся фольгой. Примеры такой отслаивающейся фольги и субстратов описаны в патенте США № 5623810, который полностью включен в настоящий документ в качестве ссылки. При необходимости для изготовления упаковок для рассасывающихся медицинских устройств вместе с металлической фольгой или вместо нее могут использоваться обычные неметаллизированные полимерные пленки. Подобные пленки являются полимерными и к ним относятся традиционно используемые полиолефины, полиэстеры, акриловые полимеры, галогенированные углеводороды и т.п., их сочетания и многослойные покрытия. Такие полимерные пленки по существу препятствуют проникновению влаги и кислорода и на них могут быть нанесены обычные покрытия, такие как, например, минеральные и минерал-оксидные покрытия, которые уменьшают или прекращают проникновение газов. Упаковка может включать в себя сочетание полимера и металлической фольги, в частности многослойный композитный материал из полимера и металлической фольги, например ламинат следующего состава: полиэстер/алюминиевая фольга/этакриловая кислота.
Нерассасывающиеся медицинские устройства могут быть упакованы в любые вышеописанные материалы. Кроме того, желательно упаковывать нерассасывающиеся медицинские устройства в упаковку, изготовленную из материала, способного обеспечить стерильность, например, в пористый материал, т.е. бумагу медицинского назначения или полимерную пленку или ткань, проницаемую для влаги и газов, например нетканый материал Tyvek® производства E. I. du Pont de Nemours and Company, Вилмингтон, штат Делавэр, США, а также изготовленную из волокон полиэтилена высокой плотности. Предпочтительно, чтобы нерассасывающиеся медицинские устройства упаковывали в те же упаковочные материалы, которые используются для рассасывающихся медицинских устройств, например герметично закрытые упаковки, если желательно, чтобы антимикробные медицинские устройства имели срок хранения не менее 6 месяцев, предпочтительно не менее 1 года, а наиболее предпочтительно не менее 2 лет.
Преобладающими микроорганизмами, ассоциирующимися с хирургическими раневыми инфекциями, передающимися через медицинские устройства, являются микроорганизмы рода Staphylococcus. Бактерии S. aureus и S. epidermidis часто присутствуют на коже пациента и, следовательно, легко попадают в рану. Антимикробным агентом, эффективно действующим на стафилококки, является 2,4,4'-трихлор-2'-гидроксидифениловый эфир. Минимальная ингибирующая концентрация (MIC) этого соединения в отношении S. aureus составляет 0,01 промилле, по данным измерения, проведенного в подходящей инкубационной среде и описанного Bhargava, H. et al в журнале American Journal of Infection Control, June 1996, стр. 209-218. Значение MIC для конкретного антимикробного агента и конкретного микроорганизма определяется как минимальная концентрация этого антимикробного агента, которая должна присутствовать в подходящей по всем прочим параметрам среде для культивирования данного микроорганизма, чтобы данная культуральная среда стала неподходящей для данного микроорганизма, т.е. это минимальная концентрация, ингибирующая рост данного микроорганизма. Фразы «количество, достаточное для по существу ингибирования образования колоний бактерий» и «эффективное количество» антимикробного агента в настоящем документе обозначают минимальную ингибирующую (или более высокую) концентрацию в отношении S. aureus.
Данное значение MIC продемонстрировано с помощью метода оценки чувствительности по диффузии с диска. Диск из фильтровальной бумаги или иного материала, пропитанный конкретным антимикробным агентом, накладывается на агар, засеянный тестовым микроорганизмом. Там, где антимикробный агент просачивается через агар, и в течение такого времени, когда концентрация антимикробного агента остается выше минимальной ингибирующей концентрации (MIC), чувствительные к агенту микроорганизмы не будут расти в области диска и на некотором расстоянии вокруг него. Это расстояние называется зоной ингибирования. Если предположить, что антимикробный агент имеет в среде (агаре) некоторую скорость диффузии, наличие зоны ингибирования вокруг диска, пропитанного антимикробным агентом, указывает на то, что рост микроорганизмов ингибируется вследствие присутствия антимикробного агента в среде, которая по всем прочим параметрам подходит для роста. Диаметр зоны ингибирования обратно пропорционален значению MIC.
В соответствии с различными способами, применяемыми в рамках настоящего изобретения, предлагается способ изготовления упакованной антимикробной шовной нити, имеющей длительный срок хранения, согласно которому:
создают внутреннюю упаковку, содержащую источник антимикробного агента;
создают адсорбирующий материал, который эффективно поглощает со временем часть антимикробного агента;
помещают шовную нить во внутреннюю упаковку, причем шовная нить имеет одну или более поверхностей;
закрывают внутреннюю упаковку внешней упаковкой, имеющей внутреннюю поверхность; и
воздействуют на шовную нить, внутреннюю упаковку и внутреннюю поверхность внешней упаковки такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к шовной нити и к внутренней упаковке, в результате чего по существу ингибируется образование колоний бактерий на шовной нити и внутренней упаковке.
Благоприятным является то обстоятельство, что произведенная таким способом упакованная антимикробная шовная нить имеет длительный срок хранения по сравнению с упакованной антимикробной шовной нитью, изготовленной без использования адсорбирующего материала.
Как будет более подробно описано далее, этап воздействия на шовную нить, внутреннюю упаковку и внутреннюю поверхность наружной упаковки условий, способствующих переносу паров эффективного количества антимикробного агента, включает в себя: помещение внешней упаковки, внутри которой находится внутренняя упаковка и шовная нить, в стерилизационное устройство, нагревание стерилизационного устройства до первой температуры, установку давления в стерилизационном устройстве в соответствии с первым значением давления, подачу пара в стерилизационное устройство с целью обработки водяным паром внутренней поверхности наружной упаковки, внутренней упаковки и нити в течение первого интервала времени, установку давления в стерилизационном устройстве в соответствии со вторым значением давления, введение химического стерилизующего реагента в стерилизационное устройство на второй интервал времени, чтобы сделать нежизнеспособным достаточное количество микроорганизмов, удаление остатков влаги и химического стерилизационного агента с шовной нити и высушивание упакованной антимикробной шовной нити до желательного уровня влажности. В одном варианте реализации изобретения этап введения химического стерилизующего агента включает подачу газообразного этиленоксида в стерилизационное устройство.
В одном варианте антимикробный агент действует непосредственно на медицинское устройство, т.е. источник антимикробного агента расположен в упаковке, содержащей медицинское устройство. Например, упаковка может содержать источник антимикробного агента, источник антимикробного агента может быть прикреплен к внутренней поверхности упаковки, или же источник антимикробного агента может быть интегрирован в один или нескольких упаковочных компонентов внутри упаковки или в саму эту упаковку. В этих вариантах медицинское устройство располагается внутри упаковки и изначально может не содержать антимикробного агента или же изначально может иметь одну или несколько поверхностей, на которые нанесен антимикробный агент. Как уже отмечалось, затем упаковка, источник антимикробного агента и медицинское устройство подвергаются действию таких температуры и давления и в течение такого времени, которые являются достаточными для переноса паров антимикробного агента от источника антимикробного агента к медицинскому устройству, что позволяет по существу ингибировать образование колоний бактерий на медицинском устройстве.
В случае, если медицинское устройство изначально не содержит антимикробного агента, антимикробный агент подается к медицинскому устройству от источника антимикробного агента, когда упаковка, источник антимикробного агента и медицинское устройство подвергаются действию таких температуры и давления и в течение такого времени, которые достаточны для частичного переноса паров антимикробного агента от источника антимикробного агента к медицинскому устройству.
В случае, если на одну или несколько поверхностей медицинского устройства изначально нанесен антимикробный агент, в течение соответствующего времени используются температура и давление, достаточные для частичного переноса паров антимикробного агента, нанесенного на медицинское устройство, и антимикробного агента, находящегося в источнике антимикробного агента, на внутреннюю поверхность упаковки. При этом на медицинском устройстве должно остаться эффективное количество антимикробного агента, что позволит по существу ингибировать образование колоний бактерий на медицинском устройстве и на внутренней поверхности упаковки. В данном варианте количество или концентрация антимикробного агента на медицинском устройстве стабилизируется путем введения дополнительного количества антимикробного агента в среду упаковки.
В ином варианте медицинское устройство может находиться внутри упаковки, и внешний источник антимикробного агента оказывает непрямое воздействие на упаковку с медицинским устройством, т.е. источник антимикробного агента является внешним по отношению к упаковке, содержащей медицинское устройство. В частности, упаковка, источник антимикробного агента и медицинское устройство внутри упаковки подвергаются действию таких температуры и давления и в течение такого времени, которые являются достаточными для переноса паров антимикробного агента от источника антимикробного агента к медицинскому устройству, что позволяет по существу ингибировать образование колоний бактерий на медицинском устройстве. В данном варианте упаковка может быть изготовлена из материала, служащего барьером для поддержания стерильности, например пористого материала или полимерной пленки, проницаемой для влаги и газов, так, чтобы газообразный антимикробный агент мог проникать или передаваться от источника в виде паров сквозь упаковку. Например, упаковка, содержащая медицинское устройство, может помещаться в герметично закрытую среду, а источник антимикробного агента может содержаться внутри герметично закрытой среды или же может подаваться в герметично закрытую среду впоследствии. Источником антимикробного агента может быть любая парообразная форма антимикробного агента.
Скорость переноса паров антимикробного агента, например триклозана, от источника антимикробного агента к медицинскому устройству в основном зависит от времени, температуры и давления, при которых осуществляется изготовление, хранение и использование упаковки с медицинским устройством. Эффективному переносу паров антимикробного агента, такого как триклозан, способствуют условия, включающие замкнутую среду, давление, равное атмосферному, и температуру более 40°C, действующие в течение периода времени от 4 до 8 часов. Также этому способствуют любые сочетания давления и температуры, которые делают парциальное давление антимикробного агента равным или превышающим парциальное давление в описанных выше условиях. При этом период времени должен быть достаточен для получения эффективной концентрации антимикробного агента на медицинском устройстве, т.е. минимальной ингибирующей концентрации (MIC) для S. aureus (или более высокой). В частности, специалисту, имеющему среднюю степень подготовки в данной области техники, известно, что, снизив давление, можно добиться того же парциального давления при более низкой температуре. В ином варианте, уменьшив давление и сохранив постоянную температуру, можно добиться того, что эффективное количество или концентрация антимикробного агента будут достигнуты быстрее. В целом, количество антимикробного агента в источнике антимикробного агента по меньшей мере таково, чтобы на медицинское устройство при воздействии описанных ниже параметров переносилось эффективное количество антимикробного агента.
Медицинские устройства, как правило, подвергаются стерилизации, чтобы находящиеся на них микроорганизмы утратили жизнеспособность. В частности, стерильностью в данной отрасли считается минимальная степень гарантированной стерильности 10-6. Примеры процессов стерилизации описаны в патентах США №№ 3815315, 3068864, 3767362, 5464580, 5128101 и 5868244, каждый из которых полностью включен в настоящий документ. В частности, рассасывающиеся медицинские устройства могут быть чувствительны к облучению и нагреву. Соответственно, может быть желательным проводить стерилизацию таких устройств с помощью обычно используемых стерилизующих газов или агентов, таких, например, как газообразный этиленоксид.
Ниже описывается процесс стерилизации этиленоксидом, поскольку параметры времени, температуры и давления, используемые в ходе процесса этиленоксидной стерилизации, являются достаточными для переноса паров антимикробного агента от источника антимикробного агента к медицинскому устройству. Однако параметры времени, температуры и давления, достаточные для переноса паров антимикробного агента от источника антимикробного агента к медицинскому устройству, могут использоваться отдельно или в другом типе процесса стерилизации, и они не ограничиваются процессом этиленоксидной стерилизации или процессами стерилизации вообще.
Как отмечалось выше, рассасывающиеся медицинские устройства являются чувствительными к влаге, и, следовательно, они часто упаковываются в герметичные фольгированные упаковки. Однако герметичная фольгированная упаковка также непроницаема и для стерилизующего газа. Чтобы компенсировать это явление и иметь возможность использовать упаковки из фольги при стерилизации газообразным этиленоксидом, были разработаны процессы, в ходе которых используются фольгированные упаковки, имеющие вентиляционные приспособления для пропускания газов (например, нетканый материал Tyvek® производства E. I. du Pont de Nemours and Company, Уилмингтон, штат Делавэр, США). Вентиляционные приспособления устанавливаются на открытый конец упаковки и пропускают воздух, водяные пары и этиленоксид внутрь упаковки. После завершения процесса стерилизации упаковку запечатывают вблизи вентиляционного приспособления так, что приспособление отделяется от запечатанной упаковки, а затем отрезается или убирается иным образом, в результате чего получается герметично запечатанная упаковка. Другим типом упаковки из фольги, имеющей вентиляционное отверстие, является упаковка типа мешка, имеющая вентиляционное приспособление, установленное вблизи одного конца упаковки, причем вентиляционное приспособление герметично закрепляется к одной из сторон упаковки, образуя вентилируемую часть. После завершения процесса стерилизации упаковку запечатывают вблизи вентилируемой части, и запечатанную упаковку отрезают у вентилируемой части.
В одном варианте источник антимикробного агента помещают внутрь упаковки, прикрепляют к внутренней поверхности упаковки или встраивают в один или несколько компонентов упаковки или в саму упаковку. После запечатывания периферических и боковых швов упаковки упакованное медицинское устройство можно помещать в обычный аппарат для стерилизации этиленоксидом. Если упаковка изготовлена из фольги, источник антимикробного агента может представлять собой любой из описанных выше источников антимикробного агента или же это может быть газопроницаемое вентиляционное приспособление, в котором содержится антимикробный агент. Например, антимикробным агентом, таким как триклозан, можно пропитать газопроницаемый вентиляционный материал Tyvek®, для чего на полосу материала Tyvek® наносят раствор этилацетата и триклозана. Содержащее антимикробный агент вентиляционное приспособление помещают внутрь упаковки и устанавливают на материал герметичной упаковки; медицинское устройство помещают внутрь материала герметичной упаковки; периферическую зону материала герметичной упаковки запечатывают так, чтобы медицинское устройство было закрыто, а газы могли проникать внутрь материала герметичной упаковки через вентиляционное приспособление; на упаковочный материал с пропитанным антимикробным агентом вентиляционным приспособлением и на медицинское устройство оказывают воздействие такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от пропитанного антимикробным агентом вентиляционного приспособления на медицинское устройство. Упаковочный материал запечатывают, закрывая медицинское устройство и отделяя вентиляционное приспособление. Вентиляционное приспособление отрезают, в результате чего получается антимикробное медицинское устройство.
В другом варианте источник антимикробного агента может вводиться в стерилизационное или иное устройство вне упаковки, содержащей медицинское устройство. Например, медицинское устройство помещают внутрь упаковки; на упаковку, содержащую медицинское устройство, оказывают воздействие со стороны источника антимикробного агента; упаковку с медицинским устройством и источник антимикробного агента подвергают действию таких температуры и давления и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента к медицинскому устройству внутри упаковки, что позволяет по существу ингибировать образование колоний бактерий на медицинском устройстве. Упаковка может быть изготовлена из материала, способного обеспечить стерильность, например из пористого материала или из полимерной пленки, проницаемой для влаги и газов, или из материала, позволяющего создать герметично закрытую упаковку.
Перед запуском цикла стерилизации внутреннюю температуру в аппарате можно довести приблизительно до 25°C. На всем протяжении циклов увлажнения и стерилизации температура в аппарате должна составлять приблизительно от 22 до 37°C. Далее в стерилизационном аппарате можно включить вакуумирование и довести разряжение приблизительно до 1,8-6,0 кПа. Затем в ходе цикла увлажнения может быть включена подача пара, служащего источником водяных паров для стерилизации изделия. Упакованные медицинские устройства можно обрабатывать паром в стерилизаторе в течение приблизительно 60-90 минут. Однако время обработки может изменяться в зависимости от стерилизуемого медицинского устройства.
После увлажняющей части цикла можно увеличить давление в стерилизационном аппарате путем подачи сухого инертного газа, например азота. Давление следует поднять так, чтобы оно находилось в диапазоне приблизительно от 42 до 48 кПа. После достижения нужного давления в стерилизационный аппарат можно подать этиленоксид, пока давление не достигнет приблизительно 95 кПа. Воздействие этиленоксидом можно осуществлять в течение времени, достаточного для эффективной стерилизации упакованного медицинского устройства. Например, для хирургических шовных нитей воздействие этиленоксидом в стерилизационном аппарате может продолжаться приблизительно от 360 до 600 минут. Время, требующееся для стерилизации других медицинских устройств, может быть иным, в зависимости от типа изделия и упаковки. Далее этиленоксид можно отвести из стерилизационного аппарата, и аппарат можно выдержать в условиях вакуума при давлении приблизительно 0,07 кПа в течение приблизительно 150-300 минут, чтобы удалить остатки влаги и этиленоксида из стерилизованных упакованных медицинских устройств. Затем давление в стерилизационном аппарате можно снова довести до атмосферного.
Следующим этапом процесса является цикл сушки. Упакованное медицинское устройство можно высушить сухим азотом или вакуумированием с использованием такого количества циклов, которое достаточно для эффективного удаления до заранее установленного уровня остаточной влаги и водяных паров из упакованного медицинского устройства. На протяжении этих циклов медицинское устройство может подвергаться действию многократных повышений и снижений давления при температурах, превышающих комнатную. В частности, температура в рубашке сушильной камеры на протяжении всего цикла сушки может поддерживаться на уровне приблизительно 53-57°C. Но в случае шовных нитей могут использоваться и более высокие температуры, например от приблизительно 65°C до 70°C, а в зависимости от стерилизуемого медицинского устройства - и еще более высокие температуры. Типичный цикл сушки включает увеличение давления до 100 кПа путем подачи азота, снижение давления в камере до приблизительно 0,07 кПа на период 180-240 минут, снова подачу азота с увеличением давления до 100 кПа и циркуляцию азота в течение приблизительно 90 минут, снижение давления в камере до приблизительно 0,01 кПа на период от приблизительно 240 до 360 минут и выдерживание при давлении не более 0,005 кПа еще в течение 4-96 часов. После завершения циклов увлажнения, стерилизации и сушки, для чего, как правило, требуется приблизительно 24 часов, давление в камере возвращается к атмосферному путем подачи сухого азота. Когда высушивание до заданного уровня содержания влаги завершено, упакованное медицинское устройство можно извлечь из сушильной камеры и хранить в помещении с контролируемой влажностью.
После завершения процесса стерилизации на антимикробном медицинском устройстве, упаковке и/или элементе упаковки будет содержаться антимикробный агент в количестве, достаточном для ингибирования по существу образования колоний бактерий на антимикробном устройстве или поблизости от него, на упаковке и/или на элементе упаковки.
Как отмечалось выше, срок хранения упакованного медицинского устройства, например шовной нити, содержащей триклозан, может ограничиваться концентрацией триклозана, которая увеличивается со временем при нормальных условиях хранения и условиях ускоренного старения. Вследствие этого явления в некоторых случаях срок хранения ограничивается периодом, не превышающим двух лет. В описанных в настоящем документе упакованных медицинских устройствах используется адсорбирующий материал с целью увеличения срока хранения по сравнению с упакованными антимикробными шовными нитями, где адсорбирующий материал не используется. В соответствии со способами, описанными здесь, в одном варианте реализации изобретения способ изготовления упакованного антимикробного устройства включает в себя этап нанесения покрытия из адсорбирующего материала по меньшей мере на часть одной поверхности внутренней упаковки. В другом варианте адсорбирующий материал формируется путем помещения адсорбирующего субстрата внутрь внешней упаковки. В еще одном варианте адсорбирующий субстрат формируется путем нанесения адсорбирующего материала на основу. В еще одном варианте адсорбирующий субстрат формируется из адсорбирующего материала. В еще одном варианте внутренняя упаковка представляет собой универсальный конверт из картонной массы, по меньшей мере одна поверхность которого покрыта адсорбирующим материалом.
К адсорбирующим материалам, которые могут использоваться при практическом применении настоящего изобретения, относятся любые материалы, обладающие адсорбирующими свойствами, включая бентонит, активированный уголь, активированный глинозем, силикагель, цеолит, полимеры со сверхвысокой адсорбирующей способностью, гигроскопические вещества, полимерные покрытия, грунтовочные полимерные покрытия, продукты природного происхождения, небумажные субстраты, а также глины, в том числе каолин. Было доказано, что глины, в особенности каолин, являются особенно эффективными.
В одном варианте реализации изобретения предлагается способ увеличения срока хранения упакованного антимикробного медицинского устройства, согласно которому:
создают внутреннюю упаковку, содержащую источник антимикробного агента;
создают адсорбирующий материал, который эффективно поглощает со временем часть антимикробного агента;
помещают медицинское устройство во внутреннюю упаковку, причем медицинское устройство имеет одну или более поверхностей;
закрывают внутреннюю упаковку внешней упаковкой, имеющей внутреннюю поверхность; и
воздействуют на медицинское устройство, внутреннюю упаковку и внутреннюю поверхность внешней упаковки такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к медицинскому устройству и к внутренней упаковке, в результате чего по существу ингибируется образование колоний бактерий на медицинском устройстве и внутренней упаковке,
причем упакованное антимикробное медицинское устройство проявляет свойства возможности хранения в течение длительного срока по сравнению с упакованным медицинским устройством, в котором адсорбирующий материал не используется.
Настоящее изобретение далее будет рассмотрено более конкретно со ссылкой на следующие не ограничивающие изобретение примеры.
Примеры
Была проведена серия исследований устойчивости с использованием шовных нитей PDS Plus® (одноволоконная нить из полидиоксанона, предлагаемая компанией Ethicon, Inc.), упакованных в универсальные конверты и раздаточные лотки. Исследования проведены на шовных нитях размера 1 и размера 3/0. Для каждого сочетания размер нити/конфигурация упаковки были приготовлены образцы с использованием бумажной массы без покрытия, производства Monadnock Paper Mills, Inc., Беннингтон, штат Нью-Гемпшир, США, и бумажной массы с покрытием из глины (Invercote T2®, производитель Iggesund Paperboard, Эдисон, штат Нью-Джерси, США). Ниже приведены обозначения, использованные при исследовании:
VAP2005-003 PDS Plus® - универсальный конверт - бумага без покрытия
VAP2007-058 PDS Plus® - универсальный конверт - бумага с покрытием
VAP2005-003 PDS Plus® - раздаточный лоток - бумага без покрытия
VAP2007-054 PDS Plus® -раздаточный лоток - бумага с покрытием.
В каждом исследовании готовое изделие хранилось при 50°C до 5 месяцев и при 25°C до 24 месяцев. В указанные сроки образцы тестировали на содержание триклозана в шовной нити, и результаты сравнивали с исходными значениями. Для каждого сочетания условий тестирования использовали множество дозировок триклозана.
Пример 1. Нить PDS Plus, размер 1, в универсальном конверте, хранили при 25°C
Исследования устойчивости проводили с использованием шовных нитей PDS Plus® размера 1, упакованных в универсальные конверты. В каждом исследовании готовое изделие хранили при 25°C до 24 месяцев. Образцы тестировали на содержание триклозана в шовной нити и результаты сравнивали с исходными значениями. Результаты исследования представлены ниже и отображены графически на фиг.7.
Пример 2. Нить PDS Plus, размер 3/0, в универсальном конверте, хранили при 25°C
Исследования устойчивости проводили с использованием шовных нитей PDS Plus® размера 3/0, упакованных в универсальные конверты. В каждом исследовании готовое изделие хранили при 25°C до 24 месяцев. Образцы тестировали на содержание триклозана в шовной нити и результаты сравнивали с исходными значениями. Результаты исследования представлены ниже и отображены графически на фиг.8.
Пример 3. Нить PDS Plus, размер 1, в универсальном конверте, хранили при 50°C
Исследования устойчивости проводили с использованием шовных нитей PDS Plus® размера 1, упакованных в универсальные конверты. В каждом исследовании готовое изделие хранили при 50°C до 5 месяцев. Образцы тестировали на содержание триклозана в шовной нити и результаты сравнивали с исходными значениями. Результаты исследования представлены ниже и отображены графически на фиг.9.
Пример 4. Нить PDS Plus, размер 3/0, в универсальном конверте, хранили при 50°C
Исследования устойчивости проводили с использованием шовных нитей PDS Plus® размера 3/0, упакованных в универсальные конверты. В каждом исследовании готовое изделие хранили при 50°C до 5 месяцев. Образцы тестировали на содержание триклозана в шовной нити и результаты сравнивали с исходными значениями. Результаты исследования представлены ниже и отображены графически на фиг.10.
Пример 5. Нить PDS Plus, размер 1, в раздаточном лотке, хранили при 25°C
Исследования устойчивости проводили с использованием шовных нитей PDS Plus® размера 1, упакованных в раздаточные лотки такого типа, как представленные на фиг.2-5. В каждом исследовании готовое изделие хранили при 25°C до 24 месяцев. Образцы тестировали на содержание триклозана в шовной нити и результаты сравнивали с исходными значениями. Результаты исследования представлены ниже и отображены графически на фиг.11.
Пример 6. Нить PDS Plus, размер 3/0, в раздаточном лотке, хранили при 25°C
Исследования устойчивости проводили с использованием шовных нитей PDS Plus® размера 3/0, упакованных в раздаточные лотки такого типа, как представленные на фиг.2-5. В каждом исследовании готовое изделие хранили при 25°C до 24 месяцев. Образцы тестировали на содержание триклозана в шовной нити и результаты сравнивали с исходными значениями. Результаты исследования представлены ниже и отображены графически на фиг.12.
Пример 7. Нить PDS Plus, размер 1, в раздаточном лотке, хранили при 50°C
Исследования устойчивости проводили с использованием шовных нитей PDS Plus® размера 1, упакованных в раздаточные лотки такого типа, как представленные на фиг.2-5. В каждом исследовании готовое изделие хранили при 50°C до 5 месяцев. Образцы тестировали на содержание триклозана в шовной нити и результаты сравнивали с исходными значениями. Результаты исследования представлены ниже и отображены графически на фиг.13.
Пример 8. Нить PDS Plus, размер 3/0, в раздаточном лотке, хранили при 50°C
Исследования устойчивости проводили с использованием шовных нитей PDS Plus® размера 3/0, упакованных в раздаточные лотки такого типа, как представленные на фиг.2-5. В каждом исследовании готовое изделие хранили при 50°C до 5 месяцев. Образцы тестировали на содержание триклозана в шовной нити и результаты сравнивали с исходными значениями. Результаты исследования представлены ниже и отображены графически на фиг.14.
Все патенты, тестовые процедуры и прочие цитированные документы, в том числе документы о приоритетах, включены путем ссылки полностью в настоящий документ в той мере, в которой раскрытие их содержания не является неприемлемым, и для всех сфер юрисдикции, в которых такое инкорпорирование является допустимым.
Хотя примеры вариантов реализации изобретения, включенные в настоящий документ, содержат детальные описания, следует понимать, что для специалиста в данной области могут быть очевидными и легко реализуемыми различные иные модификации, что не будет отклонением от духа и сферы применения содержания, изложенного в данном документе. Соответственно, не предполагается ограничивать сферу действия пунктов патентной формулы, прилагаемых к настоящему документу, примерами и описаниями, приведенными в настоящем документе. Напротив, именно пункты патентной формулы изобретения следует считать включающими все характеристики описываемых патентуемых нововведений, в том числе все характеристики, которые могли бы быть истолкованы специалистами в области, к которой относится это описание, как эквивалентные описанным.
Если в настоящем документе указываются числовые значения верхних и нижних пределов, диапазоны от любого нижнего предела до любого верхнего предела проанализированы.
Дополнительные аспекты изобретения
Как отмечалось ранее, в настоящем документе приводится описание и заявляется право на способ увеличения срока хранения упакованного медицинского устройства. В одном варианте реализации изобретения адсорбирующий материал формируется путем нанесения покрытия из адсорбирующего материала по меньшей мере на часть одной поверхности внутренней упаковки. В другом варианте адсорбирующий материал формируется путем помещения адсорбирующего субстрата внутрь внешней упаковки. В другом варианте адсорбирующий субстрат формируется путем нанесения адсорбирующего материала на основу. В другом варианте адсорбирующий субстрат формируется из адсорбирующего материала. В другом варианте внутренняя упаковка представляет собой универсальный конверт из картонной массы, по меньшей мере одна поверхность которого покрыта адсорбирующим материалом. В другом варианте адсорбирующий материал выбирают из бентонита, активированного угля, активированного глинозема, силикагеля, цеолита, полимеров со сверхвысокой абсорбирующей способностью, гигроскопических веществ, полимерных покрытий, грунтовочный полимерный покрытий, продуктов природного происхождения, небумажных субстратов, а также глин, в том числе каолина. В другом варианте внутренняя упаковка содержит защитное отделение и внешний чехол, и одна поверхность внешнего чехла покрыта адсорбирующим материалом. В другом варианте адсорбирующий материал выбирают из бентонита, активированного угля, активированного глинозема, силикагеля, цеолита, полимеров со сверхвысокой абсорбирующей способностью, гигроскопических веществ, полимерных покрытий, грунтовочных полимерных покрытий, продуктов природного происхождения, небумажных субстратов, а также глин, в том числе каолина.
Как отмечалось ранее, в настоящем документе приводится описание и заявляется право на упакованную антимикробную шовную нить, имеющую длительный срок хранения. В одном варианте реализации изобретения упакованная антимикробная шовная нить характеризуется длительным сроком хранения. В другом варианте адсорбирующий материал формируется путем нанесения покрытия из упомянутого адсорбирующего материала по меньшей мере на часть одной поверхности упомянутой внутренней упаковки. В другом варианте адсорбирующий материал формируется путем помещения адсорбирующего субстрата внутрь упомянутой внешней упаковки. В другом варианте адсорбирующий субстрат формируется путем нанесения адсорбирующего материала на основу. В другом варианте адсорбирующий субстрат формируется из адсорбирующего материала. В другом варианте антимикробный агент выбирают из упомянутой группы, состоящей из галогенированных гидроксильных простых эфиров, ацилоксидифениловых простых эфиров и их сочетаний. В другом варианте внутренняя упаковка представляет собой универсальный конверт из картонной массы, одна поверхность которого покрыта адсорбирующим материалом. В другом варианте адсорбирующий материал выбирают из бентонита, активированного угля, активированного глинозема, силикагеля, цеолита, полимеров со сверхвысокой абсорбирующей способностью, гигроскопических веществ, полимерных покрытий, грунтовочных полимерных покрытий, продуктов природного происхождения, небумажных субстратов, а также глин, в том числе каолина. В другом варианте внутренняя упаковка содержит защитное отделение и внешний чехол, и одна поверхность указанного внешнего чехла покрыта адсорбирующим материалом. В другом варианте адсорбирующий материал выбирают из бентонита, активированного угля, активированного глинозема, силикагеля, цеолита, полимеров со сверхвысокой абсорбирующей способностью, гигроскопических веществ, полимерных покрытий, грунтовочных полимерных покрытий, продуктов природного происхождения, небумажных субстратов, а также глин, в том числе каолина.
Реферат
Группа изобретений относится к медицине, а именно к медицинской технике, и предназначено для обеспечения антимикробной среды вокруг стерилизованного медицинского устройства. Для изготовления упакованной антимикробной шовной нити создают внутреннюю упаковку, содержащую источник антимикробного агента, и адсорбирующий материал, который эффективно поглощает со временем часть антимикробного агента. Шовную нить помещают во внутреннюю упаковку, причем шовная нить имеет одну или более поверхностей. Внутреннюю упаковку закрывают внешней упаковкой, имеющей внутреннюю поверхность. Затем воздействуют на шовную нить, внутреннюю упаковку и внутреннюю поверхность внешней упаковки такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к шовной нити и к внутренней упаковке. В результате чего по существу ингибируется образование колоний бактерий на шовной нити и внутренней упаковке. Также обеспечиваются упакованное медицинское устройство и способ увеличения срока хранения упакованного антимикробного медицинского устройства. Использование группы изобретений обеспечивает длительный срок хранения упакованных антимикробных медицинских устройств. 4 н. и 16 з.п. ф-лы, 14 ил., 8 табл., 8 пр.
Формула
создают внутреннюю упаковку, содержащую источник антимикробного агента;
создают адсорбирующий материал, который эффективно поглощает со временем часть антимикробного агента;
помещают шовную нить во внутреннюю упаковку, причем шовная нить имеет одну или более поверхностей;
закрывают внутреннюю упаковку внешней упаковкой, имеющей внутреннюю поверхность; и
воздействуют на шовную нить, внутреннюю упаковку и внутреннюю поверхность внешней упаковки такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к шовной нити и к внутренней упаковке, в результате чего по существу ингибируется образование колоний бактерий на шовной нити и внутренней упаковке,
причем упакованная антимикробная шовная нить проявляет свойства возможности хранения в течение длительного срока.
помещение внешней упаковки, содержащей внутреннюю упаковку и шовную нить, в аппарат для стерилизации;
нагревание аппарата для стерилизации до первой температуры;
установку давления в стерилизационном аппарате до первого значения давления;
подачу водяного пара в стерилизационный аппарат для обработки внутренней поверхности внешней упаковки, внутренней упаковки и шовной нити водяным паром на протяжении первого интервала времени;
установку давления в стерилизационном аппарате до второго значения давления;
подачу химического стерилизующего агента в стерилизующий аппарат;
выдерживание химического стерилизующего агента в стерилизационном аппарате в течение второго интервала времени, чтобы значительная часть микроорганизмов утратила жизнеспособность;
удаление остатков влаги и химического стерилизующего агента с шовной нити; и
высушивание упакованной антимикробной шовной нити до требуемого уровня содержания влаги.
создают внутреннюю упаковку, содержащую источник антимикробного агента;
создают адсорбирующий материал, который эффективно поглощает со временем часть антимикробного агента;
помещают медицинское устройство во внутреннюю упаковку, причем медицинское устройство имеет одну или более поверхностей;
закрывают внутреннюю упаковку внешней упаковкой, имеющей внутреннюю поверхность; и
воздействуют на медицинское устройство, внутреннюю упаковку и внутреннюю поверхность внешней упаковки такими температурой и давлением и в течение такого времени, которые достаточны для переноса паров эффективного количества антимикробного агента от источника антимикробного агента к медицинскому устройству и к внутренней упаковке, в результате чего по существу ингибируется образование колоний бактерий на медицинском устройстве и внутренней упаковке,
причем упакованное медицинское устройство проявляет свойства возможности хранения в течение длительного срока.
внутреннюю упаковку, имеющую источник антимикробного агента;
адсорбирующий материал, который эффективно поглощает со временем часть упомянутого антимикробного агента;
шовную нить, помещенную в указанную внутреннюю упаковку, причем указанная шовная нить имеет одну или более поверхностей; и
внешнюю упаковку, имеющую внутреннюю поверхность, причем внутри указанной внешней упаковки помещается указанная внутренняя упаковка;
причем указанная шовная нить, указанная внутренняя упаковка и указанная внутренняя поверхность указанной внешней упаковки подвергаются воздействию таких температуры и давления и в течение такого времени, которые достаточны для переноса паров эффективного количества указанного антимикробного агента от указанного источника антимикробного агента к указанной шовной нити и указанной внутренней упаковке, что позволяет по существу ингибировать образование колоний бактерий на указанной шовной нити и указанной внутренней упаковке.
внутреннюю упаковку, имеющую источник антимикробного агента;
адсорбирующий материал, который эффективно поглощает со временем часть упомянутого антимикробного агента;
медицинское устройство, помещенное в указанную внутреннюю упаковку, причем указанное медицинское устройство имеет одну или более поверхностей; и
внешнюю упаковку, имеющую внутреннюю поверхность, причем внутри указанной внешней упаковки помещается указанная внутренняя упаковка;
при этом указанное медицинское устройство, указанная внутренняя упаковка и указанная внутренняя поверхность указанной внешней упаковки подвергаются воздействию таких температуры и давления и в течение такого времени, которые достаточны для переноса паров эффективного количества указанного антимикробного агента от указанного источника антимикробного агента к указанному медицинскому устройству и указанной внутренней упаковке, что позволяет по существу ингибировать образование колоний бактерий на указанном медицинском устройстве и указанной внутренней упаковке.

Комментарии