Способ визуализации смерти клеток в области тела млекопитающего субъекта in vivo - RU2228765C2
Код документа: RU2228765C2
Чертежи


Описание
Область технике, к которой относится изобретение
Изобретение относится к исследованиям в медицине с использованием радиоизотопов и касается способа визуализации смерти клеток in vivo. В частности, оно касается использования аннексина с радиоактивной меткой для визуализации участков смерти клеток в организме млекопитающего с использованием γ-лучей для формирования изображения.
Данная работа частично поддерживалась грантом NIH HL-47151. В соответствии с этим правительство США имеет определенные права на данное изобретение.
Уровень техники
Апоптотическая или запрограммированная смерть клетки играет критическую роль в развитии и ряде гомеостатических и болезненных процессов (см. статью Thompson С.В., Science 267: 1456, 1995). Новые стратегии терапии ряда заболеваний могут вследствие этого осуществляться посредством модуляции апоптотической смерти клетки. Отсутствие неинвазивного способа(ов) детекции (обнаружения) и мониторинга апоптотической смерти клетки in vivo препятствует исследованию новых фармакологических агентов для стимуляции или ингибирования апоптотической смерти клетки.
Показана возможность применения спектроскопии протонно-ядерного магнитного резонанса (1Н-ЯМРС) липидов для детекции специфических изменений композиции и/или текучести плазматических мембран лимфобластов и других клеточных линий, подвергающихся апоптотической смерти клеток (см. статью Blankenberg F.G. и соавт., Blood 87:1951, 1996).
Клиническое применение исследования липидов с помощью1H-ЯМРС ограничивается в настоящее время сложными локальными магнитными эффектами окружающей микросреды, обнаруженными в естественных условиях во многих тканях и органах.
Сущность изобретения
В одном аспекте данное изобретение включает способ визуализации смерти клеток (например, смерти клеток вследствие апоптоза или некроза) в области тела млекопитающего субъекта in vivo. Способ включает стадии (а) введения субъекту аннексина, меченного биосовместимым радионуклидом, (b) помещение субъекта в поле обнаружения детектором излучения спустя период времени, за который меченый аннексин может достигнуть локализации в организме субъекта, и (с) измерения радиоактивной эмиссии радионуклида, локализованного в организме субъекта, с помощью детектора излучения для конструирования изображения радиоактивной эмиссии, при этом изображение представляет собой отображение смерти клеток в определенной области тела млекопитающего субъекта. В одном варианте осуществления способ дополнительно включает стадию (d) процессинга изображения для отсечения сигнала, обусловленного неспецифической локализацией меченого аннексина, такой как неспецифическая локализация в почках.
Радионуклиды, используемые в способе, включают йод 123, йод 131, галлий 67, индий 111, фтор 18 и технеций 99m (Tc99m). Следует учитывать, что фтор 18 является излучателем позитронов и может быть таким образом использован в позитронной эмиссионной томографии (ПЭТ). Йод 123, йод 131, галлий 67, индий 111 и технеций 99m используют со стандартной детекцией γ-излучения. Тс99m является предпочтительным радионуклидом для использования в способах, соответствующих изобретению. В предпочтительном варианте осуществления Тс99m связан с аннексином посредством гидразиноникотинамида (ГНА). Меченный Тс99m аннексин обычно вводят в дозе между приблизительно 5 и приблизительно 20 мКи.
В одном основном варианте осуществления изобретения детектор излучения представляет собой детектор γ-излучения, и измеряемая радиоактивная эмиссия является эмиссией γ -лучей. В другом основном варианте осуществления детектор излучения представляет собой детектор позитронной эмиссии, и измеряемая радиоактивная эмиссия является эмиссией позитронов.
В еще одном общем варианте осуществления способ далее включает повторение стадий (b) и (с) через выбранные интервалы времени, при этом повторение является эффективным для определения изменений в интенсивности излучения (например, эмиссии гамма-лучей или позитронов) из области тела в течение времени, отражая изменения числа клеток, в которых происходит клеточная смерть.
Еще один основной вариант осуществления включает повторение стадий (b) и (с) через выбранные интервалы времени, при этом повторение является эффективным для отслеживания изменений в локализации γ -излучения в области тела субъекта в течение времени, отражающих изменения в локализации клеток, в которых происходит клеточная смерть.
Детектор излучения может быть, например, γ -сцинтилляционной камерой Анджера или камерой для получения трехмерного изображения.
Предпочтительным аннексином для применения в изобретении является аннексин V. Его обычно вводят в дозах, не превышающих приблизительно 300 мкг белка/кг, предпочтительно между приблизительно 1 и 10 мкг белка/кг. Возможны различные способы введения, включая внутривенное (i.v.), внутрибрюшинное (i.p.), подоболочечное и интраплевральное введение.
Измерение γ-излучения (эмиссии γ-лучей) для конструирования изображения обычно проводят между приблизительно 5 минутами и приблизительно 2 часами после введения меченого аннексина. В одном варианте осуществления измерение эмиссии γ-лучей для конструирования изображения проводят приблизительно через один час после введения меченого аннексина.
При использовании представленного в данном описании способа могут быть получены изображения различных областей субъекта. Например, область может включать субъекта практически полностью или часть субъекта, такую как голова или ее часть, сердце или его часть, печень или ее часть и т.п.
Изобретение представляет также набор для визуализации смерти клетки in vivo. Набор включает (i) запечатанный флакон, содержащий меченный ГНА аннексин, приготовленный, например, как описано в разделе Материалы и методы (A), (ii) запечатанный флакон, содержащий раствор Sn-трицина, приготовленный, например, как описано в разделе Материалы и методы (В) и сохраняемый под N2, (iii) инструкции по получению меченного Тс99m аннексина с использованием компонентов (i) и (ii) вместе с Тс99m и (iv) инструкции по введению Тс99m-аннексина для визуализации областей смерти клеток in vivo. В одном варианте осуществления набор хранят при -70°С и транспортируют на сухом льду. В другом варианте осуществления меченный ГНА аннексин лиофилизируют.
Данные и другие объекты и признаки изобретения будут более очевидными после прочтения подробного описания в сочетании с приложенными фигурами.
Перечень фигур чертежей и иных материалов
Фиг. 1 представляет собой компьютерное изображение, показывающее Fas-опосредованный быстро развивающийся печеночный апоптоз так, как его определяют с помощью Тс99m-ГНА-аннексина V.
Фиг. 2 представляет собой компьютерное изображение, показывающее сигнал от Тс99m-ГНА-овальбумина при Fas-опосредованном быстро развивающемся печеночном апоптозе.
Фиг. 3 представляет результат количественного определения поглощения Тс99m-ГНА-аннексина V трансплантированным сердцем.
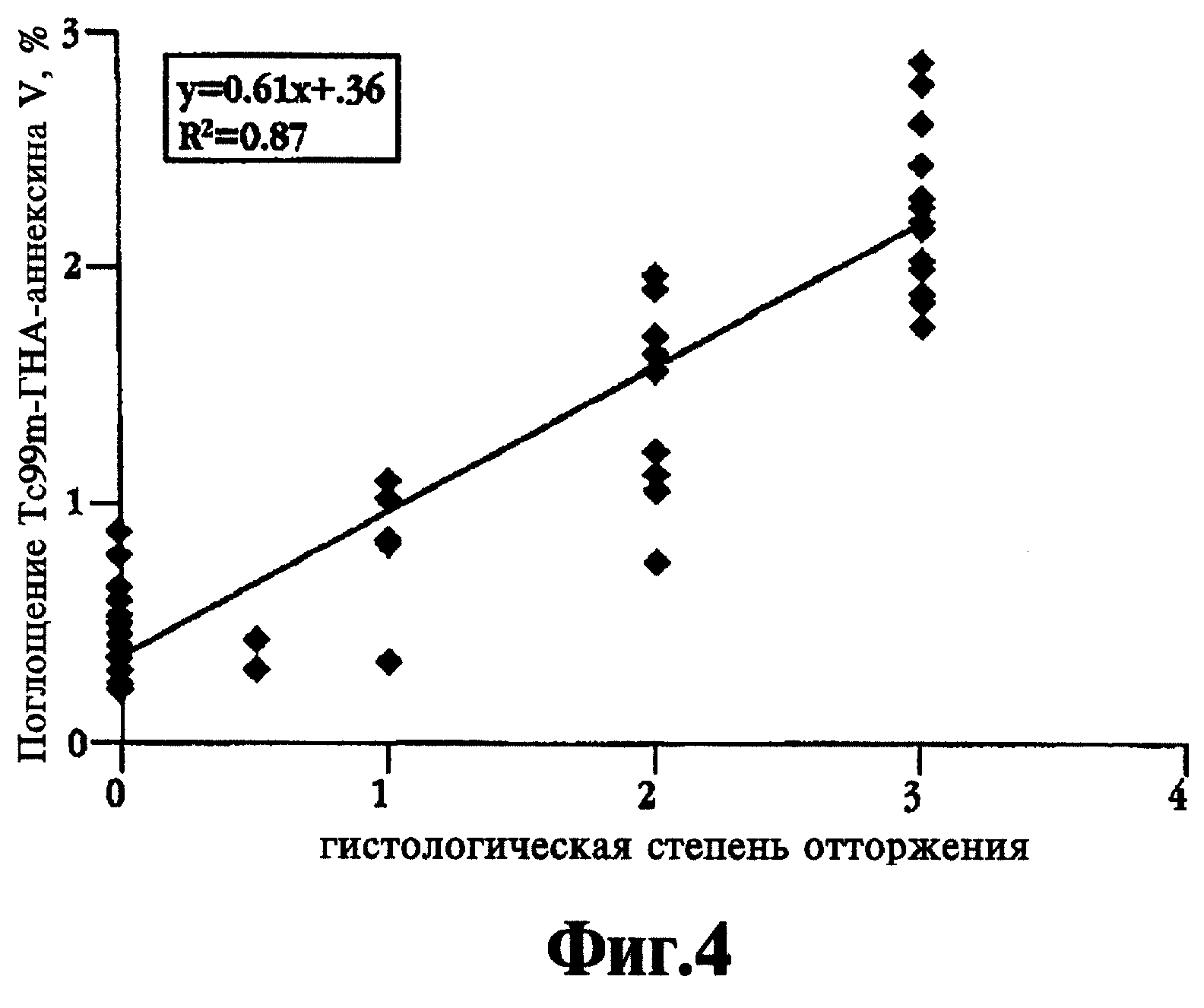
Фиг. 4 демонстрирует зависимость гистологических степеней острого отторжения от поглощения Тс99m-ГНА-аннексина V.
Сведения, подтверждающие возможность осуществления изобретения
I. Определения
Термин "смерть клеток (клетки)" в контексте "детекция смерти клеток" или "локализация смерти клеток" относится к клеткам, которые потеряли целостность плазматической мембраны, а также к процессам, при которых умирают клетки млекопитающих. Данные процессы включают апоптоз и процессы, которые, как полагают, включают апоптоз (например, старение клеток), а также некроз. Термин "смерть клеток" используют в данном контексте для обозначения смерти или приближающейся смерти ядерных клеток (например, нейронов, миоцитов, гепатоцитов и т.д.), а также смерти или приближающейся смерти безъядерных клеток (например, клеток красной крови, тромбоцитов и т.п.).
"Биосовместимый радионуклид" или "биосовместимый радиоизотоп" является изотопом, который признан применимым для инъекции пациенту при использовании в радиоизотопных исследованиях в медицине. Примеры биосовместимых радионуклидов включают йод 123, йод 131, галлий 67, индий 111, фтор 18 и технеций 99m.
II. Смерть клеток - апоптоз и некроз
Апоптоз означает "запрограммированную смерть клеток", при которой клетка выполняет программу "самоубийства клетки". В настоящее время считают, что программа апоптоза является эволюционно консервативной фактически для всех многоклеточных организмов, а также для всех клеток определенного организма. Кроме того, полагают, что во многих случаях апоптоз может являться программой "дефолта" (несоблюдения правил), которая может активно ингибироваться в здоровых жизнеспособных клетках.
Решение клетки "подчиниться" апоптозу может быть принято под влиянием ряда регуляторных стимулов и факторов окружающей среды (см. статью Tompson С.В., Science 267:1456, 1995). Физиологические активаторы апоптоза включают фактор некроза опухолей (ФНО), лиганд Fas, трансформирующий фактор роста β, нейромедиаторы, глутамат, допамин, N-метил-D-аспартат, удаление факторов роста, потерю связывания матрикса, кальций и глюкокортикоиды. Связанные с повреждениями индукторы апоптоза включают тепловой шок, вирусную инфекцию, бактериальные токсины, онкогены myc, rel и ЕIА, супрессор опухолей р53, цитолитические Т-клетки, оксиданты, свободные радикалы и лишение питательных компонентов (антиметаболиты). Ассоциированные с терапией индукторы апоптоза включают γ-облучение, УФ-облучение и ряд химиотерапевтических лекарственных препаратов, включая цисплатин, доксорубицин, блеомицин, цитозина арабинозид, азотистый иприт, метотрексат и винкристин. Связанные с токсином индукторы апоптоза включают этанол и пептид β -амилоид.
Апоптоз может иметь особенно пагубные последствия, когда он происходит патологическим образом в клетках, которые в норме не регенерируют, таких как нейроны. Поскольку данные клетки не замещаются, когда умирают, их потеря может привести к ослаблению, а иногда к фатальной дисфункции пораженного органа. Данная дисфункция доказана для ряда нейродегенеративных нарушений, которые были связаны с повышенным уровнем апоптоза, включая синдром Альцгеймера, болезнь Паркинсона, боковой амиотрофический склероз, пигментную ретинопатию и мозжечковую дегенерацию.
Последствия нежелательного апоптоза могут быть аналогичным образом пагубными также при других патологиях, включая ишемические повреждения, такие как обычно происходят в случаях инфаркта миокарда, реперфузионных повреждениях и инсульте. В частности, апоптоз, как считают, играет главную роль в очень задержанном инфаркте после мягкой локальной ишемии (см. работу Du С. и соавт., J. Cereb. Blood Flow and Metab. 16: 195-201, 1996).
Дополнительные заболевания, ассоциированные с повышенным уровнем апоптоза, включают, но не ограничиваются следующими: СПИД, миелодиспластические синдромы, такие как апластическая анемия, и индуцированное токсинами заболевание печени, включая повреждение, обусловленное излишним употреблением алкоголя.
Некроз представляет собой локализованную смерть клеток или ткани от причин, отличных от причин апоптоза (т.е. отличных от выполнения клеткой внутренней программы самоубийства). Некроз может вызываться травматическими повреждениями, бактериальной инфекцией, острой гипоксией и т.п. Существует некоторое перекрывание между двумя типами смерти клеток в том, что некоторые стимулы могут вызывать либо некроз, либо апоптоз или оба в некоторой степени в зависимости от тяжести повреждения.
III. Асимметрия биологических мембран.
В целом считают, что биологические мембраны являются асимметричными в плане специфических мембранных фосфолипидов. В частности, наружный слой плазматических мембран эукариот образован в основном холинфосфолипидами, такими как сфингомиелин и фосфатидилхолин (ФХ), тогда как внутренний слой содержит в основном аминофосфолипиды, такие как фосфатидилсерин (ФС) и фосфатидилэтаноламин (ФЭА). Данная асимметрия, как полагают, поддерживается активностью аденозинтрифосфат (АТФ)-зависимой аминофосфолипид-транслоказой, которая избирательно транспортирует ФС и ФЭА между бимолекулярными слоями (см. статью Seigneuret М. и Devaux P.F., Proc. National Acad. Sci. USA 81: 3751, 1984). Другие ферменты, которые, как полагают, участвуют в транспорте фосфолипидов между слоями, включают АТФ-зависимую флоппазу (см. статью Connor J. и соавт., J. Biol. Chem. 267:19412, 1992) и скрамблазу липидов (см. статью Zwaal R.F.A. и соавт., Biochem. Soc. Trans. 21: 248, 1993).
Поскольку асимметрия вероятно является правилом для нормальных клеток, утрата данной асимметрии ассоциирована с определенными физиологическими, а также патологическими процессами. Например, показано, что асимметрия мембраны, определяемая как присутствие ФС на наружном слое плазматической мембраны ("ФС-проявление"), является одним из самых ранних проявлений апоптоза, предшествующим фрагментации ДНК, образованию пузырьков плазматической мембраны и потере целостности мембраны (см. работы Martin S.J. и соавт., J. Exp. Med. 182: 1545, 1995; Fadok V.A. и соавт., J. of Immunol. 148:2207, 1992; J. of Immunol. 149: 4029, 1992).
Подобная переориентация была обнаружена при серповидно-клеточной болезни (см. статью Lane А. и соавт., Am. J. Hematol. 47: 295, 1994), β-талассемии (см. статью Borenstain-Ben Yashar V. и соавт., Am. J. Hematol. 44: 63, 1993), активации тромбоцитов и в ряде мутантных опухолевых клеток с дефектом транспорта ФС. Постепенное появление ФС на наружном слое, как было показано, имеет место при старении красных кровяных клеток (см. статью Tait J.F. и Gibson D., J. Lab. Clin. Med. 123: 741, 1994). Когда проявление ФС на данных клетках достигает критического уровня, клетки удаляются из кровотока макрофагами (см. статью Pak С.С. и Filder I.J., Sernin Cancer Вiоl. 2: 189, 1991). Непосредственной кульминацией всех вышеперечисленных состояний является смерть пораженных клеток (т.е. клеток со значительным проявлением ФС).
Следует учитывать, что проявление ФС является компонентом как апоптоза, так и некроза. Его роль в начальных стадиях апоптоза кратко описана выше. При достижении апоптотическими клетками конечных стадий апоптоза (т.е. потери целостности мембраны) будет учитываться, что ФС в обоих слоях плазматической мембраны будет "экспонироваться" во внеклеточной среде. Аналогичная ситуация существует при смерти клетки путем некроза, при котором потеря целостности мембраны является либо инициирующим фактором, либо существует на ранних стадиях процесса некротической смерти клетки, соответственно данные некротические клетки также "экспонировали" ФС до тех пор, пока "экспонировались" оба слоя плазматической мембраны.
IV. Аннексин
Белки семейства аннексинов используют для практической реализации данного изобретения. Высокие уровни аннексина V в норме обнаруживают в цитоплазме ряда клеток, включая плаценту, лимфоциты, моноциты, эпителий желчных протоков и почечных (кортикальных) канальцев. Хотя физиологическая функция аннексинов полностью не выяснена, некоторые свойства аннексинов обусловливают их применение в качестве диагностических и/или терапевтических агентов. В частности, было показано, что аннексины обладают очень высокой аффинностью к поверхностям анионных фосфолипидов, таким как слой мембраны, имеющий на поверхности молекулы фосфатидилсерина (ФС).
V. Обзор экспериментальных результатов
Эксперименты, проведенные для поддержки данного изобретения, продемонстрировали, что введение аннексина с радиоактивной меткой может быть использовано для визуализации смерти клеток in vivo. Например, эксперименты в Примере 1 представляют получение изображения и количественное определение Fas-опосредованной смерти гепатоцитов в ответ на инъекцию очищенного антитела Jo2 у мышей (см. статью Ogasawara J. и соавт., Nature 364: 806, 1993). Результаты данных экспериментов (см., например, фиг. 1) показали повышение в два и четыре раза поглощения печенью аннексина V с радиоактивной меткой через один и два часа, соответственно, специфически вследствие Fas-опосредованной смерти гепатоцитов после инъекции антитела Jo2. Было также отмечено временное двукратное повышение поглощения селезенкой сразу после введения, которое впоследствии падало до контрольных значений. Данное снижение сигнала от селезенки может быть обусловлено быстрым выведением лимфоцитов из кровотока и селезенки в ответ на взрыв Fas-опосредованного апоптоза после обработки.
Связывание аннексина было также отмечено в почках. Однако данное связывание имелось при отсутствии какого-либо апоптоз-индуцирующего стимула и в действительности снижалось по мере повышения сигнала от гепатоцитов. Развивающееся снижение активности почек в течение времени после введения Аb (антитела) против Fas вместе с повышением поглощения в печени в тот же период предполагает, что не связанная с апоптозом аффинность почек к аннексину V ниже, чем аффинность апоптотической ткани. Связывание коркового вещества почки инъецированного аннексина V может быть отчасти обусловленным перекрестной реактивностью аннексина с фосфолипидом почечных канальцев.
Следует отметить, что имелось незначительное выделение меченого аннексина через почки, позволяющее предположить, что радиоактивная метка (в данном случае Тс99m) оставалась связанной с аннексином во время экспериментов. Далее, инъецированный меченный Тс99m аннексин быстро выводился из кровотока, имея период полужизни в сыворотке приблизительно 3-7 минут. Данные факторы позволяли визуализировать радиофармацевтический сигнал через 1-2 часа после его введения.
Вышеописанные характеристики дают возможность проведения суточных (или двухсуточных) исследований по получению изображения, каждое из которых представляет "моментальный снимок" апоптотической активности ткани или органа, представляющих интерес, во время инъекции аннексина V с радиоактивной меткой.
VI. Визуализация смерти клеток in vivo
Данное изобретение включает в одном аспекте способ визуализации смерти клеток (вследствие, например, апоптоза или некроза) в какой-либо области млекопитающего субъекта in vivo. Согласно способу аннексин с радиоактивной меткой (например, меченный технецием 99m аннексин V) вводят субъекту. Спустя период времени, за который конъюгат может достигнуть локализации в организме субъекта, субъекта помещают в детекционное поле детектора γ-лучей. Субъекта поддерживают в практически неподвижном состоянии во время измерения γ-излучения технеция 99m с помощью детектора γ-лучей. После фазы измерения конструируют изображение эмиссии γ-лучей. Сконструированное таким образом изображение затем используют для того, чтобы обеспечить лечащего врача картой или локализацией областей смерти клеток в организме млекопитающего субъекта или в анализируемой области организма млекопитающего субъекта.
Для облегчения интерпретации изображения, полученного с использованием вышеуказанного способа, изображение может быть обработано цифровым способом (оцифровано) для фильтрации фона, шумов и/или неспецифической локализации (например, локализации в почках) конъюгата аннексин/Тс99m, как более подробно описано ниже.
Преимущество вышеописанного способа состоит в том, что посредством измерения γ -излучения и формирования изображения через выбранные интервалы способ может быть использован для отслеживания изменений в интенсивности эмиссии γ-лучей от субъекта в течение времени, отражая изменения в числе клеток, в которых происходит клеточная смерть. Данный подход может быть также использован для отслеживания изменений в локализации эмиссии γ-лучей от субъекта в течение времени, отражая изменения в распространении клеток, в которых происходит клеточная смерть.
Синтез аннексина с радиоактивной меткой
Изобретение может быть практически реализовано с использованием очищенного нативного, рекомбинантного или приготовленного синтетическим путем аннексина. Аннексин V, например, может быть соответствующим образом получен из плаценты человека (см. статью Funakoshi Т. и соавт., Biochemistry 26: 5572, 1987). Однако рекомбинантный аннексин представляет ряд преимуществ, включая простоту получения и экономическую эффективность. У человека и из других организмов был клонирован ряд различных аннексинов. Их последовательности имеются в базах данных по последовательностям, включая Genbank.
Изобретение предпочтительно реализуют практически, используя аннексин V, по нескольким причинам. Во-первых, аннексин V является одним из аннексинов, присутствующих в наибольших количествах, во-вторых, его просто получить из естественных или рекомбинантных источников и, в-третьих, он обладает высокой аффинностью к фосфолипидным мембранам (см. статью Tait J.F. и соавт., Biochem. 27: 6268, 1988). Аннексин V человека имеет мол. массу 36 кД и высокую аффинность (кД=7 нмол/л) к фосфатидилсерину (ФС). Последовательность аннексина V человека может быть получена в Genbank под регистрационными номерами U05760-U05770.
Пример системы экспрессии, пригодной для получения аннексина для использования в данном изобретении, приведен в разделе Материалы и методы. В ней используют экспрессионный вектор рЕТ12а (Novagen, Madison, Wisconsin) в Е. coli.
Другие бактериальные экспрессионные векторы также могут быть использованы. Они включают, например, плазмиду pGEX (см. статью Smith D.B. и соавт., Gene 67: 31, 1988) и ее производные (например, серию pGEX от Pharmacia Biotech, Piscataway, NJ). Данные векторы экспрессируют полипептидные последовательности клонированной инсерции, слитой в рамке считывания с глутатион S-трансферазой. Рекомбинантными плазмидами pGEX могут быть трансформированы подходящие штаммы Е. coli, и образование слитого белка может быть индуцировано добавлением изопропил-тиогалактопиранозида. Солюбилизированный рекомбинантный слитый белок затем может быть очищен из лизатов клеток индуцированных культур с использованием аффинной хроматографии на агарозе в соответствии со стандартными способами (см. монографию Ausubel F.M. и соавт., Current Protocols in Molecular Biology ("Современные протоколы в молекулярной биологии") (John Wiley and Sons, Inc., Media, PA). Другие имеющиеся в продаже системы экспрессии включают дрожжевые системы экспрессии, такие как экспрессионный набор на основе Pichia от Invitorgen (San Diego, CA); бакуловирусные системы экспрессии (см. статьи Reilly P.R. и соавт., Baculovirus expression vectors: a laboratory manual ("Лабораторное руководство по экспрессионным векторам на основе бакуловируса"), 1992; Beames и соавт., Biotechniques 11: 378, Clontech, Palo Alto CA) и системы экспрессии на основе клеток млекопитающих (Clontech, Palo Alto CA; Gibco-BRL, Gaithersburg MD).
В экспрессионные векторы может быть инженерно введен ряд признаков, таких как лидерные последовательности, которые способствуют секреции экспрессированных последовательностей в культуральную среду. Полученные рекомбинантным образом полипептиды обычно выделяют из лизированных клеток или культуральной среды.
Выделенные рекомбинантные полипептиды, полученные как описано выше, могут быть очищены стандартными способами очистки белков, включая дифференцированное осаждение, хроматографию с использованием молекулярных сит, ионообменную хроматографию, изоэлектрическое фокусирование, гель-электрофорез и аффинную хроматографию. Препараты белков могут быть также сконцентрированы, например, фильтрацией (Amicon, Danvers, Mass.).
Аннексин, полученный, как описано выше, затем метят выбранным радионуклидом. Выбор определенного изотопа будет зависеть от конкретного применения заявленного способа.
Изобретение может быть практически реализовано с использованием любого из имеющихся в настоящее время радионуклидов. При выборе подходящего радионуклида специалист-практик обычно будет подразумевать конкретное применение изобретения наряду с факторами, обычными для получения радиологического изображения в целом. Данные факторы включают (i) минимум эмиссии частиц, (ii) величину первичной фотонной энергии между приблизительно 50 и 500 кЭв, (iii) полупериод физического распада, превышающий время, необходимое для приготовления материала для введения, (iv) эффективный полупериод распада, более длительный, чем время исследования, подходящую химическую форму и реактивность, низкую токсичность и стабильность или практическую стабильность аннексина, меченного данным радионуклидом.
Примером радионуклида является Tc99m, который имеет период полураспада приблизительно 6 часов и может быть использован для мечения аннексина с высокой специфической активностью. Он удовлетворяет большинству из вышеперечисленных критериев и применяется в более чем 80% способов визуализации с использованием радиоизотопов в медицине. Другие изотопы, которые могут быть использованы, включают йод 123 (период полураспада ~ 13,2 часа), йод 131 (период полураспада ~ 8 суток), галлий 67 (период полураспада ~ 78 часов) и индий 111 (период полураспада ~ 2,8 суток).
Связывание изотопа с аннексином может быть осуществлено с использованием известных методик. Например, Tc99m может быть связан с аннексином с помощью группы гидразиноникотинамида (ГНА), имеющейся у AnorMED, Langley, British Columbia, Canada, как описано ниже в разделе Материалы и методы. Галлий 67 и Индий 111 могут быть использованы для введения в белки радиоизотопной метки с помощью, например, способа, описанного в статье Hnatowich D.J. и соавт., J. Immunol. Meth. 65: 147, 1983, включенной в данный контекст в виде ссылки.
Известны другие способы мечения белков радионуклидами. Например, в Патенте США № 5552525, выданном 03 сентября 1996 (Dean), описывают получение пептидов, меченных технецием 99m (Tc99m). Способы мечения пептидов и полипептидов Tc99m описаны также в патентах США № 5443815 и 5508020. В статье Lind и соавт., (J. Nucl. Med. 31: 417-473, 1990) описаны меченные Tc99m моноклональные антитела. В статье LaMuraglia и соавт. (J. Vasc. Surg. 10: 20-28,1989) описан111In-меченный неспецифический иммуноглобулин человека и в статье Fischman и соавт., (J. Nucl. Med. 32: 482-491, 1991) описаны конъюгаты хемотактический формилпептид (fMLF) -111In-меченная ДТПУ (диэтилентриаминпентауксусная кислота).
Введение аннексина с радиоактивной меткой
Аннексин с радиоактивной меткой может быть введен с использованием стандартных протоколов введения соединений с радиоактивной меткой. Дозировка зависит от двух основных соображений: (i) количества и типа инъецированного радионуклида и (ii) количества инъецированного белка аннексина.
Технеций (Те) 99m может быть введен взрослому человеку в дозах до приблизительно 20 мКи. Предпочтительная доза для однократного введения Тс99m (радиоактивный изотоп технеция 99т) составляет между приблизительно 5 и 20 мКи.
Аннексин V начинает проявлять фармакологические эффекты (эффекты антикоагулянта) при дозах, превышающих 300 мкг/кг. Соответственно, диагностические способы, согласно данному изобретению (в которых пытаются преодолеть фармакологические эффекты меченого аннексина), предпочтительно реализуют практически при дозах ниже, чем 300 мкг/кг, обычно ниже, чем 50 мкг/кг. Данные следовые дозы (например, от 10 мкг/кг до 50 мкг/кг) не имеют выраженного фармакологического или токсического побочного эффектов в отношении животных или человека.
Аннексин с радиоактивной меткой обычно суспендируют в подходящем носителе для доставки, таком как стерильный солевой раствор. Носитель может также содержать стабилизирующие агенты, носители, наполнители, антикоагулянты, эмульгаторы и т.п., что известно из уровня техники.
Аннексин с радиоактивной меткой может быть введен любым из ряда способов, которые известны как эффективные для введения белков с радиоактивной меткой с целью визуализации с использованием радиоизотопов в медицине. Предпочтительным способом введения является внутривенная (i.v.) инъекция. Она особенно удобна для визуализации внутренних органов с хорошей васкуляризацией, таких как сердце, легкое, селезенка и т.д. Способы внутривенного введения радиофармацевтических препаратов известны. Например, известно, что фармацевтический препарат с радиоактивной меткой обычно вводят болюсной инъекцией, используя способ Ольдендорфа/Турнике (Oldendorf/Tourniquet) или способ внутривенной интродукции (см., например, монографию Mettler F.A. и Guiberteau M.J., Essentials of nuclear medicine imaging, ("Основы визуализации при исследованиях с использованием радиоизотопов в медицине"), 2-ое изд., W. В. Saunders Company, Philadelphia, PA, 1985, Приложение D).
Для получения изображения (визуализации) мозга аннексин с радиоактивной меткой может быть введен подоболочечно. Подоболочечное введение доставляет соединение непосредственно в пространство под паутинной оболочкой, содержащее церебральную спинальную жидкость (ЦСЖ). Доставка в область позвоночника также может быть выполнена путем эпидуральной инъекции в область позвоночника над паутинной оболочкой.
Другие способы введения включают внутрибрюшинное (например, для пациентов, проходящих диализ почек) и внутриплевральное введение. При специальном применении изобретение предусматривает дополнительные способы доставки, включающие внутримышечное введение, подкожное, внутрилимфатическое, инсуффляционное и пероральное, интравагинальное и/или ректальное введение.
Способы практического осуществления вышеперечисленных вариантов введения известны в уровне техники.
Локализация аннексина с радиоактивной меткой
После введения меченого аннексина ему представляют возможность локализоваться в ткани- или органе-мишени. Локализация в данном контексте относится к состоянию, при котором в организме субъекта достигается либо равновесие, либо псевдостабильное соотношение между связанным, "локализованным", и несвязанным, "свободным", меченым аннексином. Количество времени, необходимое для данной локализации, обычно порядка нескольких минут или десятков минут. Оно может быть оценено по периоду полужизни меченого аннексина в сыворотке. В случае меченного Тс99m аннексина V, инъецируемого внутривенно, период полужизни в сыворотке составляет между приблизительно 3 и 7 минутами. Время локализации также зависит от доступности ткани для меченого аннексина. Это, в свою очередь, зависит от способа введения, как известно из уровня техники.
Визуализацию предпочтительно начинать после локализации большей части меченого аннексина на своей мишени(ях). Для введенного внутривенно меченного Тс99m аннексина V это происходит через несколько периодов полужизни. Отрезок времени приблизительно в 10 периодов полужизни (примерно 30-70 минут в случае конъюгатов аннексин/Тс99m) считают достаточным для достижения практически полной локализации. Специалист оценит, однако, что может быть желательной визуализация в течение времени, которое меньше или превышает вышеописанный отрезок в ~ 10 периодов полужизни. Например, при визуализации смерти клеток вследствие повреждения кровеносного сосуда доступность ткани-мишени является очень высокой, при этом сильный сигнал может быть получен от участка-мишени уже через несколько минут, особенно, если постепенно вводят низкую дозу меченого аннексина с целью минимизации сигнала от метки, циркулирующей в кровотоке.
Во всех вышеуказанных случаях обоснованная оценка времени, необходимого для локализации, может быть сделана специалистом. Более того, после определения локализации как функции от времени может следовать визуализация сигнала γ-лучей меченого аннексина согласно способам, соответствующим изобретению.
Устройства для детекции γ-лучей
Устройства для формирования изображения с помощью γ-излучения функционируют путем аккумуляции сигнала, получаемого от γ-лучей, испускаемых субъектом в течение времени. Одним из наиболее широко используемых способов детекции γ-лучей является использование γ-сцинтилляционной камеры Анджера (Anger) (см. монографию Mettler и Guiberteau, "Основы визуализации при исследованиях с использованием радиоизотопов в медицине", supra, 1985). Она работает путем превращения γ-лучей, испускаемых радионуклидом, в протоны (обычно с помощью кристаллов NaI(TI)), которые затем усиливают в фотоумножителе (ФУ), превращают в сигнал напряжения и используют для конструирования изображения. Компоненты сцинтилляционной камеры Анджера обычно включают коллиматор, сцинтилляционный кристалл, набор ФУ, анализатор амплитуды импульсов, электронно-лучевую трубку (ЭЛТ) и пульт для осуществления контроля. Обычно система камеры включает также компьютер. Процессинг между рядом ФУ и дисплеем (например, ЭЛТ) может быть либо аналоговым, либо цифровым. Детальное описание теории и работы γ-сцинтилляционных камер Анджера можно найти в любом из множества обзоров и/или материалов по радиоизотопным исследованиям в медицине (см., например, монографию Mettler и Guiberteau, "Основы визуализации при исследованиях с использованием радиоизотопов в медицине", 1985, введенную в данный контекст в виде ссылки).
Более информативное изображение может быть получено при использовании эмиссионно-компьютерной томографии (ЭКТ) для получения 3-мерного изображения. Двумя основными типами ЭКТ являются однофотонная эмиссионная компьютерная томография (ОФЭКТ), в которой используют изотопы, такие как Тс99m, и позитронная эмиссионная томография (ПЭТ), которая основана на аннигиляции фотонов при высоких энергиях (511 кэВ), что обеспечивает локализацию с высокой точностью. Недостаток ПЭТ состоит в том, что ее обычно используют с короткоживущими получаемыми в циклотроне изотопами, такими как11С,13N и18F. ОФЭКТ, с другой стороны, можно использовать с описанными в данном контексте радиофармацевтическими средствами (например, Тс99m).
Системы ОФЭКТ обычно включают одну или две головки γ-сцинтилляционной камеры Анджера, находящиеся под контролем компьютера, которые могут вращаться вокруг пациента по круговой или эллиптической орбите. Такие камеры ОФЭКТ имеются в продаже у ряда производителей. Например, Siemens (Des Plains, IL) продает несколько таких камер, включая "Е-САМ", "ORBITER", "ECAT", "MULTISPECT3", "MULTISPECT 2" и "DIACAM".
Камеры, как описано выше, теперь обычно включают вмонтированные процессоры изображения, которые могут манипулировать изображением, как цифровыми файлами, для того, чтобы убрать фон, добавить псевдоцвет и т.п. Когда изображения имеются в форме цифровых файлов, ими можно манипулировать с помощью ряда программ процессинга изображения (например, "ADOBE PHOTOSHOP", Adobe Systems, Adobe Systems, Mt. View, CA) на персональном компьютере, таком как IBM-совместимый ПК или Apple Macintosh (Apple Computer, Cupertino, CA) и распечатывать.
Помещение субъекта в поле устройства для обнаружения γ-лучей
1. Поле детекции устройства. Поле детекции (обнаружения) устройства определяют как участок, на котором могут быть проведены стабильные и надежные измерения эмиссии γ-лучей. При использовании ЭКТдля получения изображения полем детекции устройства является все пространство, к котором γ-излучение может быть надежно измерено или часть данного пространства, которое запрограммировано в системе ЭКТ, как включаемое в сканирование. Данное пространство обычно значительно больше, чем поле детекции одной не-ЭКТ камеры.
Следует понять, что животному или субъекту не обязательно полностью находиться в поле детекции устройства для обнаружения γ-лучей. Например, если имеется заинтересованность в проведении анализа сигнала от определенного органа, то для получения желаемой информации следует измерить только сигнал от области тела, содержащей данный орган, и достаточного участка окружающей "темной" зоны.
2. Расположение субъекта: иммобилизация. Для сбора сигнала, который используют для генерации изображения, субъекта помещают в поле обнаружения устройством для фотодетекции на период времени, в течение которого измеряют γ-излучение, которое будет использовано для конструирования изображения. Если сигнал является достаточно сильным, т.е. таким, что можно сконструировать изображение по эмиссии γ-лучей, измеренной в течение менее чем приблизительно 20 мсек, и/или субъект не двигается относительно плоскости изображения в достаточной степени для того, чтобы испортить изображение, то специальные меры для иммобилизации обычно не требуются. Требуется только, чтобы субъект был помещен в поле устройства для детекции на протяжении периода измерения.
Если, с другой стороны, измерение γ-излучения занимает более 20 мсек и субъект перемещается, должны быть предусмотрены меры для обеспечения иммобилизации субъекта во время измерения эмиссии γ-лучей, соответствующие степени подвижности субъекта, с целью сохранения пространственной информации в сконструированном изображении. Например, в случае, когда субъект представлен человеком и время измерения фотонной эмиссии составляет порядка нескольких секунд, субъекта можно просто попросить не двигаться, насколько это возможно во время измерения эмиссии γ-лучей (визуализации). С другой стороны, если субъект является животным, таким как мышь, субъект может быть иммобилизован, например, с помощью наркоза или механических удерживающих приспособлений.
Может быть сконструирован ряд удерживающих приспособлений. Например, удерживающее приспособление, эффективное для иммобилизации мыши в течение от десятков секунд до минут, может быть сконструировано путем закрепления пластины, прозрачной для γ-лучей, над пенопластовой подушкой. На одном конце подушка имеет углубление для головы животного. Животное помещают под пластину таким образом, что его голова находится над углублением, что позволяет свободно дышать, хотя движение тела ограничивается пенопластовой подушкой.
Можно понять, что изображаемая область может включать практически всего субъекта или только часть субъекта, который нуждается в диагностике или мониторинге клеточной смерти. Например, данная область может включать только придаток или часть такого придатка, голову, центральную нервную систему или внутреннюю полость, такую как грудная или брюшинная полость. В частных случаях осуществления изобретения данные области могут содержать только выбранный орган или его часть. Например, способ может быть использован для анализа смерти клеток только в центральной нервной системе, головном мозге, сердце, печени, легком, селезенке, легких, костном мозге или части любого из указанных органов. Кроме того, анализируемая область может быть ограничена опухолью, например, у ракового больного, проходящего лечение, разработанное таким образом, что вызывает смерть клеток в опухоли.
Конструирование изображения эмиссии γ-лучей: процессинг изображения
В наиболее подходящих камерах измерение эмиссии γ-лучей генерирует сигнал напряжения, который либо отображается на ЭЛТ, либо сохраняется и/или анализируется компьютером в виде последовательности чисел. Данные числа используют для создания изображения стандартными способами визуализации. Например, изображение обычно анализируют путем стандартизации одиночных импульсов γ-лучей (либо относительно фиксированного предварительно выбранного значения, либо относительно максимального числа, определенного в каком-либо пикселе (элементе изображения), и превращения стандартизированного числа в яркость (черно-белая шкала) или цвет (псевдоцвет), которые изображаются на мониторе. В псевдоцветном представлении типичные цветовые обозначения являются следующими. Пиксели с нулевыми значениями обозначают черным, с низкими значениями - синим, а увеличивающиеся значения - цветами с увеличивающейся длиной волны до красного для самых высоких значений импульсов γ-лучей. Положение цветов на мониторе представляет распределение эмиссии γ-лучей и, соответственно, положение зон смерти клеток.
Если желательно проследить локализацию и/или сигнал в течение времени, например, для регистрации эффектов лечения на распространение и/или локализацию смерти клеток, измерение γ -излучения или визуализация могут быть повторены через выбранные интервалы времени для создания серии изображений. Интервалы могут быть короткими, такими как минуты, или длинными, такими как дни, недели, месяцы или годы.
Изображения, созданные способами, соответствующими данному изобретению, могут быть проанализированы различными методами. Их диапазон распространяется от простого визуального исследования, производимой в уме оценки и/или распечатывания копий на твердом носителе до сложного анализа цифрового изображения.
VII. Применения
Основные области применения аннексина V с радиоактивной меткой включают детекцию неуместного апоптоза при болезненных состояниях, при которых он не должен происходить, например при иммунных нарушениях, таких как волчанка, отторжение трансплантата или в клетках субъекта, усиливая ишемию, и детекцию недостаточного апоптоза, когда он должен происходить, например в опухолях или клетках, инфицированных вирусом.
Результаты, приведенные в данном описании, указывают, что аннексин с радиоактивной меткой может быть использован в ряде клинических исследований, при которых необходим мониторинг апоптотической и/или некротической смерти клеток, таких как, но не ограничиваясь, отторжением или повреждением трансплантата органа или костного мозга, инфекционными и неинфекционными воспалительными заболеваниями, аутоиммунным заболеванием, инфарктом и ишемией головного мозга или миокарда, кардиомиопатиями, атеросклерозом, нервными и нервно-мышечными дегенеративными заболеваниями, серповидно-клеточными заболеваниями, β-талассемией, терапией рака, СПИДом, миелодиспластическими синдромами и индуцированным токсином заболеванием печени и т.п. Аннексин с радиоактивной меткой может быть также использован в качестве инструмента для клинических исследований с целью изучения нормальной иммунной системы, эмбрионального развития и иммунологической толерантности и аллергии.
Аннексин V с радиоактивной меткой может быть использован, например, для визуализации и количественного анализа апоптотической смерти клеток в нормальных и злокачественных тканях, подвергающихся лечению. Мониторинг апоптоза при изучении серии изображений с использованием аннексина V с радиоактивной меткой может быть использован для быстрого тестирования и разработки новых лекарственных средств и способов терапии множества заболеваний. Кроме того, способы могут быть использованы для мониторинга хода лечения, мониторинга развития заболевания или того и другого. Далее, они могут быть использованы для ранней детекции определенных болезней.
Следующие примеры иллюстрируют изобретение, но никоим образом не предназначены для ограничения данного изобретения.
Материалы и методы
А. Приготовление ГНА-меченого аннексина V
Человеческий аннексин V получали при экспрессии в Е. coli плазмиды рЕТ12а-РАРI и очищали, как описано ранее (см. статью Wood B.L. и соавт., Blood 88: 1873-1880, 1996, введенную в данный контекст в виде ссылки). 30 мМ маточного раствора ("маточный раствор сложного эфира ГНА") N-гидроксисукцинимидного сложного эфира гидразиноникотинамида (ГНА; получен от AnorМЕD, Langley, British Columbia, Canada; см. статью Babich J.W. и соавт., Journal of Nuclear Medicine 34: 1964, 1993, введенную в данный контекст в виде ссылки) готовили суспендированием 220 мкг гидрохлорида сукцинимидил 6-гидразиноникотината (СГН) в 18,5 мкл N,N-диметилформамида (ДМФА). Пять мг аннексина V, растворенные в 893 мкл буфера А (20 мМ HEPES, рН 7,4, 100 мМ NaCl), реагировали с маточным раствором сложного эфира ГНА в течение трех часов при осторожном перемешивании, в закрытом от света месте при комнатной температуре согласно способу, описанному с статье Schwartz D.A. и соавт. (Bioconjugate Chem. 2: 333, 1991), введенной в данный контекст в виде ссылки. Реакцию останавливали добавлением 500 мкл 500 мМ глицина, рН 5,3, затем проводили диализ при 4°С против 20 мМ цитрата натрия, рН 5,2, 100 мМ NaCl. Осадок удаляли центрифугированием при 1500×g в течение 10 минут. Аликвоты по 100 мкл (100 мкг) ГНА-аннексина V хранили при -70°С.
В. Введение радиоактивной метки в ГНА-аннексин V
80 мкл SnCl2 (50 мг/мл в 0,1 N HCl, через который в течение двух часов продували газообразный N2) добавляли к 50 мл 20 мМ раствора трицина (рН 7,1, через который в течение одного часа продували газообразный N2; трицин=N-[трис(гидроксиметил)метил]глицин). 200 мкл раствора Sn-трицин добавляли в 100 мкл Tc99m (активность 4-8 мКи), смешанный с аликвотой 100 мкл аннексина V (приготовленного, как описано выше) согласно способам, описанным в работах Larson и соавт., Bioconjugate Chem. 6: 635-638, 1995.
Специфическая активность аннексина с радиоактивной меткой составляла 20-200 мкКи/мкг белка (в зависимости от желаемой активности) при радиочистоте 92-97%, определенной моментальной тонкослойной хроматографией (МТСХ) с использованием солевого раствора в качестве растворителя. Активность связывания мембраны ГНА-аннексина V и меченного Тс99m ГНА-аннексина V определяли модифицированным конкурентным анализом, в котором 5 нМ ФИТЦ (флуоресцинизотиоцианат)-аннексина V замещают I125-аннексином V (см. статью Wood B.L. и соавт., Blood 88: 1873-1880, 1996). Через 15 минут выдерживания при комнатной температуре образец центрифугируют, ФИТЦ-аннексин V, связанный с пеллетами клеток, высвобождают с помощью ЭДТУ (этилендиаминтетрауксусная кислота) и определяют высвобожденный ФИТЦ-аннексин V флуориметрией. В данной системе анализа немодифицированный аннексин, ГНА-аннексин и Тс99m-ГНА-аннексин V имели конкурентное ингибирование (50% концентраций связывания ФИТЦ-аннексина V) 8 нМ, 10,5 нМ и 12,3 нМ, соответственно. Введение ГНА в аннексин V, как показано, составляет 0,9 мол/моль аннексина V.
С. Визуализация и исследования биораспределения
Мышам инъецируют 50-150 мкКи Тс99m-ГНА-аннексина (0,125-0,25 мкг белка) после определения соотношения свободного и связанного Тс99m, используя МТСХ с солевым раствором в качестве растворителя. Изображения мышей, распростертых на животе, получают через один-два часа после инъекции радиофармацевтического препарата. Изображения получают через 15 минут, используя низкоэнергетическую подвижную (LEM) сцинтилляционную камеру с высокочувствительным параллельным коллиматором и матрицей для изображения 128×128 (Siemens, Des Plains, IL). Те же протоколы использовали для всех сканирований до и после обработки.
Исследования биораспределения проводили после сбора образцов шейных лимфатических узлов/слюнных желез, головного мозга, тимуса, сердца, легких, печени, селезенки, желудка, желудочно-кишечного тракта, почек, скелетной мускулатуры, жира, крови и оставшегося скелета. Образцы подсчитывали с помощью аутограммы сцинтилляционного счетчика Packard Cobra II (Packard Instrument, Downers Grove, IL), выраженной как скорректированные импульсы/минуту для изотопной метки и фоновой активности.
D. Иммунное окрашивание связанного человеческого аннексина V и апоптотических ядер
Из фиксированных формалином погруженных в парафин тканей делают срезы толщиной 5 мкм для окрашивания гематоксилином/эозином или другими способами. Иммунное окрашивание связанного человеческого аннексина V проводили с помощью антисыворотки кролика, образующейся против человеческого плацентарного аннексина V и аффинно очищенной рекомбинантным аннексином V, связанным с Affi-гелем (Bio-Rad). Затем иммуногистохимическое определение выполняли последовательными стадиями инкубирования с меченным биотином козьим антителом против кролика и комплексом авидин-пероксидаза хрена (Jackson Immuno Research) с последующей реакцией с 3, 3'-диаминобензидином, как описано Bindl и Warnke (см. работу Bindl J.M. и Warnke R.A., Am. J. Clin. Pathol. 85: 490-493, 1986, введенную в данный контекст в виде ссылки).
Для детекции апоптотических ядер среды окрашивали, используя модификацию способа мечения УТФ-конца, опосредованного концевой дезоксинуклеотидилтрансферазой (TUNEL), который описан Gavrieli и соавт. (см. статью Gavrieli Y. и соавт, J. Cell Biol. 119: 493-501, 1992, введенную в данный контекст в виде ссылки). После ингибирования эндогенной пероксидазы депарафинированные срезы расщепляли протеиназой К (20 мкг/мл) в течение 15 минут при комнатной температуре. Затем срезы инкубировали с λ-экзонуклеазой (Life Technologies, Gaithersburg, MD) в концентрации 5 единиц/мл в течение 30 минут при 37°С с последующим уравновешиванием буфером для реакции концевой дезоксинуклеотидилтрансферазы (0,2 М какодилата калия, 25 мМ трис НСl, 0,25 мг/мл BSA (бычий сывороточный альбумин), 1,5 мМ CaCl2, 20 мг/мл поливинилпирролидона и 20 мг/мл фиколла (синтетическая среда для фракционирования клеток крови)) и 5 мкМ dATP (аденозинтрифосфат). Реакцию введения метки в конец проводили в буфере для реакции концевой дезоксинуклеотидилтрансферазы, который содержит также концевую концентрацию 75 единиц/мл концевой дезоксинуклеотидилтрансферазы и 100 мкМ 1,N-6-этенол-dATP(Sigma). После 60-минутного инкубирования при 37°С реакцию останавливали путем промывания 1×СЦС (стандартный цитратный солевой раствор). Затем среды инкубировали с мышиными mAb (моноклональными антителами) 1G4 (предоставлены Regina Santella, Columbia University), которые распознают этеноадениновую структуру (см. статью Young T.L. и Santella P.M., Carcinogenesis 9: 589-592, 1988, введенную в данный контекст в виде ссылки). Последующее иммуногистохимическое определение проводили, как описано выше, с использованием меченного биотином козьего антитела против мыши.
Пример 1
Визуализация in vivo Fas-опрсредованного апоптоза
Апоптоз в печени у мышей индуцируют инъекцией антитела против Fas, которая вызывает обширный апоптоз в печени в течение от одного до двух часов с последующей гибелью через три часа 90% обработанных животных (см. статью Ogasawara J., Nature 364: 806, 1993).
Самкам мышей Balb/с в возрасте от пяти до шести недель с массой тела 18-24 г внутривенно инъецируют очищенное моноклональное антитело хомячка против Fas (Jo2, 10 мкг/животное, Pharmingen, San Diego, CA). После инъекции антитела против Fas животным внутривенно вводят приблизительно 90 мкКи гидразиноникотинамид(ГНА)-аннексина V, меченного радиоактивным изотопом технеция 99m (Тс99m), через 0, 1 и 2 часа после введения антитела в трех раздельных экспериментах. Результаты представляют на фиг. 1.
Заметное возрастание поглощения печенью аннексина V с радиоактивной меткой наблюдают через один и два часа, равное соответственно 148% и 372% от контрольных значений, что определяют анализом изображения представляющей интерес области (ПИО), приведенным на фиг. 1. Поглощение селезенкой временно поднимается до 140% от контрольных значений через один час после введения и падает до 110% через два часа. Поглощение почками падает на 40% через один и два часа после обработки.
Другой группе мышей (контроль) инъецируют 90 мкКи Тс99m-ГНА-овальбумина (мол. масса 43 кД; 2 мкг белка) через 0, 1 и 2 часа после введения антитела Jo2. Как показывают на фиг. 2, у данных животных происходит исходное повышение поглощения печенью через один час (127%), которое остается неизменным через два часа (131%) после введения антитела против Fas. Поглощение селезенкой овальбумина с радиоактивной меткой остается неизменным относительно контрольных значений после введения. Поглощение почками овальбумина с радиоактивной меткой повышается до 138% через один час и выходит на плато 131% от контрольного значения через два часа после введения.
Третью группу мышей обрабатывают, как описано выше, и вместе с меченным Тс99m аннексином V вводят им меченный I125 человеческий сывороточный альбумин (ЧСА) через 0, 1 и 2 часа в трех раздельных экспериментах. Животных в различных экспериментах умерщвляют после каждой соответствующей точки времени и исследуют биораспространение. Результаты, выражаемые в процентах инъецированной дозы/грамм ткани (% ИД/г), представляют в табл. 1 ниже. Данные соответствуют результатам, полученным при анализе изображения ПИО, как для аннексина V, так и для ЧСА с радиоактивными метками.

Пример 2
Визуализация in vivo отторжения сердечного аллотрансплантата
Тс99m-ГНА-аннексин V готовят практически так, как описано выше. Визуализацию и исследования биораспространения выполняют, как описано выше, за исключением случаев, где указано иначе.
Взрослым самцам крыс ACI (массой тела 250-350 г) пересаживают гетеротопные сердечные аллотрансплантаты от доноров PVG (получаемых от Harlan-Spraque-Dawley), соединенные анастамозом с брюшной аортой и нижней полой веной хозяев согласно модификации способа Оnо и Lindsey (см. статью Woodley S.L. и соавт., Transplantation 56: 1443-1447, 1993, введенную в данный контекст в виде ссылки). Сингенные сердечные изотрансплантаты от доноров ACI также трансплантируют в брюшную полость крыс ACI-хозяев. При использовании вышеописанной модели начало отторжения сердечных аллотрансплантатов PVG у реципиентов ACI происходит между 4 и 5 дней после трансплантации, что оценивают по пониженной пульсации при пальпации. Через пять дней после трансплантации всем животным вводят 700-900 мкКи Тс99m-ГНА-аннексина V (10-20 мкг белка/кг) в хвостовую вену и через 1 час получают изображение. Затем животных умерщвляют и проводят сцинтилляционный подсчет и гистологическое исследование нативного и трансплантированного сердец.
Все сердечные аллотрансплантаты PVG (n=4) легко визуализируют с помощью Тс99m-ГНА-аннексина V через 5 дней после трансплантации. Сингенные сердечные изотрансплантаты АСI (n=3) не имеют видимой активности после инъекции Тс99m-ГНА-аннексина при поглощении радиофармацевтического препарата идентично нативной сердечной активности, как подтверждено подсчетом сцинтилляции в лунках. Процент активности всего тела с аллотрансплантатом PVG превышает на 213% активность изотрансплантата ACI (Р<0, 005, при использовании двустороннего t-критерия Стьюдента), что определяют по анализу изображения ПИО. Анализ подсчета сцинтилляции в лунках показывает более чем 11-кратное повышение поглощения Тс99m-ГНА-аннексина V при аллотрансплантатах PVG по сравнению с нативной сердечной активностью.
Срезы сердечных аллотрансплантатов PVG через 5 дней после трансплантации показывают заметный инфильтрат мононуклеарных клеток зоны воспаления у всех животных; никакого инфильтрата не обнаруживают в сингенных или нативных сердцах. Инфильтрат окружает области повреждения миокарда и связан с тромбозом сосудов миокарда. В центре данных областей имеется явный некроз, не окрашивающийся гематоксилином, но на периферии имеются ядра с апоптотическими изменениями, что подтверждает окрашивание TUNEL. Иммунное окрашивание Тс99m-ГНА-аннексина V наблюдают в виде гранул в кардиомиоцитах на стыке областей воспаления и некроза; ядра данных клеток еще окрашиваются гематоксилином, предполагая далее, что они являются апоптотическими, а не некротическими. Окрашивание антианнексина V является гораздо более широким в плане числа положительных миоцитов и интенсивности по сравнению с TUNEL. Антианнексиновое окрашивание является плотным и представлено отдельными группами в явно некротических областях, как ожидается, но специфическим; окрашивание не обнаруживают в сингенных или нативных сердцах или при окрашивании аллотрансплантированных сердец, в которых удалены первичные антитела.
В отдельной, но близкой серии экспериментов крысам АСI (n=6 в каждой группе) пересаживают гетеротопные сердечные аллотрансплантаты от доноров PVG. Сингенные сердечные изотрансплантаты от доноров АСI (n=3 для каждой группы) трансплантируют крысам ACI-хозяевам. Ни в одной из групп не проводят лечение, предотвращающее отторжение трансплантата.
В группах крыс-реципиентов проводят ядерное сканирование на 1, 2, 3, 4, 5, 6 и 7 дни после трансплантации. За 1 час до ядерного сканирования вводят 1 мКи Тс99m-ГНА-аннексина V.
Сердечные аллотрансплантаты PVG легко визуализируют с помощью Тс99m-ГНА-аннексина V через 4 дня после трансплантации. Сингенные сердечные изотрансплантаты ACI не имеют видимой активности после инъекции Тс99m-ГНА-аннексина V.
Анализ представляющей интерес области (ПИО) используют для количественного определения поглощения Тс99m-ГНА-аннексина V. Поглощение трансплантированным сердцем вычисляют как процент от общего поглощения телом. Результаты представляют на фиг.3.
Сразу после ядерного сканирования животных безболезненно умерщвляют. Трансплантированные сердца сохраняют для анализа. Гистологическое определение степени острого отторжения проводят на стандартных срезах, окрашенных гематоксилином и эозином. Схема определения степеней приведена в табл. 2 ниже.

Апоптотические ядра идентифицируют в гистологических срезах с помощью окрашивания TUNEL распада ядерной ДНК, используя имеющийся в продаже набор пероксидазы (APORTAG, Oncor, Gaithersburg, MD). Как указывают данные, приведенные в табл. 3, апоптоз, очевидно, происходит в миоцитах и клетках зоны воспаления во время отторжения сердечного аллотрансплантата.

Как показывают результаты, приведенные в Таблице 4 ниже, и график, представленный на фиг. 4, поглощение Тс99m-ГНА-аннексина V коррелирует с гистологическими степенями острого отторжения.

Пример 3
Визуализация in vivo леченой лимфомы у мышей
Тс99m-ГНА-аннексин V готовят практически, как описано выше. Визуализацию и исследования биораспространения выполняют, как описано выше, за исключением случаев, где указывают иначе.
Мышиные В-клеточные лимфомы 38С13 (Maloney D.J. и соавт., Hybridoma 4: 191-209, 1985) культивируют в мышах C3H.HeN (Narean Breeders, Indianapolis) после подкожной инъекции 400 опухолевых клеток, суспендированных в 200 мкл среды RPMI 1640 (без сыворотки) в левый бок. Через четырнадцать дней после имплантации мышам проводят лечение путем внутрибрюшинной инъекции 100 мг/кг циклофосфамида. Мышам внутривенно вводят 25-50 мкг/кг Тс99m-ГНА-аннексина V (100-150 мкКи/животное) через 20 часов после введения циклофосфамида. Затем получают изображение животного и умерщвляют его через 2 часа после инъекции радиофармацевтического препарата после удаления опухоли для подсчета сцинтилляции и гистологических исследований.
Нелеченые боковые опухолевые имплантаты (n=8) хорошо видны при визуализации с помощью сцинтилляционной камеры и имеют 365%-ое превышение поглощения аннексина V относительно нормальной активности здоровой мягкой ткани, как показывают посредством анализа изображения ПИО. Леченые боковые опухоли (n=6) показывают легковизуализируемое повышение активности Тс99m-ГНА-аннексина V на 78% относительно контроля, выражаемое как активность всего тела/г опухоли (Р<0,05 при использовании двустороннего t - критерия Стьюдента для определения достоверности). Данный результат подтверждают подсчетом сцинтилляции в лунках, в котором леченые опухоли демонстрируют 132%-ое повышение поглощения аннексина V, выражаемое как процент введенной дозы/г опухоли (Р<0,05) при 58%-ом снижении массы (Р<0,05) по сравнению с контролем. Активность всего тела/г опухоли, как показывает анализ изображения ПИО, имеет линейную зависимость от процента введенной дозы/г опухоли, что определяют при исследовании биораспределения (r2=0,831). Гистологический анализ демонстрирует фактически полный (более 95%) апоптоз всех лимфобластов в леченых опухолях при менее чем 5% апоптотических клеток в контролях.
Поскольку изобретение было описано со ссылками на специфические способы и варианты осуществления, учитывается возможность осуществления различных модификаций и изменений без выхода за пределы объема изобретения.
Реферат
Изобретение относится к области медицины, в частности к радиологии. Способ позволяет повысить точность визуализации смерти клеток в области тела млекопитающего субъекта. Субъекту вводят аннексин, меченный биосовместимым радионуклидом, и затем помещают субъекта в поле обнаружения детектором излучения для конструирования изображения радиоактивной эмиссии спустя период времени, за который меченый аннексин достигает локализации в организме субъекта, причем указанное изображение представляет собой отображение смерти клеток в указанной области субъекта. При этом радионуклид выбирают из группы, состоящей из йода 123, йода 131, галлия 67, индия 111, фтора 18 и технеция 99m. 27 з.п. ф-лы, 4 табл., 4 ил.


Комментарии