Повторное аннотирование электроанатомической карты - RU2758750C1
Код документа: RU2758750C1
Чертежи




Описание
Область техники
Настоящее изобретение относится, по существу, к картированию сердца и, в частности, к повторному аннотированию области электроанатомической карты.
Уровень техники
Сердечная аритмия, такая как фибрилляция предсердий, представляет собой сердечный ритм, вызывающий нерегулярные сердечные сокращения. Аритмия, как правило, возникает, когда области сердечной ткани аномально проводят электрические сигналы к смежной ткани, таким образом нарушая нормальный сердечный цикл и вызывая асинхронный ритм сердца.
Картирование электрических потенциалов сердца является широко используемым инструментом для диагностики и лечения аритмий сердца. Как правило, изменяющиеся во времени электрические потенциалы в эндокарде воспринимаются и регистрируются в зависимости от положения внутри сердца, а впоследствии применяются для картирования локальной электрограммы или времени местной активации. Время активации в эндокарде отличается от точки к точке, что обусловливается временем, необходимым для проведения электрических импульсов через сердечную мышцу. Направление этой электрической проводимости в любой точке в сердце условно представлено вектором активации, который расположен под прямым углом к изоэлектрическому фронту активации, оба из которых могут быть получены из карты времени активации. Скорость распространения фронта активации через любую точку в эндокарде может быть представлена в виде вектора скорости.
Картирование фронта активации и полей проводимости помогает врачу в выявлении и диагностике патологий, таких как желудочковая и предсердная тахикардия и фибрилляции желудочков и предсердий, которые возникают при наличии в ткани сердца областей с ухудшенным распространением электрического сигнала.
В заявке на патент США 2017/0251942 описан способ определения времени локальной активации (LAT) из по меньшей мере трех сигналов многоканальной электрограммы сердца, включая канал картирования и множество референтных каналов. Способ включает в себя сбор сигнала канала картирования и первого сигнала референтного канала для вычисления значений LAT во множестве местоположений канала картирования, контроль стабильности синхронизации сигнала первого референтного канала и, если стабильность синхронизации отслеживаемого сигнала падает ниже стандарта стабильности, использование сигнала второго референтного канала для определения значений LAT.
В заявке на патент США № 2018/0042504 описан способ аннотирования фронта импульса. Способ включает в себя прием биполярного сигнала от пары электродов вблизи миокарда человеческого индивида, прием униполярного сигнала от выбранного одного из пары электродов, предварительную обработку сигналов электродов для устранения блуждания базовой линии, низкочастотную фильтрацию и любой порядок дифференциации. Способ также включает в себя идентификацию потенциальных аннотирований в сигналах, извлечение характеристик из аннотирований, устранение любых потенциальных аннотирований, отвечающих критерию, основанному на пороговом значении характеристики, устранение любых оставшихся потенциальных аннотирований, которые являются несущественными по отношению к другой очень близкой активации, назначение количественного показателя каждому оставшемуся потенциальному аннотированию на основе его значений характеристики и формирование карты с использованием синхронизации и характеристик потенциальных аннотирований, которые превышают пороговый количественный показатель.
В патенте США № 6301496 описан способ реконструкции сетки, содержащей множество дискретных точек. Способ включает применения этапа деформации модели к сетке, на котором сетка приблизительно отрегулирована в соответствии с формой, образованной дискретными точками. Способ также включает в себя итеративный этап гибкого сопоставления, который выполняется путем точной регулировки точек сетки в соответствии с координатами дискретных точек. Способ дополнительно включает применение одного или более алгоритмов, таких как сглаживание, аффинное преобразование и/или выполнение этапа точного соответствия, приводящее к тому, что сетка включает в себя, по существу, все дискретные точки. Значения параметров, связанные с дискретными точками, могут быть интерполированы по всем точкам сетки, и сетка может быть представлена на дисплее.
В заявке на патент США № 2017/0027524 описан способ обнаружения полезных сигналов в многоканальной системе картирования, которая принимает сигналы от множества электродов. Способ включает в себя получение сигнала от данного электрода, вычисление первой производной сигнала, определение минимума и максимума производной из первой производной, определение того, отличаются ли знаки минимума и максимума производной, и в ответ на определение того, отличаются ли знаки минимума и максимума производной, отображение на устройстве отображения, является ли сигнал полезным.
Вышеприведенное описание представлено в качестве общего обзора уровня техники в данной области, и его не следует воспринимать, как признание того, что любая содержащаяся в нем информация составляет предшествующий уровень техники, противопоставляемый настоящей заявке на патент.
Документы, на которые дается ссылка в настоящей заявке на патент, следует считать неотъемлемой частью заявки, за исключением того, что, если определение терминов в этих включенных документах противоречит определениям, сделанным явным или неявным образом в настоящем описании, следует учитывать только определения настоящего описания.
Сущность изобретения
В соответствии с одним вариантом осуществления настоящего изобретения предлагается способ, включающий прием компьютером от внутрисердечного катетера, имеющего дистальный конец, включающий в себя множество электродов, расположенных в соответствующих местоположениях внутри сердца субъекта, сигналов от электродов, реагирующих на электрическую активность в ткани миокарда, в контакте с которой находятся электроды, обработку сигналов с помощью компьютера, чтобы идентифицировать для каждого заданного местоположения, с которым контактирует электрод, по меньшей мере одно соответствующее время локальной активации (LAT) в цикле сердца, идентификацию с помощью компьютера наиболее раннего LAT в цикле для каждого из местоположений, генерирование и визуализацию на дисплее электроанатомической карты, включающей в себя точки картирования, имеющие соответствующие местоположения и указывающие наиболее раннее LAT в каждом местоположении на карте, прием в компьютере входного сигнала, выбирающего подмножество точек картирования, идентификацию с помощью компьютера временного диапазона, содержащего наиболее раннее LAT большинства точек картирования в подмножестве, идентификацию в подмножестве с помощью компьютера одной или более вышележащих точек картирования, для которых наиболее раннее LAT предшествует идентифицированному временному диапазону, нахождение с помощью компьютера среди по меньшей мере одного LAT, идентифицированного в вышележащих точках картирования, соответствующего второго LAT, более позднего, чем наиболее раннее LAT в цикле сердца, и обновление и визуализацию электроанатомической карты для отображения соответствующего второго LAT, которое было найдено в одной или более из вышележащих точек картирования.
В некоторых вариантах осуществления внутрисердечный катетер включает в себя многошлицевый катетер, имеющий по меньшей мере один из электродов на каждом из шлицев.
В дополнительных вариантах осуществления сигналы включают в себя сигналы электрокардиограммы.
В дополнительных вариантах осуществления идентификация временного диапазона, содержащего наиболее раннее LAT большинства точек картирования в подмножестве, включает в себя применение алгоритма голосования большинством к LAT в подмножестве.
В дополнительных вариантах осуществления соответствующее второе LAT находится в пределах идентифицированного временного диапазона.
В других вариантах осуществления этап обновления и визуализации электроанатомической карты выполняется при приеме разрешающего сигнала.
В соответствии с одним вариантом осуществления настоящего изобретения также предлагается устройство, содержащее дисплей и процессор, выполненный с возможностью приема от внутрисердечного катетера, имеющего дистальный конец, включающий в себя множество электродов, расположенных в соответствующих местоположениях внутри сердца субъекта, сигналов от электродов, реагирующих на электрическую активность в ткани миокарда, в контакте с которой находятся электроды, обработки сигналов, чтобы идентифицировать для каждого заданного местоположения, с которым контактирует электрод, по меньшей мере одно соответствующее время локальной активации (LAT) в цикле сердца, с целью идентификации наиболее раннего LAT в цикле для каждого из местоположений, генерирования и визуализации на дисплее электроанатомической карты, включающей в себя точки картирования, имеющие соответствующие местоположения и указывающие наиболее раннее LAT в каждом местоположении на карте, приема входного сигнала, выбирающего подмножество точек картирования, идентификации временного диапазона, содержащего наиболее раннее LAT большинства точек картирования в подмножестве, идентификации в подмножестве одной или более вышележащих точек картирования, для которых наиболее раннее LAT предшествует идентифицированному временному диапазону, нахождения среди по меньшей мере одного LAT, идентифицированного в вышележащих точках картирования, соответствующего второго LAT, более позднего, чем наиболее раннее LAT в цикле сердца, и обновления и визуализации электроанатомической карты для отображения соответствующего второго LAT, которое было найдено в одной или более из вышележащих точек картирования.
В соответствии с дополнительным вариантом осуществления настоящего изобретения также предлагается компьютерный программный продукт, используемый в сочетании с внутрисердечным катетером, имеющим дистальный конец, содержащий множество электродов, для введения в сердце субъекта, причем указанный продукт содержит энергонезависимый машиночитаемый носитель, в котором хранятся команды программы, которые при их считывании компьютером инициируют на компьютере следующие действия: прием от внутрисердечного катетера, имеющего дистальный конец, включающий в себя множество электродов, расположенных в соответствующих местоположениях внутри сердца субъекта, сигналов от электродов, реагирующих на электрическую активность в ткани миокарда, в контакте с которой находятся электроды, обработка сигналов, чтобы идентифицировать для каждого заданного местоположения, с которым контактирует электрод, по меньшей мере одно соответствующее время местной активации (LAT) в цикле сердца, идентификация наиболее раннего LAT в цикле для каждого из местоположений, генерирование и визуализация на дисплее электроанатомической карты, включающей в себя точки картирования, имеющие соответствующие местоположения и указывающие наиболее раннее LAT в каждом местоположении на карте, прием входного сигнала, выбирающего подмножество точек картирования, идентификация временного диапазона, содержащего наиболее раннее LAT большинства точек картирования в подмножестве, идентификация в подмножестве одной или более вышележащих точек картирования, для которых наиболее раннее LAT предшествует идентифицированному временному диапазону, нахождение среди по меньшей мере одного LAT, идентифицированного в вышележащих точках картирования, соответствующего второго LAT, более позднего, чем наиболее раннее LAT в цикле сердца, и обновление и визуализация электроанатомической карты для отображения соответствующего второго LAT, которое было обнаружено в одной или более из вышележащих точек картирования.
Краткое описание чертежей
Настоящее изобретение описано в данном документе только в качестве примера со ссылкой на прилагаемые чертежи, на которых:
Фиг. 1A и 1B - графическое изображение медицинской системы, содержащей картирующий катетер в соответствии с вариантом осуществления настоящего изобретения;
Фиг. 2 - графическое изображение дистального конца картирующего катетера в соответствии с вариантом осуществления настоящего изобретения;
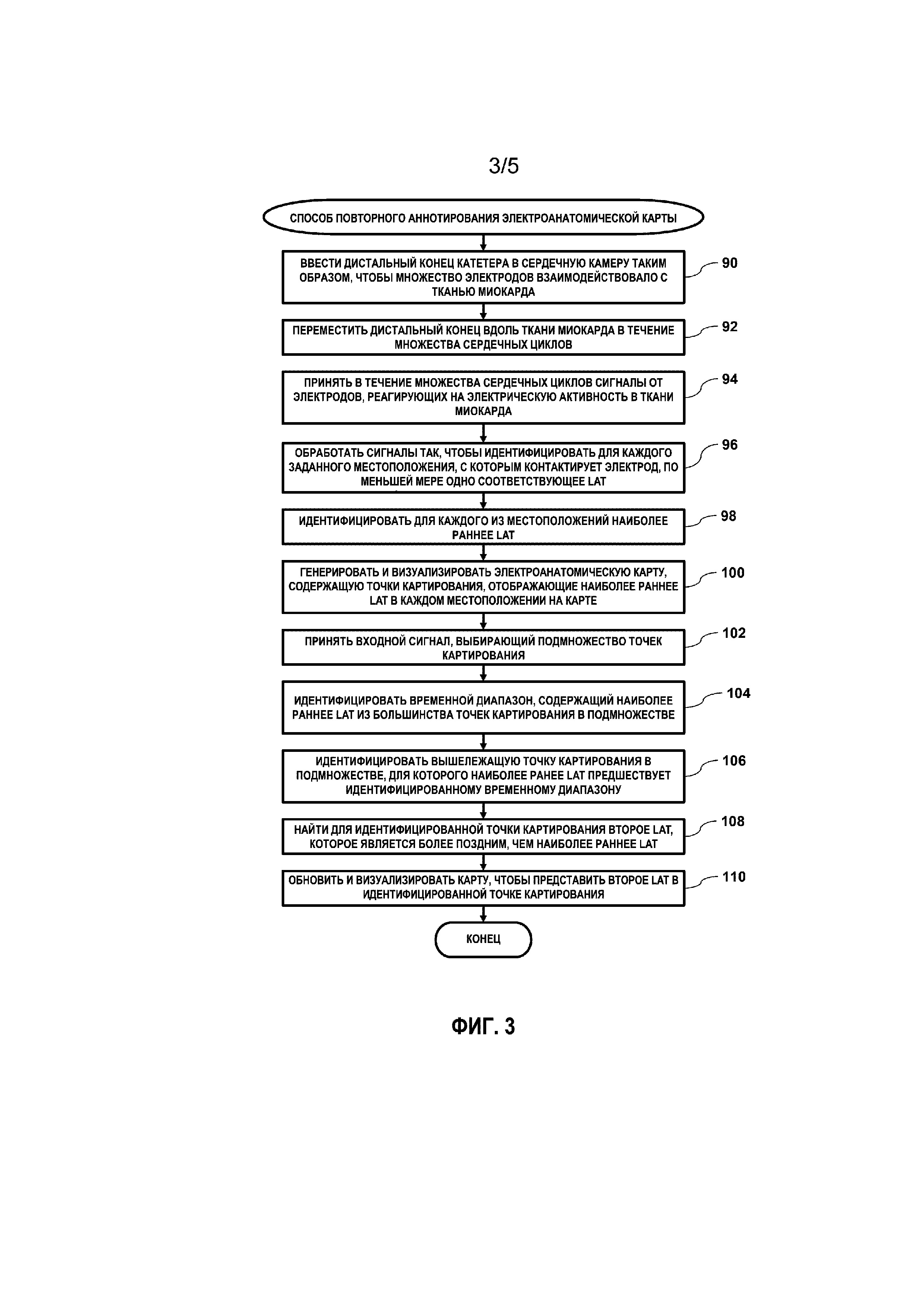
Фиг. 3 - блок-схема, которая схематически иллюстрирует способ генерирования и повторного аннотирования электроанатомической карты, основанной на сигналах, принятых от картирующего катетера, в соответствии с вариантом осуществления настоящего изобретения;
Фиг. 4 - схематический подробный вид дистального конца картирующего катетера в камере сердца во время процедуры картирования в соответствии с вариантом осуществления настоящего изобретения; и
Фиг. 5 - схематический вид электроанатомической карты, содержащей точку картирования, имеющую вышележащее время локальной активации, в соответствии с одним из вариантов осуществления настоящего изобретения.
Подробное описание вариантов осуществления изобретения
При выполнении медицинской процедуры с целью получения электроанатомической карты камеры сердца дистальный конец картирующего катетера перемещают вдоль ткани миокарда в пределах камеры и получают сигналы из разных измеренных местоположений. Сигналы автоматически анализируют, чтобы найти их соответствующие времена локальной активации (LAT), и электроанатомическую карту генерируют и визуализируют так, чтобы LAT были представлены разным цветом (т.е. для разных моментов времени) на трехмерной (3D) карте камеры.
Могут быть случаи, когда автоматический анализ сигнала генерирует на карте некоторые ошибочные значения LAT. В вариантах осуществления настоящего изобретения предложены способы и системы для коррекции любых ошибочных значений LAT, которые были получены с помощью автоматического анализа. Как описано ниже в настоящем документе, при приеме из внутрисердечного катетера, имеющего дистальный конец, содержащий множество электродов, расположенных в соответствующих местоположениях внутри сердца субъекта, сигналов от электродов, реагирующих на электрическую активность в ткани миокарда, с которой контактируют электроды, эти сигналы обрабатываются так, чтобы определять для каждого заданного местоположения, с которым контактирует электрод, по меньшей мере одно соответствующее LAT в цикле сердца. Для каждого из местоположений идентифицируют наиболее раннее LAT в цикле и генерируют и визуализируют на дисплее электроанатомическую карту, содержащую точки картирования, имеющие соответствующие местоположения на карте и указывающие наиболее раннее LAT в каждом местоположении.
После визуализации карты принимают входной сигнал, указывающий на выбранное подмножество точек картирования, и идентифицируют временной диапазон, который содержит наиболее раннее LAT большинства точек картирования в подмножестве. Идентифицируют одну или более вышележащих точек картирования в подмножестве, для которых наиболее раннее LAT предшествует идентифицированному временному диапазону, и находят среди по меньшей мере одного LAT, идентифицированного в вышележащих точках картирования, соответствующее второе LAT, более позднее, чем наиболее раннее LAT в цикле сердца, в одной или более вышележащих точках картирования. В завершение обновляют и визуализируют электроанатомическую карту для отображения соответствующего второго LAT, который был найден в одной или более из вышележащих точек картирования.
Электроанатомические карты могут содержать точки картирования на основе большого числа (возможно, ~5000) сигналов. Благодаря автоматической коррекции любых точек картирования в выбранных областях системы, реализующие варианты осуществления настоящего изобретения, позволяют медицинскому специалисту быстро корректировать подмножество (возможно, ~100) точек картирования, которые соответствуют ошибочным значениям LAT.
Описание системы
На Фиг. 1A и 1B представлены схематические, графические изображения медицинской системы 20, содержащей медицинский зонд 22 и пульт 24 управления, а на Фиг. 2 представлена схематическое наглядное изображение дистального конца 26 медицинского зонда 22 в соответствии с примером осуществления настоящего изобретения. Медицинскую систему 20 можно создать, например, на основе системы CARTO®, производимой Biosense Webster Inc. (Даймонд Бар, Калифорния, США). В примерах осуществления, описанных далее в настоящем документе, медицинский зонд 22 можно использовать для диагностической или терапевтической обработки, например, для такой как картирование электрических потенциалов сердца 28 пациента 30. В примерах осуществления, описанных в настоящем документе, медицинский зонд 22 также может называться картирующим катетером. Альтернативно медицинский зонд 22 можно использовать, после внесения соответствующих изменений, при выполнении других терапевтических и/или диагностических процедур на сердце или других органах тела.
Медицинский зонд 22 содержит вводимую трубку 32 и рукоятку 34, соединенную с проксимальным концом вводимой трубки. С помощью рукоятки 34 медицинский специалист 36 может вставить зонд 22 в полость тела пациента 30. Например, медицинский специалист 36 может вставить зонд 22 через сосудистую систему пациента 30 так, чтобы дистальный конец 26 зонда 22 входил в камеру сердца 28 и взаимодействовал с тканью миокарда в требуемом местоположении или местоположениях. В качестве примера, как показано на Фиг. 2, дистальный конец 26 зонда 22 содержит гибкие шлицы 80, образованные на конце трубчатого стержня 82. Во время медицинской процедуры медицинский специалист 36 может развернуть шлицы 80 путем вытягивания трубчатого стержня из вводимой трубки 32.
Пульт 24 управления соединен посредством кабеля 38 с электродами на поверхности тела, которые, как правило, содержат адгезивные кожные пластыри 40, прикрепленные к пациенту 30. Пульт 24 управления содержит процессор 42, который в сочетании с модулем 44 отслеживания тока определяет координаты местоположения дистального конца 26 внутри сердца 28 на основе значений импеданса, измеренных между адгезивными кожными пластырями 40 и электродами 84 для картирования, прикрепленными к шлицам 80, как показано на Фиг. 2. В примерах осуществления, описанных в настоящем документе, электроды 84 могут также быть выполнены с возможностью подачи сигнала в ткань сердца 28 и/или для измерения определенного физиологического свойства (например, локального электрического потенциала поверхности) в некотором местоположении в сердце. Электроды 84 соединены с пультом 24 управления при помощи проводов (не показаны), проходящих через медицинский зонд 22.
В то время как в примерах осуществления в настоящем документе показан зонд 22, содержащий многошлицевый внутрисердечный катетер, такой как катетер Pentaray© NAV, применение других многоэлектродных внутрисердечных катетеров, таких как катетеры Navistar®, Thermocool®, считается находящимся в пределах сущности и объема настоящего изобретения. Как катетеры Pentaray© NAV, так и катетеры Navistar® Thermocool® производятся Biosense Webster Inc.
Процессор 42 может содержать схему 46 подавления шума в режиме реального времени, как правило, выполненную в виде программируемой пользователем интегральной схемы (FPGA), за которой следует интегральная схема 48 аналого-цифрового преобразования (АЦП) сигнала ЭКГ (электрокардиографа). Процессор может передавать сигнал от схемы 48 аналого-цифрового преобразователя ЭКГ к другому процессору и/или он может быть запрограммирован на выполнение одного или более алгоритмов, описанных в настоящем документе, причем каждый из одного или более алгоритмов включает этапы, описанные ниже в настоящем документе. Процессор использует схему 46 и схему 48, а также элементы модулей, которые описаны более подробно ниже в настоящем документе, для выполнения одного или более алгоритмов.
В медицинской системе, показанной на Фиг. 1 и 2, для измерения местоположения дистального конца 26 используют измерение на основе импеданса, но можно использовать и другие способы отслеживания положения (например, способы с использованием датчиков на основе магнита). Способы отслеживания положения на основе импенданса описаны, например, в патентах США № 5983126, 6456864 и 5944022. Способы определения положения, описанные выше в данном документе, реализованы в вышеупомянутой системе CARTO® и подробно описаны в упомянутых выше патентах.
Пульт 24 управления также содержит интерфейс 50 связи ввода/вывода (I/O), посредством которого пульт управления получает сигналы от электродов 84 и адгезивных кожных пластырей 40 и/или передает на них сигналы. На основании сигналов, принятых от электродов 84 и/или адгезивных кожных пластырей 40, процессор 42 может генерировать электроанатомическую карту 52 времени локальной активации (LAT) (Фиг. 1A), на которой представлены измерения скорости сердечной проводимости, как описано в описании со ссылкой на Фиг. 5 ниже в настоящем документе.
Во время выполнения процедуры процессор 42 может отобразить электроанатомическую карту 52 LAT на дисплее 54 для медицинского работника 36 и сохранить данные, представляющие электроанатомическую карту LAT, в памяти 56, как описано в описании со ссылкой на Фиг. 1A ниже в настоящем документе. Память 56 может содержать любую приемлемую энергозависимую и/или энергонезависимую память, такую как оперативное запоминающее устройство или жесткий диск. В некоторых примерах осуществления медицинский специалист 36 может управлять картой 52 с помощью одного или более устройств 78 ввода. В альтернативных вариантах осуществления дисплей 54 может содержать сенсорный экран, который в дополнение к отображению карты 52 может быть выполнен с возможностью приема входных данных от медицинского специалиста 36.
Пульт 24 управления может также содержать электрокардиографический (ECG) модуль 58, который может быть выполнен с возможностью генерирования ЭКГ-диаграммы 60 на основе сигналов, полученных от электродов 84. В некоторых вариантах осуществления процессор 42 представляет одну или более ЭКГ-диаграмм 60 на дисплее 54 (т.е. вместе с картой 52 LAT) и сохраняет данные, представляющие карту ЭКГ-диаграммы, в памяти 56.
Как показано на Фиг. 1A, память 56 хранит данные 62 электроанатомической карты, которые процессор 42 может использовать для генерирования и визуализации электроанатомической карты 52, и сохраняет наборы 64 данных ЭКГ-диаграммы, которые процессор может использовать для генерирования и визуализации ЭКГ-диаграмм 60. Данные электроанатомической карты содержат множество записей 66 точек картирования, причем каждая из записей точек картирования содержит набор координат 68 местоположения (т.е. в пациенте 30) и время 70 локальной активации (LAT). В примерах осуществления в настоящем документе координаты 68 местоположения также могут называться местоположениями 68.
Каждый набор 64 данных сигналов ЭКГ содержит множество записей 72 точек ЭКГ-диаграммы, причем каждая из записей точек сигнала ЭКГ содержит время 74 измерения и измерение 76 электрического потенциала. В примерах осуществления в настоящем документе каждый заданный электрод 84 имеет соответствующее соответствие друг к другу с данным набором 64 данных ЭКГ-диаграммы. Другими словами, каждый заданный набор 64 данных ЭКГ-диаграммы хранит множество записей точек ЭКГ-диаграммы, в которых хранятся измерения 76 электрических потенциалов и время 74 измерения, которые процессор 42 получает от его соответствующего электрода 84.
Генерирование и повторное аннотирование электроанатомической карты
На Фиг. 3 представлена блок-схема, на которой схематически показан способ генерирования и повторного аннотирования электроанатомической карты 52 для камеры сердца 28, а на Фиг. 4 представлен схематический подробный вид шлицев 80, взаимодействующих с тканью 120 миокарда в камере, в соответствии с примером осуществления настоящего изобретения.
На этапе 90 введения медицинский специалист 36 вставляет дистальный конец 26 в камеру так, чтобы шлицы 80 взаимодействовали с тканью миокарда 120, а на стадии 92 маневрирования медицинский специалист 36 перемещает шлицы 80 на дистальном конце 26 вдоль ткани 120 миокарда во время нескольких сердечных циклов. По мере того как медицинский специалист 36 перемещает шлицы 80 вдоль ткани 120 миокарда во время нескольких сердечных циклов, процессор 42 принимает сигналы местоположения, которые указывают значения импеданса, измеренные между адгезивными кожными пластырями 40 и электродами 84.
В некоторых примерах осуществления процессор 42 может определять заданное местоположение данного электрода 84 путем передачи на модуль 44 отслеживания тока сигналов о местоположении, полученных от адгезивных кожных пластырей 40, а модуль отслеживания 44 тока может вычислять заданное местоположение с использованием вариантов осуществления, описанных выше. После приема сигналов местоположения от каждого заданного электрода 84 процессор 42 может обработать сигналы местоположения для определения соответствующих наборов координат местоположения для электродов.
На первом этапе 94 приема процессор 42 также принимает (т.е. в дополнение к приему сигналов местоположения) от электродов 84 в соответствующее времена получения выборки сигналы измерения, реагирующие на электрическую активность в ткани 120 миокарда, с которой контактируют электроды 84. На этапе 96 обработки процессор 42 обрабатывает сигналы измерения так, чтобы идентифицировать для каждого заданного набора координат местоположения, с которыми контактирует электрод, значения электрических потенциалов, указанные посредством сигналов измерения, и идентифицировать по меньшей мере одно соответствующее время локальной активации (LAT) в цикле сердца 28.
После приема и обработки сигналов картирования и определения местоположения для данного электрода 84 процессор 42 добавляет в соответствующий набор данных ЭКГ-диаграммы соответствующие записи 72 для каждого из времен получения выборки и заполняет для каждой добавленной записи 72 точки ЭКГ-диаграммы, время 74 измерения с соответствующим временем получения выборки, и измерение 76 потенциала с соответствующим значением электрического потенциала. После сохранения и заполнения наборов данных 64 ЭКГ-диаграммы процессор 42 добавляет новую запись 66 для каждого из идентифицированных LAT и заполняет для каждой добавленной записи 66 данных точки картирования (т.е. соответствующей данному LAT) местоположение 68 с координатами местоположения соответствующих LAT и LAT 70 с временем получения выборки соответствующего LAT.
На первом этапе 98 идентификации процессор 42 идентифицирует для каждого заданного набора координат 68 местоположения наиболее раннего из LAT в цикле. Как правило, процессор 42 идентифицирует одно LAT 70 для каждого заданного набора координат 68 местоположения. Однако возможны случаи, когда процессор 42 идентифицирует более одного LAT 70 для каждого заданного набора координат 68 местоположения. ЭКГ-диаграммы 60, отображающие одно и множество LAT 70 описаны в описании со ссылкой на Фиг. 5 ниже в настоящем документе.
На этапе 100 генерирования карты процессор 42 генерирует и визуализирует на дисплее 54 электроанатомическую карту 52, содержащую точки картирования, имеющие соответствующие местоположения 68 и отображающие более раннее LAT 70 в каждом из местоположения на карте.
На Фиг. 5 представлено схематическое графическое изображение, на котором показана секция карты 52 LAT, которая содержит физическую карту 130 камеры сердца 28 в соответствии с примером осуществления настоящего изобретения. На Фиг. 5 информация о времени локальной активации для карты 52 встроена в физическую карту 130 и закодирована с использованием узоров в соответствии с ключом 132. Эти узоры моделируют псевдоцвета фактической функциональной карты. В этом примере карта 52 содержит первую область 134, которая имеет относительно короткое LAT, и вторую область 136, которая имеет относительно более длительное время локальной активации.
Карта 52 LAT содержит множество точек 140 (140A и B, как описано ниже) картирования, причем каждая из точек картирования соответствует заданному набору координат 68 местоположения и заданному времени 70 локальной активации. На этапе 102 выбора процессор принимает входной сигнал (например, от устройств 78 ввода), выбирая область на карте, содержащую подмножество 138 точек картирования. В некоторых интерфейсах пользователя это устройство ввода может содержать «инструмент Кисть».
На втором этапе 104 идентификации процессор 42 идентифицирует временной диапазон, содержащий наиболее раннее LAT для большинства точек картирования в подмножестве. Например, процессор 42 для определения временного диапазона может использовать алгоритм голосования большинством Бойера-Мура. На Фиг. 5 точки 140 картирования соответствуют соответствующим ЭКГ-диаграммам 60, причем точки картирования, ЭКГ-диаграммы и соответствующие элементы ЭКГ-диаграмм могут быть дифференцированы путем присоединения буквы к идентификационному номеру, так что точки 140A картирования соответствуют ЭКГ-диаграмме 60A, а точка 140B картирования соответствует ЭКГ-диаграмме 60B.
Каждая ЭКГ-диаграмма 60 содержит траекторию, содержащую линию 142, на которой показаны измерения 76 потенциалов вдоль вертикальной оси 144 относительно времени вдоль горизонтальной оси 146, причем потенциалы измеряются как напряжения V, а время измеряется в секундах S. На ЭКГ-диаграммах 60 линии 142 представляют измерения 76 потенциала, измеренные во время одного сердечного цикла.
На ЭКГ-диаграммах, показанных на Фиг. 5, представлено время локальной активации по отношению к эталонной аннотации 148. Например, точки 140A картирования могут соответствовать ЭКГ 60A, которая содержит точку 150 LAT, которая соответствует времени 70 локальной активации, которое (в целях данного примера) составляет 10 мс после времени, указанного в эталонной аннотации 148A. В некоторых примерах осуществления точки 140A картирования могут соответствовать первому заданному LAT 70 с допуском 10 мс +/- 5 мс. Другими словами, процессор 42 может представлять точки 140A картирования для местоположений 68, времена 70 локальной активации которых находятся в пределах временного диапазона 5-15 мс после времени, указанного эталонной аннотацией 148A. В этом случае на этапе 104 процессор 42 идентифицирует временной диапазон в течение 5-15 мс после времени, указанного в эталонной аннотации 148A. В некоторых примерах осуществления временной диапазон может быть задан медицинским специалистом 36.
В примере, представленном на Фиг. 5, точка 140B картирования может соответствовать ЭКГ 60B, которая содержит точку 152 LAT, соответствующую второму заданному времени 70 локальной активации, которое (в целях данного примера) составляет 50 мс перед временем, указанным в эталонной аннотации 148B, и точку 154 LAT, которая соответствует второму заданному времени 70 локальной активации, которое составляет (например) 11 мс после времени, указанного в эталонной аннотации 148B. Как описано выше, для генерирования карты 52 процессор 42 использует наиболее раннее LAT 70 для каждого набора 68 координат местоположений. Таким образом, точка картирования 140A на карте 52 соответствует LAT, указанной точкой 152 LAT.
Возвращаясь к блок-схеме, на третьем этапе 106 идентификации процессор 42 идентифицирует одну или более вышележащих точек 60 картирования в подмножестве 138, для которой наиболее раннее соответствующее LAT 70 предшествует идентифицированному временному диапазону. В примере, показанном на Фиг. 5, процессор 42 идентифицирует точку 140B картирования в качестве вышележащей точки картирования. В этом примере координаты местоположения точки 140B картирования находятся внутри области 134, а LAT для точки 140B картирования (то есть, согласно легенде 132) аналогично точкам картирования в области 136.
На этапе 108 нахождения процессор 42 находит среди по меньшей мере одного LAT, идентифицированного на вышележащих точках картирования, соответствующее второе LAT, более позднее, чем наиболее раннее LAT в цикле сердца, в одной или более из вышележащих точек картирования. В примере, показанном на Фиг. 5, процессор 42 идентифицирует LAT, соответствующее точке 154 LAT, как более позднее LAT для местоположения, соответствующего точке 140B картирования. В некоторых примерах осуществления идентифицированное более позднее LAT находится в пределах временного диапазона, определенного на этапе 104.
В завершение на этапе 110 обновления процессор 42 обновляет и визуализирует электроанатомическую карту 52 на дисплее 54 для представления соответствующего второго LAT, которое было найдено в одной или более из вышележащих точек картирования, и способ завершается. Для обновления и визуализации электроанатомической карты 52 процессор 42 может заменить на дисплее 54 псевдоцвет для точки 140B картирования с таким же псевдоцветом, который используется для точек 140A картирования.
В некоторых примерах осуществления процессор 42 может выполнять этап 110 обновления после получения подтверждения от медицинского специалиста 36. Например, после идентификации второго LAT на этапе 108 процессор 42 может представить второе LAT на дисплее 54 и представить на дисплее сообщение с запросом на подтверждение обновления карты. После получения сообщения о подтверждении (например, от заданного устройства 78 ввода) процессор 42 может обновить и визуализировать электроанатомическую карту 52 на дисплее 54.
Следует понимать, что описанные выше варианты осуществления приведены лишь в качестве примера и что настоящее изобретение не ограничено вариантами, показанными и подробно описанными выше в настоящем документе. Напротив, объем настоящего изобретения включает как комбинации, так и подкомбинации различных элементов, описанных выше в настоящем документе, а также их варианты и модификации, которые могут быть предложены специалистами в данной области после прочтения приведенного выше описания и которые не были описаны на предшествующем уровне техники.
Реферат
Изобретение относится к медицине и может быть использовано для аннотирования электроанатомической карты. Предложен способ, включающий прием от электродов для картирования, расположенных в местоположениях внутри сердца, сигналов, указывающих на электрическую активность в контактирующих с электродами тканях, и обработку сигналов c целью идентификации, для каждого местоположения, по меньшей мере одного соответствующего LAT в цикле сердца. Для каждого местоположения идентифицируют наиболее раннее LAT в цикле и генерируют и визуализируют электроанатомическую карту, включающую в себя точки картирования, имеющие соответствующие местоположения и указывающие наиболее раннее LAT в каждом местоположении. Принимают ввод, выбирающий подмножество точек, и определяют временной диапазон, содержащий наиболее раннее LAT в большинстве точек в подмножестве. Идентифицируют одну или более вышележащих точек в подмножестве, и обнаруживают второе LAT, более позднее, чем наиболее раннее LAT в цикле, среди по меньшей мере одного идентифицированного LAT, идентифицированного в вышележащих точках. Карту обновляют для отображения найденного второго LAT. Группа изобретений обеспечивает повышение эффективности коррекции ошибочных значений LAT в цикле сердца. 3 н. и 10 з.п. ф-лы, 5 ил.

Комментарии