Энергетическая модуляция нервов - RU2523129C2
Код документа: RU2523129C2
Чертежи

































































Описание
ПРИОРИТЕТНЫЕ ДАННЫЕ
Эта заявка испрашивает приоритет и включает посредством ссылки следующие заявки:
Заявку на патент США под № 12/725450, поданную 16 марта 2010 года.
Заявку на патент США по № 12/685655, поданную 11 января 2010 года.
Предварительную заявку на патент США под № 61/250857, поданную 12 октября 2009 года.
Предварительную заявку на патент США под № 61/256983, поданную 31 октября 2009 года.
Предварительную заявку на патент США под № 61/261741, поданную 16 ноября 2009 года.
Предварительную заявку на патент США под № 61/291359, поданную 30 декабря 2009 года.
Предварительную заявку на патент США под № 61/303307, поданную 10 февраля 2010 года.
Предварительную заявку на патент США под № 61/347375, поданную 21 мая 2010 года.
Предварительную заявку на патент США под № 61/377908, поданную 27 августа 2010 года.
В эту заявку посредством ссылки также в прямой форме включены следующие заявки на патент:
Заявки на патент США под №№ 11/583569, 12/762938, 11/583656, 12/247969, 10/633726, 09/721526, 10/780405, 09/747310, 12/202195, 11/619996, 09/696076, 11/016701, 12/887178, 12/390975, 12/887178, 12/887211, 12/887232.
Следует отметить, что объекты вышеуказанных заявок и любых упомянутых посредством ссылки прочих заявок в прямой форме включены в данную заявку так, как будто они прямым образом изложены в этой заявке. Таким образом, в представленном здесь примере ссылки конкретно не помечаются как «включенные посредством ссылки» в данную заявку, по сути, они полагаются описанными в данной заявке.
Уровень техники
Передача энергии на расстояние включает передачу волн энергии для воздействия на цель, расположенную на расстоянии. Это позволяет более эффективно подавать энергию к цели и достичь более высокой экономической эффективности и технологической гибкости при создании генератора волн энергии. Например, сотовые телефоны получают координаты цели от вышек, расположенных рядом с пользователем, а сами вышки обмениваются друг с другом информацией на большом расстоянии; за счет этого сотовые телефоны могут питаться от низковольтного источника энергии и связываться друг с другом в относительно узком частотном диапазоне, но несмотря на это телефонные сети могут быстро подключаться друг к другу по всему миру. Аналогичным образом, распределение электроэнергии, произведенной большими генерирующими станциями, среди пользователей более эффективно, чем поиск решений этой проблемы самими пользователями.
Если говорить о лечении пациента, то передача энергии на расстояние предоставляет значительные преимущества там, где речь идет о точности наведения на подлежащий лечению объект, технологической гибкости и, самое важное, об ограниченной инвазивности в отношении пациента. Простая лапароскопическая хирургия заменила многие из используемых ранее процедур открытого хирургического вмешательства и привела к формированию новых процедур и созданию новых устройств, а также к появлению более эффективной последовательности врачебных процедур для лечения заболеваний. Лапароскопические инструменты на отдалении позволяют подавать энергию для хирургического воздействия на ткани пациента и, как следствие, осуществлять улучшенную визуализацию предназначенного для лечения участка, а также одновременно с этим предоставляют многим хирургам возможность сделать такой участок видимым.
Возможно, наиболее важным аспектом является тот факт, что при этом пациенты испытывают намного меньшую боль, количество осложнений уменьшается, и происходит снижение полной стоимости лечебных процедур. Происходит повышение уровня визуализации в результате появления возможности выполнения задач, связанных с визуализацией.
Продолжающийся прогресс в области вычислительной техники, миниатюризации и экономичности технологий подачи энергии, а также в области визуализации приведет к реализации существующих возможностей с более высоким потенциалом, связанных с подачей наведенной на пациента энергии из удаленного источника и с лечением заболеваний.
Сущность изобретения
В некоторых осуществлениях изобретения предоставлены некоторые процедуры и устройства, которые способствуют прогрессу в области медицинских процедур, охватывающих применение переданной энергии для лечения заболеваний. Процедуры и устройства следуют принципам: 1) передачи энергии для воздействия на пациента на расстоянии; 2) предоставления возможностей, направленных на улучшение визуализации или наведения на подлежащий лечению участок тела пациента; 3) достижения эффективности лечения за счет применения устройств большего размера и мощности на расстоянии или внутри пациента, в отличие от попыток непосредственного контакта с целью, к которым могли бы прибегнуть хирург, а также кардиолог или радиолог. Во многих случаях также используются передовые модели инструментов визуализации и локализации.
В некоторых осуществлениях изобретения способ лечения включает размещение источника энергии за пределами тела пациента, его применение таким образом, чтобы путь прохождения энергии от ее источника направлялся на нерв внутри тела пациента, при этом такой нерв является частью автономной нервной системы, и использование источника энергии, расположенного за пределами тела пациента, для подачи лечебной энергии от источника, находящегося вне тела пациента, на расположенный внутри пациента нерв для его лечения.
В некоторых осуществлениях изобретения лечебная энергия представляет собой сфокусированную энергию.
В некоторых осуществлениях изобретения лечебная энергия представляет собой несфокусированную энергию.
В некоторых осуществлениях изобретения лечебная энергия представляет собой энергию фокусированного ультразвука высокой интенсивности (HIFU).
В некоторых осуществлениях изобретения лечебная энергия представляет собой энергию фокусированного ультразвука низкой интенсивности (LIFU).
В некоторых осуществлениях изобретения лечебная энергия подается на нерв с целью его частичной абляции.
В некоторых осуществлениях изобретения лечебная энергия подается на нерв с целью его полной абляции.
В некоторых осуществлениях изобретения лечебная энергия подается для паралича нерва.
В некоторых осуществлениях изобретения нерв ведет к почке.
В некоторых осуществлениях изобретения нерв содержит почечный нерв.
В некоторых осуществлениях изобретения нерв содержит симпатический нерв, соединенный с почкой.
В некоторых осуществлениях изобретения нерв содержит центростремительный нерв, соединенный с почкой.
В некоторых осуществлениях изобретения нерв содержит почечный симпатический нерв в почечной ножке.
В некоторых осуществлениях изобретения нерв содержит нервный ствол, расположенный рядом с позвонком.
В некоторых осуществлениях изобретения нерв содержит нервный узел, расположенный рядом с позвонком.
В некоторых осуществлениях изобретения нерв содержит нерв заднего корешка спинного мозга.
В некоторых осуществлениях изобретения нерв ведет к надпочечной железе.
В некоторых осуществлениях изобретения нерв содержит двигательный нерв.
В некоторых осуществлениях изобретения нерв располагается рядом с почкой.
В некоторых осуществлениях изобретения нерв расположен за глазом.
В некоторых осуществлениях изобретения нерв содержит солнечное сплетение.
В некоторых осуществлениях изобретения нерв находится в пределах или рядом с позвоночником.
В некоторых осуществлениях изобретения нерв проходит до дугоотростчатых суставов.
В некоторых осуществлениях изобретения нерв содержит брюшной нервный узел.
В некоторых осуществлениях изобретения процесс применения источника энергии включает его позиционирование.
В некоторых осуществлениях изобретения источник энергии содержит источник ультразвуковой энергии.
В некоторых осуществлениях изобретения источник ультразвуковой энергии используется для подачи лечебной энергии на нерв с многих направлений из источника, находящегося за пределами тела пациента.
В некоторых осуществлениях изобретения лечебная энергия подается для модуляции нерва без повреждения последнего.
В некоторых осуществлениях изобретения способ дополнительно включает определение положения почечного сосуда с помощью устройства визуализации, расположенного за пределами тела пациента.
В некоторых осуществлениях изобретения положение почечного сосуда используется для определения положения нерва.
В некоторых осуществлениях изобретения устройство формирования сигналов изображения включает устройство компьютерной томографии (CT), устройство формирования изображения с использованием способа MRI (MRI), термографическое устройство, инфракрасный устройство формирования изображения, томографическое устройство с оптической когерентностью, фотоакустическое устройство формирования изображения, устройство формирования изображения для позиционно-эмиссионной томографии (РЕТ), устройство формирования изображения однофотонной эмиссионной компьютерной томографии (SPECT) или ультразвуковое устройство.
В некоторых осуществлениях изобретения способ дополнительно включает определение положения нерва внутри тела пациента.
В некоторых осуществлениях изобретения определение положения нерва внутри тела пациента включает определение положения почечного сосуда для наведения на нерв, который расположен возле почечного сосуда.
В некоторых осуществлениях изобретения почечный сосуд включает почечную артерию.
В некоторых осуществлениях изобретения процедура определения положения нерва внутри тела пациента включает применение технического приема доплеровской триангуляции.
В некоторых осуществлениях изобретения устройство формирования изображения содержит устройство формирования изображения с использованием способа MRI.
В некоторых осуществлениях изобретения устройство формирования изображения содержит устройство компьютерной томографии.
В некоторых осуществлениях изобретения лечебная энергия представляет собой энергию фокусированного ультразвукового сигнала высокой интенсивности (HIFU), а устройство формирования изображения содержит устройство формирования изображения с использованием способа MRI (MRI).
В некоторых осуществлениях изобретения лечебная энергия представляет собой энергию фокусированного ультразвука высокой интенсивности (HIFU), а устройство формирования изображения содержит ультразвуковое устройство.
В некоторых осуществлениях изобретения нерв идет к почке, а устройство формирования изображения содержит устройство формирования изображения с использованием способа MRI.
В некоторых осуществлениях изобретения нерв идет к почке, а устройство формирования изображения содержит ультразвуковое устройство.
В некоторых осуществлениях изобретения нерв идет к почке, а устройство формирования изображения используется для получения доплеровского сигнала.
В некоторых осуществлениях изобретения лечебная энергия подается на почку для снижения симпатического раздражителя, воздействующего на почку, или для снижения ответного сигнала симпатического нерва, поступающего из почки в автономную нервную систему, либо для достижения этих обеих целей.
В некоторых осуществлениях изобретения способ дополнительно включает подачу энергии тестирования на тело пациента для выявления возникшей реакции на подачу энергии тогда, когда энергия тестирования подается до подачи лечебной энергии из источника энергии.
В некоторых осуществлениях изобретения энергия тестирования представляет собой тепловую или вибрационную энергию, а способ дополнительно включает выполнение теста для обнаружения функционирования симпатического нерва.
В некоторых осуществлениях изобретения энергия тестирования представляет собой подаваемый на кожный покров раздражитель, а способ дополнительно включает выявление ответной реакции со стороны пациента.
В некоторых осуществлениях изобретения ответная реакция представляет собой частоту сердечных сокращений.
В некоторых осуществлениях изобретения энергия тестирования подается для стимулирования работы комплекса прессорного рецептора, а способ дополнительно включает подачу давящего воздействия на сонную артерию, и определение возможного снижения кровяного давления после подачи давящего воздействия на сонную артерию.
В некоторых осуществлениях изобретения энергия тестирования подается с помощью ультразвукового устройства, которое располагается вне тела пациента.
В некоторых осуществлениях изобретения лечебная энергия, поступающая из источника энергии, подается в том случае, если снижается кровяное давление, или же если кровяное давление снижается со скоростью, которая превышает предписанный порог.
В некоторых осуществлениях изобретения лечебная энергия подается для снижения гипертензии.
В некоторых осуществлениях изобретения лечебная энергия подается для лечения глаукомы.
В некоторых осуществлениях изобретения источник энергии используется таким образом, чтобы выполнялось его наведение в направлении, совпадающим с сосудом, который располагается рядом с нервом.
В некоторых осуществлениях изобретения способ дополнительно включает перемещение подвергаемого лечению участка, содержащего нерв.
В некоторых осуществлениях изобретения путь поступления энергии из ее источника направлен на нерв за счет использования местоположения кровеносного сосуда, окруженного нервом.
В некоторых осуществлениях изобретения способ дополнительно включает ввод устройства внутрь организма пациента и использование такого устройства для определения положения нерва внутри организма пациента, когда источник энергии, по меньшей мере, частично используется на основании установленного положения нерва таким образом, чтобы путь поступления энергии был направлен на нерв.
В некоторых осуществлениях изобретения устройство помещается внутрь сосуда, окруженного нервом, а положение нерва определяется косвенно на основании установленного положения кровеносного сосуда.
В некоторых осуществлениях изобретения терапевтическая система содержит источник энергии, предназначенный для размещения вне тела пациента, который конфигурируется для наведения пути подачи энергии на нерв, являющийся частью автономной нервной системы пациента, и компонуется для подачи лечебной энергии из источника, находящегося вне тела пациента, на нерв, расположенный внутри пациента, для лечения последнего.
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи сфокусированной энергии.
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи несфокусированной энергии.
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи энергии фокусированного ультразвукового сигнала высокой интенсивности (HIFU).
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи энергии фокусированного ультразвукового сигнала низкой интенсивности (LIFU).
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи лечебной энергии с целью частичной абляции нерва.
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи лечебной энергии с целью полной абляции нерва.
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи лечебной энергии с целью паралича нерва.
В некоторых осуществлениях изобретения источник энергии содержит источник ультразвуковой энергии.
В некоторых осуществлениях изобретения источник ультразвуковой энергии конфигурируется с целью подачи лечебной энергии по многочисленным направлениям из источника, расположенного за пределами тела пациента, на нерв, тогда как источник ультразвуковой энергии является стационарным относительно положения, занимаемого пациентом.
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи лечебной энергии с целью модуляции нерва без повреждения тканей, которые оказываются на пути прохождения лечебной энергии на нерв.
В некоторых осуществлениях изобретения нерв представляет собой почечный нерв, а система дополнительно содержит процессор, расположенный вне организма пациента, при этом процессор конфигурируется для получения входного сигнала, соответствующего положению почечной артерии, для определения выходного сигнала, соответствующего положению почечного нерва, с помощью модели, которая устанавливает связь между положением артерии и положением нерва, и для обеспечения подачи выходного сигнала на систему позиционирования источника энергии таким образом, чтобы такая система позиционирования могла запустить в работу источник энергии, расположенный за пределами тела пациента, с целью подачи лечебной энергии на почечный нерв для его лечения.
В некоторых осуществлениях изобретения система дополнительно содержит процессор, предназначенный для определения положения почечного кровеносного сосуда и расположенный за пределами тела пациента.
В некоторых осуществлениях изобретения система дополнительно содержит устройство формирования изображения для получения сигнала изображения, в котором процессор конфигурируется для определения положения почечного кровеносного сосуда на основании сигнала изображения.
В некоторых осуществлениях изобретения устройство формирования сигналов изображения содержит устройство компьютерной томографии (CT), устройство формирования изображения с использованием способа MRI (MRI), термографическое устройство, инфракрасное устройство формирования изображения, томографическое устройство с оптической когерентностью, фотоакустическое устройство формирования изображения, устройство формирования изображения для позиционно-эмиссионной томографии (РЕТ), устройство формирования изображения однофотонной эмиссионной компьютерной томографии (SPECT) или ультразвуковое устройство.
В некоторых осуществлениях изобретения положение почечного кровеносного сосуда используется в процессе подачи лечебной энергии на нерв, который окружает почечный кровеносный сосуд.
В некоторых осуществлениях изобретения положение почечного кровеносного сосуда определяется с помощью технического приема доплеровской триангуляции.
В некоторых осуществлениях изобретения почечный сосуд содержит почечную артерию.
В некоторых осуществлениях изобретения лечебная энергия подается на почку для снижения симпатического раздражителя, воздействующего на почку, или для снижения ответного сигнала симпатического нерва, поступающего из почки в автономную нервную систему, либо для достижения этих обеих целей.
В некоторых осуществлениях изобретения источник энергии также конфигурируется для подачи энергии тестирования на пациента для выявления возникшей реакции на воздействие энергии тестирования.
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи лечебной энергии с целью лечения гипертензии.
В некоторых осуществлениях изобретения источник энергии конфигурируется для подачи лечебной энергии с целью лечения глаукомы.
В некоторых осуществлениях изобретения источник энергии ориентирован таким образом, чтобы выполнялось его наведение в направлении, выровненным с сосудом, который располагается рядом с нервом.
В некоторых осуществлениях изобретения источник энергии сконфигурирован для отслеживания перемещения нерва.
В некоторых осуществлениях изобретения источник энергии конфигурирован для отслеживания перемещения нерва с помощью отслеживания перемещения кровеносного сосуда, расположенного рядом с нервом.
В некоторых осуществлениях изобретения источник энергии конфигурируется для наведения на нерв с помощью наведения на кровеносный сосуд, который окружен нервом.
В некоторых осуществлениях изобретения система дополнительно содержит устройство, предназначенное для размещения в организме пациента, и процессор, предназначенный для определения положения с помощью устройства, при этом источник энергии сконфигурирован для наведения подачи энергии на нерв, расположенный внутри организма пациента на основании, по меньшей мере, части данных для установленного положения нерва.
В некоторых осуществлениях изобретения устройство изготовлено такого размера, чтобы его можно было вставить в кровеносный сосуд, окруженный нервом.
В некоторых осуществлениях изобретения система подачи энергии с места, находящегося за пределами кожного покрова пациента, на нерв, окружающий кровеносный сосуд внутри организма пациента, содержит процессор, сконфигурированный для получения сигнала изображения и определения трехмерных координат кровеносного сосуда на основании сигнала изображения, и источник энергии, сконфигурированный для подачи энергии с места, находящегося за пределами кожного покрова пациента, на нерв, окружающий кровеносный сосуд, при этом процессор в этой системе сконфигурирован также для управления источником энергии на основании данных расчетной координаты.
В некоторых осуществлениях изобретения система дополнительно содержит устройство формирования сигналов изображения для обеспечения получения сигнала изображения.
В некоторых осуществлениях изобретения устройство формирования сигналов изображения содержит устройство формирования изображения с использованием способа MRI (MRI).
В некоторых осуществлениях изобретения устройство формирования сигналов изображения содержит ультразвуковое устройство.
В некоторых осуществлениях изобретения энергия представляет собой сфокусированную энергию.
В некоторых осуществлениях изобретения энергия представляет собой сфокусированный ультразвук.
В некоторых осуществлениях изобретения источник энергии содержит ультразвуковую антенную решетку, которая выравнивается относительно кровеносного сосуда.
В некоторых осуществлениях изобретения система дополнительно содержит устройство формирования изображения для обеспечения подачи ультразвуковых сигналов в B-режиме с целью формирования изображения кровеносного сосуда.
В некоторых осуществлениях изобретения система подачи энергии с места, находящегося за пределами кожного покрова пациента, на нерв, окружающий кровеносный сосуд внутри организма пациента, содержит опорную точку для проведения измерений внутри кровеносного сосуда, датчик обнаружения опорной точки для проведения измерений внутри кровеносного сосуда, процессор, сконфигурированный с целью определения трехмерных координат обнаруженной опорной точки измерений, и источник энергии, сконфигурированный для подачи энергии через кожный покров и для ее фокусирования на участке кровеносного сосуда, при этом процессор в этой системе конфигурируется для работы источника энергии на основании установленных трехмерных координат опорной точки измерений и на основании информации, касающейся кровеносного сосуда.
В некоторых осуществлениях изобретения источник энергии содержит ультразвуковое устройство, и кровеносный сосуд является почечной артерией.
В некоторых осуществлениях изобретения система дополнительно содержит ультразвуковую систему формирования изображений.
В некоторых осуществлениях изобретения опорная точка измерений фиксируется внутри кровеносного сосуда и прикрепляется к внутрисосудистому катетеру.
В некоторых осуществлениях изобретения опорная точка измерений является пассивной опорной точкой измерений, сконфигурированной для формирования ответа на внешний сигнал.
В некоторых осуществлениях изобретения опорная точка измерений является активной опорной точкой измерений, передающей координаты своего положения в устройство обнаружения.
В некоторых осуществлениях изобретения способ лечения гипертензии у пациента включает получение сигнала формирования изображения из кровеносного сосуда пациента, планирование подачи энергии на стенку кровеносного сосуда и передачу энергии с места за пределами кожного покрова пациента на автономный нерв, окружающий кровеносный сосуд.
В некоторых осуществлениях изобретения способ дополнительно включает избирательную модуляцию центростремительного нерва в пределах узла симпатического нерва.
В некоторых осуществлениях изобретения для определения воздействия подачи энергии на симпатическую нервную систему способ дополнительно включает использовании микронейрографии после подачи энергии на подлежащий лечению объект.
В некоторых осуществлениях изобретения кровеносный сосуд проходит в почку или выходит из нее, а способ дополнительно включает локализацию кровеносного сосуда с помощью ультразвукового сигнала с доплеровским сдвигом.
В некоторых осуществлениях изобретения реализована система модуляции автономного нерва пациента, в которой используется интрадермальная подача энергии; такая система содержит процессор с входом для получения информации об энергии и мощности, подаваемых на подлежащий лечению участок, содержащий нерв, и выходом, предназначенных для выдачи сигнала, при этом процессор сконфигурирован для определения положения базовой цели с места за пределами тела пациента с целью локализации положения нерва относительно базовой цели, устройство для подачи лечебной энергии, содержит преобразователь для подачи энергии извне с места за пределами тела пациента, контроллер, предназначенный для управления наведением преобразователя по меньшей мере частично на основании данных, содержащихся в сигнале, поступающем из процессора, и систему формирования изображений, подсоединенную к процессору или к устройству для подачи лечебной энергии.
В некоторых осуществлениях изобретения процессор сконфигурирован для определения положения цели в процессе работы устройства для подачи лечебной энергии.
В некоторых осуществлениях изобретения система дополнительно содержит систему сопряжения с пациентом, сконфигурированную под размещение терапевтического устройства таким образом, чтобы преобразователь наводился на кровеносный сосуд, соединенный с почкой, из положения, находящегося над ребрами, ниже подвздошного гребня и на уровне середины позвоночного столба.
В некоторых осуществлениях изобретения устройство подачи лечебной энергии сконфигурировано для подачи сфокусированного ультразвукового сигнала.
В некоторых осуществлениях изобретения базовая цель представляет собой, по меньшей мере, часть кровеносного сосуда, идущего к почке и от нее, а нерв является почечным нервом.
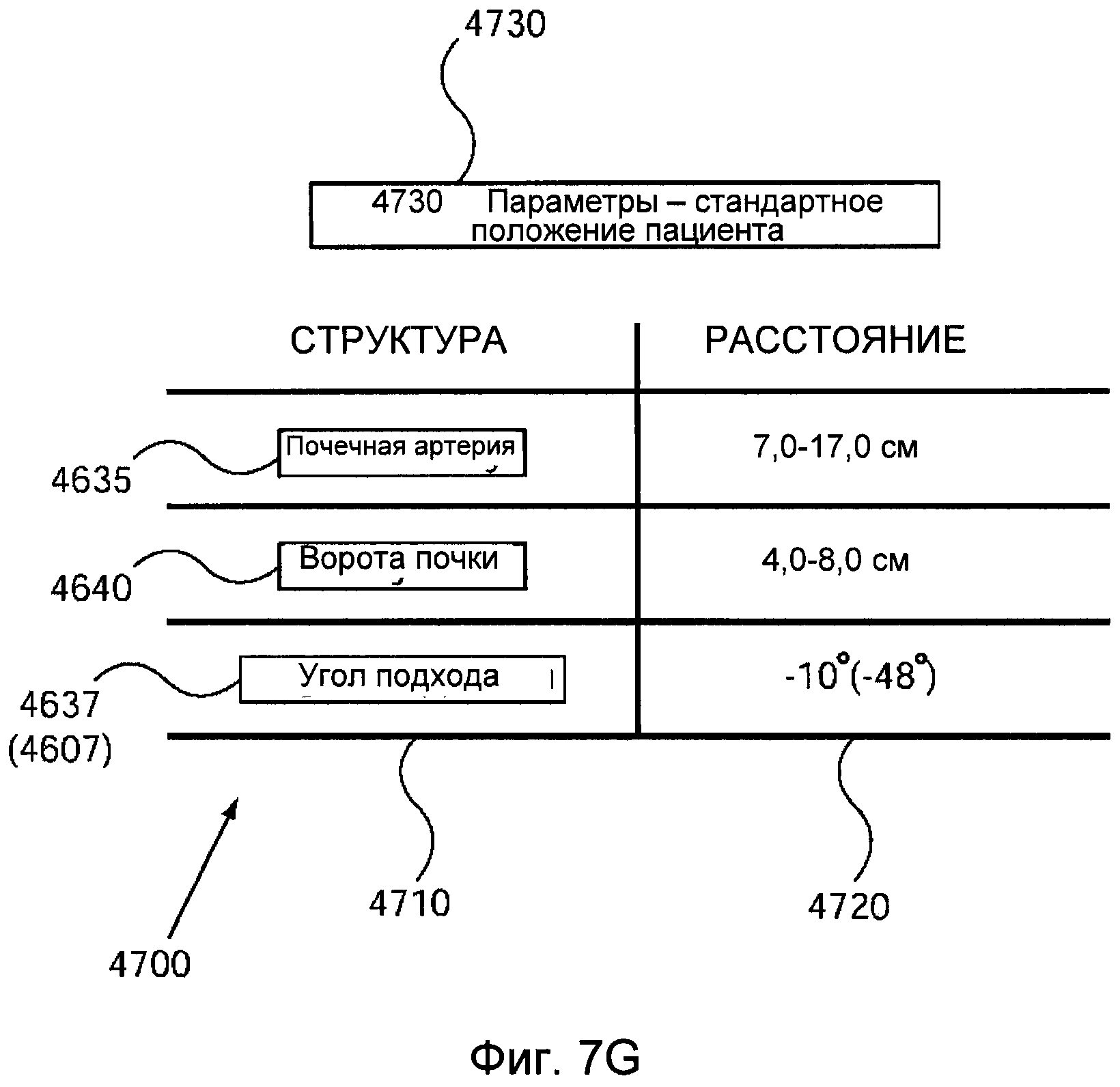
В некоторых осуществлениях изобретения преобразователь сконфигурирован для фокусирования энергии на расстоянии от 6 до 18 см.
В некоторых осуществлениях изобретения преобразователь сконфигурирован для подачи энергии в форме сфокусированного ультразвукового сигнала высокой интенсивности на почечный кровеносный сосуд под углом от приблизительно -10 градусов и до примерно -48 градусов относительно горизонтальной линии, соединяющей поперечные выступы позвоночного столба.
В некоторых осуществлениях изобретения величина энергии, поступающей из устройства подачи лечебной энергии, изменяется в диапазоне 100-2500 Вт/см2.
В некоторых осуществлениях изобретения базовой целью является постоянно установленный сосудистый катетер.
В некоторых осуществлениях изобретения система формирования изображения представляет собой магнитно-резонансную систему формирования изображения, а устройство подачи лечебной энергии представляет собой ультразвуковое устройство.
В некоторых осуществлениях изобретения система формирования изображения является ультразвуковой системой формирования изображения.
В некоторых осуществлениях изобретения процессор является частью устройства подачи лечебной энергии.
В некоторых осуществлениях изобретения процессор является частью системы формирования изображения.
В некоторых осуществлениях изобретения способ подачи энергии из положения, находящегося за пределами кожного покрова пациента, на нерв, окружающий кровеносный сосуд, включает установку устройства в положение над ребрами, ниже подвздошного гребня и латерально к позвоночному столбу, и использование этого устройства для поддержания функционирования системы подачи энергии в нужном положении относительно тела пациента таким образом, чтобы система подачи энергии могла подавать энергию через кожный покров мимо кости.
В некоторых осуществлениях изобретения система подачи энергии представляет собой систему подачи сфокусированной ультразвуковой энергии.
В некоторых осуществлениях изобретения устройство, используемое в системе с целью подачи сфокусированной ультразвуковой энергии из положения, находящегося за пределами кожного покрова пациента, на нерв, окружающий кровеносный сосуд, содержит устройство позиционирования, сконфигурированное для поддержания функционирования системы подачи энергии в нужном положении относительно тела пациента таким образом, чтобы система подачи энергии могла подавать энергию через кожный покров мимо кости, при этом устройство позиционирования сконфигурировано с возможностью расположения над ребрами, ниже подвздошного гребня и латерально к позвоночному столбу.
В некоторых осуществлениях изобретения система подачи энергии представляет собой систему подачи сфокусированной ультразвуковой энергии.
В некоторых осуществлениях изобретения устройство позиционирования сконфигурировано с целью сохранения угла установки для системы подачи сфокусированной ультразвуковой энергии так, чтобы костные структуры не попадали в зону действия ультразвукового поля.
В некоторых осуществлениях изобретения лечебная система содержит терапевтическое устройство, сконфигурированное для подачи энергии из положения за пределами тела пациента на нерв внутри тела пациента, катетер, сконфигурированный для размещения внутри кровеносного сосуда, окруженного нервом, при этом катетер сконфигурирован для передачи сигнала, и процессор, сконфигурированный для получения сигнала и определения базового положения в кровеносном сосуде, при этом терапевтическое устройство сконфигурировано для подачи энергии на нерв с учетом установленного базового положения.
В некоторых осуществлениях изобретения терапевтическое устройство содержит ультразвуковое устройство.
В некоторых осуществлениях изобретения способ подавления функции нерва, перемещающегося вместе с артерией, включает обеспечение внешнего способа формирования изображений для определения места нахождения артерии пациента, размещение артерии в первую точку отсчета трехмерной системы координат на основании полученного изображения, установку или привязку источника генерирования лечебной энергии к трехмерной системе координат первой точки отсчета, моделирование подачи энергии на адвентициальный участок артерии или на участок, расположенный рядом с артерией перемещающегося нерва, подачу лечебной энергии из источника лечебной энергии, по меньшей мере, под двумя разными углами сквозь кожу пациента для пересечения места расположении артерии или участка, расположенного рядом с артерией, и, по меньшей мере, частичное подавление функции нерва, перемещающегося вместе с артерией.
В некоторых осуществлениях изобретения способом формирования изображения является ультразвук, формирование изображений с использованием способа MRI и компьютерной томографии.
В некоторых осуществлениях изобретения лечебная энергия представляет собой ультразвуковую энергию.
В некоторых осуществлениях изобретения артерия является почечной артерией.
В некоторых осуществлениях изобретения размещение артерии в трехмерной системе координат включает определение местоположения артерии с помощью доплеровского ультразвукового сигнала.
В некоторых осуществлениях изобретения способ дополнительно включает использование опорной точки измерений, при этом опорная точка измерений располагается внутри пациента.
В некоторых осуществлениях изобретения упомянутая опорная точка измерений временно располагается в месте, находящемся внутри пациента.
В некоторых осуществлениях изобретения упомянутая опорная точка является катетером, расположенным в артерии пациента.
В некоторых осуществлениях изобретения упомянутый катетер может быть обнаружен с помощью радиочастотного сигнала, а упомянутый способ формирования изображения основан на использовании ультразвука.
В некоторых осуществлениях изобретения лечебная энергия, поступающая из источника энергии, подается с распределением вдоль артерии.
В некоторых осуществлениях изобретения лечебная энергия представляет собой ионизирующее излучение.
В некоторых осуществлениях изобретения система подавления функции нерва, перемещающегося вместе с почечной артерией, содержит детектор, предназначенный для определения места положения почечной артерии и почечного нерва из положения за пределами тела пациента, ультразвуковой компонент, предназначенный для подачи лечебной энергии, по меньшей мере, в двух направлениях через кожный покров на нерв, окружающий почечную артерию, алгоритм моделирования, охватывающий использование входных и выходных данных, при этом упомянутые входные данные для алгоритма моделирования включают пространство трехмерной системы координат, содержащее источник лечебной энергии и местоположение почечной артерии в пространстве трехмерной системы координат, а упомянутые выходные данные алгоритма моделирования включают направление и уровень подачи энергии ультразвукового компонента, опорную точку измерений, обнаруживаемую из положения за пределами тела пациента и приспособленную для временной установки в артерии пациента и для поддержания связи с детектором для определения местоположения почечной артерии в трехмерной системе координат, и информация, касающаяся упомянутого местоположения, является входными данными для модели.
В некоторых осуществлениях изобретения опорная точка измерений является пассивным отражателем ультразвукового сигнала.
В некоторых осуществлениях изобретения опорная точка измерений генерирует энергию радиочастотного сигнала.
В некоторых осуществлениях изобретения упомянутая опорная точка активируется для передачи энергии с помощью сигнала, поступающего из генератора, создающего ультразвуковое или магнитное поле.
В некоторых осуществлениях изобретения выходной сигнал модели выдает ультразвуковому компоненту команду на изменение ткани артерии, основная ось области такого изменения проходит продольно длине артерии.
В некоторых осуществлениях изобретения выходной сигнал модели выдает ультразвуковому компоненту команду на проведение одновременных изменений ткани во многих местах, расположенных вблизи артерии.
В некоторых осуществлениях изобретения выходной сигнал модели выдает ультразвуковому компоненту команду на проведение изменения ткани по окружности вблизи артерии.
В некоторых осуществлениях изобретения место изменения ткани расположено вокруг почечной артерии непосредственно проксимально к центру разветвления артерии надвое в воротах почки.
В некоторых осуществлениях изобретения способ стимуляция или подавления функции нерва, проходящего к почке или от нее, включает идентификацию акустического окна в расположенном сзади участка тела пациента, где можно визуализировать почечные артерии, передачу первого импульса энергии через кожный покров на расположенном сзади участке тела пациента, формирование изображения артериального участка с помощью первого переданного импульса энергии и подачу второго переданного импульса энергии на адвентициальную оболочку артерии посредством привязки второго переданного импульса энергии к сформированному изображению.
В некоторых осуществлениях изобретения способ дополнительно включает отслеживание изображения, созданного первым переданным импульсом энергии.
В некоторых осуществлениях изобретения способ локализации местоположения кровеносного сосуда в теле пациента включает подачу первой ультразвуковой волны в первом направлении из источника, расположенного за пределами тела пациента, на участок кровеносного сосуда, и обнаружение ее отраженного сигнала с последующим одновременным или последовательно выполняемым сравнением первой поданной волны и ее отраженного сигнала, подачу второй ультразвуковой волны во втором направлении на кровеносный сосуд и обнаружение ее отраженного сигнала с последующим объединением отраженных сигналов, полученных после подачи первой волны, и отраженных сигналов, полученных после подачи второй волны, для определения положения кровеносного сосуда в трехмерной системе координат.
В некоторых осуществлениях изобретения способ дополнительно включает этап подачи команды на ультразвуковой преобразователь терапевтического действия с целью подачи энергии в место расположения кровеносного сосуда.
Описание фигур
На фигурах 1a-b представлено фокусирование сигналов источников энергии, подаваемых на нервы автономной нервной системы.
На фигуре 1c представлена система формирования изображения для оказания помощи в наведении источников энергии.
На фигуре 2 представлено наведение и/или прохождение терапевтического ультразвукового сигнала, подаваемого через желудок на автономную нервную систему, расположенную за желудком.
На фигуре 3a представлено фокусирование волн энергии на почечных нервах.
На фигуре 3b представлена система координат, используемая во время лечения.
На фигуре 3C представлено целевая установка катетеров, расположенных в любом из почечных кровеносных сосудов.
На фигуре 3D представлена система обнаружения изображения кровеносного сосуда с установленной внутри него временной опорной точкой измерений.
На фигуре 3E представлен пример терапии для лечения и оценки величины гипертензии.
На фигуре 4a представлена подача энергии на автономную нервную систему, окружающую сонные артерии.
На фигуре 4B представлена подача энергии через кровеносные сосуды ворот почки.
На фигурах 5a-b представлена подача сфокусированной энергии на автономную нервную систему глаза.
На фигуре 6 представлено применение сдавливающих изменений ткани в отношении почки глубоко внутри ее почечных чашек.
На фигуре 7a представлен пациент в рамках системы формирования изображений, получающий лечение с помощью сфокусированных волн энергии.
На фигуре 7b представлена визуализация проходящей лечение почки.
На фигуре 7c крупным планом показано изображение участка почечного нерва проходящей лечение почки.
На фигуре 7d представлен алгоритмический способ лечения автономной нервной системы с помощью ядерного магнитного резонанса (MRI) и преобразователей, используемых для подачи энергии.
На фигуре 7e представлена геометрическая модель, полученная на основании изображений области аорты и почек, показанных в поперечном сечении.
На фигуре 7F крупным планом представлено изображение подлежащего лечению участка.
На фигуре 7G представлены результаты измерений, полученных на основании серии реконструкций изображений, показанных в поперечном сечении.
На фигуре 7H представлены результаты измерений, полученных на основании серии показанных в поперечном сечении реконструкций изображений пациента, находящегося в более оптимизированном положении.
На фигуре 7I представлена алгоритмическая методология применительно к лечению ворот почки и к подаче энергии на почечные кровеносные сосуды.
На фигуре 8a представлен чрескожный подход к лечению автономной нервной системы, окружающей почки.
На фигуре 8b представлен внутрисосудистый подход к лечению автономной нервной системы или к наведению на нее лечебной энергии.
На фигуре 8C представлен чрескожный подход к лечению почечных ворот с помощью сканирования способом компьютерной томографии и использования зонда, который может достать до почечных кровеносных сосудов.
На фигурах 9a-c представлена подача энергии изнутри аорты на участки, расположенные за пределами аорты, с целью лечения автономной нервной системы.
На фигуре 10 представлены этапы лечения заболевания с помощью сфокусированного ультразвукового сигнала высокой интенсивности (HIFU) с одновременным мониторингом хода лечения, а также перемещения проходящего лечение участка.
На фигуре 11a представлено лечение патологии мозга с помощью формирования изображений в поперечном сечении.
На фигуре 11b представлено изображение, снятое с устройства визуализации, на котором показана терапия подлежащего лечению участка мозга.
На фигуре 11c представлен другой вид пораженного участка мозга так, как его можно было бы видеть с помощью устройства формирования изображения, которое помогает лечению пораженного участка.
На фигуре 12 представлено лечение участка почечного нерва с помощью лапароскопического подхода.
На фигуре 13 представлена методология изменения участка ткани с помощью видеомаркеров, предназначенных для мониторинга хода лечения.
На фигуре 14 представлено частичное лечение участков нервного узла с помощью конвергенции волны формирования изображения и лечебной волны.
На фигуре 15a-b представлено применение сфокусированной энергии, подаваемой на позвоночный столб, для лечения различных спинных патологий, включая терапию позвоночного и внутрипозвоночных нервов.
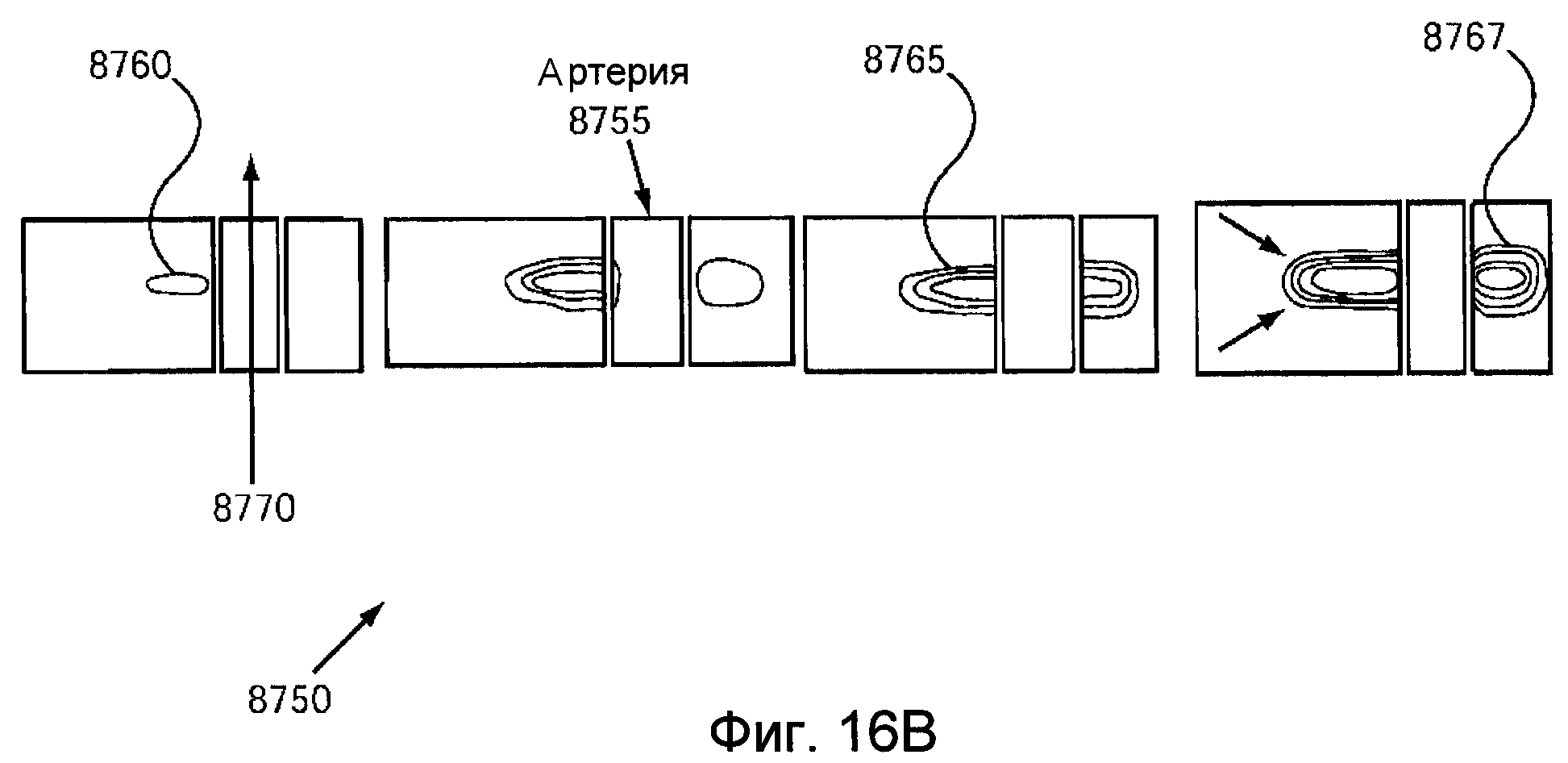
На фигуре 16A представлены типы изменений нервной ткани, которые возникают вблизи почечных артерий и оказывают влияние на ответный сигнал.
На фигуре 16B показано моделирование ультразвуковой волны вблизи кровеносного сосуда I в дополнение к фигуре 16A.
На фигуре 16C представлены данные результатов подачи ультразвуковой энергии, направленной на почечные кровеносные сосуды, и полученное в итоге изменение уровней норадреналина.
На фигуре 17A представлено применение нескольких преобразователей для лечения участков автономной нервной системы в воротах почки.
На фигурах 17B-C показаны способы использования формирования изображений для наведения лечебного действия на конкретный участок, окружающий артерию, а также для вывода на экран прогнозной морфологии поражения.
На фигуре 17D представлен способ локализации преобразователей сфокусированного ультразвукового сигнала высокой интенсивности (HIFU) относительно доплеровских ультразвуковых сигналов.
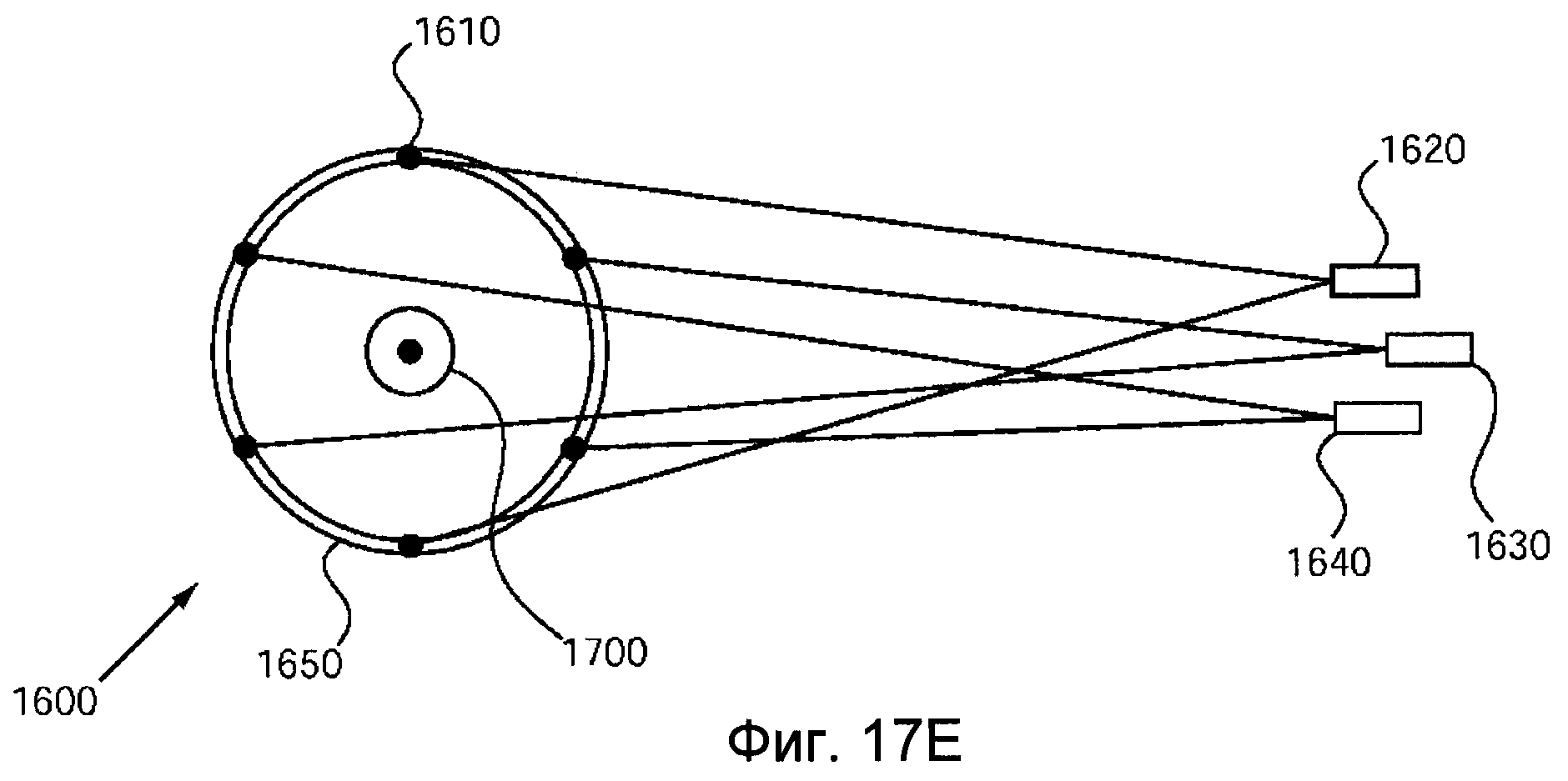
На фигуре 17E представлена компоновка преобразователей относительно подлежащего лечению объекта.
На фигуре 17F в поперечном сечении представлены зоны абляции мультифокального участка.
На фигуре 18 представлена подача энергии внутрь организма в пределах почки для оказания воздействия на специфические функциональные изменения, возникшие на региональном уровне в пределах почки.
На фигуре 19A представлено направление распространении волны энергии, предназначенной для лечения участков автономной нервной системы, расположенных вблизи области ворот почки.
На фигуре 19B представлено схематическое изображение ультразвукового сигнала в В-режиме, поступающего в направлении, установленном экспериментальным путем, для обеспечения доступа сфокусированного ультразвукового сигнала высокой интенсивности (HIFU) в почечные ворота.
На фигуре 20 представлена подача ультразвуковых волн через стенку аорты для осуществления терапевтического воздействия на автономную нервную систему.
На фигуре 21A представлено воздействие сфокусированной энергии на ресничные мышцы и выступы передней области глаза.
На фигуре 21B представлено воздействие сфокусированной неразрушающей энергии на заднюю область глаза для улучшения доставки лекарства или генов либо для усиления другого терапевтического воздействия, такого как подача ионизирующего излучения.
На фигуре 22 представлено воздействие сфокусированной энергии на нервы, окружающие коленный сустав, с целью воздействия на функционирование нерва в суставе.
На фигурах 23A-B представлено воздействие энергии на фаллопиеву трубу для стерилизации пациента женского пола.
На фигуре 24 представлен алгоритм оценки воздействия процедуры невральной модуляции автономной нервной системы. После выполнения этой процедуры в отношении почечных нервов проводится оценка ответной реакции автономной нервной системы с помощью, например, моделирования автономной нервной системы в одном или в нескольких местах.
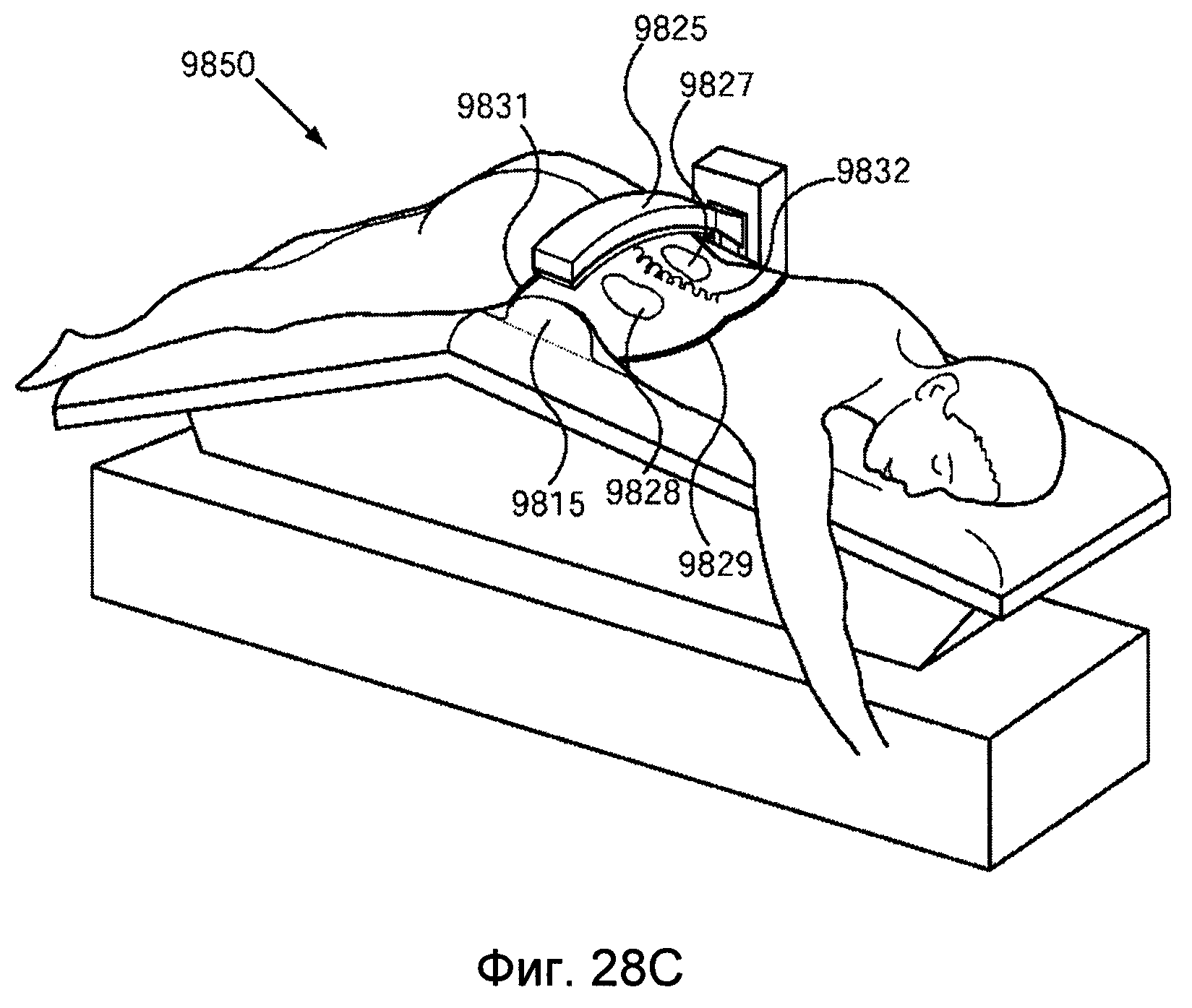
На фигуре 25 представлено оптимизированное положение устройства, предназначенного для оказания терапевтического воздействия на внутренние нервы.
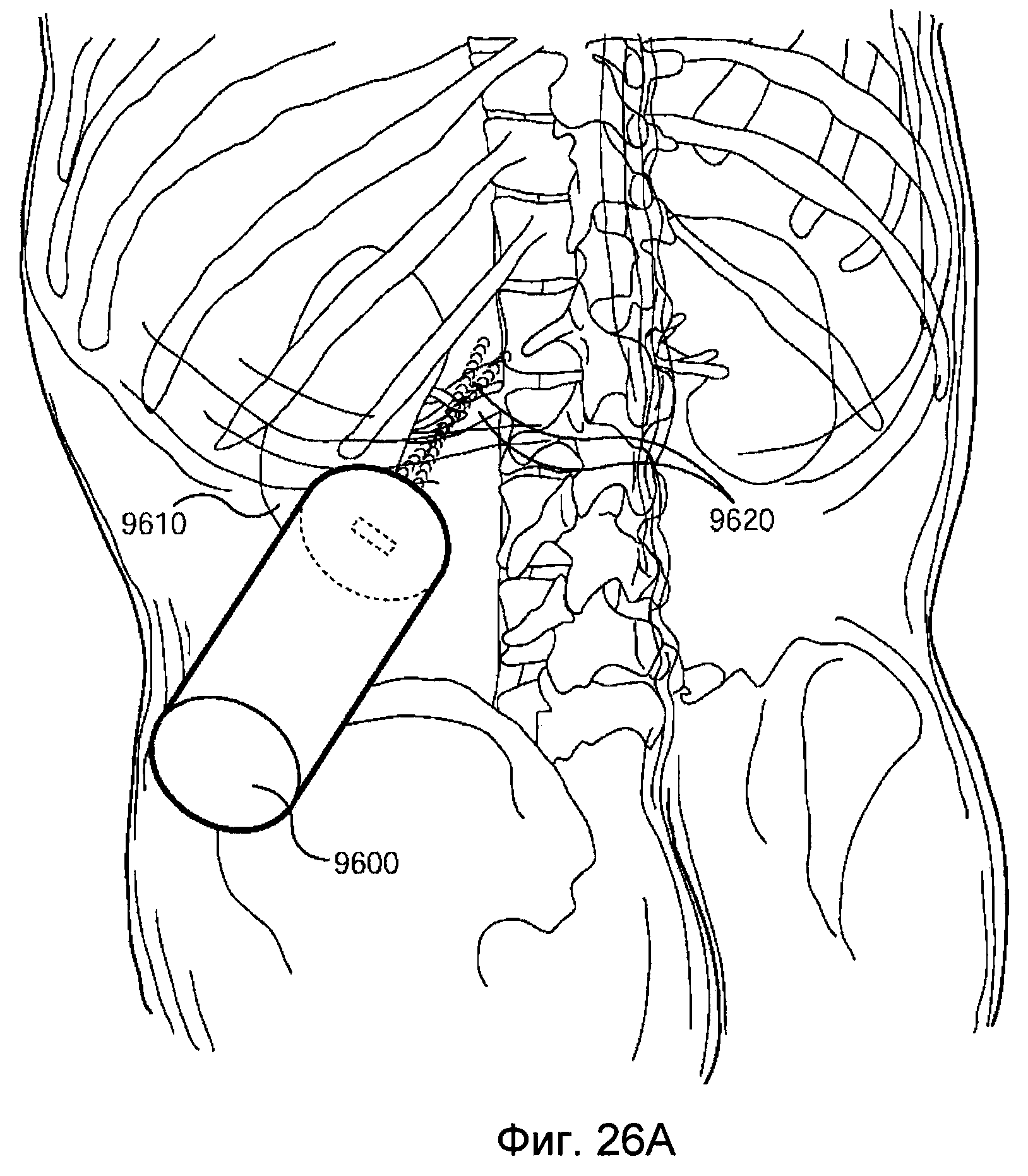
На фигуре 26A показано положение пациента, используемое в процессе получения параметров для системного проектирования.
На фигуре 26B представлена конструкция устройства, созданная согласно информации, полученной на основании результатов анализа осуществимости.
На фигуре 27 представлен клинический образец лечения почечных нервов, принадлежащих автономной нервной системе, основанный на результатах анализа осуществимости.
На фигуре 28 A-C представлена система позиционирования для проведения лечения пациента, входящая в состав системы сфокусированного ультразвукового сигнала.
На фигуре 29 A-D представлены результаты исследований в области воздействия сфокусированной энергии на нервы, окружающие артерии, и результаты исследований в области ультразвуковых сигналов, используемых для визуализации кровеносных сосудов, по которым перемещается нерв.
На фигуре 29E представлены результаты процессов проектирования, во время которых выполняется количественная оценка угла, длины и площади поверхности, полученной в результате сканирований с помощью компьютерной томографии.
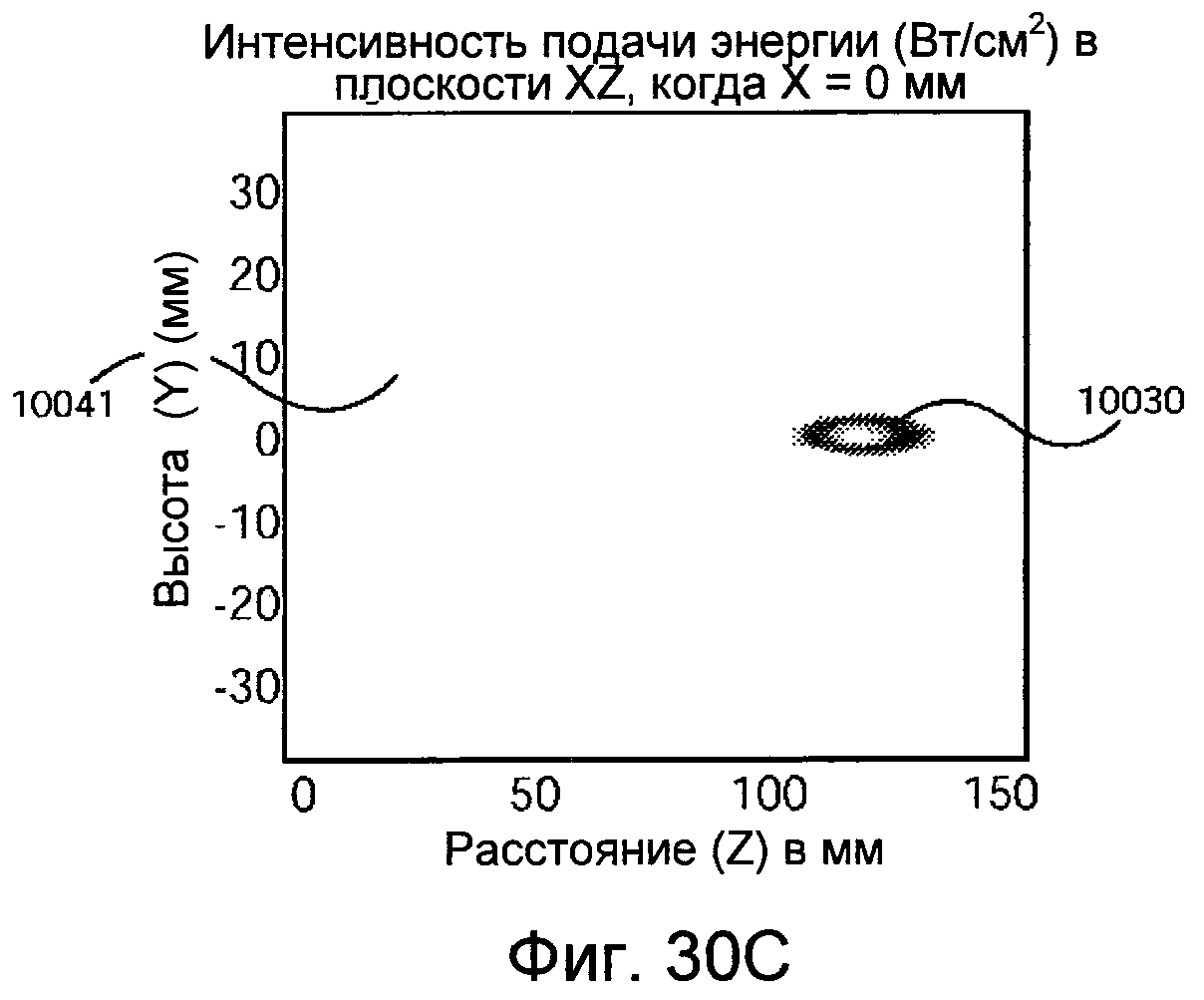
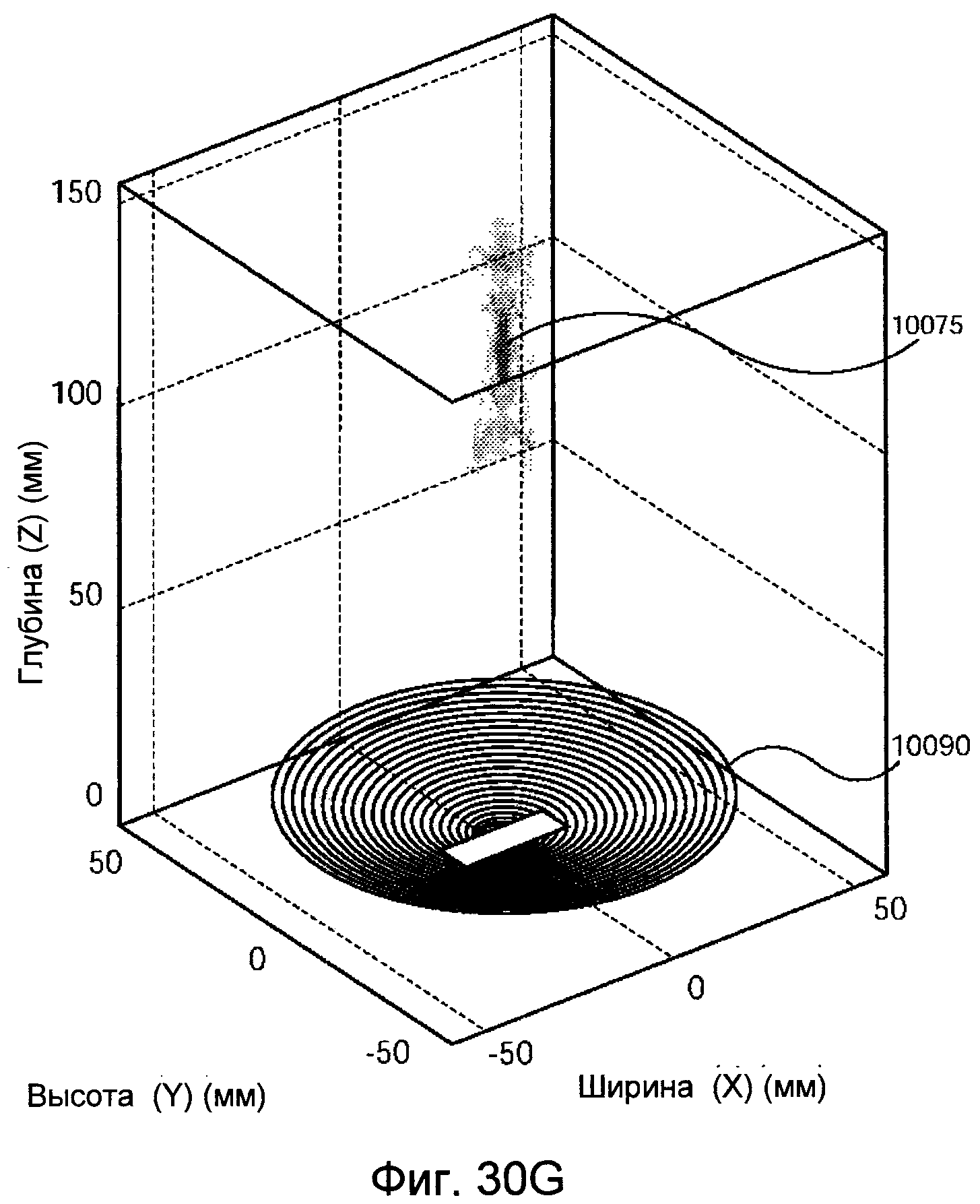
На фигурах 30A-I представлены результаты моделирований воздействия сфокусированных ультразвуковых сигналов на участок почечной артерии при использовании проектного прототипа устройства, основанного на результатах моделирования.
Подробное описание
Гипертензия - это заболевание исключительной национальной и международной значимости. Только в одних США на учет поставлены 80 миллионов пациентов, которые страдают повышенным кровяным давлением, а их число в развитых странах по всему миру составляет свыше 200 миллионов. В США 60 миллионам пациентов поставлен диагноз - неконтролируемое кровяное давление. Это означает, что они либо не поддаются лечению или не могут принимать лекарства из-за широкого профиля побочных эффектов. До 10 миллионов человек могут страдать полностью резистентной гипертензией, при которой показатели величины давления таких пациентов не достигают целевых значений независимо от режима лечения. Заболевания, связанные с неконтролируемой гипертензией, обширны, в том числе инсульт, сердечная недостаточность, отказ работы почек, заболевание периферической артериальной системы и т.д. Создание удобной процедуры прямого действия для лечения гипертензии, сопровождаемой минимальным вмешательством в организм пациента, станет крайне желательным шагом вперед в направлении лечения этого заболевания.
Застойная сердечная недостаточность ("CHF") - это такое состояние организма, которое возникает тогда, когда нарушается работа сердца, и поток крови, снабжающий органы тела, снижается. В случае существенного снижения потока крови меняется функционирование почек, что приводит к задержке вывода жидкости из организма, ненормальным секрециям гормонов и возрастающему сжатию кровеносных сосудов. Такие результаты приводят к возрастанию рабочей нагрузки на сердце и в дополнение к этому снижают функциональную активность сердца, направленную на прокачку крови через почки и сердечно-сосудистую систему.
Полагают, что постепенно снижающийся кровоток в почках является основной экстракардиальной причиной, которая сохраняет возрастающее по спирали ухудшение состояния организма, подверженного застойной сердечной недостаточности (CHF), неизменным. Например, тогда как сердце изо всех сил старается прокачать кровь, величина кардиотонических усилий на выходе сохраняется на прежнем уровне или уменьшается, в результате чего почки задерживают жидкость и электролиты для сохранения систолического объема крови сердца. Возникшее в результате этого повышение давления сверх того перегружает сердечную мышцу так, что та вынуждена работать энергичнее для прокачки крови с преодолением более высокого давления. В этом случае уже работающая с перегрузками сердечная мышца сверх того подвергается дополнительному давлению, которое ухудшает его работу. Помимо этого перегрузка жидкостью и связанные с ней клинические симптомы, появляющиеся в результате этих физиологических изменений, приводят к дополнительным потокам поступающих в клиники пациентов, низкому качеству уровня жизни и к дополнительным расходам на систему здравоохранения. Помимо обострения состояния сердечной недостаточности неудовлетворительная работа почек может привести к усиливающемуся по спирали ухудшению состояния организма и далее к ухудшению рабочей функции почек. Например, в случае описанной выше сердечной недостаточности, связанной с прямотоком крови (систолическая сердечная недостаточность) почка становится ишемической. В случае сердечной недостаточности, связанной с противотоком крови (диастолическая сердечная недостаточность), почки становятся застойными в отношении гипертензии почечных вен. Следовательно, сама почка может содействовать ухудшению своей собственной рабочей функции.
Функции почек могут быть подытожены по трем обширным категориям: фильтрация крови и вывод выделений в виде продуктов распада, полученных в результате метаболизма тела; регулирование солевого, водного, электролитического и кислотного баланса; и секреция гормонов для поддержания кровотока жизненно важных органов. Без нормального функционирования почек пациент будет страдать водоудержанием, пониженным мочеиспусканием и накапливанием токсинов, образовавшихся из выделений организма, в крови и в теле. Эти условия приводят к ухудшению состояния здоровья, начиная со снижения активности почечной функции или почечной недостаточности (неудовлетворительная работа почек), и, как полагается, увеличивают рабочую нагрузку на сердце. У пациента с застойной сердечной недостаточностью (CHF) почечная недостаточность более того приведет к ухудшению работы сердца в результате удержания жидкости в почках и накопления в крови токсинов из-за неудовлетворительного функционирования почек. Возникающая в результате гипертензия также существенно способствует развитию цереброваскулярного заболевания и возрастанию опасности инсульта.
Автономная нервная система представляет собой сеть нервов, которые в меняющейся степени влияют на работу почти каждого органа и физиологической системы в целом. Как правило, система состоит из симпатических и парасимпатических нервов. Например, симпатические нервы, проходящие к почке, пересекают цепочку симпатических нервов вдоль позвоночника и синапс, находящийся в пределах нервных узлов, или в пределах брюшных нервных узлов, и после этого продолжают иннервировать почку через постганглионарные волокна, расположенные внутри «почечных нервов». В пределах почечных нервов, которые проходят вдоль почечных ворот (артерия и до некоторой степени вена), находятся постганглионарные симпатические и центростремительные нервы, исходящие от почки. Центростремительные нервы, исходящие от почки, перемещаются в пределах заднего корешка спинного мозга (если в их состав входят болевые нервные волокна) и проходят в передний корешок спинного мозга, если они являются чувствительными волокнами, после чего они проходят в спинной мозг и в конечном счете достигают специализированных участков мозга. Центростремительные нервы, прессорные рецепторы и химиорецепторы доставляют через мозг информацию от почек обратно в симпатическую нервную систему; их абляции или подавление их работы, по меньшей мере, частично объясняет улучшение, заметное в показателях кровяного давления после абляции или денервации либо частичного изменения нервной ткани почечного нерва. Также предполагалось и частично доказано экспериментальным путем, что реакция прессорного рецептора на уровне синуса сонной артерии носит промежуточный характер в результате воздействия центростремительных нервов почечной артерии, так что потеря реакции центростремительных нервов почечной артерии ослабляет реакцию прессорных рецепторов сонной артерии на изменения артериального кровяного давления; «American J. Physiology and Renal Physiology» (Американский журнал физиологии и почечной физиологии), 279:F491-F501, 2000 год, включенный в данную заявку посредством ссылки.
При создании моделей на примере животных установлено, что состояние сердечной недостаточности приводит к отклоняющейся от нормы высокой симпатической активации работы почек. Возрастание активности почечного симпатического нерва ведет к снижению выделения воды и натрия из организма, а также к возрастанию секреции ренина, который стимулирует секрецию альдестерона из надпочечной железы. Увеличение секреции ренина может привести к повышению уровней ангиотензина II, что, в свою очередь, приводит к сужению кровеносных сосудов, снабжающих почки, а также к общему сужению сосудов, что в совокупности способствует снижению почечного кровотока и приводит к гипертензии. Снижение активности симпатического почечного нерва, например, в результате деинервации может обратить вспять эти процессы, что фактически наблюдается в условиях лечебного учреждения. Аналогично у страдающих ожирением пациентов возбудимость симпатического нерва по существу крайне высока и интуитивно предполагается одной из причин гипертензии, возникающей у таких тучных пациентов.
Последние клинические исследования показали, что деинервация цепочки почечных симпатических нервов и прочих нервов, которые входят в почку через ворота, может привести к глубоким системным воздействиям на пациентов и подопытных животных (крысы, собаки, свинья, овца и люди), страдающих гипертензией, сердечной недостаточностью и прочими системными заболеваниями органов. Такое лечение может привести к долговременному снижению потребности в лекарствах, понижающих кровяное давление, и к его нормализации (O'Brien (О'Брайен), журнал Lancet («Ланцет»), 2009 год, 373:9681, включено посредством ссылки). Устройством, используемым при проведении этого испытания, было для высокоточной высокочастотной (RF) абляции, предназначенное для абляции адвентициальной оболочки почечной артерии в случае предположения, что активность нервов, окружающих почечную артерию, также замедляется и в зоне нагревания. По существу, эта процедура замедляется вслепую из-за того, что точное местоположение нервного сплетения неизвестно ни заранее, ни во время, ни после выполнения процедуры. Помимо этого стенка почечной артерии неизменно оказывается поврежденной зондом высокочастотного сигнала, и пациенты, чьи кровеносные сосуды в значительной степени являются атеросклеротическими, не могут быть излечены с высокой степенью надежности. Помимо этого в зависимости от расстояния от нервов до стенки кровеносного сосуда подаваемая энергия не может обеспечить согласованную абляцию или прерывание ткани таких нервов. И, наконец, использование внутренних катетеров может сделать невозможным проведение лечения внутри почки или аорты, если такое лечение носит более строгий избирательный характер. Во многих случаях во избежание периферического повреждения кровеносного сосуда требуется создание защитной спирали вдоль всей протяженности и внутри самого кровеносного сосуда.
Для визуализации внутренней анатомии пациентов с помощью поля излучения (компьютерная томография) или магнитного поля (формирование изображений с использованием способа MRI) можно использовать способ формирования изображений в поперечном сечении. Также для получения поперечных сечений специфических участков можно использовать ультразвук, но только на высоких частотах; следовательно, вследствие этого, применение ультразвука, как правило, ограничено получением изображения поверхностных участков тела. Компьютерная томография и формирование изображений с использованием способа MRI зачастую более подходят для получения изображений в поперечном сечении вследствие глубокого проникновения излучения в ткани. Помимо этого в данном случае масштаб участков тела сохраняется таким, что его анатомическое строение в системе координат остается неизменным при рассмотрении таких участков относительно друг друга; то есть, можно измерить расстояние между ними.
При использовании ультразвука масштабирование может оказаться более затруднительным из-за неодинакового проникновения волн, которые распространяются глубже при прохождении через ткани. Для создания трехмерных изображений и реконструкции изображений участков тела пациентов в поперечном сечении можно использовать сканирования компьютерной томографии, формирование изображений с использованием способа MRI и даже ультразвуковые устройства; анатомическое строение частей тела может быть введено в систему координат в виде их трехмерного представления. Оказавшись зафиксированными в системе координат, устройства подачи энергии (преобразователи) могут быть установлены в нужных точках, а устройства излучения энергии наведены таким образом, чтобы их целью оказались конкретные участки тела. После того, как стало известным положение преобразователя относительно местоположения подлежащего лечению объекта на теле пациента, на него можно направить энергию.
Ультразвуковой сигнал представляет собой циклически генерируемую волну звукового давления с частотой, превышающей верхний предел человеческого слуха …20 килогерц (кГц). Ультразвуковой сигнал широко используется в медицине из-за его способности проникать в ткани тела. Отражение звуковых волн воспроизводит очертание скрытых тканей тела, и по этой причине ультразвуковой сигнал можно широко использовать для диагностики и в перспективе для терапии, а также в области медицины. В качестве терапевтического средства ультразвуковой сигнал обладает способностью, как проникать в ткани, так и фокусироваться для формирования зон абляции ткани. Вследствие этой способности одновременно с лечением формировать изображения ультразвуковой сигнал можно использовать для высокоточного наведения на пораженные участки внутри тела. Интенсивность ультразвука измеряется в единицах мощности на см2(например, в Вт/см2 при наведении на участок, подлежащий терапии). Как правило, высокая интенсивность соответствует значениям его интенсивности в диапазоне свыше 0,1-5 кВт/см2. Ультразвуковой сигнал низкой интенсивности занимает диапазон до 0,01-0,10 кВт/см2 - от приблизительно 1 или 10 Ватт на см2.
Ультразвуковой сигнал можно использовать из-за его прямо распространяющихся волн и полученных в результате отраженных волн, или там, где требуется либо воздействие энергии на ткани или нагревание или незначительное терапевтическое изменение целостности тканей. Например, вместо того, чтобы полагаться на отражения волн для формирования изображения, можно сфокусировать в глубине ткани ультразвуковые лучи более низкой частоты (например, ниже 1 МГц) для создания тепловой зоны или расчетного участка образовавшейся полости, в которой возникают микропузырьки. При этом клеточные мембраны открываются для прохода биоактивных молекул или же для терапевтического изменения целостности ткани иным способом. Для реализации этих свойств ультразвука, как правило, используются частоты в диапазоне от 0,25 Мегагерц (МГц) до 10 МГц в зависимости от глубины проникновения, требуемой для лечебного эффекта. Потребуется или может потребоваться фокусирование ультразвуковых лучей для того, чтобы поверхность ткани не оказалась чрезмерно разрушенной или перегретой такими отдельными ультразвуковыми лучами. Другими словами, можно распространять через ткани множество отдельных ультразвуковых лучей под разными углами с тем, чтобы снизить поглощение энергии вдоль любого отдельного пути их прохождения, но несмотря на это позволить лучам сходиться в фокальной точке, расположенной глубоко в ткани. Помимо этого отраженные под множеством углов лучи можно использовать для создания трехмерного представления подлежащего лечению участка в пространстве системы координат.
При планировании ультразвуковой терапии важно избегать возникновения отчетливых прерывистых поверхностей раздела. Например, кишка, легкое или кость, которые содержат воздушные и/или костные поверхности раздела, способствуют отображению резких границ между мягкими тканями. Такие поверхности раздела делают планирование и проведение терапии более затруднительным. Однако если можно избежать возникновения поверхностей раздела, то лечение будет носить более упрощенный характер по сравнению с тем, что следовало бы сделать во время терапии мозга (например, подачи высокоинтенсивного сфокусированного ультразвукового излучения, наводимого с использованием способа MRI), когда для преодоления высокого поглощения сигнала черепом требуется проведение комплексного моделирования. Представленные ниже данные отображают результаты, полученные после широкого экспериментирования в области поиска упрощений проведения такого лечения.
Измерение времени пролета при использовании ультразвука, можно использовать для определения диапазонов или расстояний между объектами в тканях. Такие измерения можно использовать для ввода информации о кровеносных сосудах в трехмерные системы координат так, чтобы энергию можно было использовать для наведения на ткани. SONAR - это сокращение слов «звуковая навигация и определение дальности». Он является способом акустической локализации местоположения объекта. Звуковые волны передаются через среду, а время возврата отраженного звука обратно является показателем местоположения представляющего интерес объекта. Доплеровские сигналы генерируются движущимся объектом. В результате изменение между параметрами прямой и отраженной волны позволяет определить скорость объекта.
Концепция отслеживания спекла - это определение и отслеживание во времени отражений конкретных тканей (IEEE Transactions on Ultrasonics, Ferroelectrics, AND Frequency Control (Протоколы института инженеров по электротехнике и электронике), том 57, № 4, апрель 2010 года, включены в данную заявку посредством ссылки). После определения местоположений точек в пространстве можно создать трехмерную базовую систему координат, в которой может осуществляться подача энергии в конкретные и точно установленные места. Для отслеживания спекла получают изображение ткани в виде отраженных ультразвуковых сигналов. В изображении определяются местоположения светлых и темных точек, которые представляют собой неоднородности в тканях. Такие неоднородности относительно постоянны, являясь, по существу, характеристиками ткани. При наличии относительно постоянных маркеров в ткани можно провести отслеживание с помощью формирования изображений маркеров в реальном времени. В случае подачи ультразвукового сигнала более чем в одной плоскости маркеры можно представить в трехмерном пространстве относительно местоположения ультразвукового преобразователя и потока лечебной энергии, поступающего в указанное положение в пределах трехмерного поля.
Когда для определения местоположения цели в трехмерном пространстве используется один или несколько из этих способов формирования изображения, терапию можно как спланировать, так и применить к конкретному участку ткани, находящемуся в пределах трехмерного пространства.
Литотрипсия стала применяться в начале 1980-ых годов. Для удаления камней из почек в литотрипсии используются ударные волны. Система литотрипсии Дорнье (Dornier) была первой системой, произведенной для этой цели. Система литотрипсии посылает ультразвуковые волны сквозь тело пациента в направлении точки для избирательного подогрева и вибрации почечных камней, то есть избирательно через расположенную рядом ткань. В настоящее время в системах литотрипсии не используется прямое наведение и формирование изображения участка, где находится почечный камень. Внушительным прогрессом в области технологии будет получение изображения участка, где находится камень, и наведение излучения на конкретный участок местоположения камня с тем, чтобы минимизировать изменение таких окружающих структур как стенки почки. При наличии почечного камня почка фактически является спеклом, что позволяет провести наведение в трехмерном пространстве и отследить его изображение с последующим применением ультразвуковых волн для раздробления этого камня. В нижеприведенных осуществлениях изобретения многие используемые способы и описанные результаты по формированию изображений могут быть применены для литотрипсии, проводимой в клинических условиях.
Гистотрипсия ткани - это термин, данный способу, при использовании которого ткань по существу испаряется посредством образования кавитации, а не просто нагревается (чрескожное нетепловое механическое фракционирование ткани). Такие мини-взрывы не требуют высокой температуры и могут происходить менее чем за секунду. Величина сгенерированной волны давления изменяется в десятках мегапаскалей (МПа) и даже достигает или превышает 100 МПа. Такой способ может оказаться очень эффективным для лечения участков ткани малой площади. Граница между жизнеспособной и нежизнеспособной тканью, как правило, хорошо заметна, а показанный механизм действия - обычное разрушение клеток.
В одном осуществлении изобретения ультразвуковой сигнал фокусируется на участке почечных артерий и/или вен, поступая из-за пределов тела пациента; ультразвуковой сигнал подается под многочисленными углами на подлежащий лечению объект, посредством чего устраняются многие недостатки предыдущих способов и устройств, предложенных для абляции почечных симпатических нервов, которые окружают почечные артерии.
Одно осуществление изобретения особенно полезно для высокоточной визуализации зоны абляции нервных тканей с тем, чтобы оператор мог быть уверенным в абляции надлежащего и в целостности непредназначенного для абляции участка. Из-за того, что некоторые осуществления изобретения не требуют прокалывания кожного покрова, они носят значительно менее инвазивный характер, что делает их более привлекательными и безопасными с точки зрения пациента. Помимо этого можно проводить лечение с помощью подачи внешней энергии, триангуляция которой осуществляется относительно почечных артерий, в условиях нестандартного анатомического строения и наличия атеросклеротических кровеносных сосудов для оказания воздействия на симпатические и центростремительные нервы, входящие в почку и соответственно исходящие из нее.
Если сослаться на фигуру 1A, то анатомическое строение почки человека состоит из почки 100, которая снабжается насыщенной кислородом кровью через почечные артерии 200 и соединена с сердцем через брюшную аорту 300. Лишенная кислорода кровь протекает из почек к сердцу через почечные вены (не показаны) и оттуда через нижнюю полую вену (не показана). Анатомическое строение почки включает корковый слой, мозговой слой и ворота. Кровь поступает в корковый слой, где она фильтруется, проходя через клубочки, и затем подается на мозговой слой, где происходит ее дополнительная фильтрация за счет ряда этапов реабсорбции и фильтрации в петлях волокон Хенле и отдельных нефронов; затем ультрафильтрат проникает в собирательную мочеточниковую систему и пересылается в мочеточник и в мочевой пузырь для окончательного выделения из организма.
Ворота - это участок, где главные кровеносные сосуды (почечная артерия и почечная вена) и нервы 150 (центробежные симпатические, центростремительные чувствительные и парасимпатические нервы) входят в почки и исходят из них. Почечные нервы 150 содержат постганглионарные центробежные нервы, которые обеспечивают симпатическую иннервацию почек. Центростремительные чувствительные нервы проходят от почек в центральную нервную систему и являются постганглионарными центростремительными нервами, тела которых подсоединены к центральной нервной системе. Эти нервы передают сенсорную информацию в центральную нервную систему и, как предполагается, регулируют значительную часть симпатических сигналов, исходящих из центральной нервной системы во все органы тела, включая кожу, сердце, почки, мозг и т.д.
При использовании одного способа энергия подается через кожный покров пациента из источника, находящегося за пределами его тела, и поступает на почечные центростремительные и/или почечные центробежные нервы. В некоторых или во многих осуществлениях изобретения можно было бы применить сверхвысокочастотное, световое, вибрационное (например, акустические волны) и ионизирующее излучение.
Преобразователи энергии 510 (фигура 1A) чрескожно подают энергию на участок симпатических нервных узлов 520 или на участок постганглионарных почечных нервов 150 либо на участок нервов, ведущих к надпочечной железе 400. Энергия генерируется за пределами организма пациента и подается из разных направлений, проходя через кожный покров на участок почечных нервов 624, расположенных возле почечной артерии 620 или симпатического нервного узла 622, который вмещает нервы. Энергия может быть сфокусирована или не сфокусирована, однако в одном предпочтительном осуществлении изобретения энергия фокусируется в виде сфокусированного ультразвукового сигнала высокой интенсивности (HIFU) или в виде сфокусированного ультразвукового сигнала низкой интенсивности.
Фокусирование при использовании сфокусированного ультразвукового сигнала низкой интенсивности (LIFU) также может выполняться преднамеренно как составляющая HIFU (участки полутени) или непреднамеренно. Механизм подавления функции нервов изменчив и зависит «низкой» или «высокой» величины сфокусированного ультразвукового сигнала. Низкий уровень энергии мог бы соответствовать значениям в диапазоне 25Вт/см2-200 Вт/см2. Сигнал более высокой интенсивности соответствует уровням энергии от 200 Вт/см2 до 1 МВт/см2. Фокусирование происходит при подаче энергии сквозь кожный покров, по меньшей мере, под двумя разными углами для того, чтобы ее лучи встретились в фокальной точке, где достигается наивысшая интенсивность и плотность энергии. В эту точку доставляется лечение, которое может заключаться в прерывании функционирования нерва на подпороговом уровне (частичная абляция), абляция (полное прерывание функционирования) нервов, управляемое прерывание способности пропускания сигналов по нервам, частичная абляция или целенаправленная подача лекарств. Участок может нагреваться до температуры менее 60 градусов по Цельсию при проведении неразрушающей терапии или свыше 60 градусов по Цельсию для разрушения с помощью подогрева (абляции). Для абляции нервов можно использовать даже температуры в диапазоне 40 градусов по Цельсию, которые в течение временного периода, превышающего несколько минут, приведут к абляции. Что касается температур, равных приблизительно 50 градусов по Цельсию, то упомянутый временной период мог бы составлять чуть меньше одной минуты. Нагрев в стороне и воздействие вибрации в течение намного меньшего периода времени при температурах ниже 60 градусов по Цельсию может привести к частичному или полному параличу в разрушении нервов. Если температура возрастает до значения свыше 50-60 градусов по Цельсию, то время, необходимое для нагрева с целью воздействия на нерв с помощью отдельного механизма нагревания, существенно уменьшается. В некоторых осуществлениях изобретения в систему также включается способ формирования изображений. Способ формирования изображений может быть основан на ультразвуке, ядерном магнитном резонансе или на компьютерной томографии (рентгеновском излучении). Способ формирования изображений может быть применен для наведения на подлежащий абляции участок и для определения расстояния до подлежащего лечению объекта.
В некоторых осуществлениях изобретения поданная энергия может быть ионизирующей или неионизирующей. Формы неионизирующей энергии могут включать электромагнитную энергию, такую как магнитное поле, свет, электрическое поле, высокочастотную энергию и энергию на основе света. Формы ионизирующей энергии включают рентгеновское излучение, пучок протонов, гамма-излучение, пучки электронов и излучение альфа-частиц. В некоторых осуществлениях изобретения способы комбинируются. Например, выполняется абляция тканей нервов с помощью тепла, после чего место абляции обрабатывается ионизирующим излучением для предотвращения регенерации этих тканей.
В качестве альтернативы ионизирующее излучение используется вначале как способ абляции нервной ткани, после чего подача тепла в случае регенерации ткани в качестве повторного облучения может оказаться невозможной (дополнительное или мультимодальное использование энергии). Ионизирующее излучение может предотвратить или замедлить регенерацию нервной ткани, расположенной возле кровеносного сосуда, если регенерация нервной ткани действительно происходит. Отсюда другой способ лечения нервов заключается вначале в их нагревании с последующей подачей ионизирующего излучения для предотвращения регенерации ткани.
В качестве приема по объединению способов терапевтического воздействия можно использовать другие способы, такие как фотодинамическая терапия, включающая использование фотосенсибилизатора и источника света для активации последнего. Большинство из химических агентов фотосенсибилизации также чувствительны к воздействию ультразвуковой энергии, создающей те же фотореактивные составляющие так, как будто они были активированы светом. Фотореактивный или фоточувствительный химический агент может быть введен в подлежащую лечению область до вставки устройства в кровеносный сосуд. Такая вставка осуществляется, например, с помощью внутривенной инъекции, подкожной инъекции и т.д. Однако должно быть понятно, что в случае необходимости устройство по желанию может содержать полость для подачи фотореактивного химического агента в подлежащую лечению область. Полученные в результате осуществления изобретения, вероятно, окажутся чрезвычайно полезными там, где поглощение фотореактивного химического агента тканями подлежащей лечению области происходит относительно быстро. Это необходимо для того, чтобы не требовалось держать устройство в кровеносном сосуде на протяжении продолжительного периода времени, пока фотореактивный химический агент распределяется среди тканей подлежащей лечению область и поглощается ими.
Матрицы источников света могут содержать источники света, которые обеспечивают более одной волны или более одного диапазона волн света. Линейные матрицы источников света особенно полезны при лечении удлиненных частей ткани. Матрицы источников света также могут содержать отражательные элементы для усиления передачи света в предпочтительном направлении. Например, устройства с пользой для дела могут содержать такие растягиваемые компоненты как надувные баллоны, преграждающие путь кровотока (они могут влиять на передачу света из источника на предназначенную для лечения ткань) и предоставляющие возможность центрирования устройства в кровеносном сосуде. Другое предпочтительное осуществление данного изобретения предполагает применение способа чрескожной фотодинамической терапии, когда система подачи химических агентов содержит систему подачи липосом, по существу состоящую из химических агентов фотосенсибилизации.
Другое осуществление настоящего изобретения относится к способу чрескожной ультразвуковой терапии, предназначенной для подлежащего лечению места поражения ткани молочной железы и осуществляемой с помощью агентов сенсибилизации. В этом осуществлении изобретения следующим способом с помощью ультразвука активируется биохимическая структура:
1) В подлежащий лечению объект вводится эффективная с терапевтической точки зрения доза ультразвуковой сенсибилизации или система подачи агентов ультразвуковой сенсибилизации либо пролекарство. После этого агент ультразвуковой сенсибилизации или система подачи агентов ультразвуковой сенсибилизации либо пролекарство выборочно связывается с плотными или тонкими новообразованиями, нервными клетками, периневриями, ядрами нервов, артериальными бляшками, клетками сосудистой гладкой мышцы и/или с внеклеточным патологическим матриксом в подлежащем лечению месте. Компоненты нервов, например периневрий, миелин и протеин S-100, также могут быть целью терапии. За этим этапом следует обработка, по меньшей мере, части подлежащего лечению объекта ультразвуковой энергией на частоте, которая активирует агент ультразвуковой сенсибилизации, или же в случае применения пролекарства - продуктом пролекарства, при этом ультразвуковая энергии обеспечивается источником излучения ультразвуковой энергии. Это осуществление изобретения далее по желанию пользователя обеспечивает удаление терапевтического лекарственного препарата, предназначенного для ультразвуковой обработки, из непредназначенных для лечения тканей до подачи излучения.
В другом предпочтительном осуществлении изобретения предполагается применение способа чрескожной ультразвуковой терапии предназначенной для лечения ткани, когда такая целевая ткань располагается рядом с кровеносным сосудом.
В других предпочтительных осуществлениях данного изобретения предполагается такое расположение источника излучения ультразвуковой энергии, которое является внешним по отношению к нетронутому кожному покрову пациента, или его установку под нетронутый кожный покров пациента, однако в месте, находящемся за пределами подлежащего лечению кровеносного сосуда. Дополнительное предпочтительное осуществление данного изобретения обеспечивает связыванием агентов ультразвуковой сенсибилизации с лигандом и, что более предпочтительно, при его использовании лиганд выбирается из группы, в которую входят антитело, предназначенное конкретно для изменения целевой ткани; пептид, предназначенный конкретно для изменения целевой ткани, и полимер, предназначенный конкретно для изменения целевой ткани. В других предпочтительных осуществлениях данного изобретения предполагается выбор агента ультразвуковой сенсибилизации из группы, состоящей из зеленого индоцианина (ICG); метиленового синего; толуидинового синего; аминолевулиновой кислоты (ALA); хлорных соединений; фталоцианинов; порфиринов; пурпуринов; тексафиринов и любых прочих химических агентов, которые поглощают свет в волновом диапазоне 500-1100 нм. В другом предпочтительном осуществлении данного изобретения предполагается, что химическим агентом сенсибилизации является зеленый индоцианин (ICG).
Другие осуществления настоящего изобретения относятся к раскрытым в данной работе способам применения чрескожной фотодинамической терапии, при использовании которых источник света располагается вблизи подлежащей лечению ткани объекта и выбирается из группы, в которую входят: источник света на светоизлучающих диодах; электролюминесцентный источник света; источник света от лампы накаливания; источник флуоресцентного света на холодном катоде; источник света на органическом полимере и источник света на неорганическом веществе. Предпочтительное осуществление изобретения состоит в применении источник света на светоизлучающих диодах.
Другие осуществления раскрытых в данной работе способов относятся к использованию света с длиной волны, которая изменяется в диапазоне от приблизительно 500 нм до приблизительно 1100 нм. Предпочтительной является длина волны приблизительно свыше 650 нм, а еще более предпочтительно, когда длина волны оказывается свыше приблизительно 700 нм. Предпочтительное осуществление настоящего способа относится к использованию света, который приводит к режиму поглощения отдельных фотонов агентом сенсибилизации.
Дополнительные осуществления настоящего изобретения включают композиции системы направленной подачи сенсибилизатора, содержащие: агент сенсибилизации и лиганд, который связывает рецептор на подлежащей лечению ткани со специфическими признаками. Предпочтительно, чтобы агент фотосенсибилизации из системы направленной подачи соединялся с лигандом, который связывает рецептор на подлежащей лечению ткани (нерв или адвентициальная стенка кровеносного сосуда) со специфическими признаками. Более предпочтительно, если лиганд содержит антитело, которое соединяется с рецептором. Более предпочтительно, если рецептор является антигеном на плотных или тонких новообразованиях, внутренних оболочках кровеносных сосудов, адвентициальных оболочках артерий, артериальных бляшках, клетках сосудистой гладкой мышцы и/или на внеклеточном патологическом матриксе в подлежащем лечению месте.
Далее в отношении предпочтительного осуществления настоящего изобретения предполагается, что агент фотосенсибилизации выбирается из группы, которая состоит из зеленого индоцианина (ICG); метиленового синего; толуидиного синего; аминолевулиновой кислоты (ALA); хлорных соединений; фталоцианинов; порфиринов; пурпуринов; тексафиринов и любых прочих химических агентов, которые поглощают свет в волновом диапазоне 500-1100 нм.
Специалистам в данной области техники известны и другие агенты фотосенсибилизации, в том числе, фотофрин, RTM, синтетический дипорфирины и дихлорины, фталоцианины с замещающей группой металлов или без нее, фталоцианин хлористого алюминия с переменными замещающимися группами или без них, сульфированный фталоцианин хлористого алюминия, O-замещенные тетрафениловые порфирины, порфирин 3,1-мезо тетракиса (О-пропиоамидофенил) порфирин, вердины, пурпурины, производные октаэтилпурпурина на основе олова и цинка, этиопурпурин, гидропорфирины, бактериохлорины на основе ряда порфирина тетра- (гидроксилфенила), хлорины, хлорин e6, моно-1-аспартил производная хлорина e6, ди-1-аспартил производная хлорина e6, хлорин e6 на основе олова(IV), мета-тетра гидроксфенилхлорин, производные бензопорфирина, производные одноосновной кислоты бензопорфирина, тетрацианоэтиленовые продукты присоединения бензопорфирина, продукты присоединения бензопорфирина на основе диметил-ацетилендикарбоксилата, продукты присоединения Дилза-Адлера (Diels-Adler), производная бензопорфирина с кольцом одноосновной кислоты "a", пропиленкарбонат сульфированного алюминия, ди-сульфированная и тетра-сульфированная производная пропиленкарбоната сульфированного алюминия, нафталоцианины сульфированного алюминия, нафталоцианины с замещаюшей группой металлов или без нее, а также с замещающими переменными группами или без них, нафталоцианин цинка, антрацендионы, антрапиразолы, аминоантрахинон, красители на основе феноксазина, производные фенотиазина, красители на основе халькогенпирилия, катионоактивные производные селена и теллурпирилия, катионоактивный пропиленкарбонат с замещенным кольцом, производная феофорбида, альфа-производные и производные в виде эфира и сложного эфира на основе феофорбида, пирофеофорбиды и производные в виде эфира и сложного эфира, встречающиеся в природе порфирины, гематопорфирин, производные гематопорфирина, эфиры и сложные эфиры на основе гематопорфирина, протопорфирин, протопорфирин IX, полученный с помощью аминолевулиновой кислоты, эндогенные метаболические прекурсоры, бензонафтопорфиразины 5- аминолевулиновой кислоты, катионоактивные соли имминиума, тетрациклины, тексафирин лютеция, олово-этио-пурпурин, порфицены, бензофенотиазиниум, пентафирины, тексафирины и гексафирины, 5-аминолевулиновая кислота, гиперицин, псевдогиперицин, гипокрелин, тертиофены, азапорфирины, азахлорины, бенгальский розовый краситель, флексин B, эритрозин, иодированные или бромированные производные флупресцина, мероцианины, производные нильского голубого красителя, производные феофитина и хлорофилла, производные бактериохлорина и бактериохлорофила, порфойианины, бензохлорины и оксобензохлорины, сапфирины, оксасапфирины, церкоспорины и связанные с ними грибковые метаболиты и их комбинации.
Несколько известных в данной области фотосенсибилизаторов получили одобрение со стороны Управления по контролю продуктов и лекарств (США) и доступны в продаже. В предпочтительном осуществлении изобретения фотосенсибилизаторов является такая производная бензопорфирина ("BPD") как BPD-MA, которая также известна в торговле под названием BPD Verteporfin (вертепорфин) или "BPD" (доступна в продаже у компании QLT). В патенте США под № 4883790 описаны составы BPD. BPD - это состав второго поколения, который лишен продолжительного токсического воздействия на кожу, присущего Photofrin® (Леви (Levy) (1994), журнал Semin Oncol (Семинары по онкологии) №21, стр.4-10). Препарат BPD основательно изучен (Рихтер и др. (Richter et al.), (1987), журнал JNCI №79, стр. 1327-1331), (Авелин и др. (Aveline et al.) (1994), журнал Photochem Photobiol (Фотохимии и фотобиология), № 59, стр. 328-35), и оказался чрезвычайно сильным фотосенсибилизатором для фотодинамической терапии.
В предпочтительном осуществлении изобретения фотосенсибилизатором является препарат олово-этил-этиопурпурин, который известен в торговле под названием пурлитин (доступен в продаже у компании Miravant).
В некоторых осуществлениях изобретения выполняется внешняя нейромодуляция, при приведении которой ультразвуковой сигнал малой мощности подается на участок расположения нервов для их модуляции. Например, ранее показано, что ультразвуковой сигнал низкой интенсивности (например, нетепловой сигнал) может воздействовать на нервы при мощности, которая изменяется в диапазоне 30-500 мВт/см2, тогда как сфокусированный ультразвуковой сигнал высокой интенсивности (тепловая модуляция), который по определению генерирует тепло в фокальной точке, требует достижения уровней мощности, превышающих 1000 Вт/см2. Фактический поток мощности, поступающий на подлежащий абляции участок, зависит от окружающих условий, включая ближний кровоток и другие структуры. При использовании ультразвукового сигнала низкой интенсивности энергия не должна слишком точно фокусироваться на подлежащем лечению объекте, потому что она не является абляционной; то есть, вибрация или механическое давление является энергией-эффектором, а объект может характеризоваться другим порогом воздействия, зависящим от ткани. Однако даже маломощному звуковому сигналу может потребоваться фокусировка, если предметом беспокойства станет чрезмерный нагрев кожного покрова, или же если на пути прохождения сигнала окажутся другие чувствительные структуры, а для успеха терапии желательно воздействие только на точечный участок, предназначенный для терапии. Тем не менее, преобразователи 500, представленные на Фигуре 1a, обеспечивают возможность подачи сигнала в диапазоне различных уровней энергии и мощности, а также возможность проведения моделирования наведений на различные участки и прогнозирования ответного сигнала.
На фигуре 1А, и в одном осуществлении изобретения выполняется обнаружение почечной артерии 640 с помощью таких устройств формирования изображения 600, как те, которые работают на доплеровском ультразвуковом сигнале, инфракрасном излучении, с помощью тепловидения, на ультразвуковом сигнале в B-режиме, с использованием способа ядерного магнитного резонанса или сканирования посредством компьютерной томографии. Вследствие необходимости обработки изображения участка можно провести во многих направлениях измерения набора срезов для создания трехмерного отображения представляющей интерес области. Посредством нахождения местоположения почечных артерий под более чем одним углом, которое выполняется с помощью доплеровской триангуляции (например) или другим способом триангуляции, можно составить трехмерную позиционную карту и внести местоположение почечной артерии в систему координат. В этом отношении даже при условии расположения почечных нервов вблизи почечных кровеносных сосудов, находящихся в воротах, локализация направления и длины кровеносных сосудов в трехмерной системе координат является превалирующей составляющей процедуры наведения носителя энергии на эти симпатические нервы. В пределах системы координат конфигурация подачи энергии может быть наложена на участок, расположенный рядом с почечной артерией, с помощью устройства, установленного довольно далеко от этого места (и вообще за пределами тела пациента), на основании информации, представленной в системе координат.
Например, если почечная артерия занесена в систему координат, в начале отсчета которой находится устройство подачи энергии, то применяется алгоритм локализации объекта наведения сфокусированного ультразвукового сигнала для подачи тепловой или механической энергии на адвентициальную оболочку и на близлежащие участки артерии, которые содержат симпатические нервы, входящие в почку, и центростремительные нервы, исходящие из почки. В результате происходит снижение уровня сигнала симпатического раздражения, поступающего в почку, и ослабление центростремительного сигнала, поступающего из почки обратно в автономную нервную систему; воздействие, оказываемое на эти объекты, будет модулировать предрасположенность к гипертензии, которая, так или иначе, возникнет. Можно провести математическое моделирование подачи ультразвуковой энергии с помощью прогнозирования рассеяния акустической волны, используя для этого значения расстояний и измерений, полученные при обращении к способам терапевтического воздействия и формирования изображений тканей, а также значений расстояния прохождения сигналов.
В одной реализации алгоритма доплеровский сигнал, отраженный от артерии, идентифицируется, по меньшей мере, с двух разных направлений, а направление прохождения самой артерии реконструируется в трехмерном пространстве. При использовании двух точек пространства создается линия, после чего, обратившись к информации о толщине кровеносного сосуда, можно воссоздать трубку или цилиндр для представления кровеносного сосуда в виде виртуальной модели. Трубка представляется во времени в трехмерном пространстве, а ее координаты относительно преобразователей терапии, расположенных за пределами кожного покрова пациента, известны. Лечебная энергия может быть подана также по нескольким направлениям и сфокусирована на цилиндре (передняя стенка кровеносного сосуда, центральная ось или задняя стенка кровеносного сосуда).
Сфокусированная энергия (например, ультразвук) может быть подана в центр кровеносного сосуда (в пределах кровотока), на заднюю стенку кровеносного сосуда, в место между артериальным и венозным кровеносными сосудами (например, когда артерия и вена вплотную прилегают друг к другу) и в другие места.
Формирование изображения симпатических нервов 600 или участка симпатических нервов (подлежащий лечению объект) также используется с тем, чтобы дать оценку направлению и ориентации преобразователей относительно подлежащего лечению объекта 620. Цель представляет собой расположенную внутри опорную точку измерений, которой в одном осуществлении изобретения является точка 610 и связанная с ней почечная артерия 620, потому что они могут быть локализованы с помощью их кровотока. Затем на основании таких данных локализации строится модель, после чего оба эти объекта могут быть использованы в качестве цели для подачи энергии. Непрерывная обратная связь местоположения преобразователей 500, 510 относительно целевого объекта 620 обеспечивается системой формирования изображений, которая сохраняет пространство координат. Формирование изображений может выполняться согласно технологии формирования изображений в поперечном сечении, такой как компьютерная томография или магнитный резонанс, либо в соответствии с технологией ультразвукового формирования изображений, которая приводит к более быстрому получению изображения в реальном времени. В некоторых осуществлениях изобретения формирование изображений может представлять комбинацию таких технологий, как сочетание ядерного магнитного резонанса/компьютерной томографии и ультразвука. Система формирования изображений может обнаруживать цель в реальном времени на частотах, изменяющихся в диапазоне от 1 Гц до тысяч и десятков тысяч изображений в секунду.
На примере такого сочетания формирование изображений в поперечном сечении (например, с использованием способа MRI/компьютерной томографии) используется для размещения размеров тела пациента в трехмерную систему координат. После этого подается ультразвуковое излучение, которое используется для отслеживания контуров тела пациента в реальном времени и для формирования изображений в поперечном сечении. Отсутствие разрешающей способности, обеспечиваемой ультразвуковым сигналом, компенсируется формированием изображений в поперечном сечении, поскольку для привязки ультразвукового изображения к изображению, полученному с использованием способа MRI, требуются лишь несколько согласованных опознавательных точек анатомического строения объекта. Так как в процессе ультразвукового облучения тело не стоит на месте, новые последовательно получаемые ультразвуковые изображения связываются с изображениями, полученными с использованием способа MRI, отсюда «перемещение» изображений, полученных с использованием способа MRI, может быть заметно на частоте, которая в других отношениях не присутствует в серии подачи энергии с использованием способа MRI.
В одном осуществлении изобретения ультразвуковой сигнал представляет собой энергию, используемую для подавления нервной проводимости симпатических нервов. В одном осуществлении изобретения сфокусированный ультразвуковой сигнал (HIFU) высокой интенсивности, поступающий через кожный покров из источника, расположенного за пределами тела пациента, представляет собой энергию, используемую для подавления симпатической стимуляции почки за счет подачи волн из источника, расположенного за пределами тела пациента, и фокусирования этих волн на находящихся внутри пациента симпатических нервах, расположенных рядом с его почечной артерией.
Как показано на фигуре 3a-b, преобразователи 900 могут излучать ультразвуковую энергию из положения за пределами тела пациента на участок почечных симпатических нервов в почечной ножке 200. Как показано на фигуре 1А, изображение почечной артерии 620, полученное с помощью ультразвука, ядерного магнитного резонанса или сканирований посредством компьютерной томографии, может быть использовано для определения местоположения почки 610 и подлежащей лечению артерии 620. Ультразвуковой доплеровский сигнал можно использовать для определения местоположения объекта и направления обратного сигнала, отраженного от артерии, и для размещения кровеносного сосуда в трехмерной системе координат 950. В результате артерии 200 и, следовательно, симпатические нервы 220 (Фигура 3a), расположенные вблизи артерии, становятся намного заметнее, что приводит к улучшению обработки изображений и последующему использованию сфокусированной внешней энергии для локализации местонахождения и проведения лечения симпатических нервов. В этом осуществлении изобретения применение ультразвука является, вероятно, наиболее подходящим способом формирования изображения.
На фигуре 1a также представлена подача сфокусированной энергии на стволы и ганглии симпатических нервов 622, которые проходят вдоль позвоночного столба и аорты 300; центробежные нервы почечной артерии проходят по этим стволам и по синапсу до нервных узлов, расположенных в пределах стволов. В другом осуществлении изобретения абляция заднего и переднего корешков спинного мозга на уровне нервных узлов и нервов заднего корешка спинного мозга у T9-T11 (через которые проходят центростремительные почечные нервы) должна привести к тому же самому или аналогичному результату по абляции нервных тканей на уровне почечных артерий.
В другом осуществлении изобретения, на фигуре 1b показано использование ионизирующей энергии применительно к участку симпатических нервов почечных артерий 620 и/или почечных вен. В общем случае для линейных ускорителей или маломощных устройств рентгеновского излучения, предназначенных для абляции нервной ткани с помощью ионизирующей энергии, потребуются уровни энергии свыше 20 Гр (грэев); однако для «оглушения», подавления функционирования нервной ткани или для предотвращения ее регенерации достаточно малого уровня энергии. В некоторых осуществлениях изобретения такие низкие уровни ионизирующей энергии, как 2-5 Гр или 5-10 Гр либо 10-15 Гр подаются в отдельных или раздельных дозах.
В этом осуществлении изобретения также можно использовать комбинации ионизирующей энергии и других форм энергии для предотвращения регенерации нервной ткани. Например, можно было бы использовать комбинацию тепла и/или вибрации, и/или кавитации, и/или ионизирующего излучения для предотвращения регенерации нервной ткани после ее частичной или полной абляции рядом с почечной артерией.
На фигуре 2 более подробно показано анатомическое строение почки и расположенных вблизи органов, при этом такие органы, как желудок 700 показаны в своем анатомическом положении выше брюшной аорты 705 и почечных артерий 715. В этом осуществлении изобретения для попадания в область, расположенную за желудком, энергия подается через желудок. В этом осуществлении изобретения желудок используется в качестве «канала» для доступа к брюшному нервному узлу 710, месту, в которое было бы затруднительно попасть иным образом. Аорта 705, показанная под желудком и брюшным нервным узлом 710, изображена вблизи расположенной выше брыжеечной артерии и аорты. Трансорально расположенная трубка 720 проходит в желудок через пищевод. При размещении в желудке трубка находится выше брюшного нервного узла и, следовательно, может быть использована для ввода симпатолитических устройств или фармацевтических препаратов, которые тормозят или возбуждают автономные брюшные нервные узлы, находящиеся за желудком. Такая терапия должна проводиться с помощью абдоминального ультразвукового или рентгеноскопического наводящего приспособления (для получения изображений), проходящего через желудок. Аналогичную терапию можно применять в отношении расположенного ниже брыжеечного нервного узла и почечных или симпатических нервов, проходящих через желудок или через другую часть желудочно-кишечного тракта вдоль аорты. Преобразователи для подачи энергии 730, 731 показаны расположенными за пределами тела пациента и могут быть использованы для усиления терапевтического воздействия на брюшной нервный узел, осуществляемого через желудок. В качестве альтернативы преобразователи для подачи энергии могут быть использованы для формирования изображений участка, подвергаемого терапевтическому воздействию.
В одном осуществлении изобретения энергия подается на участок брюшного нервного узла из места за пределами тела пациента. При этом осуществлении изобретения в желудочно-кишечную систему подается жидкость, наподобие той, которая, например, содержится в желудке или в тонкой кишке. После этого ультразвуковой сигнал может быть передан через желудочно-кишечные органы на представляющие интерес нервные узлы, расположенные за желудком.
Можно также через трубку ввести временные нейростимуляторы, такие как, например, те, что устанавливают в отделении интенсивной терапии, когда может потребоваться временное блокирование функции автономных нервных узлов. Временные нейростимуляторы можно использовать для подачи импульсов, превышающих темп работы нервных волокон брюшного нервного узла, и, как следствие, для подавления их функции в качестве нервного синапса. Подавление функции брюшного нервного узла может иметь ту же функцию, что абляция или модулирование симпатических нервов, расположенных вблизи почечных артерий. То есть снижение активности симпатических нервов почек (в настоящий момент достигнутое за счет большего приближения к точной величине подавления) приводит к снижению кровяного давления у пациента за счет снижения уровня выходного потока сигналов симпатических нервов, исходящих из окончаний симпатических нервов. В брюшных нервных узлах результат от понижения кровяного давления оказывается более значительным при условии, что брюшные нервные узлы являются преганглионарными и обладают более значительным количеством нервных волокон на большем числе участков, чем каждый из почечных нервов. Продолжительность действия вышеупомянутого достигнутого результата также, вероятно, окажется более высокой, чем в случае воздействия на постганглионарные нервные волокна.
На фиг.3a представлено более точное анатомическое строение почки, при этом почечные нервы 220, проходящие в продольном направлении вдоль почечной артерии 200, как правило, располагаются в пределах или сразу за пределами адвентициальной оболочки наружной части артерии. Артерии обычно состоят из трех слоев: первый является интимальным, второй - медиальным, а третий - адвентициальной оболочкой. Наружный адвентициальный слой представляет собой волокнистую ткань, которая содержит кровеносные сосуды и нервы. Почечные нервы, как правило, являются постганглионарными симпатическими нервами, хотя есть и некоторые нервные узлы, которые располагаются отдаленно от места отхода от аорты таким образом, что некоторые из нервных волокон, проходящие вдоль почечной артерии, фактически являются преганглионарными. К моменту подхода к почке большинство волокон становятся постганглионарными. С другой стороны, центростремительные нервы выходят из почки и являются постганглионарными до уровня, занимаемого мозгом. Эти волокна не регенерируются так быстро, как центробежные волокна, если вообще их регенерация представляется возможной.
Генераторы энергии 900 подают энергию на почечные нервы вблизи почечной артерии, распределяя ее по многим направлениям с целью подавления комплекса почечных нервов. Генераторы энергии могут подавать на участок ультразвуковую энергию, ионизирующее излучение, световую (фотонную) лечебную энергию или сверхвысокочастотную энергию. Энергия может быть несфокусированной в том случае, когда фармацевтический препарат направляется на подлежащий абляции или модуляции участок нервной ткани. Однако предпочтительно, чтобы для поступления на представляющий интерес участок (например, на симпатические нервы вблизи кровеносных сосудов) энергия фокусировалась во время подачи ее под многочисленными углами из источника, расположенного за пределами тела пациента. Местоположения преобразователей энергии 900 вводятся в систему 950 координат X-Y-Z, как и местоположения таких органов, как почки. Система координат x-y-z является реальной пространственной системой координат. Например, реальное пространство означает, что система координат идентифицируется в физическом мире подобно тому, как в случае применения GPS (глобальной системы навигации и определения положения) можно обнаружить физический объект на основании его физических координат. После ввода в систему координат x-y-z операция формирования изображения в виде поперечных сечений, осуществляемая с использованием способа MRI, способом сканирования посредством компьютерной томографии и/или с помощью ультразвука, используется для привязки внутреннего анатомического строения к преобразователям энергии. Те же самые преобразователи можно использовать для определения точки отсчета, а также для проведения терапии. Преобразователи 900 в этом осуществлении изобретения фокусируют свою энергию на участке почечных нервов на уровне почечных кровеносных сосудов, артерий и вен 200. Фокусировка излучения энергии может быть произведена внутри артерии, внутри вены, на адвентициальной оболочке артерии или на адвентициальной оболочке вены.
При подаче ультразвуковой энергии на участок почечной артерии через кожный покров в представляющей интерес точке адвентициальной оболочки кровеносного сосуда может потребоваться плотность энергии, которая возможно превысит 1 МВт/см2. Однако обычно следует ожидать, что плотность мощности от 100 Вт/см2 до 3 кВт/см2 создаст нагрев, требуемый для подавления функции этих нервов (см. работу Фоля и др. (Foley et. al) «Распад ткани периферийных нервов, выполняемый с помощью сфокусированной ультразвуковой энергии высокой интенсивности (HIFU), подаваемой по сформированному изображению для лечения мышечной спастичности и боли»; журнал «Ультразвуковой сигнал в медицине и биологии» (Ultrasound in Med & Biol.), том 30 (9), стр. 1199-1207, которая включена в эту заявку посредством ссылки). Импульсы энергии могут проходить через кожный покров без фокусирования; однако для применения тепла энергия преобразователей должна быть сфокусирована, иначе кожный покров и подкожные ткани поглотят слишком много тепла. При формировании изображения с использованием способа MRI измерения температуры можно проводить на основании такого изображения. Когда на участок подается маломощный ультразвуковой сигнал, то можно использовать плотности энергии (мощности) в диапазоне от 50 мВт/см2 до 500 мВт/см2. Маломощный ультразвуковой сигнал может оказаться достаточным для «оглушения» или частичного подавления функционирования почечных нервов особенно тогда, когда он пульсирует, а величина его зависит от желательного клинического результата. Высокоинтенсивный ультразвуковой сигнал, подаваемый на участок, температура которого возрастает только на несколько градусов, может оказать такое же воздействие, а диапазон изменения его мощности - составить 0,1-500 кВт/см2. Также можно было бы использовать серию импульсов для усиления воздействия излучения на нервную систему. Например, это может быть серия из 100 коротких импульсов, период каждого из которых составляет менее секунды, а плотность подаваемой ими энергии изменяется в диапазоне от 1 до 500 Вт/см2. В некоторых осуществлениях изобретения на кожу может быть подано охлаждение в том случае, если повышение температуры покажется слишком большим, чтобы его считали приемлемым. В качестве альтернативы ультразвуковые преобразователи могут работать в пульсирующем режиме или чередоваться в работе с другим набором преобразователей для действенного распространения тепла по поверхности кожи. В некоторых осуществлениях изобретения энергия подается в пульсирующем режиме для дополнительного снижении риска воздействии на ткани, расположенные между подлежащим лечению участком и преобразователем. Как описано, продолжительность импульсов может составлять примерно миллисекунду или длиться часами, днями или годами.
В одном способе изменения физиологического процесса симпатического почечного раздражения изображение участка, расположенного вблизи почечных артерий, формируется с помощью сканирования посредством компьютерной томографии, с использованием способа MRI, термографии, инфракрасного излучения, оптической когерентной томографии (OCT), фотоакустики, позиционно-эмиссионной томографии (РЕТ), однофотонной эмиссионной компьютерной томографии (SPECT) или с помощью ультразвукового сигнала. После этого параметры изображений вводятся в трехмерную систему 950 координат. Трехмерная система 950 координат обращается к информации о взаимосвязях между анатомическими структурами, представленными как в двух, так и в трех измерениях, после чего эти структуры помещаются в систему физических координат. Устройства формирования изображений определяют содержание системы координат. После установки системы координат преобразователи 900 формирования изображений и лечения могут быть подсоединены таким образом, чтобы информация из системы формирования изображений использовалась терапевтическими преобразователями для точного наведения подаваемой энергии. Кровеносные сосуды могут обеспечить создание полезной системы координат для поглощения энергии, так как они обладают уникальными сигнатурами своих изображений. Эхоимпульс ультразвукового сигнала может обеспечить сигнатуру доплеровского сдвига для идентификации кровеносного сосуда среди расположенной рядом ткани. При использовании способа ядерного магнитного резонанса, сканирования посредством компьютерной томографии и даже ультразвукового зондирования с целью идентификации конфигураций потока, полезных для установления системы координат поглощения энергии, можно применять внутривенные контрастные препараты. Местоположения преобразователей 900 энергии, которые могут обеспечивать подачу ультразвукового сигнала, световой энергии, излучения, ионизирующего излучения или энергию сверхвысоких частот, вводятся в ту же самую систему координат, как и в случае ввода данных о местоположении почечных артерий. По этим данным процессор (например, с использованием алгоритма) может определить направление наведения преобразователей для подачи энергии на участок 220 нервов 910. Алгоритм состоит из элемента наведения (элемент планирования), который позволяет спрогнозировать местоположение преобразователей и уровень поглощения энергии, подаваемой преобразователями 900.
После установления подключения или привязки трехмерной системы 950 координат для прецизионного позиционирования излучения энергии на подлежащий лечению объект тела можно использовать алгоритм планирования и прогнозирования.
Исходный способ формирования изображений можно использовать для локализации участка почечных симпатических нервов и для отслеживания перемещения этого участка в процессе лечения. Например, технология формирования изображения, примененная в момент времени «0», выбирается в качестве технологии базового сканирования, и последующие сканирования в момент времени t1 сравниваются с базовым сканированием t0. Частота обновлений может изменяться в диапазоне от одного сканирования длительностью несколько секунд до значительного числа сканирований в секунду. При использовании ультразвукового сигнала в качестве технологии для формирования изображений координаты объекта могли бы обновляться с частотой изменения кадров, превышающей 50 Гц и достигающей величины нескольких сотен или даже тысяч Гц. При использовании способа ядерного магнитного резонанса в качестве технологии для формирования изображений частота их обновления могла бы приближаться к 30 Гц. В других осуществлениях изобретения информация о местоположении, снятая с внутренних опорных точек измерений, передается с высокой частотой и используется для привязки цели к изначально применяемому внешнему устройству формирования изображений. Внешние опорные точки измерений могли бы содержать один или несколько воображаемых элементов, в том числе доплеровские сигналы, участки расположения кровеносных сосудов, ребер, почек, кровеносных сосудов и органов, отличных от тех, которые подлежат лечению (например, полая вена, надпочечная железа, мочеточник). Эти опорные точки измерений можно использовать для нахождения и/или проведения триангуляции подлежащего лечению участка.
В некоторых осуществлениях изобретения (Фигура 3C) на таком участке, как артерия 965, почечная вена 975, аорта 945 и/или полая вена 985, фиксируется временная опорная точка 960 измерений; такую опорную точку измерений легко представить при рассмотрении объектов из-за пределов тела пациента.
На фигуре 3D в системе 975 координат, представленной на экране монитора 950, показан воображаемый преобразователь 960, установленный в кровеносном сосуде 967. В качестве альтернативы во временной опорной точке 960 измерений установлен преобразователь, который дополнительно улучшает возможность формирования изображения и отслеживания местоположения подлежащего лечению участка для оказания на него терапевтического воздействия. Временная опорная точка измерений могла бы служить местом установки механического, оптического, электромеханического и радиочастотного радиопередающего устройства, устройства глобальной системы навигации и определения положения (GPS) или устройства, работающего на отраженных ультразвуковых сигналах. Информацию о подобных устройствах можно было бы обнаружить в патентах США 6656131 и 7470241, которые включены в данную заявку посредством ссылки.
Также можно отслеживать отражения сигналов внутри объекта (например, спеклы). Эти спеклы являются неотъемлемыми характеристиками ткани, так как попали на изображении при использовании ультразвукового сигнала. Их можно отследить и включить в алгоритм планирования лечения и затем осуществить их привязку к преобразователям лечебной энергии.
В некоторых осуществлениях изобретения на участок почечных симпатических нервов может быть направлена тестовая доза энергии, после чего проводится тест для определения эффективности воздействия этой дозы. Например, на область симпатических нервов может быть подан малый объем тепловой или вибрационной энергии. После этого можно провести тестирование симпатической активности, такой как микронейрография (выявление активности симпатических нервов, распложенных возле мускулов, и нервов, находящейся в определенной связи с ритмом биения сердца). Результаты прошлых исследований и текущие клинические данные показали, что прерывание почечных центростремительных нервов воздействует на симпатические нервы в периферийных мускулах. Уровень подъема температуры при незначительном нагревании можно определить с помощью измерения температуры при использовании способа ядерного магнитного резонанса или посредством ультразвука, а подъем температуры может быть определен или ограничен до обратимой величины.
В другом осуществлении изобретения на такой участок, как кожный покров оказывается стимулирующее воздействие, после чего проводится проверка его ответной реакции. Например, на кожный покров можно было бы направить вибрационную энергию и проверить симпатическую ответную реакцию, такую как величина пульса сердца. В другом осуществлении изобретения на кожный покров, пульс сердца и кровяное давление можно было бы воздействовать теплом или холодом; после этого можно было бы обнаружить ответную реакцию в виде сужения сосудов.
Для определения приблизительного подъема температуры участка ткани в качестве альтернативы можно использовать ультразвуковое формирование изображений. Скорость ультразвуковых волн зависит от температуры и, как следствие, относительная скорость передачи ультразвукового сигнала из подогреваемого участка также будет зависеть от температуры, следовательно, в результате на экран монитора выводятся измеряемые переменные. В некоторых осуществлениях изобретения для определения подъема температуры используются микро-пузырьки. Микро-пузырьки расширяются и затем после воздействия возрастающей температуры сдуваются таким образом, чтобы после этого с их помощью можно было бы предсказать температуру подогреваемого участка. Также можно использовать способ, называемый ультразвуковой эластографией. В этом осуществлении изобретения эластичность ткани зависит от температуры, и вследствие этого для отслеживания характеристик изменения температуры можно применить эластографию. Для усиления терапевтического воздействия на подлежащий лечению участок также можно использовать микро-пузырьки. Например, их можно использовать для высвобождения фармацевтического препарата после попадания на них ультразвукового излучения. Структура микро-пузырьков в качестве альтернативы может быть использована для увеличения изображения подлежащей лечению области с целью улучшения наведения излучения на такую область или отслеживания перемещения.
В некоторых осуществлениях изобретения используется только возможность определения температуры. То есть, при обращении к любой процедуре, во время выполнения которой осуществляется нагревание, используются осуществления изобретения и алгоритмы по считыванию температуры. Например, в том случае, когда нагревание участка почечного нерва выполняется с помощью радиочастотного сигнала, проходящего через почечную артерию, можно осуществлять формирование изображений участка с места, расположенного за пределами тела пациента, одновременно с нагреванием участка почечной артерии, используя способ с применением радиочастотного излучения. Формирование изображений можно выполнять с использованием способа MRI, с помощью ультразвуковых сигналов, инфракрасного излучения или способов оптической когерентной томографии (OCT).
В другом осуществлении изобретения можно протестировать комплекс барорецепторов в области бифуркации сонной артерии. После подачи тестовой дозы энергии на комплекс почечной артерии можно подвергнуть его сдавливанию; как правило, когда комплекс барорецепторов не подвергается воздействию, системное кровяное давление должно снизиться после сдавливания сонной артерии. Однако когда функционирование центростремительных почечных нервов подавлено, барорецепторы не будут восприимчивы к изменениям кровяного давления и, как следствие, можно определить эффективность подачи энергии на почечные нервы. Другие тесты охватывают получение показателей работы функции автономной нервной системы, таких как микронейрография, изменчивость функции автономной нервной системы и т.д.
В другом осуществлении изобретения стимулирование комплекса барорецепторов выполняется неинвазивнымобразом с помощью ультразвуковых импульсов, подаваемых извне на участок тела сонной артерии. Ультразвуковые импульсы достаточны для раздражения синуса с целью воздействия на изменение кровяного давления, изменения, на которое будет оказано воздействие, когда произойдет изменение в центростремительном нерве, таком как почечный центростремительный нерв.
Более конкретно эта методология представлена на фигуре 3E. Для раздражения сонного синуса 982, который на короткое время снизит кровяное давление посредством активации комплекса барорецепторов, используется ультразвуковой импульс 980; активация сонного синуса 980 стимулирует эффект повышения кровяного давления, который приводит к компенсирующему ответу в виде активации парасимпатических нервов, впоследствии снижающей кровяное давление. В примере, когда было проведено подавление системы центростремительных нервов (например, исходящих из почки), кровяное давление не будет поддаваться столь быстрому изменению, если вообще будет меняться. В этом случае, если стимулирование комплекса барорецепторов не приведет к снижению кровяного давления 986, то лечение было проведено успешно. Этот диагностический способ, следовательно, может быть использован для определения воздействия терапии на такую систему, как комплекс почечных нервов. Если терапия оказалась успешной, то корректирующее воздействие ультразвукового импульса на сонный синус и на кровяное давление проявляется менее резко, то есть терапия (лечение центростремительных нервов) оказалась успешной; поэтому терапию 988 можно прекратить на время или постоянно. Если кровяное давление 982 продолжает снижаться за счет раздражения барорецепторов, то результат такого лечения не достигнут, и его надлежит продолжить 984 и/или увеличить дозу подаваемой энергии. Другие способы раздражения комплекса барорецепторов заключаются в надавливании в области объекта с помощью рук, компрессионных баллонов и подобных им приспособлений.
На другие области автономной нервной системы также можно непосредственно воздействовать с помощью технологии, описанной в данной заявке, за счет применения энергии с одной области и передачи ее через ткань в другую область. Например, на фигуре 4a представлена система, в которой энергия, поступающая из места за пределами тела пациента на внутреннюю сонную артерию 1020, подается на часть автономной нервной системы и на комплекс сонного гломуса 1000 через внутреннюю яремную вену 1005 и в область сонного гломуса 1000 и/или блуждающего нерва 1020. Энергия абляции и энергия вибрационного или электрического раздражения может быть использована для воздействия на передачу сигналов в эти нервы и от них. Передача сигналов в этом комплексе может быть усилена, прервана и подавлена за счет чрезмерного раздражения или комбинации этих воздействий при подаче энергии (например, ультразвуковое и электрическое раздражение и т.д.).
Помимо этого или вместо этого в других осуществлениях изобретения энергию можно подать на периферийные нервы, которые обычно известны как двигательные нервы, однако в них содержатся автономные нервные волокна. К таким нервам относятся нерв подкожной вены ноги, бедренные нервы, поясничные нервы, срединные нервы, локтевые и радиальные нервы. В некоторых осуществлениях изобретения энергия подается на нервы, и воздействию подвергаются конкретные автономные нервные волокна, а не иные прочие волокна (например, двигательные или соматические чувствительные нервные волокна либо центробежные или центростремительные автономные нервы). В некоторых осуществлениях изобретения энергия, подаваемая изнутри или извне, воздействует на другие типы автономных нервных волокон. Например, на нервы, расположенные вблизи расположенной вверху брыжеечной артерии, расположенной внизу брыжеечной артерии, бедренной артерии, артерий почечной лоханки и т.д., можно особым образом воздействовать за счет подачи энергии так, чтобы внести изменения в автономные ответные реакции самих кровеносных сосудов или органов, связанных с кровеносными сосудами, и нервов, проходящих через или вдоль кровеносных сосудов к органам.
В другом осуществлении изобретения, представленном на фигуре 4a, во внутреннюю яремную вену 1005 вставляется катетер 1010, и после установки его в нужное положение энергия раздражения или абляционная энергия 1020 направляются из катетера, расположенного в венозной системе 1005, на автономные нервы, например, на блуждающий нерв и на сонный синус/гломус 1000.
В реализации аналогичного типа осуществления изобретения 1100 источник лечебной энергии 1110, установленный на катетере, может быть введен в область почечных артерий или почечных вен (фигура 4B) для раздражения или подавления почечных нервов либо почечной артерии 1105 или почечной вены 1106, осуществляемого изнутри кровеносного сосуда. Энергия передается через кровеносный сосуд (например, почечную вену) для подачи на нервы вблизи другого кровеносного сосуда (например, почечной артерии). Например, катетер, обеспечивающий подачу несфокусированной ультразвуковой энергии мощностью, изменяющейся в диапазоне от 50 мВт/см2 до 50 кВт/см2, может быть помещен в почечную артерию и в области расположения артерии или вены передавать в радиальном направлении энергию на расположенные рядом нервы. Как обсуждено ниже, диапазон мощности 500 мВт/см2-2500 Вт/см2 подходит для воспроизведения специфической нервной дисфункции с целью воздействия на уровни норепинефрина в почке, дисфункции, представляющей собой заменитель нервной функции, которая, как показано, приводит к снижениям кровяного давления с течением времени. На эту область может быть подан импульсный ультразвуковой сигнал, например, 100 серий импульсов, каждый из которых длится менее 1 секунды.
В другом осуществлении изобретения кровеносный сосуд обрабатывается светом изнутри. Инфракрасное, красное, голубое и ближнее инфракрасное излучение может быть использовано для воздействия на функцию нервов вблизи кровеносных сосудов. Например, источник света вводится в почечную артерию или в почечную вену 1105 и 1106, и свет поступает на участок вблизи кровеносных сосудов. В предпочтительном осуществлении изобретения, химический агент фотосенсибилизации используется для ускорения подавления или изменения ткани нервных узлов с помощью этого способа. Химические агенты фотосенсибилизации могут систематически использоваться для инфильтрации участка вблизи кровеносных сосудов. Затем изнутри кровеносного сосуда подается свет на участок нервов, расположенный за пределами кровеносного сосуда. Например, источник света помещается внутри почечной вены, и свет затем передается через стенку вены на адвентициальный участок вблизи стенки, активируя фотосенсибилизатор, и таким образом отделяя или подавляя нервы адвентициальной оболочки через проводящий путь апоптоза. Источник света может обеспечить свет, который заметен, или свет, который незаметен.
Лечебные процедуры, показанные на фигурах 4a-b, могут быть предоставлены в отделении неотложной помощи в том виде, в котором они предоставляются, например, в отделении интенсивной терапии или в реанимационном отделении. В таком случае терапия будет носить экстренный и периодический характер, когда источник энергии, расположенный за пределами тела пациента, и катетер, введенный внутрь пациента, будут установлены так, как показано на фигурах 4a-b. Терапия может быть использована во время стрессового состояния пациента, когда его симпатическая нервная система находится в подавленном состоянии. Когда госпитализация пациента в отделении интенсивной терапии близится к концу, катетер и устройство могут быть удалены из тела пациента. В одном осуществлении изобретения описан способ, при использовании которого катетер помещается в тело пациента для подачи энергии на участок тела, достаточный для частичного или полного подавления комплекса автономных нервов, находящихся в состоянии глубокой симпатической активации, такой как шок, сепсис, инфаркт миокарда, панкреатит и состояние после хирургической операции. После экстренно проведенного этапа имплантации, во время которого система симпатических нервов подвергается модулированию, устройство полностью удаляется из тела пациента.
На фиг.5a-b в деталях крупным планом показан глаз, симпатические нервы которого находятся вблизи задней стенки глаза. Глаукома глаз является проблемой мировой значимости. Наиболее повсеместным предписанным средством лечения глаукомы является тимоптик, который представляет собой неизбирательный (адренергический) препарат-антагонист группы β1 и β2. Подбор этого фармацевтического препарата является основной проблемой и ограничивает его эффективность в предотвращении осложнений глаукомы, основным из которых является прогрессирующая визуальная дисфункция.
Для фокусирования поступающей извне энергии можно использовать ультразвуковое устройство или другие преобразователи 7000 энергии (например, располагая их снаружи на некотором расстоянии от глаза) перед глазом или на участке позади глаза 2500 на узлах 2010 симпатических или парасимпатических нервов, все из которых должны воздействовать на уровень внутриглазного давления. Преобразователи 7000 энергии подают отделительную или почти отделительную энергию на адвентициальную оболочку кровеносных сосудов. В некоторых осуществлениях изобретения энергия не носит отделительный характер, а является вибрационной на частотах (например, 1-5 МГц) и проникает на глубину (например, от 0,5 мм до 0,5 см), достаточную для подавления функции нервов, от которых зависит величина внутриглазного давления. Для облегчения введения лекарственного препарата или для стимулирования ответных реакций лечебного типа со стороны ткани, которые способствуют ее выздоровлению, можно подать на глаз энергию меньшей мощности (например, отделительную энергию более низкого уровня).
На фигуре 5b представлено анатомическое строение нервов, которые перемещаются позади глаза 2500. В этом иллюстративном примере катетер 2000 проводится через сосудистую сеть до участка симпатических нервов, расположенного вблизи артерий 2010 глаза, и используется для отделения, «приглушения» или выполняемого другим способом модулирования центробежных и/или центростремительных нервов, проходящих через стенку сосудистой сети.
На фигуре 6 показано общее схематическое изображение почечной артерии, почечной вены, чашечно-лоханочной системы и кровеносных сосудов, отдаленных от центра на большее расстояние, и чашечно-лоханочной системы, расположенной в пределах почечной паренхимы. Отдельные нервы автономной нервной системы обычно проходят через сосудистую сеть и показаны очень близко 3000 к почечной артерии, если артерия входит в почку 3100 надлежащим образом. Ворота почки содержат сенсоры давления и химические сенсоры, которые воздействуют на входы в систему центробежных симпатических нервов через центростремительные нервы, проходящие от почки к центральной нервной системе и затем к центробежной нервной системе. Одна или несколько таких структур могут влиять на функционирование почки. На почечную вену, почечную артерию, аорту и/или на полую вену, на почечные ворота, почечную паренхиму, мозговой слой почки, корковое вещество почки и т.д. можно подать абляционную или неабляционную энергию.
В другом осуществлении изобретения для управления кровотоком или для препятствования его распространению к конкретным участкам почки в почечных чашках избирательно осуществляется изменение нервной ткани, сужение участков или установка имплантатов 3200. Такие изменения нервной ткани или имплантаты могут проводиться или размещаться на артериальной 3010 или венозной стороне 3220 почки. В некоторых осуществлениях изобретения изменения нервной ткани/имплантаты проводятся и устанавливаются таким образом, чтобы избирательно блокировать определенные части симпатических нервов в пределах почки. Изменения нервной ткани также можно позиционировать таким образом, чтобы провести абляцию участков почки, вырабатывающих такие гормоны, как ренин, который, будучи в избытке, может нанести вред пациенту. Имплантаты или сужения можно устанавливать или осуществлять в аорте 3210 или в почечной артерии 3230. Имплантаты могут быть имплантатами активного типа, постоянно воспроизводящими стимулирующую энергию или многократно и раздельно впрыскивающими дозы абляционного или ингибиторного препарата на протяжении указанного периода времени.
Почечная вена 3230, имплантаты 3220, 3200 могли бы стать причиной возрастания давления в пределах почки (позволяя кровотоку возвращаться в почку и повышать давление), что предотвратит спиралеобразное развитие описанной выше систолической сердечной недостаточности вследствие того, что почка будет реагировать так, как будто она испытывает на себе высокое давление. То есть, если давление в почке восстанавливается или искусственно поднимается за счет возросшего венозного давления, то связанная с этим ответная реакция в виде почечной гипотонии, направленная на задержку электролитов и воды в почке, более возникать не будет, и почка «ощутит» себя заполненной, и раздражение симпатических почечных нервов отключится. В одном осуществлении изобретения с помощью системы подачи катетера имплантируется создающий стеноз стент. В другом осуществлении изобретения с помощью подаваемого либо извне или изнутри тепла осуществляется стриктура 3220. Поставляемое извне тепло подается посредством прямого подогрева с помощью чрескожной процедуры (через кожный покров в область почки) или передается через кожу (например, с помощью сфокусированного ультразвукового излучения высокой интенсивности (HIFU), фокусируемого через кожу). В одном осуществлении изобретения имплантат располагается между фасцией (girota fascia) и корковым слоем почки. Имплантат может раздражать или подавлять нервы, расположенные возле почечных кровеносных сосудов, или даже возвращать фармацевтические препараты в систему подачи лекарственных средств.
На фигуре 7a с помощью системы формирования изображений, такой как устройство формирования изображений с использованием способа MRI или сканирующее устройство компьютерной томографии 4000, показана, по меньшей мере, частичная абляция почечных симпатических нервов 4400, проходящих к почке. Сканирование, осуществляемое с помощью компьютерной томографии/способа ядерного магнитного резонанса, в сочетании с работой устройства фокусирования ультразвукового сигнала (HIFU), используется для абляции симпатических нервов 4400, расположенных вблизи области почечной артерии 4500. Сканирование, осуществляемое с помощью компьютерной томографии/способа ядерного магнитного резонанса, формирует изображение 4010 и выполняет передачу данных (например, представляющих интерес областей в трехмерном представлении) в контроллер ультразвукового сигнала, который после этого направляет ультразвуковой сигнал низкой интенсивности в представляющую интерес область (50-1000 мВт/см2), оказывает тепловое воздействие (>1000 мВт/см2), образует полости или реализует комбинацию этих способов, и/или локально или систематично вводит усиливающий биоактивный агент (сонодинамическая (лекарственно-ультразвуковая) терапия). По выбору подается доплеровский ультразвуковой сигнал или другой ультразвуковой сигнал 3D/4D, и полученные после возвращения отраженного сигнала данные заносятся в систему формирования изображений с использованием способа MRI для облегчения локализации патологии. В качестве альтернативы данные, полученные после возвращения отраженного ультразвукового сигнала, применяются для непосредственного управления наведением энергии, которая используется для инициирования физиологических процессов. Формирования изображений с помощью компьютерной томографии/с использованием способа MRI не происходит. При использовании этой системы формирования изображения и отделения ткани с места ее расположения за пределами тела пациента можно лечить многие области почки, такие как внутренние почечные чашки 4350, корковый слой 4300, мозговой слой 4320, ворота 4330 и область 4340, расположенную возле аорты.
Помимо того к параметрам, которые можно изменить, относится температура, определяемая с помощью тепловой спектроскопии с использованием способа MRI или ультразвуковой термометрии/эластографии; тепловидение - это известное свойство сканеров, работающих с использованием способа MRI; данные для термической спектроскопии хранятся на изображении, полученном с использованием способа MRI, и могут быть экстраполированы на основании зарегистрированных в реальном времени данных за счет сравнения представляющих интерес областей до лечения, после лечения или во время лечения. Температурные данные, наложенные на изображение, отсканированное с использованием способа MRI, позволяет оператору установки визуализировать повышение температуры и, как следствие, локализовать место нагрева, что необходимо для обеспечения не вызывающей сомнения абляции требуемой области ткани и гарантии отсутствия попадания в эту область избыточного количества энергии. Наличие данных о температуре также дает возможность слежения за отделенной областью ткани постольку, поскольку для ее отделения нервы были нагреты до нужной температуры. Например, могут быть определены температурные данные, считанные в течение некоторого периода времени, которые затем по принципу обратной связи будут переданы оператору или в автоматизированную систему либо на само устройство подачи энергии. Сверх того, с помощью сканирования с использованием способа MRI можно определить другие спектроскопические параметры, такие как кислородное насыщение, кровоток или другие физиологические и функциональные параметры. В одном осуществлении изобретения для стимуляции и после этого для дополнительной стимуляции или подавления функции автономного нерва используется магнитное поле переменного тока (например, в отношении нервов, входящих в почку или исходящих из нее).
Эластография - это способ, при котором обнаруживаются сдвиговые волны ультразвукового излучения и их отражения. Характеристики ткани изменяются по мере ее нагревания, и происходит изменение ее свойств. На основании данных эластографии ткани может быть указана приблизительная температура, а процесс нагревания - проконтролирован.
Сканеры 4000 формирования изображений с использованием способа ядерного магнитного резонанса, как правило, состоят из магнита и высокочастотной катушки. В качестве магнита можно было бы использовать электромагнит или постоянный магнит. В качестве катушки обычно используется катушка с медным проводом, которая генерирует высокочастотное поле. В последнее время постоянные магниты использовались для создания сканеров, работающих с использованием способа ядерного магнитного резонанса, которые можно применять почти в любой установке, например, в установке частного офиса. Офисные сканеры, работающие с использованием способа MRI, позволяют быстро получать изображения в удобной обстановке врачебного кабинета, а также требуют меньшего уровня напряженности магнитного поля (менее 0,5 Тесла) и, как следствие, меньшего экранирования. Магниты меньшего уровня напряженности магнитного поля также обеспечивают получение особых преимуществ, что касается диверсификации процесса формирования изображений и получения разрешающей способности определенного свойства. Важно, чтобы сканеры на постоянных магнитах, работающие с использованием способа MRI, были устройствами открытого типа и во время сканирования не охватывали всего пациента излучением.
В одном осуществлении изобретения сканеры на постоянных магнитах, работающие с использованием способа MRI, применяются для формирования изображения представляющего интерес участка 4010 с использованием способа MRI. Сфокусированный ультразвуковой сигнал 4100 высокой интенсивности применяется для обработки представляющей интерес области 4600, идентифицированной с использованием способа MRI. В одном осуществлении изобретения устройство формирования изображений с использованием способа MRI применяется для обнаружения кровотока в пределах одного или нескольких кровеносных сосудов, таких как почечные артерии, почечные вены, расположенная выше брыжеечная артерия, вены, сонные артерии и вены, аортальные дугоподобные коронарные артерии и вены, то есть кровеносных сосудов, образующие подгруппу.
Изображение 4010 контролируется или может быть проконтролировано профессионалом системы здравоохранения для гарантии того, что на представляющую интерес область оказывается лечебное воздействие, которое будет приостановлено, если предполагаемая область не подлежит лечению. В качестве альтернативы алгоритм формирования изображений может быть автоматически инициирован тогда, когда автоматически идентифицируется представляющая интерес область (например, в результате обработки изображений), после чего последующие изображения сравниваются с первоначально выделенной и представляющей интерес областью.
При использовании устройства формирования изображений с использованием способа MRI, вероятно, наиболее важно, чтобы область, расположенная вблизи почечных артерий, могла быть легко представлена в виде изображения, как и любой другой объект, такой как глаз, мозг, простата, грудь, печень, толстая кишка, селезенка, аорта, бедро, колено, позвоночник, венозная система и поджелудочная железа. Получение изображений с помощью устройства формирования изображений с использованием способа MRI может быть применено для высокоточного фокусирования ультразвукового луча на представляющей интерес области, расположенной возле почечных артерий или в любом месте тела. В случае применения устройства формирования изображений с использованием способа MRI реальные нервы, которые надлежит подвергнуть изменению или модуляции, могут напрямую визуализироваться и стать объектом воздействия направленной энергии, подаваемой через тело из ультразвуковых преобразователей. Одним недостатком устройства формирования изображений с использованием способа MRI может быть частота выборки кадров (трудность отслеживания цели), а также стоимость внедрения устройств формирования изображений с использованием способа MRI в качестве компонента образца лечебной процедуры. В этих отношениях ультразвуковое формирование изображения предлагает намного более практичное решение.
На фигуре 7d представлен способ лечения объекта с помощью сфокусированного ультразвукового сигнала высокой интенсивности (HIFU). Выполняется формирование изображений с помощью устройства, работающего с использованием способа MRI 4520 или ультразвукового сигнала 4510 (предпочтительно с применением обоих принципов). Формирование изображений с помощью устройства, работающего с использованием способа MRI, можно применить напрямую или косвенно (например, применяя функциональное формирование изображений с помощью устройства, работающего с использованием способа MRI или по принципу спектроскопии) для визуализации симпатических нервов. Изображения, взвешенные на момент T1 или на момент T2, можно получать с помощью сканеров, работающих с использованием способа MRI. Помимо этого для формирования изображения анатомического строения объекта сканер, работающий с использованием способа MRI, также может получать температурные данные, касающиеся эффективности отделения нервной ткани в предназначенной для этого зоне, а также значения степени подогрева зоны и перечисление нагреваемых частей зон. Также могут быть добавлены другие спектроскопические параметры, такие как кровоток и даже активность нервной системы. Можно использовать ультразвуковой сигнал 4510 для добавления направления кровотока в изображение с применением для этого доплеровского формирования изображений. Спектроскопические данные могут быть дополнены изображениями таких компонентов, как частицы, химические агенты для формирования изображения или частицы, связанные с упомянутыми химическими агентами, которые впрыскиваются в пациента внутривенно или локально вблизи области расположения почечных артерий. Эти компоненты изображения могут быть визуализированы с помощью устройства формирования изображений с использованием способа MRI, ультразвукового сигнала или сканирования посредством компьютерной термографии. Ультразвуковой сигнал также может быть использован для определения информации, касающейся нагревания. Отражательная способность ультразвуковых волн изменяется по мере изменения температуры ткани. Сравнивая начальные изображения с последующими изображениями, полученными после нагревания, можно определить величину изменения температуры, которая произошла после подачи тепла.
В одном осуществлении изобретения почки обнаруживаются способом формирования изображений в поперечном сечении, таким как ядерный магнитный резонанс, ультразвуковой сигнал или сканирование посредством компьютерной томографии. Почечные артерии и вены обнаруживаются в пределах изображения, полученного посредством ядерного магнитного резонанса с применением контрастного красителя или без него. Затем данные изображения помещаются в трехмерную систему координат, которая привязана к одному или нескольким ультразвуковым преобразователям 4540 (например, к преобразователям, вырабатывающим сигнал HIFU), которые фокусируют ультразвуковой сигнал в области почечных артерий, представленной в системе 4530 координат. Система сопряжения или привязки формирования изображений к терапевтическим преобразователям выполняется посредством определения 3-мерного местоположения подлежащего лечению объекта в результате создания модели анатомического строения. Местоположения преобразователей также помещаются в трехмерную относительную систему координат. Например, преобразователи могут быть помещены в поле 4520 формирования изображения в процессе работы устройства, функционирующего с использованием способа MRI, или во время сканирования посредством компьютерной томографии таким образом, чтобы в картинки поперечного сечения попадали преобразователи. По желанию преобразователи будут содержать датчики движения, такие как электромагнитные, оптические, инерциальные датчики, микроэлектромеханические системы и акселерометры. Один или несколько таких датчиков позволят контролировать местоположение преобразователя в том случае, если, например, тело пациента перемещается относительно датчика, или оператор установки движется относительно тела пациента. При использовании датчиков движения местоположение датчиков может быть определено по движению, которое могло бы произойти во время терапии. После этого обновленная информация может быть передана обратно в ультразвуковое терапевтическое устройство по принципу обратной связи для того, чтобы изменить его положение.
В одном осуществлении изобретения описана система, в которой кровоток почечной артерии выявляется посредством обнаружения стенок артерии или почечной вены либо кровотока в почечной артерии или в почечной вене. Затем в терапевтический преобразователь, например, ультразвукового типа передается система координат кровеносных сосудов. Терапевтический преобразователь наводится на почечные кровеносные сосуды на основании информации, полученной в результате формирования изображений. Модель кровеносных сосудов отображает кровоток кровеносных сосудов и стенки кровеносных сосудов, где находятся нервы. Затем на отображенные моделью кровеносные сосуды подается энергия, предназначенная для лечения нервов, расположенных вблизи кровеносных сосудов.
В качестве альтернативы в другом осуществлении изобретения используется ультразвуковой сигнал, и полученное с помощью ультразвука изображение 4510 может напрямую коррелироваться относительно системы координат преобразователя формирования изображения. В некоторых осуществлениях изобретения терапевтический преобразователь 4540, такой же, как преобразователь формирования изображения и, следовательно, терапевтический преобразователь по определению связаны с системой 4540 координат, если известны координаты преобразователя формирования изображения. Если терапевтический преобразователь и преобразователь формирования изображения - разные устройства, то они могут связываться друг с другом на основании информации об относительном положении этих двух устройств. Представляющая интерес область (ROI) подсвечивается в процессе выполнения алгоритма программного обеспечения, ею могут быть, например, почечные артерии, почечные чашки, область мозгового слоя, кортикальный слой, почечные ворота, брюшные нервные узлы, аорта, а также любые из вен, входящие в венозную систему. В другом осуществлении изобретения на надпочечную железу, кровеносные сосуды, идущие к надпочечной железе, либо на автономные нервы, идущие к надпочечной железе, наводится сфокусированный ультразвуковой сигнал, после чего нервные ткани либо мозгового слоя почки или кортикального слоя надпочечной железы, либо нервов и артерий, ведущих к упомянутой железе, частично или полностью отделяются с помощью потока ультразвуковой энергии.
Область наведения или фокусирования ультразвукового сигнала - точка его максимальной интенсивности. В некоторых осуществлениях изобретения фокус наведения располагается в центре артерии таким образом, чтобы стенки с любой стороны получали эквивалентное количество энергии и могли нагреваться равномернее, чем тогда, когда наведение осуществляется на одну стенку кровеносного сосуда. В некоторых осуществлениях изобретения, где объектом лечения является кровеносный сосуд, кровеносный сосуд в виде артерии и артерия, расположенная рядом с веной (например, ножка почечной артерии/вены), центр фокусирования можно было установить на границе вены и артерии.
Когда после наведения на подлежащую лечению область на преобразователи 4550 подано питание, ткань 4560 нагревается, а для определения температуры ткани используется такой способ, как термография 4570, формирование изображений с использованием способа MRI или ультразвуковая термография. После этого во время оценки для обеспечения соответствующей степени позиционирования осуществляется ссылка на анатомические данные, полученные во время сканирования с использованием способа MRI или доплеровского ультразвукового сигнала, а в дополнение к этому уровень преобразования энергии оценивается повторно с помощью алгоритма 4545 моделирования, предназначенного для установки параметров преобразователей 4550 энергии. Если подлежащий лечению объект перемещается, то датчики могут быть выключены, а пациент поменяет свое положение. В качестве альтернативы датчики могут быть перенаправлены в другое место в пределах системы координат.
Абляция также может быть усилена с помощью таких агентов, как магнитные или липосомные наночастицы, которые реагируют на высокочастотное магнитное поле, генерируемое магнитом. Эти частицы могут избирательно нагреваться магнитным полем. Частицы также могут быть усовершенствованы таким образом, чтобы их можно было целевым образом вводить в конкретные органы и ткани с помощью таких компонентов нацеливания, как антитела, пептиды и т.д. Помимо подачи тепла частицы могут быть активированы для подачи лекарственных препаратов, биоактивных агентов или химических агентов, предназначенных для формирования изображения в области желательного воздействия (например, почечной артерии). Частицы можно вводить внутривенно, подкожно с помощью шприца, посредством прямой инъекции через кровеносный сосуд или подкожно иным способом. Как пример, магнитные наночастицы или микрочастицы реагируют на магнитное поле генерированием тепла в месте их нахождения. Аналогично липосомные частицы могли бы содержать металлические частицы внутри своей оболочки таким образом, чтобы магнитная частица нагревала область ткани возле липосомы, которая только предоставляет возможность точного нацеливания и биологическую совместимость.
Также можно обеспечить добавление доплеровского ультразвукового сигнала 4510. Данные почечных артерий (если почечные артерии или области вблизи этих артерий являются объектом лечения) вводятся в трехмерную систему координат 4530 согласно алгоритму программного обеспечения с учетом и без учета маркеров опорных точек измерений. Согласно алгоритму моделирования нагревания 4545 данные поступают в ультразвуковые преобразователи 4540, на которые подается питание соответствующей фазы и мощности, предназначенное для нагревания области почечной артерии под углом в пределах сектора между 40°C и 90°C и в течение временного периода, равного нескольким минутам. Местоположение в пределах трехмерной системы координат также включается в алгоритм лечения с тем, чтобы преобразователи можно было переместить в соответствующее положение. Ультразвуковые преобразователи могут работать на частотах ниже 1 мегагерца (МГц), в диапазоне 1-20 МГц либо выше 30 МГц или примерно на частоте 750 кГц, 500 кГц или 250 кГц. Преобразователи могут быть представлены в виде фазированной антенной решетки либо линейной или изогнутой формы или механически перемещаться с целью фокусирования ультразвукового сигнала на представляющий интерес объект. Помимо этого для определения реальной температуры нагреваемой ткани можно использовать MRI термографию 4570. Помимо того, эти данные можно вводить в систему для замедления или ускорения процесса абляции 4560, осуществляемого преобразователями 4550.
Кроме сфокусированного ультразвукового сигнала можно напрямую использовать ультразвуковые волны либо для подогрева области или для активации подачи фармацевтических препаратов в представляющей интерес области. Существует несколько методик повышения подачи лекарственных средств посредством сфокусированного ультразвукового сигнала. Например, частички после нагревания в магнитном поле могут выделять фармацевтическое средство. При активации липосом сфокусированным ультразвуковым сигналом те могут секретировать свою полезную загрузку. Ультразвуковые волны обладают природной способностью к фокусированию, если преобразователь размещается возле подлежащего лечению объекта, который содержит такую активируемую компоненту как биоактивное лекарственное средство или материал (например, наночастицу, чувствительную к воздействию акустических волн). К примерам сонодинамически активируемых компонентов относятся некоторые производные порфирина.
Поэтому для тестирования представляющей интерес области и проверки потенциального физиологического эффекта в виде абляции нервных тканей в этой области она может быть частично подогрета или подвергнута воздействию сфокусированного ультразвукового сигнала, который используется для «приглушения» или частичной абляции нервных тканей. После этого с целью гарантии выбора для абляции действительно правильной области можно провести такой физиологический тест, с помощью которого проверяется кровяное давление или измеряется уровень норэпинефрина в крови, почках и в кровеносных сосудах, идущих в почку и исходящих из нее. В зависимости от значения этих параметров можно провести дополнительное лечение.
С клинической точки зрения этот способ можно было бы назвать фракционированием терапии, что подчеркивает одно из главных преимуществ упомянутого способа - сравнение подачи энергии на почечные артерии извне с такой же подачей изнутри. Внутренний способ требует чрескожной инвазии и введения в почечную артерию полости трубчатого инструмента, что дорого и может привести к изменениям нервной ткани. Пациенты, вероятно, не согласятся на проведение многочисленных лечебных сеансов такого рода, потому что они носят чрезвычайно инвазивный характер и болезненны. Внешний способ во многих случаях позволяет провести менее инвазивное лечение и может быть осуществлен с низкими затратами и минимальным инвазивным воздействием технологии, описанной в данной заявке.
В другом осуществлении изобретения для разграничения представляющего интерес участка используется опорная точка измерений. Опорная точка измерений может быть внутренней (например, частью анатомического строения) или внешней (например, зафиксированной извне). Например, опорная точка измерений может соответствовать местоположению имплантата, находиться внутри организма или быть привязанной к устройству, помещенному в кровеносные сосуды, или к устройству, введенному чрескожно посредством катетеризации или с помощью другой процедуры. Опорная точка измерений также может находиться на кости, такой как ребро, или в другом внутреннем органе, например в печени. В одном осуществлении изобретения опорной точкой измерения является маячок или надувной баллон, вводимый в полость тела, либо такой баллон с маячком, которые становятся видимыми при подаче на них ультразвукового сигнала. В одном осуществлении изобретения кровоток в почечных артериях, обнаруживаемый при формировании изображений с помощью доплеровского сдвига или в B-режиме, является опорной точкой измерений, при этом его относительное направление определяется с помощью доплеровского анализа. После этого почечные артерии, а конкретно область вблизи почечных артерий, помещаются в трехмерную систему координат с применением для этого внутренних опорных точек измерения. Для отслеживания опорных точек измерений в пределах артерии или рядом с артериями можно использовать вариант в виде технологии глобальной системы навигации и определения положения. В этом осуществлении изобретения уколом в пах, в артерию или в вену вводится датчик положения. Местонахождение датчика контролируется после его размещения в кровеносном сосуде, и как результат, его положение в физическом пространстве относительно наружной части пациента, оператора и терапевтического преобразователя известно. Трехмерная система координат передается в терапевтические ультразвуковые преобразователи, и затем в пределах той же самой трехмерной системы координат выполняется привязка преобразователей к анатомическому строению тела. В этот момент из преобразователей поступает сфокусированный ультразвуковой сигнал высокой интенсивности (HIFU), вычисляющий положение преобразователей на основании информации о местоположении подлежащего лечению объекта в системе координат.
В одном осуществлении изобретения система формирования изображений создает виртуальную опорную точку измерений. Например, в случае такого кровеносного сосуда, как почечная артерия, изображение кровеносного сосуда может быть сформировано с помощью ультразвукового излучения в B-режиме. Такое изображение коррелируется с изображением кровеносного сосуда, представленным в непосредственном поперечном сечении (1705; на фигуре 17F). Когда кровеносный сосуд рассматривается в проекции такого типа, его центр можно выровнять относительно центра 1700 решетки ультразвукового излучения (например, решетки HIFU 1600), при этом преобразователи можно сфокусировать и направить на кровеносный сосуд, производя тепловые изменения 1680 нервной ткани на участках вблизи кровеносного сосуда 1705. Если преобразователи 1610 занимают разные положения вдоль окружности или полушария 1650, могут быть созданы изменяющиеся фокальные точки 1620, 1630 и 1640. Направленность преобразователей позволяет производить изменение (изменения) нервной ткани в точках 1620, 1630 и 1640, которые располагаются продольно вдоль кровеносного сосуда 1700. Таким образом, для обеспечения максимального подавления нервной функции вдоль артерии можно произвести продольное изменение нервной ткани в точках 1620-1640. В некоторых осуществлениях изобретения центр терапевтического ультразвукового преобразователя смещен относительно центра кровеносного сосуда таким образом, что энергия подается через стенку кровеносного сосуда под наклонным к нему углом.
В этом методе лечения такая артерия, как почечная, рассматривается в поперечном сечении или почти в поперечном сечении изображения, полученного с помощью ультразвука. В этом положении кровеносный сосуд большей частью параллелен оси сферического преобразователя для облегчения осуществления изменений нервной ткани. Установка ультразвуковых преобразователей 1600 была предварительно откалибрована для получения множественных изменений нервной ткани в фокальных точках 1620, 1630 и 1640 вдоль артерии, если артерия находится в поперечном сечении 1680.
В одном осуществлении изобретения опорной точкой измерений является такая внутрисосудистая опорная точка, как надувной баллон, вводимый в полость тела, или герметически запаянное передающее устройство. Упомянутый надувной баллон обнаруживается с помощью радиопередающего устройства, расположенного в его пределах и поддерживающего связь с внешними терапевтическими преобразователями. Надувной баллон может содержать три преобразователя, каждый из которых способен передавать данные о своем положении, так что изображение этого баллона может быть размещено в трехмерной системе координат. После ввода информации о надувном баллоне в ту же систему координат, где зафиксировано местоположение внешних преобразователей, использующих передающий маячок, устройства преобразования энергии могут подавать ее (например, сфокусированный ультразвуковой сигнал) на кровеносный сосуд (например, на почечные артерии) или на область вблизи кровеносных сосудов (например, на почечные нервы). Применение надувного баллона и передающих устройств также предоставляет возможность окончательного отслеживания местоположения сосудистой сети в случае ее смещения (например, почечных артерий). В другом осуществлении изобретения надувной баллон измеряет температуру или служит каналом для поступления охлаждающей жидкости, подаваемой в процессе нагревания артерии или нервов.
Подача терапевтической ультразвуковой энергии на ткань внутри тела осуществляется с помощью ультразвуковых преобразователей, которые наводятся для подачи энергии на подлежащий лечению объект, местоположение которого занесено в систему координат.
После ввода координат подлежащего лечению объекта в систему координат и инициирования подачи энергии важно сохранить наведение на местоположение такого объекта, особенно если эта цель представляет собой такую область малого размера, как симпатические нервы. В этом отношении местоположение подлежащей абляции области в трехмерной системе координат сравнивается с ее базовым местоположением, представленной в той же системе координат. Данные текущего позиционного контроля и информация вставляются в алгоритм, который определяет новое направление наведения волн энергии на подлежащий лечению объект. В одном осуществлении изобретения, когда местоположение объекта слишком удалено от его первоначального местоположения (например, пациент сместил свое положение), подача энергии приостанавливается, и пациент меняет свое положение. Если местоположение объекта не слишком отдалено от его первоначального местоположения, то преобразователи энергии можно переставить на другое место либо механическим путем (например, посредством механического перемещения) либо электрическим путем с помощью фазированной антенной решетки (например, в результате изменения относительной фазы волн, излучаемых преобразователями). В другом осуществлении изобретения многочисленные преобразователи размещаются в различных точках тела пациента, и каждый из них включается или выключается, сохраняя при этом необходимый объем подаваемой энергии. В случае размещения многочисленных преобразователей на теле пациента воздействие терапевтического ультразвукового сигнала может охватить более обширную территорию тела. Местоположения подлежащих терапии участков также служат в качестве мест формирования изображений, где будут зафиксированы внутренние и/или внешние опорные точки измерения.
В дополнение к использованию ультразвукового сигнала в качестве средства подачи энергии его также можно использовать для подачи кавитационной энергии, которая на определенных частотах может сделать возможной подачу лекарственного препарата. Кавитационная энергия также может привести к абляции ткани в фокальной точке подачи сигнала. Общая доза лекарственного препарата может быть доставлена в представляющую интерес область и в область, на которую направлены потоки кавитационной энергии или других форм энергии. К другим типам способов подачи лечебной энергии относятся чувствительные к ультразвуку пузырьки или чувствительные к ультразвуку наночастицы, присутствие которых усиливает воздействие энергии на подлежащий лечению и представляющий интерес объект.
На фигуре 7E представлены анатомическое строение 4600, почка 4620, почечные артерии 4630 и костная структура 4610, 4640, рассматриваемые со спины пациента. На Фигуре 7E представлено реальное расположение почечных артерий в системе координат так, как обрисовано на Фигуре 7D. Для формирования трехмерного представления почечной артерии, почки и межкорпусной области были объединены результаты сканирования, полученные с помощью компьютерной томографии с целью отображения поперечных сечений органов реальных пациентов. Плоскость 4623 является плоскостью, параллельной изображениям, снятым в поперечном сечении, а угол 4607 является тем углом, под которым должна быть видна расположенная под ребром почечная артерия.
На фигуре 7F с помощью ультразвука представлено изображение почечных артерий и почки 4605. С помощью этого способа формирования изображения можно визуализировать почечные ворота, включающие артерии и вену 4640. Это изображение обычно имеет такой вид, если рассматривать почку и почечную артерию в направлении и под углом, показанным на фигуре 7E. Важно, чтобы под углом 4607 на фигуре 7E на пути прохождения ультразвукового сигнала не оказалось ребра и каких-либо других важных структур.
После этого для обнаружения доступных промежутков, через которые можно было бы послать ультразвуковой сигнал в область почечных артерий 4630 из тыльной части тела пациента, была проделана пробная попытка формирования изображений с помощью ультразвука. Было обнаружено, что промежуток, указанный стрелкой 4600 и стрелкой 4605, полученный при формировании изображения в поперечном сечении с помощью ультразвука (Фигура 7F), обеспечивал оптимальные проходы для визуализации представляющего интерес поперечного сечения (почечная ножка 4640).
На фигуре 7G представлены некоторые важные данные, полученные при осуществлении попытки 4700, данные в «стандартном положении 4730». Эти данные 4720 можно использовать с целью определения конфигурации клинической системы HIFU, предназначенной для передачи ультразвукового сигнала в почечные ворота. Было определено, что почечная артерия 4635 находится в среднем на расстоянии 7-17 см от кожного покрова пациентов. Подход в виде подачи ультразвукового сигнала через боковую часть тела пациента в сторону его спины, как было отмечено, оптимален для изображения почечной артерии, которое обычно формировалось при прохождении ультразвука через паренхиму почки 4605 так, как показано на фигуре 7F. Ворота почек 4640 находятся на расстоянии приблизительно 4-8 см от ультразвукового преобразователя и расположены по отношению к нему под углом относительно оси, используемым при подходе 4637 (4607 на Фигуре 7E). Ось определяется линией, соединяющей два остистых выступа и расположенной перпендикулярно позвоночнику. Угол направления этой линии изменяется в диапазоне приблизительно от -10 до -48 градусов. Также было отмечено, что подход с использованием подачи ультразвукового сигнала от боковой части тела через почку оказался самым безопасным подходом, при котором шансы попадания ультразвука на другие органы, такие как кишечник, являются самыми минимальными.
В дополнительных экспериментах было обнаружено, что в результате позиционирования пациента в положении лежа на животе (спина вверху, живот внизу) исследуемые структуры 4750 …, то есть почечные артерии 4770 и 4780, а также ворота почки оказались даже ближе к кожному покрову, а респираторное движение артерии и почки заметно ослабело. На фигуре 7H представлены вышеупомянутые результаты 4750 и 4760, при которых почечная артерия 4770 располагается на расстоянии 6-10 см, а угол прохождения ультразвука (используемый при подходе 4790) относительно позвоночника 4607 оказался более пологим и изменяется в диапазоне от -5 до -20 градусов.
Поэтому в одном осуществлении изобретения при использовании этих клинических данных разработан способ лечения 4800 (фигура 7I) почечных нервов пациента, который заключается: 1) в идентификации ребра 4810 и подвздошного гребня 4840 пациента на его левом и правом боках 4810; 2) идентификации лево- и правосторонней почек с помощью ультразвукового сигнала 4820; 3) идентификации ворот почек и той протяженности почечных ворот, которая видна вдоль поверхности тела пациента 4820 при использовании технологии формирования изображений; 4) в идентификации кровеносных сосудов, ведущих к почке, с изображением их под одним или несколькими углами, и в создании видимого пространства 4860 вдоль поверхностной области спины пациента; 5) в определении расстояния до одной или нескольких почечных артерий, вен, почки и почечных ворот 4850; 6) опционально, в позиционировании пациента в положении на животе, при размещении устройства под спиной пациента или выше его живота 4830 для оптимизации обзора; 7) опционально, в определении требуемой мощности для получения воздействия терапевтической дозы на почечные ворота и на область вблизи почечных кровеносных сосудов с помощью моделирования; 8) в подаче лечебной энергии на почечные кровеносные сосуды; 9) опционально, в отслеживании области расположения кровеносных сосудов для обеспечения непрерывной подачи энергии в данную область так, как запланировано в процессе моделирования; 10) и опционально, в выключении подачи энергии в случае ее фокусирования за пределами запланированной области.
На фигуре 8A представлена процедура чрескожной терапии и устройство 5010, посредством которого извне осуществляется прямое воздействие на область вокруг почечной артерии 5030 через кожный покров. Может быть реализована комбинация формирования изображения и подачи энергии (например, для абляции нервной ткани) для абляции участка нервной ткани возле почечной артерии с целью лечения гипертензии, болезни почки на ее последней стадии и сердечной недостаточности. Зонд 5010 прокалывает кожу и располагается вблизи почки 5030. Наконечник зонда 5020 может содержать датчики, которые обнаруживают тепло и повышение температуры или могут усилить подачу лечебной энергии. С целью подавления симпатических нервов, расположенных вблизи почечной артерии, в эту область с помощью зонда 5010 можно подать разрушающую ионизирующую энергию, тепло или свет. Область симпатических нервов можно подвергнуть воздействию ультразвукового, высокочастотного и сверхвысокочастотного излучения, непосредственному нагреву и ввести в полость этой области надувной баллон с установленными внутри источниками тепла или подаваемой энергии. Формирование изображений может быть реализовано с помощью зонда или выполняться отдельно при нахождении зонда в области почечных кровеносных сосудов.
В одном осуществлении изобретения для локализации объекта лечения или для получения информации об уровне подаваемого тепла выполняется представленная на фигуре 8A чрезкожная процедура, сопровождающаяся формированием изображений с использованием способа MRI, компьютерной томографии или ультразвукового сигнала. В одном осуществлении изобретения выполняется подача ультразвукового сигнала, но на уровне ниже разрушающей ткани дозы. То есть, уровень энергии достаточен для изменения или подавления нервов, однако температура при этом такова, что нервы не разрушаются, а только парализуются или частично подавляются за счет подаваемой энергии. Особо предпочтительное осуществление изобретения должно заключаться в выполнении процедуры под управлением сканера, работающего с использованием способа MRI, потому что анатомическое строение подогреваемого участка может быть определено в реальном времени, а также посредством температурных карт. Как описано выше, изображения после нагревания можно сравнить с исходными изображениями, и провести сравнение величин сигналов при различных температурах.
В одном осуществлении изобретения выполняется абляция выбранных областей почки вдоль направления чрескожного доступа; например, областей, выделяющих гормоны, которые являются пагубными для пациента либо его почек или других органов. Использование энергии, подаваемой извне на пациента через его кожный покров под разными углами, предоставляет возможность наведения ее потока на любую область внутри и на поверхности почки либо вдоль почечных нервов или в область надпочечной железы, аорты или последовательности симпатических нервов. Такое большее значение охвата при подаче энергии на ряд подлежащих лечению областей оказывается возможным в результате комбинирования осуществляемого извне формирования изображений и подачи под множеством углов через кожный покров энергии, инициированной за пределами тела пациента и направленной на подлежащий лечению объект. Почечные нервы могут быть обработаны, начиная со своей исходной точки - аорты - в направлении почечной артерии, в местах расположения своих синапсов, входящих в состав брюшных нервных узлов, либо расположенных в точке их бифуркации, расположенной вдоль почечной артерии.
В дополнительном осуществлении изобретения во время подачи ультразвуковыми преобразователями энергии в подлежащую лечению область можно использовать зонд 5010 для определения температуры или перемещения в упомянутой области. Для реализации обратной связи от преобразователей HIFU можно использовать датчик движения, маячок местоположения или акселерометр. Помимо этого выбираемые по желанию температура и способ формирования изображений могут быть реализованы в пределах зонда 5010. Зонд 5010 также можно использовать для локализации местоположения в пределах лапараскопического поля с целью последующего выполнения абляции ткани нервов.
На фигуре 8B показаны внутрисосудистые устройства 5050 и 5055, через которые в область, расположенную возле почечных артерий 5065 и в их пределах, подается энергия. Внутрисосудистые устройства можно использовать для подачи энергии высокочастотного ионизирующего излучения и/или ультразвукового сигнала (либо сфокусированного или несфокусированного) на почечные артерии, расположенные вблизи участки. В дальнейшем для обнаружения области, куда подается тепло, пока внутрисосудистый катетер остается на месте, можно измерить температуру в процессе формирования изображений с использованием способа MRI или ультразвукового сигнала либо провести измерение температуры прямо на теле пациента.
В одном осуществлении изобретения устройства 5050 и 5055 (фигура 8B) подают ультразвуковую энергию, которая тормозит нервную функцию. Однако такое подавление происходит не за счет нагревания, а за счет таких механизмов, как периодические изменения давления, давление излучения, течения или потока в вязкой среде и давлений, связанных с кавитацией определяемых формированием отверстий, образующихся в жидких средах. К потоку этой энергии можно по желанию добавить тепло, но при этом не создавать температуру, которая разрушает нервы, а использовать только ту температуру, которая содействует механизму вибрации и давления. В этом осуществлении изобретения ультразвуковой сигнал не фокусируется, а исходит из источника энергии и, по существу, используется для созданий цилиндра ультразвуковых волн, которые пересекают стенку кровеносного сосуда. Промежуточный материал, который находится между ультразвуковым преобразователем и стенкой артерии, может быть подготовлен так, чтобы эффективно передавать ультразвуковой сигнал через стенку артерии на участок нервов, расположенных вблизи артерии. В другом осуществлении изобретения ультразвуковой сигнал проходит напрямую через кровь и распространяется вдоль облучаемой ультразвуком стенки для оказания воздействия на нервы. В некоторых осуществлениях изобретения через ультразвуковой катетер подается охлаждение, которое защищает внутреннюю часть кровеносного сосуда, хотя и позволяет ультразвуковому сигналу проникать через стенку сосуда в области, расположенные за пределами артерии. В такую процедуру также включен способ стабилизации ультразвукового зонда. В способе стабилизации можно было бы учитывать возможность вставки в зонд стабилизирующего компонента и компонента в составе дальномерного элемента ультразвукового сигнала с тем, чтобы оператор знал, куда подавать ультразвуковую энергию.
В этом осуществлении изобретения, где катетер устанавливают внутри почечных артерий, формирование изображений может быть выполнено извне или изнутри. Например, для визуализации изменений во время ультразвуковой модуляции нервных узлов извне можно формировать изображение с использованием способа MRI или ультразвукового сигнала. И действительно, эти способы формирования изображения могут быть использованы применительно к любому типу энергии, подаваемой на участок, в пределах стенки артерии. Например, подача высокочастотной энергии через стенку почечной артерии может быть проконтролирована с помощью аналогичных способов. Таким образом, мониторинг процедурного успеха способа зависит в большинстве случаев от самого способа.
В качестве альтернативы в другом осуществлении изобретения устройства 5050 и 5055 могут быть использованы для наведения подаваемой извне энергии (например, ультразвука) на нужное место вблизи артерии, потому что в эту область энергия подается с помощью преобразователей HIFU. Например, внутрисосудистый зонд 5050 можно использовать как приводной маячок при использовании комбинированной технологии формирования изображений/ лечения, к которой прибегают при подаче извне высокоинтенсивного сфокусированного ультразвукового сигнала.
На фигуре 8C представлена выполняемая чрескожно процедура, предназначенная для подавления почечных симпатических нервов. Зонд 5010 используется для подхода к области почечных ворот 5060 с тыльной стороны и со стороны почечной артерии 5065. Используя представленные ниже данные, зонд может быть снабжен возможностью подавать в подлежащую лечению область сфокусированные ультразвуковые сигналы высокой интенсивности. Представленные ниже данные указывают на возможность применения этого подхода постольку, поскольку ультразвуковой сигнал дает возможность быстро и легко денервировать кровеносные сосуды.
В другом осуществлении изобретения целью лечебного процесса является физиологический процесс артериального расширения (аневризмы). На Фигуре 9a ультразвуковой преобразователь 6005 располагается рядом со стенкой аневризмы 6030. Ультразвуковая энергия 6015 подается на стенку аневризмы 6030 для ее уплотнения и помимо этого для предотвращения расширения аневризмы. В некоторых осуществлениях изобретения целевым объектом является тромб, который находится в пределах аневризмы и подвергается воздействию ультразвуковой энергии с целью его разрыва или растворения. После нагрева стенки аневризмы с помощью ультразвуковой энергии до температуры между 40 и 70 градусов коллаген, эластин и прочие внеклеточные матриксы стенки по мере своего охлаждения затвердевают, в результате чего предотвращается дальнейшее расширение стенки.
В другом осуществлении изобретения в мешочек аневризмы помещается материал, а сфокусированный или несфокусированный ультразвуковой сигнал используется для отверждения или иного воздействия на материал, находящийся в мешочке, с тем, чтобы тот прилип к аорте или к тромбу, находящемуся в аневризме, и, как следствие, закрыл аневризму навсегда. Поэтому в одном осуществлении изобретения ультразвуковой катетер помещается в аорту в области стенки аневризмы или рядом с материалом в аневризматической стенке. Материал может быть изготовлен специалистом и помещен в аневризму оператором, или же вместо материала может быть тромб, присутствие которого в аневризме естественно. Ультразвуковой сигнал подается на стенку или на материал, что приводит к затвердеванию стенки или материала, усилению стенки аневризмы и предотвращению ее расширению. Энергия также может быть подана из места за пределами тела пациента или через чрескожно вставленный катетер, предназначенный для подачи энергии.
На фигуре 9b, где показан кровеносный сосуд 6000, представлено устройство предотвращения появления сгустков 6012 (фильтр полой вены), устанавливаемое в пределах кровеносного сосуда, такого как аорта или полая вена 6010. К устройству предотвращения сгустков (фильтру) 6012 подсоединяется ультразвуковой катетер 6005 с тем, чтобы удалить сгусток из этого устройства или отделить устройство 6012 от стенки кровеносного сосуда с целью его удаления из кровеносного сосуда 6000.
На фигуре 9c представлено устройство и способ, при использовании которого отделяются или частично нагреваются нервы солнечного сплетения 6020, расположенного рядом с аортой 6000. Тепло или вибрационная энергия поступают из источника ультразвуковой энергии 6005, который может подавать сфокусированные или несфокусированные звуковые волны 6007 в частотном диапазоне, изменяющемся от 20 килогерц до 5 МГц, и мощностью, изменяющейся от 1 мВт до свыше 100 кВт, при работе с фокусированием или без фокусирования сигнала. Полная или частичная абляция нервов солнечного сплетения 6020 может привести к снижению кровяного давления с помощью механизма, аналогичного подаче ультразвуковой энергии на почечные нервы. Катетер для абляции нервных тканей представляет собой катетер для передачи сфокусированного ультразвукового сигнала, однако он также может быть устройством для передачи прямого (несфокусированного) ультразвукового сигнала, преобразователем сверхвысокочастотных волн или резистивным нагревательным элементом. Энергия также может подаваться извне через кожный покров на аорту или в область солнечного сплетения.
На фигуре 10 представлен способ 6100, предназначенный для лечения пациента с помощью сфокусированного ультразвукового сигнала высокой или низкой интенсивности(HIFU или LIFU) 6260. На первом этапе 6110 выполняется сканирование способом компьютерной томографии или с помощью устройства, работающего с использованием способа MRI, и/или путем термографии и/или с помощью ультразвукового сигнала (1D, 2D и 3D). Опорная точка измерений или точка установки иного маркера на поверхности тела пациента или внутри него 6120 используется по желанию для фиксации положения и отслеживания перемещения пациента 6140. Опорная точка измерения может быть имплантированной опорной точкой измерений, временной опорной точкой измерений, расположенной внутри или снаружи на поверхности тела пациента или внутри него, или опорной точкой измерений, присущей только пациенту (например, кость, кровеносный сосуд, артериальная стенка), которую можно отобразить с помощью устройств 6110, работающих с использованием способа компьютерной томографии/MRI/ультразвукового сигнала. Помимо этого опорная точка измерений может быть временной опорной точкой измерений, такой как катетер, временно вставленный в артерию или в вену пациента, или же чрескожно вставленный катетер. Выполняется этап планирования 6130 для лечения посредством ультразвукового сигнала HIFU, во время которого определяются базовые значения параметров, таких как местоположение органа и температура; затем планируется лечение с помощью ультразвукового сигнала HIFU и применением модели (например, модели конечных элементов) для прогнозирования теплопередачи или давления для проведения теплопередачи, выполняемой ультразвуковыми преобразователями 6130. На этапе планирования учитывается информация о местоположении ткани или подлежащего лечению объекта, полученная из устройства формирования изображения 6110, и позволяется размещение анатомического строения в трехмерной системе координат так, чтобы можно было провести моделирование 6130.
Этап планирования 6130 включает определение местоположения ультразвуковых преобразователей, как и местоположение фокальной точки в теле пациента. Координаты X, Y и Z, а также максимум три угловые координаты используются для определения фокальной точки ультразвукового сигнала в пределах тела пациента с помощью устройства формирования изображений в поперечном сечении 6110. Преобразователи HIFU могли бы иметь свои собственные датчики положения, встроенные таким образом, чтобы можно было оценить их местоположение относительно подлежащего лечению объекта. В качестве альтернативы преобразователи HIFU можно жестко прикрепить к столу, на котором находится пациент, с тем, чтобы без труда получить их координаты относительно стола и пациента. На этапе планирования 6130 также можно смоделировать поток тепла с тем, чтобы, используя ультразвуковой сигнал, спланировать и спрогнозировать температуру в конкретной точке тела пациента. Например, волна давления, поступающая из преобразователя, моделируется по мере ее проникновения в ткань подлежащего лечению объекта. В наибольшей своей части ткань можно рассматривать как воду с минимальными потерями вследствие наличия поверхностей раздела. Данные моделирования дают прогноз о том, что так и будет. Относительная мощность и фаза ультразвуковой волны, подаваемой на подлежащий лечению объект, могут быть определены посредством позиционной стыковки между зондом и объектом лечения. Для моделирования теплопередачи с помощью кровотока, особенно в области артерии, добавляется элемент конвективной теплопередачи. В уравнении определения теплового потока и температуры также моделируется элемент проводящей теплопередачи.
Другой переменной, которая рассматривается на этапе планирования, является размер области отделяемой нервной ткани и погрешность ее расположения. При отделении областей малого размера, таких как нервы вблизи кровеносных сосудов, может потребоваться повышение температуры этих областей до 60-90 градусов по Цельсию с тем, чтобы провести перманентную абляцию этой области. Температуры в 40-60 градусов могут временно подавить или блокировать нервы в этих областях, и такие температуры можно использовать для определения реакции пациента на конкретный способ лечения без абляции области нервов на длительное время. После этого позже можно использовать дополнительную терапию с тем, чтобы завершить начатую работу или, вероятно, повторно провести подавление областей, содержащих нервы.
Во время проведения лечения, рассмотренного на Фигуре 10, также проводится анализ ошибок. Каждый элемент, соответствующий температуре и местоположению, содержит случайную ошибку, которая распространяется за счет использования уравнения, описывающего лечение. Для виртуального отображения температуры, наложенной на карту местоположений, выполняется моделирование ошибок. Во время лечения представляющей интерес области эта карта коррелируется с местоположением ультразвуковых преобразователей.
Во время проведения лечения 6260 пациент может двигаться. В этом случае опорные точки измерений 6120 отслеживают его перемещение, а местоположение объекта в зоне проведения лечения 6150 повторно анализируется, после чего лечение возобновляется, или же происходит перемещение преобразователей, осуществляемое либо механически или электрическим способом, в новое место фокусирования.
В другом осуществлении изобретения для создания изображения с наложениями, формируемого в комбинации с таким способом как подача ультразвукового сигнала, используется способ формирования изображений в виде поперечного сечения. Формирование изображений в виде поперечного сечения используется для создания набора трехмерных данных, описывающих анатомическое строение. Ультразвуковой сигнал, обеспечивающий получение двухмерных изображений, привязывается к трехмерному изображению устройством получения поперечного сечения за счет согласования опорных точек измерений в изображениях, полученных с помощью ультразвукового сигнала и с использованием MRI. По мере перемещения части тела в пределах ультразвукового поля определяются соответствующие данные (привязанные к) применительно к поперечному сечению (например, изображение, полученное устройством формирования изображений с использованием способа MRI), и на экране терапевтической установки можно показать такое перемещение, хранимое в наборе трехмерных данных. Ультразвуковой сигнал обеспечивает получение изображений в реальном времени и установление связи с формирователем изображений способом MRI, или же на другом изображении в поперечном сечении представлено местоположение объекта в трехмерном пространстве, установленное ультразвуковым сигналом.
На фигуре 11 представлено лечение 7410 другой болезни тела пациента, на этот раз болезнь затронула голову пациента. В результате кровотечения кровеносных сосудов в дуральном или в эпидуральном пространстве мозга, позвоночного столба и кожи черепа возникают дуральные и эпидуральные гематомы. На Фигуре 11 представлен сканер 7300, работающий с использованием компьютерной томографии или ядерного магнитного резонанса, и пациент 7400, находящийся в том же месте. В результате сканирования с использованием компьютерной томографии или ядерного магнитного резонанса получают изображение мозга 7000. Изображение используется для привязки зоны лечения 7100 к ультразвуковой антенной решетке, предназначенной для нагрева подлежащей лечению области. С помощью одного осуществления изобретения 7100 выполняется лечение субдуральной гематомы в острой или в хронической форме. В другом осуществлении изобретения 7200 выполняется лечение эпидуральной гематомы. В обоих осуществлениях изобретения для приостановки кровотечения выполняется нагрев области сочащихся капилляров и кровеносных сосудов или же в случае хронической субдуральной гематомы проводится процедура удаления жидкости из воспалившихся капилляров.
При использовании типичного осуществления изобретения для модуляции физиологических лечебных процессов выбирается пациент 7400, страдающий субдуральной или эпидуральной гематомой, а изображение предназначенной для лечения области создается посредством сканирования с применением способа компьютерной томографии или формирователя изображений с использованием способа MRI 7300. Затем следует планирование лечения, и на область, где находится застарелая эпидуральная 7200 или субдуральная 7010 гематома, для проведения такого лечения наводится преобразователь сфокусированного ультразвукового сигнала 7100. После этого представляющий интерес объект лечения привязывается к системе координат, как и ультразвуковые преобразователи. Терапия 7100 проводится после объединения излучений двух преобразователей. Для рассасывания сгустка и/или приостановления вытекания крови из капилляров, что может привести к скоплению жидкости возле мозга 7420, область гематомы нагревается сфокусированным ультразвуковым сигналом. Эту технологию можно использовать вместо просверливания или дополнительно к просверливанию отверстия, которое представляет собой проход в черепе, предназначенный для удаления жидкости.
На фигуре 12 представлен лапароскопический подход 8000 к обработке области почечной артерии, симпатические нервы 8210 которой могут быть перевязаны, прерваны или модулированы иным образом. При проведении лапароскопии брюшная полость пациента надувается, после чего в надутую брюшную полость вставляются лапароскопические инструменты. В забрюшинное пространство легко направить преобразователь с боковой стороны или (реже) через брюшинную (перитонеальную) область. С помощью лапароскопического инструмента 8200, снабженного периферическим наконечником 8220, можно подать тепло или другую форму энергии либо ввести лекарственный препарат в область симпатических нервов 8210. Лапароскопический инструмент также можно использовать для отделения или изменения нервной ткани в области солнечного сплетения 8300 и расположенных рядом нервных узлов. К лароскопическому инструменту можно подсоединить ультразвуковой преобразователь 8220, температурный зонд, преобразователь сверхвысокочастотных волн или преобразователь высокочастотных сигналов. Лапароскопию можно использовать для прямой абляции или «глушения» нервов (например, с помощью излучения более низкой частоты/меньшей мощности), расположенных вблизи кровеносных сосудов, или для отделения либо «глушения» нервных узлов, которые перемещаются вместе с кровеносными сосудами. Аналогичные типы моделирования и формирования изображений можно использовать как при чрескожном, так и при внешнем подходе к терапии почечных нервов. В результате экспериментов на животных (см. ниже) было сделано следующее открытие - на обширную область подлежащих подавлению нервов можно воздействовать одним ультразвуковым зондом в одном направлении (см. выше). Область расположения нервов не должна непосредственно соприкасаться с зондом. Вместо этого зонд может быть наведен в общем направлении области расположения нервов, после чего будет подан ультразвуковой сигнал. Например, зонд может быть установлен на одной стороне кровеносного сосуда и активирован для подачи сфокусированного или наполовину сфокусированного ультразвукового сигнала на обобщенную область, которая могла бы не содержать более 1 см продольной длины артерии, однако результат воздействия на нее достаточен для полного подавления функции нерва.
На фигуре 13 представлен алгоритм 8400 для лечения представляющей интерес области с помощью направленной энергии, подаваемой на расстоянии. Для разграничения представляющей интерес области (например, зоны абляции нервной ткани) можно использовать формирователь изображений с использованием MRI и/или компьютерной томографии и с участием визуализирующего агента 8410 или без него. После этого вблизи зоны, идентифицируемой визуализирующим агентом, можно выполнить абляцию нервов 8420 с использованием любого из вышеуказанных способов терапевтического воздействия. Этот алгоритм применим к любому из описанных выше терапевтических способов, включая подаваемый извне высокоинтенсивный сфокусированный ультразвуковой сигнал (HIFU), лапароскопические инструменты, внутрисосудистые катетеры, чрескожные катетеры и инструменты, а также любые области проведения лечения, включая почечные нервы, глаз, почки, аорту или любой из других нервов, расположенных вблизи периферийных артерий или вен. Формирование изображений 8430 с использованием компьютерной томографии, способа MRI, ультразвукового сигнала или позиционно-эмиссионной томографии можно использовать в реальном времени для визуализации изменяемой области. В тот момент времени, когда абляция места терапевтического изменения нервной ткани завершена 8440, формирование изображений с помощью визуализирующего агента 8410 (например, молекулярного фармацевтического средства или контрастного агента, такого как гадолиний) может быть выполнено еще раз. Также можно проконтролировать размер участка абляции нервных тканей за счет мониторинга температуры или контроля появления изображения зоны абляции с использованием способа формирования изображений. После завершения деструкции места терапевтического изменения 8440 процедура завершается. В некоторых осуществлениях изобретения для определения степени возрастания нагревания или развития процесса абляции представляющего интерес участка используются способы ультразвуковой диагностики, такие как эластография.
На фигуре 14 представлен процесс абляции, в котором специфические нервные волокна подвергаются тепловому воздействию при разных температурных градиентах, градиентах мощности или температурах 8500. Например, если температура определяется с помощью термометрии, выполняемой формирователем изображений с использованием способа MRI или другого способа, такого как ультразвуковая, инфракрасная термография или применение термопары, то температуру можно поддерживать на том уровне, на котором только некоторые нервные волокна подвергаются абляции или подавлению. В качестве альтернативы часть или весь нерв может быть временно отключен для последующего тестирования нисходящего воздействия отключенного нерва. Например, симпатические нервы, расположенные возле почечной артерии, могут быть отключены с помощью малого количества тепла или другой энергии (например, вибрационной энергии), после чего может быть определен эффект. Например, можно подвергнуть анализу уровни норэпинефрина в крови организма, почке или в почечной вене. В качестве альтернативы с помощью стимулирующего воздействия можно протестировать реакцию нервов после их временного отключения (например, в виде реакционной способности кожи, изменчивости кровяного давления, сердечной активности, легочной активности и сужения почечной артерии, которые проявляют себя в ответ на стимулирование почечных нервов). Например, в одном осуществлении изобретения проводится контроль активности симпатических нервов в пределах периферийного нерва; активность симпатических нервов, как правило, проявляет себя в виде пиковых потенциалов на ленте регистрации электрических сигналов, возникающих в пределах периферического нерва. Количество пиковых потенциалов коррелируется с уровнем активности симпатических нервов или гиперактивностью. Когда активность симпатических нервов снижается (например, в результате деинервации почечной артерии), концентрация пиковых потенциалов в цепочке периферийного нерва снижается, что указывает на успешно проведенную терапию симпатической или автономной нервной системы. Для подавления специфических нервных волокон без воздействия на другие нервные волокна можно использовать изменение частоты вибрации. Например, в некоторых осуществлениях изобретения происходит подавление волокон центробежного нерва, а в других осуществлениях изобретения выполняется подавление волокон центростремительного нерва. В некоторых осуществлениях изобретения выполняется временное или постоянное подавление обоих типов нервных волокон. В некоторых осуществлениях изобретения происходит избирательное блокирование волокон «С» 8520 при более низких уровнях нагревания, чем уровни нагревания нервных волокон «А». В другом осуществлении изобретения происходит избирательное лечение или блокирование волокон «В», а в некоторых осуществлениях изобретения осуществляется предпочтительное блокирование волокон «A» 8530. В некоторых осуществлениях изобретения происходит подавление всех волокон за счет «сшивания» нерва значительной порцией ультразвукового излучения 8510. Если основываться на результатах вышеприведенного эксперимента, то плотность мощности, необходимая для достижения полного блокирования нервов, могла бы составить 100-800 Вт/см2, а в случае некоторых других нервов - в диапазоне приблизительно от 500 до 2500 Вт/см2. В некоторых осуществлениях изобретения используется последовательность из 100 или более импульсов длительностью 1-2 секунды каждый (например) и подача мощности на уровне примерно от 50 Вт/см2 до 500 Вт/см2. И в самом деле, в ранее выпущенной литературе показано, что мощность на уровне 100 Вт/см2 или около этого достаточна для изменения или, по меньшей мере, для подавления нервной функции (Lele (Леле), статья «Воздействие сфокусированного ультразвукового излучения на периферический нерв и наблюдения влияния локального нагрева», журнал «Экспериментальная неврология» (Experimental Neurology), № 8, стр.47-83, 1963 год, включенная в данную заявку посредством ссылки).
На фигуре 15a представлено лечение тела позвонка 8600 или межпозвоночного диска 8610, нервы которых, расположенные в пределах 8640 или вблизи позвоночного столба 8630, обрабатываются волнами энергии 8625. В одном осуществлении изобретения обрабатываются нервы, расположенные вблизи дугоотростчатых суставов. В другом осуществлении изобретения воздействию подвергаются нервы, ведущие к дискам или к позвоночным концевым пластинкам. В другом осуществлении изобретения нервы, расположенные в пределах кости 8630 позвонка, подвергаются воздействию нагревания самой кости. Сенсорные нервы проходят через каналы 8635 в кости 8630 позвонка и могут быть подавлены или подвергнуты абляции в результате нагревания кости 8630.
На фигуре 15B крупным планом представлена область дугоотростчатого сустава. Сфокусированный ультразвуковой сигнал в этой области может подавить нервы, участвующие в возникновении спинной боли, которая зарождается в нерве заднего корешка спинного мозга и распространяется на дугоотростчатый сустав 8645. Отделение или подавление этих нервов может ослабить или даже вылечить спинную боль, возникшую в результате артропатии дугоотростчатого сустава. Сфокусированный ультразвуковой сигнал можно подать в область дугоотростчатого сустава с места, расположенного за пределами тела пациента, используя для этого обработку нерва с применение мощности на уровне 100-2500 Вт/см2 в течение промежутка времени, изменяющегося от 1 секунды до 10 минут.
На фигуре 16A представлен набор типов произведенных изменений нервной ткани, размеров и анатомических строений 8710a-f, которые приводят к деинервации различных частей разветвления симпатического нерва, расположенного возле почечной артерии. Например, произведенные изменения нервной ткани могут быть кольцеобразными, сигароподобными, иметь линейную форму, форму бублика и/или сферы; они могут размещаться рядом с почечными артериями 8705, внутри почки 8710 и/или вблизи аорты 8700. Например, разветвление почечной артерии надвое включает часть аорты 8700, почечные артерии 8705 и почки 8715. Произведенные изменения нервной ткани 8714 и 8716 относятся к разному типу и производятся вблизи аорты 8700 и сосудистой системы почек. Изменения нервной ткани 8712 и 8718 производятся на полюсных ответвлениях, исходящих из почечной артерии и ведущих к почке. Эти изменения подавляют функционирование нервов на ответвлениях главной почечной артерии. Эти изменения также можно произвести из положения за пределами тела пациента. Их также можно реализовать в форме спирали 8707 по всей длине артерии. Такие изменения нервной ткани можно произвести с помощью энергии, подаваемой из-за пределов кровеносных сосудов, используя полностью неинвазивный подход. При использовании такого подхода ультразвуковой сигнал подается сквозь кожу в область кровеносного сосуда, или же энергия может быть передана чрезкожно. Любой способ подачи энергии может быть реализован с тыльной стороны тела в направлении кровеносных сосудов так, как было обнаружено и описано выше.
Следовательно, при обращении к одному способу ультразвуковая энергия может быть подана на кровеносный сосуд, ведущий к почке, согласно модели кругового распространения тепла и ультразвука по кровеносному сосуду. В одном осуществлении изобретения энергия передается через кожный покров или через артерию в другом осуществлении изобретения. Как описано ниже, ультразвуковой сигнал передается на расстоянии и по сути легче подается на объект при использовании модели кругового распространения энергии, потому что в этом случае он распространяется не только за счет проводимости.
Ранее не было известно и не было обнаружено, являются ли изменения нервной ткани кольцеобразной формы, как показано на фигуре 16a, достаточными для блокирования нервной функции автономных нервов, расположенных вблизи кровеносных сосудов. Заявитель данной заявки обнаружил, что абляция нервной ткани в кольцеобразной форме 8710 не только блокирует нервную функцию, но, даже более того, полностью блокирует нервную функцию в области почечной артерии и почек, выполняя абляцию нервной ткани с минимальным ущербом (фигура 16C), если вообще с каким-либо ущербом в отношении самих артерий и вен. В этих экспериментах сфокусированный ультразвуковой сигнал был использован для блокирования нервов; ультразвуковой сигнал был передан через кровеносный сосуд и примыкаемые к нему сверху области (то есть только с одной стороны кровеносного сосуда) с мощностью на уровне 200-2 500 Вт/см2. На фигуре 16B показаны описанные ниже результаты моделирования. До и после подачи энергии были вычислены уровни содержания норэпинефрина в почке 8780, используемые для определения степени подавления нерва. Чем ниже уровни содержания норэпинефрина, тем больше нервов оказываются подавленными. В этих проведенных экспериментах уровни норэпинефрина приближались к нулю 8782 по сравнению с оставшимися высокими уровнями контрольных групп 8784. Фактически уровни норэпинефрина были равны или ниже чем у оголенных хирургическим путем кровеносных сосудов (хирургическое оголение означает непосредственный разрез нервов хирургическим путем). Важно, чтобы стенки почечной артерии и вены оставались, большей частью, неповрежденными; это, вероятно, происходит вследствие того, что при быстром потоке артериальной крови из стенки кровеносного сосуда удаляется тепло, и вследствие чрезвычайной эластичности основной почечной артерии из-за ее большого размера, высокого кровотока и плотной стенки. Если подытожить, то ультразвуковой (сфокусированный или относительно несфокусированный) сигнал был подан на одну сторону почечной артерии и комплекса вен. Маркеры подавления функции нервов - уровни содержания норэпинефрина внутри почки, как было установлено, приближаются к нулю после подачи на нервы энергии с одного направления и передачи ее через стенку артерии на нервы, расположенные возле артерии, которая имеет форму замкнутой кривой. Нулевой уровень норэпинефрина 8782 по сути указывает на полное отделение функции нерва, что доказывает фактическое формирование кольцеобразного участка терапевтического изменения нервной ткани в том виде, который показан на Фигуре 16A и смоделирован на фигуре 16B. Результаты гистологии также подтверждают кольцеобразный характер формирования изменений нервной ткани и ограниченное сопутствующее изменение нервной ткани в спрогнозированном за счет моделирования виде, результаты которого представлены на фигуре 16B.
Следовательно, в одном осуществлении изобретения ультразвуковой сигнал подается на артерию извне таким образом, чтобы создать кольцевое или полукольцевое «обрамление» из тепловой энергии по всей протяженности артерии для подавления, абляции или частичной абляции автономных нервов, расположенных вблизи артерии. Стенки кровеносной артерии можно использовать для наведения ультразвука на нервы, которые, если не визуализированы непосредственным образом, визуализируются за счет использования модели, предназначенной для аппроксимации местоположения нервов, установленного на основании информации о местоположении кровеносного сосуда.
На фигуре 16B далее представлены физические и физиологические принципы, описанные в данной заявке и отображающие теоретическое моделирование 8750 результатов описанного выше физического экспериментирования и опытов над животными. То есть при проведении компьютерного моделирования 8750 сфокусированный ультразвуковой сигнал был направлен на кровеносный сосуд. Почечная артерия 8755 изображена в пределах зоны нагревания, сгенерированной внутри поля сфокусированного ультразвукового сигнала. Показана температура за период менее 1 секунды (8760), через примерно 5 секунд (8765) и за более продолжительный временной интервал, превышающий 10 секунд (8767). Также отчетливо видно направление потока 8770. Овалы большего размера отображают более высокую температуру вместе с температурой по центру, превышающей 100°C. Ультразвуковое поле передается через артерию 8755, при этом вблизи артерии происходит накопление тепла так, как показано на тепловых картах 8765. Важно, что это теоретическое моделирование также демонстрирует способность ультразвука проходить через артерию и воздействовать на обе стенки кровеносного сосуда. Эти данные не противоречат вышеописанным результатам опытов над животными и формируют единый набор физических и экспериментальных данных.
По этой причине на основании результатов опытов над животными и теоретического экспериментирования доказана выполнимость использования ультразвукового сигнала для быстрого и эффективного подавления нервов, расположенных вблизи почечных артерий, ультразвукового сигнала, подаваемого из положения, внешнего по отношению к кровеносным сосудам, а также из положения, внешнего по отношению к кожному покрову пациента.
При использовании результатов описанных выше экспериментального моделирования и опытов над животными можно, что было и сделано, создать и испытать на пациентах клиническое устройство. На фигуре 17A представлено состоящее из множества преобразователей устройство 1100 подачи ультразвукового сигнала HIFU, которое осуществляет конечное терапевтическое изменение 1150 нервных тканей вдоль артерии 1140 (например, почечной артерии), ведущей к почке 1130. Терапевтическое изменение нервной ткани может иметь сферическую форму, сигарообразную форму 1150, кольцеобразную форму 8710 (фигура 16A) или форму в виде точки; однако в предпочтительном осуществлении изобретения терапевтическое изменение нервной ткани происходит вдоль артерии и имеет сигарообразную форму 1150. В предпочтительном осуществлении изобретения это терапевтическое изменение нервной ткани происходит в результате излучения ультразвуковой антенной решетки сферической или полусферической формы. Как показано на фигуре 17C, многочисленные изменения сигарообразной формы приводят к возникновению изменения нервной ткани кольцеобразной формы 1350.
На фигуре 17B представлен дисплей устройства формирования изображений, с экрана которого осуществляется контроль процесса лечения. Изменение 1155 нервной ткани 1150 аорты 1160 и почечной артерии отображается на дисплее формирователя изображений. Изображение могло бы отображать тепло, эластографию ткани, вибрации или могло бы основываться на моделировании местоположения области изменения 1150 ткани. На фигуре 17C представлен другой вид мониторинга изображения вместе с почечной артерией 1340, показанный в поперечном сечении. Изменение 1350 нервной ткани также отображено в поперечном сечении, представленном на этом изображении. В осуществлениях изобретения, предназначенных для многочисленных изменений нервной ткани, можно было бы рассмотреть такое изменение 1350 нервной ткани с целью ограничения размеров кровеносного сосуда 1340.
Для анализа и продолжения подачи терапевтического сфокусированного ультразвукового сигнала в артериальную область на фигуре 17D представлена методология 1500. Ключевым шагом, в первую очередь, является оптимальное размещение пациента 1510 для формирования изображения подлежащей лечению области; формирование изображения пациента могло бы охватывать использование доплеровского сигнала, формирование изображения в M-режиме, формирование изображения посредством сканирования «А» или даже сканирование для формирования изображения с использованием способа MRI или компьютерной томографии. Для получения координатных данных 1530 на основании изображения артерии, полученного в результате доплеровского сдвига, используется блок формирования изображения. После этого зонд сфокусированного ультразвукового сигнала 1520 позиционируется относительно изображенной области лечения 1510, после чего можно спланировать или применить лечение.
На фигуре 17E представлен путь прохождения акустических волн, подаваемых из ультразвуковой антенной решетки сферического или цилиндрического типа 1600. В некоторых осуществлениях изобретения преобразователь имеет асферическую форму, которая не поддерживает получение резкости фокусирования. Вместо этого, в сущности, реализуется более рассеянная фокусировка или фокусировка вне центральной оси. В качестве альтернативы асферичность можно было бы использовать для формирования различных продолжительностей путей прохождения ультразвукового сигнала вдоль оси фокусирования. Например, один край преобразователя ультразвукового сигнала мог бы способствовать увеличению такого пути прохождения сигнала на 15 см, тогда как другой его край - его увеличению только на 10 см. В результате чего могла бы потребоваться подача сигналов с комбинацией разностных частот или углов.
Ультразвуковые преобразователи 1610 выравниваются вдоль края цилиндра 1650, наведенного так, чтобы их сигналы пересекались в одной или нескольких фокальных точках 1620, 1630, 1640 вблизи кровеносного сосуда (например, почечной артерии). Преобразователи 1610 позиционируются вдоль цилиндра или сферы либо формы, приближающейся к сфере (асферической формы) 1650 таким образом, чтобы несколько преобразователей оказались ближе к одному или другому фокальной точкой так, чтобы создать диапазон расстояний 1620, 1630, 1640 до артерии. Пациент и артерия располагаются таким образом, чтобы их центры 1700 взаимно локализовались относительно центра ультразвуковой антенной решетки 1600. После того как центры взаимно локализованы, можно активировать энергию HIFU для проведения изменений нервной ткани по длине стенки артерии в точках 1640, 1620, 1630 на различных глубинах и в разных местах вблизи артерии. Естественное фокусирование преобразователей, расположенных вдоль цилиндра так, как представлено на фигуре 17E, приводит к продольному изменению нервной ткани, длина которого превышает его ширину или высоту. Оно пройдет по всей длине артерии 1155, когда артерия 1340 располагается вдоль центральной оси цилиндра. Если смотреть вдоль поперечного сечения (фигура 17F), то места абляции нервной ткани располагаются вдоль дискообразной поверхности 1680 рядом с кровеносным сосудом.
В другом осуществлении изобретения система перемещения преобразователей используется таким образом, чтобы те продвигались вдоль края сферы или цилиндра, к которому они прикреплены. Преобразователи могут перемещаться автоматически или полуавтоматически на основании данных сформированного изображения или положений располагаемых извне маркеров. Преобразователи управляются независимо с помощью электрических сигналов, однако соединены друг с другом механическим путем с помощью жестких структур.
Важно, чтобы во время проведения лечения терапевтическая рабочая станция 1300 (фигура 17C) позволяла видеть многочисленные изображения зоны лечения как в физическом виде, так и в виде анатомического строения 1350. Для прогнозирования глубины изменения нервной ткани и времени, необходимого для проведения такого изменения, выполняется моделирование физических параметров; эта информация в режиме обратной связи поступает на ультразвуковые преобразователи 1100. Также постоянно в системе трехмерных координат контролируется местоположение изменения нервной ткани и фокусирование преобразователя на центр 1150 таких изменений в контексте непрерывного обновления данных мониторинга 1300.
В некоторых осуществлениях изобретения отслеживание перемещения предотвращает слишком удаленный отход места изменения нервной ткани или пациента от зоны лечения во время проведения абляции ткани. Если во время проведения терапии пациент перемещается за пределы зоны лечения, то такую терапию можно приостановить. Отслеживание перемещения можно выполнить с помощью ультразвуковых преобразователей, отслеживающих положение системы отсчета или местоположение объекта, либо с помощью преобразователей, наводимых под многочисленными углами и создающих трехмерное изображение. В качестве альтернативы для отслеживания перемещений можно использовать как систему видеоизображения, так и набор указывающих перемещение акселерометров, установленных на теле пациента.
На фигуре 18 представлен микрокатетер 8810, который может быть установлен в почечные чашки 8820; этот катетер позволяет оператору осуществлять специфическое отделение или возбуждение областей ткани 8830 почки 8800. Помимо этого обеспечением дополнительной возможности в виде формирования изображения, реализуемого либо за счет оказания помощи в отслеживании перемещения или путем отражения ультразвуковых волн с целью создания или позиционирования места изменения нервной ткани, такой катетер можно использовать для реализации возможности наведения на область рядом с почечными артериями и почками. Катетер или устройство, располагаемое на конце катетера или рядом с ним, может передавать сигналы за пределы тела пациента для наведения устройства подачи энергии, которое передает ее через кожный покров. Подачей сигналов из-за пределов тела пациента можно осуществлять передачу таких видов энергии, как высокочастотная энергия, генерируемая за пределами тела пациента, или же высокочастотная энергия, подаваемая извне вовнутрь на область, расположенную рядом с катетером. Следующий патент и патентные заявки описывают подачу ультразвукового сигнала, осуществляемую в пределах кровеносного сосуда через наводящий катетер, и определенно включены посредством ссылки в данную заявку:
11/583569, 12/762938, 11/583656, 12/247969, 10/633726, 09/721526, 10/780405, 09/747310, 12/202195, 11/619996, 09/696076.
В одной системе 8800 микрокатетер 8810 устанавливается в почечные артерии и в ответвления почечных артерий почки 8820. Из катетера в почку и от пациента в систему подачи энергии поступает сигнал. На основании сгенерированного сигнала определяется местоположение катетера в трехмерной системе координат, а для подачи энергии 8830 в область, указанную микрокатетером 8810, активируется источник энергии.
В дополнительном осуществлении изобретения используется поддержание работы станции. Поддержание работы станции позволяет оператору сохранять положение внешнего устройства подачи энергии относительно перемещения оператора или перемещения пациента. Как пример, можно выполнять наведение на подлежащий лечению объект с помощью системы подачи энергии, и микрокатетер также можно использовать для размещения ограничителя потока внутри почки (например, внутри почечной вены) для «обмана» почки с тем, чтобы она реагировала так, будто ее внутреннее давление выше, чем оно могло бы быть. В этом осуществлении изобретения почка подает в центральную нервную систему сигналы на понижение выходной реакции симпатического нерва, предназначенные для подлежащих лечению органов в попытке снизить давление их кровотока.
В качестве альтернативы специфические области почки могли бы стать ответственны за выделение гормонов или за другие факторы, которые приводят к гипертензии или другим пагубным воздействиям на сердечно-сосудистую систему. Микрокатетер может генерировать ультразвуковые, высокочастотные, сверхвысокочастотные сигналы или энергию рентгеновского излучения. Микрокатетер можно использовать для абляции областей почечной вены, а также венозной области, расположенной внутри паренхимы. В некоторых осуществлениях изобретения абляция нервной ткани не требуется, однако вибрационная энергия, исходящая из зонда, используется для постоянного или временного воздействия на механорецепторы или хеморецепторы в месте расположения ворот почки.
На фигуре 19A представлена подача энергии 8900 в область почечной артерии 8910 и почки 8920 с использованием для этого физически разделенных преобразователей 8930 и 8931. Хотя показаны два преобразователя, преобразователем может быть отдельный преобразователь, который подсоединяется ко всему. Преобразователь (преобразователи) могут быть сферическими или асферическими, их можно напрямую или косвенно подсоединять к преобразователю формирования изображения, чей блок формирования изображения можно было бы вынести на расстояние от пациента.
В противоположность способу подачи энергии, представленному на фигуре 17, на фигуре 19A показана поперечная подача ультразвукового сигнала на почечные артерии без продольной подачи такого сигнала. Направление подачи энергии устанавливается с тыльной стороны пациента, потому что почечная артерия - это первый кровеносный сосуд, который «виден» при прохождении сигнала через кожу в направлении передней стороны пациента, что облегчает осуществление терапевтического воздействия. В одном осуществлении изобретения преобразователи 8930 и 8931 размещаются под ребром пациента или ниже его либо между ребрами пациента; после этого преобразователи выдают звуковую волну, распространяющуюся в направлении передней брюшной стенки, и формируют изображение области почечных артерий и почечных вен, отделяя их друг от друга. В некоторых осуществлениях изобретения такая подача энергии могла бы оказаться полезной, если, например, продольный вид артерии недостижим или желательно проведение более быстрого лечения. Преобразователи 8930 и 8931 связываются друг с другом и подсоединяются к компьютерной модели, построенной для представляющей интерес области (ROI), изображение ROI основано на сканировании с использованием способа MRI, выполняемого прямо перед началом процедуры и во время ее выполнения. Важно, чтобы преобразователи размещались с тыльной части тела пациента, представленного в поперечном сечении - в области с более прямым доступом в месте расположения почки. Угол между преобразователями формирования изображения в зависимости от оптимального местоположения пациента может быть таким низким как 3 градуса или настолько большим как 180 градусов.
В другом осуществлении изобретения формирование изображения с использованием способа MRI не выполняется, однако для получения всего или части вида в поперечном сечении, представленного на Фигуре 19A, используется ультразвуковой сигнал. Например, 8930 мог бы содержать преобразователь формирования изображения, а также источник лечебной энергии (например, ионизирующей энергии или сфокусированной ультразвуковой энергии высокой и низкой интенсивности и т.д.).
На фигуре 19B представлено сформированное с помощью ультразвука изображение, полученное посредством формирования изображения, иллюстрирующего пациента, которое отображает местоположение правильно уложенного пациента так, как показано ниже. Это именно то поперечное сечение, на которое можно оказывать лечебное воздействие посредством подачи управляемого изображением высокочастотного сфокусированного ультразвукового сигнала, предназначенного для обработки участка почечных ворот. Почка 8935 визуализируется в поперечном сечении, после чего ультразвуковой сигнал проходит через почечную артерию 8937 и почечную вену 8941. С помощью ультразвукового сигнала (в данном случае расстояние 8943 составляет 8 см) можно точно измерить расстояние 8943. Эта информация полезна для содействия моделированию подачи энергии на почечные кровеносные сосуды.
На фигуре 20 представлен альтернативный способ, система 9000 и устройство, предназначенное для абляции почечных нервов 9015 или нервов, ведущих к почечным нервам в отверстии 9010 «аорта - почечная артерия». Размещаемое внутрисосудистое устройство 9020 устанавливается в аорте 9050 и продвигается к участку почечных артерий 9025. Энергия поступает из преобразователя 9020 и фокусируется 9040(в случае использования HIFU, LIFU и ионизирующего излучения) на участке отхода почечных артерий 9025 от аорты 9050. Выполнение такой внутрисосудистой процедуры 9030 может проходить под управлением сформированных изображений с использованием способа MRI и/или термометрии MRI либо под управлением рентгеноскопии, ультразвукового сигнала или в процессе формировании изображений с использованием способа MRI. Вследствие того, что размер аорты больше, чем у почечных артерий, катетер, подающий ультразвуковой сигнал HIFU, можно разместить прямо в аорте, а также установить там охлаждающие катетеры. Помимо этого в других осуществлениях изобретения может применяться подача несфокусированного ультразвукового сигнала в аорту на участок рядом с почечным отверстием или выше. В некоторых осуществлениях изобретения применение несфокусированного ультразвукового сигнала может потребовать охлаждения окружающих зонд тканей с помощью одного или нескольких охладителей, однако, в некоторых осуществлениях изобретения кровь из аорты заменит охладитель в результате своего высокого кровотока; подача ультразвукового сигнала HIFU или сфокусированного ультразвукового сигнала может не требовать охлаждения, потому что его волны по определению сфокусированы под различными углами на область вблизи аорты. Также для подачи энергии в данную область, используемую в качестве средства-проводника для прохождения излучения от преобразователя сфокусированного ультразвукового сигнала, можно также использовать полую вену и почечные вены. В одном осуществлении изобретения осуществляется доступ к полой вене, и вибрационная энергия проходит сквозь стенки полой и почечной вены на почечные артерии, вблизи которых находятся нервы, поступающие в почку. Вены с более тонкими стенками облегчают прохождение энергии.
На фигуре 21a-b представлено глазное яблоко 9100. Также отображены малые зоны глаза 9130 (мышцы, которые управляют формой хрусталика) и ультразвуковой преобразователь 9120. Преобразователь 9120 подает сфокусированную ультразвуковую энергию на участок вблизи малых зон или в сами малые зоны для их уплотнения так, чтобы страдающий старческой дальнозоркостью пациент мог приспособить свое зрение и визуализировать расположенный вблизи объект. Аналогично на ресничные мышцы подаются тепловая или вибрационная энергия, что впоследствии приводит к возрастанию исходящего потока водянистой тканевой жидкости в представляющей интерес области и, как следствие, к невозможности возрастания внутриглазного давления до высокого уровня. Преобразователь ультразвукового сигнала 9120 также можно использовать для осуществления лекарственной терапии в области хрусталика 9150 глаза, ресничного тела, малых поясков, интравитриальной полости, передней полости 9140, задней полости и т.д.
В некоторых осуществлениях изобретения (фиг.21b) для лечения тканей, расположенных глубоко в пределах глаза, используются многочисленные преобразователи 9160; ультразвуковые преобразователи 9170 с многих направлений фокусируют свое излучение на конкретном участке глаза таким образом, что ткани, расположенные вдоль пути прохождения ультразвукового сигнала, не разрушаются в результате такого прохождения, а область фокусирования и область воздействия 9180 располагаются в том месте, где излучаемые волны встречаются с глазной поверхностью. В одном осуществлении изобретения преобразователи наводятся через плоскую часть ресничного тела глаза для обработки пятна 9180, расположенного в заднем полюсе глазного яблока 9175. Такая конфигурация могла бы сделать возможной подачу тепловой энергии, вибрационного раздражения, лекарственного препарата, перенесение генов, а также усиление терапевтического воздействия лазерного или ионизирующего излучения и т.д. В определенных осуществлениях изобретения подача ультразвукового сфокусированного сигнала не нужна, а характерные вибрационные волны передаются через глаз на частотах от 20 Гц до 10 МГц. Такую энергию можно использовать для разжижения сгустков, например, возникающих при закупорках в артериях или в венах сетчатки, которые приводят к появлению местной анемии в сетчатке. Эта энергия может быть применена в сочетании с медицинскими препаратами, используемыми конкретно для разжижения сгустков в венах сетчатки.
На фигуре 22 представлен периферический сустав 9200, обрабатываемый тепловой и/или вибрационной энергией. Ультразвуковой преобразователь 9210 излучает волны в направлении коленного сустава для блокировки нервов 9260, располагаемых сразу под надкостницей 9220, 9250 или ниже хряща. Хотя речь идет о коленном суставе, следует понимать, что подобным образом можно лечить многие суставы, включая малые суставы руки, межпозвоночные суставы, бедро, лодыжку, кисть и плечо. Для обратимого или необратимого подавления нервной функции в область сустава может быть подана сфокусированная или несфокусированная ультразвуковая энергия. Такое подавление нервной функции можно использовать для лечения артрита, послеоперационной боли, тендинита, болей, создаваемых новообразованиями, и т.д. В одном предпочтительном осуществлении изобретения можно применять вибрационную, а не тепловую энергию. Вибрационная энергия, подаваемая на суставные нервы, может подавить их функционирование таким образом, что болевые волокна окажутся в подавленном состоянии.
На фигуре 23a-b представлено смыкание фаллопиевой трубы 9300 матки 9320, осуществляемое с помощью подаваемого извне ультразвукового сигнала 9310 и предназначенное для предотвращения беременности. Способ MRI или предпочтительно ультразвуковой сигнал можно использовать в качестве способа терапевтического воздействия. Также может быть использована термометрия для представления истинного отделения зоны в реальном времени. Фаллопиева труба 9300 может быть визуализирована с помощью ультразвукового сигнала, формирования изображения с использованием способа MRI, сканирования способом компьютерной томографии или с помощью лапароскопа. После наведения на фаллопиеву трубу внешняя энергия 9310, например, ультразвук, может быть использована для закрытия фаллопиевой трубы с целью предотвращения беременности. Когда в фаллопиеву трубу подается тепло, коллаген в ее стенках нагревается и разбухает, после чего стенки соприкоснутся друг с другом и закроют фаллопиеву трубу, тем самым предотвращая полную овуляцию и, как следствие, возникновение беременности. Хотя в фаллопиевой трубе ультразвуковой сигнал отсутствует, технология визуализации и лечения аналогична той, что применяется в отношении артерии или другого канала. То есть выполняется идентификация и моделирование стенок трубы, после чего сфокусированный ультразвуковой сигнал подается через кожу на фаллопиеву трубу для переноса тепла на стенки полости трубчатого органа в виде фаллопиевой трубы.
На фигуре 23b показан способ, с помощью которого выполняется визуализация фаллопиевых труб 9340 с использованием способа MRI, сканирования посредством компьютерной томографии или ультразвукового сигнала. Сигнал HIFU 9350 подается в процессе выполнения визуализации с использованием способа MRI или ультразвукового сигнала. Так как фаллопиевы трубы нагреваются, температура коллагена в стенке также возрастает, пока стенки фаллопиевой трубы не сомкнутся. В этот момент происходит стерилизация пациентки 9360. В течение периода лечения может потребоваться определение эффективности хода нагревания. Если необходимо дополнительное тепло, то дополнительное ультразвуковое излучение HIFU можно направлять в фаллопиевы трубы до тех пор, пока стенки трубы не сомкнутся и не произойдет стерилизация пациентки 9360. Это - одно из преимуществ внешнего подхода, при использовании которого можно проводить неоднократное лечение пациента, каждое лечебное воздействие приводит к дополнительному закрытию фаллопиевых труб, затем после каждого проведенного лечения производится оценка степени его успешности. А после можно провести дополнительное лечение 9370.
В других осуществлениях изобретения ультразвуковой сигнал подается на матку или на фаллопиевы трубы с целью оказания помощи в зачатии за счет улучшения чувствительности спермы и/или яйцеклетки друг к другу. Такое усиление концепции также может быть применено к сперме или к яйцеклетке, находящейся за пределами матки, например, в пробирке, в том случае, когда речь идет о внематочном оплодотворении.
На фигуре 24 представлен алгоритм обратной связи, предназначенный для лечения нервов автономной нервной системы. Впоследствии важно получить оценку результата проведенного лечения. Поэтому в течение первого этапа проводится модуляция почечных нервов 9400 посредством одного или нескольких осуществлений обсужденного выше изобретения. Затем следует оценка 9410, определяющая степень эффекта, полученного в результате проведенного лечения; если получен полный или удовлетворительный результат 9420, то лечение завершено. Например, оценка 9410 могла бы охватывать результаты анализа, полученного с помощью микронейрографии, оценку реакционной способности сонного синуса (описана выше), изменчивость частоты сердцебиения, результат измерения уровней норэпинефрина и т.д. При удовлетворительной ответной реакции автономного нерва дальнейшее лечение могло бы не дать результатов или оказаться зависимым от уровня ответной реакции. Это может повлечь за собой дополнительные лечения нервов 9430.
На основании изображений, полученных в результате сканирования способом компьютерной томографии, на фигуре 25 представлена реконструкция анатомии пациента, показывающая положение почек 9520, если смотреть через кожный покров пациента 9500. Ребра 9510 частично закрывают почку, однако дают просвет для обозрения расположенного ниже полюса 9530 почки 9520. Анализ многих таких реконструкций привел к получению клинического образца, в котором у пациента идентифицируются ребра 9510, почечная лоханка 9420 и позвонки 9440, почки идентифицируются с помощью ультразвука, а почечные артерии - с помощью доплеровского ультразвукового сигнала.
Как показано на фигуре 26a, после идентификации ребер с помощью доплеровского ультразвукового сигнала можно направить на подлежащий лечению участок излучение от внешнего источника энергии 9600. Сфокусированный ультразвуковой сигнал (HIFU или LIFU) специально может быть подан на объект лечения после идентификации этих структур и терапевтического изменения нервной ткани кровеносных сосудов (почечной артерии и почечного нерва) 9620, ведущих к почке 9610. Как описано в данной заявке, местоположение ультразвукового преобразователя 9600 с тыльной стороны пациента оптимизировано так, как показано на фигуре 26A, то есть с учетом позвонка, ребер и подвздошного гребня, ограничивающих область подачи ультразвукового сигнала.
На основании вышеуказанных данных и, в особенности, на основании информации об анатомическом строении, полученном с помощью сканирования способом компьютерной томографии и представленной на фигуре 26A, на фигуре 26B показано устройство и система 9650, спроектированные для лечения этой области (кровеносные сосуды в воротах почки) организма пациента. В ее центре установлен ультразвуковой преобразователь 9675 на 0,5-3 МГц, предназначенный для формирования изображений, выключатель или место прикрепления ультразвуковой керамики (например, цирконата-титаната свинца), предназначенной для наведения диагностического ультразвукового сигнала. Система также содержит механизм перемещения 9660, предназначенный для управления местоположением терапевтического преобразователя 9670. Диагностическое ультразвуковое устройство 9675 подсоединено к терапевтическому устройству с помощью хорошо доработанного общеизвестного стыковочного приспособления. Такое стыковочное приспособление может быть изготовлено в виде жесткого или полужесткого соединения или же в виде электрического соединения, такого как инфракрасное устройство прямого подсоединения, оптомеханическое и/или электромеханическое соединение. Вдоль краев внешнего обода устройства могут быть установлены преобразователи меньшего размера 9670, приблизительно определяющие контуры тканей, через которые пройдет ультразвуковой сигнал. Например, простой и недорогой одномерный или двумерный преобразователь можно было бы использовать для определения местоположения тканей, через которые проходит ультразвуковой сигнал на пути к подлежащему лечению лечения объекту, его также можно использовать для наведения на объект лечения и в целях безопасности. С точки зрения безопасности такие данные важны для того, чтобы ультразвуковой сигнал не воздействовал на кость или на кишку, а преобразователь был надлежащим образом установлен для наведения на область, расположенную вблизи почечных кровеносных сосудов. Также в терапевтическую систему включена система охлаждения, предназначенная для переноса тепла из преобразователя в жидкость 9662, протекающую через систему. Охлаждение посредством такого механизма позволяет остудить ультразвуковой преобразователь, а также кожный покров, расположенный под системой. Дополнительным свойством системы является сенсорный механизм 9665, который подсоединяется к системе 9650 и регистрирует ее перемещение относительно базовой линии или ближайшей координаты. В одном осуществлении изобретения используется магнитный датчик, который может определить ориентирование системы относительно магнитного датчика системы. Датчик 9665 жестко прикреплен к механизму движения 9660 и к преобразователю формирования изображений 9675. Помимо магнитного датчика можно было бы использовать датчик, работающий по оптико-электрическому, акустическому или радиочастотному принципу.
Помимо этого поверхность 9672 преобразователя 9670 формуется так, чтобы ее можно было подогнать к участку кости, описанному и представленному на фигуре 26A. Например, поверхность преобразователя могла бы иметь эллиптическую либо асферическую форму или в некоторых случаях сферическую. Кроме всего прочего в некоторых осуществлениях изобретения инструмент формирования изображений с помощью ультразвукового сигнала не мог бы располагаться прямо в центре устройства. Фактически его можно было бы установить над центром ближе к расположенной выше границе очертания лица и ближе к ребрам, где с помощью зонда 9675 формирования изображений лучше визуализируется почечная артерия.
При наличии клинических данных, а также описанных выше разработанных технологий (например, фигура 26A-B), на фигуре 27 представлен новаторский план лечения 9700 с подачей энергии на нервы, расположенные рядом с почечной артерией, из положения, внешнего по отношению к пациенту.
В одном осуществлении изобретения пациент стабилизируется и/или позиционируется таким образом, чтобы оптимально локализовать почечную артерию и почки 9710. Диагностический ультразвуковой сигнал 9730 подается на подлежащий лечению участок, и по пожеланию ультразвуковой сигнал подается со второго направления 9715. Манипуляции, связанные с позиционированием и формированием изображения, позволяют установить местоположение почечной артерии, почечных ворот и почечной вены 9720. На участок почечных ворот можно подать тестовую дозу лечебной энергии 9740. В некоторых осуществлениях изобретения можно измерить температуру 9735. Эту тестовую дозу можно рассматривать как полную дозу лечебной энергии, если после одного или нескольких измерений лечение в самом деле окажется эффективным. Эти измерения можно было бы провести для определения кровяного давления 9770, падения выходного потока ответных сигналов симпатического нерва (как при измерении с помощью микронейрографии 9765), увеличения выходного потока ответных сигналов парасимпатического нерва, изменения диаметра кровеносного сосуда 9755 или снижения числа самопроизвольных пиковых потенциалов при проведении анализа активности с использованием микронейрографии периферического нерва (например, малоберцового нерва) 9765, или для проведении формирования изображения с использованием способа MRI или сканирования способом компьютерной томографии, которое укажет на изменения в анатомическом строении нервной системы 9760. В некоторых осуществлениях изобретения данные, снятые с почки, используются для передачи по обратной связи. Например, показатель резистивности, то есть измерение степени сужения сосудов в почке, проведенное с помощью доплеровского ультразвукового сигнала, является полезным показателем, связанным с активностью почечного нерва; например, когда проявляется более высокая автономная активность, показатель резистивности возрастает и наоборот.
Лечение 9745 можно было бы завершить, если кровяное давление достигает целевого значения 9770. Фактически этого могло бы никогда не быть или же такой результат мог быть достигнут только через несколько лет лечения. Кровяное давление могло быть постоянно высоким, и в течение нескольких лет применения концепции фракционирования дозы можно было бы многократно проводить лечение. Фракционирование является основным преимуществом подачи энергии из места, внешнего по отношению к участку, расположенному возле почечных артерий пациента, так как такая подача более удобна и менее дорогостояща по сравнению с инвазивными способами лечения, такими как имплантация стимулятора и проведение таких инвазивных процедур, как катетеризация почечной артерии.
Другим важным компонентом является определение местоположения почечной артерии, почечной вены и ворот почки 9720. Как обсуждено выше, использование подачи доплеровских ультразвуковых сигналов позволяет почти соответственно позиционировать нервы таким образом, чтобы ультразвуковой сигнал мог быть подан в общую область расположения нервов. Область расположения нервов можно увидеть на фигурах 29A-D. Фигуры 29A-C - эскизы реальных гистологических срезов. Расстояния от артериальной стенки можно увидеть с различных местоположений. Обычно они изменяются в диапазоне от 0,3 до 10 мм. Тем не менее эти изображения сняты с реальных почечных артерий и нервов и используются, чтобы разработать план лечения для системы. Например, после локализации артериальной стенки 9730 с помощью доплеровского или другого ультразвукового сигнала можно создать модель расположения нервов, после чего для подавления активности нервов 9720 в эту область будет подана энергия. Стоит отметить, что расстояние до многих из этих нервов, измеренное от стены кровеносного сосуда, указывает на вероятные значительные трудности получения доступа к большинству нервов, расположенных возле стенки кровеносного сосуда, при проведении терапии высоких частот для обработки стенки кровеносного сосуда изнутри.
На фигуре 29D представлено схематическое изображение реальной подачи ультразвука на человеческий организм. Как можно заметить, для попадания на ворота 8941 почки и на почечные кровеносные сосуды 8937 ультразвуковой сигнал проходит через кожу, подкожный жир, мускул и, по меньшей мере, частично через почку 8935. Это направление было оптимизировано с помощью клинического экспериментирования таким образом, чтобы под воздействие ультразвука не попадали структуры, которые имеют тенденцию рассеивать ультразвуковой сигнал, такие как кость и легкое. Экспериментирование привело к оптимизации этого местоположения применительно к формированию изображений и проведению терапии почечных нервов. Ультразвуковой сигнал проходит между осязаемыми опознавательными точками на кости с тыльной стороны пациента так, как описано выше и ниже. Позвонки располагаются посредине, ребра - выше, а подвздошный гребень - ниже. Важно, чтобы длина этих структур 8943 составляла приблизительно 8-12 см и не являлась препятствием с технической точки зрения. Поэтому данные изображения, полученные с помощью ультразвукового сигнала, находятся в соответствии с результатами сканирований, произведенных способом компьютерной томографии, которые также были ранее описаны.
На фигуре 29E представлена область поверхности 8760, доступная для размещения ультразвукового преобразователя для двух пациентов, участвующих в клиническом исследовании. Один пациент был тучным, в другой - более худым. Квантификация площади этой поверхности 8762 была проведена по следующей методологии: 1) сканирование, произведенное способом компьютерной томографии; 2) разметка границы органов, таких как позвонки, подвздошный гребень и ребра; 3) проведение линии от точечных кровеносных сосудов к точке вдоль края кости; 4) проведение перпендикуляра от крайней кости к поверхности кожи; и 5) отображение полученного набора точек, нанесенных вдоль границы кости. Область поверхности - это область поверхности между точками, а максимальный диаметр - это самое большое расстояние между границами кости. Набор точек, полученный с помощью этого метода, определяет границы области с тыльной стороны пациента, которая доступна воздействию ультразвукового преобразователя либо для визуализации или для лечения участка фокальной точки. В результате обследования ряда пациентов был определен диапазон изменения областей поверхности с тем, чтобы оказать помощь в проектировании преобразователя, который подойдет большинству пациентов. Преобразователи, смоделированные на фигуре 30, имеют области поверхности размером приблизительно 11×8 см или площадью 88 см2, свободно размещаемой в пределах области, показанной на Фигуре 29E поверхности 8762, которая является репрезентативной среди группы пациентов. Более того, длина или расстояние от почечной артерии до кожного покрова была квантифицирована с использованием наименьшей полупрямой 8764 и наибольшей полупрямой 8766. В сочетании с вышеприведенными угловыми данными представленные данные дают возможность спроектировать преобразователь для модулирования автономной нервной системы и контроля кровяного давления.
В отдельном исследовании показано, что эти нервы можно было подавить с помощью подаваемого извне ультразвукового сигнала, чьи параметры и устройства для передачи описаны в данной заявке. Анализ патологии показал, что нервы, расположенные возле артерии, были полностью подавлены и переродились, подтверждая тем самым способность данного плана лечения подавить упомянутые нервы и в конечном итоге лечить такие болезни как гипертензия. Кроме того, использование этих параметров не приводит к какому-либо изменению тканей на пути прохождения ультразвукового сигнала через почку и почечные ворота.
Также важно открытие, сделанное с помощью клинических испытаний, которое заключается в том, что при использовании ультразвука в качестве подаваемой извне энергии центрирование диагностического ультразвукового зонда, направленное на визуализацию поперечного сечения почки и кровеносных сосудов, является важным компонентом подачи терапевтического воздействия в надлежащее место вдоль кровеносных сосудов. Одним из первых этапов алгоритма 9700 является стабилизация положения пациента в стабилизирующем устройстве заказного типа, сконструированном для подачи энергии в область почечных артерий. После стабилизации положения пациента в область 9730 подается диагностический ультразвуковой сигнал для определения длины ребер, позвонков и местоположения почечной лоханки. Прощупывание опознавательных точек также позволяет определить границы представляющей интерес зоны, которая подлежит лечению. После этого с тем, чтобы избежать воздействия на кость, в пределах этих областей размещается внешняя ультразвуковая система. Тогда в результате обеспечения подачи части внешней энергии через почку (например, использование ультразвукового сигнала для визуализации), вероятность ее воздействия на кишечник полностью исключается. На фигуре 29D представлено полученное с помощью ультразвукового сигнала изображение участка мягкой ткани, начиная с места за пределами тела пациента и вплоть до почечных ворот внутри пациента. Расстояние составляет приблизительно 8-16 см. После позиционирования пациента под него подкладывается подушка 9815. В одном осуществлении изобретения подушка 9815 - просто способ создания опоры для спины пациента. В другом осуществлении изобретения подушка 9815 представляет собой растягиваемое устройство, растягивание которого подстраивается под каждого индивидуального пациента. Растягиваемый компонент 9815 позволяет сжать забрюшинное пространство (где находится почка) с целью замедления движения или успокоения почки и сохранения ее положения для организации лечения с помощью источника энергии или ультразвукового сигнала.
Тестовую дозу энергии 9740 можно подать в область ворот почки или почечной артерии и в результате получить температурное изображение 9735, достичь сужения кровеносных сосудов 9755, построить диаграмму проведенного сканирования при использовании компьютерной томографии 9760 и сформировать микронейрографическую накладку 9765 или «электрод» при использовании микронейрографии и даже повлиять на кровяное давление 9770. После этого лечение 9745 может быть завершено. Его завершения можно было бы ждать минуты, часы, дни или годы в зависимости от величины измеряемого параметра.
В результате экспериментов было определено, что область почечных ворот и почек можно стабилизировать, используя силу тяжести при местном приложении усилия на участок брюшной полости ниже ребер, но выше почечной лоханки. Например, на фигурах 28A-C представлены примеры устройств позиционирования пациентов, предназначенных для лечения области почечных кровеносных сосудов.
На фигуре 28A представлен пример размещения пациента, когда ультразвуковое диагностическое и терапевтическое оборудование 9820 установлено под пациентом. Устройство позиционирования 9810 имеет форму наклоняемой кровати. Подъемник пациента 9815, который располагается под пациентом, проталкивает участок его тела, где расположены почечные ворота, ближе к кожному покрову, этот участок может проталкиваться вперед таким же самым образом, как определено при проведении клинических испытаний, при таком типе расположения почечная артерия оказывается примерно на 2-3 см ближе к поверхности тела. Для пациентов, обследованных в рамках клинических испытаний при использовании этого типа приспособления, диапазон изменения расстояний составляет приблизительно 7-15 см. Вес пациентов позволяет выполнить некоторую стабилизацию дыхательного движения, которая, так или иначе, наступит; подъемник пациента может быть установлен с одной или другой стороны в зависимости от подлежащего лечению участка тела.
На фигуре 28B показана более подробная конфигурация формирования изображения с помощью ультразвука и терапевтический инструмент 9820. Устройство сопряжения с пациентом 9815 используется для плавного перехода ультразвуковых волн, излучаемых генератором, через кожный покров в направлении подлежащих лечению почек. Устройство сопряжения регулируется таким образом, что его можно подстроить под каждого пациента.
На фигуре 28C представлено другое осуществление устройства позиционирования 9850, на этот раз пациент должен лежать лицом вниз. В этом осуществлении изобретения пациент устраивается лицом вниз, расположившись лежа над подъемником 9815. И вновь посредством экспериментирования в клинических условиях было определено, что если пациент лежит лицом вниз, а устройство позиционирования установлено под пациентом, то почечные ворота подталкиваются к спине пациента, а почечная артерия и вена вытягиваются, что позволяет им стать более заметными для воздействия ультразвуком и доступными для поглощения энергии, подаваемой в эту область. Расположение устройства позиционирования под пациентом могло бы растянуть мочевой пузырь на одно или несколько отделений, что позволит отрегулировать величину давления, подаваемого на нижнюю сторону туловища пациента. Устройство позиционирования также могло быть оборудовано раздвижной спинной опорой 9825 для надавливания на тыльную сторону пациента в направлении передней растягиваемой части позиционирующего устройства посредством чего произошло бы сжатие растянутых почечных кровеносных сосудов для того, чтобы облегчить применение устройства подачи энергии, которая не будет проникать глубоко в ткани. Эти данные можно увидеть на фигурах 7G и 7H, где почечная артерия на самом деле располагается немного ближе к кожному покрову (от 7-17 см и до 6-10 см). На фигуре 28C отображено положение устройств подачи энергии с левой стороны пациента 9827 и с правой стороны пациента 9828. Ребра 9829 определяют границы верхней области установки устройства, а подвздошный гребень 9831 - границы нижней области установки устройства. Остистые отростки 9832 определяют границы срединного края области возможной установки устройства, а участок 9828 между ними и является местом установки терапевтического преобразователя.
Подъем лежака выполняется спереди пациента за счет направленного вверх толчка в направлении почечных ворот и почек. Передняя часть лежака может быть опущена или приподнята таким образом, чтобы позволить пациенту принимать специальные позы. Приподнятая часть лежака может содержать надувную конструкцию, которая оказывает регулируемое механическое давление на одну или другую часть туловища пациента, на его голову или таз.
На фигурах 29A-C представлена анатомическая основа 9900 описанного в данной заявке подхода к наведению лечебной энергии. Представленные на фигурах анатомические структуры получены непосредственно из гистологических срезов. Нервы 9910 можно увидеть в месте, расположенном рядом с почечной артерией 9920. Диапазон изменения радиального расстояния от артерии достигает 2 мм и даже 10 мм. Корреляция анатомического строения с результатами моделирования, представленными на фигуре 16B, указывает на возможность наведения лечебной энергии и подтверждает правильность подхода, основанного на фактической патологии, то есть подхода в виде оказания терапевтического воздействия на почечные нервы за счет наведения источника лечебной энергии на адвентициальную оболочку артерии. Это имеет большое значение, потому что методология, используемая для наведения лечебной энергии на нервы, является основанной на обнаружении отраженного от артерии доплеровского сигнала и на последующем наведении излучения лечебной энергии на стенку кровеносного сосуда возле места отражения вышеупомянутого доплеровского сигнала. Нервы 9910 можно увидеть вблизи почечной артерии 9920, что непосредственно подвергает их воздействию температурного поля, показанного на фигуре 16B, и тем самым указывает на возможность применения изложенного в общих чертах подхода, представленного на фигуре 27, и на возможность создания конфигурации из мест изменений нервной ткани, представленных на фигуре 16A. В дальнейшем экспериментирование (использование аналогичных типов патологии, а также уровней норэпинефрина в почке) показывает, что необходимая доза ультразвукового излучения, предназначенного для подачи в подлежащую лечению область с целью воздействия на изменения нервной ткани, составляет порядка 100 Вт/см2, если требуется частичное подавление нервов, и порядка 1-2 кВт/см2, если требуется полное подавление и некроз нервов. Значения этих доз или доз в диапазоне между указанными значениями можно было бы выбирать в зависимости от необходимой степени подавления нервов, желательной для выполнения плана лечения. Важно то, что далее за счет экспериментирования была обнаружена достаточность акустической плоскости, проходящей через кровеносные сосуды, для частичного или полного подавления нервов в подлежащей лечению области. То есть плоскость, через которую кровеносные сосуды проходят в перпендикулярном направлении, достаточна для абляции близлежащих к артерии нервов так, как показано на фигуре 16B. До завершения данного экспериментирования не было доказательств того, что ультразвуковое излучение окажется способным подавить близлежащие к артерии нервы за счет ориентации плоскости ультразвукового излучения в направлении, проходящем через кровеносный сосуд. И действительно было доказано, что плоскость прохождения ультразвукового излучения по сути могла бы подавлять нервы, располагаемые по окружности возле кровеносного сосуда.
На фигурах 30A-I представлены результаты моделирования в трехмерной системе координат, проведенного на основании набора сканирований, полученных с помощью компьютерной томографии при создании модели пациента, показанной на фигуре 26A. Цифровые моделирования были проведены в трех измерениях с использованием реального анатомического строения человека, полученного на основании сканирований способом компьютерной томографии. Для моделирования теоретического лечения участка почечной артерии, принимая во внимание анатомическое строение реального пациента, были использованы те же самые сканирования компьютерной томографии, которые были использованы для получения фигур 7E, 19 и 25. При использовании доз излучения для вышеуказанного экспериментирования (фигуры 29A-D) в сочетании с анатомическим строением пациента, полученным на основании сканирований способом компьютерной томографии, результаты этих моделирований указывают на то, что существует возможность подачи терапевтического ультразвукового излучения на почечные ворота извне по отношению к телу пациента. В сочетании с изображением на фигуре 29, как объяснено, представлено размещение нервов вблизи кровеносных сосудов, а также показано расположение кровеносных сосудов, находящихся под воздействием ультразвукового излучения. На фигурах 30A-I показана возможность установки ультразвукового преобразователя, который конфигурируется для подачи требуемой энергии в область ворот почки без нанесения вреда подвергшимся воздействию излучения органам. Результаты этих моделирований фактически подтверждают правильность концепции такой терапии и содержат информацию, полученную на основании исследования патологии, сканирований человеческого организма с помощью компьютерной томографии, сканирований человеческого организма с помощью ультразвукового сигнала, а также данные о ранее и выше представленных конструкциях системы.
В одном осуществлении изобретения, представленном на Фигуре 30A, максимальная интенсивность достигается в фокальной точке 10010 и приблизительно составляет 186 Вт/см2 при использовании преобразователя конструкции 10000, работающего с частотой 750 МГц; размер преобразователя составляет приблизительно 11×8 см, а его центральная часть 10050 предназначена для установки инструмента ультразвукового формирования изображений. Мощность, подаваемая на вход преобразователя, составляет приблизительно 120-150 Вт в зависимости от специфического анатомического строения пациента.
На фигурах 30B и 30C на глубине приблизительно 9-11 см в двух измерениях показаны фокальные точки 10020 и 10030. Важно, чтобы область (такие ткани как у почки, мочеточника, кожного покрова и мышцы), которая располагается ближе всего (10040 и 10041) к фокальным точкам 10020 и 10030, не отличалась каким-либо значительным поглощением акустической энергии. Это свидетельствует о безопасной подачи лечебной энергии в область почечной артерии через эти ткани так, как описано выше. Важно, чтобы ткани, подвергнутые воздействию излучения, не были повреждены во время проведения этого моделирования, что стало бы свидетельством осуществимости такого образа лечения.
На фигурах 30D-F представлено моделирование, когда преобразователь 10055 работает на частоте приблизительно в 1 МГц. На такой частоте размер фокальных точек 10070, 10040 и 10050 оказывается немного меньше (приблизительно 2 см на 0,5 см), а максимальная мощность в таких фокальных точках оказалась выше той, что показана на фигурах 30A-C, и составила приблизительно 400 Вт/см2. При моделировании человеческого организма такой показатель близок к оптимальной ответной реакции и определяет проектные параметры для расположенных извне устройств. Преобразователем этой конструкции является преобразователь прямоугольной формы (сферической формы со срезанными краями), созданный для того, чтобы оптимизировать рабочее пространство между задними ребрами и расположенной выше частью подвздошного гребня пациента. Его размер, составляющий приблизительно 11 см × 8 см, как описано выше и ниже, позволяет такому преобразователю свободно размещаться в пространстве между опознавательными точками костной системы спины пациента.
На фигурах 30G-I представлены результаты моделирования с использованием тех же переменных ультразвукового сигнала, показанных на фигурах 30D-F. Различие заключается в том, что преобразователь 10090 имел сферическую форму с центральной прорезью, а не прямоугольную форму с центральной прорезью. Установка сферического преобразователя 10090 позволяет создать более высокую концентрацию энергии в фокальной точке 1075 в результате увеличения площади поверхности, на которую подается вибрационная энергия. И действительно, максимальная энергия, поступающая из этого преобразователя (фигура 30G), составляет приблизительно 744 Вт/см2, тогда как максимальная интенсивность энергии преобразователя, показанного на фигуре 30d, составляет приблизительно 370 Вт/см2. На фигуре 30H представлена одна плоскость модели, а на фигуре 30I - ее другая плоскость. Фокальные точки 10080 и 10085 показаны в пределах подлежащих воздействию участков 10082 и 10083, свободных от воздействия акустической мощности и генерирования тепловой энергии, и аналогичны тем, что показаны на фигуре 30A-F.
Результаты этих моделирований подтверждают осуществимость лечения почечных симпатических нервов извне без повреждения подвергающихся воздействию излучения тканей или структур, таких как кости, кишечник и легкие. Лечение гипертензии является одним из клинических применений данной терапии. Преобразователь, оборудованный установленным внутри него блоком формирования изображений, используется для подачи сфокусированного ультразвукового сигнала на почечный нерв, расположенный вблизи почечной артерии. Эта терапия воздействует как на центростремительные, так и на центробежные нервы.
Возможны и другие конфигурации преобразователей. Хотя отдельный терапевтический преобразователь показан на фигурах 30A-I, возможно использование таких конфигураций, как терапевтические преобразователи, оборудованные фазированной антенной решеткой (установка более чем одного независимо управляемого терапевтического преобразователя). Такие преобразователи позволяют более точно подогнать подачу ультразвуковой энергии под индивидуального пациента. Например, преобразователь большей мощности можно было бы использовать вместе с 2, 3, 4 или большим чем 4 количеством преобразователей. Индивидуальные преобразователи можно было бы включать или выключать в зависимости от анатомического строения пациентов. Например, преобразователь, излучение которого должно охватывать ребро индивидуального пациента, можно было бы выключить во время проведения терапии.
Хотя на фигурах 30A-I центральное пространство показано в центре преобразователя, преобразователь формирования изображений можно было бы установить в любом месте в пределах поля излучения и держать его там до тех пор, пока его положение относительно терапевтических преобразователей остается хорошо известным. Например, в той степени, в какой терапевтический преобразователь подсоединен к преобразователю формирования изображений в трехмерном пространстве, причем параметры такого соединения всегда остаются известными, преобразователь формирования изображений может быть ориентирован в любом направлении относительно местоположения терапевтического преобразователя.
Реферат
Изобретение относится к системам передачи энергии на расстояние. Система подачи энергии в организм пациента включает источник энергии для подачи ультразвуковой энергии в расположенную по окружности область вблизи кровеносного сосуда пациента, при этом расположенное по окружности сплетение нервов находится в указанной области. Источник энергии выполнен с возможностью использования кровеносного сосуда в качестве опорной точки для направления энергии на нервы, окружающие кровеносный сосуд, и подачи ультразвуковой энергии для создания кольцеобразной зоны ингибирования нерва вокруг кровеносного сосуда, при этом кольцеобразная зона расположена вдоль длины кровеносного сосуда. Использование изобретения позволяет более эффективно подавать энергию к цели. 21 з.п. ф-лы, 30 ил.
Формула
источник энергии, сконфигурированный для подачи ультразвуковой энергии в расположенную по окружности область вблизи кровеносного сосуда пациента, при этом расположенное по окружности сплетение нервов находится в расположенной по окружности области;
при этом источник энергии выполнен с возможностью использования кровеносного сосуда в качестве опорной точки для направления энергии на нервы, окружающие кровеносный сосуд; и
источник энергии сконфигурирован для подачи ультразвуковой энергии для создания кольцеобразной зоны ингибирования нерва вокруг кровеносного сосуда, при этом кольцеобразная зона расположена вдоль длины кровеносного сосуда.
приема входного сигнала с информацией, касающейся местоположения почечной артерии;
определения выходного сигнала с информацией, касающейся местоположения почечного нерва, основанного на модели, связывающей местоположение артерии с местоположением нерва; и
обеспечения подачи выходного сигнала в систему позиционирования источника энергии для обеспечения возможности системе позиционирования предписывать источнику энергии подавать ультразвуковую энергию из-за пределов тела пациента на почечный нерв для лечения почечного нерва.
опорную точку измерений для ее установления внутри кровеносного сосуда;
устройство обнаружения, предназначенное для обнаружения опорной точки измерений внутри кровеносного сосуда;
процессор, сконфигурированный для определения трехмерной координаты обнаруженной опорной точки измерений и для направленной подачи ультразвуковой энергии в область, расположенную рядом с кровеносным сосудом.

Комментарии