Улучшенный способ калибровки системы слежения за катетером, использующей медицинские данные отображения - RU2434579C2
Код документа: RU2434579C2
Чертежи
Описание
Изобретение относится к способу улучшения калибровки и слежения за катетерами при кардиологическом вмешательстве с использованием предварительно полученных медицинских данных изображения.
В современном здравоохранении представлены медицинские диагностические и изображающие системы. Такие системы являются неоценимыми инструментами для определения, диагностики и лечения физических состояний и значительно уменьшают необходимость в хирургических диагностических вмешательствах. Во многих случаях окончательная диагностика и лечение проводятся только после того, как лечащий врач или рентгенолог дополнили общепринятые исследования подробным изображением соответствующих областей и тканей посредством одной или более методик изображения.
Увеличение использования минимально инвазивных хирургических методик в медицинской диагностике и терапии требует нового способа дистанционного размещения катетеров и слежения за катетерами или другими медицинскими инструментами внутри человеческого тела или тела животного. В настоящий момент рентгеновское флюороскопическое изображение представляет собой стандартную методику слежения за катетерами. Однако чрезмерное воздействие рентгеновского излучения может быть вредно и для врача, и для пациента. Следовательно, необходимы альтернативные способы слежения за катетерами.
Опубликованы некоторые альтернативные способы, включающие способы, которые используют ультразвуковые преобразователи и преобразователи, в которых используют измерения магнитного поля.
Один известный способ катетерной локализации использует один или более источников магнитного поля, которые фиксированы один относительно другого и определяют систему пространственных ориентиров, и один или более магнитных датчиков, закрепленных на наконечнике катетера. Датчики измеряют поля, создаваемые источниками, и данные измерения затем используют для определения расположения наконечника относительно пространственных ориентиров. Такой же результат может быть достигнут посредством источников, замененных датчиками, и датчиками, замененными источниками.
Описанная методика основана на точном предварительном изучении взаимного расположения источников и пространственных форм указанных магнитных полей и взаимного расположения и чувствительности датчиков. Так как невозможно изготавливать источники и датчики с идеальными свойствами, исключительно теоретические вычисления таких свойств вероятно неверны, и значит, они должны быть определены калибровкой. Одно преимущество использования магнитных полей для отслеживания катетера внутри тела человека или животного представляет собой то, что поля практически не испытывают влияния со стороны тела. Указанное является следствием очень низкой магнитной восприимчивости тканей тела. В отличие от описанного электрические или акустические поля значительно изменяются тканями тела. В результате калибровочные измерения следящей системы, основанной на магнитном поле, могут быть выполнены вне тела, до операции.
Ограничивающее условие для катетеров представляет собой то, что они должны быть достаточно маленькими в диаметре и достаточно гибкими для введения в соответствующую часть тела. Например, диаметры кардиальных катетеров должны быть приблизительно 2 мм, и гибкость их должна быть достаточной для изгибания до радиуса 10 мм и менее. Перечисленные условия и необходимость жестко закреплять датчики, установленные на катетерах, закрывать верхнюю часть катетера требуют того, что указанные датчики должны размещаться в маленьком объеме.
На сегодняшний день системы слежения за катетерами, основанные на электрическом поле, такие как NavX (ESI, St. Jude) и Localisa system (Medtronic), или следящие системы, основанные на времени прохождения ультразвука, базируются на допущении однородности и линейности электромагнитных полей или равномерности распределения скорости звука в средостении во время калибровки и процессов сбора данных. Однако пространственное распределение электрической проводимости и акустических характеристик в человеческой грудной клетке изменяется в зависимости от анатомии пациента и динамических воздействий, таких как дыхание. Следовательно, внутригрудные электромагнитные и акустические поля не являются гомогенными и линейными, приводя к большим неточностям во время слежения за катетером. В настоящий момент такие следящие устройства используют только в анатомических структурах, в которых электромагнитные и акустические поля приблизительно гомогенны, такие как кровь, содержащаяся в камерах сердца. Простые линейные способы калибровки использованы для выполнения слежения за катетером в зависимости от измерения или электрического поля или времени прохождения ультразвука в организме посредством элетромагнитных или ультразвуковых датчиков на катетере. Указанные методики еще не применялись успешно в других анатомических структурах, таких как коронарные вены, в которых неоднородное и нелинейное поле исключает достоверное слежение современными методиками калибровки с использованием линейного поля.
Системы слежения за катетерами и калибровочные системы описаны в Патенте США 5697377, опубликованном 16 декабря 1997; Патентных Заявках США 20050080328, опубликованной 14 апреля 2005; 20060058643, опубликованной 16 марта 2006; и 20050197568, опубликованной 8 сентября 2005; Патенте США 6226547, опубликованном 1 мая 2001; Международной публикации номер WO 2005/048841, опубликованной 2 июня 2005; и в опубликованной статье «A System for Real-Time XMR Guided Cardiovascular Intervention», K.S.Rhode et al., IEEE Trans. Medical Imaging, 24, (11), Nov 2005, стр.1428-1440.
Однако проблема с данными методиками еще существует. На сегодняшний день системы слежения за катетерами, основанные на электрическом поле, такие как NavX (ESI, St.Jude) и Localisa system (Medtronic) базируются на допущении однородности и линейности электрических полей во время калибровки и процессов сбора данных. Однако электрическая проводимость внутри человеческого организма, особенно в грудной клетке, изменяется в зависимости от специфики анатомии пациента и других динамических влияний, таких как акт дыхания. Электрическое поле, таким образом, не гомогенное и нелинейное, что приводит к значительным ошибкам во время слежения за катетерами. Также основанное на ультразвуке определение местоположения предполагает равномерность скорости звука в пределах ткани. Неоднородное распределение скорости звука в грудной клетке искажает определяемое ультразвуком местоположение и измерение ориентации, приводя к погрешностям локализации в пределах объема.
В соответствии с настоящим изобретением предложен новый подход, который использует специфичные для пациента данные отображения, полученные MDCT или MR для сегментации главных медиастинальных структур и построения многомерных электропроводных или акустических моделей, которые могут быть затем использованы для подсчета электрического или акустического поля для улучшения процесса калибровки и слежения за катетерами.
Задача настоящего изобретения - создать способ улучшения калибровки и слежения за электромагнитным или акустическим катетером в пределах области слежения за катетером с целью использования при кардиологическом вмешательстве для отдельного пациента, включающий: получение до или во время вмешательства блока данных изображения, относящихся к сердцу, для измеряемой области пациента посредством медицинского сканирующего устройства; сегментацию данных изображения в соответствии с областью тканей для получения медицинских изображений каждой области тканей; получение электромагнитных или акустических данных каждой области тканей; обработку электромагнитных или акустических данных для построения электромагнитной или акустической модели для одной или более сегментированных областей тканей, включающих в себя моделируемое пространство, соответствующее измеряемой области пациента и области слежения за катетером; в котором модель указывает одну или более областей искажения сигнала в пределах области слежения за катетером, что повышает точность данных; приведение в соответствие моделируемого пространства с пространством слежения за катетерами; оценку поведения катетера при слежении во время вмешательства и, с помощью ссылки на модель определение ошибок слежения за катетером вследствие влияний, искажающих сигнал; и коррекцию положения катетера во время слежения для минимизации влияний, искажающих сигнал.
Другой задачей является создание способа, в котором получение до вмешательства блока данных изображения, относящихся к сердечной деятельности, дополнительно включает: получение до вмешательства блока данных изображения, относящихся к сердечной деятельности, используя по меньшей мере одну СТ систему, MR систему, ультразвуковую систему, 3D флюороскопическую систему и PET систему.
Другой задачей является создание способа, в котором область тела дополнительно включает: по меньшей мере, одну из кардиальных вен, кардиальных артерий или аорту.
Другой задачей является создание способа, в котором обработка электромагнитных данных для создания электромагнитной модели дополнительно включает: обработку электромагнитных данных для создания 4D модели с использованием электропроводности.
Еще одной задачей является создание способа, в котором обработка акустических данных для создания акустической модели дополнительно включает в себя: обработку акустических данных для создания 3D модели с использованием скорости звука.
Еще одной задачей является создание способа, в котором приведение в соответствие моделируемого пространства с пространством слежения за катетером включает в себя: приведение в соответствие моделируемого пространства с пространством слежения за катетером, используя электромагнитные или акустические видимые поверхностные маркеры, прикрепленные к пациенту в пределах моделируемого пространства, причем положение каждого поверхностного маркера соответствует расположению базовых участков, расположенных в отмеченных положениях в пространстве слежения за катетером во время калибровки или слежения за катетером.
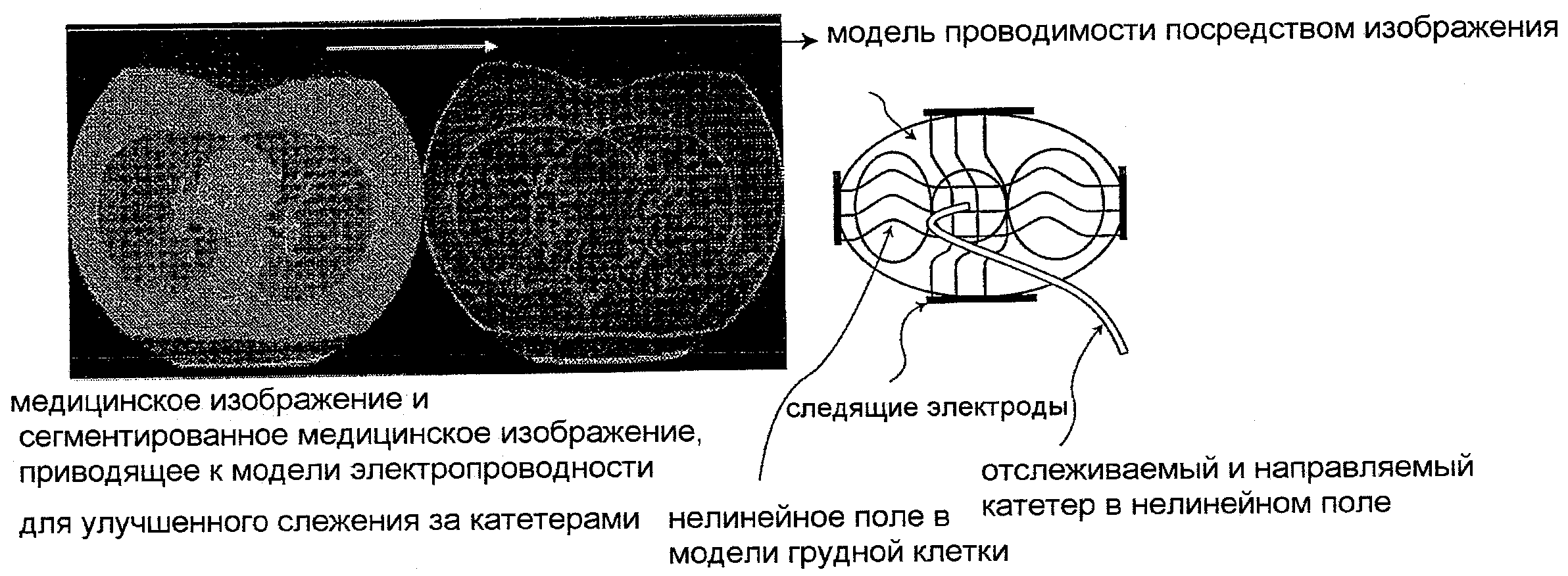
Перечисленные и другие аспекты изобретения изложены более подробно посредством ссылок на нижеуказанные варианты осуществления и ссылкой на чертеж, который иллюстрирует медицинское изображение и сегментированное медицинское изображение, приводящее к модели проводимости для улучшенного слежения за катетером.
Сердечно-сосудистые катетерные вмешательства традиционно выполняют направлением катетера под рентгеновским контролем. Такой тип направления обладает некоторыми недостатками. Во-первых, так как изображения созданы двухмерными (т.е. 2D), необходимо несколько картинок под разными углами для реконструкции трехмерного (т.е. 3D) изображения объекта, который отображают с характерными неточностями, появляющимися при визуализации 3D сегмента катетера. Во-вторых, рентген неточно улавливает изображения областей мягких тканей, таких как сердце и кровеносные сосуды. В-третьих, при рентгеновском изображении оператор и пациент подвергаются дозам радиации, которые с течением времени могут вызвать значительные проблемы со здоровьем.
На сегодняшний день системы слежения за катетерами, основанные на электрическом поле, такие как NavX (ESI, St.Jude) и Localisa system (Medtronic), базируются на допущении однородности и линейности электрических полей во время калибровки и процессов сбора данных. Однако электрическая проводимость внутри человеческого организма, особенно в грудной клетке, изменяется в зависимости от специфики анатомии пациента и других динамических влияний, таких как акт дыхания. Таким образом, электрическое поле является негомогенным и нелинейным, что приводит к значительным ошибкам во время слежения за катетерами. Таким же образом, основанное на ультразвуке определение местоположения предполагает равномерность скорости звука в пределах ткани. Неоднородное распределение скорости звука в грудной клетке искажает определяемое ультразвуком местоположение и оценки ориентации, приводя к погрешностям позиционирования в пределах объема.
В соответствие с предшествующим уровнем техники системы, такие как St. NavX, основаны на слежении за катетером в электромагнитном поле. Таким образом, 3 ортогональные поля накладывают на пациента с помощью поверхностных электродов, как описано, например, в Патенте США 5697377 Wittkampf. Так как сопротивление в организме изменяется (легкие, различные типы тканей и т.д.) электрическое поле в организме резко нелинейно. Следящий катетер может быть точно ориентирован для соответствующих положений, но точное измерение не может быть выполнено. В результате математические модели анатомических структур, созданные через облака точек отслеживаемого катетера, искажены. Также слежение могут выполнять в некоторых анатомических областях, таких как камеры сердца. В таком случае результаты слежения в кровеносных сосудах или артериях скомпрометированы большими погрешностями вследствие неоднородности среды и выраженного искажения поля.
В настоящем изобретении представлен новаторский подход, который использует данные изображения, специфичные для пациента из MDCT или MR для сегментации основных медиастинальных образований и построения многомерных моделей проводимости или акустических моделей, которые затем могут быть использованы для вычисления электрических или акустических полей с целью улучшения процесса калибровки и слежения за катетером.
В настоящем изобретении данные изображения могут быть использованы для выполнения операции, обратной свертке такого нелинейного пространства и для выполнения более точного слежения, реализуемого также в других анатомических областях, таких как кровеносные сосуды. В клинических технологических процессах данные изображения могут быть получены, например, в начале вмешательства, такие данные соотносят с обычными сопротивлениями тела и в дальнейшем используют для коррекции области слежения за катетерами. Если изображение во время вмешательства доступно, искажения могут быть скорректированы в соответствии с такими данными. Дооперативные данные могут быть получены такими методиками, как CT/MRI/рентген/US соответствующими установками для сбора таких кардиологических данных.
Настоящее изобретение предлагает использовать предварительно полученные, многомерные, специфические для пациента данные, полученные применением MRI или СТ, 3D флюороскопической системы или PET системы для построения моделей электропроводности или скорости звука для улучшения калибровки катетерных следящих систем. Модели электропроводности уже используют в области электроимпедансной томографии. Достоверное слежение в областях с быстрым изменением свойств электромагнитного или акустического полей, таких как сердечные вены и артерии, аорта и т.д., может стать возможным, используя улучшенную стратегию калибровки и слежения, основанную на использовании таких специфических для пациента моделей. Динамические влияния, такие как дыхание (изменения объема легких приводят к анатомическим изменениям и к связанным с ними изменениям проводимости и распространении звука), могут быть учтены для использования четырехмерной модели грудной клетки, полученной на основе медицинских данных изображения.
Многомерные модели электропроводности или скорости звука, например грудной клетки, получены на основе медицинских данных изображения, как показано на чертеже. Указанные данные использованы для предсказания электромагнитного и акустического полей в пределах интересующей анатомической области. Калибровка системы слежения за катетерами, основанной на электромагнитном и акустическом полях, улучшена, используя описанные, специфические для пациента модели, и слежение может быть выполнено более достоверно в областях с искажением поля вследствие быстрого изменения анатомического строения и свойств ткани. Движение пациента может быть учтено для уменьшения ошибок слежения.
Хотя настоящее изобретение описано касательно его специфических вариантов осуществления, специалистом в данной области может быть обнаружено множество модификаций, улучшений и/или изменений, которые могут быть достигнуты в объеме настоящего изобретения. Таким образом, очевидно, что изобретение ограничено только формулой изобретения.
Реферат
Изобретения относятся к области медицины. Способ включает получение до или во время вмешательства блока данных изображения для измеряемого пространства конкретного пациента посредством медицинского сканирующего устройства; сегментацию данных изображения в соответствии с областями тканей для создания медицинского изображения каждой области ткани из областей тканей; получение электромагнитных или акустических данных для каждой области ткани; обработку электромагнитных или акустических данных для создания электромагнитной или акустической модели для одной или более областей тканей, перекрывающей моделируемое пространство, соответствующей измеряемой области конкретного пациента и области слежения за катетером. При этом модель используют для прогнозирования электромагнитного или акустического поля в пределах областей тканей; приведения в соответствие моделируемого пространства с пространством слежения за катетером; измерения электромагнитного или акустического поля катетера во время вмешательства для ссылки на прогнозируемое электромагнитное или акустическое поле модели для определения ошибок слежения за катетером; и коррекции положения катетера во время слежения для минимизации ошибок слежения за катетером. Применение изобретений позволит улучшить слежение за катетером. 2 н. и 6 з.п.ф-лы, 1 ил.

Комментарии