Двухфазная волна дефибриллятора с регулируемым относительным спадом вершины импульса второй фазы - RU2539626C2
Код документа: RU2539626C2
Чертежи



Описание
Настоящее изобретение относится к дефибрилляторам для реанимации пациентов с неожиданной остановкой сердечной деятельности и, в частности, к дефибрилляторам, которые формируют двухфазные электрошоковые волны.
Внезапная сердечная смерть является основной причиной смертей в США. Общей причиной внезапной сердечной смерти является фибрилляция желудочков, когда мышечные волокна сердца сжимаются нескоординировано. Данная недостаточно скоординированная активность миокарда приводит к потере способности сердца к эффективному прокачиванию крови, что прерывает нормальный ток крови в тело. Единственным эффективным лечением при фибрилляции желудочков является электрическая дефибрилляция, которая состоит в приложении электрического шока к сердцу пациента. Сильный дефибрилляционный шок прерывает всю электрическую активность сердца. Затем автономная нервная система организма автоматически восстанавливает приложение скоординированной электрической пульсации сердца.
Для повышения эффективности дефибрилляционный шок следует давать пациенту в течение нескольких минут после наступления фибрилляции желудочков. Исследования показали, что дефибрилляционные шоки, применяемые в течение одной минуты после того, как начинается фибрилляция желудочков, обеспечивают коэффициент выживаемости до 100%. Коэффициент выживаемости снижается приблизительно до 30%, если до применения шока проходит 6 минут. По истечении 12 минут, коэффициент выживаемости достигает нуля.
Один из способов подведения быстрых дефибрилляционных шоков заключается в применении имплантируемых дефибрилляторов. Имплантируемые дефибрилляторы хирургически имплантируют пациентам, для которых высока вероятность потребности в электротерапии в будущем. Имплантируемые дефибрилляторы обычно контролируют сердечную активность пациента и автоматически подают электротерапевтические импульсы непосредственно к сердцу пациента, когда показано. Следовательно, имплантируемые дефибрилляторы позволяют пациенту, в известной степени, нормально действовать в то время, как дефибриллятор непрерывно контролирует активность сердца. Однако имплантируемые дефибрилляторы дорого стоят и применяются лишь небольшой частью от всей группы людей, подвергающейся риску внезапной сердечной смерти.
Внешние дефибрилляторы посылают электрические импульсы к сердцу пациента посредством электродов, наложенных на тело пациента. Внешние дефибрилляторы полезны в отделении неотложной помощи, операционной, автомобилях скорой медицинской помощи или других обстоятельствах, в которых может возникать неожиданная потребность в обеспечении электротерапии пациента в кратчайший срок. Преимущество внешних дефибрилляторов состоит в том, что данные дефибрилляторы можно использовать на пациенте, при необходимости, затем снимать для применения с другим пациентом. Недостаток в сравнении с имплантируемыми дефибрилляторами состоит в том, что внешний дефибриллятор должен быть способен оказывать эффективное лечебное воздействие на любого пациента, с которым его применяют. Поскольку имплантируемый дефибриллятор применяют с конкретным пациентом, то рабочие характеристики дефибриллятора регулируют для обеспечения конкретной электротерапии индивидуально для конкретного пациента. Рабочие параметры, например, амплитуды электрических импульсов и подаваемую полную энергию можно эффективно измерять и настраивать соответственно физиологии конкретного пациента для оптимизации эффективности дефибриллятора. Например, начальное напряжение, продолжительность первой фазы и общую продолжительность импульса можно устанавливать перед имплантацией устройства для подачи требуемого количества энергии или для обеспечения требуемых начальной и конечной разностей потенциалов (например, постоянный относительный спад вершины импульса). Даже когда имплантированный дефибриллятор способен изменять свои рабочие параметры для компенсации изменений импеданса отведений дефибриллятора и/или сердца пациента (как поясняется в нижеприведенном патенте Фейна (Fain)), диапазон возможных изменений импеданса при одной имплантации пациенту сравнительно невелик. Такие параметры, как импеданс пациента, можно измерить во время имплантации и настройки волны дефибриллятора соответственно характеристикам конкретного пациента.
Для сравнения, внешний дефибриллятор должен быть выполнен с возможностью работы в полном диапазоне характеристик пациентов, существующих у пациентов, с которыми может быть применен дефибриллятор. Так как электроды внешнего дефибриллятора не находятся в непосредственном контакте с сердцем пациента, и так как внешние дефибрилляторы должны обладать способностью применения с множеством разных пациентов, имеющих разнообразные физиологические различия, то внешние дефибрилляторы должны работать в соответствии с такими параметрами амплитуды и продолжительности импульсов, которые будут эффективны для большинства пациентов, независимо от физиологии пациента. Например, импеданс, создаваемый тканью между электродами внешнего дефибриллятора и сердцем пациента, изменяется от пациента к пациенту, что изменяет интенсивность и форму волны шока, подводимого к сердцу пациента при данных амплитуде и продолжительности первоначального импульса. Амплитуды и продолжительности импульсов, эффективные для лечения пациентов с низким импедансом, не обязательно обеспечивают эффективные и энергосберегающие лечебные воздействия на пациентов с высоким импедансом. Соответственно, торакальный импеданс пациента обычно измеряется дефибриллятором в процессе терапии, и волна импульса динамически регулируется, как поясняется в патентах США 5803927 (Cameron и др.) и 5749904 (Gliner и др.)
Волны дефибриллятора, т.е. графики временной зависимости подаваемых импульсов тока или напряжения, характеризуются в соответствии с формой, полярностью, продолжительностью и числом фаз импульса. Большинство современных дефибрилляторов, внутренних и внешних, используют некоторую форму укорачивания экспоненциальных двухфазных волн. Примеры двухфазных имплантируемых дефибрилляторов можно найти в патенте США № 4821723 изобретателей Baker, Jr., и др.; патенте США № 5083562 изобретателей de Coriolis и др.; патенте США № 4800883 изобретателя Winstrom; патенте США № 4850357 изобретателя Bach, Jr.; патенте США № 4953551 изобретателей Mehra и др.; и патенте США № 5230336 изобретателей Fain и др.
Один известный в технике способ решения проблемы разнообразия пациентов состоит в создании внешнего дефибриллятора с несколькими параметрами настройки энергии, которые могут быть выбраны пользователем. Общий протокол для применения данного дефибриллятора заключается в попытке дефибрилляции с начальным параметром настройки энергии, подходящим для дефибрилляции пациента со средним импедансом, и затем в повышении параметра настройки энергии для последующих попыток дефибрилляции в случае, если начальный параметр настройки не обеспечил реанимации пациента. Повторные попытки дефибрилляции требуют дополнительной энергии и повышают риск для пациента. Другой способ, как указано выше, заключается в измерении импеданса пациента во время терапии или параметра, зависимого от импеданса пациента, и в изменении формы последующего дефибрилляционного шока на основании ранее выполненного измерения. Например, имплантированный дефибриллятор, описанный в патенте Фейна (Fain), подает дефибрилляционный шок предварительно заданной формы к сердцу пациента в ответ на обнаруженную аритмию. Устройство Фейна измеряет импеданс системы во время приложения данного шока и использует измеренный импеданс для изменения формы следующего прикладываемого шока. Вариант данного метода описан в статье R. E. Kerber, и др., «Energy, current, and success in defibrillation and cardioversion: clinical studies using an automated impedance-based method of energy adjustment», Circulation том 77, стр. 1038-46 (Май 1988). В данной статье авторы дают описание внешнего дефибриллятора, который подает тестовый импульс в пациента перед приложением дефибрилляционного шока. Тестовый импульс используют для измерения импеданса пациента перед приложением шока. Затем дефибриллятор регулирует количество энергии, подаваемой шоком, в ответ на измеренный импеданс пациента. Форма подаваемой волны по Керберу с соавторами (Kerber et al.) является затухающей синусоидой.
Хотя импеданс пациента имеет большое значение и может быть измерен дефибриллятором во время терапии, другой важной характеристикой пациента является реакция клеточной мембраны миокарда пациента на электротерапию. Хотя известно, что электрический шок будет прерывать фибрилляционную электрическую активность, точное физиологическое объяснение данного феномена остается предметом предположений. Одна из гипотез предполагает, что начальный высокоэнергетический шок прекращает электрическую активность миокардиальных клеток посредством сильного электрического тока в направлении полярности шока. Преимущества двухфазной волны, которые содержат более эффективную дефибрилляцию и меньшее число вредных последействий, предполагаются обусловленными обратной полярностью второй фазы волны шока. Полагают, что упомянутое обращение тока в течение второй фазы ослабляет остаточные результаты воздействия начального шока и стабилизируют ткань посредством снятия остаточных зарядов в миокардиальных клетках. Предполагается, что миокардиальные клетки являются более чувствительными к автономному восстановлению правильной электрической пульсации, если результаты воздействия начального дефибрилляционного шока полностью устраняются так, чтобы они не препятствовали упомянутому восстановлению нормальной электрической активности. Приведенная гипотеза приводит к требованию знания точной реакции миокардиальных клеток пациента на электрошок. Хотя реакцию миокардиальных клеток измеряли в процессе клинических исследований, данную клеточную реакцию до настоящего времени еще не удавалось измерять во время терапии. Таким образом, в большинстве дефибрилляторов принимается среднее значение клеточной реакции, которое выводят из измеренных значений упомянутых исследований. Подобное применение предполагаемого среднего значения оставляет желать лучшего. Разброс клеточных реакций относительно среднего значения, в общем, мало известен, и характеристики клеточной реакции конкретного пациента сложно прогнозировать или определять. Соответственно, для внешнего дефибриллятора желательно планировать волну импульса, которая безопасна и эффективна для пациентов с разными диапазонами импедансов пациента и разными реакциями миокардиальных клеток.
В соответствии с принципами настоящего изобретения предлагается внешний дефибриллятор, который обеспечивает двухфазный дефибрилляционный импульс с различными регулируемыми параметрами. Упомянутые параметры включают в себя энергию, подлежащую подаче, начальное напряжение и ток, продолжительность фазы, продолжительность импульса и относительный спад вершины импульса, включая переменный относительный спад вершины импульса фазы 2. Переменный относительный спад вершины импульса второй фазы обеспечивается управляемым пропусканием мимо пациента какой-то части импульсного тока в течение второй фазы, что регулирует относительный спад вершины импульса второй фазы двухфазной волны. Настоящее изобретение может быть реализовано дефибриллятором с одной емкостью. На чертежах:
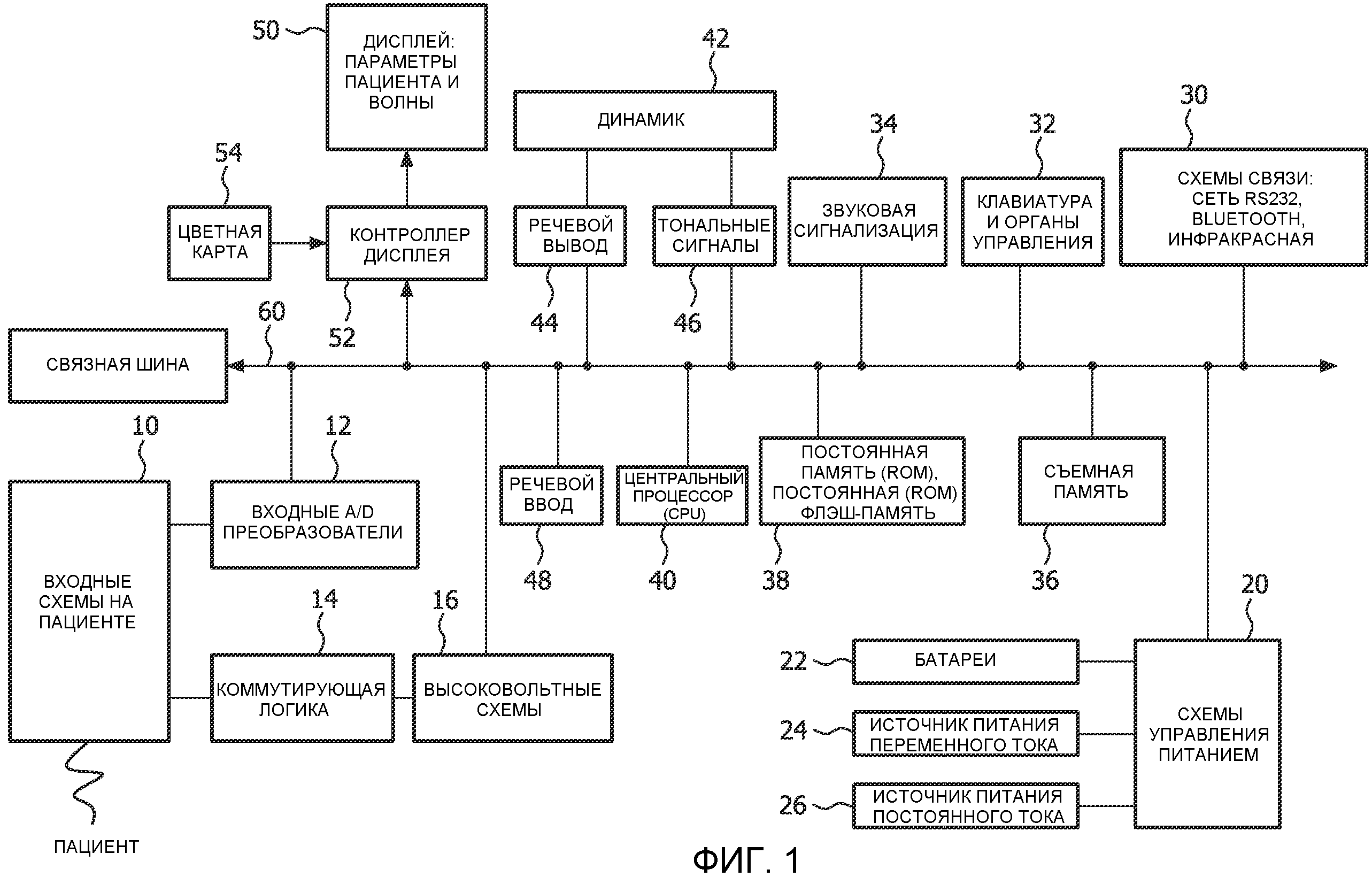
Фиг.1 - блок-схема внешнего дефибриллятора, созданного в соответствии с принципами настоящего изобретения;
Фиг.2a и 2b - двухфазные волны с характеристиками большого и небольшого относительного спада вершины импульса;
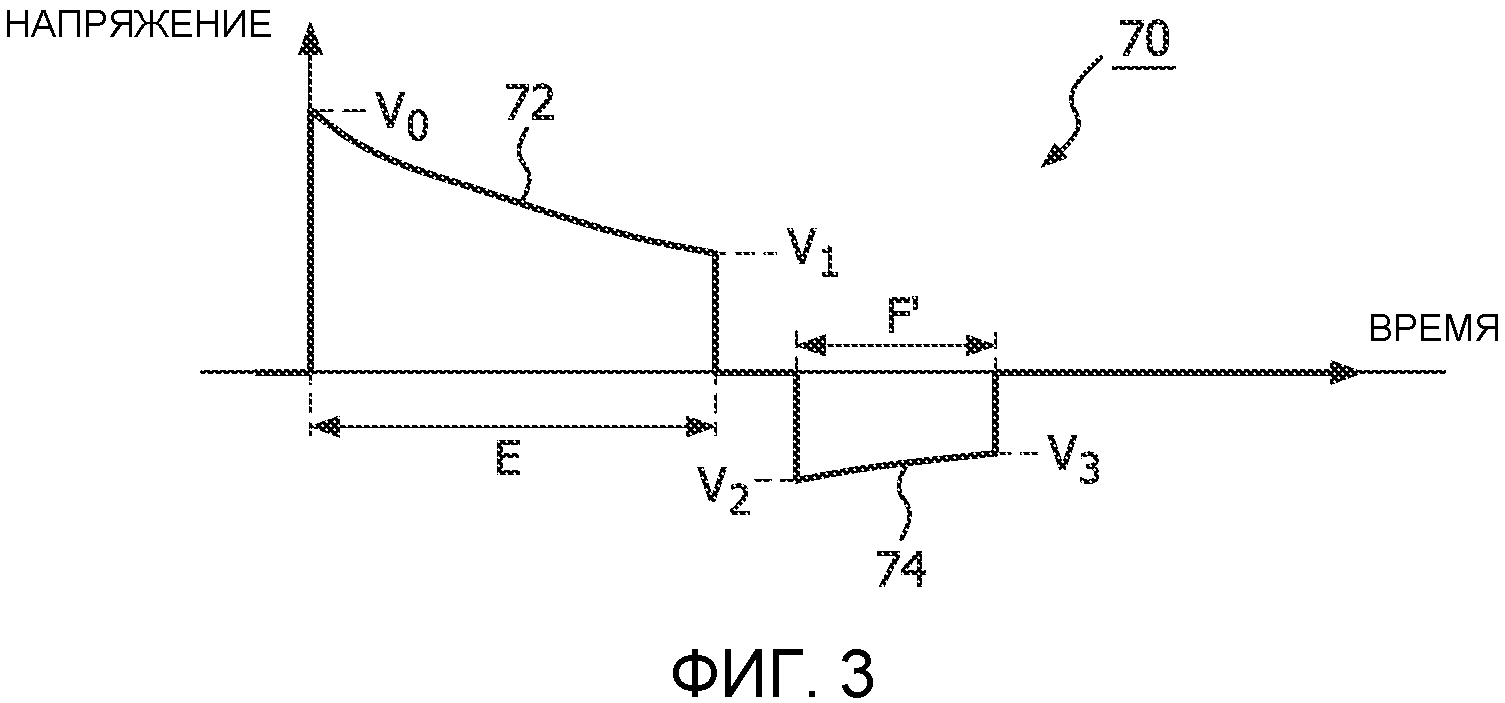
Фиг.3 - укороченная двухфазная волна;
Фиг.4a-4c - двухфазные волны дефибрилляции в сравнении с разными характеристиками реакции миокардиальных клеток;
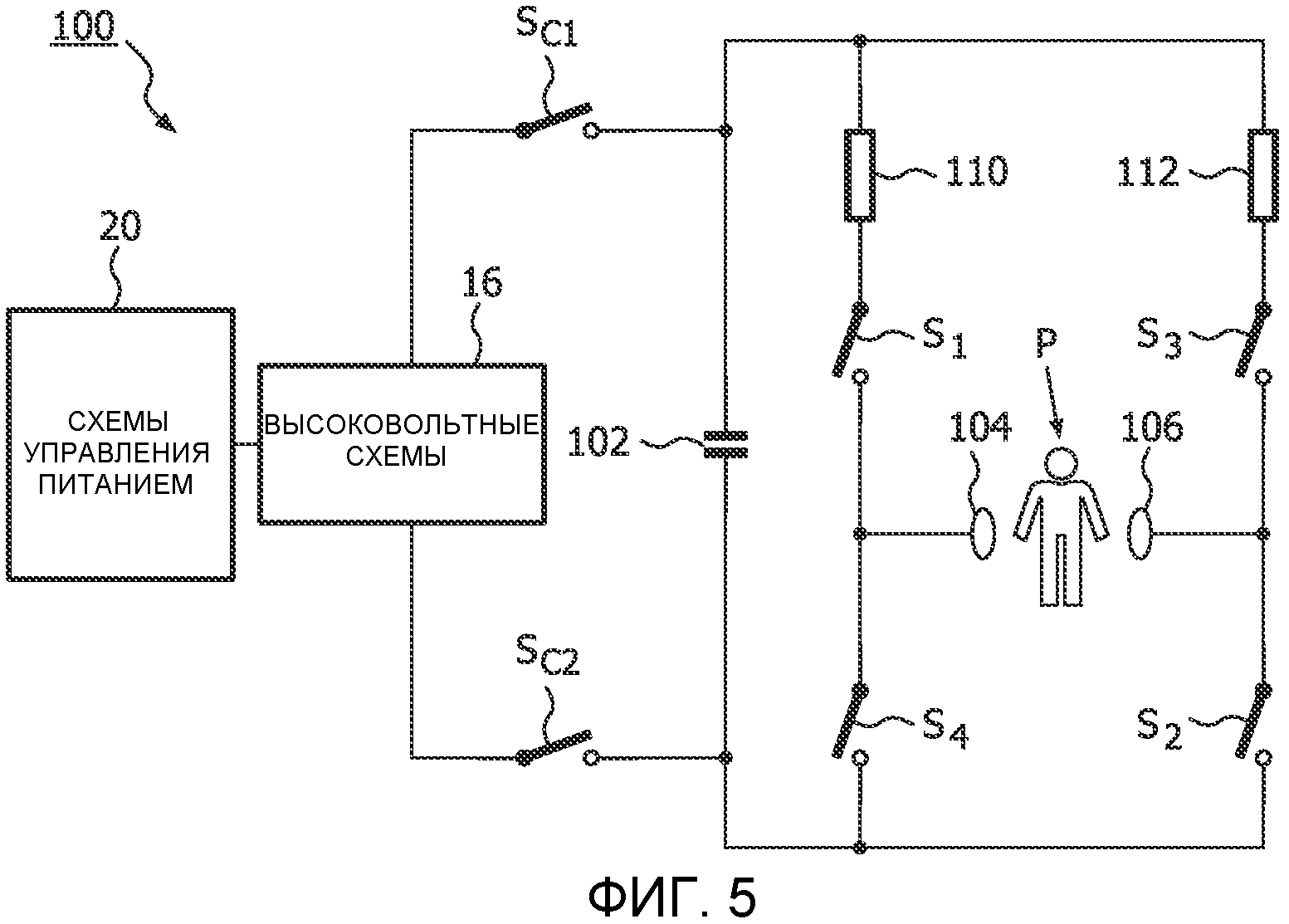
Фиг.5 - принципиальная схема дефибриллятора, который подает двухфазную волну дефибрилляции с регулируемым относительным спадом вершины импульса второй фазы в соответствии с принципами настоящего изобретения;
Фиг.6 - двухфазная волна дефибрилляции, формируемая дефибриллятором, представленным на фиг.5, в сравнении с разными характеристиками реакции миокардиальных клеток.
На фиг.1 показана блок-схема монитора/дефибриллятора пациента, выполненного в соответствии с принципами настоящего изобретения. Прибор, показанный на фиг.1, может выполнять дефибрилляцию пациента, который испытывает фибрилляцию желудочков. Данный прибор может также выполнять контроль ЭКГ, включая кардиомониторинг, необходимый для автоматического принятия решения по дефибрилляции. Показанный монитор может измерять также насыщение кислородом (SpO2), неинвазивно контролировать кровяное давление и контролировать концентрацию CO2 в конце выдоха. Данный многофункциональный прибор может также выполнять другие функции, например, инвазивный контроль кровяного давления и контроль температуры пациента. Монитор содержит множество входных и выходных каскадов сопряжения с пациентом, которые являются входными и выходными схемами для датчиков и электродов, прикрепляемых к пациенту. Кроме того, упомянутые схемы содержат традиционные измерительные и усилительные схемы для электродов ЭКГ, для оптических датчиков содержания кислорода, для измерения давления и для измерения содержания диоксида углерода. Информация, получаемая датчиками пациента и обрабатываемая входными схемами 10, оцифровывается входными A/D (аналого-цифровыми) преобразователями 12. Оцифрованная информация вводится в схемы обработки прибора по связной шине 60, которая устанавливает информационное соединение между различными модулями прибора.
Прибор содержит высоковольтные схемы 16 для работы дефибриллятора. Высоковольтные схемы формируют импульс высокого напряжения, необходимый для дефибрилляции, который подключается, в соответствующее время, коммутирующей логикой 14 к электродам дефибриллятора, подсоединенным к пациенту. Упомянутые схемы обеспечивают высоковольтный шок, необходимый для прерывания фибрилляции желудочков и возвращения сердца к нормальному ритму. Энергетический уровень и волна шока, наносимого для дефибрилляции, могут автоматически вычисляться процессором 40 в мониторе или могут быть установлены вручную опытным медицинским техником или врачом.
Питание модулей прибора подается схемами 20 управления питанием. Схемы 20 управления питанием будут распределять питание от батарей 22, от источника питания 24 переменным током или источника питания 26 постоянным током. Источники питания переменным током и постоянным током соединены также со схемами, которые заряжают батареи, когда монитор получает питание от упомянутых внешних источников питания.
Информация, получаемая прибором, может передаваться в другие приборы или места схемами 30 связи. Данные схемы могут содержать сетевое соединение, соединение RS232 или беспроводное соединение (например, Bluetooth, WiFi или инфракрасное соединение и т.п.).
Прибор работает и регулируется с помощью клавиатуры и органов 32 управления. В выполненном варианте осуществления, клавиатура является мембранной клавиатурой, обеспечивающей надежность в окружающих условиях. Могут быть также обеспечены органы управления, например, переключатель включения/выключения, органы управления уровнем мощности и подачи шока для дефибрилляции, принтера и другие функций.
Монитор работает под управлением центрального процессора (CPU) 40. Центральный процессор (CPU) исполняет программное обеспечение, записанное в постоянной памяти (ROM) 38. Предусмотрена также постоянная флэш-память для управления параметрами настройки функций и новыми или специальными возможностями, например, информацией, относящейся к волне. Предусмотрена съемная память 36 для хранения информации, созданной во время приступа пациента, например, фибрилляции желудочков. Информация о пациенте, например, кардиосигналы до и после дефибрилляции, также сохраняются в съемной памяти 36, которую можно снимать и, затем, передавать медицинскому специалисту для анализа, ведения документации и последующей диагностики. Съемная память 36 может также записывать речевую информацию от медицинского специалиста, говорящего в микрофон 48.
Звуковые сигнализаторы 34 служат для возбуждения твердотельного источника звука, который выдает короткие «пищащие» звуки. Данные звуки указывают, что самотестирование, заложенное в память прибора, обнаружило низкий уровень заряда батареи или неисправную работу компонента или группы схем, жизненно важных для пациента. На передней стороне прибора находится также специальный дисплей, который представляет большую, мигающую, красную букву X для указания низкого уровня заряда батареи или большую, постоянную, красную букву X для идентификации неисправности схемы.
Программным обеспечением формируются тональные сигналы 46, которые затем используются для возбуждения динамика 42. Данная возможность применяется в течение некоторых контрольных функций, например, короткий тональный сигнал в ответ на каждый сердечный цикл. Комбинации тональных сигналов применяются для выдачи звуковых сигналов тревоги и предупреждения, когда данные измерения жизненных функций пациента выходят за выбранные пределы аварийных сигналов. Тональные сигналы могут также вырабатываться с предусмотренной частотой для руководства медицинскому специалисту в ходе выполнения нажатий непрямого массажа сердца (CPR).
Динамик 42 может воспроизводить предварительно записанные инструкции голосом и другую информацию, сохраненную и воспроизводимую из схем 44 речевого вывода.
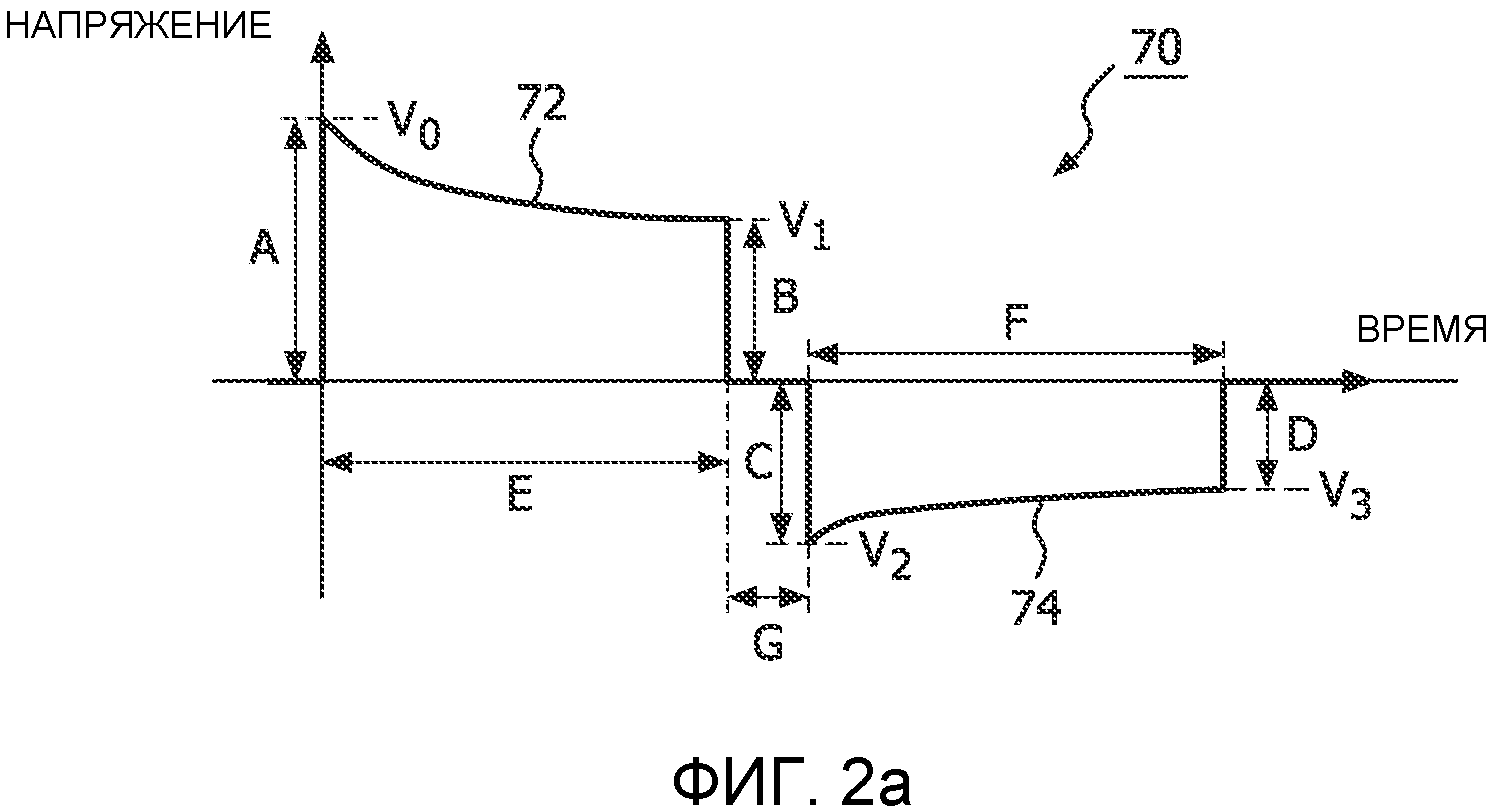
На фиг.2a изображена двухфазная волна 70 такого типа волны, которая вырабатывается дефибриллятором, выполненным в соответствии с настоящим изобретением. Двухфазная волна имеет первую фазу 72 одной полярности и вторую фазу 74 противоположной полярности. Двухфазные волны могут подаваться дефибриллятором с помощью, по меньшей мере, одного конденсатора. В случае двухконденсаторного дефибриллятора, один конденсатор будет заряжаться до максимального напряжения V0 в начале первой фазы 72, и другой конденсатор будет заряжаться до максимального напряжения V2 в начале второй фазы. Два конденсатора будут по-разному ориентированы полярностями относительно схемы подачи высокого напряжения, чтобы вырабатывались противоположные фазовых импульсов. В течение первой фазы, первый конденсатор подсоединяется к схеме подачи высокого напряжения и разряжается с пропусканием тока через электроды дефибриллятора. Когда требуется прекратить первую фазу, первый конденсатор переключается от схемы подачи высокого напряжения, и подключается второй конденсатор. Поскольку второй конденсатор подключается с полярностью, обращенной относительно полярности первого конденсатора, то разряд второго конденсатора создаст полярность импульса для второй фазы, которая является обратной полярности в первой фазе. Когда используют два конденсатора, каждый конденсатор может заряжаться до требуемого уровня напряжения, независимо от другого.
В реальных устройствах редко осуществляют двухконденсаторные компоновки. Данные компоновки имеют такие недостатки, как большие размер и стоимость. Следовательно, во внешних дефибрилляторах обычно применяют единственный конденсатор для снижения стоимости и размера. При использовании единственного конденсатора для формирования двухфазной волны, для переключения волны применяют так называемый H-мост. В течение первой фазы волны H-мост подсоединяет два вывода конденсатора к электродам. В конце первой фазы данное соединение разрывается, и выводы конденсатора переключаются для подсоединения в обратной полярности к электродам. Так как в данное время часто переключаются сильные токи, между паузами часто существует пауза, представленная интервалом G времени на фиг.2a. Поскольку применяется только один конденсатор, то напряжение на конденсаторе в конце первой фазы является начальным напряжением в начале второй фазы, когда переключается соединение конденсатора. Как показано на фиг.2a, упомянутое условие будет означать, что V2 = -V1.
На фиг.2a приведены другие параметры волны, которые важны для эффективности. Одним параметром является относительная продолжительность фазы, т.е. отношение продолжительности E первой фазы к продолжительности F второй фазы. Заданное отношение продолжительностей, которое часто применяют, составляет 60-40%. То есть желательно, чтобы из общей продолжительности волны первая фаза занимала 60% времени, и вторая фаза занимала 40% времени. Общая продолжительность волны (E+G+F) также имеет большое значение. Желательно, чтобы продолжительность волны была достаточной большой для дефибрилляции пациента, но также достаточно короткой, чтобы не причинять электрического поражения пациенту. Иначе говоря, желательно только приложить шок к пациенту в течение времени, необходимого для обеспечения дефибрилляции; и следует исключить продолжительную подачу энергии, которая не повышает эффективности дефибрилляции. Обычно используют двухфазные волны с общими продолжительностями в диапазоне 5-20 мсек.
Другим параметром волны, который имеет большее значение, является параметр, который известен под названием «относительный спад вершины импульса» («tilt») волны. Относительный спад вершины импульса является показателем подачи энергии и выражается в виде процентного отношения начального и конечного напряжений волны. Уравнение для вычисления относительного спада вершины импульса имеет вид:
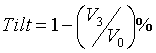
где V0 является начальным напряжением волны (амплитудой A волны), и V3 является конечным напряжением волны (амплитудой D волны) на фиг.2a. Относительный спад вершины импульса можно также вычислять для каждой фазы волны по отдельности.
На фиг.2a показана волна, известная как волна с небольшим относительным спадом вершины импульса. Волны с небольшим относительным спадом вершины импульса обычно возникают при подаче импульсной волны в пациента с высоким торакальным импедансом. С учетом того, что напряжение, ток и импеданс пациента связаны законом Ома, высокий импеданс пациента при данном начальном напряжении V0 импульса будет приводить к относительно слабому току, и снижение напряжения за продолжительность импульса будет относительно небольшим. На фиг.2a показано относительно небольшое снижение напряжения в течение первой фазы 72 волны 70 от V0 до V1 и в течение второй фазы 74 от V2 до V3.
На фиг.2b показана волна с большим относительным спадом вершины импульса, обычно возникающая в случае пациента с низким импедансом. При низком импедансе пациента протекающий ток больше при данном напряжении, и снижение напряжения в течение подачи волны оказывается больше, чем снижение напряжения волны с небольшим относительным спадом вершины импульса, показанной на фиг.2a. С того же самого начального напряжения V0, волна в первой фазе 72 снижается до V1 (амплитуды B волны) ниже, чем в случае волны с небольшим относительным спадом вершины импульса, показанной на фиг.2a. Аналогично, происходит большее снижение от V2 (амплитуды C волны) до конечного напряжения V3 в течение второй фазы 74.
Заключение по характеристике относительного спада вершины импульса состоит в том, что волна с большим относительным спадом вершины импульса будет спадать до заданного конечного напряжения за меньшее время, чем волна с небольшим относительным спадом вершины импульса до такого же конечного напряжения. Это означает, что волна с небольшим относительным спадом вершины импульса может продолжаться в течение значительного, возможно, чрезмерного промежутка времени до достижения одного и того же конечного напряжения. Поскольку предполагается, что дефибрилляция происходит обычно в течение нескольких первоначальных миллисекунд первой фазы, когда подаваемый ток является наиболее сильным, возможно в течение только первых 7 миллисекунд, когда средний ток является максимальным, то большая часть времени длительной волны с небольшим относительным спадом вершины импульса может быть терапевтически малоэффективной и, следовательно, не обязательна. Одно известное решение данной проблемы заключается в сокращении второй фазы 74 волны 70, как показано на фиг.3. Первая фаза 72 будет начинаться со своего начального уровня V0 напряжения и длиться в течение некоторой предварительно запрограммированной или адаптированной к импедансу продолжительности E или до тех пор, пока не будет достигнуто установленное напряжение V1. Вторая фаза 74 начинается со своего начального напряжения V2, как прежде, но прекращается преждевременно или укорачивается через время F'. Продолжительность F' второй фазы можно устанавливать только для второй фазы или с учетом сохранения максимальной общей продолжительности (E+F'). Например, вторую фазу 74 волны можно укоротить, когда F' равно E, и отношение продолжительностей фаз равно 50:50.
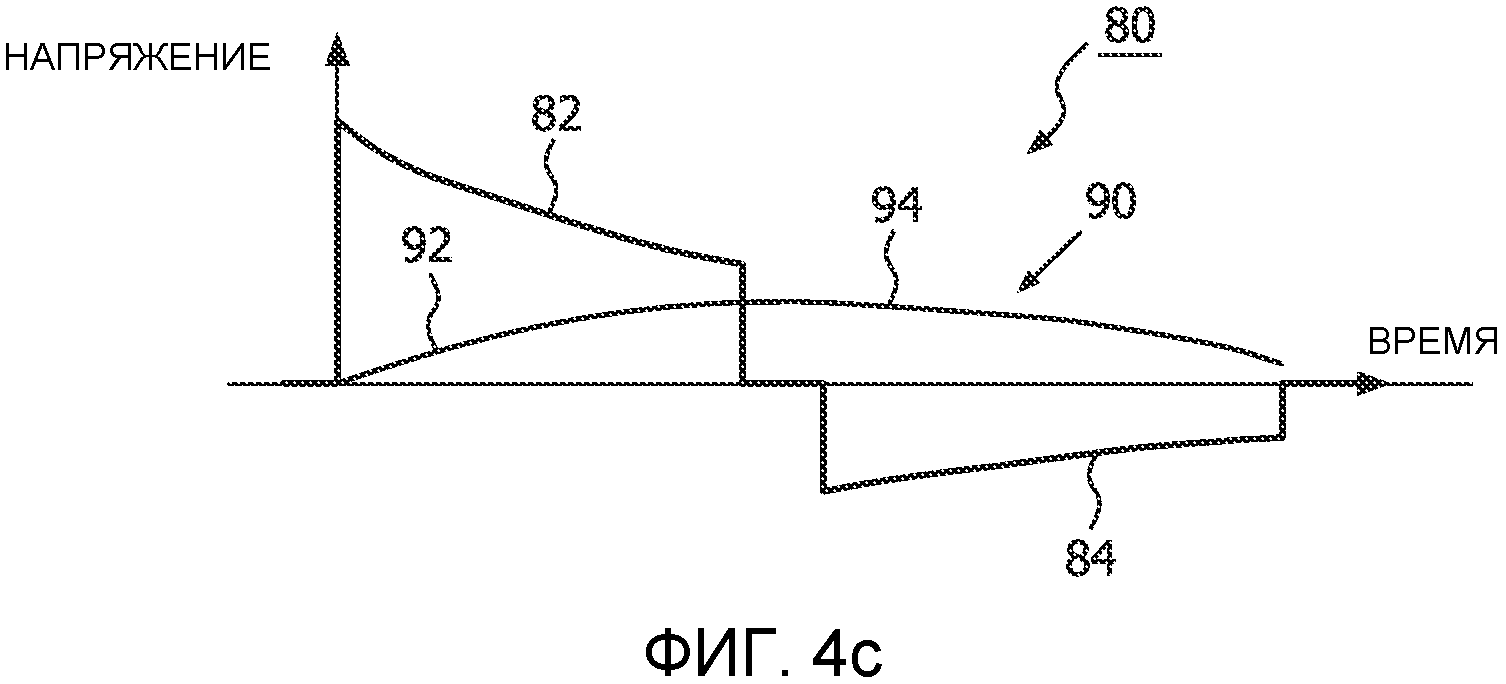
Проблема с укорачиванием второй фазы состоит в том, что вторая фаза заканчивает прикладываемый импульс на значительном напряжении, еще подводимом к миокарду в конце волны. Конечное напряжение V3, показанное на фиг.3, выше, чем будет конечное напряжение, если бы второй фазе позволили снижаться дальше. Упомянутое значительное конечное напряжение может вредно сказаться на эффективности терапии. Теоретически, желательно, чтобы конечное напряжение дефибрилляционной волны было нулевым, чтобы, после подачи импульса, на миокардиальных клетках не оставалось никакого остаточного заряда, который мог бы вредно сказаться на автономном перезапуске в теле электрической пульсации сердца. Такое удаление остаточного заряда названо одним специалистом «отрыжкой». Смотри патент США 5991658 (Brewer и др.). Другое преимущество прекращения дефибрилляционной волны на как можно меньшем напряжении состоит в том, что таким образом минимизируется чувствительность вычисления оптимальной дозы второй фазы к неопределенностям характеристик клеточной реакции, индивидуальных при применении к конкретному пациенту. Третье преимущество прекращения дефибрилляционной волны на почти нулевом напряжении состоит в исключении явления «разрушительного возбуждения», т.е. стимуляции послешоковой аритмии током, вызываемым большим изменением напряжения. Один из способов достижения упомянутой цели состоит в обеспечении возможности полного затухания фаз двухфазного импульса до нуля вольт, как показано в патенте США 6539255 (Brewer и др.). Целесообразность данного подхода можно понять из рассмотрения фиг.4a-4c, на которых показаны двухфазные волны 80, совместно с которыми проведены характеристики 90 реакций миокардиальных клеток. Как упоминалось выше, реакция миокардиальных клеток может изменяться от пациента к пациенту и даже день ото дня и, в общем, не известна для данного пациента во время спасения. На фиг.4a показано, как будет изменяться реакция миокардиальных клеток в идеальном случае. Изменение характеристики реакции миокардиальных клеток можно характеризовать постоянной εТ времени клеточной мембраны, которая номинально составляет 3,5 миллисекунд. В случае, показанном на фиг.4a, данная постоянная времени вызывает подъем характеристики 90 реакции миокардиальных клеток в течение первой фазы 82 двухфазной волны 80, пока не достигнет максимума в конце первой фазы. Когда волна импульса переключается на вторую фазу 84, характеристика реакции миокардиальных клеток снижается, как показано последним участком 94 характеристики реакции. В данном случае, в конце второй фазы 84, характеристика реакции снизилась точно до ее исходного начального уровня. Данное снижение показывает, что на клеточных мембранах миокарда не имеется никакого остаточного заряда в конце импульса 80.
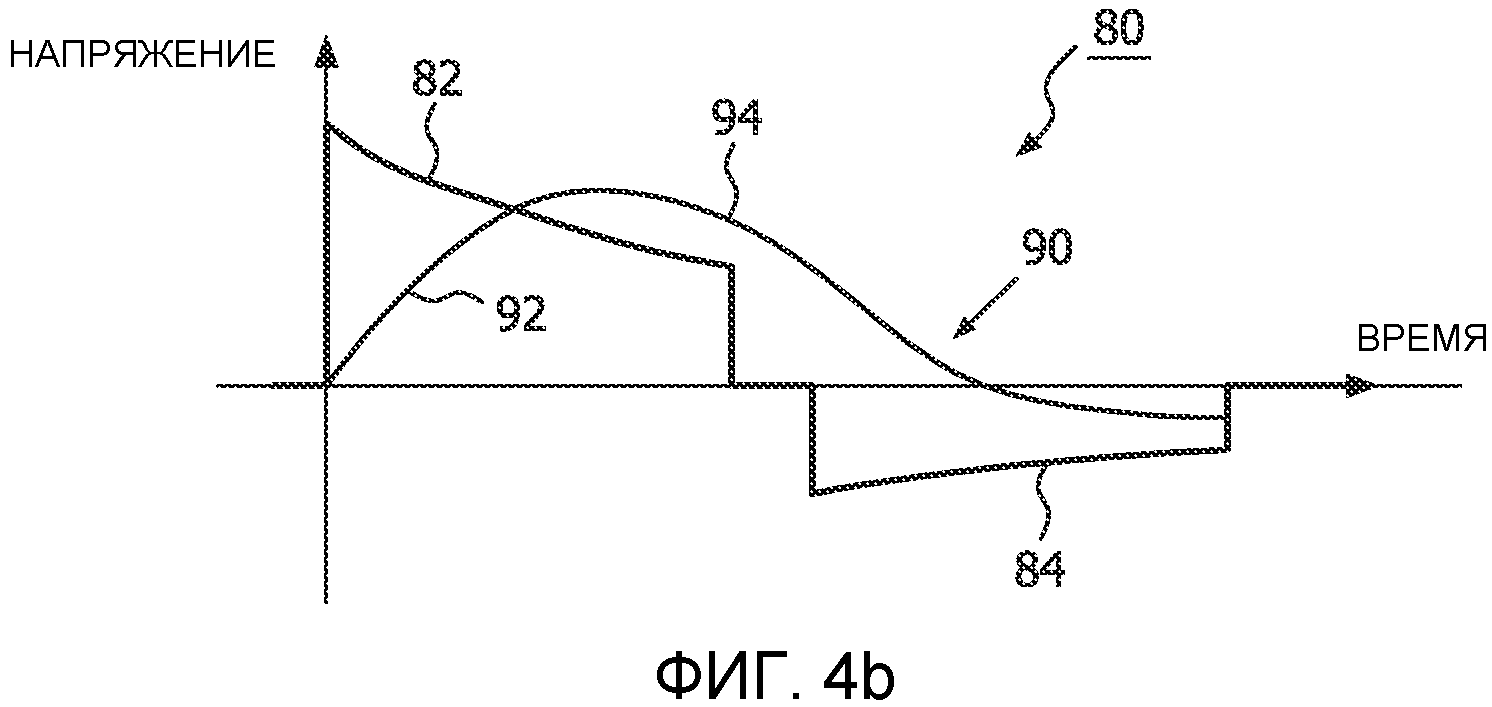
На фиг.4b показана ситуация, в которой характеристика 90 реакции миокардиальных клеток имеет меньшую постоянную εТ времени клеточной мембраны, что приводит к достижению характеристикой реакции ее максимума до окончания первой фазы 82 двухфазного импульса 80. Затем характеристика реакции снижается вместе со снижением относительного спада вершины импульса волны, т.е. имеет место реакция, которая, как полагают, дает очень малый вклад в дефибрилляцию. В течение второй фазы 84 двухфазного импульса характеристика реакции продолжает еще быстрее изменяться, со снижением ниже своего начального уровня и следованием за снижением относительного спада вершины импульса второй фазы, пока вторая фаза 84 импульса не закончится. Как видно на фигуре, в момент завершения характеристика реакции находится ниже своего начального уровня и тем самым показывает, что на мембранах миокардиальных клеток остается некоторый остаточный заряд. Данная ситуация представляет случай, который может произойти с пациентом с низким импедансом.
На фиг.4c представлена ситуация для пациента с высоким импедансом, когда характеристика 90 реакции миокардиальных клеток повышается очень медленно, как указано позицией 92, в течение первой фазы 82 двухфазной волны 80. Характеристика реакции еще повышается в момент, когда первая фаза 82 заканчивается. Когда подается вторая фаза 84 импульса, характеристика реакции начинает постепенное снижение, но не совсем достигает своего исходного начального уровня в конце второй фазы. Данная характеристика также свидетельствует о присутствии остаточного заряда на клеточных мембранах миокарда.
В соответствии с принципами настоящего изобретения, для исключения приведенных состояний предлагается схема 100 дефибриллятора, показанная на фиг.5. В данной схеме энергия для подачи двухфазного импульса накапливается в единственном конденсаторе 102. В процессе подготовки к подаче импульса, батарея или источник питания схем 20 управления питанием подсоединяют к высоковольтным схемам 16. Переключатели Sc1 и Sc2 замыкаются и высоковольтные схемы 16 заряжают конденсатор 102 до уровня V0 высокого напряжения, 2000 вольт. Когда конденсатор 102 полностью заряжается до требуемого уровня, переключатели Sc1 и Sc2 размыкаются. Затем схема H-моста, содержащая переключатели S1, S2, S3 и S4, переключается для подведения двухфазного импульса к пациенту P через электроды 104 и 106. В течение первой фазы двухфазного импульса, переключатели S1 и S2 замкнуты, и конденсатор подсоединен к электродам пациента для протекания тока через пациента в одном направлении, например, от электрода 104 на грудной клетке к электроду 106 на грудной клетке. Небольшое сопротивление 110, например, 10 Ом, ограничивает максимальный ток для предотвращения нанесения повреждения пациенту с низким импедансом. В конце первой фазы, переключатели S1 и S2 размыкаются для прекращения первой фазы двухфазного импульса, и переключатели S3 и S4 замыкаются для подведения двухфазного импульса к пациенту P. Замыкание данных переключателей приводит к тому, что ток от конденсатора 102 протекает в направлении, противоположном направлению в первой фазе, в данном примере, от электрода 106 на грудной клетке к электроду 104 на грудной клетке. В путь тока второй фазы также можно последовательно включить небольшое сопротивление 112, также 10 Ом, например. В соответствии с принципами настоящего изобретения, переключатель S1 также замыкается на некоторый промежуток времени второй фазы импульса. В предпочтительном варианте осуществления, переключатель S1 переключается между замкнутым и разомкнутым положениями в течение второй фазы посредством управления переключателем на основе широтно-импульсной модуляции. Замыкание переключателя S1 обеспечивает протекание какой-то части тока конденсатора 102 в обход пациента P по пути, созданному переключателями S1 и S4, когда переключатель S1 замыкается в течение второй фазы. В результате, напряжение конденсатора 102 снижается быстрее, чем оно снижалось бы, если бы переключатель S1 не применялся в течение второй фазы. Полученный результат с двухфазной волной показан на фиг.6, на которой видно крутое снижение (больший относительный спад вершины импульса) второй фазы 86 двухфазного импульса. С помощью управления замыканием переключателя S1, вторую фазу 86 двухфазного импульса можно довести почти до опорного потенциала в конце двухфазной волны и за меньшее время, чем в случае, если бы переключатель S1 не применяли в течение второй фазы. Посредством данной операции, конечное напряжение V3 в конце двухфазного импульса доводится почти до нуля.
Измерение импеданса интерфейса, которое можно выполнять с помощью пропускания небольшого сигнала перед применением шока, как описано в статье Кербера с соавторами (Kerber и др.), или измерения подводимого тока или прикладываемого напряжения во время фактической подачи импульсов высокого напряжения, как показано в вышеупомянутых патентах США изобретателей Фейна с соавторами (Fain и др.), Камерона с соавторами (Cameron и др.) и Глайнера с соавторами (Gliner и др.), можно применить для управления параметрами подаваемой волны шока, например, энергией, напряжением заряда конденсатора и продолжительностями волн, как поясняется в упомянутых патентах и в патенте США 5352239 (Pless).
Результатом упомянутого управляемого снижения или относительного спада вершины импульса второй фазы двухфазного импульса является то, что можно обеспечить, чтобы волна импульса заканчивалась вблизи ее опорного потенциала. Данный результат отражен тремя характеристиками реакции миокардиальных клеток, проведенными совместно с волной двухфазного импульса, на фиг.6. В случае, когда происходит точное согласование двухфазного импульса с клеточной реакцией, как отражено характеристикой 120 реакции миокардиальных клеток, характеристика реакции возрастает до почти оконечной вершины первой фазы 82 двухфазного импульса, затем снижается в течение второй фазы 86, как отражено участком 123 характеристики реакции, до тех пор, пока характеристика не заканчивается вблизи конечного уровня V3 напряжения. Для пациента с низким импедансом, как отражено характеристикой 130 реакции, характеристика реакции снова быстро повышается в течение первой фазы 82, как отражено кривой 131, и также снижается в течение второй фазы 86 двухфазного импульса до окончания вблизи конечного уровня V3 напряжения. Для пациента с высоким импедансом начальный участок 141 характеристики 140 реакции повышается в течение первой фазы 82, затем снижается до почти конечного уровня V3 напряжения. Расхождение между конечными точками всех характеристик реакции миокардиальных клеток, показанных на фиг.6, представляется очень малым, в отличие от расхождений, показанных на фиг.4a-4c, и тем самым свидетельствует, что во всех случаях на клеточных мембранах остается незначительный остаточный заряд. Напряжение волны заканчивается вблизи нуля, независимо от импеданса пациента. Данный результат достигается дефибриллятором независимо от отсутствия какой-либо априорной информации относительно характеристики реакции миокардиальных клеток.
В предпочтительном варианте осуществления, как упоминалось выше, постоянный относительный спад вершины импульса второй фазы двухфазного импульса управляемо повышается или регулируется посредством переключения переключателя S1 между разомкнутым и замкнутым состояниями в течение подачи второй фазы двухфазного импульса. Данное управление переключателем на основе широтно-импульсной модуляции может выполняться при одновременном контроле напряжения конденсатора 102. Возможно также использование других методов управления переключателем, например, замыкание переключателя S1 в течение одного интервала предварительно заданной продолжительности. В предпочтительном варианте осуществления, в качестве конденсатора 102 применен конденсатор емкостью 200 микрофарад. Настоящее изобретение может быть реализовано с помощью дефибриллятора с одним конденсатором или дефибриллятора с несколькими конденсаторами, в котором в течение двух фаз прилагаемой волны применяют разные конденсаторы или комбинации конденсаторов. В предпочтительном варианте осуществления осуществляется управление относительным спадом вершины импульса второй фазы для сохранения приблизительно 95% общего относительного спада вершины импульса. Увеличение относительного спада вершины импульса в течение второй фазы также обеспечивает полезный результат создания возможности эффективного лечебного воздействия с применением сокращенного диапазона продолжительностей волн, при этом предпочтительный вариант осуществления формирует волны двухфазных импульсов в диапазоне от 6,5 миллисекунд до 12 миллисекунд для всей совокупности импедансов пациентов, т.е. обеспечивает заметное сокращение относительно обычной максимальной продолжительности импульса, составляющей 20 миллисекунд.
Реферат
Изобретение относится к медицинской технике. Внешний дефибриллятор для подачи двухфазных дефибрилляционных импульсов содержит высоковольтную схему, с которой соединен конденсатор, а также пару электродов и множество переключателей. Высоковольтная схема выполнена с возможностью заряжать конденсатор для подачи дефибрилляционного импульса. Переключатели содержат Н-мост, подсоединены между конденсатором и электродами и выполнены с возможностью подсоединения первой и второй фаз волны двухфазного дефибрилляционного импульса к электродам. Относительный спад вершины импульса второй фазы волны является управляемо регулируемым. Управляемый путь тока включает в себя переключатель Н-моста и обеспечивает возможность управляемого обхода током электродов в течение второй фазы двухфазной волны. Применение изобретения позволит повысить безопасность и эффективность дефибрилляции. 11 з.п. ф-лы, 6 ил.
Формула
высоковольтную схему;
конденсатор, соединенный с высоковольтной схемой, который заряжается высоковольтной схемой для подачи дефибрилляционного импульса;
пару электродов пациента;
множество переключателей, содержащих Н-мост, подсоединенных между конденсатором и электродами пациента и выполненных с возможностью подсоединения первой и второй фаз волны двухфазного дефибрилляционного импульса к электродам пациента, причем относительный спад вершины импульса второй фазы волны является управляемо регулируемым; и
управляемый путь тока, который включает в себя переключатель Н-моста, и который обеспечивает возможность управляемого обхода током электродов пациента в течение второй фазы двухфазной волны.
в котором множество переключателей содержит Н-мост с одной конфигурацией замыкания переключателей для подачи одной фазы двухфазной волны и другой конфигурацией замыкания переключателей для подачи противоположной фазы двухфазной волны.
в котором конденсатор содержит одну емкость, которую используют для подачи обеих фаз двухфазной волны.
в котором конденсатор дополнительно содержит первый конденсатор, который используют для подачи первой фазы двухфазной волны, и второй конденсатор, который используют для подачи второй фазы двухфазной волны.
в котором Н-мост дополнительно содержит первый и второй переключатели, которые замыкаются для подачи импульса в течение первой фазы двухфазной волны, и третий и четвертый переключатели, которые замыкаются для подачи импульса в течение второй фазы двухфазной волны,
при этом управляемый путь тока содержит один из первого и второго переключателей.
дополнительно содержащий первый резистор, соединенный последовательно с первым и вторым переключателями, когда первый и второй переключатели замкнуты, и второй резистор, соединенный последовательно с третьим и четвертым переключателями, когда третий и четвертый переключатели замкнуты.
в котором управление управляемым путем тока осуществляется управляющим сигналом с широтно-импульсной модуляцией в течение второй фазы двухфазной волны.
в котором волна двухфазного дефибрилляционного импульса имеет:
первую фазу, в течение которой напряжение импульса повышается от опорного потенциала до максимального напряжения V0 и снижается от V0 в течение первой фазы волны; и
вторую фазу, которая начинается с начального напряжения V2 и проходит со снижением от V2 в течение второй фазы волны до уровня, равного или почти равного опорному потенциалу.
в котором напряжения V0 и V2 противоположны по знаку относительно опорного потенциала.
дополнительно содержащий схему, выполненную с возможностью измерения импеданса пациента,
при этом параметры волны двухфазного дефибрилляционного импульса устанавливаются в соответствии с измеренным импедансом пациента.
в котором общий относительный спад вершины импульса двухфазной волны выдерживается около 95% посредством управления относительным спадом вершины импульса второй фазы волны.
в котором общий относительный спад вершины импульса двухфазной волны выдерживается около 95% посредством увеличения относительного спада вершины импульса второй фазы волны.
Документы, цитированные в отчёте о поиске
Автоматический контроль скорости зарядки конденсатора дефибриллятора

Комментарии