Способ и устройство для выбора области диагностики и система диагностики для определения эластичности - RU2695619C2
Код документа: RU2695619C2
Чертежи







Описание
ОБЛАСТЬ ТЕХНИКИ
Варианты осуществления настоящего изобретения относятся к области технологии обработки медицинских снимков, в частности к способу и устройству для выбора области диагностики и к системе определения эластичности.
УРОВЕНЬ ТЕХНИКИ
Традиционная работа с медицинскими снимками, включая ультразвуковую визуализацию, магнитно-резонансную томографию (МРТ), компьютерную томографию (КТ) и т.д. используется во множестве клинических областей для позиционирования области диагностики тканей органов например, определение эластичности, цветное допплеровское ультразвуковое исследование (допплерография) и т.д.
В настоящее время область диагностики тканей органов, главным образом, выбирается следующими двумя способами: первый - ткани органа на фиксированной глубине считаются областью диагностики; второй -область диагностики тканей органа выбирается искусственно.
В первом способе, во время исследования глубина для диагностики фиксированная, однако для разных людей или для разных положений тела одного и того же человека местоположение и форма тканей может отличаться. Например, что касается устройства, доступного на рынке на сегодняшний день, для определения мгновенной эластичности, его глубина диагностики является фиксированной, т.е. ткани органа расположены на глубине 2,5-6,5 см под кожей (у людей с обычным телосложением), при этом у людей крупного или полного телосложения глубина 3,5 см может еще относиться к коре. Таким образом, способ с использованием фиксированной глубины диагностики может стать источником ошибок в случае с отдельными лицами.
Второй способ с ручным выбором области диагностики требует от врача глубокого понимания структуры и информации на изображении тканей органа, чтобы точно выбрать границы органа - к врачу предъявляются высокие требования; при этом, поскольку процесс искусственного выбора введен в процесс диагностики, продолжительность диагностики увеличивается.
Таким образом, требуется способ для автоматической корректировки области диагностики.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Цель настоящего изобретения состоит в том, чтобы предложить способ и устройство для выбора области диагностики и систему диагностики эластичности, обеспечивающий автоматическую корректировку области диагностики.
В одном из аспектов настоящее изобретение предлагает способ для выбора области диагностики, содержащий:
определение границы тканей органа в соответствии с информацией о тканях, которую необходимо распознать, и определение области, окруженной границами тканей органа, в качестве области тканей органа;
разделение информации о тканях, которую необходимо распознать, на множество подобластей диагностики и расчет характеристического параметра информации о тканях органа в подобластях диагностики;
определение граничной области тканей органа в соответствии с информацией о тканях органа, которую необходимо распознать;
определение области диагностики тканей органа в соответствии с граничной областью тканей органа и заранее заданным условием для характеристического параметра.
В другом аспекте настоящее изобретение предлагает устройство для выбора области диагностики, содержащее: блок разделения области, выполненный с возможностью разделения информации о тканях органа, которую необходимо распознать, на множество подобластей диагностики; блок расчета характеристического параметра, выполненный с возможностью расчета характеристических параметров информации о тканях органа в подобластях диагностики; блок распознавания граничной области, выполненный с возможностью определения граничной области тканей органа в соответствии с информацией о тканях органа, которую необходимо распознать; и блок определения области диагностики, выполненный с возможностью определения области диагностики тканей органа в соответствии с граничной областью тканей органа и заранее заданным условием для характеристического параметра.
В еще одном аспекте настоящее изобретение предлагает систему определения эластичности, содержащую: устройство получения информации, устройство визуализации эластичности, устройство установки датчика, обрабатывающее устройство и отображающее устройство, и дополнительно содержащее устройства для выбора области диагностики, предложенное в любом из вариантов осуществления настоящего изобретения. Устройство получения информации выполнено с возможностью получения информации о тканях органа, которую необходимо распознать; устройство установки датчика выполнено с возможностью корректировки положения датчика в устройстве визуализации эластичности, таким образом, чтобы глубина диагностики датчика включала в себя область диагностики, определенную устройством для выбора области диагностики; устройство визуализации эластичности выполнено с возможностью получения информации об эластичности тканей органа; и отображающее устройство выполнено с возможностью отображения информации об эластичности в области диагностики.
Способ и устройство для выбора области определения, а также система определения эластичности, предложенная в одном из вариантов осуществления настоящего изобретения, способны выполнять автоматическую корректировку области диагностики тканей органа. Способ для выбора области диагностики, предложенный в одном из вариантов осуществления настоящего изобретения, определяет граничную область тканей органа в соответствии с информацией о тканях органа, которую необходимо распознать, и определяет область диагностики тканей органа в соответствии с граничной областью тканей органа и заранее заданным условием для характеристического параметра. В этом способе местоположение и размеры области диагностики различаются, когда различается информация о тканях органа, т.е. способ может корректировать местоположение и размер области диагностики органа.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Чертежи, раскрытые в настоящей заявке, предназначены для предоставления дальнейшего понимания вариантов осуществления заявленного изобретения и представляют собой часть вариантов осуществления настоящего изобретения, при этом их не следует толковать в качестве ограничивающих варианты осуществления настоящего изобретения. На чертежах:
Фиг. 1 представляет собой блок-схему осуществления способа для выбора области диагностики, предложенного в первом варианте осуществления настоящего изобретения;
Фиг. 2 представляет собой блок-схему осуществления способа для выбора области диагностики, предложенного во втором варианте осуществления настоящего изобретения;
Фиг. 3 представляет собой вид выбора области диагностики тканей органа на основе ультразвукового сигнала М-типа во втором варианте осуществления настоящего изобретения;
Фиг. 4 представляет собой схематичное изображение количественной оценки модуля упругости тканей органа во втором варианте осуществления настоящего изобретения;
Фиг. 5 представляет собой блок-схему осуществления способа для выбора области диагностики, предложенного в третьем варианте осуществления настоящего изобретения;
Фиг. 6 представляет собой вид выбора области диагностики тканей органа на основе ультразвукового сигнала В-типа в третьем варианте осуществления настоящего изобретения;
Фиг. 7 представляет собой схематичное изображение количественной оценки модуля упругости тканей органа в третьем варианте осуществления настоящего изобретения;
ФИГ. 8 представляет собой блок-схему осуществления способа для выбора области диагностики, предложенного в четвертом варианте осуществления настоящего изобретения;
Фиг. 9 представляет собой вид границ трехмерной визуализации на основе тканей органа четвертого варианта осуществления настоящего изобретения;
Фиг. 10 представляет собой вид выбора области определения на основе трехмерной визуализации тканей органа в четвертом варианте осуществления настоящего изобретения;
Фиг. 11 представляет собой схематичное изображение количественной оценки модуля упругости тканей органа в четвертом варианте осуществления настоящего изобретения;
Фиг. 12 представляет собой схематичный вид структуры устройства для выбора области диагностики, предложенный в пятом варианте осуществления настоящего изобретения; и
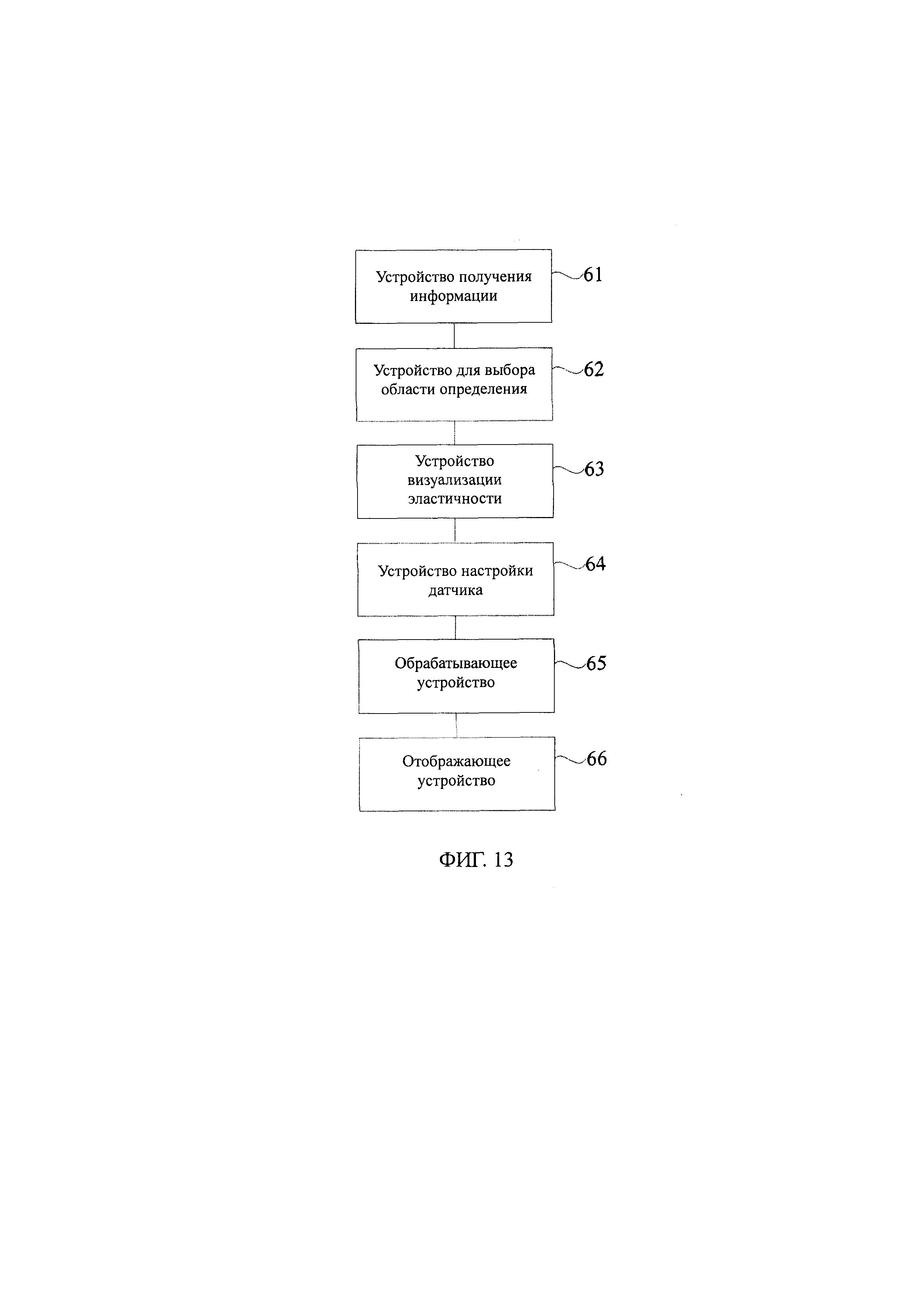
Фиг. 13 представляет собой схематичный вид структуры системы определения эластичности, предложенный в шестом варианте осуществления настоящего изобретения.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее приведено более подробное описание вариантов осуществления настоящего изобретения со ссылкой на прилагаемые чертежи и конкретные варианты осуществления. Следует понимать, что конкретные варианты осуществления, раскрытые в настоящей описании, предназначены только для целей разъяснения вариантов осуществления настоящего изобретения, и не предназначены для ограничения вариантов осуществления настоящего изобретения. Также следует обратить внимание на то, что в целях упрощения описания на прилагаемых чертежах показана лишь часть, а не все варианты осуществления настоящего изобретения.
Первый вариант осуществления изобретения:
На фиг. 1 представлена блок-схема осуществления способа для выбора области диагностики, предложенного в первом варианте осуществления настоящего изобретения. Способ может быть осуществлен устройством для выбора области диагностики. Как показано на Фиг. 1, последовательность операций при осуществлении содержит:
Шаг 11: разделение информации о тканях органа, которую необходимо распознать, на множество подобластей диагностики и расчет характеристических величин информации о тканях органа в каждой из подобластей диагностики.
В данном случае информация о тканях органа, которую необходимо распознать, может включать в себя одномерную, двухмерную или трехмерную ультразвуковую визуализацию тканей органа, и также может включать в себя одномерный, двухмерный или трехмерный ультразвуковой сигнал о тканях органа, таким образом, что информация о тканях органа может быть ультразвуковым сигналом А-типа о тканях органа, ультразвуковым сигналом М-типа о тканях органа, ультразвуковой визуализацией В-типа о тканях органа, КТ - визуализацией тканей органа или МРТ - визуализацией тканей органа. Характеристическая величина информации о тканях органа может быть средним значением информации о тканях органа или стандартным отклонением информации о тканях органа.
Шаг 12: определение граничной области тканей органа в соответствии с информацией о тканях органа, которую необходимо распознать.
Граничная область тканей органа может быть определена в соответствии с характеристическим параметром информации о тканях органа в каждой подобласти диагностики, вычисленной на шаге 11. Граничная область тканей органа в информации о тканях органа может также быть распознана посредством использования технологии обработки изображений или технологии обработки сигнала с характеристикой тканей органа в соответствии с информацией о тканях органа и характеристикой границ тканей органа.
Например, когда информация о тканях органа представляет собой одномерный ультразвуковой сигнал тканей органа или двухмерную визуализацию тканей органа, граничная область тканей органа определяется на основе характеристических параметров информации от тканях органа в подобласти диагностики; и когда информация о тканях органа представляет собой трехмерный ультразвуковой сигнал тканей органа, граничная область тканей органа в информации о тканях органа распознается на основе характеристики тканей органа и характеристики границ тканей органа.
Шаг 13: определение области диагностики тканей органа в соответствии с граничной областью тканей органа и заранее заданным условием для характеристического параметра.
Сюда относится и то, что, если информация о тканях органа представляет собой одномерное, двухмерное или трехмерное изображение или сигнал тканей органа, то заранее заданным условием для характеристического параметра может быть среднее значение и стандартное отклонение, соответствующие значению интенсивности изображения или сигнала в пределах каждой подобласти диагностики, удовлетворяющей заранее заданной глубине.
Например, если информация о тканях органа представляет собой одномерный ультразвуковой сигнал тканей органа, область диагностики тканей органа может быть определена на основе граничной области тканей органа и заранее заданного условия для характеристического параметра, которое может включать в себя условие: когда стандартное отклонение, соответствующее значению интенсивности ультразвукового сигнала в каждой из множества непрерывных подобластей диагностики в пределах граничной области тканей органа меньше, чем пороговое значение стандартного отклонения, то множество непрерывных подобластей диагностики определяются как область диагностики тканей органа.
Например, если информация о тканях органа представляет собой двухмерную ультразвуковую визуализацию тканей органа или трехмерную визуализацию тканей органа, то область диагностики тканей органа может быть определена на основе граничной области тканей органа и заранее заданного условия для характеристического параметра, которое может включать в себя: если среднее значение, соответствующее значению интенсивности визуализации в каждой из множества непрерывных подобластей в пределах граничной области тканей органа, меньше, чем пороговое среднее значение, и если стандартное отклонение, соответствующее значению интенсивности визуализации в каждой из множества непрерывных подобластей диагностики в пределах граничной зоны тканей органа, меньше чем пороговое значение стандартного отклонения, то тогда множество непрерывных подобластей диагностики определяются в качестве области диагностики тканей органа.
Следует отметить, что пороговое среднее значение может составлять 20% от максимального значения интенсивности ультразвукового сигнала или визуализации в каждой подобласти диагностики, и пороговое стандартное отклонение может составлять 5% от максимального значения интенсивности ультразвукового сигнала или визуализации в каждой подобласти диагностики. Например, диапазон интенсивности КТ - изображения в подобласти диагностики тканей печени может составлять 0…300 ед. Хаунсфилда, средний порог может составлять 60 ед. Хаунсфилда, и порог стандартного отклонения может составлять 15 ед. Хаунсфилда.
Причем, после определения области диагностики тканей органа на основе граничной области тканей органа и заранее заданного условия для характеристического параметра, способ может дополнительно содержать: расчет значения эластичности тканей органа в области диагностики тканей органа. Это представляет собой расчет значения эластичности тканей органа в определенной области диагностики тканей органа таким образом, чтобы реализовать ультразвуковую диагностику тканей органа.
Способ выбора области диагностики, предложенный в первом варианте осуществления настоящего изобретения, разделяет информацию о тканях органа на множество подобластей диагностики и рассчитывает характеристические параметры из информации о тканях органа в каждой подобласти диагностики, определяет граничную область тканей органа в соответствии с информацией о тканях органа и определяет область диагностики тканей органа в соответствии с граничной областью тканей органа и заранее заданным условием для характеристического параметра, т.е. способ способен автоматически выбирать область диагностики. Поскольку в способе для выбора области диагностики, предложенном в первом варианте осуществления настоящего изобретения, когда информация о тканях органа отличается, отличается область определения. А именно, в первом варианте осуществления настоящего изобретения местоположение и размеры области диагностики у разных людей могут быть автоматически скорректированы в соответствии с характеристиками информации о тканях органа.
Второй вариант осуществления изобретения:
На фиг. 2 представлена блок-схема осуществления способа выбора области диагностики, предложенного во втором варианте осуществления настоящего изобретения, который применим к одномерному ультразвуковому сигналу тканей органа. На фиг. 3 представлено изображение для выбора области диагностики на основе ультразвукового сигнала М-типа тканей органа во втором варианте осуществления настоящего изобретения; На фиг. 4 представлено схематичное изображение для количественного определения модуля упругости тканей органа во втором варианте осуществления настоящего изобретения. Далее со ссылкой на фиг. 2-4, способ содержит.
Шаг 21: разделение ультразвукового сигнала тканей органа на множество подобластей Si диагностики.
Одномерный ультразвуковой сигнал ткани органа может быть ультразвуковым сигналом А-типа тканей органа или ультразвуковым сигналом М-типа тканей органа. Предполагается, что один ультразвуковой сигнал содержит n точек выборки, и ультразвуковой сигнал соответствующих тканей органа обладает глубиной d сканирования (ед. изм.: мм), то n/d точек приходится на 1 мм глубины. Эти n точек выборки разделяются на несколько сегментов подобластей Si диагностики, и глубина сканирования, соответствующая подобластям Si диагностики равна di, причем i - это целое число, и глубина di сканирования может быть средним значением или конечным значением глубин подобластей Si диагностики, в данном случае глубина di сканирования - это конечное значение.
Например, n точек выборки разделены на несколько сегментов в подобластей Si диагностики с интервалами z, поскольку самая нижняя часть визуализации (т.е. соответствующая самой глубокой части глубины сканирования) в ультразвуковой визуализации, как правило, не содержит объектов диагностики, поэтому информация в самой нижней части визуализации может быть проигнорирована, в данном случае i=1, 2, …, [d/z]-1, z - размер интервала (ед. изм.: мм) подобласти диагностики, а [] - это операция округления до большего значения. В данном случае [zn/d] точек выборки включены в каждый сегмент подобласти диагностики. Например, когда глубина d сканирования ультразвукового сигнала составляет 20 мм и длина интервала z составляет 3 мм, n точек выборки разделяются на [d/z]-1=6 сегментов подобласти диагностики, а именно, S1-S6, где S1 соответствует интервалу 0~3 мм, S2 соответствует интервалу 3~6 мм, …, S6 соответствует интервалу 15~18 мм, и самая нижняя часть снимка (т.е. соответствующая интервалу 18~20 мм), как правило, игнорируется из-за того, что не содержит объектов диагностики.
Шаг 22: расчет значения mi, распределения Накагами ультразвукового сигнала Ri тканей органа в каждой подобласти Si диагностики.
В данном случае статистическая модель Накагами - это один из способов ультразвуковой характеризации тканей. В частности, значение mi распределения Накагами для ультразвукового сигнала Ri, соответствующего изображению тканей органа в каждой подобласти Si диагностики, рассчитывается по следующей формуле,
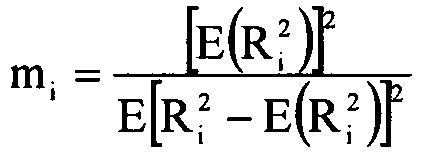
Где функция плотности распределения вероятностей для распределения Накагами равна:
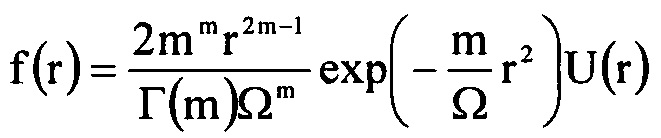
Где Е(.) - функция среднего значения, Г(.) - гамма-функция, Ω=E(r2), U(.) - единичная ступенчатая функция, m - значения распределения Накагами, r - зависимая переменная функции распределения вероятности f(r), r≥0 и m≥0; для каждой подобласти Si диагностики mi - это значение m в области Si, и Ri - это значение огибающей ультразвукового сигнала.
Одномерный ультразвуковой сигнал тканей органа соответствует до-Релеевскому распределению, когда m - это диапазон (0, 1); одномерный ультразвуковой эхосигнал соответствует Релеевскому распределению, когда m=1; и одномерный ультразвуковой эхосигнал соответствует пост-Релеевскому распределению, когда m>1.
Шаг 23: расчет веса Wi каждой подобласти Si диагностики по приведенной далее формуле и определение подобласти диагностики, соответствующей максимальному весу, в качестве граничной области тканей органа:
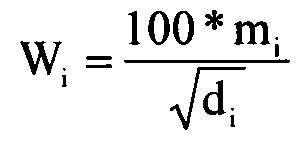
Где di - глубина сканирования в соответствии с подобластями Si диагностики, di может быть средним значением или конечным значением глубины подобластей Si диагностики. Вес Wi каждой подобласти диагностики может быть просмотрен, и подобласть диагностики, соответствующая максимальному весу, берется за граничную область тканей органа.
Шаг 24: если стандартное отклонение, соответствующее значению интенсивности одномерного ультразвукового сигнала в каждой из множества непрерывных подобластей диагностики в граничной области тканей органа меньше, чем пороговое значение стандартного отклонения, то это множество непрерывных подобластей диагностики определяются как область диагностики тканей органа.
Вычисляется стандартное отклонение SDi, соответствующее значению интенсивности ультразвукового сигнала Ri в каждой подобласти Si диагностики в граничной области тканей органа, и просматривается каждая подобласть диагностики в граничной области тканей органа; если стандартное отклонение, соответствующее значениям интенсивности одномерных ультразвуковых сигналов каждой из множества непрерывных подобластей диагностики меньше, чем пороговое значение стандартного отклонения, от определенной подобласти диагностики, то это множество непрерывных подобластей диагностики определяется как граничная область тканей органа, т.е. завершается автоматический выбор области диагностики тканей органа.
Как показано на Фиг. 4, количественная информация об эластичности может включать в себя численное значение информации о количественной оценке эластичности тканей органа в области диагностики, определенной на шаге 23, и это численное значение измеряется устройством измерения эластичности, как правило в кПа. Здесь, на вертикальной оси показана глубина сканирования, а на горизонтальной - время. Количественная информация об эластичности может также включать в себя визуализацию траектории кратковременных вибраций, распространяющихся с течением времени по глубине во время переходного процесса визуализации эластичности. Изображение также содержит линейный сегмент АВ, указывающий на распространение кратковременных вибраций. Кроме того, в соответствии с количественной информацией об эластичности тканей органа, как показано на ФИГ. 4, модуль упругости тканей органа может быть вычислен посредством расчета скорости распространения поперечной волны, создаваемой кратковременной вибрацией в области, обозначенной соответствующей отметкой.
Способ выбора области диагностики, предложенный во втором варианте осуществления настоящего изобретения, может автоматически выбирать область диагностики тканей органа посредством ультразвукового сигнала А-типа или М-типа тканей органа. Кроме того, алгоритм обладает высокой эффективностью распознавания границ тканей органа благодаря своей простоте, тем самым осуществляя автоматическую локализацию границ тканей органа в режиме реального времени.
Третий вариант осуществления изобретения:
на фиг. 5 представлена блок-схема осуществления способа выбора области диагностики, предложенного в третьем варианте осуществления настоящего изобретения; на фиг. 6 представлено изображение при осуществлении выбора области диагностики на основе ультразвукового сигнала В-типа тканей органа в третьем варианте осуществления настоящего изобретения; на фиг. 7 представлено схематичное изображение количественной оценки модуля упругости тканей органа в третьем варианте осуществления настоящего изобретения. Далее, со ссылкой на фиг. 5-7, способ содержит.
Шаг 31: разделение двухмерной ультразвуковой визуализации тканей органа на множество прямоугольных подобластей Rij диагностики, где i и j - натуральные числа для обозначения строки и столбца каждой подобласти диагностики.
Двухмерная ультразвуковая визуализация тканей органа может быть ультразвуковой визуализацией В-типа тканей органа. Исходя из допущения о том, что размер ультразвуковой визуализации В-типа составляет w*h, где w - ширина двухмерного ультразвукового изображения тканей органа, h - высота двухмерного ультразвукового изображения тканей органа (ед. изм. для w и h - пиксели), и соответствующая глубина сканирования - d (ед. изм.: мм), то h/d пикселей приходится на 1 мм глубины на линии сканирования в направлении по глубине. Изображение В-типа размером w*h разделяется на множество прямоугольных подобластей Rij диагностики.
Например, изображение В-типа размером w*h разделяется на множество квадратных подобластей Rij диагностики с длиной стороны z, аналогично первому варианту осуществления изобретения. Поскольку самая нижняя часть снимка (т.е. соответствующая самой глубокой части по глубине сканирования) и крайняя кромка в направлении по ширине ультразвуковой визуализации, как правило, не содержат объектов диагностики, то информация в самой нижней части снимка и по краям в направлении по ширине может быть проигнорирована, в данном случае

где z - это длина стороны (ед. изм.: мм) квадратной подобласти диагностики, и [] - операция округления в большую сторону. При эом как ширина, так и высота каждой квадратной подобласти Rij определения составляет [zh/d] пикселей.
Шаг 32: расчет веса Wij каждой подобласти Rij диагностики и определение подобласти диагностики, соответствующей максимальному весу, в качестве граничной области тканей органа. В данном случае, чтобы снизить объем вычислений, расчет выполняется только для половины значений веса подобласти диагностики. Например, двухмерное ультразвуковое изображение может быть разделен да две части вдоль центральной линии, и рассчитывается только вес Wkj (k=imax/2) каждой подобласти Rkj диагностики на половине двухмерного ультразвукового изображения над центральной линией, таким образом, чтобы получить граничную подобласть над центральной линией, затем граничная подобласть расширяется по направлению ширины (боковому направлению), чтобы получить цельную граничную область. Причем вес Wkj может быть вычислен по следующей формуле:

где Mkj - среднее значение градации серого для двухмерной ультразвуковой визуализации тканей органа в подобластях Rkj, SDkj - это стандартное отклонение градации серого двухмерной ультразвуковой визуализации тканей органа в областях Rkj диагностики, и dkj - это глубина сканирования подобластей Rkj диагностики. В соответствии с k=imax/2, когда двухмерная ультразвуковая визуализация тканей органа разделена на прямоугольные области с длинами сторон z,

k - целое число и imax - максимальное значение, принимаемое i.
Например, поскольку область капсулы печени демонстрирует однородный высокий эхосигнал на ультразвуковой визуализации В-типа, среднее значение градации серого граничной области тканей органа - большое; кроме того, поскольку область капсулы печени обладает однородностью в ультразвуковой визуализации В-типа, стандартное отклонение градации серого - небольшое. Чтобы избежать области черного фона с обоих сторон веерообразного ультразвукового изображения В-типа, когда для сканирования используется выпуклый аппликатор, поиск осуществляется от подобластей диагностики, расположенных на центральной линии ультразвуковой визуализации В-типа. Если подобласть Rk1 диагностики - это область с наибольшим весом среди ряда областей Rkj диагностики, подобласть Rk1 диагностики определена в качестве граничной области тканей печени.
Шаг 33: если среднее значение, соответствующее значению интенсивности изображения в каждой из множества непрерывных подобластей в граничной области тканей органа, меньше, чем порог среднего значения, и стандартное отклонение, соответствующее значениям интенсивности изображений в каждой области определения, меньше, чем порог стандартного отклонения, то это множество непрерывных подобластей диагностики определяются в качестве области диагностики тканей органа.
Начиная сканирование с определенной подобласти диагностики, если среднее значение для значений интенсивности изображения в каждой из множества непрерывных подобластей диагностики меньше, чем порог среднего значения, и стандартное отклонение значений интенсивности для изображений меньше, чем порог стандартного отклонения, то это множество непрерывных подобластей диагностики определяются в качестве области диагностики, т.е. завершен автоматический выбор области диагностики.
Как показано на Фиг. 7, количественная информация об эластичности включает в себя числовое значение (в кПа) количественной информации об эластичности тканей органа в области диагностики, показанной на структурном представлении тканей органа, полученном посредством измерения эластичности. Информация о модуле упругости включает в себя распределение модуля упругости структуры тканей органа в области диагностики. Для кодировки распределения модуля упругости может быть использовано цветовое обозначение, с различными цветами, обозначающими различные значения модуля упругости; распределение модуля упругости может быть также представлено градацией серого или другими способами, т.е. цветное кодирование или кодирование в оттенках серого, или другая форма кодирования может быть использована для представления значений интенсивности двухмерной ультразвуковой визуализации тканей органа в подобласти диагностики. Соответственно, распределение модуля диагностики дополнительно содержит шкалограмму, представляющую собой кодирование модуля упругости.
Способ выбора области диагностики, предложенный в третьем варианте осуществления настоящего изобретения, может автоматически выбирать область диагностики тканей органа посредством ультразвуковой визуализации В-типа тканей органа. Кроме того, алгоритм обладает высокой эффективностью распознавания границ тканей органа благодаря своей простоте, тем самым осуществляя автоматическую локализацию границ тканей органа в режиме реального времени.
Четвертый вариант осуществления изобретения:
на фиг. 8 представлена блок-схема осуществления способа выбора области диагностики, предложенного в четвертом варианте осуществления настоящего изобретения; на фиг. 9 представлено цветовое изображение границ трехмерной визуализации на основе тканей органа четвертого варианта осуществления настоящего изобретения; на фиг 10 представлено цветовое изображение для выбора области диагностики на основе трехмерной визуализации тканей органа в четвертом варианте осуществления настоящего изобретения; и на фиг. 11 представлено схематичное изображение количественной оценки модуля упругости тканей органа в четвертом варианте осуществления настоящего изобретения. Далее, со ссылкой на фиг. 8-11, способ содержит.
Шаг 41: извлечение бинарной визуализации кожной ткани и бинарной визуализации костной ткани на КТ - изображении (компьютерная томография) тканей органа или МРТ - изображении тканей органа, используя метод увеличения сегментации областей.
Сначала извлекается бинарная визуализация кожной ткани. Пиксель с координатами на изображении (0, 0) используется в качестве исходной точки, и бинарная визуализация кожных тканей извлекается с помощью метода разрастания сегментации, причем критерий разрастания области для КТ - значения равен [-1024, -500] (ед. Хаунсфилда, Хайнц).
Затем извлекается бинарная визуализация костной ткани, включая бинарную визуализацию позвоночника и ребер. Пороговая сегментация с пороговым диапазоном [350, 1024] ед. X. осуществляется на всем изображении, чтобы извлечь бинарную визуализацию костной ткани.
Шаг 42: расчет центроида бинарного изображения кости и расчет точки на бинарном изображении кожи, ближайшей к центроиду.
Вычисляется центроид PC бинарного изображения кости. Поскольку ребра, как правило, симметричны вокруг позвоночника, и позвоночник занимает большую часть на изображении визуализации костей, центроид визуализации кости - это центроид Рс позвонков.
Точка на бинарном изображении кожи, ближайшая к центроиду PC, обозначена как точка PN, начиная отсчет от центроида PC позвоночника.
Шаг 43: разделение информации о тканях органа на четыре квадранта на основе центроида и точки, ближайшей к центроиду.
КТ - изображение разделяется на четыре квадранта с использованием центроида PC и точки PN, ближайшей к центроиду, т.е. прямая линия, проходящая через центроид PC и точку PN, ближайшую к центроиду PC, принята за вертикальную ось, а прямая линия, проходящая через центроид PC и перпендикулярная вертикальной оси, принята за горизонтальную ось. Взяв ткани печени в качестве примера, большая часть области печени находится во втором квадранте печени.
Шаг 44: сопряжение каждой реберной точки во втором квадранте для получения сопряженной дуги ребра
Каждая точка ребра во втором квадранте сопрягается с использованием В-сплайновой кривой или кривой для кожи для получения сопряженной дуги ребра.
Шаг 45: перемещение сопряженной дуги ребра в направлении первого квадранта с использованием заранее заданного значения для того, чтобы получить граничную кривую, и определение области между этой граничной кривой и сопряженной дугой ребра в качестве граничной области тканей органа.
Поскольку дуга ребра находится рядом с капсулой печени, дуга ребра перемещается вовнутрь на заранее заданное значение и принимается за граничную кривую, а область между этой граничной кривой и сопряженной дугой ребра определяется как граничная область тканей органа.
В данном случае заранее заданное значение может составлять 5 мм.
Шаг 46: определение области, окруженной граничной областью тканей органа, в качестве области тканей органа.
Шаг 47: разделение области тканей органа на множество подобластей диагностики.
Шаг 48: расчет стандартного отклонения, соответствующего значениям интенсивности, и среднего значения, соответствующего значениям интенсивности двухмерного ультразвукового изображения тканей органа в каждой из подобластей диагностики.
Шаг 49: если среднее значение, соответствующее значению интенсивности изображения в каждой из множества непрерывных подобластей диагностики в области, окруженной граничной областью тканей органа, меньше, чем порог среднего значения, и стандартное отклонение, соответствующее значениям интенсивности изображения в каждой области определения, меньше, чем порог стандартного отклонения, то множество непрерывных подобластей диагностики определяются в качестве области диагностики тканей органа.
В каждой подобласти диагностики в границах печени выполняется исследование, начиная с границы тканей печени, и, если среднее значение для значений интенсивности изображения в каждой из множества непрерывных подобластей диагностики меньше, чем порог среднего значения, и стандартное отклонение значений интенсивности изображений меньше, чем порог стандартного отклонения, то это множество непрерывных подобластей диагностики определяются в качестве области диагностики, т.е. завершен автоматический выбор области диагностики.
Как показано на Фиг. 11, количественная информация об эластичности включает в себя числовое значение (в кПа) количественной информации об эластичности тканей органа, показанного на структурном изображении тканей органа, полученное посредством измерения эластичности. При этом информация о модуле упругости также может включать в себя распределение модуля упругости тканей в области, отмеченной индикаторной отметкой, на структурном изображении тканей. При это возможно использование цветового кодирования визуализации распределения, с использованием различных цветов для представления различных значений модуля упругости; визуализация распределения может быть также представлена в градации серого или другим способом. Соответственно, распределение модуля упругости дополнительно содержит шкалограмму, представляющую собой кодирование модуля упругости.
Следует отметить, что, когда автоматическое распознавание граничной области тканей органа и автоматическая корректировка местоположения и размера области диагностики осуществлена с использованием КТ - визуализации или МРТ - визуализации, то автоматически выбираемая область диагностики может быть 3-мерной.
Если взять последовательные КТ - изображения в качестве примера, то для каждого кадра КТ - изображения область диагностики изображения в кадре изображения тканей органа автоматически выбирается, используя способ для выбора области диагностики, предложенный в настоящем варианте осуществления изобретения. Затем трехмерная геометрия, т.е. трехмерная область диагностики, реконструируется посредством использования каждой области диагностики, соответствующей каждому кадру изображений. Датчик диагностики эластичности используется для определения информации об эластичности в двухмерной области диагностики каждого кадра КТ - изображения и реконструкции трехмерного распределения эластичности тканей органа, тем самым позволяя получить трехмерную информацию об эластичности тканей органа.
Способ для выбора области определения, предложенный в четвертом варианте осуществления настоящего изобретения, может автоматически выбирать область диагностики тканей органа, используя трехмерное изображение тканей органа, например, КТ - изображение тканей органа или МРТ - изображение тканей органа. Кроме того, алгоритм обладает высокой эффективностью распознавания границ тканей органа благодаря своей простоте, тем самым осуществляя автоматическую локализацию границ тканей органа в режиме реального времени.
Пятый вариант осуществления изобретения.
На фиг. 12 представлено схематичное изображение структуры устройства для выбора области диагностики, предложенного в пятом варианте осуществления настоящего изобретения. Как показано на Фиг. 12, устройство для выбора области диагностики, раскрытое в настоящем изобретении, содержит: блок 51 разделения области, выполненный с возможностью разделения информации о тканях органа, которую необходимо распознать, на множество подобластей диагностики; блок 52 расчета характеристического параметра, выполненный с возможностью расчета характеристического параметра информации о тканях органа в подобластях диагностики; блок 53 распознавания граничной области, выполненный с возможностью определения граничной области тканей органа в соответствии с информацией о тканях органа, которую необходимо распознать; и блок 54 определения области диагностики, выполненный с возможностью определения области диагностики тканей органа в соответствии с граничной областью тканей органа и заранее заданным условием для характеристического параметра.
Причем устройство может дополнительно содержать: блок расчета значения эластичности, выполненный с возможностью расчета значения эластичности тканей органа в области диагностики тканей органа.
При этом, если информация о тканях органа представляет собой одномерную, двухмерную или трехмерную визуализацию или сигнал тканей органа, то заранее заданным условием для характеристического параметра может быть или среднее значение или стандартное отклонение, соответствующие значению интенсивности визуализации или сигнала в пределах каждой подобласти диагностики, удовлетворяющие заранее заданной глубине.
При этом, если информация о тканях органа представляет собой одномерный ультразвуковой сигнал тканей органа, то блок 53 распознавания граничной области может содержать: вычислительный подблок, выполненный с возможностью расчета значения mi распределения Накагами одномерного ультразвукового сигнала Ri тканей органа в каждой подобласти Si диагностики; и подблок распознавания области, выполненный с возможностью расчета веса Wi каждой подобласти Si диагностики по приведенной ниже формуле и определения подобласти диагностики, соответствующей максимальному весу, в качестве граничной области органа:

Причем, если информация о тканях органа представляет собой двухмерную ультразвуковую визуализацию тканей органа, то блок 51 разделения области может быть, в частности, выполнен с возможностью расчета веса Wkj каждой подобласти Rkj в соответствии с приведенной ниже формулой, и определения подобласти, соответствующей максимальному весу, в качестве граничной области тканей органа.

где Mkj - среднее значение градации серого двухмерной ультразвуковой визуализации тканей органа в подобластях Rkj, SDkj - это стандартное отклонение градации серого двухмерной ультразвуковой визуализации тканей органа в областях Rkj диагностики, и dkj - это глубина сканирования, соответствующая областям Rkj диагностики; и k=imax/2.
Двухмерная ультразвуковая визуализация тканей органа разделена на множество прямоугольных подобластей Rij диагностики; блок 53 распознавания граничной области может быть, в частности, выполнен с возможностью расчета веса Wkj каждой подобласти Rkj в соответствии со приведенной ниже формулой, и определения подобласти, соответствующей максимальному весу, в качестве граничной области тканей органа:
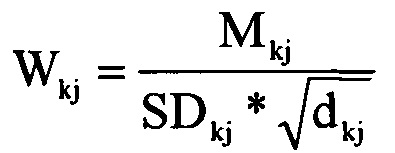
где Mkj - среднее значение градации серого двухмерной ультразвуковой визуализации тканей органа в подобластях Rkj, SDkj - это стандартное отклонение градации серого двухмерной ультразвуковой визуализации тканей органа в области диагностики, и dkj - это глубина сканирования, соответствующая областям диагностики; и k=imax/2.
При этом, если информация о тканях органа представляет собой КТ - визуализацию тканей органа или МРТ - визуализацию тканей органа, то блок 53 распознавания граничной области может, в частности, содержать: подблок получения бинарного изображения, выполненный с возможностью извлечения бинарного изображения кожи и бинарного изображения кости на КТ - изображении тканей органа или МРТ - изображении тканей органа посредством способа сегментации изображения; и подблок определения характеристической точки, выполненный с возможностью расчета центроида бинарного изображения кости и расчета точки на бинарном изображении кожи, ближайшей к центроиду; подблок разделения изображения, выполненный с возможностью разделения изображения тканей органа на четыре квадранта в соответствии с центроидом и точкой, ближайшей к центроиду; подблок сопряжения дуги, выполненный с возможностью сопряжения каждой реберной точки во втором квадранте для получения сопряженной дуги ребра; и подблок определения граничной области, выполненный с возможностью перемещения сопряженной дуги ребра в направлении к первому квадранту с использованием заранее заданного значения, чтобы получить кривую граничной области, и определения области между кривой граничной области и сопряженной дугой ребра в качестве граничной области тканей органа.
Устройство для выбора области диагностики, предложенное в пятом варианте осуществления настоящего изобретения, разделяет информацию о тканях органа, которые еобходимо распознать, на множество подобластей диагностики, вычисляет характеристический параметр информации о тканях органа в подобластях диагностики, определяет граничную область тканей органа в соответствии с информацией о тканях органа, которые необходимо распознать, и определяет область диагностики тканей органа в соответствии с определенной граничной областью тканей органа и заранее заданным условием для характеристического параметра. В этом устройстве местоположение и размер области диагностики различаются, когда отличается информация о тканях органа, т.е. устройство может корректировать местоположение и размер области диагностики.
Шестой вариант осуществления изобретения.
На фиг. 13 представлено схематичное изображение структуры системы определения эластичности, предложенной в шестом варианте осуществления настоящего изобретения. Как показано на Фиг. 13, система определения эластичности, раскрытая в настоящем варианте осуществления, может содержать устройство 61 получения информации, устройство 63 визуализации эластичности, устройство 64 настройки датчика, обрабатывающее устройство 65 и отображающее устройство 66, и дополнительно включает в себя устройство для выбора области 62 диагностики, предложенное в пятом варианте осуществления настоящего изобретения, причем устройство 61 получения информации выполнено с возможностью получения информации о тканях органа, которую необходимо распознать; устройство 64 настройки датчика выполнено с возможностью корректировки положения датчика в устройстве визуализации эластичности, таким образом, что диапазон действия датчика включает в себя область диагностики, определенную устройством для выбора области диагностики; устройство 63 визуализации эластичности выполнено с возможностью получения информации об эластичности тканей органа; обрабатывающее устройство 65 выполнено с возможностью обработки информации об эластичности, полученной устройством визуализации эластичности, тем самым получая информацию об эластичности в области диагностики; и отображающее устройство 66 выполнено с возможностью отображения информации об эластичности в области диагностики.
Система определения эластичности, предложенная в шестом варианте осуществления настоящего изобретения, способна автоматически распознавать граничную область тканей органа и автоматически корректировать положение и размер области диагностики, тем самым обеспечивая экономию времени диагностики эластичности, снижение различий в работе разных операторов и в работе одного оператора, выполняющего различные действия, и точное, быстрое определение эластичности тканей органа с высокой степенью воспроизводимости.
Описание, приведенное выше, - это не более, чем предпочтительные варианты осуществления настоящего изобретения, и не предназначено для ограничения вариантов осуществления настоящего изобретения. Различные изменения могут быть внесены в варианты осуществления настоящего изобретения специалистами в данной области техники. Любые модификации, эквивалентные замены, улучшения и т.д. в рамках объема и принципа вариантов осуществления настоящего изобретения считаются включенными в объем охраны вариантов осуществления настоящего изобретения.
Реферат
Группа изобретений относится к медицине и представлена способом, устройством выбора области диагностики и системой определения эластичности. Способ включает разделение визуализирующей информации о тканях органа, которую необходимо определить во множестве подобластей диагностики, и расчет характеристического параметра информации о тканях органа в пределах подобласти диагностики. А также определение граничной области тканей органа в соответствии с визуализирующей информацией о тканях органа, которые необходимо идентифицировать, и определение области диагностики тканей органа в соответствии с граничной областью тканей органа и заранее заданным условием для характеристического параметра. Устройство содержит: блок разделения области, блок расчета характеристического параметра, блок распознавания граничной области и блок определения области диагностики. Система содержит: устройство получения информации, устройство визуализации изображения, устройство настройки датчика и отображающее устройство, устройство для выбора области диагностики. Группа изобретений позволяет определить границы тканей органа в соответствии с визуализирующей информацией о тканях органа и автоматически корректировать область диагностики в соответствии с границами тканей органа за счет разделения визуализирующей информации о тканях, которые необходимо распознать на множество подобластей диагностики и расчета характеристического параметра визуализирующей информации о тканях органа в подобластях диагностики. 3 н. и 10 з.п. ф-лы, 13 ил.
Формула




Документы, цитированные в отчёте о поиске
Система и способ для автоматического планирования двухмерных видов в объемных медицинских изображениях

Комментарии