Устройство и способ измерения вегетативных функций для диагностики и подтверждения эффективности курса лечения пациента и его результатов - RU2722748C2
Код документа: RU2722748C2
Чертежи






















Описание
РОДСТВЕННЫЕ ПАТЕНТНЫЕ ЗАЯВКИ
Данная заявка испрашивает приоритет находящейся на рассмотрении предварительной заявки на патент США №62/101992, поданной 10 января 2015 г., под названием «METHOD AND APPARATUS FOR THE MEASUREMENT OF AUTONOMIC FUNCTION», описание которой включено в данный документ посредством ссылки в полном объеме.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к системе для измерения и диагностики боли (PMD) для биоаналитического анализа активности матрицы боли и вегетативной нервной системы для диагностики и обоснования лечения пациентов, состояния здоровья и результатов лечения. Система PMD реализована с использованием медицинских устройств для измерения и регистрации объективных измерений боли посредством мониторинга пациентов и анализа связанных с ними биологических, психологических, социальных, экологических и демографических факторов, которые могут способствовать физиологическим результатам лечения для пациентов и влиять на них, а также посредством анализа улучшить диагностику боли, оценку связанных болезненных состояний и вариантов лечения.
УРОВЕНЬ ТЕХНИКИ
В настоящее время не существует достоверного и надежного способа объективного количественного определения испытываемого чувства боли человека (Younger J и др., Pain Outcomes: A Brief Review of Instruments and Techniques. Curr Pain Headache Rep., февраль 2009 г.; 13(1):39-43). A Brief Review of Instruments and Techniques. Curr Pain Headache Rep., февраль 2009 г.; 13(1):39-43). В Соединенных Штатах Америки приблизительно 100 миллионов взрослых - больше, чем количество, пораженных сердечными заболеваниями, диабетом и раком, вместе взятые - страдают от широко распространенных хронических болевых состояний (Tsang, А и др., Common chronic pain conditions in developed and developing countries: Gender and age differences and comor- bidity with depression-anxiety disorders. Journal of Pain. 2008 г.; 9(10):883-891.) с ежегодными национальными экономическими издержками, связанными с хронической болью, которые по оценкам в 2011 году составили 560-635 миллиардов долларов США. Старение населения Соединенных Штатах Америки означает, что все большее число американцев будут страдать от болезней, с которыми связана хроническая боль, - диабет, сердечно-сосудистые расстройства, артрит и рак, наряду с некоторыми другими (Cherry и др., Population aging and the use of office-based physician services. NCHS Data Brief, №41. Хьяттсвилль, MD: Национальный центр медицинской статистики). Увеличение количества людей с ожирением приведет к большему количеству ортопедических проблем, которые связаны с разрушением хряща (Richettel и др., 2011 г.). В результате этого будет проведено большее количество операций по эндопротезированию суставов, встречающихся в более молодых группах населения (Harms, S., R. Larson, А.Е. Sahmoun, и J.R. Beal. 2007. Ожирение увеличивает вероятность тотального эндопротезирования суставов среди молодежи. International Orthopaedics 31(1):23-26.; Changulani и др., 2008 г.); что приводит к ассоциированной острой, а также потенциально к хронической боли. Увеличение количества болезненных состояний, которые связаны с болью, будет проявляться не только в США. В британском докладе от 2009 года говорится, что «хроническая боль в два-три раза чаще встречается сейчас, чем это было 40 лет назад» (Министерство здравоохранения Великобритании, 2009 г. 150 years of the chief medical officer: On the state of public health. Annual Report. Лондон: Министерство здравоохранения Великобритании, стр. 34). Нет никаких сомнений в том, что боль и другие комбинированные хронические заболевания являются серьезной проблемой общественного здравоохранения. Согласно исследованию Института медицины от 2011 года «Relieving Pain in America: A Blueprint for Transforming Prevention, Care, Education, and Research», боль является уникальным индивидуальным и субъективным ощущением, которое зависит от множества биологических, психологических и социальных факторов, и различные группы населения испытывают боль по-разному (IOM (Institute of Medicine), 2011 г. Relieving Pain in America: A Blueprint for Transforming Prevention, Care, Education, and Research. Вашингтон, округ Колумбия: The National Academies Press.). Причина, по которой один человек страдает от травмы и сообщает о небольшой боли, а другой человек с похожей травмой сообщает о сильной боли, зависит от многих факторов: генетических характеристик, общего состояния здоровья и сопутствующих заболеваний, ощущений боли с детства, системы обработки мозга, эмоционального и когнитивного контекста, в которых возникает боль, и от культурных и социальных факторов. Дорогостоящие процедуры часто выполняется в тех случаях, когда должны быть рассмотрены другие меры, такие как профилактика, консультирование и облегчение самообслуживанию, которые являются общими чертами успешного лечения. Кроме того, адекватное лечение боли и последующее наблюдение могут быть затруднены в связи с сочетанием неопределенного диагноза и социальной стигмы, сознательно или бессознательно примененной к людям, сообщающим о боли, особенно когда они не отвечают легко на лечение (IOM (Institute of Medicine), 2011 г. Relieving Pain in America: A Blueprint for Transforming Prevention, Care, Education, and Research. Вашингтон, округ Колумбия: The National Academies Press). По этим причинам является важным разработать объективный способ для измерения боли и общих физических симптомов, но в то же время для дальнейшего объединения и анализа полученных датчиком данных с дополнительными факторами, которые влияют на индивидуальное ощущение боли и другими связанными с этим проблемами здравоохранения и болезненными состояниями. В настоящее время врачи и специалист по уходу за больными берут за основу собственное описание симптомов пациента, таких как боль, что является примером физического результата, который не соответствует объективному измерению. В настоящее время для оценки боли используются одномерные шкалы. Широко используемая шкала представляет собой цифровую рейтинговую шкалу (ЦРШ), которая обычно состоит из оценок от 0 до 10, при этом крайние левые значения обозначают «отсутствие боли», а крайний правый конец шкалы означает «наихудшая боль, которую только можно вообразить». В общем, для пациента является трудным точно описать свою боль, но особенно в условиях под психологическим давлением или, например, для групп пациентов, которые могут испытывать трудности с общением, например для детей, пожилых пациентов, страдающих деменцией, и для тех, кто не говорит на том же языке как и лечащий врач. Клинические данные результатов исследования, которые можно увидеть - например, сломанная кость на рентгеновском снимке, не обязательно хорошо коррелирует со степенью тяжести боли, которую ощущает пациент. Пожилые пациенты испытывают боль в два раза чаще, чем другие люди в возрасте до 60 лет, что, как считается, связано с их неспособностью точно сообщать о боли и интенсивности или источнике боли (Herr K и др., Assessment and measurement of pain in older adults, Clin Geriatric Med, август 2001 г.; 17(3):457-vi) (Weiner D и др., 1999 г. Pain in nursing home residents: An exploration of prevalence, staff perceptions, and practical aspects of measurement. Clin of J Pain. 1999 г.; 15:92 [PubMed: 10382922]). Люди, которые страдают от боли, могут находить грубые средства неадекватного языка для того, чтобы передавать характер и интенсивность своего ощущения и его значение для них. Это может быть существенным препятствием для получения адекватного лечения (Werner, А., и K. Malterud, 2003 г. It is hard work behaving as a credible patient: Encounters between women with chronic pain and their doctors. Social Science & Medicine 57(8):1409-1419). В соответствии с данными Института медицины, (IOM, 2011 г.), боль и ее степень тяжести, то, как она развивается, и эффективность лечения зависят от совокупности биологических, психологических и социальных факторов, таких как:
Биологические - степень болезни или травмы, и имеет ли человек другие болезни, находится ли под воздействием стресса, или имеет определенные гены или предрасполагающие факторы, которые влияют на болевую толерантность или пороговые значения боли;
Психологические - тревога, страх, чувство вины, гнев, депрессия, и мысли о том, что боль представляет собой нечто худшее, чем это есть на самом деле, и что человек не в силах управлять им (Ochsner, K., J. Zaki, J. Hanelin, D. Ludlow, K. Knierim, Т. Ramachandran, G. Glover, и S. Mackey. 2008 г. Your pain or mine? Common and distinct neural systems supporting the perception of pain in self and other. Social Cognitive and Affective Neuroscience 3(2):144-160);
Социальные - реакция близких людей на боль - будь то поддержка, критика, благоприятное поведение или отталкивание - требования рабочей среды, доступ к медицинскому обслуживанию, культура и семейные отношения, а также убеждения.
Помимо отсутствия доступных в настоящее время средств для объективного измерения боли и согласия в последнее время о том, что боль и другие сложные хронические заболевания представляют собой совокупность биологических, психологических и социальных факторов, по-прежнему необходимо решать существующие проблемы с недостаточным лечением пациентов, которые страдают хронической болью, в результате сокращения пребывания в больнице и отсутствия контроля на дому и телемедицины. Как указано в докладе Института медицины «Relieving Pain in America»: В 2007 году почти половина пациентов в отделении неотложной помощи ощущала боль, которая была тяжелой в 22% случаев или умеренной в 23% случаев (Niska и др., National Hospital Ambulatory Medical Care Survey: сводка отделения неотложной помощи в 2007 году, National Health Statistics Reports 26. Хьяттсвилль, MD: Национальный центр медицинской статистики). Боль в грудной клетке или боль в брюшной полости были основной причиной обращения среди лиц в возрасте от 15 до 64 лет, в то время как боль в грудной клетке или в брюшной полости в сочетании с одышкой были главной причиной для обращения среди тех лиц, чей возраст составлял 65 лет и старше. В 2009 году было проведено 10 миллионов стационарных хирургических операций и 17,4 миллиона хирургических операций в амбулаторных отделениях больниц (AHA (Американская больничная ассоциация), 2011 г. Trendwatch chartbook 2011 г., Таблицы 3.1 и 3.4. http://www.aha.org/aha/research-and-trends/chartbook/index.html (доступ 03 марта 2011 г.)). От 10 до 50 процентов людей, которым систематически выполняются хирургические операции - пластика паховой грыжи, операции на молочной железе и торакальные операции, ампутация нижних конечностей и операции шунтирования коронарной артерии - продолжают испытывать хроническую боль, во многих случаях в связи с повреждением нервов в операционном поле во время операции (Kehlet, и др., Persistent postsurgical pain: Risk factors and prevention. Persistent postsurgical pain: Risk factors and prevention. Lancet, 2006 г.; 367(9522):1618-1625.). В настоящее время сроки пребывания в стационаре сократились, в среднем, от 7,2 дней в 1989 году до 5,4 дней в 2009 году (AHA, 2011 г.) - и тенденция в направлении амбулаторных хирургических операций не может позволить достаточную возможность оценить послеоперационную боль пациента или обеспечить соответствующий курс послеоперационной анальгезии (возможно, такой, которую можно проводить в домашних условиях), которая показала, что она является эффективной при эндопротезировании тазобедренного и коленного суставов (Schug и др., Chronic pain after surgery or injury. 2011 г., Pain Clinical Updates 19. Сиэтл, Вашингтон: Международная ассоциация по изучению боли). В настоящее время нет возможности контролировать при амбулаторном лечении ответную реакцию на фармацевтическое лечение и эффективность лечения, которое связано с болью и другими связанными с ней хроническими заболеваниями.
Недавние усовершенствования сенсорной технологии, мощные и миниатюрные микроконтроллеры, системы на чипе (SOC), беспроводная связь с низким энергопотреблением и управление питанием создают новые возможности для новых электронных устройств, носимых в качестве предмета одежды или украшения, которые обеспечивают возможность находящимся на длительном лечении пациентам на дому мониторинг физиологических измерений с использованием носимых датчиков пациента, облачную обработку данных для хранения и анализа данных, а интеграция с сетями и мобильными устройствами обеспечивает связь с поставщиками медицинских услуг и системами здравоохранения. То, что не измеряется в этих устройствах предшествующего уровня техники, так это измерение степени тяжести боли, которую пациент испытывает либо в связи с непосредственной травмой, или же как хроническое следствие болезни или пребывания в больнице. Используя систему для измерения и диагностики боли (PMD) в соответствии с данным изобретением, боль объективно измеряется для того, чтобы предоставить в настоящее время недоступную биофизическую информацию, которая будет способствовать в диагностике, выборе и подтверждении лечения и может обеспечить стимулы пациентам продолжать эффективные способы лечения. Посредством отслеживания и оценивания биофизические показатели, активность матрицы боли в форме контура модуляции боли с входами, которые возникают во многих областях, включая кортикальные участки, ростральную переднюю поясную кору (rACC), прегенуальную поясную кору (рСС), соматосенсорную кору 1 и 2, таламус и гипоталамус, островок, миндалевидное тело, область периакведуктального серого вещества головного мозга (PAG), и дополнительные нисходящие структуры путей и тонус блуждающего нерва, могут быть соотнесены для определения стресса, когнитивных функций, эмоций, болезненных состояний и оценки чувства угрозы для определения болевого состояния, модуляции боли, уровня здоровья и исцеления, а также уязвимости пациента по отношению к болезни (Ossipov и др., Central Modulation of Pain, The Journal of Clinical Investigations: ноябрь 2010 г.; 120(11): 3779-3787).
Измерения боли также могут помочь врачам назначать правильную дозировку, основанную на реакции пациента по отношению к лекарственному препарату. Пациенты получают неадекватный доступ к обезболивающим средствам из-за широко распространенного злоупотребления опиоидами, которое является результатом нежелания многих в медицинском сообществе писать рецепты для неинституционализированных пациентов. По мнению исследователей из Центра по контролю и профилактике заболеваний (CDC) для того, чтобы обратить вспять эпидемию смертей от передозировки опиоидных наркотиков и предотвратить связанную с опиоидами заболеваемость, необходимо наращивать усилия по улучшению безопасного назначения рецептурных опиоидов (Paulozzi LJ, Jones С, Mack K, Rudd R. Vital signs: overdoses of prescription opioid pain relievers - США, 1999-2008 гг., MMWR Morb Mortal Wkly Rep 2011 г..; 60:1487-92). В период между 2013 и 2014 годами стандартизированный по возрасту уровень смертности при использовании синтетических опиоидов, за исключением метадона (например, фентанила), увеличилась на 80% (Rudd и др. Increases in Drug and Opioid Overdose Deaths - США, 2000-2014 г. г.CDC: Morbidity and Mortality Weekly Report (MMWR). 01 января 2016 г. / 64(50);1378-82). В 2014 году смертность от передозировки наркотиков в Соединенных Штатах приблизительно в полтора раза превышала смертность от автомобильных аварий (CDC. Wide-ranging online data for epidemiologic research (WONDER). Атланта, Джорджия: CDC, Национальный центр медицинской статистики; 2015 г. Доступно по адресу http://wonder.cdc.gov). Адекватное лечение боли и последующее наблюдение могут быть затруднены в связи с сочетанием неопределенного диагноза и социальной стигмы, сознательно или бессознательно примененной к людям, сообщающим о боли, особенно когда они не отвечают легко на лечение (IOM, 2011 г.).
В настоящее время нет объективного критерия для боли, и в результате этого врачи сталкиваются с проблемами как при диагностике, так и при лечение боли. Монитор боли позволит разрешить вопросы, связанные с серьезным кризисом здравоохранения, путем содействия в прописывании опиоидных болеутоляющих средств поставщиками медицинских услуг; в частности, в назначении обоснованных доз. Американское гериатрическое общество ссылается на задержки в доступе к предписанным опиоидам для пациентов в домах престарелых с медицинским обслуживанием, включая тех, кто неизлечимо болен, и Американское онкологическое общество признало частую недоступность опиоидов, которые необходимы для лечения некоторых видов боли (IOM, 2011 г.). В соответствии с планом действий Белого дома, в период с 2000 года по 2009 год количество опиоидных рецептов, выданных розничными аптеками, выросло на 48 процентов до 257 миллионов. Тем не менее, по причине расширенных нормативных положений по ограничению злоупотребления опиоидами, двадцать девять процентов врачей первичной медико-санитарной помощи и 16 процентов специалистов по боли сообщают, что они назначают опиоиды реже, чем они считают целесообразным в связи с опасениями относительно последствий законодательного регулирования (Breuer и др., Pain management by primary care physicians, pain physicians, chiropractors, and acupuncturists: A national survey. Southern Medical Journal 2010 г. 103(8):738-747).
Необходимы точная дозировка лекарств, раннее вмешательство и обучение врача. Ниже приведен список потенциальной выгоды от внесения новшеств в предотвращение боли, уход, обучение и исследования в докладе Института медицины (IOM) 2011 г. Relieving Pain in America:
улучшение лечения острой боли посредством обучения самопомощи и лучшего клинического лечения для того, чтобы избежать прогрессирования хронической боли, что является более трудным и более дорогостоящим для лечения и приводит к использованию здравоохранения высокого уровня;
уменьшение проблем со здоровьем и осложнениями других физических и психических заболеваний и состояний, связанных с хронической болью, которые также являются дорогостоящими для лечения;
более рентабельный уход за людьми с хронической болью, когда чаще используются самопомощь и мультимодальные подходы, при этом врачи первичной медико-санитарной помощи получают обучение и имеют право лечить большинство людей должным образом, и избегают ненужных диагностических тестов и процедур, а также направления к специалистам;
лучший индивидуальный подход к лечению для лиц, который основан на новых данных результатов исследований, и интеграция этих данных результатов исследований в схемы лечения пациентов. Устройства для управляемой пациентом анальгезии (РСА), которые обеспечивают возможность пациенту самостоятельно вводить болеутоляющие средства, используются для введения лекарств в условиях учреждений. Несмотря на то, что в настоящее время нет коммерчески доступного способа для объективного измерения боли и растет озабоченность по поводу злоупотребления опиоидами и другими предписаниями, РСА используется и имеет преимущества. Исследования показывают, что РСА превосходит даже периодические внутривенные инъекции болеутоляющих средств (D'Arcy, Y. (2007 г.). Pain pointers: Safe pain relief at the push of a button. Nursing Made Incredibly Easy, 5(5), 9-12). Пациенты используют меньше наркотических средств, не должны ждать, пока медсестра принесет лекарственный препарат, и получают более полное удовлетворение с лучшей анальгезией и более низкими показателями боли, чем пациенты, которые получают анальгезию со стороны медсестер (Smeltzer, S., и др. (2008 г.). Textbook of medical surgical nursing (11-е изд.). Филадельфия: Липпинкотт). Контролируя боль, пациенты могут двигаться более легко, совершать глубокие вдохи и раньше начинать передвигаться, снижая при этом риск послеоперационных осложнений (D'Arcy, Y. (2008 г.). Keep your patient safe during PCA. Nursing, 38(1), 50-55).
Несмотря на эти преимущества, есть негативные моменты. Например, они не могут быть легко использованы, если и используются, то очень мало, для новорожденных, маленьких детей и других лиц, которые не могут управлять устройством либо из-за инвалидности вследствие физической причины, такой как, например, травма спинного мозга, или людей, которые не могут или не хотят понимать инструкции по использованию. Пациенты, которые страдают ожирением или астмой, или те, кто употребляют лекарственные средства, которые потенцируют действие опиатов, такие как, например, седативные средства или снотворные средства, миорелаксанты и противорвотные средства, не должны использовать РСА. Пациенты с апноэ во сне не должны использовать РСА (D'Arcy, Y. (2011 г.). New thinking about postoperative pain management. OR Nurse, 51(11): 28-36). Кроме того, имеющиеся на данный момент устройства для РСА продолжают работать на основе субъективного критерия самооценки. Без средств для нормализации самооценки пациента необоснованное лечение остается проблемой для пациентов. РСА в сочетании с объективным измерением боли с использованием медицинских устройств PainTrace, а также компонентов и функциональных возможностей системы для измерения и диагностики боли (PMD), в соответствии с данным изобретением, может уменьшить многие существующие проблемы.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Система для измерения и диагностики боли (PMD) в соответствии с данным изобретением использует медицинские устройства для получения данных и физиологических показателей, связанных с болью и демографией, медицинской информацией, физической активностью, а также информацией о пациенте и медицинском обслуживании, полученной дополнительно за счет использования компонентов и функций системы PMD для того, чтобы установить исходные уровни как для здоровых пациентов, так и для пациентов, которые могут страдать от различных болезненных состояний. При использовании системы PMD, собранные данные, имеющие отношение к боли и связанными с ней физиологическими показателями, преобразуются в диагностические показатели или инструменты для медицинского обслуживания, основанные на факторах, которые связаны с демографией пациентов, сопутствующими заболеваниями, хирургическими вмешательствами и другими известными влияющими факторами, которые влияют на общее ощущение боли и кроме того, являются показателями здоровья, включая генетические, биомаркеры, прошлые ощущения, неврологическую модуляцию боли в болевом матриксе, физическую активность, а также эмоциональные и культурные факторы влияния. Система PMD будет получать и хранить данные измерений боли, физиологические показатели и релевантные данные, соответствующие исследованиям и текущему «золотому стандарту», визуальной аналоговой шкале (ВАШ) и аналогичным шкалам для самоотчета о боли, для преобразования собранных данных, чтобы создать более точную и надежную шкалу измерения боли, а также диагностику и мониторинг связанных заболеваний на основании физиологических показателей и биопсихосоциальных факторов, связанных с ощущением боли.
Недавние данные, полученные в результате неврологических исследований, определили существование в мозге матрицы боли, ответственного за обработку и модуляцию боли. Центральное ядро миндалевидного тела (СеА) является центральным по отношению к этому болевому матриксу с неврологическими связями, связанными с областью периакведуктального серого вещества головного мозга (PAG), ответственной за нисходящие пути боли от головного мозга, и кортикальным участкам, которые вместе с миндалевидным телом обеспечивают эмоционально-аффективную модуляцию когнитивных функций при боли (Ossipov). и др. Central Modulation of Pain, The Journal of Clinical Investigations: ноябрь 2010 г.; 120(11): 3779-3787, Neugebauer и др., Forebrain pain mechanisms. Brain Res Rev. 2009 г.; 60 (1): 226-242). В частности, миндалевидное тело образует самую большую асимметрию, и исследования показали, что миндалевидное тело является критически важным компонентом матрицы боли (Veinante Р и др., The Amygdala between sensation and affect: a role in Pain. J Molec Psych 2013 г., 1:9 http://www.jmolecularpsychiatry.com/content/1/1/9). Исследования показали, что только правое центральное ядро миндалевидного тела (СеА) связано как с острой, так и с хронической болью (Ossimov, 33-40), (Ji, G. и др., Hemispheric lateralization of pain processing by amygdal neurons. J Neurophysiol. 2009 г.; 102 (4): 253-2264, Carrsquillo, Y. и др., Hemispheric lateralization of a molecular signal for pain modulation in the amygdala. Mol Pain. 2008 г.; 4:24). Посредством измерения электродермальной активности (ЭДА) с использованием контралатерального размещения датчиков или электродов, прямые измерения обработки боли головным мозгом от «матрицы боли» демонстрируют «совокупность областей мозга, которые участвуют в неврологических функциях, включающих когнитивную деятельность, эмоции, мотивацию и ощущение, а также боль» (Ossipov), и др., Central Modulation of Pain, The Journal of Clinical Investigations: ноябрь 2010 г.; 120(11): 3779-3787). Большие асимметричные различия в ЭДА между левой и правой сторонами были продемонстрированы при прямой стимуляции отдельных областей мозга, некоторые из которых образуют вышеупомянутый «болевой матрикс». Boucesin в разделе «Электродермальная активность» на стр. 41, суммирует три основных пути, связывающих центральную нервную систему (ЦНС) с ЭДА. В частности, путь, называемый «ЭДА1», возникает из лимбической области, которая включает миндалевидное тело в виде области мозга, которая вызывает ипсилатеральную ЭДА (Mangina СА, и др., Direct Electrical Stimulation of Specific Human Brain Structures and Bilateral Electrodermal Activity. Int J Psychophysiol, 1996 г. 22(1-2), 1-8; Mangina СА, и др., Even-related Brain Potentials, Bilateral Electrodermal Activity and Mangina-Test Performance in Learning Disabled/ADHD Preadolescents with Severe Behavioral Disorders as Compared to Age-matched Normal Controls. Int J Psychophysiol, 2000 г. 37(1), 71-85; Boucsein W. Electrodermal Activity, (2-е изд.), стр. 41. Springer-Verlag (Нью-Йорк, 2012 г.)).
Использование контралатеральных датчиков для измерения ЭДА и корреляции этих измерений с болью описано в патенте США №6347238 Levengood и Gedye, и др. Тем не менее, эти результаты были представлены в некоторой степени в изолированных экспериментах, а используемые устройства представляли проблемы чувствительности и повторяемости. В патенте США №8560046 Burke было описано устройство, которое достоверно измеряет боль, тем не менее, не была описана интеграция собранных данных с другими биофизическими показателями и, в частности, с ипсилатеральными показателями.
В этом патенте описываются комплексное измерение боли и диагностика, которые развивают и улучшают ранее допущенные требования для размещения контралатерального датчика при измерении функции вегетативной нервной системы и активности матрицы боли. Система PMD сочетает в себе ряд систем управления данными для получения биосигналов, интеграции информации о пациенте, проведения диагностики и терапевтических вмешательств, а также передачи результатов измерений боли и результатов диагностики, которые обеспечивают содержательную и применимую информацию для медицинского работника. В дополнение к диагностике боли, устройства для измерения боли системы PMD также обеспечивают раннюю диагностику желудочно-кишечного расстройства, аллергии и респираторной инфекции, спортивной травмы, связанной с повреждением сухожилий и связок, а также диагностику хронической боли, связанной с травмой спины, случаями зубной боли и мигрени, наряду с некоторыми другими. При использовании системы PMD была продемонстрирована статистически значимая корреляция с самооценкой боли пациентом и оценкой состояний боли до и после лечения, а также при вышеупомянутых болезненных состояниях.
Система PMD, как описано в данном документе, оценивает физиологические показатели, отслеживает активность пациента, взаимодействует с пациентом с помощью вопросов, относящихся к его диагнозу, и помогает принимать решения относительно текущих лечебных схем и изменений для улучшения результатов лечения. Физиологические показатели, оцениваемые системой PMD, могут включать в себя, но не ограничиваются ими, показатели асимметричных биосигналов, связанных с болью, специфичных для данного изобретения, частоты сердечных сокращений, вариабельности сердечного ритма, фотоплетизмограммы (ФПГ), артериального давления, температуры кожи, двигательной функции, кожно-гальванической реакции (КГР) и другие показатели жизненно важных функций. За счет использования анализа и непрерывной интеграции данных система PMD имеет эволюционный характер, в том аспекте, что она будет постоянно оценивать данные, поступающие из разных источников, например, от поставщиков медицинских услуг, которые собирают биометрические данные о пациентах, которые могут страдать от различных болезненных состояний, из новых исследований и журналов со ссылками, связанными с конкретными болезненными состояниями, и биофизические данные за счет использования множественных биосенсоров, используемых для мониторинга пациента с первоначальным объемом анализа, который включает оценку острой и хронической боли в связи с вмешательствами. Благодаря использованию сбора точек данных, которые включают биологические, психологические, социальные критерии и другие соответствующие поля данных в сочетании с точками данных диагностики болезненного состояния, система PMD будет хранить данные, собирать, отфильтровывать и анализировать данные, интегрировать и преобразовывать собранные данные в соответствии с HIPAA, или соответствующим образом защищать права пациентов на конфиденциальность для того, чтобы в режиме параллельного выполнения интегрировать данные о пациентах, используя биопсихосоциальную платформу, или такую, которая содержит другие соответствующие факторы для точек данных, для дальнейшего увеличения понимания болезненного состояния или оценки вмешательства. Система PMD может дополнительно коррелировать произведенные устройством измерения боли и активности центральной нервной системы по отношению к респираторной синусовой аритмии, частоте сердечных сокращений и вариабельности сердечного ритма, дыханию, фотоплетизмограмме (ФПГ), двигательной функции и результатам измерений температуры кожи от других датчиков для того, чтобы определить активность матрицы боли и тонус блуждающего нерва, которые могут предоставить информацию об уязвимости пациента к стрессу и болезни (Loggia и др., Autonomic responses to heat pain: Heart rate, skin conductance, and their relation to verbal ratings and stimulus intensity. Pain. 2011 г.; 152 (3): 592-598). Путем измерения проявления боли в нервной системе в сочетании с данными о биологических, поведенческих, экологических, психологических и социальных факторах, система PMD может дополнительно произвести статистические расчеты факторов пациента и населения и выделить факторы, которые будут использоваться для диагностики для того, чтобы улучшить понимание различных болезненных состояний благодаря многомерной трансформации данных посредством анализа с использованием измерений боли и физиологических измерений, производимых устройством, а также компонентов и функций, интегрированных в платформу системы PMD.
Индивидуальный характер интерпретации боли пациента и текущих биопсихосоциальных подходов к лечению сочетанных болезненных состояний представляет собой барьеры для полного понимания ощущений пациента и того, как боль связана с лечением и успешными результатами лечения. Система PMD в виде интегрированного устройства, сети и комплекса программных средств, устраняет субъективный анализ и разрешает проблемы противоречий и ограничений пациента путем интеграции объективных результатов измерений боли и активности матрицы боли центральной нервной системы, полученных с помощью датчиков, с информацией о здоровье, демографическими данными и результатами физиологических измерений через уникальный графический пользовательский интерфейс (ГПИ), который делает данные доступными и пригодными для поставщиков медицинских услуг (НСР) и пациентов. Система PMD использует программное обеспечение для сбора результатов измерений боли для того, чтобы нормализовать и сопоставить измерения, например, от матрицы боли и связанными с ним сигналами, и интегрировать аспекты этих измеренных данных боли в другие собранные с помощью датчиков данные для более эффективного представления биофизического состояния пациента в определенные временные точки. Система PMD также интегрирует информацию из конкретных областей через конкретные вопросы, которые имеют отношение к физической активности пациентов и болезненным состояниям. Например, пациент, который страдает мигренью, может получить ряд вопросов в качестве обозначенных временных точек, связанных с изменениями формы боли, которые представляют собой изменение состояния боли. Собранные ответы коррелируются и могут показать увеличение боли, которое связано с такими видами жизнедеятельности, как питание, физические упражнения, стресс и другие ежедневные взаимодействия, которые могут идентифицировать источник боли или раздражения, или улучшения состояния больного или здорового человека. Система PMD дополнительно интегрирует показатели состояния здоровья пациента, результаты измерения устройством физического биосигнала, диагностики, исследования и данные поставщика медицинских услуг (НСР) для того, чтобы укрепить положительные эмоции пациента, просвещать, пропагандировать здоровый и активный образ жизни и способствовать соблюдению предписанного режима терапии для улучшения результатов лечения посредством дистанционного взаимодействия с пациентом. Кроме того, система PMD предоставляет платформу для хранения электронной личной медицинской карты, которая будет дополнительно функционировать в качестве универсальной медицинской карты, позволяющей объединять для анализа индивидуальные данные о состоянии здоровья и деятельности с данными электронной медицинской карты. Анализ информации о состоянии здоровья, демографических данных и физиологических измерений с результатами измерений матрицы боли и нервной системы, представленных через систему PMD в соответствии с данным изобретением, обусловливает интеграцию данных и постоянный мониторинг, что приносит пользу здравоохранению и отдельным лицам при использовании индивидуального и глобального анализа факторов состояния здоровья, конкретных данных о заболевании и здоровье, а также эффективных вариантов лечения для того, чтобы в конечном итоге улучшить понимание болезненного состояния или общего состояния здоровья, связанных с факторами воздействия, а также улучшить методические рекомендации для безопасных и эффективных терапевтических вмешательств и схем лечения. Интеграция и оптимизация этих данных в ситуативных временных рамках и связанной с ними информационной базе данных пациента, представленной прикладным программным обеспечением для анализа BioTraceIT системы PMD, может оказать существенное содействие медицинским работникам в диагностике, мониторинге пациента, привлечении пациента к участию в процессе собственного лечения, а также в выборе вариантов лечения и допустимых доз.
Целью и преимуществом данного изобретения является интеграция произведенных устройством показателей боли и других биометрических датчиков, а также собранных биопсихосоциальных данных, в графическом пользовательском интерфейсе для отслеживания и оценки состояния здоровья пациента и реакции на лечение в связи с тем, что субъективный характер боли имеет много компонентов, которые могут быть потенциально объективированы в сочетании с результатами физиологического измерения боли, полученными устройством PainTrace 14 и интегрированным в систему для измерения и диагностики боли PMD 10 (Chapman и др., Pain and Stress in a Systems Perspective: Reciprocal Neural, Endocrine, and Immune Interactions. J Pain. февраль 2008 г.; 9(2): 122-145).
Еще одной целью и преимуществом данного изобретения является то, что система PMD использует компьютерную систему обработки, имеющую запоминающее устройство и хранилище данных, для обработки данных устройства для измерения электрической активности матрицы боли и центральной нервной системы.
Еще одной целью и преимуществом данного изобретения является то, что система PMD использует систему компьютерной обработки данных, имеющую запоминающее устройство и хранилище данных, для обработки данных из устройства для измерения электрической активности матрицы боли и центральной нервной системы путем измерения разности напряжения или силы тока между по меньшей мере двумя согласующими электродами и нормализованным электрическим сигналом для определения величины показателя, представляющего объективный количественный показатель активности матрицы боли, а также отображения и хранения данных из устройства для измерения боли, и использования собранных данных при оценке состояния здоровья и хорошего самочувствия.
Еще одной целью и преимуществом данного изобретения является то, что система PMD использует систему компьютерной обработки данных, имеющую запоминающее устройство и хранилище данных, для обработки данных из устройства для измерения электрической активности матрицы боли и центральной нервной системы путем измерения разности напряжения или силы тока между по меньшей мере двумя контралатерально расположенными согласующими электродами и путем измерения разности между напряжением или силой тока и нормализованным электрическим сигналом для определения величины показателя, представляющего объективный показатель активности матрицы боли, а также отображения и хранения данных из устройства для измерения боли, и использования собранных данных при оценке состояния здоровья и хорошего самочувствия.
Еще одной целью и преимуществом данного изобретения является то, что система PMD использует систему компьютерной обработки данных, имеющую запоминающее устройство и хранилище данных, для обработки данных из устройства для измерения электрической активности матрицы боли и центральной нервной системы путем измерения разности напряжения или силы тока между по меньшей мере двумя ипсилатерально расположенными согласующими электродами и путем измерения разности между напряжением или силой тока и нормализованным электрическим сигналом для определения величины показателя, представляющего объективный показатель активности матрицы боли, а также отображения и хранения данных из устройства для измерения боли, и использования собранных данных при оценке состояния здоровья и хорошего самочувствия.
Еще одной целью и преимуществом данного изобретения является то, что система PMD использует систему компьютерной обработки данных, имеющую запоминающее устройство и хранилище данных, для обработки данных из устройства для измерения электрической активности матрицы боли и центральной нервной системы путем измерения разности напряжения или силы тока между по меньшей мере двумя контралатерально расположенными согласующими электродами с учетом разности напряжения или силы тока между по меньшей мере двумя ипсилатерально расположенными согласующими электродами для калибровки показателей активности матрицы боли и центральной нервной системы, а также отображения и хранения данных из устройства для измерения боли, и использования собранных данных при оценке состояния здоровья и хорошего самочувствия.
Еще одной целью и преимуществом данного изобретения является то, что система PMD использует систему компьютерной обработки данных, имеющую запоминающее устройство и хранилище данных, для обработки данных из устройства для измерения электрической активности матрицы боли и центральной нервной системы путем измерения разности напряжения или силы тока между по меньшей мере двумя контралатерально расположенными согласующими электродами с учетом разности напряжения или силы тока между по меньшей мере двумя ипсилатерально расположенными согласующими электродами для определения и подтверждения величины показателя, представляющего объективный показатель активности матрицы боли и центральной нервной системы, а также отображения и хранения данных из устройства для измерения боли, и использования собранных данных при оценке состояния здоровья и хорошего самочувствия.
Еще одной целью и преимуществом данного изобретения является то, что устройство системы PMD для измерения показателей матрицы боли и центральной нервной системы будет использоваться в течение длительных периодов времени в качестве портативного переносного монитора на дому для мониторинга боли и состояния здоровья с данными, собранными с использованием компонентов и функций системы PMD.
Еще одной целью и преимуществом данного изобретения является то, что система PMD обеспечивает передачу сигналов тревоги на основе данных, собранных из устройства для измерения показателей матрицы боли и центральной нервной системы, которые отклоняются от заданных уровней, соответствующим поставщикам медицинских услуг.
Еще одной целью и преимуществом данного изобретения является то, что система PMD обеспечивает введение лекарственного средства через автоматизированное дозирующее устройство насосного типа на основе данных, собранных из устройства для измерения показателей матрицы боли и центральной нервной системы.
Еще одной целью и преимуществом данного изобретения является то, что система PMD посредством защитного кода обеспечивает активацию дозирующего устройства для лекарственного средства на основе данных, собранных из устройства для измерения показателей матрицы боли и центральной нервной системы.
Еще одной целью и преимуществом данного изобретения является то, что данные, собранные из одного или более физиологических мониторов системы PMD для измерения множества физиологических признаков пациента, таких как боль, частота сердечных сокращений, вариабельность сердечного ритма, температура кожи, электродермальная активность (ЭДА), показания фотоплетизмограммы (ФПГ), проводимость кожи, движение, растяжение и сжатие, используются для оценки состояния здоровья и хорошего самочувствия пациента.
Еще одной целью и преимуществом является то, что система PMD в соответствии с данным изобретением собирает данные от одного или более физиологических мониторов для измерения множества физиологических признаков.
Еще одной целью и преимуществом является то, что система PMD содержит компоненты и функции для взаимодействия с пациентом на основе их диагноза и контролируемых изменений уровней боли.
Данное изобретение относится к системе биоаналитического анализа с использованием измерений боли для диагностики и измерения эффективности результатов лечения, причем система содержит устройство для измерения активности матрицы боли; множество данных BioTrace Factors, связанных с биофизической, биологической, психологической, социальной, экологической и демографической информацией; и при этом отклонения в измерениях активности матрицы боли объединяются с данными BioTrace Factors для определения эффективности лечения пациента. Комбинация показателей активности матрицы боли и данных BioTrace Factors обеспечивает количественный показатель боли. Количественный показатель активности матрицы боли коррелирует с самооценкой боли с использованием цифровой рейтинговой шкалы. Система биоаналитического анализа содержит 10-60 передач сообщений, вызываемых комбинацией показателей активности матрицы боли, данных BioTrace Factors и интегрированного ведения журнала. Множество данных BioTrace Factors системы биоаналитического анализа включат влияющие факторы и уровни влияния факторов. Комбинация показателей активности матрицы боли и данных BioTrace Factors обеспечивает данные PainTrace Factor, которые отражают ощущение боли отдельно взятого пациента. Комбинация данных BioTrace Factors и данных PainTrace Factor обеспечивает показатель прогресса BioTrace Progress Score, отражающий эффективность лечения пациента и показатель приверженности пациента к этому лечению.
В некоторых вариантах реализации изобретения измерения активности матрицы боли в системе биоаналитического анализа производятся без подачи напряжения путем применения диапазона напряжений или токов. Устройство для измерения активности матрицы боли в системе биоаналитического анализа имеет датчики, и в некоторых вариантах реализации изобретения к датчикам с перерывами подается ток. Датчики устройства для измерения активности матрицы боли могут быть размещены контралатерально, ипсилатерально, парами размещены контралатерально и парами размещены ипсилатерально, а в некоторых вариантах реализации изобретения две пары ипсилатеральных датчиков расположены контралатерально. Устройство для измерения активности матрицы боли системы биоаналитического анализа имеет нагрузочный резистор, имеющий сопротивление от 0,5 кОм до 900 кОм. Нагрузочный резистор может представлять собой переменный резистором и способ калибровки может с дискретностью увеличивать сопротивление путем подачи напряжения для генерирования кривой линейного сопротивления. Переменный резистор может быть настроен с использованием кривой линейного сопротивления для получения максимального прохождения электрического тока.
Система биоаналитического анализа, использующая измерения боли для диагностики и оценки эффективности результатов лечения, может содержать измеритель болевого раздражения, который применяет последовательное и повторяемое количество нажатий в течение последовательного периода времени. Путем получения результатов измерения активности матрицы боли при применении раздражителя с помощью измерителя болевого раздражения, можно получить исходный уровень болевой толерантности. Система биоаналитического анализа может содержать один или все из следующих компонентов: детектор движения, монитор частоты сердечных сокращений, монитор вариабельности сердечного ритма, монитор артериального давления, устройство для измерения кожногальванической реакции и устройство для измерения температуры кожи. В некоторых вариантах реализации изобретения устройство для измерения активности матрицы боли системы биоаналитического анализа содержит устройство для мониторинга матрицы боли, монитор частоты сердечных сокращений, монитор вариабельности сердечного ритма, монитор артериального давления, устройство для измерения кожногальванической реакции, устройство для измерения температуры и детектор движения. Система биоаналитического анализа может включать предоставление в пользование готового продукта за абонентскую плату (SaaS), платформу приложений в виде услуги (PaaS) и прием заказов на вычислительные работы по требованию, а также ресурсы общего пользования в виде базы данных с использованием веб-браузера или другого интерфейса. Система биоаналитического анализа может содержать электронную схему для инициализации, идентификации, местоположения, сбора, управления и связи с устройством для измерения активности матрицы боли.
Данное изобретение относится к устройству для мониторинга вегетативных функций, содержащему:
устройство для измерения активности матрицы боли, имеющее датчики, систему сбора данных; и при этом отклонения в измерениях активности матрицы боли используются для определения уровней боли и здоровья пациента. Измерение активности матрицы боли устройством для мониторинга вегетативных функций обеспечивает количественный показатель боли. Количественный показатель активности матрицы боли коррелирует с самооценкой боли с использованием цифровой рейтинговой шкалы. Измерения активности матрицы боли могут быть произведены без подачи напряжения или путем применения диапазона напряжений и силы тока. В некоторых вариантах реализации изобретения
ток подается к датчикам с перерывами. Датчики устройства для мониторинга вегетативных функций могут быть размещены контралатерально, ипсилатерально, парами размещены контралатерально и парами размещены ипсилатерально, а в некоторых вариантах реализации изобретения две пары ипсилатеральных датчиков могут быть расположены контралатерально.
Устройство для измерения активности матрицы боли в устройстве для мониторинга вегетативных функций имеет нагрузочный резистор, имеющий сопротивление от 0,5 кОм до 900 кОм. В некоторых вариантах реализации изобретения нагрузочный резистор представляет собой переменный резистор, и сопротивление с дискретностью увеличивается, а напряжение подается для генерирования кривой линейного сопротивления При применении способов калибровки переменный резистор может быть настроен с использованием кривой линейного сопротивления для получения максимального прохождения электрического тока. Устройство для мониторинга вегетативных функций может содержать измеритель болевого раздражения, который применяет последовательное и повторяемое количество нажатий в течение последовательного периода времени. Измерения активности матрицы боли при применении раздражителя с помощью измерителя болевого раздражения, могут быть использованы для того, чтобы создать исходный уровень болевой толерантности. В некоторых вариантах реализации изобретения устройство для мониторинга вегетативных функций может содержать одно или все из следующего: детектор движения, монитор частоты сердечных сокращений, монитор вариабельности сердечного ритма, монитор артериального давления, устройство для измерения кожногальванической реакции и устройство для измерения температуры кожи. Устройство для мониторинга вегетативных функций может включать предоставление в пользование готового продукта за абонентскую плату (SaaS), платформу приложений в виде услуги (PaaS) и прием заказов на вычислительные работы по требованию, а также ресурсы общего пользования в виде базы данных с использованием веб-браузера или другого интерфейса. Устройство для мониторинга вегетативных функций может содержать электронную схему для инициализации, идентификации, местоположения, сбора, управления и связи с множеством датчиков.
Данное изобретение относится к монитору активности для измерения боли, который в некоторых вариантах реализации изобретения может содержать контралатеральные датчики, измеряющие активность матрицы боли без подачи напряжения. В других вариантах реализации изобретения монитор активности для измерения боли может содержать ипсилатеральные датчики с подачей напряжения. Монитор активности для измерения боли может содержать одно или все из следующего: монитор частоты сердечных сокращений, монитор вариабельности сердечного ритма, детектор движения, монитор артериального давления, устройство для измерения кожногальванической реакции и устройство для измерения температуры кожи. Монитор активности для измерения боли может содержать гарнитуру с датчиками. Монитор активности для измерения боли может содержать группу датчиков. Монитор активности для измерения боли может содержать электронную схему для инициализации, идентификации, локализации, сбора данных, управления и связи с множеством датчиков.
Данное изобретение дополнительно относится к гарнитуре с датчиками, содержащей гибкое устройство для прикрепления датчика, имеющее гарнитуру и проводящую полосу; и в котором гибкое устройство для прикрепления датчика обеспечивает прикрепление и электрическое соединение с множеством электродов и датчиков. Гарнитура с датчиками может содержать текстильную застежку типа Velcro для прикрепления гарнитуры с датчиками к одежде. Гарнитура с датчиками может содержать липкую полосу для прикрепления гарнитуры с датчиками к коже, одежде или другим поверхностям. Гарнитура с датчиками может содержать электронную схему для инициализации, идентификации, локализации, сбора данных, управления и связи с множеством датчиков. Гарнитура с датчиками может содержать электронную схему для беспроводной связи. Гарнитура с датчиками может содержать коммуникационные разъемы для добавления отдельных гарнитур с датчиками и дополнительных электродов и датчиков к гарнитуре с датчиками.
Данное изобретение относится к способу количественного измерения боли, включающему установление исходного уровня путем измерения активности матрицы боли во время болевого раздражения; мониторинг активности матрицы боли и отклонений от установленного исходного уровня; создание данных BioTrace Factors на основе биофизических данных пациента, демографических данных о пациенте и населении, и самооценки боли; создание данных PainTrace Factor на основе интеграции данных измерений активности матрицы боли и данных BioTrace Factors; мониторинг активности матрицы боли пациента на всем протяжении лечения; и определение разницы показателей до лечения и после лечения, указывающих на изменение состояния боли; и корреляцию измеренной разницы показателей с соответствующими шкалами боли.
Данное изобретение представляет собой способ измерения эффективности результатов лечения с использованием измерений активности матрицы боли, включающий мониторинг активности и отклонений матрицы боли для установления количественного показателя боли; мониторинг и сбор данных LifeTraceIT на основе данных об активности пациентов, участии, соблюдения предписанного режима терапии и интегрированного ведения журнала; применение итеративного анализа к данным BioTrace Factors, данным PainTrace Factors, данным LifeTraceIT, связанным с пациентом, и интеграции этого анализа для создания индивидуализированного показателя прогресса BioTrace Progress Score, который будет определяться на постоянной основе, так чтобы продолжался мониторинг действий пациента, физиологических данных, терапевтических вмешательств, и активность матрицы боли; которые в дальнейшем будут сочетаться с соответствующими тенденциями, группами населения, текущими исследованиями и историческими медицинскими данными при оценке эффективности результатов лечения.
Другие цели и преимущества данного изобретения будут очевидными для читателя, и предполагается, что эти цели и преимущества находятся в пределах объема данного изобретения. Для выполнения вышеописанных и связанных целей это изобретение может быть реализовано в форме, изображенной в прилагаемых графических материалах, при этом внимание обращается на тот факт, что графические материалы являются всего лишь иллюстративными, и что изменения могут быть выполнены в конкретной конструкции, изображенной и описанной в рамках данной заявки.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Некоторые варианты реализации данного изобретения теперь будут описаны только в качестве примера со ссылкой на прилагаемые графические материалы, на которых:
На Фиг. 1 изображен схематический вариант реализации изобретения сети системы для измерения и диагностики боли (PMD), которая может находиться в клиническом или больничном учреждении при реализации данного изобретения;
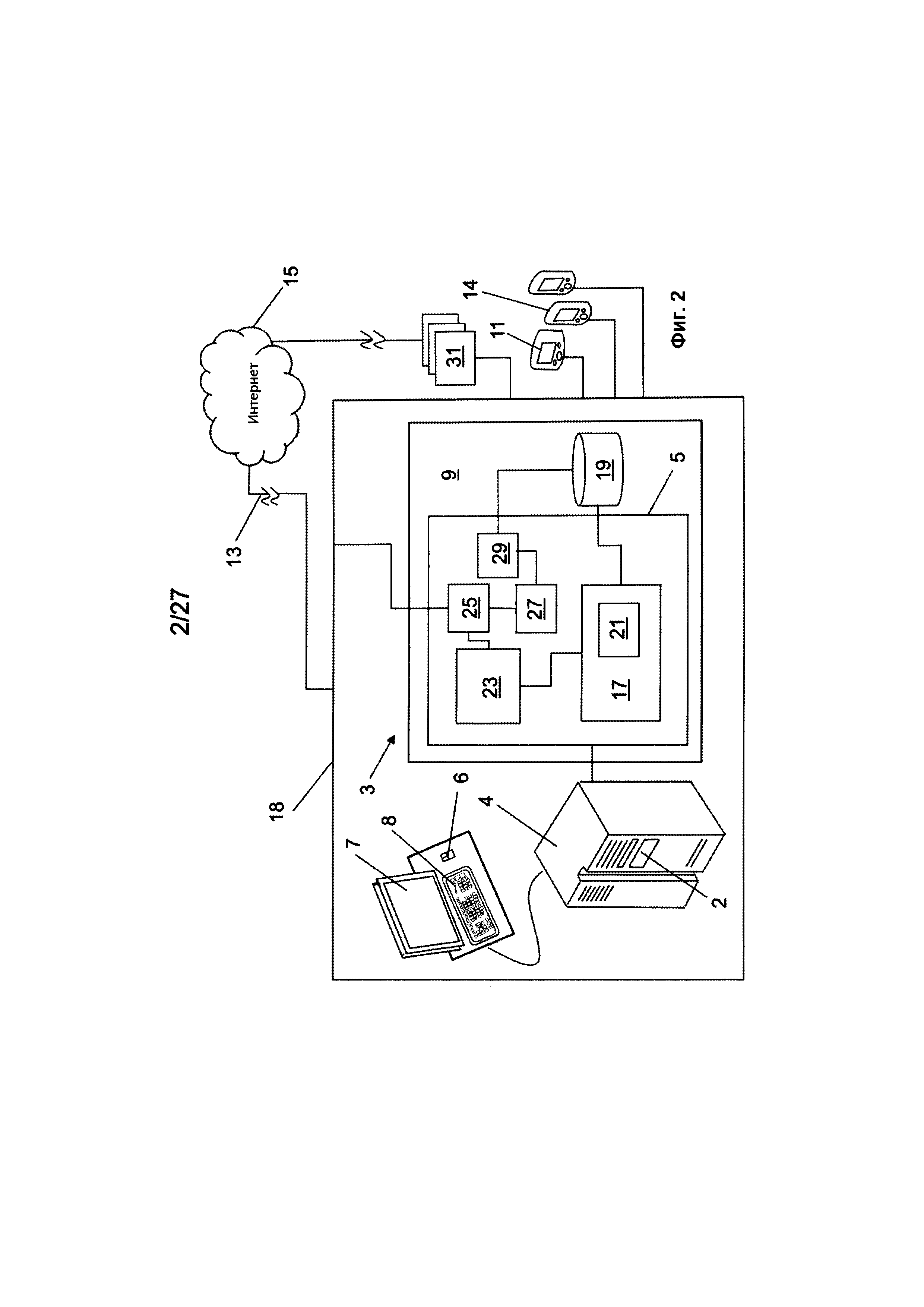
На Фиг. 2 изображен схематический вариант реализации изобретения серверной системы и интеграция одной или более серверных систем, компьютеров, мобильных устройств, биофизических устройств а также сенсоров и устройств для измерения боли в сети системы PMD при реализации данного изобретения;
На Фиг. 3 изображен схематический вариант реализации изобретения компонентов приложения в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 4 изображен схематический вариант реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 5 изображен схематический вариант реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6А изображен схематический вариант реализации изобретения датчиков для измерения боли (называемых в данном документе датчиками PainTrace или датчиками устройства PainTrace), которые предоставляют данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6В изображен схематический вариант реализации изобретения устройства PainTrace, которое предоставляет данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6С изображен схематический другой вариант реализации изобретения датчиков PainTrace, которые предоставляют данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6С изображен схематический другой вариант реализации изобретения датчиков PainTrace, которые предоставляют данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6Е схематически изображен еще однин дополнительный вариант реализации изобретения датчиков PainTrace и измерительных устройств PainTrace с датчиками, которые предоставляют данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6F изображен вид в разобранном виде схематического изображения варианта реализации изобретения датчика PainTrace и крепежного приспособления, изображенного на Фиг. 6С, которое предоставляет данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6G схематически изображен еще однин дополнительный вариант реализации изобретения измерительного устройства PainTrace с датчиками, которые предоставляют данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6Н схематически изображен еще один дополнительный вариант реализации изобретения измерительного устройства PainTrace с датчиками, изображенного на Фиг. 6G, которое предоставляет данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6I схематически изображен еще один дополнительный вариант реализации изобретения измерительного устройства PainTrace с датчиком, интегрированным в монитор артериального давления, который предоставляет данные для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 6J схематически изображен еще один дополнительный вариант реализации изобретения датчика устройства PainTrace, которое может быть использовано с измерительным устройством PainTrace и монитором артериального давления, изображенным на Фиг. 6I, для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 7А изображен вид спереди схематического изображения варианта реализации изобретения устройства PainTrace с датчиком, установленным на браслете для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 7В изображен вид сзади схематического изображения варианта реализации изобретения устройства PainTrace с датчиком, установленным на браслете для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 7С изображен вид спереди схематического изображения другого варианта реализации изобретения только датчика PainTrace, установленного на браслете для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 8А изображен вид сбоку схематического изображения варианта реализации изобретения устройства PainTrace с датчиками, для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 8В изображен вид сзади схематического изображения варианта реализации изобретения устройства PainTrace с датчиком, установленным на браслете для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
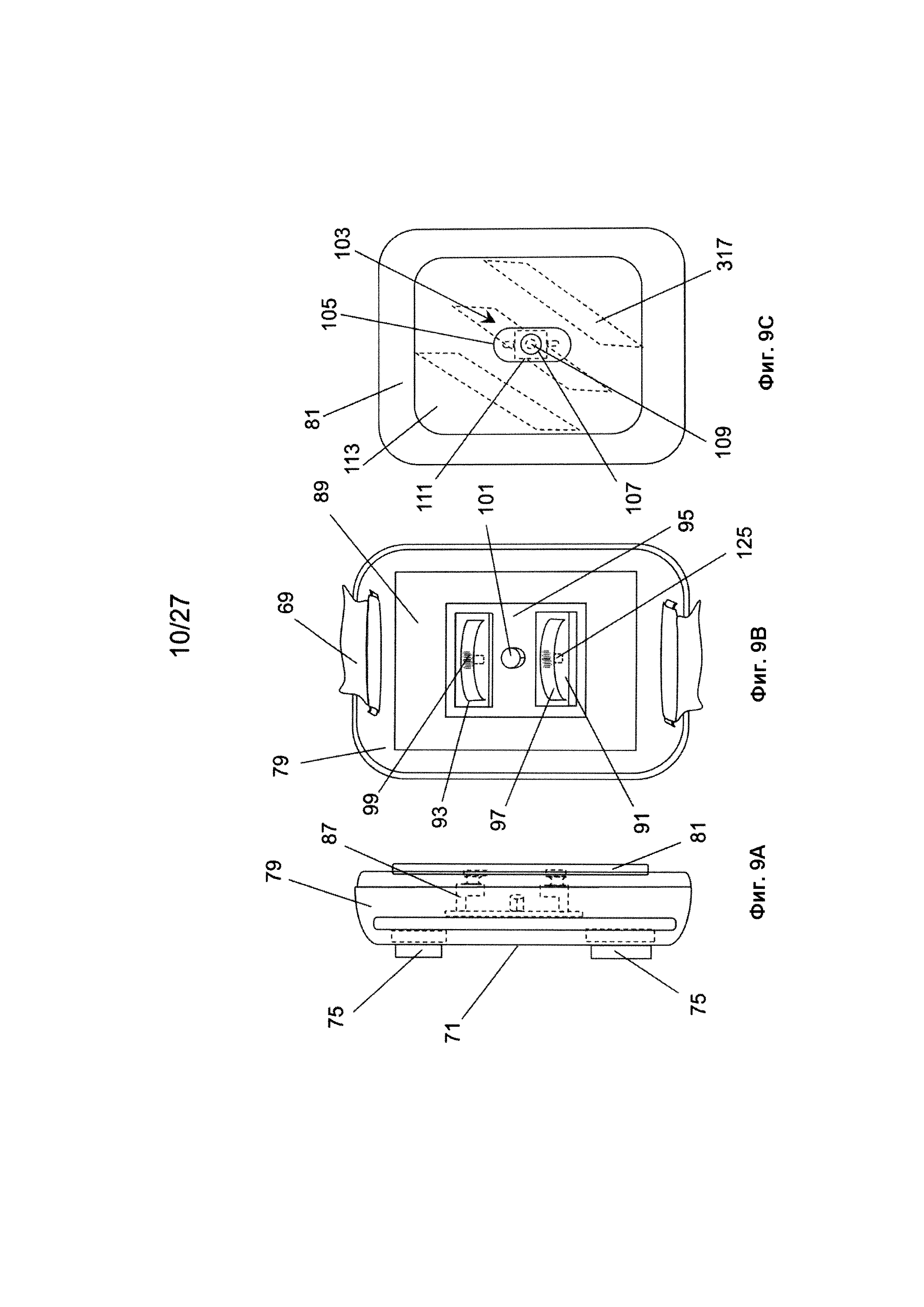
На Фиг. 9А изображен вид сбоку с внутренней стороны схематического изображения варианта реализации изобретения устройства PainTrace с датчиком, для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 9В изображен вид сзади схематического изображения варианта реализации изобретения устройства PainTrace, изображенного на Фиг. 9А, для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 9С изображен вид сзади схематического изображения варианта реализации изобретения датчика PainTrace, изображенного на Фиг. 9А, для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 10А изображен вид в перспективе схематического изображения варианта реализации изобретения датчика PainTrace, для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 10В изображен вид в перспективе схематического изображения варианта реализации изобретения разъема датчика PainTrace;
На Фиг. 10С изображен вид в перспективе схематического изображения варианта реализации изобретения разъема устройства PainTrace;
На Фиг. 11А изображен вид в перспективе схематического изображения варианта реализации изобретения датчика PainTrace, разъема датчика, и разъема устройства в разблокированном положении;
На Фиг. 11В изображен вид в перспективе схематического изображения варианта реализации изобретения датчика PainTrace, разъема датчика, и разъема устройства в заблокированном положении;
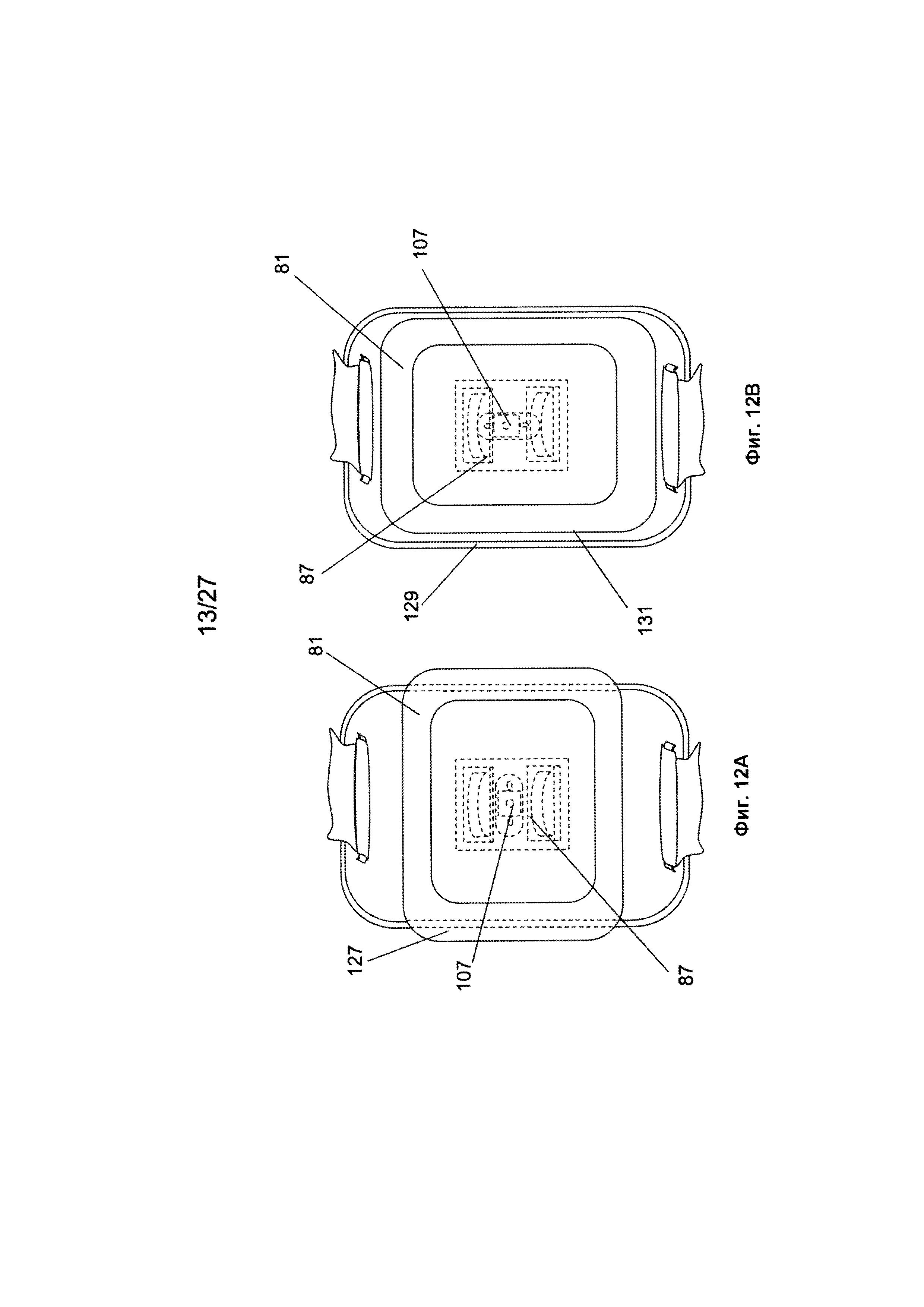
На Фиг. 12А изображен вид в перспективе схематического изображения варианта реализации изобретения датчика PainTrace, разъема датчика, и разъема устройства в разблокированном положении;
На Фиг. 12В изображен вид спереди схематического изображения варианта реализации изобретения датчика PainTrace, разъема датчика, и разъема устройства в заблокированном положении;
На Фиг. 13 изображена блок-схема варианта реализации изобретения компонентов схемы системы PMD в варианте реализации изобретения системы PDM в соответствии с данным изобретением.
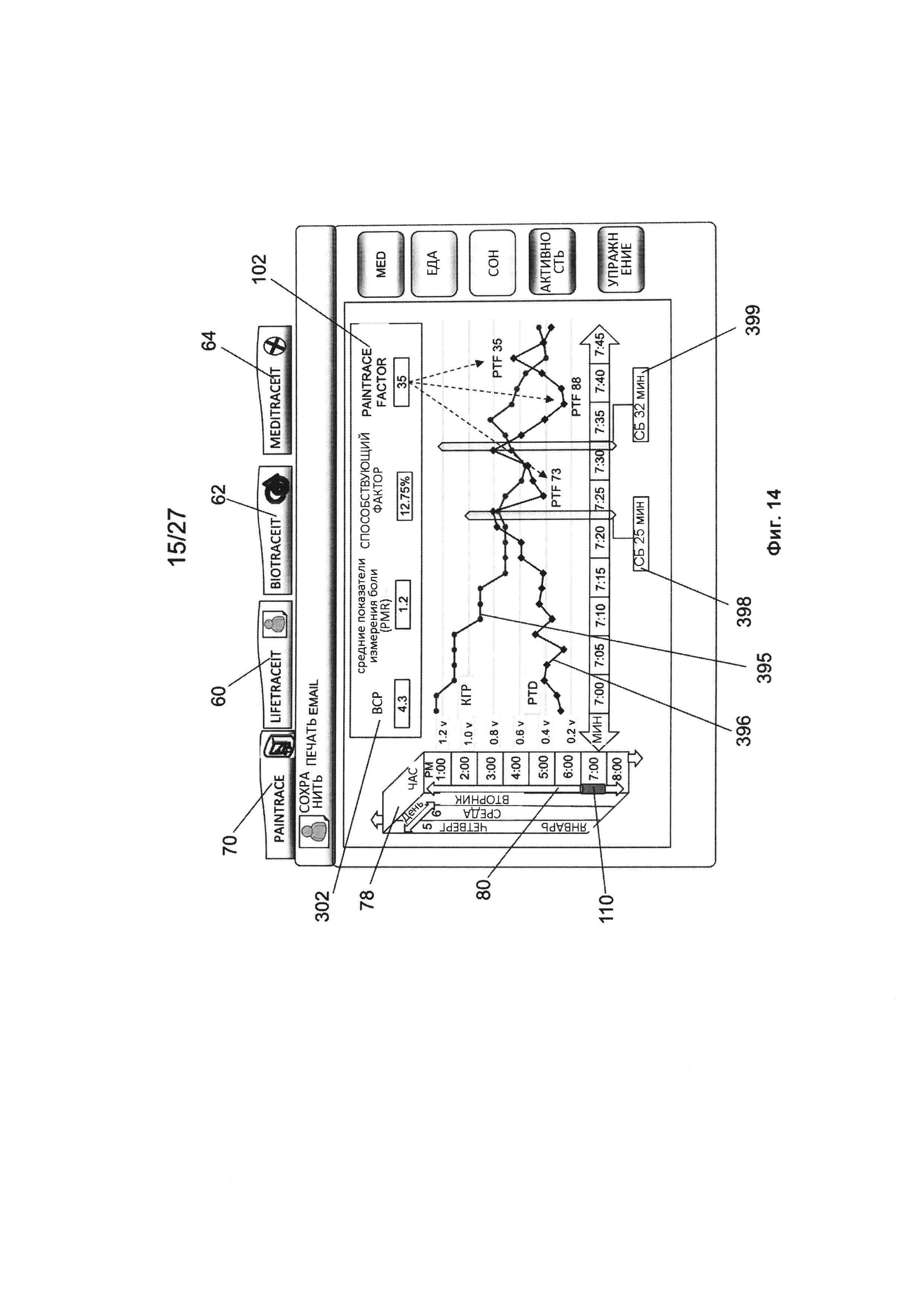
На Фиг. 14 изображен схематический вариант реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 15А изображен схематический вариант реализации изобретения гарнитуры с датчиками и датчики системы PMD, для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 15В изображен схематический вариант реализации изобретения соединения двух гарнитур с датчиками и датчиков системы PMD, для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 15С изображен вид с торца варианта реализации изобретения гарнитуры с датчиками системы PMD, и варианта реализации изобретения датчика для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 15D изображен вид с торца дополнительного варианта реализации изобретения гарнитуры с датчиками системы PMD, и варианта реализации изобретения датчика для предоставления данных для варианта реализации изобретения компонента приложения PainTrace в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
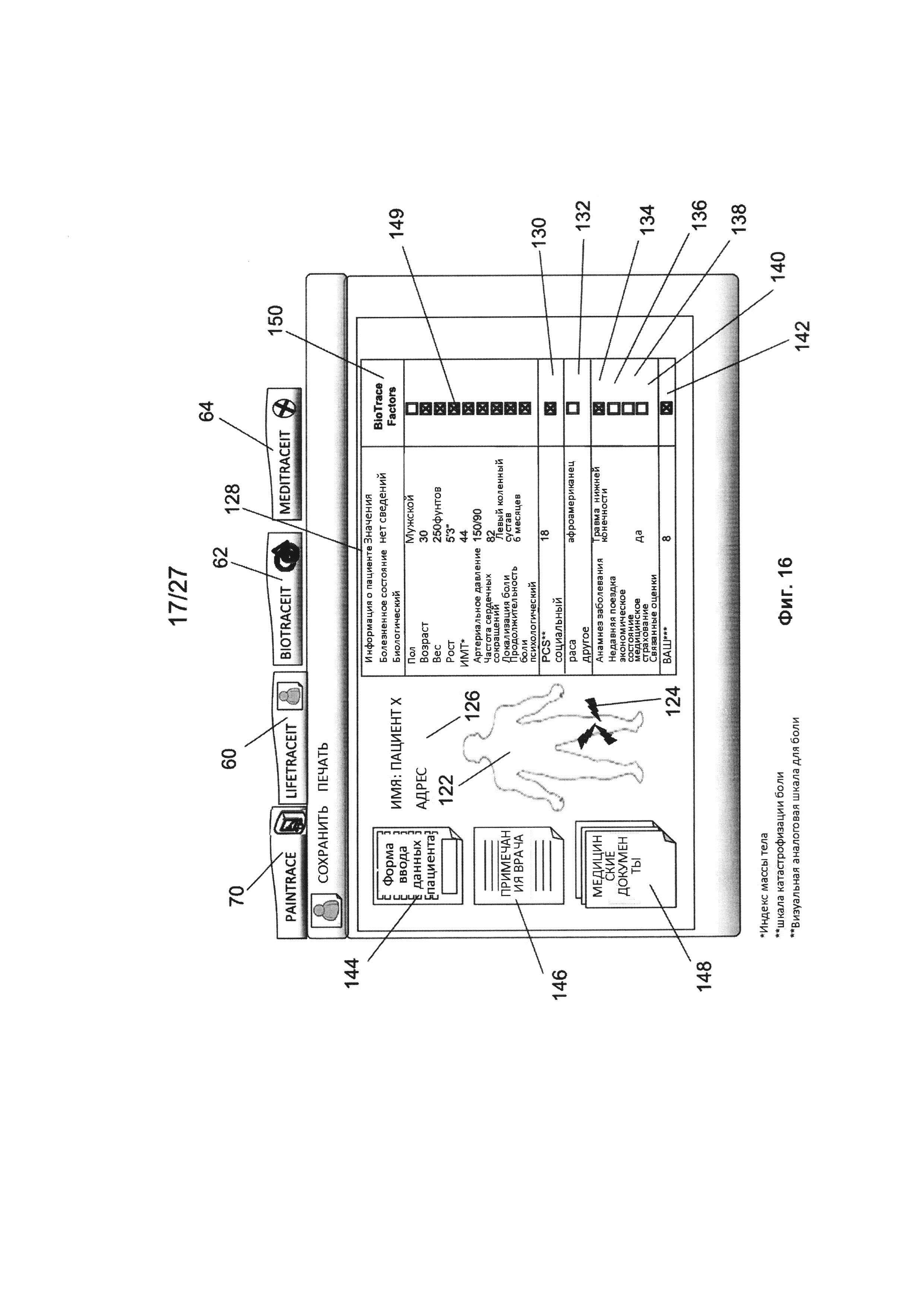
На Фиг. 16 изображен схематический вариант реализации изобретения компонента приложения BioTraceIT, включающего данные от компонента приложения LifeTraceIT в варианте реализации изобретения системы PMD в соответствии с данным изобретением; На Фиг. 17 изображен вариант реализации изобретения данных PainTrace и данных BioTrace Factors, используемых для определения данных PainTracePainTrace Factor и порогового значения болевой толерантности в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 18 изображена блок-схема последовательности операций, иллюстрирующая вариант реализации изобретения данных BioTrace Factors, которые могут быть использованы для разработки анализа BioTraceIT в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 19 изображен схематический вариант реализации изобретения компонента приложения BioTraceIT в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 20 изображен схематический другой вариант реализации изобретения компонента приложения BioTraceIT в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 21 изображено схематическое изображение еще одного варианта реализации изобретения компонента приложения BioTraceIT в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 22 изображен схематический вариант реализации изобретения компонента приложения MediTraceIT в варианте реализации изобретения системы PMD в соответствии с данным изобретением;
На Фиг. 23 изображен пример данных PainTrace, иллюстрирующий результаты измерения боли до и после лечения в варианте реализации изобретения системы PMD в соответствии с данным изобретением.
На Фиг. 24 изображен пример данных PainTrace, иллюстрирующий результаты измерения боли в сравнении со шкалой самооценки ВАШ в варианте реализации изобретения системы PMD в соответствии с данным изобретением.
На Фиг. 25 изображен пример данных PainTrace, собранных в течение шестимесячного периода от лошади, страдающей ламинитом, в варианте реализации изобретения системы PMD в соответствии с данным изобретением.
На Фиг. 26 изображен пример данных PainTrace, иллюстрирующий изменения в результатах измерения боли до и после лечения у 20 пациентов в варианте реализации изобретения системы PMD в соответствии с данным изобретением.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение представляет собой систему для измерения и диагностики центральной нервной системы и матрицы боли (PMD) 10, которая содержит одно или более медицинских устройств для объективного измерения активности матрицы боли, и способ сбора данных и анализа результатов измерений боли для диагностики болезненных состояний и состояния здоровья, а также обоснования лечения пациента и результатов лечения пациента. Система PMD 10 может быть реализована в локальной сети, а также на других устройствах, имеющих совместимую электронику. Компьютерные системы и электронные устройства интегрированы в сети и сервера для связи с одним или более устройствами для измерения показателей матрицы боли и центральной нервной системы, биосенсорами, компьютерными системами, устройствами и системами связи. В первом варианте реализации изобретения, изображенном на Фиг. 1, система PMD 10 может быть воплощена в локальной сети 12, к примеру, может находиться в клинической или госпитальной среде или использовать электронные устройства, выполненные с возможностью обмена данными с облачными вычислительными сервисами для индивидуального или удаленного мониторинга. Система PMD 10 может быть воплощена с помощью одного или более устройств, таких как смартфон, для сбора и передачи данных пациента в облачную сеть, больничную сеть, медицинские кабинеты, дома престарелых, или же другие места оказания медицинской помощи или места для получения информации, наблюдения и анализирования биофизических данных, или же для телемедицины, каждая из которых в данном документе называется как «среда сбора и обработки данных» 1 и к наружной серверной системе BioTraceIT 18 системы PMD доступной для сбора, просмотра и хранения данных пациента и биометрической информации. Система PMD 10 может обеспечивать различные уровни доступа к медицинским устройствам и конкретным компонентам, а также функциям, которые могут быть воплощены с помощью одного или более программных приложений. Административные уровни могут быть установлены и могут управляться в рамках административных инструментов программного приложения. Варианты программного приложения и уровни доступа представлены для медицинских устройств, функций и компонентов в виде особенных для конкретных аспектов лечения и для пациента, а также для медицинских специалистов, лечащих пациента. К примеру, в «среде сбора и обработки данных» 1 система PMD 10 может предоставлять функции и компоненты, доступные пациенту для личного мониторинга пациентом биофизических факторов и физической активности. Дополнительно, функции и компоненты могут быть предоставлены для поставщиков медицинских услуг (HCPs) для мониторинга пациента в месте предоставления медицинских услуг и дополнительных функций для врачей и других лиц для удаленного телемедицинского мониторинга с уровнями или безопасностью и анонимностью пациентов, предоставляемыми по мере необходимости на разных уровнях доступа. В рамках «среды сбора и обработки данных» 1 устройства и датчики, собирающие данные пациента могут иметь внутренние системы связи для отображения и передачи данных внутри системы PMD 10, которая может быть доступна через интранет и/или интернет соединение для просмотра и мониторинга собранных данных пациента на мобильном устройстве, таком как смартфон, умные часы iPhone, iPad, iPod, умные часы, пригодные для ношения очки виртуальной реальности, или же планшетном компьютере 22 для пациента, для получения доступа к самим данным и/или для поставщиков медицинских услуг (НСР), врача, физиотерапевта или другого обслуживающего персонала для пациента, или клиентов, администрации или независимых исследователей для доступа к данным.
Система PMD 10 может быть реализована через безопасный сервер и доступна через пользовательский интерфейс веб-браузера для медицинских сотрудников НСР для регистрации и сбора данных от датчиков и устройств для сбора данных в больничной сети 16. В межсетевых экранах 36 больничной сети избыточные и другие протоколы безопасности для защиты данных пациента доступны с сетевыми концентраторами 30, серверами 32, а также устройствами связи 34 для установления связи со «средой сбора и обработки данных» 1 и распространения данных через коммуникационную сеть 20 для поставщиков медицинских услуг (HSPs) и других лиц, для которых требуются данные пациента. Коммуникационная сеть 20 может включать доступ к данным пациента через систему PMD 10 на планшетных компьютерах 22, приборных панелях 24 для медицинских сестер, смартфонах 28, а также с помощью других устройств в коммуникационной сети 20.
Доступ к данным пациента через систему PMD 10 может быть дополнительно обеспечен через устройства, непосредственно подключенные и соединенные с устройствами для измерения показателей матрицы боли и центральной нервной системы или другими биосенсорами для сбора данных, к примеру, через USB разъем для «среды сбора и обработки данных» 1, которые могут быть удаленными для интернет-доступа. К примеру, в военном подразделении медицинской службы, в котором необходимы данные пациента и анализ без доступа к внешним ресурсам. Дополнительно данные пациента могут храниться на устройстве, таком как запоминающее устройство и устройства для хранения данных на устройстве PainTrace 14, которые должны передаваться при наличии проводного или беспроводного доступа. Система PMD 10 может быть предварительно загружена для того, чтобы быть единственным доступным приложением и системой мониторинга на цифровом устройстве для пациента, поставщика медицинских услуг (НСР), или врача, используемым в условиях работы без интернет-доступа, к примеру, для пациента пожилого возраста в его доме в удаленном местоположении. Данные от системы PMD 10 с использованием цифровых устройств могут быть связаны с помощью аналоговых телефонных линий или сотовых сетей 26 для обеспечения связи с поставщиками медицинских услуг (HCPs) и другими лицами в виде предупреждений, голосовой почты, текста, и/или электронной почты. Сокращенные данные и информация также могут быть доступны через систему PMD 10 с использованием программных приложений или конкретных компонентов и функций одного или более программных приложений, доступных для смартфона через сотовые сети 26. Следовательно, доступность к данным пациента через PMD 10 предоставляется в нескольких формах для размещения различных «сред сбора и обработки данных» 1, где пациент может находиться немощным в больнице, находиться в учреждении по уходу или реабилитации, находиться в своем собственном доме и/или находиться в удаленных местах с минимальным доступом или без доступа к Интернету. Таким образом, система PMD 10 может предоставить собранные данные, которые могут быть получены от одного или более устройств для измерения показателей матрицы боли и центральной нервной системы 14, а также биосенсоров 11 доступным и содержательным образом для предоставления применимой и интерпретируемой информации пациенту, поставщику медицинских услуг (НСР), а также врачу на каждом из различных доступных уровней программного приложения системы PMD и компонентов и функций аппаратных средств получения данных.
Датчики и устройства, интегрированные в компоненты и функции системы PMD 10, в значительной степени могут быть в виде датчиков и устройств для измерения показателей матрицы боли и центральной нервной системы, называемых в данном документе как устройства PainTrace 14. Устройства PainTrace 14 могут собирать и отображать данные на устройстве 14, и передавать данные в среду сбора и обработки данных 1 и в пределах больничной сети 16, а также других сетей, предпочтительно используя Bluetooth, Wi-Fi, Near Field Communication (NFC), и/или другие протоколы связи, к примеру через беспроводные модемы, в которых данные собираются от датчиков и записываются от пациентов в пределах среды сбора и обработки данных 1.
Собранные данные дополнительно могут быть переданы через безопасное интернет-соединение на серверную систему BioTraceIT 18 системы PMD, которая также имеет брандмауэры 38, протоколы резервирования и безопасности для защиты данных. Предпочтительно данные могут передаваться как непосредственно из устройства для измерения показателей матрицы боли и центральной нервной системы, так и из других датчиков, или из клинической или же больничной сети без идентификации информации, такой как имя или адрес пациента. Тем не менее, информация о пациенте, которая включает биологические, психологические, социальные и экологические факторы может быть включена, а все данные, включая информацию об идентификации пациента, могут быть немедленно доступными для оказания помощи при лечении в среде сбора и обработки данных 1 в месте предоставления медицинских услуг. Таким образом, все данные могут быть доступны в больничной сети 16 и вся деидентифицированная информация может быть скоррелирована и сохранена в базе данных, и может быть доступна через серверную систему BioTraceIT 18 системы PMD в виде исходных или обработанных данных от датчиков, включая устройство PainTrace 14 с временами сбора и датами, которые будут использоваться с биологическими, психологическими, социальными и экологическими факторами, где данные всех типов могут быть доступны для анализа данных, корреляции, а также анализа моделей для выявления и развития данных BioTrace Factors, как описано в данном документе. Серверная система BioTraceIT 18 системы PMD также имеет сервер 40, сетевые концентраторы 42, а также компьютерные системы 44. Сервер BioTraceIT 18 системы PMD может также размещать образы программного обеспечения для обновления программных компонентов и функций системы PMD 10. В некоторых приложениях системы PMD 10, как описано в данном документе, данные могут быть доступны только через прямое проводное соединение, к примеру, с использованием USB-соединения с устройством для измерения показателей матрицы боли и центральной нервной системы или с помощью беспроводной связи ближнего радиуса действия (NFC) для обеспечения ограниченного доступа и обеспечения безопасности автономного устройства, такого как дозатор лекарств, или устройств в удаленной среде сбора и обработки данных без доступа в Интернет.
Как изображено на Фиг. 2, система PMD 10 может быть реализована на компьютерном оборудовании и компьютеризированной технике. К примеру, компоненты и функции системы PMD 10 могут быть выполнены с использованием одного или более устройств для измерения показателей матрицы боли и центральной нервной системы 14 и/или других биосенсорных систем медицинских устройств 11 для измерения биофизических показателей, таких как частота сердечных сокращений, вариабельность частоты сердечных сокращений, показания фотоплетизмограммы (ФПГ), артериальное давление, температура кожи, двигательная функция, кожно-гальваническая реакция (КГР), и других показателей жизненно-важных функций. Дополнительно, система PMD 10 может быть реализована за счет использования других цифровых устройств связи и/или одного или более персональных компьютеров и серверов данных. К примеру, компоненты и функции системы PMD 10 и серверная система BioTraceIT 18 могут быть реализованы на компьютерной системе 3, которая показана с целью иллюстрации варианта реализации изобретения аппаратных компонентов, которые могут использоваться для реализации системы PMD 10. Данное изобретение не ограничивается компьютерной системой 3, изображенными программными или аппаратными компонентами, но может быть использовано с любой системой для обработки данных, к примеру, в личных или других цифровых устройствах связи, сотовых телефонах и других мобильных или носимых устройствах, планшетных компьютерах, или же любых других системах для сбора, обработки, преобразования, отображения и распространения аналоговых и цифровых данных. Компьютерная система 3 содержит серверный компьютер 4, который имеет микропроцессорный блок 5 (также называемый в данном документе как «процессор») для приема и обработки программных продуктов, а также для выполнения других функций обработки информации. Устройство вывода 7, такое как визуальное устройство отображения, электрически соединено с процессорным устройством 5 для отображения информации, связанной с пользователем и связанной с программным обеспечением, к примеру, с помощью средств графического пользовательского интерфейса. Клавиатура 8 также может быть соединена с процессорным устройством 5 для того, чтобы обеспечить возможность пользователю вводить информацию в программный продукт. Помимо всего прочего, при использовании клавиатуры 8 для ввода, также может использоваться мышь 6 для перемещения селектора на дисплее 7 и графическом пользовательском интерфейсе, или, в качестве альтернативы, сенсорный экран смартфона, умные часы iPhone, iPad, iPod, пригодные для носки очки виртуальной реальности, или же планшетный компьютер, или любое другое устройстве ввода может быть предоставлено для выбора элемента и обеспечения ввода в процессор 5. Устройства для измерения боли, которые в некоторых вариантах реализации изобретения могут упоминаться в данном документе как устройства PainTrace 14, а также другие биофизические устройства и датчики 11, интегрированы в компоненты и функции системы PMD 10, которая может быть в виде программного обеспечения и/или оборудования. Как описано в данном документе, эти функции и компоненты системы PMD 10 могут инициализировать связь с электродами и датчиками, и устанавливать протоколы связи с одним или более устройствами PainTrace 14, а также другими биофизическими устройствами и датчиками 11 для предоставления команд в виде запуска, остановки, настройки и выбора времени, частоты дискретизации, а также других параметров сбора данных. Система PMD 10 также может связывать устройства PainTrace 14 и другие биофизические устройства и датчики 11 с пациентом, протоколом лечения, одним или более поставщиками медицинских услуг НСР и/или врачами, клинической или больничной сетью, а также другой соответствующей информацией, связанной с пациентом, лечением, и полученными данными, как описано в данном документе. В системе PMD 10 устройства PainTrace 14 и другие биофизические устройства и датчики 11 могут автоматически размещаться и идентифицироваться через эти связи, для оказания помощи поставщику медицинских услуг (НРС) и четкого представления полученных данных, которые относятся к конкретному пациенту, в соответствии с соответствующими руководящими принципами здравоохранения. Компоненты и функции системы PMD 10 также могут устанавливать предупреждения и аварийные сигналы с конкретной контактной информацией для непосредственного контакта с поставщиком медицинских услуг (НСР) или врачом в случае чрезвычайных обстоятельств, доступа к устройству PainTrace 14 и другим биофизическим устройствам и датчикам 11 для замены или сброса значений, и обеспечивают отслеживание частоты измерений матрицы боли и центральной нервной системы или же других показаний датчика. Различные компоненты и функции системы PMD 10 доступны из устройства для измерения боли 14, от других биофизических датчиков 11, от планшетного компьютера или смартфона, используемого поставщиком медицинских услуг (НСР) или врачом, и/или через сетевую или серверную систему, как описано в данном документе. К примеру, поставщик медицинских услуг (НСР) по вызову, может получать предупреждение и может корректировать частоту показаний для получения большего количества данных от устройства для измерения боли с использованием смартфона в приемлемых условиях и безопасности в среде сбора и обработки данных 1 и сети 16. Следует понимать, что ввод данных не ограничивается известным устройством ввода и способами, но включает способы ввода и устройства, которые еще будут разработаны.
Запоминающее устройство и хранилище данных в любой форме могут быть включены и изображены в виде устройства с жестким диском, такого как считываемый компьютером информационный носитель 2, который может содержать программный продукт, и подключен к микропроцессорному блоку 5 для обеспечения средств ввода программных продуктов и другой информации в микропроцессорный блок 5. Также могут быть представлены множество типов запоминающего устройства, и данные могут быть записаны в любой подходящий тип запоминающего устройства. Запоминающее устройство может быть наружным и доступным, используя проводное или беспроводное соединение, как напрямую, так и через локальную или крупномасштабную сеть, такую как Интернет. Более того, как известно в данной области техники, процессорное устройство 5 может быть запрограммировано для хранения программного продукта внутренним образом. Устройство вывода 7 визуально отображает пользователю транзакционные, интерактивные или переменные данные, которые подвергались изменениям. Устройством вывода 7 может быть монитор, сенсорный экран или другой экран визуального компьютера или цифрового устройства, или же графический пользовательский интерфейс (ГПИ), регистрирующее записывающее устройство, принтер или другое устройство вывода, которое обеспечивает визуальное или другое представление конечного вывода из процессорного устройства 5. Устройство вывода 7 также может представлять собой устройство вывода в форме устройства для сбора данных, такого как устройство для измерения показателей матрицы боли и центральной нервной системы или другой системы биосенсорного медицинского устройства, которая обеспечивает данные транзакций в виде аналогового или цифрового вывода и/или в виде цифрового файла. Процессорное устройство 5 предоставляет средства для обработки и преобразования транзакционных, интерактивных или переменных данных для получения легко различимых, информационных и подготовленных изображений и данных на предполагаемом устройстве вывода или носителе. Специалисты в данной области техники поймут, что данное изобретение не ограничивается только лишь упомянутыми функциями обработки данных и преобразования данных.
Серверный компьютер 4 может хранить компьютерный программный продукт, который имеет программу, хранящуюся на считываемом компьютером информационном носителе 2, который может содержать, к примеру: магнитный носитель данных, такой как магнитный диск или магнитная лента; средства оптического хранения информации, такие как: оптический диск, оптическая лента, или машиночитаемый штриховой код; твердотельные электронные запоминающие устройства, такие как оперативное запоминающее устройство (ОЗУ), постоянное запоминающее устройство (ПЗУ) или устройства хранения данных флеш-памяти. Связанная компьютерная программа и сервер данных могут быть реализованы с помощью программного обеспечения 17 в SaaS (программное обеспечение как услуга), PaaS (платформа приложений как услуга) или по требованию вычислительной службы, такой как облачная или общая база данных ресурсов через веб-браузер или другой интерфейс. Защищенные логины и пароли могут предоставляться для удаленного доступа к различным уровням программного обеспечения 17 через интранет или интернет соединение 13. Одно или более устройств для доступа к системе PMD 10 могут быть подключены по беспроводной сети, к примеру, по сотовой сети, беспроводной сети Wi-Fi, технологии Bluetooth или другой технологии, когда устройство подключено либо напрямую, либо через сеть. Следует понимать, что такие устройства могут быть мобильными устройствами с использованием голосовых команд для ввода данных и доступа к данным с использованием цифровых устройств, которые могут быть в виде камеры, карманного персонального компьютера КПК, iPod, iPhone, iPad, планшетного компьютера, очков виртуальной реальности, цифрового дисплея, смартфона или мобильного телефона, умных часов, пригодных и других цифровых устройств, которые могут использоваться как процессорное устройство, блок преобразования данных, устройство отображения или блок для предоставления инструкций по обработке данных и как услуга, предлагаемая через Интернет.
Система PMD 10, реализованная в серверной системе BioTraceIT 18 системы PMD, в варианте реализации изобретения может иметь протоколы безопасности 9, одну или более базы данных 19, модуль административного инструмента 21, модуль сбора данных 23, для приема и преобразования данных из устройства для измерения показателей матрицы боли и центральной нервной системы или других данных датчика, модуль связи 25 для сбора и передачи данных, которые могут быть в форме писем, переданных по электронной почте, текстовых сообщений, голосовых сообщений а также других протоколов связи, модуль анализа данных 27 а также модуль компиляции данных 29. Серверная система BioTraceIT 18 системы PMD может собирать, компилировать и хранить данные из множества устройств для измерения показателей матрицы боли и центральной нервной системы и других датчиков в различных средах сбора и обработки данных 1, таких как одна или более сетей, которые включают больничную сеть 16 и мониторинг пациентов на дому. Серверная система BioTraceIT 18 системы PMD дополнительно обеспечивает передачу, сбор и хранение ссылочных данных 31 через интранет или интернет соединение, как изображено на Фиг. 2. Система PMD 10 через модуль связи 25 может дополнительно предоставлять обновления программного обеспечения и прошивки, а также ссылки на обновления для поддержания самой доступной в настоящее время информации для поставщиков медицинских услуга (НСР) и других пользователей системы PMD 10.
Система PMD 10 может быть реализована в виде мобильного приложения для iPhone, iPad, iPod, смартфона, умных часов, пригодных для носки очков виртуальной реальности, планшетного компьютера и/или другого мобильного цифрового устройства. Дополнительно, система PMD 10 может быть разработана на операционной системе компьютера, которая должна быть реализована на системных серверах 32 больничной сети 16, к примеру, в качестве приложения для приборной панели 24 для медицинских сестер, работающей на компьютерной системе, которая функционирует на базе Windows. В любом формате, система PMD 10 представлена для поставщиков медицинских услуг (НСР) для выбора устройства для измерения показателей матрицы боли и центральной нервной системы, такого как устройство PainTrace 14 или другой датчик, или медицинское устройство 11, а также сопоставления данных датчика с информацией о пациенте, и, кроме того, контроля собранных данных и получения предупреждений, основанных на пороговых значениях. В одном варианте реализации изобретения система PMD 10 может сообщаться исключительно с больничной серверной системой 16 с целью оптимизации времени обновления хранилища данных и для получения обновлений от централизованного источника-сервера 16. Затем собранные данные могут быть сжаты и переданы на внешнюю серверную систему BioTraceIT 18 системы PMD с повторяющимися интервалами для того, чтобы уменьшить необходимую пропускную способность и время передачи. В дополнительных вариантах реализации изобретения система PMD 10, которая содержит одно или более устройств для измерения показателей матрицы боли и центральной нервной системы 14 или другие биосенсоры 11, может быть реализована на мобильных устройствах для пациентов с целью контроля индивидуальных показателей состояния здоровья.
Как изображено на Фиг. 3, диаграмма представляет различные компоненты и функции программных приложений и аппаратных средств в виде устройств для сбора данных системы PMD, некоторые или все из которых могут быть включены в различные формы системы PMD 10, которая может использоваться пациентами, поставщиками медицинских услуг, страховыми компаниями, администрацией больницы и другими лицами. Компоненты и тип данных, содержащиеся в каждых компонентах, как описано в данном документе, предоставлены с общим контекстом и прикладной программой данных. Модуль сбора данных 23 системы PMD 10 является по существу основным компонентом Physiological Readings 52 для сбора данных из устройств для измерения показателей матрицы боли и центральной нервной системы, таких как устройство PainTrace 14, и для сбора других данных датчика для анализа в системе PMD 10. Эти данные собраны и скомбинированы с компонентом данных о состоянии здоровья «Patient»» 54 и компонентом 56 демографических данных о популяции пациентов, называемый «Disease Specifics», содержащий данные исследования, факторы, влияющие на восприятие боли, острые и хронические болезненные состояния и рекомендации. Компоненты и функции в системе PMD 10 могут быть дополнительно предоставлены в компоненте «Treatment» 58, предоставляя протоколы и результаты назначенных лечений. В варианте реализации изобретения система PMD 10 сочетает физиологические показатели, в данном примере связанные с измерениями показателей матрицы боли и центральной нервной системы, с соответствующими данными, относящимися к, но не ограничиваясь этим, компонентам исследования и анализа данных, для получения «объективных показателей боли» и оценки показателей результата измерения матрицы боли и центральной нервной системы в соответствии с биофизическими факторами пациента, диагнозом, полем ввода конкретных данных и лечениями.
Компонент Physiological Readings 52 получает данные, которые включают измеренные данные матрицы боли и центральной нервной системы, полученные при помощи устройства PainTrace 14, и другие ориентированные на датчик показатели, имеющие отношение к реакции организма на стресс, заболеванию и лечебно-оздоровительному опыту. Компонент данных Patient 54 предоставляет данные в виде биологических данных, относящихся к особенностям возраста пациента, здоровья и истории болезни пациента, которые включают, но не ограничивается этим, биологические, психологические, социальные и экологические факторы. Эти данные могут быть предоставлены или дополнены пациентом как часть их интеграции в лечение и дополнительно запрошены из электронных медицинских карт, записей и других данных, полученных в отношении пациента. Данные пациента, переданные в серверную систему BioTraceIT 18 системы PMD, могут быть деидентифицированы в соответствии с соответствующими руководящими принципами здравоохранения. Используя модуль анализа данных 27, собранные данные, такие как данные, собранные от устройства PainTrace 14 и других биосенсоров 11 могут быть нормализованы, усреднены и скоррелированы с конкретными видами деятельности, продуктами питания, физическими упражнениями и другими биофизическими действиями пациента. Компоненты и функции системы PMD 10 используют и объединяют преобразованные собранные данные с физиологическими показателями и биологическими, психологическими, социальными и экологическими факторами для разработки биокластерных матриц и двусторонних диаграмм, которые используя алгоритмы, использующие весовые коэффициенты коррелируют и оценивают для разработки того, что в данном документе относится к данным BioTrace 150. Путем преобразования и сопоставления исходных данных, которые являются природно субъективными, создаются объективные физиологические показатели, и данные от устройства PainTrace 14 и измерения показателей матрицы боли и центральной нервной системы а также диагностического способа становятся все более значимыми и могут использоваться для оценки восприятия и переносимости боли пациентом для улучшения правильной диагностики и лечения.
Для дополнительной стандартизации физиологической реакции на боль и последующего измерения показателей матрицы боли и центральной нервной системы с использованием устройства PainTrace 14 в системе PMD 10, вспомогательное устройство, которое доставляет стандартизированный болевой раздражитель, интегрировано в систему PMD 10 и диагностический способ. Внедрение вызывающего боль раздражителя, или болевого раздражителя, на основе существующих в настоящее время тестов для определения связанной с центральной нервной системой реакции на раздражители, таких как надавливание в надглазничной области или трение в области грудины, или периферические тесты, такие как сжатие области лунки ногтя на пальце или на большом пальце стопы, или надавливание на сторону пальца, будет повторяемым и измеряемым с помощью измерительных устройств, а также датчиков давления и натяжения для применения раздражителя с постоянной и повторяемой величиной надавливания для того, чтобы стандартизовать применяемый раздражитель. Раздражитель будет применяться в течение стандартизированного времени при измерении уровней боли пациента или активности матрицы боли, перед, во время и после применения раздражителя. «Реакция на стандартные раздражители» может измеряться в течение периодов здорового состояния, например, при ежегодном визите, или во время травмы или болезни для того, чтобы установить исходный уровень для «уровней реакции матрицы боли». Затем показатели активности матрицы боли пациента будут применены к стандартизированным шкалам, которые будут использоваться с другими факторами для создания данных PainTracePainTrace Factor, которые ссылаются на этот исходный уровень активности матрицы боли. Уровни реакции матрицы боли дополнительно перекрестно ссылаются на другие известные факторы, которые влияют на толерантность пациента к боли, которые включают, но не ограничиваются этим, возраст, пол, расу, артериальное давление, предыдущую травму, исследования показателей боли, и дополнительные физиологические и психосоциальные показатели, которые индивидуализируют измерения, которые могут представлять собой некоторые из компонентов, которые упоминаются в данном документе как данные BioTrace Factors 150. Добавление этих факторов к исходному уровню активности матрицы боли, измеренному с использованием болевого раздражителя, используется для получения персональных данных PainTracePainTrace Factor пациента.
Данные измерения показателей матрицы боли и центральной нервной системы и данные BioTrace Factors 150 могут быть дополнительно реализованы в компоненте «Treatment» 58 системы PMD 10 для отслеживания и измерения объективных физиологических показателей, относящихся к протоколам лечения и результатам лечения. Связывание курсов лечения и сравнение физиологических показателей, имеющих отношение к курсам лечения, могут привести к лучшему пониманию того, насколько эффективным является каждый курс лечения, и дополнительно, поскольку он также связан с данными пациента, предоставленными в компоненте пациента 54, существует возможность специализировать и индивидуализировать варианты лечения для отдельного пациента. Более того, анализ и связывание лечения, демографических данных пациента, а также острых и хронических болезненных состояний могут не только способствовать улучшению индивидуального ухода, но и также предоставлять более обширные данные о болезненных состояниях, что приводит в результате к более эффективному уходу за всеми пациентами и связанной с этим экономии затрат.
Более обширные данные об эффективности курсов лечения из набора физиологических показателей во время лечения, и интеграция, а также анализ этих данных, которые относятся к справочным материалам 31, предоставляются при использовании компонента «Disease Specifics» 56. Этот компонент системы PMD 10 может интегрировать данные о конкретных острых и хронических недомоганиях и болезнях с информацией, относящейся к данным BioTrace Factors 150 конкретного пациента, для обеспечения более значимого понимания физиологических показателей в мультифакториальных болезненных состояниях, таких как восприятие боли. Помимо всего прочего, эти данные, полученные из биомедицинских, медицинских, клинических и физиологических исследований могут ссылаться на соответствующих конечных пользователей, таких как медицинские работники, как для обучения, так и для создания ресурсов, доступных для медицинского персонала. Полученные демографические данные Biotrace Factor могут быть сгруппированы по основным критериям (биологическим, психологическим, социальным, экологическим, поведенческим, и т.д.), которые считаются актуальными на основании данных о пациенте. Разработка и ранжирование данных BioTrace Factors 150 могут постоянно и итерационно обновляться посредством интеграции информации о состоянии болезни и лечения в справочных материалах 31, и могут перекрестно ссылаться, используя модуль компиляции данных 29 системы PMD 10, генерирующий тенденции и потенциальные улучшения в уходе. Данные клинического исследования могут быть дополнительно связаны с использованием компонентов и функций системы PMD 10 для создания более тесной связи между исследованиями, результатами исследований и потенциальными новыми способами лечения.
Использование компонента Physiological Readings 52 вместе с компонентом Patient 54, компонентом Disease Specific 56, и данными компонента Treatment 58 будет не только создавать нормализованные, коррелятивные, объективные показатели преимущественно субъективных симптомов, но и, более того, может быть связано с самооценкой пациента, и контролируемым датчиком образом жизни, влияющим на программные приложения, упомянутыми в данном документе как компонент LifeTraceIT 60 системы PMD 10; программным обеспечением и приложениями для медицинских работников, называемым компонентом BioTraceIT 62 системы PMD 10 для оказания помощи в принятии решения для тестирования, диагностики и лечения; а также с финансовыми последствиями лечения посредством отслеживания затрат и эффективности, упомянутыми в данном документе как MediTraceIT 64 системы PMD 10 для создания комплексной системы для интеграции множества факторов, которые влияют на субъективные физиологические ощущения пациентов. Преобразованные данные могут быть использованы для создания конкретных электронных сообщений пациента, таких как с использованием текстовых сообщений через специализированные или другие мобильные устройства, для привлечения пациента к потенциальной оценке источников изменений матрицы боли, и для того, чтобы обеспечить привлечение пациентов к участию в обучении, поощрение здоровых привычек и поведения, а также отслеживание физической активности по отношению к физическим данным, создаваемым устройством. Изменения в уровнях боли могут повлечь за собой ряд вопросов. Эта функция программного обеспечения LifeTraceIT 60 будет представлять собой «интегрированное ведение журнала», которое использует физиологические вопросы, основанные на данных биосигнала, для запроса конкретной информации от пострадавшего человека для того, чтобы способствовать в обнаружении источника боли или болезненного раздражителя. Программное приложение LifeTraceIT 60 в виде компонента системы PMD 10 использует преобразованные данные в сочетании с определенными платформами взаимодействия с пациентом для взаимодействия с пациентами.
Медицинский компонент BioTraceIT 62 системы PMD 10 генерирует нормативные данные и данные BioTrace Factors для медицинских работников и будет способствовать более глубокому пониманию ощущений пациента и повышению способности оценивать эффективность лечения. Компонент BioTraceIT 62 в системе PMD 10 может приносить пользу пациенту во время оказания неотложной помощи в тех случаях, когда данные показателей измерений матрицы боли и центральной нервной системы или данные PainTrace могут указывать на степень и местоположение боли посредством анализа данных, используя компоненты и функции системы PMD 10 при проведении протокола обследования. Компонент BioTraceIT 62 может дополнительно принести пользу врачам, медицинским сестрам, физиотерапевтам и другим лицам путем предоставления данных о пациентах для того, чтобы дать представление о профиле пациента, влияющих факторах, сопутствующих заболеваниях, а затем ассоциировать релевантность этих факторов с учетом ощущений пациента и предоставить соответствующие алгоритмы лечения и данные клинических исследований для рассмотрения поставщику медицинских услуг (НСР).
Компонент LifeTraceIT 60 системы PMD 10 также опционально может быть предоставлен и доступен на устройстве PainTrace 14 и/или других медицинских устройствах на уровне доступа пациента и/или через программное приложение мобильного цифрового устройства. Сначала пациент может предоставить информацию о состоянии здоровья через определенные обследования и формы данных для медицинских учреждений и учреждений здравоохранения, использующих систему PMD 10 и/или датчик PainTrace 14 и другие медицинские датчики и устройства. В процессе заполнения и ввода данных медицинского обследования или конкретных областей пациенту может быть также предоставлена возможность использовать компонент LifeTraceIT в качестве личной электронной медицинской карты. Компонент LifeTraceIT 60 системы PMD 10 может предоставляться абоненту в нескольких режимах интерфейса, таких как следующие:
• компонент Personal Lifestyle Tracking Component - компонент LifeTraceIT 60 может использоваться для регистрации физической активности, физиологических измерений, лечения, использования лекарственных средств, отпускаемых по рецепту, а также других связанных с пациентом данных. Компонент LifeTraceIT 60 может собирать данные, полученные с использованием устройства PainTrace 14 и других физиологических измерительных датчиков, и собирать данные, имеющие отношение ко времени, которое затрачено на выполнение упражнений, сон, питание и другие виды деятельности, а также собирать эмоциональные данные для того, чтобы помочь пациенту отслеживать и использовать свои собственные данные LifeTraceIT для разработки и улучшения курсов лечения.
• Компонент Healthcare Network - персональные данные, собранные у пациента, отмеченные выше, могут дополнительно быть переданы предпочтительным поставщикам медицинских услуг, системам больниц и сетями, включая серверную систему BioTrace IT 18 системы PMD. В конечном итоге пациент улучшает свою способность восстанавливать здоровье и понимать свои физиологические симптомы путем совместного использования своих персональных данных с поставщиками медицинских услуг. Путем использования этих данных в программном компоненте BioTraceIT 62 анализ данных может привести к тому, что поставщик медицинских услуг (НСР) сможет лучше оценить эффективность вариантов лечения, варианты образа жизни и личные предпочтения для улучшения как личных, так и глобальных результатов, связанных со здоровьем и исходами заболеваний. Эти данные могут также быть использованы органами здравоохранения для улучшения понимания лечения, образа жизни и демографических факторов для создания оптимизированных медицинских вмешательств со специализированной направленностью.
• Компонент Guidance and Messaging Component - кроме того, компонент LifeTraceIT 60 может также предоставлять рекомендации и информацию, которые помогут пациенту во время лечения. Компонент LifeTraceIT 60 системы PMD 10 может собирать данные из других программных приложений для отслеживания состояния здоровья, которые пользователь может использовать и с соответствующим лицензированием, причем эти данные будут включены в LifeTraceIT и BioTraceIT. Данные могут быть интегрированы с другой информацией и собранными данными в систему PMD 10 для того, чтобы помочь пациенту адаптироваться, а также изменить определенный режим и модели поведения в рамках и в соответствии с предписанным режимом лечения. Компонент LifeTraceIT 60 может также предоставлять настраиваемый обмен сообщениями, который должен быть создан и использоваться в качестве шаблонов для обмена сообщениями с врачом, поставщиком медицинских услуг (НСР) или другим провайдером для того, чтобы обеспечить пациенту возможность мотивировать, отвечать на вопросы и уменьшить беспокойство по мере того, как происходит изменение поведенческих моделей пациента. Например, для улучшения результатов лечения пациентов с хронической болью алгоритм взаимодействия на основе полученных устройством физиологических данных может создавать шаблон обмена сообщениями для того, чтобы помочь пациенту улучшить принятие решений относительно использования предписаний для устранения боли и инициирующих факторов для того, чтобы влиять на механизмы психологической адаптации к боли нефармакологическими способами. Врачи могут считать необходимым инициировать ориентированные на лечение шаблоны обмена сообщениями для того, чтобы сделать их доступными для пациента в течение заданного периода времени, например, за счет использования ежедневного сообщения, или в определенное время, например, при введении лекарств. Изменение формы боли может инициировать «шаблон 10-60», который использует 10 вопросов о последних 60 минутах для определения источника, мотивации или данных, связанных с вмешательством. Обмен сообщениями также может включать в себя изменения в данные BioTraceFactors 150, как описано в данном документе, которые привели в качестве примера к уменьшению боли, для того, чтобы мотивировать и показать значение собранных данных и поддерживания требований предписанного лечения. В качестве альтернативы, боль или другие биофизические измерения с помощью системы PMD 10 могут инициировать сигналы тревоги, которые обеспечивают обмен сообщениями или вопросы для пациента, например, когда пороговые значения боли повышаются вследствие влияния, например, мигрени. Программное обеспечение LifeTraceIT или устройство, связанное с системой PMD 10, инициирует «10-60 Messaging» для того, чтобы привлечь пациента к определению источника боли во время изменения формы боли. В силу того, что мигрени могут быть вызваны пищей, красителями для одежды, ароматизирующими веществами и другими химическими веществами, из системы PMD 10 отправляется текстовое сообщение с вопросами об окружающей среде, физической активности или о том, какая пища была недавно употреблена, например, 10 вопросов для получения информации о последних 60 минутах. Ответ будет собран и оценен для того, чтобы помочь определить, что может вызывать усиление боли. Например, пациент отвечает, что за еда у них была в последнее время, и они выбирают из списка продуктов, которые они съели, или вводят альтернативную запись о еде, если она не включена в список. Им задают вопрос: местоположение; какие места для сидения - например, стул с спинкой или табурет без спинки варианты; были они в помещении или на открытом воздухе; если на улице они были вблизи растительности, то какого типа; был ли напиток - если да, это был алкоголь, содовая вода и т.д. Список определяется болезненным состоянием или травмой для определения источника изменения формы боли, обнаруженного с помощью устройства Pain Measurement 14, в течение определенного периода времени, когда измеряется увеличенный показатель боли. Ответы на 10-60 вопросов интегрируются в систему PMD 10, а затем в сочетании с программным приложением LifeTraceIT преобразуют физиологический симптом в инструмент диагностики и отслеживания. Другие сценарии «10-60 Messaging» могут включать в себя участие пациентов, обучение и соблюдение предписанного режима терапии, наряду с некоторыми другими.
Любое предписанное медицинское обследование и/или лечение связано с расходами, для пациентов, больниц и поставщиков страховых услуг с существующими способами в системе здравоохранения, приводящими к разобщению через сложное кодирование и кодирующие подмножества, которые необходимо вводить для каждого этапа лечения. Интеграция системы PMD 10 с электронными медицинскими картами может исключить дублирование работы и расширить использование кодов. Для крупных больниц совершенно другая группа людей из персонала от поставщика медицинских услуг (НСР) может вводить коды лечения, которые создают счета для пациентов и страховых компаний. Несмотря на то, что финансовые возмещения не должны держать в определенных пределах или ограничивать лечение, предлагаемое пациентам, дополнительные знания о продолжительности и эффективности лечения и связанных с этим расходах могут более быстро привести к изменению неэффективных способов лечения. Компонент MediTraceIT 64 системы PMD 10 объединяет медицинские карты и отслеживает лечение и лекарства, которые назначены для каждого пациента. Эта информация четко представлена врачам, поставщикам медицинских услуг (НСР) и другим лицам с временными рамками, которые минимизируют рабочую нагрузку и уменьшают дублирование и ошибки. В рамках компонента MediTraceIT предусмотрены возможности добавления кодирования и комментария для лечения таким образом, что учет, конкретный для получаемого лечения, может быть приведен в табличной форме. Система PMD 10 дополнительно предоставляет в рамках эффективного и четкого изложения комбинации лечения, предписанного пациенту, его относительную эффективность и стоимость для того, чтобы помочь поставщику медицинских услуг (НСР) с выявлением лучших вариантов лечения, оптимизацией затрат и, кроме того, помочь выявить неправильное употребление медикаментов со стороны пациента. Система PMD 10 предоставляет компонент MediTraceIT 64 в качестве системы для отслеживания затрат и эффективности, которая сочетает анализ оказания медицинской помощи от компонента BioTraceIT 62 с физиологическими показателями из собранных данных от датчиков и связанной информации об образе жизни из компонента LifeTraceIT 60. Путем отслеживания результатов оказания медицинской помощи, вариантов лечения, эффективности и затрат, компонент MediTraceIT 64 системы PMD 10 обеспечивает возможность сетям здравоохранения, больницам, поставщикам и плательщикам анализировать лучшие варианты лечения. Кроме того, с помощью компонента LifeTraceIT 60 возврат страховых премий может быть реализован путем вознаграждения пациентов, соблюдающий режим лечения, за последующие протоколы, которые основаны на фактических данных с документированными результатами лечения. Использование «MediTraceIT Treatment Protocols», означает, что если у пациента статистическая корреляция между лечением и результатом лечения, степень соблюдения пациентом предписанного режима терапии по сравнению с режимом лечения и результатами лечения через самоотчет может быть рассчитана для значимости (что означает, что пациент действительно сделал то, что ему было поручено сделать, что привело к эффективному результату лечения), то впоследствии пациент получит возврат оговоренной части его страховой премии. Таким образом, компонент MediTraceIT 64 системы PMD 10 может обеспечить способ мотивировать соблюдение пациентом предписанного режима терапии и впоследствии снизить затраты на здравоохранение за счет улучшения результатов лечения.
В варианте реализации данного изобретения, который изображен на Фиг. 4, модуль сбора данных 23 системы PMD 10 представляет собой интерфейс приложения PainTrace 70 для представления и анализа данных, полученных от устройства PainTrace 14, и биофизических устройств и датчиков 11. Устройство PainTrace 14 в качестве компонента системы PMD 10 обеспечивает результаты измерения и интеграцию данных от датчиков, которые могут быть в виде биосигналов, для анализа активности матрицы боли. Приложение PainTrace 70 содержит удаленную и встроенную в систему PMD схему, которая обеспечивает контроль сбора данных, связи и управление одним или более устройствами PainTrace и/или биофизическими устройствами и датчиками 11. Приложение PainTrace 70 дополнительно содержит функции определения местоположения и наличия для того, чтобы автоматически находить, инициализировать, отслеживать как связанные с ним электроды, устройство PainTrace 14, так и другие медицинские устройства 11 с конкретным пациентом, поставщиком медицинских услуг (НСР), врачом, клинической или больничной сетью. Приложение PainTrace обеспечивает возможность поставщику медицинских услуг (НСР) просматривать показания PainTrace в отношении активности матрицы боли и центральной нервной системы, а также парасимпатической нервной системы, которые связаны с болью, состоянием здоровья и лечением с требуемыми другими собранными биофизическими данными. Данные от датчика PainTrace 14 и/или биофизических устройств и датчиков 11 могут собираться непрерывно, с использованием модуля сбора данных 23 приложения PainTrace 70 в системе PMD 10 для отображения на устройстве и/или на других цифровых устройствах через сеть 12 в клинической или больничной среде и/или в серверной системе BioTraceIT 18 системы PMD. Модуль сбора данных 23 может улучшить качество данных за счет уменьшения шума и аномалий, и данные могут быть отобраны и сжаты для отображения в приложении PainTrace 70. Сигнал данных PainTrace 72 может быть представлен в связи с осью 74, обозначающей нулевой исходный уровень, где устройство PainTrace может измерять разницу либо в напряжении, либо в токе из измерений ЭДА, взятых из датчиков, размещенных контралатерально, а иногда ипсилатерально на пациенте с множеством источников биосигнала, потенциально способствуя полному измерению на основе регулируемого во времени мониторинга и интеграции. Сигналы данных 72, которые равны или очень близки к нулевой базовой линии, указывают на баланс в ЭДА с каждой стороны тела и коррелируют со сбалансированной активностью матрицы боли, которая не отражает состояние боли. Сигналы данных 72 выше или ниже нулевой базовой линии указывают на разницу в контралатеральной ЭДА и увеличение активности матрицы боли. Следовательно, для пациента с пиковыми значениями сигнала, которые проходят далее в направлении, обозначающем боль, без различия в отношении того являются положительными или отрицательными, как определено системой масштабирования, от оси 74, указывается на усиление боли. Как изображено на Фиг. 4, у пациента с отрицательным значением ниже исходного уровня отображается степень боли. У пациента с начальным отрицательным значением будет отображаться усиление боли в виде увеличивающегося отрицательного числа или отрицательного отклонения по отношению к исходному уровню 74. Разница между начальным результатом измерения боли и последующим результатом измерения боли представляет усиление или ослабление боли. Поэтому в этом примере отклонение в положительном направлении означает относительное ослабление боли или боль меньшей интенсивности. Система PMD 10 преобразует это отклонение, полученное как необработанный биосигнал, в показатель боли, более похожий на используемые в настоящее время стандартные шкалы для самоотчета, которые приравнивают отсутствие боли как эквивалент нулю и приравнивают худшую боль как эквивалент 100. При использовании системы PMD 10 шкалы боли могут быть стандартизированы на основе данных BioTrace Factors 150 пациента и производных данных PainTracePainTrace Factor 102. Например, молодые пациенты могут на сопоставимой основе иметь более положительные числа, и по этой причине отрицательное показание будет более значительным в этой популяции пациентов. И наоборот, пожилые пациенты могут иметь в целом более отрицательные или менее положительные показания, и по этой причине отрицательное число является связанным с другим уровнем боли. Система PMD 10 использует информацию о пациенте и других пациентах подобную демографической в нормализации данных активности матрицы боли, собранных для создания данных BioTrace Factors 150 и производных данных PainTracePainTrace Factor 102, которые характерны для пациента, но нормализованы к шкале на основе одинаковых групп населения. Дополнительные показания от ипсилатеральных датчиков также могут быть приняты и использованы для того, чтобы откалибрировать и подтвердить показания боли, поскольку эти данные также используются системой PMD 10 для нормализации собранных данных об активности матрицы боли, как описано в данном документе.
Уровень толерантности 76 может быть рассчитан специально для пациента на основе данных BioTrace Factors 150 и полученных данных PainTrace, как описано в данном документе. Уровень толерантности 76 может обозначать уровни невыносимой боли для пациента и может быть определен из максимального значения боли, ранее записанного для пациента, при этом пороговое значение увеличивается, если текущее максимальное значение превышено. Таким образом, собранные данные могут быть нормализованы с использованием факторов пациента, индивидуальной реакции на боль, и демографических данных, которые имеют известное влияние на боль, а уровень толерантности 76 может быть представлен выше или ниже нулевой базовой линии 74, как указывается с использованием данных BioTrace Factors пациента. Сигнал данных PainTrace 72 может быть представлен с использованием временного блока 78 для того, чтобы связать начало и продолжительность боли с физиологической активностью во время получения данных от устройства PainTrace 14. Поставщик медицинских услуг (НСР) может изменить шкалу времени 73 для просмотра данных, в виде более длинных или более коротких периодов времени от нескольких минут до нескольких часов, дней и других периодов времени, которые являются предпочтительными. Данные PainTrace в дальнейшем могут быть объединены и представлены с информацией об активности пациента, лекарственных препаратах и с другой информацией в пределах шкалы времени 73. Временной блок 78 может содержать функции прокрутки 80 для регулировки шкалы времени 73 для обзора данных.
Приложение PainTrace 70 дополнительно содержит значки для ввода данных и выпадающие поля, где является применяемым первый значок, предусматривающий применение лекарственного препарата, который вводится пациентом или поставщиком медицинских услуг (НСР). Значок Med 84 может расширяться и предоставить список лекарственных препаратов, прописываемых для пациента, и/или обеспечить окно ввода данных для пациента или специалиста для того, чтобы ввести информацию о, например, отпускаемом без рецепта обезболивающем лекарственном средстве. Значок Med 84 также может быть интегрирован с электронными медицинскими картами (EMR) для уменьшения дублирования или для того, чтобы расширить EMR при необходимости. Тип значков назначения 85 для лекарств может обеспечить быстрое ознакомление и проверку для поставщика медицинских услуг (НСР) в отношении того, когда и какой тип лекарственного препарата больному был введен в течение определенного периода времени. Значок Med Administration 85 позволяет пациенту или поставщику медицинских услуг (НСР) перетаскивать Medication Note 88 по временной шкале или интегрировать имеющие отношение данные из электронных медицинских карт. Если введение лекарственного средства происходит в течение определенного периода времени, например, посредством внутривенного введения (IV), поставщик медицинских услуг (НСР) может перетащить и расширить индикатор 98 в течение периода времени введения или в течение любого требуемого периода времени. Значок Nutrition 90 может предоставить для пациента или поставщика медицинских услуг (НСР) возможность вводить информацию о приеме пищи, значок Sleep 92 может предоставить информацию о времени сна, значок Activity 94 может предоставлять информацию о других видах активности, таких как работа, потребление алкоголя или другой социальной активности, и значок Exercise 96 может обеспечить время тестирования вместе с любым выбранным значком, обеспечивающим индикатор 98, который может быть расширен по временной шкале для того, чтобы отобразить фактическое затраченное время. В варианте реализации изобретения приложение PainTrace 70 может обеспечивать ввод данных, тем не менее, в предпочтительных вариантах реализации изобретения данные могут быть захвачены из компонента LifeTraceIT 60 системы PMD 10, который предоставляет физиологические данные пациента и данные об активности пациента из компонента MediTraceIT 64 системы PMD 10, которые будут интегрироваться в качестве дополнения с электронными медицинскими картами, данными о всех пациентах, которым назначают лекарства, протоколами лечения, вмешательств, другой информацией из медицинских карт о состоянии здоровья пациентов, и затратами в приложении PainTrace 70 и/или компоненте BioTraceIT 62 системы PMD 10, что может добавить предписанный протокол лечения в шкалу времени, чтобы пациент мог следовать ему и соблюдать. Затем пациент может подтвердить завершение этапов в протоколе лечения. Приложение PainTrace 70 в системе PMD 10 обеспечивает базовое сфокусированное значение боли пациента и групп, и отображает эту информацию в определенных временных рамках, а также лечение и активность пациента для того, чтобы сделать данные измерения боли и биофизическую информацию полезной для пациента или поставщика медицинских услуг (НСР). Показатель прогресса BioTrace Progress Score 280, оценивающий все эти факторы, может быть сгенерирован для каждого пациента в качестве быстрой ссылки на отслеживание совокупного прогресса пациента и улучшение или ухудшение его результатов лечения. Врачи могут дополнительно оценить совокупный прогресс путем просмотра отдельных наборов данных, включая данные BioTrace Factors 150, которые влияют на совокупный показатель прогресса BioTrace Progress Score 280.
Приложение PainTrace 70 может дополнительно предоставлять средние показатели измерения боли (PMR) 100 за любой выбранный период времени, и данные PainTracePainTrace Factor 102 на основании шкалы, полученной из измеренных физиологических данных и данных BioTrace Factors пациента. Индивидуальный ответ матрицы боли можно измерить по отношению к контролируемому и стандартизированному болевому раздражителю. Как описано выше, тест центральной нервной системы, такой как надавливание в надглазничной области или трение в области грудины, или периферические тесты, такие как сжатие области лунки ногтя на пальце или на большом пальце стопы, являются повторяемыми и измеряемыми с помощью измерительных устройств, а также датчиков давления и натяжения для стандартизации примененного раздражителя по сравнению с существующими в настоящее время процедурами тестирования, в которых подают давление или раздражитель в нестандартном режиме, основываясь на прикосновении врача или медицинского персонала. Уровни индивидуального ответа матрицы боли регистрируются в ответ на раздражитель в виде исходного уровня во время общих физических обследований для определения показателей исходного уровня во время травмы или болезни. Стандартный болевой раздражитель в сочетании с BioTrace Factors 150 формирует часть данных, которые преобразуются в PainTracePainTrace Factor 102 пациента. Contribution Factor 104, как описано в данном документе, представляет собой уровень, в котором индивидуальные биологические, поведенческие, экологические, психологические и социальные факторы, BioTrace Factors 150 относятся к PainTracePainTrace Factor 102. Приложение PainTrace 70 системы PMD 10 также может обеспечивать дополнительные физиологические измерения, такие как вариабельность частоты сердечных сокращений 302, которые могут быть использованы для определения тонуса блуждающего нерва пациента для того, чтобы обеспечить показатели для поставщика медицинских услуг (НСР) реакции пациента на стресс, болезненные состояния и уязвимости по отношению к болезни (Gunther и др. Critical Care 2013 г., 17:R51 http://ccforum.com/content/17/2/R51). В тех случаях, когда данные PainTracePainTrace Factor 102 отражают гиперактивную активность матрицы боли, но вариабельность частоты сердечных сокращений 302 демонстрирует несогласованность или гипоактивность по отношению к PainTracePainTrace Factor 102, это может служить инструментом для врача, чтобы идентифицировать источник необъяснимой хронической боли. Тонус блуждающего нерва и активность блуждающего нерва были связаны с обезболиванием путем эндогенного высвобождения эндорфинов. Указатель, подчеркивающий несоответствие этих двух диагностических показателей, может служить инструментом для дальнейшего тестирования и внимания к потенциальной медицинской проблеме. Napadow, V и др. Evoked Pain Analgesia in Chronic Pelvic Pain Patients using Respiratory-gated Auricular Vagal Afferent Nerve Stimulation. Pain Med. июнь 2012 г.; 13(6): 777-789. Опубликовано в Интернете, 8 мая 2012 г. doi: 10.1111/j.1526-4637.2012.01385.x). В любом компоненте системы PMD 10 значок 106 пациента предоставляет доступ к данным пациента, которые могут отображаться через компонент LifeTraceIT 60 или другие приложения данных пациента. Другие функциональные возможности 108 системы PMD могут быть предоставлены для сохранения, печати или отправки по электронной почте данных и создания отчетов с дисплея системы PMD.
Система PMD 10 может предоставить раскрывающийся список ПО для просмотра и сравнения данных в течение нескольких дней или даже недель для того, чтобы обнаружить отклонения и аномалии. Сигнал данных 72 из аналогичных периодов времени может быть выбран путем расширения раскрывающегося списка 110 относительно дней, представляющих интерес. Любое количество показателей 98 может быть выбрано для просмотра с тем, чтобы обеспечить сравнение этих показателей. В этом примере введение лекарственного средства показывает уменьшение сигнала данных PainTrace 72 вскоре после того, как пациенту вводили лекарственное средство, как показано в Medication Note 88 на Фиг. 4. Тем не менее, на Фиг. 5, как указано при помощи Medication Note 88, лекарство вводится, но сигнал данных PainTrace 116 демонстрирует усиление боли, схематически изображенное снижением до более отрицательного числа, в отличие от ожидаемого увеличения до положительного числа, которое будет отражать боль меньшей интенсивности после введения обезболивающих лекарственных препаратов. Как указано при помощи Medication Note 118, пациент, по-видимому, принимал обезболивающее лекарственное средство, когда уровни боли были значительно ниже оси 74 с небольшим изменением сигнала данных PainTrace 120, что, следовательно, может указывать на толерантность к лекарственным средствам, которая требует изменения дозировки, и/или на возможность неправильного употребления лекарственного средства пациентом. Система PMD 10 выделила эти различия, которые вызвали дальнейшее расследование. При рассмотрении отслеживаемой активности пациента, усиление боли после Medication Note 88 было объяснено сеансом физиотерапии непосредственно перед введенным лекарственным средствам в Medication Note 88. Информация об активности также раскрыла, что пациент съел обед непосредственно перед Medication Note 118. Прием пищи не объясняет, почему лекарственный препарат принимался, в тех случаях, когда пациент не испытывал боли, поэтому пациент был опрошен. После опроса выяснилось, что пациент считает, что прием лекарственного препарата на полный желудок уменьшит потенциальную тошноту. Понимание комбинации всех этих переменных данных было бы невозможным, или не было бы так просто замечено без системы PMD 10. Данные, отслеживание и физиологические сигналы, объединенные из сигналов данных PainTrace 72, и приложения LifeTraceIT 60 преобразуются через систему PMD 10 для того, чтобы создавать инструменты для оказания медицинской помощи, которые поддерживают грамотное принятие решений и улучшают результаты оказания медицинской помощи. Пациент получил дополнительную информацию об использовании и сроках приема лекарственного препарата для того, чтобы уменьшить частоту возникновения плохо управляемой острой боли, которая становится хронической болью, что является намного более сложным и дорогостоящим для лечения.
Устройство PainTrace 14 выполнено с возможностью измерения от момента к моменту относительного влияния матрицы боли и центральной нервной системы через обнаружение разности напряжения или силы тока между первым датчиком PainTrace, расположенным в местоположении на левой стороны тела, и вторым датчиком PainTrace, расположенным в аналогичном местоположении на правой стороны тела. Изменения активности матрицы боли и центральной нервной системы, а также тонус блуждающего нерва генерируют напряжения или ток, которые, как измерено с использованием датчиков PainTrace с низким напряжением смещения, обеспечивают согласованное количественное измерение боли. Датчики PainTrace являются пассивными и, следовательно, не требуют подведения напряжения к пациенту. Датчики PainTrace могут быть из субстрата серебра, графена или других материалов, покрытого AgCl, в качестве покрытия для достаточного проведения изменений напряжения активности матрицы боли и центральной нервной системы пациента, измеренных по всей средней линии тела. Датчики PainTrace могут быть влажными или сухими датчиками в зависимости от времени, в течение которого датчики носят во время сбора данных. Для влажных датчиков может быть использован клей для прикрепления датчика к коже, и проводящий гель может быть предварительно нанесен на местоположение на коже или на датчики для того, чтобы проводимость была стабильной от поверхности датчика PainTrace до кожи. Тем не менее, сухие датчики могут использоваться для более длительного периода ношения для мониторинга изменений боли в динамике по времени.
Для определения различий в проводимости между PainTrace датчиками на каждой из левой и правой сторон тела, особенно с использованием сухих датчиков, когда гель предварительно не применяется, измерение импеданса, проводимости и/или другие измерения могут производиться, например, путем подачи напряжения на датчики и измерения импеданса. Эти измерения также могут быть взяты от одного, либо левого, либо правого датчиков, путем подключения датчика к ипсилатеральному датчику для получения результатов измерения от одной стороны тела. Дополнительные результаты измерения могут быть взяты от пары ипсилатеральных датчиков или комплектов на контралатеральных сторонах тела, и показания могут быть использованы для калибровки показаний для каждого из датчиков PainTrace, на основе различий в контакте с кожей, состоянии кожи, движении, и других воздействий датчика на поверхность контакта с кожей и физиологических измерений. Большие различия в этих измеренных значениях могут указывать на неисправность датчика или ограниченный контакт поверхности датчика с кожей. Например, для небольших различий в импедансе в пределах указанных уровней толерантности, приложение PainTrace 70 системы PMD 10 может применять алгоритмы калибровки для регулировки смещения напряжения или силы тока между левым и правым датчиками PainTrace. Другие способы калибровки, доступные с использованием схемы системы PMD приложения PainTrace 70, могут включать в себя итеративную калибровку сопротивления для определения калибровочной кривой в связи с тем, что сопротивление систематически увеличивается и/или уменьшается, и измерения напряжения или тока проводятся при каждой регулировке импеданса. На основании калибровочной кривой переменный нагрузочный резистор через соединение с контралатеральными и/или ипсилатеральными датчиками настраивается для оптимизации напряжения и тока, и улучшения сигнала по шуму и качеству измеряемого сигнала от PainTrace или других биофизических датчиков. Например, переменный нагрузочный резистор может быть скорректирован для получения максимальной силы тока. Некоторые варианты реализации изобретения схемы системы PMD приложения PainTrace 70 содержат компоненты для подачи тока к электрохимическому конденсатору датчика PainTrace с целью улучшения энергетических и мощностных характеристик. Могут возникнуть потери в эффективности в связи с саморазрядом во время хранения датчиков или неправильного обращения во время применения, снижая общую чувствительность датчиков. Использование калибровки сопротивления или другие способы калибровки, соответствующие текущему значению могут быть определены и применяться к каждому датчику PainTrace во время инициализации или периодически во время сбора данных, и между ними, для поддержания электрохимического конденсатора датчика PainTrace в полностью заряженном состоянии.
Кроме того, поскольку движения пациента могут влиять на общее качество показаний, возможно, создавая импульсные помехи или другие аномалии, приложение PainTrace 70 может использовать один или более акселерометров на устройстве PainTrace или на других цифровых устройствах или других датчиках для корреляции импульсных помех или аномалий связанных с движениями, и использовать эту информацию для того, чтобы сгладить, уменьшить или удалить эти признаки из собранного сигнала данных PainTrace 72. Эти настройки обеспечивают для компонента приложения PainTrace 70 системы PMD 10 отображение и передачу точных сравнений измерений напряжения от левого и правого датчиков PainTrace для обеспечения согласованного количественного измерения активности матрицы боли и центральной нервной системы посредством измерения в цепи, соединяющей контралатеральные датчики PainTrace.
Как изображено на Фиг. 6А, датчики 35 PainTrace в первом варианте реализации изобретения могут быть в виде двух самоклеящихся датчиков, помещенных в ладонь каждой руки на область возвышения мизинца или возвышения большого пальца пациента, которые непосредственно соединяются с использованием проводов 33 с устройством PainTrace 14, изображенном на Фиг. 6В, и как описано в патенте США №8560045 на имя Burke. Датчики 35 PainTrace могут в некоторых вариантах реализации изобретения иметь держатель 39 со слабым клеем, который удерживает датчик 35 на месте, и который соединяет провода 33 с устройством PainTrace 14. Датчик 35 PainTrace может быть извлечен из держателя 39 и удален после одного или более считываний показаний в течение определенного периода времени. Например, медицинское физическое измерение боли может быть проведено после того, как пациент спокойно сидит в течение короткого периода времени, возможно, в течение 10 минут. Затем получают результаты измерения у пациента с использованием устройства PainTrace 14, и собранные данные могут быть использованы для вычисления данных PainTracePainTrace Factor 102, которые записываются для использования в качестве исходного уровня для будущих измерений боли, даже если пациент в настоящее время не испытывает никакой боли. Например, во время общего физикального обследования исходные уровни определяются с помощью системы PMD с комбинацией стандартизированных болевых раздражителей, реализованных посредством контролируемого и регулируемого во времени давления. Контролируемый ответ на раздражитель выражает уровни ответа матрицы боли пациента, которые в сочетании с данными пациентов BioTrace Factors 150 создают индивидуальные данные PainTracePainTrace Factor 102 для пациента. Уровни ответа матрицы боли являются доступными для немедленного использования и хранятся для последующей болезни или травмы, при которых потребуются измерения боли и физикальная диагностика. Самоклеящиеся левый и правый датчики 35 удаляются из держателя 39 и выбрасываются после однократного использования. Держатель 39 в некоторых вариантах реализации изобретения может быть прижат к коже для образования герметичного уплотнения, создавая таким образом всасывание для того, чтобы прикрепить датчик в требуемом месте, устраняя потребность в гелях. В силу того, что удаление и замена каждого датчика внутри держателя 39 может вызывать изменения в проводимости поверхности 37 датчика 35 PainTrace к коже пациента, дополнительный проводящий гель может быть нанесен на требуемую область или датчик, если используются влажные датчики, и приложение PainTrace 70 может измерить импеданс и/или запустить алгоритмы калибровки для того, чтобы отрегулировать измерения напряжения от левого и правого датчиков, чтобы они находились в допустимых диапазонах допуска друг от друга по мере необходимости на основе этих измерений.
В дополнительном варианте реализации данного изобретения, который схематично изображен на Фиг. 6С, заменяемое крепление датчика 41 снимает требование о том, чтобы удалять только датчик PainTrace 43 для замены. Держатель датчика 45 представляет собой жесткий материал с гибким адгезивным основанием 47, которое представляет собой сжимаемый проводящий материал, который обеспечивает, чтобы датчик 43 PainTrace оставался в контакте с поверхностью кожи, даже в тех случаях, когда пациент движется. Фиксирующий элемент 49, который надежно удерживает датчик 43 PainTrace в требуемом месте, прикреплен к жесткому рычагу 51, который прикладывает давление к датчику 43 PainTrace для того, чтобы выровнять и удерживать датчик 43 PainTrace относительно гибкого проводящего адгезивного основания 47, тем самым поддерживая электрический контакт с кожей. Жесткий рычаг 51 является достаточно тонким для того, чтобы минимально препятствовать двигательной возможности пациента при использовании его рук, но сделан из жесткой проволоки, которая может быть согнута для того, чтобы соответствовать ладони пациента или другой области тела при использовании крепления датчика 41 PainTrace для выравнивания и удерживания датчика PainTrace 43 на коже пациента. Заменяемое крепление датчика 41 PainTrace имеет соединитель 53, который в первом варианте реализации изобретения может быть вставлен в приемник 55, прикрепленный лентой к запястью, плечу, голени или лодыжке для того чтобы расположить крепление датчика 41 PainTrace в разных местоположениях на теле для получения приемлемых показаний. Замена крепления датчика 41 PainTrace делается очень легко, вытаскивая соединитель 53 и удаляя его из приемника 55, как изображено на Фиг. 6F, а затем заменяя крепление датчика 41 другим креплением датчика 41. Жесткий рычаг 51 и гибкое проводящее адгезивное основание 47 выравнивают и удерживают датчик 43 на коже, поэтому требуется минимальное время для замены датчика 43 PainTrace и начала приема данных датчика PainTrace 72.
Приложение PainTrace 70 может дополнительно получать импедансные и другие результаты измерения, применять алгоритмы калибровки для определения смещения напряжения левого и правого датчиков PainTrace 43, и корректировать результаты измерения напряжения, и на основе этих вычисленных значений и параметров допуска неисправный датчик PainTrace 43 может быть идентифицирован и заменен. Размер, форма и площадь поверхности датчиков PainTrace могут определяться типом пациента и на какой части тела прикреплен датчик. Датчик PainTrace 59 может быть прикреплен к опорной части 61 и прикреплен к волосам животного, как изображено на Фиг. 6D. Измерение активности матрицы боли и центральной нервной системы, связанной с болью у животного, является уникальным применением устройства PainTrace 14, когда для животного, у которого нет способности общаться, или для человека, который не может общаться, устройство 14 обеспечивает жизненно важную информацию о том, насколько пациент, который является недееспособным или некоммуникативным, может страдать от боли и неэффективности лечения. В дополнительных вариантах реализации изобретения датчики 41 PainTrace могут быть прикреплены к воротнику 65, который может быть расположен в местоположении вблизи области тела, испытывающей боль, или надет или обернут вокруг шеи для того, чтобы не препятствовать мобильности пациента, но обеспечивать постоянный мониторинг показаний датчика пациента PainTrace 72. Воротник для мониторинга 65, который изображен на Фиг. 6Е или другое пригодное для ношения устройство может дополнительно обеспечивать дополнительные датчики 63, которые должны быть прикреплены к воротнику и собирать данные, такие как частота сердечных сокращений и вариабельность частоты сердечных сокращений, фотоплетизмограмма (ФПГ), артериальное давление, температура кожи, движение, КГР и другие показатели жизненно важных функций.
В других вариантах реализации изобретения датчик PainTrace и устройство PainTrace могут быть единственным устройством измерения PainTrace 303 в небольшом корпусе без кронштейна 61 или воротника 65, и могут просто прикрепляться к пациенту с использованием клея, как изображено на Фиг. 6Е. В некоторых вариантах реализации изобретения отдельное устройство измерения PainTrace 303 будет прикреплено к левой и правой стороне тела пациента, однако в предпочтительных вариантах реализации изобретения устройство с адгезивным датчиком PainTrace 305 будет передавать сигналы данных 72 с использованием проводного соединения или беспроводного передатчика 306, такого как Bluetooth для связи с устройством измерения PainTrace 303. Устройство с адгезивным датчиком PainTrace 305 и устройство измерения PainTrace 303 могут иметь держатель датчика 308 для введения или защелкивания в датчиках 310 внутри корпуса 312. Устройство измерения PainTrace 303 с использованием приложения PainTrace 70 может обрабатывать сигналы данных от устройства с адгезивным датчиком PainTrace 305 и от датчика 310 на устройстве измерения PainTrace 303 для калибровки сигнала и определения разницы сигнала, который обеспечивает показание уровня боли 72. Устройство измерения PainTrace 303 может иметь экран дисплея 312, чтобы отображать данные PainTrace 72 и/или PainTracePainTrace Factor 102, и/или иметь светодиодные индикаторы, сигналы тревоги или другие индикаторы 314, которые показывают уровень боли, основанный, например, на цвете света, громкости звука или скорости, с которой звук повторяется для того, чтобы указать уровень боли по сравнению с уровнем толерантности к боли 76.
Аналогичные индикаторы 314 могут использоваться в дополнительном варианте реализации изобретения устройства измерения PainTrace 320, как изображено на Фиг. 6G и 6Н. В этом варианте реализации изобретения устройства измерения PainTrace 320 левый и правый датчики 322 с возможностью отсоединения прикрепляются к держателям 324, которые прикреплены к корпусу устройства 326. Затем устройство измерения PainTrace 320 прикрепляется вдоль центральной линии С тела с левым и правым датчиками 322, которые прикреплены с использованием слабого адгезива к левой и правой части тела, соответственно. Устройство измерения PainTrace 320 с использованием приложения PainTrace 70 системы PMD 10 обрабатывает сигналы данных от левого и правого датчиков 322 для калибровки сигнала и определения разницы сигнала, который обеспечивает показание уровня боли 72. Устройство измерения PainTrace 303 может иметь экран дисплея 312 для того, чтобы отображать данные PainTrace 72 и/или PainTracePainTrace Factor 102, и/или иметь светодиодные индикаторы, сигналы тревоги или другие индикаторы 314, чтобы показать уровень боли. Как в этом, так и в других вариантах реализации изобретения устройства измерения PainTrace 320, данные PainTrace 72 могут затем передаваться с использованием проводного соединения или с использованием беспроводного передатчика 306, такого как передатчик Bluetooth, на беспроводной приемник, такой как смартфон, который также может иметь приложение PainTrace 70 и/или другие компоненты и функции системы PMD 10, доступные в качестве программного приложения на смартфоне или мобильном устройстве. Смартфон может затем передавать собранные данные из среды сбора и обработки данных 1 в локальную или удаленную сеть 12, например, в клиническую или больничную среду и/или в серверную систему BioTraceIT 18 системы PMD. Собранные данные могут быть интегрированы с ранее собранными данными датчика PainTrace для обзора с использованием компонентов и функций прикладного программного обеспечения BioTrace системы PMD 10, где могут быть предусмотрены настройки толерантности для выдачи предупреждений, если любые показания датчиков находятся за пределами допустимых уровней. Любые предупреждения, которые приводят к действиям, которые могут быть предприняты для правильного размещения датчиков или устройства, могут отображаться либо через ГПИ, либо через приложения для мобильных устройств или программное обеспечение, интегрированное с постами медицинских сестер или сетями системы здравоохранения. Датчики PainTrace также могут быть интегрированы с другими медицинскими устройствами и оборудованием, такими как монитор артериального давления, как изображено на Фиг. 6I, где первый датчик PainTrace 330, например, предназначенный для левой стороны тела, может удерживаться на коже одного плеча манжетой и пневмокамерой 332 а вторая манжета 334 или полоса, как изображено на Фиг. 6J, может быть предусмотрена для удерживания второго датчика PainTrace 330, который удерживается на коже на другой стороне тела, путем аналогичного обертывания манжеты 334 вокруг другого плеча. Две манжеты 332 и 334 могут быть соединены вместе по проводной связи или могут использовать Bluetooth или другой беспроводной передатчик для считывания показаний датчика от датчика 330 на второй манжете, переданных в устройство PainTrace 336, которое может быть интегрировано с аналоговым или цифровым измерительным устройством монитора артериального давления. Держатель 338 может быть прикреплен к каждой манжете 332, 334 для того, чтобы обеспечить введение или защелкивание датчика 330 в требуемом месте для фиксации к каждой манжете 332, 334, а также либо мокрые, либо сухие датчики могут использоваться с затягиванием манжеты 332, 334, обеспечивающей достаточное натяжение для того, чтобы удерживать датчики 330 вплотную к коже. Сигнал данных PainTrace 72 от датчиков PainTrace могут быть переданы на консоль 336 цифрового дисплея монитора артериального давления, в котором приложение PainTrace 70 системы PMD 10 установлено для калибровки двух измерений датчика и определения разницы сигнала для отображения показаний уровня боли 72 и/или значений PainTracePainTrace Factor 102 для записи с показанием артериального давления. В других вариантах реализации изобретения данные PainTrace 72 могут собираться в разное время, когда показание собирается от правой стороны пациента и сохраняется, а второй результат измерения берется от левой стороны пациента, а затем калибруется с первым результатом измерения, принятым для определения разницы сигнала и отображения показания уровня боли 72 и/или данных PainTracePainTrace Factor 102.
В других вариантах реализации изобретения устройство измерения PainTrace 67 можно носить в качестве монитора активности, например, на браслете 69, как изображено на Фиг.7А и 7В, вместе с устройством датчика PainTrace 307, которое, как описано в данном документе, соединено с устройством измерения PainTrace 67 с использованием проводного соединения или беспроводного передатчика, такого как передатчик Bluetooth. Браслет 69 может регулироваться для регулировки натяжения датчика и/или быть эластичным для того, чтобы надежно удерживать датчик в требуемом месте, при этом в некоторых вариантах реализации изобретения могут быть добавлены в браслет 69 устройства для измерения деформации для измерения натяжения, причем эти результаты измерений используются в калибровке данных сигнала PainTrace. Интерфейс управления 71 устройства измерения PainTrace 67 может иметь экран дисплея 73, который может быть сенсорным экраном, ЖК-дисплеем, LED-дисплеем или дисплеем другого типа. Интерфейс управления 71 может также иметь одну или более кнопок управления 75 вокруг дисплея или внутри дисплея, как определено типом дисплея. Кнопки управления 75 могут включать и выключать питание устройства, запускать и останавливать сбор данных, калибровать устройство, обеспечивать прокрутку для просмотра собранных данных, запускать диагностические тесты, отправлять предупреждения и выполнять другие функции. Дисплей 73 может отображать собранные данные сигнала 77, отображать PainTracePainTrace Factor 102, и отображать другие компоненты и функции прикладного программного обеспечения BioTrace системы PMD 10. Например, кнопки управления 75 и/или экран дисплея 73 могут обеспечивать ввод данных, таких как физические упражнения, активность и другую информацию в компоненте LifeTraceIT системы PMD 10. Устройство датчика PainTrace 307 может иметь браслет 309 и электрические компоненты 311 для сбора и передачи данных. В одном варианте реализации изобретения опорная часть 313 может обеспечивать прикрепление электрических компонентов 311 и обеспечивать прикрепление влажного или сухого датчика 315 к опорной части 313 с использованием клея 317. В других вариантах реализации изобретения опорная часть 313 и датчик 315 могут иметь блокирующий разъем, как описано в данном документе, для обеспечения замены датчика 315 при использовании устройства датчика PainTrace 307 в течение длительных периодов времени. В некоторых вариантах реализации изобретения датчик 315, опорная часть 313 и браслет 309 могут быть одноразовыми.
Корпус 79 устройства измерения PainTrace 67 фиксирует интерфейс управления 71 таким образом, что он является легко доступным по всему запястью пользователя. Корпус 79 также фиксирует датчик PainTrace 81 в некоторых вариантах реализации изобретения. Корпус 79 является легким и имеет минимальную толщину, как схематично изображено на виде сбоку в вертикальной проекции на Фиг. 8А. Корпус 79 может дополнительно быть моделированным для комфорта и иметь по существу прямоугольную форму, для ношения поперек запястья для того, чтобы обеспечить большую площадь контактной поверхности 83 датчика и групп датчиков, как изображено на Фиг. 8В. В некоторых вариантах реализации изобретения датчик 81 может представлять собой влажный датчик, для которого требуется, чтобы проводящий гель или адгезив 317 наносились на датчик или на кожу во время использования. Например, устройство измерения PainTrace 67 и устройство датчика PainTrace 307 с влажными датчиками могут использоваться как часть медицинского оборудования, в котором поставщик медицинских услуг (НСР) может подготовить датчики с проводящим гелем или использовать датчик, на который был предварительно нанесен гель изготовителем, и может разместить устройство измерения PainTrace 67 и устройство датчика PainTrace 307 на каждом из запястий пациента, ладонях или областях соответствующей анатомии на противоположных сторонах. После пребывания в положении сидя в спокойном состоянии в течение нескольких секунд, данные об уровне боли и данные 72 об активности матрицы боли и центральной нервной системы, а также данные PainTracePainTrace Factor 102 пациента могут быть собраны вместе с другими факторами BioTrace Factors, собранными от других датчиков, которые будут использоваться в качестве исходного уровня при измерении боли вместе с другими биофизическими показаниями пациента.
Датчики PainTrace 81 и 315 могут дополнительно быть заменяемыми, при этом влажные датчики могут быть одноразовыми и использоваться, например, всего за два часа, в то время как сухие датчики могут использоваться в течение более длительного периода времени для непрерывного сбора данных. Например, сухие датчики могут заменяться ежедневно или каждые два-три дня, или после более длительного периода времени. Как схематично изображено на Фиг. 9А, датчик PainTrace 81 также может иметь минимальную толщину и может быть предусмотрена соединительная опорная часть 87 для соединения датчика PainTrace 81 с корпусом 79 с возможностью последующего отсоединения. В одном варианте реализации изобретения корпус 79 содержит печатные платы 89 и другую электронику для интерфейса управления 71 и датчика PainTrace 81, как изображено на виде снизу устройства измерения PainTrace 67 на Фиг. 9В. Соединительная опорная часть 87 может иметь левый и правый опорные кронштейны 91 и 93, которые могут быть установлены на основании 95 в центре корпуса 79. Каждый из левого и правого опорных кронштейнов 91 и 93 могут содержать пружину сжатия 97, и каждая пружина сжатия 97 может иметь тензиометрический датчик 99 для измерения давления датчика PainTrace 81 на кожу пользователя для определения равного давления между двумя измерительными устройствами PainTrace 67, которые носятся на каждом запястье пользователя во время сбора данных при измерении боли и других биофизических показаний, таких как проводимость кожи. Соединительная опорная часть 87 может также содержать центровочный штифт 101 для выравнивания разъема датчика 103 внутри соединительной опорной части 87.
Разъем датчика 103, как изображено на виде снизу датчика PainTrace 81 на Фиг. 9С, расположен в центре датчика PainTrace 81 Разъем датчика 103 может иметь пластинчатый держатель 105, который проходит от отверстия 107 в центре разъема датчика 103 параллельно более длинной по размеру контактной поверхности 83. Пластинчатый держатель 105 прикреплен к пальцу 109, который проходит к пластине 111 с пальцем 109, создавая расстояние смещения между пластинчатым держателем 105 и пластиной 111. Пластина 111 может быть прикреплена к нижней части 113 контактной поверхности 83 датчика PainTrace 81 с использованием клея или другого устройства для крепления. Как изображено на Фиг. 10А, нижняя поверхность 111 может иметь проводящие полосы 115 или другие электрические точки соединения для соединения с пружинами сжатия 97 в качестве электрических контактов или с другими электрическими контактами от соединительной опорной части 87.
Как изображено на Фиг. 10В, датчик PainTrace 81 соединен с корпусом 79 с использованием каждого конца 117 пластинчатого держателя 105 и левой и правой соединительных опорных частей 91 и 93. Соединительные опорные части 91 и 93 выполнены с вертикальным выступом 119 и нависающим выступом 121, как изображено на Фиг. 10С, при этом нависающий выступ 121 левой соединительной опорной части 91 направлен к нависающему выступу 121 правой соединительной опорной части 93. Соединительные опорные части 91 и 93 расположены на расстоянии друг от друга, которое является немного большим, чем ширина пластинчатого держателя 105 разъема датчика 103, в результате чего пластинчатый держатель 105 может быть вставлен между двумя соединительными опорными частями 91 и 93. Отверстие 107 на пластинчатом держателе 105 совмещается с центровочным штифтом 101 на основании 95 соединительной опорной части 87 и обеспечивает поворот датчика PainTrace 81 для того, чтобы концы 123 пластинчатого держателя 105 находились под нависающими выступами 121 соединительных опорных частей 91 и 93 для прикрепления датчика PainTrace 81 к корпусу 79. Пружина сжатия 97 каждой из соединительных опорных частей 91 и 93 прижимается к датчику PainTrace 81 для того, чтобы прижать датчик вплотную к коже для увеличения контакта области контактной поверхности 83 датчика PainTrace 81 с целью улучшения показаний датчика. Пружины сжатия 97 могут также соединяться с проводящими полосами 115 на нижней поверхности 111 датчика PainTrace 81 для отправки данных сигнала 77 от датчика PainTrace 81 к электронике устройства измерения PainTrace 67. Устройство измерения PainTrace 67 может отображать данные сигнала 77 в дисплее 73 интерфейса управления 71 и/или передавать данные с использованием модуля связи 25 в приложении PainTrace 70 системы PMD 10, который может быть установлен на устройстве измерения PainTrace 67 или удаленно установлен на смартфоне или другом локальном цифровом устройстве, удаленно в сети 12, например, в клинической или больничной среде, и/или передавать на серверную систему BioTraceIT 18 системы PMD.
Как изображено на Фиг. 11А, в первом положении перед соединением разъем датчика 103 датчика PainTrace 81 располагается параллельно соединительным опорным частям 91 и 93 между ними. Затем датчик PainTrace 81 поворачивается, как изображено на Фиг. 11В, для того, чтобы установить датчик PainTrace 81 перпендикулярно соединительным опорным частям 91 и 93 разъема и прижать нижнюю часть 113 контактной поверхности датчика 83 к пружинам сжатия 97. В качестве альтернативы датчик PainTrace 81 может быть введен в требуемое место в вариантах реализации изобретения разъема без центровочного штифта 101. Пружины сжатия 97 работают на растяжение, выдвигая наружу к датчику PainTrace 81 пластинчатый держатель 105 под нависающий выступ 121 соединительных опорных частей 91 и 93, прикрепляя датчик PainTrace 81 к корпусу 79. Гребень или другой выступ 123 могут быть предусмотрены на разъеме датчика 103 для блокировки датчика PainTrace 81 сообразно с углублением 125 на каждой из соединительных опорных частей 91 и 93. Как изображено на Фиг. 12А, датчик PainTrace 81 до подсоединения может выступать за пределы краев 127 корпуса 79 для того, чтобы обеспечить пользователю возможность легко манипулировать датчиком PainTrace 81 для поворота и подсоединения датчика 81. Края 127 корпуса 79 могут образовывать ободок 129 для того, чтобы посадить и установить датчик PainTrace 81 на корпусе 79. Датчик PainTrace 81 может иметь толщину немного большую, чем ободок 129 корпуса для того, чтобы обеспечить пользователю захват краев 131 для поворота и удаления датчика 81 или, альтернативно, пользователь может просто нажать на середину датчика PainTrace для того, чтобы сжать пружины 97 и отделить выступы 123 от углублений 125, и повернуть датчик для того, чтобы расположить пластинчатый держатель 105 между двумя соединительными опорными частями 91 и 93 разъема, и снять датчик PainTrace 81 с корпуса 79, и/или повернуть устройство измерения PainTrace 67 для того, чтобы датчик PainTrace 81 отсоединился и выпал из корпуса 79. Другие варианты реализации изобретения могут предусматривать, чтобы датчик PainTrace 81 и 315 защелкнулся при использовании крепежных элементов и/или запирающих язычков, которые могут иметь выступы или кнопки, которые могут быть сжаты для того, чтобы освободить датчик от язычков, фиксирующих датчики к корпусу 79. Другие варианты реализации изобретения для подключения датчиков к корпусу, браслету, воротнику, опорной части, или носимое, или другое фиксирующее приспособление для прикрепления к коже, рассматриваются в рамках данного изобретения, которое также может включать в себя средства для фиксации и прижатия датчика к коже для поддержания проводимости.
В устройстве измерения PainTrace 67 требуется измерение от каждой стороны пациента с калибровкой между датчиками PainTrace 81 или устройством датчика PainTrace 307 для минимизации шума сигнала и ограничения ошибочных показаний. Тензиометрический датчик 99 на каждой из пружин сжатия 97 или тензиометрические датчики, которые электрически соединены с другими вариантами реализации изобретения устройства PainTrace, могут обеспечивать прижатие датчика PainTrace 81 и 315 к коже для проведения измерений. Результаты измерений тензодатчиков в зависимости от размещения тензодатчика в устройстве измерения PainTrace 67, устройстве датчика PainTrace 307, браслете 697 или 309, воротнике 65 или другим носимом элементе, может обеспечить маркер для обеспечения равного давления и прижатия датчиков 81 и 315 к коже. Как описано в данном документе, измерения боли с использованием устройства PainTrace 14 являются пассивными измерениями потенциала кожи, в отличие от гальванической реакции кожи, которая применяет ток. Измерения устройством PainTrace 14 проводятся без приложения напряжения к коже, а вместо этого измеряют электрическую активность ответа матрицы боли на раздражители посредством обнаружения разности напряжения или силы тока между первым датчиком PainTrace, расположенным в местоположении на левой стороне тела, и вторым датчиком PainTrace, расположенным в аналогичном местоположении на правой стороне тела. В некоторых вариантах реализации изобретения устройство PainTrace 14 может содержать источник питания для приложения напряжения к датчикам PainTrace или связанным с ним ипсилатеральным парам датчиков, прикрепленных к устройству, для измерения импеданса и проводимости, и/или других пассивных измерений, которые также могут быть приняты перед, во время или после получения данных измерения боли и активности матрицы боли, или с периодическими интервалами при сборе данных измерения боли и активности матрицы боли для калибровки показаний для каждого датчика PainTrace 81 или группы датчиков на основе различий в контакте с кожей, свойствах кожи и воздействиях движения на датчик в зоне контакта с кожей, и дополнительных физиологических измерений. В силу того, что устройство PainTrace не прикладывает к коже напряжение, данные измерения боли и активности матрицы боли могут непрерывно собираться без каких-либо неблагоприятных воздействий на пациента, и калибровочные измерения могут периодически выполняться между сбором данных для определения требуемых смещений и калибровки устройства PainTrace. Калибровочные измерения могут дополнительно определять отказ датчика и предоставлять пользователю обозначение, что датчики PainTrace 81 и 315 должны быть заменены.
Как описано в данном документе, использование контралатеральных датчиков, которые расположены в аналогичных местоположениях на левой и правой сторонах тела, обеспечивает измерения электрической активности благодаря передачам передачи нервного импульса, которые могут осуществляться как в мозг, так и из него при реакции на местоположение боли внутри тела. Контралатеральные измерения разностей напряжений от устройства PainTrace 14 хорошо коррелируют с оценками боли, которые может предложить пациент, например, при сравнении измерений с оценками в визуальной аналоговой шкале (ВАШ). В некоторых вариантах реализации изобретения устройство PainTrace 14 может комбинировать контралатеральные датчики с ипсилатеральными датчиками на одной или обеих сторонах тела для того, чтобы обеспечить дополнительную информацию об электрической активности внутри тела. Ипсилатеральные датчики могут получать измерения пассивно или активно, например, для получения кожно-гальванической реакции (КГР) в местоположениях, сходных с контралатеральными датчиками. Данные из ипсилатеральных измерений могут использоваться для калибровки и улучшения соотношения сигнал/шум контралатеральных показаний результатов измерения боли. Данные от ипсилатеральных датчиков могут быть дополнительно скоррелированы с контралатеральными показаниями для проверки показаний измерений боли, когда последние исследования показали, что повышенная электрическая активность на одной стороне тела может быть связана с болью, стрессом и беспокойством.
В одном варианте реализации изобретения система PMD содержит один или более датчиков PainTrace и/или один или более других биофизических датчиков, которые могут быть расположены в корпусе 350 для установки и удаления из устройства PainTrace, носимого или другого измерительного устройства для того, чтобы иметь группу датчиков, которые должны быть размещены на теле в одинаковых левых и правых местоположениях. В одном варианте реализации изобретения группа датчиков может содержать один контралатеральный датчик 352 и пару ипсилатеральных датчиков 354. В других вариантах реализации изобретения каждый из контралатеральных датчиков и ипсилатеральных датчиков может располагаться в отдельных корпусах и отдельно размещаться в местоположениях на теле. Например, контралатеральный датчик может быть помещен по отдельности на левую и правую ключицу, а два ипсилатеральных датчика, в виде пары могут быть установлены на ладонь каждой руки или в других местоположениях, которые расположены вдоль левой или правой оси тела.
В варианте реализации изобретения группы датчиков, как изображено на Фиг. 13, корпус 350, удерживающий датчики, может быть изготовлен из гибкого материала с целью сгибания или незначительного изгибания для адаптации к перемещению и позиционированию кожи. Кромка 356, которая может быть подготовлена с помощью проводящего геля или которая имеет предварительно нанесенный гель, окружает поверхность 358 датчика корпуса 350 для того, чтобы прикрепить с возможностью отсоединения группу датчиков к коже. Группы датчиков, имеющие как ипсилатеральные датчики, так и контралатеральные датчики, могут размещаться в одинаковых местоположениях на левой и правой стороне тела. Ипсилатеральные датчики 354 подключаются через нагрузочный резистор 360 от 0,5 до 900 кОм, а предпочтительно 22 кОм. Контралатеральные датчики 352 также соединяются через нагрузочный резистор 362 посредством электрического соединения левой и правой групп датчиков. При соединении контралатеральных датчиков 352 провод 364 может иметь любую длину с электрическим разъемом 366, который может быть выполнен в виде зажима, защелки, двухконтактной застежки или разъема другого типа. Провод 364 может проходить от каждой группы датчиков для подключения после того, как группы датчиков были размещены в местоположении на теле, таком как область возвышения мизинца или возвышения большого пальца ладони каждой руки. Для того, чтобы закрыть схему между контралатеральными датчиками 352, разъемы 366 от левого и правого датчиков могут просто соединяться вместе.
Тем не менее, в некоторых случаях наличие провода, проходящего по всему телу, может быть неудобным или непривычным для пациента. Разъемы 364 могут быть, по этой причине, в некоторых вариантах реализации изобретения прикреплены к предмету одежды, перилам кровати или другому объекту, который электрически соединяет два провода датчика, для того, чтобы закрыть контур контралатерального датчика и по-прежнему обеспечивать мобильность пациента и использование рук. В некоторых вариантах реализации изобретения провод может иметь разъем типа USB, который должен быть вставлен в носимый элемент, размещаемый вокруг запястья или шеи пациента. Носимый элемент может быть выполнен в виде беспроводного трекера физической активности и может содержать схему, изображенную на Фиг. 13 для сбора и передачи данных от групп датчиков. В качестве альтернативы схема содержится в отдельном портативном устройстве PainTrace 14, которое может содержать беспроводную передачу или линию вывода данных в виде USB-кабеля для передачи и загрузки данных результатов измерения боли, собранных из групп датчиков PainTrace. В других вариантах реализации изобретения схема может быть включена в каждый датчик или группу датчиков.
В некоторых вариантах реализации изобретения устройство PainTrace 14 системы PMD может не иметь контралатеральных датчиков, соединенных с проводом по телу, но вместо этого иметь две пары ипсилатеральных датчиков, каждая из которых помещена контралатерально по отношению к другой. Пассивные и активные измерения могут быть выполнены каждой парой ипсилатеральных датчиков отдельно и/или одновременно, а сигналы от этих показаний объединены для определения активности матрицы боли и других биофизических измерений. Ипсилатеральные пары датчиков, которые размещены в аналогичных местоположениях тела, могут быть размещены на запястьях, где в некоторых вариантах реализации изобретения устройство PainTrace 14 может быть включено в монитор активности, и первый монитор активности помещен на запястье левой руки, а второй монитор активности помещен на запястье правой руки для получения результатов измерений боли.
В вариантах реализации изобретения схемы датчика PainTrace системы PMD схема, как показано, может включать обработку сигналов 370 и схему полосового фильтра 372 для улучшения соотношения сигнал/шум и качества сигнала. Микропроцессор 374 и таймер 376 предназначены для управления сбором, частотой дискретизации и передачей сигнала, а аналого-цифровой преобразователь 378 для преобразования измеренных ЭДА или другиханалоговых сигналов в цифровые сигналы. Программные приложения, программы управления и алгоритмы калибровки, такие как итеративная калибровка линейного сопротивления, могут быть загружены или переданы в схему с использованием схемы беспроводной связи 380 или проводного соединения, и сохранены и доступны из хранилища 382 данных и запоминающего устройства 384 внутри схемы. Схема может включать в себя выходной дисплей 386, или же данные могут отображаться на устройстве вывода, удаленном от схемы, за счет использования проводной или беспроводной передачи данных.
Использование обоих ипсилатеральных датчиков 354 и контралатеральных датчиков 352 предусматривает компаратор сигналов 388 для того, чтобы оценивать характеристики сигнала, включая напряжение, ток, частоту, линейность и амплитуду, и использовать эти результаты измерения для калибровки и регулировки напряжения или силы тока одного из сигналов левого ипсилатерального датчика, сигнала правого ипсилатерального датчика и/или сигнала контралатерального датчика, как это предписано сравнением сигналов. Как изображено на Фиг. 13, выводные провода от нагрузочного резистора 360 соединены с усилителем, где в варианте реализации изобретения указанной схемы первый усилитель обозначен как AMP 1 с идентификатором 390 для левых ипсилатеральных датчиков 354, второй усилитель обозначен как AMP 2 с идентификатором 392 для правых ипсилатеральных датчиков 354, и третий усилитель AMP 3 с идентификатором 394 соединен с выводными проводами нагрузочного резистора 362 для контралатеральных датчиков 352. Нагрузочные резисторы каждого датчика или группы датчиков в некоторых вариантах реализации изобретения могут представлять собой переменные резисторы для того, чтобы калибровать схему и регулировать напряжение и силу тока. Например, при калибровке контралатерального сигнала может использоваться переменный нагрузочный резистор 362, и может быть выполнено сравнение контралатерального сигнала с сигналом, измеренным либо от одного, или же от обоих, как от левого, так и от правого ипсилатеральных датчиков. На основании характеристик сигналов, определяемых компаратором 388 сигналов, переменный нагрузочный резистор 362, как показано в этом примере, может регулироваться для усиления компонентов сигнала и/или удаления выбросов, которые могут быть связаны с перемещением или другими помехами сигнала. Полосовой фильтр может дополнительно регулироваться по мере необходимости в одном или нескольких оптимальных диапазонах частот для устранения шума сигнала. Схема датчика PainTrace системы PMD может дополнительно включать в себя источник питания, такой как аккумулятор 368, для подачи напряжения через нагрузочные резисторы. Например, этапы калибровки могут включать в себя применение напряжения через нагрузочный резистор 362 контралатеральных датчиков 352 и/или нагрузочные резисторы 360 каждой из пар ипсилатеральных датчиков 354 для проверки электрического соединения и/или для определения проводимости кожи. Используя измерение проводимости кожи от каждого датчика, можно идентифицировать различия в контакте кожи, свойствах кожи, движении и других воздействиях датчика на поверхность контакта с кожей и физиологических измерениях. Большие различия в этих измеренных значениях могут указывать на неисправность датчика или ограниченный контакт поверхности датчика с кожей. Для меньших различий в импедансе в пределах указанных уровней толерантности, приложение PainTrace 70 системы PMD 10 может применять алгоритмы калибровки для добавления или вычитания смещения на основе разности импеданса для нормализации результатов измерений напряжения между левым и правым контралатеральными датчиками или парой ипсилатеральных датчиков.
При использовании устройства PainTrace системы PMD данные собираются без приложения напряжения к коже для измерения активности матрицы боли пациента. Тем не менее, применяя напряжение к ипсилатеральным датчикам, расположенным на либо на левой, или на правой стороне тела, можно измерить кожно-гальваническую реакцию КГР. Система PMD уникально объединяет и нормализует биофизические измерения, такие как КГР, вариабельность ритма сердца (ВРС), кровяное давление, пульс, движение, температуру кожи и другие данные сигнала с данными активности матрицы боли, собранными с использованием устройства PainTrace 14. В результате анализа системой PMD, результаты измерения активности матрицы боли могут быть скоррелированы по шкале времени для оценки пиковой активности КГР, которая может быть связана с эмоциональным откликом и точками повышенного уровня боли. Как изображено на Фиг. 14, при одновременных измерениях КГР с использованием ипсилатеральных датчиков, расположенных на пальцах правой руки для измерения, и активности матрицы боли с использованием устройства PainTrace 14 с использованием контралатеральных датчиков, помещенных в область возвышения большого пальца ладони каждой руки, активность матрицы боли измеряется в течение некоторого времени. В течение части этого периода проводился холодовый прессорный тест, который представляет собой стандартный способ для вызывания экспериментальной боли (Walsh др. Normative Model for Cold Pressor Test. American Journal of Physical Medicine and Rehabilitation. Февраль 1989 г.; 68 (1): 6-11). Использование приложения PainTrace 70 системы PMD 10 и регулирование временного блока 78 до данных часов и минут, собранных в течение непрерывного периода времени, может быть согласовано. Система PMD коррелирует измерения показаний КГР 395 и данные PainTrace 396, и отображает точки стимуляции боли через 25 минут 398 и через 32 минуты 399. Данные PainTracePainTrace Factor 102 или другие данные BioTrace Factors 150 могут быть добавлены к точкам за определенный период времени для получения дополнительной информации Например, дополнение данных PainTracePainTrace Factor 102 может быть выполнено путем перетаскивания значка PainTracePainTrace Factor 102 внутрь периода времени. В качестве альтернативы, возможность добавления данных PainTracePainTrace Factor 102 и других данных BioTrace Factors 150 через меню или другой интерфейс приложения может быть предоставлена для отображения, например, отображения данных PainTracePainTrace Factor 102 в максимальных точках отклонения, как показано стрелками пунктирной линии на дисплее. Другие биофизические показатели, такие как вариабельность сердечного ритма, могут быть индивидуально отображены для получения путем простого перетаскивания значка ВСР 302 в период времени.
Система PMD 10 обеспечивает обзор интегрированных данных или индивидуальное отображение КГР и активности матрицы боли, которые в этом примере демонстрируют обратную связь до применения болевого раздражителя. В течение этого периода времени одновременные показания были получены при включении и выключении устройства КГР с двухминутными интервалами для определения того, как применение тока воздействовало на устройство измерения PainTrace 14. Цикл КГР проводился до 25-минутной временной точки в эксперименте, когда применялся болевой раздражитель 398 после того момента времени, когда использовалось последовательное измерение КГР. Отклонения в данных PainTrace 396 уменьшались в тех случаях, когда устройство КГР работало циклами в течение более длительных периодов с увеличением циклической частоты от двух минут до трех минут. Начиная с временной точки на 25 минуте, инициируется холодовый прессорный тест, который заключается в погружении правой ноги в ледяную баню в течение 1,5 минут, что демонстрирует отрицательное отклонение сигнала матрицы боли через 26,5 минут с последующим восстановительным периодом до состояния, в котором отсутствует боль через 32 минуты, когда холодовый прессорный тест был повторен, снова демонстрируя отрицательное отклонение сигнала, обозначающее состояние боли, за которым следует восстановительный период до 41 минуты. На дисплее системы PMD корреляция активности КГР с активностью матрицы боли показывает, что во время применения болевых раздражителей сигналы КГР и матрицы боли не являются синхронными, но демонстрируют прямую связь в отличие от первоначальной обратной зависимости до применения болевого раздражителя. При использовании системы PMD 10 контралатеральные и ипсилатеральные данные датчика используются для калибровки и дальнейшего распознавания активности матрицы боли, что позволяет лучше понимать дифференциацию между различными факторами для индивидуального ощущения боли.
При использовании системы PMD 10 анализ, корреляция и преобразование данных из множества результатов биофизических измерений обеспечивает возможность для лучшего понимания активности в болевом матриксе мозга и восприимчивости пациента, а также ощущения боли. Разница в реакции, подтвержденная одновременными измерениями КГР и PainTrace, создает дополнительную информацию, относящуюся к вариабельности среди данных активности области мозга в болевом матриксе, ответа симпатической нервной системы и эмоциональной подготовки, которые являются компонентами, связанными с индивидуальным ощущением боли. Аналогичным образом система PMD 10 обеспечивает одновременное измерение и коррелирование вариабельности сердечного ритма для определения уровней активности парасимпатической нервной системы и зависимости тонуса блуждающего нерва (Farmer А и др., Psychophysiological responses to pain identify reproducible human clusters. Pain. Ноябрь 2013 г.; 154 (11): 2266-2276). Было доказано, что тонус блуждающего нерва связан с эндогенным высвобождением эндорфина в ответ на наличие боли, и поэтому измерение активности парасимпатической нервной системы и связанного с ней тонуса блуждающего нерва являются важными факторами преобразования физических биосигналов в количественные и объективные показатели уровней активности матрицы боли и центральной нервной системы, которые отражают как состояния боли, так и состояния здоровья, а также для использования в качестве инструмента диагностики и выявления основных: источников медицинского компромисса (Kollarik М и др. Vagal afferent nerves with the properties of nociceptors. Auton Neurosci. 16 февраля 2010 г.; 153(1-2): 12. Опубликовано в Интернете 13 сентября 2009 г. doi: 10.1016/j.autneu.2009.08.001). В дополнение к диагностике боли, устройства PainTrace 14 системы PMD 10 обеспечивают раннюю диагностику желудочно-кишечного расстройства, аллергии и респираторной инфекции, спортивной травмы, связанной с повреждением сухожилий и связок, а также диагностику хронической боли, связанной с травмой спины, случаями зубной боли и мигрени, наряду с некоторыми другими.
В дополнительных вариантах реализации изобретения датчики или группы датчиков могут быть пришиты или съемно прикреплены к предметам одежды или ткани с использованием гибкого держателя датчика, упомянутого в данном документе как гарнитура с датчиками 400 системы PMD. Гарнитура с датчиками 400 системы PMD представляет собой гибкое устройство для крепления датчика, которое содержит удлиненную полосу 402 из пластика, металла или другого материала, которая может быть сформирована с U-образным каналом, направляющей с двутавровым профилем, Т-образной направляющей, или в некоторых вариантах реализации изобретения представляет собой сплющенную деталь с отверстиями для крепления серии датчиков или группы датчиков, или сопрягаемый контурный канал. Как изображено на Фиг. 15А, гарнитура с датчиками 400 системы PMD может содержать электронную схему, которая может находиться внутри корпуса 404 или обеспечивать электрический выходной порт 401, такой как USB в мини- или микроразмерном исполнении для присоединения гарнитуры с датчиками 400 Система PMD к внешним электронным схемам. В других вариантах реализации изобретения система PMD является доступной удаленно через схему беспроводной связи Bluetooth, NFC или других типов протоколов беспроводной связи в корпусе 404. Система PMD обеспечивает сбор данных, управление и связь с прикрепленными электродами и датчиками гарнитуры с датчиками 400 системы PMD. Схема системы PMD также обеспечивает инициализацию для обнаружения в тех случаях, когда датчики добавляются или удаляются из датчика 400 системы PMD, и связывает электроды и датчики Вдоль полосы 402 с конкретным пациентом, поставщиком медицинских услуг (НСР), врачом и клинической или больничной сетью, как описано в данном документе. Гарнитура с датчиками 400 системы PMD может содержать источник питания 406 или батареи для датчиков мощности, и применять напряжения для калибровки датчиков. В некоторых вариантах реализации изобретения источник питания 406 может обеспечивать ток для электрохимического конденсатора одного или более датчиков PainTrace для улучшения энергетических, мощностных характеристик и чувствительности.
Текстильная застежка типа Velcro или крючок и полоска в виде застежки-фиксатора 408 могут быть предусмотрены непрерывно или вдоль участков верхней или нижней поверхности гарнитуры с датчиками 400 системы PMD для того, чтобы плотно присоединить полоску к предмету одежды или к ткани. Кроме того, в некоторых вариантах реализации изобретения полоска адгезива может быть предусмотрена либо непрерывно, либо частично вдоль верхней и/или нижней поверхностей полос для того, чтобы соединить гарнитуру с датчиками 400 системы PMD с кожей или волосами животного. Вдоль текстильной застежки типа Velcro и/или липкой полосы 408, или под ними, предусмотрены проводящие металлические полосы 410, которые могут быть электрически соединены со схемой системы PMD посредством прямого или удаленного беспроводного соединения. Проводящие полосы 410 также могут быть электрически соединены с коммуникационными разъемами 411, установленными в местоположениях вдоль полосы 402 гарнитуры с датчиками 400 системы PMD. Коммуникационные разъемы 411 могут быть двухконтактными или мультиконтактными, мини- или микро-USB или другими типами электрических разъемов, подходящих для удовлетворения требований к передаче и обмену данных датчиков, электродов и схем системы PMD, устройств PainTrace 14, других биофизических устройств 11 и компонентов и функций системы PMD 10. Коммуникационные разъемы 411 могут быть расположены в одном или в множестве местоположений вдоль, или в начале, или в конце гарнитуры с датчиками 400 системы PMD. Электрические разъемы 411 могут обеспечивать для гарнитуры с датчиками 400 системы PMD взаимное соединение для добавления или удаления датчиков для увеличения диагностической способности при необходимости. Как изображено на Фиг. 15В, гарнитура с датчиками 400 системы PMD может иметь ряд разъемов типа «папа» 413 и ряд разъемов типа «мама» 415, в результате чего электрический провод 417, такой как кабель микро-USB, может использоваться для подключения одной гарнитуры с датчиками 400 системы PMD к другой. В некоторых вариантах реализации изобретения, как изображено на Фиг. 15А группа датчиков 419 может быть соединена вдоль участка длины гарнитуры с датчиками 400 системы PMD. В других вариантах реализации изобретения дополнительная гарнитура с датчиками 400 системы PMD может быть электрически соединена с использованием концевой заглушки 421. Первый конец гарнитуры с датчиками 400 системы PMD может иметь концевую заглушку 421 типа «папа», а второй конец может иметь концевую заглушку 423 типа «мама» для электрического соединения ряда гарнитур с датчиками 400 системы PMD вместе по мере необходимости. Для связи и управления датчиками разных типов проводящая полоса 410 содержит ряд контрольных штифтов 425 локатора, которые обнаруживают и передают сигнал в тех случаях, когда датчик 412 прикреплен к гарнитуре с датчиками 400 системы PMD в этом конкретном местоположении, или отсоединен от нее. Встроенное программное обеспечение в схеме системы PMD идентифицирует тип датчика, требования к сбору данных и другие параметры, и предоставляет протоколы связи для установки времени и частоты дискретизации для сбора данных.
В некоторых вариантах реализации изобретения датчик 412 устанавливается на гарнитуре с датчиками 400 системы PMD путем перемещения крепежного элемента датчика 414 в U-образный канал 416 и вдоль U-образного канала, имеющего левую и правую опорные направляющие 418, как изображено на Фиг. 15В. Крепежный элемент датчика 414 может иметь плоскую верхнюю поверхность 420 и выступающие части с крылатой головкой 422 с закругленным основанием 427. Выступающие части с крылатой головкой 422 опираются на левую и правую опорные направляющие 418, а плоская верхняя поверхность 420 обеспечивает электрическое соединение с полосой проводимости 410, которое должно поддерживаться в связи с тем, что датчик 412 сжимается, когда прикрепленная одежда или ткань затягиваются и прижимаются к коже. Закругленное основание 427 обеспечивает перемещение крепежного элемента 414 внутри U-образной направляющей, когда закругленное основание 427 вдоль клиновидных, изогнутых или наклонных краев 429 желобчатых рельсов 418 катится перпендикулярно рельсам 418 и скользит вдоль рельсов 418 в связи с тем, что датчик 412 прижимается к коже. При формировании крепежного элемента датчика 414 с закругленным основанием 427 поверхность 446 датчика 412 остается в контакте с кожей, поскольку гарнитура с датчиками 400 системы PMD и/или одежда прижимается к коже, или когда пациент перемещается, несмотря на то, что прикреплена гарнитура с датчиками 400 системы PMD.
В другом варианте реализации изобретения гарнитура с датчиками 400 системы PMD может представлять собой плоскую полосу 430 с рядом частей кнопок 432 типа «мама», расположенных и закрепленных через отверстия в полосе 430, как изображено на Фиг. 15С. Датчик 434 имеет часть кнопки 436 типа «папа», которая должна быть вставлена в часть кнопки 432 типа «мама» и прикреплена к гарнитуре с датчиками 400 системы PMD. Части кнопок типа «мама» и типа «папа» могут быть выполнены из проводящего материала, и электрические полоски 410 могут быть предусмотрены для передачи и приема сигналов от датчиков 434. Текстильная застежка типа Velcro или липкая полоса 408 могут быть предусмотрены вдоль плоской крепежной полосы 402 гарнитуры с датчиками 400 системы PMD. Крепежный элемент датчика 436 может иметь закругленную форму для вращения в отверстии и предотвращает перемещение пациента или предохраняет полосу с датчиками 400 системы PMD от удаления датчика 430 в сторону от кожи. В других вариантах реализации изобретения крепежный элемент датчика может иметь частично овальную форму для скольжения по рельсам направляющей с двутавровым профилем или Т-образной направляющей, или любую форму, которая обеспечивает правильную ориентацию датчика и свободное перемещение крепежного элемента 436 внутри соединения с полосой 402 для предотвращения переворота датчика и его оттягивания от поверхности кожи во время движения. Другие крепежные элементы, а также формы и размеры направляющих предполагаются в рамках этого компонента системы PMD 10 в соответствии с данным изобретением.
Датчики 412 могут располагаться в оптимальных местоположениях вдоль гарнитуры с датчиками 400 системы PMD в соответствии с площадью поверхности на теле, подлежащей измерению, размером человека, одежды, количеством времени, в течение которого будут использоваться датчики 412, типом датчика 412 и другими факторами. Ряд датчиков различной мощности и электрических требований может быть обеспечен подачей питания от источника питания или аккумулятора 406 по мере необходимости. В некоторых вариантах реализации изобретения датчики могут быть постоянно прикреплены к гарнитуре с датчиками 400 системы PMD с использованием адгезивов, скобок, ниток, зажимов, защелок или других крепежных элементов. В некоторых вариантах реализации изобретения гарнитура с датчиками 400 системы PMD может быть одноразовой. Как изображено на Фиг. 15А, объемный гибкий материал гарнитуры с датчиками 400 системы PMD обеспечивает изгиб и формирование полосы 402 для правильного размещения датчиков или групп датчиков в надлежащем месте для получения данных об активности матрицы боли, ЭДА, ФПГ, ВСР, КГР и другой биофизической информации. Например, гарнитура с датчиками 400 системы PMD может обеспечивать разделение двух ипсилатеральных датчиков 440 вдоль каждой стороны, позиционирование контралатеральных датчиков 442 в аналогичных местоположениях и поддержку монитора ФПГ со всеми данными, собранными и проанализированными в системе PMD. Гарнитура с датчиками 400 системы PMD может быть закреплена в рубашке с использованием полосы текстильной застежки типа Velcro 408 для обертывания гарнитуры с датчиками 400 системы PMD вокруг шейки и плеч, и прикрепления датчиков вдоль ключицы и грудной клетки для получения показаний. Гибкость гарнитуры с датчиками 400 системы PMD обеспечивает возможность расположения поверхности 446 датчика 412 в соответствии с неровностями кожи или волос животного. На поверхность 446 каждого датчика 412 может быть нанесен слой адгезивного проводящего геля для прикрепления датчика к телу.
В еще одном варианте реализации изобретения гарнитура с датчиками 400 системы PMD может использоваться с компрессионной одеждой или тканью, такой как эластичная повязка, спортивная лента, узкий бюстгальтер без бретелей или другое изделие одежды для размещения гарнитуры с датчиками 400 системы PMD в местоположении вокруг руки, ноги, или туловища тела, и прижатия датчиков к поверхности волос или кожи. Таким образом, нет необходимости для нанесения гелей или клеев на кожу для фиксации и поддерживания электрической связи поверхности 466 датчика с кожей для оптимизации показаний. Ткань эластичной повязки или предмета одежды может быть затянута на теле для того, чтобы прижать датчики к коже с помощью текстильной застежки типа Velcro или других крепежных элементов. В составе системы PMD, которая объединяет данные от множества датчиков и ссылок, гарнитура с датчиками 400 системы PMD обеспечивает возможность легкого подключения и расположения множества датчиков и групп датчиков на коже для улучшения электрической связи каждого датчика и общих данных, полученных от PainTrace и других биофизических датчиков.
В других вариантах реализации изобретения дозировка обезболивающих лекарственных препаратов может быть оценена на основе индивидуальных факторов PainTrace 102 и прямого измерения устройством PainTrace 14 до и после введения обезболивающего лекарственного препарата. До и после введения PainTracePainTrace Factors 102 будет обеспечивать данные по эффективности на основе дозировки, а также путем мониторинга в динамике по времени может оценить толерантность и необходимость оценки альтернативных вмешательств для того, чтобы обеспечить индивидуальную схему лечения боли.
В других вариантах реализации изобретения пороговое значение толерантности к боли или показания от другого датчика могут использоваться для введения лекарственного средства через, например, автоматизированное дозирующее устройство насосного типа. Пределы дозировки и времени между введением лекарственного средства могут быть установлены, а затем на основании данных, собранных из устройства для измерения боли, насос может выдавать лекарственный препарат в тех случаях, когда показания датчика превышают установленный уровень толерантности. В частности, для недееспособного пациента автоматическая система доставки лекарственного препарата с использованием показаний датчика PainTrace может оказаться эффективной для контроля и поддержания уровней лекарственного средства по мере необходимости. Как показано выше, введение лекарственного препарата и уровни боли можно отслеживать и анализировать для того, чтобы определить эффективность лечения с использованием приложения PainTrace Application 70 и других компонентов и функций системы PMD 10.
В дополнительном варианте реализации данного изобретения система PMD 10 может идентифицировать пациентов с высоким риском зависимости от лекарственного средства. Данные датчика PainTrace могут быть использованы уникальным образом для предотвращения злоупотребления лекарственным средством путем, контролирования тех случаев, когда пациент имеет доступ к своему лекарственному препарату, исходя из собранных показаний активности матрицы боли и толерантности к боли. В первом варианте реализации изобретения контейнер для таблеток с защищенным доступом или другой дозатор лекарственного средства могут быть заблокированы с использованием электронного защитного кода. Пациенту может быть присвоен идентификационный код для того, чтобы разблокировать контейнер для таблеток, тем не менее, этот код безопасности может быть переопределен при помощи показаний датчика PainTrace в тех случаях, когда показания датчика являются значительно ниже уровней активности матрицы боли и толерантности к боли для пациента. После того как уровни допуска становятся превышенными, блокировка активируется, и пациент может ввести свой идентификационный код или, в качестве альтернативы, просто открыть контейнер для таблеток. Другим вариантом реализации изобретения является то, что если измеряются соответствующая активность матрицы боли и уровни толерантности к боли, пациент будет получать одноразовый код доступа через приложение мобильного устройства для того, чтобы открыть контейнер для таблеток один раз, а затем код доступа будет сброшен. Таким образом, количество лекарственного препарата, который принимает пациент, может контролироваться и быть доступным только в тех случаях, когда уровни боли находятся на соответствующих уровнях и требуется лечение. Таймеры, интегрированные в контейнер для таблеток с защищенным доступом, могут дополнительно препятствовать доступу к лекарственному препарату до установленного срока для того, чтобы иметь предписанные интервалы времени между введениями лекарственного препарата. Цели поставщика медицинских услуг и соглашения о лечении боли могут быть интегрированы в систему.
Компоненты и функции системы PMD 10 предоставляют биологические данные, специфичные для пациента, и объединяют эту информацию с данными приложения PainTrace 70. Эта информация может быть представлена в компоненте BioTraceIT 60, как изображено в варианте реализации изобретения на Фиг. 16, через другие компоненты системы PMD 10 и/или через другое приложение для подачи информации о пациенте. Для медицинского персонала приложение компонента BioTraceIT 60 может отображать диаграммное представление 122 человека пациента на основе биологических данных. Диаграммное представление 122 человека может не предоставлять никаких идентифицирующих признаков, но для валидации и анализа оно может помочь поставщику медицинских услуг (НСР) с общими характеристиками пола, формы и размера пациента. Диаграммное представление 122 человека может дополнительно предоставить индикатор 124 определения боли, для того, чтобы позволить поставщик медицинских услуг (НСР) быстро проверить область патологического состояния. Например, пациент невысокого роста с достаточно большими характерными особенностями, основанными на массе, росте и индексе массы тела (ИМТ) с болью в левом колене, изображен на Фиг. 16. Имя и другая идентификационная информация пациента могут быть предоставлены в некоторых вариантах реализации изобретения, при этом в других вариантах реализации изобретения для защиты конфиденциальности пациента может быть предоставлен идентификационный код пациента 126 для того, чтобы отличить запись пациента от других пациентов. Общие биологические данные могут быть перечислены в таблице 128 с метками и значениями, описывающими физикальные характеристики пациента. Биологические данные могут дополнительно содержать психологические оценки 130, социальные данные 132, историю болезни 134, данные о недавнем путешествии 136, и/или любая другая информация, которая может иметь отношение к диагностике и лечению, может быть включена в данные пациента. Данные могут дополнительно включать данные, которые могут считаться не имеющими отношение к диагностике и лечению, такие как данные, относящиеся к экономическому статусу 138 и страховому покрытию 140, которые должны использоваться в компоненте MediTraceIT 64 системы PMD 10. Если это возможно или используются функции системы PMD 10, может быть добавлена информация, в том числе данные других измерений боли или рейтингов, таких как визуальная аналоговая шкала (ВАШ), для сравнения с объективными данными PainTracePainTrace Factor 102. Система PMD 10 обеспечивает настройку дисплея для того, чтобы можно было выбрать различные факторы за пределами шаблона основного фактора, основанные на расширенных пользовательских параметрах и предпочтениях.
Данные могут быть интегрированы в системе PMD 10 с помощью электронных медицинских карт или посредством информации об обследования пациентов. При наличии таковых, записи пациента, загружаются из электронных медицинских карт (ЭМК) и связаны с идентификационным кодом 126 пациента, который связывает медицинские карты пациента с приложением LifeTraceIT 60 или другим приложением патентных данных. Если ЭМК нет в наличии, пациенту может быть предложено ввести соответствующую информацию, такой как возраст, рост, вес, сопутствующие заболевания, и другую информацию. Пациенту дополнительно может быть предоставлена форма информированного согласия, в которой информируют пациента о том, как эти данные будут использоваться, политика конфиденциальности и условия в отношении совместного использования его данных, которые будут использованы для улучшения органами здравоохранения понимания той или иной проблемы со здоровьем/болезненным состоянием и в целях улучшения диагностики и лечения. Политика конфиденциальности пациента может представить информацию о правовой и моральной ответственности за обеспечение конфиденциальности пациента и конфиденциальности всех пациентов, а также защитить конфиденциальность информации о состоянии здоровья и медицинской документации. Эти медицинские данные могут включать информацию о результатах тестов из образцов крови, физикальном обследовании, анамнезе и другие данные, собранные или пересмотренные в процессе лечения пациента. Конфиденциальная информация может также содержать личную информацию, такую как дата рождения, а также медицинскую документацию от основного врача схемы медицинского обеспечения, где любую информацию о состоянии здоровья, которая может быть использована для идентификации пациента называют «защищенной информацией о состоянии здоровья» (PHI). Серверная система BioTraceIT 18 системы PMD вне какого-либо учреждения хранит анонимность пациента и на самом деле только имеет цель изучать большие группы людей для того, чтобы лучше понять проблемы со здоровьем и улучшить результаты лечения пациентов. При запросе данных пациента для использования в программном приложении PMD 10 может потребоваться подтверждение согласия пациента для использования данных, которые не используются при получении данных от датчика PainTrace 14 и других медицинских устройств. Приложение LifeTraceIT 60 или другое приложение данных пациента может дополнительно предоставлять доступ к информации об обследовании 144, представленной пациентом врачу. Функции системы PMD 10 могут дополнительно обеспечить доступ к предшествующей медицинской документации 146 пациента и к приложению ввода данных 148 для врача для того, чтобы ввести примечания по диагностике и лечению. Обследование пациента может предоставить пациенту возможность создать личную медицинскую карту, доступ к которой он может получить через свою электронную медицинскую карту через больничную сеть 16 или через отдельные программные приложения в качестве доступных вариантов для выбора пациента, предоставляя пациенту возможность отслеживания лечения и доступа к справочным материалам, связанным с его болезненным состоянием.
Обследование пациента может иметь целый ряд вопросов, которые система PMD 10 может итерировать и направить к конкретным вопросам, исходя из полученных ответов. Таким образом, пациент будет поэтапно проходить через контроль для того, чтобы ответить на вопросы, относящиеся к его конкретной проблеме со здоровьем, симптомам, эмоциональному состоянию и болезненному состоянию. В самом простом примере, первый вопрос, является ли пациент мужчиной или женщиной программное обеспечение будет представлять вопрос о беременности в женском опросе, но не в опросе, представленном для пациента-мужчины. Вопросы опроса могут относиться к основным демографические характеристикам, конкретным поведенческим/экологическим/психологическим/социальным факторам, конкретным кратким формам и разработанным вопросникам как для оценки определенных параметров, так и для корреляции с существующими данными, уже собранными при помощи широко используемых инструментов оценки, таких как вопросники оценки и/или инструменты, связанные с болью, которые могут включать: многофакторный личностный опросник MPQ, краткий опросник оценки боли BPI, опросник TOPS, опросник SF-36, комплексный болевой опросник WHYMPI, визуальную аналоговую шкалу (ВАШ), шкалу оценки общего впечатления врача об изменении состояния пациента PGIC, цифровую рейтинговую шкалу (ЦРШ) и другие. Вопросы и опросы, включенные для сбора данных, хранятся для периодического использования, чтобы, возможно, быть снова предоставленными пациенту для переоценки корреляций между данными Biotrace Factors в связи с тем, что способы лечения и результаты лечения понимаются дополнительно.
Опрос может включать общие вопросы по возрасту, полу, этнической принадлежности, росту, весу и занятиям для того, чтобы обеспечить исходные уровни и закрепить пациента в общей популяции пациентов. Затем в опросе могут задаваться более конкретные и непосредственные вопросы для того, чтобы определить текущую физиологию, психологическое состояние и симптомы, которые в виде приводимых в качестве примера вопросов могут быть следующими, с конкретным полем выбора, шкалами оценки или полями ввода данных для ответа пациента: За последние семь дней. В общем, как бы вы оценили свое физическое здоровье?




В целом, как бы вы оценили свое психическое здоровье, в том числе ваше настроение и способность мыслить?





В целом, как бы вы оценили свое удовлетворение своими социальными действиями и отношениями?





Вы тренируетесь? Как часто?
Прогноз в случае, если какое-либо упражнение вы выполнили за последние 48 часов, или у вас был высокий уровень физической активности?
Вы принимаете какие-нибудь лекарства? Какие?
У вас была недавно травма ? Если да, пожалуйста, объясните:
есть ли у вас постоянная или регулярная боль, которую вы испытываете ежедневно? Если это так, то где? Как долго вы испытывали эту боль?
Оценка с использованием ВАШ: оцените свой уровень боли в настоящее время, если таковой имеется на шкале ниже.
Вы перенесли или в настоящее время у вас имеется одно из следующих:
список болезненных состояний, таких как рак, инсульт, сердечный приступ, состояние после хирургического вмешательства.
Другие общие вопросы о состоянии здоровья могут быть взяты из стандартного опросника о состоянии здоровья, такого как SF-36. Все ответы скомпилированы и связаны с пациентом или кодом для идентифицированного пациента и представлены в приложении компонента LifeTraceIT 60 или другом приложении данных о пациентах с использованием системы PMD 10.
Данные могут быть дополнительно связаны с приложением для анализа BioTraceIT 62 для поставщика медицинских услуг (НСР) с целью доступа к диагностическим показаниям пациента (например, уровням боли), анализа эти показания и обзора факторов, которые могут способствовать повышенным или пониженным показаниям (например, возраст, вес, сопутствующие заболевания и т.д. могут влиять на уровни боли). Модуль административных инструментов 21 системы PMD 10 может предоставлять доступ к конкретной информации, которая должна контролироваться администратором, в результате чего врачу может быть предоставлен доступ ко всей информации о пациенте, в то время как другой поставщик медицинских услуг (НСР) может при использовании логина и пароля получать, в частности, только данные о результатах тестирования, информацию о лекарственном препарате или о лечении, в случае необходимости, и имеющие отношение к его взаимодействию с пациентом.
Как изображено на Фиг. 16, врач или поставщик медицинских услуг (НСР) с надлежащим административным доступом могут просматривать биологические данные 128 и выбирать любые факторы, которые, по их мнению, имеют отношение к диагнозу, используя окна флажков 149. Эти факторы, упомянутые в данном документе как BioTrace Factors 150, также анализируются с использованием статистических и сравнительных алгоритмов в модуле анализа данных 27 по отношению к популяциям и болезненным состояниям на основе справочных материалов и накопленных данных о пациенте. В целом, система PMD 10 будет иметь эволюционный характер в том аспекте, что она будет постоянно обновляться данными, поступающими от поставщиков медицинских услуг, которые собирают данные BioTraceIT о пациентах, страдающих различными болезненными состояниями, и справочными материалами 22 из медицинских журналов и периодических изданий на основе конкретных болезненных состояний, обнаруженных в популяции пациентов, предоставляющих данные. В одном варианте реализации изобретения система PMD 10 собирает данные, относящиеся к острой и хронической боли, которые содержат биологические, психологические и социальные критерии, а также из других соответствующих областей, и объединяет эти данные с данными об остром или хроническом заболеванием, а также с диагностическими данными PainTrace и другими накопленными точками данных. Система PMD 10 интегрирует собранные данные в соответствии с HIPAA или соответствующим образом с целью защиты права пациентов на конфиденциальность для того, чтобы в режиме параллельного выполнения интегрировать данные о пациентах, используя биопсихосоциальную платформу, или такую, которая содержит другие соответствующие факторы для точек данных, для дальнейшего увеличения понимания болезненного состояния или оценки вмешательства. Например, данные PainTrace об измерении проявления боли в нервной системе, могут быть комбинированы с данными о биологических, поведенческих, экологических, психологических и социальных факторах, для того, чтобы определить влияние этих факторов на уровень боли, испытываемой пациентом. Как изображено на Фиг. 17, анализ данных Biotrace Factors 150 может быть обеспечен путем сравнения первого из общих факторов 152 с аналогичной расположенной популяцией, например, пациентами того же возраста, пола, расы и другими подобными данными BioTrace Factors, которые могут иметь значение, например, у пациентов, испытывающих боль в аналогичном местоположении. Данные популяции BioTrace Factors 154 могут быть представлены в виде ряда значений, таких как приемлемые показатели кровяного давления и частоты сердечных сокращений. Модуль анализа данных 27 системы PMD 10 сравнивает данные пациента Biotrace Factors 150 с данными популяции BioTrace Factors 154 и далее проводит глобальный анализ того, как биологические данные пациентов могут относиться к другим для того, чтобы определить уровень Factor Impact 156 по шкале 158 из примеров 1-5, а индикаторы 160 представлены для отображения уровня воздействия, который данные пациента Biotrace Factors 150 могут иметь для того, чтобы помочь поставщику медицинских услуг (НСР) в понимании важности и потенциальной озабоченности и необходимости вмешательства, связанного с Фактором. Например, индекс массы тела (ИМТ), который превышает значение 40, обозначенный ссылочной позицией 153 и показанный в рамках общих данных Population Biotrace Factors 154, может иметь самый высокий уровень Factor Impact со значением 5, как обозначено ссылочной позицией 155, для того, чтобы предупредить поставщика медицинских услуг (НСР) о рисках, которые связаны с ожирением. Модуль анализа данных 27 идентифицирует данные Biotrace Factors 150, имеющие наивысшие уровни Factor Impact 156, и выполняет поиск известных справочных материалов, связанных с этими факторами, для определения Contribution Factor 162, который представляет собой статистическую процентную оценку того, насколько данные Biotrace Factor 150 могут влиять на восприятие боли пациентом в виде увеличения или уменьшения для того, чтобы учитывать субъективный характер боли. Модуль анализа данных 27 дополнительно выполняет сравнение сигналов данных PainTrace 72 и PainTracePainTrace Factor 102 аналогичной популяции, а также определение данных Contribution Factor 162 для вычисления PainTracePainTrace Factor 102 в виде процента от вариации между ответом матрицы боли на раздражитель и ощущением пациента; при этом учитывается биопсихосоциальная оценка боли. При выводе данных PainTracePainTrace Factor 102 из соответствующих демографических данных пациента оценка и реакция на стандартизированные болевые раздражители с учетом существующих инструментов оценки, таких как ВАШ, может обеспечить более достоверные и объективные показания боли. Значения PainTracePainTrace Factor 102 по отношению к ВАШ могут быть сделаны при сравнении женщин и мужчин; молодых и пожилых людей; показатель ВАШ равный 1-3 против показателя ВАШ равного 3-6 против показателя ВАШ, равного 7-10, для определения отношения PainTracePainTrace Factor 102 к ВАШ. Тем не менее, в отличие от ВАШ, данные PainTracePainTrace Factor 102 корректируется с помощью любых ранее существовавших заболеваний, таких как, например, операция в течение последних 3 месяцев или диабет в течение последних 3 лет, что повлияет на нормализацию диагностических показаний по сравнению с данными пациентов BioTrace Factors 150. Данные PainTracePainTrace Factor 102 также могут быть использованы для установления начального уровня толерантности к боли 168. В то время как уровень начальной толерантности к боли 168 может быть скорректирован для пациента по мере сбора данных, исходный уровень обеспечивает сравнение и анализ, в частности, для пациентов, которые не являются коммуникативными или для животных. Система PMD 10 может дополнительно выполнить сравнительную калибровку выходных данных от устройства PainTrace 14 и установить смещение 166 для показаний напряжения для правильного определения результатов измерения боли.
В результате сравнения общих данных Biotrace Factors 150, уровней Factor Impact 156, данных Contribution Factors 162 и данных Population PainTrace Data 164 большое количество данных являются статистически структурированными, что позволяет системе PMD 10 выполнять анализ и сопоставление наиболее хорошо подходящих членов выбранной популяции в первую очередь. Система PMD 10 может сначала просмотреть результаты измерения боли из данных Population PainTrace 164 для членов популяции, имеющих одинаковые общие данные Biotrace Factors 154, аналогичные уровни Factor Impact 156 и соответствующие проценты Contribution Factor 162, как изображено на Фиг. 18. Исходя из выбранной популяции, имеющей эти статистические сходства, система PMD 10 выполняет анализ данных диагностики и тестов, выполненных для конкретного болезненного состояния 170. Система PMD 10 дополнительно выполняет анализ данных об эффективности лечения 172 в этой выбранной популяции. Система PMD 10 компилирует эти анализы в сводные листы, которые предоставляют основные моменты аналогичного диагноза и результатов лечения. Собранная информация затем объединяется с результатами исследования пациента 174, данными пациента PainTrace 176 и соответствующиими справочными материалами 178, а данные BioTraceIT 180 генерируются для анализа врачом в приложении компонента BioTraceIT 62. Как изображено на Фиг. 19, данные BioTraceIT 180 увеличивают понимание различных болезненных состояний посредством многомерной платформы анализа данных, полученных из статистических вычислений физиологических показаний и диагностической значимости данных BioTrace Factors 150. Как описано в данном документе, группы данных BioTrace Factor могут быть разработаны на основе общих характерных особенностей, таких как возраст, пол, раса, болезненные состояния, если они известны, но после того как выявленные различия в этих популяциях могут быть извлечены с использованием данных уровней воздействия и факторов влияния. Исходя из выбора пациентов, которые проявляют высокие уровни и большие факторы влияния, анализ данных PainTrace и значений данных PainTracePainTrace Factor 102, а также лечения в этой популяции может помочь поставщику медицинских услуг (НСР) в разработке протоколов тестов, диагностики и лечения для пациента. BioTraceIT предоставляет поставщику медицинских услуг (НСР) сводку и этот анализ. Тогда эффективность лечения может быть проанализирована. Приложение компонента BioTraceIT 62 обеспечивает анализ за счет использования биологического уровня и за счет использования клинического уровня. Анализ биологического уровня, как описано выше и изображено на Фиг. 18, анализирует комбинацию данных Patient BioTrace Factors 150, Physiological Readings от устройства PainTrace 14 или других датчиков и Contributing Factors 162, связанных с информационной базой данных об острых и хронических болезненных состояниях. Этот биологический уровень ориентирован главным образом на состояние здоровья пациента, историю, образ жизни, поскольку он относится к аналогично расположенным популяциям, физиологическим показаниям и данным BioTrace Factors 150, которые способствуют изменению субъективного восприятия боли человеком. Функциональность биологического уровня позволяет перевести субъективные данные в объективные данные посредством анализа способствующих факторов. Полученное в результате значение данных PainTracePainTrace Factor 102 может быть дополнительно сравнено с ВАШ или другими объективными показателями для улучшения общей точности нормализованного восприятия боли пациента.
Клинический уровень приложения компонента BioTraceIT 62 обеспечивает анализ комбинации симптомов, клинических данных и протоколов лечения. Клинический уровень сосредоточен главным образом на выявленных симптомах, результатах тестов, включая анализ крови и мочи, а также на соответствующих протоколах лечения. Комбинация биологического уровня и клинического уровня позволяет с использованием объективных физиологических данных при комбинированных болезненных состояниях помочь в анализе потенциально успешных протоколов лечения и подтверждении эффективности на основе улучшений, связанных с объективными измерениями. Устройство PainTrace 14 для объективных измерений боли предоставляет данные для оценки эффективности и будущего использования протоколов лечения на основе популяций пациентов, острых и хронических болезненных состояний и способствующих факторов, влияющих на субъективное ощущение отдельных пациентов.
Приложение BioTraceIT 62 обеспечивает доступ ко всей соответствующей информации через значок данных о пациенте 106, выпадающие меню, вкладки и/или другие программные функции. В выпадающем меню данные BioTrace Factors 150 могут быть перечислены в порядке релевантности, который основан на анализе значения фактора Biotrace Factor, поскольку он относится к уровню Factor Impact 156 для того, чтобы получить данные Contribution Factor 162. Чем больше значение Contribution Factor 162, тем выше значение Biotrace Factor 150 в раскрывающемся списке. Данные Biotrace Factor 150 могут быть выбраны из выпадающего меню, и их можно перетащить на дисплей для того, чтобы оценить данные Biotrace Factor 150 относительно их значимости для заболевания пациента и наблюдаемых симптомов. Доступ к дополнительным ресурсам и информации можно получить для того, чтобы обеспечить данные, объяснения, исследования и соответствующие варианты лечения, щелкнув по появляющимся новым уровням информации. Визуальный обзор данных пациента BioTrace Factors 150 и актуальность разрабатывается для быстрого анализа того, что лучше всего улучшит состояние здоровья пациента путем понимания состояния здоровья отдельного пациента и особенностей, которые в наибольшей степени влияют на симптомы пациента, которые приведут к улучшению результатов лечения.
В приложении компонента BioTraceIT 62 представления проанализированных данных могут быть представлены изменениями размера, формы и цвета значков, как изображено на Фиг. 19. Размер значка может представлять большую популяцию пациентов и/или более распространенные симптомы. Поставщик медицинских услуг (НСР) может сначала щелкнуть более крупные значки для того, чтобы рассмотреть очевидные факторы, которые изначально легко устраняются, например, стресс 190, способствующий дисфункции височно-нижнечелюстного сустава (TMD), где пациент и диагностическая информация могут быть предоставлены в диалоговом окне 192. Данные BioTrace Factors 150 оцениваются с использованием уникальных статистических алгоритмов для представления корреляций между биофизическим состоянием пациента, болезненным состоянием, историей болезни, справочными материалами и использованием других источников для определения значимости одной диагностической составляющей, такой как стресс, насколько составляющая может быть связана с болью пациента и любыми отношениями, способствующим фактором или выбросом, что может потребовать дополнительного анализа для определения или подтверждения диагноза и лечения пациента. Приложение BioTraceIT 62 может представлять возраст пациента 194 в качестве фактора, историю болезни пациента, например, идентификацию спортивной травмы 198 в области боли и информацию об ожирении 200, в качестве примера. Каждая диагностическая составляющая может быть представлена с использованием уникальных комбинаций элементов на дисплее для того, чтобы представлять редкие способствующие факторы или редкие симптомы для пациента, например, в меньших значках, и более часто распространенные факторы в более крупных значках. Посредством отображения размера и цветовых соотношений между этими данными BioTrace Factors 150 поставщик медицинских услуг (НСР) может обосновать диагноз с более крупными поддерживающими и способствующими составляющими компонентами. Тем не менее, данные BioTrace Factors 150, отображаемые в меньших и приглушенных цветных значках, могут привлечь внимание поставщика медицинских услуг (НСР) к составляющей, которая, хотя и не очевидна, может быть источником симптомов пациента, что может быть легко упущено. Например, у больного есть боль в суставах, они кажутся здоровыми, но произошло заражение микробом при выезде за границу, что может вызвать мальабсорбционный синдром, который может быть связан с болью в суставах и тошнотой.
Значок недавнего путешествия 202, хотя и является небольшим на дисплее, может указывать на альтернативный диагноз.
Цвет коррелированных данных BioTrace Factors 150 может обеспечить возможность поставщику медицинских услуг (НСР) быстро определить значение данных BioTrace Factors 150, которые, как известно, сильно коррелируют с проявленными симптомами и в значительной степени способствуют диагностике. В качестве примера основные цвета могут представить это значение. В приведенном выше примере яркая желтая иконка 202, указывающая на то, что у пациента может быть мальабсорбционный синдром, вызванный попаданием микроба, легко идентифицируется в основном цвете, заставляя врача проявлять интерес к менее распространенному BioTrace Factor 150, который имеет высокую корреляцию с данными Factor Impact 156. Factor Impact 156 может увеличиваться в зависимости от продолжительности симптома, времени возможного попадания микробов, типа микроба, известных симптомов, которые проявляются, поездки в определенные районы и других данных BioTrace Factors 150. Система PMD 10 обеспечивает индикаторы, привязанные к временным блокам, для визуального представления времени и продолжительности BioTrace Factors 150, которые могут иметь решающее значение для правильной диагностики. Приложение BioTraceIT 62 дополнительно обеспечивает корреляцию данных BioTrace Factors 150, которые имеют низкую корреляцию с симптомами и, как правило, не влияют на восприятие пациента. Эти низкие корреляции BioTrace Factors 150 могут быть представлены в виде приглушенных цветов. Индикатор в виде цветного кольца или границы 204 вокруг значка может представлять фактор, который имеет потенциал, чтобы влиять на физиологические показания датчика, в этом случае боли, как в этом примере, где стресс в приглушенном цветном кольце 206 может представлять собой BioTrace Factor 150, который может увеличить восприятие боли, и по этой причине выраженная боль пациента может быть увеличена и не являться явным индикатором степени физикальной проблемы. Приложение BioTraceIT 62 визуально представляет индикаторы в виде цвета, размера и формы для того, чтобы позволить поставщику медицинских услуг (НСР) дополнительно исследовать корреляции для того, чтобы улучшить диагностику и общее лечение пациента. Система PMD 10 также предоставляет справочные ссылки на медицинские журналы и данные пациента в пределах одной среды для того, чтобы помочь в том, чтобы поставщик медицинских услуг (НСР) получил хорошо обоснованный диагноз и план лечения как можно быстрее. Как изображено на Фиг. 20 сравнение данных BioTrace Factors 150 может предоставить врачу определение соответствующих тестов, полученных из статистического анализа и корреляции данных BioTrace Factors 150, выполненных с помощью приложения BioTraceIT 62. Протокол тестирования может быть представлен в виде другой формы, такой как треугольник для того, чтобы указать значимость корреляции и что дальнейшие тесты могут обеспечить более полный диагноз. Приложение BioTraceIT 62 обеспечивает выбор каждого значка для представления данных пациента, относящихся к данным BioTrace Factors 150, то есть веса, отслеживаемого в динамике по времени для ожирения, по сравнению с отслеживаемыми критериями результата лечения, например, ослаблением боли в динамике по времени. Статистическая релевантность любых данных BioTrace Factor 150 и/или какие схемы лечения были использованы; и соответствующие протоколы исследований и лечения, одобренные клиникой или учреждением, могут быть предоставлены и также могут быть представлены в диалоговых окнах 210, выпадающих меню и/или посредством ссылок 212, которые открывают другие компоненты и функции системы PMD 10, имеющую отношение к пациенту информацию, связанную с этими приложениями, или для открытия документов или других ресурсов данных. Значение цвета, формы и размера значков также может быть представлено в диалоговом окне 214 описания значков.
В этом примере значок 200 ОЖИРЕНИЕ, показанный как более крупный значок, может быть общим фактором у пациентов с болью в суставах. Тем не менее, пациент А 216 страдает от TMD, и поэтому дополнительный вес не будет отвечать за чрезмерное напряжение в области височно-нижнечелюстных суставах. По этой причине, в то время как значок ОЖИРЕНИЕ 200 может быть почти столь же велик, как значок СТРЕСС 190, он находится в приглушенном цвете из-за более низкой корреляции между этими данными Biotrace Factor 150 и связанными с TMD симптомами пациента. Тем не менее, фактор СТРЕСС, обозначенный значком 200, может быть несколько менее распространен в общей популяции и, следовательно, имеет меньший размер по сравнению с фактором ОЖИРЕНИЕ, обозначенным значком 200, и выполнен вторичным цветом из-за меньшей значимости среди общей популяции в целом. Стресс может вызвать физическую активность, такую как скрежетание зубами, которая может усугубить и вызвать TMD. Кроме того, стресс может увеличить ощущение боли пациентом, что может увеличить его симптомы. По этой причине у пациента В 218, в то время как стресс обозначен приглушенным цветом, имеется ОСНОВНОЕ ЦВЕТОВОЕ КОЛЬЦО, которое означает, что этот показатель BioTrace Factor 150 влияет на физиологические показания, в данном случае, боли.
Значок СПОРТИВНАЯ ТРАВМА 198 обозначает еще меньшую популяцию, но может иметь значительную корреляцию в диагностике на примерах как у пациента А 216, так и у пациента В 218, поскольку в обоих случаях боли в коленном суставе и боли при TMD могут быть вызваны предшествующей спортивной травмой. Например, если пациент А играл в хоккей и получил удар в челюсть хоккейной клюшкой, то эта травма может иметь более высокую корреляцию в зависимости от характера травмы. Сбор информации по каждому фактору BioTrace Factor 150 от каждого индивидуума, будь то физиологический или социальный по своему характеру, такой как стресс или физический по природе, например, предшествующая травма в сочетании с соответствующими физиологическими показаниями, связанными с данными PainTrace, и другими данными, полученными от других датчиков, приводит к большему пониманию эффективности и отслеживанию результатов лечения. Кроме того, длительность боли, если она не лечится и является хронической или недостаточно адаптируемой по своей природе, может увеличить восприятие боли, известное как гипералгезия, поэтому более темное окрашенное ЦВЕТНОЕ КОЛЬЦО обозначает влияние фактора спортивной травмы на восприятие симптомов. Яркий цвет значка 220 ЖЕНЩИНА, ВОЗРАСТ 30 лет, для пациента А 216 указывает на то, что TMD чаще всего встречается у женщин в возрасте 20-40 лет. Эта возрастная группа менее важна при боли в коленном суставе, поэтому значок 221 выполнен в приглушенном цвете. Из корреляции, представленной в приложении BioTraceIT, треугольник ТЕСТ ОСТЕОАРТРИТА 222 указывает, что данные BioTrace Factors 150 могут обосновать диагноз остеоартрита как значимый, когда ~ 14% страдают остеоартритом к возрасту 24 года, а после 65 лет заболеваемость возрастает до 35%. Из-за возраста пациента это будет более важным фактором у пожилого пациента. В силу того, что возраст пациента составляет 30 лет, эти данные BioTrace Factors 150 представляют небольшую популяцию, однако, если они страдают от остеоартрита, это будет иметь существенное значение. Доказательства остеоартрита отсутствуют, но тестирование/визуализация, как указано в тестовом треугольнике 222, для того, чтобы исключить артрит, могут быть действительными. Понимание способствующих факторов BioTrace Factors 150 и их значимости, а также отслеживание результатов лечения с использованием данных датчика PainTrace и данных от других датчиков могут привести к потенциально более эффективному и оперативному диагностированию и лечению, что приведет к улучшению состояния здоровья, сокращению времени для того, чтобы вернуться к работе и повседневной активности, а также последующему сокращению расходов на здравоохранение благодаря улучшенным способам лечения, что приведет к более быстрому восстановлению и сокращению потерянных рабочих дней, что еще более положительно повлияет на экономику.
За счет использования корреляции и анализа данных приложения BioTraceIT Application, которые вращаются вокруг боли в качестве центрального симптома для оценки и диагностики болезни, болезненного состояния, состояния здоровья и исцеления, поставщик медицинских услуг (НСР) может рекомендовать потерю веса и нацелиться на один или более факторов BioTrace Factors 150, которые могут быть значимыми для диагностики и лечения. Данные из приложения PainTrace Application 70 и LifeTraceIT, которые являются результатом визитов пациентов, позволят поставщику медицинских услуг (НСР) отслеживать выбранные целевые факторы с помощью приложения BioTraceIT Application 62, обеспечивающего визуальные сравнения, показывающие временной интервал, продолжительность и эффект действий и лечения, принимаемого пациентом на основе физиологических показаний и регистрируемой активности, собранных для оценки эффективности лечения и вмешательств, которые могут быть затем преобразованы в показатель прогресса BioTrace Progress Score 280, который обеспечивает совокупный балл, основанный на всех критериях для быстрой ссылки и простого отслеживания результатов. Как изображено на Фиг. 21, программное обеспечение будет автоматически отслеживать и отображать прогресс, и связывать информацию о пациенте, такую как потеря веса, и коррелировать с улучшением симптома. Целевые факторы могут быть связаны с факторами Pain Trace Factor 102, которые указывают на усиление или ослабление боли. Вес 224 человека может отслеживаться и визуально отображаться. Временной блок 78 может представлять любую приемлемую шкалу, такую как недели или месяцы, для отображения изменений целевого фактора BioTrace Factor 150. Сравнение данных в динамике по времени или относительно разных пациентов или популяций может обосновывать стратегии для получения более эффективных результатов лечения. В то время как физические упражнения, как известно, способствуют уменьшению веса, представление третьего фактора BioTrace Factor 150 упражнения 226 в течение периода времени и ведущего к потере веса, а также уменьшению боли является важной корреляцией, которая может быть эффективной, для того, чтобы заставить пациента изменить свое поведение. Сводная информация 228 и анализ данных BioTrace Factor 230 также могут быть доступны через приложение BioTraceIT Application 62. Приложение BioTraceIT Application 62 обеспечивает статистическую значимость корреляции для улучшения результатов лечения; обеспечивают средние показатели улучшения в течение определенного периода времени, например, пациент терял пять фунтов в неделю в течение двух месяцев, при этом использование программного обеспечения LifeTraceIT для схем питания и выбора продуктов питания дополнительно может быть коррелировано с улучшениями, а также оценкой целевого привлечения пациента к участию в процессе собственного лечения, и влияния на изменение поведения и принятие решений. Позитивное влияние на активность отдельных пациентов и принятие решений способствовало бы увеличению положительного показателя прогресса BioTrace Progress Score 280. Уменьшение использования лекарственного препарата и последующая экономия затрат затем будут отслеживаться компонентом MediTraceIT 64 системы PMD 10. Показатель прогресса BioTrace Progress Score 280 может использоваться в качестве метрики для программного обеспечения BioTraceIT и программных приложений MediTraceIT в системе PMD 10. Данные Biotrace Factor 150 могут быть дополнительно проанализированы для последующих обновлений программного обеспечения для системы PMD 10 с целью улучшения объективных измерений и алгоритмов воздействия факторов.
Конечные пользователи могут также просматривать данные без использования значков и просмотра в типичной форме таблицы и гистограммы. Независимо от того, просматриваете ли вы в визуальном или графическом формате, пользователь может щелкнуть по каждому из данных BioTrace Factors 150, Factor Impact 156 или Contribution Factor 162 для объяснения релевантности, ресурсов, связанных исследований, протоколов лечения и коррелированных данных пациента, а также другой информации для того, чтобы оказывать содействие и поддерживать эффективную диагностику и лечение. Если учреждение выбирает, они могут связывать эти данные с компонентом MediTraceIT 64 системы PMD 10, и посредством интеграции с их электронными медицинскими документами должны быть обеспечены представления о показателях прогресса BioTraceIT Progress Scores 280, отражающие результаты лечения, улучшающие результаты последующих посещений пациентов для того, чтобы показать эффективность лечения, проанализировать, как последующие вмешательства связаны с начальными симптомами и лечением, и дополнительно анализировать затраты на здравоохранение, связанные с лечением. Как изображено на Фиг. 22, компонент MediTraceIT 64 может предоставить интерфейс 240 панели управления, который предоставляет пользователю в качестве поставщика медицинских услуг (НСР), врача, администратора или других пользователей выбор данных пациента в модуле 242 Patient Link, рассматривает действия, предпринятые в отношении медицинского обслуживания пациента в модуле поставщика медицинских услуг (НСР) 244 и анализирует лечение в отношении затрат в рамках модуля Cost Analysis Module 246. Модуль 242 Patient Link предоставляет доступ к компонентам и функциям в системе PMD 10, связанным с данными BioTrace Factors 150 пациента, симптомами пациента 250, данными пациента PainTrace 252, и доступ к обследованиям Surveys 254 пациента, которые могут обеспечить статус текущего состояния здоровья пациента. Модуль 244 поставщика медицинских услуг (НСР) может предоставлять доступ к информации по определенному диагнозу в пункте Diagnosis 256, по лечению в пункте Treatments 258 и по рецептам в пункте Prescriptions 260, которые также могут обеспечивать доступ к информации об аллергии 262 или о взаимодействии с лекарственным средством 264. Компонент MediTraceIT 64 может дополнительно предоставлять доступ к модулю демографических данных Demographic 266 для лечения и сопоставлений затрат, представленных пациентам, имеющим аналогичные данные BioTrace Factors 150 и BioTrace IT Progress Scores 280, справочному модулю Reference 268 для предоставления информации о острых и хронических болезненных состояниях. Каждый из этих модулей компонента MediTraceIT 64 системы PMD 10 может предоставить подробную информацию о пациенте, а также о диагнозе и лечении пациента для того, чтобы позволить пользователю проверять и утверждать шаги, предпринятые поставщиком медицинских услуг (НСР) и врачами при лечении пациента.
Модуль Cost Analysis Module 246 обеспечивает расходы, связанные с шагами, предпринятыми в пунктах Treatments 270, Medications 272 Tests 274 и Hospital Visits 276. Информация о расходах 280 может быть ограничена с помощью административных инструментов, которые устанавливают уровни доступа и разрешения на основе пользователя. Тем не менее, применение приложения MediTraceIT 64 может быть ориентировано на врача и поставщика медицинских услуг с использованием данных LifeTraceIT 60 и BioTraceIT 62, и данных результатов измерения боли для того, чтобы отслеживать результаты лечения с тем, чтобы представить финансовую эффективность от реализации успешных результатов лечения. Путем отслеживания результатов лечения, положительные результаты подкрепляются на основе готовности пациента и соблюдения требований лечения, приводит к финансовым льготам, которые могут быть возвращены пациенту в виде, например, страховых скидок. Финансовые льготы также реализуются при более быстром определении врачом неэффективных методов лечения и/или устранении злоупотребления препаратом пациентом. При использовании MediTraceIT 64 с отслеживанием результатов лечения BioTraceIT 62 и физиологических показаний данных PainTrace, медицинские расходы могут непосредственно коррелировать лечение с объективными показателями улучшенных результатов лечения, о чем свидетельствует снижение уровней боли пациента. Такой комплексный подход с использованием компонентов системы PMD 10 обеспечивает улучшенный диагностический анализ, валидацию лечения и реализацию финансовых льгот в рамках легкодоступного программного приложения, которое коррелирует и представляет данные полезным и эффективном образом для пациентов, поставщиков медицинских услуг (НСР) и врачей.
Пример 1
Измерение активности матрицы боли с использованием устройства PainTrace 14 системы PMD 10 изображено до и после лечения акупунктурой на Фиг. 23. До начала лечения был зафиксирован средний уровень боли 9.4 mV у пациента, имеющего боль в нижней части спины. Значение самооценки пациента по ВАШ составляет четыре (4) до начала лечения. После лечения средний уровень боли уменьшался, что выражалось положительным показанием 6,4 мВ, а пациент сообщал значение самооценки ВАШ, равное нулю (0). При использовании системы PMD, наблюдалось изменение активности матрицы боли, указывающее на успешный ответ на лечение. Кроме того, имеется количественный показатель «здоровье», который описывается как степень отсутствия боли.
Пример 2
Как изображено на Фиг. 24, пациент, имеющий повреждение подмышечного нерва, был обследован для определения боли в плече и прогрессирования заживления. Во время получения показаний в течение семи (7) минут, на протяжении более 395 секунд, самооценка пациента начального значения ВАШ составила нуль (0) в течение начального 40-секундного записанного периода исходного уровня. Через 40 секунд плечо было ротировано наружу, отмечено как болевой раздражитель, для того, чтобы раздражать травму подмышечного нерва и вызвать боль. Активность матрицы боли увеличивалась, как измерено с использованием устройства PainTrace системы PMD, которое показало отклонение от исходного уровня до показания около -5; что отражает усиление боли. При последующих вращениях плеча, стимулирующих ответную реакцию боли в течение 200 секунд и через 290 секунд, активность матрицы боли, измеренная устройством PainTrace 14, коррелирует со значениями ВАШ при самооценке. Значение ВАШ не регистрировалось во время начального болевого раздражения через 40 секунд. Экстраполированное значение было добавлено для графических целей, что эквивалентно последующим значениям ВАШ и соответствующим измерениям устройством PainTrace 14, как показано ромбами и точками соответствия и точками перегиба измеренных данных PainTrace. Корреляция этих данных с данными BioTrace Factors 150, включая популяции пациентов, с использованием системы PMD, демонстрирует количественный показатель активности матрицы боли и мониторинга в реальном времени.
Пример 3
Как изображено на Фиг. 25, лошади с диагнозом ламинит было произведено измерение с использованием устройства PainTrace 14 системы PMD 10 перед хирургической операцией резекции нерва для облегчения боли на пораженной стопе, и показало -22 в отклонении от нулевого исходного уровня до операции. Через два дня после операции были проведены измерения боли, и было показано отклонение -45. После 10 дней восстановления активность матрицы боли уменьшилась до отклонения -5. На восемнадцатый день после операции показания увеличились до +9, а лошадь продемонстрировала послеоперационное состояние без боли. На двадцать пятый день лошадь была выведена из своего стойла в первый раз после операции и активность матрицы боли была зарегистрирована на уровне +4, который, как отклонение от показаний +9, указывает на некоторую боль или уровень усталости у животного. После шести месяцев восстановления были сделаны измерения устройством PainTrace 14, и лошадь показала те же показания без боли +9 и была диагностирована ветеринаром для того, чтобы полностью восстановиться после операции.
Пример 4
Как изображено на Фиг. 26, в исследовании двадцати (20) пациентов с болью в области нижней части спины, получавших лечение иглоукалыванием, устройство PainTrace 14 системы PMD использовалось для измерения и мониторинга активности матрицы боли до и после лечения в течение пяти (5) последовательных амбулаторных посещений пациентов. В 17 из 20 случаев лечение привело к снижению уровней показателей боли с результатами в диапазоне отклонений значений от 1,0 до 13,0. У пациентов 9, 11 и 18 наблюдалось отрицательное отклонение результатов измерения устройством PainTrace 14, указывающее на большую боль после лечения по сравнению с показателями перед лечением. Дальнейшее исследование Пациента 11 показало, что субъект упал во время визита и испытывал одновременно как ранее существовавшую боль в спине, так и недавнюю боль в ноге. Лечение иглоукалыванием проводилось специально для нижней части спины и минимально влияло на другую травму. Устройство PainTrace 14 точно обнаружило продолжающуюся боль у пациента и предоставило информацию об успешных результатах лечения для других людей в рамках исследования.
Несмотря на то, что данное изобретение было описано подробно с помощью иллюстрации и примера для ясности и понимания, конечно, будет понятно, что различные изменения и модификации могут быть сделаны в форме, деталях и конструкциях без отхода от объема изобретения.
Реферат
Изобретение относится к медицине, а именно к биоаналитическому анализу. Предложена система, использующая измерение прямых биосигналов боли для диагностики боли и оценки эффективности результатов лечения, содержащая: устройство для измерения активности матрицы боли, содержащее набор датчиков, выполненный с возможностью размещения контрлатерально на теле, и по меньшей мере один дополнительный датчик, выполненный с возможностью размещения на теле ипсилатерально, причем указанное устройство выполнено с возможностью измерения отличий в напряжении или токе, полученных из измерений контралатерального датчика для определения реакции матрицы боли как отклонения соответствующего биосигнала, указывающего на увеличение или уменьшение индивидуального ощущения боли; причем указанное устройство выполнено с возможностью измерения отличий в импедансе, проводимости, напряжении или токе на основании измерений одного из контралатеральных датчиков и по меньшей мере одного ипсилатерального датчика для калибровки и нормализации биосигнала, полученного от контралатеральных датчиков; постоянный машиночитаемый носитель в сети центральных процессоров, имеющий память и хранилище данных и содержащий реализуемую на нем компьютерную программу, побуждающую один или более центральных процессоров выполнять определенные этапы; контроллер и/или процессор, выполненный с возможностью: сбора и получения данных о деятельности матрицы боли из сигналов контралатерального и ипсилатерального датчиков; получения доступа к измеряемой активности матрицы боли и данным, связанным с биофизической, биологической, психологической, социальной, экологической и демографической информацией о пациенте и других пациентах; идентификации популяции со схожими данными, связанными с биофизической, биологической, психологической, социальной, экологической и демографической информацией о пациенте и других пациентах; определения лечения или результатов лечения пациента и схожей популяции и корреляции этого лечения и результатов лечения с отклонениями биосигнала, связанными с активностью матрицы боли для определения эффективности лечения пациента. Изобретение обеспечивает повышение эффективности биоаналитического анализа. 35 з.п. ф-лы, 47 ил.

Комментарии