Способы и композиции для очистки или выделения микровезикул и экзосом - RU2748234C2
Код документа: RU2748234C2
Чертежи










Описание
Изобретение относится к клеточным микровезикулам, в частности к экзосомам, к молекулярному моделированию и к хроматографическим способам разделения и выделения молекул, включая ионообменную хроматографию.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Ссылка на любой предшествующий уровень техники в описании не является и не должна восприниматься как подтверждение или какое-либо предположение о том, что данный уровень техники является частью известного уровня техники в Австралии или любой другой юрисдикционной территории.
Микровезикулы представляют собой гетерогенную совокупность биологических структур, связанных мембранами. Такие структуры имеют липидный бислой, и они могут находиться внутри клетки или во внеклеточном пространстве. Размер микровезикул составляет от приблизительно 20 до 1000 нм.
Экзосомы представляют собой небольшие везикулы с липидным бислоем, секретируемые многими типами клеток и имеющие диаметр от 20 до приблизительно 150 нм (как определено с помощью электронной микроскопии (ЭМ)). В отличие от других микровезикул, полученных из клеток, экзосомы образуются во внутриклеточном пространстве и затем секретируются клеткой (Raposo and Stoorvogel, 2013).
Липидный состав экзосом отличается от состава клетки, из которой они происходят, но вполне характерен для того типа клеток, от которого они происходят. Кроме того, экзосомы демонстрируют некоторые общие липидные особенности независимо от их происхождения (Urbanelli et al., 2013).
В зависимости от происхождения экзосомы могут содержать самый различный "груз", включая, но не ограничиваясь ими, пептиды, белки, липиды, транскрипционные регуляторы, матричную РНК (мРНК), некодируемую РНК (нкРНК) и двухцепочечную ДНК (дцДНК).
В настоящее время экзосомы рассматривают как средство, с помощью которого исходная клетка (то есть клетка, от которой происходит экзосома) может связываться с клеткой-мишенью в таких случаях, как нейрональные синапсы, иммунная регуляция, ангиогенез, регенерация ткани и эпигенетическая модуляция. Такая связь может быть локальной или удаленной. Действительно, экзосомы из материнского молока могут модулировать иммунные и другие функции новорожденного. Такая связь может быть даже межвидовой, например, но не ограничиваясь этим, экзосомы бычьего молока, модулирующие иммунные и другие функции у человека.
Экзосомы могут быть получены из различных биологических жидкостей, включая слюну, мочу, кровь, плазму крови, (грудное) молоко, синовиальную жидкость, асцитную жидкость, сок растений и экстракты фруктов.
Подводя итог вышесказанному, представляется, что уникальные характеристики экзосом обусловлены их размером, включением клеткой путем эндоцитоза, их "грузом" и тем, что они доставляют "сообщения", которые становятся биологически активными в клетке-мишени.
Появляется все больше данных о том, что экзосомы могут играть роль в возникновении и сохранении различных заболеваний. Экзосомы, собранные из биологических образцов, могут предоставить диагностическую информацию о текущем состоянии заболевания. Концентрация РНК в экзосомах может быть вплоть до в 60 раз выше, чем концентрация непосредственно в жидкостях организма, таких как кровь, что делает экзосомы потенциально полезными в диагностике. Например, с помощью идентификации сигнатуры онкогенной РНК в экзосомах, выделенных из жидкостей человека, потенциально можно диагностировать патологическое состояние задолго до развития инвазивного рака.
Недавно было показано, что функция терапевтических клеток мезенхимного типа зависит не от самой клетки, а от паракринных факторов, продуцируемых клеткой, включая экзосомы, что позволяет установить, что экзосомы являются частью циркулирующих факторов, секретируемых клетками, которые могут опосредовать эффект, наблюдаемый при некоторых видах клеточной терапии, бесклеточным образом (Rani et al., 2015).
Терапевтически полезные экзосомы, собранные из кондиционированных сред клеток, подвергаемых культивируемых in vitro, также можно применять в качестве бесклеточного терапевтического средства, но существует потребность в надежном и гибком способе их выделения из исходных жидкостей (Chen et al., 2010).
Кроме того, экзосомы могут обеспечить естественный носитель, упакованный терапевтическими белками и РНК, когда клеточные системы экспрессии специально адаптированы.
Экзосомы невидимы под обычным оптическим микроскопом. Технологии, применяемые для обнаружения таких ультрамикроскопических частиц, как экзосомы и микровезикулы, включают электронную микроскопию (ЭМ), проточную цитометрию, динамическое рассеяние света (ДРС) и анализ траектории наночастиц (NTA). Известно, что, в зависимости от применяемого способа, сообщаемое абсолютное количество внеклеточных везикул в литре крови может варьироваться на целых пять порядков (van der Pol et al., 2010).
Хотя экзосомы представлены в большом количестве и предполагается, что они будут полезны как в диагностическом, так и в терапевтическом смысле, средства для выделения и очистки экзосом ограничивали их клиническое применение до настоящего времени.
В целом, существующие способы выделения экзосом характеризуются двумя группами:
(i) аффинный захват из-за некоторых (возможно, уникальных) селективных внешних признаков везикулы (например, гликопротеинового маркера, трансмембранных белков, таких как тетраспанины (CD9, CD63, CD81 и CD82) и МНС класса I и II, и цитозольных белков, таких как белки теплового шока (HSP-70 и HSP-90)),
(ii) выделение или очистка на основе определенных биофизических свойств экзосомы (например, размер, плотность, дзета-потенциал, сильно изогнутая поверхность, которая содержит дефекты упаковки липидных молекул, датчики кривизны мембраны)
Ограничения указанных способов изложены в таблице ниже
В US2013/0273544 (Vlassov) и US2015/0192571 (Ghosh) раскрыто применение полимеров, включая полиэтиленгликоль и некоторые полисахариды, в качестве полимеров с исключенным объемом для осаждения микровезикул из раствора. В US20160216253 раскрыто применение гепарина для выделения внеклеточных везикул.
Существует потребность в улучшенном способе выделения экзосом, в частности, способе, который обеспечивал бы улучшенный выход экзосом, и являлся бы масштабируемым для производства или получения экзосом фармацевтической степени чистоты, и который позволил бы избежать других ограничений предшествующего уровня техники, описанных выше.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение направлено на решение одной или более из вышеупомянутых потребностей или ограничений и в одном варианте осуществления обеспечивает способ получения изолята или композиции экзосом. Способ включает следующие стадии:
- обеспечение жидкости, включающей экзосомы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы; и
- где указанный массив экзосом-связывающих лигандов позволяет экзосомам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание экзосом с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением изолята или композиции экзосом.
В другом варианте осуществления обеспечен способ получения изолята или композиции экзосом. Способ включает следующие стадии:
- обеспечение жидкости, включающей экзосомы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы при значении pH от 4 до 8, предпочтительно pH от 5 до 8, выбранной из группы, состоящей из CO2H, CH2OH, CH2OSO3H, B(OH)2 и CH2OP(О)(ОН)2, или этих групп в ионизированной форме, которые обусловлены их соответствующими значениями рKа;
- где каждый лиганд расположен на расстоянии от 4 до 5 Å от других лигандов;
- где указанный массив экзосом-связывающих лигандов позволяет экзосомам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание экзосом с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением изолята или композиции экзосом.
В другом варианте осуществления обеспечен способ получения изолята или композиции микровезикул. Способ включает следующие стадии:
- обеспечение жидкости, включающей микровезикулы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы; и
- где указанный массив экзосом-связывающих лигандов позволяет микровезикулам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание микровезикул с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением изолята или композиции микровезикул.
В другом варианте осуществления обеспечен способ получения изолята или композиции микровезикул. Способ включает следующие стадии:
- обеспечение жидкости, включающей микровезикулы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы при значении pH от 4 до 8, предпочтительно pH от 5 до 8, выбранной из группы, состоящей из CO2H, CH2OH, CH2OSO3H, B(OH)2 и CH2OP(О)(ОН)2, или этих групп в ионизированной форме, которые обусловлены их соответствующими значениями рKа;
- где каждый лиганд расположен на расстоянии от 4 до 5 Å от других лигандов.
- где указанный массив экзосом-связывающих лигандов позволяет микровезикулам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание микровезикул с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением изолята или композиции микровезикул.
Изобретение также обеспечивает аппарат или устройство, включающий подложку, как описано выше, позволяющее осуществлять описанный выше способ.
Как вышеприведенное общее описание, так и последующее подробное описание являются только иллюстративными и пояснительными и предназначены для дополнительного пояснения заявленного изобретения. Прилагаемые графические материалы включены для обеспечения дополнительного понимания изобретения, и включены в состав настоящего описания и составляют его часть, иллюстрируют несколько вариантов осуществления изобретения и вместе с описанием служат для объяснения принципов изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1 - Спроектированная структура целлюлозы/Целлуфин сульфата: (А) торцевая проекция; и (B) вид сбоку; и целлюлозы/Целлуфин фосфата: (C) торцевая проекция; и (D) вид сбоку.
Фигура 2 - Спроектированная структура хитозана (А) торцевая проекция; и (B) вид сбоку.
Фигура 3 - Спроектированная структура сополимера метилвинилового эфира и малеинового ангидрида.
Фигура 4 - Спроектированная структура гепарина.
Фигура 5 - Спроектированная структура 3-APBA.
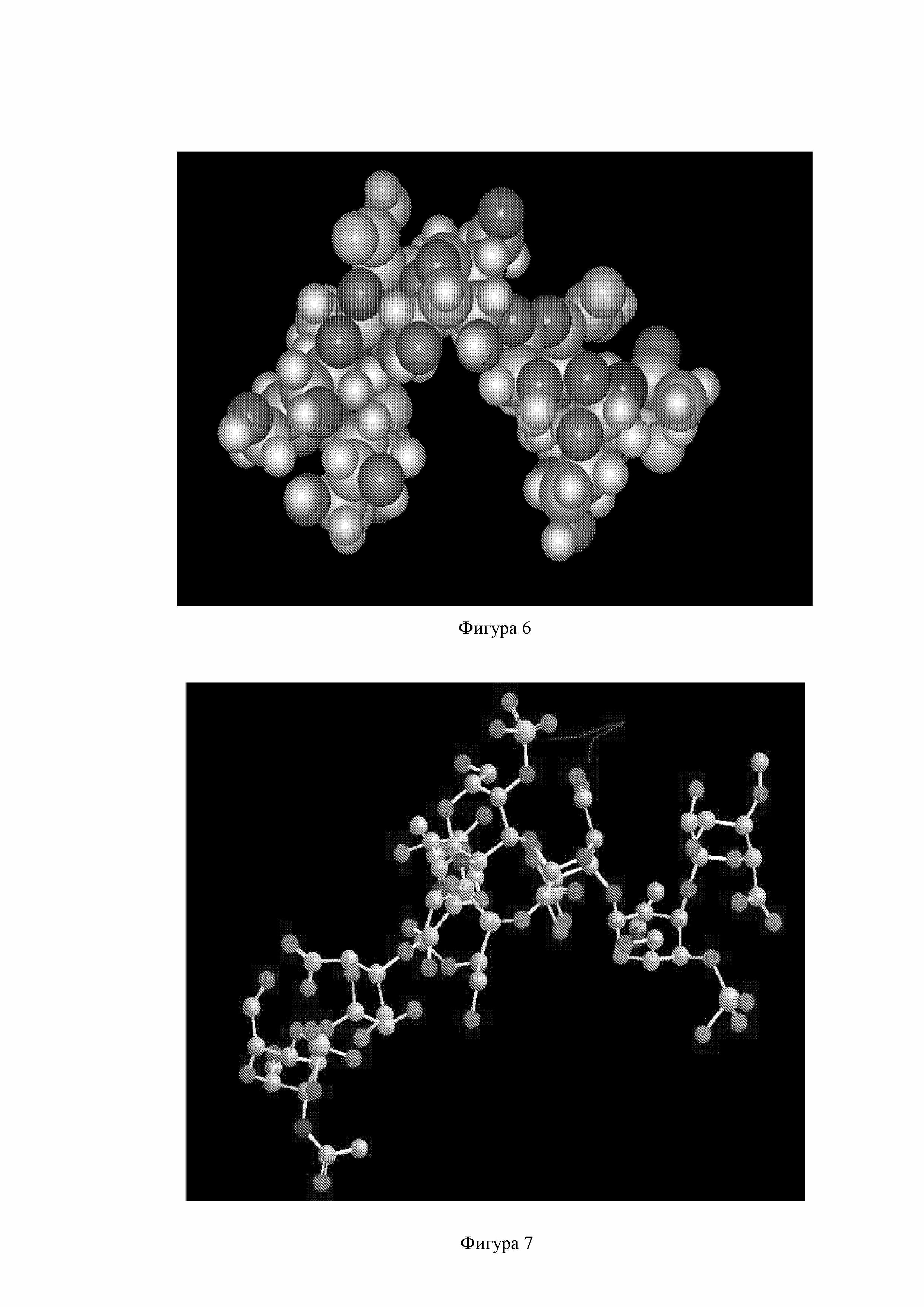
Фигура 6 - Спроектированная структура гиалуроновой кислоты.
Фигура 7 - Спроектированная структура хондроитинсульфата.
Фигура 8 - Спроектированная структура поливинилсульфата.
Фигура 9 - Спроектированная структура полиглютаминовой кислоты.
Фигура 10 - Спроектированная структура полиаспарагиновой кислоты.
Фигура 11 - Спроектированная структура полисерина.
Фигура 11(A) - Спроектированная структура биотин-C3-поли-4-гидроксибутил-β-аспарагина.
Фигура 11(B) - Спроектированная структура биотин-C3-поли-4-гидроксибензил-β-аспарагина.
Фигура 12 - Спроектированная структура поли D,L-серинсульфата
Фигура 13 - Общая структурная модель.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретение относится к разработке реагентов и способов для улучшения выделения внеклеточных везикул, особенно экзосом, из биологических источников, включая кондиционированные клеточные среды, in vivo жидкости, ткани и биопсии, а также их экстракты или фракции или изоляты. В частности, изобретение относится к реагентам и способам, которые обеспечивают улучшенный захват внеклеточных везикул из источника и их улучшенное высвобождение, приводящие к воспроизводимо более высоким выходам внеклеточных везикул. Как описано в данном документе, авторы настоящего изобретения определили до сих пор неизвестные характеристики, необходимые веществам для получения улучшенных выходов внеклеточных везикул, в частности, экзосом, из биологических источников. Эта работа позволяет выбирать и/или разрабатывать, вещества для применения в способах выделения микровезикул и экзосом.
"Внеклеточные везикулы (ВВ) или микровезикулы (МВ)" обычно относятся к гетерогенному набору in vivo мембраносвязанных биологических структур, имеющих диаметр от приблизительно 20 до 1000 нм.
"Экзосома" обычно относится к везикуле, имеющей липидный бислой и диаметр от приблизительно 20 до 200 нм, измеренный с помощью ЭМ.
"Эффективность связывания" обычно относится к показателю доли экзосом, связанных подложкой. Это разница количества экзосом, остающихся в образце после применения способа по изобретению, и количества экзосом в образце до применения способа по изобретению.
"Эффективность элюирования" обычно относится к показателю доли экзосом, элюируемых из подложки. Это разница количества экзосом в элюате после элюирования в соответствии со способом по изобретению и теоретического количества экзосом, связанных с подложкой.
"Выход" обычно относится к количеству экзосом, высвобожденных из элюата, в виде доли от общего количества экзосом до применения способа по изобретению.
"Содержать" и вариации термина, такие как "содержащий", "содержит" и "содержащийся", не исключают наличие дополнительных добавок, компонентов, чисел или стадий.
В первом варианте осуществления изобретение относится к способу получения композиции или изолята экзосом. Способ включает следующие стадии:
- обеспечение жидкости, включающей экзосомы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы; и
- где указанный массив экзосом-связывающих лигандов позволяет экзосомам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание экзосом с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением композиции или изолята экзосом.
В другом варианте осуществления обеспечен способ получения изолята или композиции микровезикул. Способ включает следующие стадии:
- обеспечение жидкости, включающей микровезикулы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы; и
- где указанный массив экзосом-связывающих лигандов позволяет микровезикулам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание микровезикул с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением изолята или композиции микровезикул.
Согласно этому варианту осуществления обеспечена подложка, имеющая поверхность. На поверхности обеспечен массив экзосом-связывающих лигандов, обеспечивающий взаимодействие экзосом-связывающих лигандов с внешней поверхностью или мембраной микровезикулы при контакте жидкости с подложкой.
Массив экзосом-связывающих лигандов представляет собой более или менее упорядоченно расположенные экзосом-связывающие лиганды на поверхности подложки. Обычно массив принимает форму множества экзосом-связывающих лигандов, которые расположены по меньшей мере на части или области поверхности подложки.
Массив может быть в форме плоского массива или линейного массива.
Плоский массив обычно простирается в 2 измерениях, определяющих его область. Плоский массив обычно может включать область экзосом-связывающих лигандов, имеющих плотность от приблизительно 1 до 10 лигандов на нм2, предпочтительно приблизительно 5 лигандов на нм2. Это дистанцирование можно определить, например, с помощью атомно-силовой микроскопии. Другие области массива могут иметь более высокую или более низкую плотность экзосом-связывающих лигандов. Таким образом, в одном варианте осуществления обеспечен способ получения композиции или изолята экзосом или микровезикул. Способ включает следующие стадии:
- обеспечение жидкости, включающей экзосомы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет плоский массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы; и
- где указанный плоский массив экзосом-связывающих лигандов позволяет экзосомам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание экзосом с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением композиции или изолята экзосом,
где указанный плоский массив предпочтительно включает область экзосом-связывающих лигандов, имеющую плотность от приблизительно 1 до 10 лигандов на нм2, более предпочтительно приблизительно 5 лигандов на нм2.
Линейный массив обычно простирается в одном измерении. В одном варианте осуществления может быть образован линейный массив, в котором экзосом-связывающие лиганды обеспечены на полимере, который имеет в целом линейное расположение на поверхности подложки. В другом варианте осуществления при применении полимер может простираться из подложки в растворитель. В линейном массиве экзосом-связывающие лиганды обычно обеспечены в диапазоне от 1 до 5 лигандов на нм, предпочтительно приблизительно 2 лиганда на нм. Это дистанцирование можно определить, например, с помощью атомно-силовой микроскопии или масс-спектрометрии. Таким образом, в другом варианте осуществления обеспечен способ получения композиции или изолята экзосом или микровезикул. Способ включает следующие стадии:
- обеспечение жидкости, включающей экзосомы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет линейный массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы; и
- где указанный линейный массив экзосом-связывающих лигандов позволяет экзосомам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание экзосом с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением композиции или изолята экзосом,
где экзосом-связывающие лиганды предпочтительно обеспечены в диапазоне от 1 до 5 лигандов на нм, более предпочтительно приблизительно 2 лиганда на нм.
В других вариантах осуществления было обнаружено, что подложка, которая имеет массив экзосом-связывающих лигандов, распределенных по поверхности подложки, соприкасающейся с поверхностью внешней мембраны микровезикулы, в котором экзосом-связывающий лиганд расположен на расстоянии не более от приблизительно 3,5 до 10 Å от другого экзосом-связывающего лиганда, образует высокоэффективную экзосом-связывающую поверхность. Как дополнительно поясняется ниже, когда массив обеспечен на поверхности подложки одним или более полимерами, которые включают экзосом-связывающие лиганды, расположенные на расстоянии от 3,5 до 10 Å, предпочтительно более 2 Å, в частности, приблизительно от 4 до 6 Å друг от друга, это относится к расстоянию, наблюдаемому при низшем энергетическом состоянии полимера, как определено способами, проиллюстрированными в настоящем документе.
Как описано далее в настоящем документе, изобретение обеспечивает структурную модель расположения экзосом-связывающих лигандов, которая позволяет прогнозировать подложки, с высокой эффективностью связывающие экзосомы. Согласно модели, вещества, которые с высокой эффективностью связывают экзосомы, обычно представляют собой подложки, которые имеют анионные или богатые электронами группы, расположенные на расстоянии от 4 до 6 Å друг от друга, как измерено в соответствии со способом, на котором основана структурная модель. Изобретение позволяет спрогнозировать эффективность связывания подложки для экзосомы или микровезикулы посредством идентификации анионных или богатых электронами групп и путем моделирования структуры подложки с применением способа получения структурной модели в данном документе.
Предпочтительно экзосом-связывающий лиганд расположен на расстоянии более 2 Å от другого экзосом-связывающего лиганда. Более предпочтительно экзосом-связывающий лиганд расположен на расстоянии от 3,5 до 6, или от 4 до 6 Å, более предпочтительно на расстоянии 3,5, 4, 5 или 6 Å от другого экзосом-связывающего лиганда в массиве.
Обычно большинство лигандов, предпочтительно 60%, или 70%, или 80%, более предпочтительно 90%, еще более предпочтительно 95%, 96%, 97%, 98% или 99% лигандов расположены на расстоянии более 2 Å, и не более приблизительно 10 Å, предпочтительно на расстоянии от 3,5 до 6, или от 4 до 6 Å от другого лиганда в массиве.
Согласно изобретению, расположение экзосом-связывающих лигандов в массиве может иметь различные уровни порядка. В одном варианте осуществления порядок расположения экзосом-связывающих лигандов в массиве может быть очень высоким. Например, каждый лиганд может быть отдален от других лигандов в массиве на точное расстояние 4 Å. Кроме того, положение каждого лиганда и/или промежутки между лигандами могут создавать определенный рисунок. При таком более высоком порядке расположения все лиганды, как правило, равномерно отдалены друг от друга в массиве. Как описано в данном документе, авторами было обнаружено, что поверхность, имеющая массив экзосом-связывающих лигандов с более высоким порядком расположения, как правило, обладает воспроизводимо более высокой эффективностью связывания экзосом или микровезикул.
В других вариантах осуществления может быть более низкий порядок расположения экзосом-связывающих лигандов в массиве. Например, большинство, но не все лиганды, могут быть расположены на расстоянии более 2 Å друг от друга, и не более приблизительно 10 Å друг от друга, предпочтительно от 3,5 до 6 или от 4 до 6 Å от другого лиганда в массиве. Кроме того, среди этого большинства лигандов может наблюдаться изменчивость в расстоянии между ними в массиве. Например, некоторые лиганды могут быть расположены на расстоянии 3,5 Å друг от друга, другие – на расстоянии 4 Å, другие – на расстоянии 5 Å, другие – на расстоянии 6 Å. При таком расположении положение каждого лиганда и/или промежутков между лигандами может не создавать различимый рисунок. Однако было обнаружено, что такой массив более низкого порядка обладает полезной эффективностью связывания в отношении связывания экзосом.
Понятно, что степень упорядоченности среди экзосом-связывающих лигандов, можно рассматривать как локальный порядок и мета-порядок. Под этим авторы подразумевают, что при взгляде на массив экзосом-связывающих лигандов на расстоянии, может показаться, что расположение лигандов случайно (т.е. они не находятся в четких ортогональных массивах) (мета-порядок), однако при этом среднее расстояние между лигандами может быть относительно плотно распределено вокруг среднего значения (локальный порядок). В настоящем изобретении авторами было обнаружено, что более высокий порядок локального порядка является предпочтительным, тогда как степень мета-порядка имеет меньшее значение. Следовательно, в определенных вариантах осуществления массив может включать области мета-порядка, при условии, что массив содержит по меньшей мере одну область локального порядка.
Массив может быть сформирован на поверхности подложки различными способами. Массив более высокого порядка может быть сформирован путем осаждения экзосом-связывающих лигандов в точных положениях на поверхности подложки. Примеры включают кристаллический кремний, керамические или полимерные поверхности с применением литографии, плазменной ионной имплантации способом погружения и осаждения (Plll&D), атомно-силового микроскопа, лазера, электрического травления, реактивного ионного травления плазмой малой плотности, мокрого травления, электронного микроскопа или других средств, известных для получения функционализированной поверхности, содержащей экзосом-связывающие лиганды.
В другом варианте осуществления массив может быть напечатан на поверхности подложки. Примеры включают функционализацию поверхности подложки с помощью химической прокладки, а затем дальнейшую дериватизацию таких прокладок с помощью фрагментов экзосом-связывающих лигандов, которые теперь химически связаны с такими прокладками.
В другом варианте осуществления массив обеспечивают на поверхности подложки одним или более полимерами, которые включают экзосом-связывающие лиганды. В этом варианте осуществления подложка может быть сформирована как единое целое из полимера, с образованием поверхности подложки. Дополнительно или альтернативно, полимер может быть соединен или иным образом связан с подложкой, с образованием поверхности подложки, например, посредством связывания биотина/стрептавидина.
В вариантах осуществления, где подложка образована из полимера, поверхность подложки может быть обработана так, чтобы активировать этот полимер для образования экзосом-связывающих лигандов на полимере.
В других вариантах осуществления полимер, включающий экзосом-связывающие лиганды, наносят на подложку в качестве покрытия с образованием экзосом-связывающих лигандов на поверхности подложки.
Как указано выше и подробно описано далее в настоящем документе, в случае, когда экзосом-связывающие лиганды должны быть обеспечены в массиве одним или более полимерами, такие полимеры выбирают в зависимости от того, расположены ли представленные ими лиганды, наблюдаемые in silico, на расстоянии более 2 Å друг от друга и не более приблизительно 10 Å друг от друга, предпочтительно от 3,5 до 6 Å или от 4 до 6 Å друг от друга, при самой низкой энергии. Вкратце, наблюдение in silico получают, подвергая субструктурную единицу (обычно от гексамера до додекамера, но могут быть и более крупные размеры) полимера, имеющего анионные или богатые электронами группы, вычислениям минимизации энергии (алгоритм MM+) для того, чтобы отобразить наиболее стабильную (с самой низкой энергией) трехмерную структуру, и, следовательно, структуру, с большей вероятностью участвующую в связывании экзосом. Расстояние между лигандами затем может быть измерено in silico для определения вероятности связывания с экзосомами. Когда минимизированная по энергии структура смоделированного олигомера содержит подходящее количество пар лигандов, в которых пары богатых электронами или анионных лигандов разделены на расстоянии от 2 до 10 Å, тогда полимер, который представляет этот смоделированный олигомер, будет подходящим для связывания экзосом или микровезикул по настоящему изобретению.
Таким образом, в другом варианте осуществления обеспечен способ получения композиции или изолята экзосом или микровезикул. Способ включает следующие стадии:
- обеспечение жидкости, включающей экзосомы или микровезикулы;
- обеспечение подложки, имеющей поверхность, причем поверхность имеет массив экзосом-связывающих лигандов;
- где каждый лиганд находится в форме анионной или богатой электронами группы; и
- где массив экзосом-связывающих лигандов позволяет экзосомам связываться с подложкой;
- взаимодействие жидкости с подложкой в условиях, обеспечивающих связывание экзосом или микровезикул с экзосом-связывающими лигандами;
- отделение подложки от жидкости;
с получением композиции или изолята экзосом или микровезикул,
где экзосом-связывающие лиганды, наблюдаемые in silico, находятся на расстоянии более 2 Å и не более приблизительно 10 Å друг от друга, предпочтительно от 3,5 до 6 Å, предпочтительно от 4 до 6 Å друг от друга в модели минимизации энергии, как описано в настоящем документе.
Упорядоченность массива, образованного из экзосом-связывающих лигандов, обеспеченных одним или более полимерами, обычно зависит от гетерогенности полимеров в отношении порядка мономеров в каждом полимере и длины каждого полимера. Предпочтительно, полимеры для применения в настоящем изобретении имеют небольшую гетерогенность или, иначе, более или менее гомогенны в отношении порядка мономеров и длины полимера. Предпочтительно полимеры являются линейными.
В этом отношении предпочтительными являются синтетические полимеры, а не полимеры, полученные из природных или биологических источников. Это связано с тем, что полимеры из биологических источников, таких как определенные полисахариды, имеют значительную гетерогенность в отношении длины полимера, разветвлений, порядка мономеров или даже функционализации мономеров. Как описано в настоящем документе, такая гетерогенность обычно способствует снижению эффективности связывания экзосом или микровезикул и более низкому выходу экзосом или микровезикул. Следовательно, в одном варианте осуществления полимер не является нефракционированным или гетерогенным из природного или биологического источника, в частности, гепарином.
Более предпочтительно, касательно содержания мономеров, полимеры имеют однородный порядок мономеров, особенно когда полимер содержит различные типы мономеров, и где только некоторые типы мономеров содержат экзосом-связывающие лиганды. Особенно важно, что однородность порядка мономеров создает однородность в отдалении друг от друга экзосом-связывающих лигандов, которые обращены к внешней поверхности мембраны экзосомы или микровезикулы. Это обычно требует наличия однородной стереохимии экзосом-связывающих лигандов для взаимодействия с экзосомами или микровезикулами.
Предпочтительно, чтобы по меньшей мере 25% мономеров, образующих полимер, предпочтительно 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% мономеров, образующих полимер, имели экзосом-связывающий лиганд, который расположен на поверхности подложки для обеспечения возможности связывания с внешней мембраной экзосомы или микровезикулы.
Особенно предпочтительно, чтобы все мономеры, образующие полимер, содержали экзосом-связывающие лиганды, расположенные на расстоянии приблизительно от 3,5 до 6 Å, от 4 до 6 Å, предпочтительно 3,5, 4, 5 или 6 Å друг от друга, обращенные к внешней поверхности мембраны экзосомы или микровезикулы.
В определенных вариантах осуществления, где полимер состоит из более чем одного типа мономера, один тип может обеспечивать один тип экзосом-связывающего лиганда, а другой тип мономера может обеспечивать другой тип экзосом-связывающего лиганда.
Кроме того, в зависимости от длины типа мономера, тип мономера может обеспечивать более чем один экзосом-связывающий лиганд (который может быть одинаковым или различным) при условии, что лиганды, обеспечиваемые типом мономера, при их обращении к внешней поверхности экзосомы или микровезикулы, расположены на расстоянии приблизительно от 3,5 до 6 Å или от 4 до 6 Å, предпочтительно 3,5, 4, 5 или 6 Å друг от друга.
Авторами настоящего изобретения неожиданно было обнаружено, что экзосомы и микровезикулы могут быть отделены от других компонентов биологической жидкости, образованной in vivo или in vitro, на основе заряда и, в частности, положительного заряда на экзосоме или микровезикуле. Это неожиданно, поскольку в целом понималось, что большинство клеточных мембран и липидных бислоев имеют суммарный отрицательный заряд, в частности возникающий из-за групп полярных головок липидных молекул, мембранных сахаров и белков, которые обычно отрицательно заряжены при физиологическом pH.
Экзосом-связывающий лиганд, применяемый в вышеописанных вариантах осуществления, находится в форме или состоит из аниона или богатой электронами группы. Экзосомы обычно стабильны при физиологическом значении pH 7,4 плюс-минус 1-1,5. Следовательно, экзосом-связывающий лиганд, как правило, представляет собой анион или в других случаях богатую электронами группу, при значении рН приблизительно от 4 до 8 или от 5 до 8.
Экзосом-связывающий лиганд может представлять собой неорганический или органический анион, или богатую электронами группу. Примеры неорганических анионов включают анионы, которые содержат атом серы, селена, бора, азота или фосфора и включают сульфаты, селенаты, фосфаты, фосфонаты, фосфинаты.
Предпочтительно лиганд представляет собой органический анион или богатую электронами группу. Примеры включают сульфатированные спирты и амины, амиды, сульфонамиды, карбоксилатные группы, спирты, простые эфиры, ангидриды, селенаты, имиды, ацилсульфонамиды, фосфонаты, фосфинаты, фосфаты и т.д.
В одном варианте осуществления массив экзосом-связывающих лигандов по изобретению может представлять собой комбинацию органических и неорганических анионов или богатых электронами групп.
Важным открытием настоящего изобретения, как описано в данном документе, является то, что, при применении полимера для обеспечения массива экзосом-связывающих лигандов, полимер выбирают на основе его способности обращать или представлять равномерно раcположенное множество экзосом-связывающих лигандов к внешней поверхности мембраны микровезикулы, а не на основе какой-либо другой характеристики основной цепи полимера. В этом отношении настоящее изобретение отличается от других подходов, раскрытых ранее, в которых применяют полимеры для осаждения микровезикул из раствора. В таких подходах обычно выбирают полимеры на основе характеристик растворимости в воде и объема эксклюзии. Типичные полимеры, применяемые в этих подходах, представляют собой полиэтиленгликоль [US2013/0273554 и US2013/0337440] и полисахариды [US20150192571].
Согласно настоящему изобретению, полимер может представлять собой полисахарид, полиэтилентерефталат или пептид с боковыми цепями, подходящие для получения производных с анионными или богатыми электронами группами, такими как полиаспарагиновая кислота, полисерин, политреонин, полиаспарагин, нуклеиновая кислота или другие органические молекулы, такие как простые полиэфиры, полиэтилен-гликоли (PEGS), сульфатированные поливиниловые спирты, полифенолы, полифенилбороновые кислоты или другие полиароматические или полигетероароматические соединения, предпочтительно синтетические.
В вариантах осуществления, где полимер получают из природного или биологического источника, и известно, что полимер обладает значительной зависимой от источника гетерогенностью, особенно в отношении длины полимера, содержания и порядка мономеров, особенно предпочтительно фракционировать природный или биологический источник, чтобы уменьшить гетерогенность и увеличить гомогенность для полимера желаемой длины, содержания или порядка мономеров.
Обычно полимер имеет молекулярную массу от 10 до 900 кДа, предпочтительно от 20 до 50 кДа для определенных полисахаридов, таких как гепарин, или от 100 до 200 кДа для некоторых других молекул, например, хитозана.
Особенно предпочтительные полимеры представляют собой синтетические или гомогенные природные или биологические источники полисахаридов, выбранные из группы пираноз, где мономеры включают (но не ограничиваются ими) декстрозу, глюкозу, галактозу, глюкозамин, галактозамин, маннозу, рибозу, арабинозу, ксилозу, ликсозу, и аминосахариды и тому подобное.
Полимеры могут быть обеспечены в форме пептидов. Особенно предпочтительный пептид представляет собой полиаспарагиновую кислоту. Как описано в настоящем документе, полиглутаминовая кислота может быть менее предпочтительной, учитывая, что расстояние между анионными боковыми цепями превышает предпочтительный диапазон изобретения, составляющий от 4 до 6 Å. Другие предпочтительные пептиды включают полисерин, политреонин, полиаспарагин, полицистеиновую кислоту, полиселеноцистеиновую кислоту и D-конфигурации их аминокислот.
Основная цепь полимера может быть водорастворимой или нерастворимой.
В особенно предпочтительном варианте осуществления полимер содержит один тип мономера, имеющий длину, приблизительно равную длине глюкозного мономера (приблизительно 1,5 нм), или представляет собой глюкозный мономер или его производное, длиной приблизительно 1,5 нм, и где каждый мономер включает анионную или богатую электронами группу, расположенную так, что каждая группа разнесена на расстоянии от приблизительно 4 до 5 Å, и где полимер содержит от приблизительно 100 до 400 мономеров, предпочтительно от приблизительно 250 до 300 мономеров, и/или имеет молекулярную массу от приблизительно 40 до 60 кДа, предпочтительно от приблизительно 45 до 55 кДа.
В предпочтительном варианте осуществления изобретения полимер представляет собой линейную молекулу целлюлозы, где каждый мономер, предназначенный для обращения к внешней поверхности мембраны экзосомы, функционализирован анионной группой или богатой электронами группой, предпочтительно сульфатной группой.
Нет необходимости, чтобы вся поверхность подложки была покрыта или содержала массив экзосом-связывающих лигандов. В одном варианте осуществления подложка состоит из области связывания экзосом или микровезикул, имеющей массив экзосом-связывающих лигандов в области, чтобы обеспечить связывание экзосомам или микровезикулам с областью связывания. Другие поверхности подложки могут быть сконструированы так, чтобы исключить связывание экзосом. Например, такие "не связывающие" области могут быть сконструированы таким образом, чтобы при применении они не обращали экзосом-связывающих лигандов к экзосомам или микровезикулам. Такое расположение областей связывания и несвязывания экзосом может быть полезным при создании устройств для получения, обнаружения или мониторинга экзосом. Такие устройства могут включать микрофлюидные устройства или более крупные устройства для культивирования клеток или медицинские устройства для клинического применения.
Подложка может иметь разные формы или конфигурации.
Поверхность подложки может быть плоской, изогнутой, с выемками или пористой. Поверхность может быть сформирована внутри устройства, трубы или лунки, или на грануле.
В одном варианте осуществления поверхность подложки приводят в связь с одним или более датчиками для определения наличия, свойств или размера экзосом или микровезикул, связанных с такой подложкой, с применением подходящих нанотехнологических аналитических способов, таких как атомно-силовая микроскопия, просвечивающая электронная микроскопия (ПЭМ), Оже-эмиссионная спектрометрия (AES), лазерная масс-спектрометрия, рентгеновская фотонная спектроскопия.
В другом варианте осуществления поверхность подложки сообщается со средством измерения для определения полезных параметров комбинации экзосома-подложка (или микровезикула-подложка), таких как один или более из (i) наличие или отсутствие экзосомы (и, следовательно, количества и плотности экзосом) (ii) размер экзосомы (iii) проводимость экзосомы (iv) поверхностный маркер экзосомы (v) жесткость экзосомы (vi) заряд экзосомы или (vii) какой-либо другой полезный параметр, с помощью таких средств, как одно или более из (а) электрические зонды, (b) встроенный лазер (c) электросиловая микроскопия (d) магнитно-силовая микроскопия (e) сканирующая затворная микроскопия или другие подходящие способы. Подложка может формировать средства измерения.
В способе по изобретению применяют подложки и экзосом-связывающие лиганды, как определено выше, для выделения микровезикул, в частности экзосом, из биологического источника на основе заряда. Как описано выше, авторами изобретения было неожиданно обнаружено, что экзосомы и микровезикулы могут быть отделены от других компонентов биологической жидкости на основе заряда и, в частности, на основе положительного заряда экзосомы или микровезикулы. На основании этого открытия авторы применяли способ ионообменной хроматографии для выделения экзосом и микровезикул.
Согласно настоящему изобретению жидкость, содержащая экзосомы или микровезикулы, взаимодействует с подложкой в условиях, обеспечивающих связывание экзосом или микровезикул в жидкости с экзосом-связывающими лигандами. Затем происходит связывание экзосом или микровезикул с подложкой, которая является основой для последующего отделения экзосом или микровезикул от жидкости, как результат отделения подложки от жидкости.
Условия для обеспечения возможности связывания экзосом или микровезикул с экзосом-связывающими лигандами обычно требуют учета содержания соли и значения pH жидкости, содержащей экзосомы или микровезикулы. Обычно значение pH жидкости определяется значением pH, при котором экзосомы или микровезикулы стабильны, и этот диапазон стабильности pH составляет приблизительно от 4 до 8.
В некоторых вариантах осуществления жидкость, содержащая экзосомы или микровезикулы, может быть предварительно обработана перед взаимодействием с подложкой. Такая обработка может включать, например, регулировку рН для оптимизации взаимодействия связывания с экзосом-связывающими лигандами. Например, может потребоваться отрегулировать рН раствора до физиологического уровня рН от 7,2 до 7,4. Это гарантирует, что фрагменты на экзосомах или микровезикулах, связываемые экзосом-связывающими лигандами, являются катионными и способны связываться с анионами или другими богатыми электронами группами экзосом-связывающих лигандов.
Обработка может также включать регулировку уровня соли, потенциально минимизацию содержания соли в жидкости, например, путем проведения стадии диализа, перед взаимодействием жидкости с подложкой.
Обычно значение рН жидкости, содержащей экзосомы или микровезикулы, составляет от 7,2 до 7,4 и содержание соли в ней составляет от 0,1 до 0,5 М, предпочтительно 0,15 М, и содержание фосфатов в ней составляет 0,01 М до взаимодействия с подложкой.
Для удаления клеточного дебриса или загрязнения, которое может помешать связыванию экзосом или микровезикул с экзосом-связывающими лигандами, может потребоваться дальнейшая обработка. Данная обработка может включать центрифугирование при 500 g с фильтрацией или без нее до приблизительно 0,22 мкм.
В одном варианте осуществления жидкость может быть в форме биологической жидкости, которую центрифугируют для образования супернатанта и осадка, содержащего микровезикулы, при этом супернатант отбрасывают, и осадок ресуспендируют в буфере для ионообменного связывания для взаимодействия с подложкой. Значение рН такого буфера обычно составляет от 7,2 от 7,4, и содержание соли в нем составляет от 0,1 до 0,2 М.
Для удаления микровезикул определенного размера из жидкости до взаимодействия жидкости с подложкой также можно применять фильтрацию. Например, жидкость можно фракционировать для удаления экзосом диаметром более 100 нм до взаимодействия жидкости с подложкой. Альтернативно, данную стадию можно выполнить по завершении элюирования микровезикул из экзосом-связывающих лигандов (как описано далее ниже).
Жидкость и подложку приводят во взаимодействие в течение времени, достаточного для того, чтобы позволить экзосомам связаться с экзосом-связывающими лигандами. Обычно данный период времени составляет от 1 минуты до 16 часов и может длиться приблизительно 15 минут. Он может составлять менее 1 минуты, например, менее 30 секунд.
Взаимодействие жидкости с подложкой может быть установлено во множестве форматов. Например, жидкость может быть перколирована через твердую смолу или гранулы, захвачена, а затем цикл перколяции и захвата повторяют в течение предварительно определенного числа циклов.
Как обсуждалось выше, особое преимущество настоящего изобретения заключается в том, что между заряженными полимерами (особенно полученными из природных источников и имеющими присущую гетерогенность) существует несоответствие в отношении их способности связываться с экзосомами или микровезикулами, и что можно добиться значительного улучшения эффективности связывания путем разумного выбора подложек или полимеров в соответствии с настоящим изобретением. В частности, в работе, описанной в настоящем документе, авторами изобретения показано, что полимеры, которые, возможно, в другом случае могли бы считаться одинаково эффективными для связывания экзосом или микровезикул, поскольку все они имеют отрицательный заряд при физиологическом рН, в действительности имеют различные уровни эффективности и что различные уровни эффективности связывания можно объяснить расположением отрицательных зарядов, обращенных к внешней поверхности мембраны экзосомы или микровезикулы.
В частности, как описано в настоящем документе, авторами настоящего изобретения определено, что общий выход выделения, который возникает главным образом из-за различий в теоретической эффективности связывания, составляет от приблизительно 4,3% (как наблюдается для гиалуроновой кислоты) до вплоть до 98% (как наблюдается для Целлуфин сульфата). Кроме того, путем определения структурной модели и модели связывания для полимеров, тестируемых на эффективность связывания, различия в эффективности связывания были объяснены с точки зрения расположения анионных и богатых электронами групп, обращенных к внешней поверхности мембраны экзосомы, что позволяет выбирать оптимальные подложки или полимеры для связывания экзосом, и, в частности, те, которые с большей вероятностью обеспечивают более высокую эффективность связывания.
Проведя эту работу с обеспечением способа выделения экзосом или микровезикул, изобретение обеспечивает более широкий диапазон вариантов связывания, чем могло бы быть применено для получения приемлемого выхода экзосом или микровезикул. Это особенно полезно в тех случаях, когда существуют ограничения в отношении значения pH или условий содержания соли в буфере для связывания.
Кроме того, изобретение обеспечивает более эффективный способ связывания, потенциально допускающий более короткие периоды связывания или допускающий меньшее количество циклов связывания там, где в противном случае потребовалось бы несколько циклов связывания. Такие улучшения позволяют уверенно переносить ионообменный способ выделения экзосом или микровезикул на обработку с высокой пропускной способностью, что в конечном итоге потребует производства, позволяющего производить экзосомы в фармацевтическом масштабе.
Конечной стадией фазы связывания способа, как указывалось выше, является отделение подложки от жидкости, тем самым отделяя экзосомы (которые связаны с экзосом-связывающими лигандами на подложке) от жидкости. Это разделение может быть достигнуто активно, путем удаления подложки из жидкости (например, путем центрифугирования подложки в форме гранул) или пассивно, путем пропускания жидкости через подложку (с извлечением экзосом из жидкости, когда жидкость отделяется от подложки).
Особенно важным преимуществом изобретения является то, что оно позволяет элюировать экзосомы и/или микровезикулы из биологического источника с получением элюата, состоящего в основном из экзосом и/или микровезикул и элюирующего буфера. Это особенно важно для регулирования контроля качества конечного продукта. Для сравнения, на сегодняшний день другие способы выделения экзосом приводят к тому, что экзосома очищается с помощью осаждающего агента, например, в форме полиэтиленгликоля или полисахарида или его фрагмента, вместе с ферментом для разложения полисахарида. Эти способы требуют дальнейших действий с конечным продуктом для удаления данных загрязнений, и такая дополнительная стадия, например, центрифугирование или фильтрация, может негативно влиять на экзосомы.
Авторами изобретения было неожиданно обнаружено, что экзосомы и микровезикулы, которые связываются с подложками по изобретению посредством взаимодействий с более высокой аффинностью или более высокой авидностью, могут быть равномерно элюированы из экзосом-связывающих лигандов, обеспечивая высвобождение экзосом из лигандов. В частности, как описано в данном документе, было обнаружено, что выбранные, но не связанные между собой подложки, а именно Целлуфин сульфат, хитозан и сополимер метилвинилового эфира и малеинового ангидрида, обладают улучшенной эффективностью связывания экзосом, и связанные с ними экзосомы можно элюировать обычным способом с применением элюирующих буферов, имеющих диапазон концентраций соли или интервалы рН, в пределах которых экзосомы остаются стабильными.
Таким образом, в одном варианте осуществления способ включает дополнительную стадию элюирования экзосом или микровезикул из экзосом-связывающих лигандов для высвобождения экзосом или микровезикул с подложки после отделения подложки от жидкости.
Согласно изобретению экзосомы или микровезикулы могут быть элюированы путем взаимодействия подложки с элюирующим буфером. Обычно содержание соли в элюирующем буфере составляет от приблизительно 0,5 до 4 М или от 0,5 до 2 М, в зависимости от рН буферной системы. При этом содержании соли обеспечивается избирательное связывание между анионными компонентами в буфере для элюирования и внешней мембраной экзосомы или микровезикулы, что приводит к элюированию.
В других вариантах осуществления содержание соли в элюирующем буфере может быть таким же, как в буфере для связывания, и элюирующий буфер может иметь более высокий рН, чем буфер для связывания. Это приводит к элюированию экзосом или микровезикул из экзосом-связывающих лигандов, когда рН буферной системы приближается к изоэлектрической точке фрагментов на экзосоме или микровезикуле, которые связываются с экзосом-связывающими лигандами. Таким образом, в одном варианте осуществления содержание соли в элюирующем буфере составляет от приблизительно 0,5 до 2 М и значение рН составляет приблизительно от 7,2 до 7,4.
В другом варианте осуществления элюирующий буфер может включать олигомеры полимера, образующего поверхность подложки, причем указанные олигомеры имеют более высокий анионный заряд или более высокий электрический потенциал, чем экзосом-связывающие лиганды на полимере, что приводит к элюированию экзосом или микровезикул. Например, когда экзосом-связывающие лиганды представлены на поверхности подложки в форме полисахарида сульфата целлюлозы, элюирующий буфер может включать олигомеры целлюлозы с более короткой цепью, имеющие более высокую степень сульфатирования.
В другом варианте осуществления элюирующий буфер может включать конкурентный лиганд, который имеет более высокую аффинность к экзосоме или микровезикуле, чем экзосом-связывающий лиганд на подложке. Например, экзосома может быть элюирована из полимера борной кислоты с помощью элюирующего буфера, содержащего избыток сахара, предпочтительно фруктозы, которая имеет более высокую аффинность к экзосомам, чем борная кислота, тем самым элюируя экзосомы с подложки.
В одном варианте осуществления элюирующий буфер наносят на подложку только один раз. В других вариантах осуществления элюирующий буфер можно непрерывно циклически применять в течение заранее определенного количества циклов.
В одном варианте осуществления способ может включать дополнительную стадию отделения высвобожденных экзосом или микровезикул от подложки. Данная стадия особенно необходима, когда экзосомы или микровезикулы остаются в растворе с подложкой по завершении элюирования. В одном примере экзосомы или микровезикулы элюируют из экзосом-связывающих лигандов, расположенных на подложке в форме гранулы, и гранулу необходимо отделить от высвобожденных экзосом или микровезикул. В других вариантах осуществления физическое разделение может происходить просто вследствие того, что экзосомы элюируются с подложки, как, например, может происходить при колоночной хроматографии.
Ясно, что изобретение, раскрытое и определенное в настоящем описании, распространяется на все альтернативные комбинации двух или более отдельных признаков, упомянутых или очевидных из текста или графических материалов. Все эти различные комбинации составляют различные альтернативные аспекты изобретения.
Примеры
Пример 1 – Выделение экзосом с применением подложек на полимерной основе
1.1 Испытуемый материал
Применяемый испытуемый материал представлял собой кондиционированную среду для культивирования клеток, полученную из нейрональной клеточной линии гипоталамуса мыши GT 1-7, культивируемой в полной культуральной среде Opti-MEM (среда с пониженным содержанием сыворотки Opti-MEM® + 10% обедненная экзосомами эмбриональная телячья сыворотка + пенициллин-стрептомицин + GlutaMAX) в течение от 48 до 72 часов.
1.2 Способ испытания
Свежесобранную кондиционированную среду для культивирования клеток центрифугировали (500 × g в течение 5 минут), чтобы удалить клетки и крупный дебрис, затем супернатант фильтровали с применением шприцевого фильтра 0,22 мкм для удаления крупных везикул и апоптотических тел. В отфильтрованной кондиционированной среде количественно определяли концентрацию частиц с применением анализа траектории наночастиц (NTA) на приборе NanoSight NS300.
В таблице 1 описан набор подложек на основе полимера, для которого были определены эффективность связывания и элюирования и общие выходы выделения.
Хитозан представлял собой 200 кДа (Биотин-) Хитозан (изготовленный на заказ). Гранулы Viroadem представляли собой Viro-Adembeads от производителя Ademtech. Superdex® 75 предоставлен компанией Sigma Aldrich #S6657. Магнитные носители BA-Magbeads были получены от Chemicell 1504-5 магнитные частицы SiMAG-Boronic Acid. ПЭГ-контроль: биотин-ПЭГ24 (в качестве контроля для 3-APBA/4-APBA, которые, строго говоря, представляют собой биотин-ПЭГ24-3APBA и биотин-ПЭГ24-4APBA (изготовлены на заказ). Контроль магнитных носителей предоставлен Spherotech SVM-40-10 магнитные частицы, покрытые авидином. Применяли набор Norgen Biotek Cell Culture Media Exosome Purification Kit (#60600). Хитозан, гепарин, 3-APBA, 4-APBA, контроль ПЭГ и гиалуроновая кислота представляли собой биотин-X, связанный с магнитными частицами, покрытыми авидином Spherotech SVM-40-10.
Лиганд, иммобилизованный на подложке в оптимизированной концентрации, инкубировали с 1 мл испытуемого материала, прошедшего количественное определение, в течение 5 часов при 4 °С на цилиндрическом вращателе (100 об/мин), чтобы проверить аффинность захвата экзосом. Твердую подложку с иммобилизованными лигандами отделяли после инкубации, и концентрацию частиц определяли в растворе после захвата (несвязанные экзосомы) с применением анализа NTA на приборе NanoSight NS300. Отделенную твердую подложку с иммобилизованными лигандами, связанную с экзосомами, инкубировали в элюирующем растворе в течение ночи при 4 °С на цилиндрическом вращателе (100 об/мин) для элюирования связанных экзосом. Твердую подложку с иммобилизованными лигандами отделяли после инкубации и определяли концентрацию частиц в растворе с применением анализа NTA на приборе NanoSight NS300.
1.3 Сбор данных
Концентрацию частиц определяли с применением анализа NTA на приборе NanoSight NS300. Стратегия сбора данных заключалась в том, чтобы получить 5 30-секундных видеозаписей в статическом режиме. Затем с помощью программного обеспечения NanoSight проанализировали 5 независимых 30-секундных видеозаписей для подготовки экспериментального отчета с данными о средней (плюс-минус стандартная ошибка) концентрации частиц.
1.4 Результаты испытания
Авторы измеряли концентрацию частиц на трех экспериментальных стадиях
(i) Преаффинное разделение (то есть концентрация частиц в испытуемом материале перед захватом)
(ii) Постаффинный захват в растворе (т.е. концентрация частиц в испытуемом материале после захвата, представляющая несвязанные экзосомы)
(iii) Постэлюирование (то есть концентрация частиц в растворе после элюирования захваченных лигандами частиц)
1.5 Способы анализа данных
Полученные результаты испытаний применяли для определения четырех параметров:
• эффективность связывания лиганда (то есть количество частиц в испытуемом материале, захваченных воздействием твердой подложки с иммобилизованными лигандами)
• эффективность элюирования лиганда (т.е. доля элюированных захваченных лигандами частиц)
• общий выход способа
1.6. Результаты
В оптимизированных условиях связывания лиганд сульфата целлюлозы в форме Целлуфин сульфата показал теоретическую эффективность связывания 77,90% при количестве теоретически связанных частиц, равном 1,31 × 1010 (таблица 1). Количество частиц, извлеченных после элюирования из гранул Целлуфин сульфата, составляло 1,64 × 1010 при количественном определении эффективности элюирования с помощью прибора на уровне 125% (таблица 1). Общий выход способа для лиганда Целлуфин сульфата составил 98% (таблица 1). Необходимо отметить, что эффективность элюирования 125% была подвержена различным отклонениям количественных данных вследствие эксплуатационных и других факторов. Можно было бы ожидать, что фактическая эффективность элюирования снизится до менее 100%.
Гранулы Viroadembead продемонстрировали теоретическую эффективность связывания 66,13% при количестве теоретически связанных частиц, равном 1,11 × 1010 (табл. 1). В тестируемых условиях элюирования авторам удалось элюировать 41% частиц, захваченных гранулами Viroadembead, со средним размером 232,4 нм (таблица 1). Общий выход способа для гранул Viroadembead составил 27% (Таблица 1).
Неожиданно, общий выход выделения частиц для выделения экзосом на основе ультрацентрифугирования составил 7,5% (таблица 1). Этот выход был значительно ниже по сравнению с общим выходом выделения, наблюдаемым с лигандами, описанными в наятоящем изобретении. Nordin и соавт. сообщили, что выход экзосом с помощью ультрацентрифугирования составляет 10% (Nordin et al., 2015). Кроме того, из 4 л культуральной среды, полученной из жировых стволовых клеток, было получено 0,9 мг экзосом с помощью ультрацентрифугирования, для чего потребовалось 23 л культуральной среды и обработка в течение от 276 до 280 часов для получения однократной дозы для человека, которая, в большинстве случаев, составляет 5 мг. Для сравнения, лиганд по настоящему изобретению с выходом экзосом 80% может давать однократную дозу для человека 5 мг из менее чем 4 л СМ, полученных из жировых стволовых клеток, с более коротким временем обработки, при обработке в режиме хроматографии. Это дополнительно подчеркивает преимущество лигандов по настоящему изобретению для выделения экзосом по сравнению с существующим золотым стандартом выделения методом ультрацентрифугирования.
Пример 2 - Определение структурно-функциональной модели способом EMIT
Для определения вероятности оптимального связывания экзосом с различными функционализированными полимерами применяли протокол минимизации энергии in silico. Олигомер, представляющий часть полимера, размер которого может варьироваться от гексамера до додекамера, был нарисован с применением правильной стереохимической конфигурации лигандов, известной, например, как в случае хитозана или Целлуфин сульфата, или определяемой, например, как в случае полиаспарагиновой кислоты. Если конфигурация была случайной или неизвестной, например, как в случае сополимера метилвинилового эфира и малеинового ангидрида, то применяли случайную олигомерную структуру без изменений. Затем структуры подвергали вычислениям минимизации энергии (MM+ или модель молекулярной механики AMBER, HyperChem версия 7,5) с применением убывающей функции Полака-Райбера. Количество вычислительных итераций, необходимых для определения минимума энергии, обычно составляло от 1000 до 2000, но если минимум энергии не был достигнут, вычислению было разрешено продолжаться до тех пор, пока не будет достигнут такой минимум. В этот момент расположение рассматривали с нескольких точек зрения, и положение лигандов оценивали по взаимному расстоянию между, например, атомами серы в случае сульфатированных полисахаридов или ангидридными карбонильными кислородами в случае сополимера метилвинилового эфира и малеинового ангидрида. Вторичная структура полимера в этих случаях иллюстрирует расположение основной цепи, состоящей из 6-12 мономерных звеньев, в форму спирали, на которой связывающие фрагменты выступают наружу. Следует понимать, что эти вычисления минимизации энергии представляют дробные части полимеров, а не полимеры в целом, как вследствие ограничений программного обеспечения/обработки, так и из-за любой изменчивости общего размера полимера. Кроме того, вычисления типа MM+/AMBER проводят в отсутствие сольватирующих молекул, таких как вода или другие компоненты, которые могут встречаться в условиях in vivo или на практике. Поскольку такие вычисления действительно выполняются только в отношении самих олигомеров, функционализированных лигандом, данный способ устраняет несоответствия и непредсказуемые компоненты, которые будут присутствовать в более сложных средах, и, таким образом, его можно считать внутренне согласованным. Кроме того, полученные результаты, с расстоянием между лигандами в минимизированных структурах, демонстрируют тенденцию, соответствующую наблюдениям эффективности связывания экзосом.
Пример 3 - Спроектированные структуры Целлуфин сульфата и Целлуфин фосфата
Целлуфин сульфат представляет собой синтетически полученную частицу сульфата целлюлозы, коммерчески доступную как Целлуфин сульфат (JNC Corporation, Япония). Способ синтеза препарата Целлуфин сульфата раскрыт в патенте EP0171086 A2. Вкратце, несшитые частицы целлюлозы получали из полимера глюкозы, полученного из 250-300 единиц глюкозы, в качестве необработанного полимера. Частицы целлюлозы затем сульфатировали с применением сульфатных реагентов до полученных гранул сульфата целлюлозы (Целлуфин сульфата). Общее содержание серы на частицах составляет 900 мкг/г сухой массы.
Модель гептамера Целлуфин сульфата сведена к минимуму, как показано (фиг. 1(A) и 1(B)), в торцевой и боковой проекции, с выборочными измерениями атомных расстояний в образце между соседними атомами сульфатного кислорода. Сульфатные фрагменты (от измеренной серы до соседней серы) находятся на расстоянии приблизительно от 6,7 до 7,9 Å, при этом заряженные атомы кислорода способны перемещаться в пределах 4,5 Å (как указано на боковой проекции). Эта модель позволяет предположить, что для связывания экзосом должен быть достаточный зазор (проекция наружу из спирали) и способность к образованию водородных связей, например, между спиртовой группой и анионным или нейтральным, богатым электронами кислородом. Следовательно, поверхностные молекулы экзосом, с которыми лиганды образуют водородные связи, вероятно, являются донорами водородных связей, такими как спирты, такими как гликоли в составе фосфолипидов или других основных компонентов клеточных мембран. В этом случае первичная спиртовая группа (CH2OH) проецируется между двумя анионными группами, такими как сульфаты, образуя клешневидную сеть водородных связей, где атом водорода спирта может взаимодействовать с двумя атомами кислорода одновременно. Вырожденная природа сульфатных атомов кислорода означает, что вероятность взаимодействия выше (три на сульфат, шесть в общей сложности на пару сульфатов) и, таким образом, увеличивается прочность сети водородных связей для связывания. См. фиг. 1 (A) и (B).
Целлуфин фосфат, аналогично, является синтетически полученной частицей фосфата целлюлозы. Он также коммерчески доступен как Целлуфин фосфат (JNC Corporation, Япония).
На фиг. 1(C) и (D) приведены торцевые и боковые проекции спиральной структуры модели, представленной в качестве додекамера для иллюстративных целей. Модель указывает на частично заряженную природу фосфатных групп (CH2OP(O)(OH)2) в виде моноанионов, фактически (CH2OP(O)(OH)O-, в соответствии с диапазоном pH ожидаемого связывания. В этом случае, так же, как и для Целлуфин сульфата, первичную спиртовую группу (CH2OH) проецируют между анионными фосфатами с образованием клешневидной сети водородных связей. Атом водорода спирта может взаимодействовать с двумя атомами кислорода одновременно. Вырожденная природа фосфатных атомов кислорода аналогична природе сульфатных атомов кислорода, хотя зависимость степени протонирования фосфата от рН будет определять вероятность взаимодействия. Как показано на фиг. 1(C) и 1(D), два атома кислорода являются вырожденными и увеличивают прочность сети водородных связей для связывания.
Пример 4 - Спроектированная структура сополимера метилвинилового эфира и малеинового ангидрида
Анионный полимер, сопополимер метилвинилового эфира и малеинового ангидрида (поли(MVE-MA)), коммерчески доступен как Viroadembeads (Ademtech, Франция). Краткий способ получения Viroadembeads описан ниже (Sakudo et al., 2009b). Небольшие (300 нм в диаметре) монозидные магнитные частицы (снижающие седиментацию и обеспечивающие широкую поверхность) с высоким содержанием феррита (позволяющим разделить поверхность под магнитным полем), полученные прививкой поли(MVE-MA) в растворе диметилсульфоксида (ДМСО)/фосфатный буфер 5/95 в течение 3 часов при 37 °С.
В случае сополимера метилвинилового эфира и малеинового ангидрида (поли(MVE-MA)) стереохимия замещения как на фурандионе так и в метокси-замещениях основной цепи является случайной и неопределенной. Для получения минимизированной по энергии структуры применяли однородную и постоянную стереохимическую конфигурацию, в результате чего получали листовую структуру, где чередующиеся фрагменты фурандиона направлены от основной цепи. Расстояние между соседними карбонилами, которые вместе могут действовать как акцепторы водородных связей для взаимодействия с фосфолипидами, составляет приблизительно 4,4 Å. См. фиг. 3.
Пример 5 - Спроектированная структура хитозана
Хитозан, природный полисахарид, получаемый в результате N-деацетилирования хитина, содержит от 60 до 100% N-деацетилированных моносахаридных звеньев. Минимизированная по энергии структура хитозана образует спираль с аминогруппами, расположенными по направлению к внутренней стороне и спиртовыми фрагментами, проецируемыми наружу из спирали, как показано ниже, на торцевой проекции. Боковая проекция иллюстрирует положение соседних первичных спиртовых групп, предложенных в данном документе как связывающие фрагменты, способные взаимодействовать с фосфолипидом экзосом. Они находятся на расстоянии приблизительно от 4,6 до 5,0 Å друг от друга, при расположении по внешней части спирали. См. фиг. 2А и 2В.
Пример 6 - Спроектированная структура гепарина
Гепарин, который менее сульфатирован, чем гепаран, состоит из фрагментов глюкуроновой кислоты, галактозамина и идуроновой кислоты. Гепарин содержит больше идуроновой кислоты, чем гепаран, который содержит больше моносахаридов глюкуроновой кислоты. Следовательно, минимизированная по энергии модель гепарина является произвольной, поскольку нельзя ожидать, что прогноз геометрии связывающих фрагментов будет согласованным по всей полимерной структуре. Поэтому предположения основаны на произвольном расположении моносахаридных звеньев, тем не менее, минимизированная по энергии структура также образует спиральную сверхструктуру, из которой сульфатные группы выступают наружу. Расстояния между соседними атомами серы составляют от 5 до 6 Å, как показано на фигуре. Учитывая, что гепарин будет содержать меньше сульфатов, чем изображено, возможно, это приведет к снижению эффективности связывания, по сравнению, например, с Целлуфин сульфатом, который содержит более упорядоченную последовательность моносахаридных звеньев. См. фиг. 4.
Пример 7. Спроектированные структуры для 3-APBA и 4-APBA.
Соединение 3-APBA относится к биотинилированной (ПЭГ-24)-3-аминофенилбороновой кислоте, которая, согласно таблице 1, плохо связывает экзосомы. Ее аналог на основе 4-аминофенилбороновой кислоты (4-APBA в приведенной выше таблице) также оказался неэффективным. Оба соединения требуют обработки ультразвуком перед применением, что позволяет предположить, что в среде они имеют тенденцию складываться сами в себя и образовывать коллоиды или другие суспензии, которые не способствуют связыванию с экзосомами.
Контроль ПЭГ (простой полиэтиленгликоль) будет иметь разные физические характеристики в растворе и не будет ассоциироваться сходным образом.
Органические полимеры, содержащие расположенные на одинаковом расстоянии массивы анионных групп, включая бороновые кислоты (такие как поли-(3-акриламидофенилбороновая кислота), занимают минимизированную по энергии геометрию, которая позволяет соседним арильным группам укладываться в тт-укладку, причем анионные придатки расположены довольно близко. Этот пример со случайной стереохимией от основного каркаса полиакриламида иллюстрирует оба признака, при этом соседние атомы бора находятся на расстоянии менее 4 Å. См. фиг. 5.
Пример 8 – Спроектированная структура гиалуроновой кислоты
Гиалуроновая кислота, состоящая из чередующихся сахаридных звеньев, соединенных в 3- и 4-положении, не может легко образовывать плотную спиральную структуру, в которой отрицательно заряженные карбоксилаты образуют конформацию, аналогичную анионным группам, присутствующим, например, в Целлуфин сульфате или гепарине. Чередующиеся дисахариды минимизированы до менее упорядоченного, не спирального массива, при этом карбоксилаты размещены в относительно случайных положениях. Такое отсутствие порядка может способствовать неспособности соединения эффективно связывать экзосомы. Здесь карбоксилаты показаны зеленым цветом на пространственной модели для иллюстрации отсутствия близости их друг к другу. См. фиг. 6.
Пример 9 - Спроектированная структура хондроитинсульфата
Хондроитинсульфат существует в различных формах из 100 или более чередующихся звеньев глюкуроновой кислоты и N-ацетилгалактозамина, где чередующиеся звенья моносахаридов соединены в различных положениях. По этой причине невозможно создать конкретную модель, с помощью которой можно предсказать его способность связывать экзосомы. Однако модель октамера с минимизацией MM2+ показывает, что соседние сульфатные и карбоксилатные группы, выступающие наружу от основного каркаса ядра, могут быть в достаточной степени открыты для способствования взаимодействию с фосфолипидами. См. фиг. 7.
Пример 10 - Спроектированная структура полиаминокислот
Полиаминокислоты – другой потенциальный тип экзосом-связывающего лиганда – включают полиглутаминовую кислоту, полиаспарагиновую кислоту, полисерин и тому подобное.
Предполагают, что гамма-полиглутаминовая кислота принимает форму листа, при этом карбоксилатные группы расположены перпендикулярно основному каркасу, на расстоянии приблизительно 12 Å: это расстояние между потенциальными связывающими фрагментами может быть недостаточным для обеспечения эффективного взаимодействия с фосфолипидами. Следовательно, преположительно этот полимер обладает низкой эффективностью в отношении связывания экзосом.
Полиаспарагиновая кислота может быть получена полностью в L-форме, полностью в D-форме или в виде смеси конфигураций различными способами синтеза. В иллюстративных целях октамер поли-L-Asp изображен как N-ацетил-Asp7NH2. В этом случае минимизированная по энергии молекула имеет вид серии чередующихся петель, на которых карбоксилаты выступают наружу, с соседними СO2-группами на расстоянии от 4,5 до 5,0 Å друг от друга (расстояние углерод-углерод). Согласно структурной модели, полиаспарагиновая кислота должна быть эффективной в отношении связывания экзосом.
Производные поли-β-аспарагина могут быть получены полностью в L-форме, полностью в D-форме или в виде смеси конфигураций различными способами синтеза, как описано в примере 11.
Основываясь на этой модели, а также наблюдениях за вторичной структурой в мультисериновых областях природных белков, можно ожидать, что синтетический полисерин также будет существовать в виде серии чередующихся петель. В этом случае предложенные экзосом-связывающие фрагменты (спиртовые фрагменты, богатые электронами, сходные с таковыми хитозана), занимают сходные соседние расстояния с другими экзосом-связывающими полимерами.
Сульфатирование серинов и других аминокислот, несущих гидроксильные группы (например, тирозина, треонина), с образованием сульфатов полисерина было раскрыто Rivier и Penke из института Salk в патенте US 4444682A (1984) с помощью солей ацетилсерной кислоты. Таким образом, получение полисеринсульфата позволяет получать пептидоподобный аналог высокосульфатированных полисахаридов, таких как Целлуфин сульфат. Геометрия этой молекулы, в силу своей асимметрии, принимает более спиральную форму, чем у несульфатированного полипептида. Как показано в рандомизированной форме боковой цепи (как видно из поли-D,L-Ser-сульфата), соседние сульфатные фрагменты располагаются наружу сходным с полисахаридами образом. Расстояния между атомами серы составляют аналогичные диапазоны: от 4,5 до 6,5 Å. См. фиг. 9-12.
Пример 11 (а). Биотин-C3-поли-4-гидроксибутил-β-аспарагин и пример 11 (b) биотин-C3-поли-4-гидроксибензил-β-аспарагин.
Синтез осуществляют обработкой полимерного ангидрида биотин C3-AspAn (биотин C3-полисукцинимид) 1-гидроксибутиламином или 4-феноксиэтиламином, как указано, с получением производных полимерного β-аспарагина с раскрытым циклом. В иллюстративных целях октамер поли-β-1-гидроксибутиласпарагина, фиг. 11(A), применяют для указания минимизированной по энергии конформации примера 11(a), а фиг. 11(B) иллюстрирует минимизированную по энергии конформацию примера 11(b). Оба примера связывают экзосомы, иллюстрируя диапазон эффективного разделения лигандов.

Пример 12 - Общая структурная модель
Таким образом, общую модель связывания полимера с экзосомами можно представить следующим образом: спираль или лист с соответствующим образом отдаленными друг от друга выступающими анионными или способными к водородному связыванию группами, простирающимися наружу, где каркас состоит из повторяющейся матрицы, и анионные группы могут быть представлены где R = CO2H, CH2OH, CH2OSO3H, B(OH)2 и CH2OP(O)(OH)2, или этими группами в ионизированной форме, которые обусловлены их соответствующими значениями рKа, и тому подобными, с которым экзосома способна связываться. Модель объясняет, что полимеры с высокой эффективностью связывания экзосом несут анионные или богатые электронами группы, где их расстояние друг от друга составляет от 4 до 5 Å. См. фиг. 13.
Пример 13 - Спроектированная структура поливинилсульфата
Атомы серы в поливинилсульфате минимизируют сами себя (в модели полимера из девяти мономерных звеньев) на расстоянии приблизительно от 4,2 до 4,5 Å. См. фиг. 8.
Пример 14 - Прогнозирование эффективности связывания экзосом-связывающих лигандов на основе структурной модели
Общую структурную модель в примере 11 применяли для прогнозирования эффективности связывания экзосом-связывающих лигандов, в том числе исследованных в вышеописанных примерах. Результаты показаны в таблице 2.
Список литературы
Raposo, G. and W. Stoorvogel, Extracellular vesicles: exosomes, microvesicles, and friends. J Cell Biol, 2013. 200(4): р. 373-83.
Urbanelli, L., Magini, A., Buratta, S., Brozzi, А, Sagini, К., Polchi, А, Tancini, В., and Emiliani, С. (2013). Signaling pathways in exosomes biogenesis, secretion and fate. Genes (Basel) 4, 152-170.
Rani, S., Ryan, АЕ., Griffin, M.D., and Ritter, Т. (2015). Mesenchymal Stem Cellderived Extracellular Vesicles: Toward Cell-free Therapeutic Applications. Mol Ther 23, 812-823.
Chen, С., Skog, J., Hsu, С.Н., Lessard, R.Т., Balaj, L., Wurdinger, Т., Carter, B.S., Breakefield, Х.О., Toner, М., and lrimia, D. (2010). Microfluidic isolation and transcriptome analysis of serum microvesicles. Lab Chip 10, 505-511.
van der Pol, Е., Hoekstra, AG., Sturk, А, Otto, С., van Leeuwen, Т.G., and Nieuwland, R. (2010). Optical and non-optical methods for detection and characterization of microparticles and exosomes. J Thromb Haemost 8, 2596-2607.
Greening, D.W., Xu, R., Ji, Н., Tauro, B.J., and Simpson, R.J. (2015). А protocol for exosome isolation and characterization: evaluation of ultracentrifugation, density gradient separation, and immunoaffinity capture methods. Methods Mol Biol 1295, 179-209.
Rider, М.А, Hurwitz, S.N., and Meckes, D.G., Jr. (2016). ExtraPEG: А Polyethylene Glycoi-Based Method for Enrichment of Extracellular Vesicles. Sci Rep 6, 23978.
Heinemann, M.L., llmer, М., Silva, L.P., Hawke, D.H., Recio, A, Vorontsova, М.А, Alt, Е., and Vykoukal, J. (2014). Benchtop isolation and characterization of functional exosomes Ьу sequential filtration. J Chromatogr A 1371, 125-135
Nordin, J.Z., Lee, У., Vader, Р., Mager, 1., Johansson, H.J., Heusermann, W., Wiklander, О.Р., Hallbrink, М., Seow, У., Bultema, J.J., et аl. (2015). Ultrafiltration with size-exclusion liquid chromatography for high yield isolation of extracellular vesicles preserving intact biophysical and functional properties. Nanomedicine 11, 879-883.
Sakudo, A, Ваbа, К., Tsukamoto, М., and lkuta, К. (2009а). Use of anionic polymer, poly(methyl vinyl ether-maleic anhydride)-coated beads for capture of respiratory syncytial virus. Bioorg Med Chem Lett 19, 4488-4491.
Таблица 1
Таблица 2. Сравнение лигандов, протестированных LEAP, и лигандов, прогнозируемых структурной моделью EMIT
Примечание: *Лиганды с общим выходом выделения 25% или более в тесте LEAP считались положительными.
Реферат
Группа изобретений относится к области биотехнологии. Предложены способ и устройство для получения композиции или изолята экзосом или микровезикул. Способ включает обеспечение включающей экзосомы или микровезикулы жидкости, обеспечение имеющей поверхность подложки с массивом экзосом-связывающих лигандов, взаимодействие жидкости с подложкой в обеспечивающих связывание экзосом или микровезикул с экзосом-связывающими лигандами условиях и отделение подложки от жидкости с получением композиции или изолята экзосом или микровезикул. Причем каждый лиганд находится в форме, богатой электронами группы при рН 4-8, и массив экзосом-связывающих лигандов позволяет экзосомам или микровезикулам связываться с подложкой. Устройство включает подложку с указанным выше массивом экзосом-связывающих лигандов. Изобретения обеспечивают улучшенный выход экзосом, масштабируемость для производства или получение экзосом фармацевтической степени чистоты. 2 н. и 16 з.п. ф-лы, 19 ил., 2 табл., 14 пр.

Комментарии