Способ, система и машиночитаемый носитель для адаптационного рекомендательного контроля сахарного диабета - RU2602040C2
Код документа: RU2602040C2
Чертежи














Описание
Родственные заявки
По настоящей заявке испрашивается приоритет по предварительной заявке на выдачу патента США №61/528129 с датой подачи 26 августа 2011 года под названием "Method, System and Computer Program Product for Adaptive Advisory Control of Diabetes (Способ, система и компьютерный программный продукт для адаптационного рекомендательного контроля сахарного диабета)", раскрытие которой, таким образом, включено в настоящий документ с помощью ссылки в полном ее объеме.
УРОВЕНЬ ТЕХНИКИ
В здоровом состоянии метаболизм глюкозы жестко подконтролен гормональной сети, включающей кишечник, печень, поджелудочную железу и головной мозг, что обеспечивает стабильные уровни глюкозы в крови (BG) натощак и временные колебания постпрандиальной глюкозы. При сахарном панкреатическом диабете 1 типа (T1DM) интенсивное лечение инсулином, в попытке приблизиться к почти нормальным уровням гликемии, значительно снижает хронические осложнения [49, 61], но может привести к возможности возникновения потенциально опасной для жизни тяжелой гипогликемии (SH), возникающей вследствие недостаточного замещения инсулина [25, 60]. Как следствие, гипогликемия была выявлена в качестве основного препятствия для оптимальной терапии сахарного диабета [15, 17]. Так, люди с T1DM сталкиваются с продолжающейся в течение всей жизни, контролируемой при помощи поведения проблемой оптимизации: сохранение строгого гликемического контроля без повышения для них риска гипогликемии [14]. Вариабельность уровня глюкозы или степень и скорость колебаний BG является как измеряемым результатом такой поведенческой оптимизации, так и основной ответной реакцией у больного на оптимизацию у него/нее контроля сахарного диабета. Другими словами, колебания BG при сахарном диабете проявляются в результате действия сложной динамической системы, в которую вносит возмущение поведенческий генератор событий, и зависят от двух метаболических процессов: (i) взаимодействие экзогенного инсулина и утилизация углеводов и (ii) гормональная защита от гипогликемии, известная как контррегуляция.
Исходя из точки зрения биологии системы, биоповеденческий контроль T1DM, следовательно, состоит из следующего: (i) запускаемые поведением процессы обычно постоянных колебаний глюкозы (например, нормальные постпрандиальные отклонения глюкозы), прерываемые обычно случайными, запускающими гипогликемию поведенческими явлениями (например, передозировка инсулином, пропущенный прием пищи или чрезмерная физическая нагрузка [9, 26]); и (ii) физиологические процессы, зависящие от характеристик метаболизма человека, таких как чувствительность к инсулину [4] или контррегуляция, которая препятствует индуцируемой инсулином гипогликемии, но также в результате происходит периодическое истощение контррегуляционных резервов, которое имеет место при повторяющейся гипогликемии и известно под названием связанная с гипогликемией вегетативная недостаточность (HAAF, [16]).
Попытки применения технологии, способствующей контролю сахарного диабета, привели к формированию идеи искусственной поджелудочной железы, которую можно проследить до разработок, имевших место более тридцати лет назад, когда возможность внешней регуляции BG у людей с сахарным диабет была установлена в результате исследований с применением измерений внутривенной (вв) глюкозы и вв инфузии глюкозы и инсулина. Были внедрены такие системы, как Biostator™, и их применяют в лечебном учреждении для поддержания нормогликемии путем осуществления как положительного (с помощью глюкозы или глюкагона), так и отрицательного (с помощью инсулина) контроля [1, 10, 39, 48, 53]. Подробное описание основных ранних разработок можно найти в [6, 11, 13, 21, 22, 52]. Затем была проведена дополнительная работа, охватывающая более широкий диапазон методик контроля BG, таких как адаптивный контроль [7, 23], физиологическое моделирование [52, 56], характерный для отделений интенсивной терапии контроль [3] или оптимизация методом линейных и квадратичных единиц Гаусса (LQG) [24, 41]. Тем не менее, вв система замкнутого управления остается затруднительной и неудобной для применения амбулаторными больными. Альтернатива экстракорпорального вв контроля была представлена имплантируемыми вв-ип системами, в которых предусмотрен внутривенный забор и интраперитонеальная (ип) подача инсулина [37, 51, 55]. Однако, для реализации этих систем необходима серьезная хирургическая операция. Таким образом, с появлением малоинвазивного подкожного (п/к) непрерывного мониторинга уровня глюкозы (CGM) усиливающаяся научная, промышленная и политическая деятельность была сфокусирована на разработке п/к-п/к систем, в которых используется CGM в сочетании с инсулиновой инфузионной помпой и алгоритмом контроля [2, 8, 29, 31]. На сегодняшний день были опубликованы обнадеживающие первоначальные результаты [12, 28, 54, 58, 62]. В первых исследованиях Hovorka et al. [27, 28, 29] и Steil et al. [58] были описаны два основных типа контроллеров, считающихся подходящими для п/к применения - МРС (контроль на основе прогностических моделей) и PID (пропорционально- интегрально-дифференциальный) контроль, соответственно. На сегодняшний день были проведены испытания полностью п/к-п/к систем исключительно с применением PID [58, 62], несмотря на это, МРС [20, 27, 38, 45] стал предпочтительным подходом, являющимся целью настоящего исследования [12, 28, 54]. Существует две основных причины, делающих МРС предпочтительным: (i) PID характеризуется превосходной обратной связью, отвечая на изменения уровня глюкозы, при этом должным образом настроенный МРС делает возможным прогноз динамики глюкозы [50, 54, 57, 65] и, в результате, уменьшение задержек по времени, присущих п/к мониторингу глюкозы [5, 36, 59, 63] и п/к инфузии инсулина [40, 64]; (ii) МРС предусматривает относительно простую персонализацию контроля с помощью специфических для больного параметров модели. Недавно были разработаны способы определения момента приема пищи или гипогликемии [18, 19], а также была протестирована технология самообучения. Было показано, что класс алгоритмов (известный как контроль от события до события) может "обучаться" специфическим особенностям распорядка дня больных (например, время приемов пищи), а затем оптимизировать ответ на последующий прием пищи с помощью такой информации [42, 43, 66] или учитывать суточное колебание резистентности к инсулину (например, наблюдаемый у некоторых людей феномен "утренней зари" [44]).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В соответствии с одним аспектом варианта осуществления настоящее изобретение относится, помимо прочего, к новой модели адаптационного рекомендательного контроля (АА контроля) - интерактивному процессу, предусматривающему оценку и связь при помощи алгоритма физиологических и поведенческих параметров и паттернов у больных сахарным диабетом с целью оказания помощи в оптимизации их гликемического контроля. В частности, настоящее изобретение относится без ограничения к приведенным далее аспектам.
Принцип стохастического процесса поведения человека: поведенческие события (приемы пищи, физическая нагрузка, отход ко сну, подъем) приводят к изменению состояния системы (человека), например, состояние натощак - сытое состояние, до-после физической нагрузки, подъем ↔ сонное состояние. Эти состояния формируют "пространство состояний" с возможными ситуациями, с которыми может столкнуться человек. Каждый переход от одного состояния к другому соответствует поведенческому событию. Другими словами, генератор поведенческих событий обуславливает переход системы из одного состояния в другое. Эти переходы имеют место с различными вероятностями для различных людей, так, каждого человека выявляют по его специфическим вероятностям перехода в его/ее поведении. Эта идея формально была описана с помощью стохастического процесса ξ(n), построенного на идее стохастических переходов, т.е. переходов, которые предусматривают у идентичных в одном состоянии прототипов иные результаты в следующем состоянии. Предположим, что на своем этапе n (n=1, 2, …) процесс ξ(η) описывается с помощью случайно переменной xn, которая имеет свои значения в некоторой группе xn. Стохастический переход процесса ξ от Хnк его Xn+1 на следующем этапе определяется вероятностями Ρ(ξ(n+1)=xn+1/ξ(n)ЄS) для любого xn+1ЄΧn+1 и SЄSn. Таким образом, каждого человека выявляют по его индивидуальной поведенческой характеристике, определяемой его/ее собственными вероятностями перехода {pij} между двумя состояниями (i) и (j). Такое представление делает возможным формальное описание поведенческих паттернов, которые можно рассматривать в качестве одного из ключевых аспектов (без ограничения) способов (и систем, и машиночитаемых носителей) по настоящему изобретению - для каждого человека вероятности перехода можно оценить из данных, которые служат в качестве основы для отслеживания поведенческих паттернов. Например, можно разработать алгоритм оценки, который перемещается по окну данных непрерывного мониторинга глюкозы (CGM) и выявляет изменения состояния системы (человека). Для иллюстрации такого действия на Фиг. 1 графически представлены экспериментальные результаты случая наблюдения за приемом пищи у субъекта из ранее изложенного исследования [32]. Алгоритм наблюдения за приемом пищи перемещается вниз по дням наблюдения (сверху вниз). Вероятность осуществления приема пищи в определенный момент времени закодировано при помощи цвета от черного (очень низкая) до белого (очень высокая). Видно, что спустя неделю наблюдений (верхняя линия) моменты времени приема пищи уже хорошо обозначены и остаются неизменными на протяжении 30 дней наблюдения. Завтрак (7:30 АМ) и ужин в 8:30 РМ, как видно, лучше всего выявлены для этого человека [46].
Кроме того, оценка риска гипогликемии у человека может быть основана на нашей теории анализа риска [35] и на наблюдении, что случаи гипогликемии обычно подчиняются выявляемым паттернам нарушений нормальной работы системы [33], как графически проиллюстрировано на Фиг. 2: спустя 10 дней наблюдения вырисовывается паттерн (черная линия), из которого видна тенденция более низкой BG в 6АМ и 12РМ. Более светлые пятна указывают на большее правдоподобие (достоверность), так, для этого человека вероятна гипогликемия перед завтраком. Наконец, можно осуществить оценку стабильности системы, как графически представлено на Фиг. 3, на которой изображена скорость изменения уровня глюкозы, из которой явно видно состояние голода в течение ночи (светлая зона, продолжающаяся до 7АМ) и обычные моменты времени подъема и отхода ко сну (11РМ) для участника в ранее указанном исследовании.
В соответствии с аспектом варианта осуществления настоящее изобретение относится к адаптационной рекомендательной (АА) системе, помогающей осуществлять контроль сахарного диабета путем распознавания ключевых связанных с лечением био-поведенческих паттернов. В способах (и системах, и машиночитаемом носителе) согласно аспекту вариантов осуществления по настоящему изобретению могут быть использованы все возможные источники информации о больном; (i) данные о BG (например, самостоятельный мониторинг уровня глюкозы в крови (SMBG) и CMG, 22), (ii) данные о инсулине (например, файлы журнала инсулиновой помпы или записи о лечении больного, 32) и (iii) самостоятельно заполняемые больным данные (например, навыки самостоятельного приема лекарственных препаратов, приемы пищи и физическая нагрузка, 52) для:
1) ретроактивной оценки риска гипогликемии, основанного на риске по результатам ретроактивной оценки уменьшения подачи инсулина, а затем сообщения больному о том, как система уменьшения подачи инсулина на основе риска сообразно действовала бы для предупреждения гипогликемии,
2) разработки и периодического усовершенствования математической модели больного, состоящей как из
а) модели динамических систем для системы глюкозы/инсулина больного, связывающей пероральный прием углеводов, физическую деятельность и подкожную инфузию инсулина с концентрацией глюкозы в крови больного, так и из
b) вероятностной модели значимых с точки зрения метаболизма поведенческих особенностей больного, которая, в частности, описывает вариабельность поведения больного, и
3) ретроактивного расчета оптимальных расписаний подачи инсулина на основе описанных выше физиологической и поведенческой моделей, а затем сообщение больному о том, как алгоритм оптимального введения дозы инсулина сообразно действовал бы для осуществления строгого гликемического контроля.
На основе описанных выше физиологических и поведенческих моделей совокупного эффекта и данных по CGM/SMBG и от инсулиновой помпы в режиме реального времени АА-система (и способ, и машиночитаемый носитель) может предоставить больному по запросу рекомендацию по поправке дозы инсулина. АА-система может быть реализована в любом современном вычислительном устройстве, в том числе портативных компьютерах, планшетах, мультимедийном проигрывателе (например, МР3-проигрывателе или видеопроигрывателе), сотовом телефоне и смартфонах (например, карманном персональном компьютере (PDA)), а также интернет-приложениях или сетевых приложениях, которые имеют доступ к потоку данных от больного.
Согласно аспекту варианта осуществления настоящее изобретение относится к основанному на устройстве обработки данных способу апостериорной оценки риска гипогликемии у больного. Способ может предусматривать следующее: осуществление алгоритма для расчета статистики, Rhypo(record), в отношении риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, который сильно коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Еhypo означает событие гипогликемии на следующий день, a record относится к хронологической записи BG, подачи инсулина и видов деятельности у субъекта; и получение рассчитанных статистических данных, Rhypo(record), посредством чего, таким образом, больному или пользователю подается реализуемое предварительное уведомление о возможности приближающейся гипогликемии у больного.
Согласно аспекту варианта осуществления настоящее изобретение относится к основанному на устройстве обработки данных способу ретроактивного обеспечения безопасного уровня инсулина у больного. Способ может предусматривать: создание алгоритма для ретроактивного расчета, основанного на оценке рисков коэффициента ослабления потребности в инсулине относительно записи подачи инсулина у субъекта; и получение рассчитанного основанного на оценке рисков коэффициента ослабления потребности в инсулине и применение основанного на оценке рисков коэффициента ослабления с тем, чтобы вывести больному или пользователю любое внутреннее пороговое значение для принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем, которое может быть реализовано.
Согласно аспекту варианта осуществления настоящее изобретение относится к основанному на устройстве обработки данных способу создания основанной на "совокупном эффекте" адаптационной модели больного. Способ может предусматривать: создание алгоритма для расчета динамической модели метаболической системы больного, причем динамическая модель включает дескриптивные параметры индивидуальной физиологии модельного больного; соответствующую выведенную хронологию поведенческой модели на основе "совокупного эффекта", которая объясняет вариабельность уровня глюкозы в хронологической записи с помощью динамической модели; причем модель на основе "совокупного эффекта" включает отклонения в представлении в математической форме у модельного больного; и коррекцию физиологических параметров больного на основе как (i) способности динамической модели прогнозировать будущий уровень BG, исходя из известных входящих данных, так и (ii) способности модели выводить характеристики совокупного эффекта, которые согласуются с записью отклонений у больного. Способ может дополнительно предусматривать вывод коррекции больному или пользователю, таким образом, больной или пользователь может использовать коррекцию для будущего плана действий.
Согласно аспекту вариант осуществления настоящее изобретение относится к способу, который может предусматривать осуществление ретроактивной оценки оптимальной скорости подачи инсулина больному, причем алгоритм: ретроактивно рассчитывает, какой была бы оптимальная скорость подачи инсулина больному на протяжении предопределенного периода времени в хронологии с учетом, что нарушения в системе являются именно хронологическими характеристиками совокупного эффекта, рассчитанными для больного на протяжении такого интервала времени, причем для каждой "хронологии" характеристик совокупного эффекта существует соответствующая "хронология" скоростей подачи инсулина, в которой учтены приемы пищи, физическая нагрузка и поправки на каждый день в рассматриваемом интервале времени; связывает характеристику совокупного эффекта для заданного дня и основанный на модели ответ контроллера оптимального уровня, причем эти одномерные массивы оптимальных ответов собирают, и анализируют, и представляют больному или пользователю для обзора по дням лечения инсулином; извлекает компоненты из оптимальных ответов, которые соответствуют важным, но случайным событиям, путем вычитания отдельных количеств инсулина, связанных с приемами пищи, или учета отдельных случаев нехватки инсулина, связанных с временными базальными дозами вблизи физической нагрузки, в результате чего остальное расписание подачи инсулина соответствует представлению "оптимального" базального паттерна для больного на каждый день в хронологической записи; и выявляет согласованность в ретроактивно рассчитанных оптимальных базальных дозах, причем такие оптимальные базальные дозы во множестве сегментов периода представляют собой период лечения больного. Способ может дополнительно предусматривать: вывод больному или пользователю среднего уровня базального инсулина, который был бы приемлем в каждом сегменте, причем больной или пользователь может использовать эту информацию для (i) принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем или (ii) уточнения долгосрочного профиля базальных доз у больного.
Согласно аспекту варианта осуществления настоящее изобретение относится к способу, который может предусматривать осуществление модели рекомендации по адаптивной поправке инсулина по запросу пользователя. Способ может предусматривать создание алгоритма, включающего следующие вычислительные операции: ретроспективное определение связанных с приемом пищи и физической нагрузкой видов деятельности; стохастическое моделирование с получением описания о времени и содержании приемов пищи и физической нагрузки; и вывод рекомендации по поправке дозы инсулина больному или пользователю, что может быть ответом на запрос больного и пользователя.
Согласно аспекту варианта осуществления настоящее изобретение относится к системе апостериорной оценки риска гипогликемии у больного. Система может включать: модуль основанной на ретроактивной оценке рисков безопасности с устройством обработки данных для расчета статистики, Rhypo(record), риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, который сильно коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, a record относится к хронологической записи BG, подачи инсулина и видов деятельности у субъекта; и
устройство обработки данных выводит рассчитанную статистику, Rhypo(record), таким образом, больному или пользователю подается реализуемое предварительное уведомление о возможности приближающейся гипогликемии у больного.
Согласно аспекту варианта осуществления настоящее изобретение относится к системе для ретроактивного обеспечения безопасного уровня инсулина у больного. Система может включать: модуль основанной на ретроактивной оценке рисков безопасности с устройством обработки данных для ретроактивного расчета, основанного на оценке рисков коэффициента ослабления потребности в инсулине относительно записи подачи инсулина у субъекта; а устройство обработки данных выводит рассчитанный основанный на оценке рисков коэффициент ослабления потребности в инсулине, и применение основанного на оценке рисков коэффициента ослабления с тем, чтобы вывести больному или пользователю любое внутреннее пороговое значение для принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем, которое может быть реализовано.
Согласно аспекту варианта осуществления настоящее изобретение относится к системе для обеспечения основанной на "совокупном эффекте" адаптационной модели больного. Система может включать: модуль оценки совокупного эффекта с устройством обработки данных для расчета динамической модели метаболической системы больного, причем динамическая модель включает дескриптивные параметры индивидуальной физиологии модельного больного; соответствующую выведенную хронологию поведенческой модели на основе "совокупного эффекта", которая объясняет вариабельность уровня глюкозы в хронологической записи с помощью динамической модели; причем модель на основе "совокупного эффекта" включает отклонения в представлении в математической форме у модельного больного; и модуль корректировки модели с устройством обработки данных для расчета коррекции физиологических параметров больного на основе как (i) способности динамической модели прогнозировать будущий уровень BG, исходя из известных входящих данных, так и (ii) способности модели выводить характеристики совокупного эффекта, которые согласуются с записью отклонений у больного. Система выводит коррекцию больному или пользователю, таким образом, больной или пользователь может использовать коррекцию для будущего плана действий.
Согласно аспекту варианта осуществления настоящее изобретение относится к системе, сконфигурированной для ретроактивной оценки оптимальной скорости подачи инсулина больному. Система включает модуль-анализатор ретроспективного оптимального контроля с устройством обработки данных, сконфигурированным для осуществления ретроактивного расчета, какой была бы оптимальная скорость подачи инсулина больному на протяжении предопределенного периода времени в хронологии с учетом, что нарушения в системе являются именно хронологическими согласно характеристикам совокупного эффекта, рассчитанным для больного на протяжении такого интервала времени, причем для каждой "хронологии" характеристик совокупного эффекта существует соответствующая "хронология" скоростей подачи инсулина, в которой учтены приемы пищи, физическая нагрузка и поправки на каждый день в рассматриваемом интервале времени; и связывания характеристики совокупного эффекта для заданного дня и основанный на модели ответ контроллера оптимального уровня, причем эти одномерные массивы оптимальных ответов собирают, и анализируют, и представляют больному или пользователю для обзора по дням лечения инсулином. Система дополнительно содержит модуль для извлечения ретрооптимальной базальной дозы с устройством обработки данных, сконфигурированным для извлечения компонентов из оптимальных ответов, которые соответствуют важным, но случайным событиям, путем вычитания отдельных количеств инсулина, связанных с приемами пищи, или учета отдельных случаев нехватки инсулина, связанных с временными базальными дозами вблизи физической нагрузки, в результате чего остальное расписание подачи инсулина соответствует представлению "оптимального" базального паттерна для больного на каждый день в хронологической записи; и выявлять согласованность в ретроактивно рассчитанных оптимальных базальных дозах, причем такие оптимальные базальные дозы во множестве сегментов периода представляют собой период лечения больного. Также система может быть сконфигурирована для вывода больному или пользователю среднего уровня базального инсулина, который был бы приемлем в каждом сегменте, причем больной или пользователь может использовать эту информацию для (i) принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем или (ii) уточнения долгосрочного профиля базальных доз у больного.
Согласно аспекту варианта осуществления настоящее изобретение относится к системе, сконфигурированной для осуществления модели рекомендации по адаптивной поправке инсулина по запросу пользователя. Система может содержать модуль для ретроспективного определения приема пищи и физической нагрузки с устройством обработки данных для осуществления ретроспективного определения связанных с приемом пищи и физической нагрузкой видов деятельности; модуль для стохастического моделирования приема пищи и физической нагрузки с устройством обработки данных для осуществления стохастического моделирования с получением описания о времени и содержании приемов пищи и физической нагрузки; и модуль для вывода рекомендации по поправочному болюсу с устройством обработки данных для представления и вывода рекомендации по поправке дозы инсулина больному или пользователю, что будет ответом на запрос больного и пользователя.
Согласно аспекту варианта осуществления настоящее изобретение относится к постоянному машиночитаемому носителю, содержащему команды управления программой для осуществления апостериорной оценки риска гипогликемии у больного, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы заставляют устройство обработки данных осуществлять следующие этапы: осуществление алгоритма для расчета статистики, Rhypo(record), риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, который сильно коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, a record относится к хронологической записи BG, подачи инсулина и видов деятельности у субъекта; и получение рассчитанных статистических данных, Rhypo(record), посредством чего, таким образом, больному или пользователю подается реализуемое предварительное уведомление о возможности приближающейся гипогликемии у больного.
Согласно аспекту варианта осуществления настоящее изобретение относится к постоянному машиночитаемому носителю, содержащему команды управления программой для ретроактивного обеспечения безопасного уровня инсулина больному, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы заставляет устройство обработки данных осуществлять следующие этапы: создание алгоритма для ретроактивного расчета основанного на оценке рисков коэффициента ослабления потребности в инсулине относительно записи подачи инсулина у субъекта; и получение рассчитанного основанного на оценке рисков коэффициента ослабления потребности в инсулине и применение основанного на оценке рисков коэффициента ослабления с тем, чтобы вывести больному или пользователю любое внутреннее пороговое значение для принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем, которое может быть реализовано.
Согласно аспекту варианта осуществления настоящее изобретение относится к постоянному машиночитаемому носителю, содержащему команды управления программой для создания основанной на "совокупном эффекте" адаптационной модели больного, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы заставляет устройство обработки данных осуществлять следующие этапы: расчет динамической модели метаболической системы больного, причем динамическая модель включает дескриптивные параметры индивидуальной физиологии модельного больного; расчет соответствующей выведенной хронологии поведенческой модели на основе "совокупного эффекта", которая объясняет вариабельность уровня глюкозы в хронологической записи с помощью динамической модели; причем модель на основе "совокупного эффекта" включает отклонения в представлении в математической форме у модельного больного; и расчет коррекции физиологических параметров больного на основе как (i) способности динамической модели прогнозировать будущий уровень BG, исходя из известных входящих данных, так и (ii) способности модели строить характеристики совокупного эффекта, которые согласуются с записью отклонений у больного; и вывод коррекции больному или пользователю, таким образом, больной или пользователь может использовать коррекцию для будущего плана действий.
Согласно аспекту вариант осуществления настоящее изобретение относится к постоянному машиночитаемому носителю, обеспечивающему осуществление ретроактивной оценки оптимальной скорости подачи инсулина больному, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы заставляет устройство обработки данных осуществлять следующие этапы: ретроактивный расчет, какой была бы оптимальная скорость подачи инсулина больному на протяжении предопределенного периода времени в хронологии с учетом, что нарушения в системе являются именно хронологическими характеристиками совокупного эффекта, рассчитанными для больного на протяжении такого интервала времени, причем для каждой "хронологии" характеристик совокупного эффекта существует соответствующая "хронология" скоростей подачи инсулина, в которой учтены приемы пищи, физическая нагрузка и поправки на каждый день в рассматриваемом интервале времени; связывание характеристики совокупного эффекта для заданного дня и основанного на модели ответа контроллера оптимального уровня, причем эти одномерные массивы оптимальных ответов собирают, и анализируют, и представляют больному или пользователю для обзора по дням лечения инсулином; извлечение компонентов из оптимальных ответов, которые соответствуют важным, но случайным событиям, путем вычитания отдельных количеств инсулина, связанных с приемами пищи, или учета отдельных случаев нехватки инсулина, связанных с временными базальными дозами вблизи физической нагрузки, в результате чего остальное расписание подачи инсулина соответствует представлению "оптимального" базального паттерна для больного на каждый день в хронологической записи; выявление согласованности в ретроактивно рассчитанных оптимальных базальных дозах, причем такие оптимальные базальные дозы во множестве сегментов периода представляют собой период лечения больного; и вывод больному или пользователю среднего уровня базального инсулина, который был бы приемлем в каждом сегменте, причем больной или пользователь может использовать эту информацию для (i) принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем или (ii) уточнения долгосрочного профиля базальных доз у больного.
Согласно аспекту варианта осуществления настоящее изобретение относится к постоянному машиночитаемому носителю, с помощью которого обеспечивают осуществление модели рекомендации по адаптивной поправке инсулина по запросу пользователя, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы заставляет устройство обработки данных осуществлять следующие этапы: ретроспективное определение связанных с приемом пищи и физической нагрузкой видов деятельности стохастическое моделирование с получением описания о времени и содержании приемов пищи и физической нагрузки; и вывод рекомендации по поправке дозы инсулина больному или пользователю, что может быть ответом на запрос больного и пользователя.
Следует понимать, что несмотря на то, что конкретный период времени может относиться к суткам, можно установить другой период времени (или дату) или по желанию или необходимости можно выставить более длительный или более короткий период времени.
Изложенные в настоящем документе эти и другие объекты, наряду с преимуществами и признаками различных аспектов вариантов осуществления по настоящему изобретению, будут более понятны из приведенного далее описания, чертежей и формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Приведенные выше и другие объекты, компоненты и преимущества настоящего изобретения, а также собственно настоящее изобретение, будут больше понятны из последующего описания предпочтительных вариантов осуществления при прочтении с учетом прилагаемых чертежей.
На Фиг. 1 графически представлены первоначальные результаты ранее упомянутого исследования в отношении наблюдения за приемами пищи у субъекта, которые отображают пример вероятностной оценки поведенческих паттернов приема пищи.
На Фиг. 2 графически проиллюстрированы результаты наблюдений, что гипогликемические приступы обычно протекают согласно выявляемым паттернам нарушений нормальной работы системы согласно данным от субъекта, которые отображают пример вероятностной оценки рисков развития гипо- и гипергликемии.
На Фиг. 3 графически изображена скорость изменения глюкозы, явно указывающая на состояние голода в течение ночи (светлая зона, продолжающаяся до 7АМ) и обычные моменты времени подъема и отхода ко сну (11РМ) для участника в ранее указанном исследовании, которая отображает пример вероятностной оценки паттернов стабильности системы (паттерны сон/бодрствование).
На Фиг. 4 приведен схематический обзор адаптационной рекомендательной (АА) системы.
На Фиг. 5 приведено схематическое изображение ретроактивной оценки основанной на оценке рисков безопасности.
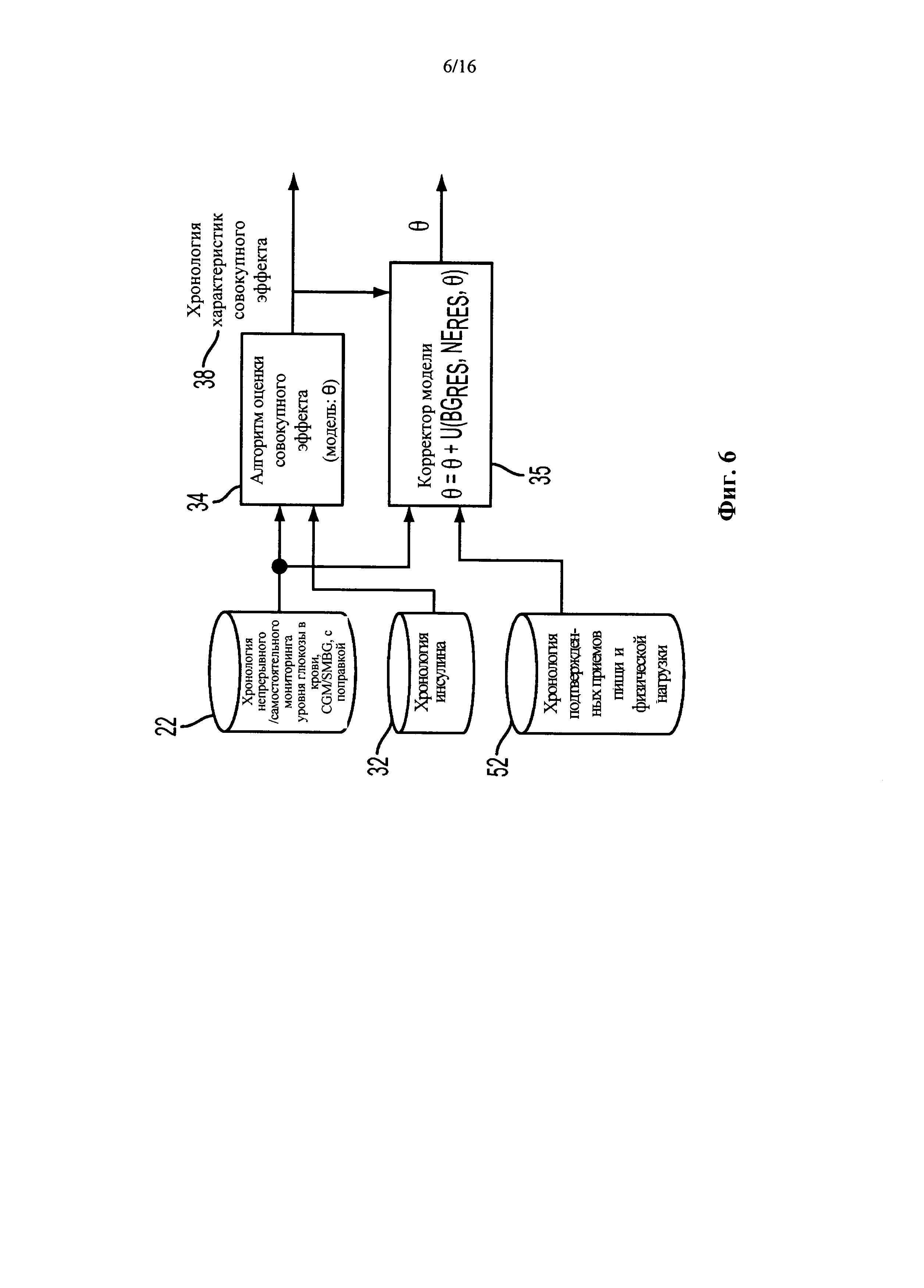
На Фиг. 6 приведено схематическое изображение основанной на "совокупном эффекте" адаптационной модели больного.
На Фиг. 7 приведено схематическое изображение ретроактивной оценки оптимальной подачи инсулина.
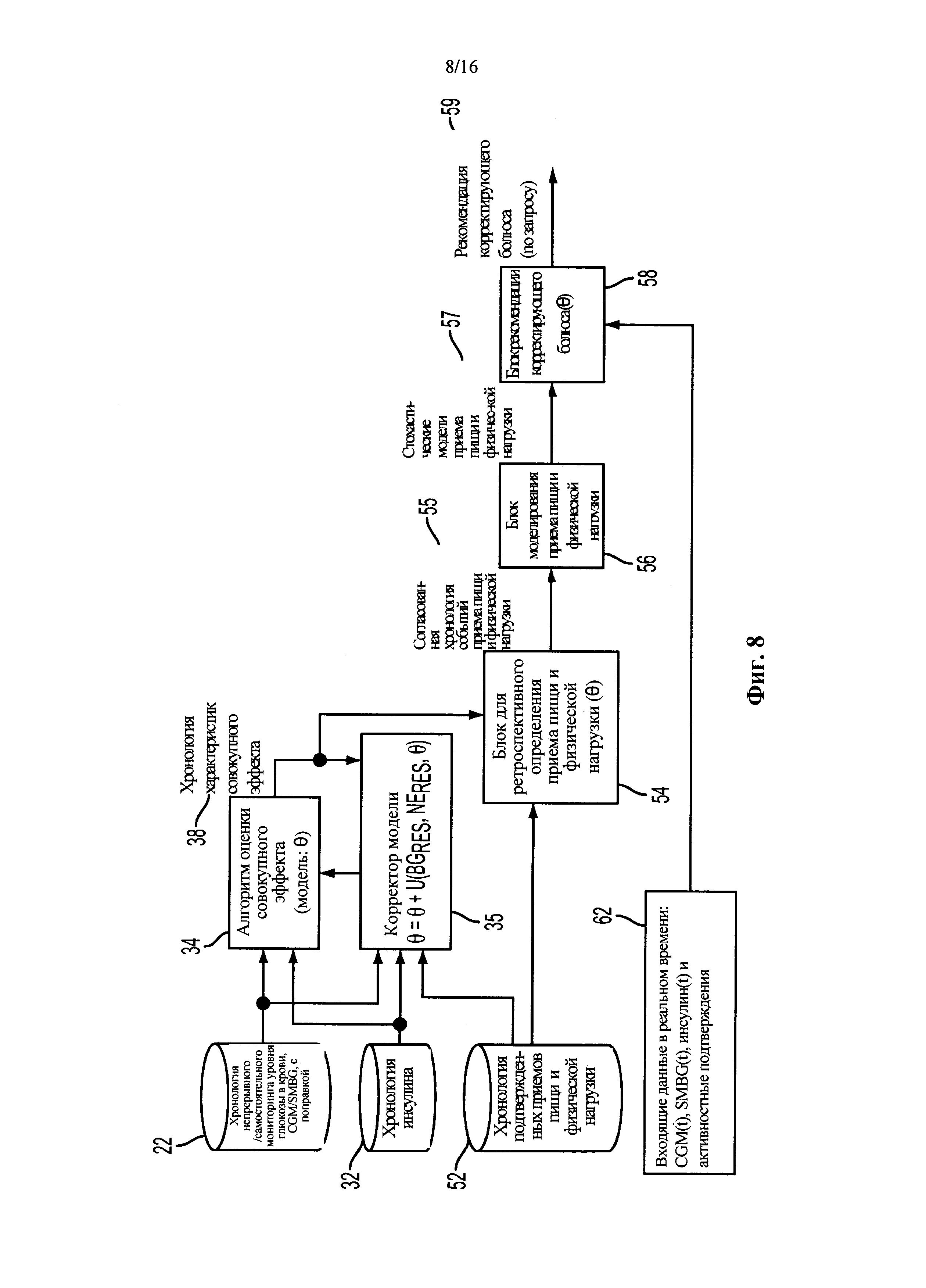
На Фиг. 8 приведено схематическое изображение рекомендации по адаптивной поправочной дозе инсулина по запросу пользователя.
На Фиг. 9 с помощью графика проиллюстрирован пример системы адаптивной поправочной дозы инсулина по запросу пользователя.
На фиг. 10-15 приведены скриншоты одной реализации варианта осуществления АА-системы.
На Фиг. 16 представлена блок-схема системы и относящемуся к ней способу согласно варианту осуществления настоящего изобретения целиком или частично.
Подробное описание настоящего изобретения
Некоторые иллюстративные элементы АА-системы 10 проиллюстрированы на Фиг. 4. Все четыре основных функциональных блока системы определяют, помимо прочего, долговременные хронологические тенденции в физиологических реакциях больного касательно поглощения углеводов и инсулина, а также навыков у больного самостоятельного лечения, поведенческих особенностей в питании и физической нагрузки. Компоненты по "ретроактивной" рекомендации предназначены для иллюстрации больному как систематизированное под контролем системы безопасности и/или оптимальное введение инсулина отличалось бы от того, что фактически делал больной, что приводит требуемые для больного доказательства в необходимости изменения его/ее навыков самостоятельного лечения. Компонент "по запросу пользователя", в основе которого лежат данные по инсулину и BG в режиме реального времени, помимо хронологической записи может давать больному рекомендации по поправочным количествам инсулина, играя роль адаптационного калькулятора болюса, т.е. адаптированные к физиологии больного, прогнозируемым будущим поведенческим особенностям и состоянию метаболизма в режиме реального времени.
Следует отметить, что упомянутую ранее АА-систему можно легко применять в сочетании с системой контроля безопасности в режиме реального времени, в которой данные по CGM и инсулину сообщают об основанных на результатах модели снижениях подачи инсулина (например, уменьшение базальной дозы) в режиме реального времени. Применение такой системы контроля безопасности является абсолютно необязательным.
В последующих подразделах приведено подробное описание четырех основных компонентов системы: (i) блок основанной на ретроактивной оценке рисков безопасности, (ii) блок основанной на "совокупном эффекте" адаптационной модели больного, (iii) блок ретроактивной оценки оптимальной подачи инсулина и (iv) блок рекомендации по адаптивной поправочной дозе инсулина по запросу пользователя.
Следует понимать, что связанные с настоящим изобретением модули, системы, подсистемы и устройства можно в целом или отдельно сформировать во множестве форм, и они могут быть связаны при помощи беспроводной или проводной связи (или комбинации той и другой) с использованием технологии и подходов, которые будут доступны специалисту в данной области. На некоторые неограничивающие примеры интерфейсов и связей устройства, модуля, сети и системы можно сослаться с помощью раскрытых в настоящем документе источников, заявок и публикаций (и, таким образом, они включены при помощи ссылки). Более того, пример возможного интерфейса и связи между различными системами, устройствами и сетями раскрыт (без ограничения) в международной патентной заявке № PCT/US 2008/082063, Magni, et al., под заголовком "Model Predictive Control Based Method for Closed-Loop Control of Insulin Delivery in Diabetes Using Continuous Glucose Sensing", дата подачи 31 октября 2008 года; заявке на выдачу патента США №12/740275, Magni, et al., под заголовком "Predictive Control Based System and Method for Control of Insulin Delivery in Diabetes Using Glucose Sensing", дата подачи 28 апреля 2010 года - см., в частности, фигуры 1-4 и 6-10 в работе Magni et al. (раскрытие обеих из которых, таким образом, включено с помощью ссылки в их полном объеме).
Компонент 1 - блок основанной на оценке рисков ретроактивной безопасности
Части системы, предназначенные для оценки основанной на оценке рисков безопасности, проиллюстрированы на Фиг.5, которые в результате выдают два основных типа выходящих данных, оба из которых могут быть отображены больному для улучшенного понимания его/ее риска гипогликемии как приведено далее.
Выходящие данные 1: апостериорная оценка риска гипогликемии. Эта часть подсистемы, основанной на ретроактивной оценке рисков безопасности, анализирует хронологическую запись и использует ядерные оценки плотности временного ряда BG больного для расчета статистики, Rhypo(record), в отношении риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, который сильно коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, а record относится к хронологический записи BG 22 больного, инсулина 32 и видов деятельности 52. В результате точного информирования больного об апостериорной вероятности гипогликемии 26 в течение следующего дня лечения больной получает возможность принять меры до появления возможности возникновения гипогликемии. Больной может использовать эту информацию для снижения своих собственных внутренних порогов для принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки. Такая "апостериорная оценка" риска гипогликемии предназначена для дополнения существующих способов расчета "профилей BG", на которых указаны "зоны риска" гипогликемии в течение всего дня лечения (как показано на Фиг. 2). Настоящее изобретение не относится к принципу "профиля BG", но скорее оно относится к способу расчета апостериорной вероятности гипогликемии с учетом хронологической записи больного (22, 32, 52).
Следует понимать, что абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM-устройства больного (или записей, или запоминающего устройства для данных показателей глюкозы), абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы больного (или записей, или запоминающего устройства для данных показателей подачи инсулина) в результате множества суточных введений. Например, в соответствии с раскрытыми в настоящем документе вариантами осуществления, в основе реализации АА-системы лежат данные от CGM и инсулиновой помпы или данные о ручном введении инсулина. Тем не менее, в соответствии с альтернативными вариантами осуществления компоненты АА-системы можно реализовать без CGM или инсулиновой помпы, хотя для осуществления вычислительных операций необходимо будет в значительной мере изменить временную шкалу. Например, можно рассчитать характеристики "совокупного эффекта" на основе данных от SMBG и инсулиновой помпы, хотя для такой методики может быть необходимо намного больше таких характеристик "совокупного эффекта" для получения точного представления поведенческой особенности больного. В качестве дополнительного примера, SMBG-устройство можно использовать с ручным устройством для введения инсулина, таким как шприц-ручка с инсулином, игла или аналогичный тип устройств.
Выходящие данные 2: подача 28 инсулина согласно данным блока ретроактивной оценки безопасности. Эта часть подсистемы основанной на ретроактивной оценке рисков безопасности анализирует хронологическую запись и производит ретроактивный расчет основанного на оценке рисков коэффициента ослабления потребности в инсулине в отношении записи подачи инсулина больному. Согласно одному варианту осуществления способа основанный на оценке рисков коэффициент ослабления (альтернативно - ограничение инсулина) будет рассчитан согласно [30]:

где R(t, τ) представляет собой меру риска гипогликемии между моментами времени t и t+τ на основе хронологической записи данных BG и инсулина до момента времени t, на основе симметризации BG функции в [34], a kpatient представляет собой специфичный для больного коэффициент "агрессивности". Существуют другие способы расчета коэффициентов ослабления, в том числе способы на основе оценки активного инсулина больного до момента времени t и поправки измеренного значения BG в момент времени t по поправочному коэффициенту больного.
Иллюстративный ключевой этап варианта осуществления по настоящему изобретению (без ограничения) заключается в том, что система (и соответствующий способ) изыскивает системность в ретроактивно рассчитанных коэффициентах ослабления. В частности, система рассчитывает ядерные оценки плотности ϕ(R(t,τ)) в 24 одночасовых ячейках, представляющих день лечения больного, а затем выводит больному среднее ослабление уровня, которое было бы приемлемо в каждом сегменте длительностью час. В этом случае также больной может использовать эту информацию для снижения своих собственных внутренних порогов для принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем.
Компонент 2: блок основанной на "совокупном эффекте" адаптационной модели больного.
Части системы, предназначенные для основанной на "совокупном эффекте" адаптационной модели больного, проиллюстрированы на Фиг. 6. Модель, которая производит АА-система, может включать (без ограничения) два следующих основных компонента: (i) динамическая модель метаболической системы больного и (ii) соответствующая, выведенная хронология поведенческих характеристик "совокупного эффекта", которые объясняют вариабельность уровня глюкозы в хронологической записи с помощью динамической модели. В соответствии с одним аспектом основанная на "совокупном эффекте" адаптационная модель больного представляет собой без ограничения формальное представление в математической форме профилей приема пищи, как те, что представлены на Фиг. 1, но также с учетом влияния других отклонений системы, таких как физическая деятельность и периоды сна/бодрствования (фигура 3).
Метаболическая модель, описывающая индивидуальные физиологические особенности больного, обеспечивает представление в математическом виде динамической взаимосвязи перорально потребленных углеводов d (г/мин), физической деятельности e (кал/мин), подкожного инсулина u (ед./ч) и одномерного массива данных χ метаболического состояния больного, элементы которого включают концентрации глюкозы и инсулина (мг/дл) в различных отделах организма и углеводной массы (мг) в кишечнике. Абстрактно, такую взаимосвязь можно описать как набор нелинейных дифференциальных уравнений для дискретного времени:


где F и G являются нелинейными уравнениями системы, и θ(k) является одномерным массивом значений параметров, которые характерны для больного, таких как масса тела, значения распределения в различных частях, различные временные постоянные, с помощью которых описывают скорости всасывания и выведения между различными частями, некоторые из которых подвержены изменению как временная функция k. Это нелинейное представление может быть линеаризовано вблизи любых необходимых рабочих точек (например, равновесной концентрации глюкозы) с получением линейной динамической модели:


где х представляет собой одномерный массив дифференциалов состояния метаболизма (от рабочей точки), uδ (ед./ч) представляет собой отклонение в подаче инсулина от равновесной (базальной) дозы подачи инсулина у больного, А, Bu, Bd, Be представляют собой матрицы пространств состояний линейной модели, а y(k) представляет собой отклонение BG от необходимой рабочей точки. (Следует отметить, что зависимость от θ(k) заложена в матрицах пространств состояний А, Bu, Bd, Be.)
Следует понимать, что альтернативно динамические взаимосвязи могут быть описаны как набор нелинейных дифференциальных уравнений для непрерывного времени:
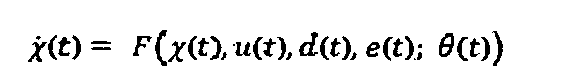

Некоторые новые элементы основанной на "совокупном эффекте" адаптационной модели больного без ограничения описаны ниже.
Алгоритм оценки 34 совокупного эффекта. Этот элемент основанной на "совокупном эффекте" адаптационной модели больного формирует "хронологию" виртуальных входящих данных системы (также известных как "совокупный эффект"), которая согласовывает хронологическую запись BG 22 и подачу инсулина 32 у больного. Более конкретно, с учетом записи концентрации BG и подачи инсулина у больного, {BG(k)}k∈day и {u(k)}k∈day, совокупный эффект, который согласовывает хронологическую информацию, представляет собой одномерный массив виртуальных входящих данных по углеводам, {dn.e.(k)}k∈day, который минимизирует интеграл вероятности ошибки:
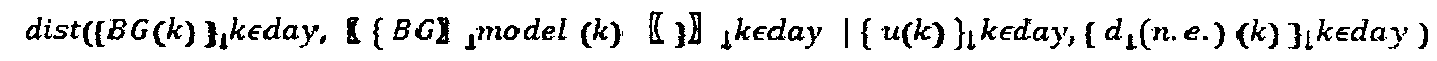
где dist является мерой различия двух одномерных массивов концентрации BG (в этом случае фактической BG по отношению прогнозируемой моделью BG) с учетом фиксированной записи подачи инсулина {u(k)}k∈day и возможного одномерного массива совокупного эффекта {dn.e.(k)}k∈day.
Следует отметить, что полученный оптимальный одномерный массив совокупного эффекта (также называемый характеристикой 38 совокупного эффекта) {dn.e.(k)}k∈day оптимально согласовывает данные по BG и инсулину, собранные от больного посредством сигнала виртуальных углеводов, который собирает информацию о всех влияниях внешних факторов на больного в виде отдельного сигнала внешней помехи, измеряемого в (мг/мин.). Если характеристика 38 совокупного эффекта является положительной, то это может соответствовать фактическому приему еды больным или это может соответствовать периоду дня, в котором больной испытывает повышенную чувствительность к инсулину. Если характеристика 38 совокупного эффекта является отрицательной, то это может соответствовать тому, что больной занимается интенсивной физической деятельностью или физической нагрузкой.
Следует отметить, что рассчитанная характеристика 38 совокупного эффекта косвенно является функцией физиологической модели больного, параметризованной по θ(k). Таким образом вероятно, что плохо адаптированная физиологическая модель дает нетипичные характеристики 38 совокупного эффекта, а побочный эффект хорошо адаптированной физиологической модели представляет собой набор характеристик совокупного эффекта, которые хорошо соответствуют записи или памяти дневных видов деятельности больного, поведенческих особенностей в питании и физической нагрузке, а также самостоятельного лечения.
Возможны различные типы измерения различий для оценки "совокупного эффекта" больного, включая взвешенные l1, l2 и l∞ критерии. Комбинация l2 критерия с линеаризированной версией физиологической модели больного делает особенно легким расчет суточного совокупного эффекта.
Корректор 35 модели: применение методик "идентификации системы" для рекурсивной коррекции параметров динамической модели является общепринятой практикой. В контексте основанной на данных модели лечении сахарного диабета такие методики делают возможной оценку параметров {θ(k)}k∈day физиологической модели больного, включая суточную вариабельность вследствие циркодианного ритма больного. Были использованы многие методики, включая подбор кривой данных линейным методом наименьших квадратов, параметрическая и непараметрическая идентификация системы, адаптационная рекурсивная оценка. Все такие методики работают для обеспечения внутрисистемной согласованности модели с данными, обычно принимая "точные сведения" входящих данных больного (приемы пищи и физическая нагрузка) за допустимые. Конечно, первоначальные сведения о точном содержании и времени приемов пищи и физической нагрузки возможны лишь в клинических условиях. И, зачастую, необходимость прохождения больным такого тестирование для отслеживания в долгосрочной перспективе вариабельности не является экономически оправданной.
Согласно аспекту варианта осуществления настоящее изобретение относится, помимо прочего, к решению последних проблем путем введения понятия совокупного эффекта в долгосрочную адаптацию параметров физиологической модели больного. Как упомянуто выше, побочный эффект хорошо адаптированной физиологической модели представляет собой набор характеристик 38 совокупного эффекта, которые хорошо соответствуют записи или памяти дневных видов деятельности больного, поведенческих особенностей в питании и физической нагрузке, а также самостоятельного лечения. В частности, в предлагаемой системе (и способе, и машиночитаемом носителе) может быть использована рекурсивная процедура для коррекции физиологических параметров больного на основе как (i) способности динамической модели прогнозировать будущий BG на основе известных входящих данных, так и (ii) способности модели выводить характеристики 38 совокупного эффекта, которые согласуются с записью поведенческих особенностей в питании, физической нагрузке и самостоятельного лечения. С математической точки зрения корректор основанной на совокупном эффекте модели имеет форму

где U является рекурсивной функцией коррекции параметров, в основе которой может лежать градиент, BGres является одномерным массивом ошибок прогноза модели BG (погрешностей), a NEres является одномерным массивом ошибок между рассчитанной характеристикой совокупного эффекта и записью фактических (проверенных) входящих поведенческих данных больного. На практике, оправдана коррекция модели на множественных временных шкалах. Например, коррекции параметра можно рассчитывать ежедневно на основе погрешностей BG:

а коррекции на основе несоответствия совокупного эффекта можно рассчитывать на временной шкале с большими временными интервалами, например, один раз в неделю или в месяц:

Компонент 3 - блок ретроактивной оценки оптимальной подачи инсулина
Части системы, предназначенные для ретроактивной оценки оптимальной подачи инсулина, проиллюстрированы на Фиг. 7. Одним из ключевых элементов подсистемы ретроактивной оценки оптимальной подачи инсулина без ограничения является (i) анализатор 42 ретроспективного оптимального контроля и (ii) модуль 44 для извлечения ретрооптимальной базальной дозы, в обоих из которых используется основанная на "совокупном эффекте" адаптационная модель больного, которая описана в последующих абзацах.
Анализатор 42 ретроспективного оптимального контроля Такой элемент подсистемы ретроактивной оценки оптимальной подачи инсулина предназначен для ретроактивного расчета, какой была бы оптимальная скорость подачи инсулина больному на протяжении предопределенного периода времени в хронологии с учетом, что нарушения в системе являются именно хронологическими характеристиками 38 совокупного эффекта, рассчитанными для больного на протяжении такого интервала времени. Так, для каждой "хронологии" характеристик совокупного эффекта существует соответствующая "хронология" скоростей подачи инсулина, в которой учтены приемы пищи, физическая нагрузка и поправки на каждый день в рассматриваемом интервале времени. Например, связав с любым днем в хронологической записи, имеем

т.е. существует связь характеристики 38 совокупного эффекта для заданного дня и основанного на модели ответа контроллера 42 оптимального уровня. Такие одномерные массивы оптимальных ответов можно собрать и проанализировать и их можно непосредственно представить больному для обзора по дням лечения инсулином. Конкретная форма такого анализа принимает вид описанного ниже блока 46 для извлечения ретрооптимальной базальной дозы.
Можно отметить, что анализатор 42 ретроспективного оптимального контроля использует оба компонента основанной на "совокупном эффекте" адаптационной модели больного, т.е. как "хронологию" рассчитанных для больного характеристик совокупного эффекта, так и адаптированную физиологическую модель больного.
Полезное свойство такой архитектуры без ограничений заключается в том, что ошибки в модели больного (т.е. θ, не адаптированная под больного) не оказывают большого влияния на анализ ретроспективного оптимального контроля. Причина этого заключается в том, что несмотря на то, что θ может быть исключена, характеристики совокупного эффекта, рассчитанные для больного, согласовываются с фактическими данными по инсулину и BG для больного посредством модели. Поскольку θ является близким значением ("приблизительным"), то ответы в отношении оптимальных контролей будут все еще адаптированы под больного.
Для расчета ответов {uopt(k)}k∈day в отношении оптимального контроля можно использовать различные типы методов оптимального контроля (известные из уровня техники, например), в том числе, например, прогностические алгоритмы контроля детерминистической и стохастической моделей [20, 27, 38, 45]. Схема контроля без обратной связи (OLFC) из [47] особенно хорошо подходить согласно различным вариантам осуществления по настоящему изобретению.
Согласно новому аспекту варианта осуществления настоящее изобретение без ограничения относится к идее, способу и системе на основе (i) подачи хронологии характеристик 38 совокупного эффекта больного в различные типы алгоритмов оптимального контроля и (ii) ретроактивного анализа оптимальных ответов и информировании больного с помощью результатов сравнительного анализа.
Блок 44 для извлечения ретрооптимальной базальной дозы. Такой элемент подсистемы ретроактивной оценки оптимальной подачи инсулина предназначен для (i) приема "хронологии 43" оптимальных ответов контроля, рассчитанных с помощью анализатора 42 ретроспективного оптимального контроля, и (ii) извлечение компонентов из оптимальных ответов, которые соответствуют важным, но случайным событиям (т.е. вычитания отдельных количеств инсулина, связанных с временными базальными дозами вблизи физической нагрузки). Остальное расписание подачи инсулина соответствует представлению "оптимального" базального паттерна для больного на каждый день в хронологической записи
Затем блок 44 для извлечения ретрооптимальной базальной дозы ищет согласованность в ретроактивно рассчитанных оптимальных базальных дозах. В частности, система рассчитывает ядерные оценки плотности оптимальных базальных доз в 24 одночасовых ячейках, представляющих день лечения больного, а затем выводит больному средний уровень базального инсулина 46, который был бы приемлем в каждом сегменте длительностью час. Больной может использовать эту информацию для (i) принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем или (ii) уточнения его/ее долгосрочного профиля базальных доз.
Компонент 4 - рекомендация по адаптивной поправочной дозе инсулина по запросу пользователя
Некоторые иллюстративные части системы, предназначенные для рекомендации по адаптивной поправочной дозе инсулина по запросу пользователя, проиллюстрированы на Фиг. 8. Основной целью, помимо прочих, этого компонента адаптационной рекомендательной системы (и соответствующего способа) является предоставление рекомендации по поправочной дозе инсулина на данный момент больному на основе как (i) хронологической записи 22, 32, 52, так и (ii) результатов измерений CGM/SMBG и данных 62 от инсулиновой помпы в режиме реального времени. Один из первых этапов в такой системе может заключаться в разработке стохастической модели предстоящих поведенческих нарушений. С помощью этой модели можно рассматривать соответствующие поправочные количества инсулина, которые предвосхищают предстоящие приемы пищи и физическую нагрузку.
Некоторыми ключевыми элементами без ограничения подсистемы рекомендации по адаптивной поправочной дозе инсулина по запросу пользователя могут быть (i) блок 54 для ретроспективного определения приема пищи и физической нагрузки, (ii) блок 56 для стохастического моделирования приема пищи и физической нагрузки и (iii) блок 58 рекомендации поправочного болюса по запросу пользователя, описанные в последующих абзацах. Эти элементы подсистемы могут работать совместно, а также в каждом элементе имеет место отдельное независимое значение.
Блок 54 для ретроспективного определения приема пищи и физической нагрузки. Этот элемент подсистемы рекомендации по адаптивной поправочной дозе инсулина по запросу пользователя предназначен для согласования 55 текущей "хронологии" характеристик 38 "совокупного эффекта" больного с хронологической записью признанных больным связанных с приемами пищи и физической нагрузкой событий с получением подтвержденной (высоко достоверной) записи релевантных поведенческих особенностей больного. Блок 54 для ретроспективного определения приема пищи и физической нагрузки изыскивает несоответствия между (i) характеристиками 38 совокупного эффекта, рассчитанными из доступных данных по BG и инсулину для больного, и (ii) связанными с приемом пищи и физической нагрузкой событиями 55, которые подтверждены 62 больным с помощью пользовательского интерфейса систем. При появлении несоответствий блок 54 для ретроспективного определения приема пищи и физической нагрузки предлагает возможные решения, такие как "Возможно между 1РМ и 2РМ у Вас был неподтвержденный прием пищи?" или "Есть признак, что Вы были заняты интенсивной физической деятельностью между 3РМ и 3:30РМ. Так ли это?" Ответы от больного затем учитывают для формирования конечной подтвержденной записи о релевантных видах деятельности больного.
По сути, блок 54 для ретроспективного определения приема пищи и физической нагрузки использует способ анализа характеристик 36 совокупного эффекта для получения отдельных оценок связанных с приемом пищи и физической нагрузкой событий. В основе способа может лежать, помимо прочего, (i) выявление значимого локального экстремума характеристик совокупного эффекта, (ii) расчет площадей под временными интервалами, которые соответствуют приемам пищи и физической нагрузке, (iii) расчет наиболее вероятного времени связанных с приемом пищи и физической нагрузкой событий, а затем (iv) подтверждение, что полученная оценка связанных с приемом пищи и физической нагрузкой поведенческих особенностей дает прогнозируемые моделью кривые BG, которые близки к фактической записи.
Блок 56 для стохастического моделирования приема пищи и физической нагрузки. Этот элемент подсистемы рекомендации по адаптивной поправочной дозе инсулина по запросу пользователя предназначен для сбора согласованной (подтвержденной) хронологии описанных выше поведенческих событий 55, а затем создания стохастической модели 57, которая описывает время и содержание приемов пищи и физической нагрузки. Модель 57 фактически описывает ежедневное поведение больного в виде последовательности неперекрывающихся связанных с приемом пищи и физической нагрузкой режимов. Каждый режим описан в виде (i) наиболее раннего возможного времени, в которое может "произойти" нарушение (например, наиболее раннее возможное время завтрака), (ii) наиболее позднего возможного времени начала нарушения (например, наиболее позднее возможное время завтрака) и (iii) распределения относительной частоты для моментов времени, в которые начинается нарушение в пределах режима, который также предусматривает возможность того, что нарушение будет "пропущено" [67].
В этом случае одним из ключевых новых аспектов является способ, с помощью которого определяют режимы приема пищи из согласованной хронологии связанных с приемом пищи и физической нагрузкой событий 55 (на основе кластерного анализа) для оценки распределения относительной частоты времени приема пищи в пределах режима и для характеристики случайной переменной, которая описывает величину связанного с приемом пищи и физической нагрузкой нарушения, которое ассоциировано с режимом.
Блок 58 рекомендации поправочного болюса. Этот элемент подсистемы рекомендации по адаптивной поправочной дозе инсулина по запросу пользователя предназначен для непрерывного мониторинга состояния больного и предложения рекомендации 59 по поправочной дозе инсулина в момент, когда больной ее запрашивает, на основе (i) описанной выше стохастической модели 57 для предстоящих поведенческих нарушений и (ii) модели текущего физиологического состояния больного (т.е. динамическая модель метаболической системы больного), что позволяет сделать прогноз влияния различных альтернативных поправочных количеств инсулина. Идея системы поправки в рекомендательном режиме на запрос пользователя проиллюстрирована на Фиг. 9. На Фиг. 9 с помощью графика проиллюстрирован пример системы адаптивной поправочной дозы инсулина по запросу пользователя. Система и способ предусматривают, что (i) больной руководит расчетом инсулиновых болюсов в моменты приема пищи с помощью традиционных способов (ii) больной применяет предлагаемую рекомендательную систему для принятия мер в связи с незапланированной гипергликемией, к примеру в показанное на фигуре время t. При активации больным рекомендательной системы он/она имеет возможность ввести информацию касательно времени и содержания следующего приема пищи, а система обрабатывает с коррекцией стохастической модели 56 времени приема пищи и физической нагрузки (называемой поведенческий профиль приема пищи и проиллюстрированной на фигуре в виде затемненных распределений вероятности). Затем система рассчитывает совет по дозе инсулина, которая оптимальна в отношении будущей (случайной) метаболической кривой больного. В частности, рекомендуемый болюс рассчитывают в качестве оптимального решения квадратичной задачи с неопределенной линией временного горизонта, характеризуемой неясным моментом времени, когда в следующих раз больной будет есть.
Одним из ключевых преимуществ предложенного способа без ограничения является то, что он является малоинвазивным и предполагает рекомендацию в ответ на взаимодействие пользователя с системой. С учетом того, что в конечном счете больной "принимает решение", он/она может легко отвергнуть решение системы в случае немоделируемых метаболических нарушений, например, интенсивной физической деятельности. Другим преимуществом системы, помимо прочего, является то, что она предусматривает реализацию больным "традиционного" принципа введения болюса во время приема пищи, включая вариант реализации увеличенного болюса при приеме пищи для случаев приема пищи с высоким содержанием жиров. Представленная в настоящем документе структура рассчитывает советы по количеству инсулина в поправочном болюсе на основе модели метаболизма больного, и такая система может адаптироваться либо к "усредненной для контингента" модели, либо к специфичным для больного моделям метаболизма. Кроме того, рекомендованные болюсы инсулина рассчитаны с учетом модели индивидуальных привычек питания у больного. В частности, система всегда предупреждает о возможности следующего приема пищи и готовится к оптимизации советов по поправке с учетом эмпирической стохастической модели времени приема пищи и количества пищи (включая вероятность того, что прием пищи будет пропущен). Зная, что больной ответственен за болюсы в моменты приема пищи, система будет избегать осуществления больших поправок непосредственно сразу после прогнозируемых приемов пищи. Наконец, выдаваемые системой советы по количеству инсулина прогнозируют связанное с лечением поведение больного во время следующего приема пищи, зная, что больной будет рассчитывать болюс в момент приема пищи на основе своего соотношения инсулина к углеводам (CR) и поправочного коэффициента (CF).
Реализация адаптационной рекомендательной системы
Фиг. 10-15 представляют собой скриншоты одной возможной реализации АА-системы на персональном компьютере. Аналогичные реализации возможны на планшете, портативных компьютерах (например, лаптопах или ноутбуках), с помощью интернет-приложений или сетевых приложений, сотовых телефонах или на смартфоне, к примеру PDA (с соответственно уменьшаемыми по желанию или необходимости текстом и графическими деталями). В частности:
Фиг. 10 представляет собой изображение начального экрана, где систему настраивают под конкретного человека;
на Фиг. 11 приведено изображение экрана, который представляет собой возможность ввода данных о потребляемых углеводов (приемах пищи) и физической деятельности по времени и количеству;
на Фиг. 12 приведено изображение экрана, который представляет собой изображение рассматриваемого дня, включающее кривые глюкозы и наложенные зависящие от особенностей поведения события;
на Фиг. 13 и 14 приведены изображения экранов, которые представляют собой суточные профили с различным уровнем детализации (простой на Фиг. 13 и с добавленными графиками вероятностей на Фиг. 14);
на Фиг. 15 приведено изображение экрана, который представляет собой экран рекомендаций, включающий выявленные периоды риска гипер- и гипогликемии в ходе обычного выходного дня (заштрихованные красные в верхнем сегменте экрана) и рекомендацию системы уменьшить дозу инсулина во избежание гипогликемии (пунктирная линия в нижнем сегменте экрана);
Фиг. 16 представляет собой блок-схему, которая иллюстрирует систему 130, включающую компьютерную систему 140 и связанное подключение к интернету 11 согласно которой можно реализовать вариант осуществления. Такую конфигурацию обычно применяют для компьютеров (главных компьютеров) с подключением к интернету 11, и выполняющих серверное или клиентское программное обеспечение (или их комбинацию). В компьютере-трансляторе, таком как лаптоп, конечном компьютере и серверах ретрансляции, например, а также любом описанном в настоящем документе компьютере или устройстве обработки данных, могут быть использованы конфигурация компьютерной системы и подключение к интернету, показанные на Фиг. 16. Систему 140 можно применять в качестве портативного электронного устройства, такого как ноутбук/лаптоп, мультимедийный проигрыватель (например, МР3-проигрыватель или видеопроигрыватель), сотовый телефон, карманный персональный компьютер (PDA), устройство обработки изображения (например, цифровая камера или видеорегистратор) и/или любые другие переносные вычислительные устройства или комбинация любых таких устройств. Следует отметить, что несмотря на то, что на Фиг. 16 проиллюстрированы различные компоненты компьютерной системы, она не предназначена для представления какой-либо конкретной архитектуры или способа взаимосвязи компонентов, поскольку такие детали не уместны для настоящего изобретения. Также будет понятно, что сетевые компьютеры, карманные компьютеры, сотовые телефоны и другие системы обработки данных, которые имеют меньшее количество компонентов и, возможно, также можно использовать более количество компонентов. Компьютерной системой на фиг. 16, например, может быть компьютер Apple Macintosh, или Power Book, или совместимый с IBM PC. Компьютерная система 140 включает шину 137, соединительный провод или другой механизм связи для передачи информации и устройство 138 обработки данных, обычно в форме интегральной схемы, связанное с шиной 137 для обработки информации и выполнения выполняемых компьютером команд. Компьютерная система 140 также включает основную память 134, такую как запоминающее устройство с произвольным доступом (RAM) или другое устройство динамической памяти, соединенное с шиной 137 для хранения информации и команд, подлежащих выполнению устройством 138 обработки данных.
Основную память 134 также можно применять для хранения временных переменных или другой промежуточной информации в ходе выполнения команд, подлежащих выполнению устройством 138 обработки данных. Компьютерная система 140 дополнительно включает постоянное запоминающее устройство (ROM) 136 (или другую энергонезависимую память) или устройство статической памяти, соединенное с шиной 137, для хранения статической информации и команд для устройства 138 обработки данных. Устройство 135 хранения информации, такое как магнитный диск или оптический диск, накопитель на жестких магнитных дисках для считывания с жесткого диска и записи на него, накопитель на магнитных дисках для считывания с магнитного диска и записи на него и/или привод оптических дисков (такой как DVD) для считывания со съемного оптического диска и записи на него, соединено с шиной 137 для хранения информации и команд. Накопитель на жесткий магнитных дисках, накопитель на магнитных дисках и привод оптических дисков можно присоединить к системной шине с помощью, соответственно, интерфейса накопителя на жесткий магнитных дисках, интерфейса накопителя на магнитных дисках и интерфейса привода оптических дисков. Приводы и связанные с ними машиночитаемые носители обеспечивают энергонезависимое запоминающее устройство машиночитаемых команд, структур данных, программных модулей и других данных для вычислительных устройств общего назначения. Обычно компьютерная система 140 включает операционную систему (OS), хранящуюся в энергонезависимом запоминающем устройстве, для управления компьютерными ресурсами и обеспечивает приложениям и программам доступ к компьютерным ресурсам и интерфейсам. Операционная система обычно обрабатывает системные данные и пользовательские входящие данные и отвечает путем распределения задач и внутренних системных ресурсов и управления ними, к примеру, контроля и распределения памяти, назначения приоритета запросов к системе, контроля устройств ввода и вывода, содействия работы сети и управления файлами. Неограничивающими примерами операционных систем являются Microsoft Windows, Mac OS X и Linux.
Термин "устройство обработки данных" понимают как включающий любую интегральную схему или другое электронное устройство (или группу устройств), способных выполнять операцию по меньшей мере по одной команде, включая без ограничения устройство обработки данных с сокращенным набором команд (RISC), CISC-микроустройства обработки данных, блоки микроконтроллера (MCU), CISC-центральные устройства обработки данных (CPU) и устройства для цифровой обработки сигналов (DSP). Аппаратное обеспечение таких устройств может быть встроено на отдельном основании (например, кремниевом кристалле) или распределено среди двух или более оснований. Более того, различные функциональные аспекты устройства обработки данных могут быть реализованы отдельно в виде программного обеспечения или аппаратно-программного обеспечения, связанного с устройством обработки данных.
Компьютерная система 140 может быть связана при помощи шины 137 с дисплеем 131, таким как электронно-лучевая трубка (CRT), жидкокристаллический дисплей (LCD), монитор с плоским экраном, монитор с сенсорным экраном или подобные устройства для отображения текстовых и графических данных пользователю. Дисплей может быть соединен с помощью видеоадаптера для поддержки дисплея. Дисплей обеспечивает пользователю изображение, ввод и/или редактирование информации, которые имеют отношение к операции системы. Устройство 132 ввода, включая буквенно-цифровые и другие коды, соединено с шиной 137 для передачи информации и выбора команд для устройства 138 обработки данных. Другим типом пользовательского устройства ввода является устройство управления 133 курсором, такое как мышь, трекбол или клавиши управления курсором, для передачи информации управления и выбора команд устройству 138 обработки данных для контроля передвижения курсора на дисплее 131. Такое устройство ввода обычно имеет две степени свободы по двум осям, первой оси (например, x) и второй оси (например, y), которые позволяют устройству уточнять положение на плоскости.
Компьютерную систему 140 можно применять для реализации описанных в настоящем документе способов и методик. Согласно одному варианту осуществления такие способы и методики выполняются компьютерной системой 140 в ответ на выполнение устройством 138 обработки данных одной или нескольких последовательностей из одной или нескольких команд, содержащихся в основной памяти 134. Такие команды могут быть считаны в основную память 134 с другого машиночитаемого носителя, такого как устройство 135 хранения информации. Выполнение последовательностей команд, содержащихся в основной памяти 134, заставляет устройство 138 обработки данных выполнять этапы описанного в настоящем документе способа. Согласно альтернативным вариантам осуществления для реализации структуры проводную схему можно применять вместо или в сочетании с командами программного обеспечения. Таким образом, варианты осуществления по настоящему изобретению не ограничены какой-либо конкретной комбинацией схем аппаратного обеспечения и программного обеспечения.
Используемый в настоящем документе термин "машиночитаемый носитель" (или "машинно-считываемый носитель") является открытым термином, который относится к любому носителю или любой памяти, которые принимают участие в передаче команд устройству обработки данных (такому как устройство 138 обработки данных) для выполнения или другому механизму для хранения или передачи информации в считываемой машиной (например, компьютером) форме. Такой носитель может хранить выполняемые компьютером команды, которые подлежат выполнению обрабатывающим элементом и/или алгоритмом управления, и данные, которыми оперируют обрабатывающий элемент и/или алгоритм управления, и может принимать множество форм, включая без ограничения энергонезависимый носитель, энергозависимый носитель и среда передачи данных. Среды передачи данных включают коаксиальные кабели, медный провод и оптоволокна, в том числе провода, которые формируют шину 137. Среды передачи данных также могут принимать форму акустических или световых волн, таких как образуемые в ходе радиоволновых и инфракрасных передач данных, или другую форму передаваемых сигналов (например, несущие волны, инфракрасные сигналы, цифровые сигналы и т.д.). Общеизвестные формы машиночитаемых носителей включают, например, гибкий магнитный диск, гибкий диск, жесткий диск, магнитную ленту или любой другой магнитный носитель, CD-ROM или другой оптический носитель, перфокарты, перфоленту и другие физические носители с паттернами из отверстий, RAM, PROM и EPROM, FLASH-EPROM, любую другую интегральную схему памяти или плату оперативной памяти, несущую волну, которые описаны в настоящем документе ниже, или любой другой носитель, с которого может считывать компьютер.
Различные формы машиночитаемых носителей могут быть связаны с переносом одной или нескольких последовательностей из одной или нескольких команд устройству 138 обработки данных для выполнения. Например, команды изначально могут быть на магнитном диске удаленного компьютера. Удаленный компьютер может загружать команды в свою динамическую память и посылать команды по телефонной линии с помощью модема. Локальный по отношению к компьютерной системе 140 модем может получать данные по телефонной линии и применять инфракрасный передатчик для преобразования данных в инфракрасный сигнал. Приемник инфракрасного излучения может получать данные, переносимые в инфракрасном сигнале, а соответствующая схема может размещать данные по шине 137. Шина 137 переносит данные в основную память 134, из которой устройство 138 обработки данные получает и выполнят команды. Получаемые основной памятью 134 команды необязательно можно хранить в устройстве 135 хранения информации либо до, либо после выполнения устройством 138 обработки данных.
Компьютерная система 140 также включает коммуникационный интерфейс 141, соединенный с шиной 137. Коммуникационный интерфейс 141 обеспечивает связь для двухсторонней передачи данных с сетевым подключением 139, которое соединено с локальной сетью 111. Например, коммуникационный интерфейс 141 может представлять собой карту для цифровой сети с предоставлением комплексных услуг (ISDN) или модем для обеспечения соединения для передачи данных с соответствующим типом телефонной линии. В качестве другого неограничивающего примера коммуникационный интерфейс 141 может представлять собой карту локальной сети (LAN) для обеспечения соединения для передачи данный с совместимой LAN. Например, можно использовать Ethernet-соединение на основе стандарта IEEE802. 3, такое как 10/100BaseT, 1000BaseT (гигабитный Ethernet), 10 гигабитный Ethernet (10 GE, или 10 GbE, или 10 GigE согласно IEEE Std 802. 3ае-2002 в качестве стандарта), 40 гигабитный Ethernet (40 GbE), или 100 гигабитный Ethernet (100 GbE согласно Ethernet-стандарта IEEE Р802. 3ba), которые описаны в Cisco Systems, Inc. Publication number 1-587005-001-3 (6/99), "Internetworking Technologies Handbook", Chapter 7: "Ethernet Technologies", pages 7-1 to 7-38, которая включена в своем полном объеме для всех целей как если бы была полностью изложена в настоящем документе. В таком случае коммуникационный интерфейс 141 обычно включает LAN-трансивер или модем, такой как LAN91C111 10/100 Ethernet-трансивер от Standard Microsystems Corporation (SMSC), описанный в спецификации от Standard Microsystems Corporation (SMSC) "LAN91C111 10/100 Non-PCI Ethernet Single Chip MAC+PHY" Data-Sheet, Rev. 15 (02-20-04), которая включена в своем полном объеме для всех целей как если бы была полностью изложена в настоящем документе.
Также могут быть реализованы беспроводные соединения. В любой такой реализации коммуникационный интерфейс 141 отсылает и получает электрические, электромагнитные или оптические сигналы, которые несут потоки цифровых данных, представляющие различные типы информации.
Сетевое соединение 139 обычно обеспечивает передачу данных через одну или несколько сетей к другим устройствам ввода-вывода данных. Например, сетевое соединение 139 может обеспечивать связь посредством локальной сети 111 с главным компьютером или оборудованием передачи данных под управлением поставщика услуг Интернет (ISP) 142. ISP 142, в свою очередь, обеспечивает службы передачи данных посредством международной сети передачи пакетных данных Интернет 11. Как в локальной сети 111, так и в Интернете 11 применяют электрические, электромагнитные или оптические сигналы, которые несут потоки цифровых данных. Сигналы по различным сетям и сигналы по сетевому соединении 139 и через коммуникационный интерфейс 141, которые несут цифровые данные к компьютерной системе 140 и от нее, являются иллюстративными формами несущих волн, которые переносят информацию.
Полученный код может выполняться устройством 138 обработки данных по мере его получения и/или храниться в устройстве 135 хранения информации или другом энергонезависимом запоминающем устройстве для последующего выполнения. Таким образом, компьютерная система 140 может получать код приложения в форме несущей волны.
Идея ретроактивной оценки риска гипогликемии, ретроактивной оценки уменьшения подачи инсулина на основе риска и сообщения о том, как предупредить гипогликемию, а также получения других связанных преимуществ можно реализовать и использовать с помощью соответствующих устройств обработки данных, сетей, компьютерных систем, Интернета и компонентов и функций согласно раскрытым в настоящем документе схемам.
Публикации
Следующие патенты, патентные заявки и публикации, которые перечислены ниже и по всему настоящему документу включены в настоящий документ с помощью ссылки в полном их объеме и которые не являются частью уровня техники по отношению к настоящему изобретению путем включения в настоящий раздел.
1. Albisser AM, Leibel BS, Ewart TG, Davidovac Z, Botz CK, Zinggg W. An artificial endocrine pancreas. Diabetes, 23: 389-396, 1974.
2. Bellazzi R, Nucci G, Cobelli C: The subcutaneous route to insulin-dependent diabetes therapy: closed-loop and partially closed-loop control strategies for insulin delivery and measuring glucose concentration. IEEE Eng Med Biol 20: 54-64, 2001.
3. Bequette BW. Analysis of Algorithms for Intensive Care Unit Blood Glucose Control. J Diabetes Sci Technol, 1: 813-824, 2007.
4. Bergman RN, Ider YZ, Bowden CR, Cobelli C. Quantitative estimation of insulin sensitivity. Am J Physiol. 236: E667-E677, 1979.
5. Boyne M, Silver D, Kaplan J, and Saudek C: Timing of Changes in Interstitial and Venous Blood Glucose Measured With a Continuous Subcutaneous Glucose Sensor. Diabetes, 52: 2790-2794, 2003.
6. Broekhuyse HM, Nelson JD, Zinman B, and Albisser AM: Comparison of algorithms for the closed-loop control of blood glucose using the artificial beta cell. IEEE Trans Biomed Eng BME-28: 678-687, 1981.
7. Brunetti P., Cobelli C., Cruciani P., Fabietti P.G., Filippucci F., Santeusanio F.: A simulation study on a self-tuning portable controller of blood glucose. Int J Artificial Organs 16: 51-57, 1993.
8. Clarke WL and Kovatchev BP. The Artificial Pancreas: How Close We Are to Closing the Loop? Ped Endocrinol Rev, 4: 314-316, 2007.
9. Clarke WL, Cox DJ, Gonder-Frederick LA, Julian DM, Kovatchev BP, Young-Hyman D. The bio-psycho-behavioral model of severe hypoglycemia II: Self-management behaviors. Diabetes Care 22: 580-584, 1999.
10. Clemens AH, Chang PH, Myers RW. The development of Biostator, a glucose-controlled insulin infusion system. Horm Metab Res Supplement, 7: 23-33, 1977.
11. Clemens AH: Feedback control dynamics for glucose controlled insulin infusion system. MedProg Technol 6: 91-98, 1979.
12. Cobelli С and Kovatchev BP. Clinical Trial of Model-Predictive Control Powered by In Silico Studies. Proc. 8th Diabetes Technology Meeting, Bethesda, MD, 2008.
13. Cobelli C, Ruggeri A: Evaluation of portal/peripheral route and of algorithms for insulin delivery in the closed-loop control of glucose in diabetes. A modelling study. IEEE Trans Biomed Eng 30: 93-103, 1983.
14. Cryer PE, Davis SN, Shamoon H. Hypoglycemia in Diabetes. Diabetes Care, 26: 1902-1912, 2003.
15. Cryer PE. Hypoglycaemia: The limiting factor in the glycaemic management of type I and type II diabetes. Diabetologia 45: 937-948, 2002.
16. Cryer ΡΕ. Iatrogenic hypoglycemia as a cause of hypoglycemia-associated autonomic failure in IDDM: A vicious cycle. Diabetes 41: 255-260, 1992.
17. Cryer PE: Hypoglycemia: The Limiting factor in the management of IDDM. Diabetes 43: 1378-1389, 1994.
18. Dassau E, Bequette BW, Buckingham ВA, Doyle FJ 3rd. Detection of a meal using continuous glucose monitoring: implications for an artificial beta-cell. Diabetes Care, 31: 295-300, 2008.
19. Dassau E, Cameron F, Neimeyer G, Chase P, Buckingham B. Real-time Hypoglycemic Prediciton Using Continuous Glucose Monitoring (CGM). Diabetes, 57 Suppl 1, 2008.
20. Dua P, Doyle FJ 3rd, Pistikopoulos EN. "Model-Based Blood Glucose Control for Type 1 Diabetes via Parametric Programming." IEEE Trans Biomed Eng. 53: 1478-1491, 2006.
21. EW, Campbell LV, Chia YO, Meler H, and Lazarus L: Control of blood glucose in diabetics using an artificial pancreas. Aust Ν Ζ J Med 7: 280-286, 1977.
22. Fischer U, Jutzi E, Freyse E-J, and Salzsieder E: Derivation and experimental proof of a new algorithm for the artificial beta-cell based on the individual analysis of the physiological insulin - glucose relationship. Endokrinologie 71: 65-75, 1978.
23. Fischer U, Schenk W, Salzsieder E, Albrecht G, Abel P, and Freyse E-J: Does physiological blood glucose control require an adaptive strategy? IEEE Trans Biomed Eng 34: 575-582, 1987.
24. Fisher ME: A semi closed-loop algorithm for the control of blood glucose levels in diabetics. IEEE Trans Biomed Eng 38: 57-61, 1991.
25. Gold AE, Deary IJ, Frier BM. Recurrent severe hypoglycaemia and cognitive function in type I diabetes. Diabet Med 10: 503-508, 1993.
26. Gonder-Frederick L, Cox D, Kovatchev B, Schlundt D, Clarke W. A biopsychobehavioral model of risk of severe hypoglycemia. Diabetes Care, 20: 661-669, 1997.
27. Hovorka R, Canonico V, Chassin LJ, et al. Nonlinear model predictive control of glucose concentration in subjects with type 1 diabetes. Physiol Meas 25: 905-920, 2004.
28. Hovorka R, Chassin LJ, Wilinska ME, et al. Closing the loop: the ADICOL experience. Diabetes Technol Ther. 6: 307-318, 2004.
29. Hovorka R: Continuous glucose monitoring and closed-loop systems. Diabet Med 23: 1-12, 2006.
30. Hughes CS, S. D. Patek SD, M. Breton MD, and BP Kovatchev. Hypoglycemia Prevention via Pump Attenuation and Red-Yellow-Green "Traffic" Lights using CGM and Insulin Pump Data, J Diab Sci and Tech, 4: 1146-1155, 2010.
31. Klonoff DC: The Artificial Pancreas: How Sweet Engineering Will Solve Bitter Problems. J Diabetes Sci Technol, 1: 72-81, 2007.
32. Kovatchev BP, Clarke WL. Continuous glucose monitoring reduces risks for hypo- and hyperglycemia and glucose variability in diabetes. Diabetes, 56, Supplement 1: 0086OR, 2007.
33. Kovatchev BP, Cox DJ, Farhy LS, Straume M, Gonder-Frederick LA, Clarke, WL. Episodes of Severe Hypoglycemia in Type 1 Diabetes are Preceded, and Followed, within 48 Hours by Measurable Disturbances in Blood Glucose. J of Clinical Endocrinology and Metabolism, 85: 4287-4292, 2000.
34. Kovatchev BP, Cox DJ, Gonder-Frederick LA, and WL Clarke. Symmetrization of the blood glucose measurement scale and its applications, Diabetes Care, 20: 1655-1658, 1997.
35. Kovatchev BP, Straume M, Cox DJ, Farhy LS. Risk analysis of blood glucose data: A quantitative approach to optimizing the control of insulin dependent diabetes. J of Theoretical Medicine, 3: 1-10, 2001.
36. Kulcu E, Tamada JA, Reach G, Potts RO, Lesho MJ: Physiological differences between interstitial glucose and blood glucose measured in human subjects. Diabetes Care, 26: 2405-2409, 2003.
37. Leblanc H, Chauvet D, Lombrail P, Robert JJ: Glycemic control with closed-loop intraperitoneal insulin in type I diabetes. Diabetes Care, 9: 124-128, 1986.
38. Magni L, Raimondo F, Bossi L, Dalla Man C, De Nicolao G, Kovatchev BP, Cobelli C. Model Predictive Control of Type 1 Diabetes: An In Silico Trial J Diabetes Sci Technol, 1: 804-812, 2007.
39. Marliss EB, Murray FT, Stokes EF, Zinman B, Nakhooda AF, Denoga A, Leibel BS, and Albisser AM: Normalization of glycemia in diabetics during meals with insulin and glucagon delivery by the artificial pancreas. Diabetes 26: 663-672, 1977.
40. Nucci G., Cobelli C. Models of subcutaneous insulin kinetics. A critical review. Comput Methods Programs Biomed., 62: 249-57 Review, 2000.
41. Ollerton RL: Application of optimal control theory to diabetes mellitus. Int J Control 50: 2503-2522, 1989.
42. Owens C, Zisser H, Jovanovic L, Srinivasan B, Bonvin D, Doyle FJ 3rd. Run-to-run control of glucose concentrations for people with Type 1 diabetes mellitus. IEEE Trans Biomed Eng. 53: 996-1005, 2006.
43. Palerm CC, Zisser H, Bevier WC, Jovanovic L, Doyle FJ 3rd. Prandial insulin dosing using run-to-run control: application of clinical data and medical expertise to define a suitable performance metric. Diabetes Care. 30: 1131-1136, 2007.
44. Palerm CC, Zisser H, Jovanovič L, Doyle FJ 3rd. A Run-to-Run Control Strategy to Adjust Basal Insulin Infusion Rates in Type 1 Diabetes. J Process Control. 18: 258-265, 2008.
45. Parker RS, Doyle FJ 3rd, Peppas NA. A model-based algorithm for blood glucose control in Type I diabetic patients. IEEE Trans Biomed Eng, 48: 148-157, 1999.
46. Patek SD, Breton MD, Cobelli C, Dalla Man C, and Kovatchev BP. Adaptive meal detection algorithm enabling closed-loop control in type 1 diabetes. Proc. 7th Diabetes Technology Meeting, San Francisco, CA, 2007.
47. Patek SD. Open-Loop Feedback Control under Multiple Disturbance Function Hypotheses, Proc. of the IEEE Conference on Decision and Control, 2010, Atlanta.
48. Pfeiffer EF, Thum Ch, and Clemens AH: The artificial beta cell - A continuous control of blood sugar by external regulation of insulin infusion (glucose controlled insulin infusion system). Horm Metab Res 487: 339-342, 1974.
49. Reichard P, Phil M. Mortality and treatment side effects during long-term intensified conventional insulin treatment in the Stockholm Diabetes Intervention study. Diabetes 43: 313-317, 1994.
50. Reifman J, Rajaraman S, Gribok A, Ward WK. Predictive monitoring for improved management of glucose levels. J Diabetes Sci Technol 1: 478-486, 2007.
51. Renard E: Implantable closed-loop glucose-sensing and insulin delivery: the future for insulin pump therapy, Current Opinion in Pharmacology, 2: 708-716, 2002.
52. Salzsieder E, Albrecht G, Fischer U, and Freyse E-J: Kinetic modeling of the gluco-regulatory system to improve insulin therapy. IEEE Trans Biomed Eng 32: 846-855, 1985.
53. Santiago JV, Clemens AH, Clarke WL, Kipnis DM. Closed-loop and open-loop devices for blood glucose control in normal and diabetic subjects. Diabetes, 28: 71-84, 1979.
54. Schaller HC, Schaupp L, Bodenlenz M, Wilinska ME, Chassin LJ, Wach P, Vering T, Hovorka R, Pieber TR: On-line adaptive algorithm with glucose prediction capacity for subcutaneous closed loop control of glucose: evaluation under fasting conditions in patients with Type 1 diabetes. Diabet Med 23: 90-93, 2006.
55. Selam JL, Micossi P, Dunn FL, and Nathan DM: Clinical trial of programmable implantable insulin pump for type I diabetes, Diabetes Care 15: 877-885, 1992.
56. Sorensen JT: A Physiologic Model of Glucose Metabolism in Man and its Use to Design and Assess Improved Insulin Therapies for Diabetes, Ph. D. dissertation, Dept Chemical Engineering, MIT, 1985.
57.Sparacino G, Zanderigo F, Corazza G, Maran A, Facchinetti A, Cobelli C. Glucose concentration can be predicted ahead in time from continuous glucose monitoring sensor time-series. IEEE Trans Biomed Eng, 54:931-937, 2007.
58. Steil GM, Rebrin K, Darwin C, Hariri F, Saad MF. Feasibility of automating insulin delivery for the treatment of type 1 diabetes. Diabetes 55: 3344-3350, 2006.
59. Stout PJ, Racchini JR, Hilgers ME: A Novel Approach to Mitigating the Physiological Lag between Blood and Interstitial Fluid Glucose Measurements. Diabetes Technol Ther, 6:635-644, 2004.
60. The Diabetes Control and Complications Trial Research Group. Hypoglycemia in the Diabetes Control and Complications Trial. Diabetes 46: 271-286, 1997.
61. The Diabetes Control and Complications Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications of insulin-dependent diabetes mellitus. N Engl J Med 329: 978-986, 1993.
62. Weinzimer SA, Steil GM, Swan KL, Dziura J, Kurtz N, Tamborlane WV: Fully automated closed-loop insulin delivery versus semi-automated hybrid control in pediatric patients with type 1 diabetes using an artificial pancreas. Diabetes Care 31: 934-939, 2008.
63. Wentholt IME, Hart AAM, Hoekstra JBL, DeVries JH. Relationship Between Interstitial and Blood Glucose in Type 1 Diabetes Patients: Delay and the Push-Pull Phenomenon Revisited. Diabetes Technol Ther, 9: 169-175, 2004.
64. Wilinska ME, Chassin LJ, Schaller HC, Schaupp L, Pieber TR, Hovorka R. Insulin kinetics in type-1 diabetes: continuous and bolus delivery of rapid acting insulin. IEEE Trans. Biomed. Eng. 52: 3-12, 2005.
65. Zanderigo F, Sparacino G, Kovatchev B, Cobelli C. Glucose Prediction Algorithms from continuous monitoring: Assessment of accuracy via Continuous Glucose-Error Grid Analysis. J Diabetes Sci Technol, 1: 645-651, 2007
66. Zisser H, Jovanovic L, Doyle FJ 3rd, Ospina P, Owens C. Run-to-Run Control of Meal-Related Insulin Dosing. Diab Technol Ther 7: 48-57, 2005.
67. C.S. Hughes, S.D. Patek, A. Taylor, R. Park, K. Laub-scher, S. Pillutla, M. Breton, and B.P. Kovatchev. In-silico experiments of human eating patterns: Making a case for behavior-informed control of T1DM. In Proc. UKACC International Conference of Control, 2010.
Перечень литературы
Устройства, системы, машиночитаемый носитель и способы различных вариантов осуществления по настоящему изобретению, раскрываемые в настоящем документе, могут использовать аспекты, раскрываемые в следующих ссылках, патентных заявках, патентных публикациях и патентах, которые включены в виде ссылки в полном их объеме и которые не являются частью уровня техники по отношению к настоящему изобретению при помощи включения в настоящий раздел:
A. Международная патентная заявка № PCT/US 2012/043910, Kovatchev, et al., "Unified Platform For Monitoring and Control of Blood Glucose Levels in Diabetic Patients", поданная 23 июня 2012 года.
B. Международная патентная заявка № PCT/US 2012/043883, Kovatchev, et al., "Methods and Apparatus for Modular Power Management and Protection of Critical Services in Ambulatory Medical Devices", поданная 22 июня 2012 года.
C. Международная патентная заявка № PCT/US 2011/029793, Kovatchev et al., под заголовком "Method, System, and Computer Program Product for Improving the Accuracy of Glucose Sensors Using Insulin Delivery Observation in Diabetes", поданная 24 марта 2011 года.
D. PCT/US 2011/028163, Breton, et al., под заголовком "Method and System for the Safety, Analysis and Supervision of Insulin Pump Action and Other Modes of Insulin Delivery in Diabetes", поданная 11 марта 2011 года.
Ε. Международная патентная заявка № PCT/US 2010/047711, Kovatchev, et al., "Tracking the Probability for Imminent Hypoglycemia in Diabetes from Self-Monitoring Blood Glucose (SMBG) Data", поданная 2 сентября 2010 года.
F. Международная патентная заявка № PCT/US 2010/047386, Kovatchev, et al., "System, Method and Computer Program Product for Adjustment of Insulin Delivery (AID) in Diabetes Using Nominal Open-Loop Profiles", поданная 31 августа 2010 года.
G. Международная патентная заявка № PCT/US 2010/040097, Kovatchev, et al., "System, Method, and Computer Simulation Environment for In Silico Trials in Prediabetes and Type 2 Diabetes", поданная 25 июня 2010 года.
Η. Международная патентная заявка № PCT/US 2010/036629, Kovatchev, et al., "System Coordinator and Modular Architecture for Open-Loop and Closed-Loop Control of Diabetes", поданная 28 мая 2010 года (публикация № WO 2010/138848, 2 декабря 2010 года).
I. Международная патентная заявка № PCT/US 2010/025405, Kovatchev, et al., под заголовком "Method, System and Computer Program Product for CGM-Based Prevention of Hypoglycemia via Hypoglycemia Risk Assessment and Smooth Reduction Insulin Delivery", поданная 25 февраля 2010 года.
J. Международная патентная заявка № PCT/US 2009/065725, Kovatchev, et al., filed November 24, 2009, под заголовком "Method, System, and Computer Program Product for Tracking of Blood Glucose Variability in Diabetes from Data."
K. Международная патентная заявка № PCT/US 2008/082063, Magni, et al., под заголовком "Model Predictive Control Based Method for Closed-Loop Control of Insulin Delivery in Diabetes Using Continuous Glucose Sensing", поданная 31 октября 2008 года; заявка на выдачу патента США №12/740,275, Magni, et al., под заголовком "Predictive Control Based System and Method for Control of Insulin Delivery in Diabetes Using Glucose Sensing", поданная 28 апреля 2010 года.
L. Международная патентная заявка № PCT/US 2008/069416, Breton, et al., под заголовком "Method, System and Computer Program Product for Evaluation of Insulin Sensitivity, Insulin/Carbohydrate Ratio, and Insulin Correction Factors in Diabetes from Self-Monitoring Data", поданная 8 июля 2008 года (публикация № WO 2009/009528, 15 января 2009 года); заявка на выдачу патента США №12/665,149, Breton, et al., "Method, System and Computer Program Product for Evaluation of Insulin Sensitivity, Insulin/Carbohydrate Ratio, and Insulin Correction Factors in Diabetes from Self-Monitoring Data", поданная 17 декабря 2009 года.
Μ. Международная патентная заявка № PCT/US 2008/067725, Kovatchev, et al., под заголовком "Method, System and Computer Simulation Environment for Testing of Monitoring and Control Strategies in Diabetes," поданная 20 июня 2008 года, (публикация № WO 2008/157781, 24 декабря 2008 года); Публикация патентной заявки на выдачу патента США №12/664444, Kovatchev, et al., поданная 14 декабря 2009 года, под заголовком "Method, System and Computer Simulation Environment for Testing of Monitoring and Control Strategies in Diabetes", (публикация №2010/0-179768, 15 июля 2010 года).
N. Международная патентная заявка № PCT/US 2008/067723, Patek, et al., под заголовком "LQG Artificial Pancreas Control System and Related Method", поданная 6/20/2008.
О. Заявка на выдачу патента США №12/51,044, Kovatchev, et al., поданная 22 мая 2009 года, под заголовком "Method, System, and Computer Program Product for the Detection of Physical Activity by Changes in Heart Rate, Assessment of Fast Changing Metabolic States, and Applications of Closed and Open Control Loop in Diabetes".
P. Международная патентная заявка № PCT/US 2007/085588, Kovatchev, et al., поданная 27 ноября 2007 года, под заголовком "Method, System, and Computer Program Product for the Detection of Physical Activity by Changes in Heart Rate, Assessment of Fast Changing Metabolic States, and Applications of Closed and Open Control Loop in Diabetes", (публикация № WO 2008/067284, 5 июня 2008 года).
Q. Заявка на выдачу патента США №11/943,226, Kovatchev, et al., поданная 20 ноября 2007 года, под заголовком "Systems, Methods and Computer Program Codes for Recognition of Patterns of Hyperglycemia and Hypoglycemia, Increased Glucose Variability, and Ineffective Self-Monitoring in Diabetes".
R. Заявка на выдачу патента США №11/578,831, Kovatchev, et al., поданная 18 октября 2006 года, под заголовком "Method, System and Computer Program Product for Evaluating the Accuracy of Blood Glucose Monitoring Sensors/Devices", (публикация № US 2007/0232878, 4 октября 2007 года), патент США №7815569, Kovatchev, et al., выданный 29 октября 2010 года.
S. Международная патентная заявка № PCT/US 2005/013792, Kovatchev, et al., поданная 21 апреля 2005 года, под заголовком "Method, System, and Computer Program Product for Evaluation of the Accuracy of Blood Glucose Monitoring Sensors/Devices", (публикация № WO 05106017, November 10, 2005.
Т. Международная патентная заявка №. PCT/US 01/09884, Kovatchev, et al., filed March 29 2001, под заголовком "Method, System, and Computer Program Product for Evaluation of Glycemic Control in Diabetes Self-Monitoring Data", (публикация № WO 01/72208, 4 октября 2001 года).
U. Заявка на выдачу патента США №10/240228, Kovatchev, et al., поданная 26 сентября 2002 года, (публикация №0212317, 13 ноября 2003 года), патент США №7025425 В2, Kovatchev, et al., выданный 11 апреля 2006 года, под заголовком "Method, System, and Computer Program Product for the Evaluation of Glycemic Control in Diabetes from Self-Monitoring Data".
V. Заявка на выдачу патента США №11/305946, Kovatchev, et al., поданная 19 декабря 2005 года, под заголовком "Method, System, and Computer Program Product for the Evaluation of Glycemic Control in Diabetes from Self-Monitoring Data" (публикация №2006/0094947, 4 мая 2009 года), патент США №7874985, Kovatchev, et al., выданный 25 января 2011 года.
W. Заявка на выдачу патента США №12/975580, Kovatchev, et al., "Method, System, and Computer Program Product for the Evaluation of Glycemic Control in Diabetes from Self-Monitoring Data", поданная 22 декабря 2010 года.
X. Международная патентная заявка № PCT/US 2003/025053, Kovatchev, et al., поданная 8 августа 2003 года, под заголовком "Method, System, and Computer Program Product for the Processing of Self-Monitoring Blood Glucose (SMBG) Data to Enhance Diabetic Self-Management", (публикация № WO 2004/015539, 19 февраля 2004 года).
Y. Заявка на выдачу патента США №10/524094, Kovatchev, et al., поданная 9 февраля 2005 года, под заголовком "Managing and Processing Self-Monitoring Blood Glucose" (публикация №2005/214892, 29 сентября 2005 года).
Ζ. Заявка на выдачу патента США №12/065257, Kovatchev, et al., поданная 29 августа 2008 года, под заголовком "Accuracy of Continuous Glucose Sensors", (публикация №2008/0314395, 25 декабря 2008 года).
АА. Международная патентная заявка № PCT/US 2006/033724, Kovatchev, et al., поданная 29 августа 2006 года, под заголовком "Method for Improvising Accuracy of Continuous Glucose Sensors and a Continuous Glucose Sensor Using the Same" (публикация № WO 07027691, 8 марта 2007 года).
ВВ. Заявка на выдачу патента США №12/159,891, Kovatchev, В., поданная 2 июля 2008 года, под заголовком "Method, System and Computer Program Product for Evaluation of Blood Glucose Variability in Diabetes from Self-Monitoring Data" (публикация №2009/0171589, 2 июля 2009 года).
СС. Международная заявка № PCT/US 2007/000370, Kovatchev, В., поданная 5 января 2007 года, под заголовком "Method, System and Computer Program Product for Evaluation of Blood Glucose Variability in Diabetes from Self-Monitoring Data" (публикация № WO 07081853, 19 июля 2007 года).
DD. Заявка на выдачу патента США №11/925689 и международная патентная заявка РСТ № PCT/US 2007/082744, Breton, et al., обе поданы 26 октября 2007 года, под заголовком "For Method, System and Computer Program Product for Real-Time Detection of Sensitivity Decline in Analyte Sensors", (публикации №2008/0172205, 17 июля 2008 года и № WO 2008/052199, 2 мая 2008 года).
ЕЕ. Заявка на выдачу патента США №10/069674, Kovatchev, et al., поданная 22 февраля 2002 года, под заголовком "Method and Apparatus for Predicting the Risk of Hypoglycemia".
FF. Международная заявка № PCT/US 00/22886, Kovatchev, et al., поданная 21 августа 2000 года, под заголовком "Method and Apparatus for Predicting the Risk of Hypoglycemia" (публикация № WO 01/13786, 1 марта 2001 года).
GG. Заявка на выдачу патента США №6923763 B1, Kovatchev, et al., выдан 2 августа 2005 года, под заголовком "Method and Apparatus for Predicting the Risk of Hypoglycemia".
HH. Публикация заявки на выдачу патента США US 2004/0254434 A1, "Glucose Measuring Module and "Insulin Pump Combination", опубликованная 16 декабря 2004 года, Goodnow, et al. №10/458,914, поданная 10 июня 2003 года.
II. Публикация заявки на выдачу патента США № US 2009/00697456 A1, Estes, et al., "Operating an Infusion Pump System", опубликованая 12 марта 2009 года. Заявка №11/851194, 6 сентября 2007 года.
JJ. Fernandez-Luque, et al., eDiab: A System for Monitoring, Assisting and Educating People with Diabetes", ICCHP 2006, LNCS 4061, pp. 1342-1349, 2006.
KK. Патент США №6602191 B2, Quy, R., Method and Apparatus for Health and Disease Management Combining больной Data Monitoring with Wireless Internet Connectivity, 5 августа 2003 года.
LL. Публикация международной патентной заявки № WO 2008/064053 А2, Patel, et al., Systems and Methods for Diabetes Management Using Consumer Electronic Devices, 29 мая 2008 года; международная патентная заявка № PCT/US 2007/084769, поданная 15 ноября 2007 года.
ММ. Публикация международной патентной заявки № WO 2010/138817 А1, Ow-Wing, K., Glucose Monitoring System with Wireless Communications, 2 декабря 2010 года; международная патентная заявка № WO 2010/138817 A1, поданная 28 мая 2010 года.
NN. Публикация международной патентной заявки № WO 2004/052204 A1, Kim, Kwan-Ho, Blood Glucose Monitoring System, 24 июня 2004 года; международная патентная заявка № PCT/KR 2003/000398, поданная 28 февраля 2003 года.
Примеры
Применение на практике аспекта варианта осуществления (или вариантов осуществления) по настоящему изобретению будет еще более понятно из приведенных далее примеров, которые представлены в настоящем документе только для иллюстрирования и не должны рассматриваться как каким бы то ни было образом ограничивающие настоящее изобретение.
Пример 1. Основанный на устройстве обработки данных способ апостериорной оценки риска гипогликемии у больного, причем указанный способ содержит:
обеспечение алгоритма для расчета статистики, Rhypo(record), риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, который сильно коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, a record относится к хронологической записи BG, подачи инсулина и видов деятельности у субъекта; и
получение рассчитанной статистики, Rhypo(record), таким образом, больному или пользователю подается реализуемое предварительное уведомление о возможности приближающейся гипогликемии у больного.
Пример 2. Способ по примеру 1, в котором абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM-устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 3. Способ по примеру 1, в котором абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 4. Способ по примеру 1, в котором абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от SMBG-устройства, и/или абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 5. Способ по примеру 1, в котором абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от SMBG-устройства, и/или абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 6. Основанный на устройстве обработки данных способ ретроактивного обеспечения безопасного уровня инсулина у больного, причем указанный способ содержит:
обеспечение алгоритма для ретроактивного расчета, основанного на оценке рисков коэффициента ослабления потребности в инсулине относительно записи подачи инсулина у субъекта; и
получение рассчитанного основанного на оценке рисков коэффициента ослабления потребности в инсулине и применение основанного на оценке рисков коэффициента ослабления с тем, чтобы вывести больному или пользователю любое внутреннее пороговое значение для принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем, которое может быть реализовано.
Пример 7. Способ по примеру 6, в котором записью подачи инсулина могут быть данные, получаемые от инсулиновой помпы.
Пример 8. Способ по примеру 6, в котором записью подачи инсулина могут быть данные, получаемые от ручного устройства для введения инсулина.
Пример 9. Способ по примеру 6, в котором основанный на оценке рисков коэффициент ослабления будет рассчитан следующим образом:

где R(t,τ) представляет собой меру риска гипогликемии между моментами времени t и t+τ на основе хронологической записи данных BG и инсулина до момента времени t, на основе симметризации BG функции, a kpatient представляет собой специфичный для больного коэффициент "агрессивности".
Пример 10. Основанный на устройстве обработки данных способ создания основанной на "совокупном эффекте" адаптационной модели больного, причем указанный способ содержит:
обеспечение алгоритма для расчета:
динамической модели метаболической системы больного,
причем указанная динамическая модель включает дескриптивные параметры индивидуальной физиологии модельного больного;
соответствующей, выведенной хронологии поведенческой модели на основе "совокупного эффекта", которая объясняет вариабельность уровня глюкозы в хронологической записи с помощью динамической модели;
причем указанная модель на основе "совокупного эффекта" включает отклонения в представлении в математической форме у модельного больного; и
коррекции физиологических параметров больного на основе как (i) способности динамической модели прогнозировать будущий уровень BG, исходя из известных входящих данных, так и (ii) способности модели выводить характеристики совокупного эффекта, которые согласуются с записью отклонений у больного; и
вывод указанной коррекции больному или пользователю, таким образом, больной или пользователь может использовать коррекцию для будущего плана действий.
Пример 11. Способ по примеру 10, в котором указанные дескриптивные параметры включают представление динамической взаимосвязи перорально потребленных углеводов d (г/мин), физической деятельности e (кал/мин), подкожного инсулина u (ед./ч) и одномерного массива данных χ метаболического состояния модельного больного, элементы которого включают концентрации глюкозы и инсулина (мг/дл) в различных отделах организма и углеводной массы (мг) в кишечнике.
Пример 12. Способ по примеру 11, в котором концентрацией глюкозы (мг/дл) могут быть данные, получаемые от CGM-устройства, а подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от инсулиновой помпы.
Пример 13. Способ по примеру 11, в котором концентрацией глюкозы (мг/дл) могут быть данные, получаемые от CGM-устройства, а подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от ручного устройства для введения инсулина.
Пример 14. Способ по примеру 11, в котором концентрацией глюкозы (мг/дл) могут быть данные, получаемые от SMBG-устройства, и/или подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от инсулиновой помпы.
Пример 15. Способ по примеру 11, в котором концентрацией глюкозы (мг/дл) могут быть данные, получаемые от SMBG-устройства, и/или подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от ручного устройства для введения инсулина.
Пример 16. Способ по примеру 11, в котором взаимосвязь указанных дескриптивных параметров может быть описана как набор нелинейных дифференциальных уравнений для дискретного времени:


где F и G являются нелинейными уравнениями системы, и θ(k) является одномерным массивом значений параметров, которые характерны для больного, таких как масса тела, значения распределения в различных частях, различные временные постоянные, с помощью которых описывают скорости всасывания и выведения между различными частями, некоторые из которых подвержены изменению как временная функция k.
Пример 17. Способ по примеру 11, в котором взаимосвязь указанных дескриптивных параметров может быть описана как набор нелинейных дифференциальных уравнений для непрерывного времени:


Пример 18. Способ по примеру 17, в котором нелинейное представление может быть линеаризовано вблизи любых необходимых рабочих точек (например, равновесной концентрации глюкозы) с получением линейной динамической модели:


где x представляет собой одномерный массив дифференциалов состояния метаболизма (от рабочей точки), uδ (ед./ч) представляет собой отклонение в подаче инсулина от равновесной (базальной) дозы подачи инсулина у больного, A, Bu, Bd, Be представляют собой матрицы пространств состояний линейной модели, a y(k) представляет собой отклонение BG от необходимой рабочей точки, а зависимость от θ(k) включена в матрицы пространств состояний A, Bu, Bd, Be.
Пример 19. Способ по примеру 10, в котором указанные отклонения включают профили приема пищи, физическую деятельность и периоды сон/бодрствование.
Пример 20. Способ по примеру 10, в котором основанная на "совокупном эффекте" модель формирует "хронологию" виртуальных входящих данных системы, которая согласовывает хронологическую запись BG больного и хронологическую запись о подаче инсулина.
Пример 21. Способ по примеру 20, в котором у больного хронологическая запись концентрации BG, {BG(k)}k∈day, и хронологическая запись подачи инсулина, {u(k)}k∈day, совокупный эффект, который согласовывает хронологическую информацию, представляет собой одномерный массив виртуальных входящих данных по углеводам, {dn.e.(k)}k∈day, который минимизирует интеграл вероятности ошибки:

где dist является мерой различия двух одномерных массивов концентрации BG (в этом случае фактической BG по отношению прогнозируемой моделью BG) с учетом фиксированной записи подачи инсулина {u(k)k∈day} и возможного одномерного массива совокупного эффекта {dn.e.(k)}k∈day.
Пример 22. Способ по примеру 21, в котором полученный оптимальный одномерный массив совокупного эффекта (также называемый характеристикой совокупного эффекта), {dn.e.(k)}k∈day, оптимально согласовывает данные по BG и инсулину, собранные от больного посредством сигнала виртуальных углеводов, который собирает информацию о всех влияниях внешних факторов на больного в виде отдельного сигнала внешней помехи, измеряемого в (мг/мин.).
Пример 23. Способ по примеру 22, в котором:
если характеристика совокупного эффекта является положительной, то это должно соответствовать фактическому приему еды больным или это может соответствовать периоду дня, в котором больной испытывает повышенную чувствительность к инсулину; и
если характеристика совокупного эффекта является отрицательной, то это должно соответствовать тому, что больной занимается интенсивной физической деятельностью или физической нагрузкой.
Пример 24. Способ по примеру 10, в котором:
параметры физиологической модели больного, {θ(k)}k∈day, включают ежедневную вариабельность в связи с циркодианным ритмом больного; и
корректор модели включает формулу, которая принимает следующий вид:

где U является рекурсивной функцией коррекции параметров, в основе которой может лежать градиент, BGres является одномерным массивом ошибок прогноза модели BG (погрешностей), a NEres является одномерным массивом ошибок между рассчитанной характеристикой совокупного эффекта и записью фактических (проверенных) входящих поведенческих данных больного.
Пример 25. Способ по примеру 24, в котором динамическую модель уточняют на множественных временных шкалах, в результате чего коррекции параметра можно рассчитывать ежедневно на основе погрешностей BG:

а коррекции на основе несоответствия совокупного эффекта можно рассчитывать на временной шкале с большими временными интервалами, например, один раз в неделю или в месяц:

Пример 26. Способ по примеру 10, дополнительно предусматривающий осуществление ретроактивной оценки оптимальной скорости подачи инсулина больному, причем указанный алгоритм:
ретроактивно рассчитывает, какой была бы оптимальная скорость подачи инсулина больному на протяжении предопределенного периода времени в хронологии с учетом, что нарушения в системе являются именно хронологическими характеристиками совокупного эффекта, рассчитанными для больного на протяжении такого интервала времени, причем для каждой "хронологии" характеристик совокупного эффекта существует соответствующая "хронология" скоростей подачи инсулина, в которой учтены приемы пищи, физическая нагрузка и поправки на каждый день в рассматриваемом интервале времени;
связывает характеристику совокупного эффекта для заданного дня и основанный на модели ответ контроллера оптимального уровня, причем эти одномерные массивы оптимальных ответов собирают, и анализируют, и представляют больному или пользователю для обзора по дням лечения инсулином;
извлекает компоненты из оптимальных ответов, которые соответствуют важным, но случайным событиям, путем вычитания отдельных количеств инсулина, связанных с приемами пищи, или учета отдельных случаев нехватки инсулина, связанных с временными базальными дозами вблизи физической нагрузки, в результате чего остальное расписание подачи инсулина соответствует представлению "оптимального" базального паттерна для больного на каждый день в хронологической записи; и
выявляет согласованность в ретроактивно рассчитанных оптимальных базальных дозах, причем такие оптимальные базальные дозы во множестве сегментов периода представляют собой период лечения больного; и
при этом указанный способ дополнительно предусматривает:
вывод больному или пользователю среднего уровня базального инсулина, который был бы приемлем в каждом сегменте, причем больной или пользователь может использовать эту информацию для (i) принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем или (ii) уточнения долгосрочного профиля базальных доз у больного.
Пример 27. Способ по примеру 10, дополнительно предусматривающий осуществление модели рекомендации по адаптивной поправочной дозе инсулина по запросу пользователя, причем указанный способ предусматривает:
создание алгоритма, включающего следующие вычислительные операции:
ретроспективное определение связанных с приемом пищи и физической нагрузкой видов деятельности;
стохастическое моделирование с получением описания о времени и содержании приемов пищи и физической нагрузки; и
вывод рекомендации по поправке дозы инсулина больному или пользователю, что может быть ответом на запрос больного и пользователя.
Пример 28. Способ по примеру 27, в котором:
указанное ретроспективное определение связанных с приемом пищи и физической нагрузкой видов деятельности включает алгоритм согласования текущей хронологии "характеристик совокупного эффекта" указанного больного с хронологической записью признанных больным связанных с приемами пищи и физической нагрузкой событий с получением подтвержденной (высоко достоверной) записи релевантных поведенческих особенностей больного; причем согласование включает выявление несоответствий между (i) характеристиками совокупного эффекта, рассчитанными из доступных данных по BG и инсулину для больного, и (ii) связанными с приемом пищи и физической нагрузкой событиями, которые подтверждены больным или пользователем с помощью пользовательского интерфейса систем; и
при этом указанный способ предусматривает:
создание предложений, исходя из указанных несоответствий, причем предложения сообщают больному или пользователю; и
получение в результате каких-либо ответов от пользователя или больного для формирования конечной подтвержденной записи о релевантных видах деятельности больного.
Пример 29. Способ по примеру 28, в котором:
указанное стохастическое моделирование включает алгоритм для получения указанной конечной подтвержденной записи о релевантных видах деятельности больного и стохастического моделирования для представления времени и содержания приемов пищи и физической нагрузки согласно поведенческой особенности больного.
Пример 30. Способ по примеру 29, в котором:
указанная поправка инсулина включает алгоритм для мониторинга состояния больного и предложение рекомендации по поправке инсулина в момент, когда больной или пользователь ее запрашивает, на основе (i) стохастического моделирования предстоящих поведенческих нарушений и (ii) текущей динамической модели метаболической системы больного, что позволяет сделать прогноз влияния различных альтернативных поправочных количеств инсулина.
Пример 31. Система осуществления апостериорной оценки риска гипогликемии у больного, причем указанная система включает:
модуль основанной на ретроактивной оценке рисков безопасности с устройством обработки данных для расчета статистики, Rhypo(record), риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, который сильно коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, a record относится к хронологической записи BG, подачи инсулина и видов деятельности у субъекта; и
указанное устройство обработки данных выводит рассчитанную статистику, Rhypo(record), таким образом, больному или пользователю подается реализуемое предварительное уведомление о возможности приближающейся гипогликемии у больного.
Пример 32. Система по примеру 31, в которой абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM-устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 33. Система по примеру 31, в которой абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM-устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 34. Система по примеру 31, в которой абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от SMBG-устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 35. Система по примеру 31, в которой абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от SMBG-устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 36. Система по примеру 31, дополнительно включающая:
CGM-устройство, причем абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM-устройства; и
инсулиновую помпу, причем абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 37. Система по примеру 31, дополнительно включающая:
CGM-устройство, причем абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM-устройства; и
ручное устройство для введения инсулина, причем абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 38. Система по примеру 31, дополнительно включающая:
SMBG-устройство, причем абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от SMBG-устройства; и/или
инсулиновую помпу, причем абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 39. Система по примеру 31, дополнительно включающая:
SMBG-устройство, причем абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от SMBG-устройства; и/или
ручное устройство для введения инсулина, причем абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 40. Система ретроактивного обеспечения безопасного уровня инсулина у больного, причем указанная система включает:
модуль основанной на ретроактивной оценке рисков безопасности с устройством обработки данных для ретроактивного расчета, основанного на оценке рисков коэффициента ослабления потребности в инсулине относительно записи подачи инсулина у субъекта; и
указанное устройство обработки данных выводит рассчитанный основанный на оценке рисков коэффициент ослабления потребности в инсулине, и применение основанного на оценке рисков коэффициента ослабления с тем, чтобы вывести больному или пользователю любое внутреннее пороговое значение для принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем, которое может быть реализовано.
Пример 41. Система по примеру 40, в которой показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 42. Система по примеру 40, в которой показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 43. Система по примеру 40, дополнительно включающая:
инсулиновую помпу, причем показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 44. Система по примеру 40, дополнительно включающая:
ручное устройство для введения инсулина, причем показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 45. Система по примеру 40, в которой основанный на оценке рисков коэффициент ослабления будет рассчитан следующим образом:

где R(t,τ) представляет собой меру риска гипогликемии между моментами времени t и t+τ на основе хронологической записи данных BG и инсулина до момента времени t, на основе симметризации BG функции, а kpatient представляет собой специфичный для больного коэффициент "агрессивности".
Пример 46. Система для создания основанной на "совокупном эффекте" адаптационной модели больного, причем указанная система включает:
модуль оценки совокупного эффекта с устройством обработки данных для расчета:
динамической модели метаболической системы больного, причем указанная динамическая модель включает дескриптивные параметры индивидуальной физиологии модельного больного; и
соответствующей выведенной хронологии поведенческой модели на основе "совокупного эффекта", которая объясняет вариабельность уровня глюкозы в хронологической записи с помощью динамической модели; причем указанная модель на основе "совокупного эффекта" включает отклонения в представлении в математической форме у модельного больного; и модуль корректировки модели с устройством обработки данных для расчета:
коррекции физиологических параметров больного на основе как (i) способности динамической модели прогнозировать будущий уровень BG, исходя из известных входящих данных, так и (ii) способности модели выводить характеристики совокупного эффекта, которые согласуются с записью отклонений у больного; и
указанная система выводит указанную коррекцию больному или пользователю, таким образом, больной или пользователь может использовать коррекцию для будущего плана действий.
Пример 47. Система по примеру 46, в которой указанные дескриптивные параметры включают представление динамической взаимосвязи перорально потребленных углеводов d (г/мин), физической деятельности e (кал/мин), подкожного инсулина u (ед./ч) и одномерного массива данных χ метаболического состояния модельного больного, элементы которого включают концентрации глюкозы и инсулина (мг/дл) в различных отделах организма и углеводной массы (мг) в кишечнике.
Пример 48. Система по примеру 47, в которой концентрацией глюкозы (мг/дл) могут быть данные, получаемые от CGM-устройства, а подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от инсулиновой помпы.
Пример 49. Система по примеру 47, в которой концентрацией глюкозы (мг/дл) могут быть данные, получаемые от CGM-устройства, а подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от ручного устройства для введения инсулина.
Пример 50. Система по примеру 47, в которой концентрацией глюкозы (мг/дл) могут быть данные, получаемые от SMBG-устройства, а подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от инсулиновой помпы.
Пример 51. Система по примеру 47, в которой концентрацией глюкозы (мг/дл) могут быть данные, получаемые от SMBG-устройства, а подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от ручного устройства для введения инсулина.
Пример 52. Система по примеру 47, дополнительно включающая:
CGM-устройство, причем концентрацией глюкозы (мг/дл) могут быть данные, получаемые от указанного CGM-устройства; и
инсулиновую помпу, причем подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от инсулиновой помпы.
Пример 53. Система по примеру 47, дополнительно включающая:
SMBG-устройство, причем концентрацией глюкозы (мг/дл) могут быть данные, получаемые от указанного SMBG-устройства; и
инсулиновую помпу или устройство для введения инсулина, причем подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от указанной инсулиновой помпы или указанного устройства для введения инсулина.
Пример 54. Система по примеру 47, в которой взаимосвязь указанных дескриптивных параметров может быть описана как набор нелинейных дифференциальных уравнений для дискретного времени:


где F и G являются нелинейными уравнениями системы, и θ(k) является одномерным массивом значений параметров, которые характерны для больного, таких как масса тела, значения распределения в различных частях, различные временные постоянные, с помощью которых описывают скорости всасывания и выведения между различными частями, некоторые из которых подвержены изменению как временная функция k.
Пример 55. Система по примеру 47, в которой взаимосвязь указанных дескриптивных параметров может быть описана как набор нелинейных дифференциальных уравнений для непрерывного времени:


Пример 56. Система по примеру 55, в которой нелинейное представление может быть линеаризовано вблизи любых необходимых рабочих точек (например, равновесной концентрации глюкозы) с получением линейной динамической модели:

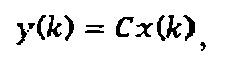
где x представляет собой одномерный массив дифференциалов состояния метаболизма (от рабочей точки), uδ (ед./ч) представляет собой отклонение в подаче инсулина от равновесной (базальной) дозы подачи инсулина у больного, A, Bu, Bd, Be представляют собой матрицы пространств состояний линейной модели, а y(k) представляет собой отклонение BG от необходимой рабочей точки, а зависимость от θ(k) включена в матрицы пространств состояний A, Bu, Bd, Be.
Пример 57. Система по примеру 46, в которой указанные отклонения включают профили приема пищи, физическую деятельность и периоды сон/бодрствование.
Пример 58. Система по примеру 46, в которой основанная на "совокупном эффекте" модель формирует "хронологию" виртуальных входящих данных системы, которая согласовывает хронологическую запись BG больного и хронологическую запись о подаче инсулина.
Пример 59. Система по примеру 58, в которой у больного хронологическая запись концентрации BG, {BG(k)}k∈day, и хронологическая запись подачи инсулина, {u(k)}k∈day, совокупный эффект, который согласовывает хронологическую информацию, представляет собой одномерный массив виртуальных входящих данных по углеводам, {dn.e.(k)}k∈day, который минимизирует интеграл вероятности ошибки:

где dist является мерой различия двух одномерных массивов концентрации BG (в этом случае фактической BG по отношению прогнозируемой моделью BG) с учетом фиксированной записи подачи инсулина {u(k)}k∈day и возможного одномерного массива совокупного эффекта {dn.e.(k)}k∈day.
Пример 60. Система по примеру 59, в которой полученный оптимальный одномерный массив совокупного эффекта (также называемый характеристикой совокупного эффекта), {dn.e.(k)}k∈day, оптимально согласовывает данные по BG и инсулину, собранные от больного посредством сигнала виртуальных углеводов, который собирает информацию о всех влияниях внешних факторов на больного в виде отдельного сигнала внешней помехи, измеряемого в (мг/мин.).
Пример 61. Система по примеру 60, в которой:
если характеристика совокупного эффекта является положительной, то это должно соответствовать фактическому приему еды больным или это может соответствовать периоду дня, в котором больной испытывает повышенную чувствительность к инсулину; и
если характеристика совокупного эффекта является отрицательной, то это должно соответствовать тому, что больной занимается интенсивной физической деятельностью или физической нагрузкой.
Пример 62. Система по примеру 46, в которой:
параметры физиологической модели больного, {θ(k)}k∈day, включают ежедневную вариабельность в связи с циркодианным ритмом больного; и
устройство обработки данных модуля корректировки модели сконфигурировано для расчета следующего:

где U является рекурсивной функцией коррекции параметров, в основе которой может лежать градиент, BGres является одномерным массивом ошибок прогноза модели BG (погрешностей), a NEres является одномерным массивом ошибок между рассчитанной характеристикой совокупного эффекта и записью фактических (проверенных) входящих поведенческих данных больного.
Пример 63. Система по примеру 62, в которой динамическая модель уточнена на множественных временных шкалах, в результате чего коррекции параметра можно рассчитывать ежедневно на основе погрешностей BG:

а коррекции на основе несоответствия совокупного эффекта можно рассчитывать на временной шкале с большими временными интервалами, например, один раз в неделю или в месяц:

Пример 64. Система по примеру 46, дополнительно сконфигурированная для осуществления ретроактивной оценки оптимальной скорости подачи инсулина больному, причем указанная система включает:
модуль-анализатор ретроспективного оптимального контроля с устройством обработки данных, сконфигурированным для:
ретроактивного расчета, какой была бы оптимальная скорость подачи инсулина больному на протяжении предопределенного периода времени в хронологии с учетом, что нарушения в системе являются именно хронологическими характеристиками совокупного эффекта, рассчитанными для больного на протяжении такого интервала времени, причем для каждой "хронологии" характеристик совокупного эффекта существует соответствующая "хронология" скоростей подачи инсулина, в которой учтены приемы пищи, физическая нагрузка и поправки на каждый день в рассматриваемом интервале времени; и
связывания характеристики совокупного эффекта для заданного дня и основанного на модели ответа контроллера оптимального уровня, причем эти одномерные массивы оптимальных ответов собирают, и анализируют, и представляют больному или пользователю для обзора по дням лечения инсулином;
модуль для извлечения ретрооптимальной базальной дозы с устройством обработки данных, сконфигурированным для:
извлечения компонентов из оптимальных ответов, которые соответствуют важным, но случайным событиям, путем вычитания отдельных количеств инсулина, связанных с приемами пищи, или учета отдельных случаев нехватки инсулина, связанных с временными базальными дозами вблизи физической нагрузки, в результате чего остальное расписание подачи инсулина соответствует представлению "оптимального" базального паттерна для больного на каждый день в хронологической записи; и
выявления согласованности в ретроактивно рассчитанных оптимальных базальных дозах, причем такие оптимальные базальные дозы во множестве сегментов периода представляют собой период лечения больного; и
причем указанная система сконфигурирована для:
осуществления вывода больному или пользователю среднего уровня базального инсулина, который был бы приемлем в каждом сегменте, причем больной или пользователь может использовать эту информацию для (i) принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем или (ii) уточнения долгосрочного профиля базальных доз у больного.
Пример 65. Система по примеру 46, дополнительно сконфигурированная для осуществления модели рекомендации по адаптивной поправке инсулина по запросу пользователя, причем указанная система включает:
модуль для ретроспективного определения приема пищи и физической нагрузки с устройством обработки данных для осуществления ретроспективного определения связанных с приемом пищи и физической нагрузкой видов деятельности;
модуль для стохастического моделирования приема пищи и физической нагрузки с устройством обработки данных для осуществления стохастического моделирования с получением описания о времени и содержании приемов пищи и физической нагрузки; и
модуль для вывода рекомендации по поправочному болюсу с устройством обработки данных для представления и вывода рекомендации по поправке дозы инсулина больному или пользователю, что может быть ответом на запрос больного и пользователя.
Пример 66. Система по примеру 65, в которой:
указанное ретроспективное определение связанных с приемом пищи и физической нагрузкой видов деятельности включает алгоритм согласования текущей хронологии "характеристик совокупного эффекта" указанного больного с хронологической записью признанных больным связанных с приемами пищи и физической нагрузкой событий с получением подтвержденной (высоко достоверной) записи релевантных поведенческих особенностей больного; причем согласование включает выявление несоответствий между (i) характеристиками совокупного эффекта, рассчитанными из доступных данных по BG и инсулину для больного, и (ii) связанными с приемом пищи и физической нагрузкой событиями, которые подтверждены больным или пользователем с помощью пользовательского интерфейса систем; и
указанная система сконфигурирована с включением:
модуля вывода для создания предложений, исходя из указанных несоответствий, причем предложения сообщаются больному или пользователю; и
модуля ввода для получения в результате каких-либо ответов от пользователя или больного с целью формирования конечной подтвержденной записи о релевантных видах деятельности больного.
Пример 67. Система по примеру 66, в которой:
указанное устройство обработки данных указанного модуля стохастического моделирования сконфигурировано для получения указанной конечной подтвержденной записи о релевантных видах деятельности больного и стохастического моделирования для представления времени и содержания приемов пищи и физической нагрузки согласно поведенческой особенности больного.
Пример 68. Система по примеру 67, в которой:
указанное устройство обработки данных у указанного модуля для вывода рекомендации по поправочному болюсу сконфигурировано для мониторинга состояния больного и осуществления вывода рекомендации по поправке инсулина в момент, когда больной или пользователь ее запрашивает, на основе (i) стохастического моделирования предстоящих поведенческих нарушений и (ii) текущей динамической модели метаболической системы больного, что позволяет сделать прогноз влияния различных альтернативных поправочных количеств инсулина.
Пример 69. Машиночитаемый носитель, содержащий команды управления программой для осуществления апостериорной оценки риска гипогликемии у больного, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы обеспечивает осуществление устройством обработки данных следующих этапов:
создание алгоритма для расчета статистики, Rhypo(record), риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, который сильно коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, a record относится к хронологической записи BG, подачи инсулина и видов деятельности у субъекта; и
получение рассчитанной статистики, Rhypo(record), таким образом, больному или пользователю подается реализуемое предварительное уведомление о возможности приближающейся гипогликемии у больного.
Пример 70. Машиночитаемый носитель по примеру 69, в котором абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM-устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 71. Машиночитаемый носитель по примеру 69, в котором абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от CGM-устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 72. Машиночитаемый носитель по примеру 69, в котором абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от SMBG-устройства, а абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от инсулиновой помпы.
Пример 73. Машиночитаемый носитель по примеру 69, в котором абсолютные уровни BG и вариабельность BG могут представлять собой данные, получаемые от SMBG-устройства, и/или абсолютные показатели подачи инсулина могут представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 74. Машиночитаемый носитель, содержащий команды управления программой для ретроактивного обеспечения безопасного уровня инсулина у больного, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы обеспечивает осуществление устройством обработки данных следующих этапов:
создание алгоритма для ретроактивного расчета, основанного на оценке рисков коэффициента ослабления потребности в инсулине относительно записи подачи инсулина у субъекта; и
получение рассчитанного основанного на оценке рисков коэффициента ослабления потребности в инсулине и применение основанного на оценке рисков коэффициента ослабления с тем, чтобы вывести больному или пользователю любое внутреннее пороговое значение для принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем, которое может быть реализовано.
Пример 75. Машиночитаемый носитель по примеру 74, в котором запись подачи инсулина может представлять собой данные, получаемые от инсулиновой помпы.
Пример 76. Машиночитаемый носитель по примеру 74, в котором запись подачи инсулина может представлять собой данные, получаемые от ручного устройства для введения инсулина.
Пример 77. Машиночитаемый носитель по примеру 202, причем основанный на оценке рисков коэффициент ослабления будет рассчитан следующим образом:

где R(t,τ) представляет собой меру риска гипогликемии между моментами времени t и t+τ на основе хронологической записи данных BG и инсулина до момента времени t, на основе симметризации BG функции, a kpatient представляет собой специфичный для больного коэффициент "агрессивности".
Пример 78. Машиночитаемый носитель, содержащий команды управления программой для создания основанной на "совокупном эффекте" адаптационной модели больного, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы обеспечивает осуществление устройством обработки данных следующих этапов:
расчет динамической модели метаболической системы больного, причем указанная динамическая модель включает дескриптивные параметры индивидуальной физиологии модельного больного;
расчет соответствующей, выведенной хронологии поведенческой модели на основе "совокупного эффекта", которая объясняет вариабельность уровня глюкозы в хронологической записи с помощью динамической модели;
причем указанная модель на основе "совокупного эффекта" включает отклонения в представлении в математической форме у модельного больного;
расчет коррекции физиологических параметров больного на основе как (i) способности динамической модели прогнозировать будущий уровень BG, исходя из известных входящих данных, так и (ii) способности модели выводить характеристики совокупного эффекта, которые согласуются с записью отклонений у больного; и
вывод указанной коррекции больному или пользователю, таким образом, больной или пользователь может использовать коррекцию для будущего плана действий.
Пример 79. Машиночитаемый носитель по примеру 78, причем указанные дескриптивные параметры включают представление динамической взаимосвязи перорально потребленных углеводов d (г/мин), физической деятельности e (кал/мин), подкожного инсулина u (ед./ч) и одномерного массива данных χ метаболического состояния модельного больного, элементы которого включают концентрации глюкозы и инсулина (мг/дл) в различных отделах организма и углеводной массы (мг) в кишечнике.
Пример 80. Машиночитаемый носитель по примеру 79, причем концентрацией глюкозы (мг/дл) могут быть данные, получаемые от CGM-устройства, а подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от инсулиновой помпы.
Пример 81. Машиночитаемый носитель по примеру 79, причем концентрацией глюкозы (мг/дл) могут быть данные, получаемые от CGM-устройства, а подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от ручного устройства для введения инсулина.
Пример 82. Машиночитаемый носитель по примеру 79, причем концентрацией глюкозы (мг/дл) могут быть данные, получаемые от SMBG-устройства, и/или подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от инсулиновой помпы.
Пример 83. Машиночитаемый носитель по примеру 79, причем концентрацией глюкозы (мг/дл) могут быть данные, получаемые от SMBG-устройства, и/или подкожным инсулином u и концентрацией инсулина (мг/дл) могут быть данные, получаемые от ручного устройства для введения инсулина.
Пример 84. Машиночитаемый носитель по примеру 79, причем взаимосвязь указанных дескриптивных параметров может быть описана как набор нелинейных дифференциальных уравнений для дискретного времени:


где F и G являются нелинейными уравнениями системы, и θ(k) является одномерным массивом значений параметров, которые характерны для больного, таких как масса тела, значения распределения в различных частях, различные временные постоянные, с помощью которых описывают скорости всасывания и выведения между различными частями, некоторые из которых подвержены изменению как временная функция k.
Пример 85. Машиночитаемый носитель по примеру 79, причем взаимосвязь указанных дескриптивных параметров может быть описана как набор нелинейных дифференциальных уравнений для непрерывного времени:


Пример 86. Машиночитаемый носитель по примеру 185, причем нелинейное представление может быть линеаризовано вблизи любых необходимых рабочих точек (например, равновесной концентрации глюкозы) с получением линейной динамической модели:


где x представляет собой одномерный массив дифференциалов состояния метаболизма (от рабочей точки), uδ (ед./ч) представляет собой отклонение в подаче инсулина от равновесной (базальной) дозы подачи инсулина у больного, A, Bu, Bd, Be представляют собой матрицы пространств состояний линейной модели, а y(k) представляет собой отклонение BG от необходимой рабочей точки, а зависимость от θ(k) включена в матрицы пространств состояний A, Bu, Bd, Be.
Пример 87. Машиночитаемый носитель по примеру 78, причем указанные отклонения включают профили приема пищи, физическую деятельность и периоды сон/бодрствование.
Пример 88. Машиночитаемый носитель по примеру 78, причем основанная на "совокупном эффекте" модель формирует "хронологию" виртуальных входящих данных системы, которая согласовывает хронологическую запись BG больного и хронологическую запись о подаче инсулина.
Пример 89. Машиночитаемый носитель по примеру 88, причем у больного хронологическая запись концентрации BG, {BG(k)}k∈day, и хронологическая запись подачи инсулина, {u(k)}k∈day, совокупный эффект, который согласовывает хронологическую информацию, представляет собой одномерный массив виртуальных входящих данных по углеводам, {dn.e.(k)}k∈day, который минимизирует интеграл вероятности ошибки:

где dist является мерой различия двух одномерных массивов концентрации BG (в этом случае фактической BG по отношению прогнозируемой моделью BG) с учетом фиксированной записи подачи инсулина {u(k)}k∈day и возможного одномерного массива совокупного эффекта {dn.e.(k)}k∈day.
Пример 90. Машиночитаемый носитель по примеру 89, причем полученный оптимальный одномерный массив совокупного эффекта (также называемый характеристикой совокупного эффекта), {dn.e.(k)}k∈day, оптимально согласовывает данные по BG и инсулину, собранные от больного посредством сигнала виртуальных углеводов, который собирает информацию о всех влияниях внешних факторов на больного в виде отдельного сигнала внешней помехи, измеряемого в (мг/мин.).
Пример 91. Машиночитаемый носитель по примеру 90, причем:
если характеристика совокупного эффекта является положительной, то это должно соответствовать фактическому приему еды больным или это может соответствовать периоду дня, в котором больной испытывает повышенную чувствительность к инсулину; и
если характеристика совокупного эффекта является отрицательной, то это должно соответствовать тому, что больной занимается интенсивной физической деятельностью или физической нагрузкой.
Пример 92. Машиночитаемый носитель по примеру 78, причем:
параметры физиологической модели больного, {θ(k)}k∈day, включают ежедневную вариабельность в связи с циркодианным ритмом больного; и
корректор модели включает формулу, которая принимает следующий вид:

где U является рекурсивной функцией коррекции параметров, в основе которой может лежать градиент, BGres является одномерным массивом ошибок прогноза модели BG (погрешностей), а NEres является одномерным массивом ошибок между рассчитанной характеристикой совокупного эффекта и записью фактических (проверенных) входящих поведенческих данных больного.
Пример 93. Машиночитаемый носитель по примеру 92, причем динамическая модель уточнена на множественных временных шкалах, в результате чего коррекции параметра можно рассчитывать ежедневно на основе погрешностей BG:

а коррекции на основе несоответствия совокупного эффекта можно рассчитывать на временной шкале с большими временными интервалами, например, один раз в неделю или в месяц:

Пример 94. Машиночитаемый носитель по примеру 78, дополнительно включающий команды для осуществления ретроактивной оценки оптимальной скорости подачи инсулина больному, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы заставляет устройство обработки данных осуществлять следующие этапы:
ретроактивный расчет, какой была бы оптимальная скорость подачи инсулина больному на протяжении предопределенного периода времени в хронологии с учетом, что нарушения в системе являются именно хронологическими характеристиками совокупного эффекта, рассчитанными для больного на протяжении такого интервала времени, причем для каждой "хронологии" характеристик совокупного эффекта существует соответствующая "хронология" скоростей подачи инсулина, в которой учтены приемы пищи, физическая нагрузка и поправки на каждый день в рассматриваемом интервале времени;
связывание характеристики совокупного эффекта для заданного дня и основанного на модели ответа контроллера оптимального уровня, причем эти одномерные массивы оптимальных ответов собирают, и анализируют, и представляют больному или пользователю для обзора по дням лечения инсулином;
извлечение компонентов из оптимальных ответов, которые соответствуют важным, но случайным событиям, путем вычитания отдельных количеств инсулина, связанных с приемами пищи, или учета отдельных случаев нехватки инсулина, связанных с временными базальными дозами вблизи физической нагрузки, в результате чего остальное расписание подачи инсулина соответствует представлению "оптимального" базального паттерна для больного на каждый день в хронологической записи;
выявление согласованности в ретроактивно рассчитанных оптимальных базальных дозах, причем такие оптимальные базальные дозы во множестве сегментов периода представляют собой период лечения больного; и
вывод больному или пользователю среднего уровня базального инсулина, который был бы приемлем в каждом сегменте, причем больной или пользователь может использовать эту информацию для (i) принятия решения о сниженных временных базальных дозах перед приемами пищи и/или после физической нагрузки в будущем или (ii) уточнения долгосрочного профиля базальных доз у больного.
Пример 95. Машиночитаемый носитель по примеру 78, дополнительно включающий команды для осуществления модели рекомендации по адаптивной поправке инсулина по запросу пользователя, причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы заставляет устройство обработки данных осуществлять следующие этапы:
ретроспективное определение связанных с приемом пищи и физической нагрузкой видов деятельности;
стохастическое моделирование с получением описания о времени и содержании приемов пищи и физической нагрузки; и
вывод рекомендации по поправке дозы инсулина больному или пользователю, что может быть ответом на запрос больного и пользователя.
Пример 96. Машиночитаемый носитель по примеру 95, причем:
указанное ретроспективное определение связанных с приемом пищи и физической нагрузкой видов деятельности включает алгоритм согласования текущей хронологии "характеристик совокупного эффекта" указанного больного с хронологической записью признанных больным связанных с приемами пищи и физической нагрузкой событий с получением подтвержденной (высоко достоверной) записи релевантных поведенческих особенностей больного; причем согласование включает выявление несоответствий между (i) характеристиками совокупного эффекта, рассчитанными из доступных данных по BG и инсулину для больного, и (ii) связанными с приемом пищи и физической нагрузкой событиями, которые подтверждены больным или пользователем с помощью пользовательского интерфейса систем; и
причем выполнение команд управления программой одним или несколькими устройствами обработки данных компьютерной системы заставляет устройство обработки данных осуществлять следующие этапы:
создание предложений, исходя из указанных несоответствий, причем предложения сообщают больному или пользователю; и
получение в результате каких-либо ответов от пользователя или больного для формирования конечной подтвержденной записи о релевантных видах деятельности больного.
Пример 97. Машиночитаемый носитель по примеру 96, причем:
указанное стохастическое моделирование включает алгоритм для получения указанной конечной подтвержденной записи о релевантных видах деятельности больного и стохастического моделирования для представления времени и содержания приемов пищи и физической нагрузки согласно поведенческой особенности больного.
Пример 98. Машиночитаемый носитель по примеру 97, причем:
указанная поправка инсулина включает алгоритм для мониторинга состояния больного и предложение рекомендации по поправке инсулина в момент, когда больной или пользователь ее запрашивает, на основе (i) стохастического моделирования предстоящих поведенческих нарушений и (ii) текущей динамической модели метаболической системы больного, что позволяет сделать прогноз влияния различных альтернативных поправочных количеств инсулина.
Следует понимать, что при желании или необходимости один или несколько примеров №№1-98 можно объединить с одним или несколькими примерами №№1-98.
Следует понимать, что обсуждаемый в настоящем документе субъект или больной может быть человеком или любым животным. Следует понимать, что животное может быть любого приемлемого типа, включая без ограничения млекопитающего, ветеринарное животное, домашний скот или домашнего любимца и т.д. Например, животное может быть лабораторным животным, специально отобранным по наличию определенных характеристик, аналогичных человеческим (например, крысой, собакой, свиньей, обезьяной), и т.д. Следует понимать, что субъектом может быть, например, любой подходящий больной человек.
Если явно не указано обратное, то не существует требований к любому конкретному описанному или проиллюстрированному действию или элементу, любой конкретной последовательности таких действий, любому конкретному размеру, скорости, материалу, длительности, форме, размеру или частоте или любому конкретному взаимодействию таких элементов. Более того, любое действие можно повторить, любое действие можно выполнить с помощью множества активных компонентов и/или любой элемент можно продублировать. Дополнительно, любое действие или элемент можно исключить, последовательность действий может варьировать и/или взаимодействие элементов может варьировать. Следует понимать, что при желании или необходимости аспекты настоящего изобретения могут характеризоваться рядом размеров, форм, очертаний, составов и материалов.
Таким образом, несмотря на то, что настоящее изобретение было описано применительно к конкретным вариантам осуществления, специалистам в данной области будут очевидны многие модификации, вариации, изменения, замены и эквивалентны. Настоящее изобретение не ограничено в объеме описанным в настоящем документе конкретным вариантом осуществления. Безусловно, исходя из приведенного выше описания и прилагаемых чертежей, специалистам в данной области будут очевидны различные модификации настоящего изобретения, помимо описанных в настоящем документе. Следовательно, настоящего изобретение необходимо рассматривать как ограничиваемое лишь идеей и объемом приведенной далее формулой изобретения, включая все модификации и эквиваленты.
Исходя из прочтения приведенного выше подробного описания и чертежей некоторых иллюстративных вариантах осуществления, специалистам в данной области станут понятны другие варианты осуществления. Следует понимать, что возможны многочисленные вариации, модификации и дополнительные варианты осуществления, и, соответственно, все такие вариации, модификации и варианты осуществления должны рассматриваться как входящие в состав идее и объема настоящей заявки. Например, независимо от содержания любой части (например, заглавия, области техники, краткого описания, реферата, чертежей и т.д.) настоящей заявки, если явно не указано обратное, нет необходимости включения в пункт приведенной в настоящем документе формулы изобретения или любой заявки, которая испрашивает приоритет согласно настоящей заявки, любого конкретного описанного или проиллюстрированного действия или элемента, любой конкретной последовательности таких действий или любого конкретного взаимодействия таких элементов. Более того, любое действие можно повторить, любое действие можно выполнить с помощью множества активных компонентов и/или любой элемент можно продублировать.
Дополнительно, любое действие или элемент можно исключить, последовательность действий может варьировать и/или взаимодействие элементов может варьировать. Если явно не указано обратное, то не существует требований к любому конкретному описанному или проиллюстрированному действию или элементу, любой конкретной последовательности таких действий, любому конкретному размеру, скорости, материалу, размеру или частоте или любому конкретному взаимодействию таких элементов. Соответственно, описания и чертежи необходимо рассматривать как иллюстративные по природе, но не как ограничивающие. Более того, при описании в настоящем документе любого числа или диапазона, если явно не указано иное, то число или диапазон являются примерными. При описании в настоящем документе любого диапазона, если явно не указано иное, то диапазон включает все входящие в него значения и все входящие в него поддиапазоны. Любая информация в любом материале (например, патенте Соединенных Штатов / патенте другой страны, заявке на патент Соединенных Штатов / заявке на патент другой страны, книге, статье и т.д.), который был включен в настоящий документ с помощью ссылки, включен с помощью ссылки до той степени, при которой нет противоречия между такой информацией и другими изложенными в настоящем документе утверждениями и чертежами. В случае такого противоречия, включая противоречие, при котором будет опорочен любой пункт приведенной в настоящем документе формулы изобретения или заявляемый согласно настоящей заявке приоритет, любая такая противоречащая информация в таком включенном с помощью ссылки справочном материале будет специально не включена в настоящий документ с помощью ссылки.
Реферат
Группа изобретений относится к медицине и может быть использована для апостериорной оценки риска гипогликемии у больного. Группа изобретений представлена способом, системой и машиночитаемым носителем. Осуществляют обеспечение алгоритма для расчета с помощью устройства обработки данных статистики R(record) риска гипогликемии на основе хронологии абсолютных значений уровней глюкозы в крови BG, абсолютного значения вариабельности глюкозы в крови BG и абсолютного значения подачи инсулина. Упомянутая статистика коррелирует с апостериорной (условной) вероятностью гипогликемии P(E|record). Eозначает событие гипогликемии на следующий день, a record относится к записи хронологических значений уровней глюкозы в крови BG, подачи инсулина и видов деятельности больного. Проводят расчет с помощью устройства обработки данных указанной статистики R(record). Осуществляют вывод рассчитанной статистики R(record) на устройстве вывода с обеспечением уведомления о возможности гипогликемии у больного. Группа изобретений позволяет проводить оценку риска гипогликемии у больного за счет комплексного учета наиболее оптимальных данных и показателей. 3 н. и 16 з.п. ф-лы, 16 ил., 98 пр.
Формула
обеспечение алгоритма для расчета с помощью устройства обработки данных статистики Rhypo(record) риска гипогликемии на основе хронологии указанного больного абсолютных значений уровней глюкозы в крови BG, абсолютного значения вариабельности глюкозы в крови BG и абсолютного значения подачи инсулина, при этом упомянутая статистика коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, a record относится к записи хронологических значений уровней глюкозы в крови BG, подачи инсулина и видов деятельности больного;
расчет с помощью устройства обработки данных указанной статистики Rhypo(record) и
вывод рассчитанной статистики Rhypo(record) на устройстве вывода с обеспечением уведомления о возможности гипогликемии у больного.
модуль безопасности, основанный на ретроактивной оценке рисков, с устройством обработки данных для расчета статистики, Rhypo(record), риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, которая коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, a record относится к хронологической записи BG, подачи инсулина и видов деятельности у субъекта; и
указанное устройство обработки данных выводит рассчитанную статистику, Rhypo(record), в качестве уведомления о возможности гипогликемии у больного.
CGM-устройство, причем абсолютные уровни BG и вариабельность BG представляют собой данные, получаемые от CGM-устройства; и
инсулиновую помпу, причем абсолютные показатели подачи инсулина представляют собой данные, получаемые от инсулиновой помпы.
CGM-устройство, причем абсолютные уровни BG и вариабельность BG представляют собой данные, получаемые от CGM-устройства; и
ручное устройство для введения инсулина, причем абсолютные показатели подачи инсулина представляют собой данные, получаемые от ручного устройства для введения инсулина.
SMBG-устройство, причем абсолютные уровни BG и вариабельность BG представляют собой данные, получаемые от SMBG-устройства; и/или
инсулиновую помпу, причем абсолютные показатели подачи инсулина представляют собой данные, получаемые от инсулиновой помпы.
SMBG-устройство, причем абсолютные уровни BG и вариабельность BG представляют собой данные, получаемые от SMBG-устройства; и/или
ручное устройство для введения инсулина, причем абсолютные показатели подачи инсулина представляют собой данные, получаемые от ручного устройства для введения инсулина.
производить расчет статистики, Rhypo(record), риска гипогликемии на основе абсолютных уровней BG, вариабельности BG и подачи инсулина, которая коррелирует с апостериорной (условной) вероятностью гипогликемии, P(Ehypo|record), где Ehypo означает событие гипогликемии на следующий день, a record относится к хронологической записи BG, подачи инсулина и видов деятельности у субъекта; и
выводить рассчитанную статистику, Rhypo(record), таким образом, подавая уведомление о возможности гипогликемии.

Комментарии