Cest-системы, проявляющие не зависящую от концентрации чувствительность - RU2605823C2
Код документа: RU2605823C2
Чертежи

















Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к области магнитно-резонансной томографии (МРТ), основанной на химическом обменном переносе насыщения (CEST). Более конкретно, оно относится к системам CEST, проявляющим не зависящую от концентрации чувствительность, и к их применению при in vivo картировании физических или химических параметров, представляющих диагностический интерес.
Уровень техники
Метод химического обменного переноса насыщения (CEST) является недавно предложенным способом визуализации, основанным на применении молекул (CEST-агентов), содержащих один или несколько пулов обмениваемого(ых) протона(ов) (см., например, Balaban RS., Methods in Biomedical Magnetic Resonance Imaging and Spectroscopy. Chichester, Великобритания: John Wiley & Sons; 2000. Vol.1, p 661-6667; под редакцией Young IR).
Данный способ визуализации основан на явлении, известном в ЯМР высокого разрешения как эксперимент по двойному резонансу, при котором прикладывают импульс второй радиочастоты (РЧ), точно отцентрированной по резонансной частоте мобильных протонов, получаемой из спектра ЯМР, для того чтобы добиться насыщения их спинов. Таким образом, создают насыщенную намагниченность, которая передается "объемной" воде посредством химического обмена, приводящего к ясному уменьшению сигнала объемной воды. Данный эффект называется переносом насыщения, или ST-эффектом. Контраст на полученном основанном на CEST МР-изображении определяется степенью переноса: чем больше количество насыщенной намагниченности, перенесенной на протоны воды, тем меньше интенсивность полученного сигнала воды, сильнее контраст (отрицательный контраст) на полученном изображении МРТ.
Основным требованием к CEST-агенту является наличие мобильного(ых) протона(ов) (или обмениваемых протонов, что в настоящем описании используется взаимозаменяемо), имеющего соответствующую скорость обмена (Kex) и подходящий интервал химического сдвига от протонов объемной воды, так чтобы существовала возможность как для активации центра обмена, так и для переноса насыщения. Ориентировочно, данное условие достигается, когда kex приближается к Δν (Kex

О парамагнитных CEST-агентах (PARACEST), преимущественно включая макроциклические тетраамидные производные DOTA, обеспечивающие четыре магнитно эквивалентных или псевдоэквивалентных пула мобильных N-H протонов, впервые сообщил Sherry (см., например, J. Am. Chem. Soc 2001; 123:1517-1518). Важные открытия, касающиеся парамагнитных CEST-агентов также рассматриваются в Magn. Reson. Med 2002; 47:639-648.
Woods et. al продемонстрировали, что OH группы также можно использовать в эксперименте CEST с зондом PARACEST, по меньшей мере, в некоторых условиях эксперимента, включая применение обезвоженных растворителей (см., например, J. Am. Chem. Soc 2006; 128:10155-10162). Тем не менее, при растворении исследуемого комплекса в чистой воде невозможно обнаружить CEST-эффект от гидроксильных и связанных с металлами протонов воды, что препятствует его возможному использованию для применений CEST "in vivo".
Позднее Morrow с сотрудниками продемонстрировали, что в чистой воде можно обнаружить CEST-эффект от спиртовых донорных групп с использованием несущих три положительных заряда макроциклических комплексов Ln(III) с нейтральными лигандами, содержащими боковые спиртовые группы (см., например, Inorg. Chem. 2009; 48:7237-7243). В данной статье рассмотрено существование нескольких стереоизомеров используемых производных циклена и делается вывод, что комплексы Ln(III), имеющие только одну диастереомерную форму в растворе, являются потенциально подходящими для экспериментов PARACEST.
Дополнительный класс особенно высокочувствительных парамагнитных CEST-агентов представлен LIPOCEST, липосомами, содержащими реагент парамагнитного сдвига для протонов воды в водной внутренней полости (см., например, Angew. Chem. Int Ed Engl 2003; 42:4527-4529).
Среди CEST-агентов класс, представляющий особый интерес, представлен "чувствительными" агентами, а именно контрастными агентами, снабженными, по меньшей мере, одним обмениваемым протоном, способность которого к переносу насыщения коррелирует с физико-химическим представляющим диагностический интерес параметром микроокружения, в котором распределен данный агент. Данные агенты, помимо действия в качестве обычных CEST-агентов и обеспечения CEST-контраста, также способны сообщать об изменениях указанного параметра, обычно выбираемого из pH, температуры, концентрации метаболитов или определенных ионов, парциального давления О2 или СО2, активности белков или ферментов, в органе тела или области, в которой они распределены, таким образом, действуя в качестве полезных биомаркеров определенного заболевания, точно связанного с данными изменениями (см., например, Top Curr. Chem. 2002, 221, 123-164).
В этом случае величина переноса насыщения (ST), наблюдаемая в способе CEST, зависит от содержания воды и CEST-зонда, т.е., другими словами, их локальной концентрации в рассматриваемой ткани. Следовательно, особенное чувствительное свойство, проявляемое данными агентами, можно соответствующим образом использовать на практике, только когда известна их фактическая концентрация.
Между тем, для эффективного применения в in vivo определениях чувствительный CEST-агент должен проявлять свою чувствительность не зависящим от концентрации образом.
Эта задача может быть решена с применением CEST-агентов, содержащих, по меньшей мере, два набора магнитно неэквивалентных протонов, ST-эффект которых демонстрирует различную зависимость от представляющего интерес физико-химического параметра. В данном случае, фактически, можно использовать логометрический подход, основанный на следующем уравнении (1):
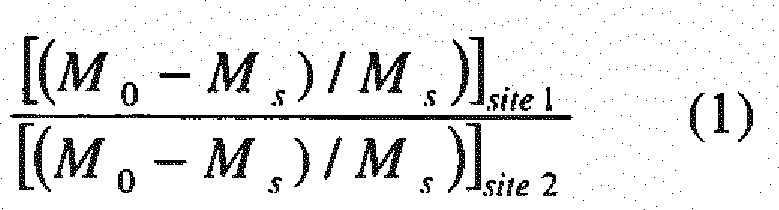
впервые раскрытый Balaban и Ward (для подробностей о приведенном выше уравнении см., например, Magn. Reson. Med. 2000; 44:799-802), использующий сравнительное отношение между ST-эффектами, вызванными селективным облучением двух различных резонансов, соответственно обозначенных как site 1 и site 2 в приведенном выше уравнении, который делает измеренную величину ST и, в свою очередь, определяемый диагностический параметр, не зависящими от абсолютной концентрации введенного CEST-зонда.
Примеры чувствительных агентов, делающих возможным применение данного логометрического подхода, включают мономолекулярные комплексы лантаноида (Ln), содержащие два магнитно неэквивалентных протонных центра, причем один, обычно принадлежит первичной(ым) амидной(ым) группе(ам) на боковом(ых) ответвлении(ях), координированном с металлическим ионом, тогда как второй, обычно представлен молекулой(ами) воды, координированной с Ln-центром хелатного комплекса (см., например, Angew. Chem. Int Ed 2002; 41:1919-1921 и 4334-4336).
Диамагнитные молекулы, такие как 5,6-дигидроурацил и йопамидол, содержащие два пула CEST-активных протонов, также были успешно испытаны в качестве не зависящих от концентрации репортеров pH (см., например, Magn. Reson. Med. 2000; 44:799-802, Invest. Radiol. 2004; 39:235-243; Magn. Reson. Med. 2005; 53:830-834 и J. Am. Chem. Soc 2005; 131:1380-1381). Альтернативно, можно использовать CEST-системы, содержащие два (или более) CEST-зонда, имеющих одинаковую картину биораспределения, но сильно различающимися свойствами ЯМР, например в зависимости от координированного иона Ln(III), каждый из которых обеспечивает различный(е) протонный(е) пул(ы) (см., например, Magn. Reson. Med. 2002; 47:639-648).
Разработка чувствительных CEST-агентов, однако, все еще остается неудовлетворительной, главным образом из-за ограниченного количества CEST-систем, проявляющих не зависящую от концентрации чувствительность.
Сущность изобретения
В соответствии с вышеуказанной задачей настоящее изобретение направлено на определение альтернативного источника магнитно неэквивалентных мобильных протонов, позволяющего разрабатывать основанные на CEST не зависящие от концентрации чувствительные способы, и на альтернативные CEST-системы, проявляющие не зависящую от концентрации чувствительность.
Решения согласно настоящему изобретению относятся к применению различимых по ЯМР стереоизомеров парамагнитного CEST-агента в качестве альтернативного источника магнитно неэквивалентных обмениваемых протонов.
Более конкретно, настоящее изобретение относится к применению различимых по ЯМР изомеров парамагнитного CEST-агента в качестве источника магнитно неэквивалентных мобильных протонов, для того чтобы разрабатывать логометрический способ визуализации с применением CEST.
В другом варианте осуществления настоящее изобретение относится к логометрическому способу CEST МРТ, который включает использование магнитно неэквивалентных мобильных протонов, принадлежащих, по меньшей мере, двум различимым по ЯМР изомерам парамагнитного CEST-агента.
В другом варианте осуществления настоящее изобретение относится к классу комплексных соединений лантаноида (III), снабженных группой обмена протонами на боковом ответвлении хелатирующего лиганда, которые демонстрируют, по меньшей мере, два различимых по ЯМР стереоизомера в растворе, и к применению данных комплексных соединений в логометрических способах визуализации с применением CEST в качестве не зависящих от концентрации контрастных CEST-агентов для получения не зависящего от концентрации CEST-контраста.
В еще одном варианте осуществления настоящее изобретение относится к применению указанных определенных комплексных соединений лантаноида (III) в качестве не зависящих от концентрации чувствительных CEST-агентов и к логометрическому способу визуализации с применением CEST, который включает их применение для получения не зависящей от концентрации карты физического или химического параметра, представляющего диагностический интерес, в органе тела, жидкости или ткани человека или животного.
Краткое описание фигур
Фиг.1: Спектр1H ЯМР YbHPDO3A в D2O (278K, 600 МГц).
Фиг.2: Панель a) Увеличение спектра YbHPDO3A в D2O (ниже) и H2O (выше), на котором отмечены различные химические сдвиги (соответственно 72 и 99 м.д. при 20°C), демонстрируемые обмениваемыми OH протонами двух различимых изомеров данного комплекса; панель b) Z-спектр YbHPDO3A (24 мМ раствор, 293K, pH 7,31, мощность облучения 24 мкΤ, время облучения 2 с).
Фиг.3: Панель a) МР-изображение in vitro (протонная плотность) фантома, содержащего растворы YbHPDO3A, все с концентрацией 24 мМ, но различными pH (капилляры 1-11) или одинаковым pH (7,31) но различными концентрациями (от 3 до 24 мМ) (капилляры 7, 12-14); панель b) легенда фантома; панель c) карта ST, полученная после облучения гидроксильных протонов при 72 м.д. (20°C; мощность импульса облучения 24 мкТл); панель d) карта ST, полученная после облучения гидроксильных протонов при 99 м.д. (20°C, мощность импульса облучения 24 мкТл); панель e) изменение ST-эффекта при изменении pH, полученное после облучения гидроксильных протонов двух изомеров, соответственно при 72 м.д. (квадраты) и 99 м.д. (кружки) (калибровочные кривые) (24 мМ раствор, 20°C; импульс облучения 24 мкТл; время облучения 2 с); панель f) логометрическая кривая, демонстрирующая зависимость логометрических значений от pH, которую получают, применяя логометрический подход к кривым ST панели e). На данной фигуре логометрическое значение (показанное на вертикальной оси (y) графика) представляет собой значение, вычисленное с применением приведенного выше уравнения (1) после облучения мобильного протона при 72 м.д. (site 1) и 99 м.д. (site 2) соответственно.
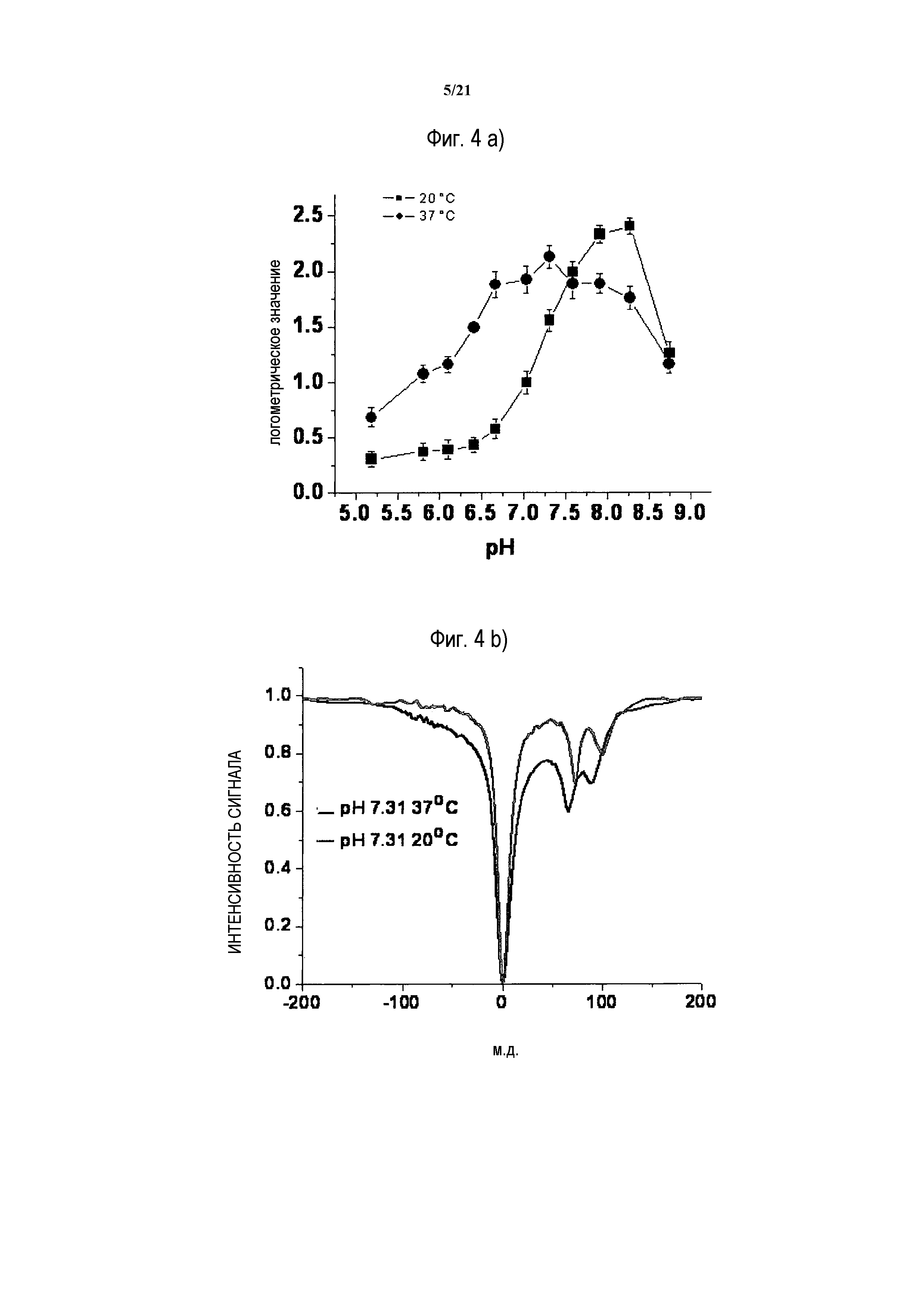
Фиг.4: Панель a) логометрическая кривая, демонстрирующая зависимость ST-эффекта от температуры (логометрическое значение, полученное посредством применения логометрического подхода к калибровочным кривым ST, полученным, соответственно, при 20°C (квадраты) и 37°C (кружки); панель b) Z-спектры YbHPDO3A (24 мМ раствор, pH 7,31), полученные при 37°C (темная линия) и 20°C, тот же pH (серая линия), с применением импульса облучения 24 мкТл.
Фиг.5: Панель a) МР-изображение in vitro фантома, содержащего 3 различных конгломерата клеток MSH, которые были инкубированы (капилляр 2) или электропорированы (капилляр 3) с раствором YbHPDO3A, или клеток, инкубированных с PBS и применяемых в качестве контроля (капилляр 1). В фантом также включен пустой капилляр (4); панели b) и c) карты ST, полученные после облучения фантома соответственно при 72 и 99 м.д., соответственно.
Фиг.6: Z-спектр, полученный из мочевого пузыря мыши, которой впрыскивали 200 мкл 150 мМ раствора YbHPDO3A, записанный на спектрометре Bruker Avance 300. В полученном спектре темная линия соответствует аппроксимирующей кривой, и светлая аппроксимирующей кривой, перенесенной, для того чтобы минимум Z-спектра соответствовал 0 м.д.
Фиг.7: Логометрическая кривая YbHPDO3A, измеренная in vitro при 33°, полученная из калибровочных кривых, полученных для данной температуры, как в примере 6.
Фиг.8: Морфологическое изображение (левые изображения) и карты ST, полученные в области опухоли мыши до (PRE) и непосредственно после (Post) в/в инъекции YbHPDO3A. ST-эффект, вычисленный после облучения, соответственно, при 66,2 и 91,6 м.д. наложили на соответствующее анатомическое изображение, на котором область опухоли выглядит как более светлый участок (красный на фактически наблюдаемом изображении). На данной фигуре символ @ указывает на частоту облучения, используемую для того, чтобы вызвать перенос насыщения, то есть, как уже сказано, 66,2 и 91,6 м.д.
Фиг.9: Формула тетрамерного производного YbHPDO3A, иначе обозначаемого как (Yb3+)4HPDO3A-тетрамер или просто тетрамер.
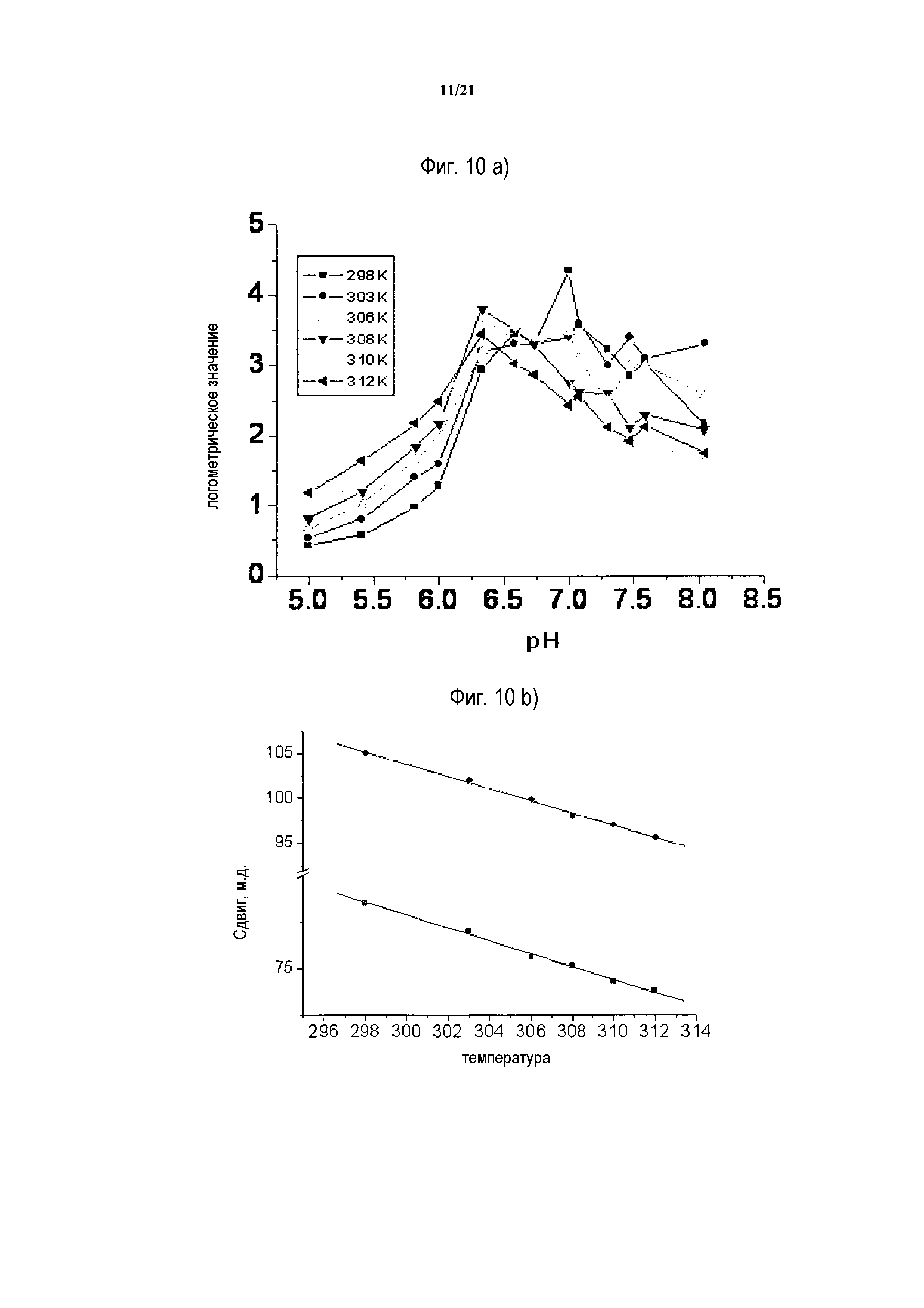
Фиг.10: Панель a) логометрические кривые, измеренные при различных температурах в диапазоне от 298 до 312K после облучения гидроксильных протонов двух изомеров YbHPDO3A-тетрамера и применения логометрического подхода; панель b) зависимость от температуры химического сдвига ЯМР гидроксильных протонов, принадлежащих двум различимым по ЯМР изомерам YbHPDO3A-тетрамера.
Фиг.11: МРТ изображения фантома, содержащего YbHPDO3A-тетрамер в различных концентрациях в диапазоне от 0,26 до 8,4 мМ (pH 7,4 и 298K). Слева T2-взвешенное изображение; справа полученная карта ST.
Фиг.12: Панель a) спектр1Н ЯМР EuHPDO3A в D2O; панель b) Увеличение спектра ЯМР EuHPDO3A в D2O, 278K, pH 2 (выше) и H2O, 310K, pH 2 (ниже), подтверждающее существование двух различимых по ЯМР изомеров, имеющих химический сдвиг 20,5 и 16,7, соответственно (pH 2 и 20°C), все еще различимых при физиологической температуре (спектрометр Advance 600).
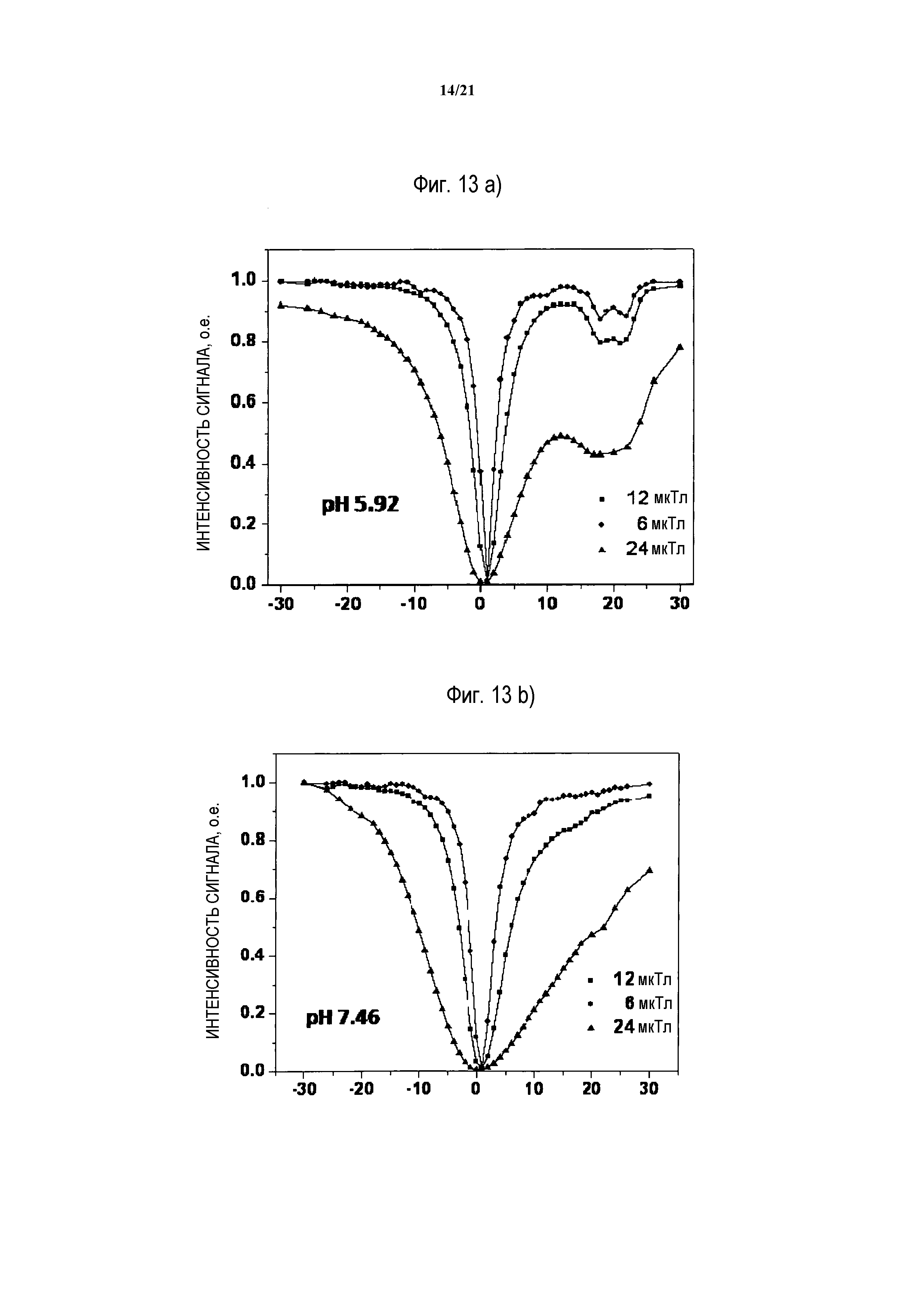
Фиг.13: Панель a) Z-спектры EU(III)HPDO3A (20 мМ) при pH 5,92 и 37°C при различных импульсах мощности; панель b) Z-спектры EU(III)HPDO3A (20 мМ) при pH 7,46 и 37°C при различных импульсах мощности; панель c) профиль ST EU(III)HPDO3A 20 мМ при pH 7,46, 37°C и мощности облучения, равной 24 мкТл.
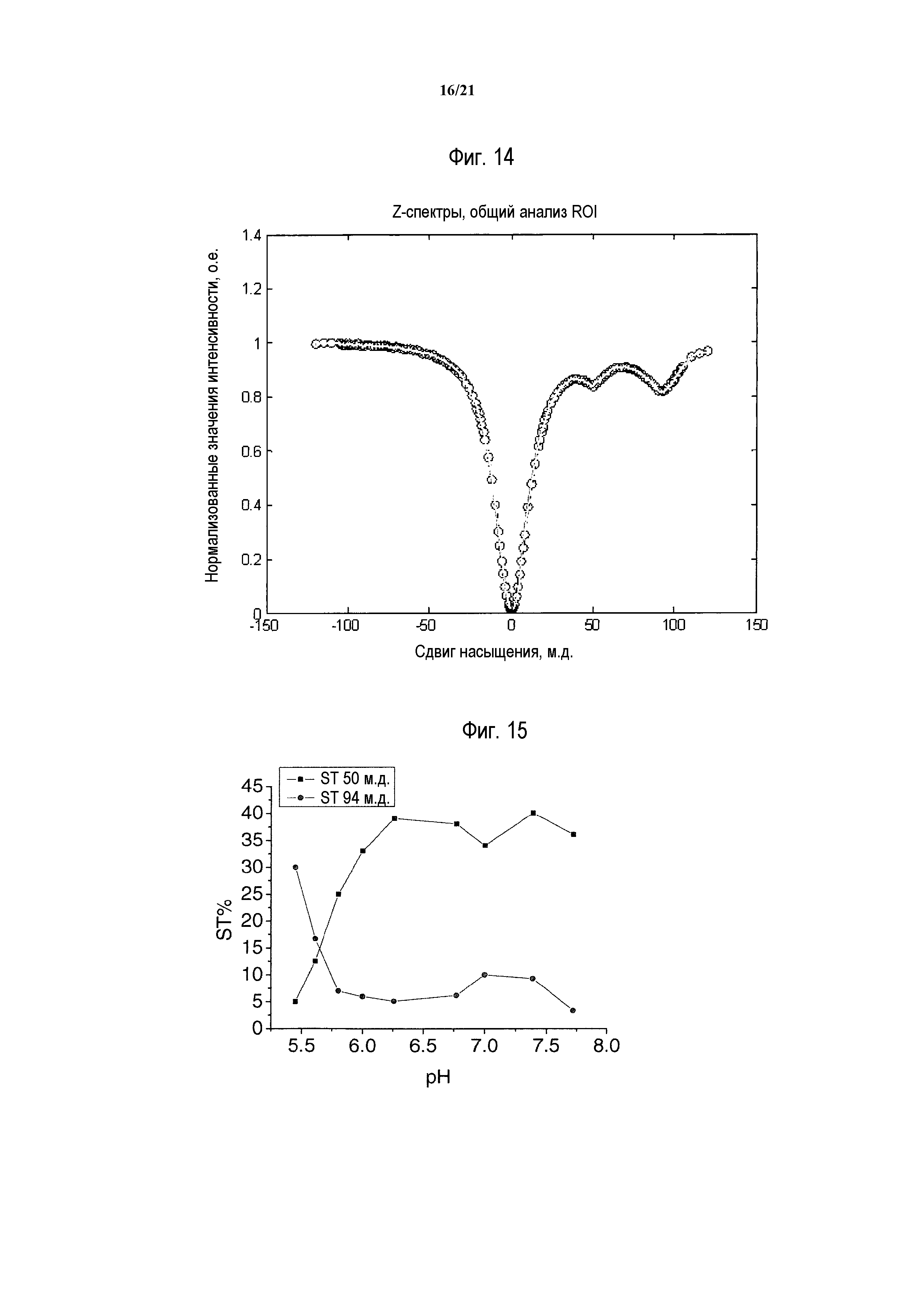
Фиг.14: Z-спектр, полученный при 7 Тл, раствора соединения 2 при pH 5,8 и 298K.
Фиг.15: Зависимость от pH ST-эффекта, полученного после облучения гидроксильных протонов двух магнитно неэквивалентных изомеров, демонстрируемых соединением 2 (при 20°C) (калибровочные кривые).
Фиг.16: Логометрическая кривая, описывающая зависимость ST (логометрические значения) от pH, полученная посредством применения логометрического подхода к кривым ST фиг.15.
Фиг.17: Сравнение спектров1H ЯМР соединения 3, полученных в D2O при 278K и 298K и магнитном поле 600 МГц. Спектр высокого разрешения, полученный при более низкой температуре, ясно показывает наличие двух наборов сигналов из-за двух основных изомеров (SAP и TSAP) в растворе. Те же самые сигналы гораздо шире при комнатной температуре.
Фиг.18: Z-спектры соединения 3, полученные в растворах (20 мМ), забуференных при различных значениях pH в диапазоне от 6,41 до 8, 20°C; магнитное поле 7 Тл, мощность облучения 24 мкТл.
Фиг.19: Профили переноса насыщения ST (слева) и соответствующие Z-спектры (справа), полученные в водных растворах (20 мМ) соединения 4, забуференных при различных значениях pH в диапазоне от 5,08 до 6,30, при 293K, магнитное поле 7 Тл, мощность облучения 24 мкТл.
Фиг.20: Логометрическая кривая ST, демонстрирующая зависимость от pH логометрических значений, вычисленных для соединения 4 из кривых ST, полученных после облучения гидроксильных протонов при 75 и 100 м.д., соответственно.
Фиг.21: Z-спектры соединения 5, полученные в водных растворах (20 мМ), забуференных при различных значениях pH в диапазоне от 5,5 до 8,1, 20°C; магнитное поле 7 Тл, мощность облучения 24 мкТл.
Подробное описание изобретения
Источник магнитно неэквивалентных мобильных протонов, позволяющий разработать не зависящий от концентрации способ CEST МРТ, раскрытый в настоящем описании, представлен мобильными протонами, принадлежащими, по меньшей мере, двум различимым по ЯМР изомерам парамагнитного CEST-агента.
При этом если не указано иное, выражение "различимые по ЯМР изомеры CEST-агента" означает стереоизомеры данного CEST-агента, обеспечивающие сигналы мобильных протонов, которые разделены и, следовательно, различимы в спектре ЯМР, или, другими словами, которые демонстрируют различные резонансы (в спектре ЯМР) для обмениваемых протонов, причем каждый резонанс соответствует одному из различимых по ЯМР стереоизомеров.
В этом отношении подходящие CEST-агенты, обеспечивающие данный тип магнитно неэквивалентных протонов, являются, предпочтительно, комплексными соединениями лантаноида (III), содержащими группу обмена протонами на боковом ответвлении хелатирующего лиганда, который демонстрирует, по меньшей мере, два различимых по ЯМР стереоизомера в растворе.
Интересно, что спектр ЯМР данных комплексных соединений, фактически, демонстрирует, по меньшей мере, два раздельных резонанса для обмениваемого протона, причем каждый соответствует одному из различимых по ЯМР изомеров, которые можно селективно облучать в логометрических способах визуализации с применением CEST.
Применение различимых по ЯМР изомеров подходящих комплексных соединений лантаноида (III) в качестве источника магнитно неэквивалентных мобильных протонов, пригодного для применения в логометрическом способе визуализации с применением CEST, составляет вариант осуществления настоящего изобретения.
В настоящее время ясно, что для правильного применения данного альтернативного источника неэквивалентных мобильных протонов в in vivo способах, основанных на CEST, необходимо, чтобы комплекс лантаноида, используемый в качестве CEST-зонда, демонстрировал несколько различимых по ЯМР стереоизомеров в физиологических условиях, или, другими словами, чтобы резонансы обмениваемых протонов различных стереоизомеров, демонстрируемых комплексом Ln(III), были еще соответствующим образом сдвинуты и хорошо детектировались в водном растворе при комнатной температуре и физиологическом pH.
В настоящем описании определен особый класс комплексных соединений Ln(III), содержащих макроциклический хелатирующий лиганд, снабженный гидроксильной (-OH) группой обмена протонами на боковом ответвлении, который существует в растворе в виде смеси нескольких различимых по ЯМР изомеров. Преимущественно, спектр ЯМР данных комплексных соединений демонстрирует, по меньшей мере, два резонанса для обмениваемых OH протонов, соответствующих различным стереоизомерам, которые при этом присутствуют и хорошо различимы в водном растворе, и в физиологических условиях по pH и температуре.
Применение данного конкретного класса комплексных соединений лантаноида (III) в логометрическом способе визуализации с применением CEST представляет предпочтительный вариант осуществления настоящего изобретения.
Таким образом, в одном варианте осуществления настоящее изобретение относится к применению комплексных соединений лантаноида (III), содержащих хелатирующий лиганд, снабженный гидроксильной группой обмена протонами на боковом ответвлении, в логометрических способах визуализации с применением CEST, которые используют магнитно неэквивалентные мобильные протоны (по меньшей мере, два), каждый из которых предоставлен различимым по ЯМР стереоизомером рассматриваемого лантаноидного комплекса.
Подходящие металлические ионы лантаноида (III) (или Ln(III)) выбирают из группы, состоящей из: празеодима (III), неодима (III), диспрозия (III), эрбия (III), тербия (III), гольмия (III), тулия (III), иттербия (III) и европия (III), где европий (III) и иттербий (III) являются предпочтительными, и иттербий (III) является особенно предпочтительным.
С другой стороны, подходящие хелатирующие лиганды согласно настоящему изобретению включают макроциклические хелатирующие лиганды, снабженные гидроксильной (OH) группой обмена протонами на одном боковом ответвлении.
Предпочтительными являются хелатирующие лиганды формулы (I):
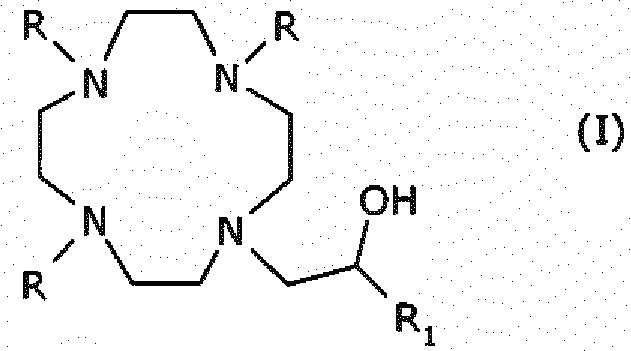
где:
R представляет собой -CH(R2)-COOH,
R1 представляет собой H или прямую, или разветвленную C1-C5алкильную цепь, которая необязательно прерывается группой, выбранной из -O-, -N-, -CO-, -NHCO-, -CONH-, и необязательно замещена одним или более атомами галогена, гидроксильными (-OH) группами, фенильной или замещенной фенильной группой или группой, выбранной из -COOH, -NHR3 или -NR4R5, где R3, R4 и R5 являются одинаковыми или различными, прямыми или разветвленными C1-C3алкильными группами, которые необязательно замещены одной или более гидроксильными группами или C1-C3алкоксигруппами,
R2 представляет собой H или C1-C5алкильную цепь, которая необязательно замещена одной или C1-C3алкоксигруппой, или гидроксиалкоксигруппой.
В этом отношении специалисту должно быть понятно, что, когда хелатирующий лиганд формулы (I) образует комплекс с несущим три положительных заряда металлическим ионом лантаноида (III), карбоксильная группа фрагмента R находится в соответствующей депротонированной (-CH(R2)-COO-) форме.
В настоящем описании, если не указано иное, под термином прямая, или разветвленная C1-C5алкильная группа подразумевают линейную или разветвленную алкильную цепь, содержащую от 1 до 5 атомов углерода. Подходящие примеры алкильных групп включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил и тому подобные.
Вышеуказанные алкильные группы могут быть дополнительно замещены и/или прерываться одной или более галогенными, гидроксильными, алкокси, амино, гидроксиалкокси, фенильными или замещенными фенильными группами, как изложено выше.
Под галогеном или атомами галогена подразумевают атомы йода, хлора, брома или фтора, причем последний является особенно предпочтительным.
Под термином замещенный фенил подразумевают фенильную группу, замещенную одним или более атомами галогена, гидроксильными группами (OH) или C1-C3алкоксигруппами или группой, выбранной из групп -(CH2)nCOOH, -NO2, -NHR3 или -NR4R5, где n равен 0 или 1, и R3, R4 и R5 определены выше.
Под термином C1-C3алкокси подразумевают любую алкилоксигруппу, в которой алкильный фрагмент включают вплоть до 3 атомов углерода.
Под гидроксиалкоксигруппой подразумевают любую из вышеуказанных C1-C3алкоксигрупп, в которой алкильный фрагмент дополнительно замещен гидроксильной группой.
Подходящие примеры алкокси- или гидроксиалкоксигрупп настоящего изобретения включают, например, метокси, этокси, н-пропокси, гидроксиметилокси, -2-гидроксиэтокси, 2,3-дигидроксипропокси и тому подобные.
Предпочтительно, в соединениях формулы (I) R2 представляет собой H, и R1 представляет собой H или прямую, или разветвленную C1-C4алкильную цепь, необязательно прерываемую атомом кислорода или замещенную -ОН, -NH2 или фенильной группой, которая может в свою очередь быть замещена или не замещена гидроксильной группой, C1-C3алкоксигруппой, нитрогруппой или карбоксильной группой.
Еще более предпочтительно, в соединениях формулы (I) R2 представляет собой H, и R1 представляет собой группу, выбранную из:
-H,
-CH3,
-CH2CH3,
-CH2OH,
-CH2-O-CH3,
-CH(CH2OH)2,
-CH2-CH(OH)-CH2OH,
-CH2-O-CH2-C6H5,
-CH2-O-CH2-(C6H5-COOH),
-CH2-O-CH2-(C6H5-NO2).
Особенно предпочтительным согласно настоящему изобретению является комплекс Ln(III) с лигандом формулы (I), где R2 представляет собой H, и R1 представляет собой -CH3, тогда как хелатный ион Ln(III) выбирают из Yb(III) или Eu(III).
Димерные или мультимерные производные, содержащие, по меньшей мере, два хелатирующих лиганда формулы (I), необязательно связанных своими группами R1, которые могут быть соответствующим образом функционализированы, если нужно, включены в настоящее изобретение, и обычно имеют повышенную чувствительность.
Соответственно, в другом варианте осуществления настоящее изобретение относится к комплексным соединениям Ln(III), в которых хелатирующий лиганд является димерным или мультимерным производным соединения формулы (I).
Одним примером данного типа соединения является, например, раскрытое в примере 1 ниже вместе со схемой его получения.
Тетрамерный хелатирующий лиганд примера 1, или HPDO3A-тетрамер, как используется в настоящем описании взаимозаменяемо, а также его соли и его хелатные комплексы с (вплоть до) четырьмя парамагнитными металлическими ионами, являются новыми и составляют дополнительный объект настоящего изобретения.
В этом отношении подходящие парамагнитные металлические ионы выбирают из следующих: Fe(2+), Fe(3+), Cu(2+), Ni(2+), Rh(2+), Co(2+), Cr(3+), Gd(3+), Eu(3+), Dy(3+), Tb(3+), Pm(3+), Nd(3+), Tm(3+), Ce(3+), Y(3+), Ho(3+), Er(3+), La(3+), Yb(3+), Mn(3+), Mn(2+). Более предпочтительно, парамагнитный металлический ион представляет собой Gd(3+) или лантаноидный металл, выбранный из Yb(3+), Eu(3+) или Dy(3+).
Дополнительным объектом настоящего изобретения является диагностическая композиция, содержащая парамагнитный или, особенно, бис- или полихелатный с Ln(III) комплекс димерного или мультимерного производного хелатирующего лиганда формулы (I) или его физиологически приемлемую соль вместе с подходящими добавками и/или носителями, для применения при МР томографии. В предпочтительном варианте осуществления указанная диагностическая композиция содержит (Yb3+)4HPDO3A-тетрамер, имеющий структуру как на фиг.9.
Может быть удобным, чтобы хелатирующий лиганд формулы (I), содержащий, по меньшей мере, три карбоксильные группы на макроциклическом остове, имел форму физиологически приемлемой соли.
Подходящие примеры катионов неорганических оснований, которые можно применять, для того чтобы образовывать соли с лигандами настоящего изобретения, содержат ионы щелочных или щелочноземельных металлов, таких как калий, натрий, кальций или магний.
Предпочтительные катионы органических оснований включают, в том числе, катионы первичных, вторичных и третичных аминов, таких как этаноламин, диэтаноламин, морфолин, глюкамин, N-метилглюкамин, N,N-диметилглюкамин.
Предпочтительные анионы неорганических кислот, которые можно соответствующим образом применять для данной цели, включают ионы галогеновых кислот, такие как хлориды, бромиды, йодиды, или другие ионы, такие как сульфаты.
Предпочтительные анионы органических кислот включают анионы кислот, обычно используемых в фармацевтических способах образования солей основных веществ, такие как, например, ацетат, сукцинат, цитрат, фумарат, малеат или оксалат.
Предпочтительные катионы и анионы аминокислот включают, например, катионы и анионы таурина, глицина, лизина, аргинина, орнитина или аспарагиновой и глутаминовой кислот.
С другой стороны, все три карбоксильные группы макроциклического лиганда участвуют в хелатировании несущего три положительных заряда иона лантаноида. В результате комплексные соединения Ln(III) формулы (I) являются нейтральными и, следовательно, подходящими для применений in vivo без какой-либо дополнительной нейтрализации или солеобразования.
В случае, вместо этого, когда хелатирующий лиганд содержит в своей структуре дополнительную кислотную группу, необходима его нейтрализация с помощью катиона, обычно используемого в фармацевтических способах, например, выбранного из перечисленных выше, для того чтобы получить его физиологически приемлемую соль.
Хелатные комплексы Ln(III) формулы (I), где R1 отличается от H, и их димерное или мультимерное производное включают хиральный центр, представленный гидроксилированным углеродом на боковом ответвлении. Поэтому в растворе они демонстрируют несколько стереоизомерных форм, различающихся, по существу, расположением ацетатных ответвлений (ориентированных по часовой стрелке или против часовой стрелки), двумя конформациями макроциклического кольца и конформацией хирального центра (R,S). В этом отношении специалисту в данной области известно, что когда R1 представляет собой H, указанный углерод утрачивает свою хиральность, но изомеры, отличающиеся расположением ацетатных ответвлений или конформацией кольца, все равно существуют.
Настоящее изобретение основано на том наблюдении, что диастереоизомеры, демонстрируемые в водном растворе при комнатной температуре данным предпочтительным классом комплексных соединений, различимы по спектру ЯМР. Более конкретно, авторы обнаружили, что комплексные соединения Ln(III) формулы (I), предлагаемые данным изобретением, демонстрируют в растворе при физиологических температуре и pH, по меньшей мере, два соответственно сдвинутых резонанса для обмениваемых OH протонов, причем они соответствуют различным различимым по ЯМР диастереоизомерам данного комплекса. Преимущественно подтверждается, что различные стереоизомеры одного и того же комплекса имеют одинаковое биораспределение in vivo и одинаковое отношение относительных концентраций с течением времени. Следовательно, несколько соответственно сдвинутых резонансов OH протонов различимых по ЯМР стереоизомеров комплексного соединения Ln(III) формулы (I), демонстрируемых в растворе, можно эффективно использовать для разработки логометрического способа CEST МРТ, пригодного для применения в условиях in vivo, для того чтобы получить CEST-изображения in vivo, которые не подвержены влиянию локальной концентрации рассматриваемого комплекса.
Кроме того, интересно, что величина переноса насыщения ST, полученного селективным насыщением обмениваемых OH протонов комплексных соединений Ln (III) согласно настоящему изобретению, является заметно чувствительной или, другими словами, восприимчивой к физическим или химическим параметрам микроокружения, в котором они распределены. В результате, особый класс комплексных соединений Ln (III), предлагаемых настоящим изобретением, помимо того, что он пригоден для применения в способе визуализации с применением CEST для получения не зависящего от концентрации CEST-контраста, может также эффективно использоваться в качестве чувствительных CEST-агентов, особенно в логометрических способах визуализации с применением CEST, позволяющих получить измерения in vivo и карты физических или химических параметров, представляющих диагностический интерес, которые не подвержены влиянию локальной концентрации самого агента.
Соответственно, в дополнительном варианте осуществления настоящее изобретение относится к применению комплексного соединения Ln (III) формулы (I) в качестве не зависящего от концентрации чувствительного CEST-агента, особенно в логометрическом способе визуализации с применением CEST для определения физических или химических параметров, представляющих диагностический интерес, in vivo.
В настоящем изобретении, если не указано иное, под физическим или химическим параметром, представляющим диагностический интерес, подразумевают параметр, выбранный из температуры, pH, парциального давления кислорода (pO2) или углекислого газа (pCO2), концентрации определенного иона или метаболита или определенной ферментативной активности.
В этом отношении в настоящее время понятно, что зная значение или карту физического(их) или химического(их) параметра(ов) в исследуемом органе тела или области, доктор может производить диагностические оценки тех физиологических или метаболических процессов, представляющих диагностический интерес, которые непосредственно зависят от указанного(ых) определяемого(ых) параметра(ов).
В другом дополнительном варианте осуществления настоящее изобретение относится к логометрическому способу CEST МРТ, который включает использование, т.е. облучение подходящим радиочастотным импульсом и, таким образом, индуцирование переноса насыщения у сигнала объемной воды, по меньшей мере, двух магнитно неэквивалентных мобильных протонов, которые предоставляются двумя или более различимыми по ЯМР стереоизомерами подходящего CEST-зонда.
В этом отношении специалисту должно быть понятно, что логометрический способ CEST МРТ, использующий магнитно неэквивалентные мобильные протоны, принадлежащие различимым по ЯМР изомерам любого подходящего CEST-зонда, включен в настоящее изобретение. В предпочтительном варианте осуществления рассматриваемый CEST-зонд представляет собой парамагнитный CEST-агент и, более предпочтительно, представляет собой комплексное соединение Ln (III), предлагаемое настоящим изобретением.
В особенно предпочтительном варианте осуществления CEST-зонд представляет собой комплекс Ln(III) с хелатирующим лигандом HPDO3A, или бис- или полихелатный комплекс его димерного или мультимерного производного, или его физиологически приемлемую соль.
Соответственно, в своем предпочтительном варианте осуществления настоящее изобретение относится к логометрическому способу CEST МРТ, который включает применение комплексного соединения Ln (III) формулы (I) или его димерного или мультимерного производного, для получения не зависящей от концентрации визуализации с применением CEST in vivo. Даже более предпочтительно, указанный логометрический способ CEST МРТ применяют для определения физического или химического параметра, представляющего диагностический интерес, in vivo в органе тела, жидкости или ткани человека или животного, которое не подвержено влиянию локальной концентрации CEST-агента.
Более конкретно, в предпочтительном варианте осуществления настоящее изобретение относится к не зависящему от концентрации способу визуализации с применением CEST для получения изображений органа тела, области, жидкости или ткани человека или животного, который включает:
a) введение хелатных комплексов Ln(III) формулы (I) или их димерного или мультимерного производного человеку или животному и необязательно получение морфологических изображений МРТ области органа тела, жидкости или ткани человека или животного, представляющих интерес, предпочтительно с применением T2-взвешенной последовательности,
b) получение Z-спектра в диапазоне частот, точно настроенном на резонансные частоты двух магнитно неэквивалентных мобильных протонов, принадлежащих различимым по ЯМР стереоизомерам введенного комплекса лантаноида, и вычисление логометрических значений из эффекта переноса насыщения (ST), измеренного для двух данных пулов мобильных протонов,
c) получение не зависящих от концентрации изображений указанных области органа тела, жидкости или ткани человека или животного,
причем стадия C данного способа, предпочтительно, включает наложение карты логометрических значений, полученных из измеренных ST-эффектов на стадии b) данного способа, на предварительно полученные морфологические изображения рассматриваемых органа тела, области, жидкости или ткани человека или животного. Для этого на стадии b) получают резонансные частоты двух магнитно неэквивалентных мобильных протонов из спектра ЯМР данного комплекса, который, если он не известен к данному моменту, может быть соответствующим образом получен до визуализации с применением CEST.
Вышеописанный способ визуализации с применением CEST может быть реализован in vitro (ex vivo) или, предпочтительно, in vivo для получения изображений органа тела, области, жидкости или ткани человека или животного in vivo.
В другом предпочтительном варианте осуществления настоящее изобретение относится к способу определения посредством применения метода CEST МРТ физического или химического параметра, представляющего диагностический интерес, в органе тела, области, жидкости или ткани человека или животного, который включает:
i) введение хелатных комплексов Ln(III) формулы (I) или их димерного или мультимерного производного человеку или животному и необязательно получение морфологического изображения МРТ органа тела, области, жидкости или ткани человека или животного, представляющих интерес,
ii) получение Z-спектра в диапазоне частот, точно настроенном на резонансные частоты двух магнитно неэквивалентных мобильных протонов, принадлежащих различимым по ЯМР стереоизомерам введенного комплекса лантаноида, и вычисление логометрических значений из эффекта переноса насыщения (ST), измеренного для двух данных пулов мобильных протонов,
iii) получение из вычисленных значений ST не зависящей от концентрации карты (или логометрической карты) представляющего интерес параметра в рассматриваемом органе тела, области, жидкости или ткани человека или животного и, необязательно, наложение указанной карты на морфологическое изображение,
причем указанное определение осуществляют in vitro (ex vivo) или, предпочтительно, in vivo, в органе тела, области, жидкости или ткани человека или животного.
В особенно предпочтительном варианте осуществления настоящее изобретение относится к не зависящему от концентрации способу визуализации с применением CEST для получения карты pH in vivo в представляющих интерес органе тела, области, жидкости или ткани человека или животного, который включает использование двух магнитно неэквивалентных мобильных протонов, принадлежащих различимым по ЯМР стереоизомерам хелатного комплекса Ln(III) с хелатирующим лигандом HPDO3A, или его димерного или мультимерного производного, или его физиологически приемлемой соли.
В этом отношении специалисту в данной области будет понятно, что стадии визуализации, подробно описанные выше, включая облучение частотой мобильных протонов, получение Z-спектра, вычисление логометрического ST-эффекта и получение с применением предварительно полученных калибровочных кривых карты требуемого физического или химического параметра в органе тела или области, осуществляются автоматически при томографии, при соответствующих установках, в соответствии со способами, применяемыми в современной диагностической практике, и с применением способов обработки данных, например раскрытых в протоколе визуализации, предлагаемом в экспериментальном разделе, и в цитируемой литературе, включенной в настоящее описание посредством ссылки.
В способах настоящего изобретения комплексное соединение Ln (III) формулы (I) (или его димер, или мультимер, или его физиологически приемлемую соль), действующее как CEST-агент согласно настоящему изобретению, вводят в форме подходящего фармацевтического препарата.
В этом отношении в соответствии с особенно предпочтительным вариантом осуществления настоящего изобретения оба вышеописанных основанных на CEST способа осуществляют на организмах человека или животного, в которые соответствующим образом предварительно вводят фармацевтический препарат, содержащий подходящее количество комплексного соединения лантаноида согласно настоящему изобретению. Другими словами, в соответствии с особенно предпочтительным вариантом осуществления настоящее изобретение относится к способу визуализации органа тела, области, жидкости или ткани человека или животного in vivo или к определению или картированию in vivo, посредством применения метода CEST МРТ, физического или химического параметра, представляющего диагностический интерес, в органе тела, области, жидкости или ткани человека или животного посредством применения основанного на CEST метода магнитно-резонансной томографии, который осуществляют на организме человека или животного, в который соответствующим образом предварительно вводят фармацевтический препарат, содержащий подходящее количество комплексного соединения лантаноида (III) согласно настоящему изобретению. Под "подходящим количеством", как применяется в настоящем описании, подразумевают любое количество контрастного вещества настоящего изобретения или его фармацевтической композиции, которое достаточно для выполнения его намеченной диагностической цели (целей): т.е., например, получения не зависящих от концентрации контрастированных изображений или получения не зависящей от концентрации карты представляющего интерес параметра в рассматриваемых органе тела, области, жидкости или ткани человека или животного, посредством применения основанного на CEST метода визуализации при помощи МРТ.
При этом указанное введение или предварительное введение можно, например, осуществлять посредством внутрисосудистой инъекции (например, внутривенной, внутриартериальной, внутрижелудочковой инъекции и так далее) или интратекально, интраперитонеально, внутрилимфатически, внутриполостно, перорально или энтерально.
Инъецируемые фармацевтические составы комплексных соединений лантаноида (III) формулы (I) обычно получают путем растворения активного ингредиента, а именно комплекса лантаноида или его фармацевтически приемлемой соли, и фармацевтически приемлемых эксципиентов в воде подходящей с фармакологической точки зрения чистоты. Полученный состав соответствующим образом стерилизуют, и его можно использовать как таковой или, альтернативно, его можно лиофилизировать и восстанавливать перед применением.
Данные составы можно вводить в концентрациях, зависящих от диагностических требований, в дозе в диапазоне от 0,01 до 0,5 ммоль на кг массы тела.
Как указано выше, особенно предпочтительным согласно настоящему изобретению является комплекс Ln(III) с лигандом формулы (I), где R2 представляет собой H, и R1 представляет собой -CH3, тогда как хелатный ион Ln (III) выбирают из Y(III) или Eu(III). Комплексные соединения лантаноида с данным лигандом, таким образом, используются в качестве неограничивающего конкретного примера настоящего изобретения.
Данный лиганд известен в данной области техники под названием HPDO3A, и его хелатный комплекс с Gd3+ является хорошо известным контрастным веществом, применяемым при обычной визуализации при помощи МРТ, который долгое время предлагается на рынке как ProHance™. Очень низкая токсичность и отличная переносимость, проявляемые данным агентом, давно известны в данной области техники и сделали его применение в способах визуализации с применением CEST особенно выгодным и безопасным, даже в дозах, которые необходимы для данного способа, составляющих вплоть до 10-кратной дозировки (0,1 ммоль/кг) по сравнению с обычно используемой в обычной МРТ.
Структура комплексов HPDO3A с Gd (III) и Yb(III) была определена с помощью рентгеновского излучения (см., например Kumar, K.; Chang, C.A.; Francesconi, L.C; Dischino, D.D.; Malley, M.F.; Gougoutas, J.Z.; Tweedle, M.F. Inorg. Chem. 1994, 33, 3567-75). В указанной статье сообщается, что, даже если начинать с рацемического раствора, наличие асимметричной части, включающей хиральную 2-гидроксипропильную группу, приводит к двум независимым комплексам, имеющим диастереомерную конформацию, отличающуюся относительной конформацией макроцикла, тогда как все координирующие элементы двух изолированных комплексов имеют одинаковую ориентацию, т.е. одинаково скручены.
В растворе комплексы HPDO3A с Ln(III), имеющие следующую структуру (в который мобильный OH протон выделен кружком):

обычно демонстрируют восемь изомерных форм, более конкретно, четыре диастереоизомера и четыре энантиомера, что схематически изображено на схеме 1 ниже.

Две диастереоизомерные формы, наиболее вероятно соотносимые с формами R и S того же самого конформера, соответственно, обнаруживаются в спектре ЯМР (показан на фиг.1) и, в частности, в Z-спектре Yb-HPDO3A (приведен на фиг.2b), что ясно показывает два участка переноса насыщения, с достаточными основаниями соотносимые с двумя главными диастереоизомерами. При этом, признаки двух других диастереоизомеров можно получить из сравнения спектров ЯМР данного комплекса, полученных при различных температурах.
В полном согласии со всем вышесказанным гидроксильные группы двух различимых по ЯМР диастереоизомеров данного комплекса демонстрируют хорошо различимые химические сдвиги, соответственно при 72 и 99 м.д. при 20°C, показанные на фиг.2a), и различные скорости обмена, что можно использовать для того, чтобы разработать логометрический способ согласно настоящему изобретению.
Чувствительность, демонстрируемую данным комплексом в отношении pH, также верифицировали посредством МРТ экспериментов in vitro, описанных подробно в экспериментальном разделе.
Полученные результаты подтверждают, что зависимость переноса насыщения от pH, демонстрируемая каждым их мобильных OH протонов диастереоизомеров Yb-HPDO3A, различна. Это делает возможным использование логометрического подхода, позволяющего не зависящее от концентрации определение внутриклеточного pH, в исследовании, проведенном над мезенхимальными стволовыми клетками.
Интересно, что карты ST, полученные в данном исследовании, показанные на фиг.5, панели b и c, соответственно, подтверждают, что ST-эффект можно наблюдать только для клеток, инкубированных или электропорированных с YbHPDO3A, тогда как какое-либо насыщение получали при отсутствии данного комплекса. Наблюдаемый ST-эффект был выше для электропорированных клеток, соответствующих измеренному pH, равному 7,00±0,2, тогда как pH, измеренный в конгломерате клеток 2, составил 6,8±0,3.
Существенно, что высокая чувствительность, продемонстрированная Yb(III)HPDO3A в отношении pH, позволила эффективно использовать его при определении pH среды в области опухоли (подкожная опухоль), как показано на фиг.8. Данный результат, насколько известно авторам, никогда не был получен ранее с помощью CEST-агентов.
Также исследовали чувствительность, демонстрируемую Yb(III)HPDO3A в отношении температуры среды. Полученные результаты подчеркивают, в частности, соответствующую чувствительность к температуре, демонстрируемую химическими сдвигами двух гидроксильных протонов двух различимых по ЯМР диастереомеров. Таким образом, поскольку химический сдвиг не зависит от концентрации, можно точно получить температуру окружающей среды просто по значению химического сдвига, наблюдаемого в Z-спектре комплекса.
Как ожидалось, авторы наблюдали значительно возросшую чувствительность, особенно в отношении температуры, с тетрамерным производным Yb(III)HPDO3A, содержащим вплоть до четырех мобильных OH протонов для каждого из различимых стереоизомеров.
Чувствительность в отношении pH, такую же, как продемонстрированная Yb(III)HPDO3A, также подтвердили для соответствующего комплексного соединения Eu(III). Спектр ЯМР данного комплекса, показанный на фиг.12, ясно демонстрирует наличие двух основных изомеров. Сигналы, принадлежащие гидроксильной группе данных изомеров, определяли посредством сравнения спектров ЯМР двух различных растворов, содержащих EuHPDO3A в воде и D2O, соответственно. Два химических сдвига (для OH протонов двух диастереоизомеров), таким образом, определены, соответственно, при 20,5 м.д. (из воды) и 16,7 м.д. при pH=2 и 37°C. Тем не менее, из фиг.13 видно, что при повышении pH раствора в сторону физиологических значений, скорость обмена протонами возрастает, и разделение по химическому сдвигу между данными двумя сигналами уменьшается, делая трудным их селективное облучение при физиологических условиях. Профиль ST, полученный с применением различных импульсов облучения, однако, показывает, что, работая на 6 мкТл (мощность облучения), можно наблюдать оба отдельных резонанса и затем осуществлять логометрическое измерение, в то время как перенос насыщения еще остается в любом случае наблюдаемым с применением промежуточного значения резонансной частоты (по отношению к действительным частотам поглощения), а именно приблизительно 18 м.д. Из всего изложенного выше следует, что YbHPDO3A и EuHPDO3A можно эффективно применять в качестве чувствительных CEST-агентов для определения pH и температуры in vivo.
В этом отношении можно уверенно предполагать, что как Yb-, так и Eu-HPDO3A обладают свойствами в отношении биораспределения, экскреции и переносимости, аналогичными свойствам, продемонстрированным ProHance®, соответствующим гадолиниевым комплексом, и они, соответственно, могут делать возможным тот же тип обычной анатомической визуализации, как и тот, в котором он участвует. Преимущественно, однако, применение Yb- и Eu-комплексов позволяет получать основанные на CEST анатомические изображения и еще больше дополнять и интегрировать анатомическую информацию, получаемую с помощью ProHance® при обычной МРТ, дополнительной информацией, касающейся pH и/или температуры указанной анатомической области, качество изображения которой повышают, в которой распределен данный агент.
В качестве дополнительного доказательства принципа также определяли чувствительность к pH, демонстрируемую Yb(III) комплексом 4-[2-гидрокси-3-[4,7,10-трис[карбоксиметил-2-(1,1-диметилэтокси)-1,4,7,10-тетраазациклододец-1-ил]пропокси]бензойной кислоты (здесь и далее соединение 2), имеющим следующую формулу:

Z-спектр соединения 2 (приведенный на фиг.14) демонстрирует два участка переноса насыщения, которые соотносятся с двумя основными диастереоизомерами данного комплекса в растворе. Наличие двух различных диастереоизомеров обеспечивает два соответствующим образом сдвинутых резонанса OH протонов, соответственно при 50 и 94 м.д.
Исследования чувствительности, проведенные с данным комплексом, подтвердили его чувствительность к pH, которая, как это видно на фиг.15 и 16, оказалась выше при более кислом pH, предпочтительно в диапазоне от 5,5 до 6,2, благодаря более высокой скорости обмена, демонстрируемой гидроксильными протонами диастереоизомеров данного комплекса, относительно мобильных протонов Yb(III)HPDO3A.
Дополнительный пример чувствительного к pH агента согласно настоящему изобретению представлен Yb3+ комплексом 1-(2-гидроксиэтил)-1,4,7,10-тетраазациклододекан-4,7,10-триуксусной кислоты, здесь и далее соединение 3, имеющий формулу:

Спектр ЯМР данного соединения, приведенный на фиг.17, демонстрирует два набора сигналов, которые можно отнести к наличию двух основных изомеров, соответствующих SAP и TSAP формам данного соединения. Действительно, в растворе присутствует четыре изомера, отличающиеся или расположением ацетатных ответвлений, или конформацией макроциклического кольца. Поскольку данные изомеры представляют собой пару энантиомеров, в спектре ЯМР ожидается, фактически, два набора сигналов, поскольку энантиомеры неотличимы с точки зрения ЯМР. В полном согласии со сказанным выше Z-спектр соединения 3 (приведенный на фиг.l8 для каждого из проверенных значений pH) демонстрирует наличие двух участков насыщения, соотносимых с OH группами на гидроксиэтильных ответвлениях двух различных изомеров данного соединения в виде квадратной антипризмы и скрученной квадратной антипризмы (SAP и TSAP), каковые резонансы сдвинуты, соответственно, на 78 и 99 м.д.
Результаты исследования чувствительности, проведенного над данным соединением в диапазоне pH от 6,4 до 8, представленные на фиг.18, подтверждают его чувствительность по отношению к pH.
Другим примером Ln (III) комплексного соединения согласно настоящему изобретению является Yb(III) комплекс 1-[2,3-дигидрокси-3-аминопропил]-1,4,7,10-тетраазациклододекан-4,7,10-триуксусной кислоты (здесь и далее соединение 4), имеющий следующую формулу:

В данном случае, наличие двух различных диастереоизомеров должно обеспечить четыре неэквивалентных мобильных протона, принадлежащий двум различным гидроксильным -OH группам на каждом из двух различных изомеров SAP и TSAP.
Действительно, Z-спектр и профили переноса насыщения ST соединения 4 (приведенные на фиг.19) подтверждают наличие трех соответствующим образом сдвинутых протонных резонансов при 10, 75 и 100 м.д., соответственно. Из них сильно сдвинутые резонансы (при 75 и 100 м.д., соответственно) могут быть с достаточным основанием соотнесены с обмениваемыми протонами ближайших к координационной сфере металлического центра групп OH двух различных изомеров (SAP и TSAP) соединения в растворе, тогда как менее сдвинутый сигнал соответствует обмениваемому протону другой группы OH, более удаленной от металлического центра. Четвертый обменный пул не обнаруживается в спектре, вероятно, из-за слишком большой по временной шкале ЯМР скорости обмена.
Исследования чувствительности, проведенные in vitro с данным комплексным соединением, подтверждают его чувствительность к pH, как видно на фиг.19 и 20.
В частности, полученные результаты подтверждают, что зависимость переноса насыщения от pH, демонстрируемая мобильными OH протонами двух диастереоизомеров соответственно при 75 м.д. и 100 м.д., различна. Это позволило использовать логометрический подход, делающий возможным не зависящее от концентрации определение внутриклеточного pH, в исследовании, проведенном над мышиными макрофагическими клетками (J774), меченными данным комплексным соединением, давший значение pH, равное 6,8.
В качестве дополнительного примера исследовали Yb комплекс 1-[1,3,4-тригидроксибутан-2-ил]-1,4,7,10-тетраазациклододекан-4,7,10-триуксусной кислоты (здесь и далее соединение 5), имеющий следующую структуру:

В этом отношении не имеет значения, что комплекс того же самого хелатирующего лиганда с Gd3+ является хорошо известным контрастным веществом, одобренным для клинического применения при обычной визуализации с помощью МРТ и продаваемым как GADOVIST®). Его получение описано в EP0448191.
Структура данного соединения включает два хиральных центра, значительно увеличивающих количество возможных стереоизомеров по сравнению, например, с Yb(III)HPDO3A.
Z-спектр данного соединения, приведенный на фиг.21, демонстрирует, по меньшей мере, 2 пика, различимых при 50 и 75 м.д., соответственно, которые обусловлены двумя наиболее распространенными стереоизомерными формами из множества возможных. Высокая скорость обмена, характеризующая мобильные протоны данного соединения, приводит к тому, что наиболее распространенные различимые по ЯМР изомеры можно обнаружить только при низких значениях pH, приблизительно 5,5. При более высоких значениях pH вместо этого в спектре появляется пик при -75, вероятно из-за изменения структуры соединения.
Хотя оно не принадлежит к комплексам лантаноида (III) формулы (I), предпочтительным согласно настоящему изобретению, вышеуказанное соединение 5 предоставляет неэквивалентные мобильные протоны, принадлежащие гидроксильным группам различимых по ЯМР стереоизомеров агента в растворе, позволяя разработать не зависящий от концентрации способ визуализации с применением CEST согласно настоящему изобретению.
Соответственно, применение лантаноидного (III) комплекса 1-[1,3,4-тригидроксибутан-2-ил]1,4,7,10-тетраазациклододекан-4,7,10-триуксусной кислоты в логометрическом способе визуализации с применением CEST согласно настоящему изобретению, а также логометрический способ CEST МРТ, использующий два магнитно неэквивалентных мобильных протона, предоставляемых двумя различимыми по ЯМР изомерами указанного Ln(III) комплекса, входят в объем настоящего изобретения и составляют дополнительный вариант его осуществления.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Хелатирующие лиганды формулы (I) известны в данной области техники или могут легко быть получены в соответствии с известными способами или путями синтеза, хорошо известными специалисту в данной области.
Неограничивающие примеры синтетических методик включены, кроме того, ниже, например, в примеры 1-3, вместе с подробным рассмотрением применения комплексных соединений лантаноида (III) согласно настоящему изобретению в логометрическом способе визуализации с применением CEST.
Способ и условия визуализации с применением CEST
Улучшение CEST МР-контраста определяли на изображениях, полученных при 7 Тл на спектрометре Bruker Avance 300, оснащенном датчиком микроизображений Micro2.5. Использовали обычную последовательность спин-эхо RARE (RARE-фактор 64) со временем эхо, равным 3,3 мс, и значением TR, равным 5 с. Использовали матрицу сбора данных 64×64 с квадратным FOV, составляющим 10 мм. Всю последовательность предваряли схемой насыщения, состоящей из непрерывного волнового импульса длительностью 2 с интенсивностью РЧ, равной 24, 12, 6 мкТл. Затем анализировали Z-спектры, для того чтобы определить логометрическе значение с применением программного обеспечения, скомпилированного на платформе MATLAB, работающего, в общих чертах, как раскрыто в Development and validation of a smoothing-splines-based correction method for improving the analysis of CEST-MR images, Stancanello J, Terreno E, Delli Castelli D, Cabella C, Uggeri F 1, Aime S.; CONTRAST MEDIA & MOLECULAR IMAGING Volume: 3, Issue: 4, Pages: 136-149, 2008; и в Methods for an improved detection of the MRI-CEST effect. Terreno E, Stancanello J, Longo D, Delli Castelli D, Milone L, Sanders HMHF, Kok MB, Uggeri F, Aime S; CONTRAST MEDIA & MOLECULAR IMAGING; Volume: 4; Issue: 5; Pages: 237-247; 2009, которые включены в настоящее описание посредством ссылки. Общую парамагнитную концентрацию раствора определяли посредством измерения магнитной восприимчивости раствора на спектрометре Bruker Avance 600 (12 Тл).
Пример 1
Получение (Yb3+)4HPDO3A-тетрамера
Тетрамерный хелатный комплекс YbHPDO3A-тетрамер получали с применением синтетической методики, схематически представленной на схеме 2, основные стадии которой подробно описаны ниже.


3,6-диокса-8-ноненовая кислота (I): Раствор 2-аллилоксиэтанола (112 г; 1,1 моль) в ТГФ (100 мл) вливали по капле в суспензию гидрида натрия (60% в масле) (88 г; 2,2 моль) в ТГФ (250 мл) при механическом перемешивании. После 20 ч при комнатной температуре, добавляли по капле раствор бромуксусной кислоты (138,9 г; 1,0 моль) в ТГФ (150 мл), вызывая спонтанное кипячение растворителя с обратным холодильником. Раствор выдерживали с условиях кипячения с обратным холодильником в течение 2 часов, затем разбавляли этанолом (50 мл) и через 30 мин суспензию концентрировали. Остаток растворяли в воде (400 мл), и раствор промывали этиловым эфиром (3×100 мл), дихлорметаном (2×100 мл); кислотность водной фазы повышали до pH 1 добавлением 37% хлористоводородной кислоты, и продукт экстрагировали дихлорметаном (300 мл+450 мл). Органическую фазу промывали водой (4×50 мл), насыщенным раствором соли (40 мл) и выпаривали до жидкого остатка, который перегоняли в вакууме при давлении 67 Па, с получением 3,6-диокса-8-ноненовой кислоты (I) в виде бесцветной жидкости (119,5 г; 0,746 моль). Выход 75%. p.eb67 Па 98-100°C. Титр 93,5%.
12,12'-бис[2-аза-3-оксо-58-диокса-11-ундеканил]-1,13-диен-4,7,17,20-триокса-9,15-диоксо-10,14-диазатрикозан (II)
3,6-Диокса-8-ноненовую кислоту (I) (40,1 г; 0,25 моль), диизопропилэтиламин (42,6 мл; 32,4 г; 0,25 моль) и гексафторфосфат O-(бензилтриазол-1-ил)-N,N,N',N'-тетраметилурония [HBTU] (96,0 г; 0,25 моль) добавляли к суспензии 2,2'-бис-аминометилен-1,3-диаминопропана (7,2 г; 0,050 моль) в диметилформамиде (200 мл). Через пять дней раствор выпаривали до остатка (200 г), который обрабатывали этиловым эфиром (4×400 мл, 4×50 мл); раствор эфира промывали 5% раствором NaHCO3 (6×50 мл), концентрированным насыщенным раствором соли и выпаривали до остатка (84,6 г), который обрабатывали водой (2×100 мл) и затем сушили при высоком вакууме (50 Па), с получением 12,12'-бис[2-аза-3-оксо-5,8-диокса-1-ундеканил]-1,13-диен-4,7,17,20-триокса-9,15-диоксо-10,14-диазатрикозана (II) в виде твердого остатка (34,5 г).
12,12'-бис[2-аза-3-оксо-5,8-диокса-10,11-оксиранундецил]-(1,2)(22,23)-диоксиран-4,7,17,20-триокса-9,15-диоксо-10,14-диазатрикозан (III)
Раствор м-хлорпербензойной кислоты (70,5%) (MCPBA) (36,9 г; 0,150 моль) в хлороформе (500 мл) выделяли из воды и добавляли по капле в раствор 12,12'-бис[2-аза-3-оксо-5,8-диокса-11-ундеканил]-1,13-диен-4,7,17,20-триокса-9,15-диоксо-10,14-диазатрикозана (II) (17,5 г; 0,025 моль) в хлороформе (300 мл) при перемешивании. После двух дней при комнатной температуре раствор промывали 5% раствора NaHCO3 до полного удаления как м-хлорпербензойной, так и м-хлорбензойной кислот, затем водой и насыщенным раствором соли. Органический раствор выпаривали до остатка, с получением 12,12'-бис[2-аза-3-оксо-5,8-диокса-10,11-оксиранундецил]-(1,2)(22,23)-диоксиран-4,7,17,20-триокса-9,15-диоксо-10,14-диазатрикозана (III) в виде воскоподобного твердого вещества (20,0 г).
1,23-бис[4,7,10-триуксусная кислота[1,4,7,10-тетраазациклододекан-(1)-ил]]-12,12'-бис[11[4,7,10-триуксусная кислота)-[1,4,7,10-тетраазациклододекан-(1)-ил]]2-аза-3-оксо-5,8-диокси-10-гидроксиундеканил]2,22-дигидрокси-4,7,17,20-тетрокси-9,15-диоксо-10,14-диазатрикозан (V)
Раствор 12,12'-бис[2-аза-3-оксо-5,8-диокса-10,11-оксиранундецил]-(1,2)(22,23)-диоксиран-4,7,17,20-триокса-9,15-диоксо-10,14-диазатрикозана (III) (3,6 г; 0,0047 моль), 1,1-диметилэтилового трис-эфира 1,4,7,10-тетраазациклододекан-1,4,7-триуксусной кислоты (10,3 г; 0,020 моль) и диизопропилэтиламина (4,0 мл; 0,047 моль) в ацетонитриле (50 мл) нагревали при 50°C в течение десяти дней. Раствор выпаривали, с получением 1,23-бис[4,7,10-трис(1,1-диметилэтилацетат)[1,4,7,10-тетраазациклодекан-(1)-ил]]-12,12'-бис[11-[4,7,10-трис(1,1-диметилэтилацетат)[1,4,7,10-тетраазациклодекан-(1)-ил]]-2-аза-3-оксо-5,8-диокси-10-гидроксиундеканил]-2,22-дигидрокси-4,7,17,20-тетрокси-9,15-диоксо-10,14-диазатрикозана (IV). Неочищенный остаток охлаждали на ледяной бане; добавляли при перемешивании трифторуксусную кислоту (20 мл); к раствору добавляли триизопропилсилан (100 мкл). Через пять дней добавляли этиловый эфир (200 мл), фильтровали и сушили осадок (13,4 г). Твердое вещество растворяли в воде (15 мл) и очищали хроматографией на Amberchrome CG161 (2,6×55 см) (AKTA FPLC), используя в качестве элюента смесь метанол/вода (градиент от 0 до 100% об/об). После сушки вымораживанием чистой фракции получали требуемый продукт (V) в виде белого твердого вещества (4,4 г);
Комплексометрический титр = 74% (с 0,1н сульфатом цинка и мурексидом при pH 10), причем основной примесью оказалась трифторуксусная кислота.
Спектр ЯМР (13C) полученного продукта соответствует структуре хелатирующего лиганда.
Иттербиевый комплекс тетра 1,23-бис[4,7,10-триацетат[1,4,7,10-тетраазациклододекан-(1)-ил]]-12,12'-бис[11-[4,7,10-триацетат)-[1,4,7,10-тетраазациклододекан-(1)-ил]]-2-аза-3-оксо-5,8-диокси-10-гидроксиундеканил]-2,22-дигидрокси-4,7,17,20-тетрокси-9,15-диоксо-10,14-диазатрикозана (1:4) (VI)
Раствор гексагидрата хлорида иттербия (3,92 моль) в воде (25 мл) добавляли к раствору лиганда (V) (3,5 г; 0,98 ммоль; точное молярное количество лиганда определяли комплексометрическим титрованием) в воде (100 мл) при перемешивании, раствор очень медленно нейтрализовали до pH 7,0 добавлением 2н гидроксида натрия (11,4 мл). Когда избыток лиганда составлял <0,2%, и pH был постоянным, раствор обессоливали с использованием колонки Sephadex G10, с получением после сушки вымораживанием требуемого комплекса, иттербиевый комплекс 1,23-бис[4,7,10-триацетат[1,4,7,10-тетраазациклододекан-(1)-ил]]-12,12'-бис[11-[4,7,10-триацетат)-[1,4,7,10-тетраазациклододекан-(1)-ил]]2-аза-3-оксо-5,8-диокси-10-гидроксиундеканил]-2,22-дигидрокси-4,7,17,20-тетрокси-9,15-диоксо-10,14-диазатрикозана (1:4) (VI) (2,3 г).
Пример 2
Получение хелатного иттербиевого комплекса 1-(2-гидроксиэтил)-1,4,7,10-тетраазациклододекан-4,7,10-триуксусной кислоты (соединение 3)
Хелатный комплекс иттербия, соответствующий соединению 3, получали с применением общей синтетической методики, схематически представленной на схеме 3, основные стадии которой подробно описаны ниже.

(1,1-диметилэтиловый эфир) 1-[2-[тетрагидропиран-(2-ил)оксо]этил]-1,4,7,10-тетраазациклододекан-4,7,10-триуксусной кислоты (VIII)
(2-Бромэтокси)тетрагидропиран (VII) синтезировали в соответствии со способом, описанным в J. Org. Chem. 1986, 51, 752-755. Данный субстрат (27,5 ммоль; 5,75 г) растворяли в 50 мл ацетонитрила и добавляли по капле к суспензии K2CO3 (75 ммоль; 10,37 г), с получением бромгидрата DO3A-трис-трет-бутилового эфира, например, как раскрыто в WO96/28433 (25 ммоль; 14,89 г), в ацетонитриле (150 мл). После одной ночи при комнатной температуре смесь фильтровали и выпаривали. Затем остаток растворяли в этилацетате (100 мл) и промывали водой и насыщенным раствором соли. Органический раствор концентрировали в вакууме, и неочищенный продукт очищали хроматографией на силикагеле с градиентом этилацетат/этанол. Фракции, содержащие требуемый продукт, объединяли и выпаривали, с получением желтого масла (8,1 г; выход 49 %).
1H-ЯМР (600 МГц, CD3Cl) и13C ЯМР (150 МГц, CD3Cl) соответствуют предполагаемой структуре.
МС [M+H]+ вычислено: 642,46, получено: 643,64.
1-(2-гидроксиэтил)-1,4,7,10-тетраазациклододекан-4,7,10-триуксусная кислота (IX)
Промежуточный продукт VIII (15 г; 21,5 ммоль) растворяли в воде (30 мл), ТГФ (60 мл) и уксусной кислоте (120 мл) и перемешивали при комнатной температуре в течение 24 ч, для того чтобы удалить ТГП фрагмент. Затем смесь концентрировали и добавляли по капле триизопропилсилан (120 мкл) и ТФУ (40 мл) при 0°C. После 3 дней при комнатной температуре неочищенный продукт осаждали диэтиловым эфиром (200 мл), отфильтровывали и очищали жидкостной хроматографией на смоле Amberchrom CG161 с использованием 0,2% ТФУ в воде. Затем фракции, содержащие требуемый продукт, объединяли и сушили вымораживанием, понижали кислотность 1н HCl (60 мл) и снова сушили вымораживанием (7,3 г; выход 80%).
1H-ЯМР (600 МГц, D2O) и13C ЯМР (150 МГц, D2O) соответствуют предполагаемой структуре.
МС [M+H]+ вычислено: 390,21, получено: 391,53.
(3-)металлат 1-(2-гидроксиэтил)-1,4,7,10-тетраазациклододекан-4,7,10-триацетата (X)
Реакции комплексообразования осуществляли с помощью MeCl3 (Me=Yb, Eu, Tm или Dy) в водном растворе при pH 6,5 способом добавления лиганда (см. J. Med. Chem. 2006, 49, 4926). Эквимолярное количество водного раствора MeCl3 медленно добавляли к водному раствору соединения IX, поддерживая pH при 6,5 0,1н NaOH. Смесь перемешивали при комнатной температуре, пока pH оставался постоянным. Когда достигали небольшого избытка металла, за чем следили с помощью теста по ксиленоловому оранжевому (см. Contrast Med. Mol. Imaging 2006, 1, 184), добавляли небольшой избыток лиганда (<2%). Затем комплексы обессоливали с использованием эксклюзионной хроматографии и сушили вымораживанием.
Титр комплекса, определенный с помощью теста Эванса (DM Corsi, C. P. Iglesias, H. van Bekkum, JA Peters, Magnetic Resonance in Chemistry, 2001, 39, (11), 723-726), составил 98%.
Пример 3
Получение хелатного комплекса иттербия 1-[2,3-дигидроксипропил]-1,4,7,10-тетраазациклододекан-4,7,10-триуксусной кислоты (соединение 4)
Хелатный комплекс иттербия, соответствующий соединению 4, получали с применением синтетической методики схемы 4, основные стадии которой подробно описаны ниже.

1-[2,3-дигидроксипропил]-1,4,7,10-тетраазациклододекан-4,7,10-триуксусная кислота (XIII)
Раствор 2,3-эпоксипропанола (12,0 г; 0,20 моль), 1,1-диметилэтилового трис-эфира 1,4,7,10-тетраазациклододекан-1,4,7-триуксусной кислоты (10,3 г; 0,020 моль) (XI) и диизопропилэтиламина (8,0 мл; 0,09 моль) в ацетонитриле (59 мл) нагревали при 59°C в течение трех дней. Раствор выпаривали, с получением 1-[2,3-дигидроксипропил]-1,4,7,10-тетраазациклододекан-4,7,10-трис(1,1-диметилэтилацетата) (XII). Неочищенный остаток растворяли в дихлорметане (100 мл) и охлаждали на ледяной бане, и затем добавляли трифторуксусную кислоту (15 мл) при перемешивании; дихлорметан выпаривали, добавляли трифторуксусную кислоту (90 мл) и триизопропилсилан (200 мкл). Через один день добавляли этиловый эфир (200 мл) и осадок отфильтровывали и сушили (16,5 г). Твердое вещество растворяли в воде (30 мл) и очищали на Amberlite XAD 1600 (5×12 см) (AKTA FPLC) с водой в качестве элюента. После сушки вымораживанием получали чистую фракцию требуемого лиганда (XIII) в виде белого твердого вещества; (10,6 г).
Спектр ЯМР (13C) соответствует структуре хелатирующего лиганда.
Затем осуществляли комплексометрическое титрование полученного лиганда (с сульфатом цинка 0,1н и мурексидом при pH 10), для определения необходимого для его полного комплексообразования количества оксида лантаноида.
Полученный титр (41,9%) подтверждает остаточное присутствие растворителя и трифторуксусной кислоты, которые удаляют после образования лигандом комплекса.
Металлат 1-[2,3-дигидрокси-3-аминопропил]-1,4,7,10-тетраазациклододекан-4,7,10-триацетата (XIV)
Оксид металла (2,21 ммоль) добавляли к раствору 1-[2,3-дигидроксипропил]-1,4,7,10-тетраазациклододекан-4,7,10-триуксусной кислоты (XII) (4,4 г; 4,43 ммоль; вычислено по комплексометрическому титрованию) в воде (30 мл) при перемешивании, раствор нагревали до 90°C. Когда оксид растворялся, раствор охлаждали, фильтровали на Millipore 0,45 мкм и медленно добавляли Relite 3ASFB до pH 7; смолу отфильтровывали, и раствор сушили вымораживанием, с получением металлата 1-[2,3-дигидроксипропил]-1,4,7,10-тетраазациклододекан-4,7,10-триацетата (XIV)
Избыток лиганда определяли посредством комплексометрического титрования 0,001M хлоридом металла с использованием ксиленолового оранжевого в качестве индикатора до pH 5,8.
Титр комплекса вместо этого определяли посредством теста Эванса (DM Corsi, C. P. Iglesias, H. van Bekkum, JA Peters, Magnetic Resonance in Chemistry, 39, 11, стр. 723-726, 2001).
Пример 4
Исследование in vitro
Чувствительность Yb(III)HPDO3A в отношении pH.
Чувствительность Yb(III)HPDO3A в отношении pH исследовали in vitro с применением фантома, содержащего 14 капилляров, из которых 11 содержали растворы YbHPDO3A с концентрацией 24 мМ при различных pH в диапазоне от 5,19 до 8,75 (капилляры 1-11), и 3 содержали растворы YbHPDO3A при pH 7,31 и концентрациях в диапазоне от 3 до 24 мМ. Эксперименты по CEST МРТ осуществляли при 20°C и 37°C. Получали МР-изображения фантома, облучаемого при 72 и 99 м.д. соответственно, и они показаны на фиг.3. В частности, на фиг.3c) продемонстрирована карта ST, полученная после облучения гидроксильных протонов при 72 м.д. (20°C; импульс мощности облучения 24 мкТл), тогда как на фиг.3d) продемонстрирована карта ST, полученная после облучения гидроксильных протонов при 99 м.д. (20°C, импульс мощности облучения 24 мкТл).
Полученные результаты подтверждают, что зависимость от pH переноса насыщения, демонстрируемая каждым из OH протонов двух диастереоизомеров Yb(III)HPDO3A в растворе, различна, причем это позволяет использовать логометрический подход. Затем получали калибровочные кривые, приведенные на фиг.3e), посредством измерения изменения ST-эффекта при изменении pH, полученного после облучения гидроксильных протонов двух изомеров соответственно при 72 м.д. и 99 м.д., позволяющие получить логометрическую кривую фиг.3f).
Пример 5
Применение Yb(III)HPDO3A для определения внутриклеточного pH
В качестве клеточной линии для данного исследования выбирали мезенхимальные стволовые клетки. Клетки, использованные в данном эксперименте, экстрагировали из мышиного костного мозга, затем культивировали в среде Alpha MEM с 20% FBS (фетальная бычья сыворотка). При первом пассаже к клеткам добавляли примоцин. Когда конфлюентность достигала приблизительно 70%, клетки снимали с помощью 0,25 трипсин-EDTA, промывали PBS и ресуспендировали с 0,15M раствором YbHPDO3A. Часть клеток инкубировали при 37°C в течение 3 часов, тогда как часть электропорировали. Затем клетки промывали в PBS и готовили для эксперимента по МРТ.
В частности: получали CEST-карты (показанные на фиг.5) для фантома, содержащего: 1) конгломерат клеток MSH, инкубированных в течение 3 часов с раствором, содержащим 0,15M YbHPDO3A в PBS, 37°, pH 7,4 (капилляр 2); 2) конгломерат клеток MSH, электропорированых с раствором 0,15M YbHPDO3A в PBS, pH 7,4 (капилляр 3); 3) конгломерат клеток MSH, инкубированных только с PBS и использованных в качестве контроля (капилляр 1), и пустой капилляр (капилляр 4). ST-эффект в % измеряли после облучения фантома при 72 и 99 м.д., соответственно. Полученные карты ST, приведенные на фиг.5, панели b и c, соответственно, демонстрируют, что ST-эффект, в %, можно наблюдать только для клеток, инкубированных или электропорированных с YbHPDO3A, тогда как какое-либо насыщение получали при отсутствии данного комплекса. Наблюдаемый ST-эффект был выше для электропорированных клеток, соответствующих измеренному pH, равному 7,00±0,2, тогда как pH, измеренный в конгломерате инкубированных клеток капилляра 2, составил 6,8±0,3.
Пример 6
Исследования in vivo
Применение Yb(III)HPDO3A для определения pH на животной модели меланомы
Измерения in vivo осуществляли после внутривенной инъекции 1,2 ммоль/кг YbHPDO3A на животной модели меланомы. Самкам мышей C57BI6 возраста от 6 до 10 недель (Charles River Laboratories, Calco, Италия) подкожно вводили в левый бок 0,2 мл одной суспензии, содержащей приблизительно 1×106 мышиных клеток меланомы B16, полученных из ATCC (Manassas, VA, США) и выращенных в среде DMEM (среда Игла, модифицированная по способу Дульбекко), дополненной 10% FBS, глутамином 2 мМ, пенициллином 100 ед/мл и стрептомицином 100 мкг/мл.
МР-изображения с улучшенным CEST-контрастом получали при 7 Тл на спектрометре Bruker Avance 300 (Bruker, Германия), оснащенном датчиком микроизображений Micro2.5.
Мышам инъецировали раствор YbHPDO3A (200 мкл 150 мМ раствора YbHPDO3A, что соответствует 1,2 ммоль/кг CEST-агента, то есть трем клинически одобренным дозам для ProHance®) через 7 дней после введения клеток, т.е. когда опухолевое образование достигало среднего диаметра, равного приблизительно 4 мм.
Z-спектры получали до и непосредственно после в/в инъекции агента с применением последовательности RARE (RARE-фактор 8, эффективное время эхо 4,1 мс), предваряемой квадратным непрерывным волновым импульсом (продолжительность 2 с, мощность 12 мкТ, диапазон частоты от -20 до 20 м.д. с шагом 1 м.д.). CEST-контраст измеряли в мочевом пузыре, почках и опухоли. Z-спектр, полученный в мочевом пузыре (приведенный на фиг.6), демонстрирует сдвиг для обменного пула, соответствующий физиологической T, более низкой (33°C), чем ожидаемая 37°C, из-за анестезии. Калибровку зависимости ST от pH затем повторяли при этой температуре, следуя способу, описанному выше в примере 2. Полученная логометрическая кривая показана на фиг.7.
Затем измеряли ST-эффект в мочевом пузыре, почках и опухоли, применяя логометрический способ, что давало pH, равный 6,06±0,2 в мочевом пузыре, 6,24±0,2 в мозговом веществе почек, 6,6±0,2 в области опухоли.
На фиг.8 вычисленную карту ST в области опухоли наложили на соответствующе анатомическое изображение, где она выглядит как более светлая область, которая является фактически ярко-красной на изображении, появляющемся на дисплее томографа.
Пример 7
Исследование in vitro
Характеристики чувствительности Yb(III)HPDO3A в отношении температуры
Для данного исследования использовали раствор Yb(III)HPDO3A (24 мМ), имеющий pH 7,31. Z-спектры данного раствора, полученные при 20° и 37°C соответственно, демонстрируют, что химический сдвиг гидроксильных протонов различимых по ЯМР диастереоизомеров Yb(III)HPDO3A в растворе является очень чувствительным к температуре. Фактически, как показано на фиг.4, панель b), при прохождении от 20° до 37°C резонансные частоты, соответствующие двум различным стереоизомерам данного комплекса, изменяются соответственно от 99 до 88 и от 72 до 64,3 м.д. Поскольку протонный химический сдвиг не зависит от концентрации агента, простое получение Z-спектра позволяет точно определять температуру среды и затем определять pH посредством подходящей калибровки in vitro.
Пример 8
Характеристики чувствительности Yb(III)HPDO3A-тетрамера в отношении температуры
Данное исследование осуществляли с помощью фантома, содержащего раствор YbHPDO3A-тетрамера в сыворотке, имеющий различные концентрации в диапазоне от 0,26 до 8,4 мМ, pH 7,4 и 298K. Зависимость химических сдвигов мобильных OH протонов (стереоизомеров тетрамерного комплекса) от температуры исследовали аналогично описанному выше для мономерного соединения. Полученные логометрические кривые, показанные на фиг.10, по существу подтверждают результаты, полученные с мономерным соединением в примере 7. Тем не менее, как и ожидалось, и как видно на фиг.10, панель b), чувствительность на молекулу тетрамерного комплекса сильно возросла (при сравнении с соответствующим мономерным комплексом).
Пример 9
Применение соединения 4 для определения внутриклеточного pH
В качестве клеточной линии для данного исследования выбирали мышиные макрофаговые клетки (J774). Диапазон чувствительности логометрической кривой, полученной с данным соединением, предварительно надлежащим образом настраивали в диапазоне внутриклеточного pH.
В частности, посредством применения логометрического подхода к кривым ST, вычисленным относительно pH после облучения двух пулов мобильных протонов с наибольшими сдвигами при 75 м.д. (site 1) и 100 м.д. (site 2) соответственно, удалось получить логометрическую кривую фиг.20, демонстрирующую изменение логометрического ST в зависимости от pH в диапазоне pH от 5,5 до 7.
Соединение 4 поглощалось мышиными макрофагическими клетками (J774). J774 получали из Американской коллекции типовых культур (ATCC, Manassass, VA). Клетки культивировали в среде Игла, модифицированной по способу Дульбекко (DMEM), дополненной 10% фетальной бычьей сывороткой (FBS), пенициллином 100 ед/мл и стрептомицином 100 мкг/мл. Их высевали в колбы с 75 см2 с плотностью приблизительно 2×l04 клеток на см2 и культивировали в увлажняемом инкубаторе с 5% CO2 при 37°C. J774 инкубировали в течение ночи с 70 мМ соединения 4. Клетки промывали и повторно инкубировали со средой для их роста в течение 3 часов. Затем клетки снимали с помощью 0,25% трипсина-EDTA и готовили для эксперимента по CEST МРТ.
Логометрическое значение переноса насыщения вычисляли, с получением Z-спектры фантома, содержащие конгломераты клеток или инкубированных в течение ночи с соединением 4, или инкубированных со средой для роста.
Наблюдаемый ST-эффект для инкубированных клеток приводил к значению pH, равному 6,8.
Пример 10
Исследование in vitro
Чувствительность соединения 4 в отношении pH
Чувствительность соединения 4 в отношении pH исследовали in vitro с применением фантома, содержащего 6 капилляров, содержащих растворы комплекса иттербия, имеющего концентрацию 20 мМ и различный pH в диапазоне от 5,08 до 7,4. Эксперименты по CEST МРТ осуществляли при 20°C. Z-спектры, полученные от фантома, облучаемого (мощность облучения 24 мкТл) при 75 и 100 м.д. соответственно, показаны на фиг.19.
Логометрическая кривая ST, которую получили как функцию pH, показана на фиг.20.
Реферат
Группа изобретений относится к медицине, конкретно к применению неэквивалентных мобильных протонов, принадлежащих к различимым по ЯМР стереоизомерам CEST-агента, в логометрическом способе визуализации с применением CEST и к комплексным соединениям лантаноида (III), демонстрирующим, по меньшей мере, два различимых по ЯМР стереоизомера в растворе, применяемых в качестве не зависящих от концентрации чувствительных CEST-агентов. Различимые по ЯМР стереоизомеры CEST-агента используют в качестве полезных биомаркеров определенного заболевания, точно связанного с данными изменениями. 5 н. и 8 з.п. ф-лы, 21 ил., 10 пр.
Формула

где:
R представляет собой -СН (R2)-СООН,
R1 представляет собой Н или прямую, или разветвленную C1-C4алкильную цепь, которая необязательно прерывается -O-, и необязательно замещена одной или несколькими гидроксигруппами или фенилом, который необязательно замещен нитро или карбоксильной группой -(СН2)nCOOH, в которой n равно 0 или 1,
R2 представляет собой Н или его мультимерное производное формулы
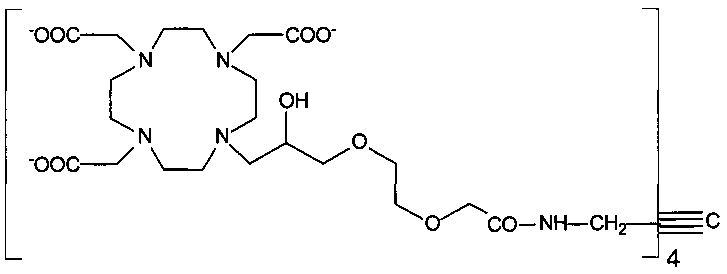
-H,
-СН3,
-СН2СН3,
-CH2OH,
-CH2-O-CH3,
-СН(СН2ОН)2,
-СН2-СН(ОН)-CH2OH,
-СН2-O-СН2-С6Н5,
-СН2-O-СН2-(С6Н5-COOH),
-СН2-О-СН2-(C6H5-NO2).

где
R представляет собой -СН(R2)-СООН,
R1 представляет собой Н или прямую, или разветвленную C1-C4 алкильную цепь, которая необязательно прерывается -O-, и необязательно замещена одной или несколькими группами гидроксила или фенилом, который необязательно замещен нитро или карбоксильной группой -(СН2)nCOOH, в которой n равно 0 или 1,
R2 представляет собой Н,
или его мультимерное производное формулы
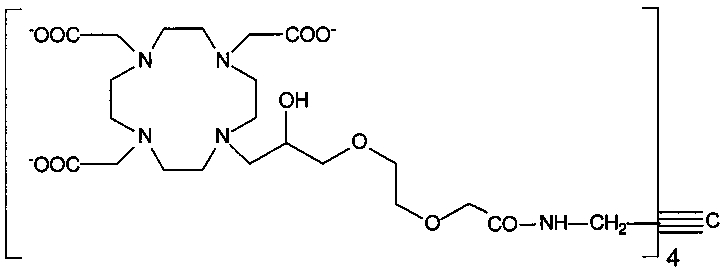
посредством метода CEST MPT, который включает:
i) необязательно получение морфологических изображений МРТ, представляющих интерес органа тела, области, жидкости или ткани человека или животного,
ii) получение Z-спектра в диапазоне частот, точно настроенном на резонансные частоты двух магнитно неэквивалентных мобильных протонов, принадлежащих различимым по ЯМР стереоизомерам предварительно введенного комплекса лантаноида, и вычисление логометрических значений из эффекта переноса насыщения ST, измеренного для данных пулов мобильных протонов,
iii) получение из вычисленных значений ST не зависящей от концентрации карты представляющего интерес параметра в рассматриваемом органе тела, области, жидкости или ткани человека или животного и, необязательно, наложение указанной карты на морфологическое изображение.

его соли и его хелатные комплексы с парамагнитными металлическими ионами.
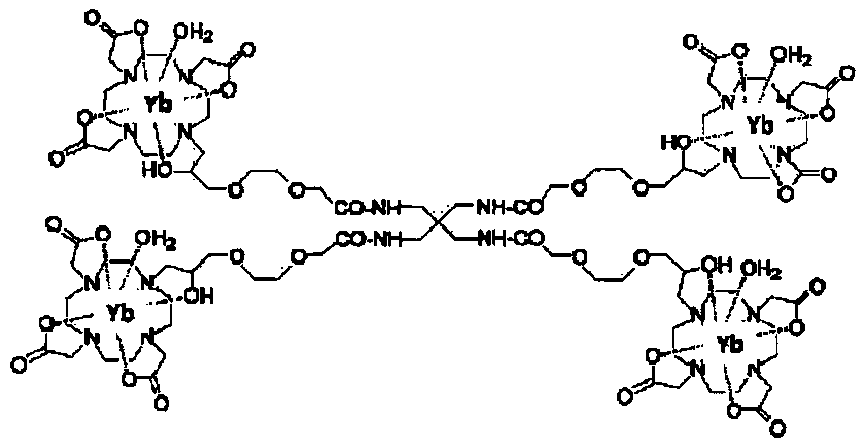
в качестве источника магнитно неэквивалентных мобильных протонов в логометрическом способе визуализации с применением CEST, вместе с подходящими физиологически приемлемыми добавками и/или носителями.

Комментарии