Материал, включающий полиазациклоалканы, привитые на полипропиленовое волокно, способ его получения и способ удаления катионов металлов из жидкости - RU2470951C2
Код документа: RU2470951C2
Чертежи






Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к материалу, включающему, предпочтительно, состоящему из полиазациклоалканов, привитых на пропиленовое волокно. Изобретение дополнительно относится к способу получения такого материала.
Наконец, изобретение относится к способу удаления катионов металлов из жидкости, конкретно из водной жидкости, путем приведения упомянутой жидкости в контакт с упомянутым материалом.
Упомянутые катионы металлов могут быть катионами тяжелых металлов, например меди, цинка, кадмия, тантала или золота, но более конкретно они являются катионами радиоактивных элементов семейства актинидов или лантанидов и настоящее изобретение таким образом относится более конкретно к полному обеззараживанию водных отходов, загрязненных источниками альфа-излучения.
Область техники, к которой относится настоящее изобретение, в общем можно определить как материалы, применяемые для тонкой (высокой) очистки жидкостей и более конкретно для адсорбционной экстракции (извлечения) загрязняющих металлов, растворенных в жидких отходах.
Уровень техники
Применение материалов, полученных по способу прививки полиазамакроциклических лигандов и конкретно тетераазамакроциклических лигандов на подложку, для проведения адсорбционной экстракции известно при применении с целью достижения исчерпывающей полной очистки сточных вод. Избирательность таких комплексообразующих молекул в отношении переходных металлов, постпереходных металлов, лантанидов и актинидов на фоне щелочных и щелочноземельных металлов, присутствующих в преобладающем количестве, делает их очень хорошими кандидатами для извлечения этих элементов, присутствующих в следовых количествах. Так, прививка полиазамакроциклов и, в частности, тетраазамакроциклических молекул на подложку из силикагеля и органических смол типа смол Меррифилда уже описана.
Прививка на подложку из силикагеля (кремнезема)
Прививка макроциклических лигандов на силикагель (в основном краун-эфиров и каликсаренов, а также полиазаоксамакроциклов и нескольких полиазамакроциклов (J.S.Bradshaw, K.E.Krakowiak, B.J.Tarbet, R.L.Bmening, L.D.Griffin, D.E.Cash, T.D.Rasmussen, R.M.Izatta, Solvent Extraction Ion Exchange, 1989, 7, 855-864) уже разрабатывается и способы адсорбционной экстракции для лабораторно-аналитического применения (анализ на присутствие свинца (R.M.Izatt, Journal of Inclusion Phenomena and Molecular Recognition in Chemistry, 1997, 29, 197-220)), промышленного применения (извлечение ценных металлов, например платины (R.M.Izatt, Journal of Inclusion Phenomena and Molecular Recognition in Chemistry, 1997, 29, 197-220)) или применения, относящегося к борьбе с загрязнениями окружающей среды (обеззараживание водных отходов ядерной промышленности: удаление стронция (R.M.Izatt, Journal of Inclusion Phenomena and Molecular Recognition in Chemistry, 1997, 29, 197-220), или плутония и америция (US 6,232,265 B1 (11/06/1999)), уже имеются на рынке.
Различные функционализированные полиазациклоалканы привиты на неорганические подложки (FR 99/01499 (09/02/1999); WO 01/46202 (12/12/2000); WO 96/11056 (04/10/1995); WO 96/11478 (04/10/1995); WO 01/15806 (25/08/2000)).
Вышеописанные исследования сделали возможным утвердить применение этой техники для полной очистки в полупромышленном масштабе. Осуществлена заключительная обработка 50 м3 радиоактивных жидких отходов с помощью материалов, состоящих из тетраазамакроциклического лиганда, привитого на силикагель (WO 01/15806 (25/08/2000)).
Вышеописанные материалы таким образом рассматриваются в нижеприведенных примерах как контрольный материал для сравнения с экстрактивными характеристиками материалов согласно изобретению.
Однако у таких хелатирующих материалов на основе силикагеля имеются недостатки, относящиеся скорее к их механическим свойствам при применении в промышленности, чем к их экстрактивным характеристикам. Подложка из силикагеля обусловливает следующие недостатки:
- ограничение формы выпуска материала порошкообразной формой, что фактически сводит его применение к колоночному способу;
- значительная потеря напора при колоночном процессе, что приводит к пониженной скорости тока при обработке (50 л/час);
- длительное кондиционирование материала, включающее множественные операции, например удаление пузырьков воздуха (обезгаживание), упаковка силикагеля и т.п.;
- износ силикагеля из-за трения, приводящий к закупориванию.
Прививка на органические смолы
1,4,8,11-тетраазациклотетрадекан (циклам) прививают на полистироловые смолы (D.Woehrle, V.Nicolaus, Polymer Bulletin, 1986, 15, 185-192) для извлечения, преимущественно, из водных растворов меди, кобальта, цинка (V.Louvet, P.Appriou, Н.Handel, Tetrahedron Letters, 1982, 23, 2445-2448; W.Szczepaniak, K.Kuczynski, Reactive Polymers, 1985, 3, 101-106) или золота (С.Kavakli, N.Ozvatan, S.A.Tuncel, B.Salih, Analytica Chimica Acta, 2002,464, 313-322).
Такие же экстрактивные свойства наблюдаются у хелатирующих смол, полученных путем радикальной полимеризации N-(4-винилбензил)циклама (ЕР 0287436 (07/04/1988); S.Amigoni-Gerbier, С.Larpent, Macromolecules, 1999, 32, 9071-9073; В.Altava, M.I.Burguete, J.С.Frias, E.Garcia-Espana, S.V.Luis, J.F.Miravet, Industrial & Engineering Chemistry Research, 2000, 39, 3589-3595). Экстрактивные свойства функционализированных тетраазамакроциклов, привитых на смолы Меррифилда, в отношении радиоактивных элементов также исследованы (WO 96/11056 (04/10/1995)).
Материалы, полученные на основе смол Меррифилда, проявляют худшие экстрактивные характеристики, что относят к гидрофобности и сильной поперечной сшитости подложки (WO 96/11056 (04/10/1995)), приводящим к замедленным кинетикам комплексообразования.
Два единственных известных носителя, к которым привиты полиазамакроциклические и, в частности, тетраазомакроциклические молекулы, являются таким образом силикагелем и органическими смолами. Ни одна из этих подложек не проявляет все необходимые свойства как в плане эффективности удаления загрязнений, так и в плане поведения в ходе относящегося к ним процесса, промышленного применения в адсорбционной экстракции.
Дополнительно, органические волокна, с другой стороны, проявляют определенные преимущества в качестве носителя (подложки) для лигандов, такие как разнообразие возможных форм материала, простая интеграция в процесс адсорбционной экстракции и возможность сжигания материала по окончании срока службы.
Применение привитых органических волокон для обработки воды описано для многих случаев, но применение такой подложкой практически неизвестно для присоединения полиазотсодержащих, например тетраазотсодержащих макроциклических лигандов. Afortiori - прививка таких макроциклов на полипропиленовое волокно никогда не упоминалась и не предлагалась в данной области техники до сих пор.
Уровень техники таким образом относится к получению хелатирующего волокна или мембран для применения при очистке водных растворов, загрязненных тяжелыми металлами или радиоактивными элементами. Например, для извлечения уранила, присутствующего в морской воде, получены «реактивные фильтры» путем введения функциональных групп амидоксимана в полиэтиленовое (S.-H. Choi, Y.С.Nho, Journal of Macromolecular Science, Pure and Applied Chemistry, 2000, A37, 1053-1068), полипропиленовое (N.Kabay, A.Katakai, T.Sugo, H.Egawa, Journal of Applied Polymer Science, 1993,49, 599-607) или целлюлозное волокно (А.М. Dessouki, M.El-Tahawy, H.El-Boohy, S.A.El-Mongy, S.M.Badawy, Radiation. Physics and Chemistry, 1999, 54, 627-635). Последний материал также получен для связывания Cr(III) и Cu(II) (R.Saliba, H.Gauthier, R.Gauthier, M.Petit-Ramel, Journal of Applied Polymer Science, 2000, 75, 1624-1631).
Подобным образом получают многочисленные материалы с волокнистой текстурой с целью полного удаления группы тяжелых металлов, эти материалы в основном получают путем модификации подложки путем введения большого количества координационных функциональных групп. Так, функциональные группы поликарбоновых кислот (H.J.Fischer, K.H.Lieser, Angewandte Makromolekulare Chemie, 1993, 208. 133-150), поликарбоксиаминов (WO 00/04931 (20/07/1998), аминов (JP 01/123381) и амидов (N.Bicak, D.С.Sherrmgton, В.F.Senkal, Reactive & Functional Polymers, 1999, 41, 69-76) прививают на целлюлозу, амидные (X.Chang, Y.Li, G.Zhan, X.Luo, W.Gao, Talanta, 1996, 43, 407-413), имидазольные (В.Gong, Talanta, 2002, 57, 89-95) и гидразиновые (Х.Chang, Q.Su, D.Liang, X.Wei, B.Wang, Talanta, 2002, 57, 253-261) функциональные группы прививают на полиакрилонитрил и иминодиуксусные (S.-H.Choi, Y.С.Nho, Journal of Applied Polymer Science, 1999, 71., 999-1006) функциональные группы прививают на полиэтилен.
С другой стороны, прививка на органическое волокно молекул (в частности, макроциклических молекул), выбранных для специфических применений с целью экстракции, является значительно более редкой. Присоединение линейного лиганда ЭГТА к целлюлозе предоставляет более высокую избирательность для извлечения кадмия по сравнению с таковой для цинка (US 6,479,159 B1 (19/04/2001)). α-Циклодекстрин, β-циклодекстрин и γ-циклодекстрин присоединяют к полипропиленовому волокну с целью извлечения органических молекул в макроциклической полости (Р.Le Thuaut, В.Martel, G.Crini, U.Maschke, X.Coqueret, M.Morcellet, Journal of Applied Polymer Science, 2000, 77, 2118-2125; В.Martel, P. Le Thuaut, G.Crini, M.Morcellet, A.-M.Naggi, U.Maschke, S.Bertini, C.Vecchi, X.Coqueret, G.Torn, Journal of Applied Polymer Science, 2000, 78, 2166-2173). Краситель Cibacron Blue F3GA, проявляющий сродство к различным тяжелым металлам и значительную избирательность по отношению к кадмию, иммобилизуют на полом полипропиленовом волокне путем адсорбции (Е.Buyuktuncel, S.Bektas, О.Gene, A.Denizli, Reactive & Functional Polymers, 2001, 47, 1-10). Описано применение в гетерогенном катализе путем прививки фталоцианина на полипропиленовое волокно (D.L.Cho, С.N.Choi, H.J.Kirn, А.K.Kirn, J.-H.Go, Journal of Applied Polymer Science, 2001, 82, 839-846) или прививки таддола на полиэтиленовое волокно (S.Degni, C.-E.Wilen, R.Leino, Organic Letters, 2001, 3, 2551-2554).
Таким образом, в свете вышеописанного ясно, что имеется потребность в материале, который сохраняя превосходную избирательность связывания, характерную для полиазамакроциклических, в частности тетраазамакроциклических молекул в отношении тяжелых металлов, лантанидов или актинидов, прост в промышленном применении, не проявляет вышеупомянутых недостатков материалов, включающих полиазамакроциклы, например полиазациклоалкана, привитого на силикагель, в плане ограничения формовки, большой потери напора, продолжительного кондиционирования и адгезии и не проявляет также недостатков в плане плохих экстрактивных свойств, присущих материалам, в которых полиазамакроциклы иммобилизованы на подложке, сделанной из органической смолы, например смолы Меррифилда.
Иными словами, имеется потребность в материале, который проявляя превосходные экстрактивные свойства, свойственные материалу, состоящему из полиазациклоалканового лиганда, привитого на силикагель, не обладает всеми его недостатками при применении, в частности в промышленности.
Раскрытие изобретения
Целью настоящего изобретения является предоставление материала, включающего полиазамакроциклы, который удовлетворяет inter alia вышеперечисленным требованиям.
Целью настоящего изобретения является также предоставление материала, включающего полиазамакроциклы, в основном предназначенного для удаления ионов металлов из жидкостей, который не обладает недостатками, дефектами, ограничениями и отрицательными чертами материалов, известных в данной области техники, например материалов, включающих полиазамакроциклы, привитые на силикагель или на смолы Меррифилда.
Целью настоящего изобретения является также предоставление такого материала, который решает проблемы материалов, известных в данной области техники.
Эта цель и дополнительно другие цели достигнуты согласно изобретению с помощью материала, включающего, преимущественно состоящего из полиазациклоалкана, привитого на полипропиленовое волокно.
Следует заметить, что в настоящем тексте термин «привитый» означает прививку путем ковалентной химической связи в противоположность физическому или электростатическому связыванию, например адсорбции.
Прививка полиазотсодержащих макроциклических лигандов, например полиазациклоалканов на органическое волокно и более того на полипропиленовое волокно, никогда не упоминалась и не предлагалась в данной области техники до сих пор.
Можно сказать, что изобретение основано на получении новых материалов, образуемых путем прививки полиазамакроциклических, например тетраазамакроциклических молекул на подложку на базе полипропиленового волокна. Полиазотсодержащие, в частности тетраазотсодержащие макроциклические лиганды являются высокоизбирательными для извлечения тяжелых металлов, лантанидов и актинидов, а полипропиленовое волокно, где пропилен является органическим и в этой связи сжигаемым (горючим) материалом, проявляет значительное разнообразие возможных применений, что делает простым включение его в процесс и дает определенные преимущества при промышленном применении. Экстрактивные свойства этих новых материалов являются высокоудовлетворительными по отношению к тяжелым металлам, например кадмию и радиоактивным элементам, например урану и плутонию. Введение этих материалов в процесс делает возможным их применение при обработке жидких промышленных отходов.
Материалы согласно изобретению неожиданно проявляют все преимущества материалов из полиазациклоалканов, привитых на подложку типа силикагеля, и все преимущества материалов из полиазациклоалканов, привитых на подложку типа органической смолы, но без всех недостатков этих двух типов материалов.
Материал согласно изобретению решает проблемы, присущие материалам, известным в данной области техники до сих пор.
Согласно первому осуществлению материал согласно изобретению можно получать путем радикальной полимеризации полиазациклоалканового мономера, несущего группу, которую можно полимеризовать в условиях образования радикалов (радикальная полимеризация) в присутствии полипропиленового волокна, несущего пероксидные и/или гидропероксидные функциональные группы, при необходимости с последующей функционализацией при необходимости свободных функциональных аминогрупп полиазациклоалкана и/или омылением, гидролизом функциональных групп сложного эфира, при необходимости присутствующих на полиазациклоалкане.
Упомянутый мономер полиазациклоалкана соответствует одной из следующих трех формул:



где n, m, p, q и r, которые могут быть идентичными или разными, равны 2 или 3;
R1 является группой, которая может вступать в реакцию полимеризации в условиях радикальной полимеризации; R2 представляет атом водорода или группу (CH2)2R3; R3 является группой, выбранной из группы, состоящей из CONH2, СН2ОН, CN и COOR4, R4 представляет Н, катион, например Na, алкильную группу, включающую от 1 до 10 атомов углерода, или бензильную группу; или R2 представляет группу -(CH2)-R5, где R5 представляет COOR6, или PO3R6, R6 представляет алкильную группу, включающую от 1 до 10 атомов углерода, атом водорода или катион, например Na.
Группу, которая может вступать в реакцию полимеризации в условиях радикальной полимеризации, предпочтительно выбирают из групп, включающих винил, стирол или акрил.
Так, группу, которая может вступать в реакцию полимеризации в условиях радикальной полимеризации, можно выбирать из групп акрилонитрила, акрилата, акриловой кислоты, винилпиридина, винилалкоксисилана и 4-винилбензила.
Предпочтительные полиазациклоалкановые мономеры выбирают из N-(4-винилбензил)циклама и N,N',N”-трис(2-этоксикарбонилэтил)-N'''-(4-винилбензил)циклама.
Материал согласно изобретению в первом осуществлении может соответствовать следующей формуле:

где - R2 имеет значение, приведенное выше;
- n1 является целым числом от 100 до 3000;
- p1 является целым числом от 10 до 1000;
R2 предпочтительно представляет Н или CH2CH2COOEt, или СН2СН2СООН, или CH2CH2COONa, или CH2COOEt, или СН2СООН, или CH2COONa.
Материал формулы (IV) получают из мономера полиазациклоалкана формулы (II). Специалист в данной области техники легко определит формулу, которой могут соответствовать материалы, полученные из мономеров полиазациклоалкана формулы (I) или (III).
Согласно второму осуществлению материал согласно изобретению можно получать с помощью следующих последовательных этапов:
а) радикальную полимеризацию одного или более мономеров, которые можно полимеризовать в условиях радикальной полимеризации, проводят в присутствии полипропиленовых волокон, несущих пероксидные и/или гидропероксидные функциональные группы, где, по меньшей мере, один из упомянутых мономеров включает, по меньшей мере, одну функциональную группу, способную реагировать со свободной функциональной аминогруппой полиазациклоалкана (это обычно относится к функциональным аминогруппам кольца, образующим целостную часть кольца полиазациклоалкана; азот аминогруппы образует часть кольца полиазациклоалкана; эти функциональные группы обычно рассматриваются как функциональные группы вторичного амина), в результате чего получается полимер, включающий упомянутые функциональные группы, способные реагировать со свободными функциональными аминогруппами полиазациклоалкана, привитый на полипропилен;
б) упомянутый полимер реагирует с полиазациклоалканом;
в) при необходимости свободную функциональную аминогруппу или аминогруппы полиазациклоалкана, при необходимости еще присутствующую, подвергают функционализации;
г) при необходимости сложноэфирные функциональные группы, при необходимости имеющиеся у полиазациклоалкана, омыляют, гидролизуют.
Функциональную группу, способную реагировать с функциональной аминогруппой полиазациклоалкана, можно выбирать из электрофильных атомов углерода, например атомов углерода, несущих галоид, функциональных групп OTs (тозилат) или OTf (трифлат) и т.п., или производных карбоновой кислоты, например ацилгалоидов, ангидридов, сложных эфиров и т.п.
Мономеры для полимеризации можно выбирать из мономеров винила, стирола или акрила и т.п. Примерами таких мономеров являются хлорметилстирол и малеиновый ангидрид.
Можно полимеризовать один вид мономера, в случае чего после завершения первого этапа получают гомополимер упомянутого мономера, например гомополимер хлорметилстирола, привитый на полипропиленовое волокно.
Альтернативно, на первом этапе можно полимеризовать смесь разных мономеров, в случае чего после завершения первого этапа получается сополимер, например чередующийся сополимер хлорметилстирола и малеинового ангидрида: поли(малеиновый ангидрид-alt-хлорметилстирол).
Полиазациклоалкан, применяемый на этапе б) по второму осуществлению, можно выбирать из полиазациклоалканов, включающих одну из трех следующих формул (V), (VI) и (VII):
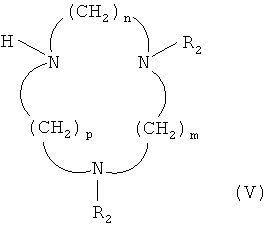


где n, m, p, q и r, которые могут быть одинаковыми или разными, равны 2 или 3; R2 представляет атом водорода или (СН2)2-R3 группу, R3 является группой, выбранной из группы, состоящей из CONH2, CH2OH, CN и COOR4, R4 представляет Н, катион, например Na, алкильную группу, включающую от 1 до 10 атомов углерода, или бензильную группу; или R2 представляет -(CH2)-R5 группу, где R5 представляет COOR6 или PO3R6, R6 представляет алкильную группу, включающую от 1 до 10 атомов углерода, атом водорода или катион, например Na.
Этот полиазациклоалкан предпочтительно выбирают из следующих соединений:




1,4,8-трис(2-карбоксиэтил)-1,4,8,11-тетраазациклотетрадекан (ТЕ3Р)
1,4,8-трис(этоксикарбонилэтил)-1,4,8,11-тетраазациклотетрадекан (ТЕ3РЕ)
1,4,8-трис(этоксикарбонилметил)-1,4,8,11-тетраазациклотетрадекан (ТЕ3АЕ)
Материал согласно второму осуществлению настоящего изобретения может соответствовать следующей формуле (VIII) или следующей формуле (IX):

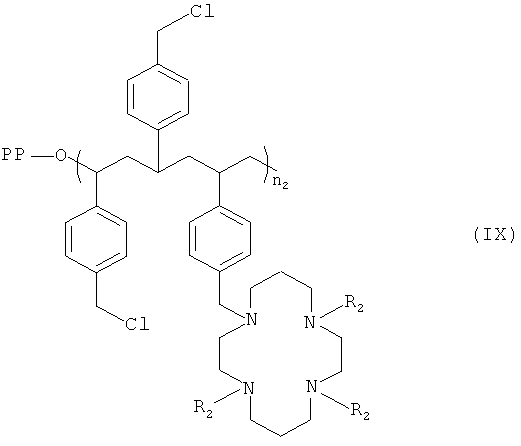
где - R2 имеет вышеприведенное значение;
- m2 является целым числом от 10 до 1000;
- n2 является целым числом от 10 до 1000;
- p2 является целым числом от 10 до 1000.
В формулах (VIII) и (IX) R2 предпочтительно представляет -(CH2)2COONa, -CH2COOEt, -(CH2)2-COOEt, -(СН2)2-СООН, -СН2-СООН или -CH2-COONa.
Материал формулы (VIII) или (IX) получают из полиазациклоалкана формулы (VI). Специалист в данной области техники легко определит формулы, которым соответствуют материалы, полученные из полиазациклоалканов формулы (V) или (VII).
В первом и втором осуществлениях материала и способа функционализация относится к материалам, в которых полиазациклоалкан (который уже зафиксирован или иммобилизован на полипропиленовых волокнах) включает свободные функциональные аминогруппы (функциональные группы вторичного амина в кольце полиазациклоалкана) и необходимо предоставить его с хелатирующими, комплексообразующими или координационными функциональными группами, например карбоксильной или карбоксилатной функциональными группами в виде ветвей, включающих карбоксил или карбоксилат на конце.
При необходимости такую функционализацию свободных функциональных аминогрупп полиазациклоалкана можно проводить путем реагирования упомянутой свободной функциональной аминогрупп или групп с соединениями, включающими функциональную группу, способную реагировать со свободной функциональной аминогруппой полиазациклоалкана, и другую функциональную группу, например функциональную группу, выбранную из R3 и R5 групп, как определено выше, которые обычно являются хелатирующими или координационными функциональными группами.
Это соединение можно, в частности, выбирать из этилбромацетата и этилакрилата.
Когда полиазациклоалкан (привитый или иммобилизованный на полиэтиленовом волокне) включает сложноэфирные функциональные группы, предпочтительно проводить гидролиз, омыление этих сложноэфирных функциональных групп с целью получения карбоксильных и/или карбоксилатных функциональных групп, например функциональных групп -COONa, проявляющих лучшие хелатирующие, комплексообразующие или координирующие свойства, чем сложноэфирные функциональные группы.
Такой гидролиз/омыление можно проводить в присутствии гидроксида натрия в водно-спиртовой среде.
Такой гидролиз/омыление одновременно приводит к остаточным концевым группам, несущим хлор, например остаточным хлорметильным функциональным группам в случае, относящемся к материалу по второму осуществлению, и когда полимер, полученный после завершения первого этапа а) и являющийся гомополимером хлорметилстирола или чередующимся сополимером хлорметилстирола и малеинового ангидрида, привитым на полипропиленовое волокно, сильно гидролизован, например приблизительно на 75%.
Предпочтительно, омыление, гидролиз функциональных групп сложного эфира проводят в условиях, обеспечивающих полный гидролиз функциональных групп сложного эфира.
Условия являются, например, следующими: реакция при 40°С в течение 18 час в присутствии 0,5 н. раствора гидроксида натрия. Такие условия позволяют провести полный гидролиз сложноэфирных функциональных групп, тогда как в отношении амидных функциональных групп наблюдается лишь частичный гидролиз.
Тот факт, что гидролиз/омыление практически всех сложноэфирных функциональных групп одновременно приводит к гидроксилированию большой части (например, 75%) остаточных концевых групп, несущих хлор, таким образом значительно повышает гидрофильность и смачиваемость привитого волокна.
Собственная гидрофобность полипропиленового волокна таким образом уравновешивается введением значительного количества гидрофильных функциональных групп, а именно концевых гидроксильных и карбоксилатных функциональных групп лиганда.
Полипропиленовое волокно, в частности, можно предоставлять в виде нетканого материала.
Полипропиленовое волокно, несущее пероксидные и/или гидропероксидные функциональные группы, получают, например, путем облучения полипропиленового волокна электронами в окислительной атмосфере, например, воздуха или кислорода.
Изобретение дополнительно относится к способу получения материалов, описанных выше.
По первому осуществлению этого способа, в котором получают материал согласно первому осуществлению материала, описанному выше, радикальную полимеризацию мономера полиазациклоалкана, несущего группу, которую можно полимеризовать в условиях радикальной полимеризации, проводят в присутствии полипропиленового волокна, несущего пероксидные и/или гидропероксидные функциональные группы, при необходимости с последующей функционализацией при необходимости свободных функциональных аминогрупп полиазациклоалкана и/или омыления, гидролиза сложноэфирных функциональных групп, при необходимости присутствующих у полиазациклоалкана.
Мономер полиазациклоалкана, несущий группы, способные к полимеризации, применяемый по этому способу, обычно соответствует одной из трех формул (I), (II) и (III):



где n, m, p, q и r, которые могут быть одинаковыми или разными, равны 2 или 3; R1 является группой, которую можно полимеризовать в условиях радикальной полимеризации; R2 представляет атом водорода или (СН2)2-R3 группу, R3 является группой, выбранной из группы, состоящей из CONH2, CH2OH, CN или COOR4, R4 представляет Н, катион, например Na, алкильную группу, включающую от 1 до 10 атомов углерода, или бензильную группу; или R2 представляет -(CH2)-R5 группу, где R5 представляет COOR6 или PO3R6, R6 представляет алкильную группу, включающую от 1 до 10 атомов углерода, атом водорода или катион, например Na.
Упомянутую группу мономера полиазациклоалкана, которую можно полимеризовать в условиях радикальной полимеризации, обычно выбирают из групп, включающих винил, акрил или стирол, в частности эту группу можно выбирать из акрилонитрила, акрилата, акриловой кислоты, винилпиридина, винилалкоксисилана и 4-винилбензола.
Предпочтительный мономер полиазациклоалкана можно выбирать из N-(4-винилбензил)циклама и N,N”,N'''-трис(2-этоксикарбонилэтил)-N”-(4-винилбензил)циклама.
Обычно полимеризацию проводят при температуре от 80°С до 120°С, например при 105°С, в растворителе, выбранном из ДМФА (диметилформамида), толуола, ацетонитрила и в течение периода времени от 2 до 24 час, например в течение 13 час.
По второму осуществлению способа согласно изобретению, в котором получают материал согласно второму осуществлению материала, описанному выше, осуществляют способ получения материала, состоящего из полиазациклоалкана, привитого на полипропиленовое волокно, причем упомянутый способ включает следующие последовательные этапы:
а) радикальную полимеризацию одного или более мономеров, которые можно полимеризовать в условиях радикальной полимеризации, проводят в присутствии полипропиленового волокна, несущего пероксидные и/или гидропероксидные функциональные группы, где, по меньшей мере, один из упомянутых мономеров включает, по меньшей мере, одну функциональную группу, способную реагировать со свободной функциональной аминогруппой полиазациклоалкана, в результате чего получают полимер, включающий упомянутые функциональные группы, способные реагировать со свободными функциональными аминогруппами полиазациклоалкана, где упомянутый полимер привит на полипропилен;
б) упомянутый полимер реагирует с полиазациклоалканом;
в) при необходимости свободную функциональную аминогруппу полиазациклоалкана, при необходимости еще присутствующую, подвергают функционализации;
г) при необходимости сложноэфирные функциональные группы, при необходимости имеющиеся у полиазациклоалкана, омыляют, гидролизуют.
Упомянутая свободная функциональная аминогруппа обычно является функциональной группой вторичного амина -(NH)-, образующей целостную часть кольца полиазациклоалкана.
Когда имеют в виду свободную аминогруппу полиазациклоалкана, это обычно относится к свободным аминам кольца полиазациклоалкана, обычно рассматриваемым как вторичные амины.
Функциональную группу, способную реагировать со свободной функциональной амигруппой полиазациклоалкана, обычно выбирают из электрофильных атомов углерода, несущих галоид, функциональные группы OTs или OTf и т.п., или производные карбоновой кислоты, например ацилгалиды, ангидриды, сложные эфиры и т.п.
Упомянутые мономеры для полимеризации таким образом предпочтительно выбирают из винила, стирола или акрила и т.п.
Примерами таких мономеров являются хлорметилстирол и малеиновый ангидрид.
Можно проводить радикальную полимеризацию только одного вида мономера (гомополимеризация), например хлорметилстирола, посредством чего получают гомополимер, привитый обычно на поверхность полипропиленового волокна.
Когда проводят полимеризацию только хлорметилстирола, такую полимеризацию обычно проводят в растворителе, выбранном из диметилформамида (ДМФА), толуола, воды или смеси метанол/вода при температуре от 80°С до 120°С при массовой концентрации хлорметилстирола в растворителе от 30 до 55% и в течение времени от 2 до 20 час.
Предпочтительно, полимеризацию хлорметилстирола проводят в чистом ДМФА при температуре от 80°С до 115°С, предпочтительно при 115°С при массовой концентрации хлорметилстирола в ДМФА, составляющей 40%, в течение 10 час.
Альтернативно, можно на этапе а) проводить полимеризацию нескольких типов мономеров (сополимеризацию). Например, можно проводить сополимеризацию малеинового ангидрида и хлорметилстирола, обычно на поверхности полипропилена. В этом случае полимеризацию проводят в растворителе, выбранном из толуола и ацетона, при температуре от 75°С до 95°С при массовой концентрации мономера в растворителе от 10% до 80%, например при 30%, и в течение времени от 4 до 30 час.
На этапе б) полиазациклоалкан можно выбирать из полиазациклоалканов, соответствующих одной из трех следующих формул (V), (VI) и (VII):



где n, m, p, q и r, которые могут быть одинаковыми или разными, равны 2 или 3; R2 представляет атом водорода или (СН2)2-R3 группу, R3 является группой, выбранной из группы, состоящей из CONH2, CH2OH, CN и COOR4, R4 представляет Н, катион, например Na, алкильную группу, включающую от 1 до 10 атомов углерода, или бензильную группу; или R2 представляет -(CH2)-R5 группу, R5 представляет COOR6 или PO3R6, R6 представляет алкильную группу, включающую от 1 до 10 атомов углерода, атом водорода или катион, например Na.
Предпочтительно, упомянутый полиазациклоалкан выбирают из следующих соединений:




1,4,8-трис(2-карбоксиэтил)-1,4,8,11-тетраазациклотетрадекан (ТЕ3Р)
1,4,8-трис(этоксикарбонилэтил)-1,4,8,11-тетраазациклотетрадекан(ТЕ3РЕ)
1,4,8-трис(этоксикарбонилметил)-1,4,8,11-тетраазациклотетрадекан (ТЕ3АЕ)
Проведение функционализации и гидролиза/омыления уже описано выше. Независимо от применяемого способа полипропиленовое волокно можно предоставлять в виде нетканого материала.
Функциональные группы пероксида и/или гидропероксида можно получать путем облучения полипропиленового волокна электронами в окислительной атмосфере, например, воздуха или кислорода.
Обычно полипропиленовое волокно облучают дозой от 20 до 60 кГр, предпочтительно, 40 кГр.
Изобретение дополнительно относится к способу удаления катионов металла, присутствующих (содержащихся) в жидкости, при котором упомянутую жидкость приводят в контакт с материалом согласно изобретению, как описано выше.
Приведение в контакт обычно проводят при температуре от 20°С до 60°С, например при 50°С.
Этот процесс преимущественно проводят непрерывно, материал согласно изобретению помещают в колонку, через которую проходит поток обрабатываемой жидкости.
Способ предпочтительно дополнительно включает этап регенерации материала, когда последний насыщается адсорбируемыми металлами.
Упомянутые катионы металлов обычно выбирают из переходных металлов, тяжелых металлов, металлов группы III A Периодической системы, лантанидов, актинидов и щелочноземельных металлов, в частности из катионов U, Pu, Am, Ce, Eu, Al, Gd, Cr, Mn, Fe, Co, Ni, Cu, Zn, Ag, Cd, B, Au, Hg, Pb, As, Ca, Sr, Mg, Be, Ba и Ra.
Обрабатываемая жидкость, в частности, является водной жидкостью, например радиоактивными сточными водами с низкой активностью.
Такие жидкие отходы являются, например, сточными водами с низкой активностью, образующимися в промышленном испарителе станции по обработке сточных вод ядерных установок.
Как указано выше, одним из непосредственных применений материала согласно изобретению, а именно макроциклических, в частности содержащих четыре атома азота лигандов, привитых на полипропиленовое волокно согласно изобретению, является их применение в адсорбционной экстракции с целью обработки (очистки) сточных вод, загрязненных тяжелыми металлами или радиоактивными элементами.
Свойства материалов согласно изобретению позволяют им включаться в процесс обработки, отвечающий потребностям промышленности и не ограниченный лабораторным применением.
Комитетом по атомной энергии (Commissariat á 1'Energie Atomique, (CEA)) в центре Валдюк признана потребность в применении новых материалов согласно изобретению в процессе, который будет включен в работу станцию по очистке жидких сточных вод этого центра.
CEA в Валдюк отмечает очень низкие нормы выброса для радиоактивных или нерадиоактивных жидких отходов, например общая активность радиоактивных сточных вод должна быть ниже 5 Бк/м3 или действующая норма выброса кадмия в нерадиоактивных сточных водах составляет 5 ppb. Эти нормы ставят технику обработки воды на уровень тонкой очистки. Сточные воды с низкой активностью, производимые этим центром, в настоящее время обрабатывают путем выпаривания при пониженном давлении в промышленном испарителе и затем полностью обеззараживают с помощью установки для микрофильтрации. Последняя технология отделяет только те твердые частицы, которые достаточно велики, и не позволяет обрабатывать получающиеся в отдельных случаях сточные воды, в которых радиоактивные элементы присутствуют в растворенном виде. В таких исключительных случаях сточные воды повторно вводят в контур обработки.
Способ адсорбционной экстракции с применением избирательных комплексообразующих материалов согласно изобретению особенно подходит для обработки таких сточных вод, в которых загрязняющие элементы находятся в растворенном виде. Эта техника дополняет способы, применяемые в настоящее время в центре Валдюк. Эта техника может действительно практически полностью вытеснить выпаривание, являющееся сравнительно громоздким в применении техникой и потребляющее много энергии.
Возможность сжигать материал согласно изобретению по окончании его времени жизни также вносит ценный вклад в стратегию снижения отходов в ядерной промышленности.
Что касается выброса кадмия и в более общей форме выброса тяжелых металлов, в случае очистки нерадиоактивных сточных вод, включающих такие металлы, особенно при случайном загрязнении, введение в технологию нового материала согласно изобретению является средством на случай загрязнения, например, водохранилища местного стока жидких отходов, и таким образом привносит новое непосредственное применение для таких материалов.
В общем, возможным приложением материалов согласно изобретению является их применение в очистке жидких промышленных отходов, загрязненных тяжелыми металлами, лантанидами или актинидами. Избирательность по отношению к соответствующим металлам обеспечивается путем подбора функционализации макроциклических лигандов, например лигандов, содержащих четыре атома азота.
Лучшее понимание изобретения будет достигнуто по прочтении последующего детального описания и приложенных фигур.
Краткое описание чертежей
Фигура 1 представляет график, показывающий действие дозы облучения на прививку полихлорметилстирола на полипропиленовое волокно.
По оси ординат показано содержание хлора (ммоль/г), по оси абсцисс показана доза облучения (кГр).
Верхняя кривая (серия №1) относится к чистому хлорметилстиролу при времени реакции 16 час и температуре 115°С, нижняя кривая (серия №2) относится к 50% хлорметилстиролу в воде при времени реакции 6 час и температуре 100°С.
Фигура 2 представляет график, который показывает действие температуры на прививку полихлорметилстирола на (к) полипропиленовое волокно.
По оси ординат показано содержание хлора (ммоль/г), по оси абсцисс показана температура (°С).
Верхняя кривая (серия №1) относится к способу, который проводят с полипропиленовым волокном, облученным при 40 кГр и при времени реакции 16 час с чистым хлорметилстиролом, нижняя кривая (серия №2) относится к способу, который проводят с полипропиленовым волокном, облученным при 20 кГр и при времени реакции 15 час 30 мин с 40% хлорметилстиролом в ДМФА; вертикальная пунктирная линия указывает начало разложения волокна.
Фигура 3 представляет график, который показывает влияние массовой концентрации (%) хлорметилстирола в растворе ДМФА на прививку полихлорметилстирола на полипропиленовое волокно.
По оси ординат показано содержание хлора (ммоль/г), по оси абсцисс показана концентрация хлорметилстирола в массовых процентах в растворе ДМФА.
Верхняя кривая относится к волокну, облученному при 40 кГр (серия №1) при времени реакции 4 часа и температуре реакции 115°С.
Нижняя кривая также относится к волокну, облученному при 40 кГр (серия №2) при времени реакции 4 часа и температуре реакции 115°С.
Фигура 4 представляет график, который показывает влияние времени реакции на прививку полихлорметилстирола на полипропиленовое волокно.
По оси ординат показано содержание хлора (ммоль/г), по оси абсцисс показано время или продолжительность реакции (час).
Представленная кривая относится к прививке на полипропиленовое волокно, облученное при 40 кГр (серия №1) и при концентрации 50% хлорметилстирола в растворе ДМФА при температуре 115°С.
Фигура 5 представляет увеличенный вид спектра1H ЯМР (500 MHz, (CD3)CO) комплекса с переносом заряда на основе малеинового ангидрида и хлорметилстирола, образованного из эквимолярной смеси двух мономеров, выдержанного с обратным холодильником в присутствии дейтерированного ацетона в течение 1 часа.
Фигура 6 представляет схематическое изображение вида сбоку на разрез экспериментальной установки, применяемой для тестирования адсорбционной экстракции в равновесных условиях с помощью материала согласно изобретению и контрольного материала.
Осуществление изобретения
Настоящее изобретение описывает прививку полиазамакроциклических, в частности тетраазамакроциклических лигандов на полипропиленовое волокно.
Одной из конкретных проблем, возникающих при применении такой подложки, является ее гидрофобность. Это свойство может уменьшить смачиваемость подложки и таким образом уменьшать доступность металлов, растворенных в жидкости, для образования комплекса с тетраазамакроциклическими молекулами, привитыми на подложку. Способ прививки согласно изобретению делает возможным, в частности, бороться с гидрофобностью материала путем введения достаточного количества гидрофильных функциональных групп. Последние сконцентрированы близко к участкам комплексообразования. Способ прививки, разработанный согласно изобретению, также делает возможным контролировать количество макроциклических молекул, присоединенных к поверхности материала, что позволяет менять количество участков связывания загрязнений, таких как катионы металлов, в соответствии с применением, для которого материал предназначен.
Примеры материалов согласно изобретению относятся к следующему типу:

PP-ClSt-ТЕ3А
где PP - полипропиленовое волокно
CISt - полихлорметилстирол (разделительная ветвь)
ТЕ3А - макроциклический лиганд, содержащий четыре атома азота.

где РР - полипропиленовое волокно
MAnClSt - поли(малеиновый ангидрид-alt-хлорметилстирол) (разделительная ветвь)
ТЕ3А - макроциклический лиганд, содержащий четыре атома азота.
В этих формулах n и m являются целыми числами от 10 до 1000.
Получение новых материалов
Принцип прививки полиазамакроциклических, в частности тетраазамакроциклических молекул на полипропилен согласно изобретению, основан на реакции радикальной полимеризации на поверхности полипропилена.
Реакцию полимеризации инициируют радикалы, возникающие при нагревании предварительно облученного полипропиленового волокна. Мономером, применяемым при получении материалов согласно изобретению, как по первому, так и по второму осуществлению является, например, звено стирола. Разработаны два способа присоединения полиазамакроциклов, например тетраазамакроциклов на полипропилен согласно первому и второму осуществлению материала и способов согласно изобретению:
- «прямая прививка» путем полимеризации звеньев, например, типа стирола, несущих макроцикл, например макроцикл, содержащий четыре атома азота,
- прививка разделительной ветви путем полимеризации функционального мономера в присутствии полипропилена с последующим присоединением полиазамакроцикла, например тетраазамакроцикла, к реактивной функциональной группе упомянутого мономера. Конкретно, привиты две разделительные ветви, отличающиеся по химической природе.
В нижеследующем изложении различные операции, приводящие к получению новых материалов согласно изобретению, рассмотрены более детально.
В последующем описании материалов и способов согласно изобретению для иллюстрации приведены конкретные соединения, реактивные функциональные группы, конкретные условия и т.п.Эти соединения (например, полиазациклоалкан), функциональные группы или условия приведены только с иллюстративной целью и никоим образом не ограничивают изобретение, описанное выше и в формуле изобретения.
Специалист в данной области, основываясь на последующем описании, легко сможет применить изобретение ко всем возможным соединениям, условиям, реактивным функциональным группам и т.п., большая часть которых определена выше.
Способ прививки
Молекулярная структура полипропилена (РР):

где n обычно является целым числом от 100 до 3000.
Полипропиленовое волокно, применяемые в качестве основы материала, обычно находится в форме нетканого материала и предварительно облучено, например, на линейном ускорителе электронов в атмосфере воздуха или кислорода.
Облучение в атмосфере воздуха приводит к образованию пероксидов и/или гидропероксидов, предподчительно на атомах третичного углерода (см молекулярную структуру полипропилена выше). Совершенно очевидно, что можно применять другие технологии, известные специалисту в данной области, для получения полипропилена с такими пероксидными или гидропероксидными функциональными группами. Гидропероксиды и пероксиды претерпевают термальное разложение (выше 80°С) и образуют окси-радикалы на волокне, которые инициируют полимеризацию на поверхности волокна в присутствии мономера, который может вступать в реакцию полимеризации в условиях радикальной полимеризации, например мономера винила. Известно, что различные мономеры, способные к полимеризации в условиях радикальной полимеризации, привиты по этому способу: акрилонитрил (N.Kabay, A.Katakai, Т.Sugo, Н.Egawa, Journal of Applied Polymer Science, 1993, 49, 599-607), акрилат (L.С.Lopergolo, L.Н.Catalani, L.D.B.Machado, P.R.Rela, A.B.Lugao, Radiation Physics and Chemistry, 2000, 57, 451-454), акриловая кислота (Y.Lu, Z.Zhang, Н.Zeng, Journal of Applied Polymer Science, 1994, 53, 405-410; D.Chen, N.Shi, D.Xu, Journal of Applied Polymer Science, 1999, 73, 1357-1362; S.Н.Choi, Н.J.Kang, E.N.Ryu, K.P.Lee, Radiation Physics and Chemistry, 2001. 60, 495-502; Z.Xu, J.Wang, L.Shen, D.Men, Y.Xu, Journal of Membrane Science, 2002. 196. 221-229), винилпиридин (I.Kaur, S.Kumar, B.N.Misra, Polymers & Polymer Composites, 1995, 3, 375-383; S.Tan, G.Li, J.Shen, Journal of Applied Polymer Science, 2000, 77, 1861-1868), винилалкоксисилан (S.S.Ivanchev, M.Ratzsch, A.M.Mesh, S.Y.Khaikin, Н.Bucka, A.Hesse, Vysokomolekulyamye Soedineniya, Seriya A i Seriya B, 2001, 43, 793-798) и т.п.
Прямая прививка

R2=H, CH2CH2COOEt (например)
Два тетраазамакрициклических мономера, М-(4-винилбензил)циклама и N,N',N"-трис(2-этоксикарбонилэтил)-N"-(4-винилбензил)циклам в абсолютно идентичных условиях подвергают реакции полимеризации на поверхности полипропиленового волокна. Содержание привитого макроциклического лиганда приведено в таблице 1 ниже.
Прививка разделительной ветви
Прививка полихлорметилстирола
Полимеризация хлорметилстирола на поверхности полипропилена, представленная схематически ниже, приводит к волокнистому композитному материалу, называемому здесь PP-ClSt.
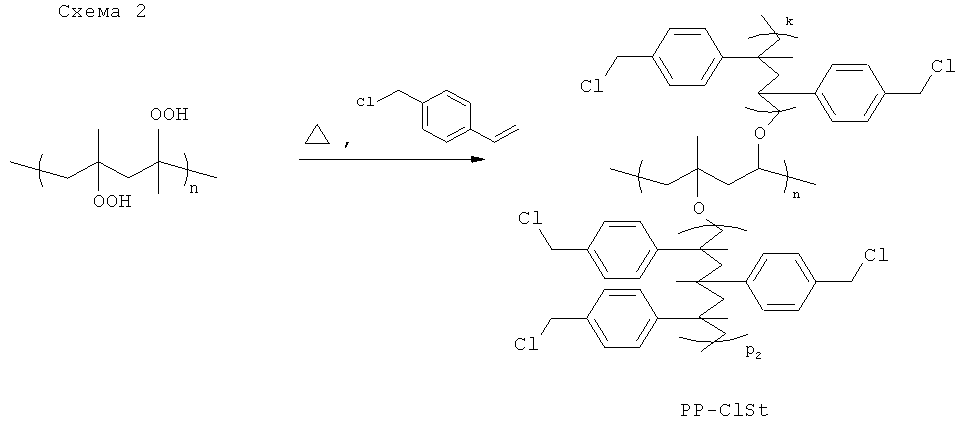
На схеме 2 n является целым числом от 100 до 3000 и k и p2 являются целыми числами от 10 до 1000.
Хлорметильная функциональная группа PP-ClSt волокна впоследствии способна к реакции в гетерогенной фазе с функциональной аминогруппой макроциклического лиганда. Содержание привитых макроциклических молекул таким образом обычно регулируют путем реакции полимеризации хлорметилстирола обычно на поверхность полипропилена. На реакцию полимеризации влияют известные параметры реакции полимеризации: природа растворителя, температура, концентрация мономера, время реакции и концентрация инициатора.
Одно из преимуществ этих материалов (обычно) особенно относительно полученных на основе силикагеля состоит в том обстоятельстве, что можно задавать и изменять количество участков комплексообразования, которые будут присутствовать в материале, что осуществляется путем контроля степени полимеризации во время прививки разделительной ветви.
Влияние вышеперечисленных параметров исследовано и полученные результаты представлены в примерах, приведенных ниже (пример 1).
Таким образом можно определить оптимальные параметры:
- растворитель ДМФА (диметилформамид),
- доза облучения 40 кГр,
- раствор с разведением 40% мономера в ДМФА,
- температура 115°С,
- время реакции 10 час (для получения содержания хлорметильных групп порядка 2 ммоль/г).
Эти оптимальные параметры определены для того, чтобы обеспечить получение материалов, проявляющих хорошее сочетание нужной степени прививки и сохранения целостности и свойств полипропиленового волокна.
Однако получение материалов согласно изобретению не ограничено исключительным и преобладающим применением параметров, приведенных выше.
Прививка поли(малеиновый ангидрид-alt-хлорметилстирола)
Для введения большего числа карбоксилатных функциональных групп, являющихся гидрофильными функциональными группами, участвующих в связывании тяжелых металлов, лантанидов и актинидов, проводят получение чередующегося сополимера из звеньев малеинового ангидрида и хлорметилстирола, привитого на поверхность полипропиленового волокна. Единообразие чередования звеньев хлорметилстирола и малеинового ангидрида обеспечивается путем образования комплекса с переносом заряда (КПЗ) на основе этих двух мономеров, демонстрация чего с помощью ЯМР спектроскопии приведена в примере 2 и на фигуре 5. Комплекс с переносом заряда обладает свойством полимеризоваться легче, чем отдельные мономеры.
Образование чередующегося сополимера из звеньев малеинового ангидрида и стирола описано как в растворе (Е.Tsuchida, Т.Tomono, Makromolekulare Chemie, 1971, 141, 265-298), так и на различных полимерных подложках: целлюлозе (G.S.Chauhan, L.K.Guleria, В.N.Misra, I.Kaur, Journal of Polymer Science, Part A: Polymer Chemistry, 1999, 37, 1763-1769), полиэтиленовых пленках (Н.A.A. El-Rehim, Е.A.Hegazy, A.E.-H. Ali, Reactive & Functional Polymers, 2000, 43, 105-116) и на литом полиэтилене (D.С.Clark, W.Е.Baker, R.A.Whitney, Journal of Applied Polymer Science, 2000, 79, 96-107). Проведено также исследование этой реакции с полипропиленом при химической инициации с помощью перекиси бензоила (D.Jia, Y.Luo, Y.Li, Н.Lu, W.Fu, W.L.Cheung, Journal of Applied Polymer Science, 2000, 78, 2482-2487) или с помощью ионизирующей обработки (озонирование и облучение γ-лучами) (Р.Citovicky, V.Chrastova, M.Foldesova, European Polymer Journal, 1996, 32, 153-158). Из малеинового ангидрида в качестве исходного материала получены различные КПЗ при добавлении стирола (L.J.Andrews, R.M.Keefer, Journal of the American Chemical Society, 1953, 75, 3776-3779), винилтриэтоксисилана (Z.M.Rzaev, L.V.Bryksina, S.I.Sadykh-Zade, Journal of Polymer Science, 1973, 42, 519-529) или 1,4-диоксана (S.Iwatsuki, Y.Yamashita, Makromol. Chem., 1965, 89, 205-213), как показано с помощью УФ и ЯМР спектроскопии. С другой стороны, образование КПЗ на основе малеинового ангидрида и хлорметилстирола никогда не упоминалось, насколько нам известно.
Сополимеризация малеинового ангидрида и хлорметилстирола на поверхности полипропилена, схематически представленная ниже, приводит к получению волокнистого композитного материала, известного под названием PP-MAnClSt.

На схеме 3 n является целым числом от 10 до 3000 и m является целым числом от 10 до 1000.
Влияние на степень прививки таких параметров, как растворитель, температура и время реакции, исследовано и представлено в примере 3. Из этого сделано заключение, что реакцию прививки поли(малеиновый ангидрид-alt-хлорметилстирола) на полипропиленовое волокно можно успешно контролировать путем применения ацетона в качестве растворителя, температуры 90°С (реакция под давлением) и общего содержания мономеров равного 30%. Степень прививки дополнительно контролируется с помощью времени реакции. Наличие эквимолярных количеств двух мономеров на поверхности полипропиленового волокна также подтверждено.
Присоединение макроциклических лигандов к материалу предшественника
Синтез лигандов
Синтезированы два типа макроциклических лигандов с целью присоединения к материалам PP-ClSt and PP-MAnClSt:
- нефункционализированные лиганды. Циклам получают согласно способу, приведенному в патенте (ЕР 0427595 (31/10/1990)).
Молекулярная структура циклама

- лиганды кислотного типа. Они несут функциональные группы карбоновой кислоты или сложного эфира. Триэфирные соединения являются «промежуточными лигандами», применяемыми для ускорения присоединения лигандов к материалам. После прививки их подвергают гидролизу с получением соответствующих карбоновых кислот.
Молекулярные структуры макроциклических предшественников



1,4,8-трис(2-карбоксиэтил)-1,4,8,11-тетраазациклотетрадекан (ТЕ3Р)
1,4,8-трис(этоксикарбонилэтил)-1,4,8,11-тетраазациклотетрадекан (ТЕ3РЕ)
1,4,8-трис(этоксикарбонилметил)-1,4,8,11-тетраазациклотетрадекан (ТЕ3АЕ)
(ТЕ - тетрадекан, 3 - число ветвей, Pr - пропионовая кислота, РЕ - этилпропионат, АЕ - этилацетат).
Обычно тетраазамакроциклические соединения с ветвями, трижды замещенными карбоновой кислотой, получают по следующему плану: введение однократной защиты в циклам с помощью бензильной группы, функционализация оставшихся трех вторичных аминов и затем отщепление бензильной группы (WO 96/11189 (05/10/1995)). Этот синтез включает несколько последовательных этапов и сопровождающие этапы очистки.
Материалы, описанные в данном изобретении, получают с целью промышленного применения, что означает необходимость их получения в большом количестве при ограничении вклада продолжительных операций (например, очистки). Разработанные новые пути синтеза двух макроциклических лигандов отвечают этим задачам, поскольку требуемые молекулы получают с необходимым выходом в один этап и без операций, которые сложно применять в промышленности.
Так, циклам 2, трижды функционализированный ацетатными ветвями, синтезируют с выходом 48% из циклама с применением 3,2 эквивалентов этилбромацетата (схема 4). Основной побочный продукт реакции, четырежды замещенное соединение 3, отделяют от реакционной смеси путем осаждения из этанола. Другие побочные продукты, однозамещенные, двузамещенные и кватернизованные соединения, являются нерастворимыми в пентане. Требуемый триэфир 2 получают путем простой экстракции этим растворителем.

Соответствующий пропионатно-сложноэфирный продукт 4 получают подобным образом с выходом 75% путем реакции циклама с избытком этилакрилата в хлороформе (схема 5). Реакция останавливается на трижды функционализированном соединении, тогда как полное замещение проходит в таком растворителе, как ацетонитрил.

Присоединение к PP-ClSt
Иммобилизации макроциклических молекул на волокнах PP-ClSt предшествует реакция нуклеофильного замещения между функциональными группами, например хлорметильными функциональными группами субстрата и функциональными группами вторичного амина у лиганда. Выход реакции прививки рассчитывают по содержанию хлора в материале предшественника и по содержанию связанных макроциклов (элементарный анализ азота в конечном материале). Это принимает в расчет увеличение массы материала при присоединении лиганда.
Присоединение нефункционализированного лиганда: циклам

На схеме 6 n2, p2 и m2 являются целыми числами от 10 до 1000.
У полученных материалов содержание привитого циклама варьирует от 0,2 ммоль/г до 1,1 ммоль/г, причем это значение прямо связано со степенью полимеризации материала PP-ClSt. Полученные результаты присоединения показывают, что в среднем циклам присоединяется к твердой подложке через ковалентные связи (схема 6). Эту схему можно конечно применять для любого полиазациклоалкана. Во время последующего этапа функционализации в среднем вводится только одна (или возможно две) координационная функциональная группа.
На этом этапе функционализации одна или более из трех свободных функциональных аминогрупп, например, замещается R2 группой, отличной от водорода, как определено выше.
Основанный на силикагеле контрольный материал получают по сходной схеме с последующей функционализацией лиганда после прививки на материал. В этом случае также присутствует только одна или две комплексообразующие карбоксилатные функциональные группы на лиганд.
Присоединение лигандов с тройной функционализацией
Присоединение лигандов с тройной функционализацией обеспечивает в отличие от этого систематическое присутствие трех комплексообразующих карбоксилатных функциональных групп на молекулу макроцикла, присоединенную к материалу, что обеспечивает более эффективное извлечение тяжелых металлов, лантанидов и актинидов.

На схеме 7 n2 является целым числом от 10 до 1000.
Присоединение лиганда N,N',N”-трис(2-натрийоксикаробонилэтил)циклама (R2=(CH2)2COONa)
Эту реакцию (схема 7) проводят в воде и она приводит к истинной прививке, хотя и небольшой. Присоединение циклама в органическом растворителе (ацетонитриле) в идентичных условиях реакции происходит таким образом значительно лучше (таблица 2).
Присоединение лигандов N,N',N”-трис(метоксикарбонилэтил)циклама (ТЕ3АЕ) (R2=CH2COOEt) и 7УД'Д"-трис(этоксикарбонилэтил)циклама (ТЕ3РЕ) (R2=(CH2)2COOEt).
Присоединение триэфиров ТЕ3АЕ (2) и ТЕ3РЕ (4) к PP-ClSt проводят в органическом растворителе, в ацетонитриле (схема 7). Эту схему можно применять для любого полиазациклоалкана. Содержание привитого лиганда зависит от содержания хлорметильных групп, присутствующих в PP-ClSt, а также от избытка лиганда, применяемого в реакции присоединения (таблица 3). Выход реакции прививки возрастает при избытке макроциклического соединения, применяемого в реакции. Однако наблюдается предел эффективности присоединения, связанный со стерическими препятствиями и составляющий примерно 50%.
На втором этапе координационные карбоксильные функциональные группы обычно получают путем омыления сложноэфирных групп макроциклических лигандов в присутствии гидроксида натрия в водно-спиртовой среде. Этот этап одновременно приводит к гидроксилированию значительной части (примерно 75%) остаточных концевых хлорсодержащих групп, сильно увеличивая таким образом гидрофильность и смачиваемость привитого волокна. Таким образом, присущая полипропиленовому волокну гидрофобность компенсируется путем введения значительного количества гидрофильных функциональных групп, концевых гидроксильных и карбоксилатных функциональных групп лиганда.
Присоединение к PP-MAnClSt
Прививка на PP-MAnClSt материалы ограничена присоединением ТЕ3РЕ и ТЕ3АЕ лигандов. Максимальное содержание привитого макроцикла составляет 0,6 ммоль/г.
Показано, что при двух возможных путях реакции присоединения вторичного амина к PP-MAnClSt материалам, которыми являются реакция нуклеофильного замещения по атому углерода, соединенному с атомом хлора, и конденсация с малеиновым ангидридом с образованием амидной функциональной группы, присоединение лиганда на две трети проходит по второму пути.
Последующий этап омыления сложноэфирной группы иммобилизованного лиганда сопровождается, как описано выше, гидроксилированием большой части (75%) остаточных хлорметильных функциональных групп материала. Следует отметить, что применяемые условия реакции (реакция при 40°С в течение 18 час в присутствии 0,5 н. раствора гидроксида натрия) делает возможным полный гидролиз сложноэфирных функциональных групп, тогда как в отношении амидных функциональных групп наблюдается только частичный гидролиз: макроциклический лиганд остается связанным на 85%.
Изобретение далее описано с помощью примеров, приведенных с иллюстративными целями, а не для ограничения области применения изобретения.
Пример 1. Влияние различных параметров на прививку полихлорметилстирола на полипропиленовое волокно
В этом примере исследуют действие различных параметров на прививку полихлорметилстирола на полипропиленовое волокно.
Это полипропиленовое волокно находится в форме нетканого материала и предоставлено после облучения Французским институтом текстиля и одежды (Institut Francais du Textile et de L'Habillement).
Прежде всего следует отметить, что качество прививки можно оценивать с помощью элементарного анализа на атомы хлора или путем определения увеличения массы материала во время прививки. Эти два способа оценки дают согласующиеся результаты, когда волокно не подвергается декомпозиции во время прививки (сопровождающейся потерей массы). Результаты прививки, приведенные ниже, выражены в данном случае в виде функции содержания хлора.
1А. Выбор растворителя
Различные исследования упоминают применение таких растворителей, как метанол (Y.С.Nho, J.Chen, J.H.Jin, Radiation Physics and Chemistry, 1999, 54, 317-322), вода (А.С.Patel, R.В.Brahmbhatt, Р.V.С.Rao, K.V.Rao, S.Devi, European Polymer Journal, 2000, 36, 2477-2484; I.Kaur, S.Kumar, B.N.Misra, G.S.Chauhan, Materials Science & Engineering, A: Structural Materials: Properties, Microstructure and Processing, 1999, A270, 137-144) или водно-метанольная смесь (1:1) (I.Kaur, S.Kumar, B.N.Misra, Polymers & Polymer Composites, 1995, 3, 375-383) для прививки стирола на полипропилен.
Дополнительно к растворителям, упомянутым выше для полимеризации полистирола на полипропилене, тестируют растворители толуол и N,N-диметилформамид (ДМФА) для полимеризации хлорметилстирола на поверхности полипропиленового волокна.
Применение последнего растворителя (ДМФА) приводит к наилучшим результатам, поскольку оно предоставляет хорошую гомогенность прививки, делает возможным растворять побочный продукт, а именно гомополимер, и не ускоряет декомпозиции материала.
ДМФА представляется подходящим растворителем для этой реакции.
1Б. Действие дозы облучения
Доза облучения отражает энергию излучения, полученную материалом.
В настоящих исследованиях полипропиленовое волокно облучают тремя различными дозами: 20 кГр, 40 кГр и 60 кГр (1 кГр=1 Дж/кг).
Полученные результаты (фигура 1) показывают большее количество привитого полихлорметилстирола в случае более высоких доз облучения. Однако при 60 кГр волокна частично растворяются в среде, что является последствием укорочения полипропиленовых цепочек в результате реакции расщепления. Действие облучения, хотя и детектируется, остается ограниченным, однако, оно значительно ослабляется после последующего присоединения макроциклического соединения к PP-ClSt материалу.
Облучение дозой 40 кГр представляется оптимальным для сохранения целостности волокна, предоставляя при этом требуемую степень прививки.
1 В. Действие температуры
Температура принимает участие в распаде пероксидных связей с образованием оксо-радикалов. Увеличение их числа обусловливает возрастание количества мест инициации радикальной полимеризации и вследствие этого приводит к возрастанию количества привитого полихлорметилстирола (фигура 2).
Однако существует предел температуры, установленный началом растворения полипропилена в реакционной среде. Волокна не подвергаются декомпозиции вплоть до 120°С при времени реакции 16 час, когда хлорметилстирол растворен в ДМФА в концентрации 40%.
Температура реакции таким образом ограничена 115°С.
1Г. Действие концентрации хлорметилстирола в ДМФА
Исследование действия концентрации мономера хлорметилстирола в ДМФА в интервале 30-50% демонстрирует оптимум реакции прививки на полипропиленовое волокно при концентрации хлорметилстирола около 40% (фигура 3). Такое прохождение через максимум упоминается многими группами исследователей для различных систем:
максимум достигается при 55% в случае акриловой кислоты в воде (D.Chen, N.Shi, D.Xu, Journal of Applied Polymer Science, 1999, 73, 1357-1362), 40% в случае метилметакрилата в смеси метанола с декалином (L.С.Lopergolo, L.Н.Catalani, L.D.В.Machado, P.R.Rela, А.В.Lugao, Radiation Physics and Chemistry, 2000, 57, 451-454), 40% в случае стирола в воде (I.Kaur, S.Kumar, В.N.Misra, Polymers & Polymer Composites, 1995, 3, 375-383) и 25% в случае стирола в метаноле (Y.С.Nho, J.Chen, J.Н.Jin, Radiation Physics and Chemistry, 1999, 54, 317-322).
Концентрация 40% хлорметилстирола в ДМФА является таким образом оптимальной для реакции полимеризации этого мономера на поверхности полипропилена.
1Г. Влияние времени реакции
Эта реакция отличается латентным периодом перед началом полимеризации. Он соответствует периоду времени, необходимому для доведения волокон до нужной температуры и для потребления стабилизаторов мономера (фигура 4).
Контроль времени реакции делает возможным контролировать количество групп хлорметилстирола, присоединенных к полипропиленовым волокнам, и впоследствии содержание макроциклического лиганда, присоединенного к материалу в дальнейшем. Целью не является достижение максимальной иммобилизации макроциклического лиганда, поскольку это привело бы к сильной модификации материала и потере волокном исходных свойств.
Следовательно время реакции, составляющее примерно 10 час (примерно 2 ммоль/г функциональных групп хлорметила), представляется хорошим компромиссом между необходимой степенью прививки и сохранением характеристик подложки.
Пример 2. Образование комплекса с переносом заряда на основе малеинового ангидрида и хлорметилстирола
Образование комплекса с переносом заряда на основе малеинового ангидрида и хлорметилстирола в растворе показано с помощью ЯМР спектроскопии (фигура 5). После перемешивания двух реагентов в ацетоне в течение одного часа с обратным холодильником спектр ЯМР реакционной смеси показывает появление нового сигнала этилена, экранированного по сравнению с соответствующим сигналом свободных мономеров.
Равновесие этой реакции (схема 8) сдвинуто в сторону свободных мономеров, однако, образование некоторого количества комплекса (с переносом заряда), а также предпочтительная его полимеризация делает возможным проведение прививки чередующегося сополимера на поверхность полипропилена.

Пример 3. Действие различных параметров на прививку поли(малеинового ангидрида-alt-хлорметилстирола) на полипропиленовое волокно
В этом примере исследуют действие различных параметров на прививку поли(малеинового ангидрида-alt-хлорметилстирола) на полипропиленовое волокно.
Результаты прививки поли(малеинового ангидрида-alt-хлорметилстирола) на полипропиленовое волокно, выраженные в терминах увеличения массы, приведены ниже для различных условий реакции.
Полимеризация не происходит в ДМФА, она быстрее происходит в толуоле, чем в ацетоне. Однако поскольку ацетон в отличие от толуола растворяет оба мономера и гомополимер, он является предпочтительным растворителем для проведения реакции. Гомогенность прививки при этом обеспечена.
Присоединение каждого мономера к полипропилену качественно подтверждается с помощью инфракрасной спектроскопии и количественно с помощью микроанализа элементов хлора и кислорода. При увеличении массы на 32% количество привитого малеинового ангидрида и привитого хлорметилстирола составляют 0,97 ммоль/г для каждого в случае регулярной чередующейся последовательности двух мономеров (таблица 5). Экспериментальные результаты (1,03 ммоль/г малеинового ангидрида и 0,94 ммоль/г хлорметилстирола) подтверждают наличие чередования двух мономеров в сополимере, таким образом поддерживая полимеризацию комплекса с переносом заряда на поверхности полипропилена.
В следующих примерах 4 и 5 приведено описание синтеза макроциклических лигандов, применяемых для прививки на полипропиленовое волокно согласно изобретению.
Пример 4. Получение лигандов, применяемых для прямой прививки
Пример 4А. Получение 1-(4-винилбензил)-1,4,8,11-тетраазациклотетрадекана
40 г циклама (соединение 1) (200 ммоль) растворяют в 1 л ДМФА при 70°С. К раствору добавляют 25 г (181 ммоль) карбоната калия. По каплям медленно (9 час) при перемешивании добавляют раствор 5,9 г (38,7 ммоль) хлорметилстирола в 500 мл ДМФА. Реакционную смесь перемешивают при 70°С в течение еще одного часа. После возвращения к температуре окружающей среды избыток циклама и карбоната натрия удаляют путем фильтрации. Фильтрат упаривают и остаток отбирают диэтиловым эфиром. После выпаривания растворителя соединение получают в виде светло-желтого маслянистого вещества (11,2 г; 35,4 ммоль). Выход 91%.
1H NMR (200 MHz; CDCl3) δ (ppm):
1.52 (m, 2H, СН2-β); 1.69 (m, 2H, CH2-β); 2.2-2.7 (broad unresolved peak, 16H, CH2-α); 3.40 (s, 2H, CH2-φ); 5.06 (d, JBX=11.0 Hz, 1H, HB); 5.54 (d, JAX=17.6 Hz, 1H, HA); 6.52 (dd, JBX=11.0 Hz, JAX=17.6 Hz, 1H, HX); 7.1-7.2 (broad unresolved peak, 4H, H-Ar).
13C NMR (50 MHz; CDCl3) δ (ppm):
26.3; 28.7 (CH2-β); 47.5; 48.0; 49.0; 49.1; 49.3; 50.8; 53.2; 54.7 (CH2-α); 57.5 (CH2-φ); 113.3 (=СН2); 126.0; 129.3 (CH-Ar); 136.2 (C-Ar); 136.7 ((φ-CH=); 138.4 (C-Ar).
Масс-спектрометрия (MALDI/TOF): m/z=316,88 (M+•)
Пример 4Б. Получение 1-(4-винилбензил)-1,4,8-трис(этоксикарбонилэтил)-1,4,8,11-тетраазациклотетрадекана
15,0 г (47,4 ммоль) соединения 2 полученного в Примере 4А, растворяют в 700 мл этанола. При перемешивании добавляют 72,0 г (720 ммоль) этилакрилата в 400 мл этанола путем быстрого добавления по каплям (продолжительность добавления 1 час). Реакционную смесь держат с обратным холодильником в течение 43 час. После выпаривания этанола остаток отбирают с помощью 100 мл пентана. Растворитель выпаривают и соединение очищают на колонке с окисью алюминия (элюент - смесь этилацетат:гексан 50:50). Соединение получают в виде светло-желтого маслянистого вещества (25,1 г, 40,7 ммоль). Выход 86%.
1H NMR (200 MHz; CDCl3) δ (ppm):
1.18 (t, J=7.1 Hz, 3H, СН3-СН2); 1.20 (t, J=7.1 Hz, 3Н, СН3-СН2); 1.22 (t, J=7.1 Hz, 3H, СН3-СН2); 1.56 (m, 4H, CH2-β); 2.3-2.5 (broad unresolved peak, 22H, CH2-α); 2.6-2.8 (broad unresolved peak, 6H, CH2-CO); 3.45 (s, 2H, CH2-φ); 4.04 (q, J=7.1 Hz, 2H, СН3-СН2); 4.06 (q, J=7.1 Hz, 2H, СН3-СН2); 4.09 (q, J=7.1 Hz, 2H, СН3-СН2); 5.16 (dd, 1H, JAB=1.0 Hz, JBX=11.0 Hz, HB); 5.68 (dd, 1H, JAB=1.0 Hz, JAX=17.6 Hz, HA); 6.66 (dd, 1H, JBX=11.0 Hz, JAX=17.6 Hz, HX); 7.2-7.3 (broad unresolved peak, 4H, H-Ar).
13C NMR (50 MHz; CDCl3) δ (ppm):
14.3 (3C) (СН3-СН2); 23.7; 24.1 (CH2-β); 32.6; 32.7 (2C) (CH2-CO); 50.6 (4C); 51.2 (4С); 51.4 (3С) (CH2-α); 59.4 (СН2-φ); 60.4 (3С) (СН3-СН2); 113.3 (=CH2); 129.0; 129.1 (СН-Ar); 136.2 (C-Ar); 136.8 ((β-CH-); 139.8 (C-Ar); 172.9 (3С) (С=O).
Macс-спектрометрия (MALDI/TOF): m/z=616.83 (M+•).
Элементарный анализ:
Расчетное: С: 66.23; Н: 9.09; N: 9.09
Экспериментальное: С: 66.42; Н: 9.11; N: 9.13
Пример 5. Получение лигандов, применяемых при двухступенчатой прививке
Пример 5А. Получение 1,4,8-трис(этоксикарбонилметил)" 1,4,8,11-тетраазациклотетрадекана (соединение 2)
5 г (25 ммоль) циклама растворяют в 400 мл ацетонитрила в присутствии 15 г (109 ммоль) карбоната калия. По каплям быстро добавляют 8 г (80 ммоль) этилбромацетата. Реакционную смесь и держат с обратным холодильником в течение 22 час. Избыток карбоната натрия отфильтровывают и растворитель выпаривают. Добавление 100 мл этанола к остатку приводит к осаждению белого твердого вещества. После фильтрации и сушки получают 4,57 г соединения 3. Фильтрат упаривают и остаток отбирают с помощью 50 мл пентана. После выпаривания растворителя получают соединение 2 в виде бесцветной маслянистой жидкости (5,5 г, 12,0 ммоль). Выход 48%.
Продукт можно очищать на колонке с окисью алюминия (элюент - смесь дихлорметан: метанол от 99:1 до 95:5).
1H NMR (300 MHz; CDCl3) δ (ppm):
1.17 (t, J=7.1 Hz, 3H, CH3-CH2); 1.19 (t, J=7.1 Hz, 3Н, CH3-СН2); 1.20 (t, J=7.1 Hz, 3Н, СН3-СН2); 1.53 (m, 2H, СН2-β); 1.64 (m, 2H, СН2-β); 2.5-2.8 (broad unresolved peak, 17H, CH2-α and NH); 3.27 (s, 2H, CH2-CO); 3.28 (s, 2H, CH2-CO); 3.32 (s, 2H, CH2-CO); 4.05 (q, J=7.1 Hz, 2H, СН3-СН2); 4.06 (q, J=7.1 Hz, 2H, СН3-CH2); 4.07 (q, J=7.1 Hz, 2H, СН3-СН2).
13С NMR (75 MHz; CDCl3) δ (ppm):
14.6 (ЗС) (СН3-СН2); 25.5; 26.3 (СН2-β); 47.7; 47.8; 48.8; 50.0; 50.4; 51.8; 52.6; 53.8; 53.9; 54.1; 55.6 (CH2-α); 60.1; 60.2 (2С) (СН3-СН2); 171.5; 171.6; 171.7 (С=O).
ИК спектроскопия (KBr, см-1):
1736 υ(C=O).
Масс-спектрометрия (MALDI/TOF): m/z=457.95 (M+•).
Элементарный анализ:
(соединение 2)·2H2O
Расчетное: С: 53,64; Н: 9,00; N: 11,37
Экспериментальное: С: 53,48; Н: 8,81; N: 11,40
Пример 5Б. Получение 1,4,8,11-тетра(этоксикарбонилметил)-1,4,8,11-тетраазациклотетрадекана (соединение 3)
Это соединение является побочным продуктом синтеза соединения 2. Выход 34%.
1Н NMR (500 MHz; CDCl3) δ (ppm):
1.23 (t, J=7.1 Hz, 12H, СН3-СН2); 1.59 (qt, 4H, J=6.6 Hz, СН2-β); 2.68 (t, 8H, J=6.6 Hz, CH2-α); 2.72 (s, 8H, СН2-α); 3.34 (s, 8H, CH2-СО); 4.12 (q. J=7.1 Hz, 8H, СН3-СН2).
13С NMR (125 MHz; CDCl3) δ (ppm):
14.8 (СН3-СН2); 25.8 (CH2-β); 51.5; 51.6 (CH2-α); 55.9 (CH2-CO); 60.6 (СН3-CH2); 172.1 (C=O).
ИК спектроскопия (KBr, см-1):
1729 υ(C=0).
Масс-спектрометрия (MALDI/TOF):
m/z=544.99 (M+•).
Элементарный анализ:
(соединение 3)·2H2O
Расчетное: С: 57,33; Н: 8,88; N: 10,29
Экспериментальное: С: 57,03; Н: 8,92; N: 10,24
Пример 5 В. 1,4,8-трис(этоксикарбонилэтил)-1,4,8,11-тетраазациклотетрадекан (соединение 4)
16,2 г (81 ммоль) циклама (соединения 1) растворяют в 1,3 л хлороформа с обратным холодильником. Добавляют 40 г (400 ммоль) этилакрилата. После инкубации с обратным холодильником в течение 48 час хлороформ выпаривают и остаток отбирают с помощью 200 мл пентана. В результате выпаривания получают 30,3 г (60,5 ммоль) слегка желтоватой маслянистой жидкости. Выход грубого вещества 75%.
Продукт можно очищать на колонке с силикагелем путем градиентной элюции смесью дихлорметан:метанол:триэтиламин от 89:1:10 до 85:5:10. Выход после колонки 65%.
1Н NMR (500 MHz; CDCl3) δ (ppm):
1.15 (t, J=7.1 Hz, 3Н, СН3-СН2); 1.16 (t, J=7.1 Hz, 3Н, CH3-CH2); 1.17 (t, J=7.1 Hz, 3Н, CH3-СН2); 1.52 (m, 2H, CH2-β); 1.64 (m, 2H, CH2-β); 2.3-2.6 (broad unresolved peak, 23H, CH2-α and NH); 2.69 (t, J=7.2 Hz, 2H, CH2-CO); 2.70 (t, J=7.2 Hz, 2H, CH2-CO); 2.71 (t, J=7.2 Hz, 2H, CH2-CO); 4.01 (q, J=7.1 Hz, 2H, СН3-СН2); 4.02 (q, J=7.1 Hz, 2H, СН3-СН2); 4.03 (q, J=7.1 Hz, 2H, CH3-CH2).
13С NMR (125 MHz; CDCl3) δ (ppm):
14.6 (3С) (СН3-СН2); 25.3; 25.9 (CH2-β); 31.5; 31.9; 31.9 (CH2-CO); 47.4; 48.3; 49.1; 49.2; 49.4; 50.3; 50.7; 51.4; 52.0; 52.7; 53.6 (CH2-α); 60.7 (3С) (СН3-СН2); 173.2 (СО) (3С).
ИК спектроскопия (KBr, см-1):
1729 υ(C=0).
Масс спектрометрия (MALDI/TOF):
m/z=500.82 (M+•).
Элементарный анализ:
Расчетное: С: 59,97; Н: 9,66; N: 11,03
Экспериментальное: С: 59,68; Н: 10,49; N: 11,19
В нижеследующих примерах описан синтез материалов согласно изобретению.
Пример 6. Получение материала согласно изобретению путем прямой прививки на полипропиленовое волокно
Пример 6А. Прививка поли-N-(4-винилбензил)-циклама на полипропиленовое волокно
1,2 г (3,8 ммоль) соединения N-(4-винилбензил)-циклам растворяют в 8 г ДМФА. К этому раствору добавляют полипропиленовое волокно (109,5 мг), облученные дозой 40 кГр. После продувки азотом в течение 30 мин реакционную смесь нагревают при 105°С в течение 13 час. Волокно промывают толуолом, этанолом и эфиром и под конец сушат под вакуумом. Получают 115,9 мг волокна.
Элементарный анализ:
N: 1,10%, т.е. 0,20 ммоль/г циклама.
Пример 7. Получение материала согласно изобретению путем двухступенчатой прививки на полипропиленовое волокно
NB: в нижеследующем тексте римские цифры, идентифицирующие соединения, не имеют отношения к номерам формул, приведенным выше и в формуле изобретения.
7А. PP-ClSt I
Суспензию из 2,47 г полипропиленового волокна, облученного дозой 40 кГр, в растворе 45 г (295 ммоль) хлорметилстирола в 45 г ДМФА дегазируют под азотом в течение 30 мин. Реакционную смесь далее доводят до температуры 115°С в атмосфере азота и выдерживают в течение 4 час. Затем волокно последовательно промывают толуолом, этанолом и эфиром и под конец сушат под вакуумом. PP-ClSt I получают в виде нетканого материала (2,78 г). Увеличение массы составляет 13%.
Элементарный анализ: Cl: 2,75%, т.е. 0,77 ммоль/г функциональных групп хлорметила.
7Б. PP-ClSt-циклам II

Пример
11 ммоль CH2Cl функциональных групп
0,88 ммоль циклама
0,40 ммоль остаточных CH2Cl функциональных групп
В вышеприведенных формулах n2, m2 и p2 являются целыми числами от 10 до 1000.
Суспензию 2,73 г материала PP-ClSt I и 3,5 г (24,3 ммоль) карбоната калия в растворе 3,5 г (17,5 ммоль) циклама (1) в 300 мл ацетонитрила нагревают при 60°С в течение 60 час. Волокно промывают смесью вода:этанол пока реакция промывных вод не вернется к нейтральной, затем этанолом, толуолом и под конец эфиром. После сушки под вакуумом получают PP-ClSt-циклам II в виде нетканого материала (2,84 г).
Элементарный анализ:
N: 1,72%, т.е. 0,31 ммоль/г циклама;
Cl: 0,49%, т.е. 0,14 ммоль/г остаточных функциональных групп хлорметила.
7 В. PP-ClSt III
Суспензию полипропиленового волокна (1,39 г), облученного дозой 40 кГр, в растворе 24 г (157 ммоль) хлорметилстирола в 56 г ДМФА дегазируют под азотом в течение 30 мин. Реакционную смесь далее доводят до температуры 115°С в атмосфере азота и выдерживают в течение 17 час. Волокно последовательно промывают толуолом, этанолом и затем эфиром и под конец высушивают под вакуумом. PP-ClSt III получают в виде нетканого материала (2,28 г). Увеличение массы составляет 64%.
Элементарный анализ:
Cl: 8,17%, т.е. 2,30 ммоль/г функциональных групп хлорметила.
ИК спектроскопия (КВг, см-1):
3087; 3025 υ(=C-H); 2960; 2922; 2837; 1724; 1611; 1512 υ (C=C); 1451; 1377; 1264 5(CH2); 1167; 1110; 1020; 998; 872; 840; 809 υ (C=C-H); 708; 674.
7Г. PP-ClSt-ТЕЗАЕ IV

Пример
0,90 ммоль CH2Cl функциональных групп
0,29 ммоль ТЕ3АЕ
0,55 ммоль CH2Cl остаточных функциональных групп
0,27 ммоль ТЕ3А
0,14 ммоль CH2Cl остаточных функциональных групп
n=10-1000
Суспензию 0,39 г материала PP-ClSt III и 5,5 г (39,9 ммоль) карбоната калия в растворе 1,67 г (3,65 ммоль) триэфира 10 (ТЕЗАЕ) в 50 мл ацетонитрила нагревают при 40 С в течение 70 час.Волокно промывают смесью вода:этанол пока реакция промывных вод не вернется к нейтральной, затем этанолом, толуолом и под конец эфиром. После сушки под вакуумом получают PP-ClSt-ТЕЗАЕ IV в виде нетканого материала (0,54 г).
ИК спектроскопия (KBr, см-1):
3453; 2961; 2924; 2837; 1727 υ(C=0); 1634; 1611; 1511; 1449; 1376; 1261; 1153; 1111; 1028; 997; 971; 839; 807; 707; 671.
Элементарный анализ:
N: 3,02%, т.е. 0,54 ммоль/г ТЕ3АЕ
Cl: 3,59%, т.е. 1,01 ммоль/г остаточных функциональных групп хлорметила.
7Д. PP-ClSt-ТЕ3А V
1 М раствор гидроксида натрия получают в водно-этанольной смеси с объемным соотношением 1:1. Материал PP-ClSt-ТЕЗАЕ IV (0,51 г) добавляют к 80 мл такого раствора. Реакционную смесь интенсивно перемешивают в течение 30 час. Волокно промывают смесью вода:этанол пока реакция промывных вод не вернется к нейтральной, затем этанолом, толуолом и под конец эфиром. Получают PP-ClSt-ТЕ3А V в виде нетканого материала (0,48 г).
ИК спектроскопия (KBr, см-1):
3437; 2963; 2922; 2851; 1627; 1594 υas(CO); 1511; 1452; 1419 υs(C=O); 1384; 1261; 1097; 997; 972; 840; 807; 708.
Элементарный анализ:
N: 3,05%, т.е. 0,54 ммоль/г ТЕ3А
Cl: 1,03%, т.е. 0,29 ммоль/г остаточных функциональных групп хлорметила.
7Е. PP-MAnClSt VI
Суспензию полипропиленового волокна (2,44 г), облученного при 40 кГр, в растворе 24 г (245 ммоль) малеинового ангидрида и 36 г (236 ммоль) хлорметилстирола в 94 мл ацетона дегазируют под азотом в течение 30 мин в автоклаве. Далее реакционную смесь нагревают до 90°С в атмосфере азота и держат в течение 20 час. Волокно последовательно промывают ацетоном, толуолом и затем эфиром и под конец сушат под вакуумом. PP-MAnClSt VI получают в виде нетканого материала (3,28 г). Увеличение массы составляет 35%.
ИК спектроскопия (KBr, см-1):
3402; 2959; 2925; 2838; 1858 υas(C=O); 1782 υs(C=O); 1710; 1454; 1377; 1262 δ(CH2); 1222; 1167; 1093 υ(C=O); 998; 973; 841; 806 δ(C=C-H); 711.
Элементарный анализ:
Cl: 3,53%, т.е. 0,99 ммоль/г функциональных групп хлорметила
О: 4,63%, т.е. 0,96 ммоль/г функциональных групп ангидрида.
7 Ж. PP-MAn-ClSt-ТЕ3РЕ VII

Пример
0,39 ммоль CH2Cl функциональных групп
0,14 ммоль ТЕ3РЕ
0,34 ммоль CH2Cl остаточных функциональных групп
0,12 ммоль TE3Pr
0,06 ммоль CH2Cl остаточных функциональных групп
Где m=10-1000.
Суспензию 0,40 г материала PP-MAnClSt VI и 2,8 г (20,3 ммоль) карбоната калия в растворе 7,2 г (14,4 ммоль) триэфира 11 (ТЕ3РЕ) в 350 мл ацетонитрила нагревают при 50°С в течение 60 час. Волокно промывают смесью вода:этанол пока реакция промывных вод не вернется к нейтральной, затем этанолом, толуолом и под конец эфиром. После сушки под вакуумом получают PP-MAn-ClSt-ТЕ3РЕ VII в виде нетканого материала (0,46 г).
ИК спектроскопия (KBr, см-1):
3430; 2957; 2921; 2837; 1855; 1781; 1733 υ(C=O)ester; 1631 υ (C=O)amide; 1456; 1377; 1256;1167;1100;997;972; 840; 808;710.
Элементарный анализ:
N: 1,74%, т.е. 0,31 ммоль/г ТЕ3РЕ
Cl: 2,59%, т.е. 0,73 ммоль/г остаточных функциональных групп хлорметила.
73. PP-MAn-ClSt-TE3Pr VIII
0,5 М раствор гидроксида натрия получают в водно-этанольной смеси с объемным соотношением 1:1. Материал PP-MAn-ClSt-ТЕ3РЕ VII (0,42 г) добавляют к 80 мл такого раствора. Реакционную смесь интенсивно перемешивают при комнатной температуре в течение 18 час и затем при 40°С в течение 16 час. Волокно промывают смесью вода:этанол пока реакция промывных вод не вернется к нейтральной, затем этанолом, толуолом и под конец эфиром. После сушки под вакуумом получают PP-MAn-ClSt-TE3Pr VIII в виде нетканого материала (0,41 г).
ИК спектроскопия (KBr, см-1):
3427; 2958; 2922; 2837; 1717; 1582 υas(C=O); 1456; 1407 υs(C=O); 1377; 1261; 1166; 1093;997; 972; 841;807;709.
Элементарный анализ:
N: 1,51%, т.е. 0,27 ммоль/г ТЕ3Рr
Cl: 0,46%, т.е. 0,13 ммоль/г остаточных функциональных групп хлорметила.
Пример 8. Экстрактивные свойства материалов
В этом примере исследуют экстрактивные свойства материалов согласно изобретению по отношению к катионам уранила, плутония и кадмия.
Способность материалов согласно изобретению извлекать радиоактивные элементы сравнивают с таковой контрольного материала, у которого лиганд TE3Pr привит на силикагель; этот материал известен как Si2323Pr ("путь 1"), полученный согласно публикации (WO-A-01/15806). Ссылка конкретно относится к стр.22-24 этого документа.
Далее показано, что способность отдельных материалов согласно изобретению извлекать радиоактивные элементы выше, чем у контрольного материала с подложкой из силикагеля.
Экстрактивные свойства материалов оценивают путем определения количества металла, связанного в равновесии, на грамм материала. Эту величину, измеренную для каждого материала в абсолютно идентичных условиях, называют qe и выражают в ммоль/г. Экспериментальная установка, применяемая для определения значений qe, приведена на фигуре 6.
Известно, что в эксперименте принцип адсорбционной экстракции состоит в приведении комплексообразующего материала в контакт с раствором известной концентрации металла Со в условиях высокой специфичности в течение времени, необходимого для достижения равновесия.
Для облегчения контакта между раствором и твердым веществом применяют специальную экспериментальную установку, включающую контейнер (1), содержащий раствор (2), снабженный, например, магнитной мешалкой (3), шланговый насос (4) для обеспечения циркуляции раствора (5) по трубкам (6), катушку (7) для термостатирования, например при 50°С, и держатель фильтра (8), в который помещают материал. Раствор, содержащий катионы металлов, таким образом циркулирует по петле в течение, например, 18 час для обеспечения достижения равновесия.
Пример 8А. Экстракция уранила и плутония
Количества металлов, удаленных твердым веществом, qe для различных полученных волокнистых материалов, а также для контрольного материала на основе силикагеля, применяемого в полупромышленной опытной установке (F. Barbette, These de I'Universite de Bourgogne [Thesis of the University of Burgundy], 1999) и известного как «силикагель (путь 1)», приведены в таблице 6 для экстракции уранила и в таблице 7 для экстракции плутония.
Вышеприведенные таблицы 6 и 7 показывают, что непривитый полипропилен неспособен связывать уранил или плутоний (и в общем ни один из растворенных металлов), что означает, что извлечение этих элементов обеспечено исключительно путем комплексообразования с макроциклическими лигандами.
Отсутствие участия полипропиленовой подложки в извлечении металлов обеспечивает сохранение избирательности при образования комплексов молекул макроциклов, содержащих четыре атома азота, с металлами-мишенями. Для сравнения известно, что немодифицированный силикагель сам по себе проявляет сильную адсорбционную способность по отношению к уранилу (J.D.Prikryl, A.Jain, D.R.Turner, R.Т.Pabalan, Journal of Contaminant Hydrology, 2001, 47, 241-253) и определенную способность связывать плутоний (Н. Chollet, Thése de l'Université de Bourgogne [Thèsis of the University of Burgundy], 1994).
Материалы, полученные из разделительной ветви хлорметилстирола, т.е. материалы, называемые PP-ClSt, проявляют более высокую способность связывать радиоактивные элементы, чем контрольный материал. Улучшенные характеристики этого модифицированного органического волокна относят к более высокому содержанию лиганда и к функционализации макроциклов с помощью трех ветвей с координационными свойствами. В общем, материалы, полученные из второй разделительной ветви, называемые PP-MAnClSt материалами, менее эффективны для связывания этих двух радиоактивных элементов.
Лиганд ТЕ3А, обладающий самыми короткими (ацетатными) ветвями, проявляет лучшую эффективность в извлечении сферического иона плутония, тогда как пропионатные ветви лиганда ТЕ3Рr больше подходят для образования комплекса с палочкообразным уранилом.
Материалы согласно изобретению обладают способностью к избирательному удалению уранила в присутствии конкурентных ионов кальция, калия и натрия, которые являются тремя преобладающими катионами металлов в реальных сточных водах.
Из эквимолярной смеси ионов только уранил извлекается материалом и количество извлеченного радиоактивного элемента не уменьшается в присутствии других катионов (таблица 8).
Пример 8Б. Экстракция кадмия
Полипропиленовое волокно, модифицированное с помощью макроциклических лигандов с четырьмя атомами азота, проявляет истинную способность извлекать кадмий. Эту способность оценивают по количеству металла qe, связанного материалом в равновесии (таблица 9).
Экспериментальное сравнение двух материалов из привитого волокна показывает значительно большее связывание кадмия в случае иммобилизации лиганда, несущего ацетатные функциональные группы ТЕ3А.
Реферат
Изобретение относится к материалам, применяемым для тонкой очистки жидкостей. Предложен материал, включающий полиазациклоалкан, привитый на полипропиленовое волокно, способ получения такого материала, и способ удаления катионов металлов, присутствующих в жидкости, путем приведения этой жидкости в контакт с упомянутым материалом. Технический результат - предложенный материал совмещает превосходную избирательность связывания тяжелых металлов, лантанидов или актинидов с прекрасными эксплуатационными характеристиками. 4 н. и 51 з.п. ф-лы, 6 ил., 9 табл., 8 пр.
Формула
а) радикальную полимеризацию одного или более мономеров, которые можно полимеризовать в условиях радикальной полимеризации, проводят в присутствии полипропиленового волокна, несущего пероксидные и/или гидропероксидные функциональные группы, где по меньшей мере один из упомянутых мономеров включает по меньшей мере одну функциональную группу, способную реагировать со свободной функциональной аминогруппой полиазациклоалкана, в результате чего получается полимер, включающий упомянутые функциональные группы, способные реагировать со свободными функциональными аминогруппами полиазациклоалкана, привитый на полипропилен;
б) упомянутый полимер реагирует с полиазациклоалканом;
в) при необходимости свободную функциональную аминогруппу или аминогруппы полиазациклоалкана, при необходимости еще присутствующую, подвергают функционализации;
г) при необходимости сложноэфирные функциональные группы, имеющиеся у полиазациклоалкана, омыляют, гидролизуют.



где n, m, р, q и r, которые могут быть идентичными или разными, равны 2 или 3; R1 является группой, которая может вступать в реакцию полимеризации в условиях радикальной полимеризации; R1 представляет атом водорода или группу (CH2)2-R3, где R3 является группой, выбранной из группы, состоящей из CONH2, СН2ОН, CN и COOR4, R4 представляет Н, катион, например Na, алкильную группу, включающую от 1 до 10 атомов углерода, или бензильную группу; или R2 представляет -(CH2)-R5 группу, где R5 представляет COOR6 или PO3R6, R6 представляет алкильную группу, включающую от 1 до 10 атомов углерода, атом водорода или катион, например Na.

где
- R2 имеет значение как определено по п.4;
- n1 является целым числом от 100 до 3000;
- p1 является целым числом от 10 до 1000.



где n, m, р, q и r, которые могут быть одинаковыми или разными, равны 2 или 3; R2 представляет атом водорода или (CH2)2-R3 группу, R3 является группой, выбранной из группы, состоящей из CONH2, СН2ОН, CN и COOR4, R4 представляет Н, катион, например Na, алкильную группу, включающую от 1 до 10 атомов углерода, или бензильную группу; или R2 представляет -(CH2)-R5 группу, где R5 представляет COOR6 или PO3R6, R6 представляет алкильную группу, включающую от 1 до 10 атомов углерода, атом водорода или катион, например Na.



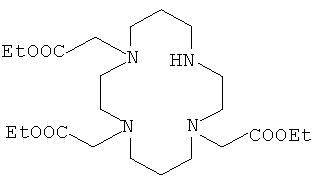


где
- R2 имеет значение как определено по п.4;
- m2 является целым числом от 10 до 1000;
- n2 является целым числом от 10 до 1000;
- р2 является целым числом от 10 до 1000.



где n, m, р, q и r, которые могут быть идентичными или разными, равны 2 или 3; R1 является группой, которая может вступать в реакцию полимеризации в условиях радикальной полимеризации; R2 представляет атом водорода или группу (CH2)2-R3, где R3 является группой, выбранной из группы, состоящей из CONH2, СН2ОН, CN и COOR4, где R4 представляет Н, катион, например Na, алкильную группу, включающую от 1 до 10 атомов углерода, или бензильную группу; или R2 представляет -(CH2)-R5 группу, где R5 представляет COOR6 или PO3R6, R6 представляет алкильную группу, включающую от 1 до 10 атомов углерода, атом водорода или катион, например Na.
а) радикальную полимеризацию одного или более мономеров, которые можно полимеризовать в условиях радикальной полимеризации, проводят в присутствии полипропиленового волокна, несущего пероксидные и/или гидропероксидные функциональные группы, где по меньшей мере один из упомянутых мономеров включает по меньшей мере одну функциональную группу, способную реагировать со свободной функциональной аминогруппой полиазациклоалкана, в результате чего получается полимер, включающий упомянутые функциональные группы, способные реагировать со свободными функциональными аминогруппами полиазациклоалкана, привитый на полипропилен;
б) упомянутый полимер реагирует с полиазациклоалканом;
в) при необходимости свободную функциональную аминогруппу полиазациклоалкана, при необходимости еще присутствующую, подвергают функционализации;
г) при необходимости сложноэфирные функциональные группы, имеющиеся у полиазациклоалкана, омыляют, гидролизуют.



где n, m, р, q и r, которые могут быть одинаковыми или разными, равны 2 или 3; R2 представляет атом водорода или (CH2)2-R3 группу, R3 является группой, выбранной из группы, состоящей из CONH2, СН2ОН, CN и COOR4,
где R4 представляет Н, катион, например Na, алкильную группу, включающую от 1 до 10 атомов углерода, или бензильную группу; или R2 представляет -(CH2)-R5 группу, где R5 представляет COOR6 или PO3R6, где R6 представляет алкильную группу, включающую от 1 до 10 атомов углерода, атом водорода или катион, например Na.




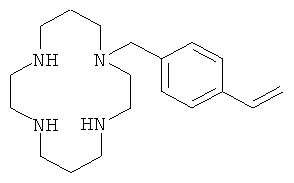










Комментарии