Способ обработки лигноцеллюлозных материалов - RU2709345C2
Код документа: RU2709345C2
Чертежи











Описание
Уровень техники
В настоящее время, растворы сахаров очищают с помощью экстракционных и/или хроматографических технологий или их сочетаний. Хроматографические технологии, хотя они хорошо разработаны, доставляют проблемы с обслуживанием при работе на промышленном уровне. Несколько экстракционных технологий широко используются в качестве ранних стадий очистки, но требуется дополнительная очистка для получения фракций сахаров высокой чистоты (>80%). Такие экстракционные технологии часто осуществляются посредством объединения растворителей, таких как алканолы, и экстрагентов, таких как амины, с хроматографическими технологиями, такими как хроматография с псевдодвижущимся слоем помощью (Simulated Moving Bed, SMB) или с последовательными псевдодвижущимися слоями (Sequential Simulated Moving Bed, SSMB). Иллюстративные подходы описаны в WO2012061085. В настоящем документе предлагаются процедуры, которые упрощают процесс очистки сахара посредством уменьшения необходимости во многих стадиях, используемых при обычных подходах.
Сущность изобретения
Описывается способ генерирования потока рафинированного сахара, который содержит ксилозу, из гидролизного раствора биомассы. Способ включает приведение в контакт гидролизного раствора биомассы, который содержит множество смешанных сахаров, включая олигомерные сахара и мономерные сахара, предпочтительно, ксилозу, кислоту и примеси, с экстрагентом с расслоением фаз при нагреве, например, с простым эфиром этиленгликоля или пропиленгликоля, таким как 2-бутоксиэтанол или 1-пропокси-2-пропанол, или с любым их сочетанием, с формированием экстракционной смеси; и выделение из указанной экстракционной смеси первого потока, который содержит выбранный растворитель или растворители на основе гликоля, кислоту и примеси, и второго потока, потока рафинированного сахара, предпочтительно, потока сахаров, содержащих ксилозу.
Сама экстракционная смесь содержит гидролизный раствор биомассы, который содержит множество смешанных сахаров, включая мономерные и олигомерные сахара, предпочтительно, обогащенные ксилозой, кислоту и примеси, и экстрагент с расслоением фаз при нагреве. В одной из альтернатив, экстрагент с расслоением фаз при нагреве представляет собой простой эфир этиленгликоля или пропиленгликоля, такой как 2-бутоксиэтанол (EB), или 1-пропокси-2-пропанол (PP), или любое их сочетание.
Некоторые из альтернатив, описанных в настоящем документе, относятся к способам генерирования потока рафинированного сахара, который содержит ксилозу, из гидролизного раствора биомассы. Некоторые подходы включают стадии: (i) приведения в контакт гидролизного раствора биомассы, которая содержит множество смешанных сахаров, содержащих ксилозу, кислоту, например, HCl или H2SO4, и примеси, с растворителем с расслоением фаз при нагреве, например, с простым эфиром этиленгликоля или пропиленгликоля, таким как 2-бутоксиэтанол, или 1-пропокси-2-пропанол, или любое их сочетание, для того, чтобы сформировать экстракционную смесь; и (ii) выделения из указанной экстракционной смеси первого потока, содержащего растворитель с расслоением фаз при нагреве, кислоту и примеси, и второго потока, потока рафинированного сахара, который содержит ксилозу. В некоторых альтернативах, способ включает приведение в контакт потока указанного гидролизного раствора биомассы, который содержит указанное множество смешанных сахаров, содержащих ксилозу, с сильнокислотной катионообменной смолой, предпочтительно, перед стадией (i). В некоторых альтернативах, способ включает приведение в контакт потока из указанного гидролизного раствора биомассы, который содержит указанное множество смешанных сахаров, содержащих ксилозу, со слабо основной анионообменной смолой, предпочтительно, после того как указанный поток приводится в контакт с указанной сильнокислотной катионообменной смолой и перед стадией (i). В некоторых альтернативах, способ включает нагрев указанной экстракционной смеси до температуры от 30 до 100°C. В некоторых альтернативах, способ дополнительно включает выделение указанного второго потока, потока рафинированного сахара, который содержит ксилозу, посредством хроматографии SSMB или SMB. В некоторых альтернативах, способ дополнительно включает выделение, выпаривание, очистку или концентрирование ксилозы из потока рафинированного сахара, который содержит ксилозу. В некоторых альтернативах, ксилоза, полученная с помощью этих процедур, имеет чистоту 75%-96%, например, 80%-96%.
Экстракционная смесь также представляет собой один из аспектов настоящего изобретения. Экстракционная смесь содержит гидролизный раствор биомассы, который содержит множество смешанных сахаров, содержащих ксилозу, кислоту и примеси; и растворитель с расслоением фаз при нагреве, например, простой эфир этиленгликоля или пропиленгликоля, такой как 2-бутоксиэтанол (EB) или 1-пропокси-2-пропанол (PP), или любое их сочетание. В некоторых альтернативах, экстракционная смесь также содержит алканол, такой как гексанол или 2-этилгексанол, с аминовым экстрагентом, таким как трилауриламин (TLA), в гексаноле, или без него.
Краткое описание чертежей
Фиг.1 иллюстрирует схему разделения или очистки потока сахаров, обогащенного мономерными сахарами, предпочтительно, ксилозой.
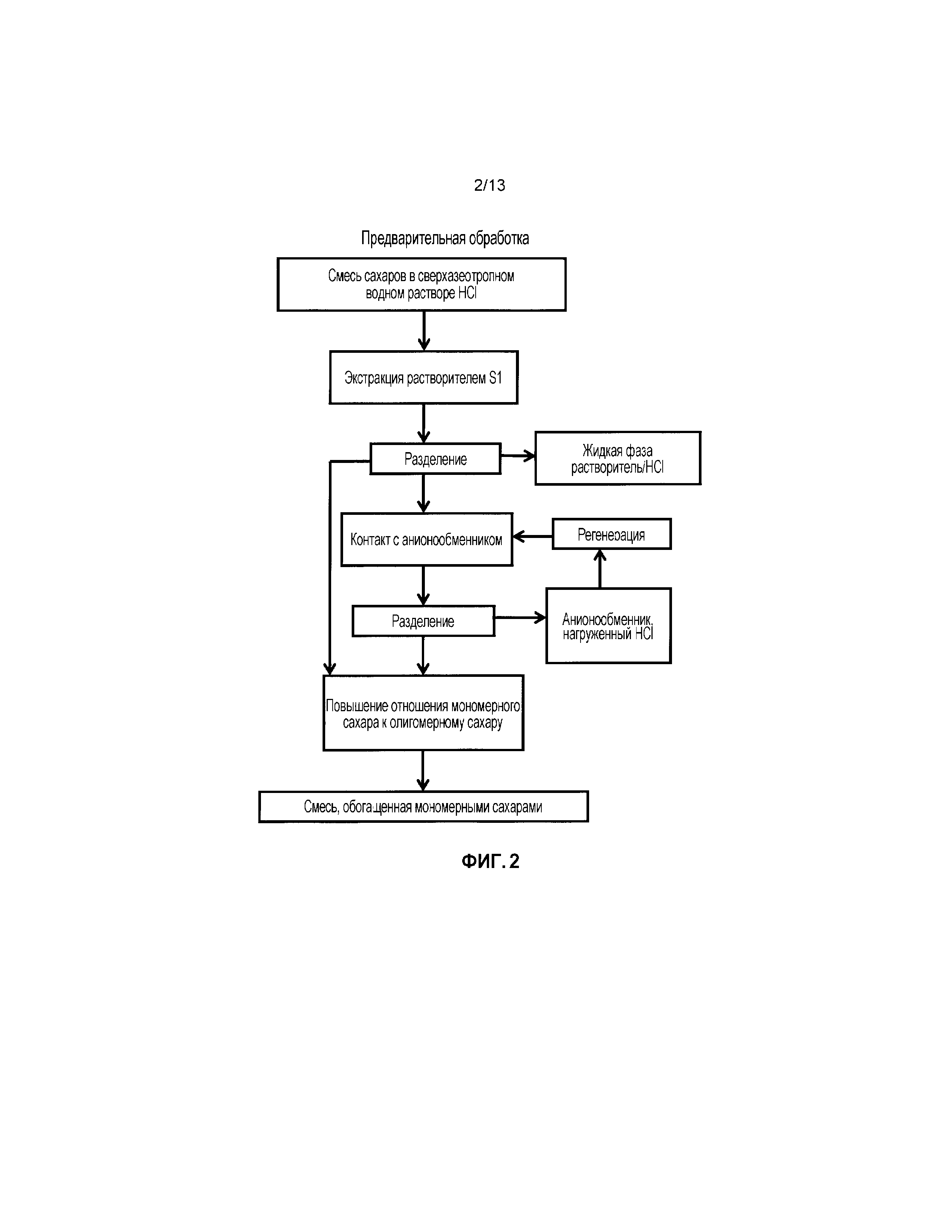
Фиг.2 иллюстрирует подходспредварительной обработкой гидролизного раствора биомассы с получением смеси, обогащенной мономерными сахарами, предпочтительно, содержащей ксилозу.
Фиг.3 иллюстрирует подход с предварительной обработкой гидролизного раствора биомассы с получением фракции олигомерных сахаров и смеси, обогащенной мономерными сахарами, предпочтительно, содержащей ксилозу, где фракция олигомерных сахаров подвергается воздействию дополнительного кислотного гидролиза и рециклируется посредством анионообменного разделения с получением дополнительных смесей, обогащенных мономерными сахарами, которые предпочтительно содержат ксилозу.
Фиг.4 иллюстрирует подход предварительной обработки гидролизного раствора биомассы с получением фракции олигомерных сахаров и смеси, обогащенной мономерными сахарами, предпочтительно, содержащей ксилозу, где фракция олигомерных сахаров подвергается воздействию дополнительного кислотного гидролиза и рециклируется посредством анионобменного разделения с получением дополнительных смесей, обогащенных мономерными сахарами, которые предпочтительно содержат ксилозу.
Фиг.5 иллюстрирует блок-схему способа экстракции, где содержание мономерных сахаров, предпочтительно, содержащих ксилозу, обогащается посредством экстракции и выделения в органическую фазу, содержащую экстракционный растворитель с расслоением фаз при нагреве, предпочтительно, 2-бутоксиэтанол (EB) или 1-пропокси-2-пропанол (PP), и содержание мономерных сахаров, предпочтительно, содержащих ксилозу, обогащается, они выделяются или изолируются из органической фазы посредством нагрева (30°C-100°C). После обогащения, выделение, очистка и/или кристаллизация желаемого мономерного сахара, предпочтительно, ксилозы, может осуществляться посредством выпаривания с получением, например, ксилозы с чистотой от 75% до 96%, например, от 80% до 96%.
Фиг.6 представляет собой хроматограмму водной фазы, полученной после экстракции EB.
Фиг.7 представляет собой хроматограмму водной фазы, полученной после экстракции PP.
Фиг.8 представляет собой спектр ЯМР коммерческого EB в CDCl3.
Фиг.9 представляет собой спектр ЯМР рециклированного и дистиллированного EB в CDCl3.
Фиг.10 представляет собой спектр ЯМР коммерческого PP в CDCl3.
Фиг.11 представляет собой спектр ЯМР рециклированного и дистиллированного EB в CDCl3.
Фиг.12 представляет собой хроматограмму смеси до гидролиза после экстракции EB с использованием рециклированного растворителя.
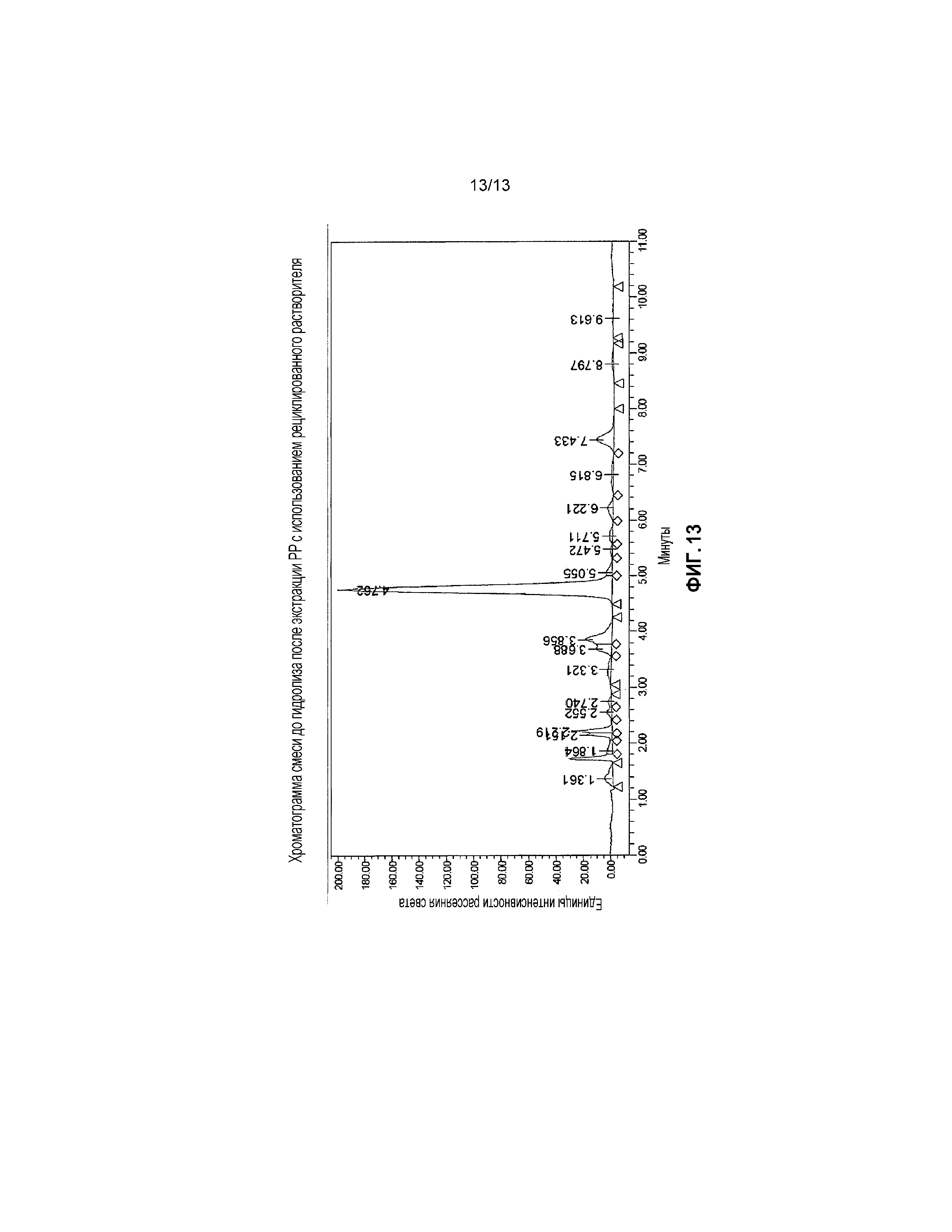
Фиг.13 представляет собой хроматограмму смеси до гидролиза после экстракции PP с использованием рециклированного растворителя.
Подробное описание предпочтительного варианта осуществления
Аспекты настоящего изобретения относятся к переработке и рафинированию лигноцеллюлозной биомассы с получением гемицеллюлозных сахаров, целлюлозных сахаров, мономерных сахаров, предпочтительно, ксилозы, лигнина, целлюлозы и других ценных продуктов. В некоторых альтернативах, описаны способы генерирования потокарафинированного мономерного сахара, который содержит ксилозу, из гидролизного раствора биомассы. Эти способы включают приведение в контакт гидролизного раствора биомассы, который содержит множество олигомерных сахаров и мономерных сахаров, предпочтительно, ксилозу, кислоту и примеси, с экстрагентом с расслоением фаз при нагреве, например, простым эфиром этиленгликоля или пропиленгликоля, таким как 2-бутоксиэтанол или 1-пропокси-2-пропанол, или любое их сочетание, с формированием экстракционной смеси; и выделение из указанной экстракционной смеси первого потока, который содержит выбранный растворитель или растворители на основе гликоля, кислоту и примеси, и второго потока, потока рафинированных или обогащенных сахаров, который содержит олигомерные и/или мономерные сахара, предпочтительно, ксилозу. Второй поток рафинированных или обогащенных сахаров, содержащий олигомерные и/или мономерные сахара, предпочтительно, ксилозу, и экстрагент с расслоением фаз при нагреве, например, простой эфир этиленгликоля или пропиленгликоля, такой как 2-бутоксиэтанол, или 1-пропокси-2-пропанол, или любое их сочетание, может дополнительно разделяться, обогащаться, выделяться и/или очищаться посредством воздействия на второй поток нагрева (например, 30°C-100°C), с последующим выделением, обогащением и/или очисткой олигомерных сахаров и мономерных сахаров, предпочтительно, ксилозы, посредством хроматографии (например, хроматографии SMB и/или SSMB), концентрирования и/или выпаривания.
Желательно, чтобы аспекты настоящего изобретения, описанные в настоящем документе, делали возможным выделение потока сахаров, которые обогащены мономерными и/или олигомерными сахарами, такого как поток сахаров, обогащенный ксилозой, после одной единственной экстракции гидролизного раствора биомассы, например, экстрагентом с расслоением фаз при нагреве, таким как простой эфир этиленгликоля или пропиленгликоля, например, 2-бутоксиэтанол или 1-пропокси-2-пропанол, или любое их сочетание. После того как гидролизный раствор биомассы приводится в контакт с экстрагентом с расслоением фаз при нагреве, нагрев, например, при 30°C-100°C, делает возможным выделение потока сахаров, которые обогащены мономерными и/или олигомерными сахарами, такого как поток сахаров, обогащенных ксилозой, и такое обогащение или выделение сахаров может осуществляться в отсутствие хроматографических процедур, которые обычно необходимы для обогащения потока сахаров мономерными и/или олигомерными сахарами, такими как ксилоза. Неожиданно обнаружено, что класс растворителей, который не замечался ранее в отношении экстракции сахаров, очень эффективно отделяет мономерные и/или олигомерные сахара, такие как ксилоза, от кислоты, используемой при гидролитической переработке лигноцеллюлозной биомассы, а также, от примесей, генерируемых в способе, без необходимости в использовании хроматографических стадий, что значительно понижает затраты на обогащение и очистку сахаров в промышленном масштабе.
Экстракционные смеси, описанные в настоящем документе, также представляют собой аспекты настоящего изобретения. Такие экстракционные смеси содержат гидролизный раствор биомассы, который содержит олигомерные и/или мономерные сахара, предпочтительно, ксилозу, кислоту, примеси и экстрагент с расслоением фаз при нагреве, например, простой эфир этиленгликоля или пропиленгликоля, такие как 2-бутоксиэтанол, или 1-пропокси-2-пропанол, или их любое сочетание.
Способы переработки и рафинирования лигноцеллюлозной биомассы, описанные в настоящем документе, включают: (1) предварительное кондиционирование лигноцеллюлозной биомассы с последующим гидролизом и переработкой после гидролиза (например, хроматографическим разделением, таким как анионный обмен, например, слабо основной анионный обмен и/или катионный обмен, такой как сильнокислотный катионный обмен); (2) экстракцию с расслоением фаз при нагреве (например, с использованием простого эфира этиленгликоля или пропиленгликоля, такого как 2-бутоксиэтанол или 1-пропокси-2-пропанол, или любого их сочетания); и (3) выделение, рафинирование, обогащение или очистку фракций, содержащих обогащенные олигомерные и/или мономерные сахара, предпочтительно, ксилозу, например, с помощью хроматографии SMB или SSMB, предпочтительно, с последующим выпариванием. Раздел, ниже, описывает более подробно предварительное кондиционирование лигноцеллюлозной биомассы с последующим гидролизом и переработкой после гидролиза.
Предварительное кондиционирование лигноцеллюлозной биомассы, гидролиз и переработка после гидролиза
Лигноцеллюлозная биомасса, такая как багасса, представляет собой желательный исходный материал для очистки сахаров. Переработка и рафинирование лигноцеллюлозной биомассы начинается с кондиционирования лигноцеллюлозной биомассы, при этом биомассу окоривают, рубят на щепу, превращают в стружку, сушат и/или измельчают до частиц для того, чтобы генерировать кондиционированный препарат лигноцеллюлозы. Затем кондиционированную лигноцеллюлозную биомассу гидролизуют с помощью органической и/или минеральной кислоты, предпочтительно, при низких концентрациях, при нагреве и, необязательно, под давлением, для того, чтобы получить кислотный поток гемицеллюлозного сахара и поток лигноцеллюлозного остатка. Лигноцеллюлозный остаток содержит в основном целлюлозу и лигнин. В некоторых способах, лигноцеллюлозный остаток дополнительно перерабатывается с получением биоэнергетических гранул, которые могут сжигаться в качестве топлив. В некоторых способах, лигноцеллюлозный остаток может непосредственно перерабатываться для извлечения лигнина и/или может дополнительно гидролизоваться и перерабатываться с использованием способов, описанных в настоящем документе, например, для генерирования улучшенных выходов олигомерных и мономерных сахаров, таких как ксилоза. Этот способ производит лигнин высокой чистоты и целлюлозу высокой чистоты. Способ очистки лигнина, рассматриваемый в настоящем документе, может использовать растворитель с ограниченной растворимостью, предпочтительно алканол, такой как метилэтилкетон (MEK), и может давать лигнин, имеющий чистоту больше чем 99%.
Перед гидролизом лигноцеллюлозы и экстракцией гемицеллюлозного сахара, лигноцеллюлозная биомасса предпочтительно предварительно кондиционируется для того, чтобы усилить гидролиз. Предварительное кондиционирование в этом контексте относится к уменьшению размеров биомассы и разрушению ее структуры (например, к механическому разрушению, с выпариванием или без него), которое не влияет существенно на композиции лигнина, целлюлозы и гемицеллюлозы биомассы. Предварительное кондиционирование, таким образом, облегчает более эффективную и экономичную переработку в следующем далее способе (например, при гидролизе и экстракции гемицеллюлозного сахара). Предпочтительно, лигноцеллюлозную биомассу окоривают, рубят на щепу, превращают в стружку и/или сушат с получением предварительно кондиционированной лигноцеллюлозной биомассы (упоминается также как кондиционированный препарат лигноцеллюлозы). Предварительное кондиционирование лигноцеллюлозной биомассы может также использовать, например, ультразвуковую энергию или гидротермическую обработку, включая воду, тепло, водяной пар или водяной пар высокого давления. Предварительное кондиционирование может осуществляться или использоваться в различных типах контейнеров, реакторов, труб, проточных ячеек, и тому подобное. В некоторых способах, предпочтительно иметь лигноцеллюлозную биомассу, предварительно кондиционированную перед гидролизом и экстракцией гемицеллюлозного сахара и разделением олигомерных и мономерных сахаров. В некоторых способах, в зависимости от исходных материалов биомассы, предварительного кондиционирования не требуется, например, лигноцеллюлозная биомасса, такая как потоки, содержащие высвобожденные олигомерные сахара и/или гемицеллюлозу, может непосредственно отправляться на стадию гидролиза.
Необязательно, лигноцеллюлозная биомасса может перемалываться или измельчаться для уменьшения размеров частиц. В некоторых вариантах осуществления, лигноцеллюлозная биомасса измельчается таким образом, что средний размер частиц находится в пределах от 100 до 10000 микрон, предпочтительно, от 400 до 5000, например, от 100 до 400, от 400 до 1000, от 1000 до 3000, от 3000 до 5000 или от 5000 до 10000 микрон, или до размера в пределах, определяемых любыми двумя размерами из тех, которые рассмотрены выше. В некоторых вариантах осуществления, лигноцеллюлозная биомасса измельчается таким образом, что средний размер частиц меньше чем 10000, 9000, 8000, 7000, 6000, 5000, 4000, 3000, 1000, или 400 микрон, или он находится в пределах, определяемых любыми двумя размерами из тех, которые рассмотрены выше. По сравнению с неизмельченными частицами, такими как стружка, измельченные частицы могут суспендироваться в гидролизной жидкости, и они могут легко циркулировать от контейнера до контейнера. Измельченные частицы из различных материалов лигноцеллюлозной биомассы могут перерабатываться на одном и том же наборе оборудования с использованием сходных или одинаковых рабочих параметров. Уменьшение размеров частиц может значительно ускорить процесс гидролиза целлюлозы.
Для гидролиза целлюлозы можно использовать любые способы и/или системы гидролиза, включая ферментативные средства и/или химические способы. Например, можно использовать любую из процедур из описанных в WO2012061085 (включаемой в явном виде в настоящий документ в качестве ссылки во всей своей полноте). В одной из альтернатив, гидролиз и высвобождение целлюлозных сахаров осуществляется с использованием системы гидролиза в танке с перемешиванием. Эта противоточная система является желательной для кислотного гидролиза целлюлозных сахаров. Когда используется множество танков, система делает возможным отдельный контроль температуры для каждого индивидуального танка. Система может адаптироваться для различных материалов лигноцеллюлозной биомассы. После предварительного кондиционирования лигноцеллюлозной биомассы для того, чтобы получить кондиционированный лигноцеллюлозный препарат, кондиционированный лигноцеллюлозный препарат подвергается воздействию кислотного гидролиза, например, с помощью HCl или H2SO4,для того, чтобы генерировать гидролизную смесь биомассы (например, кислотный поток гемицеллюлозного сахара) и поток лигноцеллюлозного остатка. В некоторых альтернативах, способ использует аутогидролиз, где кондиционированный препарат лигноцеллюлозы или смешанный препарат сахаров подвергается воздействию гидролиза без добавления экзогенной кислоты (например, кондиционированный препарат лигноцеллюлозы или смешанный препарат сахаров гидролизуется с помощью кислоты, уже присутствующей в препарате, и дополнительная органическая и/или неорганическая кислота, экзогенно добавляемая кислота, не предусматривается). С помощью некоторых подходов, кислота, необходимая для гидролиза, присутствует в кондиционированном лигноцеллюлозном препарате, и в кондиционированный лигноцеллюлозный препарат дополнительную кислоты не добавляют. В некоторых вариантах осуществления, кислотный гидролиз осуществляют под давлением и/или при нагреве, например, с помощью варки под давлением. После гидролиза, поток лигноцеллюлозного остатка может отделяться от кислотного потока гемицеллюлозных сахаров с помощью нескольких подходов, включая фильтрование, центрифугирование или седиментацию, с формированием потока жидкости и потока твердых продуктов. Кислотный поток гемицеллюлозных сахаров содержит гемицеллюлозные сахара и примеси. Поток лигноцеллюлозного остатка в основном содержит целлюлозу и лигнин. Поток лигноцеллюлозного остатка может подвергаться воздействию других сеансов предварительного кондиционирования (например, измельчения) и/или гидролиза.
Поток лигноцеллюлозного остатка может также промываться для извлечения дополнительных гемицеллюлозных сахаров и кислотного катализатора, захваченного в порах биомассы. После извлечения, этот раствор может рециклироваться обратно в кислотный поток гемицеллюлозных сахаров или рециклироваться обратно для осуществления дополнительного гидролиза. Поток лигноцеллюлозного остатка может механически прессоваться для увеличения содержания твердых продуктов (например, до содержания сухих твердых продуктов 40-60%). Фильтрат со стадии прессования также может рециклироваться обратно в кислотный поток гемицеллюлозных сахаров или рециклироваться обратно для осуществления дополнительного кислотного гидролиза. Необязательно, оставшийся лигноцеллюлозный остаток измельчается для уменьшения размеров частиц. Необязательно, прессованный лигноцеллюлозный остаток сушится для уменьшения содержания влажности, например, до меньшего, чем 15%. Высушенное вещество может дополнительно гидролизоваться для извлечения лигнина и целлюлозных сахаров, как приведено выше. Альтернативно, высушенное вещество может гранулироваться в виде гранул, которые могут сжигаться в качестве источника энергии для получения тепла и электричества или могут использоваться в качестве исходных материалов для преобразования в бионефть.
Предпочтительно, для гидролиза лигноцеллюлозной биомассы используют кислый водный раствор. Кислый водный раствор может содержать любые кислоты, неорганические или органические. Предпочтительно, используется неорганическая кислота. Например, раствор может представлять собой кислотный водный раствор, содержащий неорганическую или органическую кислоту, такую как H2SO4, H2SO3 (которая может вводиться как растворенная кислота или как газообразный SO2), HCl и/или уксусная кислота. Кислотный водный раствор может содержать кислоту в количестве от 0 до 2% кислоты или больше, например, 0-0,2%, 0,2-0,4%, 0,4-0,6%, 0,6-0,8%, 0,8-1,0%, 1,0-1,2%, 1,2-1,4%, 1,4-1,6%, 1,6-1,8%, 1,8-2,0% или более масс/масс, или в количестве в пределах, определяемых любыми двумя количествами из тех, которые рассмотрены выше. Предпочтительно, водный раствор для экстракции содержит 0,2-0,7% H2SO4 и 0-3000 м.д. SO2. pH кислотного водного раствора может находиться, например, в пределах от 1 до 5, предпочтительно, от 1 до 3,5, например, представлять собой pH 1, 2, 3, 4, или 5 или находиться в пределах, определяемых любыми двумя значениями pH из тех, которые рассмотрены выше.
В некоторых вариантах осуществления, при гидролизе используется повышенная температура или давление. Например, можно использовать температуру в пределах от 100 до 200°C или большую, чем 50°C, 60°C, 70°C, 80°C, 90°C, 100°C, 110°C, 120°C, 130°C, 140°C, 150°C, 160°C, 170°C, 180°C, 190°C, или 200°C, или температуру в пределах, определяемых любыми двумя температурами из тех, которые рассмотрены выше. Предпочтительно, температура находится в пределах 110-160°C или 120-150°C. Давление может находиться в пределах от 1 до 10 МПа, предпочтительно, от 1 до 5 МПа, например 1, 2, 3, 4, 5, 6, 7, 8, 9, или 10 МПа, или в пределах, определяемых любыми двумя давлениями из тех, которые рассмотрены выше. Раствор может нагреваться в течение 0,5-5 часов, предпочтительно, 0,5-3 часов, 0,5-1 часа, 1-2 часов или 2-3 часов, или в течение времени в пределах, определяемых любыми двумя временами из тех, которые рассмотрены выше, необязательно, с периодом охлаждения один час.
В некоторых альтернативах, кондиционированный лигноцеллюлозный препарат и/или поток лигноцеллюлозного остатка после первого сеанса гидролиза подвергается дополнительному гидролизу целлюлозы для получения потока кислотного гидролизата и потока кислотного лигнина, следующим образом. Лигноцеллюлозный поток (например, поток кондиционированного лигноцеллюлозного препарата или лигноцеллюлозного остатка) доводится до содержания влажности от 5 до 85% масс/масс (например, посредством сушки), а затем полученный в результате продукт перемалывается или измельчается до размера частиц от 400 до 5000 микрон (предпочтительно, -1400 микрон) с помощью любой промышленной мельницы, включая молотковую мельницу или игольчатую мельницу. Если содержание влажности выше, чем 15%, измельченный лигноцеллюлозный остаток сушится до получения влажности <15%. Система гидролиза содержит танки с перемешиванием в количестве n (например, n=1-9, предпочтительно, 4), соединенные последовательно. Водная жидкость в танке, содержащая кислоту, растворенный сахар и суспендированную биомассу, рециклируется с помощью насоса высокого давления с высокой скоростью потока, осуществляющего перемешивание раствора в каждом танке. Проточная линия также соединена с разделительным устройством твердый продукт/жидкость (например, с фильтром, мембраной, центрифугой или гидроциклоном), через которые может проникать, по меньшей мере, некоторое количество жидкости и растворенных молекул, например, кислоты и сахаров, с получением при этом потокапермеата (или фильтрата). По меньшей мере, некоторая часть поступающей жидкости удерживается разделительным устройством твердый продукт/жидкость с получением потокаретентата.
В некоторых альтернативах, в танк n вводится сверхазеотропный раствор HCl с концентрацией кислоты, по меньшей мере, 41%. Пермеат разделительного узла танка n вводится в реактор n-1, при этом, по меньшей мере, часть ретентата рециклируется обратно в танк n. Пермеат из танка n-1 вводится в танк n-2, в то время как ретентат рециклируется обратно в танк n-1, и так далее. Пермеат, покидающий танк 1 из этого ряда, представляет собой поток кислотного гидролизата. Концентрация твердых продуктов в каждом реакторном танке с перемешиванием может поддерживаться в пределах 3-15%, 3-5%, 5-10%, или 10-15% масс/масс или в пределах, определяемых любыми двумя значениями из тех, которые рассмотрены выше. В целом, биомасса удерживается в системе в течение 10-48 часов. Температура каждого реактора контролируется отдельно в пределах от 5 до 40°C.
В некоторых альтернативах, поток измельченного, кондиционированного лигноцеллюлозного препарата или измельченного лигноцеллюлозного остатка добавляется в первую ступень ряда реакторных танков с перемешиванием (например, из 1-9 реакторов, предпочтительно, из 4 реакторов). Суспензия перемешивается посредством взбалтывания или рециркуляции жидкости в реакторах. По меньшей мере, часть ретентата из танка 1 вводится в танк 2; по меньшей мере, часть ретентата из танка 2 вводится в танк 3, и так далее. В конечном счете, поток кислотного лигнина покидает танк n в систему промывки лигнина.
В некоторых вариантах осуществления, в последний реактор ряда добавляется концентрированная хлористоводородная кислота (>35%, 36%, 37%, 38%, 39%, 40%, 41% или, предпочтительно, 42%, или процент в пределах, определяемых любыми двумя процентами из тех, которые рассмотрены выше), и менее концентрированная хлористоводородная кислота (~25%, 26%, 27%, 28%, 29%, 30%, или предпочтительно, 31%) выходит из первого реактора в этом ряду. В некоторых вариантах осуществления, гидролизованные сахара выходят из первого реактора в этом ряду.
Поток кислотного гидролизата, содержащий кислоту и целлюлозные сахара, переносится из последнего реактора во второй - последний реактор, и так далее, до тех пор, пока гидролизат не покинет первый реактор для дополнительной очистки. В иллюстративной системе реакторов, гидролизат, покидающий первый реактор, содержит в пределах 8-16% сахаров и хлористоводородную кислоту. В некоторых вариантах осуществления, поток кислотного гидролизата может содержать более чем 8%, 9%, 10%, 11%, 12%, 13%, 14% или процент в пределах, определяемых любыми двумя процентами растворенных сахаров из тех, которые рассмотрены выше. В некоторых вариантах осуществления, поток кислотного гидролизата может содержать более чем 22%, 24%, 26%, 28%, 30%, 32% 34%, 36%, или процент в пределах, определяемых любыми двумя процентами растворенных сахаров HCl из тех, которые рассмотрены выше. В некоторых вариантах осуществления, поток кислотного гидролизата может содержать меньше чем 32%, 30%, 28%, 26%, 24%, 22%, или 20%, или процент в пределах, определяемых любыми двумя процентами HCl из тех, которые рассмотрены выше.
Температура во всех реакторах предпочтительно поддерживается в пределах 5-80°C, например, 15-60°C, предпочтительно 10-40°C, или как температура в пределах, определяемых любыми двумя температурами из тех, которые рассмотрены выше. Общее время удерживания биомассы во всех реакторах может находиться в пределах от 1 до 5 дней, например, от 1 до 3 дней, предпочтительно, от 10 до 48 часов, или представлять собой отрезок времени в пределах, определяемых любыми двумя отрезками времени из тех, которые рассмотрены выше.
Предпочтительно, когда используется множество реакторных танков с перемешиванием, по меньшей мере, часть потока водного раствора кислотного гидролизата, покидающего промежуточный реактор (например, реактор 2 или 3), смешивается с потоком кондиционированного, лигноцеллюлозного препарата или измельченного лигноцеллюлозного остатка перед тем, как поток вводится в первый реактор. Поток может предварительно гидролизоваться с помощью потока водного раствора кислотного гидролизата из промежуточного реактора перед тем, как он приводится в контакт с сильной кислотой в первом реакторе. Предпочтительно, смесь до гидролиза нагревается до температуры в пределах от 15 до 60°C, предпочтительно, от 25 до 40°C, наиболее предпочтительно, до 40°C или до температуры в пределах, определяемых любыми двумя температурами из тех, которые рассмотрены выше, в течение от 5 минут до 1 дня, предпочтительно, от 15 до 20 минут, или в течение отрезка времени в пределах, определяемых любыми двумя отрезками времени из тех, которые рассмотрены выше.
В некоторых вариантах осуществления, гидролиз олигомерных сахаров в смешанном потоке сахаров осуществляется при температуре больше чем 60°C, необязательно, в пределах между 70°C и 130°C, необязательно, в пределах между 80°C и 120°C и необязательно, в пределах между 90°C и 110°C, или при температуре в пределах, определяемых любыми двумя температурами из тех, которые рассмотрены выше. В некоторых вариантах осуществления, гидролиз осуществляется, по меньшей мере, 10 минут, необязательно, в пределах между 20 минутами и 6 часами, необязательно, между 30 минутами и 4 часами и необязательно, между 45 минутами и 3 часами, или в течение отрезка времени в пределах, определяемых любыми двумя отрезками времени из тех, которые рассмотрены выше.
Можно использовать систему, которая включает установку вторичного гидролиза, адаптированную для приема входного потока, который содержит смесь сахаров в сверхазеотропном водном растворе HCl. Установка вторичного гидролиза может также адаптироваться для увеличения отношения мономерных сахаров к олигомерным сахарам в выходном потоке. В некоторых вариантах осуществления, вторичный гидролиз при рассмотренных выше условиях увеличивает выход мономерных сахаров с небольшой деградацией сахаров или без нее. В некоторых вариантах осуществления, мономеры как доля от сахаров в целом составляют больше чем 70%, необязательно, больше, чем 80%, необязательно, больше, чем 85% и необязательно, больше, чем 90%, или составляют процент в пределах, определяемых любыми двумя процентами массовыми после гидролиза из тех, которые рассмотрены выше. В некоторых вариантах осуществления, деградация мономерных сахаров во время гидролиза меньше чем 1%, необязательно, меньше, чем 0,2%, необязательно, меньше, чем 0,1% и необязательно, меньше, чем 0,05%, или составляет процент в пределах, определяемых любыми двумя процентами массовыми из тех, которые рассмотрены выше.
В некоторых вариантах осуществления, этот вторичный гидролиз продолжается в течение, по меньшей мере, 1, по меньшей мере, 2 или, по меньшей мере, 3 часов или в течение отрезка времени в пределах, определяемых любыми двумя отрезками времени из тех, которые рассмотрены выше. Необязательно, этот вторичный гидролиз продолжается в течение 1-3 часов, необязательно, примерно 2 часов. В некоторых вариантах осуществления, температура поддерживается ниже 150, 140, 130, 120, 110, 100 или ниже 90°C или представляет собой температуру в пределах, определяемых любыми двумя температурами из тех, которые рассмотрены выше. В некоторых вариантах осуществления, температура поддерживается в пределах между 60°C и 150°C, между 70°C и 140°C или между 80°C и 130°C, или температура находится в пределах, определяемых любыми двумя температурами из тех, которые рассмотрены выше. В некоторых вариантах осуществления, вторичный гидролиз дает в результате пропорцию мономерных сахаров от 80 до 90%, необязательно, от 85 до 88%, необязательно, примерно 86% от сахаров в целом, или представляет собой процент в пределах, определяемых любыми двумя процентами из тех, которые рассмотрены выше. В некоторых вариантах осуществления, вторичный гидролиз дает в результате пропорцию мономерных сахаров, по меньшей мере, 72%, 74%, 76%, 78%, 80%, 82%, 84%, 86%, 88% или даже, по меньшей мере, 90% масс/масс сахара в целом, или процент в пределах, определяемых любыми двумя процентами из тех, которые рассмотрены выше. В некоторых вариантах осуществления, полученный в результате вторичный гидролизат содержит, по меньшей мере, 20%, 22, 24%, 26%, 28%, 30%, 32%, 34%, 36%, 38%, 40%, 42%, 44%, 46%, 48% или 50% сахаров в целом, или содержит их процент в пределах, определяемых любыми двумя процентами масс/масс сахаров в целом из тех, которые рассмотрены выше.
В некоторых вариантах осуществления, гидролизный реактор (реакторы) работает при 95, 100, 105, 110, 115, 120 или 125°C или при температуре в пределах, определяемых любыми температурами двумя из тех, которые рассмотрены выше. В некоторых вариантах осуществления, гидролизный реактор (реакторы) работает при давлении 1,8, 1,9, 2,0, 2,1 или 2,2 бар, или при давлении в пределах, определяемых любыми двумя давлениями из рассмотренных выше. В некоторых вариантах осуществления, реакция гидролиза продолжается в течение 1-3 часов, 1,5-2,5 часов или 1,7-2 часов, или в течение времени в пределах, определяемых любыми двумя отрезками времени из тех, которые рассмотрены выше. В некоторых вариантах осуществления, реакция гидролиза осуществляется при 95°C в течение примерно 2 часов при атмосферном давлении. В других иллюстративных вариантах осуществления, реакция гидролиза осуществляется при 125°C в течение примерно 1,7 часа примерно при 2 бар.
В одном из примеров, гидролизуется кондиционированный эвкалипт с использованием реакторных танков с перемешиванием. При начальном введении кондиционированной древесины эвкалипта в кислоту, вязкость сначала возрастает в результате быстрого растворения олигомеров целлюлозных сахаров, высокая вязкость ухудшает возможности для прокачки и рециркулирования водного раствора через систему; короткое перемешивание потока измельченного, кондиционированного лигноцеллюлозного препарата или измельченного лигноцеллюлозного остатка вместе с гидролизатом из промежуточного реактора при повышенной температуре ускоряет дальнейший гидролиз растворенных олигомеров до мономеров, сопровождаемый уменьшением вязкости. В другом примере, кондиционированный эвкалипт сначала вступает в контакт с раствором кислоты, поступающим из ступени 2 (например, при концентрации ~33%), при 35-50°C, в течение 15-20 минут. Предварительно гидролизованный кондиционированный эвкалипт можно вводить в систему гораздо быстрее, и он дополнительно гидролизуется в реакторных танках с перемешиванием. Реакторные танки с перемешиванием могут использоваться сходным образом для различных источников биомассы, включая древесину твердых пород, древесину мягких пород и багассу. После гидролиза целлюлозы, оставшиеся остатки в лигноцеллюлозной биомассе формируют поток кислотного лигнина. Поток кислотного гидролизата, получаемого посредством гидролиза целлюлозы, может дополнительно рафинироваться, как описано ниже.
Кислотный поток гемицеллюлозного сахара может дополнительно рафинироваться перед экстракцией сахара и очисткой с использованием хроматографических процедур и/или процедур выпаривания. Кислотный поток гемицеллюлозного сахара предпочтительно нейтрализуется или кислота удаляется из потока гемицеллюлозного сахара, и/или поток гемицеллюлозного сахара отделяется, рафинируется или обогащается посредством приведения его в контакт с ионообменной смолой, например, с помощью ионообменной хроматографии, предпочтительно, посредством приведения в контакт с сильнокислотной обменной смолой или посредством хроматографии на этой смоле и с необязательным последующим контактом со слабо основной анионообменной смолой или посредством хроматографии на этой смоле, например, хроматографии с такой смолой в качестве неподвижной фазы. Поток нейтрализованного гемицеллюлозного сахара может, необязательно, выпариваться с формированием более концентрированной смеси гемицеллюлозных сахаров. Необязательно, поток гемицеллюлозных сахаров дополнительно рафинируется посредством приведения в контакт с гранулированным активированным углем до или после выпаривания.
В некоторых альтернативах, обедненный кислотой поток гемицеллюлозных сахаров может рафинироваться с использованием дистилляционной колонны с насадкой. Процесс дистилляции может удалять, по меньшей мере, 70%, 80%, 90%, или 95% разбавителя, или количество разбавителя в пределах, определяемых любыми двумя значениями из тех, которые рассмотрены выше, в обедненном кислотой потоке гемицеллюлозных сахаров. С дистилляцией разбавителя или без нее, обедненный кислотой поток гемицеллюлозных сахаров может вступать в контакт с сильнокислотной катионообменной смолой (SAC), например, посредством хроматографии, для того, чтобы удалить любые оставшиеся металлические катионы. Предпочтительно, обедненный кислотой поток гемицеллюлозных сахаров очищается с использованием дистилляционной колонны с набивкой с последующей хроматографией на сильнокислотной катионообменной смоле (SAC). В некоторых аспектах, поток гемицеллюлозных сахаров приводится в контакт со слабо основной анионообменной смолой (WBA), например, посредством хроматографии, для того, чтобы удалить избыточные протоны. Нейтрализованный поток гемицеллюлозных сахаров может подвергаться регулировке pH и выпариваться до 25-65%, а предпочтительно, до 30-40% масс/масс растворенных сахаров в любом обычном испарителе, например, в многоступенчатом испарителе или испарителе с механической рекомпрессией паров (MVR).
В некоторых альтернативах, обедненный кислотой поток гемицеллюлозных сахаров приводится в контакт с сильнокислотной катионообменной смолой (SAC), например, с помощью хроматографии, для того, чтобы удалить любые оставшиеся металлические катионы, предпочтительно, с последующим приведением в контакт со слабо основной анионообменной смолой (WBA), например, с помощью хроматографии, для того, чтобы удалить избыточные протоны. Нейтрализованный гидролизат может подвергаться регулировке pH и выпариваться до 25-65%, а предпочтительно, до 30-40% масс/масс растворенных сахаров в любом обычном испарителе, например, в многоступенчатом испарителе или в испарителе с механической рекомпрессией паров (MVR). Необязательно, концентрированный раствор сахаров может приводиться в контакт с активированным углем для удаления оставшихся органических примесей. Концентрированный раствор сахаров может также приводиться в контакт с системой со смешанным слоем смолы для того, чтобы удалить любые оставшиеся ионы или окрашенные включения. Обедненный кислотой поток гемицеллюлозных сахаров и/или концентрированный раствор сахаров может затем экстрагироваться экстрагентом с расслоением фаз при нагреве и дополнительно обогащаться олигомерными сахарами и мономерными сахарами, предпочтительно, ксилозой, с использованием подходов, описанных в разделе, ниже.
Экстракция с расслоением фаз при нагреве
Обращаясь к фигурам 1-4, здесь, в некоторых альтернативах, способ включает одну или несколько стадий гидролиза, где кондиционированный препарат лигноцеллюлозы или смешанный препарат сахаров гидролизуется с помощью минеральной и/или органической кислоты, такой как HCl или H2SO4(также упоминается как гидролизный раствор биомассы), с последующими одной или несколькими стадиями после гидролиза, где смесь сахаров, генерируемая посредством гидролиза препарата лигноцеллюлозы или смешанного препарата сахаров, экстрагируется растворителем, таким как алканол (например, гексанол), и/или растворителем и смесью растворителей с расслоением фаз при нагреве, и обработанный растворителем смешанный поток сахаров разделяется с помощью хроматографии (например, анионного обмена, такого как слабо основной анионный обмен, и/или катионного обмена, такого как сильнокислотный катионный обмен), для того, чтобы удалить примеси и увеличить отношение мономерных сахаров к олигомерным сахарам (смотриФигуры2-4). В некоторых альтернативах, способ включает автогидролиз, где кондиционированный препарат лигноцеллюлозы или смешанный препарат сахаров подвергается гидролизу без добавления кислоты (например, кондиционированный препарат лигноцеллюлозы или смешанный препарат сахаров гидролизуется с помощью кислоты, уже присутствующей в препарате). Эта процедура гидролиза и дополнительного гидролиза может повторяться 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 раз или более, например, посредством рециклирования сахаросодержащего потока через дополнительные стадии переработки гидролиза и дополнительного гидролиза для того, чтобы увеличить отношение мономерных сахаров к олигомерным сахарам, предпочтительно, способствуя повышению концентрации ксилозы в потоке сахаров (смотри Фигуры 3 и 4). Поток лигноцеллюлозного остатка может подвергаться помолу и гранулированию с получением гранулированных продуктов лигноцеллюлозы (смотри Фиг.1).
Смесь, обогащенная мономерными сахарами, полученная после гидролиза, а в некоторых альтернативах, полученная после переработки дополнительного гидролиза, затем приводится в контакт с растворителем с расслоением фаз при нагреве, таким как простой эфир этиленгликоля или пропиленгликоля, такой как 2-бутоксиэтанол, 1-пропокси-2-пропанол или любое их сочетание, и осуществляется разделение водной и органической фаз для того, чтобы получить водную фазу, содержащую выделенный или обогащенный поток олигомерных и/или мономерных сахаров, предпочтительно, содержащий повышенное количество мономерных сахаров, таких как ксилоза, и имеющий уменьшенной количество примесей. Смесь, содержащая в органической фазе экстрагент с расслоением фаз при нагреве, содержащая примеси и неразделенные мономерные и олигомерные сахара, может затем подвергаться нагреву, например, при 30°C-100°C, для того, отделять, выделять, обогащать или очищать поток олигомерных и/или мономерных сахаров, предпочтительно, содержащий повышенное количество мономерных сахаров, таких как ксилоза, от экстрагента с расслоением фаз при нагреве и примесей. Поток сахаров, предпочтительно, содержащих повышенное количество мономерных сахаров, таких как ксилоза, полученных после термической обработки, может также рециклироваться при последующих сеансах процедур экстракции и обогащения, описанных выше, например, вместе с дополнительными смешанными потоками сахаров, содержащими олигомерные и мономерные сахара, как показано на Фиг.1. Выделенные потоки сахаров, которые обогащены олигомерными и мономерными сахарами, предпочтительно, ксилозой, также могут подвергаться дополнительной очистке или обогащению, например, с помощью хроматографии, например, SMB и/или SSMB, и/или выпариванию, для того, чтобы получить фракцию мономерных сахаров, предпочтительно, содержащих ксилозу, более высокой чистоты. Эти стадии обогащения и/или очистки могут повторяться 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 раз или более для того, чтобы непрерывно обогащать поток сахаров мономерными сахарами, предпочтительно, содержащими ксилозу.
Обращаясь к Фиг.5, здесь, в одной из альтернатив, поток гидролизного раствора биомассы, который содержит множество олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, отделяется с помощью слабо основной анионообменной смолы, предпочтительно, после этого указанный поток разделяется на сильнокислотной катионообменной смоле. После этих хроматографических стадий предварительной обработки, гидролизный раствор биомассы, который содержит множество олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, кислоту и примеси, приводится в контакт с экстрагентом с расслоением фаз при нагреве, таким как простой эфир этиленгликоля или пропиленгликоля, такой как 2-бутоксиэтанол, 1-пропокси-2-пропанол, или любое их сочетание, для того, чтобы сформировать экстракционную смесь. После экстракции экстрагентом с расслоением фаз при нагреве и разделения фаз, первая водная фракция, содержащая мономерные и олигомерные сахара и воду, отделяется, и эта первая водная фракция может рециклироваться для последующих сеансов экстракции с расслоением фаз при нагреве, как показано на Фиг.5, для того, чтобы улучшить выход мономерных сахаров, предпочтительно, ксилозы, из гидролизного раствора биомассы.
Вторая органическая фракция, содержащая экстрагент с расслоением фаз при нагреве, примеси и олигомерные и/или мономерные сахара, предпочтительно, ксилозу, может выделяться и подвергаться воздействию дополнительных стадий обогащения и/или очистки, как показано на Фиг.5. В одной из альтернатив, вторая органическая фракция, содержащая экстрагент с расслоением фаз при нагреве, примеси и олигомерные и/или мономерные сахара, предпочтительно, ксилозу, нагревается до температуры от 30°C до 100°C, например, до 30°C, 35°C, 40°C, 45°C, 50°C, 55°C, 60°C, 65°C, 70°C, 75°C, 80°C, 85°C, 90°C, 95°C или 100°C, или до температуры в пределах, определяемых любыми двумя температурами из тех, которые рассмотрены выше. После термической обработки второй органической фракции, содержащей экстрагент с расслоением фаз при нагреве, примеси и олигомерные и/или мономерные сахара, предпочтительно, ксилозу, экстрагент с расслоением фаз при нагреве и примеси отделяются от потока олигомерных и/или мономерных сахаров. Поток олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, может затем подвергаться дополнительному разделению, обогащению, выделению и/или очистке посредством хроматографии, такой как SMB и/или SSMB, и/или выпариванию, для того, чтобы выделить, обогатить или очистить олигомерные и/или мономерные сахара, предпочтительно, содержащие ксилозу. В некоторых альтернативных подходах вторая органическая фракция, содержащая экстрагент с расслоением фаз при нагреве, примеси и любые оставшиеся сахара, рециклируется на последующих сеансах экстракции и термической обработки, как описано выше и показано на Фиг.5. В некоторых альтернативах, поток олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, которые выделяются после термической обработки, подвергается дополнительному гидролизу, воздействию хроматографических стадий, предварительной переработке, экстракции с расслоением фаз при нагреве, термическому разделению, обогащению или выделению потока, содержащего мономерные сахара, и дополнительному воздействию хроматографии, такой как SMB и/или SSMB, и/или выпариванию. Эта процедура дополнительного обогащения и/или очистки может повторяться 1, 2, 3, 4, 5, 6, 7, 8, 9, или 10 раз или более, для того, чтобы непрерывно обогащать поток сахаров мономерными сахарами, предпочтительно, содержащими ксилозу. В одной из альтернатив, извлеченная ксилоза имеет чистоту 75%-96%, например, 80%-96%.
Рафинирование, выделение и дополнительная очистка сахаров
После экстракции экстрагентом с расслоением фаз при нагреве (например, простым эфиром этиленгликоля или пропиленгликоля, таким как 2-бутоксиэтанол, 1-пропокси-2-пропанол или любое их сочетание) и отделения, выделения или обогащения потока олигомерных и/или мономерных сахаров, предпочтительно, содержащего ксилозу, от экстрагента с расслоением фаз при нагреве и примесей (например, с использованием нагрева при 30°C-100°C), поток олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, может дополнительно рафинироваться, выделяться или очищаться посредством приведения в контакт полученного в результате потока олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, с ионообменной смолой, например, с помощью хроматографии на этой смоле. В некоторых альтернативах, поток олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, приводится в контакт с сильнокислотной катионообменной смолой (SAC), предпочтительно, посредством хроматографического разделения. В некоторых альтернативах, поток олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, выделенных после разделения на смоле SAC, приводится в контакт со слабо основной анионообменной смолой (WBA), предпочтительно, посредством хроматографического разделения. В некоторых альтернативах, поток олигомерных и/или мономерных сахаров, предпочтительно, содержащих ксилозу, выделенных после разделения на смоле WBA, выпаривают до 25-65%, например, до 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60% или 65% растворенных сахаров, или до их содержания в пределах, определяемых любыми двумя процентами из тех, которые рассмотрены выше, а предпочтительно, до 30-40%, масс/масс, в обычном испарителе, например, в многоступенчатом испарителе или в испарителе с механической рекомпрессией паров (MVR). В некоторых альтернативах, концентрированный раствор сахаров, выделенный после выпаривания, дополнительно рафинируется посредством приведения в контакт со смешанным слоем смолы, предпочтительно, посредством хроматографического разделения. В некоторых альтернативах, после выделения из смешанного слоя смолы, концентрированный раствор, содержащий олигомерные и/или мономерные сахара, дополнительно фракционируется (например, посредством хроматографического разделения) для получения обогащенного потока мономерных сахаров, такого как поток, обогащенный ксилозой, содержащий более чем 75, 78, 80, 82, 84, 85, 86, 88, 90% ксилозы или ее количество в пределах, определяемых любыми двумя количествами из тех, которые рассмотрены выше, и фракция остатка гемицеллюлозных сахаров, содержащая мономерные сахара (например, ксилозу), удаляется. Фракционирование может осуществляться с использованием различных способов, включая, но, не ограничиваясь этим, хроматографию с псевдодвижущимся слоем (SMB) или с последовательными псевдодвижущимися слоями (SSMB). Примеры таких процессов SMB и SSMB описаны, например, в патентах США №№ 6379554, 5102553, 6093326, 6187204, 4332623, 4379751 и 4970002, а также, в GB 2240 053, содержания каждого из них тем самым включается в явном виде в качестве ссылки во всей своей полноте.
В иллюстративной системе SMB или SSMB, слой смолы разделяется в ряду отдельных емкостей, в каждой из них поток проходит через ряд из 4 зон (введения, разделения, введение/разделение/рафинирование и безопасности), и емкости соединяются с помощью контуров рециркуляции. Коллекторная система соединяет емкости и направляет в соответствующей последовательности в каждую емкость (или из нее), каждую из четырех сред, приспособленных для процесса. Эти среды в целом упоминаются как исходные материалы, элюент, экстракт и рафинат. Например, исходные материалы могут представлять собой смесь гемицеллюлозных сахаров, элюент может представлять собой воду, экстракт представляет собой обогащенный раствор ксилозы и рафинат представляет собой водный раствор, содержащий высокомолекулярные сахара и другие мономерные сахара, например, арабинозу, галактозу и глюкозу. Необязательно, элюент может представлять собой водный раствор, содержащий низкую концентрацию иона гидроксида, для поддержания смолы в гидроксильной форме, или элюент может представлять собой водный раствор, содержащий низкую концентрацию кислоты, для поддержания смолы в протонированной форме. Например, исходные материалы, содержащие 30% смесь сахаров, где ксилоза составляет примерно 65-70% смеси, может фракционироваться с использованием SSMB с получением экстракта, содержащего примерно 16-20% сахаров, где ксилоза составляет примерно 82% или более, и рафината, содержащего смесь с 5-7% сахаров только с 15-18% ксилозы. В некоторых альтернативах, после хроматографии SMB или SSMB, поток рафинированных сахаров, содержащих преимущественно мономерные сахара, например, ксилозу, при чистоте 75%, 80%, 85%, 90% или 95%, или в пределах, определяемых любыми двумя процентами из тех, которые рассмотрены выше, затем концентрируется или выпаривается, например, с использованием многоступенчатого испарителя или испарителя с механической рекомпрессией паров (MVR). В некоторых альтернативах, олигомерные сахара, отделенные от мономерных сахаров, например, с помощью хроматографии SSMB, рециклируются в способ для дополнительного гидролиза.
Хроматографическое фракционирование, которое можно использовать в способах, описанных в настоящем документе (например, SMB и/или SSMB, а также предварительное хроматографическое разделение перед SMB и/или SSMB), для того, чтобы достичь рафинирования, выделения или обогащения мономерного сахара (например, ксилозы) из смешанного раствора олигомерных и мономерных сахаров, могут осуществляться с помощью ионообменных смол (например, катионообменной смолы и анионообменной смолы) в качестве материала для набивки колонны. Катионообменные смолы, пригодные для использования в этих способах, включают сильнокислотные катионообменные смолы и слабо кислотные катионообменные смолы. Сильнокислотные катионообменные смолы могут находиться в форме с одновалентным или многовалентным катионом металла, например, в форме с H+, Mg2+, Ca2+ или Zn2+. Предпочтительно, смолы находятся в форме с Na+. Сильнокислотные катионообменные смолы, как правило, имеют стирольный скелет, который предпочтительно поперечно сшивается с помощью 3-8%, предпочтительно, с 5-6,5% дивинилбензола. Слабо кислотные катионообменные смолы могут находиться в форме с одновалентным или многовалентным катионом металла, например, в форме с H+, Mg2+или Ca2+, предпочтительно, в форме с Na+.
Температура хроматографического фракционирования, как правило, находится в пределах от 20 до 90°C, например, составляет 20°C, 30°C, 40°C, 50°C, 60°C, 70°C, 80°C или 90°C, предпочтительно, от 40°C до 65°C, или представляет собой температуру в пределах, определяемых любой температурой из тех, которые рассмотрены выше. pH раствора, который должен фракционироваться, может быть кислотным или доводиться до диапазона от 2,5 до 7, предпочтительно, от 3,5 до 6,5, и наиболее предпочтительно, от 4 до 5,5, или представлять собой pH в пределах, определяемых любым значением pH из тех, которые рассмотрены выше. Как правило, фракционирование может осуществляться при линейной скорости потока примерно 1 м/час-10 м/час в разделительной колонне.
Фракционирование мономерного сахара, такого как ксилоза, из смешанного раствора рафинированных сахаров может предпочтительно достигаться с использованием сильноосновного анионообменника (SBA), имеющего размер частиц ~280-320 мкм. Этот больший размер частиц является преимущественным по сравнению с гораздо меньшими размерами частиц, используемыми в патенте США № 6451123 (включаемом в явном виде в настоящий документ в качестве ссылки для всех целей). Больший размер частиц уменьшает обратное давление колонны до пределов, практичных для промышленного применения. Пригодные для использования коммерческие смолы SBA можно купить у Finex (AS 510 GC Type I, Strong Base Anion, форма геля), сходные сорта можно купить у других производителей, включая Lanxess AG, Purolite, Dow Chemicals Ltd. или Rohm & Haas. Смола SBA может находиться в сульфатной форме или хлоридной форме, предпочтительно, в сульфатной форме. SBA частично импрегнируется гидроксильными группами с помощью NaOH при низкой концентрации, пределы отношения основания к сульфату составляют от 3-12% до 97-88%, соответственно. Для поддержания этого уровня группы OH в смоле, низкий уровень NaOH, достаточный для замены гидроксила, удаляемого посредством адсорбции сахара, может включаться в импульс десорбции, вызывая, таким образом, более продолжительное удерживание ксилозы, чем других сахаров на этой смоле. Фракционирование может осуществляться в режиме SSMB примерно при 40°C-50°C, с получением в результате потока, обогащенного ксилозой, содержащего, по меньшей мере, 79%, по меньшей мере, 80%, по меньшей мере, 83%, предпочтительно, по меньшей мере, 85% ксилозы из сахаров в целом, и смешанного потока сахаров, при извлечении, по меньшей мере, 80%, по меньшей мере, 85% ксилозы.
В некоторых способах, последовательность SSMB включает три стадии. На первой стадии, поток продукта экстрагируется посредством экспонирования и промывки адсорбента потоком десорбента (стадия "от десорбента до экстракта"). Одновременно с этим, поток исходных материалов поступает в адсорбент и поток рафината смывается с адсорбента (стадия "от исходных материалов до рафината"). На второй стадии, поток рафината экстрагируется посредством экспонирования и промывки адсорбента потоком десорбента (стадия "от десорбента до рафинат"). На третьей стадии, десорбент рециклируется обратно в адсорбент (стадия "рецикла").
Как правило, продукт мономерных сахаров (например, ксилозы) экстрагируется таким образом, что поток рафината равен потоку десорбента, но это дает в результате высокое потребление десорбента для достижения извлечения целевого продукта. Предпочтительно, в некоторых последовательностях SSMB, продукт экстрагируется на нескольких стадиях (например, не только на стадии 1, но также и на стадии 2). В некоторых способах, поток продукта экстрагируется не только на первой стадии, но также экстрагируется и на второй стадии (то есть, на стадии "от десорбента до рафината"). Когда продукт экстрагируется на нескольких стадиях, скорость потока десорбента равна сумме скорости потока экстракта и скорости потока рафината. В некоторых вариантах осуществления, скорость потока десорбента является примерно такой же, как сумма скорости потока экстракта и скорости потока рафината. В некоторых вариантах осуществления, скорость потока десорбента находится в пределах 50-150%, 60-140%, 70-130%, 80-120%, 90-110%, 95-105%, 96-104%, 97-103%, 98-102%, 99-101% или 99,5-100,5%, или представляет собой скорость потока в пределах, определяемых любыми скоростями потоков из тех, которые рассмотрены выше, из суммы скорости потока экстракта и скорости потока рафината, или представляет собой скорость в пределах, определяемых любыми двумя скоростями из тех, которые рассмотрены выше. Это изменение в последовательности SSMB уменьшает необходимое количество десорбента, приводя в результате к извлечению целевого продукта при гораздо меньшем объеме десорбента, поддерживая в то же время хроматографические профили SSMB в четырех (4) зонах и шести (6) колоннах и чистоту.
После фракционирования SMB или SSMB, выделенные потоки мономерных и/или олигомерных сахаров (например, поток, содержащий ксилозу) могут необязательно приводиться в контакт со слабо кислотной катионообменной смолой (WAC) в форме с H+ для нейтрализации потока сахаров. Это подкисление делает возможным выпаривание потока сахаров, в то время, поддерживая стабильность сахаров. Смола WAC может регенерироваться с помощью минеральной кислоты или, предпочтительно, посредством приведения в контакт с потоком отработанной кислоты от смолы SAC, используемой на стадии рафинирования сахаров. В некоторых альтернативах, после стадии нейтрализации WAC, поток олигомерных сахаров направляется в испаритель, в то время как поток, обогащенный ксилозой, направляется в кристаллизатор для сахаров. В некоторых альтернативах, когда для фракционирования используется SSMB, ксилоза покидает поток экстракта, и высшие сахара, а также, глюкоза, галактоза и арабиноза, покидают поток рафината. Поток ксилозы может необязательно дополнительно рафинироваться посредством приведения в контакт с гранулированным активированным углем и/или смешанным слоем смолы перед выпариванием для повышения концентрации. Затем поток рафинированной ксилозы необязательно снова выпаривается и кристаллизуется. Продукты представляют собой кристаллы ксилозы и смесь гемицеллюлозных сахаров с удаленной ксилозой.
Чистая ксилоза, как известно, кристаллизуется из перенасыщенных смешанных растворов сахаров. Для достижения этого, поток раствора сахаров, полученный в результате рафинирования сахаров, концентрируется посредством выпаривания и фракционируется с помощью хроматографического разделения с получением потока, обогащенного ксилозой, содержащего более чем 75, 78, 80, 82, 84, 85, 86, 88, 90% ксилозы или ее процент в пределах, определяемых любыми двумя процентами из тех, которые рассмотрены выше, и смеси гемицеллюлозных сахаров с удаленной ксилозой. Поток, обогащенный ксилозой, поступающий от фракционирования, вводится в модуль кристаллизации для получения кристаллов ксилозы.
В некоторых способах, поток, обогащенный ксилозой, необязательно дополнительно выпаривается перед тем, как его вводят в модуль кристаллизации для получения кристаллов ксилозы. Кристаллы могут собираться из маточной жидкости с помощью любых пригодных для использования средств, например, центрифугирования. В зависимости от технологии кристаллизации, кристаллы могут промываться соответствующим раствором, например, водным раствором или растворителем. Кристаллы могут либо сушиться, либо повторно растворяться в воде с получением сиропа ксилозы. Как правило, выход 45-60% потенциальной ксилозы может кристаллизоваться в 20-35, предпочтительно, 24-28-часовом цикле.
После кристаллизации, смесь гемицеллюлозных сахаров маточной жидкости может рециклироваться обратно на стадию фракционирования, поскольку она содержит очень высокое содержание ксилозы, например, >57% ксилозы, >65%, а чаще, >75% ксилозы. Альтернативно, смесь гемицеллюлозных сахаров маточной жидкости может рециклироваться для дополнительных сеансов гидролиза. Раздел, ниже, описывает некоторые из продуктов, которые становятся доступными с помощью способов рафинирования, описанных в настоящем документе.
Продукты
В некоторых альтернативах, желаемый продукт представляет собой получаемый в результате поток сахаров, который получается от одного или нескольких способов рафинирования, описанных в настоящем документе, в частности, смесь сахаров, содержащую большее количество или больший процент массовый мономерных сахаров, по сравнению с олигомерными сахарами. В некоторых продуктах, смесь сахаров содержит отношение моносахаридов к растворенным сахарам, в целом, которое равно или больше чем 0,50, 0,60, 0,70, 0,75, 0,80, 0,85, 0,90, или 0,95 масс/масс, или представляет собой отношение в пределах, определяемых любыми двумя отношениями из тех, которые рассмотрены выше. В некоторых вариантах осуществления, продукт представляет собой смесь сахаров, содержащую уменьшенное количество глюкозы. В некоторых смесях сахаров, отношение глюкозы к моносахаридам в целом меньше чем 0,25, 0,20, 0,15, 0,13, 0,10, 0,06, 0,05, 0,03, или 0,02 масс/масс или представляет собой отношение в пределах, определяемых любыми двумя отношениями из тех, которые рассмотрены выше. В некоторых вариантах осуществления, продукт представляет собой смесь сахаров с обогащенным содержанием ксилозы. В некоторых продуктах, отношение ксилозы к моносахаридам в целом больше чем 0,10, 0,15, 0,18, 0,20, 0,30, 0,40, 0,50, 0,60, 0,70, 0,80 или 0,85 масс/масс, или представляет собой отношение в пределах, определяемых любыми двумя отношениями из тех, которые рассмотрены выше.
В некоторых смесях сахаров, отношение фруктозы к растворенным сахарам, в целом, меньше чем 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,08, 0,09, 0,10, 0,15, 0,20, 0,25 или 0,30 масс/масс, или представляет собой отношение в пределах, определяемых любыми двумя отношениями из тех, которые рассмотрены выше. В некоторых смесях сахаров, отношение фруктозы к растворенным сахарам, в целом, больше чем 0,001, 0,002, 0,005, 0,006, 0,007, 0,008, 0,009, 0,01, 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,08, или 0,09 масс/масс, или представляет собой отношение в пределах, определяемых любыми двумя отношениями из тех, которые рассмотрены выше.
Эти смеси сахаров предпочтительно содержат низкую концентрацию примесей (например, фурфуралей и фенолов). В некоторых продуктах, смесь сахаров содержит фурфурали в количестве до 0,1%, 0,05%, 0,04%, 0,03%, 0,04%, 0,01%, 0,075%, 0,005%, 0,004%, 0,002% или 0,001% масс/масс, или представляет собой количество в пределах, определяемых любыми двумя количествами из тех, которые рассмотрены выше. В некоторых продуктах, смесь сахаров содержит фенолы в количестве до 500 м.д., 400 м.д., 300 м.д., 200 м.д., 100 м.д., 60 м.д., 50 м.д., 40 м.д., 30 м.д., 20 м.д., 10 м.д., 5 м.д., 1 м.д., 0,1 м.д., 0,05 м.д., 0,02 м.д. или 0,01 м.д., или представляет собой их количество в пределах, определяемых любыми двумя количествами из тех, которые рассмотрены выше.
Рассмотренные выше продукты растворов сахаров высокой чистоты можно использовать для получения дополнительных промышленных продуктов и потребительских продуктов, таких как продукты, описанные в PCT/IL2011/00509 (включается в явном виде в настоящий документ в качестве ссылки во всей своей полноте), например, продукты ферментации, такие как корма. В некоторых вариантах осуществления, сахара, полученные с помощью иллюстративных способов, описанных в настоящем документе, включаются в продукт ферментации, как описано в следующих патентах США, содержание каждого из них тем самым в явном виде включается в качестве ссылки во всей своей полноте: патент США № 7678768; патент США № 7534597; патент США № 7186856; патент США № 7144977; патент США № 7019170; патент США № 6693188; патент США № 6534679; патент США № 6452051; патент США № 6361990; патент США № 6320077; патент США № 6229046; патент США № 6187951; патент США № 6160173; патент США № 6087532; патент США № 5892109; патент США № 5780678 и патент США № 5510526.
Продукты ферментации включают, по меньшей мере, один продукт, выбранный из группы, состоящей из спиртов, карбоновых кислот, аминокислот, мономеров для полимерной промышленности и белков, где способ дополнительно включает переработку указанного продукта ферментации для получения продукта, выбранного из группы, состоящей из детергента, продуктов на основе полиэтилена, продуктов на основе полипропилена, продуктов на основе полиолефина, продуктов на основе полимолочной кислоты (полилактида), продуктов на основе полигидроксиалканоата и продуктов на основе соединений полиакрила. Эти продукты ферментации могут использоваться сами по себе или вместе с другими компонентами в качестве пищевого продукта или корма, фармацевтических препаратов, нутрицевтиков, пластиковых деталей или компонентов для изготовления различных потребительских продуктов, топлива, бензина, химических добавок или поверхностно-активного вещества. Рассмотренные выше продукты растворов сахаров высокой чистоты являются пригодными также для химических каталитических преобразований, поскольку катализаторы являются обычно чувствительными к примесям, связанным с продуктами деградации биомассы и сахаров.
В некоторых альтернативах, продукт сахаров высокой чистоты, полученный с помощью одного или нескольких способов, описанных в настоящем документе, может использоваться в ферментационном процессе. Такой ферментационный процесс может использовать микроорганизм или генетически модифицрованный микроорганизм (GMO) из рода Clostridium, Escherichia (например, Escherichia coli), Salmonella, Zymomonas, Rhodococcus, Pseudomonas, Bacillus, Enterococcus, Alcaligenes, Lactobacillus, Klebsiella, Paenibacillus, Corynebacterium, Brevibacterium, Pichia, Candida, Hansenula и Saccharomyces. Хозяева,которыемогут представлять особенный интерес, включают Oligotropha carboxidovorans, Escherichia coli, Bacillus licheniformis, Paenibacillus macerans, Rhodococcus erythropolis, Pseudomonas putida, Lactobacillus plantarum, Enterococcus faecium, Cupriavidus necator, Enterococcus gallinarium, Enterococcus faecalis, Bacillus subtilis и Saccharomyces cerevisiae. Также, любой из известных штаммов этих видов может использоваться в качестве исходного микроорганизма. Необязательно, микроорганизм может представлять собой актиномицет, выбранный из Streptomyces coelicolor, Streptomyces lividans, Streptomyces hygroscopicus, или Saccharopolyspora erytraea. В различных иллюстративных вариантах осуществления, микроорганизм может представлять собой эубактерию, выбранную из Pseudomonas fluorescens, Pseudomonas aeruginosa, Bacillus subtilis или Bacillus cereus. В некоторых примерах, микроорганизм или генетически модифицированный микроорганизм представляет собой грам-отрицательную бактерию.
Продукты преобразования, полученные с помощью ферментации, могут представлять собой, например, спирт, карбоновую кислоту, аминокислоту, мономер для полимерной промышленности или белок. Конкретный пример представляет собой молочную кислоту, которая представляет собой мономер, составляющий полимолочную кислоту, полимер с многочисленными применениями. Продукт преобразования может перерабатываться для получения потребительского продукта, выбранного из группы, состоящей из детергента, продукта на основе полиэтилена, продукта на основе полипропилена, продукта на основе полиолефина, продукта полимолочной кислоты на основе (полилактида), продукта на основе полигидроксиалканоата и продукта на основе соединения полиакрила. Детергент может включать поверхностно-активное вещество на основе сахаров, поверхностно-активное вещество на основе жирных кислот, поверхностно-активное вещество на основе жирных спиртов или фермент, полученный из культуры клеток.
В некоторых вариантах осуществления, продукт преобразования может представлять собой, например, спирт, карбоновую кислоту, аминокислоту, мономер для полимерной промышленности и белок. В некоторых вариантах осуществления, продукт преобразования перерабатывается для получения потребительского продукта, выбранного из группы, состоящей из детергента, продукта на основе полиэтилена, продукта на основе полипропилена, продукта на основе полиолефина, продукта на основе полимолочной кислоты (полилактида), продукта на основе полигидроксиалканоата и продукта на основе соединения полиакрила. Необязательно, детергент включает поверхностно-активное вещество на основе сахаров, поверхностно-активное вещество на основе жирных кислот, поверхностно-активное вещество на основе жирных спиртов или ферментов, полученных из культуры клеток. Необязательно, продукт на основе соединения полиакрила представляет собой пластик, лак для полов, ковер, краску, покрытие, адгезив, дисперсию, флокулянт, эластомер, акриловое стекло, поглощающее изделие, урологические прокладки, гигиенические салфетки, продукт гигиены женщин и подгузник. Необязательно, продукты на основе полиолефина представляют собой бутылку для молока, бутылку для детергента, тюбик для маргарина, контейнер для мусора, водопроводную трубу, поглощающее изделие, подгузник, нетканый материал, игрушку из HDPE или упаковку из HDPE для детергента. Необязательно, продукт на основе полипропилена представляет собой поглощающее изделие, подгузник или нетканый материал. Необязательно, продукт на основе полимолочной кислоты представляет собой упаковку сельскохозяйственного продукта или молочного продукта, пластиковую бутылку, биологически деградируемый продукт или одноразовое изделие. Необязательно, продукт на основе полигидроксиалканоата представляет собой упаковку для сельскохозяйственного продукта, пластиковую бутылку, бумагу с покрытием, формованное или экструдированное изделие, продукт гигиены женщин, аппликатор для тампона, поглощающее изделие, одноразовый нетканый материал или салфетку, медицинскую хирургическую спецодежду, адгезив, эластомер, пленку, покрытие, водный дисперсант, волокно, промежуточный продукт фармацевтического препарата или связующее. Продукт преобразования может также представлять собой этанол, бутанол, изобутанол, жирную кислоту, сложный эфир жирной кислоты, жирный спирт или биодизельное топливо. Продукты сахаров, генерируемые с помощью одного или нескольких способов, описанных в настоящем документе, могут преобразовываться в продукты топлива, например, продукт конденсации изобутена, топливо для реактивных двигателей, бензин, бензоспирт, дизельное топливо, альтернативное топливо, пригодное для обычных двигателей, добавку в дизельное топливо или их предшественник. Это преобразование может осуществляться посредством ферментации или посредством катализируемого химического преобразования Бензоспирт может представлять собой бензин, обогащенный этанолом, и/или бензин, обогащенный бутанолом.
Потребительский продукт может иметь отношение углерода-14 к углероду-12 примерно 2,0 × 10-13 или больше. Потребительский продукт может включать ингредиент потребительского продукта, как описано выше и дополнительный ингредиент, полученный из исходного материала иного, чем лигноцеллюлозный материал. В некоторых случаях, ингредиент и дополнительный ингредиент, полученный из исходного материала иного, чем лигноцеллюлозный материал, имеют по существу одинаковую химическую композицию. Потребительский продукт может содержать маркерную молекулу при концентрации, по меньшей мере, 100 миллиардных долей. Маркерная молекула может представлять собой, например, гексанол, 1-этилгексанол, фурфураль или гидроксиметилфурфураль, продукты конденсации фурфураля или гидроксиметилфурфураля, окрашенные соединения, полученные при карамелизации сахаров, левулиновую кислоту, уксусную кислоту, метанол, галактуроновую кислоту или глицерол.
Потребительские продукты, предшественники потребительских продуктов или ингредиенты потребительских продуктов могут также быть получены из потока лигнина. В некоторых вариантах осуществления, потребительский продукт отличается содержанием золы меньше чем 0,5% масс и/или содержанием углеводов меньше чем 0,5% масс и/или содержанием серы меньше чем 0,1% масс и/или содержанием экстрагируемых веществ меньше чем 0,5% масс. В некоторых вариантах осуществления, потребительский продукт, полученный из потока лигнина, включает один или несколько продуктов из бионефти, карбоновых и жирных кислот, дикарбоновых кислот, гидроксилкарбоновых кислот, гидроксилдикарбоновых кислот и гидроксил-жирных кислот, метилглиоксаля, моно-, ди- или многоатомных спиртов, алканов, алкенов, ароматических соединений, альдегидов, кетонов, сложных эфиров, биополимеров, белков, пептидов, аминокислот, витаминов, антибиотиков и фармацевтических препаратов. В некоторых вариантах осуществления, потребительский продукт включает один или несколько продуктов из диспергирующих веществ, эмульгаторов, комплексообразующих веществ, флокулянтов, агломерирующих веществ, гранулирующих добавок, смол, углеродных волокон, активированного угля, антиоксидантов, жидкого топлива, ароматических химикалиев, ванилина, адгезивов, связующих, поглотителей, веществ, связывающих токсины, пен, покрытий, пленок, каучуков и эластомеров, секвестрантов, топлив и веществ для увеличения объема. В некоторых вариантах осуществления, продукт используется в области, выбранной из группы, состоящей из пищевых продуктов, кормов, материалов, сельского хозяйства, транспорта и строительства. Необязательно, потребительский продукт имеет отношение углерода-14 к углероду-12 примерно 2,0 × 10-13 или больше.
Ксилоза, полученная с помощью одного или нескольких способов, описанных в настоящем документе, может использоваться в качестве исходных материалов для бактериального и химического получения фурфураля и тетрагидрофурана. Ксилоза может также использоваться в качестве исходных материалов для приготовления ксилитола, низкокалорийного альтернативного подсластителя, который имеет полезные свойства для ухода за зубами и питания диабетиков, и, как показано, вносит вклад в лечение инфекций ушей и верхних дыхательных путей. Благодаря этим полезным свойствам, ксилитол включается в пищевые продукты и безалкогольные напитки, в зубные пасты и продукты для полоскания полости рта, в жевательные резинки и кондитерские продукты. Мировой рынок ксилитола является ограниченным из-за его высокой цены по сравнению с другим невосстанавливающими полиоловыми сахарами (например, сорбитолом, маннитолом).
Ксилоза, полученная с помощью одного или нескольких способов, описанных в настоящем документе, может также взаимодействовать с хлорамбуцилом с получением бензолбутановой кислоты, 4-[бис(2-хлорэтил)амино]-2-P-D-ксилопиранозилгидразида, гликозилированного аналога хлорамбуцила, который является пригодным в качестве противоопухолевого и/или антиметастатического агента. Ксилоза может взаимодействовать с фенэтилбромидом и 1-бром-3,3-диметоксипропаном с получением (2S,3S,4S)-2H-пиррола, 3,4-дигидро-3,4-бис(фенил-метокси)-2-[(фенилметокси)метил]-1-оксида, используемого в качестве ингибитора α-глюкозидазы для предотвращения и/или лечения сахарного диабета, гиперлипидемии, новообразования и вирусной инфекции. Следующие далее примеры приводятся для дополнительной иллюстрации аспектов настоящего изобретения, но не предназначены для ограничения рамок настоящего изобретения.
Примеры
Понятно, что примеры и варианты осуществления, описанные в настоящем документе, приводятся только для целей иллюстрации и не предназначены для ограничения рамок заявляемого изобретения. Понятно также, что различные модификации или изменения в свете примеров и вариантов осуществления, описанных в настоящем документе, будут предложены специалистам в данной области, и они должны включаться в истинный смысл и границы настоящего изобретения и в рамки прилагаемой формулы изобретения. Все публикации, патенты и заявки на патенты, цитируемые в настоящем документе, тем самым включаются в качестве ссылок во всей своей полноте для всех целей.
Пример 1 - Экстракция ксилозы с помощью растворителя с расслоением фаз при нагреве
Жидкость до гидролиза смешивают с равным объемом либо 2-бутоксиэтанола (EB), либо 1-пропокси-2-пропанола (PP) в качестве экстракционного растворителя. Полученную гомогенную жидкость нагревают до температуры выше, чем нижняя критическая температура растворимости указанной смеси, например, до 60°C, чтобы вызвать разделение фаз. Фазы расслаиваются, и водная фаза подвергается анализу с помощью UPLC (сверхвысокоэффективной жидкостной хроматографии).
Чистоту ксилозы анализируют с помощью способа LC (жидкостной хроматографии) с использованием системы UPLC Waters Acuity, снабженной колонкой BEH C18 1,7 мкм, 2,1 × 50 мм, и используя смесь MeOH/H2O, 95:5, в качестве элюента.
Хроматограмма водной фазы, полученная после экстракции EB, показана на Фиг.6. Чистота ксилозы составляет 66%.
Хроматограмма водной фазы, полученная после экстракции PP, показана на Фиг.7. Чистота ксилозы составляет 66%.
Рециклирование этих растворителей достигается с помощью вакуумной дистилляции. Уровень вакуума зависит от используемого растворителя. Температуры кипения используемых растворителей, полученные из литературы, составляют 169°C для EB и 140°C для PP.
Спектр ЯМР коммерческого EB в CDCl3 показан на Фиг.8. Спектр ЯМР рециклированного и дистиллированного EB в CDCl3 показан на Фиг.9. Спектр ЯМР коммерческого PP в CDCl3 показан на Фиг.10. Спектр ЯМР рециклированного и дистиллированного EB в CDCl3 показан на Фиг.11.
Хроматограмма смеси перед гидролизом после экстракции EB с использованием рециклированного растворителя показана на Фиг.12. Чистота ксилозы составляет 66%.
Хроматограмма смеси перед гидролизом после экстракции PP с использованием рециклированного растворителя показана на Фиг.13. Чистота ксилозы составляет 63%.
Хотя настоящее изобретение описывается со ссылками на варианты осуществления и примеры, должно быть понятно, что различные модификации могут осуществляться без отклонения от духа изобретения. Соответственно, настоящее изобретение ограничивается только следующей далее формулой изобретения. Все ссылки, цитируемые в настоящем документе, тем самым в явном виде включаются в качестве ссылок во всей своей полноте.
Реферат
Изобретение относится к процессам очистки сахара. Описан способ генерирования потока рафинированных сахаров, которые содержат ксилозу, из гидролизного раствора биомассы, включающий: (i) приведение в контакт гидролизного раствора биомассы, который содержит множество смешанных сахаров, содержащих ксилозу, кислоту и примеси, с растворителем с расслоением фаз при нагреве, таким как растворитель на основе гликоля, с образованием экстракционной смеси; и (ii) выделение из указанной экстракционной смеси первого потока, содержащего растворитель с расслоением фаз при нагреве, кислоту и примеси, и второго потока рафинированного сахара, который содержит ксилозу. Также описана экстракционная смесь для экстракции сахаров. Технический результат: повышение качества очистки сахара и уменьшение стадий процесса. 2 н. и 19 з.п. ф-лы, 13 ил.

Комментарии