Пептидные композиции - RU2015145593A
Код документа: RU2015145593A
Формула
1. Выделенный полипептид нижеследующей структурной формулы (I):

или его фармацевтически приемлемая соль, где:
R1 обозначает Н или С1-С6 ацил;
R2 обозначает -NR3R4, или -OR5, где каждый из R3, R4 и R5 независимо обозначает Н или С1-С6 алкил;
А1 обозначает аминокислотный остаток, выбранный из Arg, Lys, Orn, His, Nle, Phe, Val, Leu, Trp, Tyr, Ala, Ser, Thr, Gln, Asn, Asp, Glu или TzAla; или
А1 обозначает фрагмент, выбранный из необязательно замещенного С1-С12 алкила, необязательно замещенного С6-С18 арила, необязательно замещенного С5-С18 гетероарила, аралкила, в котором арильная часть представляет собой необязательно замещенный С6-С18 арил, а алкильная часть представляет собой необязательно замещенный С1-С12 алкил, или гетероаралкил, где гетероарильная часть представляет собой необязательно замещенный С5-С18 гетероарил, а алкильная часть представляет собой необязательно замещенный С1-С12 алкил; или
А1 отсутствует; или
каждый из А2 и А8 независимо обозначает остаток аминокислоты, выбранный из Cys, hCys, Pen, Asp, Glu, Lys, Orn, Dbu или Dpr, где пары А2 и А8 выбирают таким образом, чтобы обеспечить возможность образования ковалентной связи между соответствующими боковыми цепями;
А3 обозначает аминокислотный остаток, выбранный из Ala, Tle, Val, Leu, Ile, Cha, Pro, Ser, Thr, Lys, Arg, His, Phe, Gln, Sar, Gly, Asn, Aib, или
А3 отсутствует; или
А3 обозначает остаток Y, где Y обозначает аминокислоту, имеющую одну из следующих структурных формул:



где каждый из R11 и R12 независимо обозначает Н, -СН3, фенил или бензил;
каждый из R21, R22, R23 и R24 независимо обозначает Н, -СН3, -CF3, фенил, бензил, F, Cl, Br, I, -ОСН3 или -ОН;
каждый из R31, R32, R33, R34, R41, R42 и R43 независимо обозначает Н, -СН3, -CF3, фенил, бензил, F, Cl, Br, I, -ОСН3 или -ОН;
А4 отсутствует или обозначает аминокислотный остаток, выбранный из Atc, Ala, QAla, Aib, Sar, Ser, Thr, Pro, Hyp, Asn, Gln, необязательно замещенного His, Trp, Tyr, Lys, Arg, sChp, или остаток X, где X обозначает аминокислоту, имеющую одну из следующих структурных формул:




где каждый из R51 и R52 независимо обозначает Н, -СН3, фенил или бензил;
каждый из R61, R62, R63 и R64 независимо обозначает Н, -СН3, -CF3, фенил, бензил, F, Cl, Br, I, -ОСН3 или -ОН;
каждый из R71, R72, R73, R74, R81, R82 и R83 независимо обозначает Н, -СН3, -CF3, фенил, бензил, F, Cl, Br, I, -ОСН3 или -ОН;
А5 обозначает необязательно замещенный Phe, необязательно замещенный 1-Nal, или необязательно замещенный 2-Nal;
А6 обозначает Arg; и
А7 обозначает Trp,
где любой аминокислотный остаток может находиться в L- или в D-конфигурации, при условии, что:
1) А3 и А4 одновременно не отсутствуют;
2) если А4 обозначает аминокислоту, А3 отличается от Aib или Gly; и
3) если А4 обозначает His, а А5 обозначает D-Phe или 2-Nal, А3 отличается от D-аминокислоты или L-Ala;
4) если каждый из А2 и А8 независимо выбран из Cys, hCys или Pen, то:
(a) если А4 отсутствует, А3 отличается от L-His;
(b) если А3 отсутствует, А4 отличается от L-His; и
(c) если А4 обозначает His, А3 отличается от Glu, Leu или Lys.
2. Выделенный полипептид по п. 1,
где R1 обозначает Н или С1-С6 ацил;
R2 обозначает -NR3R4, или -OR5, где каждый из R3, R4 и R5 независимо обозначает Н или С1-С6 алкил;
А1 отсутствует; или
А1 обозначает аминокислотный остаток, выбранный из Arg, Lys, Orn, His, Nle, Phe, Val, Leu, Trp, Tyr, Ala, Ser, Thr, Gln, Asn, Asp, Glu или TzAla; или
А1 обозначает фрагмент, выбранный из необязательно замещенного С1-С12 алкила, необязательно замещенного С6-С18 арила, необязательно замещенного С5-С18 гетероарила, аралкила, в котором арильная часть представляет собой необязательно замещенный С6-С18 арил, а алкильная часть представляет собой необязательно замещенный С1-С12 алкил, или гетероаралкила, где гетероарильная часть представляет собой необязательно замещенный С5-С18 гетероарил, а алкильная часть представляет собой необязательно замещенный С1-С12 алкил;
каждый из А2 и А8 независимо обозначает остаток аминокислоты, выбранный из Cys, hCys, Pen, Asp, Glu, Lys, Orn, Dbu или Dpr, где пары А2 и А8 выбирают таким образом, чтобы обеспечить возможность образования ковалентной связи между соответствующими боковыми цепями;
А3 обозначает аминокислотный остаток, выбранный из Ala, Tle, Val, Leu, Ile, Cha, Pro, Ser, Thr, Lys, Arg, His, Phe, Gln, Sar, Gly, Asn или Aib;
А4 отсутствует или обозначает аминокислотный остаток, выбранный из Atc, Ala, QAla, Aib, Sar, Ser, Thr, Pro, Hyp, Asn, Gln, необязательно замещенного His, Trp, Tyr, Lys, Arg, sChp, или остаток X, где X обозначает аминокислоту, представленную следующей структурной формулой:

А5 обозначает необязательно замещенный Phe, необязательно замещенный 1-Nal, или необязательно замещенный 2-Nal;
А6 обозначает Arg; и
А7 обозначает Trp,
где любой аминокислотный остаток может находиться в L- или в D-конфигурации.
3. Полипептид по п. 1 или 2, где А3 обозначает D-аминокислоту.
4. Полипептид по п. 1 или 2, где А4 обозначает L-аминокислоту.
5. Полипептид по п. 1 или 2, где А4 отсутствует.
6. Полипептид по п. 1, где А5 обозначает необязательно замещенный D-Phe.
7. Полипептид по п. 1, где А5 необязательно замещен по любому из пяти ароматических атомов углерода заместителем, выбранным из F, Cl, Br, I, -СН3, -ОН, -CN, амина, -NO2 или -ОСН3.
8. Полипептид по п. 1, где А5 обозначает остаток D-аминокислоты, выбранный из:
Phe, Phe(2'-F), Phe(2'-Cl), Phe(2'-Br), Phe(2'-I), Phe(2'-CN), Phe(2'-CH3), Phe(2'-OCH3), Phe(2'-CF3), Phe(2'-NO2), Phe(3'-F), Phe(3'-Cl), Phe(3'-Br), Phe(3'-I), Phe(3'-CN), Phe(3'-CH3), Phe(3'-OCH3), Phe(3'-CF3), Phe(3'-NO2), Phe(4'-F), Phe(4'-Cl), Phe(4'-Br), Phe(4'-I), Phe(4'-CN), Phe(4'-CH3), Phe(4'-OCH3), Phe(4'-CF3), Phe(4'-NO2), Phe(4'-t-Bu), Phe(2',4'-diF), Phe(2',4'-diCl), Phe(2',4'-diBr), Phe(2',4'-diI), Phe(2',4'-di-CN), Phe(2',4'-di-CH3), Phe(2',4'-di-OCH3), Phe(3',4'-diF), Phe(3',4'-diCl), Phe(3',4'-diBr), Phe(3',4'-diI), Phe(3',4'-di-CN), Phe(3',4'-di-CH3), Phe(3',4'-di-OCH3), Phe(3',5'-diF), Phe(3',5'-diCl), Phe(3',5'-diBr), Phe(3',5'-diI), Phe(3',5'-di-CN), Phe(3',5'-diCH3), Phe(3',5'-di-OCH3) или Phe(3',4',5'-triF).
9. Полипептид по п. 1, где А4 обозначает His, необязательно замещенный по любому замещаемому положению заместителем, выбранным из F, Cl, Br, I, -СН3, -ОН, -CN, амина, -NO2 или -ОСН3.
10. Полипептид по п. 1 или 2, представленный одной из нижеследующих структурных формул:


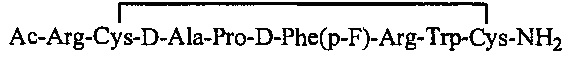

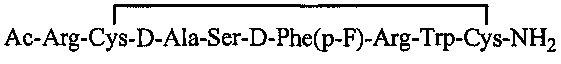







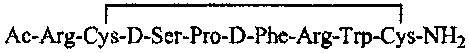
или его фармацевтически приемлемая соль.
11. Полипептид по п. 1 или 2, представленный одной из нижеследующих структурных формул:









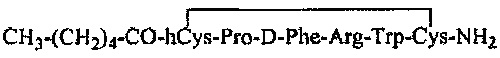

или его фармацевтически приемлемая соль.
12. Полипептид по п. 1 или 2, представленный одной из нижеследующих структурных формул:



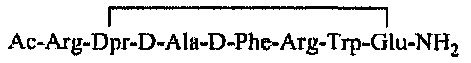







или его фармацевтически приемлемая соль.
13. Полипептид по п. 1 или 2, где А4 обозначает аминокислотный остаток, выбранный из Atc, Ala, QAla, Aib, Sar, Ser, Thr, Pro, Hyp, Asn, Gln, необязательно замещенного His, Trp, Tyr, Lys, Arg, sChp, или остаток X.
14. Полипептид по п. 13, представленный одной из нижеследующих структурных формул:
Ac-Arg-цикло[Cys-D-Ala-His(3-Me)-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 36)
Ac-Arg-цикло[Cys-D-Ala-His(1-Me)-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 37)
Ac-Arg-цикло[Cys-D-Ala-Trp-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 9)
Ac-Arg-цикло[Cys-D-Ala-Gln-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 8)
Ac-Arg-цикло[Cys-D-Ala-Asn-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 7)
Ac-Arg-цикло[Cys-D-Ala-Arg-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 38)
Ac-Arg-цикло[Cys-D-Ala-Tyr-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 39)
Ac-Arg-цикло[Cys-D-Ala-D-Pro-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 40)
Ac-Arg-цикло[Cys-D-Ala-Pro-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 2)
Ac-Arg-цикло[Cys-D-Ala-Pro-D-Phe(p-F)-Arg-Trp-Cys]-NH2; (SEQ ID NO: 4)
Ac-Arg-цикло[Cys-D-Ala-Atc-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 41)
Ac-Arg-цикло[Cys-D-Ala-QAla-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 42)
Ac-Arg-цикло[Cys-D-Ala-sChp-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 43) или
Ac-Arg-цикло[Cys-D-Ala-X-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO: 44)
или его фармацевтически приемлемая соль.
15. Полипептид по п. 1 или 2, представленный одной из нижеследующих структурных формул:
Ac-Arg-цикло[hCys-Ala-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 15)
Ac-Arg-цикло[hCys-D-Ala-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 14)
Ac-Arg-цикло[hCys-D-Ala-D-Phe-Arg-Trp-Pen]-NH2; (SEQ ID NO: 45)
Ac-Arg-цикло[Glu-D-Ala-D-Phe-Arg-Trp-Dpr]-NH2; (SEQ ID NO: 26)
Ac-Arg-цикло[Glu-Ala-D-Phe-Arg-Trp-Dpr]-NH2; (SEQ ID NO: 27)
Ac-Arg-цикло[hCys-Aib-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 46)
Ac-Arg-цикло[hCys-Sar-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 47)
Ac-Arg-цикло[hCys-Val-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 48)
Ac-Arg-цикло[hCys-D-Val-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 49)
Ac-Arg-цикло[hCys-Gln-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 50)
Ac-Arg-цикло[hCys-D-Gln-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 51)
Ac-Arg-цикло[hCys-Ala-D-Phe-Arg-Trp-Pen]-NH2; (SEQ ID NO: 52)
Ac-Arg-цикло[D-Pen-D-Ala-D-Phe-Arg-Trp-hCys]-NH2; (SEQ ID NO: 53)
Ac-Arg-цикло[Cys-D-Ala-D-Phe-Arg-Trp-hCys]-NH2; (SEQ ID NO: 17)
Ac-Arg-цикло[Pen-D-Ala-D-Phe-Arg-Trp-hCys]-NH2; (SEQ ID NO: 54)
Ac-Arg-цикло[D-hCys-D-Ala-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 55)
Ac-Arg-цикло[hCys-Pro-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 20) или
Ac-Arg-цикло[hCys-D-Pro-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO: 56)
или его фармацевтически приемлемая соль.
16. Полипептид по п. 1 или 2, где:
А3 обозначает аминокислотный остаток, выбранный из Tle, Val, Leu, Ile, Cha, Pro, Ser, Thr, Lys, Arg, His, Phe, Gln, Sar, Gly, Asn или Aib; a
А4 обозначает аминокислотный остаток, выбранный из Atc, Ala, QAla, Aib, Sar, Ser, Thr, Pro, Hyp, Asn, Gln, необязательно замещенного His, Trp, Tyr, Lys, Arg, sChp, или остаток X.
17. Полипептид по п. 16, представленный одной из нижеследующих структурных формул:
Ac-Arg-цикло[Cys-Val-Gln-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 57)
Ac-Arg-цикло[Cys-D-Val-Gln-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 11) или
Ac-Arg-цикло[Cys-D-Val-His(1-Me)-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO: 58)
или его фармацевтически приемлемая соль.
18. Полипептид по п. 1 или 2, представленный одной из нижеследующих структурных формул:
Ac-TzAla-цикло[Cys-Ala-Gln-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 59) или
Ac-Glu-цикло[Cys-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO: 60)
или его фармацевтически приемлемая соль.
19. Полипептид по п. 1 или 2, представленный одной из нижеследующих структурных формул:
Ac-Arg-цикло[Cys-D-Ala-His(1-Me)-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 37)
Ac-Arg-цикло[Cys-D-Ala-Gln-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 8) или
Ac-Arg-цикло[Cys-D-Ala-Asn-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO: 7)
или его фармацевтически приемлемая соль.
20. Полипептид по п. 1 или 2, представленный одной из нижеследующих структурных формул:
Ac-Arg-цикло[Cys-D-Ala-His(1-Me)-D-2-Nal-Arg-Trp-Cys]-NH2; (SEQ ID NO: 64)
Ac-Arg-цикло[Cys-D-Ala-Gln-D-2-Nal-Arg-Trp-Cys]-NH2; (SEQ ID NO: 65) или
Ac-Arg-цикло[Cys-D-Ala-Asn-D-2-Nal-Arg-Trp-Cys]-NH2, (SEQ ID NO: 66)
или его фармацевтически приемлемая соль.
21. Полипептид по п. 1 или 2, представленный одной из нижеследующих структурных формул:
Ac-Arg-цикло[Cys-D-Ala-His(1-Me)-D-Phe-Arg-Trp-Cys]-OH; (SEQ ID NO: 67)
Ac-Arg-цикло[Cys-D-Ala-Gln-D-Phe-Arg-Trp-Cys]-OH; (SEQ ID NO: 68) или
Ac-Arg-цикло[Cys-D-Ala-Asn-D-Phe-Arg-Trp-Cys]-OH, (SEQ ID NO: 69)
или его фармацевтически приемлемая соль.
22. Выделенный полипептид одной из нижеследующих структурных формул:
Ac-Arg-цикло[Cys-D-Leu-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 61)
Ac-Arg-цикло[Cys-D-Ile-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 62)
Ac-Arg-цикло[Cys-D-Tle-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO: 63) или
Ac-Arg-цикло[Cys-D-Val-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO: 10)
или его фармацевтически приемлемая соль.
23. Способ лечения расстройства, чувствительный к модуляции MC4R у индивидуума, нуждающегося в этом, включающий в себя введение указанному индивидууму эффективного количества полипептида по п. 1 или 2, или его фармацевтически приемлемой соли.
24. Способ по п. 23, в котором расстройство, чувствительное к модуляции MC4R, представляет собой диабет типа 1, диабет типа 2, ожирение, инсулинорезистентность, метаболический синдром, мужскую эректильную дисфункцию, женское половое расстройство, неалкогольную жировую дистрофию печени или неалкогольный стеатогепатит.
25. Фармацевтическая композиция, содержащая полипептид по п. 1 или 2 или его фармацевтически приемлемую соль, в фармацевтически приемлемом носителе.

Комментарии